
第99.1展示文本

2024年6月,我們是Optejet®公司,在具有高未滿足需求的大市場中開發和商業推廣眼科治療和OptecareΡ服務。EYEN-COM-V2-0021

前瞻性聲明除歷史信息外,本演示文稿中包含的所有聲明、期望和假設均為前瞻性聲明。前瞻性聲明包括但不限於表達我們意圖、信仰、期望、策略、預測或任何其他文件與我們未來活動或其他未來事件或條件有關的聲明,包括我們產品、產品候選人和平臺技術的預計市場機會的陳述。這些聲明基於管理層所做的假設,當前的期望、估計和預測,包括部分基於我們業務的假設。這些聲明不是未來業績的保證,涉及風險、不確定性和假設,這些風險、不確定性和假設難以預測。因此,由於文檔中反覆討論過的許多因素,實際結果和結果可能(而且在某些情況下可能)與前瞻性聲明中表達或預測的有所不同。此外,這些聲明可能會受到與其他事情有關的風險和不確定性的影響:我們和我們的許可方的臨牀試驗風險,包括但不限於此類試驗的費用、設計、啟動和招募、時間安排、進展和結果;時機和我們的許可方能夠提交申請、獲得和維持Mydcombi、類脂酸酯丙酸霜和我們的產品候選人的監管批准的能力;Mydcombi、類脂酸酯丙酸霜和我們產品候選人的潛在優勢以及許可交易的潛在收入;Mydcombi、類脂酸酯丙酸霜和我們產品候選人的市場接受度和臨牀水平;我們對Mydcombi、類脂酸酯丙酸霜和我們產品候選人的潛在市場機會的估計;依賴第三方發展和商業推廣MydcombiΡ、類脂酸酯丙酸霜和我們某些產品候選人的能力;我們及合作伙伴及時開發、實施和保持Mydcombi、類脂酸酯丙酸霜和我們產品候選人的製造、商業化和市場營銷能力和策略;知識產權風險;我們經營市場的法律、監管、立法和地緣政治環境的變化以及這些變化對我們獲得產品監管批准的能力的影響;以及我們的競爭地位。任何前瞻性聲明僅於其發佈日期發表,除適用證券法規定外,Eyenovia不承擔任何更新任何前瞻性聲明的義務。2
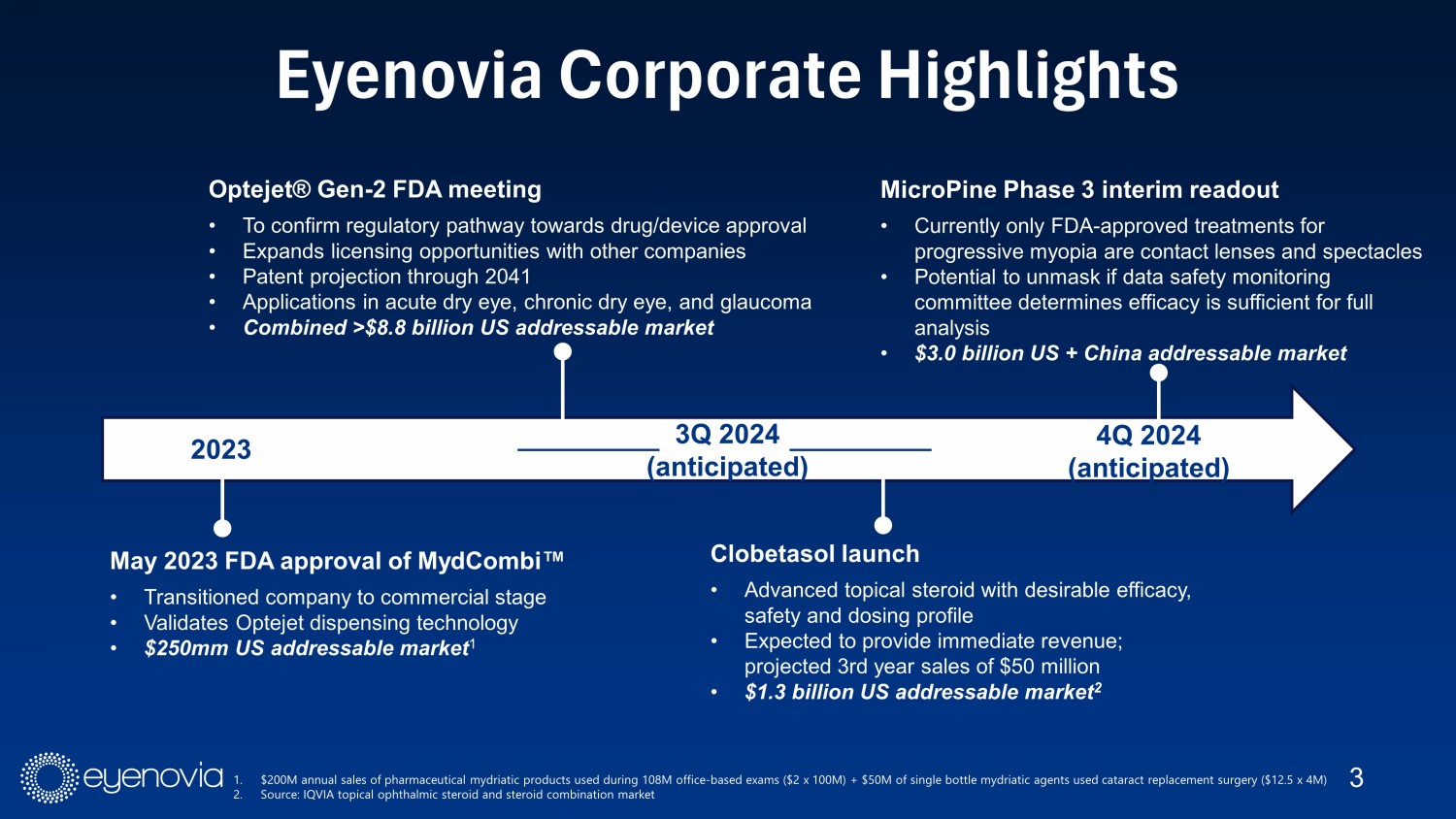
3 Eyenovia公司亮點2023年5月MydCombiŒ獲得FDA批准•使公司向商業化階段轉變•驗證了Optejet配藥技術•2.5億美元的美國可尋址市場2024年第3季(預計)Optejet® Gen-2 FDA會議•確定藥品/設備批准的監管途徑•通過其他公司擴大許可機會•專利預測到2041年•應用於急性乾眼症、慢性乾眼症和青光眼•結合的超過88億美元的美國可尋址市場Clobetasol推出•高效、安全、給藥剖面理想的先進局部類固醇•預計提供即時收益;預計第三年銷售額為5000萬美元•13億美元的美國可尋址市場2MicroPine第3期臨時查漏報告•目前唯一獲得FDA認可的漸進性近視治療是隱形眼鏡和眼鏡•可能揭示如果數據安全監測委員會確定足夠用於全面分析的療效•30億美元的中國市場+可尋址市場4Q2024(預計)1.每年2億美元的製藥性瞳孔擴張劑用於1.08億辦公室檢查中(每百萬2美元)+單瓶瞳孔擴張劑用於白內障替換手術(每12.5美元4百萬)2.來源:IQVIA眼科局部類固醇和類固醇組合市場

MicroPine Atropine Ophthalmic Metered Spray我們的優質近期機會,在市場價值數十億的小兒漸進性近視市場中。4

未滿足的醫療需求當前的選項不適用於所有患者,且不能消除進展風險。3.0億美元的市場在美國和中國。這是全球眼科護理市場中最大的市場之一。5個月內預計有重要的臨牀里程碑CHAPERONE數據監測委員會2024年第四季度審查期望5種資產亮點製造業CMO製造藥品;EyeNova進行器械和無菌填充成型強大的IP,不可替代獨特的FDA表格和方法專利,保護期限到2041年Optejet技術易於使用和自我管理,具有數字能力來跟蹤依從性和合規性。
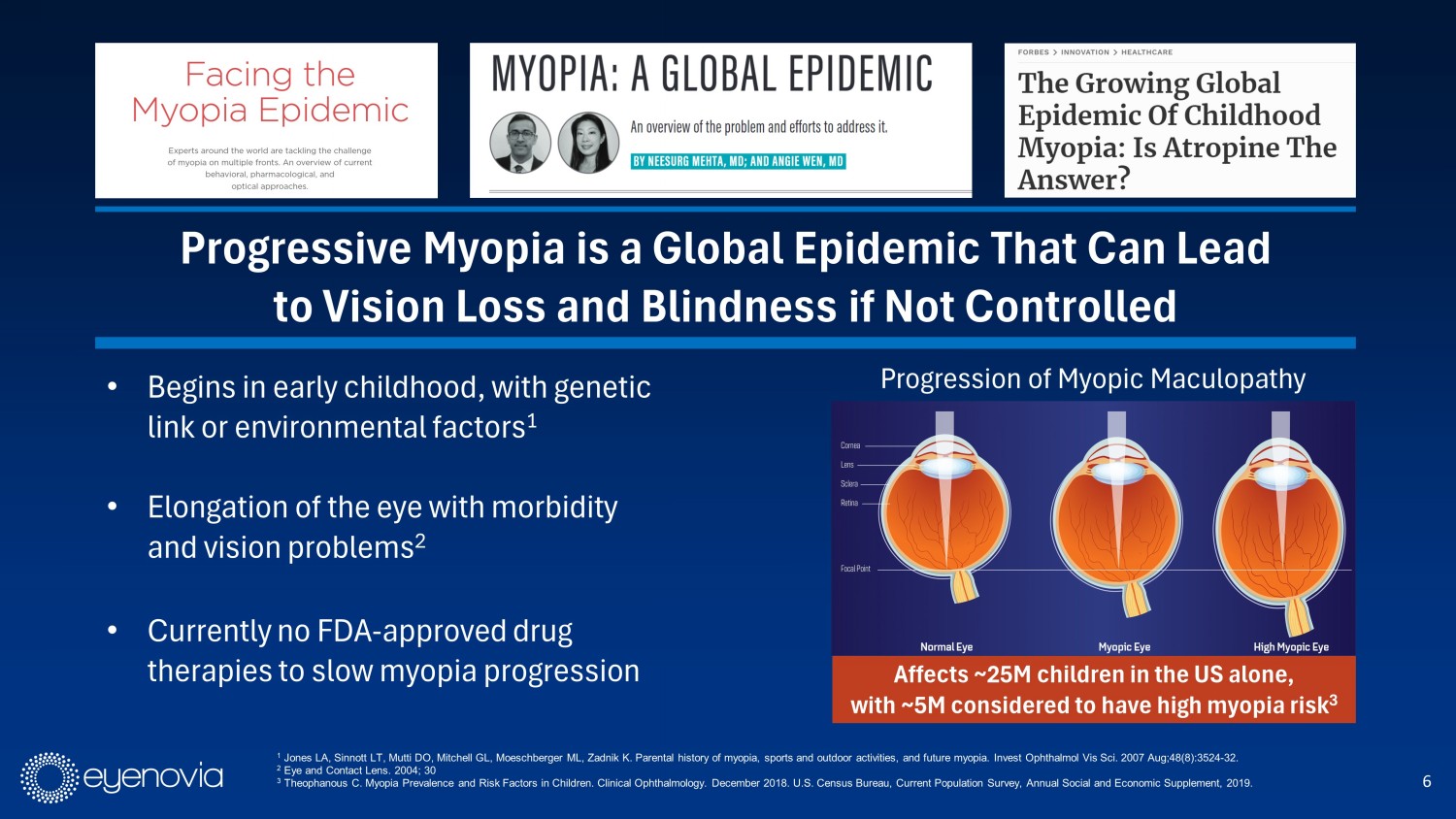
6•從兒童早期開始,往往伴隨遺傳聯繫或環境因素1•眼睛延長帶來發病率和視覺問題2•目前沒有FDA批准的藥物治療可以減緩近視的進展影響超過2500萬美國兒童,其中約500萬被認為有高度近視風險31Jones LA,Sinnott LT,Mutti DO,Mitchell GL,Moeschberger ML,Zadnik K.近視的父母史、體育和户外活動以及未來的近視。Invest Ophthalmol Vis Sci。2007年8月;48(8):3524-32.2 Eye and Contact Lens。2004年;30 3 Theophanous C.兒童近視的盛行率和危險因素。臨牀眼科學。2018年12月。美國人口普查局,目前人口調查,2019年。漸進性近視是導致視力損失和失明的全球流行病。近視黃斑病變的進展
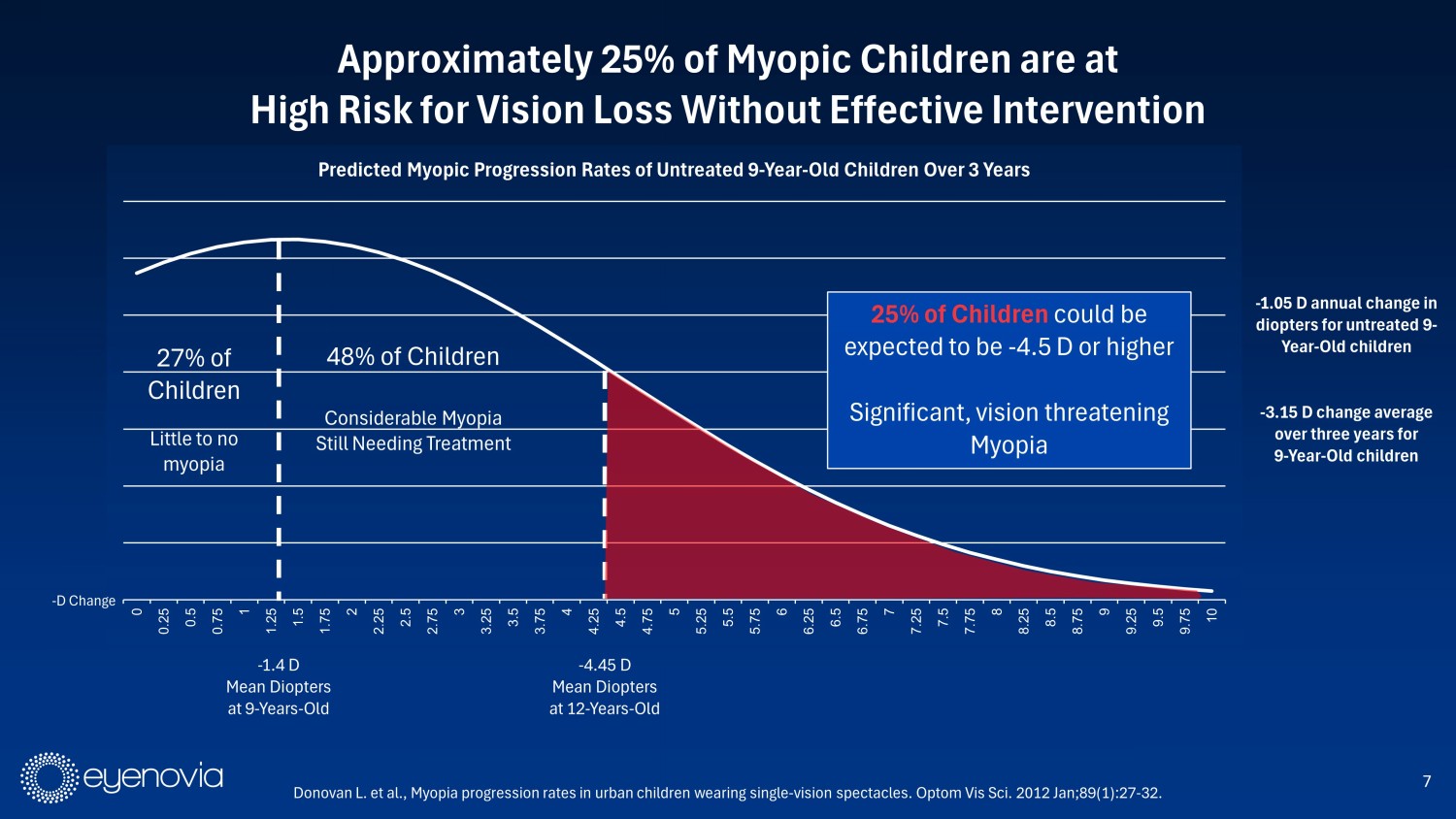
7大約有25%的近視兒童處於視力喪失的高風險狀態,沒有有效的幹預方法-9歲時平均為1.4D的屈光度Donovan L.等人,Urban children wearing single-vision spectacles in myopia progression rates。Optom Vis Sci。2012年1月;89(1):27-32.0 0.25 0.5 0.75 1 1.25 1.5 1.75 2 2.25 2.5 2.75 3 3.25 3.5 3.75 4 4.25 4.5 4.75 5 5.25 5.5 5.75 6 6.25 6.5 6.75 7 7.25 7.5 7.75 8 8.25 8.5 8.75 9 9.25 9.5 9.75 10預測未治療9歲兒童的近視進展率在3年內-4.45D的平均屈光度在12歲時為4.45D的平均屈光度有25%的孩子可能出現>-4.5D重大、威脅視力的近視48%的兒童需要治療27%的孩子沒有或幾乎沒有近視-對於未經治療的9歲兒童,每年的屈光度變化為-1.05D-對於經過3年的平均9歲兒童,平均屈光度變化為-3.15DChange

今天是唯一獲FDA認證的治療方法-在眼鏡中使用隱形眼鏡——眼科醫療和視覺科學94(6):638-646,2017年6月;國際衞生科學(卡西姆)。2013 年11月;7(3):291-9 doi:10.12816/0006057。然而,超過75%的驗光師認為,在10歲以下患者中使用隱形眼鏡是不合適的,微生物角膜炎成為隱形眼鏡佩戴者的一個嚴重問題。
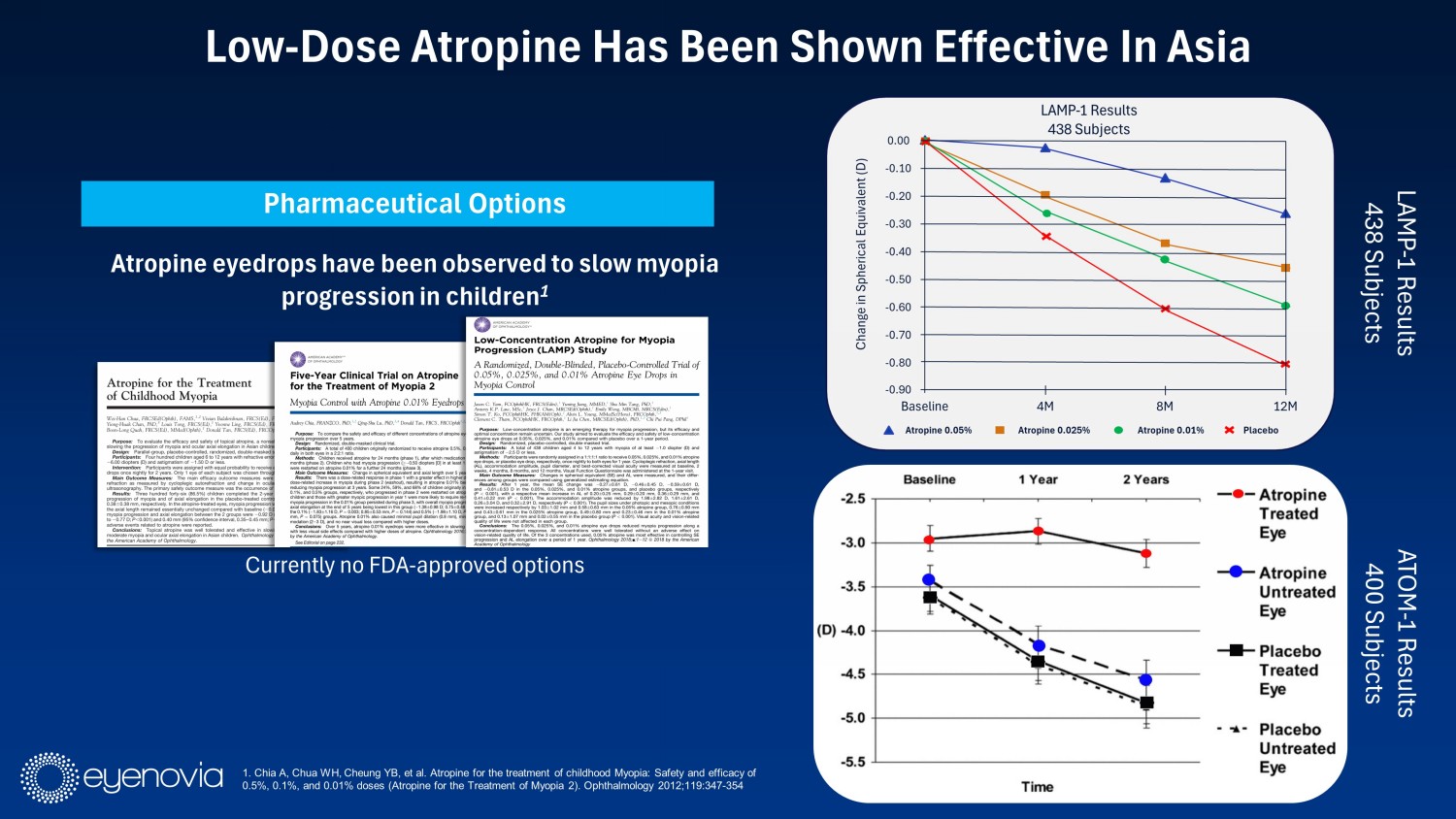
藥品期權:瞳孔散瞳藥水已經被觀察到可以減緩兒童近視的進展1,目前尚未有FDA批准的其他期權。在亞洲,低劑量瞳孔散瞳劑已經顯示出有效性1。ATOM-1結果400名受試者LAMP-1結果438名受試者。
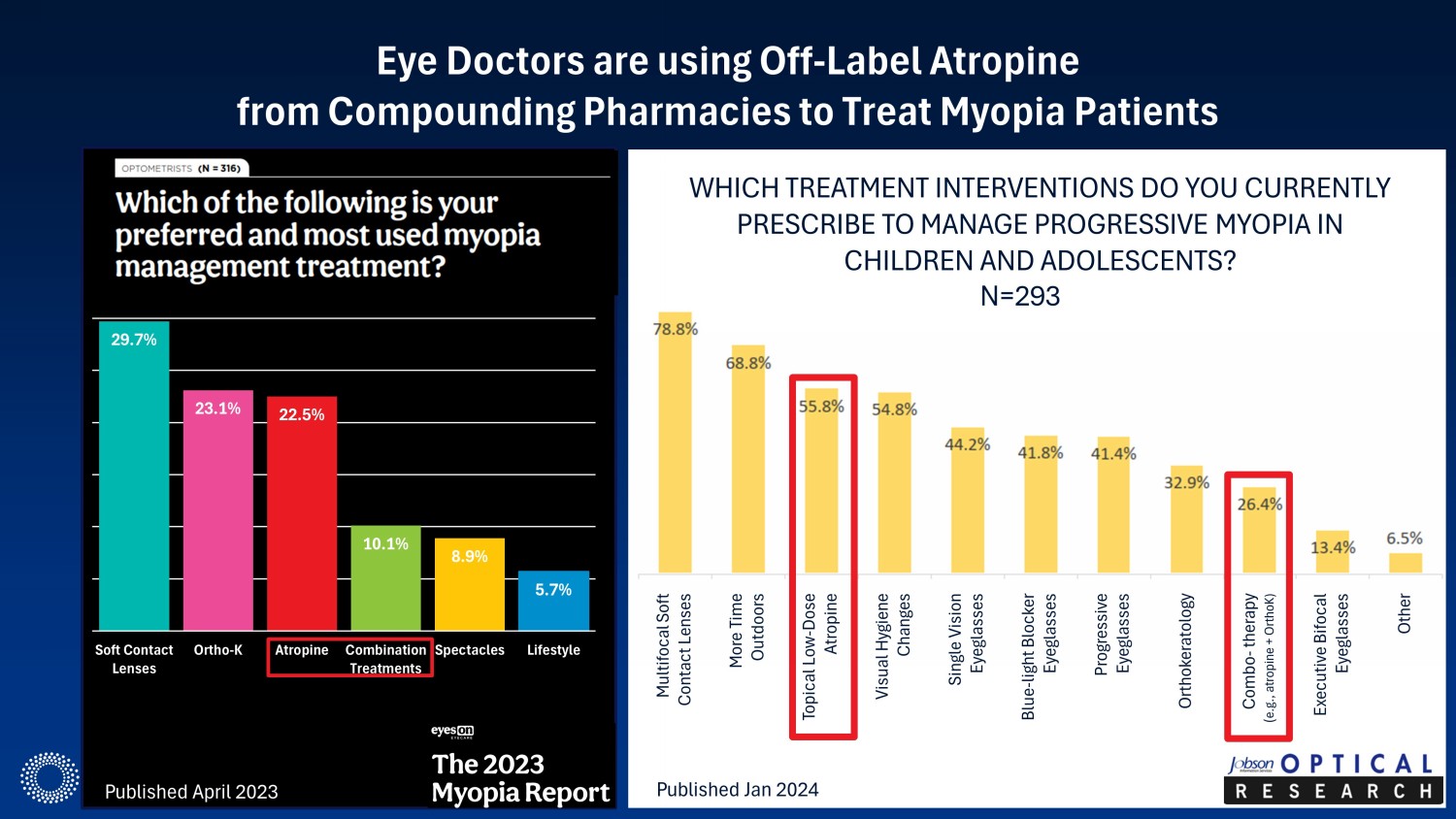
眼科醫生正在使用複合藥店的未標籤批准測試劑治療近視患者,以及逐步增加單光學鏡片和近放大鏡鏡片,視覺衞生習慣的變化,防藍光眼鏡和視力矯正手術等方法。

MicroPine是逐步近視的首選藥物和設備產品,有望實現以下目標:1年後對球面鏡度數小於-0.25D的眼睛顯示出60%的近視減緩且無需回落;每天每隻眼睛噴一次,非常適合兒童使用;使用舒適,對眼睛表面沒有太大的影響;局部副作用較小,系統暴露風險極低;Optecare P合規系統為醫生提供了服藥提醒和產品使用歷史紀錄,以提高治療的成功率;估計的淨銷售價格為每月200美元,COGS低於每月20美元。

CHAPERONE只需要一次單一的3階段試驗便可獲得FDA的批准。三個部分,分別以8微升眼科噴霧劑的劑量進行計量:安慰劑,0.01%和0.1%的瞳孔散瞳劑;在美國,有近視風險的兒童的年齡在3歲至13歲之間;每晚每隻眼睛噴一次MicroPine;3年後的有效終點——小於0.5度逐漸減少的近視發展;迄今為止的掩蓋數據表明,SAE的比率非常低(每1000個患者月的治療少於1個);所有的SAE都被調查人員判斷與治療無關。治療依從性似乎比眼用藥研究歷史上更高。
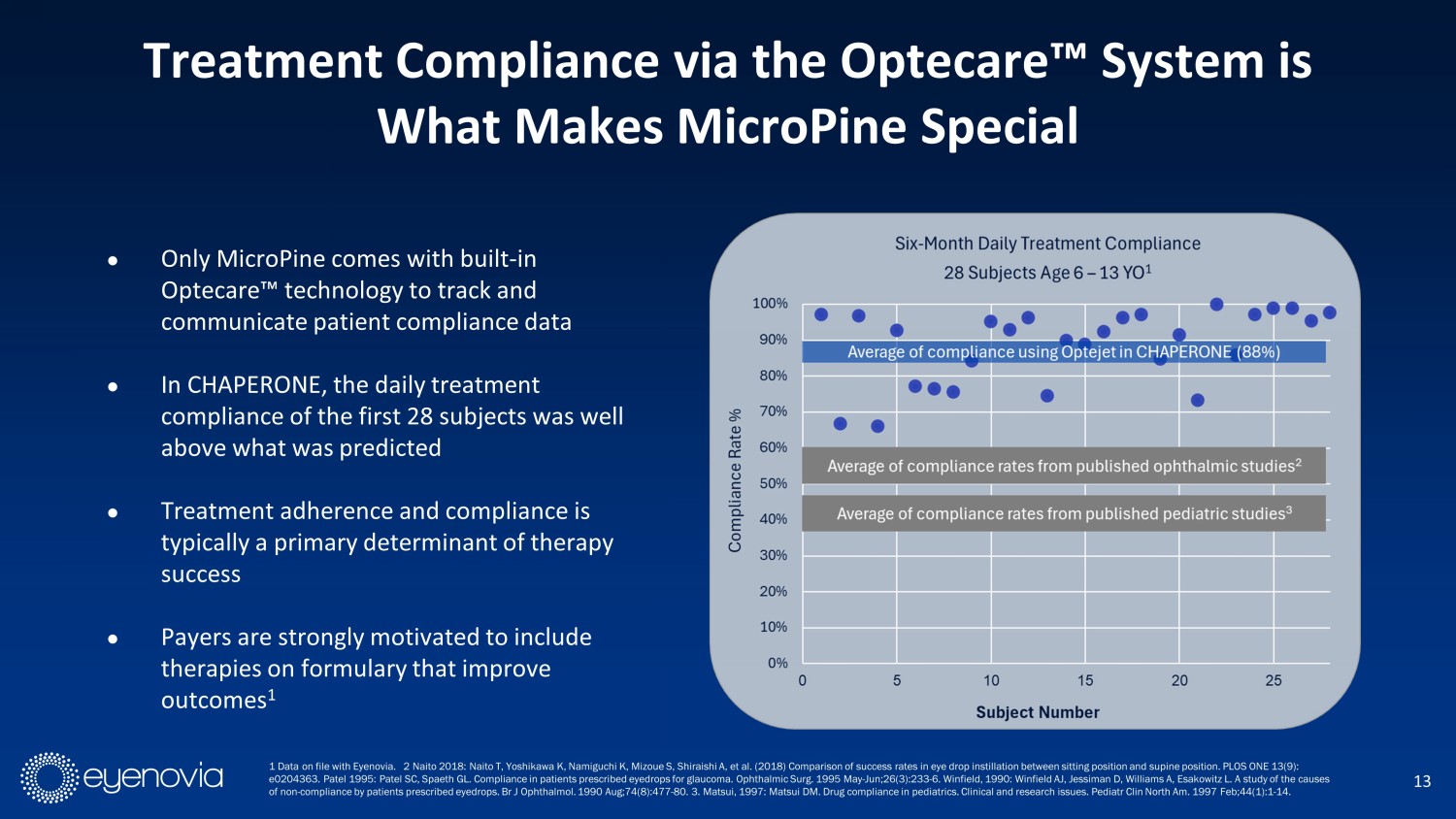
只有MicroPine配備了內置的Optecare P技術,以跟蹤和傳達患者依從性數據;在CHAPERONE中,前28名患者的每日治療依從性遠高於預期;治療依從性通常是治療成功的主要決定因素;賠付人強烈動力要將改善結果的治療方法納入目錄中。

可能的頂峯銷售額超過十億美元2027年2028年2029年2030年2031年2032年2033年2034年2035年2036年潛在用户數500萬505萬1.005萬4.008萬5.203.020 525萬255.0505.307.6015.360.6775478.2845.468.426概括的市場份額0.5%1%2%4%6%7%8%9%10%10%墨盒數量150,000 375,000937,5001,640,6252,460,9383,076,1723,537,598 4,068,2374,678,4735,380,244產品價格(淨減折扣)200.00美元200.00美元200.00美元200.00美元200.00美元200.00美元200.00美元200.00美元200.00美元200.00美元總營銷額3000萬美元7500萬美元187.5億美元3.28億美元4.92億美元6.1523.437.52億美元8.1364.746.80億美元10.7604.88億美元假設-潛在用户基於美國高風險兒童的數量。-每月400美元的淨價格減免多達50%(眼科學領域新產品的典型營銷比例)-每年每位患者八個墨盒(墨盒延伸)-基礎可以以可能建立實踐的成本向醫生出售。
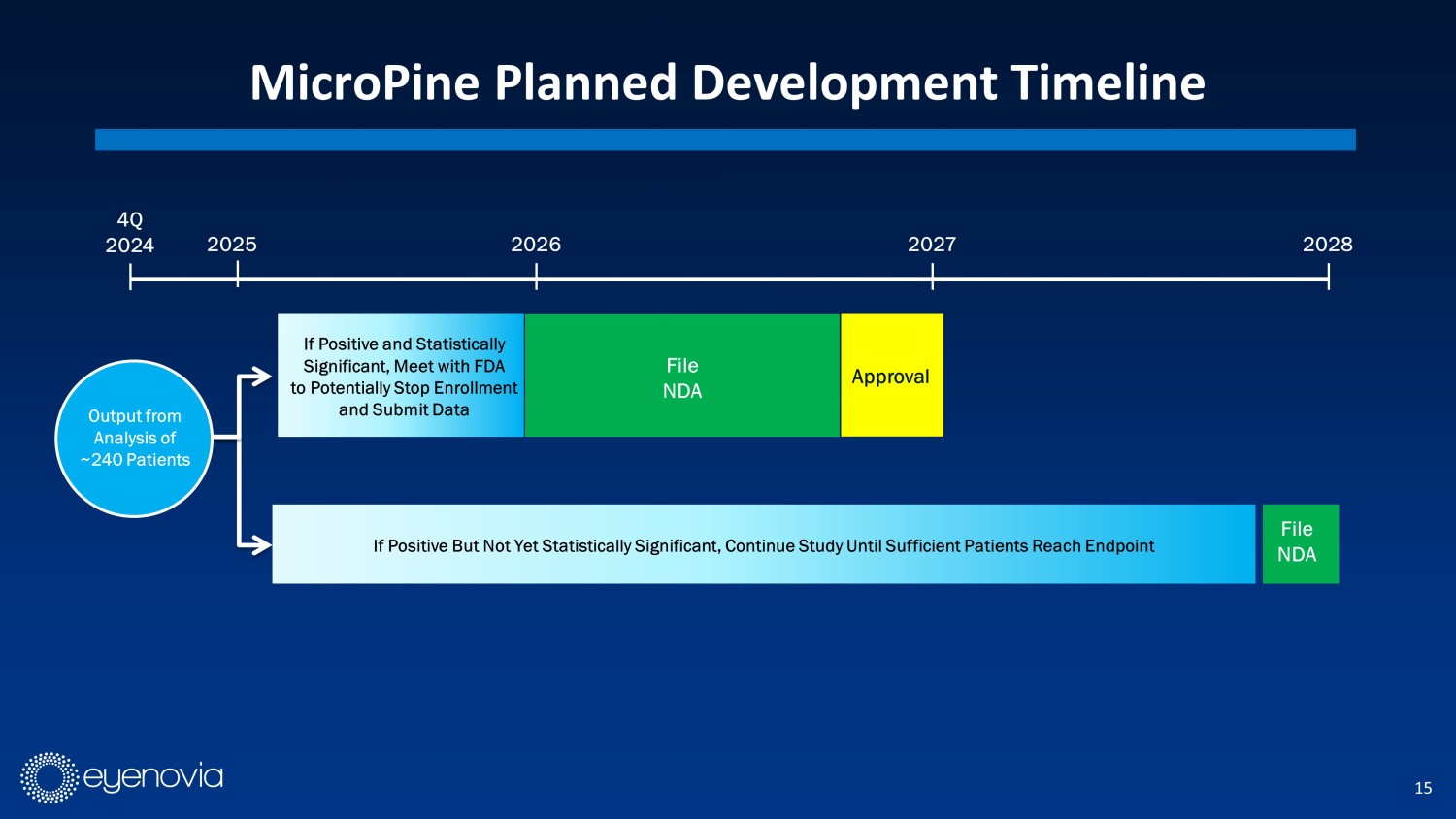
MicroPine計劃的發展時間表2024年2026年2027年2028年2025年如果積極但尚未達到統計顯著性,請繼續研究,直到足夠數量的患者到達終點;提交新藥申請(NDA)提交新藥申請(NDA)如果結果積極且具有統計顯著性,請會見FDA,以潛在停止入組並提交數據分析的數據端點

Optejet®數字眼科計量噴霧裝置是唯一獲FDA批准的眼科數字藥物遞送平臺,將於2024年6月發佈。

旨在解決使用便捷性和劑量精度問題,同時提高療效,減少副作用,並減少成本,特別是數字Optecare capabilities2 Optejet®與微劑陣列印刷技術相似的技術,以“印刷”藥物的微滴到眼睛上,並且使用四分之一的傳統滴眼劑劑量以保持療效和最小限度的耐受性問題。

Optejet®由可更換的墨盒(COGS為20美元)和耐用基座組成,該噴頭有109個激光鑽孔口、快門激活按鈕、人體工程學設計和由Eyenovia製造的專有預充藥物墨盒。 Optejet的使用技術類似於噴墨打印機,使用微藥滴印刷技術將藥物的微滴“印刷”到眼睛上,每次使用的劑量為傳統眼藥水的四分之一,以保持療效,最小化耐受性問題。

人體工程學設計改善了易用性,水平傳遞,壓鍵計量和無突出尖頭;使用滴眼瓶的治療需要頭部傾斜,而擠壓和依靠重力,滴眼瓶的尖端可能會觸及患者的眼睛表面並滴下藥物,而Optejet的使用可以水平地進行,並通過按鈕進行操作,具有減少交叉污染的遮擋噴嘴。

經過 20 次設備全面測試,確保藥品輸送無菌。結果:使用 1x10 6 微生物生長挑戰協議,Optejet滿足了通過標準。•所有測試單元在 28 天模擬使用期間均未顯示生長•所有陽性對照單元顯示生長•所有陰性對照單元未顯示生長Whitcomb, J. & Lam, P. (2023 年 10 月 11-14 日)。演示多劑型眼科醫療噴霧藥品設備微生物完整性。美國驗光學會,新奧爾良,LA,美國。
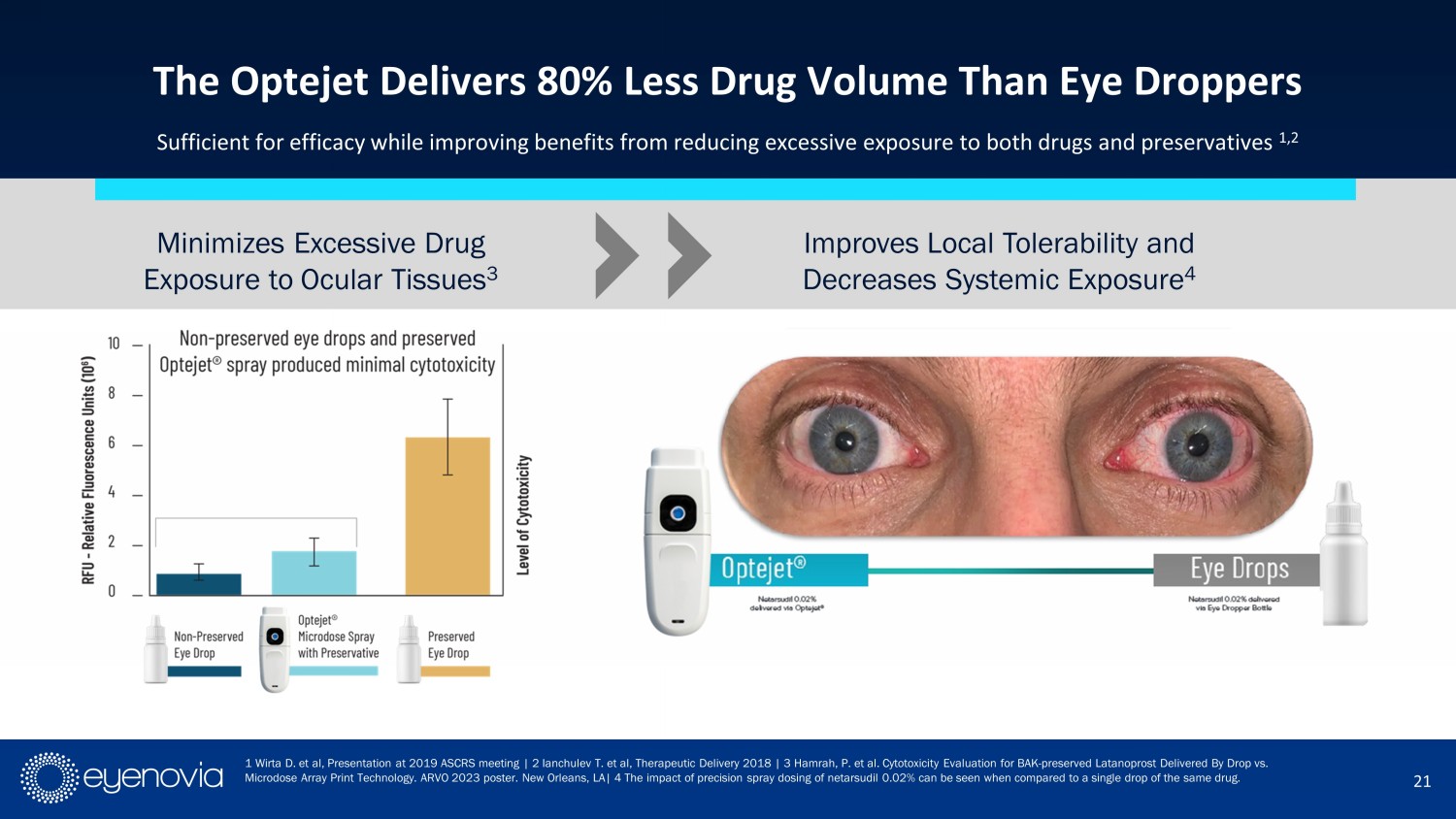
Optejet 比眼滴少使用 80% 的藥物劑量,足以保證療效,同時通過減少對藥物和防腐劑的過度暴露來提高益處。1、2 1 Wirta D. 等,2019 ASCRS 會議演示|2 Ianchulev T. 等,Therapeutic Delivery 2018 |3 Hamrah,P. 等人。通過滴眼和微劑量陣列印刷技術提供 BAK-保存的拉坦前列素的細胞毒性評估。ARVO 2023 年海報。新奧爾良,LA |4 通過與同種藥物的單次滴眼劑量相比較,微量的 netarsudil 0.02% 的噴霧劑量調節也會減少給藥局部的耐受性不良反應和減輕全身曝露4,減小藥物過度暴露給眼部組織3,當耐受性不良時,患者很有可能停止服藥或向眼科醫生施加壓力以更改其治療 5 3 4

Optejet 數字技術是 Optecare ΡOptejet® 能夠自動跟蹤使用OPTECARE:各利益相關者的多重利益患者•提醒服藥•能夠跟蹤遵守情況•品牌特定鼓勵的機會•可以通過應用程序訂閲服務賺錢醫生•更快行動,更準確的數據•計費的機會:CPT 編碼(98980)用於月度遵從數據檢查支付者•節省成本:如果遵守情況是問題,就不太可能讓患者使用第二種藥物•更好的結果:服藥遵從性已被證明可以減緩疾病進展1 Shu YH 等人。在開放性青光眼的階段性藥物飲用和視野發展中,載體醫學2021
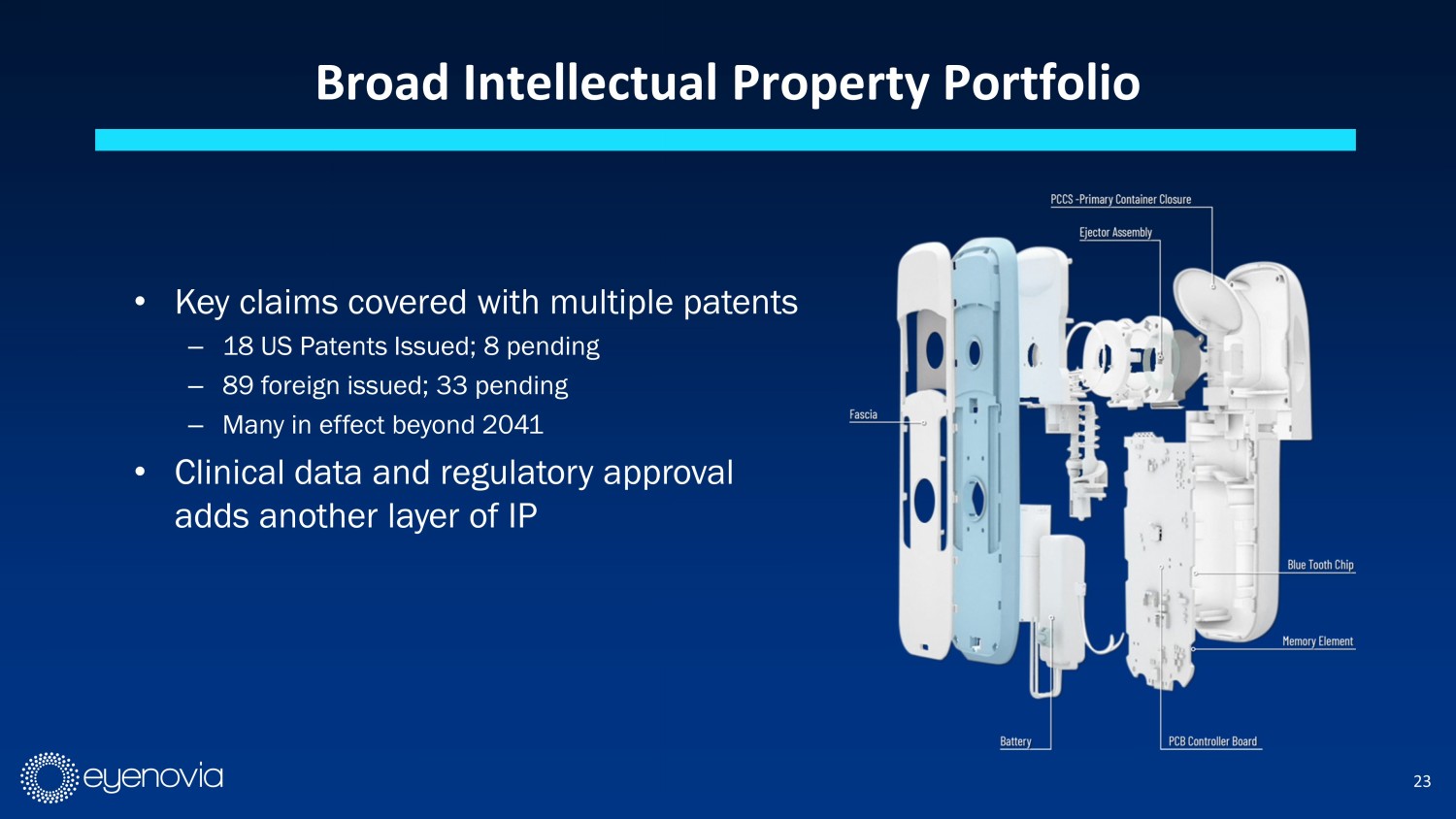
寬廣的知識產權組合•關鍵主張由多個專利覆蓋-18 項美國專利已頒佈;8項未決-89項外國已頒佈;33未決-許多超過2041年有效•臨牀數據和監管批准增加了另一層知識產權
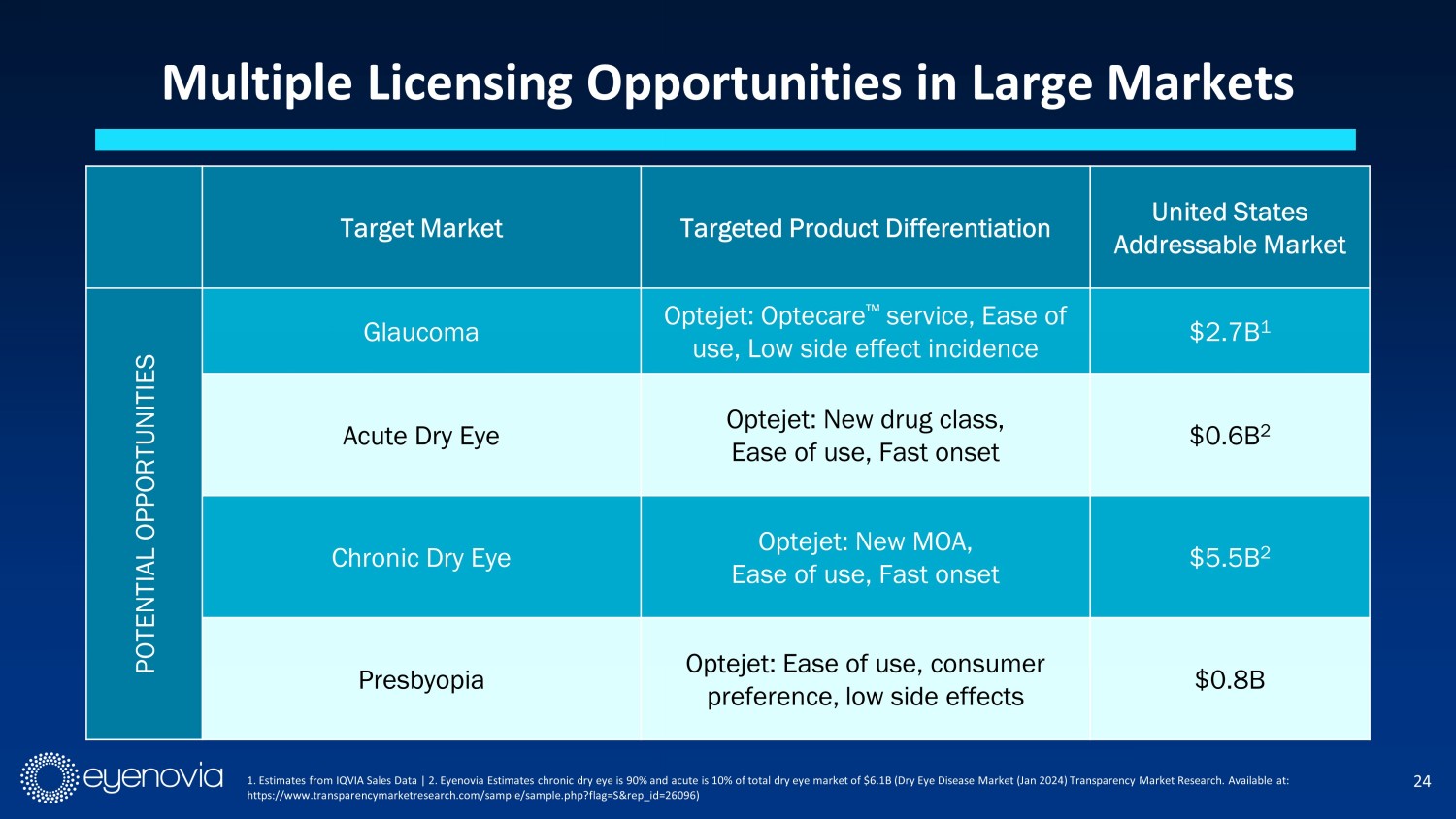
在大型市場上有多個許可證機會1.根據 IQVIA 銷售數據估計|2.Eyenovia 估計慢性乾眼症佔乾眼症總市場的 90% ,急性乾眼症佔 10% ,市場規模為 61 億美元。(Jan 2024 年)透明市場研究。https://www.transparencymarketresearch.com/sample/sample.php?flag=S&rep_id=26096)目標市場目標產品差異化美國可解決的市場潛力青光眼Optejet:Optecare Œ服務,使用方便,副作用低27 億美元1 急性乾眼症Optejet:新的藥物類別,使用方便,快速起效6億美元2 慢性乾眼症Optejet:新的 MOA,使用方便,快速起效550億美元2老視Optejet:使用方便,消費者偏好,副作用低8億美元
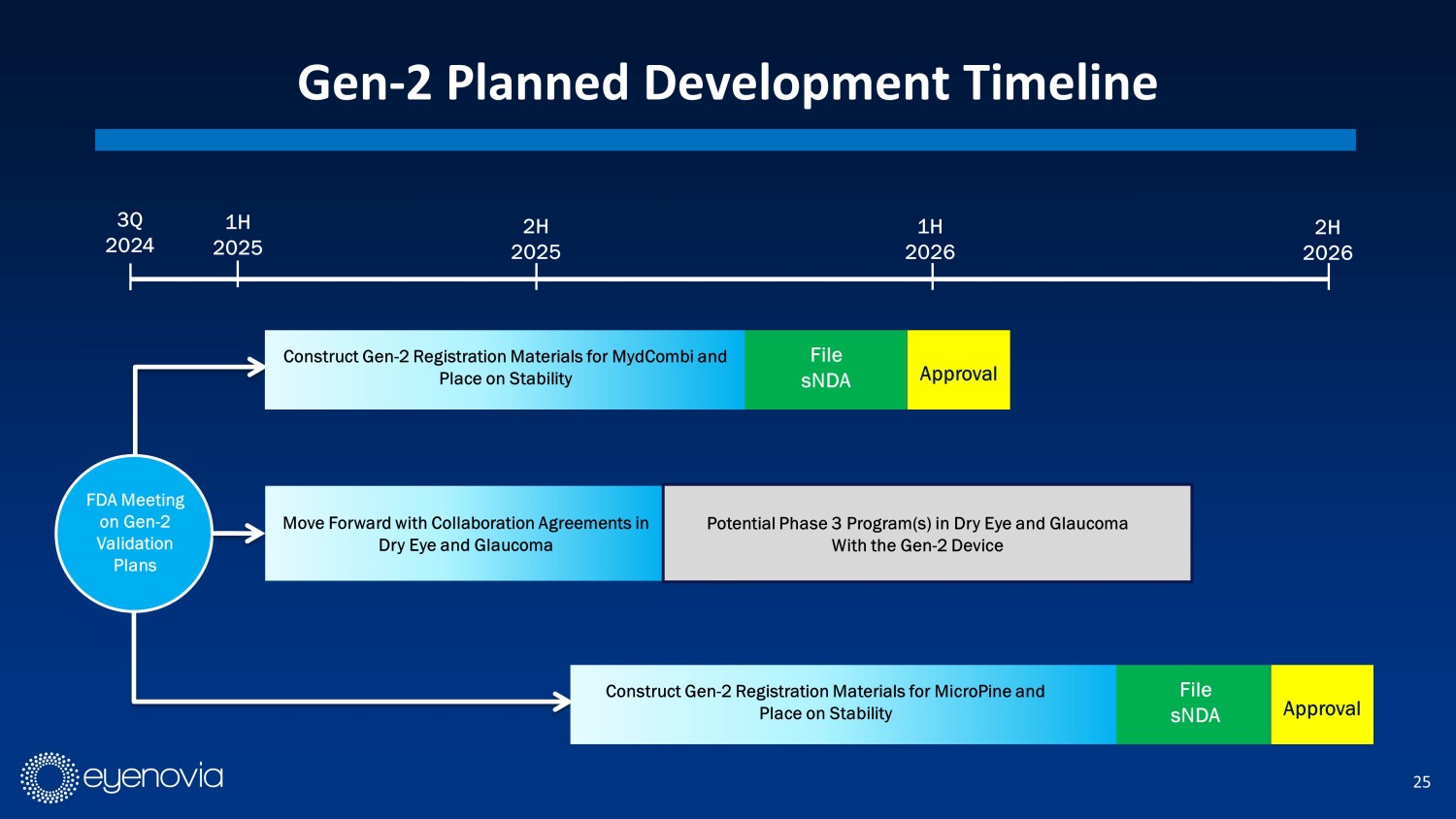
第二代規劃開發時間表第三季度20244 第二個詳細資料微劑聯合我的康比,放在穩定文件中的 2H 20251H 2026 2H2026 1H2025使用 Gen-2 設備構造註冊材料在乾眼症和青光眼中前進合作協議的 sNDAFDA 會議對 Gen -2 進行驗證計劃批准乾眼症和青光眼的第三期計劃

Clobetasol Propionate Ophthalmic Suspension 0.05% 獲FDA批准,用於治療眼科手術後的炎症和疼痛。本演示不是關於可的鬆丙酸酯的廣告。

安全信息重要的安全信息:0.05%的醋酸氯倍他索滴眼液適用於眼部手術後的炎症和疼痛治療。禁忌症:角膜和結膜的大多數活動性病毒性疾病,包括上皮性單純皰疹角膜炎(樹突狀角膜炎),牛痘和水痘,以及眼炎桿菌感染和眼部結構的真菌病。警告和注意事項:眼壓增高:皮質類固醇的長期使用可能導致青光眼,損害視神經,在視力和視野方面出現缺陷。在青光眼存在的情況下應小心使用類固醇。如果該產品使用 10 天或更長時間,則應監測眼壓。白內障:皮質類固醇的長期使用可能導致後囊下玻璃體混濁的白內障形成。延遲癒合:青光眼手術後使用類固醇可能會延遲癒合,增加脈絡膜皰疹的發生率和造成絲狀隆起的頻率。角膜和鞏膜融化:在那些引起角膜或鞏膜變薄的疾病中,使用局部類固醇的過程中已知發生穿孔。醫生應該在放大幫助下以像狹縫燈生物顯微鏡檢查患者並在適當情況下進行熒光素染色後才能進行初始處方和續方。細菌感染:激素的長期使用可能抑制宿主反應,從而增加眼部二次感染的危險。在急性化膿性情況下,類固醇可能掩蓋感染或增強現有感染。如果症狀和體徵在兩天後未改善,則應重新評估患者。病毒感染:用皮質類固醇治療有單純皰疹病毒史的患者需要極度小心。使用眼科類固醇可能延長眼部病毒感染(包括單純皰疹病毒)的病程並加重其嚴重程度。真菌感染:角膜的真菌感染尤其容易在長期局部應用類固醇的同時發生。在使用或使用類固醇的情況下持續存在的任何持久性角膜潰瘍中都必須考慮到真菌入侵。在適當時應進行真菌培養。不良反應:在接受醋酸氯倍他索滴眼液 0.05% 的臨牀研究中,發生在≥1% 受試者眼部的不良反應包括眼部炎症(2%),角膜水腫(2%),前房炎症(2%),囊性黃斑水腫(2%),眼內壓增高(1%),畏光(1%)和玻璃體脱離(1%)。其中許多反應可能是手術過程的結果。請參閲 CLOBETASOLBID.COM 的完整處方信息

預計為 Optejet 項目提供短期營收28年眼科學第一道新類固醇閾15醫生現在可以使用具有優越特性的已經很好描述的類固醇 * https://www.formosapharma.com/technology/ Clobetasol Propionate Ophthalmic Suspension 0.05%,雙重,有效地減輕疼痛和減少炎症,安全耐受,眼壓波動低,患者使用便捷,每日兩次,受到專利保護 APNT* Science 可以為所有患者提供保證的訪問權限不考慮他們的保險狀況CD11

29 Clobetasol 利用 APNT * 技術 * https://www.formosapharma.com/technology/ Clobetasol Propionate Ophthalmic Suspension 0.05%,BID 活性成分與鹽和糖一起磨細到納米粒度,主動製藥納米技術:增加溶解度•穩定的優異分散性增加生物利用度Clobetasol Propionate 不需要搖動其他類固醇
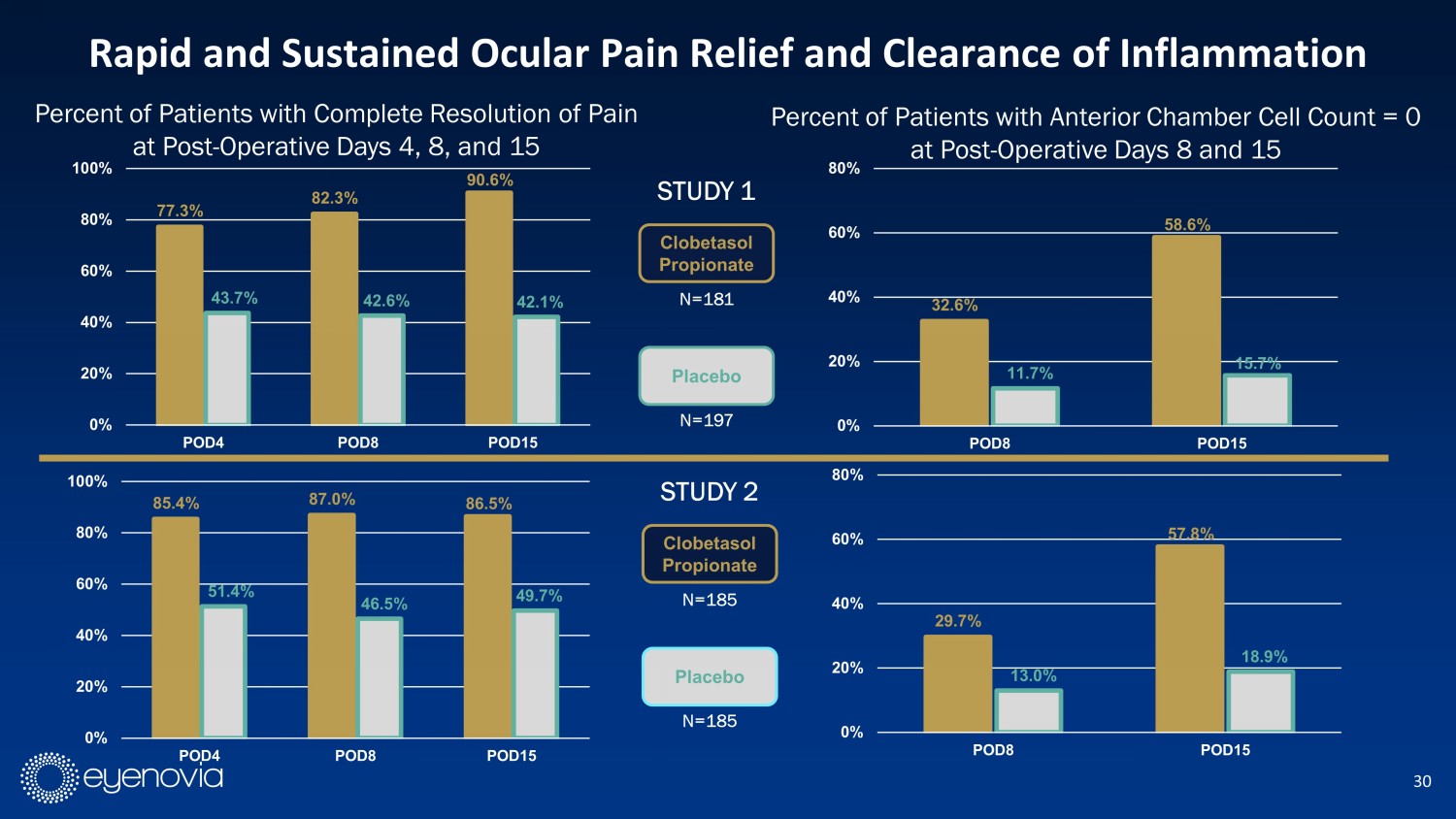
30 77.3% 82.3% 90.6% 43.7% 42.6% 42.1% 0% 20% 40% 60% 80% 100% 所有板塊4天、8天和15天的手術後痛苦完全消失患者的百分比 85.4% 87.0% 86.5% 51.4% 46.5% 49.7% 0% 20% 40% 60% 80% 100% 所有板塊8和15天的手術後前房細胞計數為0的患者百分比 32.6% 58.6% 11.7% 15.7% 0% 20% 40% 60% 80% 所有板塊8和15天的手術後前房細胞計數為0的患者百分比 29.7% 57.8% 13.0% 18.9% 0% 20% 40% 60% 80% 賽富時普羅匹酮鹽安慰劑n=181 n=197 研究1 賽富時普羅匹酮鹽安慰劑n=185 n=185 研究2
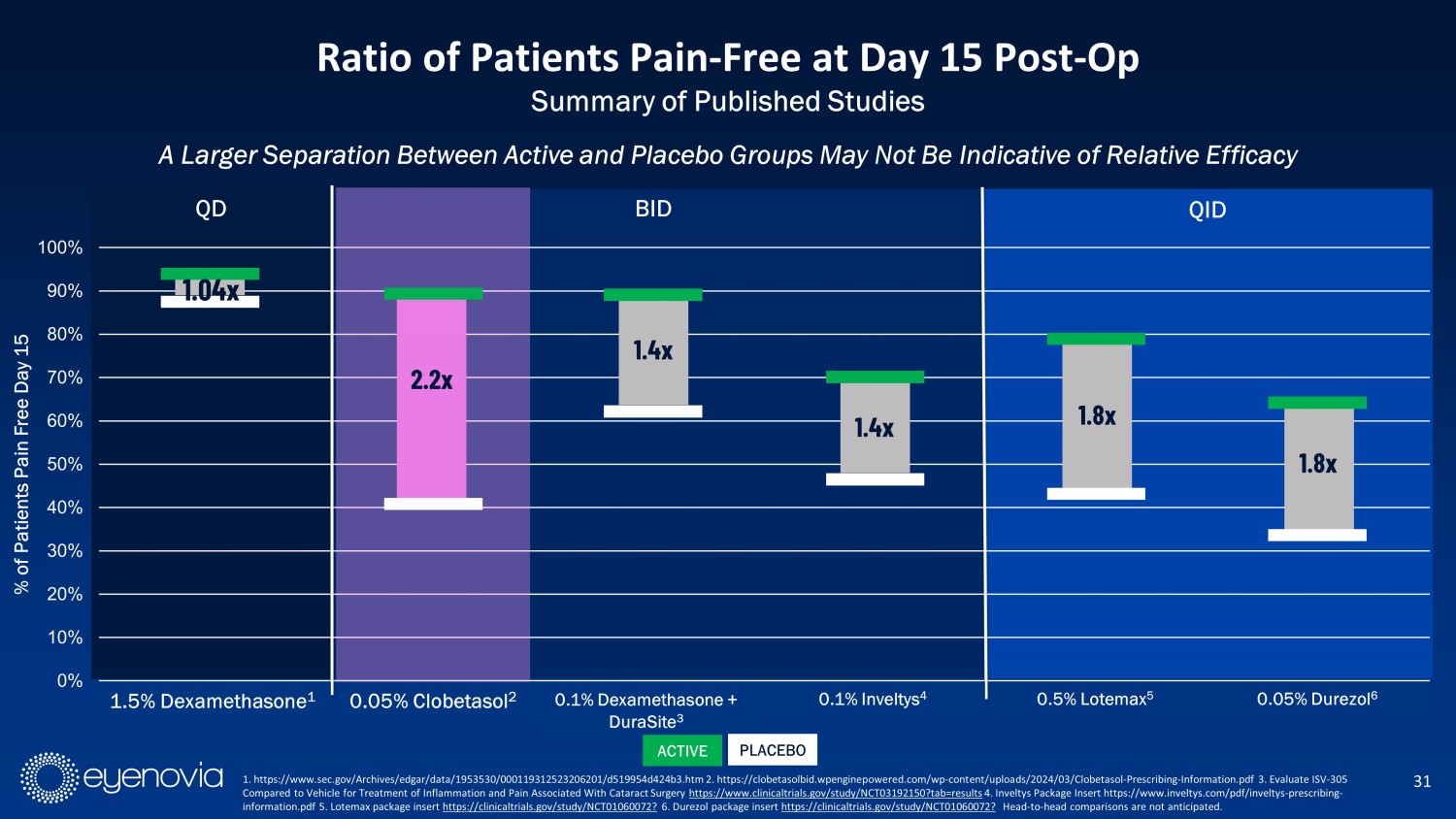
0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100% 1.5%地塞米松0.05%氯倍他索0.1%地塞米松+DuraSite0.1% Inveltys0.5% Lotemax 0.05% Durezol疼痛完全消失的患者百分比15天活躍和安慰劑組之間的更大分離可能不代表相對功效 31 在手術後第15天沒有發炎的患者比例 所有板塊 QD QID 2.2 x 1.4x 1.8 x 1.4 x 1.8 x 0.05%氯倍他索 2 0.1%地塞米松+DuraSite 3 0.1%Inveltys 4 0.5%Lotemax 5 0.05% Durezol 6 BID 1. https://www.sec.gov/Archives/edgar/data/1953530/000119312523206201/d519954d424b3.htm 2. https://clobetasolbid.wpenginepowered.com/wp-content/uploads/2024/03/Clobetasol-Prescribing-Information.pdf 3. 評估ISV-305與針對與白內障手術相關的炎症和疼痛的車輛相比較 https://clinicaltrials.gov/study/NCT03192150?tab=results 4. Inveltys包裝插入 https://www.inveltys.com/pdf/inveltys-prescribing-information.pdf 5. Lotemax包裝説明書 https://clinicaltrials.gov/study/NCT01060072? 6. Durezol包裝説明書 https://clinicaltrials.gov/study/NCT01060072? 不預期面對面的比較 1.04x 1.5%地塞米松 1活性安慰劑
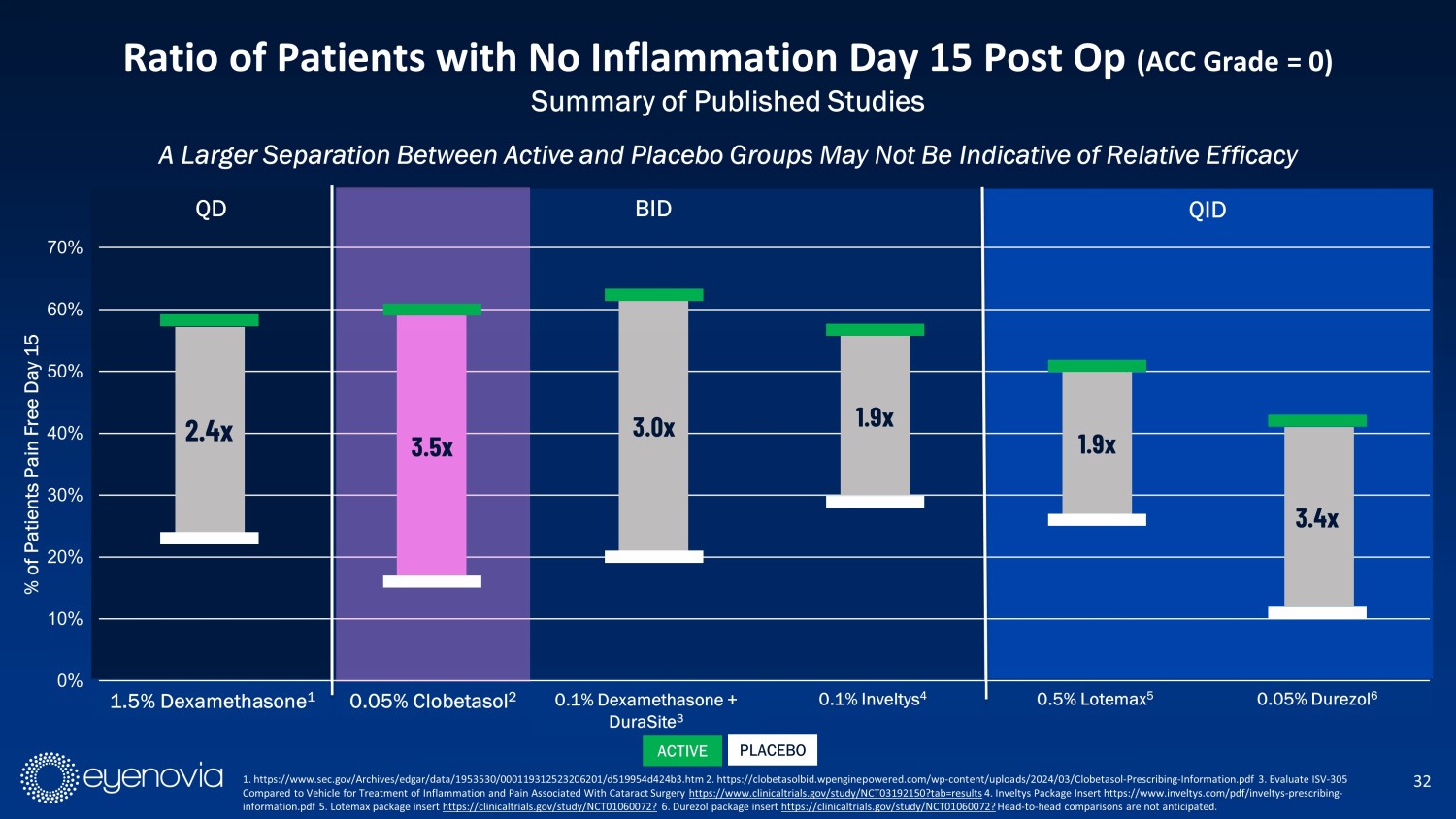
0% 10% 20% 30% 40% 50% 60% 70% 1.5%地塞米松0.05%氯倍他索1 0.1%地塞米松+DuraSite 2 0.1%Inveltys 3 0.5%Lotemax 4 0.05% Durezol 5 疼痛完全消失的患者百分比15天活躍和安慰劑組之間的更大分離可能不代表相對功效 32 在發表研究的情況下手術後第15天沒有炎症的患者比例(ACC級別= 0) 所有板塊 QD QID 3.5x 3.0x 1.9x 1.9x 3.4x 0.05%氯倍他索2 0.1%地塞米松+DuraSite 3 0.1%Inveltys 4 0.5%Lotemax 5 0.05% Durezol 6 BID 1. https://www.sec.gov/Archives/edgar/data/1953530/000119312523206201/d519954d424b3.htm 2. https://clobetasolbid.wpenginepowered.com/wp-content/uploads/2024/03/Clobetasol-Prescribing-Information.pdf 3.評估ISV-305與針對與白內障手術相關的炎症和疼痛的車輛相比較https://clinicaltrials.gov/study/NCT03192150?tab=results 4. Inveltys包裝插入 https://www.inveltys.com/pdf/inveltys-prescribing-information.pdf 5. Lotemax包裝説明書https://clinicaltrials.gov/study/NCT01060072? 6. Durezol包裝説明書 https://clinicaltrials.gov/study/NCT01060072? 不預期面對面的比較 2.4x 1.5%地塞米松1活性安慰劑

33 1. https://clobetasolbid.wpenginepowered.com/wp-content/uploads/2024/03/Clobetasol-Prescribing-Information.pdf Clobetasol低不良反應率,所有反應均在2%或更少的患者中發生;許多這些反應可能是手術程序的後果 *眼睛炎症(2%)*角膜水腫(2%)*前房炎症(2%)*囊性黃斑水腫(2%)*眼內壓升高(1%)*光噁心(1%)*玻璃體脱離(1%)

●NovaBay和Eyenovia共同推廣Avenova和Clobetasol●隸屬於Eyenovia的銷售團隊將支持Clobetasol在未涵蓋的地理區域的銷售●Eyenovia將通過其銷售團隊推廣Avenova●沒有額外的促銷費用,每個公司將獲得增量銷售的比例Avenova符合Eyenovia的推廣框架,為眼科手術前後的醫生和患者提供卓越的體驗 所有板塊 NovaBay共推廣請參見NovaBay.com和Eyenovia.com。 術前 術後 ●清潔眼瞼和睫毛●殺死大多數病原菌●衞生擴張(無觸)●有效且耐受●眼科領域的新類固醇疼痛和炎症藥物●療效顯著且耐受●每天兩次服用●清潔眼瞼和睫毛●殺死大多數病原菌Avenova Clobetasol MydCombi Avenova

MydCombi Ρ眼科噴霧劑(1%託品酰胺和2.5%苯腎上腺素)經FDA批准供辦公室或手術前短期瞳孔擴張使用35此演示文稿不是MYDCOMBI的廣告。

安全信息重要的安全信息:MYDCOMBI(託品酰胺和苯腎上腺素氫溴酸鹽眼科噴霧劑)1%/2.5%適用於誘導常規診斷程序的瞳孔擴大和短暫期望瞳孔擴大的情況。禁忌症:對配方中任何成分已知過敏。警告和注意事項:用於局部眼科用途。不適用於注射。此製劑可能會引起兒童中的中樞神經系統紊亂,可能很危險。應考慮由於對抗膽鹼能藥物過敏引起的精神病反應和行為障礙的可能性。擴瞳劑可能會產生短暫的眼壓升高。已報告顯著的血壓升高。高於安慰劑的Miosis在鏡後一天報告。使用前請取下隱形眼鏡。藥物相互作用:類似於阿托品的藥物:可能會誇大腎上腺能壓力反應。膽鹼能激動劑和眼科膽鹼酯酶抑制劑:可能會干擾卡巴賈林,毛果芸香鹼或眼科膽鹼酯酶抑制劑的降壓作用。強效吸入麻醉劑:可能會增強某些吸入麻醉劑的心血管抑制作用。不良反應:最常見的眼部不良反應包括短暫的視力模糊,降低的視力,對光過敏,淺表性角膜上皮炎和輕微的眼部不適。使用擴瞳劑後已報告眼內壓升高。使用託品酰胺後已報告系統性不良反應,包括口乾,心動過速,頭痛,過敏反應,噁心,嘔吐,蒼白,中樞神經系統障礙和肌肉僵硬。請前往MYDCOMBI.com獲取完整的處方信息36

37 MydCombi Ρ 現代散瞳:一種簡單的擴大瞳孔的方法。適應症:MYDCOMBI(託吡酯1%和苯腎上腺素HCl 2.5%)眼用噴霧劑適用於日常診斷程序和需要短期擴大瞳孔的疾病。重要的安全信息:禁忌:對任何成分過敏的患者。警告和注意事項:僅供局部眼科使用。不用於注射。此製劑可能引起中樞神經系統紊亂,對兒科患者可能會產生危險。應考慮抗膽鹼能藥物過敏引起的精神病反應和行為紊亂。散瞳劑可能會引起短暫的眼壓升高。已報告有顯着的血壓升高。高血壓患者要小心。其餘的出現瞳孔收縮的情況已報告一天後使用。使用前請取下隱形眼鏡。藥物相互作用:類似阿托品的藥物可能會誇大腎上腺素的加壓反應。膽鹼能激動劑和眼科膽鹼酯酶抑制劑:可能會干擾carbachol,pilocarpine或眼科膽鹼酯酶抑制劑的降壓作用。強效吸入麻醉劑:可能會強化某些吸入麻醉劑的心血管抑制作用。不良反應:最常見的眼部不良反應包括短暫的視力模糊,視力降低,光過敏,淺表的翼狀內障和輕微的眼部不適。散瞳劑的使用後已報告過高眼壓的出現。已報告過有幹口,心動過速,頭痛,過敏反應,噁心,嘔吐,蒼白,中樞神經系統紊亂和肌肉僵硬的系統不良反應。要報告疑似不良反應,請致電Eyenovia公司1-833-393-6684或FDA1-800-FDA-1088(www.fda.gov/medwatch)www.mydcombi.com瞭解完整的處方信息。領先的擴張學藥物的唯一FDA批准的固定劑量組合和Optejet Œ的驗證交付平臺快速實現臨牀必要的擴張和可靠的時間分辨率。在臨牀研究中,耐受性良好,在患者中97%沒有副作用。將Eyenovia轉變為商業階段的公司,同時創建了一個內部銷售部門和分銷渠道,在250MM可尋址市場中為患者,醫生和技術人員引入了易於使用的藥物交付和Optejet Œ體驗。
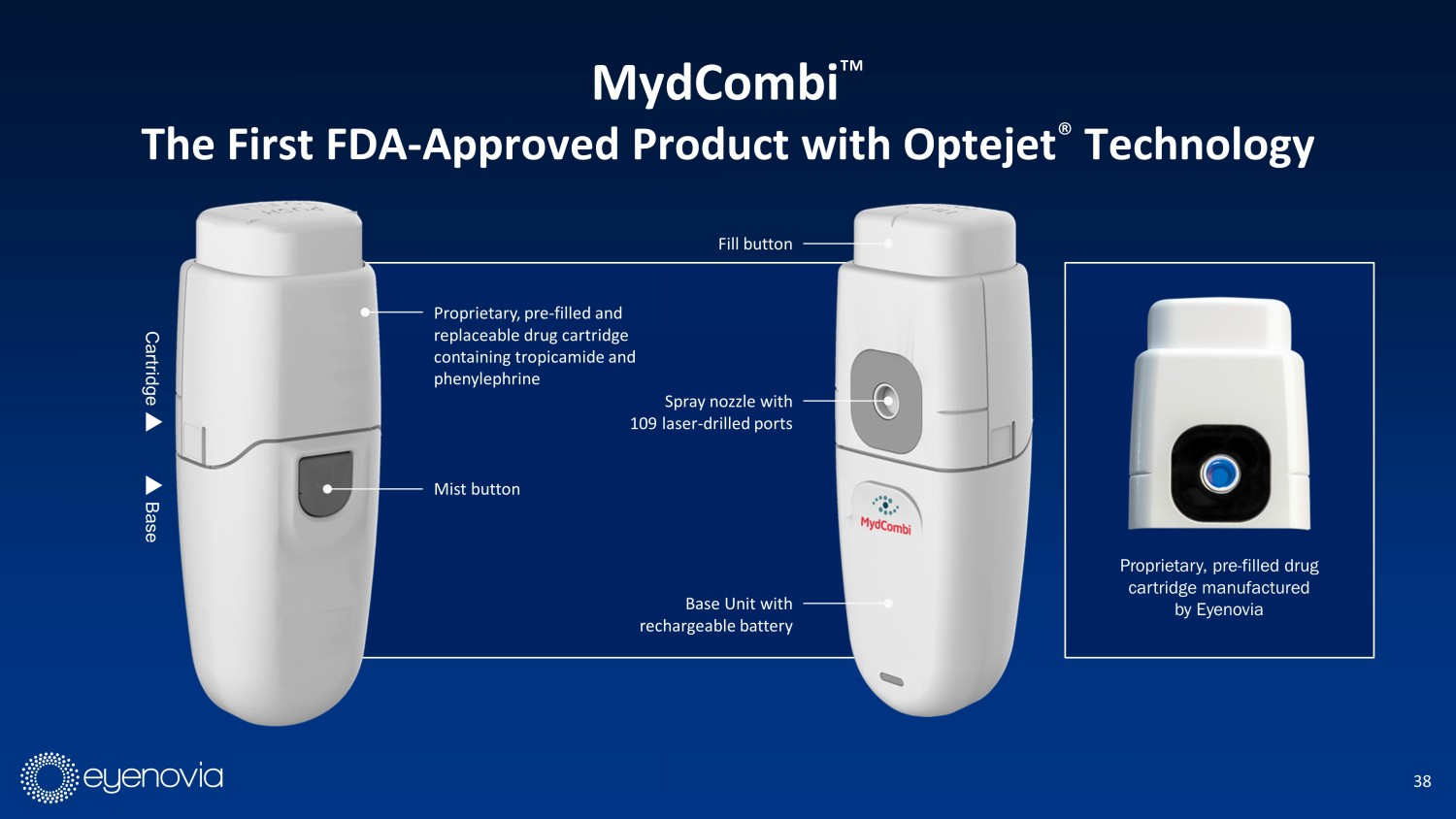
38 噴霧噴嘴,帶有109個激光鑽孔。霧化按鈕。專有的、預裝的、可更換的藥物彈藥盒,內含託吡酯和苯腎上腺素。填充按鈕。帶有可充電電池的基本單元。藥彈藥盒底部。Eyenovia製造的專有、預裝藥物彈藥盒。MydCombi Ρ是Optejet ®技術的第一款FDA批准的產品。

39 辦公室和外科瞳孔擴張市場25億美元的機會1在美國。1.每年有大約1.08億個辦公室擴大瞳孔的檢查使用製藥類散瞳劑的總銷售額為2億美元($2×100M),加上單瓶用於白內障置換手術的製藥類散瞳劑的總銷售額為5000萬美元($12.5×4M)。領先的瞳孔擴張藥物是託吡酯和苯腎上腺素,它們可以單獨或聯合使用,並以眼藥水的形式給予。在美國每年進行大約1.08億個辦公室擴大瞳孔的檢查,目前的流程存在許多缺陷:通常需要多次滴眼藥,病人會感到不適,需要花費長時間進行管理並緩慢恢復到“正常”狀態,存在交叉污染的風險。
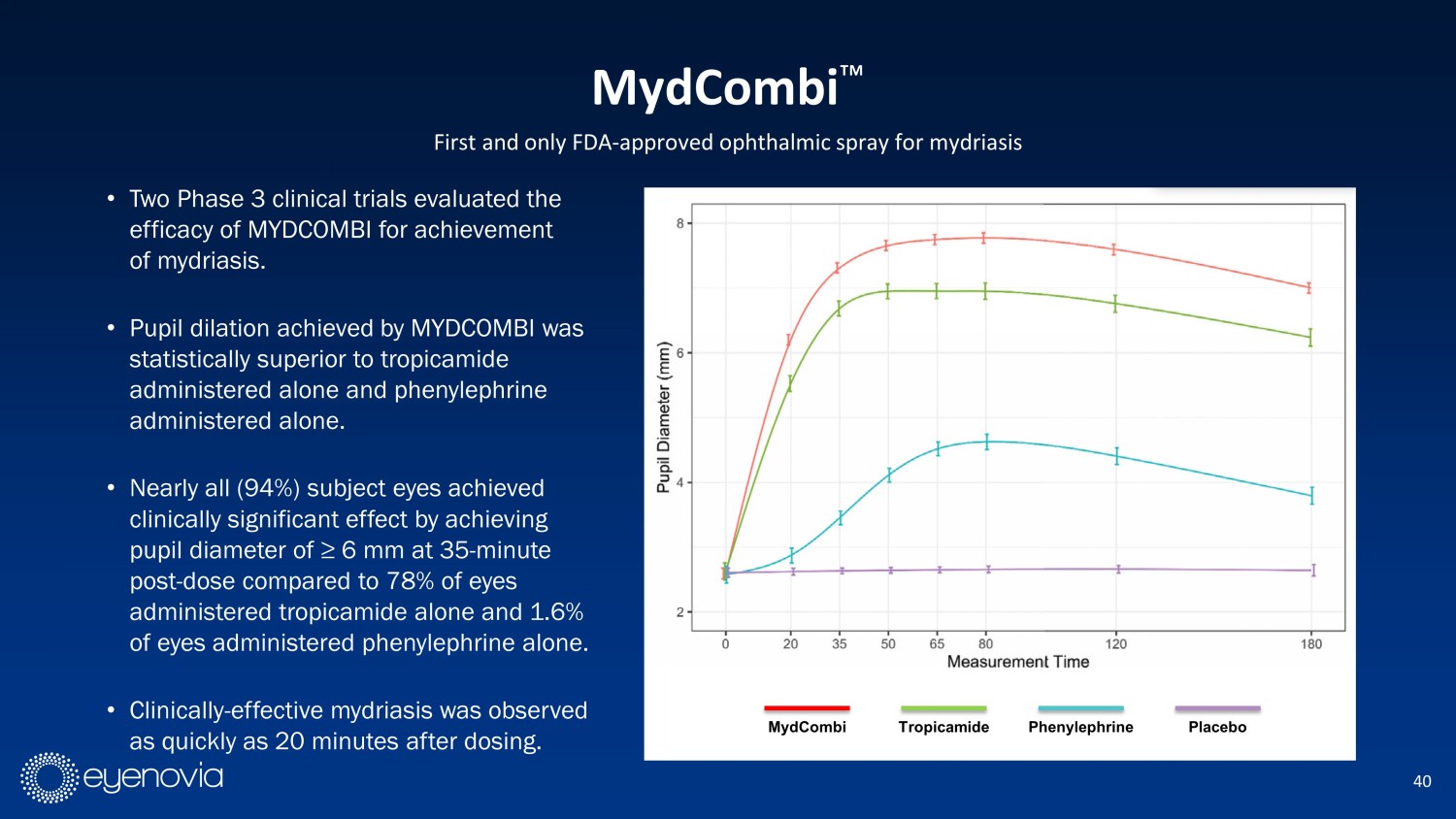
40 第一個也是唯一一個被FDA批准用於散瞳的眼科噴霧劑。兩個III期臨牀試驗評估了MYDCOMBI的療效。與單獨應用託吡酯和單獨應用苯腎上腺素相比,由MYDCOMBI引起的瞳孔擴張優於統計學。94%的受試眼球在使用後35分鐘達到了瞳孔直徑≥6毫米的臨牀顯着效果,而單獨應用託吡酯的眼球僅有78%,單獨應用苯腎上腺素的眼球僅有1.6%。在使用後20分鐘即可觀察到臨牀有效的瞳孔擴張。MydCombi Ρ MydCombi託吡酯苯腎上腺素安慰劑
41 財務快照(2024年3月)納斯達克:EYEN普通股總股本為4740萬美元。股票計劃下的股權授予為630萬美元。可轉換票據為230萬美元。認股權證為1090萬美元。完全稀釋後的股票為6690萬。現金800萬美元。債務為1560萬美元。

42 經驗豐富的領導團隊Bren Kern首席運營官Michael Rowe首席執行官John Gandolfo首席財務官Norbert Lowe商業運營副總裁Greg Bennett臨牀項目策略和發展副總裁Malini Batheja,博士藥學R&D和CMC Regulatory Enrico Brambilla器械研發和工程副總裁Lauren Gidden質量和監管事務副總裁Rob Richardson製造副總裁