

附錄 99.1《消滅癌症之旅》埃拉斯卡投資者最新消息 2024 年 5 月

免責聲明:前瞻性陳述和市場數據我們提醒您 本演示文稿包含前瞻性陳述。除本演示文稿中包含的歷史事實陳述以外的所有陳述,包括有關我們未來的經營業績和財務狀況、業務 戰略、研發計劃、預期時間(包括啟動時間和數據讀出時間)、成本、我們正在進行和計劃中的臨牀前研究和臨牀試驗的設計和實施、候選產品的潛在治療益處以及我們當前或未來的潛在益處的陳述與第三方的安排,包括與Medshine Discovery Inc. 和Joyo Pharmatech Co., Ltd.簽訂許可協議的預期收益、我們計劃和目標成功的時機和可能性、某些計劃取消優先順序的影響以及預期產品開發工作的未來結果,均為前瞻性陳述。 在某些情況下,您可以使用 “可能”、“將”、“應該”、“預期”、“計劃”、“預期”、“可能”、“打算”、 “目標”、“項目”、“考慮”、“相信”、“估計”、“預測”、“潛在” 或 “繼續” 等術語來識別前瞻性陳述,或者這些術語或其他類似術語的否定性 表達式。我們不應將納入前瞻性陳述視為我們對任何計劃將實現的陳述。由於我們的業務固有的風險和不確定性 ,實際結果可能與本演示文稿中列出的有所不同,包括但不限於:我們基於關閉 RAS/MAPK 途徑的唯一重點來發現和開發候選產品的方法,這是一種未經證實的新方法;我們對 ERAS-0015 或 ERAS-4001 開發潛力的假設在很大程度上基於許可方生成的臨牀前數據,我們可以觀察當我們進行計劃研究時,結果存在重大和不利的差異;我們只有一種產品 候選產品處於臨牀開發階段,所有其他開發工作都處於臨牀前或研發階段;我們對哪些項目可能更有可能成功的假設可能不準確,我們可能會將有限的 資源用於研究特定的候選產品和/或適應症,而未能利用具有更大開發或商業潛力的候選產品或適應症;啟動、註冊、數據讀取方面的潛在延遲,以及 完成臨牀試驗和臨牀前研究;我們在製造、研究、臨牀前和臨牀測試方面對第三方的依賴;我們的候選產品 出現意想不到的不良副作用或療效不足,這些副作用可能會限制其開發、監管批准和/或商業化,或可能導致召回或產品責任索賠;臨牀前研究或臨牀試驗的不利結果;臨牀前研究或早期 臨牀試驗的結果不一定能預測未來的結果;我們計劃中的SEACACA RAFT 試驗可能不會支持納泊非尼的註冊;無法從我們當前的許可、收購或合作中獲得任何好處, 任何未來的許可、收購或合作,以及我們履行此類安排義務的能力;美國和國外的監管發展;美國食品和藥物管理局或歐盟衞生當局的後續發展 可能與迄今為止收到的有關我們的開發計劃和試驗設計的反饋不一致;我們的獲取能力並維護知識產權保護為我們的候選產品提供保障,並維護我們在知識 產權許可下的權利;我們用當前的現金、現金等價物和有價證券為運營計劃提供資金的能力;以及我們先前向美國證券交易委員會(SEC)提交的文件中描述的其他風險,包括截至2023年12月31日的10-K表年度報告中 “風險因素” 標題下的風險,以及隨後向美國證券交易委員會提交的任何文件。提醒您不要過分依賴這些前瞻性陳述,截至本文發佈之日,這些陳述僅代表了 ,我們沒有義務更新此類陳述以反映在本聲明發布之日之後發生的事件或存在的情況。所有前瞻性陳述均受這份警告 聲明的全部限制,該聲明是根據1995年《私人證券訴訟改革法》的安全港條款作出的。本演示文稿還包含獨立方和我們提供的與市場規模和 增長相關的估計和其他統計數據以及有關我們行業的其他數據。這些數據涉及許多假設,請您不要過分重視此類估計。此外,對我們的未來表現以及我們經營所在市場的未來 表現的預測、假設和估計必然受到高度的不確定性和風險的影響。這些因素和其他因素可能導致結果與獨立方 和我們的估計結果存在重大差異。2

今天更新的重點我們的使命是我們的使命:消滅癌症 1 願景有朝一日作為全球領先的腫瘤公司每年消滅至少10萬名患者的癌症經驗豐富的領導團隊和SAB有着連環成功的記錄 • 由Jonathan Lim和Kevan Shokat博士圍繞 顛覆性想法創立,旨在瞄準RAS •由RAS/MAPK途徑領先先驅組成的世界級科學顧問委員會 • 在全球有效規劃和執行方面擁有豐富經驗的團隊臨牀試驗業界領先的研發渠道專注於 關閉 RAS/MAPK 途徑 • Naporafenib pan-RAFI 具有同類首創 (FIC) 潛力,可快速獲得 RAS Q61X 實體瘤和其他 RAS/MAPK 靶向藥物中的 nRasm 黑色素瘤和 FIC 潛力 • ERAS-0015 pan-RAS 分子膠在克拉斯實體瘤中具有 FIC 潛力 • 在 Krasm 實體瘤中具有 FIC 潛力的 ERAS-4001 pan-KRASI 財務狀況良好,具有高質量投資者基礎和行業知名度 2 • 3.34億美元現金,現金 等價物和有價證券 • Fierce Biotech 2021 年 “Fierce 15” 最有前途的生物技術公司之一 CNS =中樞神經系統 1 截至2024年3月31日未經審計(包括2024年3月27日公佈的股權融資 淨收益4,370萬美元 ),按無病存活率(輔助設置)和無進展存活率(轉移設置)衡量的 2 未經審計(包括2024年3月27日公佈的4,370萬美元股權融資 淨收益)3

Erasca 投資者更新議程 ERAS-0015:pan-RAS 分子膠水 靶向 RAS 的特許經營權 ERAS-4001:Pan-KRAS 抑制劑管道和資源優先順序企業最新動態關鍵里程碑和臨牀試驗讀物問答環節 4

針對 RAS 的特許經營權
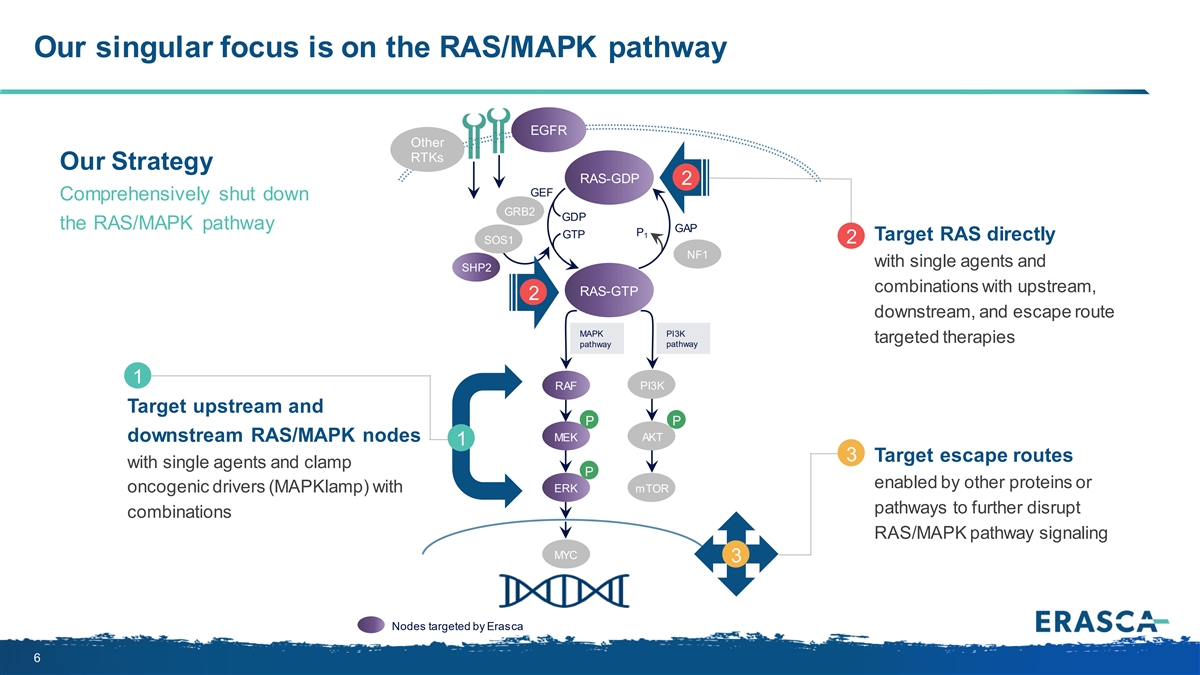
我們的唯一重點是 RAS/MAPK 途徑 EGFR 其他 RTK 我們的 戰略 RAS-GDP 2 GEF 全面關閉 GRB2 GDP RAS/MAPK 途徑 GAP P GTP 1 直接靶向 RAS SOS1 2 NF1 使用單一藥物和 SHP2 組合與上游、下游 RAS-GTP 2 和逃脱途徑 PI3K MAPK 靶向療法 途徑 1 RAF PI3K 靶向上遊和 P P MEK AKT 下游 RAS/MAPK 節點 1 3 使用單一藥物靶向逃逸路線,使用 ERK mTOR 通路通過其他蛋白質或致癌驅動因素 (MapKLamp) 抑制 P,進一步破壞 組合 RAS/MAPK 通路信號 Erasca 6 所針對的 MYC 3 節點
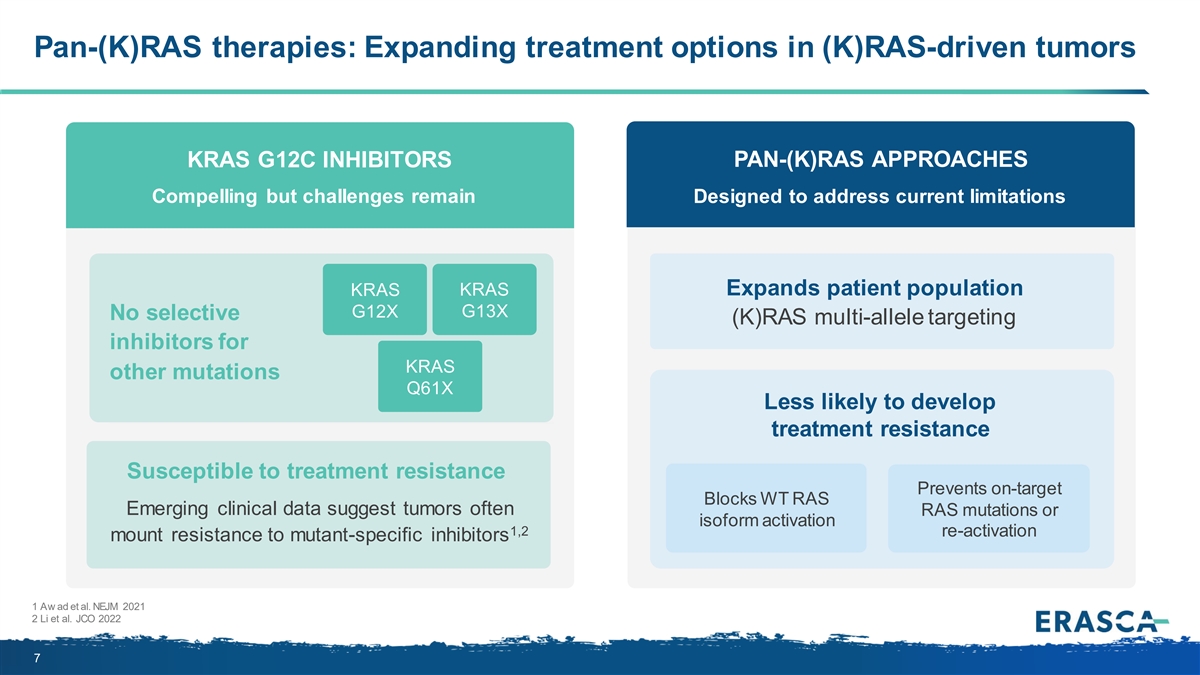
Pan-(K) RAS 療法:擴大 (K) RAS 驅動的 腫瘤的治療選擇 KRAS G12C 抑制劑 PAN-(K) RAS 方法引人注目但挑戰仍然存在旨在解決當前侷限性擴大患者羣體 KRAS KRAS G12X G13X 針對 KRAS 其他突變的無選擇性 (K) RAS 多等位基因靶向抑制劑 Q61X 不太可能產生治療耐藥性不易受治療耐藥性影響 target Blocks WT RAS 新興臨牀數據表明,腫瘤通常是 RAS 突變或亞型激活 1,2 再激活對 突變體的耐藥性-特異性抑制劑 1 Aw 等人NEJM 2021 2 Li 等人JCO 2022 7
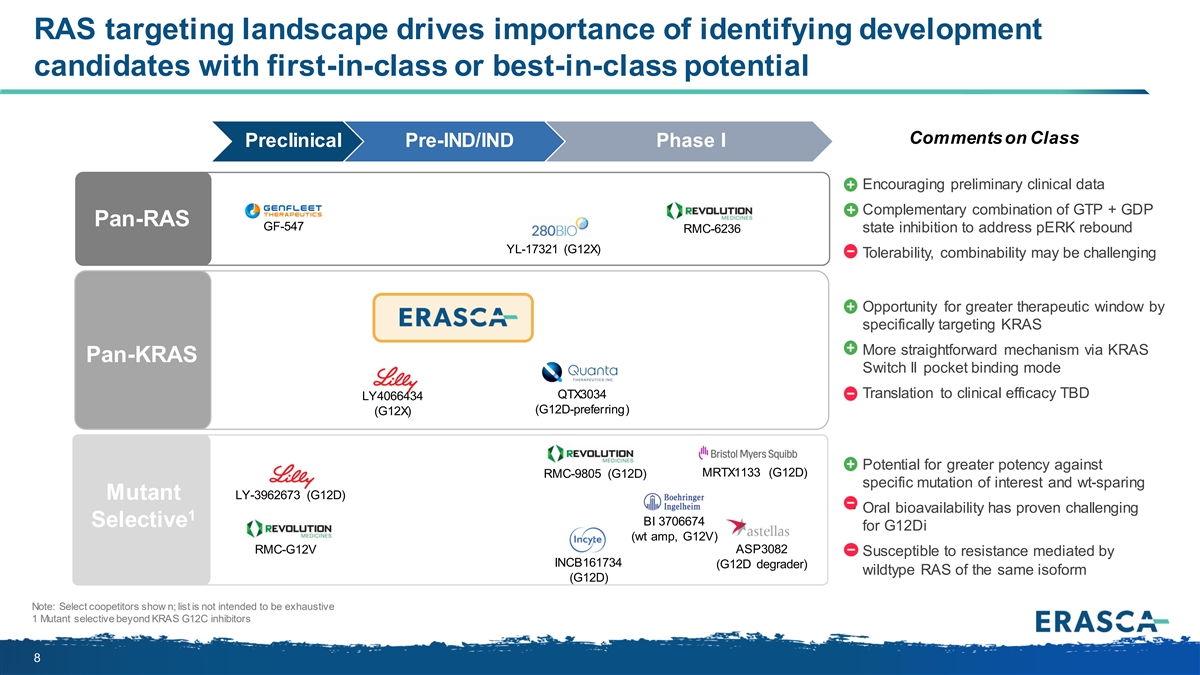
RAS 靶向格局推動了確定具有同類首創或同類最佳潛力的開發 候選藥物的重要性 • 對該類臨牀前臨牀前 IND/IND I 期的評論 • 令人鼓舞的初步臨牀數據 • GTP + GDP pan-RAS GF-547 RMC-6236 狀態抑制的互補組合 解決 perK 反彈 YL-17321 (G12X) • 耐受性、可組合性可能具有挑戰性 • 通過專門靶向 KRAS 來獲得更直接的機制 • 通過 KRAS Pan-更直接的機制 KRAS Switch II 口袋 綁定模式 QTX3034 •轉化為臨牀療效待定 LY4066434(首選 G12D)(G12X)• 對抗感興趣的 MRTX1133 (G12D) RMC-9805 (G12D) 特異突變和保濕突變體 LY-3962673 (G12D) • 事實證明,口服生物利用度具有挑戰性 1 BI 3706674 對於 G12Di(wt amp,G12V)的選擇性 RMC-G12V ASP3082 • 易受由 INCB161734 介導的耐藥性影響(G12D 降解劑)相同異構體的野生型 RAS(G12D)注意:選擇 合作競爭對手顯示 n;清單並非詳盡無遺 1 除 KRAS G12C 抑制劑之外的選擇性突變體 8
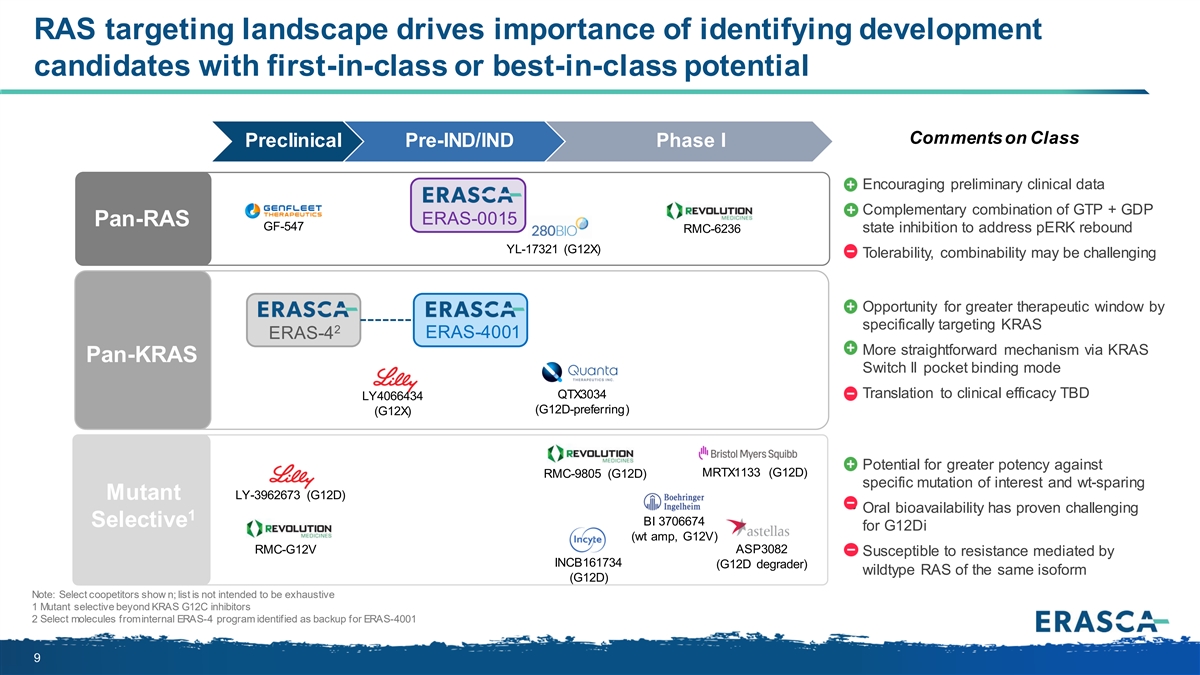
RAS 靶向格局推動了確定具有同類首創或同類最佳潛力的開發 候選藥物的重要性 • 對該類臨牀前臨牀前 IND/IND I 期的評論 • 令人鼓舞的初步臨牀數據 • GTP + GDP ERAS-0015 pan-RAS GF-547 RMC-6236 態 抑制劑的補充組合,以解決 PerK 反彈 YL-17321 (G12X) • 耐受性、可組合性可能具有挑戰性 • 通過專門靶向 KRAS 2 ERAS-4 ERAS-4001 來獲得更大治療窗口的機會 • 更直接的機制通過 KRAS Pan-KRAS Switch II 口袋結合模式 QTX3034 • 轉化為臨牀療效待定 LY4066434(首選 G12D)(G12X) • 對於 MRTX1133 (G12D) RMC-9805 (G12D) 特定突變和 保濕突變體 LY-3962673 (G12D) 具有更大效力 • 事實證明,口服生物利用度具有挑戰性 1 BI 3706674 對G12Di(wt amp,G12V)的選擇性 RMC-G12V ASP3082 由 相同同種型 (G12D) 的 INCB161734(G12D 降解劑)野型 RAS 介導。注意:精選競爭對手顯示 n;清單不打算詳盡無遺 1 個 KRAS G12C 之外的選擇性突變體抑制劑 2 從內部 ERAS-4 程序中選擇被確定為 ERAS-4001 9 備份的分子
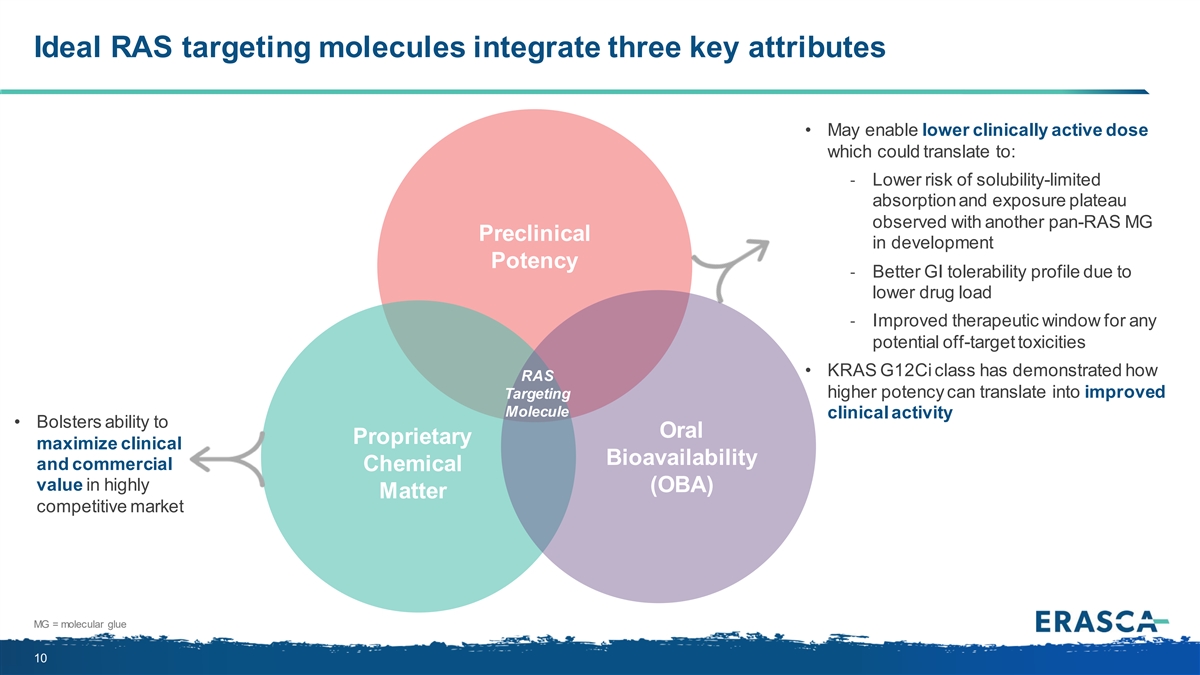
理想的 RAS 靶向分子整合了三個關鍵特性 • 可以降低臨牀活性劑量,這可能轉化為:-使用另一款 pan-RAS MG 臨牀前在研效中觀察到的溶解度受限吸收和暴露平原的風險降低-由於較低的 藥物負荷改善了胃腸道耐受性-改善了任何潛在脱靶毒性的治療窗口 • KRAS G12Ci 類已經證明 RAS 更高的效力如何轉化為臨牀靶向分子的改善活性 • 增強口服 專有最大限度的能力高度競爭的 (OBA) 物質市場中的臨牀生物利用度和商業化學價值 MG = 分子膠水 10

ERAS-0015 和 ERAS-4001 的競爭格局超過了我們的 TPP 1 2 OBA IP 臨牀前(體外和體內)效力 TPP:目標產品概況;OBA:口服生物利用度;IP:知識產權;FIC:同類首創;BIC:同類最佳;WT:wildtype;sMI:小分子抑制劑;MG:分子膠水; DC:開發候選物 1 2 3 4 體外效能由 CTG 2D 和 3D 細胞增殖測定 IC 進行評估;OBA 或口服生物利用度由 %F 評估;根據分子分佈進行預測;沒有任何專利期限調整或延期 50 11

ERAS-0015 和 ERAS-4001 的競爭特徵超過了我們的 TPP 1 2 OBA IP 臨牀前(體外和體內)效力 KRAS G12D:0.2 — 13.3 nM KRAS G12D:PK-59 CDX 小鼠的腫瘤迴歸:48% IP(物質成分、方法 KRAS G12V:0.4 — 2.5 nM 模型在 0.3 mpk PO QD 下使用,以及製造大鼠的方法 :38% ERAS-0015 KRAS G12C:0.8 — 1.4 nM KRAS G12V:NCI-H727 許可化合物的腫瘤迴歸,包括 pan-RAS KRAS G12X:1 mpk 時的 4.1 — 7.4 nM CDX 模型(QD Dog:22% 電流 DC)具有潛在的覆蓋範圍 Molecular 4 KRAS G13D:2.8 — 5.5nM KRAS G12R:PSN1 CDX 到 2043 年的腫瘤迴歸 Monkey:17% Glue KRAS WT:4.1 — 13.8 nM 模型,5 mpk PO QD 3 H/NRAS WT:用於 RasM 實體瘤的活性電位 BIC pan-RAS MG,其效力高出約 5 到 10 倍,動物物種的 ADME 特性和 PK 表現良好(與當前開發中的 pan-RAS MG 相比)TPP: 目標產品簡介;OBA:口服生物利用度;IP:知識產權;FIC:同類首創;BIC:同類最佳;WT: w ildtype;sMI:小分子抑制劑;MG:分子膠水;DC:體外開發候選物 1 2 3 4效力由 CTG 2D 和 3D 細胞增殖測定 IC 進行評估;OBA 或口服生物利用度由 %F 評估;根據分子 特徵進行預測;沒有任何專利期限調整或延期 50 12
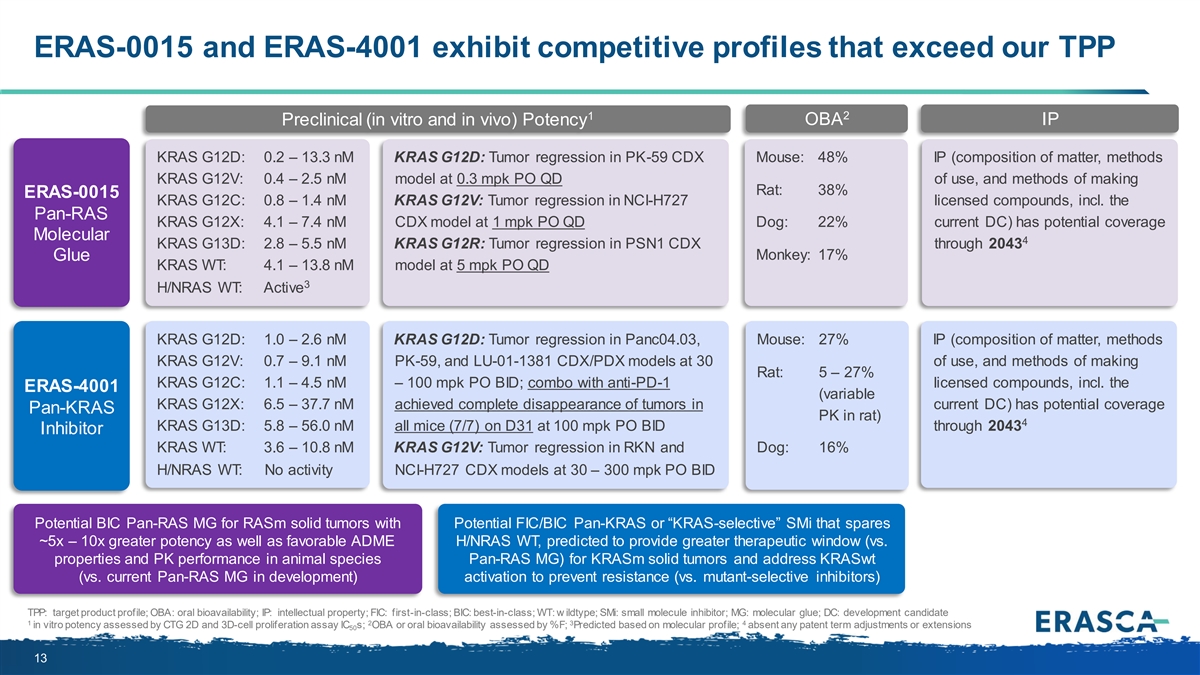
ERAS-0015 和 ERAS-4001 的競爭特徵超過了我們的 TPP 1 2 OBA IP 臨牀前(體外和體內)效力 KRAS G12D:0.2 — 13.3 nM KRAS G12D:PK-59 CDX 小鼠的腫瘤迴歸:48% IP(物質成分、方法 KRAS G12V:0.4 — 2.5 nM 模型在 0.3 mpk PO QD 下使用,以及製造大鼠的方法 :38% ERAS-0015 KRAS G12C:0.8 — 1.4 nM KRAS G12V:NCI-H727 許可化合物的腫瘤迴歸,包括 pan-RAS KRAS G12X:1 mpk 時的 4.1 — 7.4 nM CDX 模型(QD Dog:22% 電流 DC)具有潛在的覆蓋範圍 Molecular 4 KRAS G13D:2.8 — 5.5nM KRAS G12R:PSN1 CDX 到 2043 年的腫瘤迴歸 Monkey:17% Glue KRAS WT:4.1 — 13.8 nM 模型 PO QD 3 H/NRAS WT:活性 KRAS G12D:1.0 — 2.6 nM KRAS G12D:Panc04.03 中的腫瘤迴歸,鼠標: 27% IP(物質成分,方法 KRAS G12V:0.7 — 9.1 nM PK-59 和 LU-01-1381 CDX/PDX 模型的使用量為 30%,以及製造 Rat 的方法:5 — 27% KRAS G12C:1.1 — 4.5 nM — 100 mpk PO BID;與獲得 PD-1 許可的 化合物組合,包括 ERAS-4001(變量 KRAS G12X:6.5 — 37.7 nM 在當前 DC 中實現腫瘤完全消失)有大鼠的潛在覆蓋範圍 pan-KRAS PK)4 KRAS G13D:5.8 — 56.0 nM 所有小鼠(7/7)在 D31 上以 100 mpk PO BID 到 2043 抑制劑 KRAS WT:3.6 — 10.8 nM KRAS G12V:RKN 和狗的腫瘤迴歸:16% H/NRAS WT:30 — 300 mpk 的 NCI-H727 CDX 模型無活性 PO BID PAN-RAS MG 在 RKN 和 Dog 中的潛在 BIC pan-RAS MG 具有潛在的 FIC/BIC pan-KRAS 或 “KRAS選擇性” SMI 的實體瘤,其效力可提高約 5 到 10 倍,同時具有有利的 ADME H/NRAS WT,預計將提供更大的治療窗口(與動物物種 pan-RAS MG 的特性和藥效相比)Krasm 實體瘤並解決激活KrasWT(與當前開發中的pan-RAS MG相比)以防止耐藥性(與突變選擇性抑制劑相比)TPP:目標產品概況;OBA:口服生物利用度;IP:知識產權:FIC:同類首創;BIC: 同類最佳;WT:wildtype;SMI:小分子抑制劑;MG:分子膠水;DC:維生素中的候選藥物1 2 3 4 ro 效力由 CTG 2D 和 3D 細胞增殖測定 IC 進行評估;OBA 或口服生物利用度由 %F 評估;根據 分子譜進行預測;沒有任何專利期限調整或擴展 50 13
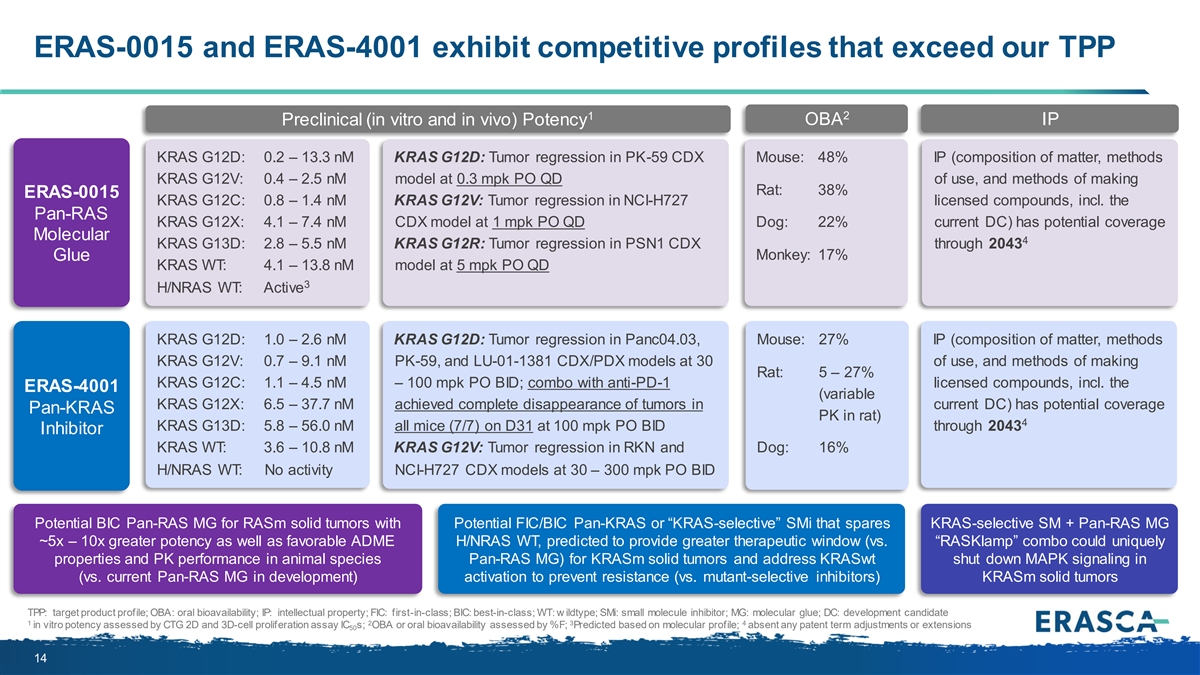
ERAS-0015 和 ERAS-4001 的競爭特徵超過了我們的 TPP 1 2 OBA IP 臨牀前(體外和體內)效力 KRAS G12D:0.2 — 13.3 nM KRAS G12D:PK-59 CDX 小鼠的腫瘤迴歸:48% IP(物質成分、方法 KRAS G12V:0.4 — 2.5 nM 模型在 0.3 mpk PO QD 下使用,以及製造大鼠的方法 :38% ERAS-0015 KRAS G12C:0.8 — 1.4 nM KRAS G12V:NCI-H727 許可化合物的腫瘤迴歸,包括 pan-RAS KRAS G12X:1 mpk 時的 4.1 — 7.4 nM CDX 模型(QD Dog:22% 電流 DC)具有潛在的覆蓋範圍 Molecular 4 KRAS G13D:2.8 — 5.5nM KRAS G12R:PSN1 CDX 到 2043 年的腫瘤迴歸 Monkey:17% Glue KRAS WT:4.1 — 13.8 nM 模型 PO QD 3 H/NRAS WT:活性 KRAS G12D:1.0 — 2.6 nM KRAS G12D:Panc04.03 中的腫瘤迴歸,鼠標: 27% IP(物質成分,方法 KRAS G12V:0.7 — 9.1 nM PK-59 和 LU-01-1381 CDX/PDX 模型的使用量為 30%,以及製造 Rat 的方法:5 — 27% KRAS G12C:1.1 — 4.5 nM — 100 mpk PO BID;與獲得 PD-1 許可的 化合物組合,包括 ERAS-4001(變量 KRAS G12X:6.5 — 37.7 nM 在當前 DC 中實現腫瘤完全消失)有大鼠的潛在覆蓋範圍 pan-KRAS PK)4 KRAS G13D:5.8 — 56.0 nM 所有小鼠(7/7)在 D31 上以 100 mpk PO BID 到 2043 抑制劑 KRAS WT:3.6 — 10.8 nM KRAS G12V:RKN 和狗的腫瘤迴歸:16% H/NRAS WT:30 — 300 mpk 的 NCI-H727 CDX 模型無活性 PO BID PAN-RAS MG 在 RKN 和 Dog 中的潛在 BIC pan-RAS MG 具有潛在的 FIC/BIC pan-KRAS 或 “KRAS選擇性” SMI 的 ASM 實體瘤,可避免 KRAS-選擇性 SM + pan-RAS MG 的效力提高約 5 倍 — 10 倍,而且有利的 ADME H/NRAS WT,預計將提供更大的治療窗口(與 “RaskLamp” 組合相比, 可以獨一無二KrasM 實體瘤動物物種 pan-RAS (MG) 的特性和 PK 性能,解決了 KrasWT 關閉 MAPK 信號(與當前開發中的 pan-RAS MG 相比)激活以防止耐藥性(與突變選擇性抑制劑相比) Krasm 實體瘤 TPP:目標產品簡介;OBA:口服生物利用度;IP:知識產權;FIC:同類首創;BIC:同類最佳;WT:wildtype;sMI:小分子抑制劑;MG:分子膠水;DC:通過 CTG 2D 和 3D 細胞增殖試驗 IC 評估的 體外效力 1 2 3 4 的開發候選物;OBA 或口服生物利用度由 %F 評估;根據分子特徵進行預測;沒有任何專利期限調整或延期 50 14

ERAS-0015 和 ERAS-4001 的競爭特徵超過了我們的 TPP • 效力高出約 5 到 10 倍,同時也具有有利的 ERAS-0015:動物 Pan-RAS MG 物種的潛在 BIC ADME 特性和 PK 性能(相對於目前開發中的 Pan-RAS MG)• 專為節省 H/NRAS WT 而設計,預計 為 ERAS-4001 提供更大的治療窗口(與 pan-RAS MG 相比):潛在的 FIC KRASM 實體瘤 pan-KRAS 或 “KRAS-選擇性” SM 抑制劑 • 旨在解決 KrasWT 激活以防止耐藥性(與突變選擇性 抑制劑相比)TPP = 目標產物概況;BIC:同類最佳;FIC:同類首創;MG:分子膠;SM:小分子;ADME:吸收、分佈、代謝和排泄;PK:藥代動力學 15
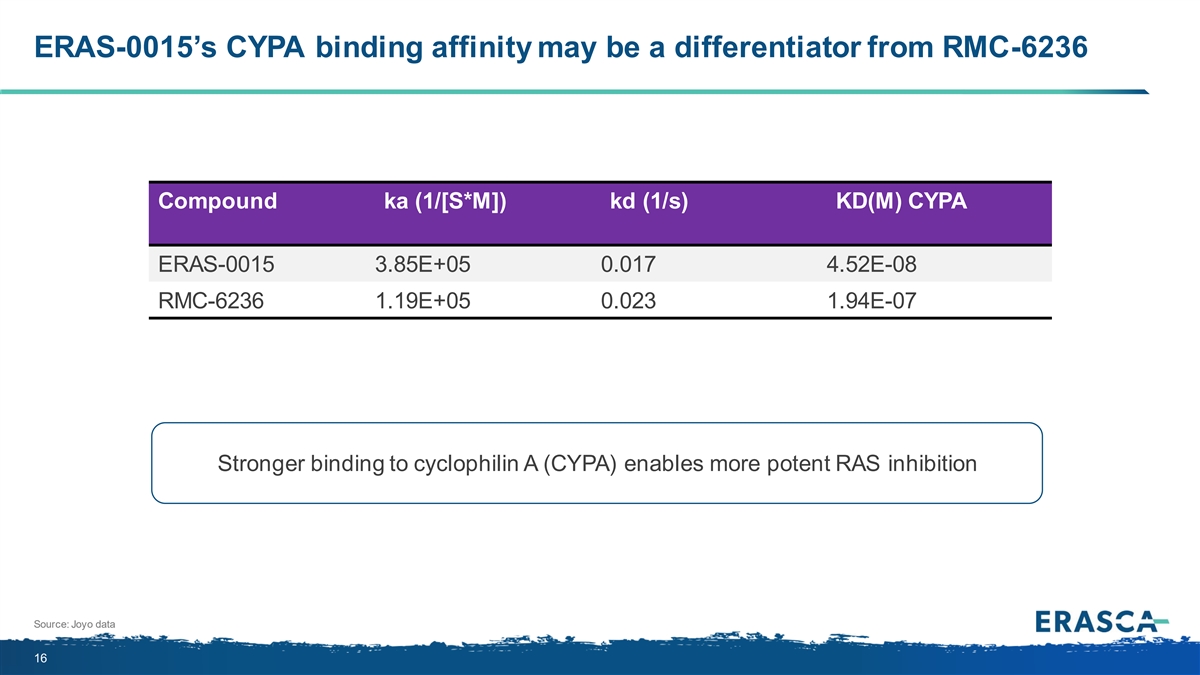
ERAS-0015 的 CYPA 結合親和力可能與 RMC-6236 化合物 ka (1/[S*M]) kd (1/s) KD (M) CYPA ERAS-0015 3.85E+05 0.017 4.52E-08 RMC-6236 1.19E+05 0.023 1.94E-07 與親環素 A (CYPA) 的結合力更強可實現更強的 RAS 抑制來源:Joyo 數據 16
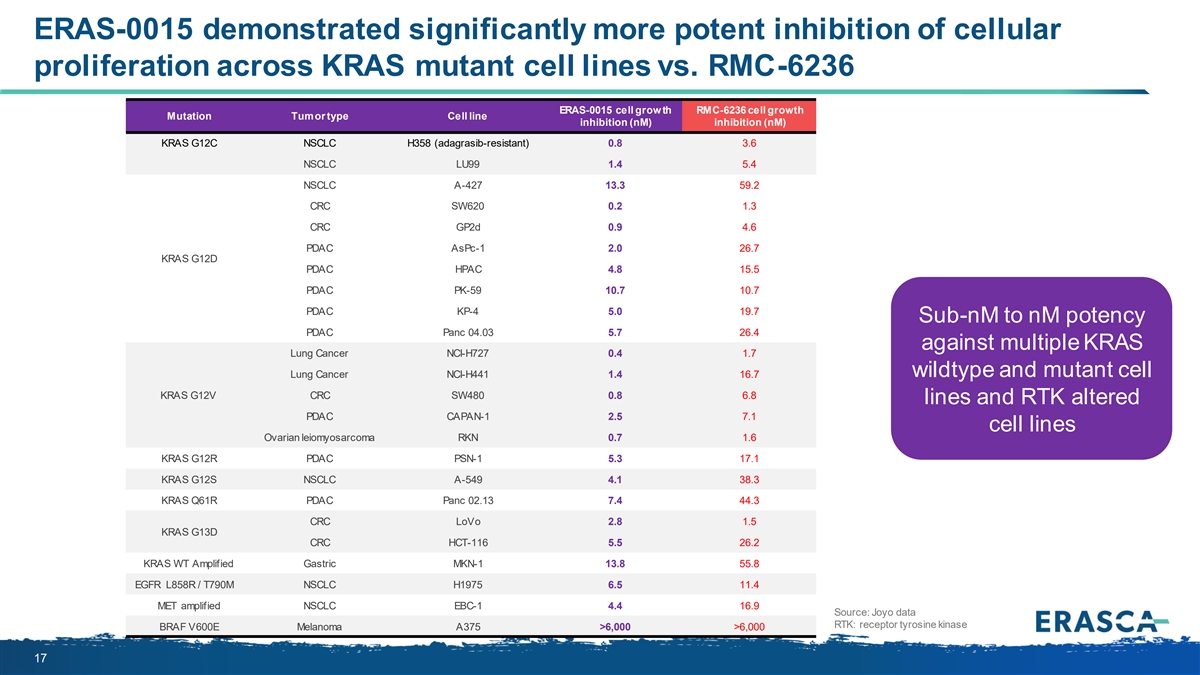
ERAS-0015 與 RMC-6236 ERAS-0015 細胞生長 RMC-6236 細胞生長突變腫瘤類型細胞系抑制 (nM) 抑制 (nM) KRAS G12C NSCLC H358(耐阿達格拉西布)0.8 3.6 NSCLC LU99 1.4 5.4 NSCLC A-427 13.3 59.2 SW620 0.2 CRC 0.2 Gp2D 0.9 PCRC 0.9 PCRC 0.9 PCRC 0.9 PCRC 0.9 PCRC 0.9 PCRC 0.9 PCRC 0.9 PSC 0.9 PCRC 0.9 PCRC 0.9 PCRC 0.9 PSC 0.9 PCRC 0.9 PCRC 0.9 PSC 0.9 PCRC 0.9 PCRC 0.9 PSC 0.9 PCRC 0.9 PSC 0.9 PSC aspc-1 2.0 26.7 KRAS G12D PDAC HPAC 4.8 15.5 PDAC PK-59 10.7 10.7 PDAC KP-4 5.0 19.7 亞納米到 nM 效力 PDAC Panc 04.03 5.7 5.7 26.4 對抗多發 KRAS 肺癌 NCI-H727 0.4 1.7 野生型和突變體 細胞肺癌 NCI-H441 1.4 16.7 KRAS G12V CRC SW480 0.8 6.8 系和 RTK 改變的 PDAC CAPAN-1 2.5 7.1 細胞系卵巢平滑肌肉瘤 RKN 0.7 1.6 KRAS G12R PSN-1 5.3 17.1 KRAS G12S NSCLC A-549 4.1 38.3 KRAS Q61R PDAC Panc 02.13 7.4 44.3 CRAS G13D HCT-116 5.5 26.2 KRAS WT 放大胃癌 MKN-1 13.8 55.8 EGFR L858R/T790M NSCLC H1975 6.5 11.4 MET 擴增非小細胞肺癌 EBC-1 4.4 16.9 來源:Joyo 數據 RTK:受體酪氨酸激酶 BRAF 黑色素瘤 A375 >6,000 >6,000 17 V600E
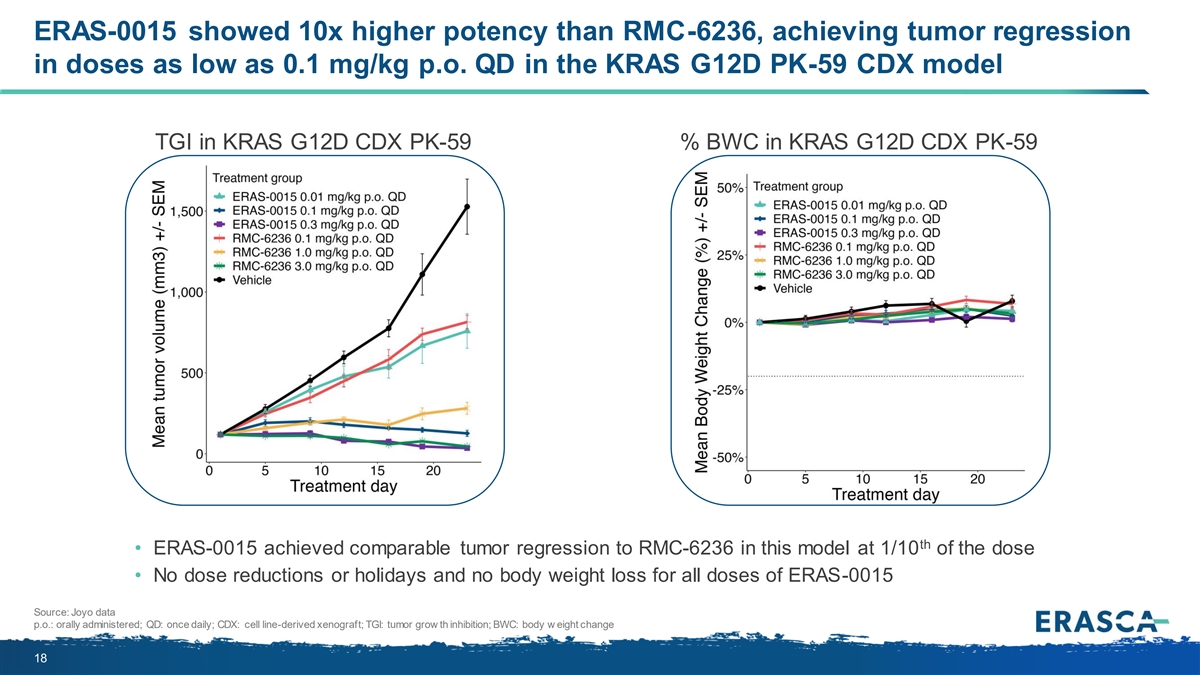
ERAS-0015 的效力比 RMC-6236 高 10 倍,在 KRAS G12D PK-59 CDX 模型中實現了腫瘤 迴歸劑量低至 0.1 mg/kg p.o. QD。KRAS G12D 適用於所有劑量 ERAS-0015 來源:Joyo data p.o.:口服;QD:每日一次;CDX:細胞系衍生異種移植;TGI:抑制腫瘤生長;《生物武器公約》:體重變化 18 PK-59 PK-59 ERAS-0015 RMC-6236
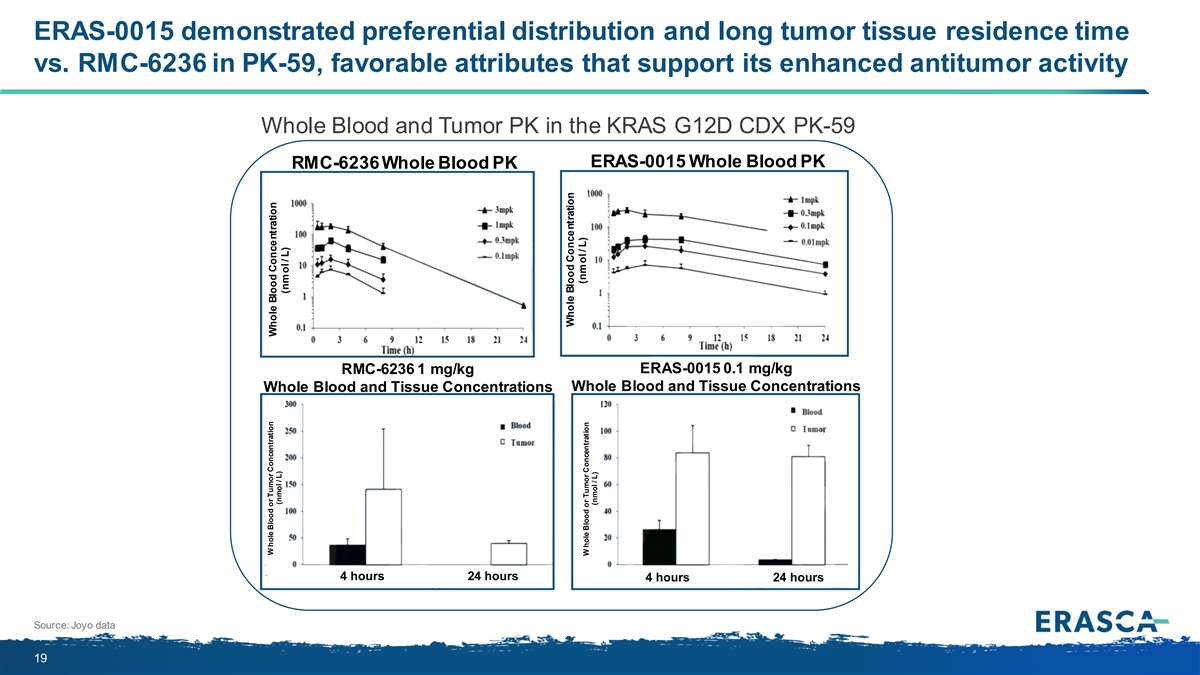
與 PK-59 中的 RMC-6236 相比,ERAS-0015 表現出優先分佈和較長的腫瘤組織 停留時間,有利的屬性支持其增強的抗腫瘤活性 KRAS G12D CDX PK-59 ERAS-0015 全血 PK RMC-6236 全血 PK RMC-6236 1 mg/kg ERAS-0015 0.1 mg/kg 全血 血液和組織濃度 4 小時 24 小時 24 小時 24 小時 24 小時來源:Joyo 數據 19 W 孔血液或腫瘤濃度全血濃度 (nmol/L) (nmol/L) 全血濃度 (nmol/L)W 孔血或腫瘤濃度 (nmol/L)
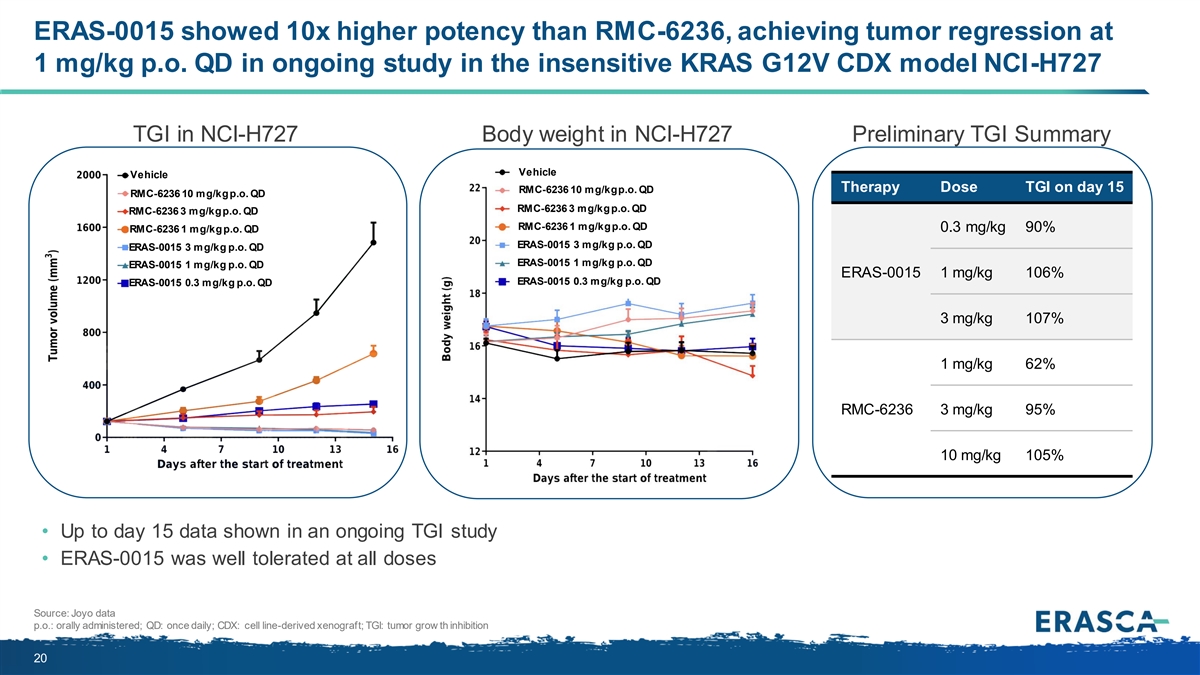
ERAS-0015 的效力比 RMC-6236 高 10 倍,在不敏感的 KRAS G12V CDX 模型中正在進行的研究中,腫瘤 迴歸率為 1 mg/kg p.o. QD p.o. QD RMC-6236 1 mg/kg p.o. qd p.o. 1mg/kg p.o. qd 0.3 mg/kg 90% p.o. qd 3 mg/kg p.o. qd 3 mg/kg p.o. QD 1 mg/kg p.o. QD 1mg/kg p.o. 106% {br NCI-H727 NCI-H727 NCI-H727 RMC-6236 RMC-6236 RMC-6236 RMC-6236 RMC-6236 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015} ERAS-0015 0.3 mg/kg p.o. QD ERAS-0015 0.3 mg/kg p.o. QD 3 mg/kg 107% 1 mg/kg 62% RMC-6236 3 mg/kg 95% 10 mg/kg 105% • 正在進行的 TGI 研究顯示截至第 15 天的數據 • ERAS-0015 在所有劑量下均具有良好的耐受性來源:Joyo 數據 p.o.: 口服;QD:每日一次;CDX:細胞系衍生異種移植;TGI: 腫瘤生長抑制作用 20
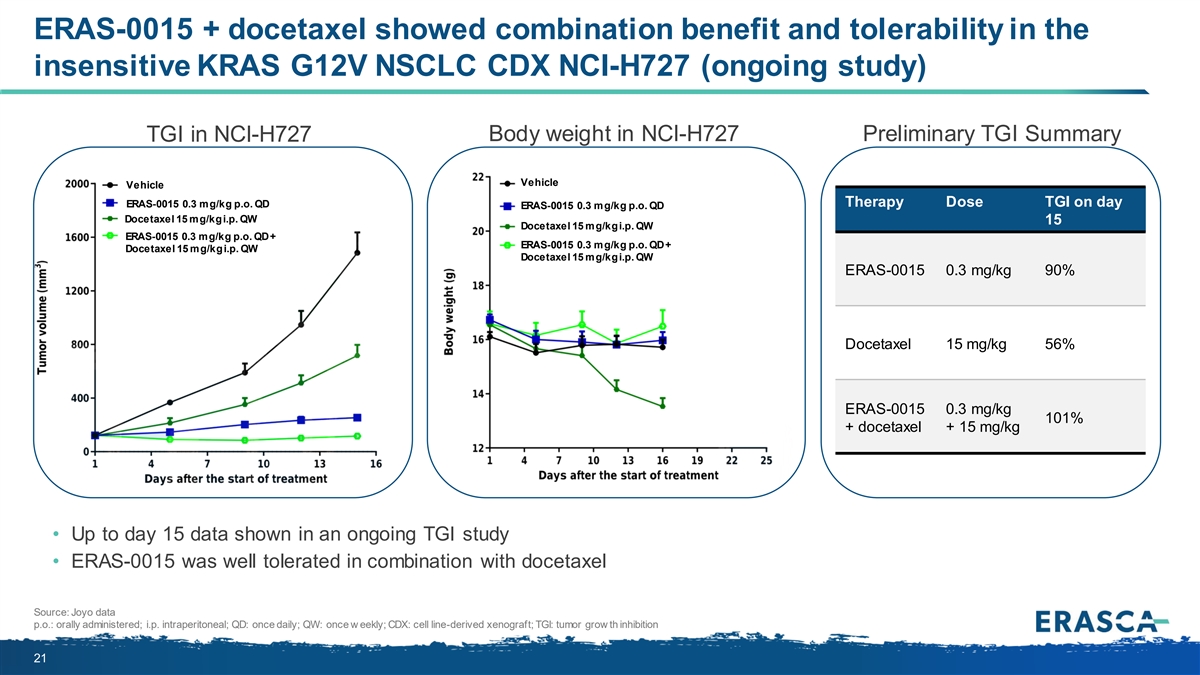
ERAS-0015 + 多西他賽在 不敏感的 KRAS G12V NSCLC CDX NCI-H727(正在進行的研究)中顯示出組合的益處和耐受性 NCI-H727 的初步 TGI 摘要 NCI-H727 車輛 ERAS-0015 0.3 mg/kg p.o. QD 當天 TGI 的劑量 ERAS-0015 0.3 mg/kg p.o. QD docetaxel 15 mg/kg i.p. QD docetaxel 15 mg/kg i.p.. QW ERAS-0015 0.3 mg/kg p.o. QD + ERAS-0015 0.3 mg/kg p.o. QD + Docetaxel 15 mg/kg i.p. QW docetaxel 15 mg/kg i.p. qw ERAS-0015 0.3 mg/kg 90% 多西他賽 15 mg/kg 56% ERAS-0015 0.3 mg/kg 101% + 多西他賽 + 15 mg/kg • 向上 一項正在進行的 TGI 研究顯示了至第 15 天的數據 • ERAS-0015 與多西他賽聯合使用時耐受性良好。來源:Joyo data p.o.:口服;即腹膜內給藥;QD:每天一次;QW:每週一次;CDX:細胞系衍生異種移植; TGI:腫瘤生長抑制 21
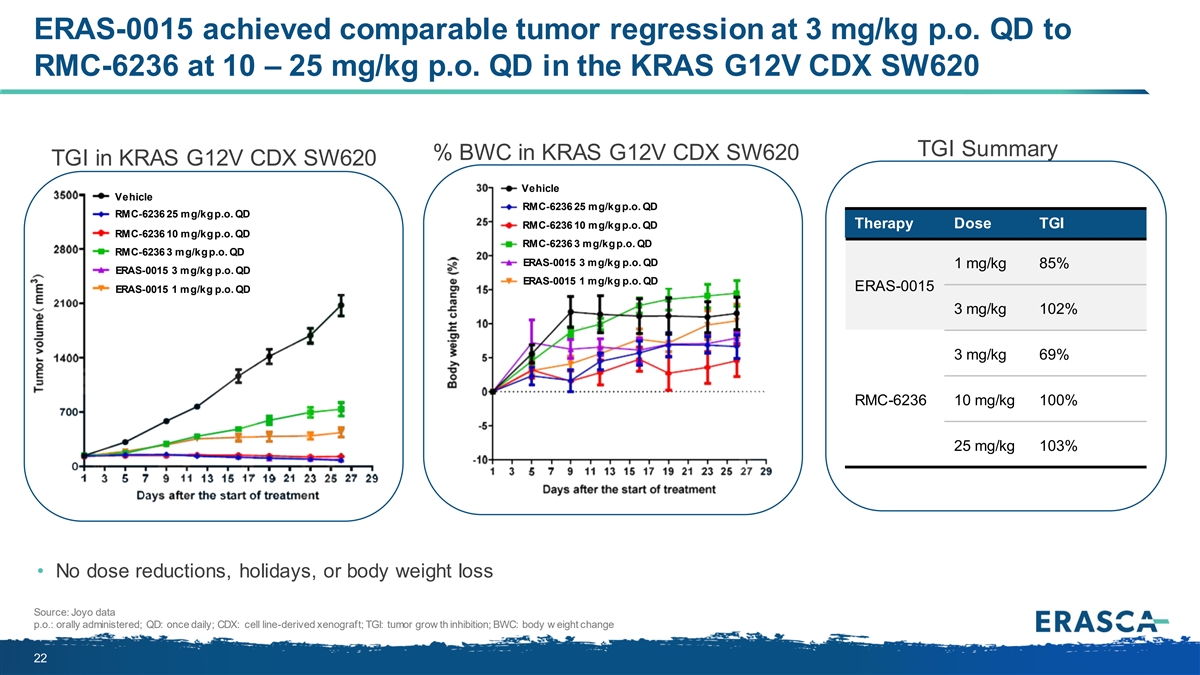
ERAS-0015 在 KRAS G12V CDX SW620 TGI 中實現了與 RMC-6236 在 10 — 25 mg/kg p.o. QD 相似的腫瘤迴歸率 KRAS G12V CDX TGI 摘要 KRAS G12V CDX SW620 TGI 中 KRAS G12V CDX TGI 車輛 RMC-6236 25 mg/kg p.o. QD GI RMC-6236 10 mg/kg p.o. QD 3 mg/kg p.o. QD RMC-6236 3 mg/kg p.o. QD 3 mg/kg p.o. QD 1 mg/kg p.o. 85 mg/kg p.o. QD 1 mg/kg p.o. QD 3 mg/kg p.o. QD 3 mg/kg p.o. 10mg/kg p.o. 100% 25 SW620 RMC-6236 RMC-6236 RMC-6236 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015 RMC-6236mg/kg 103% • 不減少劑量、節假日或減肥來源:Joyo 數據期限:口服;QD:每日一次;CDX:細胞系衍生異種移植;TGI:腫瘤生長抑制;BWC:體重變化 22
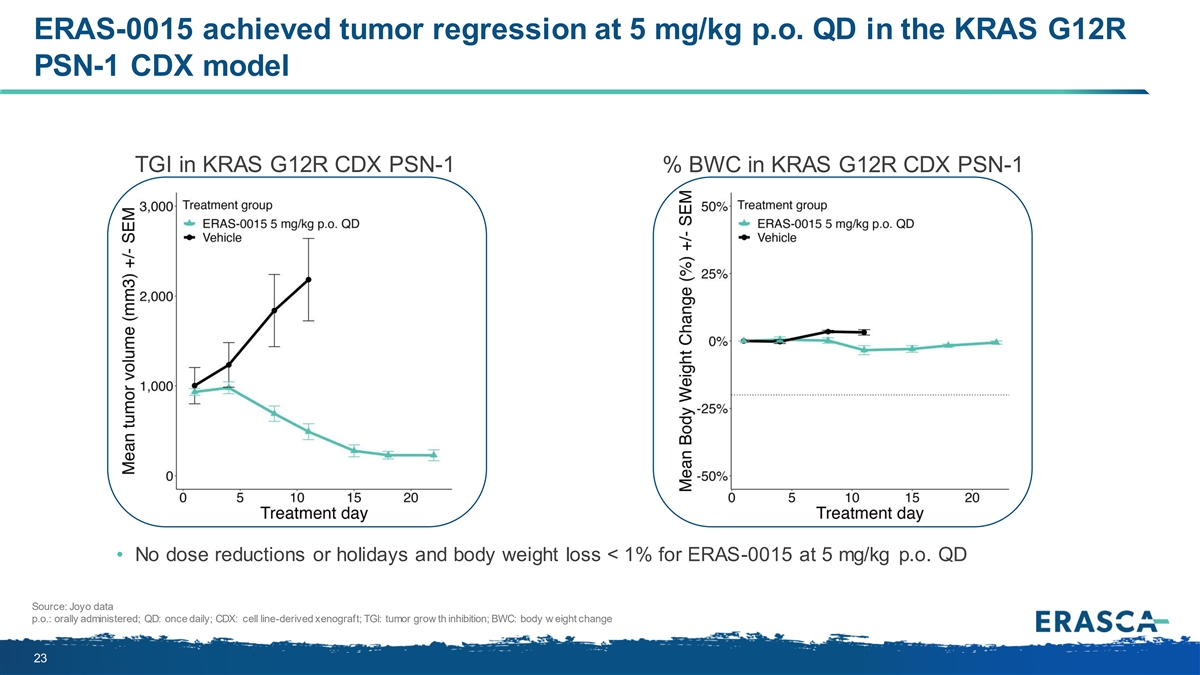
ERAS-0015 在 KRAS G12R PSN-1 CDX 模型 TGI 在 KRAS G12R CDX PSN-1% BWC 中實現了腫瘤消退 KRAS G12R CDX PSN-1 中的 KRAS G12R% BWC • 不減少劑量、節假日和體重減輕
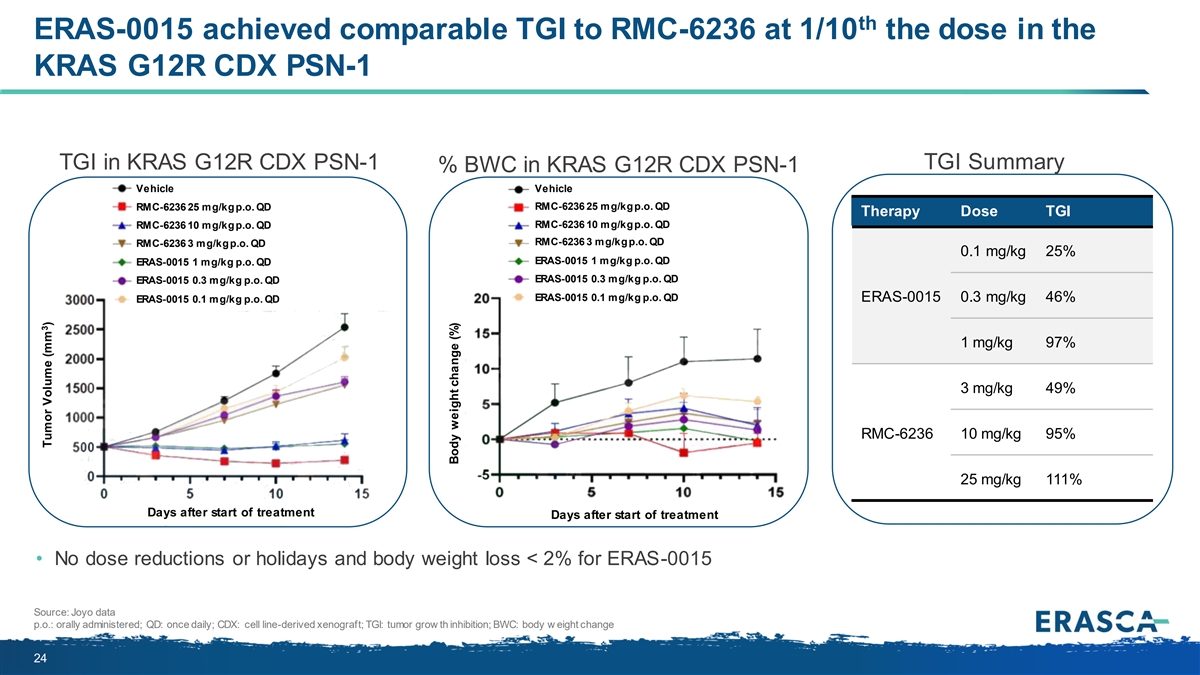
ERAS-0015 在 KRAS G12R CDX PSN-1 TGI 的劑量為 劑量的 1/10 時達到的 TGI 與 RMC-6236 相當 KRAS G12R CDX TGI 摘要 KRAS G12R CDX PSN-1 車輛 RMC-6236 25 mg/kg p.o. QD RMC-6236 25 mg/kg p.o. QD RMC-6236 10 mg/kg p.o. QD RMC-6236 10mg/kg p.o. QD 3 mg/kg p.o. QD RMC-6236 3 mg/kg p.o. QD 0.1 mg/kg 25% p.o. 1 mg/kg p.o. QD 0.3 mg/kg p.o. QD 0.3 mg/kg p.o. QD 0.1 mg/kg p.o. QD 0.1 mg/kg p.o. QD 0.1 mg/kg p.o. QD 0.1 mg/kg p.o. QD 0.3 mg/kg p.o. 46% 1 mg/kg 97% 3 PSN-1 RMC-6236 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015 ERAS-0015mg/kg 49% RMC-6236 10 mg/kg 95% 25 mg/kg 111% 治療開始後的幾天治療開始後的幾天 • 沒有減少劑量或節假日和體重減輕
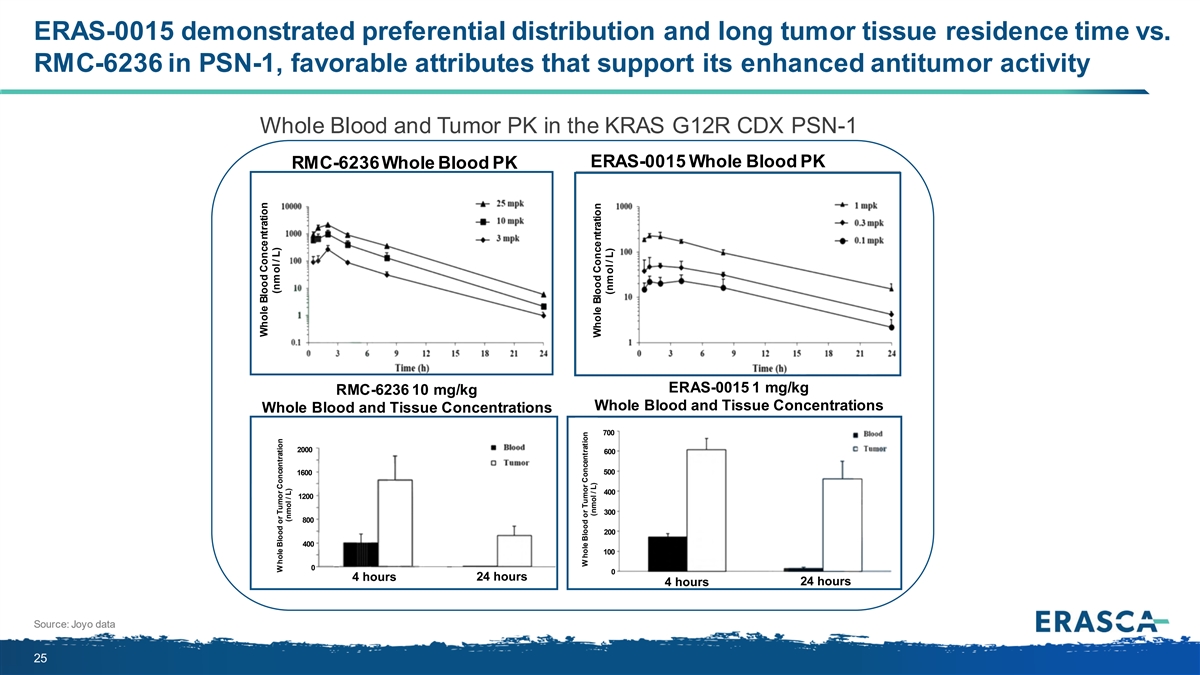
與 PSN-1 中的 RMC-6236 相比,ERAS-0015 表現出優先分佈和較長的腫瘤組織 停留時間,有利的屬性支持其增強的抗腫瘤活性 KRAS G12R CDX PSN-1 ERAS-0015 全血 PK RMC-6236 全血 PK ERAS-0015 1 mg/kg RMC-6236 10 mg/kg 全血 血液和組織濃度全血和組織濃度 700 2000 600 1600 400 400 200 400 0 0 0 4 小時 24 小時 24 小時 4 小時來源:Joyo 數據 25 全血濃度 (nmol/L) W 全血或腫瘤 濃度 (nmol/L) W 孔血或腫瘤濃度 W 孔血或腫瘤濃度 (nmol/L) (nmol/L) (nmol/L) 全血濃度 (nmol/L) 全血濃度 (nmol/L)
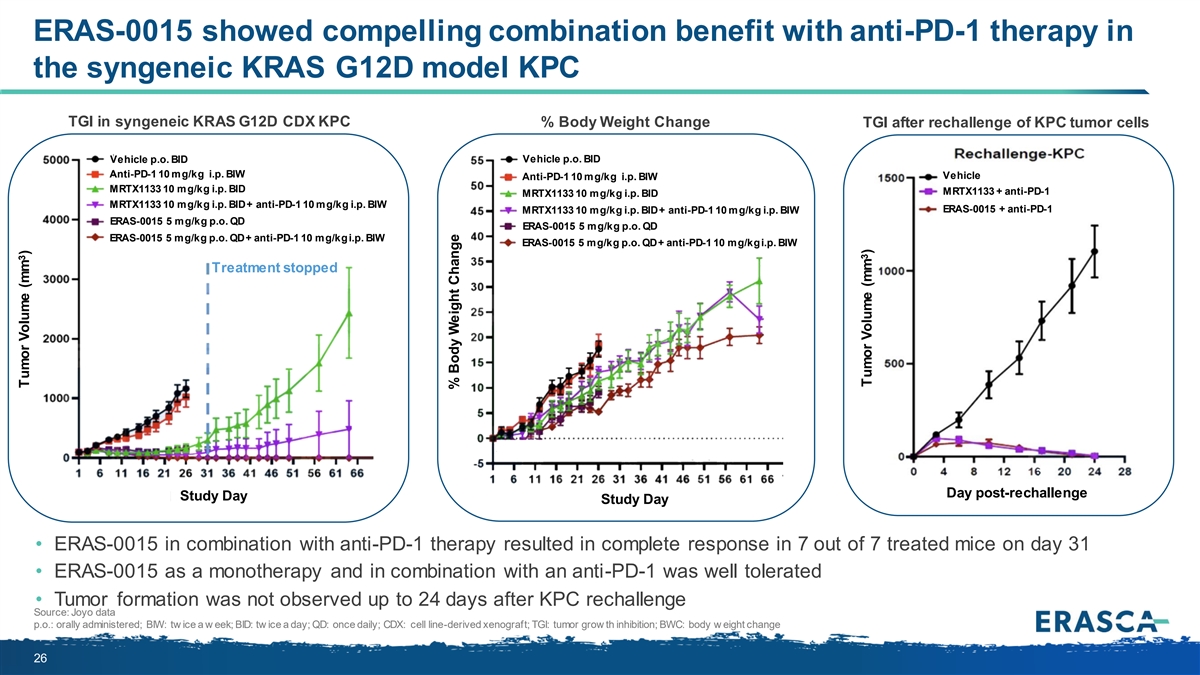
在同基因 KRAS G12D 模型中,ERAS-0015 與抗 PD-1 療法 顯示出令人信服的聯合益處 在同基因 KRAS G12D CDX CDX KPC% 體重變化 TGI 車輛 p.o. BID 抗PD-1 10 mg/kg i.p. BIW Vehicle 抗 PD-1 10 mg/kg i.p. BIW MRTX1133 10 mg/kg i.p. BIW 10 mg/kg i.p. BID MRTX1133 + 抗 PD-1 MRTX1133 10 mg/kg i.p. BID MRTX1133 10 mg/kg i.p. BID + 抗 PD-1 10 mg/kg i.p. biw ERAS-0015 + 抗 PD-1 MRTX1133 10 mg/kg i.p. bid + 抗 PD-1 10 mg/kg i.p. biw ERAS-0015 5 mg/kg p.o. QD ERAS-0015 5 mg/kg p.o.QD ERAS-0015 5 mg/kg p.o. QD + 抗 PD-1 10 mg/kg ip. BIW ERAS-0015 5 mg/kg p.o. QD + 抗 PD-1 10 mg/kg ip。BIW 治療在再挑戰後的第二天研究日停止 • ERAS-0015 與抗 PD-1 療法聯合使用在第 31 天使 7 只接受治療的小鼠中有 7 只產生完全的 反應 • ERAS-0015 作為單一療法和抗體聯合使用 PD-1 耐受性良好 • 在 KPC 再挑戰後 24 天內未觀察到腫瘤形成來源:Joyo data p.o.:口服 給藥;BIW:每週兩次冰;BID:每天兩次冰;QD:每日一次;CDX:細胞線源異種移植;TGI:腫瘤生長抑制;《生物武器公約》:體重變化 26 3 腫瘤體積 (mm)% 體重變化 3 腫瘤體積 (mm)% 體重變化 3 腫瘤體積 (mm)
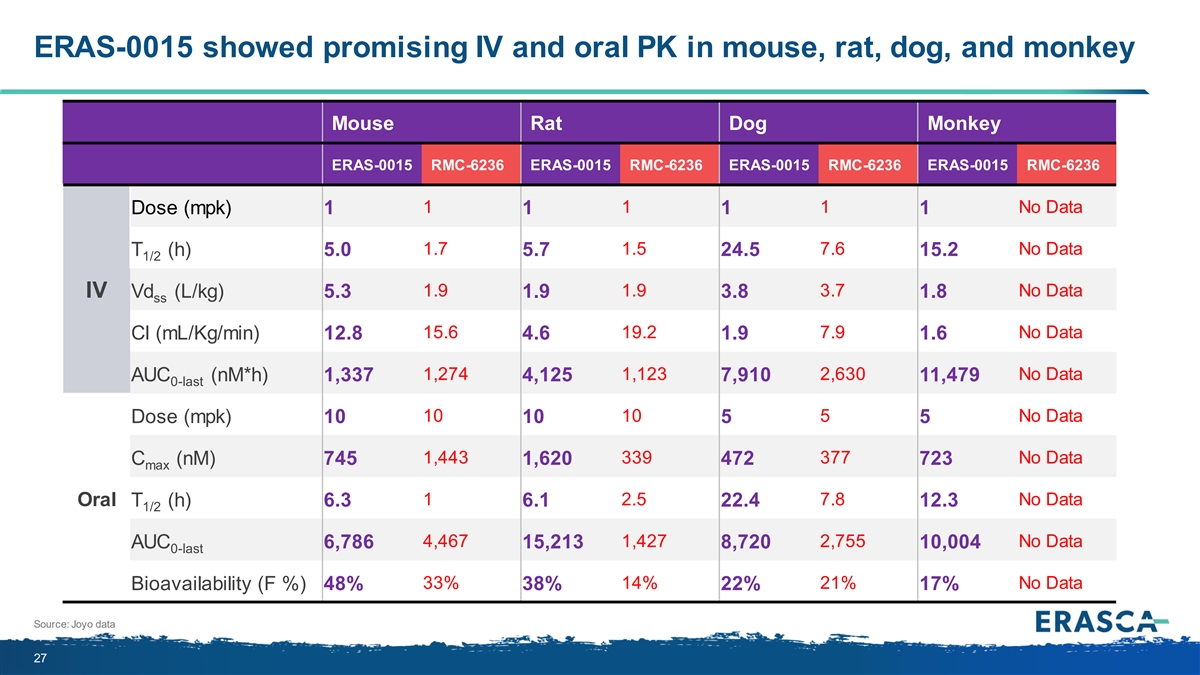
ERAS-0015 在小鼠、大鼠、狗和 猴子中表現出良好的靜脈注射和口服 PK Monkey ERAS-0015 RMC-6236 ERAS-0015 RMC-6236 ERAS-0015 RMC-6236 ERAS-0015 RMC-6236 1 1 1 無數據劑量 (mpk) 1 1 1 1.7 1.7 7.6 無數據 T (h) 5.0 5.7 24.5 15.2 1/2 1.9 3.7 無數據 IV Vd (L/kg) 5.3 1.9 1.8 ss 15.6 19.2 7.9 無數據 Cl (ml/kg) 12.8 4.6 1.9 1.6 1,274 1,123 2,630 無數據 AUC (nm*H) 1,337 4,125 7,910 11,479 0-last 10 10 5 無數據劑量 (mpk) 10 10 5 1,443 339 377 無數據 C (nM) 745 1,620 472 723 max 1 2.5 7.8 無數據口服 6.3 22.4 12.3 1/2 4,467 1,427 2,755 無數據 AUC 6,786 15,213 8,720 10,004 0-last 33% 14% 21% 無數據生物利用度 (F%) 48% 38% 22% 17% 來源:Joyo 數據 27
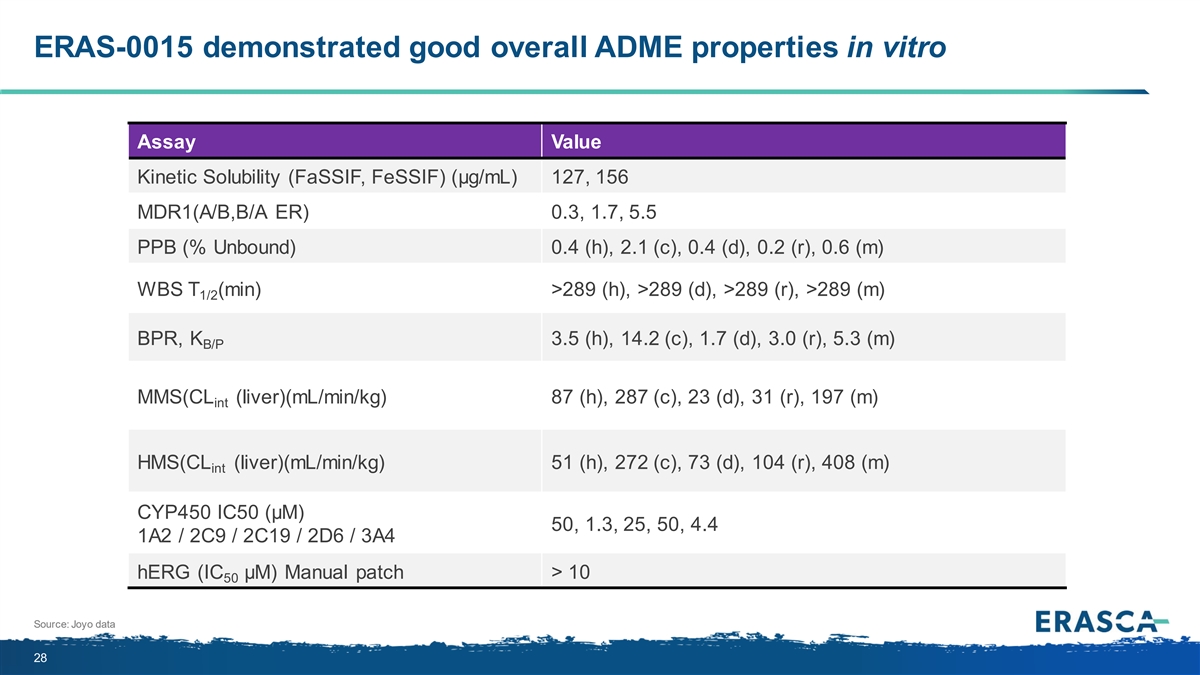
ERAS-0015 在體外分析中表現出良好的整體 ADME 特性 數值動力學溶解度 (fassIF、fesSIF) (μg/mL) 127、156 MDR1 (A/B、B/A ER) 0.3、1.7、5.5 PPB(未結合百分比)0.4 (h)、2.1 (c)、0.4 (d)、0.2 (r)、0.6 (m) WBS T (min) >289 (h))、>289 (d)、>289 (r)、>289 (m) 1/2 BPR、K 3.5 (h)、14.2 (c)、 1.7 (d)、3.0 (r)、5.3 (m) B/P 彩信 (CL (肝臟) (mL/min/kg) 87 (h)、287 (c)、23 (d)、31 (r)、197 (m)) int HMS(CL(肝臟)(mL/min/kg)51(h)、272(c)、73(d)、104(r)、408(m)int CYP450 IC50(µM)50、1.3、25、50、4.4 1A2/2C9/2C19/2D6/3A4 HerG (IC μM) 手冊補丁 > 10 50 來源:Joyo 數據 28
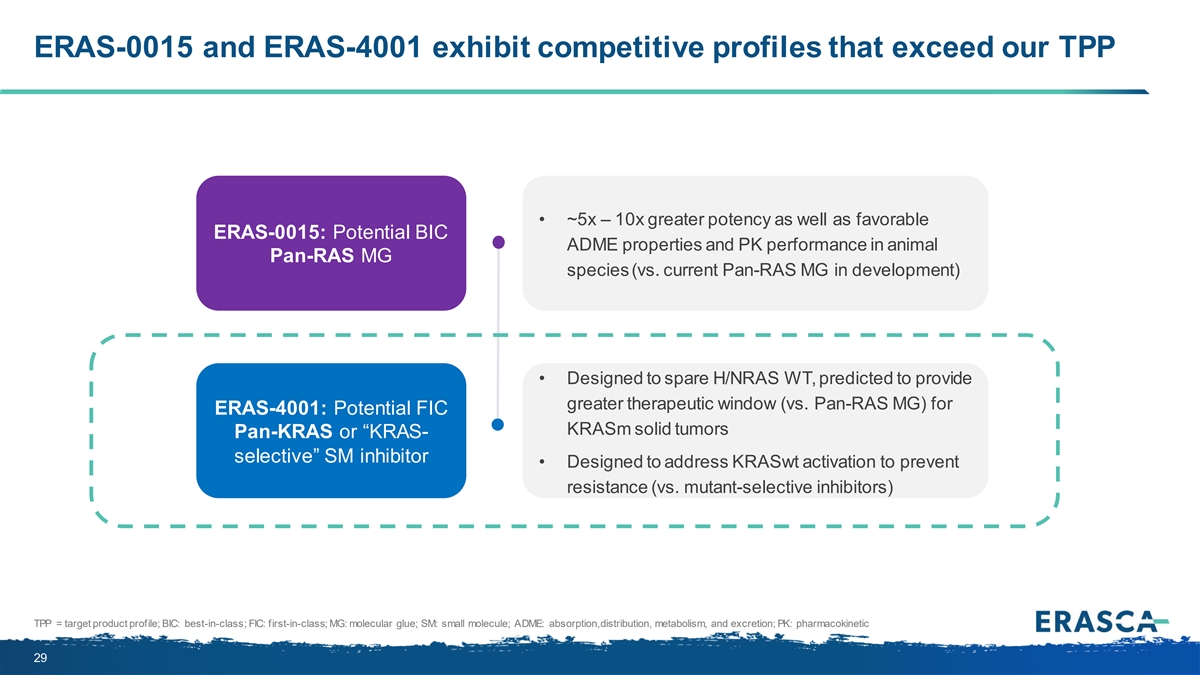
ERAS-0015 和 ERAS-4001 的競爭特徵超過了我們的 TPP • 效力提高了約 5 到 10 倍,同時也表現出有利的 ERAS-0015:動物 Pan-RAS MG 物種的潛在 BIC ADME 特性和 PK 性能(與目前正在開發的 Pan-RAS MG 相比)• 專為節省 H/NRAS WT 而設計,預計 為 ERAS-4001 提供更大的治療窗口(與 pan-RAS MG 相比):潛在的 FIC KRASM 實體瘤 pan-KRAS 或 “KRAS-選擇性” SM 抑制劑 • 旨在解決 KrasWT 激活以防止耐藥性(與突變選擇性 抑制劑相比)TPP = 目標產物概況;BIC:同類最佳;FIC:同類首創;MG:分子膠;SM:小分子;ADME:吸收、分佈、代謝和排泄;PK:藥代動力學 29
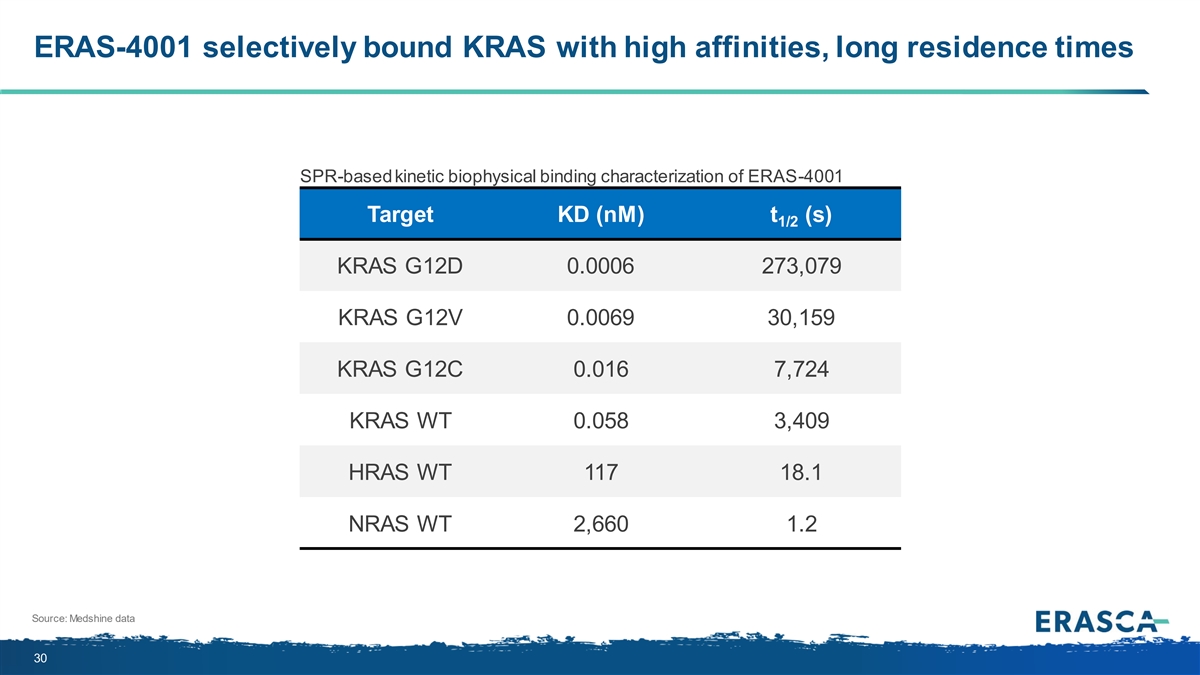
ERAS-4001 選擇性結合 KRAS 具有高親和力、長駐留 次基於 SPR 的 ERAS-4001 目標 KD (nM) t (s) 1/2 KRAS G12D 0.0006 273,079 KRAS G12V 0.0069 30,159 KRAS G12C 0.016 7,724 KRAS WT 0.058 3,409 HRAS WT 117 18.1 NRAS WT 2,660 1.2 來源:Medshine 數據 30
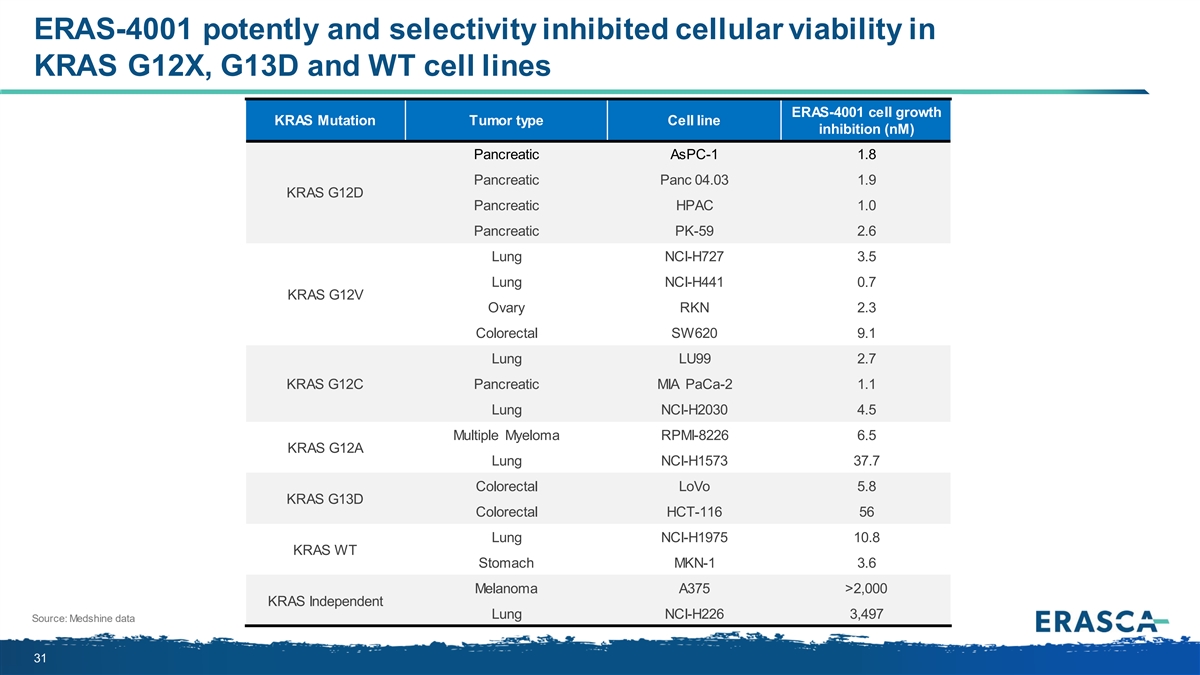
ERAS-4001 有效和選擇性抑制了 KRAS G12X、G13D 和 WT 細胞系中的細胞活力 ERAS-4001 細胞生長 KRAS 突變腫瘤類型細胞系抑制 (nM) 胰腺 ASPC-1 1.8 胰腺 04.03 1.9 KRAS G12D 胰腺 HPAC 1.0 胰腺 PK-59 2.6 肺 NCI-H441 0.7 KRAS G12V 卵巢 RKN 2.3 結直腸 SW620 9.1 肺 LU99 2.7 KRAS G12C 胰腺 MIA paca-2 1.1 肺 NCI-H2030 4.5 多發性骨髓瘤 RPMI-8226 6.5 KRAS G12A 肺 NCI-H1573 37.7 結直腸 LoVo 5.8 KRAS G13D 結直腸癌 HCT-116 56 肺 NCI-H1975 10.8 KRAS WT {NCI-H727br} 胃部 MKN-1 3.6 黑色素瘤 A375 >2,000 KRAS 獨立肺部 NCI-H226 3,497 來源:Medshine 數據 31
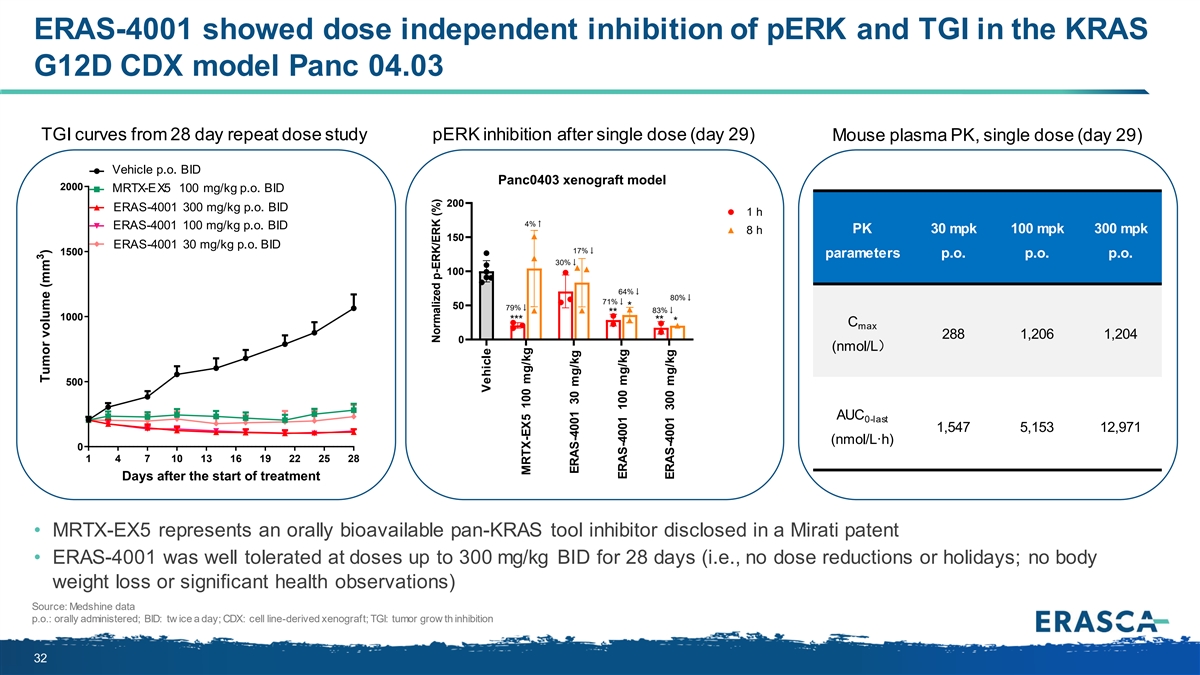
ERAS-4001 在 KRAS G12D CDX 模型中顯示出對 perK 和 TGI 的劑量無關的抑制 Panc 04.03 TGI 曲線 Panc 04.03 單劑量(第 29 天)小鼠血漿 PK、單劑量(第 29 天)載體 po.bid panc0403 異種移植模型 2000 MRTX-EX5 100 mg/kg p.o. BID panc0403 異種移植模型 2000 100 mg/kg p.o. BID p.o. BID panc0403 異種移植模型 2000 100 mg/kg p.o. bid p.o. MRP TX-EX5,100 mg/kg,p.o.,BID 200 ERAS-4001 300 mg/kg p.o. BID WXSHA015,300 mg/kg,p.o.,BID 1 h 4% ↑ ERAS-4001 100 mg/kg p.o. BID WXSHA015,100 mg/kg,p.o.,BID 8 h PK 30 mpk 300 mpk 300 mpk 150 mpk 150 W ER XA S H -4 A 00 01 15 3,3 00 m m g/g k/g k g p.,o p..o B.I, D 出價 17% ↓ 1500 個參數年利率 30% ↓ 100 64% ↓ 80% ↓ 71% ↓ 50 * 79% ↓ 83% ↓ ** 1000 *** ** * C max 288 1,204 1,204 0 (nmol/L) 500 AUC 0-last 1,5153 12,971 (nmol/L·H) 0 1 4 7 10 13 16 19 22 25 25 天后 28 天治療 • MRTX-EX5 是 Mirati 專利中披露的一種口服生物可利用的 pan-KRAS 工具抑制劑 • ERAS-4001 在劑量高達 300 mg/kg BID 時耐受性良好,持續 28 天(即 不減少劑量或節假日;沒有體重減輕或出現重大健康觀察)來源:Medshine 數據 p.o.:口服;出價:tw一天兩次;CDX:細胞系衍生異種移植;TGI:腫瘤生長抑制 32 載體 Ex.5 100 mpk WX-A015 30 mpk WX-A015 100 mpk WX-A015 300 mpk 3 腫瘤體積 (mm) 標準化 p-erk/erK (%) 載體 MRTX-EX5 100 mg/kg ERAS-4001 30 mg/kg ERAS-4001 100 mg/kg ERAS-4001 300 mg/kg 300 mg/kg 300 mg/kg
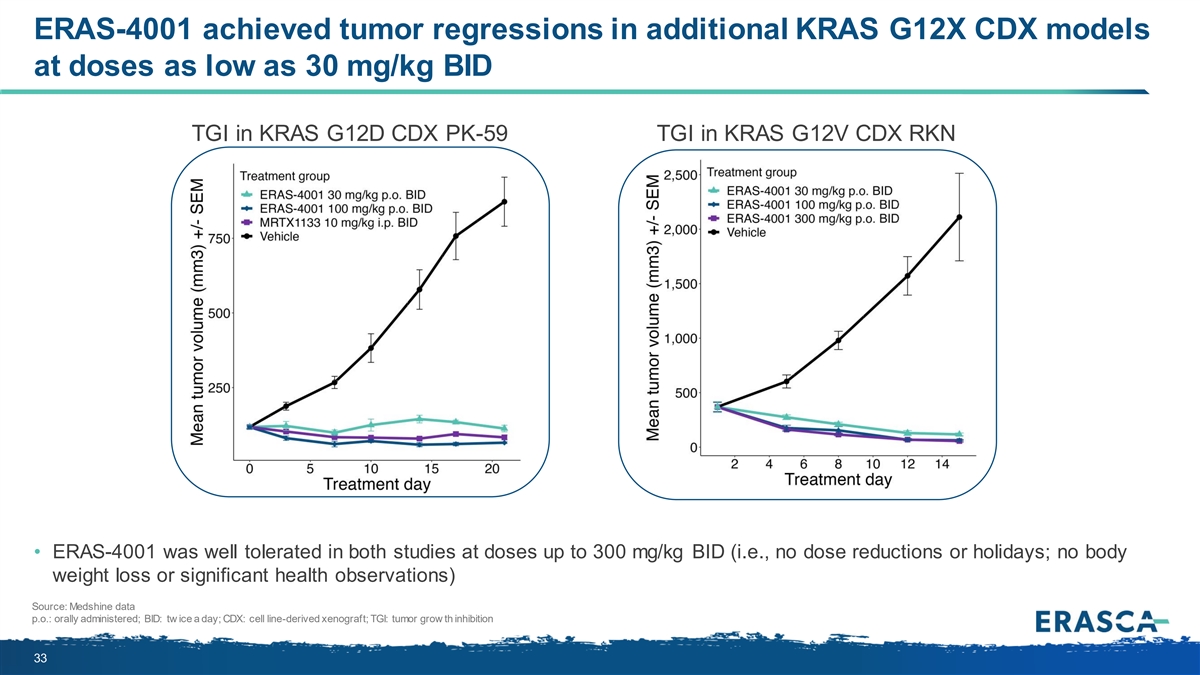
ERAS-4001 在其他 KRAS G12X CDX 模型 中實現了腫瘤迴歸 劑量低至 30 mg/kg BID KRAS G12D CDX PK-59 TGI KRAS G12V CDX RKN • ERAS-4001 在劑量高達 300 mg/kg BID(即不減少劑量或節假日;體重減輕或顯著健康 觀察)的兩項研究中均具有良好的耐受性 來源:Medshine data p.o: 口服;BID:每天兩次;CDX:細胞系衍生異種移植;TGI:腫瘤生長抑制劑 33
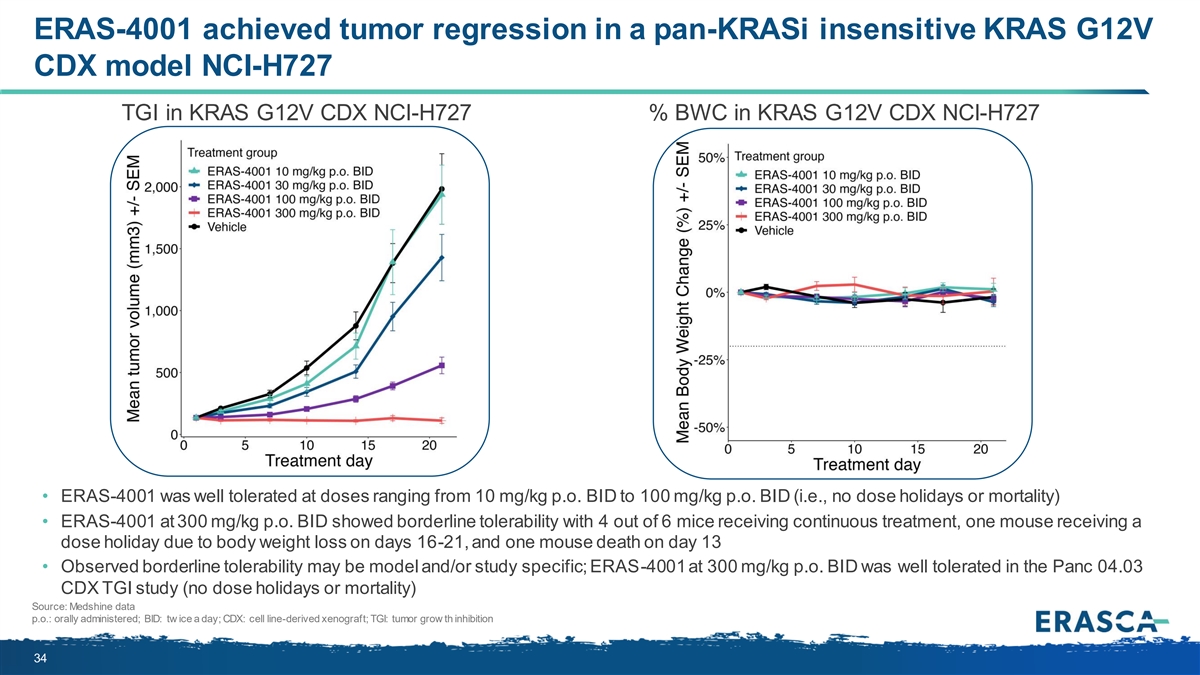
ERAS-4001 在泛-KRASI 不敏感的 KRAS G12V CDX 模型中實現了腫瘤消退 NCI-H727 KRAS G12V CDX NCI-H727% BWC KRAS G12V CDX NCI-H727 • ERAS-4001 在劑量從 10 mg/kg p.o. BID 到 100 mg/kg p.o. BID(即無劑量假日或死亡率)不等的劑量下表現出臨界耐受性在接受持續治療的 6 只小鼠中,一隻小鼠在第 16-21 天因體重減輕而獲得劑量減免,一隻小鼠在第 13 天死亡 • 觀察到的臨界耐受性可能是模型和/或 ERAS-4001特定研究;在 Panc 04.03 CDX TGI 研究中,300 mg/kg p.o. BID 的 ERAS-4001 耐受性良好(無劑量假期或死亡率)來源:Medshine 數據 p.o.:口服;BID:每天兩次;CDX:細胞系衍生異種移植; TGI:腫瘤生長抑制作用 34
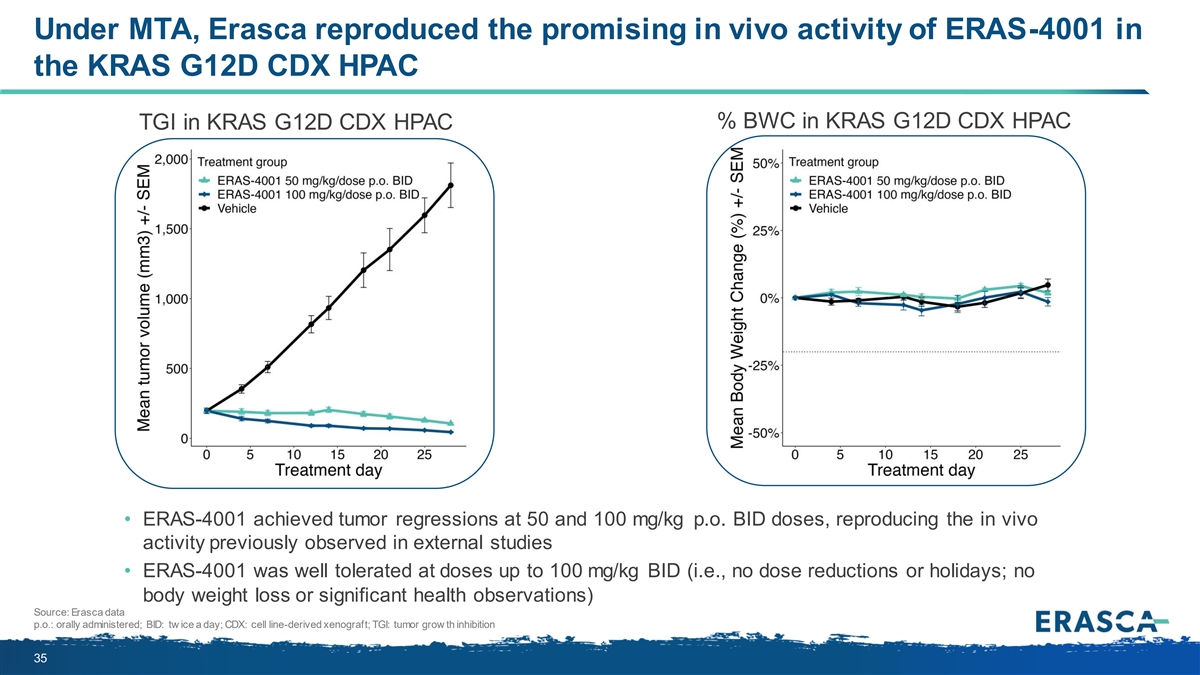
在 MTA 下,埃拉斯卡在 KRAS G12D CDX HPAC 的 KRAS G12D CDX HPAC% BWC 中重現了 ERAS-4001 在 KRAS G12D CDX HPAC TGI 中令人鼓舞的體內活性 • ERAS-4001 在 50 和 100 mg/kg p.o. BID 劑量下實現了腫瘤迴歸,重現了先前在外部研究中觀察到的體內活性 • ERAS-4001 在增加劑量時耐受性良好至100 mg/kg BID(即不減少劑量或節假日;沒有體重減輕或明顯的健康觀察)來源:Erasca 數據 p.o.:口服;BID:每天兩塊冰;CDX:細胞系衍生的 異種移植;TGI:腫瘤生長抑制作用 35
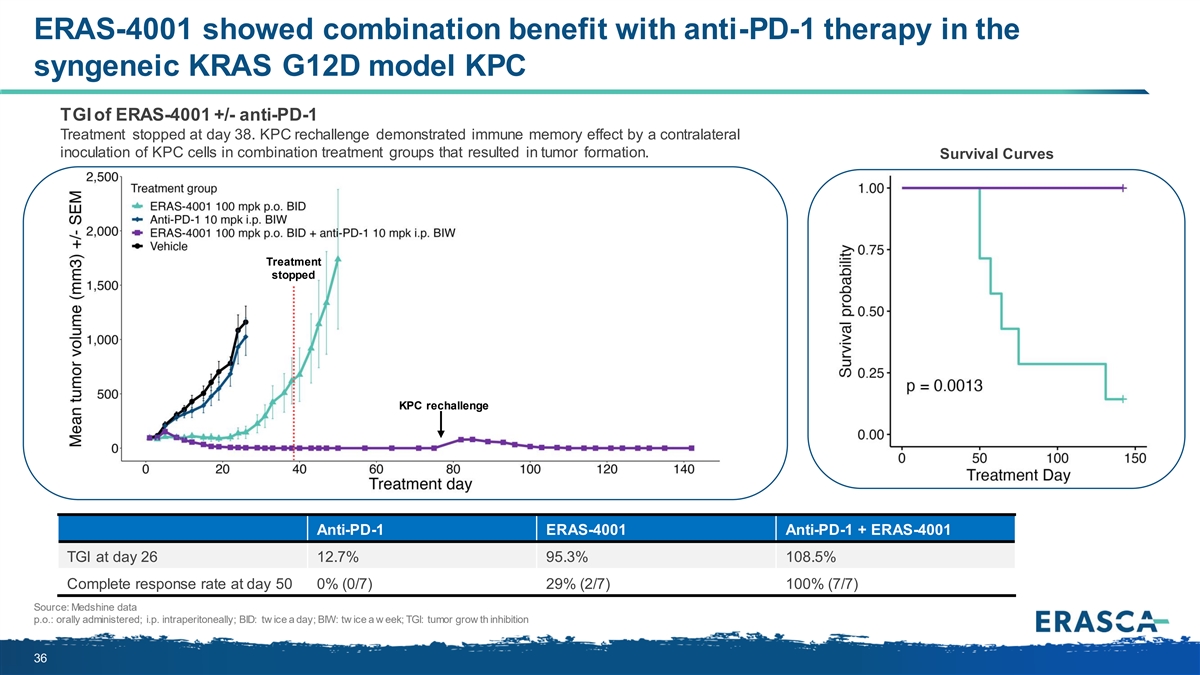
在 同源 KRAS G12D 模型 KPC TGI 的 ERAS-4001 +/-抗 PD-1 治療在第 38 天停止,ERAS-4001 顯示出與抗 PD-1 療法的聯合益處。KPC 再挑戰通過對側接種聯合治療組中的 KPC 細胞來顯示出免疫記憶效應,從而導致腫瘤的形成。 生存曲線治療在第 26 天停止了 KPC 再挑戰抗 PD-1 ERAS-4001 抗 PD-1 + ERAS-4001 TGI 12.7% 95.3% 108.5% 第 50 天的完全回覆率 0% (0/7) 29% (2/7) 100% (7/7) 來源:Medshine 數據 p.o.:口服;i.p. 腹腔注射;出價:一天兩冰;BIW:每週兩次冰; TGI: 腫瘤生長的抑制作用 36
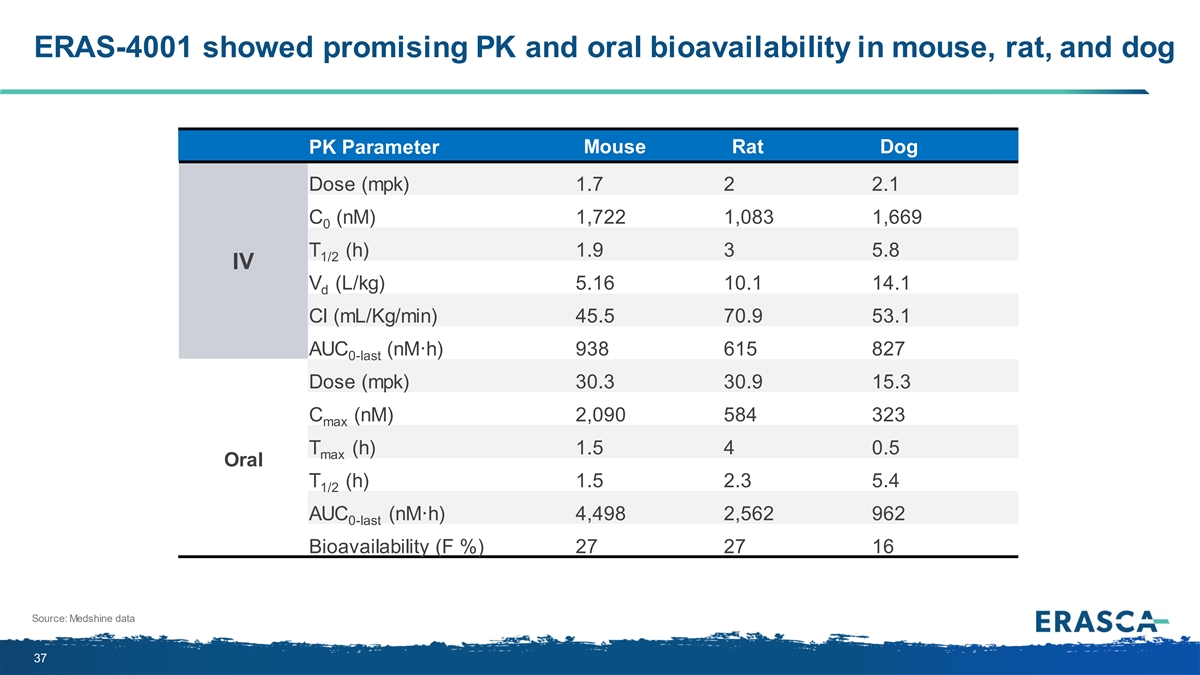
ERAS-4001 在小鼠、大鼠、 和狗 PK 參數中顯示出可觀的 PK 和口服生物利用度。小鼠大鼠狗劑量 (mpk) 1.7 2 2.1 C (nM) 1,722 1,083 1,669 T (h) 1.9 3 5.8 1/2 IV (L/kg) 5.16 10.1 14.1 d Cl (mL/kg) 45.5 70.9 53.1 AUC (n·mH) 0-38 615 827 last 劑量 (mpk) 30.3 30.9 15.3 C (nM) 2,090 584 323 max T (h) 1.5 4 0.5 最大口服 T (h) 1.5 2.3 5.4 1/2 AUC (nm·H) 4,498 2,562 962 0-last 生物利用度 (F%) 27 27 16 來源:Medshine 數據 37
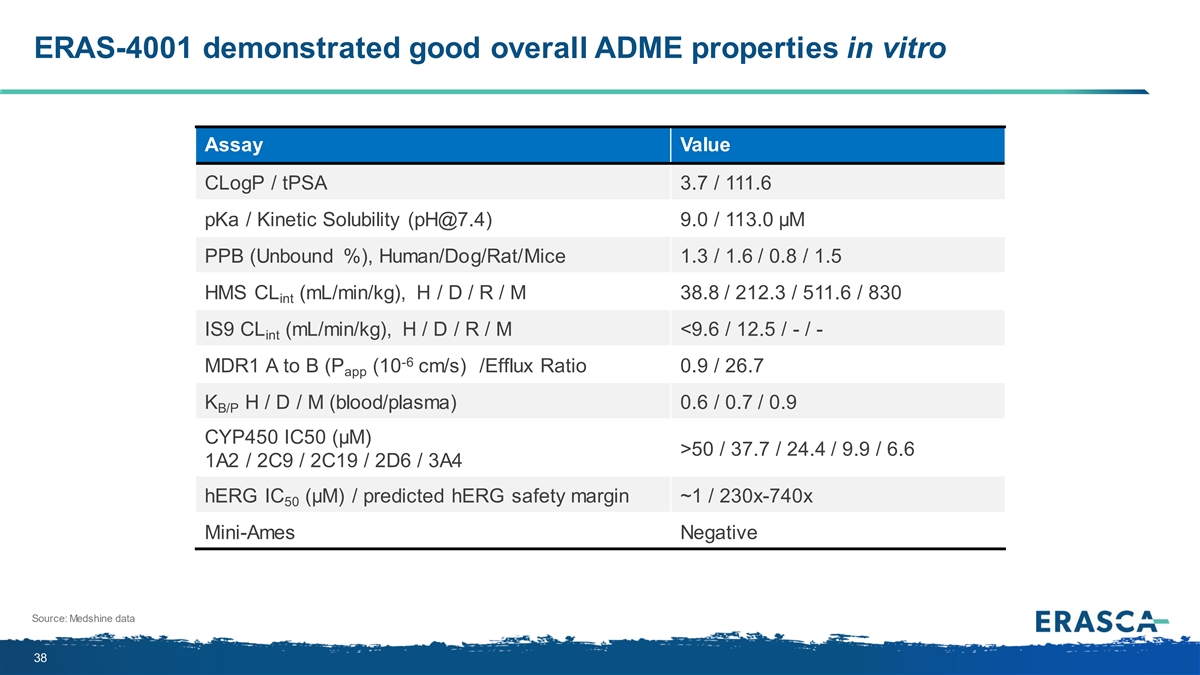
ERAS-4001 在體外分析中表現出良好的整體 ADME 特性 值 cloGP/tpSA 3.7/111.6 pKa/動力學溶解度 (pH @7 .4) 9.0/113.0 µM PPB(未結合百分比),人/狗/大鼠/小鼠 1.3/1.6/0.8/1.5 HMS CL(ml/min/kg),H/D/R/M 38.8/212.3/512.3/512.3/512.3/512.3/512.3/512.3/512.3/MIN 11.6/830 int IS9 CL (mL/min/kg),H/D/R/M 50/37.7/24.4/9.9/6.6 1A2/2C9/2C19/2D6/3A4 HerG IC (µM) /預計的 hERG 安全性 邊距 ~1/230x-740x 50 Mini-Ames 負面來源:Medshine 數據 38
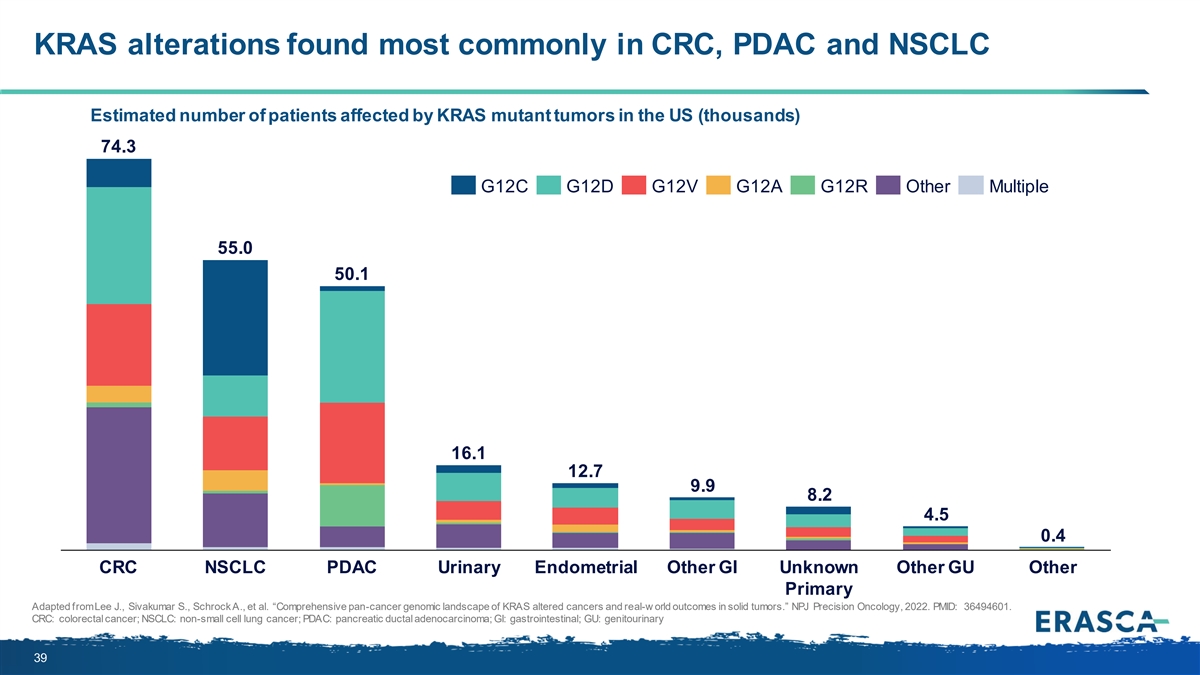
KRAS 變異最常見於 CRC、PDAC 和 NSCLC 中估計 美國受 KRAS 突變腫瘤影響的患者人數(千人)74.3 G12C G12D G12V G12A G12R 其他多發性 55.0 50.1 16.1 12.7 9.9 8.2 4.5 0.4 CRC 非小細胞肺癌 PDAC 尿路子宮內膜其他胃腸道未知其他 GU 其他原發改編自 Lee J., SivAkumar S.、Schrock A. 等“KRAS的全面泛癌基因組格局改變了癌症和實體瘤的真實世界預後。”NPJ 精準腫瘤學,2022年。PMID:36494601。CRC:結直腸癌;NSCLC:非小細胞 肺癌;PDAC:胰腺導管腺癌;胃腸道:胃腸道;GU:泌尿生殖系統 39
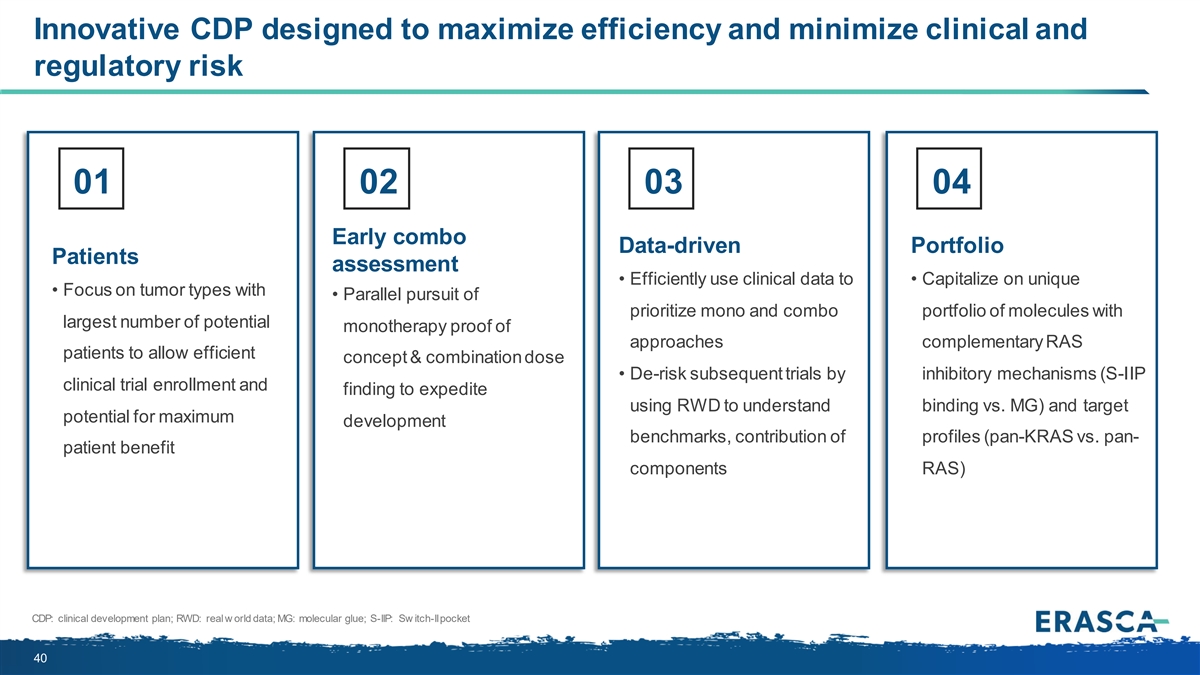
創新的CDP旨在最大限度地提高效率並最大限度地降低臨牀 和監管風險 01 02 03 04 早期組合數據驅動的患者評估 • 有效利用臨牀數據 • 利用獨特性 • 關注腫瘤類型 • 平行追求具有最大潛在單一療法的單一和複方分子組合 方法作為補充 RAS 患者以允許有效的概念和組合劑量 • 通過抑制機制降低後續試驗的風險(S-IIP 臨牀試驗 註冊並加快招生工作使用 RWD 瞭解結合(與 MG)和靶向最大開發基準的潛力、概況的貢獻(Pan-KRA 與全患者福利成分 RAS)CDP:臨牀開發計劃;RWD:真實的 w 世界數據;MG:分子膠水;S-IIP:Sw Itch-II pocket 40

Erasca ERAS-0015 pan-RAS 分子膠的關鍵許可條款 • 許可方:Joyo Pharmatech Co., Ltd. 財務條款金額(百萬美元,特許權使用費除外)• 許可範圍:獨家許可涵蓋 ERAS-0015(預付 12.5 RAS)和許可專利涵蓋的任何其他 Pan-RAS 分子共計 開發里程碑高達 17.5 1 • 領域:所有使用領域監管里程碑總計高達 34 商業里程碑總數高達 125 個 • 地區:全球,不包括中國、香港和澳門;視下文所述的 “中國 收購” 為準銷售 0 2 基於分層銷售的里程碑最多 125 • 中國收購:在第 2 期 FPD 或 NDA 提交之前,Erasca 可隨時根據我們的唯一選擇將該地區轉換為全球交易總價值 一次性付款;付款金額取決於該特許權使用費和中國收購期權的行使時間中國收購和里程碑最多 56 或 156 • IP:物質成分、使用方法的潛在覆蓋範圍 特許權使用費分級(低至中)個位數百分比和製造許可化合物的方法,包括當前的DC,到2043年 1涵蓋美國、歐盟和日本的多個適應症 2 個里程碑,基於淨銷售等級,最高可達 20 億美元 FPD:首例 患者劑量;NDA:新藥申請;DC:開發候選藥物41

Erasca ERAS-4001 Pan-KRAS 抑制劑的關鍵許可條款 Financial 條款金額(百萬美元,特許權使用費除外)• 許可方:Medshine Discovery, Inc. 預付總計 10 • 許可範圍:獨家許可涵蓋 ERAS-4001(總開發里程碑高達 10 KRAS)和 許可專利涵蓋的任何其他 Pan-KRAS 分子 1 總監管里程碑最多 20 個 • 領域:所有使用領域總商業里程碑向上至 130 首次商業銷售 0 • 地區:全球 2 基於銷售的分層里程碑最多 130 • IP:潛在的 覆蓋範圍包括事項、使用方法、不計特許權使用費的總交易價值最多 170 美元以及製造特許化合物的方法,包括當前的 DC,直至 2043 年的特許權使用費低個位數百分比 1 涵蓋美國、歐盟和日本或中國 2 里程碑,基於淨銷售等級,最高可達 30 億美元 DC:發展候選人 42

公司最新消息
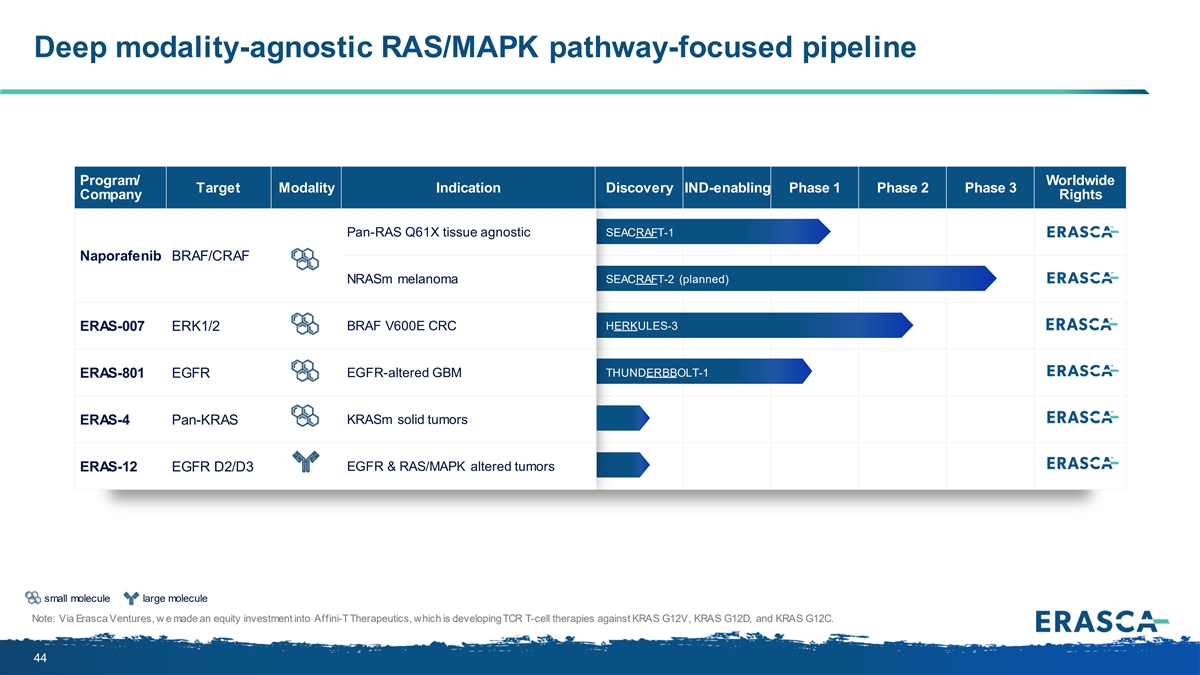
深度模態無關的 RAS/MAPK 以路徑為重點的管道項目/ 全球目標模態適應症發現支持 IND 的第 1 期第 2 期公司版權 pan-RAS Q61X 組織無關 SEACRAFT-1 Naporafenib BRAF/CRAF nRasm 黑色素瘤 SEACRAFT-2(計劃中)BRAF V600E CRC HERKULES-3 ERAS-007 ERK1/2 THUNDERBBOLT-1 ERAS-801 EGFR 表皮生長因子改變的 GBM KRASM 實體瘤 ERAS-4 pan-KRAS EGFR D2/D3 表皮生長因子和 RAS/MAPK 改變了腫瘤小分子大分子注意:我們通過 Erasca Ventures 對 Affini-T Therapeutics 進行了股權投資, ERAS-12開發針對 KRAS G12V、KRAS G12D 和 KRAS G12C 的 TCR T 細胞療法。44

數據驅動的優先順序將精力和資源重新集中在 機會上,以最重要的未滿足需求為目標,患者的 PO 最高 PO 重新調整工作重點行動理由臨牀療效數據不支持對非優先級 HERKULES-3 的持續評估:EC-naive CRC 細分市場中的這種組合此適應症中的這種組合暫停了埃拉斯卡希望將內部資源集中在 rgBM 贊助的試驗系列探索中將內部資源集中在納波拉非尼和 RAS THUNDERBBOLT-1: ERAS-801 上;通過 IST 取得進展 ERAS-0015、ERAS-4001 的許可; select ERAS-007現有的非優先級 ERAS-4:Pan-KRAS 研究計劃分子作為潛在的 ERAS-4001 備用包含在 Pan-KRAS 許可證中。優先開發功能應使埃拉斯卡能夠儘快高效地進行重組約 18% 的進度 最高優先級項目 POS = 成功概率;EC:encorafenib + cetuximab;CRC:結直腸癌;rgBM:複發性膠質母細胞瘤;IST = 贊助的研究者試驗; 45

埃拉斯卡的AURORAS和BOREALIS試驗旨在解決RAS機遇 在任何漫長的航海旅程中,一望無際的大海往往會使人的時間和地點感迷失方向。黎明或極光的出現為新的一天提供了明確的方向感和歡迎信號。在 Erasca, 幫助患者是我們的指路明燈。通過AURORAS和BOREALIS的研究,我們希望我們的強效、選擇性、口服生物可利用的pan-RAS 分子膠水 ERAS-0015 和 pan-KRAS 抑制劑 ERAS-4001 能夠為 (K) Rasm 實體瘤患者帶來益處。1.AURORAS-1 預計將成為初步的 1 期試驗,該試驗將單獨評估 ERAS-0015 pan-RAS 分子膠和 1 種聯合用於治療 RasM 實體瘤患者,其臨牀試驗的目標是在 2025 年上半年進行 2。 BOREALIS-1 預計將成為最初的 1 期試驗,該試驗將單獨評估 ERAS-4001 pan-Krasi 和聯合用於治療 Krasm 實體瘤患者,其臨牀試驗的目標是在 2025 年第一季度進行。注:未來的 AURORA BOREALIS 試驗可能會探討 分子相互組合 1 IND 的時間有待調整(可能移至 2025 年第三季度),主要是詳細的計劃規劃按 CMC 時間軸 46
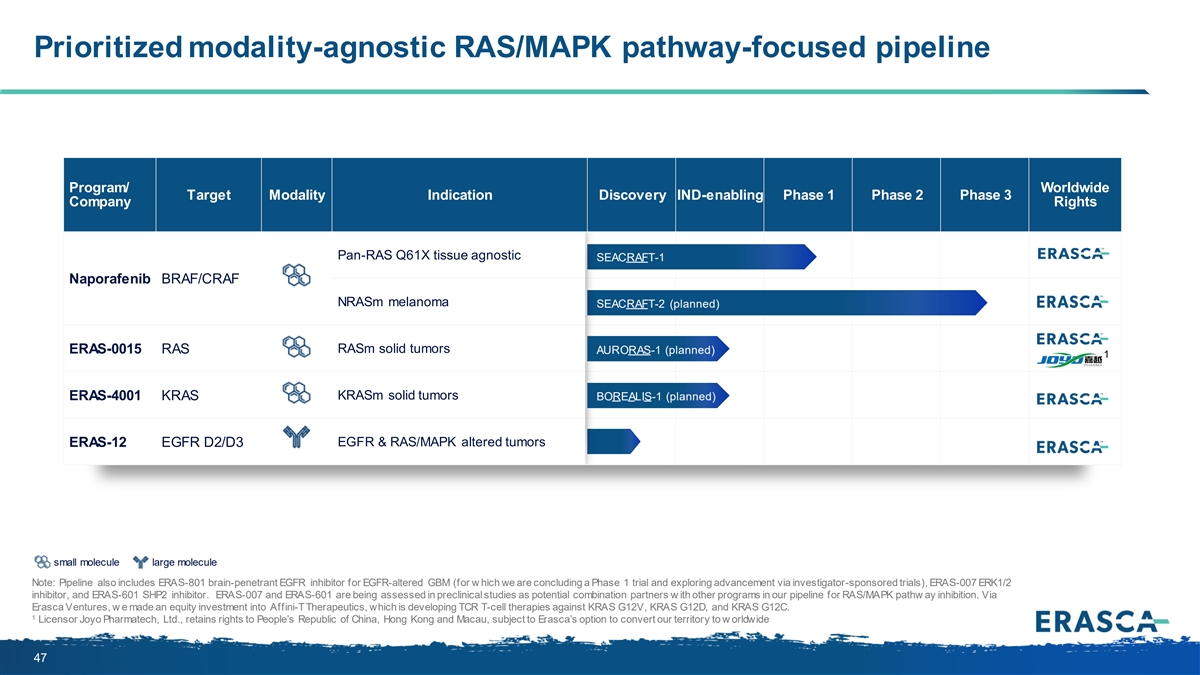
優先與模式無關的 RAS/MAPK 以路徑為重點的管道 計劃/全球靶向模式適應症發現支持 IND 的第 1 期第 2 期第 3 期公司版權 pan-RAS Q61X 組織無關 SEACRAFT-1 Naporafenib BRAF/CRAF nRasm nrasm SEACRAFT-2(計劃中)ERAS-0015 RAS Rasm 實體瘤 AURORAS-1(計劃中)1 ERAS-4001 KRAS KRasm BOREALIS-1 實體瘤(計劃中)EGFR 和 RAS/RASM 實體瘤(計劃中)MAPK 改變的腫瘤 ERAS-12 表皮生長因子 D2/D3 小分子大分子注意:管道中還包括用於表皮生長因子改變的 GBM(用於 w 的腦穿透表皮生長因子抑制劑)ERAS-801正在結束一期試驗,並通過研究者贊助的試驗)、ERAS-007 ERK1/2 抑制劑和 ERAS-601 SHP2 抑制劑探索進展。在臨牀前研究中,ERAS-007 和 ERAS-601 被評估為潛在的組合 合作伙伴,以及我們正在研發的其他 RAS/MAPK 路徑抑制項目。我們通過Erasca Ventures對Affini-T Therapeutics進行了股權投資,該公司正在開發針對KRAS G12V、KRAS G12D和KRAS G12C的TCR T細胞療法。1 許可方Joyo Pharmatech, Ltd. 保留中華人民共和國、香港和澳門的權利,前提是埃拉斯卡選擇將我們的領土改為全球47

預期的關鍵里程碑和臨牀試驗讀數計劃試驗 名稱預期里程碑機制適應症(組合合作伙伴,如果適用)SEACRAFT-1 1 RAS Q61X 實體瘤 • 2024 年第四季度:Ph 1b 組合數據(+ 曲美替尼)Naporafenib pan-RAF 抑制劑 SEACRAFT-2 • 2024 年第二季度:Ph 3 關鍵試驗 啟動 nRasm 黑色素瘤 1 • 2025 年:Ph 3 階段 1 隨機劑量優化數據(+ trametinib)inib) 2 • 2025 年上半年:IND 申報 ERAS-0015 AURORAS-1 3 pan-RAS 分子膠 rasM 實體瘤 • 2026 年:Ph 1 單一療法數據 • 2025 年第一季度: IND 備案 ERAS-4001 BOREALIS-1 3pan-KRAS 抑制劑 krasM 實體瘤 • 2026:Ph 1 單一療法數據 1 數據包括相關人羣中相關劑量的安全性、藥代動力學(PK)和療效 2 IND 的時機有待調整,有待詳細的計劃規劃,主要受CMC時間表驅動 3 在詳細的計劃規劃之前可能會發生變化,但假設美國IND的目標申請時間已經到來,數據將包括安全性,相關人羣的 PK 和 相關劑量下的療效 48

謝謝!