
附錄 99.1

亞當·舍恩菲爾德,紀念斯隆·凱特琳癌症中心,美國紐約州紐約 1.LN-145 TIL 細胞療法加派姆單抗治療ICI患者的多中心二期試驗——天真轉移性非小細胞肺癌亞當·舍恩菲爾德 1;Kai He 2;Jason Chesney 3;Edward Garon 4;Jorge Nieva 5;Adrian Sacher 6;Sylvia Lee 7;弗里德里希·格拉夫·芬肯斯坦 8;Rana Fiaz 8;Melissa Catlett 8;Guang Chen 8;Viktoria Gontcharova 8;Benjamin C. Creelan 9 1 美國紐約州紐約斯隆·凱特琳紀念癌症中心;2 美國俄亥俄州哥倫布市俄亥俄州立大學詹姆斯癌症中心;3 肯塔基州路易斯維爾路易斯維爾大學詹姆斯·格雷厄姆·布朗癌症中心,美國;4 美國加利福尼亞州洛杉磯的加州大學洛杉磯分校;5 美國加利福尼亞州洛杉磯的南加州大學;6 加拿大安大略省多倫多的瑪格麗特公主癌症中心;7 美國華盛頓州西雅圖的弗雷德·哈欽森癌症中心;8 美國加利福尼亞州聖卡洛斯的 Iovance Biotherapeutics, Inc.;9 H. Lee Moffitt 癌症中心和研究所,佛羅裏達州坦帕;9 H. Lee Moffitt 癌症中心和研究所,美國佛羅裏達州坦帕

亞當·舍恩菲爾德,紀念斯隆·凱特琳癌症中心,美國紐約州紐約 2.IOV-COM-202 3A:LN-145 + anti-145 + anti — PD-1 在 ICI 中——天真 mnSCLC 合併強效免疫療法模式 1.Schoenfeld A 等人J. 2021 年 Immunother Cancer;9(補編 2): A458。2.Creelan BC 等人Nat Med 2021;27 (8): 1410 — 1418。a 每 8 — 12 小時(完成 LN 輸液後 3-24 小時——145 次輸液)。CY,環磷酰胺;EOA,評估結束;EOS,研究結束;EOT,治療結束;流感,氟達拉濱;GMP,Good Manufactu rin g Practe;ICI,免疫檢查點抑制劑;IU-2,白介素-2;IU,國際單位;mnsCLC,轉移性非小細胞肺癌;NMA-LD,非髓系消融性淋巴癌耗盡;PD-1,程序性細胞死亡蛋白 1;PD-L1,程序性死亡 h 配體-1;TIL,腫瘤——浸潤淋巴細胞。LN-145 製造的篩查入組/腫瘤組織採購單劑量 Pembrolizumab(200 mg 或 400 mg)NMA-LD 日-7 至第 6 天:CY(每天 60 mg/kg i 2 劑 i 2 劑量)第 5 天-1:流感(25 mg/m 2 每日 5 劑)LN-145 輸液第 0 天(1 × 10 9 到 150 × 10 9 細胞)伊利諾伊州-2 天 0 或 1 天至第 3 天或 4 ≤6 劑量 a(600,000 IU/kg)Pembrolizumab Q3W(200 mg)或 Q6W(400 mg),持續 ≤24 個月療效隨訪——長期隨訪——向上圖 1。治療方案和 IL-2 種給藥方法和目標 • IOV-COM-202 (NCT03645928) 是一項針對實體瘤患者的自體 TIL 細胞療法的全球性 2 期、多中心、多隊列開放標籤研究 • 隊列 3A 包括抗-PD-1/PD-L1 天真的局部晚期或轉移性非小細胞肺癌患者並伴有疾病進展 • 我們報告了 3A 隊列中接受治療的患者的數據 LN-145 plus pembrolizumab(圖 1)GMP 製造(22 天)評估期:EOA EOA EOT 進展或新療法簡介的第 0 天 • 受益於前線 ICI ± mnsCLC 患者的化療受到原發耐藥和繼發耐藥性的限制 • TIL 細胞療法對經過廣泛預處理的 mnSCLC 患者產生了持久的客觀反應 1,2 • 將 TIL 細胞療法整合到一線方案中可能會改善長期益處

亞當·舍恩菲爾德,紀念斯隆·凱特琳癌症中心,美國紐約州紐約 3.特徵隊列 3A(N=19)中位年齡,y(最小,最大)55.4(35、68)從不吸煙,n(%)a 7(36.8)按先前治療亞組劃分的全身治療中位數,n(最小、最大)1(0、4)治療——天真(n=5)b 0(0,1)化療後(n=7)c 1(1,3) 表皮生長因子突變後——TKI (n=7) d 2 (1, 4) 非鱗狀組織學細胞類型,n (%) e 18 (94.7) 驅動突變——陽性,n (%) f 13 (68.4) EGFR 7 (36.8) KRAS g 6 (31.6) NTRK 1 (5.3) PD-L1 腫瘤比例分數,n (%) h

亞當·舍恩菲爾德,美國紐約州紐約紀念斯隆·凱特琳癌症中心 4. • 研究隨訪中位數為18.2個月 • 76.5%的患者腫瘤負擔減輕了(圖2)• ORR為42.1%(表4);先前治療的ORR為:• 治療——天真:80.0%(4/5)• 化療後:42.9%(3/7)• EGFR-帖子——TKI:14.3%(1/7)• 治療——天真或化療後:58.3%(7/12)最佳總體反應隊列 3A(N=19)n/n%(95% 置信區間)ORR 8/19 42.1(20.3、66.5)DCR 15/19 78.9(54.4、93.9)CR 2/19 10.5 PR 6/19 31.6 SD 7/19 36.8 PR 2/1910.5 NE 2/19 10.5 表 4。最佳總體反應結果:ICI 的臨牀療效——天真的 mnSCLC 反應(RECIST v1.1)獨立於 PD — L1 狀態 *PD-L1 狀態(%),根據現場報告數據和中心實驗室數據進行裁定。CR,完全反應;DCR,疾病控制率;ICI,免疫檢查點抑制劑;mnSCLC,轉移性非小細胞肺癌;NE,不可評估;ORR,客觀反應率;PD-L1,程序性死亡配體-1;PD,進行性疾病;PR,部分反應;SD,穩定疾病;SOD,直徑之和;TKI,酪氨酸激酶抑制劑。圖 2。可評估患者的目標病變 SOD 與基線相比變化的最佳百分比 ORR(95% 置信區間):80.0%(28.4%,99.5%)ORR(95% 置信區間):14.3%(0.4%,57.9%)100 80 60 40 20 0-20-40-60-100 治療-天真後-化療後表皮生長因子-突變後-TKI ≥50*
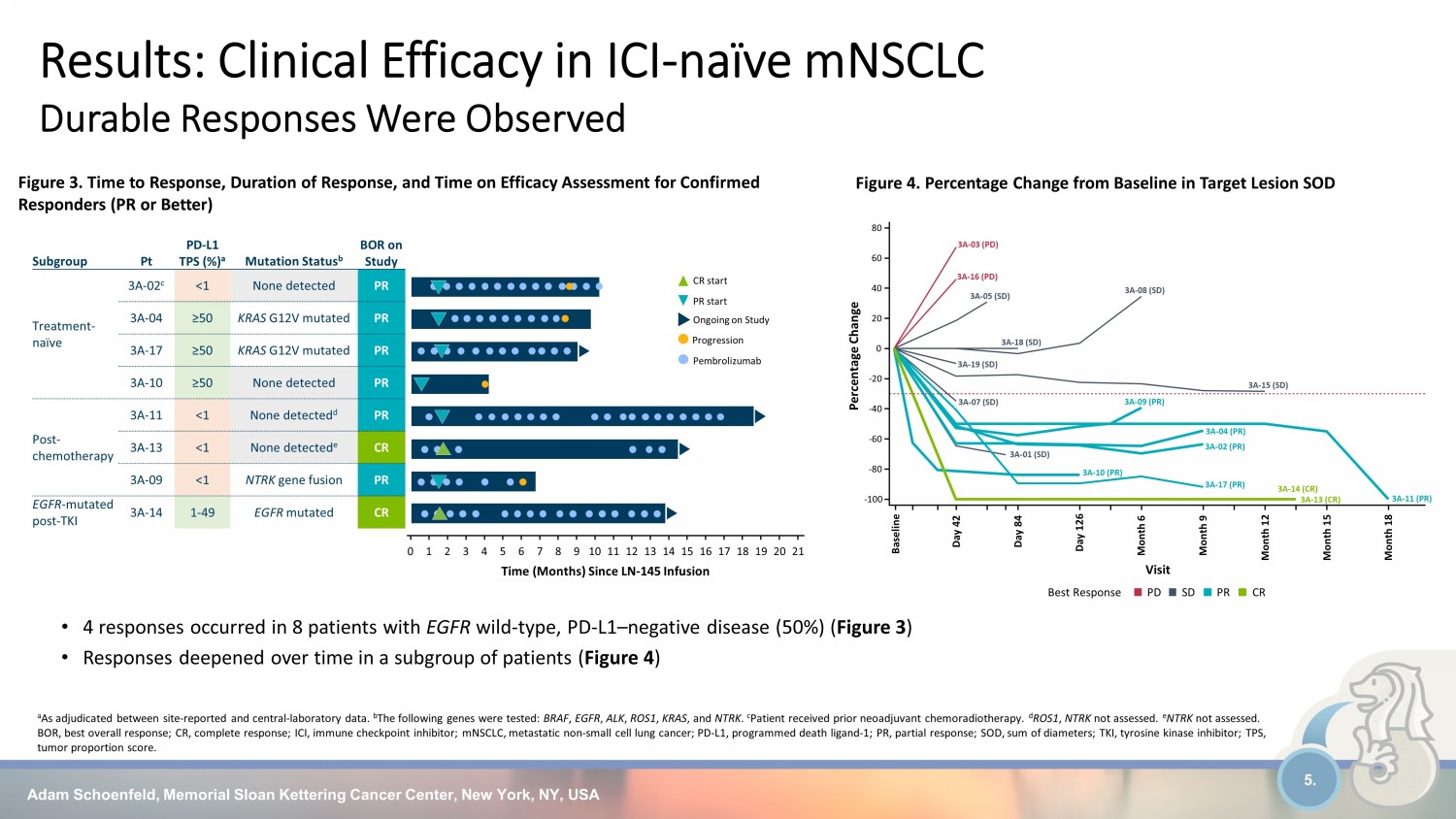
亞當·舍恩菲爾德,紀念斯隆·凱特琳癌症中心,美國紐約州紐約 5.結果:ICI 的臨牀療效——觀察到天真的 mnsCLC 持久反應 a 根據報告部位和中心實驗室數據之間的判斷。b 測試了以下基因:BRAF、EGFR、ALK、ROS1、KRAS 和 NTRK。c 患者先前接受過新輔助化療。d ROS1,NTRK 未評估。e NTRK 未評估。BOR,總體反應最佳;CR,完全反應;ICI,免疫檢查點抑制劑;mnSCLC,轉移性非小細胞肺癌 er;PD-L1,程序性死亡配體-1;PR,部分反應;SOD,直徑之和;TKI,酪氨酸激酶抑制劑;TPS,腫瘤比例評分。圖 3。確診應答者的反應時間、反應持續時間和療效評估時間(PR或更好)• 8例表皮生長因子野生型、PD-L1——陰性疾病(50%)的患者出現了4種反應(圖3)• 一組患者的反應隨着時間的推移而加深(圖 4)圖 4。目標病變 SOD CR PR SD PR SD PR 3A-16 (PD) 3A-03 (PD) 3A-15 (SD) 3A-15 (SD) 3A-19 (SD) 3A-18 (SD) 3A-05 (SD) 3A-07 (SD) 3A-08 (SD) 3A-01 (SD) 3A-04 (PR) 3A-11 (PR) 3A-11 (PR) 3A-11 (PR) 3A-07 (SD) 3A-08 (SD) 3A-01 (SD) 3A-04 (PR) 3A-11 (PR) 3A-11 (PR) 3A-17 (PR) 3A-02(PR)3A-10(PR)3A-09(PR)3A-14(CR)3A-13(CR)基準日 42 天 84 天 126 個月 6 月 9 個月 12 個月 15 個月 18 訪問-100-80-60-40-20 0 20 40 60 80百分比變化最佳反應亞組 Pt-L1 TPS (%) a 突變狀態 b 研究中 BOR 治療——天真 3A-02 c

Adam Schoenfeld,紀念斯隆·凱特琳癌症中心,美國紐約州紐約 6。• 注入 TIL 產品的克隆體在應答者和非應答者中同樣存在(圖 5)* 條形代表標準誤差。TCR,T-細胞受體;TIL,腫瘤-浸潤淋巴細胞。圖 5。注入 TIL* 注入 TICR 克隆型的持續時間和注入的細胞劑量 TIL 在外周血和細胞劑量中持續存在的反應沒有差異 • 應答者和無反應者中注入的細胞總劑量相似(圖 6)圖 6。細胞總劑量時間百分比 TCR Repertoire 輸液前第 4 天 0 50 100 天 42 無反應者響應者總劑量(十億)0 20 40 60 p = 0.62

• 在 ICI(天真 mnSCLC)患者中,LN-145 加上 pembrolizumab 的活性大於先前報道的 LN-145 單一療法或單獨使用pembrolizumab的活性,並且不受PD-L1 TPS的限制 • 總體而言,ORR為42.1% • 治療——天真:80.0%(4/5)• 化療後:42.9%(3/7)• 化療後:42.9%(3/7)• 表皮生長因子突變後——TKI:14.3%(1/7)• 治療——天真或化療後:58.3%(7/12)• 表皮生長因子野生長——型,PD — L1 — 陰性疾病:50.0%(4/8)• 在 LN-145 方案中添加pembrolizumab後未觀察到新的安全信號 • 耐用且觀察到反應加深(長達15.4個月且持續),輸液後TIL克隆仍然存在 • 在為應答者和無反應者注入的細胞劑量方面沒有觀察到任何差異 • 這些結果支持了對ICI中145的LN——天真mnSCLC的進一步臨牀研究,併為LN-14 5的3期研究的設計提供了依據,該研究已添加到mnsCLC患者一線護理治療標準中 Adam Schoenfeld,Memorial Sloenfeld,Memorial Sloenfeld 美國紐約州紐約市凱特琳癌症中心 7.ICI,免疫檢查點抑制劑;mnSCLC,轉移性非小細胞肺癌;ORR,客觀反應率;PD-L1,程序性死亡配體-1;TKI,酪氨酸激酶抑制劑;TPS,腫瘤比例評分。試驗結論 TIL 細胞療法活性可能獨立於 ICI 中的 PD — L1 狀態——天真 mnSCLC 通過 QR(快速響應)和/或文本密鑰代碼獲得的本演示文稿的副本僅供個人使用,未經作者書面許可,不得複製。