

附錄 99.2 2023 年 11 月公司演講

法律披露本演示文稿包含前瞻性陳述, 所有這些陳述均受本警示性陳述的全面限制。此處包含的許多前瞻性陳述可以通過使用前瞻性詞語來識別,例如可能、預期、相信、可能、預期、應該、 計劃、打算、估計、將來、潛在和持續等,儘管並非所有前瞻性陳述都包含這些識別詞。這些前瞻性陳述包括有關我們的研發項目以及我們當前和未來的臨牀前研究和臨牀試驗的啟動、時間、進展、結果、 和成本的陳述,包括關於啟動和完成研究或試驗的時間以及相關準備工作的陳述、試驗結果公佈的 期以及我們的研發計劃;我們成功製造臨牀前藥物和候選產品的能力,對於臨牀試驗和更大規模的 商業用途(如果獲得批准);我們的第三方戰略合作者繼續與我們的候選開發和產品相關的研發活動的能力和意願;我們為完成候選產品的進一步開發和商業化所必需的運營獲得 資金的能力;我們獲得和維持候選產品的監管批准的能力; 候選產品的市場規模和增長潛力,還有我們的為這些市場服務的能力;我們的財務業績;以及我們的商業模式的實施,以及針對我們的業務和候選產品的戰略計劃。除非另有説明,否則這些前瞻性 陳述僅代表截至本演講之日,我們沒有義務更新或修改任何此類陳述以反映本演示之後發生的事件或情況。由於前瞻性陳述 本質上受風險和不確定性的影響,其中一些是無法預測或量化的,有些是我們無法控制的,因此您不應依賴這些前瞻性陳述作為對未來事件的預測。有關 這些風險和不確定性以及其他重要因素的討論,其中任何一個都可能導致我們的實際業績與前瞻性陳述中包含的有所不同,請參閲我們最近向美國證券交易委員會提交的10-K表年度報告和10-Q表季度報告中標題為 “風險因素” 的章節,以及我們隨後向美國證券交易委員會提交的其他文件中對潛在風險、不確定性和其他重要因素的討論 交易所委員會。我們的前瞻性陳述中反映的事件和情況可能無法實現或發生,實際結果可能與前瞻性陳述中的預測存在重大差異。我們提醒您不要過分依賴本演示文稿中包含的前瞻性陳述。本演示文稿討論了正在進行臨牀前或臨牀評估且尚未獲得美國食品和 藥物管理局或任何其他監管機構批准上市的候選產品。在臨牀研究報告最終確定之前,此處提供的臨牀試驗數據仍有待根據臨牀現場審計和其他審查流程進行調整。 未就這些候選產品的安全性或有效性作出任何陳述,以供研究此類候選產品的用途。根據任何此類州或其他司法管轄區的證券法,在註冊或獲得資格認證之前,在任何州或其他司法管轄區的要約、招標或出售為非法的州或其他司法管轄區,本演示不構成賣出要約或徵求買入要約,也不得出售 任何此類證券。2
Aura Biosciences重點介紹病毒樣藥物偶聯物-用於治療實體瘤的新型 藥物——雙重作用機制:靶向細胞毒性和免疫激活(VDC)——與美國食品藥品管理局達成的特別協議評估(SPA)協議:-全球Ph 3研究設計和分析支持初級 脈絡膜黑色素瘤眼部腫瘤系列的監管申報——Ph 2數據支持Ph 3研究的假設(功率為95%)-全球Ph 3 正在進行中,美國有許多站點已啟用-我們認為初步數據支持雙重諒解備忘錄,並且經組織病理學泌尿外科腫瘤學特許經營權證實單劑後免疫 激活——更新後的協議包括NMIBC和MIBC——目前的現金流預計將為2025年下半年的運營提供資金強勁的現金狀況 3
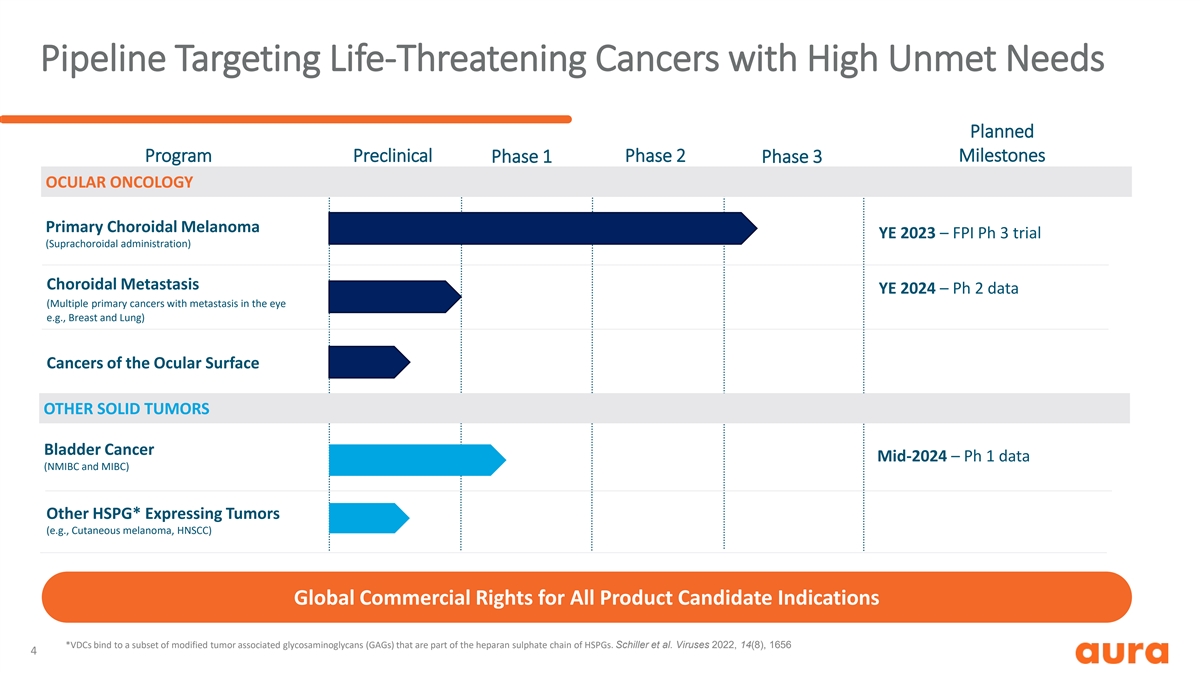
針對需求量高的危及生命的癌症的管線 計劃中的里程碑計劃臨牀前 1 期 2 期 3 期眼部腫瘤原發性脈絡膜黑色素瘤 YE 2023 — FPI Ph 3 試驗(脈絡膜上給藥)脈絡膜轉移 YE 2024 — Ph 2 數據(眼部有 轉移的多種原發性癌症,例如乳腺和肺部)眼表癌其他實體性膀胱腫瘤癌症 2024 年中期 — Ph 1 數據(NMIBC 和 MIBC)其他 HSPG* 表達腫瘤(例如皮膚黑色素瘤、HNSCC)所有 產品的全球商業權候選適應症 *VDC 與一部分改性腫瘤相關糖胺聚糖 (GAG) 結合,這些糖胺聚糖是 HSPG 硫酸肝素鏈的一部分。席勒等病毒 2022, 14 (8), 1656 4

靶向腫瘤學平臺:病毒樣藥物偶聯物(VDC)潛在的 治療病毒樣顆粒與腫瘤相關 HSPG* 選擇性結合到細胞毒性載荷多實體瘤 Cx 病毒樣藥物病毒樣顆粒細胞毒性藥物偶聯物(VDC)(VLP)潛在的關鍵區別:效力、 多價結合和選擇性 Kines 等人;《國際癌症雜誌》,138; 901—911,2016 年 2 月;Kines 等人;分子癌症療法,2018 年 2 月 17 (2) 日;Kines 等人;癌症免疫學研究,2021 年 5 月 5 *VDC 與 改性腫瘤相關糖胺聚糖 (GAG) 的子集,它們是 HSPG 硫酸肝素鏈的一部分。席勒等病毒 2022, 14 (8), 1656
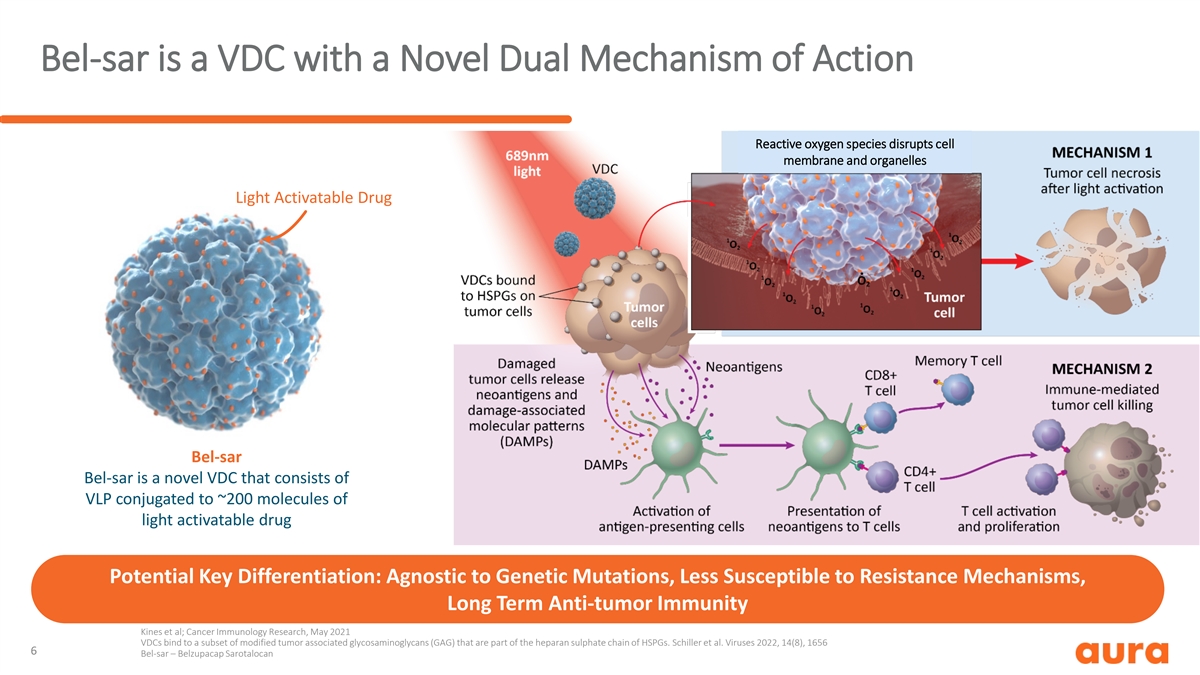
Bel-SAR 是一種具有新型雙重作用機制的 VDC 活性氧 物種破壞細胞膜和細胞器光活化藥物 Bel-SAR Bel-SAR 是一種新型 VDC,由與約 200 個光活化藥物分子偶聯的 VLP 組成,潛在的關鍵區別:不受基因突變影響,不易受耐藥機制影響,長期抗腫瘤免疫 Kines 等;癌症免疫學研究,2021 年 5 月 VDC 與一部分改性腫瘤相關糖胺聚糖 (GAG) 結合,這些糖胺聚糖是 HSPG 硫酸肝素鏈的一部分。 席勒等人。病毒 2022, 14 (8), 1656 6 Bel-sar — Belzupacap Sarotalocan

眼部腫瘤學 Bel-SAR 特許經營店:belzupacap sarotalocan 靶標 適應症:• 早期脈絡膜黑色素瘤 • 脈絡膜轉移 • 其他眼癌 7
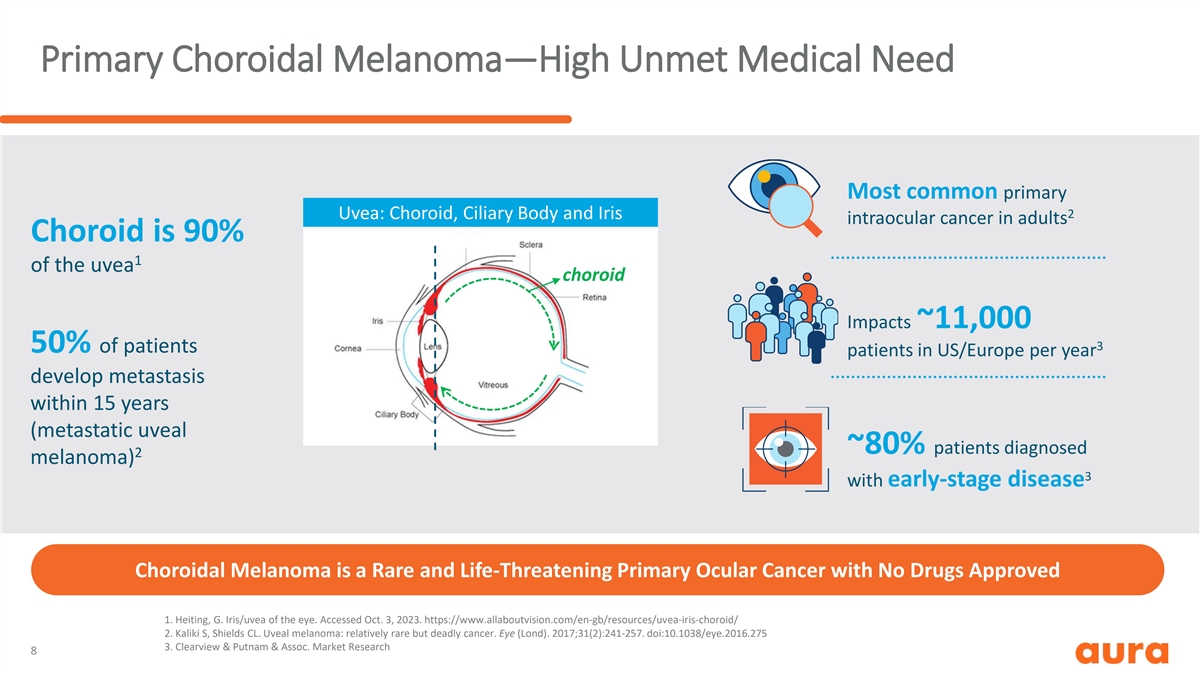
原發性脈絡膜黑色素瘤——高未得到滿足的醫療需求最常見的 原發性葡萄膜:成人的脈絡膜、睫狀體和虹膜 2 眼內癌脈絡膜是 90% 1 的葡萄膜脈絡膜影響約為 11,000 3 50% 的患者在 15 年內出現轉移(轉移性葡萄膜 ~ 80% 患者 被診斷為 2 黑色素瘤)3 伴有耳朵慢性病脈絡膜黑色素瘤是一種罕見且危及生命的原發性眼癌,未獲批准任何藥物 1.Heiting,G. Iris/UVEA of the eye。已於 2023 年 10 月 3 日訪問。 https://www.allaboutvision.com/en-gb/resources/uvea-iris-choroid/ 2.Kaliki S,Shields CL。葡萄膜黑色素瘤:相對罕見但致命的癌症。眼睛(倫敦大學)。2017;31 (2): 241-257. doi: 10.1038/eye.2016.275 3.Clearview & Putnam & Assoc。市場 研究 8

放射治療是早期疾病的護理標準。脈絡膜黑色素瘤的近距離放射治療需要進行具有不可逆轉併發症的侵入性手術 2 (A) 示意圖顯示了協作性眼部黑色素瘤研究 (COMS) 式斑塊使用縫合在鞏膜上的釕106斑塊近距離療法 1 對大型 脈絡膜黑色素瘤進行手術治療上面覆蓋葡萄膜黑色素瘤(B)術中照片,顯示COMS斑塊到位。斑塊在原位停留 3 1 到 7 天黃斑病變、 白內障、青光眼、玻璃體脱落和玻璃體出血 3 是近距離放射治療中常見的威脅視力的併發症 1。最新。葡萄膜黑色素瘤的斑塊近距離放療。已於 2023 年 9 月 20 日訪問。 https://ykhoa.org/d/image.htm?imageKey=ONC/116591 2.Kim M,Lee SM,Lee。大型脈絡膜黑色素瘤的手術治療。美國驗光學會2022年視頻節目。2023 年 3 月 1 日。已於 2023 年 9 月 20 日訪問。 https://www.aao.org/education/annual-meeting-video/surgical-treatment-of-large-choroidal-melanoma 9 3.Peddada KV、Sangani R、Menon H、Verma V. 眼部黑色素瘤斑塊近距離放射治療的併發症和不良事件。J Contemp 近距離放射療法。 2019; 11 (4): 392-397. doi: 10.5114/jcb.2019.87407

接受放射治療後,高達 87% 的患者會失明 對比度在近距離放射治療後的第一年合法失明(BCVA)的患者比例範圍內顯著降低,並且繼續保持近距離放射治療後合法盲人 1、d 2 (BCVA ≤20/200) 的患者比例 隨時間推移在短距離治療後的 1、2 ≤20/200) 100% 80% 40% 20% 基準年 0% 第 2 年第 3 年正常視力下降的長期視力對比度靈敏度視力、色覺和對比度靈敏度在正常視力範圍內顯著下降 治療後的第一年,並隨着時間的推移繼續減少 1.Jarczak J、Karska-Basta I、Romanowska-Dixon B. 葡萄膜黑色素瘤的近距離放射治療和質子治療後的視力下降以及對抗這種 併發症的方法,根據最近的出版物。醫學(考納斯). 2023; 59 (6): 1131. 2.Tsui I、Beardsley RM、McCannel TA、Oliver SC 等對脈絡膜和 纖體黑色素瘤進行碘125近距離放射三年後的視力、對比敏感度和色覺。Open Ophathalmol J. 2015;9:131-5. 10

放射治療的益處/風險驅動 早期疾病早期晚期轉移性疾病 2 不確定病變和小型 PCM 中型/大型 PCM (~2,000) 1 1 (~8,000) (~2,300) 觀察並等待/近距離放射治療系統化療近距離放療:視力喪失/失明 (KIMMTRAK) 不可避免地是可解決的問題由於與治療相關的視力喪失和嚴重合並症的風險,人羣未接受治療 1.Clearview & Putnam & Assoc。市場研究 11 2.Kaliki S,Shields CL。葡萄膜黑色素瘤:相對 罕見但致命的癌症。眼部(倫敦大學)。2017;31 (2): 241-257。doi: 10.1038/eye.2016.275 當前患病率:治療患者美國/歐盟
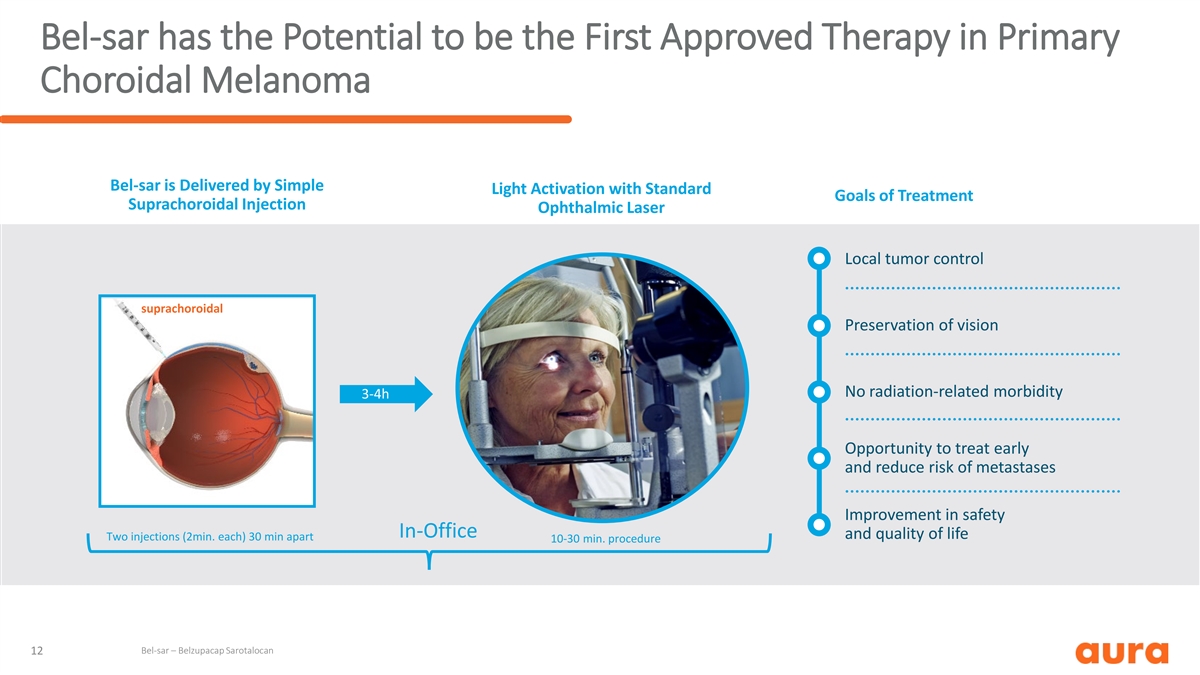
Bel-sar 有可能成為首款獲批准的原發性 脈絡膜黑色素瘤療法 bel-SAR 通過簡單的光激活提供,具有治療的標準目標眼科激光局部腫瘤控制脈絡膜上腔保持視力無輻射相關發病率 3-4h 機會 早期治療並降低轉移風險改善辦公室安全性和生活質量兩次注射(2 分鐘)每) 間隔 30 分鐘 10-30 分鐘手術 Bel-sar — Belzupacap Sarotalocan 12

眼部腫瘤特許經營權代表着數十億美元的潛在市場機會 每年約 66,000 名患者/年 11,000 名患者/年眼部腫瘤特許經營權總潛在市場(美國/歐盟)每年診斷的脈絡膜黑色素瘤患者(美國/歐盟)3 1 ~35,000 名患者/年 11,000 名患者當前的放射治療 ~ 80% 患者的眼表癌脈絡膜黑色素瘤的治療是確診後,約 87% 的患者在早期階段會出現數十億美元的嚴重不可逆視力喪失(不確定病變(IL)和小腫瘤)市場 機會
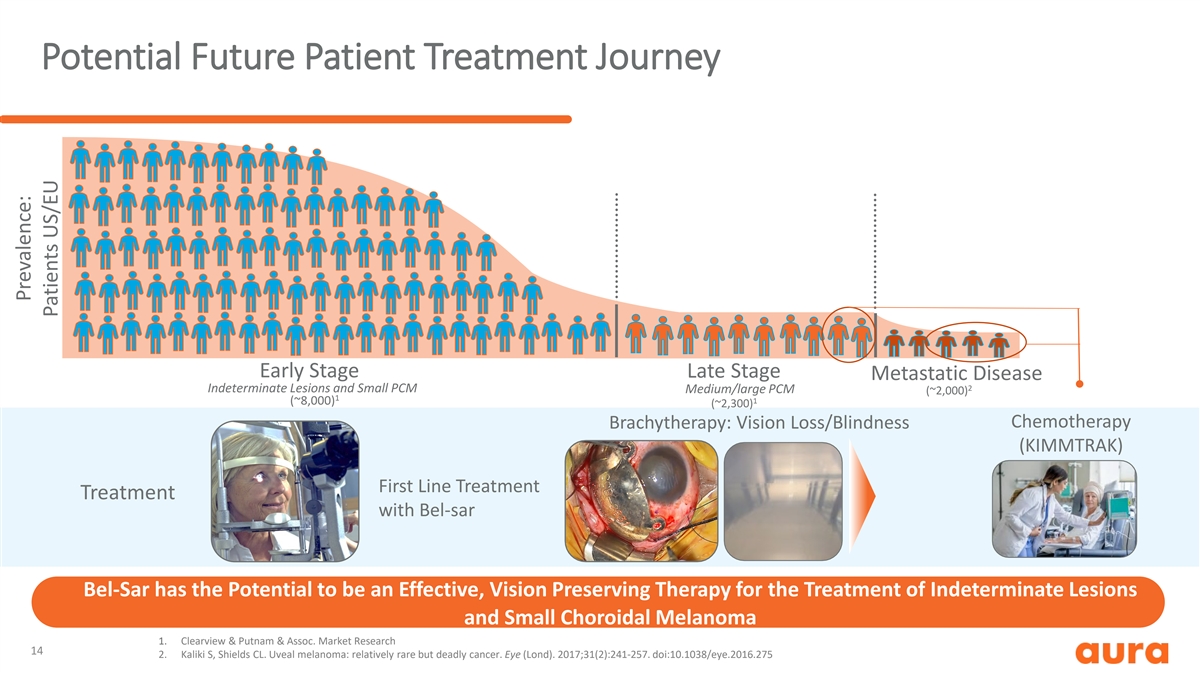
潛在的未來患者治療歷程早期晚期 轉移性疾病 2 不確定病變和小中型/大型 PCM (~2,000) 1 1 (~8,000) (~2,300) 化療近距離放療:Bel-SAR Bel-Sar 的一線治療有可能成為治療不確定病變的 有效視力保持療法和小脈絡膜黑色素瘤 1.Clearview & Putnam & Assoc市場研究 14 2.Kaliki S,Shields CL。葡萄膜黑色素瘤:相對罕見但致命的癌症。Eye (倫敦)。2017;31 (2): 241-257。doi: 10.1038/eye.2016.275 患病率:患者美國/歐盟

Bel-sar 在治療 早期疾病方面表現出良好的形象 Darovasertib + Crizotinib 1 KIMMTRAK Bel-Sar 2 組合不良事件或不良反應任何等級任何級別*細胞因子釋放綜合徵 89% 未披露 0% 皮疹 83% 未披露 0% 瘙癢 69% 未披露 0% 疲勞 64% 40% 噁心 0% 79% 0% 嘔吐未披露 52% 0% 寒戰 48% 未披露 0% 減退/色素沉着 47% 未披露 0% 腹痛 45% 未披露 0% 水腫 45% 57% 0% 痤瘡樣皮炎不 已披露 44% 0% 低血壓未披露 34% 0% 低白蛋白血癥未披露 32% 0% 頭暈未披露 28% 0% 1。Immunocore 公司介紹。2023 年 8 月。幻燈片 12。 https://ir.immunocore.com/static-files/415c5cbb-caae-4ffa-9beb-cb40cfcfc132 2.IDEAYA 臨牀最新簡報。2023 年 4 月 24 日。幻燈片 10。注意:本演示文稿中的某些數據基於跨試驗比較,並非基於任何 頭對頭臨牀試驗。交叉試驗比較本質上是有限的,可能暗示誤導性的相似或差異。正面比較的結果可能與此處列出的結果有顯著差異。15 *幻燈片 22 中顯示了 正在進行的使用 bel-sar 進行的 Ph2 研究的安全結果

脈絡膜黑色素瘤 Ph 2 數據 16
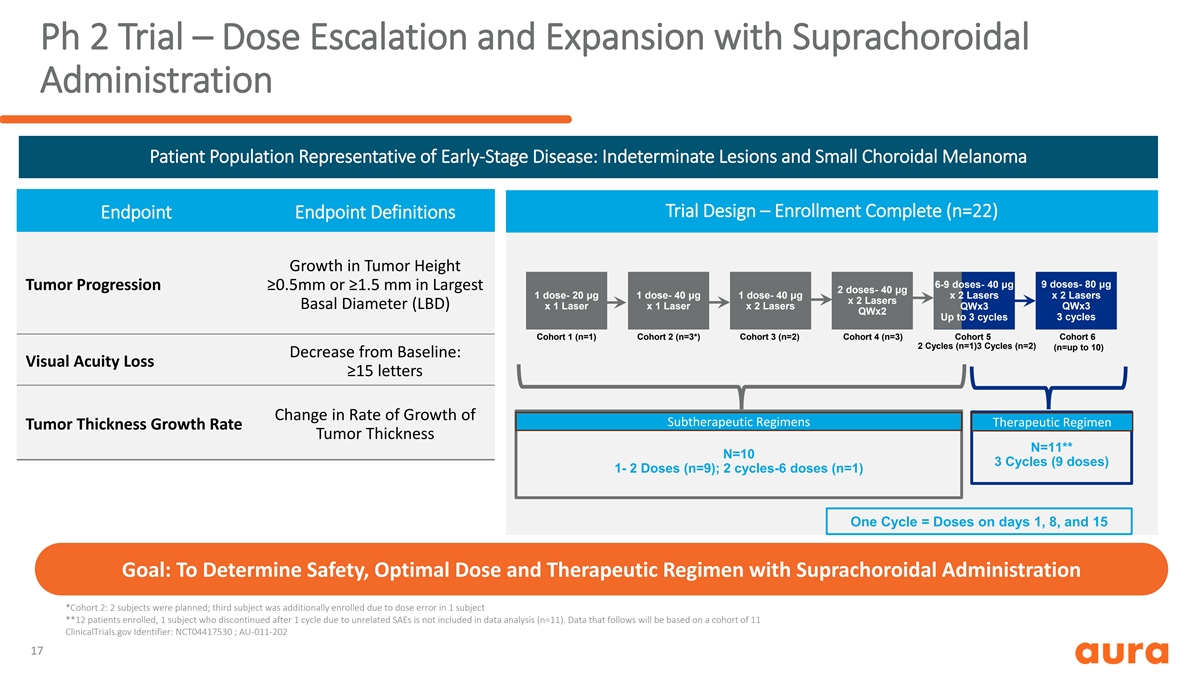
Ph 2 試驗 — 劑量遞增和擴大,使用上腔體 給藥患者羣體代表性早期疾病:不確定病變和小脈絡膜黑色素瘤試驗設計 — 註冊完成 (n=22) 終點定義腫瘤高度增長 9 劑量-80 μg 6-9 劑量-40 μg 腫瘤進展 ≥0.5mm 或 ≥1.5 mm,最大劑量 2 劑-40 μg 1 劑量-20 μg 1 劑量-20 μg 40 μg 1 劑量-40 μg x 2 激光器 x 2 個激光器基礎直徑 (LBD) x 1 激光 x 1 個激光 x 2 個激光器 qwx3 qwx2 最多 3 個週期 3 個週期 3 個週期隊列 1 (n=1) 隊列 2 (n=3*) 隊列 3 (n=2) 隊列 4 (n=3) 隊列 6 2 個週期 (n=1) 3 個週期 (n=2)(n = 最多 10)較基線下降:視力喪失 ≥ 15 個字母 亞治療方案生長速度的變化治療方案腫瘤厚度增長率腫瘤厚度 N=11** N=10 3 個週期(9 劑量)1-2 劑量(n=9);2 個週期-6 劑量(n=1)一個週期 = 第 1、8 和 15 天的劑量目標:確定安全性、最佳劑量和 使用上絡膜給藥的治療方案 *隊列 2:計劃了 2 名受試者;第三名受試者由於劑量而額外入組1 名受試者的錯誤 **12 名入組患者,1 名因無關的 SAE 而在 1 個週期後停止治療的受試者 不包括在數據分析中(n=11)。以下數據將基於 11 個 ClinicalTrials.gov 組成的隊列標識符:NCT04417530;AU-011-202 17

觀察到較高的腫瘤控制率 — 在 12 個月內可持續 向上劑量反應:> 90% 已完成 12 個月亞治療與治療方案患者總數腫瘤控制劑量/方案 (n) 率 100% 亞治療方案 80% 80% 單劑量最多 2 個週期 10 20% (2/10) 60% 治療方案 3 個週期 (n=11) 11 73% (8/11) 40% 3 個週期和 Ph 3 合格 (n=10) * 10 80% (8/10) 20% 20% * 不包括 1 名患有環乳頭狀腫瘤但不符合 Ph 3 標準的受試者 0% 最多 2 個週期方案 (n=10) 3 個週期方案 (n=10) 腫瘤進展: 變化2023 年 8 月 3 日,存檔數據 Aura Biosciences 對於 Ph 3 符合條件且具有活性 生長活躍的患者的治療方案具有較高的腫瘤控制率和治療方案;在 2023 年 8 月 3 日的至少一次重複評估中證實了 LBD ≥1.5mm

在使用 治療方案亞治療方案(n=10)活性生長和三週期方案(n=10)治療的 Ph 3 人羣中觀察到的腫瘤控制率較高的腫瘤控制率在 12 個月內腫瘤厚度與基線相比變化 12 個月內腫瘤厚度與基線的變化 2.00 1.75 1.50 1.25 0.00 0.25 -0.50 0 90 180 270 360 450 治療隨訪時間框架時間框架有入院時生長記錄的患者 (n=6) 入院時有生長記錄的患者 (n=10) 沒有 記錄的患者入學時生長(n=4)進展定義基於腫瘤厚度(增大 ≥0.5mm)進展定義基於腫瘤厚度(增大 ≥0.5mm)2023 年 8 月 3 日,存檔數據 Aura Biosciences Ph 2 臨時數據 顯示腫瘤控制率為 80%,隨訪 12 個月時 90% 的患者腫瘤厚度(mm)與基線相比腫瘤厚度(mm)變化 19
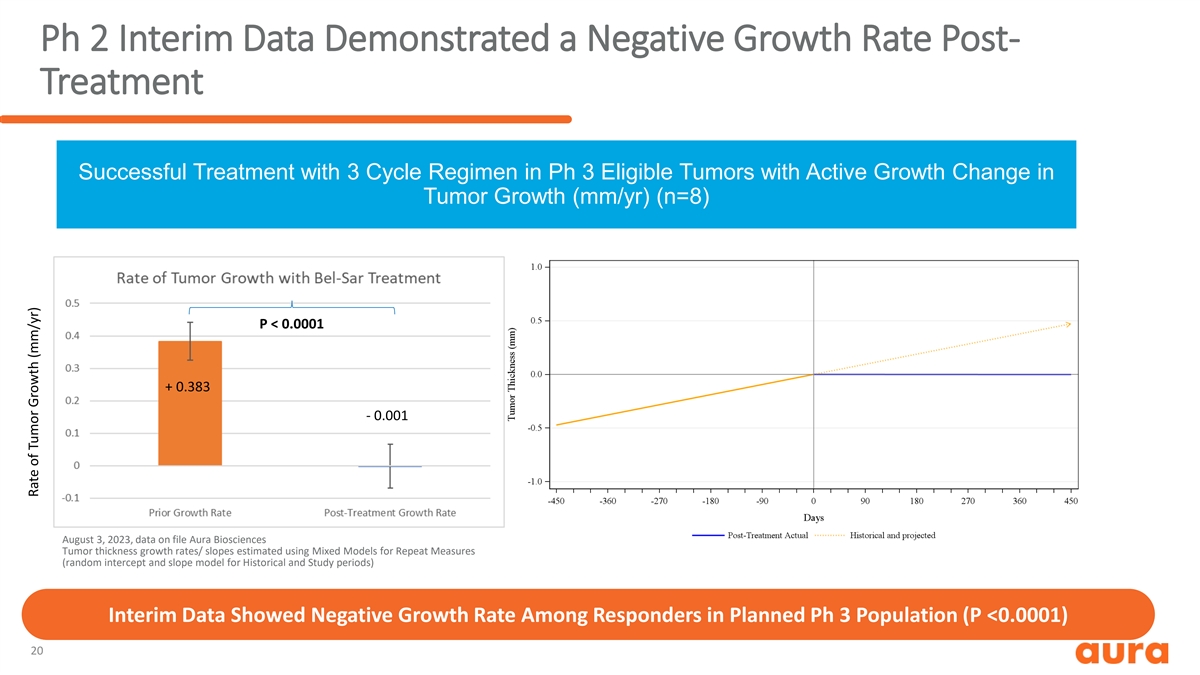
第 2 期中期數據顯示,治療後生長率為負 對符合 Ph 3 條件且腫瘤生長髮生活躍變化 (mm/yr) (n=8) P 的腫瘤進行了成功的三週期治療

儘管 80% 的患者處於 視力喪失的高風險,但仍保持 90% 的視力 > 90% 的患者完成了 12 個月。視力總患者失敗率保持 Ph3 合格人羣中 BCVA 的中位數變化 (n) (n) 對接受治療方案的患者 (n=10) 所有劑量隊列 3 1 所有 接受治療的患者 22 1 96% -1 亞治療 -3 -5 最多 2 個週期的單劑量 10 0 100% -7 治療方案 -9 -11 3 個週期 (n=11) 11 1 91% -13 3 個週期且符合 Ph 3 個週期 (n=11) =10) * -15 10 1 90% 0 3 6 9 12 *不包括一名患有環乳頭狀腫瘤 但不符合 Ph 3 標準的受試者月視力下降定義基於 ETDRS 視力喪失(15 個字母)BCVA 信函分數(距基線 ≥ 15 個字母)2023 年 8 月 3 日,存檔數據 Aura Biosciences 90% 視力 保存數據支持成為早期疾病前線治療的潛力 21 與基線的變化

Ph 2 安全數據支持有可能成為 早期疾病 + 不良事件放射治療的一線治療* Bel-Sar 持續 Ph 2 安全結果 SC 給藥 + 繼發於 AE 的手術(例如白內障)40% + 0% 所有接受治療的受試者(n=22)放射性視網膜病變 40% + 0% 三級藥物/激光 相關不良事件 I 級 > 5% 受試者* 新生血管青光眼 10% 0% 前房乾眼症 20% 0% 18% 18% 炎症斜視 2% + 0% 前房細胞 9% 0 9% 視網膜脱離 1-2% 0% 眼痛 9% 9% 眼痛 9% 0% 視力喪失(≥15 個字母)~ 70% ~ 5% + 嚴重不良事件放射治療* Bel-Sar 表按嚴重程度和總體情況顯示了與 bel-sar 或激光相關的不良反應的受試者的百分比;AE 大於 1 的受試者被計入最高 嚴重程度組 *1 名患者中與 bel-sar 或激光相關的治療緊急不良事件或

隨機對照全球 Ph 3 試驗 23
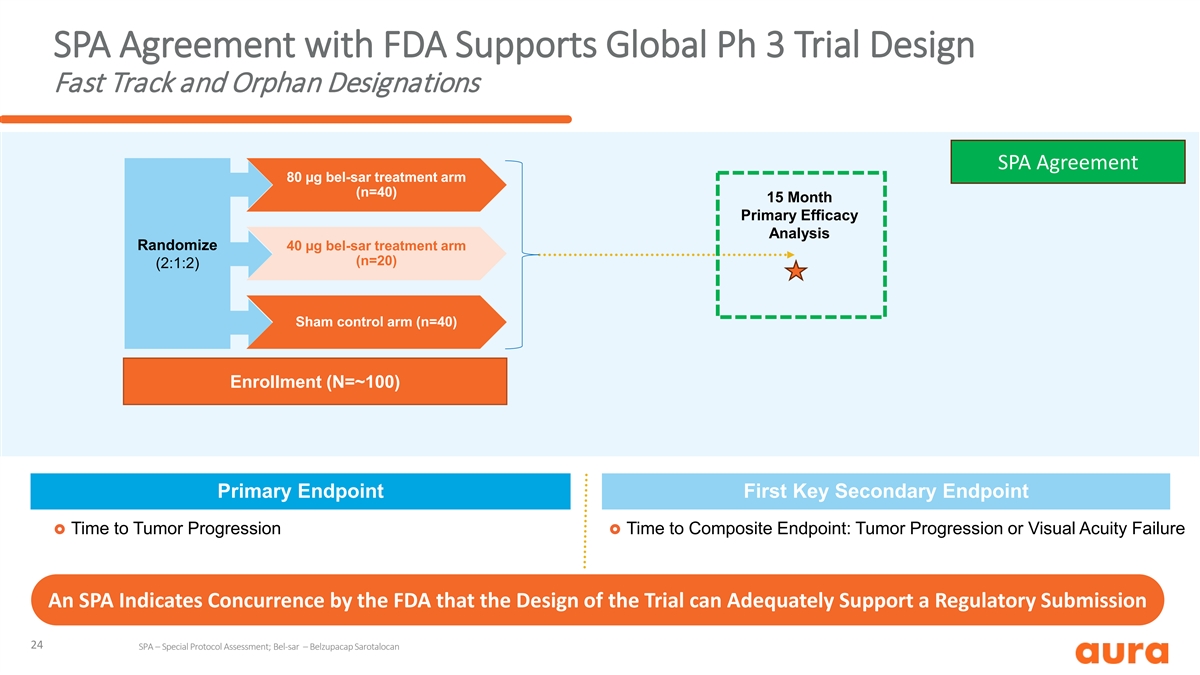
SPA 與 FDA 的協議支持全球 Ph 3 試驗設計快速通道和 孤兒名稱 SPA 協議 80 µg bel-sar 治療組 (n=40) 15 個月主要療效分析隨機化 40 µg bel-sar 治療組 (n=20) (2:1:2) Sham 對照組 (n=40) 入組 (N=~100) 主要終點第一關鍵次要 終點 £ 腫瘤進展時間到複合終點時間:腫瘤進展或視力衰竭 SPA 表示美國食品和藥物管理局同意該試驗的設計足以支持監管機構提交的文件 24 SPA — 特殊協議評估;Bel-SAR — Belzupacap Sarotalocan
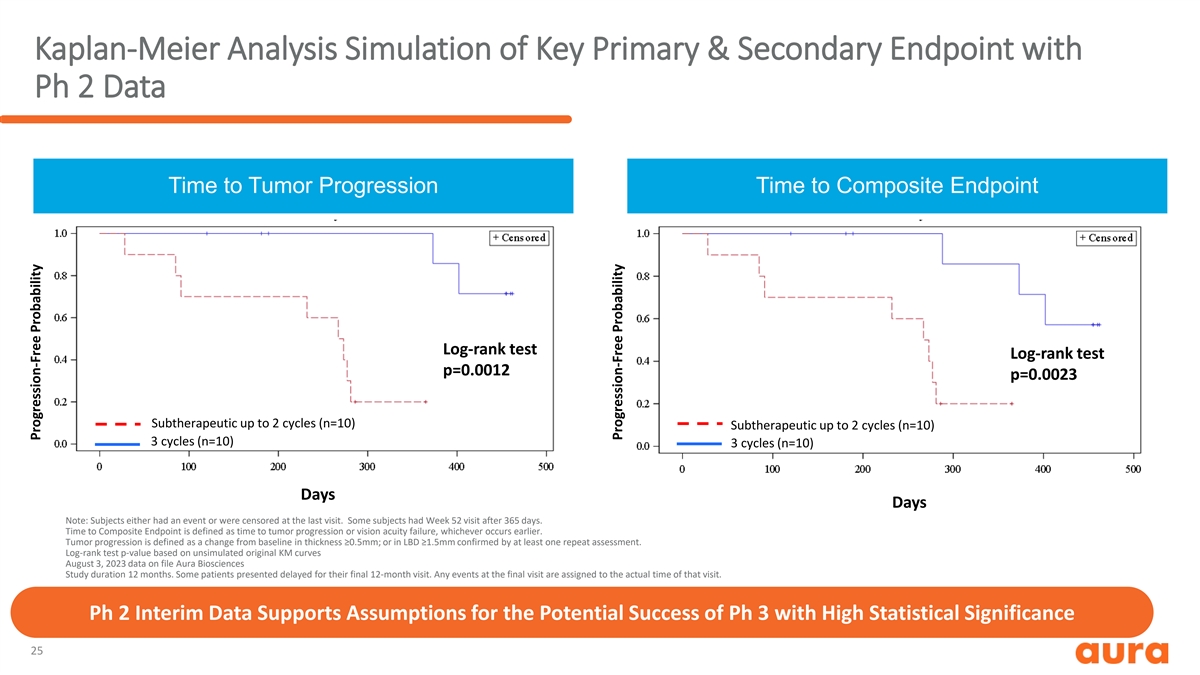
Kaplan-Meier 分析模擬具有 Ph 2 數據的主要和次要 終點腫瘤進展時間到複合終點的時間 log-rank 測試 log-rank 測試 p=0.0012 p=0.0023 亞治療最多 2 個週期 (n=10) 3 個週期 (n=10) 3 個週期 (n=10) 天注意: 受試者要麼有事件要麼接受了審查在上次訪問時。有些受試者在 365 天后接受了第 52 周的就診。到達複合終點的時間定義為腫瘤進展或視力衰竭的時間,以較早發生者為準。腫瘤進展 定義為厚度與基線相比的變化 ≥0.5mm;或經至少一次重複評估確認的 LBD ≥1.5 毫米的變化。對數排名測試 p 值基於未模擬的原始 KM 曲線 2023 年 8 月 3 日存檔數據 Aura Biosciences Study 持續時間 12 個月。一些患者出現了最後12個月的就診延遲。最後一次訪問中的任何活動都將以該次訪問的實際時間為準。Ph 2 中期數據支持假設 Ph 3 的潛在成功率具有高 統計顯著性 25 無進展概率無進展概率

支持潛在批准與 監管機構一致的臨牀終點假設終點定義 Bel-SAR:35% 腫瘤進展腫瘤高度≥0.5mm 或腫瘤進展假設:80% 腫瘤進展大於1.5 mm bel-SAR:15% VA 損失 較基線下降:2% VA 損失 ≥15 個字母腫瘤進展視力損失假設 80% 13% 45% 15% 2% Sham Bel-SAR Sham Bel-SAR 保守假設為 監管的潛力提供了支持提交(第三階段試驗的支持率為 95%)注:腫瘤高度是腫瘤厚度的代名詞;VA — 視力;Bel-sar — Belzupacap Sarotalocan 26 複合終點

脈絡膜轉移 27

脈絡膜轉移是未得到滿足的高度醫療需求標準是 每日放射治療源自多個持續4周的原發癌乳腺皮膚(例如乳房和肺癌)40-53% 2% 20,000/年眼睛在美國腎臟確診的肺部 20-29% 2% 88% 伴有脈絡膜位置 GI 前列腺 72% 單側和孤立性 4% 視力 喪失和輻射相關的 2% 併發症脈絡膜轉移導致視力下降以及抗擊轉移癌症患者的生活質量下降Mathis等人脈絡膜轉移的新概念,視網膜和眼科研究進展 (2019),Cohen,《眼部轉移》,《眼部轉移》(2014),Shields等人。對 520 只有 28 個葡萄膜轉移的眼睛進行了調查。眼科(1997),納馬德等人。來自非小肺癌的雙側脈絡膜轉移,腫瘤醫學病例報告(2014)。

脈絡膜轉移 — Ph 2 試驗設計研究設計 (n=12*) 隊列 1a 隊列 2a 隊列 3a 隊列 3a 隊列 3b N=3 患者 N=3 患者 N=3 患者 N=3 患者 80µg x 2L 140µg x 2L 200µg x 2L 1 週期 1 個週期 1 個週期 2 個週期研究目標研究人羣 • 安全/DLT • 單側單灶脈絡膜轉移的患者 • 療效 • 乳房或肺部原發性 • 脈絡膜腫瘤進展 • 併發全身性無變化 • 計劃使用脈絡膜腫瘤生長速率藥物 • 視力改善亮點:一個月後的主要終點-治療;腫瘤萎縮的可能性;美國食品藥品管理局腫瘤學部 29 *3+3 設計。每個隊列將至少有3名患者,最多6名患者。
泌尿外科腫瘤學 Bel-sar INN:belzupacap sarotalocan 靶標 適應症:膀胱癌 30

膀胱癌是未得到滿足的高度醫療需求 61,000 20,000 ~500,000 1 1 2 美國每年新增病例/年全球新增病例/年肌肉浸潤性膀胱癌未滿足的需求復發、多次 TURBT 手術、疾病進展、 膀胱/膀胱切除術流失、疾病進展、轉移損失和膀胱/囊腫存活率 Tomy 31 1.Putnam & Assoc。流行病學分析 2.Campbell-Walsh-Wein 泌尿外科,2021 年,第 12 版;第 137 章,第 3112 頁

Bel-Sar 有可能成為與 TURBT 輔助泌尿科醫生治療聯合使用的最前線 Bel-SAR 尿液內復發免疫療法 (Keytruda) 輔助性尿液內復發免疫療法 (Keytruda) 輔助 泌尿科醫生治療 bel-SAR 膀胱內注射療法 + 診斷和基因療法膀胱切除術卡介苗 >6 tx 卡介苗難治性 (Adstiladrin) 尿中血液治療計劃 TURBT 全身免疫療法靜脈注射 (Keytruda) 化療添加 bel-SAR 罐 有可能:• 預防 TURBT 後復發 • 避免需要輔助化療 • 避免需要六個週期的卡介苗 • 提高檢查點抑制劑 BCG — Bacillus Calmette Guerin 的療效;• 預防 膀胱切除術 32 TURBT-膀胱腫瘤經尿道切除術説明當前膀胱癌膀胱癌患者旅程的示意性未來膀胱癌患者旅程
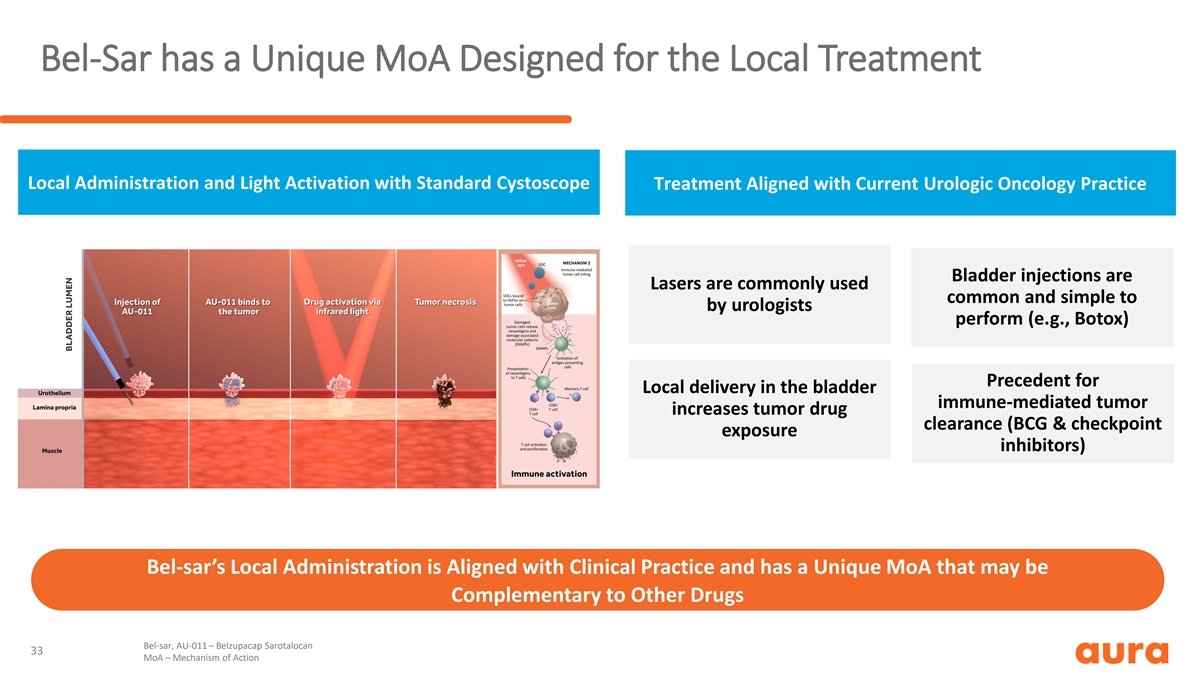
Bel-Sar 擁有獨一無二的 MoA,專為局部治療局部 給藥和光激活而設計,符合當前泌尿外科腫瘤學實踐膀胱注射通常是泌尿科醫生常用的(例如肉毒桿菌毒素)膀胱免疫介導的腫瘤局部 遞送可提高腫瘤藥物清除率(卡介苗和檢查點暴露抑制劑)Bel-SAR 的地方管理部門贊同臨牀實踐且具有獨特的 MoA,可能與其他 藥物互補 bel-sar,AU-011 — Belzupacap Sarotalocan 33 MoA — 作用機制

旨在評估安全性、可行性和 MoA 研究的 Ph 1 試驗 目標研究設計和目標 (n=19) • 安全性/DLT • 技術可行性已完成第 1 部分 (n=5) • bel-sar 的焦點分佈 Bel-sar 僅有治療相關的 Bel-SAR • 局灶壞死不良事件、嚴重不良事件、嚴重不良事件 事件或劑量-• 在 5 名患者研究羣體中發現了免疫激活限制毒性的標誌物 TURL • BT 和膀胱切除術患者第 2 部分 (n=14) 正在進行中 • NMIBC 和 MIBC 患者 bel-SAR + 聚焦光激活 Ph 1 數據有望為未來提供支持開發用於治療 NMIBC 和 MIBC Bel-SAR 的 Bel-SAR — Belzupacap Sarotalocan MoA — 作用機制 34 TURBT-經尿道膀胱腫瘤切除術
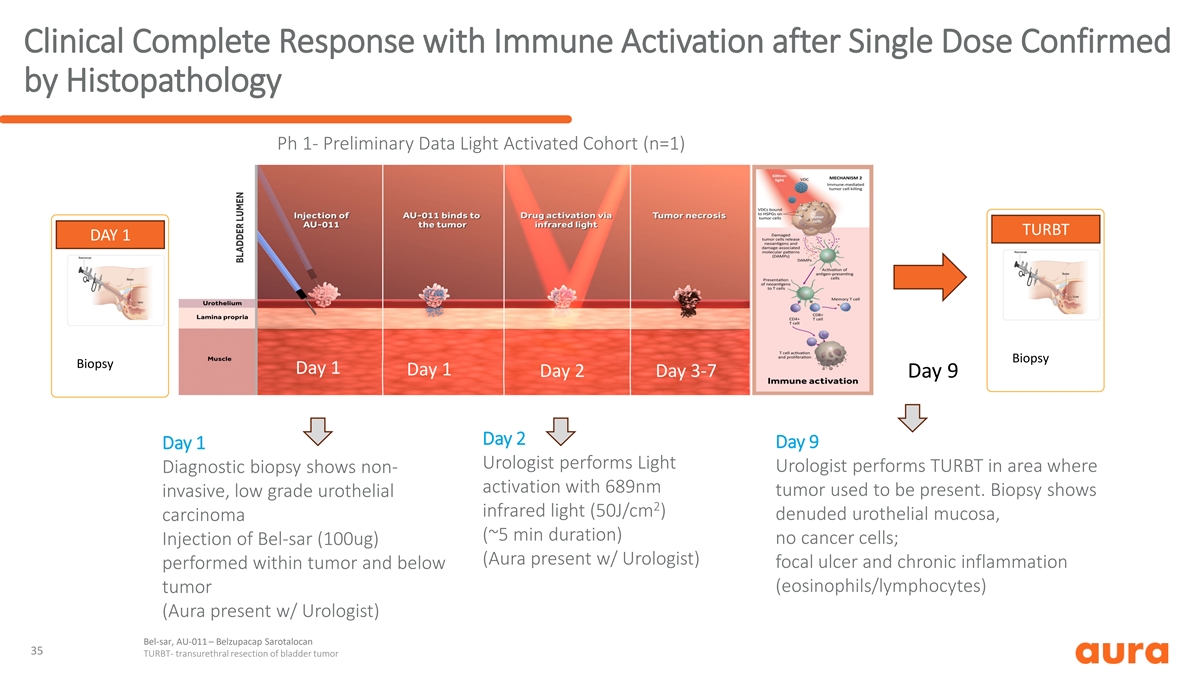
經組織病理學 Ph 1 確認單劑量 後免疫激活的臨牀完全反應-初步數據光激活隊列 (n=1) TURBT 第 1 天活檢第 1 天 2 天 3-7 天 9 天第 2 天第 9 天第 1 天第 1 天泌尿科醫生在診斷活檢顯示有 689nm 腫瘤存在非 活化的區域進行輕度泌尿外科醫生 TURBT。活檢顯示侵入性、低等級尿路上皮 2 紅外光 (50J/cm) 裸露的尿路上皮粘膜、癌(持續約 5 分鐘)無癌細胞;注射 Bel-SAR(100ug)(Aura 與泌尿科醫生一起出現) 局灶性潰瘍和慢性炎症發生在腫瘤內及以下(嗜酸性粒細胞/淋巴細胞)腫瘤(Aura 在泌尿科醫生的陪同下)) Bel-sar,AU-011 — Belzupacap Sarotalocan 35 TURBT-經尿道膀胱腫瘤切除術

治療前活檢(第 1 天)顯示乳頭狀尿路上皮癌 H&E Stain 乳頭狀尿路上皮癌乳頭狀癌(Ta)注射前膀胱活檢顯示低度乳頭狀尿路上皮癌;非侵入性。36

單劑量 bel-SAR 治療和免疫激活後所有癌細胞消失後,組織病理學證實臨牀完全反應免疫浸潤壞死治療後 TURBT 顯示壞死、炎症浸潤,無殘留癌。圓圈區域顯示 壞死區域;箭頭表示炎性浸潤邊緣。首例患者單劑量治療後腫瘤細胞缺失可完全緩解的證據 37
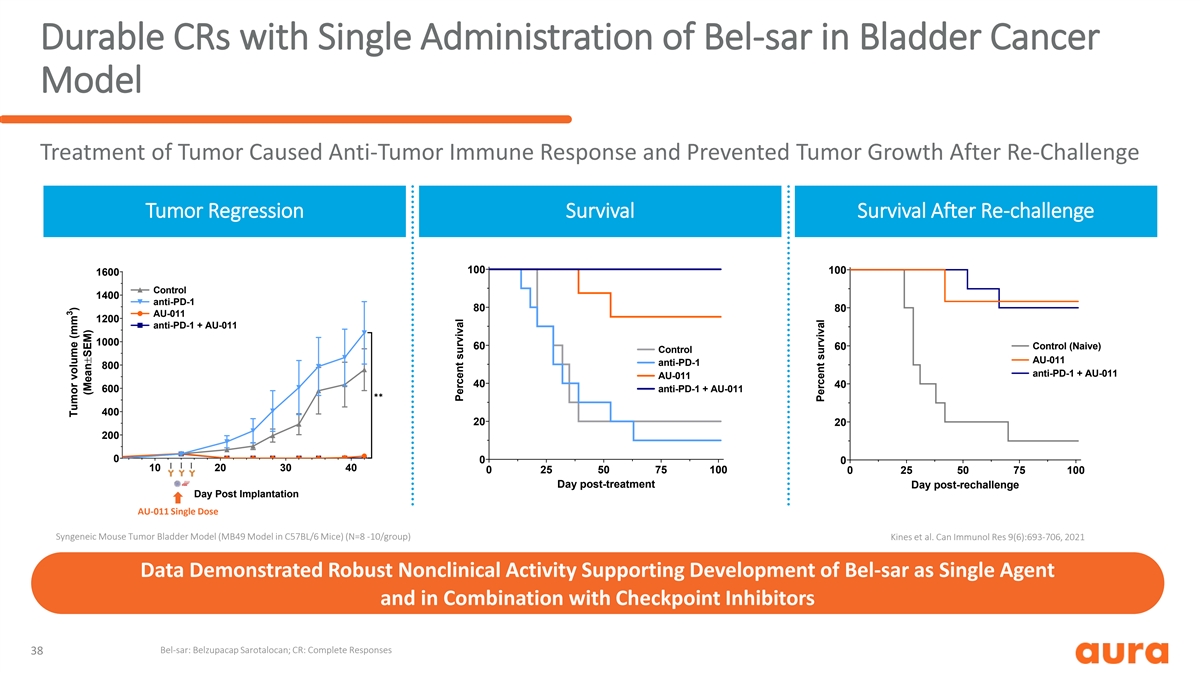
膀胱癌單次給藥 Bel-SAR 的耐用 CR 腫瘤的模型治療可引起抗腫瘤免疫反應並阻止腫瘤生長再挑戰腫瘤迴歸後的存活率 100 100 1600 對照 1400 抗 PD-1 80 80 AU-011 1200 抗 PD-1 + AU-011 1000 60 60 對照 AU-011 800 抗 PD-1 + AU-011 40 40 600 抗 PD-1 + AU-011 ✱✱ 400 20 200 0 0 0 0 0 10 20 20 0 0 10 20 20 0 0 20 20 0 0 0 20 20 0 0 20 20 0 0 0 20 20 0 0 20 20 0 0 0 20 20 0 0 20 20 0 0 0 20 20 0 0 20 0 0 20 20 0 0 20 0 0 20 20 0 0 20 0 0 20 20 0 0 20 0 0 20 20 0 0 20 0 0 20 20 0 0 30 40 0 25 50 75 100 0 25 50 75 100 治療後一天再挑戰後一天植入後一天 AU-011 單劑量同基因 AU-011小鼠腫瘤膀胱模型(C57BL/6 小鼠中的 MB49 模型)(N=8 -10/組)Kines 等人Can Immunol Res 9 (6): 693-706,2021 年的數據顯示出強大的非臨牀活性支持 Bel-SAR 作為單一藥物的開發以及 與檢查點抑制劑聯合使用 Bel-SAR:Belzupacap Sarotalocan;CR:完全反應 38 3 腫瘤體積 (mm) (平均值±SEM) 存活百分比存活率

戰略和關鍵里程碑 39
Aura Biosciences投資亮點 • 原發性脈絡膜 黑色素瘤 • 與美國食品藥品管理局的SPA協議支持監管機構申報 • Ph 2數據支持Ph 3研究的假設(支持率為95%)關鍵亮點 • 膀胱癌 (NMIBC/MIBC)• 我們認為初步數據支持雙重諒解備忘錄,臨牀完全反應和免疫激活已得到組織病理學原發脈絡膜的證實黑色素瘤:• YE 2023:全球 Ph 3 試驗的首位患者劑量預計 臨牀里程碑脈絡膜轉移:6-12 個月內 • 2024 年:Ph 2 數據膀胱癌 (NMIBC/MIBC):• 2024 年中期:1 期數據 40


Bel-Sar 在第 3 期符合條件的患者基準特徵基準特徵中顯示出長期持久反應且視力保持不變 符合條件的受試者記錄的腫瘤生長是基線時的腫瘤大小 AU-011 治療週期腫瘤高度 1.03 mm 最大基底直徑 (LBD) 6.12 mm 危險因素視網膜下積液 (F) 是的橙色色素 (O) 是的由腫瘤引起的視力下降是的基線 Wk 4 Wk 6 Wk 12 Wk 16 Wk k 30 Wk 39 Wk 52 到 Fovea 的位置距離 0 mm 0 mm BCVA 79 87 84 85 85 80 85 85 80 85 85 85 85 85 85 到視神經的距離(4 個時鐘 小時).) 42