
美國
美國證券交易委員會
華盛頓特區,20549
表格
(標記一)
根據1934年《證券交易法》第13或15(D)條提交的年度報告 |
截至本財政年度止
或
根據1934年《證券交易法》第13或15(D)條提交的過渡報告 |
的過渡期 至
委託文檔號
(註冊人的確切姓名載於其章程)
|
||
(述明或其他司法管轄權 公司或組織) |
|
(税務局僱主 識別號碼) |
(
(註冊人主要執行辦公室的地址,包括郵政編碼和電話號碼,包括區號)
根據該法第12(B)條登記的證券:
每個班級的標題 |
交易代碼 |
註冊的每個交易所的名稱 |
根據該法第12(G)條登記的證券:
無
如果註冊人是一個著名的經驗豐富的發行人,則通過複選標記進行註冊,如《證券法》第405條所定義。 是 ☒
如果註冊人根據法案第13條或第15條(d)款不需要提交報告,則用複選標記進行標記。 是 ☒
用複選標記表示註冊人(1)是否在過去12個月內(或註冊人被要求提交此類報告的較短時間內)提交了1934年《證券交易法》第13條或15(D)節要求提交的所有報告,以及(2)在過去90天內是否符合此類提交要求。☒
用複選標記表示註冊人是否在過去12個月內(或在註冊人被要求提交此類文件的較短時間內)以電子方式提交了根據S-T法規第405條(本章232.405節)要求提交的每一份交互數據文件。☒
用複選標記表示註冊人是大型加速申報公司、加速申報公司、非加速申報公司、較小的報告公司或新興成長型公司。請參閲《交易法》第12b-2條規則中“大型加速申報公司”、“加速申報公司”、“較小申報公司”和“新興成長型公司”的定義。
大型加速文件服務器 |
☐ |
|
|
加速文件管理器 |
☐ |
☒ |
|
|
規模較小的報告公司 |
||
|
|
|
|
新興成長型公司 |
如果是一家新興的成長型公司,用複選標記表示註冊人是否已選擇不使用延長的過渡期來遵守根據《交易所法》第13(A)節提供的任何新的或修訂的財務會計準則。☐
用複選標記表示註冊人是否提交了一份報告,證明其管理層根據《薩班斯-奧克斯利法案》(《美國聯邦法典》第15編,第7262(B)節)第404(B)條對其財務報告的內部控制的有效性進行了評估,該評估是由編制或發佈其審計報告的註冊會計師事務所進行的。
如果證券是根據該法第12(B)條登記的,應用複選標記表示登記人的財務報表是否反映了對以前發佈的財務報表的錯誤更正。
用複選標記表示這些錯誤更正中是否有任何重述需要對註冊人的任何執行人員在相關恢復期間根據第240.10D-1(B)條收到的基於激勵的補償進行恢復分析。☐
通過複選標記確定註冊人是否為空殼公司(如《交易法》第12b—2條所定義):
截至2023年6月30日,非關聯公司持有的註冊人有表決權和無表決權普通股的總市值約為美元,
自.起2024年3月14日,
以引用方式併入的文件
本年度報告表格10—K的第三部分通過引用的方式納入了註冊人2024年年度股東大會的最終委託書的某些信息,該註冊人打算根據第14A條在註冊人的財政年度結束後不遲於120天內向美國證券交易委員會提交。 2023年12月31日.除本表10—K中以引用方式特別納入的信息外,委託書不視為作為本表10—K的一部分提交。
與我們的業務相關的重大風險和其他風險摘要
i
目錄
|
|
|
|
頁面 |
關於前瞻性陳述的特別説明 |
|
3 |
||
|
|
|
|
|
第一部分 |
|
|
|
5 |
第1項。 |
|
業務 |
|
5 |
第1A項。 |
|
風險因素 |
|
37 |
項目1B。 |
|
未解決的員工意見 |
|
87 |
項目1C。 |
|
網絡安全 |
|
87 |
第二項。 |
|
屬性 |
|
87 |
第三項。 |
|
法律訴訟 |
|
87 |
第四項。 |
|
煤礦安全信息披露 |
|
88 |
|
|
|
|
|
第II部 |
|
|
|
89 |
第五項。 |
|
註冊人普通股、相關股東事項和發行人購買 |
|
89 |
第六項。 |
|
[已保留] |
|
89 |
第7項。 |
|
管理層對財務狀況和經營成果的探討與分析 |
|
90 |
第7A項。 |
|
關於市場風險的定量和定性披露 |
|
100 |
第八項。 |
|
財務報表和補充數據 |
|
101 |
第九項。 |
|
會計與財務信息披露的變更與分歧 |
|
101 |
第9A項。 |
|
控制和程序 |
|
101 |
項目9B。 |
|
其他信息 |
|
102 |
項目9C。 |
|
關於妨礙檢查的外國司法管轄區的披露 |
|
102 |
|
|
|
|
|
第三部分 |
|
|
|
103 |
第10項。 |
|
董事、高管與公司治理 |
|
103 |
第11項。 |
|
高管薪酬 |
|
103 |
第12項。 |
|
某些實益擁有人的擔保所有權以及管理層和相關股東的事項 |
|
103 |
第13項。 |
|
某些關係和相關交易,以及董事的獨立性 |
|
103 |
第14項。 |
|
首席會計師費用及服務 |
|
103 |
|
|
|
|
|
第四部分 |
|
|
|
104 |
第15項。 |
|
展品和財務報表附表 |
|
104 |
第16項。 |
|
表格10-K摘要 |
|
136 |
II
關於前向弧圈球的特別説明King聲明和行業數據
這份Form 10-K年度報告包含涉及重大風險和不確定性的前瞻性陳述。除有關歷史事實的陳述外,本Form 10-K年度報告中包含的所有陳述,包括有關我們的戰略、未來運營、未來財務狀況、未來收入、預計成本、前景、管理計劃和目標以及預期市場增長的陳述,均為前瞻性陳述。“預期”、“相信”、“繼續”、“可能”、“估計”、“預期”、“打算”、“可能”、“計劃”、“潛在”、“預測”、“項目”、“應該”、“目標”、“將”等類似表述旨在識別前瞻性表述,儘管並不是所有前瞻性表述都包含這些識別詞語。
這些前瞻性陳述包括,除其他外,關於以下方面的陳述:
3
我們可能無法實際實現我們的前瞻性聲明中披露的計劃、意圖或預期,您不應過度依賴我們的前瞻性聲明。實際結果或事件可能與我們在前瞻性陳述中披露的計劃、意圖和預期大不相同。我們在以Form 10-K格式提交的年度報告中的警示聲明中包含了重要因素,特別是在“風險因素”部分,這些因素可能會導致實際結果或事件與我們所作的前瞻性聲明大不相同。我們的前瞻性陳述不反映我們可能進行或進入的任何未來收購、合併、處置、合作、合資或投資的潛在影響。
您應閲讀本年度報告中的Form 10-K以及我們在此引用的文件,這些文件已作為附件完整地存檔或合併,並應瞭解我們未來的實際結果可能與我們預期的大不相同。我們不承擔任何義務更新任何前瞻性陳述,無論是由於新信息、未來事件或其他原因,除非法律要求。
本表格10—K年度報告包括我們從行業出版物和第三方進行的研究、調查和研究中獲得的統計和其他行業和市場數據。行業出版物和第三方研究、調查和研究報告通常表明,其信息是從據信可靠的來源獲得的,儘管它們不保證此類信息的準確性或完整性。我們負責本年報10—K表格中包含的所有披露,我們相信這些行業出版物和第三方研究、調查和研究是可靠的。
4
部分 I
本報告中出現的所有品牌名稱或商標均為其各自所有者的財產。除文意另有所指外,本報告中所提述“Adicet Bio”、“Adicet”、“本公司”、“我們”、“我們”及“我們的”指Adicet Bio,Inc.。及其附屬公司,如適用。
項目1.B有用處。
概述
我們是一家臨牀階段的生物技術公司,發現和開發用於自身免疫性疾病和癌症的同種異體γ δ T細胞療法。我們正在推進一個“現成的”γ δ T細胞的管道,用嵌合抗原受體(CAR)工程,以促進患者的持久活性。
我們的方法激活,工程和生產來自無關供體外周血細胞的同種異體γ δ T細胞候選產品,使我們能夠以快速和具有成本效益的方式生成新的產品候選。我們的同種異體“現成”生產工藝旨在允許不相關供體的產品按需儲存和銷售,以治療患者而不會誘導移植物抗宿主免疫應答。這與基於α β T細胞的產品相反,α β T細胞必須為每個患者從他或她自己的T細胞中生產,或者如果T細胞來自與患者無關的供體,則需要進行重大的基因編輯來生產。
我們的主要候選產品ADI—001是一種表達靶向CD 20的CAR的同類第一種同種異體γ δ T細胞療法,正在開發用於潛在治療自身免疫性疾病和複發性或難治性侵襲性B細胞非霍奇金淋巴瘤(NHL)。我們的產品線還包括我們的主要臨牀前候選藥物ADI—270,這是一種靶向腎細胞癌的裝甲γ δ CAR T細胞候選藥物,具有其他CD70+實體瘤和血液惡性腫瘤適應症的潛力。我們的管道有幾個額外的內部γ δ T細胞治療計劃,用於血液惡性腫瘤和實體瘤的發現和臨牀前開發。我們預計將繼續基於我們的γ δ T細胞平臺開發自身免疫性疾病和癌症的候選產品,使用先前驗證的抗原或我們使用CAR和其他技術識別和靶向的抗原。我們計劃每12—18個月提交一份新的新藥(IND)申請,包括2024年上半年的ADI—270 IND。
ADI—001
自身免疫性疾病
2023年12月,美國食品藥品監督管理局(FDA)批准了我們ADI—001治療狼瘡腎炎的IND申請,狼瘡腎炎是一種由系統性紅斑狼瘡(SLE)引起的自身免疫性疾病。狼瘡性腎炎是SLE的一種嚴重併發症,在估計的325例中,我們預計在2024年第二季度啟動ADI—001治療狼瘡性腎炎的I期臨牀試驗,並在2024年第二季度和第三季度將候選藥物的開發擴展到一至兩種額外的自身免疫適應症。在這些適應症中,需獲得IND的批准。我們認為ADI—001在B細胞介導的自身免疫性疾病中的潛在市場機會是巨大的,歐盟5、中國和日本超過170萬名自身免疫性疾病患者,其中CAR—T細胞療法已證明臨牀概念驗證,包括SLE(包括狼瘡性腎炎)、系統性硬化症和特發性炎性肌病。
我們預計在2024年第四季度或2025年第一季度提供ADI—001治療狼瘡性腎炎的I期臨牀試驗的初步臨牀數據,取決於研究中心激活和入組情況,並從2024年第四季度或2025年上半年開始提供其他自身免疫適應症的初步臨牀數據。取決於這些適應症中IND的批准,以及成功啟動研究中心並在相關臨牀方案中入組患者。
複發性或難治性侵襲性B細胞NHL
2021年3月,我們啟動了首項人體I期(GLEAN)試驗,以評估ADI—001在複發性或難治性侵襲性B細胞NHL患者中的安全性和療效。該研究包括劑量遞增部分,隨後是劑量擴展隊列,以探索ADI—001在多種NHL亞型中的活性。2022年4月,FDA授予ADI—001用於NHL的快速通道指定。截至2023年5月4日截止日期,在GLEAN試驗的24例可評價受試者中,18例患有大B細胞淋巴瘤(LBCL),5例患有套細胞淋巴瘤(MCL),1例患者患有濾泡性淋巴瘤。大多數患者接受了大量的預治療,中間有4線既往治療,12名患者(50%)既往接受過治療。
5
在CAR T細胞治療後進展。儘管基線時患者的性質是晚期,但我們觀察到MCL患者的完全緩解(CR)率高,持久性好。在所有劑量的MCL患者中,我們觀察到6個月時的總緩解率(ORR)為80%(4/5患者),CR率為80%(4/5患者)和CR率為60%(3/5患者)。截至2023年5月4日,ADI—001的安全性特徵總體良好,未觀察到細胞因子釋放綜合徵(CRS)、免疫效應細胞相關神經毒性綜合徵(ICANS)或T細胞惡性腫瘤的顯著風險。2023年11月,我們在CAR T後LBCL啟動了一個擴展隊列EXPAND。2024年1月,我們宣佈決定降低LBCL患者入組GLEAN試驗的優先級,以專注於推進MCL入組。
我們預計將提供NHL患者I期研究的臨牀更新,其中將包括療效數據,包括6個月CR率,以及2024年下半年其他MCL患者的安全性數據。根據臨牀數據和監管反饋,我們計劃在2025年上半年為ADI—001在MCL中的潛在關鍵II期研究確定監管路徑,並在2025年下半年提供進一步的臨牀更新。
我們通過將製造工藝轉移到一個能夠在更大規模生產下運營的額外合同開發和製造組織(CDMO),擴大了ADI—001的製造能力。
ADI—270
ADI—270是一種研究性同種異體γ δ CAR T細胞療法,通過CD27配體靶向CD70,用於治療腎細胞癌(RCC),並具有其他實體瘤適應症的潛力。ADI—270設計用於治療實體瘤,具有高度特異性的CD 70靶向部分和轉化生長因子(TGF)β顯性陰性受體的鎧裝技術,以解決腫瘤微環境中的免疫抑制因子。 基於γ δ 1組織對實體瘤的嗜性和三種抗腫瘤活性機制(CAR、先天性和適應性),CAR γ δ 1 T細胞可能很好地定位於解決實體瘤。我們計劃在2024年第二季度提交ADI—270治療腎癌的IND申請,並在2025年上半年提供臨牀數據,這取決於監管部門的批准和研究啟動活動。我們還在考慮在2025年上半年擴展到其他CD70+腫瘤適應症,2025年下半年此類研究的潛在臨牀數據,但需獲得監管部門批准和研究啟動活動。
我們的管道
我們目前正在開發一種同種異體“現成”γ δ T細胞療法的管道,使用之前驗證的抗原或我們使用CAR和其他技術識別和靶向的抗原。我們正在開發的最先進的候選產品ADI—001正在進行一項針對複發性或難治性侵襲性B NHL的I期臨牀試驗,靶向B細胞抗原CD20,我們預計將在2024年第二季度啟動ADI—001治療狼瘡性腎炎的I期臨牀試驗。我們還正在開發一個管道,以推進自身免疫性疾病,血液惡性腫瘤和實體瘤適應症的同種異體CAR T細胞候選產品的研究和開發。我們預計將繼續基於我們的γ δ T細胞平臺開發自身免疫性疾病和癌症的候選產品,使用先前驗證的抗原或我們使用CAR和其他技術識別和靶向的抗原。
我們的管道如下圖所示:
6

* —如果第2階段是註冊的,則可能不需要第3階段
1—Adicet專注於推進GLEAN試驗的MCL入組,並降低了入組大B細胞淋巴瘤患者的優先級。
圖1.公司管道
我們的戰略
我們的目標是成為領先的生物技術公司,開發用於自身免疫性疾病和癌症的同種異體γ δ T細胞療法。我們的策略的關鍵元素包括我們的計劃:
7
背景
自身免疫性疾病與複發性或難治性侵襲性B細胞NHL
自身免疫性疾病
CAR T療法最初是作為癌症治療而開發的,最近已經成為自身免疫性疾病越來越受關注的主題,因為它有可能在短時間內用單劑量或治療去除引起疾病的免疫細胞。目前批准的用於自身免疫適應症的療法僅用慢性治療方案治療症狀,不被認為是治癒性的。目前沒有FDA批准的用於自身免疫適應症的CAR T療法。最初對CAR T療法用於自身免疫適應症的支持和興趣的增加是基於Georg Schett博士在美國風濕病學院和2023年美國血液學學會會議上提出的持久的概念驗證數據,該數據顯示CD19靶向CAR T細胞在三種不同的自身抗體依賴性自身免疫疾病中誘導持續的無藥緩解,耐受性良好。
ADI—001在NHL中的臨牀數據顯示,在系統性紅斑狼瘡、系統性硬化症和特發性炎性肌病患者的學術臨牀研究中,B細胞消耗反映了自身α β CD 19靶向CAR T的B細胞消耗。鑑於γ δ 1 T細胞優先運輸到器官和組織,ADI—001設計為靶向和消耗外周B細胞, 次級淋巴器官、腎臟和其他器官,這在自身免疫性疾病中是高度需要的。我們認為ADI—001的現成可用性和在癌症環境中良好的安全性特徵支持門診給藥的潛力。
複發性或難治性侵襲性B細胞NHL
近年來,免疫腫瘤學已使許多癌症治療方法取得進展。免疫腫瘤學利用免疫系統來攻擊癌症,在某些情況下,甚至消滅癌症。免疫腫瘤學的一個關鍵突破涉及使用T細胞,免疫系統的關鍵元素,並將其轉化為更強大的腫瘤細胞特異性殺手。研究人員已經通過將編碼CAR的基因加載到T細胞中來實現了這種改進和靶向。這些工程受體代表了一個強大的組合,首先,一個區域與癌細胞上的靶點結合,並將T細胞束縛在其上;其次,一個信號激活T細胞以消除束縛的癌細胞。據我們所知,所有市售CAR T細胞主要含有α β T細胞。雖然我們認為CAR T細胞療法的使用是有前途的,但傳統的CAR T細胞療法也存在一些關鍵缺陷,我們認為,可以通過使用細胞羣體來解決,特別是γ δ T細胞而不是α β T細胞。
現有批准的CAR T細胞治療癌症
截至2023年12月31日,FDA已批准四種靶向CD 19的CAR T細胞療法用於治療B細胞淋巴瘤:由Kite Pharma(現為Gilead Sciences,Inc.)開發的axicabtagene ciloleucel(Yescarta ®)和brexucabtagene autoleucel(Tecartus)。(Gilead);由Novartis開發的tisagenlecleucel(Kymriah ®);和由Juno Therapeutics,Inc.開發的lisocabtagene maraleucel(Breyanzi ®)。(now Bristol Myers Squibb Company。我們認為,儘管迄今為止取得了進展,但目前可用的CAR T細胞療法尚未達到其全部承諾,我們的同種異體γ δ CAR T細胞方法有可能是一個重大的改進。
目前已批准的用於B細胞淋巴瘤的CAR T細胞療法,以Yescarta ®、Tecartus ®、Breyanzi ®和Kymriah ®為代表,是自體細胞療法,即它們基於從患者中分離的免疫細胞,在實驗室中修飾和擴增,然後重新引入同一患者。採用這種自體方法的一個關鍵原因是細胞毒性或細胞殺傷細胞主要是用於產生這些療法的α β T細胞,並且是免疫系統用來識別和攻擊外來細胞的細胞。如果將這些類型的T細胞從無關供體引入患者體內,則供體T細胞將攻擊整個患者的健康組織,
8
移植物抗宿主病(GvHD)可能導致多器官衰竭和死亡。
用於第一代CAR T細胞療法的T細胞來自一種高度豐富的T細胞亞類,稱為α-βT細胞。α-βT細胞約佔體內循環中T細胞的95%,它能夠區分它們遇到的細胞是屬於體內的正常細胞還是需要摧毀的外來或受損細胞。阿爾法貝塔T細胞有自然產生的T細胞受體(TCR),它由阿爾法和貝塔蛋白鏈組成。這些TCR識別細胞上的靶標,也稱為抗原,這些靶標由主要組織相容性複合體(MHC)編碼的抗原提呈分子呈現。MHC包含的基因編碼了許多具有多個變種的蛋白質,因此大多數人都有不同的MHC圖譜。在正常的T細胞發育過程中,那些識別特定MHC特徵和特定個體健康細胞呈現的抗原組合的T細胞被清除,導致T細胞羣體在全身循環,警惕地檢查異常抗原或外來細胞,包括來自另一個個體的T細胞。
在一種被稱為過繼細胞療法的細胞免疫療法中,來自患者的自然產生的免疫細胞被分離出來,並使用細胞因子和腫瘤特異性抗原激活,以刺激患者體內已經存在的低丰度抗腫瘤T細胞的生長和擴張。在實驗室中激活和擴增後,大量準備好識別腫瘤的T細胞被重新注入同一患者體內。
CAR T細胞療法是這種過繼細胞療法的變種,在這種療法中,將一種旨在識別特定腫瘤抗原的CAR基因引入T細胞,而不是試圖基於TCR識別腫瘤抗原的能力來激活T細胞。然後,這些CAR T細胞能夠完全獨立於MHC摧毀任何表達適當抗原的細胞。然而,如果沒有進一步的基因工程,來自α-βT細胞的CAR T細胞仍然具有內源性TCR,這限制了它們對原始患者的使用。
自體細胞療法的侷限性
Kite Pharma和Novartis開發的自體細胞療法有一些侷限性,包括但不限於以下幾點:
自體細胞療法,如從α-βT細胞衍生的CAR-T細胞,已在血液系統惡性腫瘤的初步應用中獲得成功。此外,他們還提供了關鍵數據,證明瞭免疫細胞癌症療法的潛力。然而,這些細胞的製造施加了一些關鍵的限制,如果開發出類似的同種異體細胞療法,無論細胞的捐贈者是誰,這些限制都可以被最小化。我們認為,同種異體細胞療法為優化治療途徑提供了巨大的希望,克服了自體細胞療法與製造和成本相關的限制。
9
基於Gamma Delta T細胞治療的潛在優勢
與使用其他細胞類型開發的其他療法相比,使用伽馬增量T細胞開發的免疫療法具有許多潛在或預期的優勢,包括:
10
我們的同種異體γ Δ T細胞技術
人類γ δ T細胞可以根據其TCR δ鏈的使用分為三個主要亞羣:V δ 1,V δ 2和V δ 3。循環系統中最豐富的γ δ T細胞亞羣V δ 2細胞也是研究最充分的。然而,V δ 1亞羣主要存在於組織中,並對靶細胞表現出良好的細胞毒性特徵,我們使用我們的專有平臺技術激活和生產。
Vδ1個γ Δ T細胞
V δ 1細胞具有先天性和適應性免疫系統的特性,這意味着它們可以被腫瘤特異性抗原以及受損或異常細胞常見的一般激活劑激活。與其他T細胞類似,它們表達TCR,但也表達在天然免疫細胞(如自然殺傷(NK)細胞)上發現的細胞毒性受體。這些γ Δ T細胞可以通過多種機制誘導腫瘤細胞死亡,包括分泌細胞毒性蛋白,如粒酶和穿孔素,以及通過分泌細胞因子,如干擾素γ(IFN γ)和腫瘤壞死因子α(TNF α)。
在體外和體內臨牀前模型中,V δ 1細胞具有更強的細胞毒性,並且可能比V δ 2細胞具有更長的耐久性。V δ 1細胞對活化誘導細胞死亡(AICD)也更有抵抗力,這在慢性刺激V δ 2細胞後的臨牀試驗中造成了嚴重的問題。V δ 1細胞通常存在於組織中,它們能夠適應較低的營養可用性和較低的氧氣水平,這些條件類似於與某些實體瘤相關的微環境或局部區域中的條件。這些γ δ T細胞在典型的腫瘤低氧(缺氧)條件下孵育已顯示增強其細胞毒性。
V的預期優勢δ1 γ Δ T細胞優於基於NK細胞的治療
開發同種異體CAR T細胞的另一種方法包括基於工程NK細胞的治療。雖然γ δ T細胞和NK細胞治療通常不會引起GvHD,但NK細胞表達廣泛的抑制性和激活性受體庫,並且腫瘤誘導的多種細胞因子分泌更有限。我們認為,我們正在開發的γ δ T細胞技術比這種方法有幾個優勢。與工程NK細胞不同,V δ 1 γ δ T細胞具有以下優點:
我們相信,這些優勢使基於γ δ T細胞的療法成為許多自身免疫性和癌症適應症和治療線的NK療法的有吸引力的替代品。
V的預期優勢δ1 γ Δ T細胞優於其他方法來生成同種異體CAR T細胞
開發同種異體γ δ CAR T細胞的另一種方法包括引入遺傳修飾,使來自與患者無關的供體的α β T細胞中的TCR失活。這個過程防止這些細胞攻擊患者的健康細胞。我們認為不相關的供體源性γ δ T細胞
11
這種技術缺乏攻擊無關個體健康細胞的能力,與這種方法相比,它有許多優點。在異基因範式中,與α β T細胞不同,V δ 1 γ δ T細胞具有以下優點:
我們相信這些優勢使基於γ δ T細胞的療法成為基於α β T細胞的療法的有吸引力的替代品。
V的預期優勢δ1 γ Δ T細胞超過雙特異性抗體T細胞募集用於腫瘤免疫治療
開發同種異體CAR T細胞的另一種方法由設計用於將T細胞交聯至腫瘤上的特定靶標的雙特異性抗體組成。這種方法通常需要健康和功能性的T細胞能夠在引導到表達靶抗原的腫瘤時攻擊腫瘤。我們認為,不相關的供體衍生γ δ T細胞技術比這種方法有許多潛在的優勢。與雙特異性抗體不同,V δ 1 γ δ T細胞具有以下優點:
我們相信,這些優勢使基於γ δ T細胞的療法成為許多自身免疫和癌症適應症和治療線的雙特異性療法的有吸引力的替代品。
我們的主要預期差異化從γ Δ T細胞競爭對手
我們認為,我們正在開發的γ δ T細胞技術相對於γ δ T細胞競爭對手公司的技術具有許多潛在優勢,包括以下內容:
我們相信,這些優勢使我們基於γ δ T細胞的療法成為其他γ δ T細胞競爭對手公司所使用的技術的有吸引力的方法。
γ δ T細胞的生產
為了生產基於γ δ T細胞的候選產品,我們從無關供體分離外周血單核細胞,這些細胞符合所有人類細胞、組織以及供體細胞和組織產品(HCT/P)的安全性標準,
12
FDA在聯邦法規(CFR)第21篇第1271部分中概述。然後,我們使用專有的激動性抗體和細胞因子激活V δ 1 γ Δ T細胞,所述細胞因子在用含有CAR構建體編碼序列的無複製能力的逆轉錄病毒載體轉導之前擴增這些細胞。這些CAR修飾的細胞以顯著數量級進一步擴增,通常在臨牀規模上擴增超過6,000倍,產生主要由所需γ δ T細胞組成的細胞培養物。為了減少患者發生GvHD的機會,然後使用α—β特異性的抗體技術耗盡剩餘的α β T細胞。然後將所得γ δ T細胞配製在可輸注溶液中以形成最終藥物產品,將其填充到小瓶中,然後冷凍以使得能夠遞送解凍後細胞劑量的CAR—T細胞。 我們的大規模生產流程示意圖見下圖。
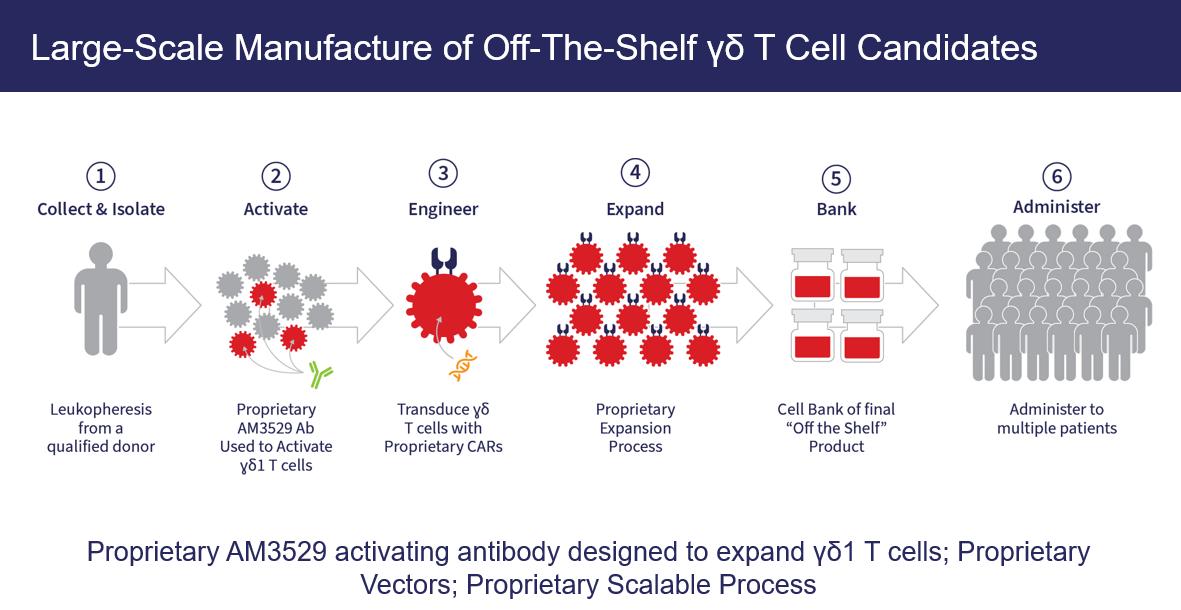
圖2.γ δ T細胞的生產
ADI—001,一種抗CD20 CAR γ δ T細胞候選產品,靶向自身免疫性疾病和侵襲性復發/難治性NHL
我們的解決方案,ADI—001
ADI—001是我們的γ δ CAR T細胞候選產品,旨在通過抗CD20 CAR和γ δ T細胞內源性受體靶向惡性B細胞,我們正在開發其作為治療B細胞NHL的異基因免疫細胞療法。ADI—001由分離自無關供體的V δ 1 γ δ T細胞產生。在現行藥品生產質量管理規範(cGMP)合規條件下批量生產,預期作為立即可用的"現成"抗CD20 CAR T細胞治療藥物供應。
ADI—001含有一種抗CD20 CAR,該CAR具有專有抗原結合結構域,該結構域識別與利妥昔單抗識別區域不同的CD20區域。與其他CAR—T細胞(包括用於創建Kymriah ®的細胞)相似,我們的CAR—T細胞含有臨牀驗證的來自4—1BB和CD3 β的共刺激結構域。
ADI—001開發計劃
自身免疫性疾病
我們在狼瘡性腎炎中的ADI—001 I期研究將從1億個CAR+細胞的單位劑量開始進行3 + 3劑量遞增。根據安全性研究結果,將探索更高劑量高達10億個CAR+細胞。在ADI—001輸注前,每例患者將接受環磷酰胺和氟達拉濱淋巴細胞清除調節。劑量限制性毒性報告窗口設置為42天;該期間的安全性事件將推動劑量遞增決策。首次安全性評估計劃在輸注後第28天進行,然後在之後的第3—6—9—12—18和24個月進行。一旦最大耐受劑量
13
確定後,將開放劑量擴展隊列,以進一步表徵ADI—001在狼瘡性腎炎患者中的安全性和療效。主要終點將側重於安全性。有關ADI—001在狼瘡性腎炎中的I期研究設計,請參見下圖3。
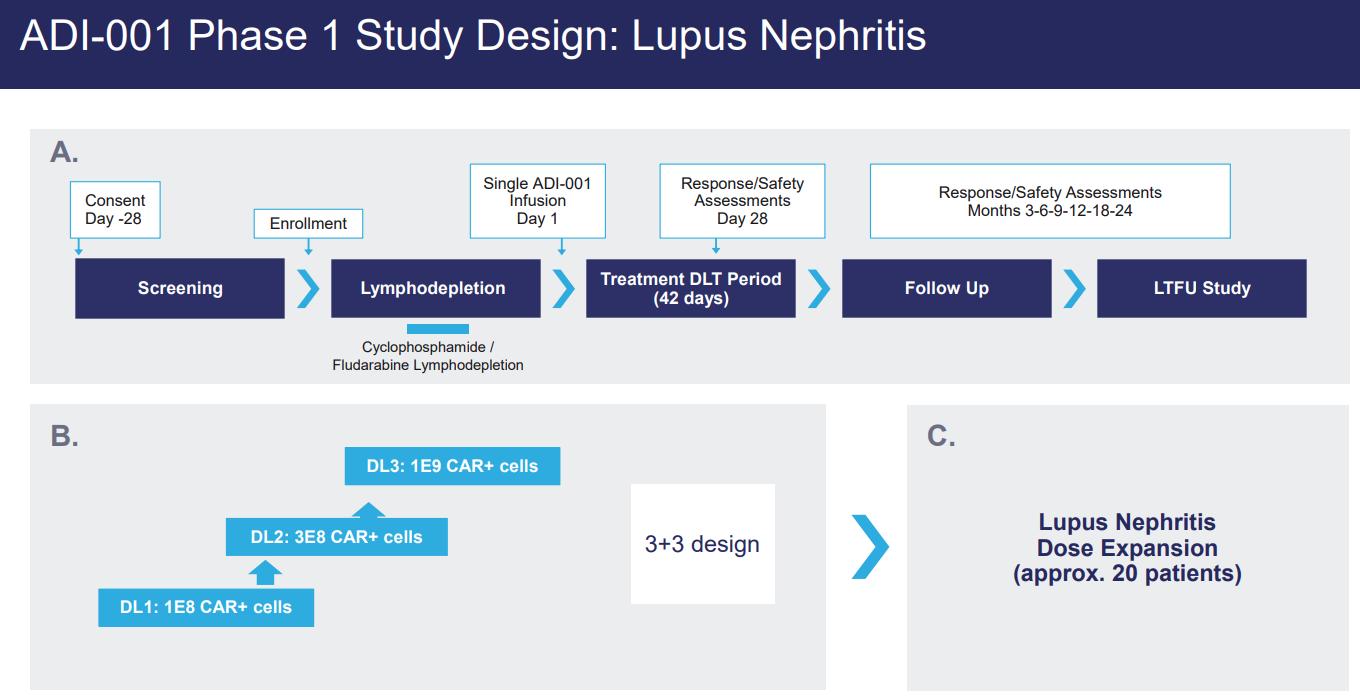
圖3.計劃的ADI—001 I期研究設計:狼瘡性腎炎
侵襲性復發和難治性NHL
2020年10月,FDA批准了ADI—001治療NHL的IND申請。活性IND使我們得以於二零二一年第一季度啟動首項人體臨牀試驗,以評估ADI—001在NHL患者中的安全性和療效。正在進行的ADI—001 I期研究將在美國多個癌症中心招募多達80名晚期NHL患者。該研究包括劑量探索部分,隨後是劑量擴展隊列,以探索ADI—001在多種NHL亞型中的活性。本試驗將包括因醫療、技術、後勤或財務原因而無法接受批准的自體CAR T細胞療法的既往治療患者,以及接受自體CAR T細胞療法後復發的患者。
入組試驗的MCL患者將接受3天的化療淋巴細胞清除,隨後在第5天接受ADI—001輸注給藥。患者將在第一年的四周、12周和每三個月進行一次評估,以及治療後的第18和24個月。選擇推薦劑量後,ADI—001治療後出現臨牀獲益的患者可能有資格接受再治療。參見圖4。I期ADI—001研究患者流程。
14

圖4.第1階段ADI-001研究患者流程
目前正在進行ADI-001第一階段臨牀研究的登記,以提供更多的耐用性數據,並進一步支持推薦的第二階段劑量。請參閲“正在進行的ADI-001治療復發或難治性非霍奇金淋巴瘤的1期試驗結果獲取有關近期中期業績的信息。
正在進行的ADI-001治療復發或難治性非霍奇金淋巴瘤的1期試驗結果
2023年6月26日,我們宣佈了正在進行的ADI-001治療複發性或難治性NHL的第一階段研究的中期結果。截至2023年5月4日截止日期的研究數據摘要如下。
15
ADI-270,一種通過CD27配體靶向CD70的同種異體伽瑪-CAR T細胞療法治療腎癌
ADI-270是一種通過CD27配體靶向CD70的同種異體伽瑪-CAR T細胞療法,用於治療腎癌,在其他實體腫瘤適應症中具有潛力。 是為實體瘤設計的,具有高度特異性的CD70靶向部分和顯性負性轉化生長因子β受體的盔甲技術,以解決腫瘤微環境中的免疫抑制因素。ADI-270建立在伽馬三角洲1組織對實體腫瘤的趨向性和在臨牀前模型中觀察到的三種抗腫瘤活性機制(CAR,先天和適應性)的基礎上,CAR伽瑪三角洲1 T細胞可能被很好地定位於治療實體瘤。
我們計劃在2024年第二季度向RCC提交ADI-270的IND申請,並在2025年上半年提供臨牀數據,這取決於監管批准和研究啟動活動。我們還在考慮在2025年上半年擴大到更多CD70+腫瘤適應症的可能性,2025年下半年此類研究的潛在臨牀數據將取決於監管批准和研究啟動活動。
其他臨牀前計劃(CAR和其他技術)
我們的管道還包括額外的內部γ δ T細胞治療計劃,用於發現和臨牀前開發的自身免疫性疾病,血液惡性腫瘤和實體瘤。這些管道程序是通過整合γ δ 1組織歸巢、分化的作用機制、靶向增強和工程化裝甲等方面選擇的。我們相信,我們用CAR或其他技術工程化的γ δ T細胞的組合為新一代γ δ T細胞療法提供了基礎,這些療法有可能改變實體瘤的治療。
抗GPC3 CAR γ Δ T細胞候選產品ADI—002
2022年1月28日,根據我們於2016年簽署的協議,Regeneron行使了其全球獨家授權ADI—002的選擇權,這是一種抗GPC3同種異體CAR γ δ T細胞候選產品。在行使其選擇權的同時,Regeneron向我們支付了2000萬美元的行使費。我們選擇不行使我們的選擇權,共同資助ADI—002的進一步開發。因此,Regeneron負責ADI—002的所有開發、生產和商業化,且我們有權獲得Regeneron今後銷售此類產品的特許權使用費。見附註8。第三方協議我們的合併財務報表在本年報表格10—K。
我們的戰略協議
我們已經簽署了多項戰略協議和合作,包括我們與Regeneron的許可和合作協議,以及我們與Twist Bioscience Corporation的抗體發現協議。我們還對這些原始協議進行了修訂。有關我們重大協議的其他資料,請參閲附註8。本年度報告其他地方出現的合併財務報表的第三方協議,表格10—K。
我們的知識產權
我們基於γ δ T細胞的候選產品和幾乎所有的知識產權都是由我們開發的,其中某些抗原結合結構域來自我們與Regeneron的合作。2016年,通過收購Applied Immune Technologies Ltd.(AIT),收購了更多的知識組合資產,AIT現在是我們的全資擁有
16
我們致力於保護和增強對我們業務具有商業意義的專有技術、發明和改進,包括尋求、維護和捍衞我們的專利權。
我們的政策是發展和維護我們的專利地位,除其他方法外,通過提交或授權與我們的技術、發明和改進相關的美國和外國專利和申請,這些對我們的業務的發展和實施至關重要。我們還依賴商標、商業祕密、專有技術、持續技術創新、保密協議和發明轉讓協議來發展和維持我們的專利地位。
我們的專利組合包括我們的主要候選產品ADI—001和ADI—270以及我們的合作項目ADI—002和其他幾個研究階段候選產品的物質成分、處理方法和製造工藝保護。截至2024年3月14日,有多個專利系列,包括四個未決的美國非臨時申請和超過50個相應的已授予外國專利和未決外國專利申請,這些國家包括澳大利亞,加拿大,中國,歐洲,以色列,日本,韓國,墨西哥,俄羅斯,新加坡和南非的權利要求涉及用於γ δ T細胞擴增和所得γ δ T細胞物質組合物的特定試劑和相關方案,其中包括工程化的γ δ CAR T細胞,如果發行,預計將在2035年至2038年之間到期。我們原始專利家族中的第一個美國非臨時申請以美國專利號11,135,245獲得授權,有效期為2038年5月19日,我們第二個專利家族中的第一個美國非臨時申請以美國專利號11,299,708獲得授權,有效期為2037年12月26日。在這兩個專利家族中,其他的美國非臨時申請正在等待中。
特別是對於我們的ADI—001項目,有一個專利系列,包括一個美國非臨時申請和相應的外國專利申請,如澳大利亞、加拿大、中國、歐洲、以色列、日本、韓國、墨西哥、新西蘭、俄羅斯、新加坡和南非,其權利要求涉及與ADI—001相關的CAR構建體和抗原結合結構域,以及它們在某些適應症中的使用方法、預處理方法和給藥方案,如果發佈,將於2039年到期。此外,我們還有一個未決的國際專利合作條約(PCT)申請,涉及使用ADI—001的某些治療方法,其中後續的國家階段申請聲稱該PCT申請的利益,假設它們在適當的時候提交和發佈,將在2042年到期。
對於我們的研究階段項目,我們有三個未決的國際PCT申請,分別集中在CD70,前列腺特異性成員抗原和B7—H6,其中任何後續聲稱這些PCT申請的利益的國家階段申請將在2043年到期,假設它們在適當的時候提交和發佈。我們還有兩個未決的美國臨時專利申請,涉及T細胞工程的某些改進,以及一個未決的美國臨時專利申請,涉及一般用於過繼細胞療法的伴隨診斷和相關輔助療法,其中聲稱這些臨時申請的利益的申請將在2044年到期,假設它們在適當時候被轉換,起訴和發佈。 在美國和國際上,我們的TPRL平臺技術也有多項已授予專利和待審專利申請,將於2023年至2037年到期,其中包括三項針對某些癌症、黑色素瘤和膠質母細胞瘤靶點的待審專利系列,將於2036年至2037年到期。
對於我們與Regeneron合作的ADI—002項目,有一個專利家族,包括一個美國非臨時申請和相應的外國專利申請,這些申請在澳大利亞、加拿大、中國、歐洲、以色列、日本、韓國、墨西哥、新西蘭、俄羅斯、新加坡和南非等司法管轄區正在申請,其權利要求涉及與ADI—002相關的CAR構建體和抗原結合結構域,以及它們在某些適應症中的使用方法、預處理方法和給藥方案,如果發佈,將於2039年到期。我們還有一個專利家族,包括一個美國非臨時申請和在諸如澳大利亞、加拿大、中國、歐洲、以色列、日本、韓國、墨西哥、新西蘭、新加坡和南非等司法管轄區未決的相應外國專利申請,其涉及針對GPC 3的某些專有抗體及其使用方法,如果在適當的時候發佈,要求享有本PCT申請利益的國家階段申請將於2042年到期。
個人專利的期限取決於獲得專利的國家的法律期限。在我們提出申請的大多數國家,專利期限為20年,自第一份非臨時申請提出申請之日起,並要求優先權。在美國,專利期限的調整可以延長,這是為了補償專利權人在授予專利時的行政延誤,或者如果專利被終止放棄,則可以縮短專利期限。在美國,涵蓋FDA批准的藥物的專利期限也可能有資格根據哈奇—韋克斯曼法案獲得最多五年的專利期限延長,該法案旨在補償FDA監管審查過程中損失的專利期限。專利期限延長的長度涉及一個複雜的計算,基於監管審查所需的時間長度。根據《哈奇—韋克斯曼法案》的專利期限延長不能延長專利的剩餘期限,自產品批准之日起總共超過14年,並且僅可延長一項適用於獲批藥物的專利。此外,專利只能延期一次,因此,如果
17
單一專利適用於多個產品,只能基於一個產品進行擴展。歐洲和某些其他外國司法管轄區也有類似的規定,以延長涵蓋已批准藥物的專利期限。
我們的商業成功在一定程度上取決於我們是否有能力為候選產品、新發現、核心技術和訣竅獲得和維護專利保護,以及我們是否有能力在不侵犯他人的專利權的情況下進行運營,並防止他人侵犯我們的專利權。
像我們這樣的公司的專利地位通常是不確定的,涉及複雜的法律、科學和事實問題。此外,專利申請中所要求的覆蓋範圍在專利發佈前可能會大幅減少,其範圍在發佈後可能會被重新解釋。因此,我們不知道我們的任何候選產品是否會受到保護或繼續受到可執行專利的保護,或者是否會在保護我們的商業產品及其使用和製造方法方面具有商業價值。我們也無法預測其目前正在進行的專利申請是否會在任何特定司法管轄區作為專利發佈,或任何已發佈專利的權利要求是否會提供足夠的專利保護,免受競爭對手的侵害。我們持有或控制的任何專利都可能被第三方質疑、規避或無效。此外,雖然我們對我們的協議和安全措施有信心,但任何一項都可能被違反,我們可能沒有足夠的補救措施。此外,我們的商業祕密可能會被競爭對手所知或獨立發現。
我們已將各種知識產權和商業祕密授權給第三方,用於合作、產品開發和研發。
製造業
我們正在開發和實現可擴展的和專有的當前符合GMP(GMP)的生產工藝。我們已投入資源優化我們的製造流程,並計劃維持該投資,以隨着時間的推移不斷改善我們的生產和供應鏈能力。
我們生產基於細胞的免疫治療產品,其基於從與待治療患者無關的供體血液中獲得的γ δ T細胞。這些產品被歸類為同種異體細胞治療產品。將來自供體的血液產品分級分離,並在未來生產活動中使用之前將含有γ δ T細胞的部分冷凍。我們相信,我們對供體血液製品的冷凍和儲存使我們能夠有效地安排後續生產步驟。在從無關供體獲得血液製品後,生產過程首先使用我們專有的抗體激活γ δ T細胞亞羣,稱為Vd1 T細胞。這種抗體與包括細胞因子IL—2在內的其他因子結合,誘導γ Δ T細胞增殖,於是我們將細胞暴露於病毒載體,該病毒載體將編碼CAR的基因序列或其他基因序列轉移到增殖細胞。該步驟被稱為轉導步驟。在轉導步驟之後,在富集步驟之前用IL—2誘導γ δ T細胞進一步增殖,所述富集步驟增加γ δ T細胞的比例,去除不想要的殘餘α β T細胞併產生CAR修飾的γ δ T細胞藥物產品。CAR修飾的γ δ T細胞產品然後冷凍在一次性小瓶中,以便在低温下長期儲存。這些儲存條件旨在確保基於細胞的藥物產品長期穩定。一次性小瓶儲存旨在簡化處理和治療給藥。在給藥前,將小瓶解凍,然後將內容物輸注患者體內。我們相信,我們正在開發的單一生產工藝將能夠在大約兩週內完成,並將產生足夠數量的藥物產品來治療許多患者。
迄今為止,我們目前依賴並預計將繼續依賴第三方來生產我們的候選產品和我們可能開發的任何產品。我們選擇與美國的多個CMMO合作,以獲得特定的能力,以確保生產過程具有高度可擴展性,並完全符合cGMP要求。這一戰略使我們能夠保持更靈活的基礎設施,同時專注於開發產品。除戰略生產夥伴所採用的質量管理體系外,我們還建立了質量控制和質量保證計劃,其中包括一套標準操作程序和規範,旨在確保我們的產品按照cGMP和其他適用的國內外法規生產。
例如,我們目前與多家第三方製造商合作,生產病毒載體和藥品。我們還將在加利福尼亞州紅木城1000 Bridge Parkway工廠(1000 Bridge Parkway)進行內部GMP細胞處理和載體生產業務,用於生產用於I/II期臨牀試驗的藥物產品。我們還利用單獨的第三方承包商生產用於生產我們候選產品的符合cGMP的起始材料和關鍵材料,例如供體血液製品、γ δ T細胞激活抗體和用於將適用的CAR基因導入T細胞的病毒載體。我們相信所有材料和組件
18
用於生產活化抗體生產細胞系的病毒載體和最終γ δ T細胞產品可從合格的供應商處獲得,並適合於關鍵工藝開發,準備註冊和商業化。展望未來,我們打算通過與領先的細胞療法和病毒載體CDMO達成協議,繼續擴大我們的生產能力。
如果第三方製造或我們自己的內部細胞或載體制造出現挫折或延誤,我們相信有許多潛在的替代品,儘管我們可能會在識別和鑑定這些替代品方面出現一些延誤。我們計劃繼續建立一個強大的供應鏈,擁有由內部和外部基礎設施組成的宂餘供應來源。
競爭
製藥和生物技術行業的特點是技術發展迅速,競爭激烈,並高度重視專利產品。我們面臨着來自許多不同來源的潛在競爭,包括生物製藥公司、學術研究機構、政府機構和公共和私人研究機構開發的現有和新療法,以及標準護理治療。
諾華和Kite Pharma(現在的Gilead)是第一批獲得FDA批准的自體T細胞療法。2017年8月,諾華公司獲得美國食品和藥物管理局的批准,將Kymriah®商業化,用於治療患有難治性或至少復發兩次的B細胞急性淋巴細胞白血病(ALL)的兒童和年輕人。2018年5月,Kymriah®獲得FDA批准,用於治療復發或難治性(R/R)大B細胞淋巴瘤。2017年10月,Kite Pharma獲得美國食品和藥物管理局的批准,將Yescarta®商業化,這是第一個用於治療成人R/R大B細胞淋巴瘤的CAR T細胞候選產品。2020年7月,Gilead獲得了FDA的批准,將首個用於治療成人R/R MCL患者的CAR T細胞產品Tecartus®商業化。2021年2月,百時美施貴寶獲得美國食品和藥物管理局批准,將Breyanzi®商業化,用於治療成人R/R大B細胞淋巴瘤。2022年,Yescarta和Breyanzi都被FDA批准用於治療二線LBCL的成年患者子集,這是對早期三線批准的生產線的擴展。
由於T細胞療法在臨牀試驗中具有良好的治療效果,我們預計來自開發這些療法的現有公司和新公司以及同種異體T細胞療法開發的競爭將越來越激烈。潛在的T細胞療法競爭對手包括但不限於:
自身免疫競爭
癌症大賽
儘管我們相信,由於我們相信這些細胞的巨大潛力,我們開發的用於設計和製造表達CARS的伽馬三角洲T細胞的專利工藝是獨一無二的,但可能會出現額外的競爭,來自目前專注於開發阿爾法貝塔或伽馬三角洲T細胞療法的現有公司,或者來自該領域的新進入者。
競爭也可能來自非細胞免疫癌症平臺。例如,我們可能會遇到來自Amgen Inc.等公司的競爭,百時美施貴寶公司Hoffmann—La Roche AG,Genmat A/S,GlaxoSmithKline plc,MacroGenics,Inc.,Merus N.V.,Regeneron Pharmaceuticals,Inc.,和Xencor公司,他們在追求
19
雙特異性抗體,其靶向癌抗原和T細胞受體,從而使癌細胞和T細胞兩者緊密接近以最大化對癌細胞的免疫應答的可能性。此外,諾華公司,F. Hoffmann—La Roche AG,Biogen Inc.,和GSK plc正在開發針對B細胞抗原和其他靶點的基於抗體的療法,用於治療自身免疫性疾病。此外,安進公司等公司,AbbVie Inc.,Daiichi Sankyo Company,Limited,GSK plc,Immunomedics,Inc.,和輝瑞公司,目前正在尋求抗體藥物綴合物,其利用抗體的靶向能力將細胞殺傷劑直接遞送到癌細胞。MCL的進一步競爭可能來自Bruton酪氨酸激酶抑制劑,包括阿斯利康公司,BeiGene有限公司批准和正在開發的那些抑制劑,Merck KGaA和Eli Lilly and Company
我們的許多競爭對手,無論是單獨或與合作伙伴合作,在研發、臨牀前試驗、臨牀試驗、製造和營銷方面的財力和專業知識都比我們多得多。未來的合作和併購可能會導致資源進一步集中在數量較少的競爭對手中。
如果我們的競爭對手開發和商業化的產品比我們可能開發的產品更安全、更有效、副作用更少或更不嚴重、更方便或更便宜,我們的商業潛力可能會減少或消除。我們的競爭對手也可能更快地獲得FDA或其他監管機構的批准,比我們獲得自己的產品批准,這可能導致我們的競爭對手在我們能夠進入市場之前就建立了強大的市場地位,或使我們的發展變得更加複雜。影響我們所有項目成功的關鍵競爭因素可能是療效、安全性和耐受性、便利性、價格、報銷和生產成本。
這些競爭對手還可能爭奪類似的合格科學和管理人才庫、臨牀試驗場所和患者羣體、投資者資本以及補充或必要的技術。
政府管制與產品審批
作為一家在美國運營的生物製藥公司,我們受到廣泛的監管。我們的細胞產品將作為生物製品進行監管。根據這一分類,我們的產品的商業生產將需要在符合生物製品cGMP的註冊工廠進行。FDA將基於人類細胞或組織的產品分類為最低限度操作或超過最低限度操作,並確定超過最低限度操作的產品需要臨牀試驗來證明產品的安全性和有效性,並向FDA提交BLA以獲得上市許可。我們的產品被認為不僅僅是最低限度的操作,需要在臨牀試驗中進行評估,並提交BLA並獲得批准,然後才能上市。通常,在新藥或生物製劑上市之前,必須獲得大量證明我們質量、安全性和療效的數據,並將其組織成每個監管機構的特定格式,提交監管機構審查和批准。
美國(聯邦、州和地方各級)和其他國家的政府當局廣泛監管生物製藥產品的研究、開發、測試、製造、質量控制、批准、標籤、包裝、儲存、記錄保存、促銷、廣告、分銷、批准後監測和報告、營銷、進出口等。我們的候選產品在美國合法上市前必須獲得FDA的批准,在外國合法上市前必須獲得相應的外國監管機構的批准。一般而言,我們在其他國家的活動將受到與美國類似的性質和範圍的監管,儘管可能會有很大的差異。此外,歐洲監管的一些重要方面是集中處理的,但在許多方面,針對具體國家的監管仍然至關重要。獲得監管上市批准的過程以及隨後遵守適當的聯邦、州、地方和外國法規和法規需要花費大量的時間和財政資源。
美國產品開發流程
在美國,FDA根據《聯邦食品、藥品和化粧品法》(FDCA)、《公共衞生服務法》(PHSA)及其實施條例對藥品和生物製品進行監管。獲得監管批准的過程以及隨後遵守適當的聯邦、州、地方和外國法規和法規需要花費大量的時間和財政資源。在產品開發過程、批准過程或批准後的任何時候,如不遵守適用的美國要求,申請人可能受到行政或司法制裁。FDA的制裁措施包括,除其他行動外,拒絕批准待決申請、撤回批准、臨牀暫停、警告信、產品召回或從市場撤出、產品扣押、全部或部分
20
停止生產或銷售禁令、罰款、拒絕政府合同、歸還、沒收財產或民事或刑事處罰。任何機構或司法執法行動都可能對我們產生重大不利影響。FDA要求生物製品在美國上市之前的流程通常包括以下內容:
在人體內測試任何候選生物產品(包括我們的候選產品)之前,候選產品進入臨牀前測試階段。臨牀前試驗,也稱為非臨牀研究,包括產品化學、毒性和配方的實驗室評價,以及評估候選產品潛在安全性和活性的動物研究。關鍵臨牀前試驗的實施必須符合聯邦法規和要求,包括GLP。IND申請是向FDA請求授權,將研究產品用於人體,必須在人體臨牀試驗開始前生效。臨牀試驗申辦者必須將臨牀前試驗結果連同生產信息、分析數據、任何可用的臨牀數據或文獻以及擬定的臨牀方案提交給FDA,作為IND的一部分。IND自FDA收到30天后自動生效,除非FDA對擬議臨牀試驗提出關注或疑問,並要求提供更多信息和/或在30天內暫停臨牀試驗。在這種情況下,IND申辦者和FDA必須在臨牀試驗開始前解決任何懸而未決的問題。FDA還可以在臨牀試驗前或臨牀試驗期間的任何時候,由於安全性問題或不符合要求,對候選生物製品實施臨牀暫停。如果FDA強制暫停臨牀試驗,未經FDA授權,試驗不得重新開始,只能在FDA授權的條件下進行。因此,我們不能確定提交IND申請將導致FDA允許臨牀試驗開始,或者一旦開始,不會出現暫停或終止此類試驗的問題。
臨牀試驗涉及在獨立臨牀研究中心/醫院的合格研究者、非由試驗申辦者僱用或控制的醫生的監督下,向患者施用候選生物製品。臨牀試驗根據方案進行,其中詳細説明瞭臨牀試驗的目的、給藥程序、受試者選擇和排除標準以及用於監測受試者安全性的參數,包括確保在發生某些不良事件時停止臨牀試驗的停止規則。每個方案和方案的任何修訂都必須作為IND的一部分提交給FDA。臨牀試驗必須按照FDA的法規進行和監測,包括所有研究患者提供知情同意的要求。此外,每項臨牀試驗必須由臨牀試驗實施的每個機構的IRB進行審查和批准。IRB負責保護試驗參與者的福利和權利,並考慮以下事項:
21
參與臨牀試驗的個人所面臨的風險是否已減至最低,以及相對於預期受益而言是否合理。IRB還批准知情同意書的形式和內容,知情同意書必須由每個臨牀試驗受試者或其法定代表人簽署,並且必須對臨牀試驗進行監測直至完成。一些研究還包括由臨牀研究申辦者組織的獨立合格專家組(稱為數據安全監測委員會)進行監督,該委員會授權研究是否可以根據對研究的某些數據的訪問在指定檢查點進行,如果確定受試者存在不可接受的安全風險或其他原因,則可以停止臨牀試驗。例如沒有顯示功效。此外,還規定了向公共登記處報告正在進行的臨牀研究和臨牀研究結果的要求。
申辦者希望在美國境外進行臨牀試驗,可以(但不需要)獲得FDA授權,根據IND進行臨牀試驗。如果國外臨牀試驗未根據IND進行,申辦者可以向FDA提交臨牀試驗數據以支持BLA。在美國以外的臨牀試驗也可以在國家/地區類似監管機構的授權下進行。FDA將接受一項設計良好且未按照IND進行的國外臨牀研究,如果該研究是按照GCP要求進行的,並且FDA能夠在必要時通過現場檢查來驗證數據。
人體臨牀試驗通常分三個連續階段進行,這些階段可能重疊或合併:
批准後臨牀試驗,有時稱為4期臨牀試驗,可能在首次上市批准後進行。這些臨牀試驗用於從預期治療適應症患者的治療中獲得額外經驗,特別是用於長期安全性隨訪。如果BLA基於有限的臨牀數據加速批准,FDA可能會在完全批准之前授權進行4期臨牀試驗。在臨牀開發的所有階段,監管機構要求對所有臨牀活動、臨牀數據和臨牀試驗研究者進行廣泛的監測和審計。詳細説明臨牀試驗結果的年度進展報告必須提交給FDA。對於嚴重和非預期不良事件、其他研究的任何發現、實驗室動物試驗,必須及時向FDA和研究者提交書面IND安全性報告, 體外培養提示對人類患者有重大風險的檢測,或嚴重疑似不良反應發生率高於方案或研究者手冊中列出的任何臨牀重要增加。申辦者必須在申辦者確定信息符合報告條件後15個日曆日內提交IND安全性報告。申辦者還必須在申辦者首次收到信息後7個日曆日內通知FDA任何非預期致死性或危及生命的疑似不良反應。
I期、II期和III期臨牀試驗可能無法在任何指定時間內成功完成(如果有的話)。FDA或申辦者或其數據安全監測委員會可隨時基於各種理由暫停或終止臨牀試驗,包括髮現研究患者暴露於不可接受的健康風險,包括從其他無關免疫治療試驗推斷的風險。同樣,如果臨牀試驗未按照IRB的要求進行,或者生物製品與患者意外嚴重傷害相關,IRB可以暫停或終止其機構的臨牀試驗批准。
在臨牀試驗的同時,公司通常完成額外的研究,還必須開發有關生物製品物理特性的額外信息,以及根據cGMP要求確定商業批量生產產品的工藝。為了幫助降低使用生物製品時引入外源因子的風險,PHSA強調了對屬性無法精確定義的產品進行生產控制的重要性。生產工藝必須能夠持續生產候選產品的質量批次,除其他外,申辦方必須根據臨牀開發階段的要求開發用於檢測最終生物製品的鑑別、規格、質量、效價和純度的方法。
22
此外,必須選擇並檢測適當的包裝,並進行穩定性研究,以證明候選生物製品在有效期內不會發生不可接受的變質。
美國審查和審批流程
在生物製品的臨牀試驗完成後,必須在生物製品商業銷售前獲得FDA對BLA的批准。BLA提交必須包括產品安全性、有效性、開發、實驗室和動物研究、人體試驗、產品生產和組成信息、擬定標籤和其他相關信息的結果。測試和批准過程需要大量的時間和精力,無法保證或保證FDA將接受BLA進行備案,即使提交,任何批准將及時獲得。
根據經修訂的處方藥使用費法(PDUFA),每個BLA必須附有一筆可觀的使用費。FDA每年調整PDUFA用户費用。PDUFA還對生物製品徵收年度計劃費。在某些情況下,費用減免或減免是可用的,包括對小企業首次提交申請的申請費減免。此外,對於指定為孤兒藥的產品,不對BLA進行用户費用評估,除非該產品還包括非孤兒適應症。
在提交申請後的60天內,FDA審查提交的BLA,以確定其在FDA接受提交之前是否基本完整。FDA可以拒絕提交其認為不完整或在提交時無法適當審查的任何BLA,並可以要求提供更多信息。在這種情況下,必須重新提交BLA和附加信息。重新提交的申請在FDA接受申請之前也要接受審查。根據FDA在PDUFA下同意的目標和政策,FDA自申請之日起有10個月的時間完成對原始BLA的初步審查並回復申請人,自申請之日起有6個月的時間完成指定進行優先審查的原始BLA。FDA並不總是符合其標準和優先BLA的PDUFA目標日期,並且FDA要求提供更多信息或澄清通常會延長審查過程。
一旦提交被接受備案,FDA將開始對BLA進行深入的實質性審查。FDA審查BLA,以確定擬定產品是否安全、有效和/或其預期用途有效,並具有可接受的純度特徵,以及產品是否按照cGMP生產,以確保和保持產品的特性、安全性、強度、質量、效力和純度。FDA可能會將新生物製品或生物製品的申請提交給諮詢委員會,通常是一個包括臨牀醫生和其他專家的小組,以進行審查,評估和建議是否應該批准申請以及在什麼條件下批准。FDA不受諮詢委員會建議的約束,但在作出決定時會仔細考慮這些建議。
在生物製品審批過程中,FDA還將確定是否需要風險評估和緩解戰略(REMS)來確保生物製品的安全使用。REMS是一種安全策略,用於管理已知或潛在的與藥物相關的嚴重風險,並通過管理藥物的安全使用使患者能夠繼續獲得此類藥物,可能包括藥物指南、醫生溝通計劃或確保安全使用的要素,如受限分配方法、患者登記和其他風險最小化工具。如果FDA得出結論認為需要REMS,則BLA的贊助商必須提交一份建議的REMS。如果需要,FDA將不會批准沒有REMS的BLA。
在批准BLA之前,FDA將檢查生產該產品的設施。FDA將不會批准該產品,除非它確定製造工藝和設施符合cGMP要求,並足以確保產品在所要求的規格下一致生產。對於細胞免疫治療產品,如果製造商在適用的範圍內不符合cGTPS,FDA也不會批准該產品。這些是FDA的法規和指導文件,部分管理用於製造人類細胞、組織和Hct/Ps的方法、設施和控制,這些細胞或組織是用於植入、移植、輸注或轉移到人類受者體內的人類細胞或組織。CGTP的主要目的是確保以細胞和組織為基礎的產品的製造方式旨在防止傳染病的引入、傳播和傳播。FDA的規定還要求組織機構向FDA登記和列出他們的HCT/P,並在適用的情況下通過篩選和測試對捐贈者進行評估。此外,在批准BLA之前,FDA通常會檢查一個或多個臨牀地點,以確保臨牀試驗是按照IND試驗要求和GCP要求進行的。為了確保符合cGMP、cGTP和GCP,申請者必須在培訓、記錄保存、生產和質量控制方面花費大量的時間、金錢和精力。
23
儘管提交了相關數據和信息,FDA可能最終決定BLA不符合其批准的監管標準並拒絕批准。從臨牀試驗中獲得的數據並不總是決定性的,FDA對數據的解釋可能與我們對相同數據的解釋不同。如果FDA決定不批准目前形式的BLA,FDA將發佈一封完整的回覆信,描述FDA確定的BLA中的所有具體缺陷。所確定的缺陷可能是微小的,例如,需要標籤改變,或者是重大的,例如,需要額外的臨牀試驗。此外,完整的回覆信可以包括申請人可能採取的將申請置於批准條件下的建議行動。如果發出了完整的回覆信,申請人可以重新提交BLA,解決信中確定的所有不足之處,或者撤回申請。
如果產品獲得監管部門的批准,批准可能僅限於特定的疾病和劑量,或者使用適應症可能會受到限制,這可能會限制該產品的商業價值。此外,FDA可能要求在產品標籤中包括某些禁忌症、警告或預防措施。FDA可以風險管理計劃的形式對產品分銷、處方或配藥施加限制和條件,或以其他方式限制任何批准的範圍。此外,FDA可能要求進行上市後臨牀試驗,有時被稱為第四階段臨牀試驗,旨在進一步評估生物製品的安全性和有效性,並要求進行測試和監督計劃,以監測已商業化的批准產品的安全性。
兒科信息
此外,根據《兒科研究公平法》,BLA或補充BLA必須包含數據,以評估該產品在所有相關兒科亞羣中聲稱的適應症的安全性和有效性,並支持該產品對每個安全有效的兒科亞羣的劑量和給藥。FDA可以批准推遲提交數據,或者給予全部或部分豁免。計劃提交一種藥物的營銷申請的贊助商必須在第二階段會議結束後60天內提交一份初步兒科研究計劃(PSP),如果沒有這樣的會議,則必須在第三階段或第二/3階段研究開始之前儘早提交一份初步兒科研究計劃。最初的PSP必須包括贊助者計劃進行的一項或多項兒科研究的概要,包括研究目標和設計、年齡組、相關終點和統計方法,或不包括此類詳細信息的理由,以及任何要求推遲兒科評估或完全或部分免除提供兒科研究數據和支持信息的要求。FDA和贊助商必須就PSP達成協議。如果需要根據從臨牀前研究、早期臨牀試驗和/或其他臨牀開發計劃收集的數據考慮兒科計劃的變化,贊助商可以隨時提交對商定的初始PSP的修正案。
孤兒藥物名稱
根據《孤兒藥品法》,FDA可以授予用於治療罕見疾病或疾病的藥物或生物製劑的孤兒稱號,這種疾病或疾病通常在美國影響不到20萬人,在美國影響超過20萬人,而且沒有合理的預期在美國開發和提供治療這種疾病或疾病的藥物或生物製劑的成本將從該藥物或生物製劑在美國的銷售中收回。在提交BLA之前,必須申請指定孤兒藥物。在FDA批准孤兒藥物指定後,FDA公開披露治療劑的仿製藥身份及其潛在的孤兒用途。孤兒藥物的指定不會在監管審查或批准過程中傳遞任何優勢,也不會縮短監管審查或批准過程的持續時間。
如果一種具有孤兒藥物指定的產品隨後獲得了FDA對其具有這種指定的疾病的第一次批准,該產品有權獲得孤兒產品排他性,這意味着FDA可能不會批准任何其他申請,包括完整的BLA,在七年內銷售相同的生物適應症,除非在有限的情況下,例如顯示出相對於具有孤兒藥物排他性的產品的臨牀優勢。孤兒藥物排他性並不妨礙FDA批准針對相同疾病或狀況的不同藥物或生物製劑,或針對不同疾病或狀況的相同藥物或生物製劑。指定孤兒藥物的其他好處包括某些研究的税收抵免和免除BLA申請使用費。
指定的孤兒藥物如果被批准用於比其獲得孤兒指定的適應症更廣泛的用途,則不得獲得孤兒藥物排他性。此外,如果FDA後來確定指定請求存在重大缺陷,或者如果製造商無法保證足夠數量的產品來滿足這種罕見疾病或疾病患者的需求,則可能會失去在美國的獨家營銷權。
加快發展和審查計劃
24
FDA提供的計劃旨在促進和加快新產品的開發和審查,這些新產品旨在解決嚴重或危及生命的疾病或狀況的治療中未得到滿足的醫療需求。這些計劃被稱為快速通道指定、優先審查指定、加速批准、再生醫學高級治療(RMAT)指定和突破性治療指定。此外,根據2022年食品和藥物綜合改革法案(FDORA),指定平臺技術的贊助商可以加快開發和審查使用或採用平臺技術的藥物或生物的任何後續申請。
快速通道計劃旨在加快或促進審查符合特定標準的新產品的過程。具體地説,如果新產品旨在治療嚴重或危及生命的疾病或狀況,並顯示出滿足該疾病或狀況未得到滿足的醫療需求的潛力,則有資格獲得快速通道指定。快速通道指定適用於產品和正在研究的特定適應症的組合。FDA可在提交完整申請之前滾動考慮審查BLA的部分,如果贊助商提供了提交BLA部分的時間表,FDA同意接受BLA的部分並確定該時間表是可接受的,並且贊助商在提交BLA的第一部分時支付任何所需的使用費。
提交FDA審批的任何產品,包括具有快速通道指定的產品,也可能有資格參加旨在加速開發和審查的其他類型的FDA項目,例如優先審查和加速批准。如果產品有可能提供安全有效的治療,但沒有令人滿意的替代療法,或與上市產品相比,在疾病的治療、診斷或預防方面有顯著改善,則該產品有資格進行優先審評。FDA將嘗試將額外資源用於評估指定為優先審查的新產品的申請,以努力促進審查。此外,產品可能有資格獲得加速批准。對於在治療嚴重或危及生命的疾病或病症方面的安全性和有效性進行研究的產品,如果確定該產品對合理可能預測臨牀獲益的替代終點或對可早於不可逆發病率或死亡率的臨牀終點有影響,則可獲得加速批准,考慮到病情的嚴重性、罕見性或流行性以及替代治療的可用性或缺乏,合理可能預測對不可逆的發病率或死亡率或其他臨牀益處的影響。作為批准的條件,FDA可以要求獲得加速批准的藥物或生物製品的申辦者進行充分和良好控制的上市後臨牀研究,根據FDORA,FDA現在可以要求(視情況而定)此類試驗在批准前或在獲得加速批准的產品批准日期後的特定時間段內進行。根據FDORA,FDA增加了快速程序的權力,以撤銷加速批准下批准的藥物或適應症的批准,例如,確證性試驗未能驗證產品的預期臨牀益處。此外,對於考慮加速批准的產品,FDA通常要求,除非FDA另行通知,所有擬在上市批准後120天內傳播或出版的廣告和宣傳材料,在批准前審查期間提交給FDA審查,這可能會對產品商業上市的時間產生不利影響。
RMAT名稱由FDA於2017年設立,旨在促進任何符合以下標準的藥物的有效開發計劃,並加快審查:(1)RMAT的資格,其定義為細胞療法,治療性組織工程產品,人類細胞和組織產品,或使用這些療法或產品的任何組合產品,有限的例外;(2)預期用於治療、改善、逆轉或治癒嚴重或危及生命的疾病或病症;(3)初步臨牀證據表明該藥物有潛力解決此類疾病或病症未得到滿足的醫療需求。RMAT指定提供了潛在的好處,包括與FDA更頻繁的會議,討論候選產品的開發計劃以及滾動審查和優先審查的資格。根據合理可能預測長期臨牀獲益的替代終點或中間終點,或依賴於從大量研究中心獲得的數據(包括通過擴展至其他研究中心),獲得RMAT認證的產品也有資格獲得加速批准。一旦獲得批准,在適當的情況下,FDA可以通過提交臨牀證據、臨牀研究、患者登記或其他真實世界證據來源(如電子健康記錄)來滿足批准後的要求;通過收集更大的確證性數據集;或通過批准前對所有接受治療的患者進行批准後監測。
突破性治療指定還旨在加快治療嚴重或危及生命疾病的產品的開發和審查。FDA的指定需要初步臨牀證據,證明候選產品單獨或與其他藥物和生物製劑聯合使用,在一個或多個臨牀顯著終點(例如在臨牀開發早期觀察到的顯著治療效果)上顯示出比目前可用的治療方法有實質性改善。突破性治療指定具有快速通道指定的所有好處,這意味着如果滿足某些條件,包括與FDA就提交部分申請的擬議時間表和支付適用的用户費用的協議,申辦者可以滾動提交BLA的部分以供審查。
25
快速通道指定、優先審查、RMAT和突破性治療指定不會改變批准標準,但可能會加快我們產品的開發或監管審批過程。
此外,根據FDORA,在下列情況下,納入生物製品或由生物製品利用的平臺技術有資格被指定為指定平臺技術:(1)平臺技術被納入或被根據BLA批准的生物製品使用;(2)由獲得許可的生物製品的發起人或已被授予對該生物製品申請中提交的數據的參考權的發起人提交的初步證據表明,該平臺技術有可能被併入或被不止一種生物製品使用,而不會對質量、製造或安全產生不利影響;(3)適用人員提交的數據或信息表明,平臺技術的納入或利用有合理的可能性為生物製品開發或製造過程以及審查過程帶來顯著的效率。贊助商可以在提交生物製品IND的同時或之後的任何時間,請求FDA將一種平臺技術指定為指定的平臺技術,該生物製品合併或使用作為請求標的的平臺技術。如果被指定,FDA可以加快開發和審查使用或採用該平臺技術的生物製品的任何後續原始BLA。指定平臺技術狀態並不能確保生物製品開發得更快或獲得FDA的批准。此外,如果FDA確定一項指定的平臺技術不再符合此類指定的標準,FDA可以撤銷該指定。
審批後要求
我們獲得FDA批准的任何產品都必須受到FDA的持續監管,其中包括記錄保存要求、產品不良反應報告、向FDA提供最新的安全和療效信息、產品抽樣和分銷要求以及遵守FDA的宣傳和廣告要求,其中包括,除其他外,針對直接面向消費者的廣告的標準、對用於產品批准用途或在患者羣體中未描述的產品的限制(稱為非標籤使用)、對行業贊助的科學和教育活動的限制,以及涉及互聯網的促銷活動的要求。儘管醫生可以開出合法的產品用於非標籤用途,但如果醫生認為這種產品在他/她的專業醫學判斷中是合適的,製造商不得銷售或推廣標籤外用途。然而,在某些情況下,允許分享與產品批准的標籤一致的真實且不具誤導性的信息。
此外,FDA對批准或營銷的額外限制可能會限制產品的商業推廣、分銷、處方或分發。產品審批可能會因不符合監管標準或在初始營銷後出現問題而被撤回。新發現或開發的安全性或有效性數據可能需要更改產品批准的標籤,包括增加新的警告和禁忌症,還可能需要實施其他風險管理措施,包括REMS,或進行上市後研究以評估新發現的安全問題。
此外,質量控制和生產程序必須在批准後繼續符合適用的生產要求,以確保產品的足夠穩定性。cGMP法規要求質量控制和質量保證以及相應的記錄和文件維護以及調查和糾正任何與cGMP的偏差的義務。製造商和其他參與生產和分銷獲批產品的實體必須向FDA和某些州機構註冊,並接受FDA和某些州機構的定期突擊檢查,以符合cGMP和其他法律。處方藥產品的藥品供應鏈中涉及的製造商和其他各方還必須遵守產品跟蹤和追蹤要求,並將假冒、轉移、被盜和故意摻假產品或不適合在美國銷售的產品通知FDA。因此,製造商必須繼續在生產和質量控制領域花費時間、金錢和精力,以保持cGMP合規性。在批准後發現產品的問題可能會導致對產品、製造商或已批准BLA持有人的限制,包括召回或從市場撤回產品。 根據FDORA,獲批藥物和生物製品的申辦者必須提前6個月通知FDA上市狀態的任何變化,例如產品的撤回,否則FDA將該產品列入停產產品名單,這將取消該產品的上市能力。此外,生產工藝的變更受到嚴格監管,根據變更的重要性,可能需要事先獲得FDA批准方可實施。對已批准產品的其他類型的變更,如增加新的適應症和聲明,也需要進一步FDA審查和批准。
我們依賴並預期將繼續依賴第三方根據cGMP法規生產臨牀和商業數量的產品。這些製造商必須遵守cGMP法規,其中要求,除其他外,質量控制和質量保證、記錄和文件的維護以及調查和糾正的義務。
26
與cGMP的任何偏差。生產商和參與生產和分銷獲批生物製品的其他實體必須在FDA和某些州機構註冊其機構,並接受FDA和某些州機構的定期突擊檢查,以符合cGMP要求和其他法律。
FDA還可能要求上市後測試,即所謂的第四階段測試,並進行監測,以監測批准的產品的效果。發現產品以前未知的問題或未能遵守適用的FDA要求可能會產生負面後果,包括負面宣傳、司法或行政執法、FDA的警告信、強制要求的糾正廣告或與醫生的溝通以及民事或刑事處罰等。新發現或開發的安全性或有效性數據可能需要更改產品批准的標籤,包括增加新的警告和禁忌症,還可能需要實施其他風險管理措施。此外,可能會建立新的政府要求,包括由新立法產生的要求,或者FDA的政策可能會改變,這可能會推遲或阻止監管部門批准我們正在開發的產品。
美國營銷排他性
2009年《生物製品價格競爭和創新法案》(BPCIA)修訂了PHSA,授權FDA批准類似版本的創新生物製品,通常稱為生物仿製藥。尋求生物仿製藥批准的競爭對手必須提交申請,以確定其分子與獲批的創新生物製劑高度相似,以及其他要求。然而,BPCIA禁止FDA在創新生物產品獲得首次上市批准後的12年內批准生物仿製藥申請。如果FDA要求創新公司對該產品進行兒科臨牀研究,則該12年的數據獨佔期可能會延長6個月,總計12.5年。
根據FDA批准使用我們候選產品的時間、持續時間和細節,我們的部分美國專利(如果獲得批准)可能符合1984年《藥品價格競爭和專利期限恢復法案》(通常稱為Hatch—Waxman法案)的有限專利期限延長。Hatch—Waxman法案允許專利恢復期長達五年,作為對產品開發和FDA監管審查過程中損失的專利期的補償。然而,專利期限恢復不能延長專利的剩餘期限,自產品批准之日起總共超過14年。專利期恢復期一般為IND生效日期與BLA提交日期之間時間的一半,加上BLA提交日期與該申請批准之間時間的一半。只有一項專利適用於已批准的產品有資格獲得延期,並且延期申請必須在專利期滿前提交。美國專利商標局與FDA協商,審查並批准任何專利期限延長或恢復的申請。未來,我們可能打算申請恢復我們目前擁有或授權的其中一項專利的專利期,以延長專利有效期至其當前有效期後,具體取決於臨牀試驗的預期長度及提交相關BLA所涉及的其他因素。
兒科排他性是美國兒科排他性的另一種監管市場排他性,如果獲得批准,將為生物製劑的所有制劑、劑型和適應症增加六個月的現有排他性期。這六個月的排他性,從其他排他性保護的結束運行,可以授予的基礎上自願完成兒科試驗根據FDA發佈的“書面請求”這樣的試驗。
其他美國醫保法和合規性要求
在美國,除FDA外,我們的活動還可能受到各種聯邦、州和地方當局的監管,包括但不限於醫療保險和醫療補助服務中心(CMS)、美國衞生與公眾服務部(HHS)的其他部門(例如,監察長辦公室、美國司法部(DOJ)和司法部內的個別聯邦檢察官辦公室,以及州和地方政府)。例如,我們的商業行為,包括我們的任何研究和未來的銷售、營銷和科學/教育資助計劃,可能需要遵守《社會保障法》的反欺詐和濫用條款、虛假申報法、1996年《健康保險可攜帶性和責任法案》(HIPAA)的患者數據隱私和安全條款、透明度要求以及類似的州、地方和外國法律(均已修訂)。
除其他事項外,聯邦反回扣法規禁止任何個人或實體故意或故意以現金或實物直接或間接、公開或隱蔽地提供、支付、索取或接受任何報酬,以誘導或作為購買、租賃、訂購或安排購買、租賃或安排購買、租賃或訂購根據Medicare、Medicaid或其他聯邦醫療保健計劃可報銷的任何物品、商品、設施或服務的回報。薪酬一詞被廣泛解讀為包括任何有價值的東西。聯邦反回扣法規被解釋為一方面適用於藥品製造商與處方者、購買者、處方經理和其他個人和實體之間的安排。有許多法律例外和監管安全港保護一些常見的活動不受
27
起訴。例外和安全港是狹義的,需要嚴格遵守才能提供保護。涉及可能被指控旨在誘使開處方、購買或推薦的報酬的做法,如果不符合例外或安全港的資格,可能會受到審查。沒有滿足特定適用的法定例外或監管安全港的所有要求,並不意味着這種行為本身就是《反回扣條例》所規定的非法行為。取而代之的是,將根據對所有事實和情況的累積審查,逐案評估這一安排的合法性。我們的做法可能在所有情況下都不符合法定例外或監管安全港保護的所有標準。
此外,個人或實體不需要實際瞭解聯邦反回扣法規或違反該法規的具體意圖。相反,如果薪酬的“一個目的”是為了誘導推薦,那麼聯邦反回扣法規就被違反了。違規行為將被處以民事和刑事罰款,每一次違規行為都將受到懲罰,外加最高三倍的薪酬、監禁和被排除在政府醫療保健計劃之外。此外,ACA編纂了判例法,即根據聯邦民事虛假索賠法(下文討論),包括因違反聯邦反回扣法規而產生的物品或服務的索賠構成虛假或欺詐性索賠。
民事罰款法規對任何人或實體,除其他外,被確定已提出或導致提出索賠,其中包括,聯邦醫療保健計劃,該人知道或應該知道是醫療或其他項目或服務,沒有提供聲稱或是虛假或欺詐。
除其他事項外,聯邦民事虛假索賠法禁止任何個人或實體故意向聯邦政府提交或導致提交虛假索賠,以要求聯邦政府付款或批准,或故意製作、使用或導致製作或使用虛假記錄或陳述,以向聯邦政府提出虛假或欺詐性索賠。由於2009年《欺詐執法和追回法》的修改,索賠包括對提交給美國政府的金錢或財產的“任何請求或要求”。例如,製藥和其他醫療保健公司一直並將繼續受到這些法律的調查或起訴,因為它們涉嫌向客户免費提供產品,期望客户會為產品向聯邦計劃開具賬單,並因公司營銷產品用於未經批准的用途而導致提交虛假聲明,因此是不可報銷的。根據聯邦虛假索賠法案,即使製造商沒有直接向政府付款人提交索賠,如果他們被認為“導致”提交虛假或欺詐性索賠,他們也會被追究責任。聯邦虛假申報法還允許充當“告密者”的個人代表聯邦政府提起訴訟,指控違反了聯邦虛假申報法,並分享任何金錢追回。
HIPAA制定了額外的聯邦刑法,禁止故意和故意執行或試圖執行計劃,以虛假或欺詐性的藉口、陳述或承諾的方式詐騙或獲取任何醫療福利計劃(包括私人第三方付款人)擁有或控制或保管的任何金錢或財產,並明知而故意通過詭計、計劃或裝置、重大事實或作出任何重大虛假、虛構或欺詐性陳述來偽造、隱瞞或掩蓋與提供或支付醫療福利、項目或服務有關的信息。與聯邦反回扣法規類似,個人或實體不需要實際瞭解該法規或違反該法規的具體意圖即可實施違規。
此外,許多州都有類似的欺詐和濫用法規或法規,如州反回扣和虛假索賠法,這可能在範圍上更廣泛,適用於無論付款人。這些法律由各國家機構和私人行動執行。一些州法律要求製藥公司遵守制藥行業的自願合規指南和相關的聯邦政府合規指南,要求製藥商向醫生和其他醫療保健提供者報告與支付和其他價值轉移相關的信息,並限制營銷行為或要求披露營銷支出。此外,某些州和地方法律要求藥品銷售代表註冊。
我們可能受聯邦政府和我們開展業務所在州的數據隱私和安全法規的約束。經《經濟和臨牀健康衞生信息技術法》(HITECH)及其實施條例修訂的HIPAA,對某些類型的個人和實體提出了與個人可識別健康信息的隱私、安全和傳輸有關的要求。除其他事項外,HITECH使HIPAA的隱私和安全標準直接適用於作為受保護實體的獨立承包商或代理商的商業夥伴,這些實體接收或獲取與代表受保護實體提供服務有關的受保護健康信息。HITECH還設立了四個新的民事罰款級別,修訂了HIPAA,使民事和刑事處罰直接適用於商業夥伴,並賦予州檢察長新的權力,以在聯邦法院提起民事損害賠償或禁令,以執行聯邦HIPAA法律,並尋求與進行聯邦民事訴訟相關的律師費和費用。此外,州法律在特定情況下管理健康信息的隱私和安全,其中許多情況在很大程度上彼此不同,可能產生不同的效果,從而使合規工作複雜化。州和外國法律,
28
例如,歐盟《通用數據保護條例》(European Union General Data Protection Regulations)也在某些情況下管理健康信息的隱私和安全,其中許多情況在很大程度上彼此不同,並且通常不會被HIPAA搶先,從而使合規工作複雜化。關於遵守這些州要求的要求存在模糊不清,如果我們未能遵守適用的州法律要求,我們可能會受到處罰。最後,有國家和外國的法律管理健康信息的隱私和安全,其中許多法律在很大的方面彼此不同,往往沒有被HIPAA搶先,從而使合規工作複雜化。
我們還可能受到聯邦政府價格報告法的約束,這些法律要求我們計算複雜的定價指標,並以準確和及時的方式向政府項目報告,以及聯邦消費者保護法和不公平競爭法,這些法律廣泛規範了潛在損害消費者的市場活動。
此外,《平價醫療法案》中的聯邦醫生支付陽光法案及其實施條例要求,某些藥物、設備、生物和醫療用品製造商根據醫療保險、醫療補助或兒童健康保險計劃付款,(除某些例外情況外)每年向CMS報告與向醫生支付或分配的某些付款或其他價值轉移有關的信息,根據法律的定義,某些其他持牌醫療保健從業人員和教學醫院,或應醫生和教學醫院的要求或代表醫生和教學醫院指定的實體或個人,以及醫生及其直系親屬持有的某些所有權和投資權益。
為了以商業方式分銷產品,我們必須遵守州法律,要求在一個州對藥品和生物製品的製造商和批發商進行登記,包括在某些州將產品運往該州的製造商和經銷商,即使這些製造商或批發商在該州沒有營業地點。一些州還要求製造商和分銷商在分銷鏈中建立產品的譜系,包括一些州要求製造商和其他州採用能夠跟蹤和追蹤產品在分銷鏈中流動的新技術。幾個州已經頒佈了立法,要求製藥和生物技術公司建立營銷合規計劃,向州政府提交定期報告,定期公開銷售、營銷、定價、臨牀試驗和其他活動,和/或註冊其銷售代表,並禁止藥店和其他醫療保健實體向製藥和生物技術公司提供某些醫生處方數據用於銷售和營銷,並禁止某些其他銷售和營銷行為。我們的所有活動都可能受到聯邦和州消費者保護以及不正當競爭法律的約束。
如果發現我們的運營違反了上述任何聯邦和州醫療保健法或適用於我們的任何其他政府法規,我們可能會受到處罰,包括但不限於民事、刑事和行政處罰、損害賠償、罰款、剝奪、監禁、禁止參與政府計劃,如Medicare和Medicaid,拒絕允許我們簽訂政府合同、合同損害、聲譽損害、行政負擔、利潤和未來收益減少、額外的報告要求和/或監督,如果我們成為企業誠信協議或類似協議的約束,以解決不遵守這些法律的指控,以及我們的業務縮減或重組,其中任何可能對我們的業務經營能力和經營業績造成不利影響。
承保範圍、定價和報銷
我們獲得監管部門批准的任何候選產品的覆蓋範圍和報銷狀況存在重大不確定性。在美國和其他國家的市場,我們獲得監管部門批准商業銷售的任何產品的銷售將部分取決於第三方付款人提供的保險範圍,併為此類產品建立適當的補償水平。在美國,第三方支付者包括聯邦和州醫療保健計劃、私人管理的醫療服務提供者、醫療保險公司和其他組織。用於確定第三方付款人是否將為產品提供保險的過程可以與用於設定產品價格或用於確定該付款人將為產品支付的償還率的過程分開。第三方支付者可能會將承保範圍限制在批准清單上的特定產品,也稱為處方集,其中可能不包括FDA批准的特定適應症的所有產品。第三方支付者越來越多地挑戰價格,審查醫療必要性,審查醫療產品、療法和服務的成本效益,並質疑其安全性和有效性。我們可能需要進行昂貴的藥物經濟學研究,以證明我們產品的醫療必要性和成本效益,以及獲得FDA批准所需的費用。我們的候選產品可能不被認為是醫療必需或成本效益。付款人決定為產品提供保險並不意味着將批准適當的償還率。此外,一個付款人決定為某一產品提供保險,並不保證其他付款人也將為該產品提供保險。可能無法獲得足夠的第三方補償,以使我們能夠維持足夠的價格水平,以實現我們在產品開發方面的投資的適當回報。
29
其他國家的定價和償還辦法各不相同。在歐盟(EU),政府通過其定價和報銷規則以及控制國家醫療保健系統來影響藥品的價格,這些系統為消費者支付這些產品的大部分成本提供資金。有些司法管轄區實行肯定和否定清單制度,在這種制度下,只有在商定了補償價格後,才能銷售產品。為了獲得報銷或定價批准,其中一些國家可能要求完成臨牀試驗,將特定候選產品與當前可用療法的成本效益進行比較。其他成員國允許公司自行定價藥品,但監督和控制公司利潤。從歷史上看,在歐盟推出的產品並不遵循美國的價格結構,通常價格往往會大幅降低。醫療保健費用的下行壓力已經變得非常大。因此,新產品進入市場的壁壘越來越高。此外,在一些國家,從低價市場的跨界進口對國內的定價造成了商業壓力。
如果政府和第三方付款人未能提供足夠的保險和報銷,我們獲得商業銷售監管批准的任何候選產品的適銷性可能會受到影響。此外,美國對管理式醫療的重視有所增加,我們預計將繼續增加醫療定價的壓力。保險政策和第三方報銷率可能隨時更改。即使我們獲得監管批准的一種或多種產品獲得了有利的覆蓋和報銷狀態,未來可能會實施不太有利的覆蓋政策和報銷率。
醫療改革
在美國和一些外國司法管轄區,已經並將繼續存在幾項關於醫療保健系統的立法和監管變更以及擬議變更,這些變更可能會阻止或延遲候選產品的上市批准,限制或監管批准後活動,並影響獲得上市批准的候選產品的盈利性銷售能力。在美國和其他地方的決策者和支付者中,有很大興趣促進保健制度的改革,其明確目標是控制保健費用、提高質量和/或擴大獲得機會。在美國,製藥業一直是這些工作的重點,並受到重大立法措施的重大影響。
例如,ACA大大改變了政府和私人保險公司的醫療融資和交付。除了上述條款外,《反腐敗法》中對製藥和生物技術行業具有重要意義的條款如下:
30
可能會通過進一步的立法或法規,損害我們的業務、財務狀況和經營業績。自《反腐敗法》頒佈以來,還提出並通過了其他立法修改:
此外,美國對特種藥物定價做法的立法和執法興趣也在增加。具體而言,最近有幾項美國國會調查和聯邦和州立法活動旨在,除其他事項外,提高藥品定價的透明度,降低處方藥在醫療保險下的成本,審查定價和製造商患者計劃之間的關係,並改革政府計劃的藥物報銷方法。
拜登總統發佈了多項行政命令,試圖降低處方藥費用。2023年2月,HHS還發布了一份提案,以迴應拜登總統2022年10月的行政命令,其中包括一個擬議的處方藥定價模型,該模型將測試有針對性的醫療保險支付調整是否足以激勵製造商完成通過FDA加速批准途徑批准的藥物的確認性試驗。儘管這些和其他擬議措施中的一些措施可能需要通過額外立法授權才能生效,拜登政府可能會推翻或以其他方式改變這些措施,但拜登政府和國會都表示將繼續尋求新的立法措施來控制藥品成本。
2022年的《降低通貨膨脹法案》(IRA)包括幾項可能會在不同程度上影響我們的業務的條款,包括從2025年開始將Medicare Part D受益人的自付上限降低至2,000美元的條款。根據醫療保險D部分對某些藥物施加新的製造商財務責任,允許美國政府就某些高成本藥物和生物製劑的醫療保險B部分和D部分價格上限進行談判,沒有仿製藥或生物類似藥的競爭,要求公司向醫療保險支付回扣,以支付某些藥品價格上漲速度超過通貨膨脹,並推遲限制藥房福利經理收取費用的回扣規則。此外,根據IRA,孤兒藥可免於醫療保險藥品價格談判計劃,但前提是它們有一個孤兒指定,並且唯一批准的適應症是針對該疾病或病症。 如果產品獲得多個孤兒藥指定或具有多個批准的適應症,則可能沒有資格獲得孤兒藥豁免。IRA的實施目前正受到對IRA醫療保險藥品價格談判計劃合憲性提出質疑的訴訟。IRA對我們的業務和整個醫療保健行業的影響尚不清楚。
31
美國各州也越來越多地通過立法和實施了旨在控制藥品定價的條例,包括價格或病人報銷限制、折扣、對某些產品准入和銷售成本披露的限制和透明度措施,在某些情況下,旨在鼓勵從其他國家進口藥品和大宗採購。美國各州也越來越多地通過立法和實施條例,以控制藥品和生物產品定價,包括價格或病人報銷限制、折扣、對某些產品准入和銷售成本披露的限制和透明度措施,在某些情況下,還旨在鼓勵從其他國家進口和大宗採購。
我們預計,這些和其他醫療改革措施將繼續對覆蓋範圍和任何獲批產品的價格造成額外的下行壓力,並可能對我們的業務造成重大損害。醫療保險和其他政府計劃的任何報銷減少都可能導致私人支付者支付的類似減少。成本控制措施或其他醫療改革的實施可能會阻礙我們創造收入、實現盈利或將我們的產品商業化。該等改革可能會對我們可能成功開發並可能獲得監管部門批准的候選產品的預期收益產生不利影響,並可能影響我們的整體財務狀況和開發候選產品的能力。
《反海外腐敗法》
《反海外腐敗法》禁止任何美國個人或企業向任何人提供、支付、承諾支付或授權支付金錢或任何有價值的物品,而明知這些金錢或有價值的物品的全部或部分將直接或間接提供、給予或承諾給任何外國官員、政黨或候選人,以影響外國官員的官方身份。誘使外國官員從事或不從事違反其合法職責的行為,或獲取任何不正當利益,以協助有關個人或企業獲得或保留業務。
FCPA還要求證券在美國上市的公司遵守某些會計規定,這些規定要求我們保存準確、公平地反映公司(包括國際子公司)所有交易的賬簿和記錄,並設計和維護適當的內部會計控制系統。遵守《反海外腐敗法》既昂貴又困難,特別是在腐敗是公認問題的國家。此外,《反海外腐敗法》對製藥行業提出了特別的挑戰,因為在許多國家,醫院由政府擁有和運營,醫生和其他醫院員工就該法規而言被視為外國官員。與臨牀試驗和其他工作有關的某些付款被認為是對政府官員的不當付款,並導致了《反海外腐敗法》的執法行動。各種法律、條例和行政命令還限制在美國境外使用和傳播,或與某些非美國國民分享為國家安全目的而分類的信息,以及某些產品和與這些產品有關的技術數據。
因此,如果我們將業務擴展到美國以外的地區,我們將需要投入額外資源,以遵守其計劃運作的每個司法管轄區的法律和法規。因此,這可能妨礙我們在美國境外開發、製造或銷售某些產品和候選產品,這可能會限制我們的增長潛力並增加我們的開發成本。
美國的包裝和分銷
如果我們的產品提供給總務管理局聯邦供應計劃的授權用户,則適用其他法律和要求。產品必須符合《美國有毒預防包裝法》中適用的兒童安全包裝要求。製造、銷售、促銷和其他活動也可能受到聯邦和州消費者保護和不公平競爭法的約束。
醫藥產品的分銷須遵守額外的要求和條例,包括廣泛的記錄保存、許可證、儲存和安全要求,旨在防止未經授權銷售醫藥產品。公司未能遵守任何這些法律或監管要求,可能會受到法律或監管行動。根據具體情況,未能滿足適用的監管要求可能導致刑事起訴、罰款或其他處罰、禁令、聯邦醫療保健計劃排除、召回請求、扣押產品、全部或部分暫停生產、拒絕或撤回產品批准,或拒絕允許公司簽訂供應合同,包括政府合同。任何針對我們違反這些法律的訴訟,即使我們成功地進行了抗辯,也可能導致我們產生鉅額法律費用,並轉移我們管理層對我們業務運營的注意力。禁止或限制銷售或撤回由我們銷售的未來產品可能對我們的業務產生重大不利影響。
32
法規、法規或現有法規的解釋的變化可能會影響我們未來的業務,例如,要求:(I)改變我們的製造安排;(Ii)增加或修改產品標籤;(Iii)召回或停產我們的產品;或(Iv)額外的記錄保存要求。如果強制實施任何此類變化,可能會對我們的業務運營產生不利影響。
附加法規
除上述規定外,有關環境保護和有害物質的州和聯邦法律,包括《職業安全和健康法》、《資源保護和回收法》和《有毒物質控制法》,都會影響我們的業務。這些法律及其他法律規範我們使用、處理和處置各種生物、化學和放射性物質,以及我們業務所產生的廢物。
即使我們與第三方簽訂了處理這些材料和廢料的合同,我們也無法完全消除這些材料造成的污染或傷害風險。如果我們的運營導致環境污染或使個人接觸有害物質,我們可能會承擔損害賠償和政府罰款的責任,任何責任可能超出我們的資源。我們亦可能因未能遵守該等法律及法規而招致與民事或刑事罰款及處罰有關的重大成本。我們維持工人補償保險,以支付因僱員受傷而可能產生的成本及開支,但該保險未必能為潛在責任提供足夠保障。然而,我們不為可能針對其提出的環境責任或有毒侵權索賠投保。此外,我們可能會為遵守當前或未來的環境、健康和安全法律法規而承擔大量費用。當前或未來的環境法律法規可能會損害我們的研究、開發或生產努力。此外,未能遵守這些法律和法規可能導致鉅額罰款、處罰或其他制裁。
我們相信,我們嚴格遵守適用的環境法律,持續遵守有關法律不會對我們的業務造成重大不利影響。然而,我們無法預測這些法律的變化會如何影響我們未來的運營。
歐洲/世界其他地區的政府監管
除了美國的法規,我們將受其他司法管轄區的多項規例規管,其中包括規管我們產品的臨牀試驗及商業銷售及分銷。無論我們是否獲得FDA的產品批准,我們必須在開始臨牀試驗或產品在國外上市前獲得監管機構的必要批准。美國以外的某些國家有類似的程序,要求在開始人體臨牀試驗之前提交臨牀試驗申請,就像IND一樣。例如,在歐盟,臨牀試驗申請必須提交給每個國家的國家衞生當局和獨立的倫理委員會,很像FDA和IRB。一旦臨牀試驗申請按照國家的要求獲得批准,臨牀試驗開發就可以進行。由於生物來源的原材料具有獨特的污染風險,因此在某些國家可能會限制其使用。
指導進行臨牀試驗、產品許可、定價和報銷的要求和程序因國家而異。在所有情況下,臨牀試驗都必須根據GCP以及源於《赫爾辛基宣言》的適用法規要求和倫理原則進行。
2014年4月,歐盟通過了新的臨牀試驗法規(EU)No 536/2014(法規),取代了2022年1月31日的臨牀試驗指令2001/20/EC(指令)。新法規改革了歐盟目前的臨牀試驗批准制度。具體而言,新法規直接適用於所有歐盟成員國(意味着每個歐盟成員國不需要國家實施立法),旨在簡化和簡化歐盟臨牀試驗的審批。該條例的主要特點包括:簡化了通過臨牀試驗信息系統(CTIS)的單一輸入點的申請程序;為申請準備和提交的單一文件,簡化了臨牀試驗申辦者的報告程序;以及統一的臨牀試驗申請評估程序。
為了獲得歐盟監管體系下的藥品監管批准,我們必須提交MAA。該集中程序規定,歐盟委員會(EC)授予單一的上市許可,該許可在整個歐盟以及歐洲經濟區的其他成員國(冰島、列支敦士登和挪威)有效。先進治療藥物產品(ATMPS)的MAA(包括基因治療,體細胞治療和組織工程藥物)的科學評估主要由一個稱為先進委員會的專業科學委員會進行。
33
治療(CAT)。CAT準備了一份關於ATMP的質量、安全性和有效性的意見草案,這是MAA的主題,該草案被送往人用藥品委員會(CHMP)進行最終批准。然後將CHMP建議發送給歐共體,歐共體通過一項對所有歐盟成員國具有約束力的決定。ATMP的MAA評估的最長期限為收到有效MAA之日起210天,不包括申請人在回答禁止酷刑委員會和/或CHMP提出的問題時提供補充信息或書面或口頭解釋。停止計時可能會大大延長評估MAA的時間框架,使其超過210天。如果CHMP給出了肯定的意見,EMA將該意見和支持文件一起提供給EC,後者在收到EMA的建議後67天內做出授予營銷授權的最終決定。在特殊情況下,當一種醫藥產品具有重大公共衞生利益時,特別是從治療創新的角度來看,CHMP可能會批准加速評估。如果CHMP接受這樣的請求,210天的評估時限將減少到150天(不包括時鐘停止),但如果CHMP確定申請不再適合進行加速評估,它可能會恢復到中央程序的標準時限。
在歐盟被指定為孤兒的產品可以獲得十年的市場排他性,在此期間,相同適應症的“類似醫藥產品”不得投放市場。“類似醫藥產品”的定義是含有與批准的孤兒醫藥產品中所含的一種或多種類似活性物質的醫藥產品,其目的是用於相同的治療適應症。孤兒產品還可以在歐盟獲得額外兩年的市場排他性,在歐盟,兒科研究的商定兒科調查計劃已得到遵守。歐盟對“孤兒藥品”的認定標準原則上與美國相似。根據條例(EC)141/2000第3條,符合以下標準的藥品可被指定為孤兒藥品:(1)其目的是診斷、預防或治療危及生命或慢性衰弱的疾病;(2)或者(I)在提出申請時,這種疾病在歐盟的流行率不得超過萬分之五,或者(Ii)如果沒有孤兒身份帶來的好處,該藥品的銷售不太可能在歐盟產生足夠的回報,以證明其開發所需的投資是合理的;以及(3)沒有令人滿意的診斷、預防或治療這種疾病的方法被授權在歐盟市場銷售,或者如果有這樣的方法,產品將對(EC)847/2000法規所定義的受這種疾病影響的人有重大好處。孤兒醫藥產品有資格獲得財政獎勵,如降低費用或免除費用,並在獲得營銷授權後,有權獲得經批准的治療適應症的十年市場排他性。在申請上市許可之前,必須提交孤兒指定申請。如果孤兒被指定為孤兒,申請人將獲得MAA費用減免,但如果在提交營銷授權時該指定仍在等待中,則不會。孤兒指定不會在監管審查和批准過程中傳遞任何優勢,也不會縮短監管審查和批准過程的持續時間。如果在第五年結束時確定該產品不再符合指定孤兒的標準,例如,如果該產品的利潤足夠高,不足以證明維持市場排他性是合理的,則10年的市場排他性可以減少到6年。否則,只有在非常特殊的情況下,才可以撤銷孤兒藥品的銷售排他性,例如:(I)第二申請人可以證明其產品雖然相似,但更安全、更有效或在臨牀上更好;(Ii)授權孤兒產品的營銷授權持有人同意第二次孤兒藥品申請;或(Iii)授權孤兒產品的營銷授權持有人不能供應足夠的孤兒藥品。
對於歐盟以外的其他國家,例如東歐、拉丁美洲或亞洲的國家,對進行臨牀試驗、產品許可、定價和報銷的要求因國家而異。再次重申,在所有情況下,臨牀試驗都必須根據GCP以及源於《赫爾辛基宣言》的適用法規要求和倫理原則進行。
如果我們或我們的潛在合作者未能遵守適用的外國監管要求,我們可能會面臨罰款、暫停或撤回監管批准、產品召回、產品扣押、運營限制和刑事起訴等。
歐盟一般數據保護條例
除了與我們產品的批准和商業化相關的歐盟法規外,我們還可能受歐盟的一般數據保護法規(GDPR)的約束。GDPR對歐盟個人數據的控制人和處理者施加了嚴格的要求,例如,包括更嚴格地向個人披露信息和加強個人數據權利制度,確保個人數據的處理具有法律基礎或條件,與數據泄露通知有關的規則,對保留信息的限制,增加與特殊類別數據(如健康數據)有關的要求,以及當我們與第三方處理者簽訂與個人數據處理有關的合同時,承擔額外義務。GDPR還對將個人數據從歐盟轉移到美國和其他國家實施了嚴格的規則
34
第三國。此外,GDPR規定,歐盟成員國可以制定自己的進一步法律和法規,限制個人數據的處理,包括基因、生物識別或健康數據。
GDPR適用於治外法權,我們可能會受到GDPR的約束,因為我們的數據處理活動涉及位於歐盟的個人數據,例如與我們的歐盟臨牀試驗有關的數據。不遵守GDPR的要求和歐盟成員國適用的國家數據保護法可能會導致高達20,000,000歐元的罰款或上一財政年度全球年營業額的4%(以較高者為準),以及其他行政處罰。GDPR法規可能會對我們處理的個人數據施加額外的責任和責任,我們可能需要建立額外的機制,以確保遵守新的數據保護規則。
此外,在英國退出歐盟後,英國2018年《歐盟(退出)法案》將英國GDPR納入英國法律。英國GDPR和2018年英國數據保護法規定了英國的數據保護制度,該制度獨立於歐盟的數據保護制度,但與歐盟的數據保護制度保持一致。違反英國GDPR可能會導致高達1750萬GB或全球收入4%的罰款,以金額較高者為準。儘管英國被視為歐盟GDPR下的第三個國家,但歐盟現在已經發布了一項決定,承認英國在歐盟GDPR下提供了足夠的保護,因此,源自歐盟的個人數據轉移到英國仍然不受限制。與歐盟GDPR一樣,英國GDPR將個人數據轉移到英國以外的國家,這些國家不被英國視為提供了足夠的保護。英國政府證實,個人數據從英國轉移到歐洲經濟區(EEA)仍然是自由流動的。
為了能夠將個人數據轉移到歐洲經濟區或英國以外的地區,必須按照歐洲和英國的數據保護法實施足夠的保障措施。2021年6月4日,歐共體發佈了新形式的標準合同條款,用於從歐盟/歐洲經濟區(或以其他方式受GDPR約束)的控制器或處理器向歐盟/歐洲經濟區以外(不受GDPR約束)的控制器或處理器傳輸數據。英國不受歐盟新標準合同條款的約束,但已經發布了專門針對英國的轉移機制草案,該機制將允許從聯合王國轉移(國際數據轉移附錄)。在歐盟和英國GDPR下進行受限數據傳輸時,我們將被要求實施這些新的保障措施,這樣做將需要大量的努力和成本。
遵守這些和任何其他適用的隱私和數據安全法律法規是一個嚴格和耗時的過程,我們可能需要建立額外的機制,以確保遵守新的數據保護規則。倘吾等未能遵守任何該等法律或法規,吾等可能面臨重大罰款及處罰,從而可能對吾等的業務、財務狀況及經營業績造成不利影響。
美國數據隱私法
《加州消費者隱私法》(CCPA)於2020年1月1日生效,為消費者創造了全面的個人隱私權(因為該詞在法律中有廣泛的定義),並對處理消費者或家庭個人數據的實體增加了隱私和安全義務。CCPA要求被覆蓋的公司向加州消費者提供新的披露,為這些消費者提供新的選擇退出某些個人信息銷售的方式,並允許對數據泄露提出新的私人訴訟理由。《加州隱私權法案》(CPRA)於2023年1月1日生效,並對該法案涵蓋的公司施加了額外的義務。《公民權利法》重大修改了《公民權利法》,並設立了一個國家機構,負責實施和執行《公民權利法》。隨着我們業務的發展,CCPA可能會對我們的業務活動產生影響(可能是顯著的),並使我們的業務在與個人數據和受保護的健康信息相關的不斷變化的監管環境中變得脆弱。
許多其他州也通過並提出了類似的法律。這些法律在範圍上基本相似,幷包含許多與CCPA相同的要求和例外,包括臨牀試驗數據的一般豁免和由HIPAA監管的實體的有限義務。還有一些州專門規範健康信息。例如,華盛頓州最近通過了一項健康隱私法,將規範健康信息的收集和共享,該法律還具有私人訴訟權,這進一步增加了相關的合規風險。
此類已頒佈和擬議的立法可能會增加額外的複雜性、要求、限制和潛在的法律風險,需要在合規計劃、影響策略和以前有用的數據的可用性方面投入額外的資源,並可能導致合規成本增加和/或業務慣例和政策的改變。美國不同州的全面隱私法的存在將使我們的合規義務更加複雜和昂貴,並可能增加我們可能受到執法行動或以其他方式承擔不遵守責任的可能性。
35
人力資本
截至2023年12月31日,我們共有143名全職員工。我們的員工沒有工會代表或集體談判協議涵蓋。我們認為我們與員工的關係良好。
我們通過共同創造公司價值觀、使命和願景,建立了強大的文化。我們透過定期的員工敬業度調查,尋求員工對我們文化的意見。我們提供有吸引力的福利,包括有競爭力的工資、優質的醫療保險和401K匹配。我們致力於薪酬公平,不論性別、種族/民族或性取向如何,並每半年進行全面的薪酬公平分析。在薪酬公平審查期間,我們評估並確保不同羣體的薪酬平等,以確保公平。 除了為員工提供強大的福利外,我們相信透過為員工提供各種專業發展機會,提升個人及組織的效能。我們相信,投資於員工的職業發展,為個人和組織提供了有效應對當前和未來業務需求的知識和技能,並支持組織的發展努力。我們的文化是積極支持在工作中應用新知識和技能。此外,我們在一年中確認了幾個文化節日,以支持我們多樣化的員工隊伍。2024年,我們計劃隨着增長繼續增加人力資本資源。我們亦正監察目前與僱員整體薪酬有關的工資通脹及勞工短缺情況。
企業信息
我們擁有或擁有我們在業務運營中使用的各種商標、服務標記和商號的權利。表格10—K的本年報亦可能包含第三方的商標、服務標記及商號,這些均為其各自擁有人的財產。我們在本年報表格10—K中使用或展示第三方的商標、服務標記、商號或產品,並非有意,亦不暗示與我們有關係,亦不表示我們的認可或贊助。僅為方便起見,本年報10—K表格中提及的商標、服務標記和商號可能沒有®、LOGO或SM符號出現,但省略該等提及並不以任何方式表示我們不會在適用法律的最大範圍內主張我們的權利或這些商標、服務標記和商號的適用所有人的權利。
可用信息
我們的網址是www.adicetbio.com。我們的10—K表格年度報告,10—Q表格季度報告,8—K表格當前報告,包括證據,委託書和信息聲明,以及根據1934年證券交易法第13(a),第14和第15(d)條提交或提供的這些報告的修訂,(《交易法》),在我們以電子方式向美國證券交易委員會(SEC)提交此類材料後,在合理可行的範圍內儘快通過我們網站的"投資者"部分免費獲得。本公司網站上的信息並非本年報表格10—K或本公司任何其他證券文件的一部分,除非以引用方式特別納入本年報。此外,我們向SEC提交的文件可以通過SEC的交互式數據電子應用系統訪問, Www.sec.gov。我們在任何證券備案文件中作出的所有陳述,包括所有前瞻性陳述或信息,都是在包含該陳述的文件日期作出的,除非法律要求我們這樣做,否則我們不承擔或承擔任何更新這些陳述或文件的義務。
36
第1A項。風險因素。
投資我們的普通股風險很大.在評估公司和我們的業務時,您應仔細考慮以下風險和不確定性,以及本年度報告10—K表格中的所有其他信息,包括我們的合併財務報表和相關附註和“管理層對財務狀況和經營結果的討論和分析”,以及我們向SEC提交的其他文件,然後再投資我們的普通股。我們下文所述的任何風險因素均可能對我們的業務、財務狀況或經營業績造成不利影響。如果一個或多個風險或不確定性實際發生,導致您損失全部或部分投資於我們的普通股,我們的普通股的市場價格可能會下跌。以下所述的風險和不確定性並非我們面臨的唯一風險。我們目前不知道或我們目前認為不重大的額外風險和不確定性也可能損害我們的業務。以下若干陳述為前瞻性陳述。請參閲本年報表格10—K中“前瞻性陳述及行業數據的特別説明”一節。
與我們的商業和工業有關的風險
與操作歷史相關的風險
我們的運營歷史有限,在建設能力的過程中面臨着巨大的挑戰和開支。
生物製藥產品開發是一項高度投機的事業,涉及相當大的風險。我們於2014年11月開始運營。我們的經營歷史有限,有人可以據此評估我們的業務和前景,並受到任何早期公司固有的風險,包括(其中包括)我們可能無法聘請足夠的合格人員和建立經營控制和程序的風險。我們目前沒有完整的內部資源來啟用我們的γ δ T細胞平臺。在我們建立自己的能力的同時,我們預計會遇到成長型公司在新的和快速發展的領域經常遇到的風險和不確定性,包括本文所述的風險和不確定性。因此,如果我們有成功開發和商業化生物製藥產品的歷史,對我們未來的成功或可行性的任何預測都可能不那麼準確。
我們自成立以來已產生淨虧損,並預期我們將於未來產生重大淨虧損。
我們是一家早期臨牀階段的生物製藥公司。對生物製藥產品開發的投資具有高度的投機性,因為它涉及大量的前期資本支出和重大風險,即任何潛在的候選產品將無法證明足夠的效果或可接受的安全性,獲得監管部門的批准併成為商業可行性。我們並無獲批准作商業銷售的產品,至今亦無任何產品銷售收入,我們將繼續產生與持續經營有關的重大研發及其他開支。因此,我們並沒有盈利,自成立以來已產生淨虧損。到目前為止,我們的運營資金主要來自我們的許可證和合作協議以及發行和出售我們的股本,包括最近的:(i)扣除銷售代理佣金後,但未扣除與該等銷售有關的任何開支前,所得款項淨額約為1930萬美元,2024年1月根據我們的“在市場上”計劃出售我們的普通股,以及(ii)淨所得款項約9180萬美元,扣除承銷折扣和佣金以及其他估計發行費用後,於2024年1月在承銷的公開發行中出售我們的普通股和預融資權證。截至2023年12月31日止年度,我們錄得淨虧損1.427億美元。截至2023年12月31日,我們的累計赤字為3.808億美元。
我們預計在可預見的未來將產生大量支出,隨着我們繼續研發基於我們的γ δ T細胞平臺(包括ADI—001和ADI—270)的候選產品,並尋求監管部門批准,這些支出將增加。即使我們成功地將一個或多個候選產品商業化,我們仍將繼續投入大量研發和其他支出,以開發和營銷其他候選產品。我們可能會遇到不可預見的費用、困難、併發症、延誤及其他可能對我們業務造成不利影響的未知因素。我們未來淨虧損的規模將部分取決於我們未來開支的增長率以及我們創造收入的能力。我們的過往虧損及預期未來虧損已經並將繼續對我們的股東權益及營運資金產生不利影響。此外,即使我們確實實現了盈利,我們可能無法維持或增加季度或年度的盈利能力。我們未能實現並保持盈利將壓低公司的價值,並可能損害我們籌集資金、擴大業務、維持研發努力、多樣化候選產品甚至繼續運營的能力,其中任何一項都可能對我們的業務產生重大不利影響。
37
業務、財務狀況、經營業績和前景,並導致投資者損失全部或部分投資。
我們的經常性虧損和預期支出的歷史可能會令人對我們作為一個持續經營企業的能力產生重大懷疑。
截至10—K表格的年度報告日期,我們相信,截至2023年12月31日,現金及現金等價物為1.597億美元,以及年底後通過我們的ATM計劃和承銷的公開發行籌集的資金,我們將資本化到2026年下半年。我們要想在這一點之後繼續作為一個持續經營的企業,就需要我們獲得額外的資金。倘吾等未能取得足夠資金,吾等之業務、前景、財務狀況及經營業績將受到重大不利影響,吾等或無法持續經營。如果我們無法在需要時或以可接受的條款籌集資金,我們將被迫延遲、限制、減少或終止我們的產品開發或未來一個或多個候選產品的商業化努力,或可能被迫減少或終止我們的業務。如果我們無法繼續作為一個持續經營的企業,我們可能不得不清算我們的資產,並可能獲得低於該等資產在我們經審計財務報表中的價值,投資者很可能會損失全部或部分投資。在我們未來要求的季度評估中,我們可能再次得出結論,認為我們的持續經營能力存在重大疑問,而我們獨立註冊會計師事務所未來的報告也可能包含對我們的持續經營能力表示重大疑問的聲明。倘我們尋求額外融資以資助未來的業務活動,而對我們的持續經營能力存在重大疑問,投資者或其他融資來源可能不願按商業上合理的條款向我們提供額外融資(如有的話)。
與我們的候選產品相關的風險
我們的業務高度依賴於ADI-001的成功。如果我們不能在一個或多個適應症上獲得監管部門對ADI-001的批准,並有效地將ADI-001商業化,用於治療我們獲得批准(如果有)的適應症患者,我們的業務將受到嚴重損害。
我們的業務和未來的成功取決於我們能否獲得監管部門的批准,然後成功將我們最先進的候選產品ADI—001商業化。ADI—001正處於開發的早期階段,一項正在進行的I期研究旨在評估ADI—001在複發性或難治性侵襲性非霍奇金淋巴瘤(NHL)患者中的安全性和療效,該研究於2021年3月開始,我們計劃在2024年第二季度啟動ADI—001治療狼瘡性腎炎(LN)的I期研究。
我們的臨牀前結果或迄今為止的臨牀結果可能無法預測我們計劃或正在進行的試驗或任何未來ADI—001或任何其他同種異體γ δ T細胞候選產品的研究結果。由於迄今為止臨牀上缺乏對同種異體產品和γ δ T細胞治療產品的評估,任何此類產品的失敗,或其他同種異體T細胞治療或γ δ T細胞治療的失敗,可能會嚴重影響醫生和監管機構對我們整個同種異體T細胞治療產品線可行性的意見,這可能會對我們的聲譽產生重大不利影響。如果我們的γ δ T細胞療法被認為不如自體療法或其他同種異體T細胞療法安全或有效,我們開發其他同種異體γ δ T細胞療法的能力可能會受到顯著損害。
我們的所有候選產品(包括ADI—001)都需要額外的臨牀和非臨牀開發、多個司法管轄區的監管審查和批准、大量投資、獲得足夠的商業生產能力和重大的營銷努力,才能從產品銷售中獲得任何收入。此外,由於ADI—001是我們最先進的候選產品,並且由於我們的其他候選產品基於類似的技術,如果ADI—001遇到安全性或有效性問題、製造問題、開發延遲、監管問題或其他問題,我們的開發計劃和業務將受到嚴重損害,這可能會對我們的業務、聲譽和前景造成重大不利影響。
我們的伽馬增量T細胞候選代表了一種治療自身免疫性疾病和癌症適應症的新方法,這給我們帶來了巨大的挑戰。
我們正在開發一個候選γ δ T細胞產品的管道和一個新的抗體平臺,旨在用於某些自身免疫性疾病和癌症患者。推進這些新的候選產品給我們帶來了重大挑戰,包括:
38
我們業務的成功,包括我們在未來獲得融資和產生任何收入的能力,將主要取決於我們候選產品在臨牀試驗中的積極療效和安全性以及耐用性,監管部門批准,我們的新候選產品的成功開發和商業化,以及我們建設我們的製造能力的能力,這可能永遠不會發生。我們尚未成功且可能無法成功地證明我們任何候選產品在臨牀試驗中的療效、安全性或耐久性,或其後獲得上市批准。考慮到我們的早期開發階段,如果有的話,我們可能需要幾年的時間才能證明候選產品的安全性和有效性足以保證批准商業化。倘我們未能開發或獲得監管部門批准,或(如獲批准)成功將候選產品商業化,則我們可能無法產生足夠收益以繼續經營業務,這可能會對我們的經營業績及前景造成重大不利影響。
我們的候選產品基於新技術,這使得很難預測此類候選產品的可能成功程度,以及開發和獲得監管部門批准的時間和成本。
我們已將我們的研究和開發努力集中在我們的同種異體γ δ T細胞治療,我們未來的成功取決於這種治療方法的成功開發。我們正處於開發我們的平臺和候選產品的早期階段,我們無法保證我們經歷或將來可能遇到的任何開發問題不會導致重大延誤或導致不可預見的問題或意外成本,或任何此類開發問題或問題可以被克服。我們還可能會在開發可持續、可複製和可擴展的生產工藝或將該工藝轉移給商業合作伙伴方面遇到延誤,這可能會阻礙我們完成未來的臨牀研究或及時或有利可圖地將我們的產品商業化。此外,我們對同種異體γ δ T細胞治療平臺相對於其他療法的優勢的期望可能無法實現或實現,
39
我們預期的程度。此外,隨着我們開發候選產品並瞭解這些關鍵因素,我們的可擴展性和製造成本可能會有很大差異。
此外,FDA、歐洲藥品管理局(EMA)和其他監管機構的臨牀研究要求,以及這些監管機構用於確定候選產品安全性和有效性的標準,根據潛在產品的類型、複雜性、新穎性和預期用途和市場來確定。像我們這樣的新型候選產品的監管審批過程可能更復雜,因此更昂貴,比其他更知名或廣泛研究的藥物或其他候選產品需要更長的時間。EMA和FDA對現有自體CAR T細胞療法(如Kymriah ®和Yescarta ®)的批准,以及其他批准途徑,可能並不表明這些監管機構可能需要什麼來批准我們的療法。此外,雖然我們預計與自體產品相比,我們候選產品的變異性降低,但我們沒有顯著的臨牀數據支持較低變異性的任何益處。更一般地説,任何監管機構的批准可能不表明任何其他監管機構可能需要哪些批准,或這些監管機構可能需要哪些與新候選產品有關的批准。
我們的候選產品也可能無法在臨牀試驗中取得成功,或者可能與不良事件有關,這些事件與先前已批准的自體CAR T細胞療法或未來可能批准的α β T細胞療法相區別。意外的臨牀結果可能會對我們的業務、經營業績及前景造成重大不利影響。
我們的候選產品可能會導致不良副作用或具有其他特性,這些特性可能會阻止我們的臨牀開發,阻止我們的監管批准,限制我們的商業潛力或導致重大的負面後果。
我們的候選產品引起的不良或不可接受的副作用可能會導致我們或監管機構中斷、推遲或停止臨牀試驗,並可能導致更嚴格的標籤,或者推遲或拒絕FDA、EMA或其他類似外國監管機構的監管批准。我們的臨牀試驗結果可能會顯示副作用或意想不到的特徵的嚴重程度和流行程度。已批准的自體CAR T細胞療法和正在開發的療法已顯示出頻繁的細胞因子釋放綜合徵和神經毒性的發生率,不良事件已導致患者死亡。此外,在2023年11月,FDA宣佈對接受了BCMA指導或CD19指導的自體CAR T細胞免疫療法的患者中的T細胞惡性腫瘤的報告進行調查。2024年1月,FDA決定,所有由BCMA和CD19指導的轉基因自體T細胞免疫療法的標籤中應包括與T細胞惡性腫瘤相關的新的盒式警告語言。雖然我們認為我們的伽馬增量T細胞方法可能會減少此類結果,但我們的異基因伽馬增量T細胞候選產品可能會發生類似或其他不良事件,並可能導致政府監管增加,公眾的負面看法和宣傳,對我們臨牀試驗登記的潛在影響,我們候選產品測試或批准的潛在監管延遲,對獲得批准的候選產品更嚴格的標籤要求,以及對任何此類候選產品的需求減少。此外,雖然我們預計我們對伽馬三角洲T細胞的關注可能會降低GvHD的可能性,但相對於依賴無關的阿爾法βT細胞的治療,我們的同種異體伽馬三角洲T細胞候選產品可能會發生類似或其他不良事件。
如果我們的候選產品在開發過程中出現不可接受的毒性,我們可以暫停或終止我們的試驗,或者FDA或類似的外國監管機構可以命令我們停止臨牀試驗,或者拒絕批准我們的候選產品用於任何或所有目標適應症。數據安全監測委員會還可以隨時以各種理由暫停或終止臨牀試驗,包括髮現研究患者面臨不可接受的健康風險,包括從其他無關的免疫療法試驗中推斷的風險。與治療相關的副作用也可能影響患者招募或受試者完成試驗的能力或導致潛在的產品責任索賠。新的候選治療方法,如我們正在開發的那些,可能會導致治療醫務人員可能無法適當識別或管理的新的副作用特徵。我們預計必須對使用我們的候選產品的醫務人員進行培訓,以瞭解我們的臨牀試驗和任何候選產品商業化時我們候選產品的副作用情況。在識別或管理我們的候選產品的潛在副作用方面培訓不足,可能會導致嚴重的不良事件,包括患者死亡。根據現有的臨牀前數據和其他細胞治療藥物的臨牀經驗,我們的候選流水線產品的安全性預計將包括細胞因子釋放綜合徵、神經毒性和可能的其他不良事件。這些情況中的任何一種都可能對我們的業務、財務狀況和前景產生實質性的不利影響。
除了我們可能開發的任何候選產品引起的副作用和不良事件外,我們候選產品可能使用的調理、給藥流程或相關程序也可能導致不良副作用。接受T細胞治療的患者通常會使用細胞毒性藥物從骨骼中去除幹細胞。
40
在骨髓中創造足夠的空間,讓修飾後的幹細胞植入併產生新的細胞。這一過程會產生副作用,在其他潛在風險中,可能會暫時損害患者的免疫系統,稱為中性粒細胞減少症,並減少血液凝結,稱為血小板減少症。如果我們不能證明這些不良事件是由所使用的調理方案、給藥過程或相關程序引起的,FDA、EMA或其他監管機構可以命令我們停止進一步開發或拒絕批准我們可能為任何或所有目標適應症開發的任何候選產品。即使我們能夠證明不良事件與我們的候選產品無關,此類事件也可能影響患者招募、登記患者完成臨牀試驗的能力或任何獲得監管批准的候選產品的商業可行性。
與臨牀試驗相關的風險
我們的臨牀試驗可能無法證明我們的任何候選產品的安全性和有效性,這將阻止或推遲監管部門的批准和商業化。
在我們的候選產品商業化銷售獲得監管批准之前,我們必須通過漫長、複雜和昂貴的臨牀前測試和臨牀試驗來證明我們的候選產品在每個目標適應症中都是安全和有效的。臨牀測試費用昂貴,可能需要數年時間才能完成,其結果本身也不確定。在臨牀試驗過程中,任何時候都可能發生失敗。我們候選產品的臨牀前研究和早期臨牀試驗的結果可能不能預測後期臨牀試驗的結果。
通常,由於候選產品在臨牀試驗中失敗而導致的自然流失率極高。儘管在臨牀前研究和初步臨牀試驗中取得了進展,但臨牀試驗後期階段的候選產品可能無法顯示出所需的安全性和有效性。生物製藥行業的一些公司在高級臨牀試驗中遭受了重大挫折,原因是缺乏療效、療效持久性不足或不可接受的安全性問題,儘管在早期的試驗中取得了良好的結果。大多數開始臨牀試驗的候選產品從未被批准為產品。
此外,對於正在進行的ADI—001 I期研究以及未來可能完成的任何試驗,我們不能保證FDA或外國監管機構將像我們一樣解讀結果,在我們提交候選產品之前,可能需要進行更多的試驗。如果FDA或外國監管機構對臨牀試驗結果不滿意,無法支持上市申請,我們候選產品的批准可能會被顯著推遲,或者我們可能需要花費大量額外資源(我們可能無法獲得)來進行額外試驗,以支持我們候選產品的潛在批准。上述任何情況均可能對我們的業務、前景及財務狀況造成重大不利影響。
我們可能無法提交新藥(IND)申請,以在我們預期的時間表上開始額外的臨牀試驗,即使我們能夠這樣做,FDA也可能不允許我們繼續進行。
2020年10月,FDA批准用於治療NHL患者的先導候選產品ADI—001的IND,用於NHL患者的臨牀試驗。2023年12月,FDA批准我們的IND在LN患者中進行ADI—001臨牀試驗。我們的產品線還包括ADI—270,這是一種針對CD70+癌症的裝甲γ δ CAR T細胞候選產品。我們有幾個額外的內部γ δ T細胞治療項目在臨牀前開發。我們之前宣佈,計劃每12—18個月提交一次新IND,包括在2024年上半年提交ADI—270的IND。我們可能無法在我們預期的時間表上提交這些文件,這可能會導致更多臨牀試驗的開始延遲。即使該等監管機構同意IND申請或臨牀試驗申請中規定的臨牀試驗的設計和實施,我們也不能保證該等監管機構將來不會改變其要求。此外,我們不能確定提交任何其他候選產品的IND申請將導致FDA允許開始試驗,或者一旦開始,不會出現導致我們、獨立機構審查委員會(IRB)或獨立倫理委員會,或FDA、EMA或其他監管機構決定暫停或終止臨牀試驗的問題。例如,我們可能會遇到生產延遲或其他延遲,因為IND使能研究,FDA、EMA或其他監管機構可能需要額外的臨牀前研究,這是我們沒有預料到的。此外,我們不能保證提交IND申請將導致FDA允許臨牀試驗開始,或者一旦開始,不會出現導致我們、IRB或獨立倫理委員會或FDA、EMA或其他監管機構決定暫停或終止臨牀試驗的問題,包括臨牀暫停。此外,即使這些監管機構同意IND申請或臨牀試驗申請中規定的臨牀試驗的設計和實施,我們不能保證這些監管機構將來不會改變其要求。無法啟動臨牀試驗
41
我們在當前預期的時間軸上的任何候選產品都可能對我們的業務、經營業績和前景產生重大不利影響。
我們的臨牀試驗可能會遇到很大的延誤,或者可能無法在我們預期的時間線上進行試驗。
臨牀測試是昂貴的,耗時的,並受到不確定性的影響。我們不能保證任何臨牀研究將按計劃進行或如期完成(如果有的話)。即使這些試驗按計劃開始,也可能出現可能暫停或終止此類臨牀試驗的問題。一項或多項臨牀研究的失敗可能發生在測試的任何階段,我們未來的臨牀研究可能不會成功。可能妨礙臨牀開發成功或及時完成的事件包括:
42
我們為候選產品提交IND的時間取決於進一步的臨牀前和生產成功,我們與多個第三方合作。我們不能確定我們是否能夠及時提交IND(如果有的話),或者提交IND申請或IND修正案將導致FDA允許開始測試和臨牀試驗,或者一旦開始,不會出現暫停或終止此類臨牀試驗的問題。
任何無法成功完成臨牀前和臨牀開發的情況都可能導致我們增加成本或損害我們創造收入的能力。此外,如果我們對候選產品進行了生產或配方變更,我們可能會被要求或選擇進行額外研究,以將候選產品與早期版本連接起來。臨牀研究的延遲還可能縮短我們產品享有專利保護的任何時間,並可能使我們的競爭對手在我們之前將產品推向市場,這可能會削弱我們成功將候選產品商業化的能力,並可能損害我們的業務和經營成果。
監測接受我們候選產品的患者的安全性是具有挑戰性的,這可能會對我們獲得監管批准和商業化的能力產生不利影響。
在我們目前和計劃進行的候選產品臨牀試驗中,我們已與並預期將繼續與在臨牀試驗期間產生的毒性評估和管理方面經驗豐富的學術醫療中心和醫院簽訂合同。儘管如此,這些中心和醫院可能難以觀察患者和治療毒性,這可能更具有挑戰性,由於人員變動,經驗不足,輪班變化,家庭工作人員覆蓋率或相關問題。這可能導致更嚴重或更長時間的毒性,甚至患者死亡,這可能導致我們或FDA推遲,暫停或終止我們的一項或多項臨牀試驗,並可能危及監管部門的批准。中心用於幫助管理ADI—001不良副作用的藥物可能無法充分控制副作用和/或可能對治療療效產生不利影響。這些藥物的使用可能會隨着新的醫生和中心管理我們的候選產品而增加,其中任何一個都可能對我們獲得監管批准和在預期時間表上商業化的能力產生重大不利影響,這可能對我們的業務和運營結果產生重大不利影響。
如果我們在臨牀試驗中招募患者時遇到困難,我們的臨牀開發活動可能會被推遲或受到其他不利影響。
由於各種原因,我們在臨牀試驗中可能會遇到患者入組困難。根據方案及時完成臨牀試驗取決於我們是否有能力招募足夠數量的患者,直至研究結束。患者的入組取決於許多因素,包括:
43
此外,我們的臨牀試驗將與其他臨牀試驗爭奪與我們的候選產品在相同治療領域的產品,這一競爭將減少我們可以使用的患者的數量和類型,因為一些可能選擇參加我們的試驗的患者可能會選擇參加由我們的競爭對手進行的試驗。由於合格臨牀研究人員的數量有限,我們的一些臨牀試驗地點也被我們的一些競爭對手使用,這可能會減少該臨牀試驗地點可用於我們臨牀試驗的患者數量。
此外,由於我們的候選產品代表未經驗證的治療自身免疫性疾病和癌症的方法,潛在的患者和他們的醫生可能傾向於使用傳統療法,而不是參加我們的臨牀試驗。對於癌症,他們可以使用化療和造血細胞移植或自體CAR T細胞療法。有資格接受同種異體CAR T細胞療法,但由於侵襲性癌症和無法等待自體CAR T細胞療法而不符合自體CAR T細胞療法資格的患者,可能面臨更大的併發症和治療死亡風險。對於自身免疫性疾病,潛在的患者可能會使用側重於緩解症狀的治療方法。
患者登記的延遲可能會導致成本增加,或者可能會影響我們正在進行的臨牀試驗和計劃中的臨牀試驗的時間或結果,這可能會阻止這些試驗的完成,並對我們推進候選產品開發的能力產生不利影響。
臨牀試驗既昂貴、耗時,又難以設計和實施。
人體臨牀試驗費用昂貴,難以設計和實施,部分原因是它們受到嚴格的監管要求。由於我們的Gamma Delta T細胞候選產品基於新技術,將需要建立大規模生產的“現成”產品的庫存,我們預計我們將需要廣泛的研究和開發,並有相當大的製造和加工成本。此外,治療自身免疫性疾病和癌症患者以及治療我們的候選產品可能導致的潛在副作用的成本可能會很高。因此,我們的臨牀試驗成本可能顯著高於更傳統的治療技術或藥物產品,這預計將對我們的財務狀況和實現盈利的能力產生重大不利影響。
因此,由於我們的財務和管理資源有限,我們可能會放棄或推遲尋找其他候選產品或後來被證明具有更大商業潛力的其他跡象的機會。例如,2023年11月,我們宣佈暫停ADI-925的臨牀前開發,以優先考慮ADI-270的企業資源;2024年1月,我們宣佈取消了非霍奇金淋巴瘤ADI-001第一階段臨牀試驗中LBCL患者的登記。我們的資源分配決策可能會導致我們無法利用可行的商業產品或有利可圖的市場機會。我們在當前和未來研發計劃以及特定適應症候選產品上的支出可能不會產生任何商業上可行的產品。如果不能成功地分配資源或利用戰略,將對我們的業務、財務狀況和運營結果產生不利影響。
與在國外進行研究和臨牀試驗以及在國際上營銷我們的候選產品相關的各種風險可能會對我們的業務產生實質性的不利影響。
我們計劃在全球範圍內開發我們的候選產品。因此,我們預計我們的發展項目將面臨與在國外運營相關的額外風險,包括:
44
與我們潛在國際業務相關的該等風險及其他風險可能會對我們開發候選產品以及實現或維持盈利經營的能力造成重大不利影響,從而可能對我們的業務及經營業績造成重大不利影響。
與營銷我們的候選產品相關的風險
我們候選產品的市場機會可能僅限於那些不符合或未能通過先前治療的患者,而且可能很小。
FDA通常批准新療法最初僅用於目前尚未使用目前批准的療法充分治療的患者。我們希望在此情況下首先尋求ADI—001和我們的其他候選產品的批准。隨後,對於那些被證明是足夠有益的產品(如果有的話),我們希望在早期治療線尋求批准,並可能作為一線治療。我們不能保證我們的候選產品,即使獲得批准,也會被批准用於早期治療線,並且,在任何此類批准之前,我們將不得不進行額外的臨牀試驗,包括與獲批治療的潛在比較試驗。我們還針對類似的患者人羣作為自體CAR T細胞候選產品,包括獲批的自體CAR T細胞產品。我們的療法可能不如自體CAR T細胞療法安全有效,並且僅可能被批准用於不適合自體CAR T細胞療法的患者。
我們對具有我們針對的適應症的人羣數量以及具有這些適應症的人羣中有能力接受二線或後續治療以及有可能從我們候選產品治療中受益的人羣數量的預測是基於我們的信念和估計。這些估計數來自各種來源,包括科學文獻、患者基礎或市場研究,可能被證明是不正確的。此外,新的研究可能會改變這些適應症的估計發生率或流行率。患者人數可能比預期的要少。此外,我們候選產品的潛在可尋址患者人羣可能有限,或可能無法接受我們候選產品的治療。即使
45
我們的候選產品獲得了巨大的市場份額,因為潛在的目標人羣很少,如果沒有獲得監管部門的批准,我們可能永遠無法實現盈利。
如果我們不能開發更多的候選產品,我們的商業機會將受到限制。
我們的核心策略之一是追求ADI—001以外的其他候選產品的臨牀開發。我們的產品線還包括ADI—270,這是一種針對CD70+癌症的裝甲γ δ CAR T細胞候選產品,處於臨牀前開發階段。此外,我們有幾個額外的內部γ δ T細胞治療項目在臨牀前開發。我們計劃每12—18個月向FDA提交一份新的IND,包括2024年上半年的ADI—270 IND。開發、獲得監管部門批准和商業化其他γ δ T細胞候選產品將需要大量額外資金,並且容易面臨醫療產品開發固有的失敗風險。我們無法向您保證,我們將能夠在開發過程中成功地推進這些額外候選產品中的任何一個。
即使我們獲得FDA批准,可以銷售用於治療我們目標適應症的候選產品,我們也不能向您保證任何此類候選產品將成功商業化、在市場上被廣泛接受或比其他市售替代品更有效。如果我們無法成功開發和商業化其他候選產品,我們的商業機會將受到限制。此外,未能就額外候選產品獲得監管部門批准可能會對任何其他候選產品的批准過程產生負面影響,或導致任何已批准候選產品失去批准,從而可能對我們的業務和前景造成重大不利影響。
我們目前沒有營銷和銷售組織,作為一家公司,我們沒有產品營銷經驗。如果我們無法建立市場營銷和銷售能力,或與第三方達成協議以營銷和銷售我們的候選產品,如果獲得批准,我們可能無法產生產品收入。
我們目前沒有銷售、營銷或分銷能力,作為一家公司,我們沒有產品營銷經驗。我們可能會發展營銷組織和銷售隊伍,這將需要大量的資本支出、管理資源和時間。我們將不得不與其他製藥和生物技術公司競爭,招聘、僱用、培訓和留住市場和銷售人員。
如果我們無法或決定不建立內部銷售、營銷和分銷能力,我們將尋求關於我們產品的銷售和營銷的合作安排;然而,不能保證我們能夠建立或保持這種合作安排,或者如果我們能夠這樣做,它將擁有有效的銷售隊伍。我們獲得的任何收入都將取決於這些第三方的努力,而這可能不會成功。我們可能很少或根本無法控制這些第三方的營銷和銷售活動,我們的產品銷售收入可能會低於我們自己將候選產品商業化的收入。我們在尋找第三方來幫助我們銷售和營銷我們的候選產品時也面臨着競爭。
不能保證我們能夠發展內部銷售和分銷能力,或與第三方合作伙伴建立或保持關係,將任何在美國或海外獲得監管批准的產品商業化。如果我們不能成功地營銷和分銷我們的產品,我們的業務、運營結果和前景可能會受到實質性的不利影響。
我們面臨着來自其他生物技術和製藥公司的激烈競爭,如果我們不能有效競爭,我們的經營業績將受到影響。
生物製藥行業的特點是競爭激烈,創新迅速。我們的競爭對手可能能夠開發出其他化合物或藥物,能夠達到類似或更好的效果。我們的潛在競爭對手包括大型跨國製藥公司、老牌生物技術公司、專業製藥公司和大學等研究機構。我們的許多競爭對手擁有更多的財務、技術和其他資源,例如更多的研發人員和經驗豐富的營銷和製造組織,以及完善的銷售隊伍。規模較小或處於早期階段的公司也可能成為重要的競爭對手,特別是通過與大型老牌公司的合作安排。生物技術和製藥行業的合併和收購可能會導致更多的資源集中在我們的競爭對手身上。由於技術的商業適用性的進步和投資這些行業的資本的增加,競爭可能會進一步加劇。我們的競爭對手,無論是單獨或與合作伙伴合作,都可能在獨家基礎上成功開發、獲得或許可比以下更有效、更安全、更容易商業化或成本更低的藥物或生物產品
46
我們的產品可能或可能開發我們可能需要的專有技術或專利保護,以開發我們的技術和產品。
具體地説,工程T細胞在CAR和T細胞受體(TCR)技術領域都面臨着來自多家公司的激烈競爭。即使我們獲得了監管機構對我們候選產品的批准,我們競爭對手的產品的供應和價格也可能限制我們對我們候選產品的需求和價格。如果我們對候選產品的接受受到價格競爭的影響,或者醫生不願從現有的治療方法轉向我們的候選產品,或者如果醫生改用其他新藥或生物產品,或者選擇保留我們的候選產品在有限的情況下使用,我們可能無法實施我們的業務計劃。
與製造業相關的風險
我們的製造工廠尚未開始生產運營,目前依賴於與我們簽約的第三方供應商和製造商的能力,特別是在我們的候選產品(包括ADI-001)的及時生產和交付方面。這種對第三方的依賴增加了我們無法以可接受的成本獲得足夠數量的候選產品或產品或此類數量的風險,這可能會推遲、阻止或損害我們的開發或商業化努力。
儘管我們在2022年第四季度建立了紅木城工廠的製造能力,但我們在很大程度上並預計將繼續依賴第三方生產我們的臨牀前和臨牀開發候選產品。我們自己或通過我們的CDMO可能無法實現臨牀或商業製造和細胞處理,包括及時供應“現成”產品以滿足支持我們任何候選產品的臨牀試驗的需求。如果我們不能及時獲得現成產品的供應,我們臨牀試驗的預期時間和我們候選產品的開發可能會受到不利影響。很少有公司有從無關捐贈者的血液中提取的伽馬三角洲T細胞療法的製造經驗,而伽馬三角洲T細胞在作為大規模生產的現成產品提供之前,需要幾個複雜的製造步驟。我們在管理同種異體伽馬三角洲T細胞工程過程方面的經驗有限,而且我們的同種異體過程可能比我們的競爭對手採取的方法更困難或更昂貴。我們不能確定由我們或以我們的名義採用的製造過程是否會產生安全有效的T細胞。
我們的運營仍然受到FDA的審查和監督,FDA可能會反對我們使用任何製造設施。即使我們的候選產品獲得批准,我們也將受到FDA和相應州機構的持續定期突擊檢查,以確保嚴格遵守當前的良好製造規範(CGMP)和其他政府法規。我們的候選產品製造許可證將接受持續的監管審查。
我們的商品成本開發還處於早期階段。製造和加工我們的候選產品的實際成本可能比我們預期的要高,並可能對我們候選產品的商業可行性產生重大和不利的影響。
生物製藥產品的製造是複雜的,需要大量的專業知識,包括開發先進的製造技術和工藝控制。細胞治療產品的製造商在生產中經常遇到困難,特別是在擴大規模和驗證初始生產以及確保沒有污染方面。這些問題包括生產成本和產量方面的困難,質量控制,包括產品的穩定性,質量保證測試,操作員錯誤,合格人員短缺,以及遵守嚴格執行的聯邦、州和外國法規。任何此類問題的發生都可能對我們臨牀試驗和商業銷售的產品供應產生不利影響。此外,如果在我們的候選產品供應或製造設施中發現污染物,這些製造設施可能需要關閉很長一段時間,以調查和補救污染。我們過去曾經歷過由於這些問題而導致的製造延遲,不能向您保證未來不會發生與我們候選產品的製造有關的任何穩定性或其他問題。
我們的候選產品和我們可能開發的任何產品都可能與其他候選產品和批准的產品競爭製造設施。在cGMP法規下運營的製造商數量有限,可能有能力為我們製造產品。
47
我們可能無法管理存儲和運輸我們的候選產品的物流。存儲故障、發貨延遲以及由我們、我們的供應商或我們無法控制的其他因素引起的問題,例如天氣,可能會導致可用產品丟失或阻止或延遲向患者交付候選產品。
由於資源限制或勞資糾紛,我們還可能經歷內部和外部的製造困難。我們過去經歷過外部製造困難;如果我們繼續遇到這些困難中的任何一個,我們向患者提供我們的候選產品的能力將受到威脅,這可能對我們的業務、運營結果和前景產生實質性的不利影響。
與我們的運營相關的風險
我們高度依賴我們的關鍵人員,如果我們不能成功地吸引和留住高素質的人才,我們可能就無法成功地實施我們的業務戰略。
我們能否在競爭激烈的生物技術和製藥行業中競爭,取決於我們能否吸引和留住高素質的管理、科學和醫療人員。我們高度依賴我們的管理、科學和醫療人員。失去我們的任何高管、其他關鍵員工和其他科學和醫療顧問的服務,以及我們無法找到合適的替代者,都可能導致產品開發的延遲,並損害我們的業務。
我們幾乎所有的業務都在舊金山灣區的設施中進行。該地區是許多其他生物製藥公司以及許多學術和研究機構的總部。這個市場對技術人員的競爭非常激烈,可能會限制我們以可接受的條件聘用和留住高素質人員的能力,甚至根本不能。
為了吸引有價值的員工留在我們公司,除了工資和現金激勵外,我們還提供了股票期權和隨着時間推移授予的限制性股票單位。隨着時間的推移,股票期權對員工的價值可能會受到我們股價波動的重大影響,這些波動超出了我們的控制範圍,在任何時候都可能不足以抵消其他公司提供的更有利可圖的報價。儘管我們努力留住有價值的員工,但我們的管理、科學和開發團隊的成員可能會在短時間內終止與我們的僱傭關係。雖然我們與我們的關鍵員工有僱傭協議,但這些僱傭協議規定可以隨意僱用,這意味着我們的任何員工都可以在任何時候離開我們的工作,無論是否通知。我們不為這些個人或我們任何其他員工的生命維持“關鍵人物”保險單。我們的成功還取決於我們能否繼續吸引、留住和激勵高技能的初級、中級和高級管理人員以及初級、中級和高級科學和醫療人員。為了提供額外的激勵措施來留住和激勵關鍵貢獻者,我們的董事會最近批准了2023年8月的股票期權重新定價。儘管如此,我們可能很難留住關鍵人員,這可能會對我們的業務和我們候選產品的進一步開發產生不利影響。見標題為“”的部分管理層對財務狀況和經營結果的討論和分析-最新發展-期權重新定價“有關股票期權重新定價的資料,請參閲本年度報告10-K表格的其他部分。
48
我們將需要大量的額外資金來開發我們的候選產品並實施我們的運營計劃。如果我們不能獲得額外的融資,我們可能無法完成我們候選產品的開發和商業化。
我們預計將在候選產品的臨牀開發上投入大量資金,包括正在進行的ADI-001第一階段臨牀試驗、ADI-001潛在的關鍵第二階段研究以及包括ADI-270在內的其他內部伽瑪增量T細胞治療計劃的臨牀前開發。我們將需要大量的額外資金來開發我們的產品和實施我們的運營計劃。特別是,我們將需要大量額外資金,以使我們的產品能夠商業化生產,並啟動和完成多種產品的註冊試驗。此外,如果獲得批准,我們將需要大量額外資金才能推出我們的候選產品並將其商業化。
截至10—K表格的年度報告日期,我們相信,截至2023年12月31日,現金及現金等價物為1.597億美元,以及年底後通過我們的ATM計劃和承銷的公開發行籌集的資金,我們將資本化到2026年下半年。然而,不斷變化的環境可能會導致我們消耗資本的速度比我們目前的預期要快得多,而且由於我們無法控制的情況,我們可能需要花費比目前預期更多的資金。我們可能需要額外的資金來進一步開發和商業化我們的候選產品,包括為我們的內部製造能力提供資金,如果我們選擇比我們目前預期更快地擴張,可能需要更快地籌集額外的資金。
我們不能肯定是否會以可接受的條件提供額外的資金,或根本無法確定。除了融資協議和貸款協議(定義如下)與加利福尼亞銀行(前稱太平洋西部銀行),我們沒有額外資本的承諾來源,如果我們無法籌集足夠金額或以我們可以接受的條款籌集額外資本,我們可能不得不大幅延遲,縮減或停止我們候選產品的開發或商業化或其他研發計劃。如果我們無法履行協議項下的付款義務,我們的許可協議也可能被終止。我們可能會被要求在較早的階段為我們的候選產品尋找合作者,或以低於其他可能獲得的優惠條款為我們的候選產品,或在我們本來會尋求開發或商業化的市場上放棄或以不利條款授權我們的候選產品的權利。此外,美國及全球經濟不確定性、利率上升及信貸供應減少,可能限制我們以優惠條款承擔債務的能力。此外,地緣政治緊張局勢的影響,如美國和中國雙邊關係的惡化、俄羅斯和烏克蘭衝突的升級或以色列和加沙地帶持續的武裝衝突,包括任何由此產生的制裁、出口管制或其他限制性行動,也可能導致全球市場的混亂、不穩定和波動,這可能會影響我們獲得額外資金的能力。
上述任何事件都可能嚴重損害我們的業務、前景、財務狀況和經營結果,並導致我們的普通股價格下跌。
我們已經迅速發展,需要繼續擴大我們組織的規模,在管理這種增長方面可能會遇到困難。
隨着我們的發展和商業化計劃和戰略的發展,以及我們已經過渡到上市公司的運營,我們的員工基礎迅速擴大,並期望繼續增加管理,運營,銷售,研發,營銷,財務和其他人員。當前和未來的增長給管理層成員帶來了重大的額外責任,包括:
我們未來的財務表現和我們將候選產品商業化的能力,部分取決於我們有效管理增長的能力,我們的管理層可能還不得不轉移不成比例的資金
49
我們的注意力從日常活動上移開,以便投入大量的時間來管理這些增長活動。
我們目前並在可見的將來將繼續主要依賴若干獨立組織、顧問及顧問,根據一段時間後到期的安排,提供若干服務,包括若干研究及開發以及一般及行政支援。我們無法保證獨立組織、顧問和顧問的服務將繼續在需要時及時為我們提供,也無法保證我們能夠找到合格的替代者。此外,如果我們無法有效管理我們的外包活動,或者如果顧問提供的服務的質量或準確性因任何原因而受到影響,我們的臨牀試驗可能會被延長、延遲或終止,我們可能無法獲得監管部門對候選產品的批准或以其他方式推進我們的業務。我們無法保證我們將能夠管理現有的顧問或以經濟合理的條款找到其他合資格的外部承包商和顧問。
如果我們無法通過僱傭新員工和擴大顧問和承包商團隊來有效地擴大我們的組織,我們可能無法成功地執行進一步開發和商業化候選產品所需的任務,因此,可能無法實現我們的研究、開發和商業化目標,這可能會對我們的業務、經營業績和前景產生重大不利影響。
我們可能會在未來形成或尋求戰略聯盟或達成額外的許可安排,但我們可能沒有意識到這種聯盟或許可安排的好處。
我們可能會與第三方建立或尋求戰略聯盟、創建合資企業或合作或達成額外的許可協議,我們認為這些協議將補充或增強我們在候選產品和我們可能開發的任何未來候選產品方面的開發和商業化努力。任何這些關係都可能要求我們承擔非經常性費用和其他費用,增加我們的近期和長期開支,發行證券稀釋我們現有股東或擾亂我們的管理和業務。此外,我們在尋求合適的戰略夥伴方面面臨重大競爭,談判過程耗時複雜。此外,我們在為候選產品建立戰略合作伙伴關係或其他替代安排的努力中可能無法成功,因為候選產品可能被視為處於合作努力的早期開發階段,第三方可能不認為候選產品具有證明安全性和有效性的必要潛力。任何延遲訂立與我們候選產品相關的新戰略合作協議,可能會延遲我們候選產品在某些地區的開發和商業化,這將損害我們的業務前景、財務狀況和經營業績。
如果我們授權產品或業務,如果我們無法成功地將其與我們現有的運營和公司文化整合,我們可能無法實現此類交易的利益。例如,我們與Regeneron Pharmaceuticals,Inc.簽訂的許可證和合作協議(Regeneron協議)。(Regeneron)需要重大的研發承諾,這可能不會導致候選產品的開發和商業化。我們無法確定,在戰略性交易或許可後,我們將實現證明該交易合理的業績、收入或特定淨收入,這可能對我們的業務和經營業績產生重大不利影響。
與業務中斷有關的風險
業務中斷可能會嚴重損害我們未來的收入和財務狀況,並增加我們的成本和支出。
我們以及我們的CDMO、CRO和其他承包商和顧問的運營可能會受到地震、電力短缺、電信故障、水資源短缺、洪水、颶風、颱風、火災、極端天氣條件、醫療流行病(如公共衞生危機或其他自然或人為災害或業務中斷)的影響。發生任何該等業務中斷均可能嚴重損害我們的營運及財務狀況,並增加我們的成本及開支。
如果我們或供應商的營運受到人為或自然災害的影響,而全球氣候變化或其他業務中斷可能會加劇其嚴重程度及頻率,則我們生產候選產品的能力可能會受到影響。我們在加利福尼亞州靠近主要地震斷層和火災區的設施。對我們、我們的主要供應商和我們的一般基礎設施的最終影響,
50
地震斷層和火災區以及在某些地區的鞏固情況尚不清楚,但一旦發生重大地震,火災或其他自然災害,我們的營運和財務狀況可能會受到影響。
全球衝突可能會增加供應中斷的可能性,這可能會影響我們找到製造候選產品所需的材料的能力。
持續不斷的衝突,包括俄羅斯和烏克蘭以及以色列和哈馬斯之間的衝突,可能會增加供應中斷的可能性,並阻礙我們找到製造我們的候選產品所需的材料的能力。供應中斷使我們更難為所需的材料找到合理的定價和可靠的來源,這增加了我們的成本壓力,並增加了我們可能無法獲得必要的商品和服務以成功製造我們的候選產品的風險。如果我們遇到這些困難中的任何一個,我們向臨牀前研究或臨牀試驗中的患者提供我們的候選產品的能力可能會被推遲或暫停,例如我們正在進行或計劃中的ADI-001臨牀試驗。試驗材料供應的任何延遲或中斷都可能推遲此類試驗的完成,增加與維持這些研究和開發活動相關的成本,並根據延遲的時間段,要求我們以額外費用開始新的臨牀前研究或臨牀試驗,或完全終止此類試驗。
美國食品和藥物管理局、美國證券交易委員會和其他政府機構的資金不足,包括政府停擺或這些機構運營的其他中斷,可能會阻礙它們僱用和保留關鍵領導層和其他人員的能力,阻止新產品和服務的及時開發或商業化,或者以其他方式阻止這些機構履行我們候選產品的批准所依賴的正常業務職能,這將對我們的業務產生負面影響。
FDA審查和批准新產品的能力可能受到各種因素的影響,包括政府預算和資金水平、充足的人員配備、休假、僱用和留住關鍵人員以及接受用户費用支付的能力,以及法定、監管和政策變化。因此,該機構的平均審查時間近年來一直在波動。此外,政府對我們行動可能依賴的其他政府機構的資助,包括那些為研發活動提供資金的機構,受到政治進程的影響,這一進程本質上是不穩定和不可預測的。
FDA和其他機構的中斷也可能會減緩新藥審查和/或批准所需的時間,這將對我們的業務產生不利影響。例如,在過去十年裏,美國政府多次關門,某些監管機構,如食品和藥物管理局和美國證券交易委員會,不得不讓關鍵員工休假,停止關鍵活動。如果政府長期停擺,可能會嚴重影響FDA及時審查和處理我們提交的監管文件的能力,這可能會對我們的業務產生實質性的不利影響,包括我們進入公開市場並獲得必要資本以適當資本化和繼續運營的能力。此外,未來政府關門可能會影響我們進入公開市場並獲得必要資本的能力,以便適當地利用資本並繼續為我們的業務提供資金。
與醫療監管相關的風險
我們與客户、醫生(包括臨牀研究人員、臨牀研究組織和第三方付款人)的關係直接或間接受到聯邦和州醫療欺詐和濫用法律、虛假索賠法律、醫療信息隱私和安全法律、透明度法律、政府價格報告和其他醫療法律法規的約束。如果我們或我們的員工、獨立承包商、顧問、商業合作伙伴、供應商或其他代理商違反這些法律,我們可能面臨重大處罰。
這些法律可能會影響我們的臨牀研究計劃,以及我們計劃和未來的銷售、營銷和教育計劃。特別是,醫療保健產品和服務的促銷、銷售和營銷受到旨在防止欺詐、回扣、自我交易和其他濫用行為的廣泛法律和法規的約束。這些法律法規可以限制或禁止廣泛的定價、折扣、營銷和促銷、銷售佣金、客户激勵等業務安排。我們還可能受到管理可識別患者信息的隱私和安全的聯邦、州和外國法律的約束。欲瞭解更多信息
51
有關美國醫療保健法規的討論,請參閲標題為“企業-政府法規和產品審批-其他美國醫療法律和合規性要求“在這份表格10-K的年度報告中。
這些法律的範圍和執行都是不確定的,並受到當前醫療改革環境的快速變化的影響。聯邦和州執法機構最近加強了對醫療保健公司與醫療保健提供者之間互動的審查,這導致了醫療保健行業的一系列調查、起訴、定罪和和解。由於這些法律的廣泛性,以及現有的法定例外情況和監管安全港的狹窄程度,我們的一些商業活動或我們與醫生的安排可能會受到一項或多項此類法律的挑戰。如果我們或我們的員工、獨立承包商、顧問、商業合作伙伴和供應商違反了這些法律,我們可能會受到調查、執法行動和/或重大處罰。
我們已採納商業行為及道德守則,但並非總能識別及阻止員工不當行為或業務違規行為,而我們為偵測及防止不當行為而採取的預防措施未必能有效控制未知或未管理的風險或損失,或保護我們免受政府調查或因未能遵守該等法律或法規而導致的其他行動或訴訟。為確保我們的業務安排符合適用的醫療保健法律所做的努力可能涉及大量成本。政府和執法機構可能會得出結論,我們的業務實踐可能不符合當前或未來的法規、法規或判例法,解釋適用的欺詐和濫用或其他醫療保健法律法規。如果對我們提起任何此類訴訟,而我們未能成功地為自己辯護或維護我們的權利,這些訴訟可能會對我們的業務產生重大影響,包括施加民事、刑事和行政處罰、損害賠償、沒收、罰款、可能被排除參與醫療保險、醫療補助和其他聯邦醫療保健計劃、合同損害、名譽損害,利潤和未來收益減少、額外的報告要求和/或監督,如果我們受到企業誠信協議或類似協議的約束,以解決不遵守這些法律的指控和我們的業務削減,其中任何情況可能對我們的業務經營能力和我們的經營業績造成不利影響。此外,我們的任何候選產品在美國境外的批准和商業化也可能會使我們受到上述醫療保健法律的外國等同條款以及其他外國法律的約束。
數據保護、隱私和類似法律限制信息的訪問、使用和披露,不遵守或適應這些法律的變化可能會對我們的業務造成重大不利影響。
我們受聯邦和州數據隱私和安全法律法規的約束,與隱私相關的法律和期望不斷髮展。這些法律的變更可能會限制我們的數據訪問、使用和披露,並可能需要增加支出。此外,數據保護、隱私和類似法律保護的不僅僅是患者信息,儘管它們因司法管轄區而異,但這些法律可以擴展到員工信息、業務聯繫信息、提供者信息以及與可識別個人相關的其他信息。例如,《加州消費者隱私法》(CCPA)要求所涵蓋的企業,除其他外,向加州消費者提供關於收集、使用和披露此類消費者個人信息的通知,並給予此類消費者關於其個人信息的新權利,包括選擇退出某些個人信息銷售的權利。此外,修改了CCPA的《加州隱私權法案》(CPRA)於2023年1月1日生效,並對該法案涵蓋的公司施加了額外的義務。《公民權利法》修改了《公民和公民保護法》,並設立了一個國家機構,負責實施和執行《公民和公民保護法》。還有一些州專門規範健康信息。例如,華盛頓州最近通過了一項健康隱私法,將規範健康信息的收集和共享,該法律還具有私人訴訟權,這進一步增加了相關的合規風險。此後,許多其他州也通過了類似的法律,其他州也提出了類似的新隱私法。
我們認為,在數據隱私領域,其他司法管轄區可能會加強監管。上述任何情況都可能對我們為患者提供服務的能力產生重大不利影響,進而對我們的運營結果產生重大不利影響。
歐洲經濟區(EEA)個人健康數據的收集和使用受《通用數據保護條例》(GDPR)管轄。GDPR適用於在歐洲經濟區成立的任何公司,以及在歐洲經濟區以外成立的公司,這些公司處理與向歐洲經濟區內的數據主體提供商品或服務或監控歐洲經濟區內數據主體行為有關的個人數據。GDPR加強了個人數據控制者的數據保護義務,包括有關確保適當法律法規的嚴格要求。
52
適用於個人數據處理的基礎或條件,有關獲取數據主體同意的更嚴格要求,有關收集敏感數據的更嚴格要求(例如健康數據)、擴大個人數據使用方式的披露、對"高風險"處理進行數據保護影響評估的要求、對保留個人數據的限制、強制性資料泄露通知及"設計隱私"規定,實施保障措施以保障個人資料的安全及機密性,並對作為處理者的服務提供者產生直接責任。GDPR還對將個人數據傳輸到歐洲經濟區以外的國家(如美國)實施了嚴格的規則。
在英國退出歐盟後,英國的《2018年歐盟(退出)法案》將GDPR納入英國法律,稱為英國GDPR。《英國通用數據保護條例》和《2018年英國數據保護法》規定了英國的數據保護制度,該制度獨立於歐盟的數據保護制度,但與歐盟的數據保護制度保持一致。雖然GDPR和英國GDPR目前規定的義務基本相似,但隨着時間的推移,英國GDPR可能會變得不那麼符合GDPR。英國政府現已在英國立法程序中引入了一項數據保護和數字信息法案(“英國法案”),旨在通過該法案改革英國脱歐後的數據保護制度。如果通過,英國法案的最終版本可能會進一步改變英國和歐盟數據保護制度之間的相似之處。這可能會導致額外的合規成本,並可能增加我們的整體風險。未來英國法律和法規及其與歐盟法律和法規的互動缺乏明確性,可能會增加我們處理歐盟個人信息以及隱私和數據安全合規計劃的法律風險、不確定性、複雜性和成本,並可能要求我們為英國和歐盟實施不同的合規措施。不遵守英國GDPR可能導致高達1750萬英鎊或全球收入的4%的罰款,以較高者為準。雖然英國被視為歐盟GDPR下的第三國,但歐盟委員會現在發佈了一項決定,承認英國在歐盟GDPR下提供了足夠的保護,因此,來自歐盟的個人數據傳輸到英國仍然不受限制。與歐盟GDPR一樣,英國GDPR限制將個人數據傳輸到英國不認為提供足夠保護的國家。英國政府已確認,個人數據從英國傳輸到歐洲經濟區仍然是自由流動的。
為了使個人數據能夠在歐洲經濟區或英國以外的地區傳輸,必須根據歐洲和英國的數據保護法實施充分的保護措施。歐盟委員會發布了從歐盟/歐洲經濟區(或受GDPR約束)的控制器或處理器向歐盟/歐洲經濟區以外(不受GDPR約束)的控制器或處理器傳輸數據的標準合同條款格式。英國不受歐盟新標準合同條款的約束,但已發佈了《英國國際數據傳輸協議》和新標準合同條款的國際數據傳輸附錄(IDTA),允許從英國進行數據傳輸。對於新的轉移,IDTA已經需要到位,並且必須在2024年3月21日之前對所有來自英國的現有轉移到位。根據歐盟法院在數據保護專員訴Facebook愛爾蘭有限公司和Maximillian Schrems案C—311/18(Schrems II)中的裁決,依賴標準合同條款來管理個人數據傳輸到第三國(特別是美國)的公司將需要評估數據輸入者是否能夠確保充分保障GDPR下的個人數據。該評估包括評估第三方供應商是否也能確保這些保證。對《工業發展協定》所管轄的轉讓也需要進行同樣的評估。此外,歐盟和美國已經通過了歐盟—美國數據隱私框架(框架)的充分性決定,該框架於2023年7月11日生效。該框架規定,歐盟和美國之間傳輸的個人數據的保護與歐盟提供的保護相當。這為確保按照GDPR進行向美國的轉移提供了另一個途徑。該框架已得到擴展,以涵蓋聯合王國向美國的轉讓。該框架可能會像其前身框架一樣受到挑戰。我們將被要求在根據GDPR進行限制性數據傳輸時實施這些新的保障措施,這樣做將需要大量的努力和成本。
不遵守GDPR或英國GDPR的要求以及歐洲經濟區成員國的相關國家數據保護法可能會導致高達2000萬歐元的罰款或公司上一財年全球年收入的4%,以較高者為準。此外,GDPR和英國GDPR授予數據主體要求因侵犯GDPR或UK GDPR而造成的物質和非物質損害的權利。鑑於數據保護義務變化的廣度和深度,維持對GDPR和英國GDPR的遵守將需要大量的時間、資源和費用,我們可能需要建立額外的機制,以確保遵守新的數據保護規則。這可能是繁重的,並對我們的業務、財務狀況、運營結果和前景產生不利影響。
此外,歐洲以外的許多其他司法管轄區也在考慮和/或制定新的和/或修訂的全面數據保護立法。我們還繼續看到司法管轄區實施數據本地化法律。這些法規可能會干擾我們預期的業務活動,抑制我們向這些市場擴張的能力,或者
53
禁止我們在沒有重大額外成本的情況下繼續在這些市場提供服務。由於許多隱私和數據保護法律(包括GDPR)、商業框架和標準的解釋和應用不確定,這些法律、框架和標準的解釋和應用可能與我們現有的數據管理實踐和政策不一致。如果是這樣的話,除了罰款、訴訟、違約索賠以及其他索賠和處罰的可能性外,我們還可能被要求從根本上改變我們的業務活動和做法或修改我們的解決方案,這可能會對我們的業務產生不利影響。任何不能充分解決隱私和安全問題(即使毫無根據)或遵守適用的隱私和安全或數據安全法律、法規和政策的情況,都可能導致我們承擔額外的成本和責任,損害我們的聲譽,抑制我們進行審判的能力,並對我們的業務產生不利影響。
數據保護、隱私和類似法律保護的不僅僅是患者信息,儘管它們因司法管轄區而異,但這些法律可以擴展到員工信息、業務聯繫信息、提供商信息和其他與可識別身份的個人相關的信息。不遵守這些法律可能會導致民事和刑事責任、負面宣傳、損害我們的聲譽以及合同條款下的責任等。此外,遵守此類法律可能會增加我們的成本,或者可能要求WEW在未來不提供某些類型的服務。
人工智能帶來的風險和挑戰可能會影響我們的業務,包括對我們的機密信息、專有信息和個人數據構成安全風險。
人工智能的開發和使用中的問題,再加上不確定的監管環境,可能會對我們的業務運營造成聲譽損害、責任或其他不利後果。與許多技術創新一樣,人工智能帶來的風險和挑戰可能會影響我們的業務。我們預計,與人工智能使用和倫理相關的政府和超國家監管將會增加,這也可能顯著增加這一領域的研發和合規的負擔和成本。例如,歐盟的人工智能法案(AI Act)-世界上第一部全面的人工智能法律-預計將於2024年春季生效,除一些例外情況外,將在24個月後生效。這項立法對高風險人工智能系統的提供者和部署者施加了重大義務,並鼓勵人工智能系統的提供者和部署者在開發和使用這些系統時遵守歐盟的道德原則。如果我們開發或使用受人工智能法案管轄的人工智能系統,可能需要確保數據質量、透明度和人類監督的更高標準,以及遵守具體的、可能負擔沉重和代價高昂的道德、問責和管理要求。對於經過法律和信息安全審查的特定用例,我們可能會採用生成性人工智能工具並將其集成到我們的系統中。我們的供應商可能會在不向我們披露其使用情況的情況下,將生成性人工智能工具整合到其產品中,並且這些生成性人工智能工具的提供商可能無法滿足有關隱私和數據保護的現有或快速演變的法規或行業標準,並可能會抑制我們或我們的供應商維持足夠水平的服務和體驗的能力。如果我們、我們的供應商或我們的第三方合作伙伴因使用生成性人工智能而經歷實際或預期的違規或隱私或安全事件,我們可能會丟失寶貴的知識產權和機密信息,我們的聲譽和公眾對我們安全措施有效性的看法可能會受到損害。此外,世界各地的不良行為者使用越來越複雜的方法,包括使用人工智能,從事涉及盜竊和濫用個人信息、機密信息和知識產權的非法活動。這些結果中的任何一個都可能損害我們的聲譽,導致寶貴的財產和信息損失,並對我們的業務造成不利影響。
與我們的財務狀況有關的風險
通過貸款安排籌集資金可能會限制我們的運營或產生其他不利結果。
我們與加利福尼亞銀行的現行貸款和擔保協議,於2020年7月8日、2020年9月14日、2020年9月15日、2021年10月21日、2022年12月2日和2023年5月30日修訂根據貸款協議,貸款協議項下定期貸款的利率為(i)當時有效的最優惠利率加0. 25%及(ii)4. 25%兩者中的較高者。貸款協議包含各種肯定和否定的契約,包括所需的財務報告、在加利福尼亞銀行維持若干結餘的要求、對某些資產處置的限制、對產生額外債務的限制以及其他要求。為確保我們履行本貸款協議項下的義務,我們向加利福尼亞銀行授予了我們絕大部分資產(某些知識產權資產除外)的擔保權益,併發出認股權證以購買我們的股本。
54
於2023年3月13日,我們簽署了一封信函,同意儘管貸款協議第五修正案中包含的條款,日期為2022年12月2日,(2022年貸款修正案),截至6月30日,2023年(i)我們及我們的子公司將無需維持2億美元或70%(以較低者為準)我們與加利福尼亞銀行的活期存款賬户、貨幣市場基金和/或保險現金掃付(ICS)賬户的合併餘額;(ii)我們必須在加利福尼亞銀行或其附屬公司(包括太平洋西部資產管理公司)維持我們的合併餘額。在執行這封信後,我們從加州銀行的ICS賬户中滙了1.872億美元給太平洋西部資產管理公司,後者隨後將這些資金投資於美國銀行全國協會託管的貨幣市場基金。
於2023年5月30日,我們訂立貸款協議第六次修訂,日期為2023年5月30日(2023年貸款修訂)。根據2023年貸款修正案,我們必須維持(i)3500萬美元或(ii)本公司在活期存款賬户、貨幣市場賬户和/或加州銀行的保險現金清掃賬户中的所有合併餘額中的較小者。如果我們的現金和投資總額下降到3500萬美元以下,2023年貸款修正案允許我們在加州銀行以外的一個或多個賬户中保留現金和/或投資,總額不超過250萬美元。截至2023年12月31日,我們已遵守該等契諾。
我們未能遵守貸款協議中的約定,包括由於我們某些賬户的狀況發生變化,未能在信函到期時將資金轉回加州銀行,我們的還款業務前景、業務或財務狀況、我們償還貸款的能力或價值出現重大減值,加州銀行對我們資產的留置權的完善或優先權,由太平洋西部確定,或某些其他特定事件的發生可能導致違約事件,如果不糾正或放棄,可能導致我們的全部或大部分債務加速償還,我們資產的潛在喪失抵押品贖回權和其他不利後果。此外,吾等受若干負面契約約束,其中列明未經加州銀行同意,不得在貸款協議期限內採取的行動,包括但不限於產生若干額外債務、作出若干資產處置、訂立若干合併、收購或其他業務合併交易或對吾等資產產生任何不允許留置權或其他擔保。上述對我們營運的禁令和限制可能導致我們無法:(a)按預期的時間表或條款收購有前途的知識產權或其他資產;(b)通過出售資產或業務分部來降低成本;(c)視乎各種全球銀行業務活動而重新分配我們的若干現金存款和貨幣市場賬户;(d)透過承擔額外債務刺激公司進一步增長或發展;或(e)訂立其他安排,以致有必要對公司資產施加留置權。此外,倘加州銀行提供的同意書中所載的條件未獲達成,或倘吾等不遵守函件的條款,吾等實際上將需要終止貸款協議,並償還任何未償還貸款資金或向另一貸款人再融資。截至本年報表格10—K之日期,並無根據貸款協議提取任何款項。
影響金融服務業的不利事態發展,例如涉及流動資金、金融機構或交易對手違約或不履行的實際事件或擔憂,可能會對我們當前和預計的業務運營及其財務狀況和運營結果產生不利影響。
涉及流動性有限、違約、不履約或其他不利發展影響金融機構、交易對手方或金融服務行業或一般金融服務行業的其他公司的實際事件,或對此類事件或其他類似風險的擔憂或謠言,在過去並可能在未來導致整個市場的流動性問題。例如,2023年3月10日,硅谷銀行(SVB)被加州金融保護和創新部關閉,該部門指定聯邦存款保險公司(FDIC)為接管人。同樣,2023年3月12日,Signature Bank和Silvergate Capital Corp.分別被捲入破產管理。儘管財政部、美聯儲和聯邦存款保險公司的一份聲明稱,SVB的所有儲户將在關閉一個工作日後獲得所有資金,包括未保險存款賬户中持有的資金,根據信貸協議、信用證和SVB的某些其他金融工具,Signature Bank或被FDIC置於接管的任何其他金融機構可能無法訪問其下的未提取金額。雖然我們不是SVB、Signature或任何其他金融機構目前處於接管狀態的任何此類工具的借款人或一方,但如果我們的任何貸款人或任何此類工具的對手方(包括加利福尼亞銀行或其附屬公司)被接管,我們可能無法獲得此類資金。此外,SVB信貸協議和安排的交易對手以及信用證受益人等第三方可能會受到SVB關閉的直接影響,而更廣泛的金融服務行業的流動性擔憂仍存在不確定性。類似的影響在過去也發生過,例如在2008—2010年金融危機期間。
55
通貨膨脹和利率的快速上升導致之前發行的利率低於當前市場利率的政府債券的交易價值下降。儘管美國財政部、聯邦存款保險公司和聯邦儲備委員會已經宣佈了一項計劃,向以金融機構持有的某些此類政府證券為擔保的金融機構提供高達250億美元的貸款,以降低出售此類工具可能造成的潛在損失的風險,但金融機構對客户提款的廣泛需求或金融機構對立即流動性的其他需求可能會超出此類計劃的能力。不能保證美國財政部、FDIC和聯邦儲備委員會在未來其他銀行或金融機構倒閉的情況下會提供未投保的資金,也不能保證他們會及時這樣做。
儘管我們認為有必要或適當地評估我們的銀行關係,但我們獲得資金來源和其他信貸安排的機會可能會受到影響我們、與我們有直接信貸協議或安排的金融機構、或整個金融服務業或整體經濟的因素的嚴重影響,這些資金來源和其他信貸安排足以為我們當前和預計的未來業務運營提供資金或資本。除其他外,這些因素可能包括流動性緊張或失敗、履行各類金融、信貸或流動資金協議或安排下的義務的能力、金融服務業或金融市場的中斷或不穩定,或對金融服務業公司前景的擔憂或負面預期。這些因素可能涉及與我們有金融或業務關係的金融機構或金融服務業公司,但也可能包括涉及金融市場或一般金融服務業的因素。
涉及一個或多個這些因素的事件或擔憂的結果可能包括對我們當前和預計的業務運營以及我們的財務狀況和運營結果產生的各種重大和不利影響。這些可能包括但不限於以下內容:
如果不能實現並保持對財務報告的有效內部控制,可能會損害我們的業務,並對我們的普通股價值產生負面影響。
對財務報告的有效內部控制對於我們提供可靠的財務報告是必要的,並與適當的披露控制和程序一起旨在防止欺詐。任何未能實施所需的新的或改進的控制措施,或在執行過程中遇到的困難,都可能導致我們無法履行我們的報告義務。此外,我們根據第404條進行的任何測試,或我們的獨立註冊會計師事務所隨後進行的任何測試,可能會揭示我們在財務報告內部控制方面的缺陷,這些缺陷被認為是重大弱點,或可能需要對我們的財務報表進行前瞻性或追溯性的更改,或者可能會發現需要進一步關注或改進的其他領域。較差的內部控制也可能導致投資者對我們報告的財務信息失去信心,這可能會對我們股票的交易價格產生負面影響。
我們被要求每季度披露內部控制和程序的變化,我們的管理層被要求每年評估這些控制的有效性。然而,只要我們是非加速申請者,我們的獨立註冊會計師事務所就不需要根據修訂後的2002年薩班斯-奧克斯利法案第404條證明我們對財務報告的內部控制的有效性。只要我們有資格成為《交易法》第12b-2條規定的“較小的報告公司”,我們將繼續作為非加速申報公司,只要(I)非關聯公司持有的我們普通股的市值低於2.5億美元,或(Ii)在最近完成的交易中,我們的年收入低於1.00億美元
56
截至上一財年6月30日,非關聯公司持有的我們普通股的市值不到7.0億美元。對我們財務報告內部控制有效性的獨立評估可能會發現我們管理層的評估可能無法發現的問題。我們對財務報告的內部控制存在未被發現的重大缺陷,可能會導致財務報表重述,並要求我們產生補救費用。
我們預計將繼續努力改進我們的控制程序,儘管不能保證我們的努力最終會成功或避免未來潛在的重大弱點,我們預計這些努力將繼續招致額外的費用。如果我們無法成功補救未來財務報告內部控制中的任何重大弱點,或者如果我們發現任何其他重大弱點,我們的財務報告的準確性和時機可能會受到不利影響,我們可能無法繼續遵守證券法關於及時提交定期報告的要求,以及適用的證券交易所上市要求,投資者可能會對我們的財務報告失去信心,我們的股票價格可能會因此下跌。我們還可能成為納斯達克、美國證券交易委員會或其他監管機構調查的對象,這可能會損害我們的聲譽和財務狀況,或者轉移我們核心業務的財務和管理資源。
與税收有關的風險
我們利用我們的淨營業虧損結轉和某些其他税務屬性的能力可能是有限的。
根據修訂後的1986年《國税法》(IRC)第382節和第383節,如果一家公司經歷了“所有權變更”(一般定義為一個或多個股東或股東團體,他們擁有公司至少5%的股本,在三年期間內,他們的股權總變化(按價值計算)超過50個百分點),公司使用其變動前淨營業虧損結轉和某些其他變動前税收屬性來抵消變動後收入的能力可能是有限的。類似的規則可能適用於州税法。我們過去可能經歷過這樣的所有權變化,未來可能會因為我們股票所有權的隨後變化而經歷所有權變化。截至2023年12月31日,我們有大約2.948億美元的聯邦淨營業虧損結轉,我們利用這些淨營業虧損結轉的能力可能會受到如上所述的“所有權變更”的限制,或者受到其他限制的限制,這可能會導致我們未來的納税義務增加。
税法或其實施或解釋的變化可能會對我們的業務和財務狀況產生不利影響。
涉及美國聯邦、州和地方所得税的規則不斷受到參與立法過程的人員以及美國國税局(IRS)和美國財政部的審查。税法的變化(這些變化可能具有追溯力)可能會對我們或我們普通股的持有者產生不利影響。近年來,已經發生了許多變化,未來可能還會繼續發生變化。例如,根據守則第174條,在2021年12月31日之後的納税年度,在美國發生的研發費用將被資本化和攤銷,這可能會對我們的現金流產生不利影響。此外,目前尚不清楚美國聯邦所得税的這些變化將如何影響州和地方税收。
目前正在考慮對美國聯邦所得税法進行進一步修改,税法的未來變化可能會對我們的業務、現金流、財務狀況或經營業績產生重大不利影響。無法預測新税法是否會在何時、以何種形式或生效日期頒佈,或根據現行税法或新税法頒佈、頒佈或發佈規章和裁定,這可能會導致我們或我們的股東税務責任或要求改變我們的經營方式,以儘量減少或減輕税法或其解釋。建議您諮詢您的税務顧問,瞭解税法的潛在變化對我們普通股投資的影響。
與第三方有關的風險
如果我們與Regeneron的合作被終止,或者Regeneron嚴重違反其義務,我們的業務、前景、經營業績和財務狀況將受到實質性損害。
我們的財務表現可能會受到Regeneron合作的顯著影響,我們已經進入該合作,開發下一代工程免疫細胞療法,使用針對疾病特異性細胞表面抗原的全人類CAR和TCR,以實現精確接合和殺死腫瘤細胞。根據Regeneron協議,Regeneron向我們支付了不可退還的預付款2500萬美元,截至2023年12月31日,總共支付了2000萬美元的額外研究資金,我們將與
57
Regeneron用於識別和驗證靶點,並開發針對選定靶點的工程免疫細胞療法管道。Regeneron可選擇獲得雙方開發的若干候選產品的開發權和商業權,但須就每一候選產品支付期權付款。2022年1月28日,我們收到Regeneron支付的2000萬美元,用於行使其對ADI—002的獨家許可權,我們於2022年第一季度完成了向Regeneron的相關許可權的轉讓。如果Regeneron在特定候選產品上行使其選擇權,那麼我們可以選擇參與該產品的開發和商業化。如果我們不行使我們的選擇權,我們將有權就Regeneron未來銷售的此類產品收取版税。我們沒有行使參與ADI—002開發和商業化的選擇權。作為合作的一部分,除了開發用於新型免疫細胞療法的CAR和TCR外,Regeneron還有權在合作之外的其他抗體項目中使用這些CAR和TCR。Regeneron還將有權就我們根據協議開發和商業化的產品的未來銷售獲得版税。如果Regeneron終止與我們的合作協議,我們可能沒有資源或技能來取代我們的合作者,這可能需要我們尋求額外的資金或其他可能無法以優惠條件或根本無法獲得的合作,並可能導致開發和/或商業化努力的重大延誤,並導致我們大量額外成本。終止該等合作協議或失去根據該協議提供給我們的權利可能會對我們產品的成功開發和商業化帶來重大新的和額外的風險,並可能對我們的財務狀況和經營業績造成重大損害。
Regeneron可能會改變其戰略重點或尋求替代技術,從而導致我們根據協議獲得的收入減少、延遲或無收入。Regeneron擁有多種上市產品和候選產品,無論是自己還是與其他公司(包括我們的一些競爭對手)合作,Regeneron的企業目標可能不符合我們的最佳利益。Regeneron可能會改變其參與和資助我們和Regeneron聯合活動的立場,這可能會影響我們成功實施該計劃的能力。
我們現有的和未來的合作對我們的業務將非常重要。如果我們無法維持這些協作中的任何一個,或者如果這些協作不成功,我們的業務可能會受到不利影響。
我們已經並計劃與其他公司進行合作,包括我們與Regeneron的合作協議和與Twist Bioscience Corporation(Twist)的發現協議,我們相信這些協議可以為我們提供對我們業務有益的額外能力。與Regeneron的合作為我們的項目和技術提供了重要的技術、專業知識和資金。根據我們與Twist的發現協議,Twist將利用其專有的平臺技術來幫助我們發現與我們的γ δ T細胞治療計劃相關的新型抗體。我們可能會在未來的其他合作下獲得額外的技術、專業知識和資金。我們現有的治療合作,以及我們未來的任何合作,可能會帶來許多風險,包括:
58
如果我們的治療合作不會導致產品的成功發現、開發和商業化,或者如果我們的合作者之一終止與我們的協議,我們可能不會收到任何未來的研究資金或里程碑或合作的版税。如果我們得不到根據這些協議預期的資金,我們的技術和候選產品的開發和商業化可能會被推遲,我們可能需要額外的資源來開發候選產品和我們的技術。這些風險因素中描述的與產品發現、開發、監管批准和商業化相關的所有風險也適用於我們的治療合作者的活動。
除了上述Regeneron合作,對於我們的一些項目,我們可能在未來決定與製藥和生物技術公司合作,以發現,開發和潛在的治療產品的商業化。我們在尋求合適的合作者方面面臨着巨大的競爭,因為例如,第三方也擁有同種異體T細胞技術的權利。例如,2020年4月,強生與Fate Therapeutics(一家也在使用同種異體T細胞技術的公司)達成合作協議,最多可提供四種CAR自然殺傷(NK)和CAR T細胞療法。我們能否就合作達成最終協議,除其他外,將取決於我們對合作者的資源和專業知識的評估、擬議合作的條款和條件以及擬議合作者對若干因素的評估。如果我們無法及時、以可接受的條款或根本無法與合適的合作者達成協議,我們可能不得不減少發現工作或候選產品的開發,減少或推遲我們的開發計劃或我們的一個或多個其他開發計劃,推遲我們的潛在生產或商業化,或減少任何銷售或營銷活動的範圍。或者增加支出,以我們的費用進行開發或商業化活動。如果我們選擇自行資助和進行發現、開發、製造或商業化活動,我們可能需要獲得額外的專業知識和額外的資本,而這些知識和資本可能無法以可接受的條件或根本無法獲得。如果我們未能達成合作,並且沒有足夠的資金或專業知識來進行必要的發現、開發、製造和商業化活動,我們可能無法進一步開發我們的產品
59
我們的業務可能會受到重大不利影響。
根據我們與Regeneron的協議,我們須遵守若干排他性義務。
在Regeneron協議生效日期後的五年內,除某些有限的例外情況外,我們不得直接或間接研究、開發、生產或商業化γ δ免疫細胞產品(ICP)或授予進行上述活動的許可,但根據Regeneron協議的條款除外。雙方也有義務不研究、開發、製造或商業化目標與一方正在研究計劃下開發或商業化目標相同的ICP(以及協議下的版税),只要此類活動正在發生。這些排他性義務僅限於工程化的γ δ免疫細胞,用於合理地認為在癌症中具有治療相關性的靶點。如果我們與Regeneron的合作不成功,包括由前述段落中列出的風險導致的任何失敗,並且協議和研究項目沒有終止,我們可能無法與其他公司就ICP進行合作,我們的業務可能會受到不利影響。
Regeneron協議項下的獨家經營責任已於二零二一年七月二十九日屆滿。在此有效期之前,我們推進與Regeneron商定的研究計劃範圍以外的任何γ δ免疫細胞治療的能力受到限制。根據Regeneron協議對內部開發的限制可能導致我們發現和開發針對與Regeneron合作未涵蓋的靶點的γ δ免疫細胞療法的能力延遲,並失去獲得額外研究資金和推進我們自己的技術的機會,與Regeneron合作分開。如果我們因Regeneron協議而延遲推進技術的能力,我們的業務可能會受到損害。
我們依賴並將繼續依賴第三方進行臨牀試驗。如果這些第三方未能成功履行其合同職責或在預期的最後期限內完成,我們可能無法獲得監管部門對我們的候選產品的批准或將其商業化。
我們目前依賴並將繼續依賴獨立研究者和合作者,如大學、醫療機構、CRO和戰略合作伙伴,根據與我們的協議進行臨牀前和臨牀試驗。
我們與CRO和學習網站談判預算和合同,這可能會導致我們的開發時間表延遲和成本增加。在我們的臨牀試驗過程中,我們將嚴重依賴這些第三方,我們只控制他們活動的某些方面。然而,我們有責任確保我們的每項研究都是按照適用的協議、法律、法規和科學標準進行的,我們對第三方的依賴不會免除我們的監管責任。我們和這些第三方必須遵守GCP,這是FDA和類似的外國監管機構在臨牀開發中對候選產品執行的法規和指導方針。監管當局通過定期檢查試驗贊助商、主要調查人員和試驗地點來執行這些GCP。如果我們或這些第三方中的任何一方未能遵守適用的GCP法規,在我們的臨牀試驗中產生的臨牀數據可能被認為是不可靠的,FDA或類似的外國監管機構可能會要求我們在批准我們的上市申請之前進行額外的臨牀試驗。我們不能向您保證,在檢查後,這些監管機構將確定我們的任何臨牀試驗是否符合GCP規定。此外,我們的臨牀試驗必須使用cGMPs下生產的生物製品進行,需要大量的測試患者。我們或這些第三方未能遵守這些規定或未能招募足夠數量的患者可能需要我們重複臨牀試驗,這將推遲監管批准過程。此外,如果其中任何第三方違反聯邦或州欺詐和濫用或虛假索賠法律法規或醫療保健隱私和安全法,我們的業務可能會受到牽連。
進行我們臨牀試驗的任何第三方都是我們的員工,也不會是我們的員工,除了根據我們與這些第三方達成的協議我們可以獲得的補救措施外,我們無法控制他們是否將足夠的時間和資源投入到我們正在進行的臨牀前、臨牀和非臨牀項目中。這些第三方也可能與其他商業實體有關係,包括我們的競爭對手,他們可能還在為這些實體進行臨牀研究或其他藥物開發活動,這可能會影響他們代表我們的表現。如果這些第三方未能成功履行其合同職責或義務或在預期期限內完成,如果他們需要更換,或者如果他們獲得的臨牀數據的質量或準確性因未能遵守我們的臨牀方案或監管要求或其他原因而受到影響,我們的臨牀試驗可能會被延長、推遲或終止,我們可能無法完成我們候選產品的開發、獲得監管部門的批准或成功地將其商業化。因此,我們的財務業績和候選產品的商業前景將受到損害,我們的成本可能會增加,我們創造收入的能力可能會被推遲。
60
如果我們與臨牀試驗機構的任何關係或我們將來可能使用的任何CRO終止,我們可能無法與替代臨牀試驗機構或CRO達成協議,或以商業上合理的條款達成協議。切換或增加第三方進行我們的臨牀試驗將涉及大量成本,並需要大量的管理時間和重點。此外,當新的第三方開始工作時,有一個自然的過渡期。因此,出現延誤,這可能會嚴重影響我們滿足預期臨牀開發時間表的能力。
我們目前依賴第三方生產我們的臨牀產品供應,如果獲得批准,我們可能不得不依賴第三方生產和加工我們的候選產品。
我們目前使用並希望繼續使用第三方來生產我們的候選產品。如果細胞治療領域繼續擴大,我們可能會遇到越來越多的競爭和這些材料和服務的成本。細胞治療領域對第三方製造的需求可能會以比現有產能更快的速度增長,這可能會破壞我們尋找和留住能夠以可接受的成本或根本生產足夠數量的候選產品的第三方製造商的能力。我們尚未促使我們的候選產品以商業規模生產或加工,且可能無法實現商業規模的生產和加工,因此可能無法創建批量生產的“現成”產品庫存,以滿足我們任何候選產品的需求。
我們尚未掌握足夠資料可靠地估計候選產品的商業生產及加工成本,而候選產品的實際生產及加工成本可能對候選產品的商業可行性造成重大不利影響。因此,我們可能永遠無法開發出商業上可行的產品。
此外,我們預計依賴數量有限的第三方製造商可能會對我們的運營造成不利影響,並使我們面臨以下風險:
如果與我們簽訂合同的任何CDMO未能履行其義務,我們可能會被迫自己製造材料,而我們可能沒有能力或資源,或者與不同的CDMO達成協議,而我們可能無法以合理的條件這樣做,如果根本沒有的話。在任何一種情況下,隨着我們建立替代供應來源,我們的臨牀試驗供應可能會顯著延遲。在某些情況下,製造我們的候選產品所需的技術技能可能是原始CDMO獨有的或專有的,我們可能會遇到困難,或者可能存在合同限制,禁止我們將此類技能轉讓給備用或替代供應商,或者我們可能根本無法轉讓此類技能。此外,如果我們因任何原因被要求更換CDMO,我們將被要求核實新的CDMO保持符合質量標準的設施和程序
61
以及所有適用的法規。我們還需要驗證,例如通過生產可比性研究,任何新的生產工藝都將根據之前提交給FDA或其他監管機構的質量標準生產我們的候選產品。與新CDMO驗證相關的延遲可能會對我們及時或在預算內開發候選產品或將產品商業化的能力產生負面影響。此外,CDMO可能擁有獨立擁有的與我們候選產品製造相關的技術。這將增加我們對該CDMO的依賴,或要求我們從該CDMO獲得許可證,以便讓另一家CDMO生產我們的候選產品。此外,製造商的變更通常涉及生產程序和工藝的變更,這可能要求我們在臨牀試驗中使用的先前臨牀供應品與任何新制造商的供應品之間進行橋接研究。我們可能無法證明臨牀供應品的可比性,這可能需要進行額外的臨牀試驗。
我們的合約製造商亦會面臨與我們在發展自身製造能力時所面臨的相同風險,如上文所述。這些風險中的每一個都可能延遲我們的臨牀試驗、FDA對我們候選產品的批准(如果有的話)或我們候選產品的商業化,或導致更高的成本或剝奪我們的潛在產品收入。此外,我們將依賴第三方在交付給患者之前對我們的候選產品進行放行測試。如果這些測試沒有正確進行,測試數據不可靠,患者可能會面臨嚴重傷害的風險。
基於細胞的治療依賴於特殊原材料的可用性,這些原材料可能無法以可接受的條件提供給我們,或者根本無法獲得。
我們的候選產品需要許多特殊的原材料,包括將靶向部分和其他基因傳遞給候選產品的病毒載體。我們目前通過合同製造商進行生產,其中一些合同製造商的資源和經驗有限,支持商業產品,這些供應商可能無法提供符合我們規格的原材料。這些供應商通常支持基於血液的醫院業務,通常沒有能力支持生物製藥公司根據cGMP生產的商業產品。供應商可能無法滿足我們的需求,特別是在非常規情況下,如FDA檢查或醫療危機,如廣泛污染。我們亦沒有與許多供應商訂立合約,我們可能無法以可接受的條款或根本無法與他們訂立合約。因此,我們可能會延遲接收關鍵原材料以支持臨牀或商業生產。
此外,我們候選人生產中使用的部分原材料目前可從單一供應商或少數供應商處獲得。我們不能確定這些供應商將繼續經營,或者它們不會被我們的競爭對手之一或另一家對繼續生產這些材料不感興趣的公司購買。此外,與新供應商建立關係所需的交付時間可能會很長,如果我們必須切換到新供應商,我們可能會在滿足需求方面遇到延誤。為新供應商資格所需的時間及精力可能導致額外成本、資源轉移或生產產量下降,任何情況均會對我們的經營業績造成負面影響。我們可能無法按商業上合理的條款與新供應商訂立協議,這可能會對我們的業務造成重大不利影響。
如果我們或我們的第三方供應商以造成傷害或違反適用法律的方式使用危險、非危險、生物或其他材料,我們可能要承擔損害賠償責任。
我們的研究和開發活動涉及控制使用潛在危險物質,包括化學和生物材料。我們和我們的供應商受美國聯邦、州和地方法律法規規管醫療和危險材料的使用、製造、儲存、處理和處置。雖然我們相信我們和我們的供應商使用、處理、儲存及處置該等物料的程序符合法律規定的標準,但我們和我們的供應商無法完全消除因醫療或有害物料而造成的污染或傷害的風險。由於任何此類污染或傷害,我們可能承擔責任,或者地方,城市,州或聯邦當局可能會限制這些材料的使用並中斷我們的業務運營。如果發生事故,我們可能會承擔損害賠償責任或處以罰款,責任可能超出我們的資源。遵守適用的環境法律及法規成本高昂,而當前或未來的環境法規可能會損害我們的研究、開發和生產努力,從而損害我們的業務、前景、財務狀況或經營業績。
62
我們的內部計算機系統,或我們的CRO或其他承包商或顧問使用的計算機系統,可能會出現故障或遭受安全漏洞。
我們的內部計算機系統以及我們的CRO、承包商和顧問的系統容易受到網絡安全威脅。此外,我們在一個混合的工作環境中運作。由於我們的員工及業務合作伙伴的員工在家工作並遠程訪問我們的系統,我們可能面臨更高的安全和隱私風險,包括網絡攻擊和隱私事件的風險。網絡安全威脅可能包括但不限於社會工程攻擊(包括通過網絡釣魚攻擊)、企業電子郵件泄露、在線和離線欺詐、惡意代碼(如病毒和蠕蟲)、惡意軟件(包括由於高級持續威脅入侵造成的)、拒絕服務攻擊、訪問攻擊(例如憑據填充)、人員不當行為或錯誤、勒索軟件攻擊、供應鏈攻擊、軟件錯誤、服務器故障、軟件或硬件故障、數據或其他信息技術資產丟失、廣告軟件、電信故障以及其他網絡安全風險。威脅行為者及其技術經常變化,往往性質複雜,可能直到安全事故發生後才被發現。我們可能會花費大量資源來試圖保護我們的系統免受這些威脅。某些數據隱私和安全法律以及行業最佳實踐標準可能要求我們實施和維護安全措施。雖然我們已經實施了旨在保護我們的系統以及機密和敏感數據的安全措施,但無法保證這些措施會有效。
雖然我們迄今尚未經歷任何此類重大系統故障或安全漏洞,但如果此類事件發生並導致我們的運營中斷,則可能導致我們的開發計劃和業務運營受到重大幹擾。例如,未來臨牀試驗數據的丟失可能導致我們的監管審批工作延遲,並顯著增加我們恢復或複製數據的成本。如果任何中斷或安全漏洞導致我們的數據或應用程序丟失或損壞,或不當披露機密或專有信息,我們可能會承擔責任,我們候選產品的進一步開發和商業化可能會被推遲。其他後果可能包括:政府執法行動(例如,調查、罰款、處罰、審計和檢查);額外的報告要求和/或監督;對處理敏感數據的限制(包括個人資料);訴訟(包括集體索賠);賠償義務;負面宣傳;聲譽損害;貨幣資金轉移;我們的業務中斷(包括數據的可用性);經濟損失;和其他類似的傷害。此外,我們的保險範圍在類型或金額上可能不足以保護我們免受或減輕因我們的隱私和安全慣例而產生的責任。
我們可能沒有意識到收購資產或其他戰略交易的好處。
我們持續積極評估各項戰略交易。我們可能會收購其他業務、產品或技術,以及尋求合資企業或投資互補業務。我們的策略性交易及任何未來策略性交易的成功取決於所涉及的風險及不確定因素,包括:
如果發生任何這些風險或不確定性,我們可能無法實現任何收購或戰略交易的預期利益。此外,海外收購和合資企業面臨額外風險,包括與跨文化和語言的業務整合有關的風險、貨幣風險、海外業務的潛在不利税務後果以及與特定國家相關的特定經濟、政治和監管風險。
63
未來收購或出售可能導致發行股本證券,產生債務、或然負債或攤銷開支或商譽撇銷,其中任何一項均可能對我們的財務狀況造成重大不利影響。
與政府監管相關的風險
與監管審批相關的風險
FDA的監管審批過程既漫長又耗時,我們可能會在臨牀開發和我們候選產品的監管審批方面遇到重大延誤。
包括生物製品在內的藥品的研究、測試、製造、標籤、批准、銷售、進口、出口、營銷和分銷都受到FDA和美國其他監管機構的廣泛監管。在我們獲得FDA批准的生物製品許可證申請(BLA)之前,我們不被允許在美國銷售任何生物藥物產品。我們之前沒有向FDA提交過BLA,也沒有向EMA或類似的外國當局提交過類似的批准文件。BLA必須包括廣泛的臨牀前和臨牀數據和足夠的支持信息,以確定每個所需適應症的候選產品的安全性和有效性。BLA還必須包括有關產品的化學、製造和控制的重要信息。
我們預計,我們候選產品的新穎性將在獲得監管部門批准方面帶來進一步的挑戰。例如,FDA在針對自身免疫性疾病和癌症的同種異體T細胞療法的商業開發方面經驗有限。FDA還可能要求一個專家小組,稱為諮詢委員會,審議支持許可的安全性和有效性數據的充分性。諮詢委員會的意見雖然沒有約束力,但可能會對我們根據已完成的臨牀試驗獲得候選產品許可證的能力產生重大影響,因為FDA經常遵守諮詢委員會的建議。因此,我們候選產品的監管審批途徑可能是不確定的、複雜的、昂貴的和漫長的,可能無法獲得批准。
我們也可能在獲得監管批准方面遇到延誤,包括但不限於:
64
如果醫生在招募患者參加我們候選產品的臨牀試驗而不是開出已建立安全性和有效性檔案的現有治療方案時,遇到未解決的倫理問題,我們也可能遇到延誤。此外,臨牀試驗可能被我們、正在進行此類試驗的機構的IRBs或FDA、EMA或其他監管機構暫停或終止,原因包括未能根據法規要求或我們的臨牀規程進行臨牀試驗、FDA、EMA或其他監管機構對臨牀試驗操作或試驗地點的檢查導致實施臨牀暫停、安全問題或不良副作用、未能證明使用候選產品的好處、政府法規或行政行動的變化、缺乏足夠的資金來繼續臨牀試驗,或基於數據安全監測委員會的建議。如果我們遇到任何候選產品的臨牀試驗終止或延遲完成的情況,我們候選產品的商業前景將受到損害,我們創造產品收入的能力將被推遲。此外,完成臨牀試驗的任何延誤都將增加我們的成本,減緩我們的產品開發和審批過程,並危及我們開始產品銷售和創造收入的能力。
導致或導致臨牀試驗開始或完成延遲的許多因素最終可能導致我們的候選產品得不到監管批准。
我們預計我們開發的候選產品將作為生物製品或生物製品受到監管,因此它們可能受到來自生物相似產品的競爭。
作為《平價醫療法案》的一部分,頒佈了《生物製品價格競爭和創新法》(BPCIA),為批准生物相似和可互換的生物製品建立了一條簡化的途徑。這個
65
監管途徑為FDA建立了審查和批准生物相似生物製品的法律權威,包括根據生物相似物與批准的生物製品的相似性,可能將其指定為“可互換的”。根據BPCIA,生物相似產品的申請只有在參考產品根據BLA獲得批准12年後才能獲得FDA的批准。這項法律很複雜,FDA仍在解釋和實施。
我們認為,我們的任何候選產品,如果根據BLA在美國被批准為生物製品,都應該有資格獲得12年的參考產品獨家經營期。然而,由於國會的行動或其他原因,這種排他性可能會縮短,這可能會比預期更早地為生物相似競爭創造機會。此外,一旦獲得批准,生物相似物將在多大程度上以類似於非生物製品的傳統仿製藥替代的方式取代任何參考產品,這將取決於一些仍在發展中的市場和監管因素,包括州法律。
管理我們的候選產品的監管環境尚不確定;與更成熟的細胞治療產品相關的法規仍在制定中,監管要求的變化可能會導致我們候選產品的開發延遲或中斷,或者在獲得監管批准時發生意外成本。
美國聯邦、州和地方各級以及其他國家的政府當局除其他外,對藥品和生物製品的研究、開發、測試、製造、質量控制、批准、標籤、包裝、儲存、記錄保存、推廣、廣告、分銷、批准後的監測和報告、營銷和進出口等方面進行監管。一般來説,在一種新藥或生物製劑上市之前,必須獲得大量數據,證明其質量、安全性、有效性和效果的持久性,組織成每個監管機構特有的格式,提交審查並得到監管機構的批准。
由於我們正在開發新的同種異體細胞免疫療法候選產品,我們將受到的監管要求並不完全明確。即使是屬於細胞療法類別的更成熟的產品,監管格局仍在發展中。例如,管理細胞治療產品的監管要求經常發生變化,未來可能還會繼續變化。此外,現有細胞治療產品的監管存在大量重疊,有時甚至是不協調的。
其他司法管轄區也存在複雜的監管環境,我們可能會考慮為候選產品尋求監管部門的批准,從而進一步使監管環境複雜化。例如,在歐盟,根據關於先進治療藥品(ATMP)的法規(EC)No 1394/2007在EMA內成立了一個名為“先進治療委員會”(CAT)的專門委員會,以評估ATMP的質量、安全性和有效性,並跟蹤該領域的科學發展。ATMP包括體細胞治療產品和組織工程產品。這些不同的監管審查委員會和諮詢小組以及他們不時頒佈的新的或修訂的指導方針可能會延長監管審查過程,要求我們進行額外的研究,增加我們的開發成本,導致監管立場和解釋的變化,延遲或阻止我們候選產品的批准和商業化,或導致重大的批准後限制或限制。由於我們的γ δ CAR T細胞候選產品的監管環境是新的,我們可能面臨比細胞治療產品新出現的監管更繁瑣和複雜的監管。此外,即使我們的候選產品獲得了所需的監管批准,該等批准稍後可能會因法規變更或適用監管機構對法規的解釋而被撤銷。
延遲或未能獲得將潛在產品推向市場所需的監管批准,或獲得監管批准的意外成本,可能會降低我們產生足夠產品收入以維持業務的能力。
FDA可能不同意我們的監管計劃,我們可能無法獲得候選產品的監管批准。
FDA批准新生物製劑或藥物的一般方法是,申辦方提供相關生物製劑或藥物在相關患者人羣中進行的兩項良好對照的III期臨牀研究的處置陽性數據。3期臨牀研究通常涉及數百名患者,成本高昂,需要數年時間才能完成。我們預計,我們候選產品的註冊試驗旨在在已用盡可用治療選擇的患者中進行的開放標籤、非比較、兩階段、關鍵、多中心、單組臨牀試驗中評價候選產品的療效。如果結果足夠令人信服,我們打算與FDA討論相關候選產品的BLA申報。根據臨牀數據和監管反饋,我們計劃在2025年上半年為ADI—001的潛在關鍵II期研究確定監管路徑,並在2025年下半年提供進一步的臨牀更新。然而,臨牀開發的過程本質上是不確定的,我們沒有獲得FDA的任何協議或指導,表明我們未來的監管開發計劃是
66
可以接受或足以支持BLA的提交。例如,我們可能會為我們的一個或多個候選產品尋求FDA、EMA或類似的外國監管機構的加速批准途徑。倘吾等決定提交加速審批申請,則無法保證該申請將獲接納,或任何批准將獲及時或根本不會獲批准。
FDA可能會對符合加速批准標準的候選產品給予加速批准。作為加速批准的條件,FDA可能要求獲得加速批准的藥物或生物製劑的申辦者進行上市後研究,以驗證和描述對不可逆發病率或死亡率或其他臨牀終點的預測影響。根據《2022年食品藥品綜合改革法案》(FDORA),FDA有權酌情要求在批准前或在批准後的指定時間內進行批准後確證性研究。FDORA還要求申辦者每隔180天向FDA發送一次關於此類研究狀態的更新,包括入組目標的進展,FDA必須立即公開發布這些信息。FDORA還賦予FDA更大的權力,如果申辦者未能及時進行此類研究,向FDA發送必要的更新,或者如果此類批准後研究未能驗證藥物的預期臨牀益處,FDA可以迅速撤回對獲得加速批准的藥物或生物製劑的批准。根據FDORA,FDA有權對未能盡職調查進行任何批准後確證性研究或及時向FDA提交進展報告的公司採取行動,例如罰款。即使我們尋求利用加速批准途徑,我們也可能無法獲得加速批准,即使我們這樣做,我們也可能無法對該產品進行更快的開發、監管審查或批准流程。此外,收到加速批准並不能保證產品的加速批准最終會轉換為傳統批准。此外,護理標準可能會隨着我們正在研究的相同適應症的新產品的批准而改變。這可能導致FDA、EMA或其他監管機構要求進行額外研究,以評估我們的候選產品相對於新產品。
我們的臨牀試驗結果可能也不支持批准。此外,我們的候選產品可能因多種原因而無法獲得監管部門的批准,其中包括:
我們可能會為不同適應症的部分或所有候選產品尋求孤兒藥指定,但我們可能無法獲得此類指定或維持與孤兒藥指定相關的利益,包括市場獨佔權,這可能導致我們的收入(如有)減少。
根據《孤兒藥法》,FDA可以授予用於治療罕見疾病或病症的藥物或生物製劑孤兒稱號,該罕見疾病或病症定義為在美國患者人數少於20萬的疾病或病症,或者在美國患者人數超過20萬,如果沒有合理的預期,
67
在美國開發和供應該藥物或生物製品的成本將從該藥物或生物製品在美國的銷售中收回。為了獲得孤兒藥指定,必須在提交BLA之前提出申請。在美國,孤兒藥指定使一方獲得財政獎勵,如臨牀試驗費用、税收優惠和用户費用減免等機會。在FDA授予孤兒藥稱號後,FDA公開披露該藥物的通用名稱及其潛在的孤兒用途。孤兒藥指定不會在監管審查和批准過程中帶來任何好處或縮短持續時間。
如果具有孤兒藥物名稱的產品隨後獲得FDA對其具有此類名稱的疾病的特定產品的第一次批准,則該產品有權獲得孤兒產品排他性,這意味着FDA可能在七年內不批准任何其他申請,包括BLA,以銷售相同適應症的相同生物(即具有相同主要分子結構特徵的產品)。除非在有限的情況下,如顯示出對具有孤兒藥物排他性的產品的臨牀優勢,或者FDA發現孤兒藥物排他性持有者沒有證明它可以確保獲得足夠數量的孤兒藥物,以滿足患有指定藥物的疾病或狀況的患者的需求。因此,即使我們的一個候選產品獲得了孤兒排他性,FDA仍然可以批准其他不具有相同主要分子結構特徵的生物製品在排他期內用於治療相同的適應症或疾病,或針對不同的適應症或疾病使用相同的生物製劑。此外,如果我們無法生產足夠的產品供應,或者如果隨後的申請者表現出比我們的產品更好的臨牀優勢,FDA可以放棄孤兒排他性。
我們可能會在特定的孤兒適應症中為我們的部分或所有候選產品尋求孤兒藥物稱號,在這些適應症中,這些產品的使用有醫學上可信的基礎。即使我們獲得了孤兒藥物指定,如果我們尋求批准一個比孤兒指定適應症更廣泛的適應症,那麼我們在美國的獨家營銷權可能會受到限制,如果FDA後來確定指定請求存在重大缺陷,或者如果我們無法保證足夠數量的產品來滿足患有罕見疾病或疾病的患者的需求,或者如果後續申請者證明其臨牀優勢超過我們的產品,則可能會失去獨家營銷權。此外,儘管我們可能會為其他候選產品尋求孤兒藥物指定,但我們可能永遠不會獲得這樣的指定。此外,FDA可能會進一步重新評估其在《孤兒藥物法案》下的法規和政策。我們不知道FDA是否、何時或如何在未來改變孤兒藥物的法規和政策,也不確定任何變化可能如何影響我們的業務。根據FDA可能對其孤兒藥物法規和政策做出的變化,我們的業務可能會受到不利影響。
FDA的快速通道指定,即使授予我們的任何候選產品,也可能不會導致更快的開發或監管審查或批准過程,也不會增加我們的候選產品獲得上市批准的可能性。
我們已獲得ADI-001治療非霍奇金淋巴瘤的快速通道指定。如果一種藥物或生物藥物用於治療嚴重或危及生命的疾病,而候選產品顯示出解決這種疾病未得到滿足的醫療需求的潛力,則產品候選贊助商可以申請特定適應症的快速通道指定。我們可能會為我們的某些候選產品尋求快速通道認證,但不能保證FDA會將這一地位授予我們的任何候選產品。根據FDA提供的政策和程序,具有快速通道指定的候選產品的贊助商提交的營銷申請可能有資格獲得優先審查,但快速通道指定並不保證任何此類資格或最終獲得FDA的上市批准。FDA擁有廣泛的自由裁量權,是否授予快速通道認證,因此,即使我們認為特定的候選產品有資格獲得這種認證,也不能保證FDA會決定授予它。即使我們確實獲得了快速通道指定,與傳統的FDA程序相比,我們可能不會經歷更快的開發過程、審查或批准,並且獲得快速通道指定並不能保證FDA最終獲得批准。此外,如果FDA認為我們的臨牀開發計劃的數據不再支持快速通道指定,它可能會撤回該指定。此外,FDA可以隨時撤回任何快速通道的指定。
即使為我們的任何候選產品授予RMAT認證,也可能不會加快開發或監管審查或審批過程,也不會增加我們的候選產品獲得上市批准的可能性。
我們可能會為我們的一個或多個候選產品尋求RMAT認證。2017年,FDA設立了RMAT指定,以加快對細胞療法、治療性組織工程產品、人類細胞和組織產品或使用此類療法或產品的任何組合產品的審查,旨在治療、修改、逆轉或治癒嚴重或危及生命的疾病或狀況的有限例外,並且初步臨牀證據表明,解決此類疾病或狀況的未滿足醫療需求的可能性。RMAT名稱
68
提供潛在的好處,包括更頻繁地與FDA開會討論候選產品的開發計劃,以及滾動審查和優先審查的資格。被授予RMAT認證的產品也有資格根據合理地可能預測長期臨牀益處的替代物或中間終點,或依賴於從大量地點獲得的數據,包括通過擴展到更多地點,獲得加速批准。不能保證我們的任何候選產品都能獲得RMAT認證。RMAT指定不會改變FDA的產品批准標準,也不能保證這樣的指定會加速審查或批准,也不能保證批准的適應症不會比指定所涵蓋的適應症更窄。此外,如果隨着臨牀數據的出現而不再符合資格標準,RMAT的指定可能會被撤銷。
早期臨牀前研究和臨牀試驗的陽性結果不一定預測我們產品候選產品未來臨牀試驗的結果,可能會隨着更多患者數據的獲得而發生變化,並受到審計和驗證程序的影響,這些程序可能會導致最終數據發生重大變化。如果我們不能在未來的臨牀試驗中複製我們候選產品的早期臨牀前研究和臨牀試驗的積極結果,我們可能無法成功開發、獲得監管部門對我們候選產品的批准並將其商業化。
我們可能會不時公佈我們的臨牀前研究或臨牀試驗的中期、頂級或初步結果。這樣的臨牀結果面臨這樣的風險,即隨着患者登記的繼續和更多患者數據的獲得,一個或多個臨牀結果可能會發生實質性變化。初步或最重要的結果也仍然受到審計和核查程序的制約,這可能會導致最終數據與我們以前公佈的初步數據有很大不同。因此,在獲得最終數據之前,應謹慎看待中期和初步數據。我們可能完成的臨牀試驗數據面臨這樣的風險,即隨着患者登記的繼續和更多患者數據的獲得,一個或多個臨牀結果可能會發生實質性變化。我們還作出假設、估計、計算和結論,作為我們數據分析的一部分,我們可能沒有收到或沒有機會全面和仔細地評估所有數據。初步數據或“頂線”數據仍需接受審計和核實程序,這可能會導致最終數據與我們先前宣佈的初步數據有很大不同。因此,在最終數據可用之前,應謹慎看待中期、“頂線”和初步數據。初步或中期數據與最終數據之間的不利差異可能會嚴重損害我們的業務前景。公佈中期業績的時間也很難預測。
因此,我們的臨牀前研究以及我們候選產品的正在進行和未來的臨牀試驗的任何積極結果可能不一定預測到所需的後續臨牀試驗的結果。同樣,即使我們能夠根據我們目前的開發時間表完成我們計劃的臨牀前研究或任何未來的臨牀試驗,這些臨牀前研究和臨牀試驗的積極結果可能不會在後續的臨牀前研究或臨牀試驗結果中複製。
製藥和生物技術行業的許多公司在早期開發取得積極成果後,在後期臨牀試驗中遭受了重大挫折,我們不能確定我們不會面臨類似的挫折。除其他外,這些挫折是由臨牀試驗進行期間的臨牀前發現,或在臨牀前研究和臨牀試驗中進行的安全性或有效性觀察引起的,包括以前未報告的不良事件。此外,臨牀前和臨牀數據往往容易受到不同解釋和分析的影響,許多公司認為他們的候選產品在臨牀前研究和臨牀試驗中表現令人滿意,但仍未能獲得FDA或類似監管部門的批准。
此外,我們正在進行的臨牀試驗採用了“開放標籤”試驗設計,在計劃的未來臨牀試驗中可能會出現這種情況。“開放標籤”臨牀試驗是指患者和研究者都知道患者是否正在接受候選試驗藥物或現有獲批藥物或安慰劑的臨牀試驗。最典型的是,開放標籤臨牀試驗只檢測候選研究藥物,有時可能在不同的劑量水平下進行。開放標籤臨牀試驗受各種限制,可能會誇大任何治療效果,因為開放標籤臨牀試驗中的患者在接受治療時都知道。開放標籤臨牀試驗可能會受到“患者偏見”的影響,患者認為他們的症狀已經改善,只是因為他們意識到接受實驗性治療。此外,開放標籤臨牀試驗可能會受到"研究者偏倚"的影響,即那些評估和審查臨牀試驗的生理結局的人知道哪些患者接受了治療,並可能更有利地解釋治療組的信息。當在對照環境中使用安慰劑或活性對照進行研究時,開放標籤試驗的結果可能無法預測我們任何候選產品的未來臨牀試驗結果。
69
如果我們報告的臨牀更新或中期、“頂線”或初步數據與實際結果不同,或者其他人(包括監管機構)不同意得出的結論,我們獲得候選產品批准和商業化的能力、我們的業務、經營成果、前景或財務狀況可能會受到損害。
在一個司法管轄區獲得並保持對我們候選產品的監管批准,並不意味着我們將成功地在其他司法管轄區獲得我們候選產品的監管批准。
在一個司法管轄區獲得並維持我們候選產品的監管批准並不保證我們能夠在任何其他司法管轄區獲得或維持監管批准,而在一個司法管轄區未能獲得監管批准或延遲獲得監管批准可能會對其他司法管轄區的監管批准過程產生負面影響。例如,即使FDA批准候選產品的上市許可,外國司法管轄區的類似監管機構也必須批准候選產品在這些國家的生產、營銷和推廣。批准程序因司法管轄區而異,可能涉及的要求和行政審查期不同於或長於美國的要求和行政審查期,包括額外的臨牀前研究或臨牀試驗,因為在一個司法管轄區進行的臨牀研究可能不被其他司法管轄區的監管機構接受。在美國以外的許多司法管轄區,候選產品必須獲得報銷批准,然後才能批准在該司法管轄區銷售。在某些情況下,我們打算為我們的產品收取的價格也需要得到批准。
我們也可以在其他國家提交營銷申請。美國以外司法管轄區的監管機構對候選產品的批准有要求,我們在這些司法管轄區上市前必須遵守這些要求。獲得外國監管批准和遵守外國監管要求可能會給我們帶來重大延誤、困難和成本,並可能推遲或阻止我們的產品在某些國家/地區推出。如果我們未能遵守國際市場的監管要求和/或獲得適用的營銷批准,我們的目標市場將會減少,我們充分發揮我們候選產品的市場潛力的能力將受到損害。
此外,2016年6月23日,英國舉行全民公決,多數選民批准退出歐盟或英國脱歐,英國於2020年1月31日正式離開歐盟。歐盟製藥法有一段過渡期,在此期間,歐盟製藥法繼續適用於英國,該過渡期已於2020年12月31日到期。然而,歐盟和英國已經簽署了一項貿易與合作協定(TCA),該協定自2021年1月1日起暫時適用,並自2021年5月1日起正式適用。《TCA》包括了與藥品有關的具體條款,其中包括GMP的相互承認、藥品生產設施的檢查和GMP文件的發佈,但沒有預見到英國和歐盟藥品法規的大規模相互承認。目前,英國已通過《2012年人用藥品條例》(經修訂)執行歐盟關於藥品營銷、推廣和銷售的立法(根據《北愛爾蘭議定書》,歐盟監管框架將繼續適用於北愛爾蘭)。因此,英國的監管制度目前在很大程度上與歐盟的監管制度保持一致,但由於英國的監管制度獨立於歐盟,而且《貿易法》沒有規定英國和歐盟的藥品立法相互承認,這些制度將來可能會有所不同。例如,2022年1月31日在歐盟生效的新《臨牀試驗條例》,規定了涵蓋多個歐盟成員國的簡化臨牀試驗申請和評估程序,但尚未落實到英國法律中,需要單獨提交申請才能獲得英國的臨牀試驗授權。英國和歐盟之間的監管制度不同,可能會增加我們在英國和歐盟申請和獲得授權的監管負擔。
即使我們的候選產品獲得監管部門的批准,我們仍將面臨持續的監管義務和持續的監管審查,這可能導致重大額外開支,如果我們未能遵守監管要求或我們的候選產品出現意外問題,我們可能會受到處罰。
我們就候選產品獲得的任何監管批准都需要上市後監督,以監控候選產品的安全性和有效性。FDA還可能要求制定風險評估和緩解策略(REMS),以批准我們的候選產品,這可能需要藥物指南、醫生溝通計劃或其他確保安全使用的元素,如限制分銷方法、患者登記和其他風險最小化工具。此外,如果FDA或類似的外國監管機構批准了我們的候選產品,我們的候選產品的生產工藝、標籤、包裝、分銷、不良事件報告、儲存、廣告、促銷、進口、出口和記錄保存將受到廣泛和持續的監管要求的約束。這些要求包括提交安全性和其他上市後信息和報告、註冊以及持續遵守cGMP和GCP,以滿足任何
70
我們在批准後進行的臨牀試驗。因此,我們和我們的合同製造商必須向FDA和某些州機構註冊企業,並將接受FDA和州機構的持續審查和突擊檢查,以評估是否遵守cGMP,遵守任何BLA、其他上市申請和先前對檢查結果的回覆中所作承諾。製造商和製造商的設施必須遵守廣泛的FDA和類似的外國監管機構要求,包括確保質量控制和生產程序符合cGMP法規和適用的產品跟蹤和追溯要求。處方藥產品的藥品供應鏈中涉及的製造商和其他各方還必須通知FDA假冒、轉移、盜竊和故意摻假的產品或不適合在美國銷售的產品。因此,我們和其他與我們合作的人必須繼續在所有監管合規領域(包括製造、生產和質量控制)投入時間、金錢和精力。此外,FDA可能會要求我們進行另一項研究,以獲得額外的安全性或生物標誌物信息。
此外,即使候選產品獲得上市批准,該批准也可能受限於產品可能上市的指定用途或批准條件,或包含對昂貴的上市後檢測和監督的要求,以監測產品的安全性或有效性。我們還將被要求遵守FDA的促銷和廣告規則,其中包括直接面向消費者的廣告標準,限制在產品批准用途中未描述的用途或患者人羣中推廣產品(稱為"標籤外使用"),對行業贊助的科學和教育活動的限制以及對涉及互聯網和社交媒體的宣傳活動的要求。FDA和其他機構積極執行禁止推廣標籤外使用的法律法規,被發現不當推廣標籤外使用的公司可能會承擔重大責任。然而,醫生可以根據其獨立的醫學判斷,處方合法可用的產品用於標籤外使用。FDA並不規範醫生在治療選擇方面的行為,但FDA確實限制製造商就標籤外使用其產品的主題進行溝通。稍後發現我們候選產品之前未知的問題,包括非預期嚴重度或頻率的不良事件,或我們的第三方供應商或生產工藝,或未能遵守監管要求,可能導致修訂批准的標籤以增加新的安全性信息;強制進行上市後研究或臨牀研究以評估新的安全性風險;或在REMS計劃下施加分配限制或其他限制。其他潛在後果包括:
FDA和其他監管機構的政策可能會改變,可能會頒佈額外的政府法規,以阻止、限制或推遲對我們候選產品的監管批准。我們無法預測美國或國外未來的立法或行政或行政行動可能產生的政府監管的可能性、性質或程度。如果我們緩慢或無法適應現有要求的變化或採用新的要求或政策,或者如果我們無法保持監管合規性,我們可能會失去我們可能獲得的任何營銷批准,我們可能無法實現或維持盈利。
即使我們的候選產品獲得監管機構的批准,這些產品也可能無法獲得醫生、患者、醫院、癌症治療中心和醫學界其他人的市場接受,從而對我們實現商業和財務預測的能力產生不利影響。
使用經過改造的伽馬增量T細胞作為自身免疫性疾病和癌症的潛在治療方法是最近的發展,可能不會被醫生、患者、醫院、癌症治療中心和醫學界的其他人廣泛接受。我們預計,包括風濕科醫生、腎病學家和腫瘤學家在內的內科醫生對我們產品的市場接受度尤其重要,而我們可能無法對他們進行有關
71
使用我們的候選產品的好處有很多原因。其他因素將影響我們的候選產品是否被市場接受,包括:
如果我們的候選產品獲得批准,但未能獲得醫生、患者、醫院、癌症治療中心或醫學界其他人的市場認可,我們將無法產生可觀的收入。即使我們的產品獲得市場認可,如果推出了比我們的產品更受歡迎、更具成本效益或使我們的產品過時的新產品或技術,我們可能無法隨着時間的推移保持市場接受度。
在某些細分市場中,我們的候選產品的覆蓋範圍和報銷可能有限或不可用,這可能使我們難以在獲得批准的情況下銷售我們的候選產品。
我們候選產品的成功銷售,如果獲得批准,取決於第三方付款人的承保範圍和足夠的補償,包括政府醫療保健計劃,如聯邦醫療保險和醫療補助、管理式醫療組織和商業付款人等。對於我們獲得監管部門批准的任何候選產品的覆蓋範圍和報銷狀態,存在重大不確定性。此外,由於我們的候選產品代表了治療自身免疫性疾病和癌症的新方法,我們無法準確估計我們候選產品的潛在收入。關於承保範圍和補償事項的進一步討論,見題為企業-政府監管和產品審批-覆蓋範圍、定價和報銷在……裏面 年度報告10-K表格
為自己的病情提供醫療服務的患者通常依靠第三方付款人來報銷與其治療相關的全部或部分費用。從第三方付款人那裏獲得保險和足夠的補償對新產品的接受度至關重要。
72
第三方付款人決定他們將覆蓋哪些藥物和治療以及報銷金額。第三方付款人的報銷可能取決於許多因素,包括但不限於第三方付款人對產品使用情況的確定:
從政府或其他第三方付款人那裏獲得產品的保險和報銷是一個既耗時又昂貴的過程,這可能需要我們向付款人提供支持我們產品使用的科學、臨牀和成本效益數據。即使我們獲得了特定產品的保險,如果由此產生的報銷率不足,醫院可能不會批准我們的產品在其設施中使用,或者第三方付款人可能要求患者發現無法接受的高得令人無法接受的共同付款。患者不太可能使用我們的候選產品,除非提供保險,而且報銷足以支付我們候選產品的很大一部分成本。產品本身可能會單獨報銷,也可能不會。相反,醫院或主管醫生可能只會因提供使用我們產品的治療或程序而獲得報銷。此外,醫療保險和醫療補助服務中心(CMS)不時修訂用於向醫療保健提供者報銷的報銷制度,包括聯邦醫療保險醫生收費表和門診預期付款制度,這可能會導致醫療保險付款減少。在某些情況下,私人第三方支付者依賴全部或部分聯邦醫療保險支付系統來確定支付率。改變政府醫療保健計劃,減少這些計劃下的付款,可能會對私人第三方付款人的付款產生負面影響,並降低醫生使用我們的候選產品的意願。
在美國,第三方付款人之間沒有統一的產品承保和報銷政策。因此,產品的承保範圍和報銷範圍因付款人而異。此外,一個付款人決定為一種產品提供保險並不能保證其他付款人也會為該產品提供保險。可能沒有足夠的第三方報銷來使我們能夠維持足夠的價格水平,以實現我們在產品開發方面的投資的適當回報。由於我們的候選產品可能比傳統療法具有更高的商品成本,並且可能需要長期的後續評估,因此覆蓋範圍和報銷率可能不足以使我們實現盈利的風險可能更大。與新批准的產品的保險覆蓋和報銷有關的不確定性很大。目前很難預測第三方付款人將就我們的候選產品的承保範圍和報銷做出什麼決定。此外,支付方法可能會受到醫療保健立法和監管舉措的影響。預計未來將採取更多的州和聯邦醫療改革措施,其中任何一項都可能限制聯邦和州政府為醫療產品和服務支付的金額,這可能導致對某些藥品的需求減少或額外的定價壓力。具體地説,美國國會已經進行了幾次調查以及聯邦和州立法,旨在提高藥品定價的透明度,降低聯邦醫療保險下處方藥的成本,審查定價與製造商患者計劃之間的關係,以及改革政府計劃的藥品報銷方法。我們預計,由於管理型醫療保健的趨勢、醫療保健組織日益增長的影響力、成本控制舉措和額外的立法變化,我們將面臨與銷售我們的任何候選產品相關的定價壓力。
藥品的淨價可能會通過政府醫療保健計劃或私人付款人要求的強制性折扣或回扣,以及未來任何限制從可能以低於美國價格銷售的國家進口藥品的法律的放鬆來降低。越來越多的第三方付款人要求製藥公司在標價的基礎上向他們提供預定的折扣,並對醫療產品的定價提出挑戰。此外,許多製藥商必須計算並向政府報告某些價格報告指標,如平均銷售價格和最佳價格。在某些情況下,當這些指標沒有準確和及時地提交時,可能會適用處罰。此外,這些藥品的價格可能會通過政府醫療保健計劃要求的強制性折扣或回扣來降低。支付方法可能會受到醫療保健立法和監管舉措的影響。
73
我們打算尋求批准,在美國和選定的外國司法管轄區銷售我們的候選產品。美國和海外政府和第三方支付機構加大力度限制或降低醫療費用,可能會導致此類組織限制新批准產品的覆蓋範圍和報銷水平,因此,他們可能無法為我們的候選產品支付或提供足夠的支付。如果我們的候選產品在一個或多個外國司法管轄區獲得批准,我們將遵守這些司法管轄區的規則和法規。在一些外國國家,特別是歐洲國家,生物製品的定價受政府控制。在這些國家,在獲得候選產品的上市批准後,與政府當局的定價談判可能需要相當長的時間。其中一些國家可能需要完成臨牀試驗,將特定候選產品與現有治療方法的成本效益進行比較。其他歐盟成員國允許公司自行定價藥品,但監督和控制公司利潤。醫療保健費用的下行壓力已經變得非常大。因此,新產品進入市場的壁壘越來越高。此外,在一些國家,從低價市場的跨界進口對國內的定價造成了商業壓力。
如果政府和其他第三方付款人未能提供保險和足夠的補償,我們獲得監管部門批准進行商業銷售的任何候選產品的適銷性可能會受到影響。我們預計藥品價格下行壓力將持續。此外,承保政策和第三方報銷費率可能隨時發生變化。即使我們獲得監管部門批准的一個或多個產品獲得了有利的承保和報銷狀態,未來也可能實施不太有利的承保政策和報銷費率。
醫療改革的進展可能會對我們銷售候選產品的能力產生負面影響,如果獲得批准,盈利。
第三方支付者,無論是國內還是國外,政府還是商業,正在開發越來越複雜的控制醫療成本的方法。在美國和某些外國司法管轄區,醫療保健系統發生了許多立法和監管變化,這些變化可能會影響我們銷售候選產品的能力,如果獲得批准,盈利。有關醫療改革事宜的進一步討論,請參閲題為"商業—政府監管和產品審批—醫療改革“在這份表格10-K的年度報告中。
外國、聯邦和州各級已經有並可能繼續有立法和監管提案,旨在擴大醫療保健的可用性,並控制或降低醫療保健成本。
成本控制措施或其他醫療改革的實施可能會阻礙我們創造收入、實現盈利或將我們的產品商業化。該等改革可能會對我們可能成功開發並可能獲得監管部門批准的候選產品的預期收益產生不利影響,並可能影響我們的整體財務狀況和開發候選產品的能力。此外,鑑於處方藥和生物製品價格上漲,美國政府加強了對藥品和生物製品定價做法的審查。這種審查導致了各種國會調查,並提出並頒佈了聯邦和州立法,旨在提高產品定價的透明度,審查定價與製造商患者計劃之間的關係,並改革政府計劃的產品報銷方法。
我們預計未來將採取額外的美國聯邦醫療改革措施,其中任何一項措施都可能限制美國聯邦政府為醫療保健藥品和服務支付的金額,這可能導致對我們候選藥物的需求減少或額外的定價壓力。美國各州也越來越積極地通過立法和實施旨在控制藥品和生物產品定價的條例,包括價格或病人報銷限制、折扣、對某些藥品准入和銷售成本披露的限制和透明度措施,以及旨在鼓勵從其他國家進口和大宗採購的措施。第三方付款人對付款金額的法定價格控制或其他限制可能會損害我們的業務、財務狀況、經營業績和前景。此外,地區醫療保健當局和個別醫院越來越多地使用招標程序來確定哪些藥品和哪些供應商將被納入其處方藥和其他醫療保健計劃。這可能會減少對我們藥物的最終需求或對我們的藥物定價造成壓力,從而可能對我們的業務、財務狀況、經營業績和前景造成負面影響。政府、保險公司、管理式醫療機構和其他醫療服務支付方為控制或降低醫療成本和/或實施價格控制而持續努力可能會對以下方面造成不利影響:
74
聯邦醫療保險或其他政府計劃報銷的任何減少都可能導致私人支付者支付的類似減少,這可能會對我們未來的盈利能力產生不利影響。
與我們的知識產權有關的風險
與我們的知識產權有關的風險
如果我們保護與我們的技術相關的知識產權的專有性質的努力不夠,我們可能無法在我們的市場上有效地競爭。
我們依靠專利、商業祕密保護和許可協議的組合來保護與我們的技術相關的知識產權。任何向第三方披露或盜用我們的機密專有信息,都可能使競爭對手迅速複製或超越我們的技術成果,從而削弱我們在市場上的競爭地位。
我們已經提交了額外的專利申請,我們預計將在美國和其他國家提交額外的專利申請。然而,我們無法預測:
生物和製藥產品的物質組成專利,如基於CAR的候選產品,通常為這些類型的產品提供強有力的知識產權保護,因為這些專利提供的保護不考慮任何使用方法。我們無法確定我們的未決專利申請中涵蓋我們候選產品物質組成的權利要求是否被美國專利商標局(USPTO)或外國專利局視為可申請專利,或者我們的任何已發佈專利中的權利要求是否被美國或外國法院視為有效和強制執行。使用方法專利保護特定方法的產品使用。此類專利並不妨礙競爭對手製造和銷售與我們產品相同的產品,用於超出專利方法範圍的適應症。此外,即使競爭對手不積極宣傳他們的產品以滿足我們的目標適應症,醫生也可能會開出“標籤外”的處方。雖然標籤外處方可能侵犯或助長侵犯使用方法專利的行為,但這種做法很常見,很難防止或起訴此類侵權行為。
專利在生物技術和製藥領域的實力涉及複雜的法律和科學問題,可能是不確定的。我們擁有或正在授權的專利申請可能無法導致已發佈的專利,其權利要求涵蓋我們的候選產品或其在美國或其他外國的用途。即使專利確實成功發佈,第三方也可以質疑專利的可專利性、有效性、可轉讓性或範圍,例如通過專利權授予後審查或USPTO的單方面複審。
75
或在外國司法管轄區的異議和其他類似程序,這可能導致該等專利被取消、縮小、無效或無法執行。此外,即使我們的專利和專利申請沒有受到質疑,我們的專利和專利申請可能無法充分保護我們的知識產權,或阻止他人設計他們的產品以避免被我們的索賠所覆蓋。如果我們所持有的專利和專利申請所提供的保護範圍或強度受到威脅,可能會阻止公司與我們合作開發候選產品,並威脅到我們將候選產品商業化的能力。此外,如果我們在臨牀試驗中遇到延誤,我們可以在專利保護下銷售候選產品的時間將縮短。美國專利申請包含或在任何時候包含的權利要求在2013年3月16日之前無權享有優先權的權利要求,受美國發明法(2011)實施的“先申請”制度的約束。
這種先申請制度將要求我們認識到從發明到專利申請提交的時間。由於美國和大多數其他國家的專利申請在提交後的一段時間內是保密的,我們不能確定它是否是第一個提交與我們的候選產品相關的專利申請。此外,對於所有權利要求均享有2013年3月16日之前的優先權的美國申請,第三方或USPTO可以發起干涉程序,以確定誰是第一個發明我們申請的專利權利要求所涵蓋的任何主題。對於包含在2013年3月16日之前無權享有優先權的權利要求的美國申請,鑑於《美國發明法》的通過,專利法的不確定性更大,該法案對美國專利法產生了重大變化,包括對專利申請和已頒發專利提出質疑的新程序。
我們可能無法成功地通過收購和許可證內許可來獲得或維護我們開發流程中的產品組件和流程的必要權利。
我們可能需要訪問其他知識產權,以開發我們當前或未來的候選產品。因此,我們業務的增長可能部分取決於我們收購、授權或使用該等所有權的能力。
我們的候選產品也可能需要特定的配方以有效和高效地工作,這些權利可能由其他人持有。我們可能無法從我們識別的第三方獲取或授權任何組成、使用方法、流程或其他第三方知識產權。我們可能無法以合理的成本或合理的條款獲得這些許可證,這將損害我們的業務。即使我們能夠獲得許可證,它也可能是非排他性的,從而使我們的競爭對手能夠獲得與我們相同的技術。在這種情況下,我們可能需要花費大量的時間和資源來開發或授權替代技術。我們可能需要停止使用此類第三方知識產權所涵蓋的組合物或方法。
第三方知識產權的許可和收購是一個競爭領域,可能比我們更成熟或擁有更多資源的公司也可能採取我們認為必要或有吸引力的第三方知識產權許可或收購戰略,以便將我們的候選產品商業化。更成熟的公司可能比我們更具競爭優勢,因為它們的規模、現金資源以及更強的臨牀開發和商業化能力。
我們可能會捲入保護或強制執行我們的專利或我們許可人的專利的訴訟,這可能是昂貴、耗時和不成功的。
競爭對手可能侵犯我們的專利或我們許可方的專利。為了對抗侵權或未經授權的使用,我們可能需要提交侵權索賠,這可能是昂貴和耗時的。此外,在侵權訴訟中,法院可能會裁定我們的一項或多項專利無效或不可強制執行,或以我們的專利不涵蓋所涉技術為由拒絕阻止另一方使用所涉技術。任何訴訟或辯護程序中的不利結果都可能使我們的一項或多項專利面臨無效、無法執行或狹義解釋的風險,並可能使我們的專利申請面臨無法發佈的風險。為這些索賠辯護,無論其價值如何,將涉及大量訴訟費用,並將大量轉移員工資源從我們的業務。如果對我們的侵權索賠成功,我們可能需要支付大量的損害賠償,包括三倍的損害賠償和故意侵權的律師費,從第三方獲得一個或多個許可,支付版税或重新設計我們的侵權產品,這可能是不可能的或需要大量的時間和金錢支出。
第三方或USPTO提起的干涉訴訟可能是必要的,以確定與我們的專利或專利申請或我們的許可人的專利或專利申請有關的發明的優先權。不利的結果可能導致我們失去現有的專利權,並可能要求我們停止使用相關技術或試圖從獲勝方獲得該技術的許可。如果獲勝的一方這樣做,我們的生意可能會受到損害
76
不給我們提供商業上合理的許可證。訴訟或幹預程序可能導致對我們利益不利的決定,即使我們成功,也可能導致鉅額成本並分散我們的管理層和其他員工的注意力。我們可能無法單獨或與我們的許可人一起防止我們的商業祕密或機密信息被盜用,特別是在法律可能不像美國那樣充分保護這些權利的國家。
此外,由於知識產權訴訟需要大量的披露,在這類訴訟期間,我們的一些機密信息可能會因披露而被泄露。此外,可能會公佈聽證會、動議或其他臨時程序或事態發展的結果。如果證券分析師或投資者認為這些結果是負面的,可能會對我們普通股的價格產生重大不利影響。
獲得和維護我們的專利保護有賴於遵守政府專利機構提出的各種程序、文件提交、費用支付和其他要求,如果不符合這些要求,我們的專利保護可能會減少或取消。
任何已發佈專利的定期維護費應在專利有效期內分幾個階段向美國專利商標局和外國專利代理機構支付。美國專利商標局和各種外國政府專利機構要求在專利申請過程中遵守一些程序、文件、費用支付和其他類似規定。雖然在許多情況下,意外失效可以根據適用規則通過支付逾期費或其他方式來補救,但在某些情況下,不遵守規定可能導致專利或專利申請的放棄或失效,導致專利權在相關司法管轄區的部分或全部喪失。可能導致專利或專利申請放棄或失效的違規事件包括但不限於未能在規定的時限內對官方行為作出迴應、未支付費用以及未能適當合法化和提交正式文件。在此情況下,我們的競爭對手可能會進入市場,這將對我們的業務造成重大不利影響。
我們專利的有效期可能不足以有效保護我們的產品和業務。
專利的壽命有限。在美國,專利的自然到期通常是在其首次有效申請日之後的20年。雖然可以提供各種擴展,但專利的壽命及其提供的保護是有限的。即使獲得了涵蓋我們候選產品的專利,一旦產品的專利壽命到期,我們可能會面臨來自生物仿製藥或仿製藥的競爭。此外,雖然在美國發布時,患者的生命可以基於USPTO引起的某些延遲而增加,但這種增加可以基於專利申請人在專利申請期間引起的某些延遲而減少或消除。如果我們沒有足夠的專利有效期來保護我們的產品,我們的業務和經營業績將受到不利影響。
我們可能會受到質疑我們專利和其他知識產權發明權的索賠。
我們將來可能會受到聲稱前僱員、合作者或其他第三方作為發明人或共同發明人對我們的專利或其他知識產權有利益的指控。例如,我們可能會有因顧問或參與開發我們候選產品的其他人的義務衝突而引起的發明爭議。訴訟可能是必要的,以防禦這些和其他挑戰發明人的索賠。如果我們未能為任何此類索賠進行辯護,除了支付金錢損失外,我們還可能失去寶貴的知識產權,例如寶貴知識產權的專屬所有權或使用權。有關結果可能對我們的業務造成重大不利影響。即使我們成功地為此類索賠辯護,訴訟也可能導致鉅額成本,並分散管理層和其他員工的注意力。
如果在法庭或USPTO上受到質疑,涵蓋我們候選產品的已發佈專利可能被認定為不可申請專利、無效或無法執行。
如果我們或我們的一個許可合作伙伴對第三方提起法律訴訟,以強制執行覆蓋我們某個候選產品的專利,被告可以反訴覆蓋我們候選產品的專利(如適用)無效和/或不可執行。在美國的專利訴訟中,被告反訴聲稱無效和/或不可撤銷是常見的,並且有許多理由可以讓第三方斷言專利無效或不可撤銷。第三方也可以向美國或國外的行政機構提出類似的要求,甚至在訴訟範圍之外。這類機制包括美國的知識產權審查、單方面複審和授予後複審,以及外國法域的同等程序(例如,反對訴訟)。此類訴訟可能導致我們的專利被撤銷或修改,
77
他們不再覆蓋和保護我們的候選產品。在法律上聲稱不可專利性、無效性和不可撤銷性之後,其結果是不可預測的。例如,關於有效性問題,我們不能確定是否存在無效的現有技術,而我們、我們的專利律師和專利審查員在起訴時都不知道。如果被告以不可專利性、無效性和/或不可撤銷性的法律主張獲勝,我們將失去至少部分甚至全部對我們候選產品的專利保護。該等喪失專利保護可能對我們的業務造成重大不利影響。
第三方知識產權相關風險
我們依賴從第三方授權的知識產權,終止這些授權中的任何一項都可能導致重大權利的損失,這將損害我們的業務。
我們依賴於專利、專門知識和專有技術,包括我們自己的和從他人獲得的許可。我們在很大程度上依賴於我們與Regeneron的許可協議。這些許可證可在某些條件下終止。終止這些許可證可能導致我們失去重要權利,並可能損害我們將候選產品商業化的能力。如果這些許可方未能履行其在許可協議下的義務(我們不受控制),我們可能會失去與這些許可方簽訂的許可協議的利益。未來,我們還可能簽訂額外的許可協議,這些協議對我們的候選產品的開發至關重要。
我們與我們的許可方之間也可能發生關於受許可協議約束的知識產權的爭議,包括與以下方面有關的爭議:
如果我們已授權或將來授權的知識產權發生爭議,妨礙或損害我們以可接受的條款維持現有授權安排的能力,我們可能無法成功開發受影響的候選產品並將其商業化。
我們通常還面臨與我們許可的知識產權保護有關的所有風險,正如我們對我們擁有的知識產權的保護一樣,如下所述。如果我們或我們的許可方不能充分保護這一知識產權,我們的產品商業化能力可能會受到影響。
與員工和第三方達成的保密協議可能無法阻止未經授權泄露商業祕密和其他專有信息。
除了專利提供的保護外,我們尋求依賴商業祕密保護和保密協議來保護不可申請專利的專有技術、專利難以執行的工藝以及我們產品發現和開發工藝中涉及專利不包括的專有技術、信息或技術的任何其他元素。然而,商業祕密可能很難保護。雖然我們要求所有員工將他們的發明轉讓給我們,並要求所有員工和關鍵顧問誰可以訪問我們的專有技術,信息或技術簽署保密協議,我們不能確定我們的商業祕密和其他機密專有信息不會被泄露,或者競爭對手不會以其他方式獲得我們的商業祕密或獨立開發。基本上等同的信息和技術。此外,某些外國的法律並不像美國的法律那樣保護所有權,因此,我們在美國和海外保護和捍衞我們的知識產權方面可能會遇到重大問題。如果我們不能阻止
78
如果未經授權向第三方披露我們的知識產權,我們將無法在市場上建立或維持競爭優勢,這可能會對我們的業務、經營業績和財務狀況造成重大不利影響。
第三方對知識產權侵權的索賠可能會阻礙或推遲我們的產品發現和開發工作。
我們的商業成功部分取決於我們避免侵犯第三方的專利和所有權。在生物技術和製藥行業,有大量涉及專利和其他知識產權的訴訟。在我們開發候選產品的領域中,存在着許多由第三方擁有的美國和外國頒發的專利和待審專利申請。隨着生物技術和製藥行業的擴張以及更多專利的發佈,我們的候選產品可能引起侵犯他人專利權的索賠的風險增加。
我們知道第三方持有的與γ δ T細胞擴增方案和相關組合物有關的美國和外國專利,根據信息和信念,這些專利無效和/或未被侵犯。如果這些專利被成功地針對我們的候選產品(如ADI—001、ADI—270和ADI—002)或使用我們的前體電池生產這些候選產品,此類訴訟可能會對我們在這些司法管轄區商業化這些候選產品的能力產生負面影響。我們也知道第三方持有的與某些CAR物質成分、製造方法和使用方法有關的美國和外國專利,根據信息和信念,這些專利無效和/或未被侵犯。然而,第三方可能聲稱我們侵犯了他們的專利或未經授權使用他們的專有技術,並可能起訴我們。一般來説,在美國進行臨牀試驗和其他開發活動不被視為侵權行為。如果ADI—001、ADI—270、ADI—002或其他基於CAR的候選產品獲得FDA批准,第三方可能會通過對我們提起專利侵權訴訟來尋求執行其專利。在美國依法頒發的專利享有有效性推定,只有通過"明確和令人信服"的證據才能推翻這一推定,這是一種更高的證明標準。我們可能無法在訴訟中證明任何針對我們強制執行的專利無效和/或未被侵犯。
此外,可能存在我們目前不知道的第三方專利,涉及與使用或生產我們候選產品相關的材料、配方、製造方法或治療方法。由於專利申請可能需要很多年的時間才能發佈,因此目前可能有一些未決的專利申請,這些專利可能會導致我們的候選產品可能會侵犯我們的專利。此外,第三方可能在未來獲得專利,並聲稱使用我們的技術侵犯了這些專利。如果任何第三方專利由具有管轄權的法院持有,涵蓋我們候選產品的製造過程、製造過程中使用或形成的結構或分子,或任何最終產品本身,任何此類專利的持有人可能會阻止我們將候選產品商業化的能力,除非我們獲得適用專利項下的許可。或直到這些專利到期或最終被認定為未被侵犯、不可專利、無效或不可強制執行。同樣,如果任何第三方專利被具有管轄權的法院持有,涵蓋我們的製劑、生產工藝或使用方法的各個方面,包括聯合治療或患者選擇方法,任何此類專利的持有人都可能阻止我們開發和商業化候選產品的能力,除非我們獲得了許可證,或直到該專利到期或最終被確定為不持有,侵權、不可專利、無效或不可強制執行。在任何一種情況下,此類許可證可能無法以商業上合理的條款提供或根本無法提供。如果我們無法以商業上合理的條款或根本無法獲得第三方專利的必要許可,我們將候選產品商業化的能力可能會受到損害或延遲,這反過來又可能嚴重損害我們的業務。
對我們提出索賠的當事人可能會尋求並獲得禁令或其他公平救濟,這可能會有效地阻礙我們進一步開發和商業化候選產品的能力。為這些索賠辯護,無論其價值如何,將涉及鉅額訴訟費用,並將大量挪用員工資源,並可能影響我們的聲譽。如果對我們的侵權索賠成功,我們可能需要支付大量的損害賠償,包括三倍的損害賠償和故意侵權的律師費,從第三方獲得一個或多個許可,支付版税,或重新設計我們的侵權產品,這可能是不可能的或需要大量的時間和金錢支出。我們無法預測任何此類許可證是否會在所有或是否會在商業上合理的條款下提供。此外,即使沒有訴訟,我們也可能需要從第三方獲得許可,以推進我們的研究或允許我們的候選產品的商業化。我們可能無法以合理的成本或合理的條款獲得任何這些許可證(如果有的話)。在這種情況下,我們將無法進一步開發和商業化我們的候選產品,這可能會嚴重損害我們的業務。
79
與知識產權法有關的風險
美國專利法的修改可能會降低專利的總體價值,從而削弱我們保護產品的能力。
與其他生物製藥公司一樣,我們的成功在很大程度上依賴於知識產權,特別是專利。在生物製藥行業中獲得和執行專利涉及技術和法律的複雜性,因此成本高昂、耗時且固有的不確定性。最近的美國聯邦巡迴上訴法院和最高法院的裁決縮小了在某些情況下可用的專利保護範圍,並削弱了專利所有人在某些情況下的權利。除了我們未來獲得專利的能力增加不確定性外,這些事件的組合也對專利一旦獲得的價值造成了不確定性。根據美國國會、聯邦法院和USPTO的決定,管理專利的法律和法規可能會以不可預測的方式發生變化,這將削弱我們獲得新專利或執行現有專利和我們將來可能獲得的專利的能力。
我們可能無法在世界各地保護我們的知識產權。
我們可能無法在美國以外保護我們的知識產權在全球所有國家申請、起訴和捍衞候選產品的專利將非常昂貴,而且我們在美國以外的一些國家的知識產權可能比在美國更廣泛。有些外國的法律對知識產權的保護程度不如美國聯邦和州法律。因此,我們可能無法阻止第三方在美國以外的所有國家實踐我們的發明,或在美國或其他司法管轄區以外銷售或進口使用我們的發明製造的產品。競爭對手可能會在我們尚未獲得專利保護的司法管轄區使用我們的技術來開發自己的產品,並且可能會將其他侵權產品出口到我們有專利保護的地區,但執法力度不如美國強。這些產品可能與我們的產品競爭,我們的專利或其他知識產權可能不有效或不足以阻止它們競爭。
許多公司在外國司法管轄區保護和捍衞知識產權方面遇到了重大問題。某些國家,特別是某些發展中國家的法律制度不贊成專利、商業祕密和其他知識產權保護的實施,特別是與生物製藥產品有關的保護,這可能使我們難以阻止侵犯我們的專利或銷售競爭產品,侵犯我們的所有權。在外國司法管轄區執行我們的專利權的訴訟可能會導致大量成本,並轉移我們的精力和注意力,使我們的專利面臨被無效或狹義解釋的風險,我們的專利申請面臨無法發出的風險,並可能引發第三方對我們提出索賠。我們可能不會在我們發起的任何訴訟中獲勝,並且所判的損害賠償或其他補救措施(如有)可能沒有商業意義。因此,我們在世界各地執行知識產權的努力可能不足以從其開發或許可的知識產權中獲得重大商業優勢。
我們可能會受到員工、顧問或獨立承包商不當使用或泄露第三方機密信息的索賠。
我們已從第三方收到機密和專有信息。此外,我們還僱用以前受僱於其他生物技術或製藥公司的個人。我們可能會被指我們或我們的員工、顧問或獨立承包商無意中或以其他方式使用或泄露了這些第三方或我們員工的前僱主的機密信息。可能有必要提起訴訟來抗辯這些指控。即使我們成功地對這些索賠進行了辯護,訴訟也可能導致鉅額成本,並分散我們管理層和員工的注意力。
與我們普通股所有權相關的風險
與所有權有關的風險
我們普通股的交易價格波動很大,這可能會給我們普通股的購買者帶來巨大損失。涉及我們公司或我們管理團隊成員的證券集體訴訟或其他訴訟也可能對我們的業務、財務狀況和運營結果造成實質性損害。
80
我們的股票價格波動很大。一般的股票市場,特別是較小的製藥和生物技術公司的市場,經歷了極端的波動,而這種波動往往與特定公司的經營業績無關。此外,如果製藥和生物技術股票市場或更廣泛的股票市場繼續經歷投資者信心喪失,我們的普通股交易價格可能會因與我們的業務、財務狀況或經營業績無關的原因而下跌。由於這種波動性,您可能無法以或高於購買價出售您的普通股,您可能會損失部分或全部投資。我們普通股的市場價格可能受到許多因素的影響,包括:
過去,證券集體訴訟往往是在公司證券市價下跌後對公司提起的。這種風險對生物製藥公司尤其重要,近年來,這些公司股價出現了大幅波動。我們一直及將來可能會受到董事會真誠釐定的與企業管治事宜有關的證券訴訟,包括根據二零一五年計劃及二零一八年計劃的條款於二零二三年八月重新定價股票期權。即使對我們的指控毫無根據或我們最終不負責任,我們也可能經歷相關的負面宣傳,從而損害我們的聲譽。此外,為自己辯護的費用可能很高,訴訟可能會使我們承擔
81
我們可能會因重大和解、罰款、處罰或判決而消耗管理層的帶寬和注意力,其中部分或全部可能會對我們的財務狀況和經營業績產生負面影響。
我們普通股的活躍交易市場可能無法維持。如果交易市場不保持活躍,我們未來籌集資金的能力可能會受到削弱。
我們的普通股於2018年1月26日開始在納斯達克全球精選市場交易,現在在納斯達克全球市場交易代碼為“ACET”。鑑於我們普通股的交易歷史有限,我們股票的活躍交易市場可能無法持續,這可能會對我們普通股的市場價格造成下行壓力,從而影響您出售您購買的股票的能力。我們普通股的不活躍交易市場也可能損害我們通過出售股份籌集資金以繼續為我們的運營提供資金的能力,並損害我們通過以我們的股份為代價收購其他公司或技術的能力。
我們的主要股東和管理層擁有我們相當大比例的股票,並將能夠對有待股東批准的事項施加重大控制。
截至2023年12月31日,我們的執行人員、董事及5%股東合共實益擁有約56. 9%的已發行有投票權普通股。因此,這些股東將有能力通過該所有權地位影響我們,並顯著影響所有需要股東批准的事項的結果。例如,這些股東可能能夠顯著影響董事選舉的結果,修改我們的組織文件,或批准任何合併,出售資產或其他重大公司交易。這可能會阻止或阻止未經請求的收購建議或要約我們的普通股,您可能認為符合您作為我們的股東之一的最佳利益。
與市場不穩定有關的風險
不穩定的市場和經濟狀況可能會對我們的業務、財務狀況和股票價格產生嚴重的不利影響。
過去幾年,全球信貸和金融市場經歷了極端動盪和混亂,包括流動性和信貸供應嚴重減少、利率波動、通貨膨脹率上升和波動、企業盈利能力下降、消費者信心下降、經濟增長下降、失業率上升和經濟穩定不確定。美國債務上限和預算赤字擔憂增加了美國信用評級進一步下調和經濟放緩或經濟衰退的可能性。儘管美國國會議員多次通過提高聯邦債務上限的立法,但評級機構已下調或威脅下調美國長期主權信用評級。此次或任何進一步下調美國政府主權信用評級或其可信度的影響可能對美國和全球金融市場和經濟狀況造成不利影響。此外,美國的通貨膨脹率最近上升到幾十年來從未見過的水平。
我們認為,全球經濟狀況特別不穩定和不確定,可能對我們按預期規模和時間表進行臨牀試驗的能力產生負面影響。無法保證信貸和金融市場以及對經濟狀況的信心不會進一步惡化。我們的整體業務策略可能會受到任何該等經濟衰退、動盪的商業或政治環境或持續不可預測及不穩定的市況的不利影響。如果目前的股票和信貸市場惡化,可能會使獲得任何必要的債務或股票融資變得更加困難、成本更高和稀釋性更大。例如,由於國外政治、社會和經濟不穩定,包括武裝衝突、戰爭或戰爭威脅,特別是俄羅斯和烏克蘭之間當前的衝突,包括由此產生的制裁、恐怖主義活動和其他一般安全問題,全球金融市場可能受到嚴重破壞,削弱我們在需要時以可接受的條件籌集資金的能力。如果有的話。未能及時以優惠條款獲得任何必要的融資,可能會對我們的增長戰略、財務表現和股價產生重大不利影響,並可能要求我們推遲或放棄臨牀開發計劃。此外,我們目前的一個或多個服務供應商、製造商和其他合作伙伴可能無法在經濟衰退中生存下來,這可能直接影響我們按計劃和預算實現運營目標的能力。倘我們的盈利能力及策略因整體經濟狀況的低迷或波動而受到負面影響,則我們的業務及經營業績可能會受到重大不利影響。
我們的業務受到宏觀經濟狀況的影響,包括不斷上升的通脹、利率和供應鏈限制。
82
多種宏觀經濟因素可能對我們的業務、經營業績及財務狀況造成不利影響,包括通脹、利率及整體經濟狀況的變動,以及全球金融市場當前及未來狀況所帶來的不確定因素。例如,利率上升影響了我們的淨收入。近期的供應鏈限制導致通脹上升,如果持續下去,可能對我們的產品開發和運營造成負面影響。如果通貨膨脹或其他因素顯著增加我們的業務成本,我們開發現有產品線和新治療產品的能力可能會受到負面影響。當前的資本市場狀況,包括通脹的影響,已增加借貸利率,預期將顯著增加我們的資本成本,並可能影響我們以優惠條款籌集資本的能力,或根本,以資助我們的運營。同樣,這些宏觀經濟因素可能會影響我們的第三方供應商和製造商為我們的候選產品生產臨牀試驗材料的能力。
與我們的憲章和附例有關的風險
我們的章程文件和特拉華州法律中的反收購條款可能會推遲或阻止控制權的變更,這可能會限制我們普通股的市場價格,並可能阻止或挫敗我們的股東更換或罷免我們目前管理層的嘗試。
我們的第三次修訂和重述的公司註冊證書以及修訂和重述的章程包含可能延遲或阻止我們公司控制權的變更或我們的董事會變更的條款,而我們的股東可能認為是有利的。其中一些規定包括:
此外,由於我們在特拉華州註冊成立,我們受特拉華州一般公司法第203條的規定管轄,該條可能禁止持有我們15%或以上已發行表決權股份的股東進行某些業務合併。這些反收購條款以及我們經修訂和重述的公司註冊證書以及經修訂和重述的章程中的其他條款可能會使股東或潛在收購人更難獲得我們董事會的控制權或發起被當時董事會反對的行動,也可能會延遲或阻礙涉及我們公司的合併、要約收購或代理權爭奪。這些條款也可能阻礙代理權競爭,使您和其他股東更難選舉您選擇的董事或導致我們採取您希望的其他公司行動。控制權變更交易或董事會變動的任何延遲或阻止都可能導致我們普通股的市場價格下跌。
我們的修訂和重申的章程規定,除非我們書面同意選擇替代法院,否則特拉華州法院將是我們與股東之間大多數法律訴訟的唯一和專屬法院,這可能會限制我們的股東獲得有利的司法法院與我們或我們的董事,高級職員,僱員或代理人的糾紛。
83
本公司經修訂及重述的章程規定,除非本公司書面同意選擇替代法院,否則特拉華州高等法院將是唯一且專屬的法院,以處理以下事項:(i)代表本公司提起的任何衍生訴訟或訴訟;(ii)聲稱本公司任何董事、高級職員或其他僱員違反本公司或本公司股東所負的誠信責任的任何訴訟;(iii)根據特拉華州普通公司法或重述的公司註冊證書或經修訂和重述的章程的任何條文而提出的主張的任何訴訟,或(iv)根據內部事務原則對我們提出主張的任何訴訟(特拉華州論壇條款);但是,特拉華論壇條款不適用於根據證券法或交易法產生的任何訴訟原因。本公司修訂和重申的細則中包含的法院選擇條款將不適用於根據證券法或交易法產生的任何訴訟原因。任何購買或以其他方式收購本公司股本股份的任何權益的個人或實體應被視為已通知並已同意本公司上述經修訂和重述的章程的規定;但股東不能也不會被視為放棄本公司遵守美國聯邦證券法及其相關規則和法規。
我們認為,這一規定使我們受益,因為它使在解決公司糾紛方面特別有經驗的總理在適用特拉華州法律方面更加一致,與其他法院相比,以更快的時間表有效地管理案件,並保護我們免受多法院訴訟的負擔。然而,該條款可能會阻止針對我們的董事、高級管理人員、員工和代理人提起訴訟,因為它可能會限制任何股東在司法法庭上提出該股東認為有利於與我們或我們的董事、高級管理人員、員工或代理髮生糾紛的索賠的能力。其他公司的章程或公司註冊證書中類似選擇法院條款的可執行性已在法律程序中受到挑戰,在針對我們提起的任何適用訴訟中,法院可能會發現我們修訂和重述的章程中包含的選擇法院條款在此類訴訟中不適用或不可執行。如果法院發現我們修訂和重述的章程中包含的法院條款的選擇在訴訟中不適用或不可執行,我們可能會在其他司法管轄區產生與解決此類訴訟相關的額外費用,這可能會對我們的業務、財務狀況或運營結果產生不利影響。
一般風險因素
我們是SRC,適用於SRC的信息披露要求降低可能會降低我們的普通股對投資者的吸引力。
根據《交易法》第12b-2條,我們被視為SRC。因此,我們有權依賴某些減少的披露要求,例如豁免提供選定的財務數據和高管薪酬信息。由於我們是一家規模較小的報告公司,這些豁免和在我們提交給美國證券交易委員會的文件中披露的減少也意味着我們的審計師不需要審查我們對財務報告的內部控制,可能會使投資者更難分析我們的運營結果和財務前景。我們無法預測投資者是否會因為我們可能依賴這些豁免而發現我們的普通股吸引力下降。如果一些投資者因此發現我們的普通股吸引力下降,我們的普通股可能會有一個不那麼活躍的交易市場,我們的普通股價格可能會更加波動。只要(I)非關聯公司持有的普通股市值低於2.5億美元,或(Ii)在最近結束的會計年度,我們的年收入低於1.00億美元,並且截至前一年6月30日,非關聯公司持有的我們普通股的市值低於7.00億美元,我們仍將是一家規模較小的報告公司。
我們對現金和現金等價物的使用擁有廣泛的自由裁量權,可能無法有效地使用它們。
我們的管理層擁有廣泛的自由裁量權,可以使用我們的現金和現金等價物為我們的運營提供資金,並可以將這些資金用於不改善我們的運營結果或提高我們普通股價值的方式。如果我們的管理層未能有效地使用這些資金,可能會導致財務損失,這可能會對我們的業務產生實質性的不利影響,導致我們的普通股價格下跌,並推遲我們候選產品的開發。在我們用來為運營提供資金之前,我們可能會以不產生收入或失去價值的方式投資我們的現金和現金等價物。
我們預計在可預見的未來不會為我們的股本支付任何現金股息。因此,股東必須依賴資本增值(如果有的話)才能獲得投資回報。
我們從未宣佈或支付過我們股本的現金股息。我們目前計劃保留我們未來的所有收益,如果有的話,為我們業務的運營、發展和增長提供資金。此外,未來任何債務或信貸協議的條款可能會阻止我們支付股息。因此,我們普通股的資本增值(如果有的話)將是您在可預見的未來唯一的收益來源。
84
如果證券或行業分析師不發表關於我們業務的研究報告,或發表不準確或不利的研究報告,我們的股價和交易量可能會下降。
我們普通股的交易市場將受到行業或證券分析師發佈的關於我們或我們業務的研究和報告的影響。如果跟蹤我們的一位或多位分析師對我們的公司發表了負面看法,我們的股價可能會下跌。如果這些分析師中的一位或多位停止對我們的研究報道,或未能定期發佈有關我們的報告,我們可能會在金融市場失去可見性,這反過來可能導致我們的股價或交易量下降。
如果對我們提起產品責任訴訟,我們可能會承擔大量責任,並可能被要求限制我們候選產品的商業化。
由於我們候選產品的未來臨牀測試,我們面臨着固有的產品責任風險,如果我們將任何產品商業化,我們將面臨更大的風險。例如,如果我們的候選產品在臨牀測試、製造、營銷或銷售期間導致或被認為造成傷害,或被發現在其他方面不適合,我們可能會被起訴。任何此類產品責任索賠可能包括對製造缺陷、設計缺陷、未能就產品固有危險發出警告、疏忽、嚴格責任或違反保修的指控。根據州消費者保護法,索賠也可以主張。如果我們不能成功地在產品責任索賠中為自己辯護,我們可能會招致重大責任或被要求限制我們候選產品的商業化。即使是成功的防禦也需要大量的財政和管理資源。無論案情如何或最終結果如何,賠償責任可能會導致:
我們無法以可接受的成本獲得足夠的產品責任保險,以防範潛在的產品責任索賠,這可能會阻止或阻礙我們單獨或與公司合作伙伴開發的產品的商業化。我們的保險單也可能有各種例外,我們可能會受到產品責任索賠的影響,而我們沒有承保範圍。假設我們為我們的臨牀試驗購買了臨牀試驗保險,我們可能不得不支付法院裁決的或在和解協議中達成的超出我們承保範圍限制或不在我們保險覆蓋範圍內的金額,而我們可能沒有或能夠獲得足夠的資本來支付這些金額。即使我們與任何未來的公司合作伙伴達成的協議使其有權獲得損失賠償,如果出現任何索賠,這種賠償可能是不可用的或足夠的。
我們的現有股東在公開市場上出售大量普通股可能會導致我們的股票價格下跌。
在公開市場上出售我們的大量普通股隨時都有可能發生。這些出售,或市場上認為大量股票持有者打算出售股票的看法,可能會降低
85
我們普通股的市場價格。根據條件,我們普通股的某些持有人有權要求我們提交關於他們股票的登記聲明,或將他們的股票包括在我們可能為自己或其他股東提交的登記聲明中。根據修訂後的1933年《證券法》(《證券法》)登記這些股票,將使這些股票在《證券法》下不受限制地自由交易,但根據《證券法》第144條的規定,由關聯公司持有的股票除外。這些股東的任何證券出售都可能對我們普通股的交易價格產生實質性的不利影響。
於2022年3月15日,吾等向美國證券交易委員會提交了S-3表格登記書(檔號333-263587),該登記書經2022年3月16日提交給美國證券交易委員會的S-3表格登記書第1號修正案修訂,並於2022年5月9日(2022年擱置登記書)宣佈生效,涉及登記普通股、優先股、債務證券、權證和/或其任何組合的單位,以便不時在一次或多次發行中銷售我們的普通股、債務證券或其他股權證券。根據2022年1月22日提交的《2022年貨架登記聲明》和2024年1月25日提交的招股説明書補充資料,我們於2024年1月25日完成了32,379,667股普通股的承銷公開發行,其中包括5,325,000股在承銷商全面行使其購買額外普通股的選擇權時出售和發行的股票,以及代替向某些投資者提供普通股的預資金權證,以購買8,445,333股普通股。普通股的公開發行價為每股2.4美元,預融資權證的公開發行價為每股預融資權證2.3999美元,即每股普通股的公開發行價減去每股預融資權證的行使價0.0001美元。在扣除承銷折扣和佣金以及發行費用之前,我們從此次發行中總共獲得了9800萬美元的毛收入。作為此次發行的結果,我們的股東經歷了嚴重的稀釋。如果我們根據2022年貨架登記聲明或其他條款出售大量普通股,或市場認為我們打算出售大量普通股,我們普通股的市場價格可能會大幅下跌。
我們還提交了S-8表格的登記聲明,登記我們的股權補償計劃下已發行或預留供未來發行的普通股的發行。以S-8表格登記的股份一經發行即可在公開市場自由出售,並一經歸屬,受適用於聯屬公司的數量限制和上述鎖定協議的限制。如果這些額外的股票中的任何一股在公開市場上出售,或者如果人們認為它們將被出售,我們普通股的市場價格可能會下降。
此外,我們的某些員工、高管和董事可能會加入規則10b5-1,規定不定期出售我們普通股的股票。根據規則10b5-1交易計劃,經紀人根據員工、董事或高級職員在進入計劃時建立的參數執行交易,而無需員工、高級職員或董事的進一步指示。在某些情況下,規則10b5-1的交易計劃可能會被修改或終止。我們的員工、高管和董事也可以在不掌握重大、非公開信息的情況下,購買或出售規則10b5-1交易計劃之外的額外股票。
86
項目1B。未解決的員工評論。
不適用。
項目1C。網絡安全。
網絡風險管理與策略
該公司依靠電子系統和信息技術開展業務。我們根據我們的風險狀況和業務,採用並維護了一項網絡安全風險管理計劃,該計劃由行業標準提供信息。
我們利用第三方信息技術和安全提供商的支持,包括執行滲透測試和威脅情報分析。我們此前進行了網絡安全風險評估,旨在考慮不斷變化的網絡威脅格局和行業最佳實踐,我們努力調整我們的網絡風險戰略,以緩解新出現的網絡安全風險。我們對網絡安全實施多層次方法,包括例如員工安全意識培訓、各種安全工具和技術以及事件響應計劃。
雖然網絡安全威脅的風險迄今尚未受到重大影響,且我們認為這些風險不可能合理地對我們、我們的業務策略、經營業績或財務狀況造成重大影響,但我們可能不時遇到與我們和我們的第三方供應商的信息系統有關的威脅和安全事故。有關更多信息,請參閲本年報表格10—K中標題為“風險因素”的章節。
與網絡安全風險相關的治理
我們的信息技術(“IT”)高級總監直接向我們的首席財務官彙報,並在我們的信息安全副總監兼IT高級經理的支持下,負責我們的網絡安全計劃的戰略領導和方向。憑藉超過20年的IT和網絡安全風險管理經驗,我們的高級IT總監與公司其他管理職能部門的個人一起工作,以建立和實施我們的網絡安全風險管理戰略。
我們的審計委員會直接向董事會報告,根據審計委員會的章程,負責監督我們的網絡安全風險管理計劃。審計委員會定期從我們的IT高級董事接收有關網絡安全風險、緩解策略的最新信息,並在必要時接收事件響應活動的最新信息。審計委員會可以根據需要向董事會全體成員通報與網絡安全風險管理有關的事項。
項目2.新聞歌劇。
我們在馬薩諸塞州的波士頓和加利福尼亞州的紅杉市設有辦事處。我們的主要執行辦公室位於馬薩諸塞州波士頓達特茅斯街131號3樓。2024年1月31日,我們在馬薩諸塞州波士頓伯克利街200號的租約因辦公空間關閉而被房東終止。2024年1月19日,我們與勤勞的Bos 131 Dartoss Street LLC簽訂了一項會員協議,購買馬薩諸塞州波士頓達特茅斯街131號的辦公空間(達特茅斯街協議)。達特茅斯街協議於2024年2月1日開始生效,2025年1月31日到期。
我們還租用了位於加利福尼亞州雷德伍德市橋公園大道1000號的辦公和實驗室空間。租約於2020年3月31日開始,2030年2月28日到期。此外,我們還在加利福尼亞州雷德伍德市的Bridge Parkway 1200號租賃了辦公空間。本租約於2022年6月17日開始,2025年6月30日到期。
我們相信,我們的辦公室和實驗室空間足以滿足我們目前的需求,並將在需要時提供適當的額外空間。
項目3.法律法律程序。
我們目前沒有受到任何實質性法律程序的影響。我們可能會不時地受到各種法律程序和索賠的影響,這些訴訟和索賠是在我們正常的業務活動過程中出現的。雖然訴訟和索賠的結果無法準確預測,但截至本報告日期,我們不相信我們是任何索賠或訴訟的一方,如果這些索賠或訴訟的結果被確定為對我們不利,則有理由預計其結果將對我們的業務產生重大不利影響。無論結果如何,由於辯護和和解成本、管理資源分流等因素,訴訟可能會對我們產生不利影響。
87
項目4.地雷安全安全披露。
不適用。
88
部分第二部分:
項目5.註冊人普通股市場,相關股票持股人重要和發行人購買股票證券。
我們的普通股在納斯達克全球市場交易,代碼為ACET。我們的普通股於2018年1月26日開始交易,與我們的resTORbio首次公開募股相關。在此之前,我們的普通股還沒有建立起公開交易市場。
截至2024年3月14日,我們大約有16名普通股持有者。我們普通股的實際持有者人數超過了這一記錄持有者的數量,包括作為實益所有者的股東,但其股票由經紀商以街頭名義持有或由其他被提名者持有。這一數量的登記持有人也不包括其股份可能由其他實體以信託形式持有的股東。
分紅
我們從未宣佈或支付過普通股的任何現金股息。我們目前打算保留所有可用的資金和任何未來的收益,以支持我們業務的發展和增長。我們預計在可預見的未來不會支付任何現金股息。任何未來派發股息的決定將由我們的董事會酌情決定,並將取決於各種因素,包括適用的法律、我們的運營結果、財務狀況、未來前景、適用的合同限制以及我們董事會認為相關的任何其他因素。投資者不應期望獲得現金股利而購買我們的普通股。
股權薪酬計劃
表格10—K第5項所要求的有關股權補償計劃的資料,已參考本年報有關表格10—K的第III部分第12項而納入本報告。
最近出售的未註冊證券
沒有。
發行人及關聯購買人購買股權證券
於本年報涵蓋的期間內,吾等並無以表格10—K購買任何股本證券。
第六項。[已保留].
89
項目7.管理層對以下問題的討論和分析財務狀況及經營業績。
閣下應閲讀以下有關本公司財務狀況及經營業績的討論及分析,連同本年報表格10—K其他地方所載的綜合財務報表及相關附註。本年度報告表格10—K的討論和其他部分包含涉及風險和不確定性的前瞻性陳述,例如我們的計劃,目標,期望,意圖和信念。我們的實際結果可能與這些前瞻性陳述中討論的結果有重大差異。可能導致或促成此類差異的因素包括但不限於下文所述及本年報表格10—K其他地方標題為“風險因素”一節中討論的因素。
概述
我們是一家臨牀階段的生物技術公司,發現和開發用於自身免疫性疾病和癌症的同種異體γ δ T細胞療法。我們正在推進一個“現成的”γ δ T細胞的管道,用嵌合抗原受體(CAR)工程,以促進患者的持久活性。
我們的方法激活,工程和生產來自無關供體外周血細胞的同種異體γ δ T細胞候選產品,使我們能夠以快速和具有成本效益的方式生成新的產品候選。我們的同種異體“現成”生產工藝旨在允許不相關供體的產品按需儲存和銷售,以治療患者而不會誘導移植物抗宿主免疫應答。這與基於α β T細胞的產品相反,α β T細胞必須為每個患者從他或她自己的T細胞中生產,或者如果T細胞來自與患者無關的供體,則需要進行重大的基因編輯來生產。
我們的主要候選產品ADI—001是一種表達靶向CD 20的CAR的同類第一種同種異體γ δ T細胞療法,正在開發用於潛在治療自身免疫性疾病和複發性或難治性侵襲性B細胞非霍奇金淋巴瘤(NHL)。我們的產品線還包括我們的主要臨牀前候選藥物ADI—270,這是一種靶向腎細胞癌的裝甲γ δ CAR T細胞候選藥物,具有其他CD70+實體瘤和血液惡性腫瘤適應症的潛力。我們的管道有幾個額外的內部γ δ T細胞治療計劃,用於血液惡性腫瘤和實體瘤的發現和臨牀前開發。我們預計將繼續基於我們的γ δ T細胞平臺開發自身免疫性疾病和癌症的候選產品,使用先前驗證的抗原或我們使用CAR和其他技術識別和靶向的抗原。我們計劃每12—18個月提交一份新的新藥(IND)申請,包括2024年上半年的ADI—270 IND。
ADI—001
自身免疫性疾病
2023年12月,美國食品藥品監督管理局(FDA)批准了我們ADI—001治療狼瘡腎炎的IND申請,狼瘡腎炎是一種由系統性紅斑狼瘡(SLE)引起的自身免疫性疾病。狼瘡性腎炎是SLE的一種嚴重併發症,在估計的325例中,我們預計在2024年第二季度啟動ADI—001治療狼瘡性腎炎的I期臨牀試驗,並在2024年第二季度和第三季度將候選藥物的開發擴展到一至兩種額外的自身免疫適應症。在這些適應症中,需獲得IND的批准。我們認為ADI—001在B細胞介導的自身免疫性疾病中的潛在市場機會是巨大的,歐盟5、中國和日本超過170萬名自身免疫性疾病患者,其中CAR—T細胞療法已證明臨牀概念驗證,包括SLE(包括狼瘡性腎炎)、系統性硬化症和特發性炎性肌病。
我們預計在2024年第四季度或2025年第一季度提供ADI—001治療狼瘡性腎炎的I期臨牀試驗的初步臨牀數據,取決於研究中心激活和入組情況,並從2024年第四季度或2025年上半年開始提供其他自身免疫適應症的初步臨牀數據。取決於這些適應症中IND的批准,以及成功啟動研究中心並在相關臨牀方案中入組患者。
複發性或難治性侵襲性B細胞NHL
2021年3月,我們啟動了人類首個1期(GLEEP)試驗,以評估ADI-001在復發或難治性侵襲性B細胞NHL患者中的安全性和有效性。這項研究包括劑量遞增部分和隨後的劑量擴展隊列,以探索ADI-001在多個亞型NHL中的活性。2022年4月,FDA授予非霍奇金淋巴瘤ADI-001快速通道稱號。截至2023年5月4日截止日期,在GLEAN試驗的24名可評估受試者中,有18人
90
大B細胞淋巴瘤(LBCL),套細胞淋巴瘤(MCL)5例,濾泡性淋巴瘤1例。大多數患者都接受了嚴格的預治療,中位數為4行之前的治療,12名患者(50%)以前在接受CAR T細胞治療後進展。儘管患者在基線水平處於進展期,我們觀察到MCL患者有較高的完全緩解率(CR)和良好的耐受性。在所有劑量的MCL患者中,我們觀察到6個月時總有效率(ORR)為80%(4/5例),CR率為80%(4/5例),CR率為60%(3/5例)。截至2023年5月4日,ADI-001的安全性總體良好,沒有觀察到細胞因子釋放綜合徵(CRS)、免疫效應細胞相關神經毒性綜合徵(ICANS)或T細胞惡性腫瘤的顯著風險。2023年11月,我們在後CAR T LBCL發起了一個擴展隊列,Expand。2024年1月,我們宣佈決定取消LBCL患者參加GLEAN試驗的資格,以便專注於推進MCL的登記。
我們預計將提供NHL患者I期研究的臨牀更新,其中將包括療效數據,包括6個月CR率,以及2024年下半年其他MCL患者的安全性數據。根據臨牀數據和監管反饋,我們計劃在2025年上半年為ADI—001在MCL中的潛在關鍵II期研究確定監管路徑,並在2025年下半年提供進一步的臨牀更新。
我們通過將製造工藝轉移到一個能夠在更大規模生產下運營的額外合同開發和製造組織(CDMO),擴大了ADI—001的製造能力。
ADI—270
ADI—270是一種研究性同種異體γ δ CAR T細胞療法,通過CD27配體靶向CD70,用於治療腎細胞癌(RCC),並具有其他實體瘤適應症的潛力。ADI—270設計用於治療實體瘤,具有高度特異性的CD 70靶向部分和轉化生長因子(TGF)β顯性陰性受體的鎧裝技術,以解決腫瘤微環境中的免疫抑制因子。 基於γ δ 1組織對實體瘤的嗜性和三種抗腫瘤活性機制(CAR、先天性和適應性),CAR γ δ 1 T細胞可能很好地定位於解決實體瘤。我們計劃在2024年第二季度提交ADI—270治療腎癌的IND申請,並在2025年上半年提供臨牀數據,這取決於監管部門的批准和研究啟動活動。我們還在考慮在2025年上半年擴展到其他CD70+腫瘤適應症,2025年下半年此類研究的潛在臨牀數據,但需獲得監管部門批准和研究啟動活動。
最新發展動態
1000大橋大道租賃和信用證
2023年1月9日,我們與Westport Office Park,LLC(Westport)簽訂了第三次租約修正案(第三修正案)。第三修正案進一步修訂了紅杉城市租賃,並從2023年1月1日起將租户改善津貼額外增加了300萬美元。我們預計將利用全部津貼繼續在Bridge Parkway 1000號建造辦公和實驗室空間。根據本次修訂的條款,這項額外津貼將在租賃期內以按月等額支付本金攤銷和利息的方式償還,年利率為8%(8%)。我們在2023年2月21日收到了津貼。
2023年8月7日,我們與Westport簽訂了第四次租約修正案(第四修正案)。第四修正案修訂了第三修正案中收到的租户改善津貼的攤銷期限,並確定了我們每月應支付的攤銷。
2023年9月1日,我們修改了與Westport的信用證。該修正案將與我們的1000 Bridge Parkway設施相關的信用證金額減少了210萬美元,導致更新後的信用證金額為210萬美元。
期權重新定價
2023年8月8日,我們的董事會根據我們2015年股票激勵計劃和2018年計劃(統稱為計劃)的條款,批准了股票期權重新定價(期權重新定價),自2023年8月14日(生效日期)起生效。根據期權重新定價,在一年懸崖期間的規限下,先前根據該計劃授予的總計6,431,910份購股權的行權價進行了修訂,將該等期權的行權價降至每股2.14美元,即我們的普通股在納斯達克全球市場生效日期的收市價。根據期權重新定價的條款,如果在生效日期一週年之前,(A)吾等有理由或期權持有人終止僱用期權持有人,或(B)期權持有人已行使期權,重新定價的期權將回復至其原來的行使價。重新定價的期權在其他方面保留了計劃和適用的授標協議中規定的現有條款和條件。
91
此外,截至生效日期,我們根據2018年計劃向截至2023年8月8日持有激勵獎勵的合格員工發放了1,418,042份普通股購買期權。這些新期權之所以發放給符合條件的員工,是因為他們根據納斯達克上市規則第5635(C)(4)條授予的誘人獎勵不符合重新定價的資格。按照原來的條款,先前的激勵獎仍然懸而未決。
承銷的公開發行
於2024年1月22日,吾等作為承銷商(承銷商)的代表與Jefferies LLC及Guggenheim Securities,LLC訂立承銷協議(承銷協議),內容涉及公開發行32,379,667股本公司普通股,其中包括5,325,000股於承銷商悉數行使其購買額外普通股的選擇權時出售及發行的股份,以及為代替向某些投資者購買普通股而預先提供資金的認股權證,以購買8,445,333股普通股。普通股的公開發行價為每股2.4美元,預融資權證的公開發行價為每股預融資權證2.3999美元,即每股普通股的公開發行價減去每股預融資權證的行使價0.0001美元。在扣除承銷折扣、佣金和其他估計發行費用後,我們從此次發行中獲得的淨收益約為9180萬美元。我們可以從行使預付資權證中獲得名義收益(如果有的話)。
在市場(ATM)服務
2024年1月,我們根據我們的“在市場上”發行計劃,在一系列銷售中共出售了6,350,000股普通股。(ATM計劃)與JonesTrading Institutional Services LLC(銷售代理),平均價格為每股3.13美元,扣除銷售代理佣金後,所得款項淨額總額約為1930萬美元,但未扣除與該等銷售有關的任何開支。截至10—K表格的年度報告之日,我們的普通股中有高達8010萬美元仍可不時根據我們的ATM計劃出售。2024年3月,我們終止了ATM計劃。
財務運營概述
收入
我們沒有獲準商業銷售的產品,除非及直至我們成功完成研發並獲得監管部門的批准,我們預計至少在數年內(如果有的話)不會從產品銷售中產生收入。迄今為止,我們的收入來自我們與Regeneron Pharmaceuticals,Inc.的許可證和合作協議。(Regeneron)和稱為“Regeneron協議”的協議。
我們於2016年7月29日簽署Regeneron協議後收到Regeneron預付款2500萬美元的不可退還預付款,截至2023年12月31日,我們已收到Regeneron提供的總計2000萬美元的額外研究資金。我們於Regeneron協議項下的責任已於二零二二年第一季度完成。Regeneron將來可能需要向我們支付額外金額,包括若干專業間合作實踐(ICP)的總計高達8000萬美元的期權行使費。2022年1月28日,我們收到Regeneron支付的2000萬美元,用於行使其ADI—002獨家許可權的選擇權,Regeneron可能在Regeneron協議下對其他協作ICP目標擁有更多選擇權。我們拒絕行使與Regeneron共同資助ADI—002開發的選擇權,因此,Regeneron還必須向我們支付較高的單位數專利費,即ADI—002或任何其他選擇性ICP的淨銷售額百分比,並向我們支付較低的單位數專利費,即任何非ICP產品包含我們通過使用Regeneron專利小鼠生成的靶點。我們必須向Regeneron支付中位數至低兩位數的使用費,作為我們已行使獨家權利的目標的協作ICP淨銷售額的百分比,以及低至中位數的使用費,作為我們使用Regeneron專有鼠標的許可證所產生的目標部分的淨銷售額的百分比。專利權使用費應支付至許可專利權到期或無效或自首次商業銷售起12年(以較長者為準)。
我們使用成本輸入法計量比例表現,並計算根據Regeneron協議確認的相應收入金額。在應用以成本為基礎的輸入法確認收入時,我們使用實際產生的成本相對於預算成本來履行合併履約責任。收入乃根據實際成本佔總預算成本的百分比確認,因為我們於研究期內完成履約責任。以成本為基礎的收入確認輸入法要求我們估計完成履約責任的成本,這需要作出重大判斷以評估與成本估計有關的假設。修訂完成履約責任的估計成本的累計影響於已識別變動且金額可合理估計的期間內記錄。
92
費用
研究與開發
研發開支(主要包括與開發候選產品有關的成本)於產生時支銷。研發費用主要包括:
我們不會按候選產品分配成本,因為大量研發開支並不由候選產品跟蹤,我們相信,該等成本的分配將是任意的,且不會提供有意義的評估,因為我們已在多個候選產品研發計劃中使用員工和基礎設施資源。
我們將所有資源集中在候選產品的開發上。目前,我們無法合理估計或瞭解完成候選產品開發所需努力的性質、時間和估計成本。我們亦無法預測何時(如果有的話)將從我們的候選產品銷售開始重大淨現金流入。我們候選產品的臨牀試驗和開發的持續時間、成本和時間取決於多種因素,包括:
與我們的任何候選產品開發相關的任何這些或其他變量的結果發生變化,可能會顯著改變與該候選產品開發相關的成本和時間。此外,我們的經營計劃未來可能會有所改變,我們將繼續需要額外資本以滿足與該等經營計劃相關的經營需要及資本要求。
我們可能無法以可接受的條件或根本無法獲得足夠的資金。我們未能在需要時籌集資金,可能會對我們的財務狀況及我們推行業務策略的能力造成負面影響。如果我們無法在需要時籌集額外資金,我們可能會被要求推遲、減少或終止部分或全部開發項目和臨牀試驗,或者我們可能會被要求在某些地區或我們希望自己開發和商業化的適應症出售或授予我們的候選產品的其他權利。如果我們被要求進行合作和其他
93
在補充資金的安排中,我們可能不得不放棄某些限制我們開發和商業化候選產品的能力的權利,或可能有其他不利於我們或我們的股東的條款,這可能會對我們的業務和財務狀況造成重大影響。
一般和行政
一般及行政開支主要包括薪金及人事開支(包括薪金及花紅、福利及股票薪酬開支)、法律、諮詢、會計及税務服務之專業費用、已分配間接開支(包括租金、設備、折舊、資訊科技成本及公用事業),以及其他並無分類為研發開支之一般營運開支。
我們預計,在可預見的將來,我們的一般和行政開支將增加,原因是與作為上市公司運營相關的開支,包括與人事成本、擴大基礎設施以及與遵守適用納斯達克和SEC要求相關的更高諮詢、法律和會計服務成本、投資者關係成本以及董事和高級管理人員保險費有關的開支。
商譽減值
商譽指收購價超出我們與resTORBio,Inc.合併時收購的有形及已識別無形資產淨值公平值的差額。2020年9月商譽不會攤銷,惟至少每年評估減值,或當事實及情況變動顯示商譽之公平值可能低於賬面值時。倘報告單位之公平值低於賬面值,則吾等將減值虧損金額(如有)計量為賬面值超出報告單位之公平值之差額。該金額於期內確認為商譽減值支出。本公司於2023年第三季度進行商譽減值中期測試,確定商譽餘額全部減值。
利息收入
利息收入主要包括現金及現金等價物所賺取的利息。
利息支出
利息開支主要包括與貸款協議(定義見下文)有關的成本的非現金攤銷。
其他費用,淨額
其他支出淨額主要包括與收入無關的州特許經營權和資本税。
經營成果
截至二零二三年及二零二二年十二月三十一日止年度之比較
下表彙總了我們在所示期間的業務結果(除百分比外,以千計):
|
|
截至12月31日的12個月, |
|
|
|
|
|
|
|
|||||||
|
|
2023 |
|
|
2022 |
|
|
變化 |
|
|
更改百分比 |
|
||||
營收相關方 |
|
$ |
— |
|
|
$ |
24,990 |
|
|
$ |
(24,990 |
) |
|
|
(100 |
%) |
運營費用 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
研發 |
|
|
106,043 |
|
|
|
71,246 |
|
|
|
34,797 |
|
|
|
49 |
% |
一般和行政 |
|
|
26,533 |
|
|
|
26,295 |
|
|
|
238 |
|
|
|
1 |
% |
商譽減值 |
|
|
19,462 |
|
|
|
— |
|
|
|
19,462 |
|
|
|
100 |
% |
總運營費用 |
|
|
152,038 |
|
|
|
97,541 |
|
|
|
54,497 |
|
|
|
56 |
% |
運營虧損 |
|
|
(152,038 |
) |
|
|
(72,551 |
) |
|
|
(79,487 |
) |
|
|
110 |
% |
利息收入 |
|
|
9,978 |
|
|
|
3,760 |
|
|
|
6,218 |
|
|
|
165 |
% |
利息支出 |
|
|
(25 |
) |
|
|
(80 |
) |
|
|
55 |
|
|
|
69 |
% |
其他費用,淨額 |
|
|
(573 |
) |
|
|
(919 |
) |
|
|
346 |
|
|
|
38 |
% |
所得税優惠前虧損 |
|
|
(142,658 |
) |
|
|
(69,790 |
) |
|
|
(72,868 |
) |
|
|
104 |
% |
所得税撥備 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
0 |
% |
淨虧損 |
|
$ |
(142,658 |
) |
|
$ |
(69,790 |
) |
|
$ |
(72,868 |
) |
|
|
104 |
% |
94
收入
截至2023年12月31日止年度的收益較截至2022年12月31日止年度減少25. 0百萬元或100%。減少乃由於本期間並無根據Regeneron協議確認收入所致。我們與Regeneron的合併履約責任項下的責任已於2022年第一季度完成,導致截至2022年3月31日根據協議全面確認收入。
研究與開發
|
|
截至12月31日的12個月, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
薪金和人事費(1) |
|
$ |
42,744 |
|
|
$ |
31,201 |
|
根據與顧問、社區發展管理組織和區域合作組織的協議發生的費用 |
|
|
29,963 |
|
|
|
19,233 |
|
實驗室材料、用品和設備維護 |
|
|
11,065 |
|
|
|
6,929 |
|
其他研發費用(2) |
|
|
22,271 |
|
|
|
13,883 |
|
研發費用總額 |
|
$ |
106,043 |
|
|
$ |
71,246 |
|
(1) 員工相關成本,包括研發員工的薪金、福利、獎金和股票補償費用。
(2) 分配的設施相關費用,如租金、水電費、保險、維修和保養、折舊和攤銷、信息技術費用和一般支助事務。
截至2023年12月31日止年度,研發開支較截至2022年12月31日止年度增加34. 8百萬元或49%。研究和開發費用增加的主要原因是,與CDMO和其他外部進行的研究和開發有關的費用增加了1 070萬美元,以及由於總人數增加,工資和人事費增加了1 150萬美元。此外,本期間分配的設施費用增加了850萬美元,實驗室費用增加了410萬美元。這一增加額被專業人員費用減少20萬美元部分抵消。
一般和行政
截至二零二三年十二月三十一日止年度,一般及行政開支較截至二零二二年十二月三十一日止年度增加0. 2百萬元或1%。一般和行政費用增加的主要原因是薪金和人事費增加330萬美元,其中包括薪金和福利增加100萬美元、承包商費用增加90萬美元、股票報酬增加120萬美元和徵聘費增加30萬美元。這些增加是由於本期員工人數增加所致。增加額被分配設施費用減少260萬美元部分抵消。本期間的專業人員費用也減少了50萬美元。
商譽減值
截至2023年12月31日止年度,商譽減值支出較截至2022年12月31日止年度增加19,500,000元或100%。從二零二三年第三季度開始,我們的股價大幅下跌。我們的結論是,股價下跌持續,而我們單一報告單位的公平值較有可能低於其賬面值。因此,我們進行了中期商譽減值測試,
95
2023年9月30日根據我們的中期減值測試,我們於截至2023年12月31日止年度錄得商譽減值支出19,500,000美元,相當於商譽的全部餘額。
利息收入
截至2023年12月31日止年度,利息收入較截至2022年12月31日止年度增加6. 2百萬元或165%,主要由於利率上升以及我們於國債及貨幣市場基金的投資。
其他費用,淨額
截至2023年12月31日止年度,其他開支較截至2022年12月31日止年度減少30萬元或38%,主要由於期內特許經營權及資本税減少所致。
所得税優惠
截至二零二三年及二零二二年十二月三十一日止年度,概無所得税開支或利益。
流動性與資本資源
流動資金來源
我們過去主要通過合作和許可安排、公開和私募股權證券和債務以及在與resTORbio,Inc.合併中收到的現金為我們的業務提供資金。
於2022年8月,我們根據ATM計劃與銷售代理出售普通股股份所得款項淨額4360萬美元,於2024年1月,我們根據ATM計劃出售普通股股份所得款項淨額1930萬美元。根據我們的ATM計劃,高達8010萬美元的普通股仍可供出售,為我們提供了額外的流動性來源,取決於市場條件。2024年3月,我們終止了ATM計劃。
此外,於2024年1月,我們完成了發售,扣除承銷折扣和佣金以及其他估計發售開支後,我們獲得了約9180萬美元的所得款項淨額。吾等亦可能因行使預撥資金認股權證而收取象徵性所得款項(如有)。
截至2023年12月31日,我們擁有現金及現金等價物1.597億美元。我們預計,我們的現金及現金等價物,連同年底後通過我們的ATM計劃和發售籌集的所得款項,將足以為我們的預測運營開支,資本開支需求和債務還本付息支付提供資金,自本年度報告10—K表格中包含的綜合財務報表發佈後至少未來12個月。
貸款協議
於2020年4月28日,我們簽訂了貸款和擔保協議,並於2020年7月8日、2020年9月14日、2020年9月15日、2021年10月21日、2022年12月2日和2023年5月30日修訂(貸款協議),與加利福尼亞銀行(前稱太平洋西部銀行)為我們在紅木城的設施的租賃改善提供資金,加利福尼亞州和貸款協議允許的其他用途。
於2023年5月30日,我們修訂了與加利福尼亞銀行的貸款協議(2023年貸款修訂案)。根據2023年貸款修正案,我們必須維持以下兩者中的較小者:(i)3500萬美元或(ii)我們在活期存款賬户、貨幣市場賬户和/或加州銀行的保險現金掃賬賬户中的所有合併餘額。如果我們的現金和投資總額下降到3500萬美元以下,2023年貸款修正案允許我們在加州銀行以外的一個或多個賬户中保留現金和/或投資,總額不超過250萬美元。
截至2023年12月31日,我們根據貸款協議有1270萬美元可用。截至本年報表格10—K日期,吾等已遵守該等契諾,並無根據貸款協議欠下任何未償還債務。
96
未來的資金需求
我們自成立以來已產生虧損,截至2023年及2022年12月31日止年度分別產生虧損1.427億美元及6980萬美元。截至2023年12月31日,我們的累計赤字為3.808億美元。
截至2023年12月31日,我們擁有現金及現金等價物1.597億美元。2023年12月31日之後,我們通過ATM計劃籌集了約1930萬美元的總所得款項淨額,並通過此次發行籌集了約9180萬美元的總所得款項淨額。我們相信,我們的現金和現金等價物,連同年底後通過我們的ATM計劃和發行籌集的所得款項,將足以為我們的運營提供資金,自我們的綜合財務報表發佈日期起至少12個月,截至2023年12月31日止年度,包括在本年度報告表格10—K其他地方。我們的估計是基於可能被證明是錯誤的假設,我們可能會比預期更快地耗盡可用的資本資源。由於與候選產品的研究、開發和商業化相關的風險和不確定性,我們無法估計我們的營運資金需求的確切金額。
迄今為止,我們所有的收入都來自Regeneron協議,這是一項合作和許可協議。在我們獲得監管部門批准並將我們的任何候選產品商業化或與第三方簽訂額外合作協議之前,我們預計不會產生任何重大的產品收入,我們不知道何時或是否會發生。我們預計在可預見的未來將繼續產生重大虧損,隨着我們繼續開發候選產品並尋求監管部門的批准,並開始將任何已批准的產品商業化,我們預計虧損將增加。我們面臨與開發新候選產品有關的所有風險,我們可能會遇到不可預見的費用、困難、併發症、延誤及其他可能對我們業務造成不利影響的未知因素。
在可預見的將來,我們將繼續需要額外資金來開發我們的候選產品和基金運營。我們可能會尋求通過私募股權或公共股權或債務融資、與企業來源的合作或其他安排,或通過其他融資來源籌集資金。我們預計,我們將需要籌集大量額外資本,其需求將取決於多個因素,包括:
與我們的任何候選產品開發相關的任何這些或其他變量的結果發生變化,可能會顯著改變與該候選產品開發相關的成本和時間。此外,我們的經營計劃未來可能會有所改變,我們將繼續需要額外資本以滿足與該等經營計劃相關的經營需要及資本要求。我們可能無法以可接受的條件或根本無法獲得足夠的資金。
97
我們未能在需要時籌集資金,可能會對我們的財務狀況及我們推行業務策略的能力造成負面影響。如果我們無法在需要時籌集額外資金,我們可能會被要求推遲、減少或終止部分或全部開發項目和臨牀試驗,或者我們可能會被要求在某些地區或我們希望自己開發和商業化的適應症出售或授予我們的候選產品的其他權利。如果我們需要達成合作和其他安排以補充資金,我們可能不得不放棄某些限制我們開發和商業化候選產品能力的權利,或可能有其他不利於我們或我們的股東的條款,這可能會對我們的業務和財務狀況造成重大影響。
請參閲本年報表格10—K的一節,標題為“風險因素對於與我們的大量資本要求相關的額外風險。
現金流量彙總表
下表載列我們於下文呈列各期間現金、現金等價物及受限制現金的主要來源及用途(以千計):
|
|
截至12月31日的12個月, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
提供的現金淨額(用於): |
|
|
|
|
|
|
||
經營活動 |
|
$ |
(93,717 |
) |
|
$ |
(44,765 |
) |
投資活動 |
|
|
(4,464 |
) |
|
|
(16,782 |
) |
融資活動 |
|
|
236 |
|
|
|
41,509 |
|
現金和現金等價物淨減少 |
|
$ |
(97,945 |
) |
|
$ |
(20,038 |
) |
經營活動的現金流
截至2023年12月31日的一年中,用於經營活動的現金淨額為9370萬美元。業務活動中使用的現金包括由4870萬美元的非現金調整和淨增加的30萬美元的業務資產和負債抵消的淨虧損。非現金項目主要包括1,950萬美元的商譽減值、2,030萬美元的股票補償支出、610萬美元的折舊和攤銷以及280萬美元的非現金租賃支出。資產和負債淨增加的主要原因是預付費用和其他流動資產增加90萬美元,其他非流動資產賬户增加40萬美元。應計負債及其他流動和非流動負債也增加了80萬美元。應付賬款減少170萬美元,部分抵消了這一增加。
截至2022年12月31日的一年中,用於經營活動的現金淨額為4480萬美元。業務活動中使用的現金包括淨虧損和非現金調整數2230萬美元以及資產和負債增加270萬美元。非現金項目主要包括基於股票的1710萬美元的薪酬支出、240萬美元的非現金租賃支出以及260萬美元的折舊和攤銷。資產和負債淨變化的主要原因是應計負債及其他流動和非流動負債增加580萬美元,應付賬款增加170萬美元,預付費用和其他流動資產增加130萬美元。與Regeneron協議有關的遞延收入減少480萬美元和經營租賃負債減少230萬美元,部分抵消了這一增加。
投資活動產生的現金流
在截至2023年12月31日的一年中,用於投資活動的現金淨額為450萬美元,其中包括購買與我們在加利福尼亞州雷德伍德城的設施建設相關的財產和設備。
截至2022年12月31日的年度,用於投資活動的現金淨額為1680萬美元,其中包括購買與我們在加利福尼亞州雷德伍德城的設施建設相關的財產和設備。
融資活動產生的現金流
在截至2023年12月31日的一年中,融資活動提供的現金淨額為20萬美元,這主要與發行與我們的員工股票購買計劃相關的普通股的淨收益40萬美元有關。這部分被為股權獎勵的淨股票結算所預扣的税款支付的20萬美元現金所抵消。
在截至2022年12月31日的一年中,融資活動提供的現金淨額為4,150萬美元,其中主要包括根據我們的自動櫃員機計劃發行普通股的4,340萬美元收益,以及根據我們的員工股票購買計劃行使股票期權和購買的170萬美元現金收益。融資活動提供的現金淨額被與員工股權獎勵的淨股份結算相關的320萬美元預扣和支付的税款以及與遞延發行成本相關的40萬美元部分抵消。
98
關鍵會計政策、重大判斷和估計的使用
我們對我們的財務狀況和經營結果的討論和分析是基於我們的綜合財務報表,這些報表是根據公認會計準則(GAAP)編制的。在編制我們的合併財務報表時,我們需要做出影響合併財務報表中資產、負債、收入和費用的報告金額以及或有資產和負債的披露的估計和判斷。在不同的假設或條件下,實際結果可能與這些估計值不同,並可能對我們報告的結果產生實質性影響。雖然我們的重要會計政策在本年度報告10-K表格中其他地方的綜合財務報表附註中有更全面的描述,但我們認為以下會計政策對於理解我們在編制綜合財務報表時使用的判斷和估計是最關鍵的:
應計CDMO、CRO和研發費用
我們已經與CDMO和CRO達成了各種協議。我們的研究和開發應計費用是根據所提供的服務水平、研究進展(包括活動的階段或完成)和合同成本進行估計的。已提供但尚未開具發票的研究和開發的估計成本計入綜合資產負債表的應計負債和其他流動負債。如果實際提供服務的時間或努力程度與原先估計的不同,我們會相應調整應計項目。在提供相關服務之前,根據此等安排向CDMO和CRO支付的款項在綜合資產負債表中作為預付費用和其他流動資產入賬。到目前為止,我們估計的應計項目與實際成本沒有實質性差異。
基於股票的薪酬
我們使用公平值法將所有與僱員及非僱員有關的股票薪酬安排入賬,包括股票期權及限制性股票獎勵。我們採用柏力克—舒爾斯期權定價模式釐定購股權於授出日期的公平值。授出購股權之公平值乃按購股權持有人須提供服務以換取購股權獎勵之期間(稱為所需服務期,通常為歸屬期)以直線法確認。就具有表現條件的獎勵而言,本公司根據其對在明示或隱含服務期內達到表現條件的概率的評估,使用加速歸因模型確認補償開支。我們會對發生的損失進行核算。於釐定授出購股權之公平值時,吾等採用柏力克—舒爾斯期權定價模式,該模式要求輸入主觀假設。該等假設包括估計僱員在行使其已歸屬股票期權前將保留其已歸屬股票期權的時間長度(預期期限)、本公司普通股價格在預期期限內的估計波動性(預期波動性)、無風險利率及預期股息。以下假設的變動可能會對公允價值的估計以及最終確認的股票補償費用數額產生重大影響;而由此產生的公允價值變動(如有)在提供相關服務期間內於我們的綜合經營報表中確認。該等輸入數據屬主觀性,一般需要進行重大分析及判斷。以下假設之變動可對以股票為基礎之補償之公平值之估計產生重大影響:
商譽
商譽指收購價超出業務合併中收購之有形及已識別無形資產淨值公平值之差額。商譽不會攤銷,惟至少每年評估減值,或當事實及情況變動顯示商譽之公平值可能低於賬面值時。
99
商譽於第四季度每年於報告單位層面進行減值測試,或於事件或情況變動顯示資產可能出現減值時更頻密。此類事件或情況的例子包括但不限於法律或商業環境的重大不利變化、不利的監管行動或意外競爭。我們已確定我們於單一經營分部經營,並擁有單一報告單位。
於進行減值測試前,吾等評估定性因素,以釐定事件或情況的存在是否顯示報告單位的公平值較有可能低於賬面值。倘吾等於評估整體事件或情況後釐定報告單位之公平值較有可能低於賬面值,吾等將進行量化減值測試。
定量減值測試涉及比較報告單位的公平值與賬面值。倘報告單位之公允價值超過淨資產賬面值,商譽不減值,且無需進一步測試。倘報告單位之公平值低於賬面值,則吾等將減值虧損金額(如有)計量為賬面值超出報告單位之公平值之差額。我們於截至2023年12月31日止財政年度第三季度進行商譽減值中期測試,並確定商譽已減值。
較小的報告公司
我們是《交易法》中定義的“小型報告公司”。作為一家規模較小的申報公司,我們可能會利用特定的減少披露和其他一般適用於非規模較小申報公司的上市公司的要求。這些規定包括:(i)不要求遵守經修訂的2002年《薩班斯·奧克斯利法案》第404(b)條的審計師證明要求;(ii)按比例披露高管薪酬;(iii)只提供兩年而不是三年的經審計財務報表的選擇。
我們將繼續是一個規模較小的報告公司,只要我們繼續有(i)低於2.5億美元的非關聯公司持有的股份截至我們第二財政季度的最後一個營業日,或(ii)低於美元,我們最近一個財年的1億美元年收入在第二個財政季度的最後一個工作日之前完成,截至我們第二財政季度最後一個營業日,非關聯公司持有的股票低於7億美元。
我們可以選擇利用部分但不是全部這些豁免。因此,此處包含的信息可能與您從您持有股票的其他上市公司收到的信息不同。我們已選擇豁免延遲採納若干會計準則,因此,我們不受與其他並非規模較小報告公司的公眾公司相同的新訂或經修訂會計準則規限。
近期發佈和採納的會計公告
見標題為“”的部分重要會計政策摘要“我們的財務報表附註2載於本年報其他地方,表格10—K以獲取更多信息。
第7A項。定量和合格關於市場風險的披露。
利率風險
截至2023年12月31日,我們擁有現金及現金等價物1.597億美元,包括現金和國庫證券。利息收入對一般利率水平敏感;然而,基於該等投資的性質,利率即時變動10%不會對我們的現金及現金等價物、財務狀況或經營業績造成重大影響。
外幣兑換風險
我們的總部位於美國,我們的大部分一般和行政開支以及研發成本均以美元支付。隨着業務增長,我們的經營業績及現金流量可能會因外幣匯率而波動。迄今為止,我們認為外幣匯率波動對我們於本文所列任何期間的經營業績並無重大影響。
通貨膨脹風險
我們的資產主要為貨幣,包括現金及現金等價物。由於這些資產的流動性,這些資產不受通貨膨脹的直接影響。由於我們打算保留並繼續使用我們的設備、傢俱、固定裝置和辦公室設備、計算機硬件和軟件以及租賃改善,我們相信增量通脹與
100
該等項目的重置成本不會對我們的營運造成重大影響。通貨膨脹通常通過增加我們的勞動力成本、臨牀試驗和製造成本來影響我們。截至二零二三年及二零二二年十二月三十一日止年度,我們認為通脹對我們的業務、財務狀況或經營業績並無重大影響。
項目8.財務狀況TS和補充數據。
本報告要求提交的所有財務報表和補充數據均按照本年度報告第15(a)項的表格10—K項下的規定提交,並通過引用併入本文。
項目9.與Accou的變更和分歧會計與財務信息披露專業。
沒有。
第9A項。控制和程序。
對披露控制和程序的評價
於二零二三年十二月三十一日,我們的管理層在首席執行官及首席財務官(分別為首席執行官及首席財務官)的參與下,評估了披露監控及程序的有效性。《交易法》第13a—15(e)條和第15d—15(e)條所界定的"披露控制和程序"一詞是指公司為確保公司根據《交易法》提交或提交的報告中所要求披露的信息被記錄、處理、彙總和報告而設計的控制和其他程序,在SEC規則和表格中規定的時間內。
披露控制和程序包括但不限於旨在確保公司根據《交易法》提交或提交的報告中要求披露的信息得到積累並酌情傳達給公司管理層,包括其首席執行官和首席財務官,以便及時就所要求的披露作出決定的控制和程序。
管理層認識到,任何控制和程序,無論設計和運作如何良好,只能提供實現其目標的合理保證,管理層在評估可能的控制和程序的成本效益關係時,必須運用其判斷。任何披露控制和程序制度的有效性都存在固有的侷限性。這些限制包括人為錯誤的可能性、規避或超越控制措施和程序以及合理的資源限制。此外,由於我們已根據若干我們認為合理的假設設計我們的監控系統,我們的監控系統在所有可能的未來情況下可能無法達到其預期目的。因此,我們的披露控制及程序提供合理保證,但並非絕對保證,以達致其目標。
管理層財務報告內部控制年度報告
我們的管理層負責建立和維護對我們的財務報告的充分內部控制(定義見交易法第13a—15(f)條和第15d—15(f)條)。我們對財務報告的內部控制旨在為財務報告的可靠性和根據美國公認會計原則編制綜合財務報表提供合理保證,幷包括以下政策和程序:
由於其固有的侷限性,財務報告的內部控制可能無法防止或發現錯誤陳述。此外,對未來期間進行任何有效性評估的預測都有這樣的風險,即由於條件的變化,控制可能變得不充分,或者對政策或程序的遵守程度或遵守情況可能惡化。
我們的管理層在首席執行官及首席財務官的參與下,評估了我們於二零二三年十二月三十一日對財務報告的內部監控。管理層根據特雷德韋委員會贊助組織委員會發布的內部監控綜合框架所確立的標準進行評估,並得出結論認為,截至2023年12月31日,我們對財務報告的內部監控在合理的保證水平下有效。
101
這份10-K表格年度報告不包括我們的註冊會計師事務所關於財務報告的內部控制的證明報告。由於我們是一家非加速申報公司,管理層的報告不受我們註冊會計師事務所的認證。
我們不能向您保證未來不會發生重大缺陷或重大缺陷,也不能保證我們能夠及時糾正這些缺陷或缺陷,因為這些缺陷或缺陷可能會削弱我們準確和及時報告財務狀況、經營成果或現金流的能力。有關更多信息,請參閲本年度報告表格10-K中題為“風險因素”一節的相關風險。
財務報告內部控制的變化
除上文所述外,於截至2023年12月31日止年度內,吾等對財務報告的內部控制(定義見外匯法案第13a-15(F)及15d-15(F)條)並無發生重大影響或合理地可能會對財務報告的內部控制產生重大影響的變動。
項目9B。其他信息。
(A)沒有。
正如之前披露的,2021年3月12日,我們與Jones Trading Institution Services LLC(銷售代理)簽訂了按需資本銷售協議(銷售協議),根據該協議,我們可以隨時通過我們的銷售代理(ATM計劃),根據我們的選擇,出售總計75,000,000美元的普通股(ATM股票)。2022年11月8日,我們提交了一份新的招股説明書補充文件,其中包括根據自動櫃員機計劃提供和出售高達1.00億美元的普通股,其中包括根據現有招股説明書未出售的3000萬美元的普通股,以及高達7000萬美元的額外普通股。
2024年3月13日,我們向我們的銷售代理髮出書面通知,要求終止銷售協議,根據銷售協議第12(B)條,自2024年3月15日起生效。我們不受任何與終止銷售協議相關的終止處罰。於終止前,已售出6,490萬元自動櫃員機股份,而根據銷售協議,仍有8,010萬元自動櫃員機股份可供出售。由於銷售協議終止,我們不會根據自動櫃員機計劃提供或出售任何額外的股份。
(B)沒有。
項目9C。披露妨礙檢查的外國司法管轄區。
不適用。
102
部分(三)
項目10.董事、執行董事非營利組織與公司治理。
本項目要求的有關董事、高管和公司治理的信息將包括在我們的2024年委託書中,我們打算根據Form 10-K的一般指示G(3)在我們的財政年度結束後120天內向美國證券交易委員會提交該委託書,並通過引用將其併入本文(不包括薪酬與業績披露)。
我們通過了一套針對董事、高級管理人員和員工的商業行為和道德準則,稱為《商業行為和道德準則》。《商業行為和道德準則》可在我們的網站上查閲,網址為https://investor.adicetbio.com/corporate-governance/governance-highlights.我們將在我們的網站上及時披露(I)適用於我們的首席執行官、首席財務官或控制人或執行類似職能的人員的任何保單修訂的性質,以及(Ii)授予這些特定個人的保單條款的任何豁免的性質,包括默示放棄、獲得豁免的人的姓名和豁免的日期。股東可向我們的合規官員索要一份《商業行為和道德準則》的免費副本,地址為Adicet Bio,Inc.,地址:馬薩諸塞州波士頓達特茅斯街131號,郵編:02116。
項目11.行政人員E補償。
本項目要求的有關高管薪酬的信息將包括在我們的2024年委託書中,根據Form 10-K的一般指示G(3),我們打算在財政年度結束後120天內向美國證券交易委員會提交委託書,並通過引用將其併入本文中(不包括薪酬與績效的披露)。
項目12.某些受益所有者的擔保所有權業主和管理層及相關股東事宜。
本項目所要求的有關某些受益所有人和管理層的擔保所有權以及根據股權補償計劃授權發行的證券的信息將包括在我們的2024年委託書中,我們打算根據Form 10-K一般指示G(3)在本財年結束後120天內向美國證券交易委員會提交該委託書,並將其併入本文作為參考。
本項目所要求的有關某些關係和相關交易以及董事獨立性的信息將包括在我們的2024年委託書中,我們打算根據Form 10-K的一般指示G(3)在我們的財政年度結束後120天內向美國證券交易委員會提交委託書,並將其併入本文中以供參考。
第14項.本金賬户律師費和服務費。
我們的獨立會計師事務所是位於馬薩諸塞州波士頓的畢馬威會計師事務所(PCAOB審計師ID:
本項目要求的有關主要會計費用和服務的信息將包括在我們的2024年委託書中,我們打算根據Form 10-K的一般指示G(3)在我們的財政年度結束後120天內向美國證券交易委員會提交該委託書,並通過引用將其併入本文。
103
部分IV
項目15.展品和展品社會報表明細表。
(A)本年報的表格10-K包括下列文件:
104
ADICET BIO,INC.
合併財務報表索引
|
頁面 |
|
|
獨立註冊會計師事務所報告(KPMG LLP,Boston,MA,審計師事務所ID:185) |
F-2 |
合併財務報表 |
|
截至2023年12月31日和2022年12月31日的合併資產負債表 |
F-3 |
截至2023年12月31日和2022年12月31日的合併業務報表 |
F-4 |
截至2023年12月31日和2022年12月31日止年度股東權益綜合報表 |
F-5 |
截至2023年12月31日和2022年12月31日的合併現金流量表 |
F-6 |
合併財務報表附註 |
F-7 |
F-1
獨立註冊會計師事務所報告
致股東和董事會
Adicet Bio,Inc.:
對合並財務報表的幾點看法
我們審計了Adicet Bio公司及其子公司(本公司)截至2023年12月31日和2022年12月31日的合併資產負債表,截至2023年12月31日和2022年12月31日的相關綜合經營報表、股東權益和現金流量,以及相關的附註(統稱為綜合財務報表)。我們認為,綜合財務報表在所有重要方面都公平地反映了公司截至2023年12月31日和2022年12月31日的財務狀況,以及截至2023年12月31日和2022年12月31日止年度的經營結果和現金流量,符合美國公認會計原則。
意見基礎
這些合併財務報表由公司管理層負責。我們的責任是根據我們的審計對這些合併財務報表發表意見。我們是一家在美國上市公司會計監督委員會(PCAOB)註冊的公共會計師事務所,根據美國聯邦證券法以及美國證券交易委員會和PCAOB的適用規則和法規,我們必須與公司保持獨立。
我們是按照PCAOB的標準進行審計的。這些準則要求我們計劃和執行審計,以獲得關於合併財務報表是否沒有重大錯報的合理保證,無論是由於錯誤還是舞弊。本公司並無被要求對其財務報告的內部控制進行審計,我們也沒有受聘進行審計。作為我們審計的一部分,我們被要求瞭解財務報告的內部控制,但不是為了對公司財務報告內部控制的有效性發表意見。因此,我們不表達這樣的意見。
我們的審計包括執行評估合併財務報表重大錯報風險的程序,無論是由於錯誤還是欺詐,以及執行應對這些風險的程序。這些程序包括在測試的基礎上審查關於合併財務報表中的金額和披露的證據。我們的審計還包括評價管理層使用的會計原則和作出的重大估計,以及評價合併財務報表的整體列報。我們相信,我們的審計為我們的觀點提供了合理的基礎。
關鍵審計事項
關鍵審計事項指在對合並財務報表進行當期審計時產生的、已傳達或要求傳達給審計委員會的事項:(1)涉及對綜合財務報表具有重大意義的賬目或披露;(2)涉及我們特別具有挑戰性的、主觀的或複雜的判斷。我們確定不存在關鍵的審計事項。
/s/
自2020年以來,我們一直擔任本公司的審計師。
2024年3月19日
F-2
Adicet Bio公司
合併B配額單
(單位為千,不包括每股和每股金額)
|
|
十二月三十一日, |
|
|
十二月三十一日, |
|
||
資產 |
|
|
|
|
|
|
||
流動資產: |
|
|
|
|
|
|
||
現金和現金等價物 |
|
$ |
|
|
$ |
|
||
預付費用和其他流動資產 |
|
|
|
|
|
|
||
*流動資產總額 |
|
|
|
|
|
|
||
財產和設備,淨額 |
|
|
|
|
|
|
||
經營性租賃使用權資產 |
|
|
|
|
|
|
||
商譽 |
|
|
|
|
|
|
||
其他非流動資產 |
|
|
|
|
|
|
||
*總資產 |
|
$ |
|
|
$ |
|
||
負債與股東權益 |
|
|
|
|
|
|
||
流動負債: |
|
|
|
|
|
|
||
應付帳款 |
|
$ |
|
|
$ |
|
||
應計負債和其他流動負債 |
|
|
|
|
|
|
||
經營租賃負債 |
|
|
|
|
|
|
||
流動負債總額 |
|
|
|
|
|
|
||
經營租賃負債,扣除當期部分 |
|
|
|
|
|
|
||
其他非流動負債 |
|
|
|
|
|
|
||
總負債 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
股東權益: |
|
|
|
|
|
|
||
優先股,$ |
|
|
|
|
|
|
||
普通股,$ |
|
|
|
|
|
|
||
額外實收資本 |
|
|
|
|
|
|
||
累計赤字 |
|
|
( |
) |
|
|
( |
) |
股東權益總額 |
|
|
|
|
|
|
||
總負債和股東權益 |
|
$ |
|
|
$ |
|
||
附註是這些合併財務報表的組成部分。
F-3
Adicet Bio公司
業務處合併報表口糧
(單位為千,不包括每股和每股金額)
|
|
截至十二月三十一日止的年度: |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
收入—關聯方 |
|
$ |
|
|
$ |
|
||
運營費用: |
|
|
|
|
|
|
||
研發 |
|
|
|
|
|
|
||
一般和行政 |
|
|
|
|
|
|
||
商譽減值 |
|
|
|
|
|
|
||
總運營費用 |
|
|
|
|
|
|
||
運營虧損 |
|
|
( |
) |
|
|
( |
) |
利息收入 |
|
|
|
|
|
|
||
利息支出 |
|
|
( |
) |
|
|
( |
) |
其他費用,淨額 |
|
|
( |
) |
|
|
( |
) |
所得税前虧損準備 |
|
|
( |
) |
|
|
( |
) |
所得税撥備 |
|
|
|
|
|
|
||
淨虧損 |
|
$ |
( |
) |
|
$ |
( |
) |
每股基本和稀釋後淨虧損 |
|
$ |
( |
) |
|
$ |
( |
) |
用於計算每股淨虧損的加權平均普通股,基本和攤薄 |
|
|
|
|
|
|
||
附註是這些合併財務報表的組成部分。
F-4
Adicet Bio公司
合併報表股東權益
(單位為千,不包括份額)
|
|
普通股 |
|
|
其他內容 |
|
|
累計 |
|
|
總計 |
|
||||||||
|
|
股票 |
|
|
金額 |
|
|
資本 |
|
|
赤字 |
|
|
權益 |
|
|||||
2021年12月31日的餘額 |
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
|
||||
行使股票期權時發行普通股 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
受限制股票歸屬時發行普通股 |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
在認股權證行使時發行普通股 |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
扣繳税款的股份 |
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
員工購股計劃下的普通股申購 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
根據市場發售發行普通股,扣除發行成本$ |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
基於股票的薪酬費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
淨虧損 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2022年12月31日的餘額 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||||
行使股票期權時發行普通股 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
受限制股票歸屬時發行普通股 |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
扣繳税款的股份 |
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
員工購股計劃下的普通股申購 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
基於股票的薪酬費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
淨虧損 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2023年12月31日的餘額 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||||
附註是這些合併財務報表的組成部分。
F-5
Adicet Bio公司
合併狀態現金流項目
(單位:千)
|
|
截至12月31日的12個月, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
經營活動的現金流 |
|
|
|
|
|
|
||
淨虧損 |
|
$ |
( |
) |
|
$ |
( |
) |
對淨虧損與經營活動中使用的現金淨額進行的調整: |
|
|
|
|
|
|
||
折舊及攤銷費用 |
|
|
|
|
|
|
||
非現金租賃費用 |
|
|
|
|
|
|
||
基於股票的薪酬費用 |
|
|
|
|
|
|
||
處置財產、廠房和設備的損失 |
|
|
( |
) |
|
|
|
|
商譽減值 |
|
|
|
|
|
|
||
處置租賃資產損失 |
|
|
|
|
|
( |
) |
|
遞延債務發行成本攤銷 |
|
|
|
|
|
|
||
經營性資產和負債變動情況: |
|
|
|
|
|
|
||
預付費用和其他流動資產 |
|
|
|
|
|
|
||
其他非流動資產 |
|
|
|
|
|
|
||
應付帳款 |
|
|
( |
) |
|
|
|
|
合同負債—關聯方 |
|
|
|
|
|
( |
) |
|
經營租賃負債 |
|
|
( |
) |
|
|
( |
) |
應計負債及其他流動和非流動負債 |
|
|
|
|
|
|
||
用於經營活動的現金淨額 |
|
|
( |
) |
|
|
( |
) |
投資活動產生的現金流 |
|
|
|
|
|
|
||
購置財產和設備 |
|
|
( |
) |
|
|
( |
) |
用於投資活動的現金淨額 |
|
|
( |
) |
|
|
( |
) |
融資活動產生的現金流 |
|
|
|
|
|
|
||
根據市場發售發行普通股所得,扣除發行成本 |
|
|
|
|
|
|
||
行使股票期權所得收益 |
|
|
|
|
|
|
||
員工購股計劃的收益 |
|
|
|
|
|
|
||
與股權獎勵的淨份額結算有關的扣繳和支付的税款 |
|
|
( |
) |
|
|
( |
) |
遞延發行成本 |
|
|
|
|
|
( |
) |
|
融資活動提供的現金淨額 |
|
|
|
|
|
|
||
現金和現金等價物淨變化 |
|
|
( |
) |
|
|
( |
) |
期初現金及現金等價物 |
|
|
|
|
|
|
||
期末現金及現金等價物 |
|
$ |
|
|
$ |
|
||
補充現金流量信息 |
|
|
|
|
|
|
||
非現金投資和融資活動的補充披露 |
|
|
|
|
|
|
||
應付賬款和應計費用中所列財產和設備的購置 |
|
$ |
|
|
$ |
|
||
以經營性租賃負債換取的經營性使用權資產 |
|
$ |
|
|
$ |
|
||
附註是這些財務報表不可分割的一部分。
F-6
Adicet Bio公司
綜合備註財務報表
1.業務的組織和性質
Adicet Bio,Inc.(前身為resTORBio,Inc.(resTORbio)及其子公司(本公司)是一家臨牀階段生物技術公司,發現和開發用於自身免疫性疾病和癌症的同種異體γ δ T細胞療法。該公司正在推進一個“現成的”γ δ T細胞的管道,工程與嵌合抗原受體(CAR),以促進持久的活性在患者。該公司激活、工程和製造來自無關供體外周血細胞的同種異體γ δ T細胞候選產品的方法使其能夠以快速和具有成本效益的方式生成新的產品候選。
Adicet Bio,Inc. (when在合併之前,Former Adicet)於2014年11月在特拉華州註冊成立。於二零二零年九月十五日,Former Adicet完成與resTORbio的合併(Merger),據此,Former Adicet與resTORbio的全資附屬公司合併,以與Former Adicet作為resTORbio的全資附屬公司存續,並更名為“Adicet Therapeutics,Inc”的全股份交易。(Adicet Therapeutics)。就合併而言,本公司更名為“resTORBio,Inc.”。Adicet Bio,Inc.該公司的主要行政辦公室位於馬薩諸塞州波士頓。該公司還在加利福尼亞州紅木城設有辦事處。
Adicet Bio Israel Ltd.(前身為Applied Immune Technologies Ltd.)(Adicet Israel)為本公司的全資附屬公司,位於以色列海法。Adicet Israel成立於2006年。於二零一九年,本公司整合其在美國的業務,包括研發活動,因此大幅減少其在以色列的業務。
流動性
本公司已產生重大淨經營虧損及經營產生負現金流量,累計虧損為美元,
於2021年3月12日,本公司與JonesTrading Institutional Services LLC(作為銷售代理)訂立一份按需資本銷售協議(銷售協議),以規定發售、發行及銷售總額最多為$
於二零二三年十二月三十一日後,本公司籌集所得款項淨額總額約為$
本公司預計,其現金及現金等價物,連同年底後通過我們的ATM計劃和發售籌集的所得款項,將足以為其自發布該等綜合財務報表起至少未來12個月的預測運營開支、資本開支需求和償債支付提供資金。
到目前為止,該公司的所有收入都來自與Regeneron製藥公司(Regeneron)的合作和許可協議。在獲得監管機構對本公司任何候選產品的批准並將其商業化或與第三方簽訂額外的合作協議之前,該公司預計不會產生任何重大產品收入,而且它不知道何時或是否會發生這兩種情況。該公司預計在可預見的未來將繼續遭受重大虧損,隨着公司繼續開發其候選產品並尋求監管機構的批准,並開始將任何經批准的產品商業化,預計虧損將會增加。該公司面臨與開發新產品相關的所有風險,包括但不限於籌集額外資本、競爭對手開發新技術創新、臨牀前和臨牀失敗的風險
F-7
Adicet Bio公司
合併財務報表附註
本公司產品的安全性和有效性、其候選產品在臨牀試驗中的安全性和有效性、依賴外部方(如合同研究機構(CRO)和合同開發和製造組織(CDMO))的風險、監管審批過程、一旦獲得批准後市場對公司產品的接受程度、缺乏營銷和銷售歷史、對關鍵人員的依賴和對專有技術的保護,以及可能會遇到不可預見的費用、困難、併發症、延誤和其他可能對其業務產生不利影響的未知因素。
在公司能夠從產品銷售中獲得可觀的收入之前,公司預計將通過出售股權、債務融資、與公司或其他融資來源的合作或其他安排來為其運營提供資金。按照可接受的條款,公司可能得不到足夠的資金,或者根本不能。該公司未能在需要時籌集資金,可能會對其財務狀況和公司實施其業務戰略的能力產生負面影響。儘管本公司繼續執行這些計劃,但不能保證本公司將成功地以本公司可接受的條款獲得足夠的資金,為持續運營提供資金,如果有的話。
2.主要會計政策摘要
陳述的基礎
綜合財務報表和相關披露是按照美利堅合眾國公認的會計原則(美國公認會計原則或公認會計原則)編制的。
合併原則
合併財務報表包括本公司及其全資子公司的賬目。在合併中,所有公司間賬户和交易都已取消。美元是公司及其子公司的職能貨幣和報告貨幣。
預算的使用
按照公認會計準則編制合併財務報表要求管理層作出估計和假設,以影響合併財務報表日期的資產和負債額以及或有負債的披露,以及報告期內的收入和支出的報告金額。這些估計包括遞延税項資產、財產和設備的使用壽命、研究和開發活動的應計項目、收入確認和基於股票的補償以及公司的遞增借款利率。實際結果可能與這些估計不同。
商譽
商譽指收購價超出業務合併中收購之有形及已識別無形資產淨值公平值之差額。商譽不會攤銷,惟至少每年評估減值,或當事實及情況變動顯示商譽之公平值可能低於賬面值時。
商譽在第四季度每年在報告單位層面進行減值測試,或更頻繁地在事件或情況變化表明資產可能減值時進行測試。此類事件或情況的例子包括但不限於,法律或商業環境的重大不利變化、不利的監管行動或意外的競爭。該公司已確定其在單一經營部門中運營,並擁有單一報告單位。
在進行減值測試前,本公司評估定性因素,以確定事件或情況的存在是否表明報告單位的公允價值比賬面價值更有可能低於賬面價值。如在評估整體事件或情況後,本公司認為報告單位的公允價值極有可能少於賬面值,則本公司將進行量化減值測試。
量化減值測試涉及將報告單位的公允價值與賬面價值進行比較。如果報告單位的公允價值超過淨資產的賬面價值,商譽不會減損,也不需要進一步測試。如果報告單位的公允價值低於賬面價值,本公司將減值損失金額(如有)計量為報告單位賬面價值超過公允價值的部分。公司在截至2023年12月31日的財年第三季度進行了商譽減值中期測試並認定商譽受損。有關本評估的更多信息,請參閲附註16.我們合併財務報表的商譽。
F-8
Adicet Bio公司
合併財務報表附註
細分市場
公司以以下方式經營和管理其業務
信用風險集中
可能使本公司承受集中信貸風險的金融工具主要包括現金及現金等價物。公司的現金和現金等價物存放在美國的兩家金融機構和以色列的一家金融機構,這些金額有時可能超過保險限額。本公司將其現金等價物投資於貨幣市場基金及國庫證券。本公司通過將現金等價物放置於其認為具有高度信譽和高評級投資的銀行和機構,以限制其與現金等價物相關的信貸風險。截至目前,本公司並無就其現金及現金等價物存款產生任何虧損。
該公司擁有
風險和不確定性
本公司面臨生物技術行業早期公司常見的風險和不確定性,包括但不限於競爭對手開發新技術創新、保護專利技術、依賴關鍵人員、遵守政府法規以及需要獲得額外融資以資助運營。目前正在開發的候選產品將需要大量額外的研發工作,包括廣泛的臨牀前研究、臨牀試驗和監管部門的批准,然後才能商業化。這些努力需要大量額外資金、足夠的人員基礎設施以及廣泛的遵守和報告。
該公司的候選產品仍在開發中,迄今為止,該公司的候選產品都沒有被批准銷售,因此,該公司沒有從產品銷售中產生任何收入。
無法保證公司的研發工作將順利完成,公司的知識產權將獲得或保持充分的保護,開發的任何產品將獲得必要的政府監管批准,或任何批准的產品將在商業上可行。即使公司的產品開發努力是成功的,它是不確定何時,如果有的話,公司將產生收入從產品銷售。本公司在技術迅速變化和來自其他製藥和生物技術公司的激烈競爭的環境中經營。
現金和現金等價物
本公司認為,自購買日期起三個月或以下到期的所有高流動性投資均為現金等價物。截至2023年12月31日及二零二二年,現金及現金等價物包括存放於銀行的現金,自購買當日起三個月或以下到期的貨幣市場基金投資,以及隔夜國庫證券。
金融工具的公允價值
本公司若干金融工具(包括現金等價物、應收賬款、應付賬款及應計賬款及其他流動負債)的賬面值因其到期日相對較短而與公允值相若。
財產和設備,淨額
屬性及設備按成本減累計折舊及攤銷列賬。折舊乃按相關資產之估計可使用年期(一般為三年)以直線法計算。租賃物業裝修以直線法按資產估計可使用年期或剩餘租賃年期兩者中較短者攤銷。保養及維修於產生時計入營運費用。當資產報廢或以其他方式處置時,成本和
F-9
Adicet Bio公司
合併財務報表附註
累積折舊從綜合資產負債表中剔除,而由此產生的任何損益反映在已實現期間的綜合業務報表中。
長期資產減值準備
倘有事件或情況變動顯示資產或資產組之賬面值可能無法收回,本公司會檢討長期資產是否減值。可收回性乃按資產或資產組之賬面值與該資產或資產組預期產生之未來現金流量淨額之比較計量。該資產或資產組被認為發生減值的,以該資產或資產組的賬面價值超過該資產或資產組的公允價值的金額計量。本公司於2023年第三季度結合商譽減值測試進行了長期資產減值測試,得出結論認為,
收入確認
在ASC 606下,與客户簽訂合同的收入(ASC本公司於客户取得承諾貨品或服務的控制權時確認收入,金額應反映本公司預期就交換該等貨品或服務而收取的代價。為確定本公司確定在ASC 606範圍內的安排的收入確認,本公司執行ASC 606規定的以下五個步驟:
與客户的合同存在於(i)本公司與客户訂立法律上可強制執行的合同,該合同界定了各方對待轉讓產品或服務的權利,並確定了與這些產品或服務相關的付款條款,(ii)合同具有商業實質,以及(iii)本公司根據客户的情況,支付承諾對價的意圖和能力。
在合同開始時,一旦合同被確定為在ASC 606的範圍內,公司識別承諾的商品或服務,並通過評估每個承諾的商品或服務是否不同來確定履約義務。不明確的商品或服務與合同中的其他商品或服務捆綁在一起,直至一個明確的商品或服務捆綁在一起。本公司隨後於履約責任獲履行時(或當)分配至相關履約責任的交易價格金額確認為收益。
本公司截至2022年12月31日止年度的所有收入均來自與Regeneron簽訂的許可證和合作協議(見附註8)。截至二零二三年十二月三十一日止年度,本公司並無任何收入。
就收入確認而言,本公司透過評估現有及可強制執行權利及義務存在的期間釐定其特許或合作協議的期限。除其他因素外,這一決定受到實質性解僱處罰的存在的影響。
本公司根據ASC 606範圍內的公司許可證或合作協議確認收入。這些協議包括與知識產權和研發服務許可證有關的承諾。如果本公司知識產權的許可被確定為不同於該安排中確定的其他履約義務,則本公司在許可轉讓給被許可人且被許可人能夠使用和受益於該許可時確認分配給該許可的不可退還預付費用的收入。就與其他承諾捆綁的牌照而言,本公司運用判斷評估合併履約責任的性質,以釐定合併履約責任是否隨時間或於某一時間點達成,以及(倘隨時間)計量進度的適當方法,以確認來自不可退還預付費用的收入。因此,交易價格一般包括於合約開始時及於指定未來日期到期的固定費用、於達成指定事件時到期的里程碑付款形式的可變代價及客户確認特許產品銷售淨額時賺取的分層特許權使用費。本公司根據其預期的代價金額計量交易價格,
F-10
Adicet Bio公司
合併財務報表附註
以換取將承諾的商品和/或服務轉讓給客户。本公司採用“最可能金額”法估計其將有權就該合約收取的可變代價金額。可變代價金額乃計入交易價格,惟當與可變代價有關的不確定性其後獲解決時,已確認的累計收益金額可能不會出現重大撥回。於每項包括開發及監管里程碑付款的安排開始時,本公司評估相關事件是否被認為最有可能達成,並估計將計入交易價格的金額。
公司研發工作的付款或補償,如果這些工作被視為一部分或單一履約義務,則使用最能反映公司履行義務的進度衡量標準隨時間確認。
預付款項於收到或到期時記錄為合約負債,並可能要求將收益確認延遲至未來期間,直至本公司履行其根據該等安排之責任為止。當本公司收取代價之權利為無條件時,應付本公司之款項入賬列為應收賬款。倘於合約開始時預期客户付款與向客户轉讓承諾貨品或服務之間的期間為一年或以下,本公司不會評估合約是否具有重大融資成分。
就包括基於銷售額的特許權使用費(包括基於銷售水平的里程碑付款)的安排,以及特許權被視為特許權使用費相關的主要項目而言,本公司於(i)相關銷售發生時,或(ii)已分配部分或全部特許權使用費的履約責任已獲履行(或部分履行)時(以較遲者為準)確認收入。迄今為止,本公司尚未確認其合作安排產生的任何特許權使用費收入。
研究和開發費用
研究和開發費用包括與開展研究和開發計劃直接相關的成本,包括工資和相關費用、CDMO成本、CRO成本、材料、供應品、研究設備的折舊和維護、諮詢成本以及設施成本的分配部分,如租金、水電費、保險費、維修和維護費、折舊費、信息技術費用和一般支助事務。所有與研究及開發有關的成本於產生時於綜合經營報表內支銷。
如果獲得許可的技術尚未達到技術可行性且未來沒有替代用途,則獲得技術許可所產生的成本將計入所獲得的正在進行的研究和開發費用。
應計CRO、CDMO和研發費用
該公司已與CDMO和CRO簽訂了各種協議。該公司的研究和開發應計項目是根據所提供的服務水平、研究進展(包括活動的階段或完成)以及合同成本進行估算的。已提供但尚未開具發票的研發估計成本計入綜合資產負債表的應計負債及其他流動負債。如果實際執行服務的時間或努力程度與最初估計的不同,本公司將相應調整應計項目。在提供相關服務之前,根據此等安排向CDMO和CRO支付的款項在綜合資產負債表中作為預付費用和其他流動資產入賬。至2023年12月31日曾經有過
租契
與ASU 2016-02號一致,租賃(主題842)(ASU 2016-02),公司確定一項安排在開始時是否為租約或包含租約。租期超過12個月的租賃在資產負債表上確認為使用權(ROU)資產以及流動和長期經營租賃負債(視情況而定)。本公司已選擇不在資產負債表上確認12個月或以下的租約。該公司在評估租賃安排時通常只包括初始租賃期。除非有合理確定本公司會續期,否則續訂租約的選擇並不包括在本公司的評估內。該公司監督其不少於每季度續訂租約的計劃。此外,本公司的租賃協議一般不包含任何剩餘價值擔保或限制性契諾。
根據ASU 2016-02,ROU資產和租賃負債是根據租賃期內未來最低租賃付款的現值確認的。由於公司的大部分租約沒有提供隱含利率,公司使用其增量借款利率(IBR)來確定未來的現值,IBR是公司為完全抵押借款支付的估計利率,相當於租賃期內的總租賃付款
F-11
Adicet Bio公司
合併財務報表附註
最低租賃費。最低租賃付款的租賃費用在租賃期限內以直線基礎確認。對於採用ASU 2016-02後簽訂或重新評估的租賃協議,本公司不合並租賃和非租賃部分。可變租賃付款是指已發生的費用。
本公司於開始日期作出的假設於發生若干事件(包括租賃修訂)時重新評估。當租賃修訂授予承租人原租賃中未包括的額外使用權,且租賃付款增加與額外使用權的獨立價格成比例時,租賃修訂構成一份單獨合同。倘租賃修訂導致獨立合約,則按與新租賃相同的方式入賬。
基於股票的薪酬
本公司採用公允價值方法核算與僱員和非僱員的股票薪酬安排,這要求確認與所有股票支付相關的成本的補償費用,包括股票期權。公允價值法要求公司在授予之日使用期權定價模型估計基於股票的支付獎勵的公允價值。該公司使用布萊克-斯科爾斯期權定價模型來估計授予的期權的公允價值,這些期權是在必要的服務期(通常是歸屬期間)內以直線方式支出的。本公司對發生的沒收行為進行核算。期權估值模型,包括布萊克-斯科爾斯期權定價模型,需要輸入幾個假設。所用假設的改變會對授標日期的公允價值產生重大影響。這些假設包括無風險利率、預期股息收益率、預期波動率和獎勵的預期壽命。對於有業績條件的獎勵,公司根據其對業績條件在顯式或隱式服務期內達到業績條件的概率的評估,確認補償費用。
所得税
本公司採用資產負債法對所得税進行會計處理,該方法要求就用於財務報告目的的資產和負債賬面值與用於所得税報告目的的金額以及用於經營虧損和税收抵免結轉的金額之間的差異所產生的預期未來税收後果確認遞延所得税資產和負債。遞延所得税資產和負債的變動計入所得税撥備。
本公司的遞延税項資產及負債按預期於該等暫時差額預期收回或結算的年度適用的已頒佈税率計量。倘確定全部或部分遞延税項資產很可能無法變現,則會記錄估值撥備以減少遞延税項資產。本公司在評估遞延税項資產未來變現的可能性時會考慮許多因素,包括近期盈利業績、未來應課税收入的預期、可用的結轉期及其他相關因素。本公司於作出釐定期間記錄所需估值備抵的變動。
本公司根據管理層對截至報告日期的事實、情況和信息的評估,評估其所得税狀況,並記錄所有需要審查的年度的税收優惠。對於那些更有可能維持税收優惠的税務頭寸,本公司記錄了最大金額的税收優惠,在與完全瞭解所有相關信息的税務機關最終達成和解時實現的可能性超過50%。對於那些税收優惠不太可能持續的所得税頭寸,本公司不會在合併財務報表中確認税收優惠。本公司將與不確定税務狀況有關的利息和罰款(如果適用)記錄為所得税支出(福利)的一個組成部分。
每股淨虧損
基本信息每股普通股淨虧損的計算方法是將淨虧損除以當期已發行普通股的加權平均數,不考慮潛在的稀釋證券。每股攤薄淨虧損的計算方法是將淨虧損除以當期已發行的普通股和潛在攤薄證券的加權平均數。公司的潛在攤薄股份,包括已發行的股票期權、員工購股計劃(ESPP)獎勵和未歸屬的限制性股票單位(RSU),被視為普通股等價物,只有在其影響是攤薄的情況下才包括在每股攤薄淨虧損的計算中。基本及攤薄每股淨虧損按參與證券所需的兩級法列報。兩級法根據宣佈或累積的股息以及未分配收益的參與權來確定每一類普通股和參股證券的每股淨收益(虧損)。兩級法要求普通股股東在該期間可獲得的收入(虧損)在普通股和參股證券之間根據他們各自分享未分配收益的權利進行分配,就像該期間的所有收入(虧損)都已分配一樣。本公司的參與證券不承擔分擔本公司損失的合同義務。因此,淨虧損完全歸因於普通股股東。自.以來
F-12
Adicet Bio公司
合併財務報表附註
公司已報告所有列報期間的淨虧損,稀釋後的每股普通股淨虧損與該期間的每股普通股基本淨虧損相同。
後續活動考慮事項
本公司考慮在資產負債表日之後但在綜合財務報表發佈之前發生的事件或交易,以便為某些估計提供額外證據或確定需要額外披露的事項。後續活動已按要求進行了評估。本公司已評估所有後續事項,並確定除綜合財務報表附註所披露的事項外,並無重大已確認或未確認後續事項需要披露。請參閲附註17.後續事件。
近期會計公告
新的會計聲明不時由財務會計準則委員會或其他準則制定機構發佈,並於指定生效日期起由本公司採納,除非下文另有討論。
最近採用的會計公告
2016年6月,FASB發佈了ASU第2016-13號,金融工具.信用損失(主題326):金融工具信用損失的測量(ASU 2016-13),其中要求計量和確認以攤銷成本持有的金融資產的預期信貸損失。這個ASU用預期損失模型取代了現有的已發生損失減值模型。它還消除了非臨時性減值的概念,並要求與可供出售債務證券有關的信貸損失通過信貸損失準備而不是作為證券攤銷成本基礎的減少來記錄。這些變化將導致更早地確認信貸損失。對於有資格成為較小報告公司的美國證券交易委員會申請者,本會計準則在2022年12月15日之後的財年以及這些財年內的過渡期內有效。允許及早領養。公司在2023年第一季度採用了ASU 2016-13。這對其合併財務報表和相關披露的影響並不大。
2017年1月,FASB發佈了ASU第2017-04號,無形資產-商譽和其他(話題350):簡化商譽減值測試(ASU 2017-04)。新指引取消了兩步減值測試的第二步,簡化了後續商譽的計量。修訂要求實體通過將報告單位的公允價值與其賬面金額進行比較來進行年度或中期商譽減值測試。實體仍可選擇對報告單位進行定性評估,以確定是否有必要進行量化減值測試。有資格成為較小報告公司的美國證券交易委員會申請者,應在2022年12月15日之後的財年開始的年度或任何中期商譽減值測試中採用本更新中的修正案。修正案應在預期的基礎上適用。允許在2017年1月1日之後的測試日期進行中期或年度商譽減值測試,提前採用。公司於2023年第一季度採用ASU 2017-04。這對其合併財務報表和相關披露的影響並不大。
尚未採用的會計公告
2023年9月,FASB發佈了ASU 2023-09號,所得税(話題740): 改進所得税披露,這提高了所得税披露的透明度和有用性。該修訂要求公眾發行人在税率對賬中披露特定類別,併為符合數量閾值的對賬項目提供額外信息(如果這些對賬項目的影響等於或大於税前收入或虧損乘以適用法定所得税率計算的金額的5%)。此外,該修正案要求發行人披露繳納的所得税數額,(扣除收到的退款淨額)(國家)、州和外國税以及按個別司法管轄區分列的已繳納所得税(扣除所得税)數額(扣除所得税)等於或大於已繳納所得税(扣除所得税)總額(扣除所得税)的5%。對於SEC申報人,該ASU在2025年12月15日之後開始的財政年度有效。允許提前收養。本公司目前正在評估採納該會計處理單位對其綜合財務報表及相關披露的影響。
3.公允價值計量
本公司採用公平值等級制度釐定金融及非金融資產及負債的公平值,該等級制度建立可用於計量公平值的三個輸入數據等級,如下:
第一級-可觀察的輸入數據,如相同資產或負債在活躍市場上的報價。
F-13
Adicet Bio公司
合併財務報表附註
第2級-第1級價格以外的可觀察輸入數據,例如類似資產或負債的報價、不活躍市場的報價,或其他可觀察或可由資產或負債大致整個期間的可觀察市場數據證實的輸入數據。
第三級—不可觀察輸入數據,反映管理層對市場參與者於計量日期為資產或負債定價所用的最佳估計。本集團已考慮估值技術的固有風險及模型輸入數據的固有風險。
在釐定公允價值時,本公司採用估值技術,最大限度地利用可觀察到的投入及儘量減少使用不可觀察到的投入,並在評估公允價值時考慮交易對手的信用風險。
按公允價值計量的資產和負債按對公允價值計量重要的最低投入水平進行整體分類。本公司對某一特定投入對整個公允價值計量的重要性的評估要求管理層作出判斷,並考慮該資產或負債的具體因素。
下表介紹了該公司按公允價值經常性計量的金融資產和負債的信息,並顯示了用於確定此類公允價值的公允價值等級(以千計):
|
|
2023年12月31日 |
|
|||||||||||||
|
|
1級 |
|
|
2級 |
|
|
3級 |
|
|
總計 |
|
||||
資產: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
國庫證券(1)(2) |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
資產公允價值總額 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
|
|
2022年12月31日 |
|
|||||||||||||
|
|
1級 |
|
|
2級 |
|
|
3級 |
|
|
總計 |
|
||||
資產: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
貨幣市場基金(1)(3) |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
資產公允價值總額 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
4.預付費用和其他流動資產
預付費用和其他流動資產包括以下內容(以千計):
|
|
十二月三十一日, |
|
|
十二月三十一日, |
|
||
預付保險 |
|
$ |
|
|
$ |
|
||
預付軟件訂閲費和許可費 |
|
|
|
|
|
|
||
預付維修費 |
|
|
|
|
|
|
||
預付費專業服務 |
|
|
|
|
|
|
||
對CRO和CDMO的預付款 |
|
|
|
|
|
|
||
應收利息 |
|
|
|
|
|
|
||
其他預付費用和流動資產 |
|
|
|
|
|
|
||
預付費用和其他流動資產總額 |
|
$ |
|
|
$ |
|
||
F-14
Adicet Bio公司
合併財務報表附註
5.財產和設備,淨額
財產和設備,淨值如下(以千計):
|
|
使用壽命 |
|
十二月三十一日, |
|
|
十二月三十一日, |
|
||
租賃權改進 |
|
|
$ |
|
|
$ |
|
|||
實驗室設備 |
|
|
|
|
|
|
|
|||
傢俱和固定裝置 |
|
|
|
|
|
|
|
|||
軟件 |
|
|
|
|
|
|
|
|||
在建工程 |
|
|
|
|
|
|
|
|||
計算機設備 |
|
|
|
|
|
|
|
|||
財產和設備,毛額 |
|
|
|
|
|
|
|
|
||
減去:累計折舊和攤銷 |
|
|
|
|
( |
) |
|
|
( |
) |
財產和設備,淨額 |
|
|
|
$ |
|
|
$ |
|
||
截至2023年12月31日和2022年12月31日,本公司的所有財產和設備均位於美國。2022年是$
在建工程減少了美元
6.應計負債和其他流動負債
應計負債和其他流動負債包括以下各項(以千計):
|
|
十二月三十一日, |
|
|
十二月三十一日, |
|
||
應計補償 |
|
$ |
|
|
$ |
|
||
CDMO應計費用 |
|
|
|
|
|
|
||
應計專業服務 |
|
|
|
|
|
|
||
應計其他研究和開發費用 |
|
|
|
|
|
|
||
應計CRO費用 |
|
|
|
|
|
|
||
應計其他負債 |
|
|
|
|
|
|
||
應計負債和其他負債總額 |
|
$ |
|
|
$ |
|
||
7.定期貸款
於2020年4月28日,本公司訂立貸款及擔保協議(貸款協議)於2020年7月8日、2020年9月14日、2020年9月15日、2021年10月21日、2022年12月2日修訂(2022年貸款修正案)及2023年5月30日與加利福尼亞銀行(前稱太平洋西部銀行)就位於加利福尼亞州紅木城的設施租賃改善提供資金,以及貸款協議允許的其他用途。根據2021年10月21日的修正案,加州銀行將提供一項或多項定期貸款(定義見2021年貸款修正案),以及不超過美元的非公式輔助服務。
於2023年3月13日,本公司與加利福尼亞銀行簽署了一份函件,同意儘管2022年貸款修訂案中包含的契諾,直至2023年6月30日(i)本公司及其附屬公司將無需維持美元中的較小者。
F-15
Adicet Bio公司
合併財務報表附註
市場(ii)本公司必須在加利福尼亞銀行或其附屬公司(包括太平洋西部資產管理公司)維持其合併餘額。
於2023年5月30日,本公司進一步修訂其與加利福尼亞銀行的貸款協議(2023年貸款修訂)。根據二零二三年貸款修訂本,本公司必須維持(i)元(以較低者為準)
截至2023年12月31日,該公司擁有
8.第三方協議
再生
於2016年7月29日,本公司與Regeneron訂立許可證及合作協議,該協議於2019年4月修訂,該修訂對Regeneron於2019年7月投資本公司B系列可贖回可轉換優先股私募交易(經修訂,Regeneron協議)生效。
財務條款。公司收到了一筆不可退還的預付款#
2022年1月28日,根據Regeneron協議,Regeneron行使其全球獨家許可權,授權ADI—002是一種針對Glypican—3的同種異體γ δ CAR T細胞療法。在行使期權的同時,Regeneron支付了1000美元的行使費,
Regeneron負責ADI—002的所有開發、製造和商業化,並且必須向公司支付較高的單位數特許權使用費,即ADI—002淨銷售額的百分比,期限從第一次商業銷售開始,直至(i)特許專利權到期或無效,或(ii)自第一次商業銷售起的低兩位數的金額(較長者)。
自.起於二零二三年及二零二二年十二月三十一日,概無與再生能協議有關的合約資產。下表呈列本公司截至2023年及2022年12月31日止年度合約負債的變動(單位:千):
截至2023年12月31日的12個月 |
|
餘額為 |
|
|
扣除額 |
|
|
餘額為 |
|
|||
合同責任 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
F-16
Adicet Bio公司
合併財務報表附註
截至2022年12月31日的12個月 |
|
餘額為 |
|
|
扣除額 |
|
|
餘額為 |
|
|||
合同責任 |
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||
Twist Bioscience
於二零二一年三月,本公司與Twist Bioscience Corporation(Twist)訂立抗體發現協議(Twist協議)。根據Twist協議的條款,Twist將利用其專有平臺技術協助本公司發現與本公司選定的靶抗原相關的新型抗體。本公司保留對根據Twist協議發現的任何程序抗體的唯一和專有權利,並有權根據協議對任何工作產品進行專利、轉讓、許可或轉讓。此外,本公司有權將其抗體編程的權利轉授給第三方。本公司可隨時終止本協議,不論是否有任何理由,經指定期限提前書面通知。
根據協議的條款,公司將支付Twist預付,不可退還的項目啟動費,技術訪問費,以及根據協議簽訂的每個項目的項目費。此外,該公司將支付數千萬美元的開發和監管里程碑費用,以及根據協議啟動的項目向Twist淨銷售額的低個位數版税。於2022年11月,本公司訂立扭曲協議之修訂(扭曲修訂)。Twist修正案更新了與Twist審計權相關的語言,以及與技術訪問費相關的金額。
截至2023年12月31日,累計本公司已產生並支出美元
9.承付款和或有事項
經營租約
該公司在加利福尼亞州紅木城和馬薩諸塞州波士頓租賃辦公室和實驗室空間。
紅杉城
於二零一八年,Adicet Therapeutics簽署一份不可撤銷租賃協議(經二零二二年修訂),據此,本公司租賃位於加利福尼亞州紅木城1000 Bridge Parkway及1200 Bridge Parkway部分的辦公室及實驗室設施(紅木城租約)。
2023年1月9日,Adicet Therapeutics與Westport Office Park,LLC簽訂了第三次租約修訂案(第三次修訂案)。第三修正案進一步修改了紅木城租約,並從2023年1月1日起增加租户改善津貼,
2023年8月7日,Adicet Therapeutics與Westport Office Park,LLC簽訂了第四次租約修訂案。第四修正案修正了第三修正案中收到的租户改善津貼將被攤銷的期限,並確定了公司應支付的每月攤銷額。
2023年9月1日,Adicet Therapeutics修訂了與Westport Office Park,LLC的信用證。該修正案減少了與1000 Bridge Parkway有關的信用證金額,
波士頓
F-17
Adicet Bio公司
合併財務報表附註
於2018年,本公司就位於馬薩諸塞州波士頓Boylston St 500號的辦公空間(500 Boylston Lease)訂立租賃協議,並於2019年修訂。根據第500號Boylston租約的條款,本公司經業主同意,獲準轉讓、轉租或轉讓本租約。
於2021年7月19日,本公司與RFS OPCO LLC(分承租人)訂立轉租協議,據此,本公司同意將所有
|
|
十二月三十一日, |
|
|
2024 |
|
|
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
2027年及其後 |
|
|
— |
|
總計 |
|
$ |
|
|
公司確認扣除分租收入後的租金支出為#美元。
此外,該公司仍有責任支付500 Boylston租約項下的剩餘租金,共計#美元。
所有不可撤銷經營租賃義務項下的未來最低租賃付款2023年12月31日的情況如下(單位:千):
|
|
十二月三十一日, |
|
|
2024 |
|
|
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
2027年及其後 |
|
|
|
|
未貼現的租賃付款總額 |
|
|
|
|
減去:推定利息 |
|
|
|
|
經營租賃總負債 |
|
|
|
|
減:當前部分 |
|
|
|
|
經營性租賃負債,扣除當期到期日 |
|
$ |
|
|
我們設施的基準利率和剩餘租賃期限及其加權平均基準利率和剩餘期限如下:2023年12月31日:
租賃地點 |
|
IBR |
|
剩餘條款 |
|
|
加利福尼亞州雷德伍德城(1000 Bridge Parkway) |
|
|
|
|
||
加利福尼亞州雷德伍德城(1200 Bridge Parkway) |
|
|
|
|
||
馬薩諸塞州波士頓 |
|
|
|
|
||
加權平均 |
|
|
|
|
||
F-18
Adicet Bio公司
合併財務報表附註
下表顯示截至該年度的經營租賃成本及與經營租賃使用權資產、淨負債及經營租賃負債有關的資料。2023年12月31日(千人):
|
|
截至12月31日的12個月, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
租賃費 |
|
|
|
|
|
|
||
經營租賃成本 |
|
$ |
|
|
$ |
|
||
短期租賃成本 |
|
|
|
|
|
|
||
轉租收入 |
|
|
( |
) |
|
|
( |
) |
總租賃成本 |
|
$ |
|
|
$ |
|
||
其他信息 |
|
|
|
|
|
|
||
用於租賃負債的經營現金流量 |
|
$ |
( |
) |
|
$ |
|
|
加權平均剩餘租賃期限--經營租賃 |
|
|
|
|
|
|
||
加權平均貼現率-經營租賃 |
|
|
% |
|
|
% |
||
截至2023年12月31日,經營使用權資產為美元,
本公司持有美元的信用證
賠償協議
在日常業務過程中,本公司訂立協議,其中可能包括賠償條款。根據該等協議,本公司可就受償方蒙受或招致之損失作出賠償、使其免受損害及抗辯。有些規定將損失限於第三方行動造成的損失。在某些情況下,賠償將在協議終止後繼續進行。本公司根據該等條文可能須作出的未來付款的最高潛在金額無法確定。本公司從未為訴訟辯護或解決與該等賠償條款相關的索賠而產生任何物質費用。本公司亦已與董事及高級管理人員訂立彌償協議,要求本公司(除其他外)在特拉華州公司法允許的最大範圍內,就因其作為董事或高級管理人員的身份或服務而可能產生的某些責任彌償。本公司目前已購買董事及高級職員責任保險。
10.股東權益
普通股
經修訂的公司註冊證書授權公司簽發,
公司董事會董事會宣佈股息時,普通股股東有權獲得股息,但須遵守優先股股東的優先權利。截至2023年12月31日,
該公司有以下普通股預留供未來發行:
|
|
十二月三十一日, |
|
|
十二月三十一日, |
|
||
可供將來授予的股票期權和限制性股票單位 |
|
|
|
|
|
|
||
已發行和未償還的股票期權 |
|
|
|
|
|
|
||
未歸屬的限制性股票單位 |
|
|
|
|
|
|
||
預留普通股總數 |
|
|
|
|
|
|
||
F-19
Adicet Bio公司
合併財務報表附註
11.基於股票的薪酬
基於股票的薪酬費用
下表列示了公司綜合經營報表中反映的基於股票的補償費用(千):
|
|
截至十二月三十一日止的年度: |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
研發 |
|
$ |
|
|
$ |
|
||
一般和行政 |
|
|
|
|
|
|
||
基於股票的薪酬總額 |
|
$ |
|
|
$ |
|
||
下表按獎勵類型呈列以股票為基礎的補償開支(千):
|
|
截至十二月三十一日止的年度: |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
股票期權 |
|
$ |
|
|
$ |
|
||
受限制股票單位(包括基於業績的受限制股票單位) |
|
|
|
|
|
|
||
員工購股計劃 |
|
|
|
|
|
|
||
總計 |
|
$ |
|
|
$ |
|
||
股票期權
截至該年度的股票期權活動摘要2023年12月31日載列如下(以千計,除股份及每股數據外):
|
|
數量 |
|
|
加權 |
|
|
加權的- |
|
|
集料 |
|
||||
未清償,2022年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
授予的期權 |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
行使的期權 |
|
|
( |
) |
|
$ |
|
|
|
|
|
|
|
|||
被沒收或取消的期權 |
|
|
( |
) |
|
$ |
|
|
|
|
|
|
|
|||
未清償,2023年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
可行使期權,2023年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
已歸屬和預期歸屬,2023年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
柏力克斯科爾斯模型計算以股份為基礎之薪酬所採用之假設如下:
|
|
截至十二月三十一日止的年度: |
||
|
|
2023 |
|
2022 |
普通股公允價值 |
|
$ |
|
$ |
預期期限(年) |
|
|
||
波動率 |
|
|
||
無風險費率 |
|
|
||
股息率 |
|
|
||
每個股票期權的公允價值是在授予之日利用布萊克-斯科爾斯期權定價模型估計的,該模型採用以下假設:
F-20
Adicet Bio公司
合併財務報表附註
假設如下:
本公司將繼續使用判斷來評估預期波動率、無風險利率、股息率和預期期限,用於基於預期的股票補償。
總內在價值是指相關股票期權的行權價格與公司普通股在2023年12月31日和2022年12月31日的現金股票期權的公允價值之間的差額。於截至2023年12月31日及2022年12月31日止年度內行使的股票期權的內在價值合計不足$
截至2023年12月31日及2022年12月31日止年度內歸屬的期權的總公平價值為$
截至2023年12月31日,與未歸屬股票期權有關的未確認股票薪酬支出總額為#美元。
限售股單位
截至年底的RSU活動摘要和相關信息2023年12月31日規定如下:
|
|
未完成的單位數量 |
|
|
加權平均 |
|
||
未清償,2022年12月31日 |
|
|
|
|
$ |
|
||
已批准的RSU |
|
|
|
|
$ |
|
||
歸屬的RSU |
|
|
( |
) |
|
$ |
|
|
被沒收的RSU |
|
|
( |
) |
|
$ |
|
|
未清償,2023年12月31日 |
|
|
|
|
$ |
|
||
該公司授予
截至2023年12月31日,大約有
期權重定價
在……上面2023年8月8日,董事會批准根據本公司2015年股票激勵計劃和2018年計劃(統稱為該等計劃)的條款於2023年8月14日(生效日期)生效的股票期權重新定價(期權重新定價)。根據購股權重新定價,並受一年懸崖期規限,各股份之行使價
F-21
Adicet Bio公司
合併財務報表附註
選擇權以前根據計劃批准的,總計
經重新定價的購股權保留計劃及適用授標協議所載的現有條款及條件。股票期權修改導致增加補償成本約為美元,
此外,截至生效日期,本公司已發行
12.每股淨虧損
下表列出了每股基本淨虧損和攤薄淨虧損的計算方法(單位為千,不包括每股和每股數據):
|
|
截至十二月三十一日止的年度: |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
淨虧損--基本虧損和稀釋虧損 |
|
$ |
( |
) |
|
$ |
( |
) |
用於計算每股淨虧損的加權平均股份,基本股份和攤薄股份 |
|
|
|
|
|
|
||
每股基本和稀釋後淨虧損 |
|
|
( |
) |
|
|
( |
) |
截至2023年和2022年12月31日,本公司的潛在攤薄股份,包括未行使的股票期權和未歸屬的受限制股份單位,被視為普通股等價物,僅在其影響具有攤薄性時才計入每股攤薄淨虧損的計算中。
於呈列期間,下列潛在攤薄證券之已發行股份不包括在計算每股攤薄淨虧損時,原因是包括該等股份會產生反攤薄影響:
|
|
截至12月31日, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
購買普通股的期權 |
|
|
|
|
|
|
||
未歸屬的限制性股票單位 |
|
|
|
|
|
|
||
總計 |
|
|
|
|
|
|
||
F-22
Adicet Bio公司
合併財務報表附註
13.所得税
所得税(受益)準備金的組成部分如下(以千計):
|
|
十二月三十一日, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
當前: |
|
|
|
|
|
|
||
聯邦制 |
|
$ |
|
|
$ |
|
||
狀態 |
|
|
|
|
|
|
||
外國 |
|
|
|
|
|
|
||
總電流 |
|
|
|
|
|
|
||
延期: |
|
|
|
|
|
|
||
聯邦制 |
|
|
|
|
|
|
||
狀態 |
|
|
|
|
|
|
||
外國 |
|
|
|
|
|
|
||
延期合計 |
|
|
|
|
|
|
||
所得税準備金(受益於) |
|
$ |
|
|
$ |
|
||
曾經有過
就以下税率表而言,所得税收益(撥備)與按聯邦法定税率計算税前虧損的預期金額不同如下:
|
|
截至十二月三十一日止的年度: |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
聯邦法定所得税率 |
|
|
% |
|
|
% |
||
税收抵免 |
|
|
|
|
|
( |
)% |
|
州所得税 |
|
|
( |
)% |
|
|
% |
|
更改估值免税額 |
|
|
( |
)% |
|
|
( |
)% |
162米限制 |
|
|
|
|
|
( |
)% |
|
基於股票的薪酬 |
|
|
( |
)% |
|
|
( |
)% |
商譽減值 |
|
|
( |
)% |
|
|
|
|
其他永久性差異 |
|
|
( |
)% |
|
|
( |
)% |
所得税撥備 |
|
|
( |
)% |
|
|
( |
)% |
遞延税項資產之暫時差異及結轉之税務影響呈列如下(千):
|
|
十二月三十一日, |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
遞延税項資產: |
|
|
|
|
|
|
||
淨營業虧損結轉 |
|
$ |
|
|
$ |
|
||
經營租賃使用權資產負債 |
|
|
|
|
|
|
||
遞延收入 |
|
|
|
|
|
|
||
基於股票的薪酬 |
|
|
|
|
|
|
||
無形資產 |
|
|
|
|
|
|
||
固定資產 |
|
|
|
|
|
|
||
應計項目和準備金 |
|
|
|
|
|
|
||
美國證券交易委員會174資本化研發 |
|
|
|
|
|
|
||
研發信貸結轉 |
|
|
|
|
|
|
||
税收抵免 |
|
|
|
|
|
|
||
遞延税項總資產 |
|
|
|
|
|
|
||
減去:估值免税額 |
|
|
( |
) |
|
|
( |
) |
遞延税項資產,扣除估值準備後的淨額 |
|
|
|
|
|
|
||
遞延税項負債: |
|
|
|
|
|
|
||
固定資產 |
|
|
|
|
|
|
||
基礎差 |
|
|
|
|
|
|
||
經營性租賃使用權資產 |
|
|
( |
) |
|
|
( |
) |
遞延税項淨資產 |
|
$ |
|
|
$ |
|
||
F-23
Adicet Bio公司
合併財務報表附註
於二零二零年九月十五日,Adicet Bio與resTORBio完成合並,Adicet Bio成為合併集團的母公司。由於該合併被視為免税合併,故該合併並無為資產的税基增加基礎。上述遞延税項表包括與resTORBio有關的遞延税項。
本公司已就其遞延税項資產設立估值撥備,原因是有關變現資產的不確定性。IRC第174條,經2017年《減税和就業法案》修訂,不再允許在產生此類成本的納税年度立即扣除研究和開發支出。因此,本公司於二零二三年所得税撥備中將該等成本資本化,導致遞延税項資產增加。
ASC 740要求,淨經營虧損、暫時性差異和信用結轉的税收利益應記作資產,但管理層評估認為實現的可能性"更大"。未來税收優惠的實現取決於公司在結轉期內產生足夠應納税收入的能力。由於本公司最近的經營虧損歷史,管理層認為,確認由上述未來税務利益產生的遞延税項資產目前不太可能實現,因此,已提供估值撥備。
估值免税額增加#美元。
截至2023年12月31日,該公司的淨經營虧損結轉為美元,
該公司還擁有約$
淨經營虧損結轉和研發税收抵免結轉的使用可能會受到1986年國內税收法典第382條和州法律的相應規定的年度限制,原因是以前發生的或將來可能發生的所有權變更。
本公司在美國聯邦司法管轄區、加利福尼亞州、馬薩諸塞州和以色列提交所得税申報表。2016至2023年課税年度仍須接受美國聯邦及州政府審查,惟以營運虧損淨額及信貸結轉之使用為限。此外,該公司目前正在接受加州特許經營税委員會(FTB)關於2017年納税年度收入分配的審計,並可能有義務根據審查結果向該州支付與該納税年度相關的未來款項。該公司正在評估FTB的提案並評估其行動方針。
截至2023年12月31日,該公司有未確認的税務優惠,
對期初和期末未確認税收優惠金額的調節如下(以千為單位):
|
|
截至十二月三十一日止的年度: |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
年初餘額 |
|
$ |
|
|
$ |
|
||
根據與上一年度有關的税務狀況進行調整 |
|
|
|
|
|
( |
) |
|
根據與本年度有關的税務狀況進行調整 |
|
|
|
|
|
|
||
年終結餘 |
|
$ |
|
|
$ |
|
||
F-24
Adicet Bio公司
合併財務報表附註
本公司在所得税費用(收益)中確認與上述未確認税務利益有關的利息費用和罰款。管理層確定,截至2023年12月31日,無需計提利息和罰款.
14.關聯方交易
截至2023年12月31日Regeneron擁有
15.界定供款計劃
本公司根據《國內税收法典》第401(k)條維持一項界定供款計劃,涵蓋幾乎所有全職美國僱員。僱員供款為自願性,並按個人基準釐定,惟須符合聯邦税務條例所允許的最高限額。截至二零二三年十二月三十一日止年度及2022年,本公司合共作出配對供款,
16.商譽
關於2022年第四季度進行的年度商譽減值分析,本公司確定其唯一報告單位的公允價值超過其賬面價值,因此,
於二零二三年第三季度,本公司股價大幅下跌。截至2023年9月30日,公司股價下跌
於釐定本公司於中期測試日期之中期減值分析之唯一報告單位之公平值時,本公司採用市場為基礎之方法,此方法之主要輸入數據為活躍市場之市場報價。為確定本公司單一報告單位的估計公允價值,本公司根據其股票價格計算其市值。根據本公司截至中期測試日期的中期減值分析,本公司單一報告單位的賬面值超過其公允價值。因此,已進行第二步商譽減值測試。於進行第二步商譽減值測試時,本公司使用可觀察輸入數據,並得出結論認為,減值開支對全部商譽而言是必要的。由於第二步評估,本公司錄得商譽減值費用為美元,
17.後續活動
自動櫃員機計劃
2024年1月,
承銷的公開發行
於2024年1月22日,Adicet與Jefferies LLC及Guggenheim Securities,LLC(包銷商)就包銷公開發售(發售)訂立包銷協議(包銷協議),
F-25
Adicet Bio公司
合併財務報表附註
承銷商公司的收入是$
F-26
展品索引
展品 數 |
|
展品説明 |
|
|
|
3.1 |
|
第三次修訂和重述的註冊人註冊證書(目前有效)(通過引用註冊人於2018年1月30日向SEC提交的關於表格8—K的當前報告(文件編號001—38359)的附件3.1納入)。 |
|
|
|
3.2 |
|
ResTORBio,Inc.第三次修訂和重述的註冊證書的修訂證書與反向股票拆分有關,日期為2020年9月15日(通過引用註冊人於2020年9月16日提交給SEC的當前表格8—K報告(文件編號001—38359)的附件3.1)。 |
|
|
|
3.3 |
|
ResTORBio,Inc.第三次修訂和重述的註冊證書的修訂證書2020年9月15日,與名稱變更有關(2020年9月16日向SEC提交的註冊人當前表格8—K報告(文件編號001—38359)的附件3.2)。 |
|
|
|
3.4 |
|
修訂和重述的註冊人章程(目前有效)(通過引用註冊人於2018年1月30日向SEC提交的當前表格8—K報告(文件編號001—38359)中的附件3.2納入). |
|
|
|
4.1 |
|
證券描述(通過引用於2020年3月12日向SEC提交的註冊人年度報告10—K表格(文件編號:001—38359)的附件4.3)。 |
|
|
|
4.2 |
|
修訂和重申的投資者權利協議,日期為2017年11月29日,註冊人和其他各方之間(通過引用我們於2017年12月29日向SEC提交的表格S—1(文件號333—222373)的註冊聲明的附件4.2納入)。 |
|
|
|
4.3 |
|
普通股證書樣本(通過引用2022年3月15日向SEC提交的註冊人年度報告10—K表格(文件編號001—38359)的附件4.3)。 |
|
|
|
4.4 |
|
預出資權證表格(通過引用註冊人於2024年1月24日向SEC提交的關於8—K表格(文件編號001—38359)的當前報告中的附件4.1納入)。 |
|
|
|
10.1 |
|
貸款和擔保協議,日期為2020年4月28日,由加利福尼亞銀行,Inc. Adicet Therapeutics,Inc.(通過引用註冊人於2020年9月16日向SEC提交的表格8—K(文件編號001—38359)的當前報告的附件10.26)。 |
|
|
|
10.2 |
|
貸款和擔保協議第一修正案,日期為2020年7月8日,由加利福尼亞銀行,Inc. Adicet Therapeutics,Inc.(通過引用註冊人於2020年9月16日向SEC提交的表格8—K(文件編號001—38359)的當前報告的附件10.32)。 |
|
|
|
10.3 |
|
2020年9月14日,由加利福尼亞銀行(Bank of California,Inc.)簽署的貸款和擔保協議第二次修正案。Adicet Therapeutics,Inc.(通過引用註冊人於2020年9月16日向SEC提交的表格8—K(文件編號001—38359)的當前報告的附件10.3合併)。 |
|
|
|
10.4 |
|
2020年9月15日,由加利福尼亞銀行(Bank of California,Inc.)簽署的貸款和擔保協議第三次修訂案。Adicet Therapeutics,Inc.(通過引用註冊人於2020年9月16日向SEC提交的表格8—K(文件編號001—38359)的當前報告的附件10.4)。 |
|
|
|
10.5 |
|
變更指令1,日期為2021年9月23日,由Adicet Therapeutics,Inc. CP Enterprises,Inc. d/b/a CP Construction(通過引用註冊人於2022年3月24日向SEC提交的當前表格8—K報告(文件編號001—38359)中的附件10.1合併)。 |
|
|
|
10.6 |
|
2號變更指令,日期為2022年3月18日,由Adicet Therapeutics,Inc. CP Enterprises,Inc. d/b/a CP Construction(通過引用註冊人於2022年3月24日向SEC提交的當前表格8—K報告(文件編號001—38359)中的附件10.2合併)。 |
|
|
|
10.7 |
|
變更指令3,日期為2022年3月18日,由Adicet Therapeutics,Inc. CP Enterprises,Inc. d/b/a CP Construction(通過引用註冊人於2022年3月24日向SEC提交的當前表格8—K報告(文件編號001—38359)中的附件10.3合併)。 |
|
|
|
10.8 |
|
2022年6月16日,Adicet Therapeutics,Inc.作為承租人,Westport Office Park,LLC作為業主(通過引用註冊人於2022年6月21日向SEC提交的關於表格8—K的當前報告(文件編號001—38359)的附件10.1納入)。 |
|
|
|
10.9+ |
|
抗體發現協議,日期為2021年3月23日,由註冊人和Twist Bioscience Corporation簽署(通過引用2022年11月8日向SEC提交的註冊人關於表格10—Q的季度報告(文件編號001—38359)的附件10.1合併)。 |
|
|
|
10.10+ |
|
抗體發現協議的第一修正案,日期為2022年11月8日,由註冊人和Twist Bioscience Corporation(通過引用2023年3月15日向SEC提交的註冊人年度報告10—K表(文件編號001—38359)的附件10.11合併)。 |
|
|
|
10.11+ |
|
Adicet Therapeutics,Inc.於2021年10月21日簽署的貸款和擔保協議第四次修正案。加利福尼亞銀行(Banc of California,Inc.)(通過引用2021年10月25日向SEC提交的註冊人當前表格8—K報告(文件編號001—38359)的附件10.1合併)。 |
|
|
|
10.12 |
|
第五修正案貸款和擔保協議,日期為2022年12月2日,由Adicet Treeutics,Inc.和加州銀行公司簽訂(通過參考註冊人於2022年12月8日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)的附件10.1而併入)。 |
|
|
|
10.13 |
|
無條件擔保,日期為2020年9月15日(通過引用附件10.7併入登記人於2020年9月16日提交給美國證券交易委員會的當前8-K表格報告(文件編號001-38359)中)。 |
|
|
|
10.14+ |
|
確認和修訂擔保,日期為2021年10月21日,註冊人和加州銀行,Inc.(通過引用附件10.2併入註冊人於2021年10月25日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)中)。 |
|
|
|
10.15# |
|
第二次修訂和重新啟動2018年股票期權和激勵計劃及其下的獎勵協議格式(通過引用附件10.1併入註冊人於2023年6月5日提交給美國證券交易委員會的當前8-K表格報告(文件編號001-38359)中)。 |
|
|
|
10.16# |
|
2017年股票激勵計劃及其獎勵協議格式(參考2018年1月16日提交給美國證券交易委員會的註冊人登記説明書附件10.1修訂後的S-1表格(第333-222373號文件)). |
|
|
|
10.17# |
|
2015年股票激勵計劃及其獎勵協議格式(通過引用附件10.13併入註冊人於2020年9月16日提交給美國證券交易委員會的當前8-K表格報告(文件編號001-38359)中)。 |
|
|
|
10.18# |
|
修訂和重啟2018年員工購股計劃(參考2022年3月15日提交給美國證券交易委員會的註冊人10-K年報(文件編號001-38359)附件10.14併入)。 |
|
|
|
10.19# |
|
2022年誘導計劃及其下授予協議的格式(通過引用附件10.15併入註冊人於2022年3月15日提交給美國證券交易委員會的10-K表格年度報告(文件編號001-38359)中)。 |
|
|
|
10.20# |
|
2022年誘導計劃第一修正案(通過引用註冊人於2023年3月15日提交給美國證券交易委員會的10-K表格年度報告(文件編號001-38359)附件10.23併入)。 |
|
|
|
10.21# |
|
僱傭協議表格(參考註冊人於2022年3月15日提交給美國證券交易委員會的10-K表格年度報告(文件編號001-38359)的附件10.16)。 |
|
|
|
10.22 |
|
註冊人與其每一名董事和高管之間的賠償協議表(通過參考註冊人於2022年3月15日提交給美國證券交易委員會的10-K表格年度報告的附件10.17而併入)。 |
|
|
|
10.23# |
|
修訂和重新制定了非僱員董事薪酬政策(通過引用登記人於2023年5月9日提交給美國證券交易委員會的10-Q季度報告(文件編號001-38359)的附件10.18而併入)。 |
|
|
|
10.24# |
|
修訂和重新制定的高級管理人員現金激勵獎金計劃(通過引用註冊人於2022年3月15日提交給美國證券交易委員會的10-K表格年報(文件編號001-38359)附件10.19併入)。 |
|
|
|
10.25 |
|
Adicet Bio,Inc.作為承租人,Westport Office Park LLC作為業主簽署的、日期為2018年10月31日的租賃協議(通過引用註冊人於2020年9月16日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)的附件10.23而併入)。 |
|
|
|
10.26 |
|
截至2020年12月30日,Adicet Treateutics,Inc.作為承租人,Westport Office Park,LLC作為業主(通過引用註冊人於2021年1月5日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)的附件10.1併入)。 |
|
|
|
10.27 |
|
第三次修訂租約,日期為2023年1月9日,租户為阿迪凱特治療公司,業主為韋斯特波特辦公園區公司(通過引用2023年3月15日提交給美國證券交易委員會的註冊人10-K年度報告(文件編號001-38359)的第10.34號附件納入)。 |
|
|
|
10.28 |
|
寫字樓租賃協議,日期為2018年1月8日,由resTORbio,Inc.與500 Boylston和222 Berkeley Owner(DE)LLC簽訂(通過參考2018年1月16日提交給美國證券交易委員會的註冊人登記聲明表格S-1(文件編號333-222373)附件10.15合併)。 |
|
|
|
10.29 |
|
寫字樓租賃第一修正案,日期為2019年4月1日,由resTORbio,Inc.與500Boylston和222 Berkeley Owner(DE)LLC(通過引用2019年5月15日提交給美國證券交易委員會的註冊人季度報告10-Q表格(文件編號001-38359)第10.2號合併)。 |
|
|
|
10.30 |
|
轉租協議,日期為2021年7月19日,由Adicet Bio,Inc.和RFS Opco LLC之間簽訂(通過引用註冊人於2021年7月23日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)的附件10.1而併入)。 |
|
|
|
10.31 |
|
業主和承包商之間的標準協議格式,其中付款基礎是由業主Adicet Treateutics,Inc.和承包商CP Enterprises,Inc.d/b/a CP Construction之間規定的金額,自2021年4月2日起生效(通過引用註冊人於2021年4月9日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)的附件10.1). |
|
|
|
10.32+ |
|
修訂和重新簽署的許可協議,日期為2014年5月21日,由代表自己和以色列理工學院的Technion研究和發展基金會有限公司與Adicet Treateutics,Inc.作為應用免疫技術有限公司的權益繼承人(通過引用註冊人於2020年9月16日提交給美國證券交易委員會的當前8-K報告(文件編號001-38359)的附件10.27併入)。 |
|
|
|
10.33+ |
|
修訂和重新簽署的許可協議的第1號修正案,日期為2015年6月30日,由代表自身和以色列理工學院的Technion研究與發展基金會有限公司和應用免疫技術有限公司(通過引用註冊人於2020年9月16日提交給美國證券交易委員會的當前8-K報告(文件編號001-38359)的附件10.28併入)。 |
|
|
|
10.34+ |
|
修訂和重新簽署的許可協議的第2號修正案,日期為2016年1月13日,由Technion研究和發展基金會有限公司、應用免疫技術有限公司和Adicet Treateutics,Inc.(通過引用註冊人於2020年9月16日提交給美國證券交易委員會的當前8-K表格報告(文件編號001-38359)的附件10.29併入)。 |
|
|
|
10.35+ |
|
許可和合作協議,日期為2016年7月29日,由Adicet Bio,Inc.和Regeneron PharmPharmticals,Inc.(通過引用註冊人於2020年9月16日提交給美國證券交易委員會的當前8-K表格報告(文件編號001-38359)的附件10.30併入)。 |
|
|
|
10.36+ |
|
對許可和合作協議的第1號修正案,日期為2019年4月24日,由Adicet Bio,Inc.和Regeneron PharmPharmticals,Inc.簽訂(通過引用註冊人於2020年9月16日提交給美國證券交易委員會的當前8-K表格報告(文件編號001-38359)的附件10.31併入)。 |
|
|
|
10.37 |
|
《貸款和擔保協議第六修正案》,日期為2023年5月30日,由加州銀行和Adicet Treateutics,Inc.(通過引用註冊人於2023年6月5日提交給美國證券交易委員會的8-K表格當前報告(文件編號001-38359)的附件10.1併入)。 |
|
|
|
10.38 |
|
截至2023年8月7日,Adicet Treateutics,Inc.作為承租人,Westport Office Park,LLC作為業主(通過引用2023年8月9日提交給美國證券交易委員會的註冊人季度報告10-Q表(文件編號001-38359)的第10.2號附件納入)。 |
|
|
|
10.39*+ |
|
會員協議,日期為2024年1月19日和2024年3月12日,由註冊人和勤奮的Bos 131 Dartoss Street LLC之間簽訂。 |
|
|
|
19.1* |
|
Adicet Bio,Inc.內幕交易政策。 |
|
|
|
21.1 |
|
註冊人的子公司(通過引用註冊人於2021年3月12日提交給美國證券交易委員會的10-K表格年度報告(文件編號001-38359)附件21.1合併)。 |
|
|
|
23.1* |
|
經獨立註冊會計師事務所畢馬威會計師事務所同意。 |
|
|
|
24.1* |
|
授權書(包括在簽名頁上)。 |
|
|
|
31.1* |
|
根據根據2002年《薩班斯-奧克斯利法案》第302節通過的1934年《證券交易法》第13a-14(A)條和第15d-14(A)條頒發的首席執行幹事證書。 |
|
|
|
31.2* |
|
根據根據2002年薩班斯-奧克斯利法案第302節通過的1934年《證券交易法》規則13a-14(A)和規則15d-14(A)認證首席財務官。 |
|
|
|
32.1** |
|
根據2002年《薩班斯-奧克斯利法案》第906節通過的《美國法典》第18編第1350節對首席執行官和首席財務官的認證。 |
|
|
|
97.1#* |
|
Adicet Bio,Inc.薪酬追回政策。 |
|
|
|
101.INS* |
|
內聯XBRL實例文檔 |
|
|
|
101.Sch* |
|
內聯XBRL分類擴展架構文檔 |
|
|
|
101.卡爾* |
|
內聯XBRL分類擴展計算鏈接庫文檔 |
|
|
|
101.定義* |
|
內聯XBRL分類擴展定義Linkbase文檔 |
|
|
|
101.實驗所* |
|
內聯XBRL分類擴展標籤Linkbase文檔 |
|
|
|
101.前期* |
|
內聯XBRL分類擴展演示文稿Linkbase文檔 |
|
|
|
104* |
|
封面交互數據文件 |
*現送交存檔。
+ 根據法規S—K第601(b)(10)項,本證物的部分(以附圖標記表示)已被省略。
#表示管理合同或任何補償計劃、合同或安排。
* * 本協議附件32.1中提供的證明應視為隨本年度報告10—K表格,且不應視為根據1934年證券交易法第18條(經修訂)之目的“已提交”。此類認證將不被視為通過引用納入根據《1933年證券法》(經修訂)或《1934年證券交易法》(經修訂)提交的任何文件中,除非註冊人以引用方式特別納入該文件。
I項目16. 10—K總結
不適用。
標牌縫隙
根據1934年《證券交易法》第13或15(D)節的要求,註冊人已正式授權下列簽署人代表其簽署本報告。
|
Adicet Bio公司 |
|
|
|
|
日期:2024年3月19日 |
發信人: |
/s/陳朔 |
|
|
陳紹爾 董事首席執行官總裁 (首席行政主任) |
授權委託書
以下個人簽名的每一人特此授權並任命Chen Schor和Nick Harvey,以及他們中的每一人,具有完全的替代和再替代的權力,以及完全的權力,作為他或她的真實和合法的事實上的代理人和代理人,以他或她的名義、地點和代替行事,並以每個人的名義和代表每個人,單獨和以下述每一種身份執行,並將本年報的任何及所有修訂以表格10—K存檔,並將該等修訂連同其所有證物及其他相關文件送交證券交易監察委員會存檔,授予上述事實律師及代理人及他們每一人作出及執行每一項作為及事情的全部權力及權限,批准和確認上述代理人或他們中的任何人或他們的替代人可以合法地作出或安排作出的所有事情。
根據1934年《證券法》的要求,本10-K表格年度報告已由以下人員在指定日期以指定身份簽署。
簽名 |
|
標題 |
|
日期 |
|
|
|
|
|
/s/陳朔 |
|
|
|
|
陳紹爾 |
|
董事首席執行官總裁(首席執行官) |
|
2024年3月19日 |
/s/Nick Harvey |
|
|
|
|
尼克·哈維 |
|
首席財務官(首席財務官和首席會計官) |
|
2024年3月19日 |
/S/傑弗裏·喬達克維茨 |
|
|
|
|
傑弗裏·喬達克維茨醫學博士 |
|
董事 |
|
2024年3月19日 |
/s/Steve Dubin |
|
|
|
|
史蒂夫·杜賓 |
|
董事 |
|
2024年3月19日 |
/S/卡爾·L·戈登 |
|
|
|
|
卡爾·L·戈登博士 |
|
董事 |
|
2024年3月19日 |
/s/Aya Jakobovits |
|
|
|
|
Aya Jakobovits博士 |
|
董事 |
|
2024年3月19日 |
/s/Michael Kauffman |
|
|
|
|
邁克爾·考夫曼醫學博士博士 |
|
董事 |
|
2024年3月19日 |
/s/Katie Peng |
|
|
|
|
彭麗萍 |
|
董事 |
|
2024年3月19日 |
/s/Andrew Sinclair |
|
|
|
|
安德魯·辛克萊博士 |
|
董事 |
|
2024年3月19日 |