
每個班級的標題 |
交易代碼 |
註冊的每個交易所的名稱 |
美國存托股份 每個代表1股 |
NVS |
紐約證券交易所 |
普通股,面值0.50瑞士法郎/股 * |
NOVN |
紐約證券交易所* |
大型加速文件服務器x |
加速文件管理器o |
非加速文件管理器o |
新興成長型公司o |
美國公認會計原則o |
國際會計準則理事會發布的國際財務報告準則x |
其他o |
目錄
某些術語的引入和使用
前瞻性陳述
第一部分
項目1.董事、高級管理人員和顧問的身份
項目2.報價統計數據和預期時間表
項目3.關鍵信息
3.A部分財務數據
|
Year ended December 31,
|
|||||||||||
|
(百萬美元,不包括每股信息)
|
2019
|
2018
|
2017
|
2016
|
2015
|
||||||
|
損益表數據1
|
|
|
|
|
|
||||||
|
持續運營對第三方的淨銷售額
|
47 445
|
44 751
|
42 338
|
41 975
|
42 641
|
||||||
|
持續經營的營業收入
|
9 086
|
8 403
|
8 702
|
8 248
|
8 522
|
||||||
|
來自相聯公司的收入
|
659
|
6 438
|
1 108
|
703
|
266
|
||||||
|
利息支出
|
– 850
|
– 932
|
– 750
|
– 675
|
– 637
|
||||||
|
其他財務收支
|
45
|
186
|
42
|
– 385
|
– 433
|
||||||
|
持續經營的税前收入
|
8 940
|
14 095
|
9 102
|
7 891
|
7 718
|
||||||
|
税費
|
– 1 793
|
– 1 295
|
– 1 603
|
– 1 095
|
– 1 066
|
||||||
|
持續經營淨收益
|
7 147
|
12 800
|
7 499
|
6 796
|
6 652
|
||||||
|
來自已終止經營業務之淨(虧損)╱收入(扣除分派收益前)。諾華股東
|
– 101
|
– 186
|
204
|
– 98
|
376
|
||||||
|
Alcon Inc.諾華公司股東
|
4 691
|
|
|
|
|
||||||
|
與投資組合轉換交易有關的淨收入
|
|
|
|
|
10 766
|
||||||
|
非持續經營業務的淨收益
|
4 590
|
– 186
|
|
204
|
|
– 98
|
|
11 142
|
|||
|
集團年終利潤
|
11 737
|
12 614
|
7 703
|
6 698
|
17 794
|
||||||
|
歸因於:
|
|
|
|
|
|
||||||
|
諾華製藥的股東
|
11 732
|
12 611
|
7 703
|
6 712
|
17 783
|
||||||
|
非控制性權益
|
5
|
3
|
0
|
– 14
|
11
|
||||||
|
|
|
|
|
|
|||||||
|
基本每股收益(美元)
|
|
|
|
|
|
||||||
|
持續運營
|
3.12
|
5.52
|
3.20
|
2.86
|
2.77
|
||||||
|
停產經營
|
2.00
|
– 0.08
|
0.08
|
– 0.04
|
4.63
|
||||||
|
總計
|
5.12
|
5.44
|
3.28
|
2.82
|
7.40
|
||||||
|
|
|
|
|
|
|||||||
|
稀釋後每股收益(美元)
|
|
|
|
|
|
||||||
|
持續運營
|
3.08
|
5.46
|
3.17
|
2.84
|
2.72
|
||||||
|
停產經營
|
1.98
|
– 0.08
|
0.08
|
– 0.04
|
4.57
|
||||||
|
總計
|
5.06
|
5.38
|
3.25
|
2.80
|
7.29
|
||||||
|
現金股利2
|
6 645
|
6 966
|
6 495
|
6 475
|
6 643
|
||||||
|
每股現金股息(瑞士法郎)3
|
2.95
|
2.85
|
2.80
|
2.75
|
2.70
|
||||||
|
持續運營的人員成本4, 5
|
13 843
|
13 515
|
12 009
|
11 950
|
11 336
|
||||||
|
年終持續業務的全職等值助理5
|
103 914
|
104 780
|
102 467
|
99 747
|
99 624
|
||||||
|
|
|||||||||||
|
1 持續經營包括創新藥品和Sandoz部門的業務以及企業活動。已終止的業務包括於2019年剝離的Alcon業務;於2015年剝離的動物保健和疫苗業務;以及消費者保健業務,該業務也於2015年注入新實體葛蘭素史克消費者保健控股有限公司(GSK消費者保健),諾華擁有36.5%的權益。該新創建的實體於2018年出售給GSK。為了反映這些交易,諾華根據國際財務報告準則的要求,將集團2019年至2015年的財務業績報告為“持續經營”和“已終止經營”。
|
|||||||||||
|
2 現金股利是指適用年度的現金支付,通常與上一年的收益有關。
|
|||||||||||
|
3 每股現金股息指與本年度盈利有關的建議股息。二零一五年至二零一八年之股息已於各股東周年大會上獲批准,而二零一九年之股息將於二零二零年二月二十八日提呈股東周年大會以供批准。
|
|||||||||||
|
4 人員成本包括工作人員的工資、薪金、津貼、佣金和獎金、加班費、獎勵、假日工資、遣散費和社會福利費用。
|
|||||||||||
|
5 自己的員工。
|
|||||||||||
|
Year ended December 31,
|
|||||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
2016
|
2015
|
||||||
|
資產負債表數據
|
|
|
|
|
|
||||||
|
現金、現金等價物、有價證券和衍生金融工具
|
11 446
|
15 964
|
9 485
|
7 777
|
5 447
|
||||||
|
盤存
|
5 982
|
6 956
|
6 867
|
6 255
|
6 226
|
||||||
|
其他流動資產
|
11 235
|
11 836
|
11 856
|
10 899
|
11 172
|
||||||
|
非流動資產
|
88 866
|
110 000
|
104 871
|
105 193
|
108 711
|
||||||
|
出售集團持有待售資產1
|
841
|
807
|
|
|
|
||||||
|
總資產
|
118 370
|
145 563
|
133 079
|
130 124
|
131 556
|
||||||
|
應付貿易帳款
|
5 424
|
5 556
|
5 169
|
4 873
|
5 668
|
||||||
|
其他流動負債
|
22 809
|
24 000
|
18 234
|
17 336
|
18 040
|
||||||
|
非流動負債
|
34 555
|
37 264
|
35 449
|
33 024
|
30 726
|
||||||
|
出售集團持有待售資產的負債1
|
31
|
51
|
|
|
|
||||||
|
總負債
|
62 819
|
66 871
|
58 852
|
55 233
|
54 434
|
||||||
|
Novartis AG股東應佔已發行股本及儲備
|
55 474
|
78 614
|
74 168
|
74 832
|
77 046
|
||||||
|
非控制性權益
|
77
|
78
|
59
|
59
|
76
|
||||||
|
總股本
|
55 551
|
78 692
|
74 227
|
74 891
|
77 122
|
||||||
|
負債和權益總額
|
118 370
|
145 563
|
133 079
|
130 124
|
131 556
|
||||||
|
淨資產
|
55 551
|
78 692
|
74 227
|
74 891
|
77 122
|
||||||
|
已發行股本
|
856
|
875
|
869
|
896
|
890
|
||||||
|
總流通股(百萬股)
|
2 265
|
2 311
|
2 317
|
2 374
|
2 374
|
||||||
|
1 持作出售之出售組別涉及山德士美國皮膚科業務及仿製美國口服固體產品組合出售給Aurobindo Pharma USA Inc.的資產及負債,如2018年9月6日宣佈的(見第18項。財務報表—附註2。重大未決交易”)。
|
|||||||||||
|
|
|||||||||||
|
|
|||||||||||
|
年掙了 |
月和 支付年份 |
總股息
每股 (瑞士法郎) |
總股息
每股 (美元) |
||||
|
2015
|
2016年3月
|
2.70
|
2.70
|
||||
|
2016
|
2017年3月
|
2.75
|
2.72
|
||||
|
2017
|
2018年3月
|
2.80
|
2.94
|
||||
|
2018
|
2019年3月
|
2.85
|
2.84
|
||||
|
2019 1
|
2020年3月
|
2.95
|
3.04 2
|
||||
|
|
|||||||
|
1 於二零二零年二月二十八日召開之股東周年大會上建議派發股息,並於二零二零年三月五日派發。
|
|||||||
|
2 2019年12月31日換算成美元,匯率為1.032美元兑瑞士法郎。此換算僅為示例,不應解釋為瑞士法郎金額所代表的、或已或可能按該匯率或任何其他匯率換算成美元。
|
|||||||
3.B資本化和債務
3.C提供和使用收益的理由
3.D風險因素
項目4. 公司信息
4.諾華的歷史與發展
4.B業務概述
創新藥物
|
項目/ 產品 |
普普通通 名字 |
機理 行動中的 |
潛在適應症 |
業務 特許經營 |
配方/ 路線: 行政管理 |
年項目
vt.進入,進入 當前 發展 相位 |
計劃中的備案 日期/當前 相位 |
||||||||
|
ABL001
|
阿司米尼
|
Bcr-abl抑制劑
|
慢性粒細胞白血病,3研發線
|
腫瘤學
|
口頭的
|
2016
|
2021/III
|
||||||||
|
ACZ885
|
Canakinumab
|
抗白細胞介素1β單抗
|
2發送非小細胞肺癌
|
腫瘤學
|
皮下注射
|
2017
|
2021/III
|
||||||||
|
|
|
1ST非小細胞肺癌
|
腫瘤學
|
皮下注射
|
2017
|
2021/III
|
|||||||||
|
|
|
輔助性非小細胞肺癌
|
腫瘤學
|
皮下注射
|
2017
|
2022/III
|
|||||||||
|
AVXS-1011
|
奧納塞姆諾—基因abepar—vovec
|
運動神經元生存 (SMN)基因 替代療法
|
脊髓性肌萎縮 (IV配方)
|
神經科學
|
靜脈輸注
|
2018
|
美國批准的歐盟註冊
|
||||||||
|
|
|
脊髓性肌萎縮 (IT配方)2
|
神經科學
|
鞘內注射
|
2018
|
2020/I
|
|||||||||
|
AVXS—201
|
TBD
|
甲基化cpg結合 蛋白2基因 替代療法
|
雷特綜合徵
|
神經科學
|
鞘內注射
|
2018
|
2023/I
|
||||||||
|
BYL7193
|
阿爾貝利西布
|
PI3K-α抑制物
|
PIK3CA突變體激素受體陽性 (HR+)/人表皮生長因子 受體2陰性(HER 2—) 絕經後晚期乳腺癌, 2發送線路(+Fulvestrant)
|
腫瘤學
|
口頭的
|
2018
|
美國批准歐盟註冊
|
||||||||
|
|
|
PIK3CA相關過度生長譜
|
腫瘤學
|
口頭的
|
2019
|
2020/III
|
|||||||||
|
|
|
三陰性乳腺癌
|
腫瘤學
|
口頭的
|
2019
|
2023/III
|
|||||||||
|
|
|
激素受體陰性(HR—)/人表皮生長因子受體2陽性(HER 2+)晚期乳腺癌
|
腫瘤學
|
口服
|
2019
|
2023/III
|
|||||||||
|
|
|
卵巢癌
|
腫瘤學
|
口頭的
|
2019
|
2023/III
|
|||||||||
|
|
|
頭頸部鱗狀細胞癌
|
腫瘤學
|
口頭的
|
2019
|
≥ 2024/III
|
|||||||||
|
CEE321
|
TBD
|
泛—jak抑制劑
|
特應性皮炎
|
免疫學, 肝病學和 皮膚科
|
局部
|
2019
|
≥ 2024/II
|
||||||||
|
CFZ533
|
伊卡利單抗
|
阻塞,非消耗, 抗CD40單克隆抗體 抗體
|
實體器官移植
|
免疫學, 肝病學和 皮膚科
|
靜脈輸注
|
2017
|
2023/II
|
||||||||
|
|
|
舍格倫綜合徵
|
免疫學, 肝病學和 皮膚科
|
靜脈輸注
|
2018
|
≥ 2024/II
|
|||||||||
|
科森提克斯
|
secukinumab
|
抗白細胞介素—17 單克隆抗體
|
非放射性軸性脊柱關節炎
|
免疫學, 肝病學和 皮膚科
|
皮下注射
|
2015
|
美國/歐盟註冊
|
||||||||
|
|
|
銀屑病關節炎與Humira的面對面研究®(阿達木單抗)
|
免疫學, 肝病學和 皮膚科
|
皮下注射
|
2015
|
2020/III
|
|||||||||
|
|
|
強直性脊柱炎與Sandoz生物相似的面對面研究赫裏莫茲(阿達莫單抗)
|
免疫學, 肝病學和 皮膚科
|
皮下注射
|
2015
|
2022/III
|
|||||||||
|
|
|
化膿性汗腺炎
|
免疫學, 肝病學和 皮膚科
|
靜脈輸注
|
2017
|
2022/III
|
|||||||||
|
|
|
鉅細胞動脈炎
|
免疫學, 肝病學和 皮膚科
|
靜脈輸注
|
2018
|
≥ 2024/II
|
|||||||||
|
|
|
扁平苔蘚
|
免疫學, 肝病學和 皮膚科
|
靜脈輸注
|
2019
|
≥ 2024/II
|
|||||||||
|
CSJ117
|
待定
|
抗胸腺基質淋巴生成素單抗片段
|
重度哮喘
|
呼吸性
|
吸入
|
2018
|
2023/II
|
||||||||
|
ECF843
|
待定
|
邊界潤滑劑
|
乾眼症
|
眼科
|
滴眼液
|
2017
|
2022/II
|
||||||||
|
Entresto
|
伐沙坦和薩舒比利(鈉鹽複合體)
|
血管緊張素受體/Neprilysin抑制劑
|
射血分數保留的慢性心力衰竭
|
心血管、腎臟和代謝
|
口頭的
|
2012
|
2020/III
|
||||||||
|
|
|
急性心肌梗死後
|
心血管、腎臟和代謝
|
口服
|
2015
|
2021/III
|
|||||||||
|
|
|||||||||||||||
|
1 在美國被批准為佐爾根斯馬治療脊髓性肌萎縮症(IV配方)
|
|||||||||||||||
|
2 根據一項小型臨牀前動物研究的結果,FDA已經部分臨牀擱置了AVXS-101用於脊髓性肌萎縮症患者的鞘內試驗。
|
|||||||||||||||
|
3 在美國被批准為皮克雷發送線路(+Fulvestrant)
|
|||||||||||||||
|
項目/ 產品 |
普普通通 名字 |
機理 行動中的 |
潛在適應症 |
業務 特許經營 |
配方/ 路線: 行政管理 |
年項目
vt.進入,進入 當前 發展 相位 |
計劃中的備案 日期/當前 相位 |
||||||||
|
INC280
|
卡馬替尼
|
C-MET抑制劑
|
非小細胞肺癌
|
腫瘤學
|
口頭的
|
2014
|
美國註冊
|
||||||||
|
|
|
實體瘤
|
腫瘤學
|
口頭的
|
2019
|
≥2024/II
|
|||||||||
|
雅卡維
|
魯索利替尼
|
JAK1/2抑制劑
|
acute graft—versus—host disease
|
腫瘤學
|
口頭的
|
2016
|
2021/III
|
||||||||
|
|
|
慢性移植物抗宿主病
|
腫瘤學
|
口頭的
|
2016
|
2021/III
|
|||||||||
|
KAE609
|
西帕加明
|
PfATP4抑制劑
|
瘧疾
|
既定藥物
|
口服
|
2012
|
≥ 2024/II
|
||||||||
|
|
|
嚴重瘧疾
|
既定藥物
|
口服
|
2019
|
≥ 2024/II
|
|||||||||
|
KAF156
|
加納普拉賽德
|
咪唑哌嗪 衍生物
|
瘧疾
|
既定藥物
|
口服
|
2014
|
≥ 2024/II
|
||||||||
|
基斯卡利
|
核糖核素
|
CDK4/6抑制劑
|
HR +/HER 2—乳腺癌(輔助治療)
|
腫瘤學
|
口頭的
|
2018
|
2022/III
|
||||||||
|
KJX839
|
inclisiran
|
小幹擾RNA(PCSK9)
|
高血脂
|
心血管、腎臟和代謝
|
皮下注射
|
2019
|
美國/歐盟 登記
|
||||||||
|
|
|
心血管的二級預防 水平升高患者發生的事件 的ldl—c
|
心血管、腎臟和代謝
|
皮下注射
|
2019
|
≥ 2024/III
|
|||||||||
|
金利亞
|
蒂桑—萊克盧塞爾
|
CD19靶向嵌合體 抗原受體t細胞 免疫治療
|
複發性/難治性濾泡性淋巴瘤
|
腫瘤學
|
靜脈輸注
|
2017
|
2021/II
|
||||||||
|
|
|
複發性/難治性瀰漫性大B細胞 淋巴瘤1ST舊病復發
|
腫瘤學
|
靜脈輸注
|
2018
|
2021/III
|
|||||||||
|
|
|
復發/難治性瀰漫性大B細胞淋巴瘤(+pembrolizumab)
|
腫瘤學
|
靜脈輸注
|
2017
|
≥ 2024/II
|
|||||||||
|
LAM320
|
氯法齊明
|
分枝桿菌 dna結合
|
耐多藥結核病
|
既定藥物
|
口服
|
2016
|
2021/III
|
||||||||
|
LJC242
|
tropifexor, cenicriviroc (in固定劑量複方製劑)
|
FXR激動劑, CCR2/5抑制劑
|
非酒精性脂肪肝炎
|
免疫學、肝病學和皮膚科
|
口頭的
|
2017
|
≥2024/II
|
||||||||
|
LJN452
|
託洛伊克索
|
FXR激動劑
|
非酒精性脂肪性肝炎
|
免疫學, 肝病學和 皮膚科
|
口服
|
2015
|
≥ 2024/II
|
||||||||
|
LMI070
|
布拉帕拉姆
|
SMN2RNA剪接調製器
|
脊髓性肌萎縮
|
神經科學
|
口服
|
2017
|
≥ 2024/II
|
||||||||
|
LNP023
|
TBD
|
B因子抑制物
|
IGA腎病
|
心血管、腎臟和代謝
|
口服
|
2018
|
2023/II
|
||||||||
|
|
|
C3腎小球病變
|
心血管、腎臟和代謝
|
口服
|
2018
|
2023/II
|
|||||||||
|
|
|
陣發性睡眠性血紅蛋白尿
|
心血管、腎臟和代謝
|
口服
|
2019
|
2023/II
|
|||||||||
|
|
|
膜性腎病
|
心血管、腎臟和代謝
|
口服
|
2018
|
≥ 2024/II
|
|||||||||
|
LOU064
|
TBD
|
BTK抑制劑
|
慢性自發性蕁麻疹
|
免疫學, 肝病學和 皮膚科
|
口服
|
2017
|
2023/II
|
||||||||
|
177Lu—PSMA—617
|
待定
|
靶向dna 破壞通過 β粒子 輻射
|
轉移性去勢抵抗性 前列腺癌
|
腫瘤學
|
靜脈輸注
|
2018
|
2020/III
|
||||||||
|
LXE408
|
TBD
|
動質體蛋白酶體抑制劑
|
內臟利什曼病
|
既定藥物
|
口服
|
2019
|
≥ 2024/II
|
||||||||
|
MBG453
|
待定
|
tim—3拮抗劑
|
骨髓增生異常綜合徵
|
腫瘤學
|
靜脈輸液
|
2018
|
2021/II
|
||||||||
|
|
|
急性髓性白血病
|
腫瘤學
|
靜脈輸液
|
2019
|
≥2024/II
|
|||||||||
|
OMB157
|
ofatumumab
|
抗CD20單克隆抗體 抗體
|
復發型多發性硬化
|
神經科學
|
皮下注射
|
2015
|
美國/歐盟註冊
|
||||||||
|
PDR001
|
斯帕他珠單抗
|
抗—pd—1單克隆 抗體
|
轉移性BRAF V600+黑色素瘤(w/ 塔芬拉爾 + 麥金主義者)
|
腫瘤學
|
靜脈輸注
|
2017
|
2020/III
|
||||||||
|
|
|
轉移性黑色素瘤(組合)
|
腫瘤學
|
靜脈輸液
|
2017
|
2023/II
|
|||||||||
|
QBW251
|
待定
|
CFTR型增強器
|
慢性阻塞性肺疾病
|
呼吸性
|
口頭的
|
2017
|
≥2024/II
|
||||||||
|
QGE031
|
利吉珠單抗
|
高親和力抗IgE 單克隆抗體
|
慢性自發性蕁麻疹/ 慢性特發性蕁麻疹
|
免疫學, 肝病學和 皮膚科
|
皮下注射
|
2017
|
2021/III
|
||||||||
|
QMF149
|
茚達特羅, 莫米鬆 糠酸 (in固定劑量 組合)
|
長效β2- 腎上腺素能激動劑和 吸入性皮質類固醇
|
哮喘
|
呼吸
|
吸入
|
2019
|
歐盟註冊
|
||||||||
|
項目/ 產品 |
普普通通 名字 |
機理 行動中的 |
潛在適應症 |
業務 特許經營 |
配方/ 路線: 行政管理 |
年項目
vt.進入,進入 當前 發展 相位 |
計劃中的備案 日期/當前 相位 |
||||||||
|
QVM149
|
吲哚卡特羅、呋喃莫米鬆、溴化吡咯銨(固定劑量組合)
|
長效β2-腎上腺素能激動劑、長效M受體拮抗劑和吸入性皮質類固醇
|
哮喘
|
呼吸性
|
吸入
|
2019
|
歐盟註冊
|
||||||||
|
RTH2 584
|
溴珠單抗
|
抗VEGF單鏈 抗體片段
|
新生血管性(濕性)年齡相關性黃斑 變性
|
眼科
|
玻璃體內注射
|
2019
|
美國批准的歐盟註冊
|
||||||||
|
|
|
糖尿病黃斑水腫
|
眼科
|
玻璃體內注射
|
2017
|
2021/III
|
|||||||||
|
|
|
視網膜靜脈阻塞
|
眼科
|
玻璃體內注射
|
2018
|
2023/III
|
|||||||||
|
|
|
增殖性糖尿病視網膜病變
|
眼科
|
玻璃體內注射
|
2019
|
2023/III
|
|||||||||
|
SAF312
|
待定
|
TRPV1拮抗劑
|
慢性眼表疼痛
|
眼科
|
局部
|
2019
|
≥2024/II
|
||||||||
|
SEG1015
|
crizanlizumab
|
P—選擇素抑制劑
|
鐮狀細胞病
|
腫瘤學
|
靜脈輸注
|
2019
|
美國批准的歐盟註冊
|
||||||||
|
TQJ230
|
TBD
|
抗apo(a)反義 寡核苷酸
|
心血管的二級預防 水平升高患者發生的事件 脂蛋白(a)
|
心血管, 腎臟和 代謝
|
皮下注射
|
2018
|
≥ 2024/III
|
||||||||
|
中國人844
|
TBD
|
減少 二硫鍵
|
老花眼
|
心血管、腎臟和代謝
|
滴眼液
|
2017
|
≥ 2024/II
|
||||||||
|
VAY736
|
亞納魯單抗
|
抗BAFF(B細胞— 活化因子) 單克隆抗體
|
自身免疫性肝炎
|
免疫學, 肝病學和 皮膚科
|
皮下注射
|
2016
|
≥ 2024/II
|
||||||||
|
|
|
原發性乾燥綜合徵
|
免疫學, 肝病學和 皮膚科
|
皮下注射
|
2015
|
≥ 2024/II
|
|||||||||
|
VPM087
|
TBD
|
白細胞介素—1 β 中和 單克隆抗體
|
結直腸癌,1ST腎細胞癌1例ST線
|
腫瘤學
|
靜脈輸注
|
2018
|
≥2024/I
|
||||||||
|
Xolair
|
omalizumab
|
抗ige單克隆 抗體
|
鼻息肉
|
呼吸
|
皮下注射
|
2017
|
美國/歐盟 登記
|
||||||||
|
|
|
食物過敏
|
呼吸性
|
皮下注射
|
2019
|
2021/III
|
|||||||||
|
ZPL389
|
阿德里福朗
|
組胺h4受體 拮抗劑
|
特應性皮炎
|
免疫學, 肝病學和 皮膚科
|
口服
|
2017
|
≥ 2024/II
|
||||||||
|
|
|||||||||||||||
|
4 在美國被批准為Beovu新生血管性(濕性)年齡相關性黃斑變性
|
|||||||||||||||
|
5 在美國被批准為阿達克維奧鐮狀細胞病
|
|||||||||||||||
|
項目/產品
|
潛在適應症
|
變化
|
事理
|
||||
|
ABL001
|
慢性髓系白血病,1例ST線
|
已刪除
|
開發中止
|
||||
|
AVXS-101
|
脊髓性肌萎縮症1型(IV製劑)
|
現已披露為脊髓性肌萎縮症(IV配方)
|
|
||||
|
脊髓性肌萎縮症2/3型(IT配方)
|
現已披露為脊髓性肌萎縮症(IT配方)
|
|
|||||
|
BAF312
|
繼發性進行性多發性硬化症
|
商業化為 梅曾特
|
|
||||
|
BYL719
|
激素受體陽性(HR+)/人表皮生長因子受體2陰性(HER2-)晚期乳腺癌(絕經後婦女),2發送線路(+Fulvestrant)
|
現已披露為PIK3CA突變激素受體陽性(HR+)/人表皮生長因子受體2陰性(HER2-)絕經後晚期乳腺癌,2發送線路(+Fulvestrant)
|
|
||||
|
PIK3CA相關過度生長譜
|
增列
|
進入驗證性開發階段
|
|||||
|
三陰性乳腺癌
|
增列
|
進入驗證性開發階段
|
|||||
|
激素受體陰性(HR-)/人表皮生長因子受體2陽性(HER2+)晚期乳腺癌
|
增列
|
進入驗證性開發階段
|
|||||
|
卵巢癌
|
增列
|
進入驗證性開發階段
|
|||||
|
頭頸部鱗狀細胞癌
|
增列
|
進入驗證性開發階段
|
|||||
|
CAD106
|
阿爾茨海默病
|
已刪除
|
開發中止
|
||||
|
CEE321
|
特應性皮炎
|
增列
|
進入驗證性開發階段
|
||||
|
CNP520
|
阿爾茨海默病
|
已刪除
|
開發中止
|
||||
|
科森提克斯
|
鉅細胞動脈炎
|
增列
|
進入驗證性開發階段
|
||||
|
扁平苔蘚
|
增列
|
進入驗證性開發階段
|
|||||
|
EMA401
|
外周神經性疼痛
|
已刪除
|
開發中止
|
||||
|
HDM201
|
急性髓細胞性淋巴瘤
|
已刪除
|
開發中止
|
||||
|
INC280
|
非小細胞肺癌(EGFR突變)
|
已刪除
|
開發中止
|
||||
|
實體瘤
|
增列
|
進入驗證性開發階段
|
|||||
|
KAE609
|
嚴重瘧疾
|
增列
|
進入驗證性開發階段
|
||||
|
KJX839
|
高血脂
|
添加
|
收購時, 藥品公司
|
||||
|
心血管事件的二級預防 在LDL—C水平升高的患者中,
|
添加
|
收購時, 藥品公司
|
|||||
|
金利亞
|
慢性淋巴細胞白血病
|
已刪除
|
開發中止
|
||||
|
LCI699
|
庫欣病
|
已刪除
|
剝離給Recordati S.p.A.
|
||||
|
LNP023
|
C3腎小球病變
|
增列
|
進入驗證性開發階段
|
||||
|
陣發性睡眠性血紅蛋白尿
|
增列
|
進入驗證性開發階段
|
|||||
|
盧森提斯
|
早產兒視網膜病變
|
商業化
|
|
||||
|
糖尿病視網膜病變
|
商業化
|
|
|||||
|
LXE408
|
內臟利什曼病
|
增列
|
進入驗證性開發階段
|
||||
|
MBG453
|
骨髓增生異常綜合徵
|
增列
|
進入驗證性開發階段
|
||||
|
急性髓性白血病
|
增列
|
進入驗證性開發階段
|
|||||
|
mor106
|
特應性皮炎
|
已刪除
|
開發中止
|
||||
|
PDR001
|
惡性黑色素瘤(組合)
|
現在公開為轉移性黑色素瘤(combination)
|
|
||||
|
普羅馬克塔/ 起義
|
重度再生障礙性貧血,1例ST線
|
已刪除
|
發展中斷
|
||||
|
QAW039
|
哮喘
|
已刪除
|
開發中止
|
||||
|
RTH2 58
|
新生血管性年齡相關黃斑變性
|
現公開為新生血管(濕)年齡相關 黃斑變性
|
|
||||
|
增殖性糖尿病視網膜病變
|
增列
|
進入驗證性開發階段
|
|||||
|
Rydapt
|
急性髓性白血病(FLT3野生型)
|
已刪除
|
開發中止
|
||||
|
SAF312
|
慢性眼表疼痛
|
增列
|
進入驗證性開發階段
|
||||
|
TQJ230
|
脂蛋白(A)升高患者心血管事件的二級預防
|
添加
|
進入驗證性開發階段
|
||||
|
VAY785
|
非酒精性脂肪性肝炎
|
已刪除
|
開發中止
|
||||
|
Xolair
|
食物過敏
|
增列
|
進入驗證性開發階段
|
||||
|
2019年第三方淨銷售額
|
|||||
|
數百萬美元
|
%
|
||||
|
美國
|
13 789
|
37
|
|||
|
歐洲
|
12 818
|
34
|
|||
|
亞洲、非洲、澳大拉西亞
|
8 458
|
22
|
|||
|
加拿大和拉丁美洲
|
2 649
|
7
|
|||
|
總計
|
37 714
|
100
|
|||
|
其中在成熟市場 *
|
28 573
|
76
|
|||
|
其中新興增長市場 *
|
9 141
|
24
|
|||
|
* 新興增長市場包括除美國、加拿大、西歐、日本、澳大利亞和新西蘭的成熟市場以外的所有市場。
|
|||||
桑多茲
|
產品
|
原研藥
|
描述
|
|||
|
阿莫西林/克拉維酸
|
提示:®
|
抗生素
|
|||
|
唑來膦酸
|
阿拉斯塔
|
骨質疏鬆症治療
|
|||
|
乙酰半胱氨酸
|
五花八門
|
粘液溶解劑
|
|||
|
芬太尼
|
五花八門
|
疼痛治療
|
|||
|
活性成分
|
描述
|
||
|
口服和無菌青黴素類藥物
|
抗感染藥
|
||
|
口服和無菌頭孢菌素
|
抗感染藥
|
||
|
克拉維酸及其與克拉維酸的混合物
|
β-內酰胺類抑制劑
|
||
|
經典紅黴素和半合成紅黴素
|
抗感染藥
|
||
|
|
|||
|
中間體
|
描述
|
||
|
各種頭孢菌素中間體
|
抗感染藥
|
||
|
紅黴素鹼基
|
抗感染藥
|
||
|
發酵產生的各種粗製化合物
|
環孢黴素、子囊黴素、雷帕黴素、黴酚酸等。
|
||
|
產品
|
原研藥
|
描述
|
|||
|
泛繩
|
吉諾託品®
|
重組人生長激素
|
|||
|
雙斜晶石和Epoetin Alfa十六進制
|
eprex®/Erypo®
|
用於治療貧血的重組蛋白
|
|||
|
Zarzio,Zarxio和非格司亭
|
Neupogen®
|
重組蛋白在腫瘤學中的應用
|
|||
|
格拉託帕
|
Copaxone®
|
多發性硬化症的治療
|
|||
|
埃雷齊 1
|
Enbrel®
|
治療多發性炎症性疾病
|
|||
|
裏克斯託
|
美羅華®
|
血癌和免疫性疾病的治療
|
|||
|
赫裏莫茲
|
Humira®
|
治療多發性炎症性疾病
|
|||
|
扎姆
|
Remicade®
|
胃腸病、風濕病和皮膚病的治療
|
|||
|
濟延索
|
紐拉斯塔®
|
減少化療引起的中性粒細胞減少的持續時間和化療引起的發熱中性粒細胞減少的發生率(慢性粒細胞白血病和骨髓增生異常綜合徵除外)
|
|||
|
1 2016年在美國獲得批准。在美國上市,等待與Amgen的訴訟最終解決,Amgen負責銷售Enbrel®。2019年8月9日,美國新澤西州地區法院做出了不利於桑多斯的裁決;桑多茲對裁決不服,並提出上訴。上訴法院聽證會定於2020年3月4日舉行。
|
|||||
|
項目/
產品 1 |
普普通通
名字 |
作用機制 |
潛在適應症/適應症 |
治療區域 |
路線:
行政管理 |
當前相 |
|||||||
|
GP2017
|
阿達木
|
腫瘤壞死因子-α抑制劑
|
關節炎(類風濕性關節炎,強直性關節炎 脊椎炎、銀屑病關節炎)、斑塊狀銀屑病 和其他(與發起人相同)
|
免疫學
|
皮下
|
歐盟:已批准美國:已批准2
|
|||||||
|
GP2411 3
|
denosumab
|
RANKL抑制劑
|
骨質疏鬆症,骨丟失,預防擴散到骨骼的癌症的骨併發症(適應症在美國和歐盟有所不同)
|
內分泌學, 神經病學
|
皮下
|
iii期
|
|||||||
|
EGI014A1 4
|
曲妥珠單抗
|
抗HER2單抗
|
乳腺和胃腫瘤
|
腫瘤學
|
靜脈
|
第三階段
|
|||||||
|
DST356A1 5
|
natalizumab
|
抗α4(α4)整合素單抗
|
緩解複發性多發性硬化症(RRMS)的單一療法;美國活動性克羅恩病的二線治療
|
神經病學, 免疫學(僅限美國)
|
靜脈
|
iii期
|
|||||||
|
1 La-EP2006(Pegfilgratim)在歐盟獲得批准並作為濟延索2018年11月,並於2019年11月在美國獲批並推出。
|
|||||||||||||
|
2 啟動時為赫裏莫茲2018年10月在歐盟。同樣在2018年10月,我們宣佈了一項全球解決方案,解決了與AbbVie有關阿達利單抗的所有知識產權訴訟。根據協議條款,AbbVie授予我們與Humira相關的AbbVie知識產權的非獨家許可®,從艾伯維擁有知識產權的某些國家/地區的某些日期開始。我們沒有資格發射赫裏莫茲在美國,直到2023年下半年。
|
|||||||||||||
|
3 與Hexal AG合作開發。
|
|||||||||||||
|
4 與EirGenix,Inc.合作開發
|
|||||||||||||
|
5 與PolPharma Biologics合作開發。
|
|||||||||||||
|
2019年第三方淨銷售額
|
|||||
|
數百萬美元
|
%
|
||||
|
歐洲
|
5 115
|
53
|
|||
|
美國
|
2 491
|
26
|
|||
|
亞洲、非洲、澳大拉西亞
|
1 341
|
14
|
|||
|
加拿大和拉丁美洲
|
784
|
7
|
|||
|
總計
|
9 731
|
100
|
|||
|
其中在成熟市場 *
|
7 111
|
73
|
|||
|
其中新興增長市場 *
|
2 620
|
27
|
|||
|
* 新興增長市場包括除美國、加拿大、西歐、日本、澳大利亞和新西蘭的成熟市場以外的所有市場。
|
|||||
4.C組織結構
4.D不動產、廠場和設備
|
位置 |
場地面積(單位:
平方米) |
主要活動 |
|||
|
瑞士巴塞爾--聖約翰
|
589 000
|
全球集團總部;全球創新藥物事業部總部;全球Sandoz事業部;研發;藥物物質和藥物中間體的生產
|
|||
|
昆德爾和沙夫特瑙,奧地利
|
480 000
|
生產生物技術產品、藥品和成品、抗感染藥, 活性原料藥、產品開發
|
|||
|
新澤西州東漢諾威
|
391 000
|
創新藥品事業部美國總部,研發
|
|||
|
巴萊本,德國
|
340 000
|
生產廣泛的仿製藥成品劑型
|
|||
|
馬薩諸塞州坎布里奇
|
205 000
|
研發
|
|||
|
上海,中國
|
106 500
|
研發
|
|||
|
盧布爾雅那,斯洛文尼亞
|
83 000
|
生產各種成品固體和無菌製劑
|
|||
|
印度海得拉巴
|
80 500
|
綜合行政和發展全球服務中心
|
|||
|
科羅拉多州朗蒙特
|
65 032
|
AveXis的生產、倉庫和行政辦公室
|
|||
|
斯坦因,瑞士
|
64 700
|
生產無菌小瓶、預充注射器和安瓿;吸入膠囊, 片劑和透皮製劑;活性藥物成分,細胞和基因療法
|
|||
|
德國霍爾茲基興
|
64 200
|
全球山德士事業部總部,生產口服膜,透皮給藥系統, 基質貼片,產品開發
|
|||
|
蒙格斯,斯洛文尼亞
|
62 400
|
藥物和藥物中間體的生產
|
|||
|
斯特里科夫,波蘭
|
45 000
|
生產各種散裝口服固體劑型和包裝
|
|||
|
胡寧格,法國
|
35 000
|
臨牀和商業用藥品的生產
|
|||
|
新加坡
|
35 000
|
創新藥物固體和生物製品的生產
|
|||
|
巴貝拉,西班牙
|
33 000
|
片劑、膠囊劑和吸入劑產品的生產
|
|||
|
瑞士巴塞爾—Schweizerhalle
|
31 700
|
藥物和藥物中間體的生產
|
|||
|
2、魯伊爾-馬爾邁森,法國
|
29 500
|
創新藥物管理辦公室
|
|||
|
普爾斯,比利時
|
27 500
|
創新藥物眼科產品的生產
|
|||
|
日本東京
|
20 000
|
創新藥品和山德士行政辦公室
|
|||
|
新澤西州莫里斯平原
|
15 600
|
創新藥物生產部門細胞和基因療法
|
|||
|
新澤西州普林斯頓
|
14 300
|
山德士分部美國總部
|
|||
|
利伯蒂維爾
|
9 800
|
AveXis的生產、倉庫和行政辦公室
|
|||
|
羅馬尼亞塔爾古穆列什
|
9 070
|
創新藥物和Sandoz固體的生產
|
|||
|
Les Ulis,法國
|
5 920
|
創新藥物生產部門細胞和基因療法
|
|||
|
米爾本
|
1 400
|
AAA放射性配體治療的主要生產地點
|
|||
|
Colleretto Giacosa/Ivrea,意大利
|
1 200
|
AAA放射性配體治療的主要生產地點
|
|||
項目4A. 未解決的工作人員意見
項目5.業務和財務回顧及展望
5.A經營業績
|
(除非另有説明,否則為百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % 2 |
|||||
|
持續運營對第三方的淨銷售額
|
47 445
|
44 751
|
6
|
9
|
|||||
|
對停產業務的銷售
|
53
|
82
|
– 35
|
– 31
|
|||||
|
持續經營的淨銷售額
|
47 498
|
44 833
|
6
|
9
|
|||||
|
其他收入
|
1 179
|
1 266
|
– 7
|
– 7
|
|||||
|
銷貨成本
|
– 14 425
|
– 14 510
|
1
|
– 2
|
|||||
|
持續經營毛利
|
34 252
|
31 589
|
8
|
12
|
|||||
|
銷售、一般和行政管理
|
– 14 369
|
– 13 717
|
– 5
|
– 8
|
|||||
|
研發
|
– 9 402
|
– 8 489
|
– 11
|
– 13
|
|||||
|
其他收入
|
2 031
|
1 629
|
25
|
27
|
|||||
|
其他費用
|
– 3 426
|
– 2 609
|
– 31
|
– 33
|
|||||
|
持續經營的營業收入
|
9 086
|
8 403
|
8
|
14
|
|||||
|
淨銷售額回報率(%)
|
19.2
|
18.8
|
|
|
|||||
|
來自相聯公司的收入
|
659
|
6 438
|
NM
|
NM
|
|||||
|
利息支出
|
– 850
|
– 932
|
9
|
8
|
|||||
|
其他財務收支
|
45
|
186
|
– 76
|
– 69
|
|||||
|
持續經營的税前收入
|
8 940
|
14 095
|
– 37
|
– 33
|
|||||
|
税費
|
– 1 793
|
– 1 295
|
– 38
|
– 46
|
|||||
|
持續經營淨收益
|
7 147
|
12 800
|
– 44
|
– 41
|
|||||
|
停止經營的淨虧損扣除分配給諾華製藥股東的收益前的淨虧損
|
– 101
|
– 186
|
NM
|
NM
|
|||||
|
愛爾康公司向諾華製藥股東分派的收益
|
4 691
|
|
|
|
|||||
|
非持續經營的淨收益/(虧損)
|
4 590
|
– 186
|
NM
|
NM
|
|||||
|
淨收入
|
11 737
|
12 614
|
– 7
|
– 3
|
|||||
|
歸因於:
|
|
|
|
|
|||||
|
諾華製藥的股東
|
11 732
|
12 611
|
– 7
|
– 3
|
|||||
|
非控制性權益
|
5
|
3
|
NM
|
NM
|
|||||
|
持續經營基本每股收益(美元)
|
3.12
|
5.52
|
– 43
|
– 40
|
|||||
|
非持續經營的基本每股收益(美元)
|
2.00
|
– 0.08
|
NM
|
NM
|
|||||
|
每股基本收益合計(美元)
|
5.12
|
5.44
|
– 6
|
– 2
|
|||||
|
來自持續經營的經營活動現金流量淨額
|
13 547
|
13 049
|
4
|
|
|||||
|
持續運營的自由現金流 2
|
12 937
|
11 256
|
15
|
|
|||||
|
1 持續經營業務包括創新藥品及Sandoz部門的業務,持續經營業務及已終止經營業務包括Alcon眼科護理設備業務及分拆前Alcon業務應佔的若干企業業務、Alcon Inc.的分銷收益。2019年向諾華公司股東支付的費用以及與分配有關的其他費用。見"項目18。財務報表—注1。重要會計原則",第18項財務報表—附註2。重大交易—二零一九年重大交易”及“第18項財務報表—附註30。停止運營”。
|
|||||||||
|
2 關於非IFRS計量和對賬表的解釋,請參見"項目5.A經營成果—Novartis定義的非IFRS計量。”
|
|||||||||
|
NM=沒有意義
|
|||||||||
|
(百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
創新藥物
|
37 714
|
34 892
|
8
|
11
|
|||||
|
桑多茲
|
9 731
|
9 859
|
– 1
|
2
|
|||||
|
持續運營對第三方的淨銷售額
|
47 445
|
44 751
|
6
|
9
|
|||||
|
(百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
諾華腫瘤業務部門合計
|
14 370
|
13 428
|
7
|
10
|
|||||
|
諾華製藥業務部門合計
|
23 344
|
21 464
|
9
|
12
|
|||||
|
眼科
|
4 776
|
4 558
|
5
|
8
|
|||||
|
免疫學、肝病學和皮膚病學
|
4 222
|
3 392
|
24
|
27
|
|||||
|
神經科學
|
3 773
|
3 429
|
10
|
13
|
|||||
|
呼吸性
|
1 825
|
1 767
|
3
|
9
|
|||||
|
心血管、腎臟和代謝
|
1 750
|
1 050
|
67
|
70
|
|||||
|
已建立的藥物
|
6 998
|
7 268
|
– 4
|
0
|
|||||
|
創新藥物總量
|
37 714
|
34 892
|
8
|
11
|
|||||
|
|
|||||||||
|
|
|||||||||
|
|
|
我們
|
世界其他地區
|
總計
|
|||||||||||||||||
|
品牌 |
商業特許經營權 |
指示 |
百萬美元 |
%
變化 美元/cc 2 |
百萬美元 |
%
變化 美元 |
%
變化 抄送 2 |
百萬美元 |
%
變化 美元 |
%
變化 抄送 2 |
|||||||||||
|
科森提克斯
|
免疫學, 肝病和皮膚病學
|
銀屑病,強直性脊柱炎 脊柱炎和 銀屑病關節炎
|
2 220
|
33
|
1 331
|
14
|
20
|
3 551
|
25
|
28
|
|||||||||||
|
吉倫亞
|
神經科學
|
複發性多發性硬化症
|
1 736
|
– 2
|
1 487
|
– 6
|
0
|
3 223
|
– 4
|
– 1
|
|||||||||||
|
盧森提斯
|
眼科
|
老年性黃斑變性
|
|
|
2 086
|
2
|
7
|
2 086
|
2
|
7
|
|||||||||||
|
塔西尼亞
|
腫瘤學
|
慢性髓系白血病
|
804
|
0
|
1 076
|
1
|
5
|
1 880
|
0
|
3
|
|||||||||||
|
Entresto
|
心血管,腎臟 和代謝
|
慢性心力衰竭
|
925
|
66
|
801
|
70
|
77
|
1 726
|
68
|
71
|
|||||||||||
|
善得定
|
腫瘤學
|
類癌和肢端肥大症
|
881
|
8
|
704
|
– 9
|
– 3
|
1 585
|
0
|
2
|
|||||||||||
|
Afinator/Votubia
|
腫瘤學
|
乳腺癌/TSC
|
1 003
|
8
|
536
|
– 15
|
– 10
|
1 539
|
– 1
|
1
|
|||||||||||
|
Promacta/Revolade
|
腫瘤學
|
免疫性血小板減少症 (ITP)嚴重再生障礙 貧血(SAA)
|
691
|
19
|
725
|
22
|
27
|
1 416
|
21
|
23
|
|||||||||||
|
塔芬拉爾 + 麥金主義者
|
腫瘤學
|
BRAF V600+轉移性和佐劑性黑色素瘤;晚期非小細胞肺癌
|
481
|
5
|
857
|
23
|
30
|
1 338
|
16
|
20
|
|||||||||||
|
加爾沃斯集團化
|
已建立的藥物
|
糖尿病
|
|
|
1 297
|
1
|
5
|
1 297
|
1
|
5
|
|||||||||||
|
Gleevec/Glivec
|
腫瘤學
|
慢性粒細胞 白血病和GIST
|
334
|
– 24
|
929
|
– 17
|
– 14
|
1 263
|
– 19
|
– 17
|
|||||||||||
|
Xolair 1
|
呼吸性
|
重度過敏性哮喘 (SAA)和慢性 自發性蕁麻疹 (CSU)
|
|
|
1 173
|
13
|
19
|
1 173
|
13
|
19
|
|||||||||||
|
雅卡維
|
腫瘤學
|
骨髓纖維化(MF), 單純性紅細胞增多症
|
|
|
1 114
|
14
|
20
|
1 114
|
14
|
20
|
|||||||||||
|
Diovan集團化
|
已建立的藥物
|
高血壓
|
86
|
2
|
978
|
4
|
10
|
1 064
|
4
|
9
|
|||||||||||
|
Exforge集團化
|
已建立的藥物
|
高血壓
|
13
|
– 32
|
1 012
|
3
|
8
|
1 025
|
2
|
7
|
|||||||||||
|
Exjade/Jadeu
|
腫瘤學
|
慢性鐵超負荷
|
450
|
– 14
|
525
|
– 9
|
– 6
|
975
|
– 11
|
– 9
|
|||||||||||
|
Votrient
|
腫瘤學
|
腎細胞癌
|
332
|
– 18
|
423
|
0
|
5
|
755
|
– 9
|
– 6
|
|||||||||||
|
伊拉里斯
|
免疫學, 肝病和皮膚病學
|
自身炎症(CAPS, 陷阱,HIDS/MKD,FMF,SJIA, AOSD和痛風)
|
304
|
16
|
367
|
26
|
33
|
671
|
21
|
25
|
|||||||||||
|
佐瑞斯/認證
|
已建立的藥物
|
移植
|
169
|
17
|
316
|
– 1
|
4
|
485
|
5
|
8
|
|||||||||||
|
基斯卡利
|
腫瘤學
|
HR +/HER2—轉移性乳腺癌
|
250
|
45
|
230
|
NM
|
NM
|
480
|
104
|
111
|
|||||||||||
|
前20名產品合計
|
|
|
10 679
|
11
|
17 967
|
5
|
11
|
28 646
|
7
|
11
|
|||||||||||
|
投資組合的其餘部分
|
|
|
3 110
|
39
|
5 958
|
– 1
|
4
|
9 068
|
10
|
13
|
|||||||||||
|
部門銷售總額
|
|
|
13 789
|
16
|
23 925
|
4
|
9
|
37 714
|
8
|
11
|
|||||||||||
|
1 淨銷售額反映Xolair所有適應症的銷售額。
|
|||||||||||||||||||||
|
2 不變貨幣(Cc)是非《國際財務報告準則》的衡量標準。關於非國際財務報告準則計量的解釋,見“--項目5.a經營成果--諾華公司定義的非國際財務報告準則計量”。
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||
|
(百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
零售業泛型1
|
7 590
|
7 880
|
– 4
|
0
|
|||||
|
生物製藥
|
1 607
|
1 436
|
12
|
16
|
|||||
|
抗腫瘤藥(合作伙伴標籤/API)
|
534
|
543
|
– 2
|
2
|
|||||
|
Sandoz共計
|
9 731
|
9 859
|
– 1
|
2
|
|||||
|
|
|||||||||
|
1 其中7.84億美元(2018年:8.26億美元)代表以Sandoz名義銷售的抗感染藥物
|
|||||||||
|
(百萬美元) |
截至的年度 2019年12月31日 |
的百分比 淨銷售額 |
截至的年度 2018年12月31日 |
的百分比 淨銷售額 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||||
|
創新藥物
|
9 287
|
24.6
|
7 871
|
22.6
|
18
|
24
|
|||||||
|
桑多茲
|
551
|
5.7
|
1 332
|
13.5
|
– 59
|
– 53
|
|||||||
|
公司
|
– 752
|
|
– 800
|
|
6
|
4
|
|||||||
|
持續經營的營業收入
|
9 086
|
19.2
|
8 403
|
18.8
|
8
|
14
|
|||||||
|
|
|||||||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
持續經營的核心毛利
|
37 392
|
34 886
|
7
|
10
|
|||||
|
銷售、一般和行政管理
|
– 14 319
|
– 13 690
|
– 5
|
– 7
|
|||||
|
研發
|
– 8 386
|
– 8 154
|
– 3
|
– 5
|
|||||
|
其他收入
|
495
|
558
|
– 11
|
– 9
|
|||||
|
其他費用
|
– 1 070
|
– 1 043
|
– 3
|
– 5
|
|||||
|
持續運營的核心運營收入
|
14 112
|
12 557
|
12
|
17
|
|||||
|
佔淨銷售額的百分比
|
29.7
|
28.1
|
|
|
|||||
|
1 關於非IFRS計量和對賬表的解釋,請參見"項目5.A經營成果—Novartis定義的非IFRS計量。”
|
|||||||||
|
(百萬美元) |
截至的年度 2019年12月31日 |
的百分比 淨銷售額 |
截至的年度 2018年12月31日 |
的百分比 淨銷售額 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||||
|
創新藥物
|
12 650
|
33.5
|
11 151
|
32.0
|
13
|
18
|
|||||||
|
桑多茲
|
2 094
|
21.5
|
2 002
|
20.3
|
5
|
10
|
|||||||
|
公司
|
– 632
|
|
– 596
|
|
– 6
|
– 9
|
|||||||
|
持續運營的核心運營收入
|
14 112
|
29.7
|
12 557
|
28.1
|
12
|
17
|
|||||||
|
|
|||||||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
研究和探索性開發
|
– 2 855
|
– 2 770
|
– 3
|
– 4
|
|||||
|
驗證性發展
|
– 5 297
|
– 4 905
|
– 8
|
– 10
|
|||||
|
創新藥物司研發費用共計
|
– 8 152
|
– 7 675
|
– 6
|
– 8
|
|||||
|
創新藥物淨銷售額佔第三方的百分比
|
21.6
|
22.0
|
|
|
|||||
|
核心研究和探索性開發1
|
– 2 706
|
– 2 665
|
– 2
|
– 2
|
|||||
|
核心驗證性發展1
|
– 4 879
|
– 4 675
|
– 4
|
– 6
|
|||||
|
核心創新藥物司研發費用共計
|
– 7 585
|
– 7 340
|
– 3
|
– 5
|
|||||
|
創新藥物淨銷售額佔第三方的百分比
|
20.1
|
21.0
|
|
|
|||||
|
1 核心不包括減值、攤銷及若干其他項目。關於非IFRS計量和對賬表的解釋,請參見"—項目5.A經營成果—諾華定義的非IFRS計量。”
|
|||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
持續經營的營業收入
|
9 086
|
8 403
|
8
|
14
|
|||||
|
來自相聯公司的收入
|
659
|
6 438
|
NM
|
NM
|
|||||
|
利息支出
|
– 850
|
– 932
|
9
|
8
|
|||||
|
其他財務收支
|
45
|
186
|
– 76
|
– 69
|
|||||
|
持續經營的税前收入
|
8 940
|
14 095
|
– 37
|
– 33
|
|||||
|
税費
|
– 1 793
|
– 1 295
|
– 38
|
– 46
|
|||||
|
持續經營淨收益
|
7 147
|
12 800
|
– 44
|
– 41
|
|||||
|
停止經營的淨虧損扣除分配給諾華製藥股東的收益前的淨虧損
|
– 101
|
– 186
|
NM
|
NM
|
|||||
|
愛爾康公司向諾華製藥股東分派的收益
|
4 691
|
|
|
|
|||||
|
非持續經營業務的淨收益
|
4 590
|
– 186
|
NM
|
NM
|
|||||
|
淨收入
|
11 737
|
12 614
|
– 7
|
– 3
|
|||||
|
歸因於:
|
|
|
|
|
|||||
|
諾華製藥的股東
|
11 732
|
12 611
|
– 7
|
– 3
|
|||||
|
非控制性權益
|
5
|
3
|
NM
|
NM
|
|||||
|
持續經營基本每股收益(美元)
|
3.12
|
5.52
|
– 43
|
– 40
|
|||||
|
非持續經營的基本每股收益(美元)
|
2.00
|
– 0.08
|
NM
|
NM
|
|||||
|
每股基本收益合計(美元)
|
5.12
|
5.44
|
– 6
|
– 2
|
|||||
|
|
|||||||||
|
NM=沒有意義
|
|||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2019年12月31日 |
截至的年度 2018年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
持續運營的核心運營收入
|
14 112
|
12 557
|
12
|
17
|
|||||
|
聯營公司的核心收入
|
1 086
|
1 113
|
– 2
|
– 2
|
|||||
|
核心利息支出
|
– 850
|
– 932
|
9
|
8
|
|||||
|
核心其他財務收入和支出
|
56
|
186
|
– 70
|
– 63
|
|||||
|
持續經營的核心税前收入
|
14 404
|
12 924
|
11
|
16
|
|||||
|
核心税種
|
– 2 300
|
– 2 004
|
– 15
|
– 19
|
|||||
|
持續運營的核心淨收入
|
12 104
|
10 920
|
11
|
15
|
|||||
|
持續運營的核心基本每股收益(美元)
|
5.28
|
4.71
|
12
|
17
|
|||||
|
1 關於非IFRS計量和對賬表的解釋,請參見"項目5.A經營成果—Novartis定義的非IFRS計量。”
|
|||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % 2 |
|||||
|
持續運營對第三方的淨銷售額
|
44 751
|
42 338
|
6
|
5
|
|||||
|
對停產業務的銷售
|
82
|
43
|
91
|
76
|
|||||
|
持續經營的淨銷售額
|
44 833
|
42 381
|
6
|
5
|
|||||
|
其他收入
|
1 266
|
1 023
|
24
|
24
|
|||||
|
銷貨成本
|
– 14 510
|
– 13 633
|
– 6
|
– 5
|
|||||
|
持續經營毛利
|
31 589
|
29 771
|
6
|
6
|
|||||
|
銷售、一般和行政管理
|
– 13 717
|
– 12 465
|
– 10
|
– 9
|
|||||
|
研發
|
– 8 489
|
– 8 389
|
– 1
|
0
|
|||||
|
其他收入
|
1 629
|
1 922
|
– 15
|
– 16
|
|||||
|
其他費用
|
– 2 609
|
– 2 137
|
– 22
|
– 21
|
|||||
|
持續經營的營業收入
|
8 403
|
8 702
|
– 3
|
– 3
|
|||||
|
淨銷售額回報率(%)
|
18.8
|
20.6
|
|
|
|||||
|
來自相聯公司的收入
|
6 438
|
1 108
|
NM
|
NM
|
|||||
|
利息支出
|
– 932
|
– 750
|
– 24
|
– 27
|
|||||
|
其他財務收支
|
186
|
42
|
NM
|
NM
|
|||||
|
持續經營的税前收入
|
14 095
|
9 102
|
55
|
55
|
|||||
|
税費
|
– 1 295
|
– 1 603
|
19
|
19
|
|||||
|
持續經營淨收益
|
12 800
|
7 499
|
71
|
71
|
|||||
|
淨(虧損)/非持續經營收入
|
– 186
|
204
|
NM
|
NM
|
|||||
|
淨收入
|
12 614
|
7 703
|
64
|
64
|
|||||
|
歸因於:
|
|
|
|
|
|||||
|
諾華製藥的股東
|
12 611
|
7 703
|
64
|
64
|
|||||
|
非控制性權益
|
3
|
0
|
NM
|
NM
|
|||||
|
持續經營基本每股收益(美元)
|
5.52
|
3.20
|
73
|
73
|
|||||
|
非持續經營的基本每股收益(美元)
|
– 0.08
|
0.08
|
NM
|
NM
|
|||||
|
每股基本收益合計(美元)
|
5.44
|
3.28
|
66
|
66
|
|||||
|
來自持續經營的經營活動現金流量淨額
|
13 049
|
11 419
|
14
|
|
|||||
|
持續運營的自由現金流 2
|
11 256
|
9 791
|
15
|
|
|||||
|
1 持續經營業務包括創新藥品及Sandoz部門的業務,而持續經營業務及已終止經營業務包括Alcon眼科護理設備業務及分拆前Alcon業務應佔的若干企業業務,以及與分銷有關的若干其他開支。見"項目18。財務報表—注1。重要會計原則",第18項財務報表—附註2。重大交易—二零一九年重大交易”及“第18項財務報表—附註30。停止運營”。
|
|||||||||
|
2 關於非IFRS計量和對賬表的解釋,請參見"項目5.A經營成果—Novartis定義的非IFRS計量。”
|
|||||||||
|
NM=沒有意義
|
|||||||||
|
(百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
創新藥物
|
34 892
|
32 278
|
8
|
8
|
|||||
|
桑多茲
|
9 859
|
10 060
|
– 2
|
– 3
|
|||||
|
持續運營對第三方的淨銷售額
|
44 751
|
42 338
|
6
|
5
|
|||||
|
|
|||||||||
|
|
|||||||||
|
(百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
諾華腫瘤業務部門合計
|
13 428
|
12 274
|
9
|
9
|
|||||
|
諾華製藥業務部門合計
|
21 464
|
20 004
|
7
|
7
|
|||||
|
眼科
|
4 558
|
4 621
|
– 1
|
– 2
|
|||||
|
神經科學
|
3 429
|
3 287
|
4
|
4
|
|||||
|
免疫學、肝病學和皮膚病學
|
3 392
|
2 474
|
37
|
37
|
|||||
|
呼吸性
|
1 767
|
1 617
|
9
|
8
|
|||||
|
心血管、腎臟和代謝
|
1 050
|
524
|
100
|
100
|
|||||
|
已建立的藥物
|
7 268
|
7 481
|
– 3
|
– 3
|
|||||
|
創新藥物總量
|
34 892
|
32 278
|
8
|
8
|
|||||
|
|
|||||||||
|
|
|||||||||
|
|
|
我們
|
世界其他地區
|
總計
|
|||||||||||||||||
|
品牌 |
商業特許經營權 |
指示 |
百萬美元 |
%
變化 美元/cc 2 |
百萬美元 |
%
變化 美元 |
%
變化 抄送 2 |
百萬美元 |
%
變化 美元 |
%
變化 抄送 2 |
|||||||||||
|
吉倫亞
|
神經科學
|
複發性多發性硬化症
|
1 765
|
3
|
1 576
|
7
|
5
|
3 341
|
5
|
4
|
|||||||||||
|
科森提克斯
|
免疫學、肝病學和皮膚科
|
銀屑病,強直性脊柱炎 脊柱炎和 銀屑病關節炎
|
1 674
|
31
|
1 163
|
46
|
44
|
2 837
|
37
|
36
|
|||||||||||
|
盧森提斯
|
眼科
|
老年性黃斑變性
|
|
|
2 046
|
8
|
7
|
2 046
|
8
|
7
|
|||||||||||
|
塔西尼亞
|
腫瘤學
|
慢性髓系白血病
|
806
|
0
|
1 068
|
4
|
3
|
1 874
|
2
|
1
|
|||||||||||
|
善得定
|
腫瘤學
|
類癌和肢端肥大症
|
817
|
– 2
|
770
|
– 1
|
– 1
|
1 587
|
– 2
|
– 2
|
|||||||||||
|
Gleevec/Glivec
|
腫瘤學
|
慢性粒細胞白血病與GIST
|
440
|
– 30
|
1 121
|
– 15
|
– 16
|
1 561
|
– 20
|
– 20
|
|||||||||||
|
Afinator/Votubia
|
腫瘤學
|
乳腺癌/TSC
|
929
|
13
|
627
|
– 11
|
– 12
|
1 556
|
2
|
2
|
|||||||||||
|
加爾沃斯集團化
|
已建立的藥物
|
糖尿病
|
|
|
1 284
|
4
|
6
|
1 284
|
4
|
6
|
|||||||||||
|
Promacta/Revolade
|
腫瘤學
|
免疫性血小板減少症 (ITP)嚴重再生障礙 貧血(SAA)
|
581
|
30
|
593
|
41
|
40
|
1 174
|
35
|
35
|
|||||||||||
|
塔芬拉爾 + 麥金主義者
|
腫瘤學
|
BRAF V600+轉移性和佐劑性黑色素瘤;晚期非小細胞肺癌
|
457
|
35
|
698
|
31
|
29
|
1 155
|
32
|
31
|
|||||||||||
|
Exjade/Jadeu
|
腫瘤學
|
慢性鐵超負荷
|
521
|
1
|
578
|
6
|
5
|
1 099
|
4
|
3
|
|||||||||||
|
Xolair 1
|
呼吸性
|
重度過敏性哮喘 (SAA)和慢性 自發性蕁麻疹 (CSU)
|
|
|
1 039
|
13
|
12
|
1 039
|
13
|
12
|
|||||||||||
|
Entresto
|
心血管,腎臟 和代謝
|
慢性心力衰竭
|
556
|
87
|
472
|
125
|
124
|
1 028
|
103
|
102
|
|||||||||||
|
Diovan集團化
|
已建立的藥物
|
高血壓
|
84
|
– 3
|
939
|
8
|
8
|
1 023
|
7
|
7
|
|||||||||||
|
Exforge集團化
|
已建立的藥物
|
高血壓
|
19
|
– 32
|
983
|
5
|
5
|
1 002
|
4
|
4
|
|||||||||||
|
雅卡維
|
腫瘤學
|
骨髓纖維化(MF), 單純性紅細胞增多症
|
|
|
977
|
26
|
24
|
977
|
26
|
24
|
|||||||||||
|
Votrient
|
腫瘤學
|
腎細胞癌
|
404
|
– 1
|
424
|
6
|
5
|
828
|
2
|
2
|
|||||||||||
|
伊拉里斯
|
免疫學、肝病學和皮膚科
|
自身炎症(CAPS、TRAPS、HIDS/MKD、FMF、SJIA、AOSD和痛風)
|
262
|
34
|
292
|
42
|
44
|
554
|
38
|
39
|
|||||||||||
|
曲伏前列素組
|
眼科
|
降低升高的 眼壓
|
194
|
– 10
|
323
|
– 13
|
– 13
|
517
|
– 12
|
– 12
|
|||||||||||
|
佐瑞斯/認證
|
已建立的藥物
|
移植
|
145
|
12
|
319
|
12
|
12
|
464
|
12
|
12
|
|||||||||||
|
前20名產品合計
|
|
|
9 654
|
11
|
17 292
|
10
|
9
|
26 946
|
10
|
10
|
|||||||||||
|
投資組合的其餘部分
|
|
|
2 210
|
4
|
5 736
|
0
|
0
|
7 946
|
1
|
1
|
|||||||||||
|
部門銷售總額
|
|
|
11 864
|
9
|
23 028
|
8
|
7
|
34 892
|
8
|
8
|
|||||||||||
|
1 淨銷售額反映Xolair所有適應症的銷售額。
|
|||||||||||||||||||||
|
2 不變貨幣(Cc)是非《國際財務報告準則》的衡量標準。關於非國際財務報告準則計量的解釋,見“--項目5.a經營成果--諾華公司定義的非國際財務報告準則計量”。
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||
|
(百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
零售業泛型1
|
7 880
|
8 409
|
– 6
|
– 7
|
|||||
|
生物製藥
|
1 436
|
1 135
|
27
|
24
|
|||||
|
抗腫瘤藥(合作伙伴標籤/API)
|
543
|
516
|
5
|
3
|
|||||
|
Sandoz共計
|
9 859
|
10 060
|
– 2
|
– 3
|
|||||
|
|
|||||||||
|
1 其中8.26億美元(2017年:8.8億美元)是以山德士名義銷售的抗感染藥物
|
|||||||||
|
(百萬美元) |
截至的年度 2018年12月31日 |
的百分比 淨銷售額 |
截至的年度 2017年12月31日 |
的百分比 淨銷售額 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||||
|
創新藥物
|
7 871
|
22.6
|
7 595
|
23.5
|
4
|
4
|
|||||||
|
桑多茲
|
1 332
|
13.5
|
1 368
|
13.6
|
– 3
|
– 2
|
|||||||
|
公司
|
– 800
|
|
– 261
|
|
NM
|
NM
|
|||||||
|
持續經營的營業收入
|
8 403
|
18.8
|
8 702
|
20.6
|
– 3
|
– 3
|
|||||||
|
NM=沒有意義
|
|||||||||||||
|
|
|||||||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
持續經營的核心毛利
|
34 886
|
32 374
|
8
|
7
|
|||||
|
銷售、一般和行政管理
|
– 13 690
|
– 12 468
|
– 10
|
– 9
|
|||||
|
研發
|
– 8 154
|
– 7 808
|
– 4
|
– 4
|
|||||
|
其他收入
|
558
|
748
|
– 25
|
– 26
|
|||||
|
其他費用
|
– 1 043
|
– 1 132
|
8
|
9
|
|||||
|
持續運營的核心運營收入
|
12 557
|
11 714
|
7
|
7
|
|||||
|
佔淨銷售額的百分比
|
28.1
|
27.7
|
|
|
|||||
|
1 關於非IFRS計量和對賬表的解釋,請參見"項目5.A經營成果—Novartis定義的非IFRS計量。”
|
|||||||||
|
(百萬美元) |
截至的年度 2018年12月31日 |
的百分比 淨銷售額 |
截至的年度 2017年12月31日 |
的百分比 淨銷售額 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||||
|
創新藥物
|
11 151
|
32.0
|
10 019
|
31.0
|
11
|
11
|
|||||||
|
桑多茲
|
2 002
|
20.3
|
2 080
|
20.7
|
– 4
|
– 3
|
|||||||
|
公司
|
– 596
|
|
– 385
|
|
– 55
|
– 52
|
|||||||
|
持續運營的核心運營收入
|
12 557
|
28.1
|
11 714
|
27.7
|
7
|
7
|
|||||||
|
|
|||||||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
研究和探索性開發
|
– 2 770
|
– 2 729
|
– 2
|
– 1
|
|||||
|
驗證性發展
|
– 4 905
|
– 4 886
|
0
|
0
|
|||||
|
創新藥物司研發費用共計
|
– 7 675
|
– 7 615
|
– 1
|
0
|
|||||
|
創新藥物淨銷售額佔第三方的百分比
|
22.0
|
23.6
|
|
|
|||||
|
核心研究和探索性開發1
|
– 2 665
|
– 2 603
|
– 2
|
– 2
|
|||||
|
核心驗證性發展1
|
– 4 675
|
– 4 431
|
– 6
|
– 5
|
|||||
|
核心創新藥物司研發費用共計
|
– 7 340
|
– 7 034
|
– 4
|
– 4
|
|||||
|
創新藥物淨銷售額佔第三方的百分比
|
21.0
|
21.8
|
|
|
|||||
|
|
|||||||||
|
1 核心不包括減值、攤銷及若干其他項目。關於非IFRS計量和對賬表的解釋,請參見"—項目5.A經營成果—諾華定義的非IFRS計量。”
|
|||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
持續經營的營業收入
|
8 403
|
8 702
|
– 3
|
– 3
|
|||||
|
來自相聯公司的收入
|
6 438
|
1 108
|
NM
|
NM
|
|||||
|
利息支出
|
– 932
|
– 750
|
– 24
|
– 27
|
|||||
|
其他財務收支
|
186
|
42
|
NM
|
NM
|
|||||
|
税前收入
|
14 095
|
9 102
|
55
|
55
|
|||||
|
税費
|
– 1 295
|
– 1 603
|
19
|
19
|
|||||
|
持續經營淨收益
|
12 800
|
7 499
|
71
|
71
|
|||||
|
淨(虧損)/非持續經營收入
|
– 186
|
204
|
NM
|
NM
|
|||||
|
淨收入
|
12 614
|
7 703
|
64
|
64
|
|||||
|
歸因於:
|
|
|
|
|
|||||
|
諾華製藥的股東
|
12 611
|
7 703
|
64
|
64
|
|||||
|
非控制性權益
|
3
|
0
|
NM
|
NM
|
|||||
|
持續經營基本每股收益(美元)
|
5.52
|
3.20
|
73
|
73
|
|||||
|
非持續經營的基本每股收益(美元)
|
– 0.08
|
0.08
|
NM
|
NM
|
|||||
|
每股基本收益合計(美元)
|
5.44
|
3.28
|
66
|
66
|
|||||
|
|
|||||||||
|
NM=沒有意義
|
|||||||||
|
(除非另有説明,否則為百萬美元) |
截至的年度 2018年12月31日 |
截至的年度 2017年12月31日 |
變化 以美元為單位 % |
更改中
常量 貨幣 % |
|||||
|
持續運營的核心運營收入
|
12 557
|
11 714
|
7
|
7
|
|||||
|
聯營公司的核心收入
|
1 113
|
1 335
|
– 17
|
– 17
|
|||||
|
核心利息支出
|
– 932
|
– 750
|
– 24
|
– 27
|
|||||
|
核心其他財務收入和支出
|
186
|
42
|
NM
|
NM
|
|||||
|
持續經營的核心税前收入
|
12 924
|
12 341
|
5
|
5
|
|||||
|
核心税種
|
– 2 004
|
– 1 867
|
– 7
|
– 7
|
|||||
|
持續運營的核心淨收入
|
10 920
|
10 474
|
4
|
4
|
|||||
|
持續運營的核心基本每股收益(美元)
|
4.71
|
4.46
|
6
|
5
|
|||||
|
|
|||||||||
|
1 關於非IFRS計量和對賬表的解釋,請參見"項目5.A經營成果—Novartis定義的非IFRS計量。”
|
|||||||||
|
NM=沒有意義
|
|||||||||
|
(百萬美元) |
2019 |
以%計
銷售總額 |
2018 |
以%計
銷售總額 |
2017 |
以%計
銷售總額 |
|||||||
|
創新藥物銷售總額需扣除
|
52 956
|
100.0
|
47 785
|
100.0
|
43 127
|
100.0
|
|||||||
|
特定於美國的醫療保健計劃和計劃回扣
|
– 4 824
|
– 9.1
|
– 3 921
|
– 8.2
|
– 3 303
|
– 7.7
|
|||||||
|
非特定於美國的醫療計劃和計劃回扣
|
– 3 438
|
– 6.5
|
– 3 140
|
– 6.6
|
– 2 652
|
– 6.1
|
|||||||
|
非醫療保健計劃和計劃相關的回扣、退貨和其他扣除
|
– 6 980
|
– 13.2
|
– 5 832
|
– 12.2
|
– 4 894
|
– 11.4
|
|||||||
|
創新藥物總額對淨銷售額的調整
|
– 15 242
|
|
– 28.8
|
|
– 12 893
|
– 27.0
|
– 10 849
|
– 25.2
|
|||||
|
創新藥物淨銷售額
|
37 714
|
71.2
|
34 892
|
73.0
|
32 278
|
74.8
|
|||||||
|
|
|
||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
持續經營的營業收入
|
9 086
|
8 403
|
8 702
|
||||
|
財產、廠房和設備折舊
|
1 345
|
1 482
|
1 303
|
||||
|
使用權資產折舊 1
|
305
|
|
|
||||
|
無形資產攤銷
|
2 836
|
2 587
|
2 624
|
||||
|
不動產、廠場和設備以及無形資產的減值
|
1 340
|
1 142
|
809
|
||||
|
來自持續運營的EBITDA 1
|
14 912
|
13 614
|
13 438
|
||||
|
非持續經營的營業收入
|
71
|
– 234
|
– 73
|
||||
|
財產、廠房和設備折舊
|
42
|
235
|
217
|
||||
|
使用權資產折舊
|
9
|
|
|
||||
|
無形資產攤銷
|
174
|
1 052
|
1 066
|
||||
|
不動產、廠場和設備以及無形資產的減值
|
|
394
|
57
|
||||
|
非持續業務的EBITDA
|
296
|
1 447
|
1 267
|
||||
|
EBITDA合計 1
|
15 208
|
15 061
|
14 705
|
||||
|
|
|
|
|||||
|
1 於二零一九年,由於租賃費用分類為使用權資產折舊(3. 14億美元,其中3. 05億美元持續經營業務)及利息費用(6,600萬美元),故於二零一九年,EBITDA因於二零一九年一月一日採納國際財務報告準則第16號租賃而受到正面影響。於過往年度,租賃費用確認為營業收入內的功能性費用(2018年集團租賃費用為3. 83億美元,其中3. 31億美元來自持續經營業務,2017年3. 37億美元來自持續經營業務,其中2. 92億美元來自持續經營業務)。
|
|||||||
|
(百萬美元
除非另有説明,否則) |
2019年12月31日 1 |
2018年12月31日 |
2017年12月31日 |
||||
|
市值
|
214 815
|
196 950
|
195 541
|
||||
|
非控制性權益
|
77
|
78
|
59
|
||||
|
非流動金融債務
|
20 353
|
22 470
|
23 224
|
||||
|
流動金融債務和衍生金融工具
|
7 031
|
9 678
|
5 308
|
||||
|
有價證券、商品、定期存款和衍生金融工具
|
– 334
|
– 2 693
|
– 625
|
||||
|
現金和現金等價物
|
– 11 112
|
– 13 271
|
– 8 860
|
||||
|
企業價值
|
230 830
|
213 212
|
214 647
|
||||
|
|
|||||||
|
1 2019年12月31日不包括愛爾康的業務,後者於2019年4月剝離為一家獨立交易的公司。詳情見“項目18.財務報表--附註2.重大交易”。
|
|||||||
|
創新藥物
|
桑多茲
|
公司
|
集團化
|
||||||||||||||
|
(除非另有説明,否則為百萬美元)
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
|||||||||
|
國際財務報告準則持續經營的營業收入
|
9 287
|
7 871
|
551
|
1 332
|
– 752
|
– 800
|
9 086
|
8 403
|
|||||||||
|
無形資產攤銷
|
2 447
|
2 158
|
314
|
363
|
|
|
2 761
|
2 521
|
|||||||||
|
減值
|
|
|
|
|
|
|
|
|
|||||||||
|
無形資產
|
632
|
592
|
503
|
249
|
|
|
1 135
|
841
|
|||||||||
|
與整個集團生產基地合理化有關的財產、廠房和設備
|
83
|
170
|
69
|
63
|
|
|
152
|
233
|
|||||||||
|
其他財產、廠房和設備
|
10
|
65
|
33
|
|
|
|
43
|
65
|
|||||||||
|
總減值費用
|
725
|
827
|
605
|
312
|
|
|
1 330
|
1 139
|
|||||||||
|
收購或撤資業務及相關項目
|
|
|
|
|
|
|
|
|
|||||||||
|
- 收入
|
– 8
|
|
|
|
– 108
|
– 21
|
– 116
|
– 21
|
|||||||||
|
- 費用
|
87
|
126
|
|
|
115
|
29
|
202
|
155
|
|||||||||
|
企業及相關項目的收購或撤資總額,淨額
|
79
|
126
|
|
|
7
|
8
|
86
|
134
|
|||||||||
|
其他項目
|
|
|
|
|
|
|
|
|
|||||||||
|
撤資收益
|
– 1 091
|
– 482
|
|
– 78
|
2
|
– 56
|
– 1 089
|
– 616
|
|||||||||
|
金融資產—公允價值調整
|
– 18
|
– 107
|
|
|
– 20
|
113
|
– 38
|
6
|
|||||||||
|
結構調整和有關項目
|
|
|
|
|
|
|
|
|
|||||||||
|
- 收入
|
– 58
|
– 25
|
– 7
|
– 12
|
– 6
|
– 2
|
– 71
|
– 39
|
|||||||||
|
- 費用
|
509
|
665
|
390
|
179
|
113
|
106
|
1 012
|
950
|
|||||||||
|
與法律有關的項目
|
|
|
|
|
|
|
|
|
|||||||||
|
- 收入
|
|
– 1
|
– 32
|
– 63
|
|
|
– 32
|
– 64
|
|||||||||
|
- 費用
|
999
|
36
|
156
|
90
|
|
|
1 155
|
126
|
|||||||||
|
額外收入
|
– 316
|
– 73
|
– 4
|
– 171
|
– 95
|
– 19
|
– 415
|
– 263
|
|||||||||
|
額外費用
|
87
|
156
|
121
|
50
|
119
|
54
|
327
|
260
|
|||||||||
|
其他項目合計
|
112
|
169
|
624
|
– 5
|
113
|
196
|
849
|
360
|
|||||||||
|
調整總額
|
3 363
|
3 280
|
1 543
|
670
|
120
|
204
|
5 026
|
4 154
|
|||||||||
|
持續運營的核心運營收入
|
12 650
|
11 151
|
2 094
|
2 002
|
– 632
|
– 596
|
14 112
|
12 557
|
|||||||||
|
佔淨銷售額的百分比
|
33.5%
|
32.0%
|
21.5%
|
20.3%
|
|
|
29.7%
|
28.1%
|
|||||||||
|
來自相聯公司的收入
|
1
|
1
|
2
|
5
|
656
|
6 432
|
659
|
6 438
|
|||||||||
|
對關聯公司收入的核心調整,税後淨額
|
|
|
|
|
427
|
– 5 325
|
427
|
– 5 325
|
|||||||||
|
利息支出
|
|
|
|
|
|
|
– 850
|
– 932
|
|||||||||
|
其他財務收支
|
|
|
|
|
|
|
45
|
186
|
|||||||||
|
對其他財務收入和支出的核心調整
|
|
|
|
|
|
|
11
|
|
|||||||||
|
按上述項目調整的税款(核心税款)
|
|
|
|
|
|
|
– 2 300
|
– 2 004
|
|||||||||
|
持續運營的核心淨收入
|
|
|
|
|
|
|
12 104
|
10 920
|
|||||||||
|
非持續經營業務的核心淨收入 1
|
|
|
|
|
|
|
278
|
1 018
|
|||||||||
|
核心淨收入
|
|
|
|
|
|
|
12 382
|
11 938
|
|||||||||
|
諾華製藥公司股東應佔核心淨收入
|
|
|
|
|
|
|
12 377
|
11 935
|
|||||||||
|
持續運營的核心基本每股收益(美元) 2
|
|
|
|
|
|
|
5.28
|
4.71
|
|||||||||
|
非持續運營的核心基本每股收益(美元) 2
|
|
|
|
|
|
|
0.12
|
0.44
|
|||||||||
|
核心基本每股收益(美元) 2
|
|
|
|
|
|
|
5.40
|
5.15
|
|||||||||
|
1 關於從《國際財務報告準則》到核心淨收入的非連續性業務對賬的詳情,請參閲第109頁。
|
|||||||||||||||||
|
2 每股收益(EPS)按諾華製藥股東應佔淨收益金額計算。
|
|||||||||||||||||
|
創新藥物
|
桑多茲
|
公司
|
集團化
|
||||||||||||||
|
(除非另有説明,否則為百萬美元)
|
2018
|
2017
|
2018
|
2017
|
2018
|
2017
|
2018
|
2017
|
|||||||||
|
國際財務報告準則持續經營的營業收入
|
7 871
|
7 595
|
1 332
|
1 368
|
– 800
|
– 261
|
8 403
|
8 702
|
|||||||||
|
無形資產攤銷
|
2 158
|
2 119
|
363
|
454
|
|
|
2 521
|
2 573
|
|||||||||
|
減值
|
|
|
|
|
|
|
|
|
|||||||||
|
無形資產
|
592
|
591
|
249
|
61
|
|
|
841
|
652
|
|||||||||
|
與整個集團生產基地合理化有關的財產、廠房和設備
|
170
|
7
|
63
|
60
|
|
|
233
|
67
|
|||||||||
|
其他財產、廠房和設備
|
65
|
77
|
|
13
|
|
|
65
|
90
|
|||||||||
|
金融資產 1
|
|
|
|
|
|
197
|
|
197
|
|||||||||
|
總減值費用
|
827
|
675
|
312
|
134
|
|
197
|
1 139
|
1 006
|
|||||||||
|
收購或撤資業務及相關項目
|
|
|
|
|
|
|
|
|
|||||||||
|
- 收入
|
|
– 2
|
|
|
– 21
|
– 115
|
– 21
|
– 117
|
|||||||||
|
- 費用
|
126
|
32
|
|
|
29
|
130
|
155
|
162
|
|||||||||
|
企業及相關項目的收購或撤資總額,淨額
|
126
|
30
|
|
|
8
|
15
|
134
|
45
|
|||||||||
|
其他項目
|
|
|
|
|
|
|
|
|
|||||||||
|
撤資收益
|
– 482
|
– 368
|
– 78
|
|
– 56
|
|
– 616
|
– 368
|
|||||||||
|
金融資產—公允價值調整 1
|
– 107
|
|
|
|
113
|
|
6
|
|
|||||||||
|
結構調整和有關項目
|
|
|
|
|
|
|
|
|
|||||||||
|
- 收入
|
– 25
|
– 53
|
– 12
|
– 7
|
– 2
|
– 1
|
– 39
|
– 61
|
|||||||||
|
- 費用
|
665
|
268
|
179
|
134
|
106
|
– 9
|
950
|
393
|
|||||||||
|
與法律有關的項目
|
|
|
|
|
|
|
|
|
|||||||||
|
- 收入
|
– 1
|
– 21
|
– 63
|
|
|
|
– 64
|
– 21
|
|||||||||
|
- 費用
|
36
|
35
|
90
|
|
|
|
126
|
35
|
|||||||||
|
額外收入
|
– 73
|
– 534
|
– 171
|
– 3
|
– 19
|
– 372
|
– 263
|
– 909
|
|||||||||
|
額外費用
|
156
|
273
|
50
|
|
54
|
46
|
260
|
319
|
|||||||||
|
其他項目合計
|
169
|
– 400
|
– 5
|
124
|
196
|
– 336
|
360
|
– 612
|
|||||||||
|
調整總額
|
3 280
|
2 424
|
670
|
712
|
204
|
– 124
|
4 154
|
3 012
|
|||||||||
|
持續運營的核心運營收入
|
11 151
|
10 019
|
2 002
|
2 080
|
– 596
|
– 385
|
12 557
|
11 714
|
|||||||||
|
佔淨銷售額的百分比
|
32.0%
|
31.0%
|
20.3%
|
20.7%
|
|
|
28.1%
|
27.7%
|
|||||||||
|
來自相聯公司的收入
|
1
|
– 1
|
5
|
23
|
6 432
|
1 086
|
6 438
|
1 108
|
|||||||||
|
對來自聯營公司的收入的核心調整,扣除税項
|
|
1
|
|
|
– 5 325
|
226
|
– 5 325
|
227
|
|||||||||
|
利息支出
|
|
|
|
|
|
|
– 932
|
– 750
|
|||||||||
|
其他財務收支
|
|
|
|
|
|
|
186
|
42
|
|||||||||
|
按上述項目調整的税款(核心税款)
|
|
|
|
|
|
|
– 2 004
|
– 1 867
|
|||||||||
|
持續運營的核心淨收入
|
|
|
|
|
|
|
10 920
|
10 474
|
|||||||||
|
非持續經營業務的核心淨收入 2
|
|
|
|
|
|
|
1 018
|
917
|
|||||||||
|
核心淨收入
|
|
|
|
|
|
|
11 938
|
11 391
|
|||||||||
|
諾華製藥公司股東應佔核心淨收入
|
|
|
|
|
|
|
11 935
|
11 391
|
|||||||||
|
持續運營的核心基本每股收益(美元) 3
|
|
|
|
|
|
|
4.71
|
4.46
|
|||||||||
|
非持續運營的核心基本每股收益(美元) 3
|
|
|
|
|
|
|
0.44
|
0.40
|
|||||||||
|
核心基本每股收益(美元) 3
|
|
|
|
|
|
|
5.15
|
4.86
|
|||||||||
|
1 就按公平值計入損益的金融工具而言,由於國際財務報告準則第9號的變動,於二零一八年一月一日,金融資產的未實現收益╱虧損於“金融資產—公平值調整”項下呈列。
|
|||||||||||||||||
|
2 有關已終止經營業務從國際財務報告準則至核心淨收入對賬的詳情,請參閲第110頁。
|
|||||||||||||||||
|
3 每股收益(EPS)按諾華製藥股東應佔淨收益金額計算。
|
|||||||||||||||||
|
|
|||||||||||||||||
|
2019年(除非另有説明,否則為百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 3 |
其他 物品 4 |
核心成果 |
|||||||
|
持續經營毛利
|
34 252
|
2 711
|
85
|
48
|
296
|
37 392
|
|||||||
|
持續經營的營業收入
|
9 086
|
2 761
|
1 330
|
86
|
849
|
14 112
|
|||||||
|
持續經營的税前收入
|
8 940
|
3 188
|
1 330
|
86
|
860
|
14 404
|
|||||||
|
持續經營所得税款 5
|
– 1 793
|
|
|
|
|
– 2 300
|
|||||||
|
持續經營淨收益
|
7 147
|
|
|
|
|
12 104
|
|||||||
|
非持續經營業務的淨收益 6
|
4 590
|
|
|
|
|
278
|
|||||||
|
淨收入
|
11 737
|
|
|
|
|
12 382
|
|||||||
|
來自持續經營業務的基本每股收益(美元) 7
|
3.12
|
|
|
|
|
5.28
|
|||||||
|
中斷業務的基本每股收益(美元) 7
|
2.00
|
|
|
|
|
0.12
|
|||||||
|
基本每股收益(美元) 7
|
5.12
|
|
|
|
|
5.40
|
|||||||
|
|
|||||||||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
其他收入
|
1 179
|
|
|
|
– 66
|
1 113
|
|||||||
|
銷貨成本
|
– 14 425
|
2 711
|
85
|
48
|
362
|
– 11 219
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 14 369
|
|
|
10
|
40
|
– 14 319
|
|||||||
|
研發
|
– 9 402
|
50
|
1 078
|
10
|
– 122
|
– 8 386
|
|||||||
|
其他收入
|
2 031
|
|
– 2
|
– 116
|
– 1 418
|
495
|
|||||||
|
其他費用
|
– 3 426
|
|
169
|
134
|
2 053
|
– 1 070
|
|||||||
|
|
|||||||||||||
|
以下是達到税前核心收入的調整
|
|
|
|
|
|
|
|||||||
|
來自相聯公司的收入
|
659
|
427
|
|
|
|
1 086
|
|||||||
|
其他財務收支
|
45
|
|
|
|
11
|
56
|
|||||||
|
|
|||||||||||||
|
1 無形資產攤銷:銷售成本包括已收購的市場產品和其他與生產相關的無形資產的攤銷;研究和開發包括已收購的技術權利的攤銷;來自聯營公司的收入包括諾華在估計羅氏核心項目中的份額4.27億美元
|
|||||||||||||
|
2 損傷:銷售貨品成本及研發成本包括與無形資產有關的減值支出;研發亦包括減值支出撥回;銷售貨品成本、其他收入及其他支出包括與物業、廠房及設備有關的減值支出淨額
|
|||||||||||||
|
3 收購或剝離業務及相關項目,包括重組和整合費用:銷售成本、銷售成本、一般和行政管理成本、研發成本、其他收入和其他支出包括與收購相關的淨支出;其他收入和其他支出還包括過渡服務費收入和與投資組合轉型和Alcon分拆相關的支出
|
|||||||||||||
|
4 其他項目:其他收入包括來自外發許可協議的收入和與修訂合作協議有關的收入;銷售貨物成本、其他收入和其他支出包括重組淨額和與集團範圍內生產基地合理化有關的其他支出;銷售成本,研發成本,銷售成本,一般成本和管理成本,其他收入及其他開支包括其他重組收入及支出及相關項目;銷售貨品成本及研發成本亦包括或然代價負債之公平值調整;銷售成本還包括存貨核銷和其他準備金;銷售、一般和管理包括應收款預期信用損失準備金和其他準備金;其他收入及其他開支包括公平值調整及金融資產及法定資產的剝離收益及虧損,相關項目以及環境準備金;其他收入還包括剝離產品和不動產、廠房和設備以及撥備釋放的淨收益;其他支出包括繁重合同的準備金和其他準備金;其他財務收入和支出包括通過Alcon分配產生的財務負債的重估影響,
|
|||||||||||||
|
5 國際財務報告準則與核心業績之間的調整所產生的税項,就調整所包含的每一個別項目而言,均會考慮最終適用於該項目的税率(基於調整最終會產生税務影響的司法管轄區)。一般而言,這會導致無形資產的攤銷及減值以及收購相關重組及整合項目產生全部税務影響。其他項目通常會受到税務影響,但某些司法管轄區的法律解決產生的項目並非總是如此。有關來自聯營公司之收入之調整乃扣除任何相關税項影響入賬。由於這些因素以及不同司法管轄區的有效税率不同,持續經營業務的55億美元調整總額為5.07億美元,以達到税前核心業績。調整後的平均税率為9. 3%。
|
|||||||||||||
|
6 有關國際財務報告準則與核心淨收入對賬的詳情,請參閲第109頁。
|
|||||||||||||
|
7 每股收益(EPS)是根據諾華製藥股東應佔淨收益計算的。
|
|||||||||||||
|
2018年(百萬美元,除非另有説明) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 3 |
其他 物品 4 |
核心成果 |
|||||||
|
持續經營毛利
|
31 589
|
2 342
|
488
|
5
|
462
|
34 886
|
|||||||
|
持續經營的營業收入
|
8 403
|
2 521
|
1 139
|
134
|
360
|
12 557
|
|||||||
|
持續經營的税前收入
|
14 095
|
2 965
|
1 139
|
– 5 656
|
381
|
12 924
|
|||||||
|
持續經營所得税款 5
|
– 1 295
|
|
|
|
|
– 2 004
|
|||||||
|
持續經營淨收益
|
12 800
|
|
|
|
|
10 920
|
|||||||
|
非持續經營業務的淨收益 6
|
– 186
|
|
|
|
|
1 018
|
|||||||
|
淨收入
|
12 614
|
|
|
|
|
11 938
|
|||||||
|
來自持續經營業務的基本每股收益(美元) 7
|
5.52
|
|
|
|
|
4.71
|
|||||||
|
中斷業務的基本每股收益(美元) 7
|
– 0.08
|
|
|
|
|
0.44
|
|||||||
|
基本每股收益(美元) 7
|
5.44
|
|
|
|
|
5.15
|
|||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 14 510
|
2 342
|
488
|
5
|
462
|
– 11 213
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 13 717
|
|
|
28
|
– 1
|
– 13 690
|
|||||||
|
研發
|
– 8 489
|
179
|
167
|
23
|
– 34
|
– 8 154
|
|||||||
|
其他收入
|
1 629
|
|
|
– 21
|
– 1 050
|
558
|
|||||||
|
其他費用
|
– 2 609
|
|
484
|
99
|
983
|
– 1 043
|
|||||||
|
以下是達到税前核心收入的調整
|
|
|
|
|
|
|
|||||||
|
來自相聯公司的收入
|
6 438
|
444
|
|
– 5 790
|
21
|
1 113
|
|||||||
|
1 無形資產的攤銷:出售商品的成本包括對市場上產品和其他與生產相關的無形資產的已獲得權利的攤銷;研究和開發包括已獲得權利的攤銷,包括技術平臺;來自關聯公司的收入包括諾華在估計的羅氏核心項目中的份額4.44億美元
|
|||||||||||||
|
2 減值:商品銷售成本和研發費用包括與無形資產有關的減值費用;研發還包括財產、廠房和設備的減值沖銷;其他費用包括與財產、廠房和設備有關的減值費用;售出商品成本和其他費用包括與出售集團商譽和當前銷售的產品有關的減值費用
|
|||||||||||||
|
3 收購或撤資業務及相關項目,包括重組和整合費用:出售商品的成本、銷售、一般和管理、研發和其他費用包括與收購相關的費用;其他收入和其他費用包括過渡服務費收入和支出,以及與投資組合轉型相關的其他項目;來自關聯公司的收入包括出售GSK Consumer Healthcare Holdings Ltd.36.5%的投資所產生的58億美元的税前收益。
|
|||||||||||||
|
4 其他項目:銷售商品成本、其他收入和其他支出包括與整個集團生產基地合理化有關的淨重組和其他費用;銷售商品成本、銷售、一般和管理、研發、其他收入和其他支出包括其他重組收入和費用及相關項目;銷售商品成本和其他支出包括與合同協議變更有關的費用;銷售商品成本還包括庫存註銷和其他與產品召回有關的成本;銷售、一般和管理包括撥備的沖銷;研究和開發包括或有對價負債的公允價值調整和對繁重合同的收費;其他收入和其他費用包括金融資產的公允價值調整和撤資損益;其他收入還包括產品撤資收益、財產、廠房和設備的撤資收益、應計項目的釋放和法律和解收益;其他費用包括與法律有關的項目和重組費用;來自關聯公司的收入包括諾華在估計的葛蘭素史克消費者保健控股有限公司核心項目中所佔份額的2100萬美元的調整。
|
|||||||||||||
|
5 國際財務報告準則與核心結果之間的調整的税收考慮到,對於調整中包括的每個單獨項目,根據調整將最終產生税收影響的司法管轄區,最終適用於該項目的税率。一般來説,這會導致無形資產的攤銷和減值,以及與收購相關的重組和整合項目產生全面的税務影響。通常對其他項目有税收影響,儘管在某些法域,因法律和解而產生的項目並不總是如此。與聯營公司收入相關的調整在扣除任何相關税項影響後入賬。由於這些因素和不同司法管轄區不同的實際税率,為實現税前核心結果而進行的12億美元總調整的税額為7.09億美元。不包括出售葛蘭素史克Cosumer Healthcare Holdings Ltd.36.5%投資的收益,為實現税前核心業績而進行的46億美元調整的總税額為7700億美元。不包括這筆交易的調整的平均税率為16.7%。
|
|||||||||||||
|
6 關於從“國際財務報告準則”到核心淨收入的非連續性業務對賬的詳情,請參閲第110頁。
|
|||||||||||||
|
7 每股收益(EPS)是根據諾華製藥股東應佔淨收益計算的。
|
|||||||||||||
|
2017年(除非另有説明,否則為百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 3 |
其他 物品 4 |
核心成果 |
|||||||
|
毛利
|
29 771
|
2 386
|
92
|
|
125
|
32 374
|
|||||||
|
營業收入
|
8 702
|
2 573
|
1 006
|
45
|
– 612
|
11 714
|
|||||||
|
税前收入
|
9 102
|
2 949
|
1 007
|
45
|
– 762
|
12 341
|
|||||||
|
税費 5
|
– 1 603
|
|
|
|
|
– 1 867
|
|||||||
|
持續經營淨收益
|
7 499
|
|
|
|
|
10 474
|
|||||||
|
非持續經營業務的淨收益 6
|
204
|
|
|
|
|
917
|
|||||||
|
淨收入
|
7 703
|
|
|
|
|
11 391
|
|||||||
|
來自持續經營業務的基本每股收益(美元) 7
|
3.20
|
|
|
|
|
4.46
|
|||||||
|
中斷業務的基本每股收益(美元) 7
|
0.08
|
|
|
|
|
0.40
|
|||||||
|
基本每股收益(美元) 7
|
3.28
|
|
|
|
|
4.86
|
|||||||
|
|
|||||||||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 13 633
|
2 386
|
92
|
|
125
|
– 11 030
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 12 465
|
|
|
|
– 3
|
– 12 468
|
|||||||
|
研發
|
– 8 389
|
187
|
594
|
|
– 200
|
– 7 808
|
|||||||
|
其他收入
|
1 922
|
|
– 9
|
– 117
|
– 1 048
|
748
|
|||||||
|
其他費用
|
– 2 137
|
|
329
|
162
|
514
|
– 1 132
|
|||||||
|
|
|||||||||||||
|
以下是達到税前核心收入的調整
|
|
|
|
|
|
|
|||||||
|
來自相聯公司的收入
|
1 108
|
376
|
1
|
|
– 150
|
1 335
|
|||||||
|
1 無形資產的攤銷:出售商品的成本包括對市場產品和其他與生產相關的無形資產的已獲得權利的經常性攤銷;研究和開發包括對技術平臺已獲得權利的經常性攤銷;來自關聯公司的收入包括諾華在估計的羅氏核心項目中的份額3.76億美元
|
|||||||||||||
|
2 減值:商品銷售成本和研發費用包括與無形資產相關的減值費用;研發、其他收入和其他費用包括與財產、廠房和設備減值相關的沖銷和費用;其他費用還包括與金融資產相關的減值費用
|
|||||||||||||
|
3 收購或撤資業務及相關項目,包括重組和整合費用:其他收入和其他費用包括過渡性服務費收入和費用,以及與投資組合轉型有關的其他項目
|
|||||||||||||
|
4 其他項目:銷售成本、其他收入和其他支出包括與整個集團生產基地合理化有關的淨重組和其他費用;銷售商品成本、研發、銷售、一般和管理、其他收入和其他支出包括其他重組收入和費用及相關項目;銷售、一般和管理包括撥備釋放的收入;研究和開發包括對或有對價負債的公允價值調整;其他收入和其他支出包括與法律有關的項目;其他收入還包括瑞士養老金計劃修正案的收益、產品和金融資產撤資收益、解決合同糾紛的收入和對或有對價銷售里程碑應收款的公允價值調整;其他費用還包括合同終止費用準備金、繁重合同費用和瑞士養老金計劃修正案;關聯公司的收入包括諾華在估計的葛蘭素史克消費者保健控股有限公司核心項目中所佔份額的1.5億美元的調整。
|
|||||||||||||
|
5 國際財務報告準則與核心結果之間的調整的税收考慮到,對於調整中包括的每個單獨項目,根據調整將最終產生税收影響的司法管轄區,最終適用於該項目的税率。一般來説,這會導致無形資產的攤銷和減值,以及與收購相關的重組和整合項目產生全面的税務影響。通常對其他項目有税收影響,儘管在某些法域,因法律和解而產生的項目並不總是如此。與聯營公司收入相關的調整在扣除任何相關税項影響後入賬。由於這些因素和不同司法管轄區不同的實際税率,為實現税前核心結果而進行的32億美元總調整的税額為2.64億美元。調整後的平均税率為8.2%。
|
|||||||||||||
|
6 關於從“國際財務報告準則”到核心淨收入的非連續性業務對賬的詳情,請參閲第110頁。
|
|||||||||||||
|
7 每股收益(EPS)是根據諾華製藥股東應佔淨收益計算的。
|
|||||||||||||
|
2019 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 3 |
其他 物品 4 |
核心成果 |
|||||||
|
毛利
|
29 539
|
2 397
|
|
48
|
116
|
32 100
|
|||||||
|
營業收入
|
9 287
|
2 447
|
725
|
79
|
112
|
12 650
|
|||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
其他收入
|
1 092
|
|
|
|
– 66
|
1 026
|
|||||||
|
銷貨成本
|
– 10 050
|
2 397
|
|
48
|
182
|
– 7 423
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 11 617
|
|
|
10
|
25
|
– 11 582
|
|||||||
|
研發
|
– 8 152
|
50
|
632
|
10
|
– 125
|
– 7 585
|
|||||||
|
其他收入
|
1 586
|
|
– 1
|
– 8
|
– 1 230
|
347
|
|||||||
|
其他費用
|
– 2 069
|
|
94
|
19
|
1 326
|
– 630
|
|||||||
|
1 無形資產攤銷:銷售成本包括已取得的市場產品權利和其他與生產有關的無形資產的攤銷;研究和開發包括已取得的技術權利的攤銷
|
|||||||||||||
|
2 損傷:研究和開發包括與無形資產有關的減值費用和減值費用轉回;其他收入和其他支出包括與不動產、廠房和設備有關的減值費用淨額
|
|||||||||||||
|
3 收購或剝離業務及相關項目,包括重組和整合費用:銷售成本、銷售成本、一般和行政管理成本、研發成本、其他收入和其他支出包括與收購相關的淨支出;其他收入和其他支出還包括過渡服務費收入和與投資組合轉型和Alcon分拆相關的支出
|
|||||||||||||
|
4 其他項目:其他收入包括來自外發協議的淨收入和與修訂合作協議有關的收入;銷售貨品成本、其他收入和其他支出包括重組和與集團範圍內生產基地合理化有關的其他支出;銷售貨品成本、研發、其他收入和其他支出包括其他重組收入和支出以及相關項目;銷售、一般及行政包括其他撥備;其他收入及其他開支包括公平值調整及金融資產的出售收益及虧損;其他收入還包括剝離產品和財產、廠房和設備以及撥備釋放的淨收益;其他支出包括法律相關項目
|
|||||||||||||
|
2018 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 3 |
其他 物品 4 |
核心成果 |
|||||||
|
毛利
|
26 951
|
1 979
|
423
|
5
|
329
|
29 687
|
|||||||
|
營業收入
|
7 871
|
2 158
|
827
|
126
|
169
|
11 151
|
|||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 9 870
|
1 979
|
423
|
5
|
329
|
– 7 134
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 10 907
|
|
|
28
|
– 11
|
– 10 890
|
|||||||
|
研發
|
– 7 675
|
179
|
167
|
23
|
– 34
|
– 7 340
|
|||||||
|
其他收入
|
977
|
|
|
|
– 671
|
306
|
|||||||
|
其他費用
|
– 1 475
|
|
237
|
70
|
556
|
– 612
|
|||||||
|
1 無形資產攤銷:出售貨物的成本包括對市場產品和其他與生產有關的無形資產所獲得的權利的攤銷;研究和開發包括對所獲得的權利的攤銷,包括技術平臺
|
|||||||||||||
|
2 減值:商品銷售成本和研發費用包括與無形資產有關的減值費用;研發還包括財產、廠房和設備的減值沖銷;其他費用包括與財產、廠房和設備有關的減值費用
|
|||||||||||||
|
3 收購或撤資業務及相關項目,包括重組和整合費用:出售貨物的成本、銷售、一般和行政、研發和其他費用包括與收購有關的費用;其他費用還包括與投資組合轉型有關的項目
|
|||||||||||||
|
4 其他項目:銷售成本和其他費用包括與整個集團生產基地合理化有關的重組和其他費用,以及與合同協議變更有關的費用;銷售商品成本、研發、其他收入和其他支出包括其他重組收入和費用及相關項目;銷售商品成本和研發還包括或有對價負債的公允價值調整;銷售商品成本還包括存貨註銷;銷售、一般和行政費用包括沖銷撥備;研究和開發包括繁重合同的費用;其他收入和其他支出包括金融資產和法律相關項目的公允價值調整;其他收入還包括產品撤資收益和應計項目的釋放。
|
|||||||||||||
|
2017 (百萬美元) |
國際財務報告準則 結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 3 |
其他 物品 4 |
核心成果 |
|||||||
|
毛利
|
25 194
|
1 932
|
31
|
|
56
|
27 213
|
|||||||
|
營業收入
|
7 595
|
2 119
|
675
|
30
|
– 400
|
10 019
|
|||||||
|
|
|||||||||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 8 650
|
1 932
|
31
|
|
56
|
– 6 631
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 9 887
|
|
|
|
– 3
|
– 9 890
|
|||||||
|
研發
|
– 7 615
|
187
|
594
|
|
– 200
|
– 7 034
|
|||||||
|
其他收入
|
1 027
|
|
– 9
|
– 2
|
– 665
|
351
|
|||||||
|
其他費用
|
– 1 124
|
|
59
|
32
|
412
|
– 621
|
|||||||
|
1 無形資產攤銷:銷售商品成本包括對市場產品和其他與生產有關的無形資產的已獲得權利的經常性攤銷;研究和開發包括技術平臺已獲得權利的經常性攤銷
|
|||||||||||||
|
2 減值:商品銷售成本和研發費用包括與無形資產有關的減值費用;研發、其他收入和其他費用包括與財產、廠房和設備減值有關的沖銷和費用
|
|||||||||||||
|
3 收購或撤資業務及相關項目,包括重組和整合費用:其他收入包括過渡服務費收入;其他費用包括與投資組合轉型有關的項目和與收購有關的成本
|
|||||||||||||
|
4 其他項目:銷售商品成本、其他收入和其他支出包括與整個集團生產基地合理化有關的淨重組和其他費用;銷售商品成本、研發、銷售、一般和管理、其他收入和其他支出包括其他重組收入和費用及相關項目;銷售、一般和管理包括撥備發佈的收入;研究和開發包括對或有對價負債的公允價值調整;其他收入和其他支出包括與法律有關的項目;其他收入還包括瑞士養卹金計劃修正案的收益、解決合同糾紛的收入以及產品和金融資產撤資收益;其他費用還包括合同終止費用準備金、瑞士養卹金計劃修正案、繁重合同費用和其他費用。
|
|||||||||||||
|
|
|||||||||||||
|
2019 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
4 601
|
314
|
85
|
|
180
|
5 180
|
|||||||
|
營業收入
|
551
|
314
|
605
|
|
624
|
2 094
|
|||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 5 334
|
314
|
85
|
|
180
|
– 4 755
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 2 218
|
|
|
|
15
|
– 2 203
|
|||||||
|
研發
|
– 1 250
|
|
446
|
|
3
|
– 801
|
|||||||
|
其他收入
|
167
|
|
– 1
|
|
– 39
|
127
|
|||||||
|
其他費用
|
– 749
|
|
75
|
|
465
|
– 209
|
|||||||
|
1 無形資產攤銷:銷售成本包括已收購的市場產品權利和其他與生產有關的無形資產的攤銷,
|
|||||||||||||
|
2 損傷:銷售成本、研發成本包括與無形資產有關的減值支出;銷售成本、其他收入和其他支出包括與物業、廠房及設備有關的減值支出淨額
|
|||||||||||||
|
3 其他項目:銷售貨品成本及其他開支包括重組淨額及與本集團範圍內生產基地合理化有關的其他開支;銷售貨品成本、銷售、一般及行政開支、其他收入及其他開支包括重組收入及開支及相關項目;銷售貨品成本亦包括存貨核銷及其他撥備;銷售、一般和管理包括應收款預期信用損失準備金和其他準備金;其他收入和其他費用也包括法律相關項目;其他費用還包括環境準備金、繁重合同準備金和其他準備金,
|
|||||||||||||
|
2018 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
4 568
|
363
|
65
|
|
133
|
5 129
|
|||||||
|
營業收入
|
1 332
|
363
|
312
|
|
– 5
|
2 002
|
|||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 5 530
|
363
|
65
|
|
133
|
– 4 969
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 2 305
|
|
|
|
10
|
– 2 295
|
|||||||
|
其他收入
|
505
|
|
|
|
– 295
|
210
|
|||||||
|
其他費用
|
– 622
|
|
247
|
|
147
|
– 228
|
|||||||
|
1 無形資產攤銷:銷售成本包括已收購的市場產品權利和其他與生產有關的無形資產的攤銷,
|
|||||||||||||
|
2 減值:銷貨成本包括與無形資產有關的減值費用,以及與待售處置集團有關的當前銷售產品的減值費用;其他費用包括與財產、廠房和設備有關的減值費用,以及與待售處置集團有關的商譽減值費用
|
|||||||||||||
|
3 其他項目:銷售貨品成本、其他收入及其他開支包括重組淨額及與本集團整體生產基地合理化有關的其他開支;銷售貨品成本亦包括存貨核銷及其他產品回收相關成本;銷售貨品成本、銷售、一般及行政、其他收入及其他開支包括其他重組收入及開支及相關項目;其他收入還包括產品撤資收益、合法結算收益和或有對價負債的公允價值調整;其他支出包括法律相關項目和重組費用
|
|||||||||||||
|
2017 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
4 415
|
454
|
61
|
|
69
|
4 999
|
|||||||
|
營業收入
|
1 368
|
454
|
134
|
|
124
|
2 080
|
|||||||
|
|
|||||||||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 5 800
|
454
|
61
|
|
69
|
– 5 216
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
其他收入
|
204
|
|
|
|
– 10
|
194
|
|||||||
|
其他費用
|
– 351
|
|
73
|
|
65
|
– 213
|
|||||||
|
1 無形資產攤銷:銷售貨物成本包括對市場上產品和其他與生產有關的無形資產的收購權利的經常性攤銷,
|
|||||||||||||
|
2 損傷:銷售成本包括與無形資產有關的減值費用;其他費用包括與不動產、廠房和設備有關的減值費用
|
|||||||||||||
|
3 其他項目:銷售貨品成本、其他收入及其他開支包括重組淨額及與整個集團生產基地合理化有關的其他開支,以及其他重組收入及開支及相關項目;其他收入亦包括瑞士退休金計劃修訂案的收益
|
|||||||||||||
|
2019 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 |
減值 |
收購或
撤資 企業和 相關項目 1 |
其他 物品 2 |
核心成果 |
|||||||
|
毛利
|
112
|
|
|
|
|
112
|
|||||||
|
營業虧損
|
– 752
|
|
|
7
|
113
|
– 632
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
其他收入
|
278
|
|
|
– 108
|
– 149
|
21
|
|||||||
|
其他費用
|
– 608
|
|
|
115
|
262
|
– 231
|
|||||||
|
1 收購或剝離業務及相關項目,包括重組及整合費用:其他收入及其他支出包括過渡服務費收入及與投資組合轉型及Alcon分拆相關的支出
|
|||||||||||||
|
2 其他項目:其他收入及其他開支包括金融資產的公允價值調整及剝離損益、重組收入及支出及相關項目,以及環境準備金
|
|||||||||||||
|
2018 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 |
減值 |
收購或
撤資 企業和 相關項目 1 |
其他 物品 2 |
核心成果 |
|||||||
|
毛利
|
70
|
|
|
|
|
70
|
|||||||
|
營業虧損
|
– 800
|
|
|
8
|
196
|
– 596
|
|||||||
|
以下是達到核心運營虧損的調整
|
|
|
|
|
|
|
|||||||
|
其他收入
|
147
|
|
|
– 21
|
– 84
|
42
|
|||||||
|
其他費用
|
– 512
|
|
|
29
|
280
|
– 203
|
|||||||
|
1 收購或撤資業務及相關項目,包括重組和整合費用:其他收入和其他費用包括過渡性服務費收入和費用,以及與投資組合轉型有關的其他項目
|
|||||||||||||
|
2 其他項目:其他收入及其他支出包括金融資產的公允價值調整、剝離收益及虧損,以及重組收入及支出及相關項目;其他收入亦包括物業、廠房及設備的剝離收益
|
|||||||||||||
|
2017 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 |
減值 1 |
收購或
撤資 企業和 相關項目 2 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
162
|
|
|
|
|
162
|
|||||||
|
營業虧損
|
– 261
|
|
197
|
15
|
– 336
|
– 385
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營虧損的調整
|
|
|
|
|
|
|
|||||||
|
其他收入
|
691
|
|
|
– 115
|
– 373
|
203
|
|||||||
|
其他費用
|
– 662
|
|
197
|
130
|
37
|
– 298
|
|||||||
|
1 減值:其他費用包括與金融資產有關的減值費用
|
|||||||||||||
|
2 收購或撤資業務及相關項目,包括重組和整合費用:其他收入和其他費用包括過渡性服務費收入和費用,以及與投資組合轉型有關的其他項目
|
|||||||||||||
|
3 其他項目:其他收入包括對或有對價銷售里程碑應收賬款、瑞士養老金計劃修正案和其他項目的公允價值調整;其他收入和其他費用包括重組收入和費用及相關項目;其他費用還包括對瑞士養老金計劃的修正案。
|
|||||||||||||
|
2019 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 |
收購或
撤資 企業和 相關項目 2 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
949
|
165
|
|
|
9
|
1 123
|
|||||||
|
已終止經營業務的營業收入
|
71
|
167
|
|
|
112
|
350
|
|||||||
|
已終止經營的税前收入
|
58
|
|
|
|
|
337
|
|||||||
|
税費 4
|
– 159
|
|
|
|
|
– 59
|
|||||||
|
愛爾康公司向諾華製藥股東分配收益前的非持續經營淨虧損/收益
|
– 101
|
|
|
|
|
278
|
|||||||
|
Alcon Inc.諾華公司股東
|
4 691
|
|
|
– 4 691
|
|
|
|||||||
|
非持續經營業務的淨收益
|
4 590
|
|
|
|
|
278
|
|||||||
|
基本每股收益(美元) 5
|
2.00
|
|
|
|
|
0.12
|
|||||||
|
|
|||||||||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 860
|
165
|
|
|
9
|
– 686
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 638
|
|
|
|
14
|
– 624
|
|||||||
|
研發
|
– 142
|
2
|
|
|
4
|
– 136
|
|||||||
|
其他收入
|
15
|
|
|
|
– 3
|
12
|
|||||||
|
其他費用
|
– 113
|
|
|
|
88
|
– 25
|
|||||||
|
1 無形資產攤銷:銷售成本包括已取得的市場產品權利和其他與生產有關的無形資產的攤銷;研究和開發包括已取得的技術權利的攤銷
|
|||||||||||||
|
2 收購或剝離業務及相關項目是指與愛爾康公司(剝離)向諾華製藥股東分配相關的免税、非現金收益調整
|
|||||||||||||
|
3 其他項目:銷售成本、銷售成本、一般及行政成本、研發成本及其他支出包括其他重組費用及相關項目;研發還包括期權權攤銷及或然代價負債的公允價值調整;其他收入包括金融資產的公允價值調整;其他支出還包括法律相關項目
|
|||||||||||||
|
4 國際財務報告準則與核心結果之間的調整的税收考慮到,對於調整中包括的每個單獨項目,根據調整將最終產生税收影響的司法管轄區,最終適用於該項目的税率。一般來説,這會導致無形資產的攤銷和減值,以及與收購相關的重組和整合項目產生全面的税務影響。通常對其他項目有税收影響,儘管在某些法域,因法律和解而產生的項目並不總是如此。由於這些因素以及不同司法管轄區的不同實際税率,不包括Alcon Inc.向諾華製藥股東分派(剝離)以實現核心税前業績的2.79億美元的非應税、非現金收益,總調整的税額為1億美元。2019年的核心税率為17.5%,不包括收益對愛爾康公司向諾華製藥股東分配的影響。
|
|||||||||||||
|
5 每股收益(EPS)按諾華製藥股東應佔淨收益金額計算。
|
|||||||||||||
|
2018 (百萬美元) |
國際財務報告準則結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
3 170
|
996
|
389
|
|
– 23
|
4 532
|
|||||||
|
已終止經營業務的經營虧損/收入
|
– 234
|
1 007
|
391
|
|
102
|
1 266
|
|||||||
|
已終止經營業務税前虧損/收入
|
– 260
|
|
|
|
|
1 240
|
|||||||
|
税費 4
|
74
|
|
|
|
|
– 222
|
|||||||
|
非持續經營的淨虧損/淨收益
|
– 186
|
|
|
|
|
1 018
|
|||||||
|
基本每股收益(美元) 5
|
– 0.08
|
|
|
|
|
0.44
|
|||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 3 983
|
996
|
389
|
|
– 23
|
– 2 621
|
|||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
銷售、一般和行政管理
|
– 2 754
|
|
2
|
|
13
|
– 2 739
|
|||||||
|
研發
|
– 585
|
11
|
|
|
47
|
– 527
|
|||||||
|
其他收入
|
61
|
|
|
|
– 23
|
38
|
|||||||
|
其他費用
|
– 126
|
|
|
|
88
|
– 38
|
|||||||
|
1 無形資產攤銷:銷售成本包括已收購的市場產品權利和其他與生產有關的無形資產的攤銷;研發包括已收購的技術平臺權利的攤銷
|
|||||||||||||
|
2 減值:商品銷售成本和銷售成本,一般和行政費用包括與無形資產有關的減值費用
|
|||||||||||||
|
3 其他項目:貨品銷售成本,銷售成本,一般及行政成本,以及研發成本,包括與產品自願退出市場有關的費用及費用轉回;貨品銷售成本,一般及行政成本,研究開發成本,其他收入及其他開支亦包括其他重組收入及費用及相關項目;研究和開發還包括期權權的攤銷和或有對價負債的公允價值調整;其他收入包括金融資產的公允價值調整;其他支出包括法律相關項目
|
|||||||||||||
|
4 國際財務報告準則與核心業績之間的調整所產生的税項,就調整所包含的每一個別項目而言,均會考慮最終適用於該項目的税率(基於調整最終會產生税務影響的司法管轄區)。一般而言,這會導致無形資產的攤銷及減值以及收購相關重組及整合項目產生全部税務影響。其他項目通常會受到税務影響,但某些司法管轄區的法律解決產生的項目並非總是如此。由於這些因素以及不同司法管轄區的有效税率不同,為達到税前核心業績而進行的15億美元的總調整所得税達2.96億美元。2018年核心税率為17.9%。
|
|||||||||||||
|
5 每股收益(EPS)按諾華製藥股東應佔淨收益金額計算。
|
|||||||||||||
|
2017 (百萬美元) |
國際財務報告準則 結果 |
攤銷 無形的 資產 1 |
減值 2 |
收購或
撤資 企業和 相關項目 |
其他 物品 3 |
核心成果 |
|||||||
|
毛利
|
3 189
|
1 015
|
|
|
|
4 204
|
|||||||
|
已終止經營業務的經營虧損/收入
|
– 73
|
1 025
|
86
|
|
98
|
1 136
|
|||||||
|
已終止經營業務税前虧損/收入
|
– 103
|
|
|
|
|
1 106
|
|||||||
|
税費 4
|
307
|
|
|
|
|
– 189
|
|||||||
|
非持續經營業務的淨收益
|
204
|
|
|
|
|
917
|
|||||||
|
基本每股收益(美元) 5
|
0.08
|
|
|
|
|
0.40
|
|||||||
|
|
|||||||||||||
|
以下是為實現核心毛利而進行的調整
|
|
|
|
|
|
|
|||||||
|
銷貨成本
|
– 3 588
|
1 015
|
|
|
|
– 2 573
|
|||||||
|
|
|||||||||||||
|
以下是達到核心運營收入的調整
|
|
|
|
|
|
|
|||||||
|
研發
|
– 583
|
10
|
86
|
|
– 18
|
– 505
|
|||||||
|
其他收入
|
47
|
|
|
|
– 17
|
30
|
|||||||
|
其他費用
|
– 194
|
|
|
|
133
|
– 61
|
|||||||
|
1 無形資產攤銷:銷售商品成本包括對市場產品和其他與生產有關的無形資產的已獲得權利的經常性攤銷;研究和開發包括技術平臺已獲得權利的經常性攤銷
|
|||||||||||||
|
2 減值:研究和開發包括與無形資產和金融資產有關的減值費用
|
|||||||||||||
|
3 其他項目:研發包括對或有對價負債的公允價值調整;其他收入和其他支出包括重組收入和費用以及相關項目;其他收入還包括瑞士養卹金計劃修正案的收益和前期費用的部分轉回;其他支出還包括法律相關項目
|
|||||||||||||
|
4 國際財務報告準則與核心業績之間的調整所產生的税項,就調整所包含的每一個別項目而言,均會考慮最終適用於該項目的税率(基於調整最終會產生税務影響的司法管轄區)。一般而言,這會導致無形資產的攤銷及減值以及收購相關重組及整合項目產生全部税務影響。其他項目通常會受到税務影響,但某些司法管轄區的法律解決產生的項目並非總是如此。由於這些因素以及不同司法管轄區的有效税率不同,為達到税前核心業績而進行的12億美元的總調整税額為4.96億美元。2017年核心税率為17.1%。
|
|||||||||||||
|
5 每股收益(EPS)按諾華製藥股東應佔淨收益金額計算。
|
|||||||||||||
|
|
|||||||||||||
5.b流動資金和資本資源
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
持續經營業務的經營活動現金流量淨額
|
13 547
|
13 049
|
11 419
|
||||
|
已終止經營業務的經營活動現金流量淨額
|
78
|
1 223
|
1 202
|
||||
|
用於持續業務投資活動的現金流量淨額
|
– 1 067
|
– 4 590
|
– 2 344
|
||||
|
用於投資活動的非持續業務現金流量淨額
|
– 1 159
|
– 1 001
|
– 775
|
||||
|
持續經營業務籌資活動所用現金流量淨額
|
– 16 884
|
– 4 077
|
– 7 318
|
||||
|
來自/用於已終止經營業務融資活動的現金流量淨額
|
3 257
|
– 167
|
– 415
|
||||
|
匯率變動對現金及現金等價物的影響
|
69
|
– 26
|
84
|
||||
|
現金和現金等價物淨變化
|
– 2 159
|
4 411
|
1 853
|
||||
|
有價證券、商品、定期存款和衍生金融工具的變化
|
– 2 359
|
2 068
|
– 145
|
||||
|
流動及非流動金融債務及衍生金融工具變動
|
4 764
|
– 3 616
|
– 4 730
|
||||
|
淨債務變動
|
246
|
2 863
|
– 3 022
|
||||
|
截至1月1日的淨債務
|
– 16 184
|
– 19 047
|
– 16 025
|
||||
|
截至12月31日的淨債務
|
– 15 938
|
– 16 184
|
– 19 047
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
非流動金融債務
|
– 20 353
|
– 22 470
|
– 23 224
|
||||
|
流動金融債務和衍生金融工具
|
– 7 031
|
– 9 678
|
– 5 308
|
||||
|
金融債務總額
|
– 27 384
|
– 32 148
|
– 28 532
|
||||
|
流動性減少
|
|
|
|
||||
|
現金和現金等價物
|
11 112
|
13 271
|
8 860
|
||||
|
有價證券、商品、定期存款和衍生金融工具
|
334
|
2 693
|
625
|
||||
|
總流動資金
|
11 446
|
15 964
|
9 485
|
||||
|
截至12月31日的淨債務
|
– 15 938
|
– 16 184
|
– 19 047
|
||||
|
2019
|
|||||||||||||
|
(百萬美元) |
截止日期為 一個月 |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
截止日期晚於
一年 但不到 五年 |
截止日期為 五年 |
總計 |
|||||||
|
流動資產
|
|
|
|
|
|
|
|||||||
|
原到期日超過90天的有價證券、定期存款和短期投資
|
20
|
26
|
16
|
3
|
57
|
122
|
|||||||
|
商品
|
|
|
|
|
110
|
110
|
|||||||
|
衍生金融工具和應計利息
|
14
|
79
|
3
|
3
|
3
|
102
|
|||||||
|
現金和現金等價物
|
9 712
|
1 400
|
|
|
|
11 112
|
|||||||
|
流動金融資產總額
|
9 746
|
1 505
|
19
|
6
|
170
|
11 446
|
|||||||
|
|
|
|
|
|
|
||||||||
|
非流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
|
|
|
– 9 110
|
– 11 243
|
– 20 353
|
|||||||
|
金融債務--未貼現
|
|
|
|
– 9 150
|
– 11 355
|
– 20 505
|
|||||||
|
非流動金融債務共計
|
|
|
|
– 9 110
|
– 11 243
|
– 20 353
|
|||||||
|
|
|
|
|
|
|
||||||||
|
流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
– 4 243
|
– 1 373
|
– 1 230
|
|
|
– 6 846
|
|||||||
|
金融債務--未貼現
|
– 4 243
|
– 1 373
|
– 1 230
|
|
|
– 6 846
|
|||||||
|
衍生金融工具
|
– 130
|
– 29
|
– 26
|
|
|
– 185
|
|||||||
|
流動金融債務總額
|
– 4 373
|
– 1 402
|
– 1 256
|
|
|
– 7 031
|
|||||||
|
|
|
|
|
|
|
||||||||
|
淨債務
|
5 373
|
103
|
– 1 237
|
– 9 104
|
– 11 073
|
– 15 938
|
|||||||
|
2018
|
|||||||||||||
|
(百萬美元) |
截止日期為 一個月 |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
截止日期晚於
一年 但不到 五年 |
截止日期為 五年 |
總計 |
|||||||
|
流動資產
|
|
|
|
|
|
|
|||||||
|
原到期日超過90天的有價證券、定期存款和短期投資
|
39
|
56
|
2 091
|
198
|
63
|
2 447
|
|||||||
|
商品
|
|
|
|
|
104
|
104
|
|||||||
|
衍生金融工具和應計利息
|
40
|
75
|
27
|
|
|
142
|
|||||||
|
現金和現金等價物
|
3 571
|
9 700
|
|
|
|
13 271
|
|||||||
|
流動金融資產總額
|
3 650
|
9 831
|
2 118
|
198
|
167
|
15 964
|
|||||||
|
|
|
|
|
|
|
||||||||
|
非流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
|
|
|
– 8 980
|
– 13 490
|
– 22 470
|
|||||||
|
金融債務--未貼現
|
|
|
|
– 9 025
|
– 13 623
|
– 22 648
|
|||||||
|
非流動金融債務共計
|
|
|
|
– 8 980
|
– 13 490
|
– 22 470
|
|||||||
|
|
|
|
|
|
|
||||||||
|
流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
– 5 217
|
– 4 084
|
– 319
|
|
|
– 9 620
|
|||||||
|
金融債務--未貼現
|
– 5 217
|
– 4 084
|
– 319
|
|
|
– 9 620
|
|||||||
|
衍生金融工具
|
– 16
|
– 34
|
– 8
|
|
|
– 58
|
|||||||
|
流動金融債務總額
|
– 5 233
|
– 4 118
|
– 327
|
|
|
– 9 678
|
|||||||
|
|
|
|
|
|
|
||||||||
|
淨債務
|
– 1 583
|
5 713
|
1 791
|
– 8 782
|
– 13 323
|
– 16 184
|
|||||||
|
流動性 % 2019 1 |
流動性 2018年百分比 1 |
流動性 2017年百分比 1 |
金融
債務(%) 2019 2 |
金融
債務(%) 2018 2 |
金融
債務(%) 2017 2 |
||||||||
|
美元
|
72
|
83
|
77
|
53
|
60
|
63
|
|||||||
|
CHF
|
14
|
7
|
5
|
12
|
10
|
11
|
|||||||
|
歐元
|
7
|
6
|
8
|
29
|
25
|
20
|
|||||||
|
日元
|
1
|
|
1
|
3
|
3
|
4
|
|||||||
|
其他
|
6
|
4
|
9
|
3
|
2
|
2
|
|||||||
|
100
|
100
|
100
|
100
|
100
|
100
|
||||||||
|
1 流動資金包括現金及現金等價物、有價證券、商品及定期存款。
|
|||||||||||||
|
2 金融債務包括非流動金融債務和流動金融債務。
|
|||||||||||||
|
2019
|
2018
|
2017
|
|||||||||||
|
貨幣 |
淨銷售額 % |
運營中
費用 % 1 |
淨銷售額 % |
運營中
費用 % 1 |
淨銷售額 % |
運營中
費用 % 1 |
|||||||
|
美元(U.S.)
|
37
|
36
|
35
|
31
|
36
|
37
|
|||||||
|
歐元(歐元)
|
28
|
26
|
29
|
27
|
28
|
24
|
|||||||
|
瑞士法郎(瑞士法郎)
|
2
|
16
|
2
|
20
|
2
|
17
|
|||||||
|
日元(JPY)
|
6
|
3
|
6
|
3
|
6
|
5
|
|||||||
|
人民幣(CNY)
|
5
|
4
|
4
|
3
|
4
|
3
|
|||||||
|
加元(CAD)
|
3
|
2
|
3
|
2
|
3
|
1
|
|||||||
|
英鎊(GBP)
|
2
|
2
|
2
|
2
|
2
|
2
|
|||||||
|
巴西雷亞爾(BRL)
|
2
|
1
|
2
|
1
|
2
|
1
|
|||||||
|
俄羅斯盧布(盧布)
|
2
|
1
|
2
|
1
|
2
|
1
|
|||||||
|
澳元(AUD)
|
1
|
1
|
1
|
1
|
2
|
1
|
|||||||
|
其他貨幣
|
12
|
8
|
14
|
9
|
13
|
8
|
|||||||
|
1 營業費用包括銷售商品的成本;銷售、一般和行政費用;研究和開發;其他收入和其他費用。
|
|||||||||||||
|
年平均數
|
年終
|
||||||||||||
|
單位美元
|
2019
|
2018
|
變動率%
|
2019
|
2018
|
變動率%
|
|||||||
|
澳元(AUD)
|
0.695
|
0.748
|
– 7
|
0.701
|
0.707
|
– 1
|
|||||||
|
巴西雷亞爾(BRL)
|
0.254
|
0.275
|
– 8
|
0.249
|
0.258
|
– 3
|
|||||||
|
加元(CAD)
|
0.754
|
0.772
|
– 2
|
0.767
|
0.735
|
4
|
|||||||
|
瑞士法郎(瑞士法郎)
|
1.006
|
1.023
|
– 2
|
1.032
|
1.014
|
2
|
|||||||
|
人民幣(CNY)
|
0.145
|
0.151
|
– 4
|
0.144
|
0.145
|
– 1
|
|||||||
|
歐元(歐元)
|
1.120
|
1.181
|
– 5
|
1.121
|
1.144
|
– 2
|
|||||||
|
英鎊(GBP)
|
1.277
|
1.336
|
– 4
|
1.313
|
1.274
|
3
|
|||||||
|
日元(JPY(100))
|
0.918
|
0.906
|
1
|
0.920
|
0.907
|
1
|
|||||||
|
俄羅斯盧布(RUB(100))
|
1.546
|
1.600
|
– 3
|
1.613
|
1.437
|
12
|
|||||||
|
年平均數
|
年終
|
||||||||||||
|
單位美元
|
2018
|
2017
|
變動率%
|
2018
|
2017
|
變動率%
|
|||||||
|
澳元(AUD)
|
0.748
|
0.766
|
– 2
|
0.707
|
0.779
|
– 9
|
|||||||
|
巴西雷亞爾(BRL)
|
0.275
|
0.313
|
– 12
|
0.258
|
0.302
|
– 15
|
|||||||
|
加元(CAD)
|
0.772
|
0.771
|
0
|
0.735
|
0.797
|
– 8
|
|||||||
|
瑞士法郎(瑞士法郎)
|
1.023
|
1.016
|
1
|
1.014
|
1.024
|
– 1
|
|||||||
|
人民幣(CNY)
|
0.151
|
0.148
|
2
|
0.145
|
0.154
|
– 6
|
|||||||
|
歐元(歐元)
|
1.181
|
1.129
|
5
|
1.144
|
1.195
|
– 4
|
|||||||
|
英鎊(GBP)
|
1.336
|
1.288
|
4
|
1.274
|
1.347
|
– 5
|
|||||||
|
日元(JPY(100))
|
0.906
|
0.892
|
2
|
0.907
|
0.888
|
2
|
|||||||
|
俄羅斯盧布(RUB(100))
|
1.600
|
1.715
|
– 7
|
1.437
|
1.734
|
– 17
|
|||||||
|
更改中 美元% 2019 |
更改中
常量 貨幣% 2019 |
百分比
點數貨幣 影響 2019 |
更改中 美元% 2018 |
更改中
常量 貨幣% 2018 |
百分比
點數貨幣 影響 2018 |
||||||||
|
合計組
|
|
|
|
|
|
|
|||||||
|
持續運營對第三方的淨銷售額
|
6
|
9
|
– 3
|
6
|
5
|
1
|
|||||||
|
持續經營的營業收入
|
8
|
14
|
– 6
|
– 3
|
– 3
|
0
|
|||||||
|
持續經營淨收益
|
– 44
|
– 41
|
– 3
|
71
|
71
|
0
|
|||||||
|
持續經營基本每股收益(美元)
|
– 43
|
– 40
|
– 3
|
73
|
73
|
0
|
|||||||
|
持續運營的核心運營收入
|
12
|
17
|
– 5
|
7
|
7
|
0
|
|||||||
|
持續運營的核心淨收入
|
11
|
15
|
– 4
|
4
|
4
|
0
|
|||||||
|
持續運營的核心基本每股收益(美元)
|
12
|
17
|
– 5
|
6
|
5
|
1
|
|||||||
|
|
|
|
|
|
|
||||||||
|
創新藥物
|
|
|
|
|
|
|
|||||||
|
對第三方的淨銷售額
|
8
|
11
|
– 3
|
8
|
8
|
0
|
|||||||
|
營業收入
|
18
|
24
|
– 6
|
4
|
4
|
0
|
|||||||
|
核心營業收入
|
13
|
18
|
– 5
|
11
|
11
|
0
|
|||||||
|
|
|
|
|
|
|
||||||||
|
桑多茲
|
|
|
|
|
|
|
|||||||
|
對第三方的淨銷售額
|
– 1
|
2
|
– 3
|
– 2
|
– 3
|
1
|
|||||||
|
營業收入
|
– 59
|
– 53
|
– 6
|
– 3
|
– 2
|
– 1
|
|||||||
|
核心營業收入
|
5
|
10
|
– 5
|
– 4
|
– 3
|
– 1
|
|||||||
|
|
|
|
|
|
|
||||||||
|
公司
|
|
|
|
|
|
|
|||||||
|
營業虧損
|
6
|
4
|
2
|
NM
|
NM
|
NM
|
|||||||
|
鐵心運行損耗
|
– 6
|
– 9
|
3
|
– 55
|
– 52
|
– 3
|
|||||||
|
|
|||||||||||||
|
NM=沒有意義
|
|||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
持續經營的營業收入
|
9 086
|
8 403
|
8 702
|
||||
|
對非現金項目的調整
|
|
|
|
||||
|
折舊、攤銷和減值
|
5 788
|
5 217
|
4 963
|
||||
|
準備金和其他非流動負債的變化
|
1 871
|
895
|
86
|
||||
|
其他
|
– 476
|
– 229
|
– 465
|
||||
|
經非現金項目調整後的營業收入
|
16 269
|
14 286
|
13 286
|
||||
|
從聯營公司及其他公司收取的股息
|
463
|
719
|
987
|
||||
|
利息及其他財務收入
|
242
|
459
|
97
|
||||
|
利息和其他財務付款
|
– 826
|
– 847
|
– 967
|
||||
|
已繳納的税款
|
– 1 876
|
– 1 506
|
– 1 487
|
||||
|
從準備金和非流動負債中的其他淨現金流動中支付
|
– 924
|
– 638
|
– 829
|
||||
|
存貨和貿易應收款減去貿易應收款的變動
|
– 809
|
– 679
|
– 776
|
||||
|
其他流動資產淨值和其他經營性現金流量項目變動
|
1 008
|
1 255
|
1 108
|
||||
|
來自持續經營的經營活動現金流量淨額
|
13 547
|
13 049
|
11 419
|
||||
|
購置房產、廠房和設備
|
– 1 379
|
– 1 254
|
– 1 325
|
||||
|
出售財產、廠房和設備所得收益
|
857
|
102
|
91
|
||||
|
購買無形資產
|
– 878
|
– 1 394
|
– 969
|
||||
|
出售無形資產所得款項
|
973
|
823
|
640
|
||||
|
購買金融資產
|
– 302
|
– 205
|
– 354
|
||||
|
出售金融資產所得收益 1
|
176
|
165
|
328
|
||||
|
購買其他非流動資產
|
– 60
|
– 39
|
– 40
|
||||
|
出售其他非流動資產所得款項
|
3
|
9
|
1
|
||||
|
持續運營的自由現金流
|
12 937
|
11 256
|
9 791
|
||||
|
非持續經營產生的自由現金流 2
|
– 62
|
461
|
637
|
||||
|
自由現金流總額
|
12 875
|
11 717
|
10 428
|
||||
|
1 就自由現金流量而言,出售金融資產所得款項不包括出售Alcon Inc.部分的現金流入。某些合併基金會通過Alcon分拆獲得的股份,金額為9.76億美元。見"項目18。財務報表—附註2二零一九年重大交易。”
|
|||||||
|
2 2019年,終止經營業務自由現金流量為現金流出6200萬美元(2018年:4.61億美元現金流入,2017年:6.37億美元現金流入)包括7800萬美元來自已終止經營業務的經營活動淨現金流入(2018年和2017年:12億美元),12億美元用於已終止經營的投資活動的淨現金流量(2018年:10億美元,2017年:7.75億美元)經收購和剝離業務淨現金流出3.62億美元調整(2018年:2.39億美元,2017年:2.10億美元)及分拆Alcon業務應佔現金流出6.57億美元(2018年及2017年:無)。
|
|||||||
|
(百萬美元)
|
2019年12月31日
|
2018年12月31日
|
變化
|
||||
|
資產
|
|
|
|
||||
|
財產、廠房和設備
|
12 069
|
15 696
|
– 3 627
|
||||
|
使用權資產
|
1 677
|
|
1 677
|
||||
|
商譽
|
26 524
|
35 294
|
– 8 770
|
||||
|
商譽以外的無形資產
|
28 787
|
38 719
|
– 9 932
|
||||
|
金融資產和其他非流動資產
|
19 809
|
20 291
|
– 482
|
||||
|
非流動資產總額
|
88 866
|
110 000
|
– 21 134
|
||||
|
盤存
|
5 982
|
6 956
|
– 974
|
||||
|
應收貿易賬款
|
8 301
|
8 727
|
– 426
|
||||
|
其他流動資產及應收所得税
|
2 934
|
3 109
|
– 175
|
||||
|
現金、有價證券、商品、定期存款和衍生金融工具
|
11 446
|
15 964
|
– 4 518
|
||||
|
出售集團持有待售資產
|
841
|
807
|
34
|
||||
|
流動資產總額
|
29 504
|
35 563
|
– 6 059
|
||||
|
總資產
|
118 370
|
145 563
|
– 27 193
|
||||
|
權益和負債
|
|
|
|
||||
|
總股本
|
55 551
|
78 692
|
– 23 141
|
||||
|
金融債務
|
20 353
|
22 470
|
– 2 117
|
||||
|
租賃負債
|
1 703
|
|
1 703
|
||||
|
遞延税項負債
|
5 867
|
7 475
|
– 1 608
|
||||
|
準備金和其他非流動負債
|
6 632
|
7 319
|
– 687
|
||||
|
非流動負債總額
|
34 555
|
37 264
|
– 2 709
|
||||
|
貿易應付款
|
5 424
|
5 556
|
– 132
|
||||
|
金融債務和衍生金融工具
|
7 031
|
9 678
|
– 2 647
|
||||
|
租賃負債
|
246
|
|
246
|
||||
|
準備金及其他流動負債和流動所得税責任
|
15 532
|
14 322
|
1 210
|
||||
|
出售集團持有待售資產的負債
|
31
|
51
|
– 20
|
||||
|
流動負債總額
|
28 264
|
29 607
|
– 1 343
|
||||
|
總負債
|
62 819
|
66 871
|
– 4 052
|
||||
|
權益和負債總額
|
118 370
|
145 563
|
– 27 193
|
||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
未逾期
|
7 763
|
7 916
|
|||
|
逾期不超過一個月
|
161
|
296
|
|||
|
逾期一個月以上三個月以下
|
123
|
194
|
|||
|
逾期三個月以上六個月以下
|
103
|
136
|
|||
|
逾期六個月以上一年以下
|
96
|
98
|
|||
|
逾期一年以上
|
150
|
213
|
|||
|
可疑貿易應收賬款撥備
|
– 95
|
– 126
|
|||
|
應收貿易賬款總額,淨額
|
8 301
|
8 727
|
|||
|
已發行股份數(百萬股)
|
諾華股份公司股東應佔已發行股本和儲備
|
||||||||||||
|
2019 |
2018 |
變化 |
2019
數百萬美元 |
2018
數百萬美元 |
變化
數百萬美元 |
||||||||
|
年初餘額
|
2 311.2
|
2 317.5
|
– 6.3
|
78 614
|
74 168
|
4 446
|
|||||||
|
會計政策變化的影響 1
|
|
|
|
3
|
60
|
– 57
|
|||||||
|
於1月1日重列權益
|
|
|
|
78 617
|
74 228
|
4 389
|
|||||||
|
被收購的股份將被註銷
|
– 60.3
|
– 23.3
|
– 37.0
|
– 5 351
|
– 1 859
|
– 3 492
|
|||||||
|
其他股票購買
|
– 1.7
|
– 1.2
|
– 0.5
|
– 160
|
– 114
|
– 46
|
|||||||
|
行使期權和員工交易
|
5.5
|
7.8
|
– 2.3
|
210
|
434
|
– 224
|
|||||||
|
其他股份銷售
|
|
3.0
|
– 3.0
|
|
263
|
– 263
|
|||||||
|
基於股權的薪酬
|
9.4
|
7.4
|
2.0
|
833
|
756
|
77
|
|||||||
|
由於Alcon分拆而交付給Alcon員工的股份
|
0.9
|
|
0.9
|
18
|
|
18
|
|||||||
|
庫藏股交易税 2
|
|
|
|
– 189
|
|
– 189
|
|||||||
|
股份回購交易計劃下庫存股回購義務減少/(增加)
|
|
|
|
284
|
– 284
|
568
|
|||||||
|
交易成本,税後淨額 3
|
|
|
|
– 253
|
– 79
|
– 174
|
|||||||
|
分紅
|
|
|
|
– 6 645
|
– 6 966
|
321
|
|||||||
|
實物股息,以實現愛爾康公司的剝離。 4
|
|
|
|
– 23 434
|
|
– 23 434
|
|||||||
|
諾華股份公司股東應佔年度淨收入
|
|
|
|
11 732
|
12 611
|
– 879
|
|||||||
|
合併實體所有權變更的影響
|
|
|
|
– 3
|
– 13
|
10
|
|||||||
|
Novartis AG股東應佔其他全面收益
|
|
|
|
– 207
|
– 401
|
194
|
|||||||
|
其他動作 5
|
|
|
|
22
|
38
|
– 16
|
|||||||
|
年終餘額
|
2 265.0
|
2 311.2
|
– 46.2
|
55 474
|
78 614
|
– 23 140
|
|||||||
|
1 2019年,會計政策變更的影響包括與實施國際財務報告準則第16號租賃有關的300萬美元(見“第18項。財務報表—注1。重大會計政策”)。2018年,會計政策變更的影響包括與實施IFRS 15有關的6000萬美元,以及與實施IFRS 9有關的1.77億美元。
|
|||||||||||||
|
2 2019年計入與庫藏股遞延税項負債重估有關的6900萬美元影響。這一重估源於2019年5月頒佈的瑞士聯邦税制改革(見“項目18.財務報表--附註12.遞延税項資產和負債”)。
|
|||||||||||||
|
3 交易成本,扣除税項3600萬美元(2018年:2000萬美元),直接歸因於向諾華股東潛在分配(分拆)。財務報表—注1。重大會計政策”)。
|
|||||||||||||
|
4 Alcon Inc.的實物股息公允價值。在2019年2月28日舉行的2019年年度股東大會上批准的諾華股份和ADR(美國存託憑證)持有人。分派於2019年4月8日生效,據此,諾華股份公司的每位股東和ADR持有人獲得了一個Alcon Inc.。2019年4月8日營業結束時,每持有5股諾華股份/美國存託憑證(見“項目18。財務報表—注1。重大會計政策”)。
|
|||||||||||||
|
5 惡性通貨膨脹經濟體的影響(見"項目18。財務報表—注1。重大會計政策”)。
|
|||||||||||||
5.研究和開發、專利和許可證
5.D趨勢信息
5.E資產負債表外安排
5.F合同義務的表格披露
|
按期間到期的付款
|
|||||||||||
|
(百萬美元) |
總計 |
少於
1年 |
2-3年 |
4-5年 |
之後
5年 |
||||||
|
非流動金融債務,包括當期部分
|
22 355
|
2 002
|
4 650
|
4 460
|
11 243
|
||||||
|
非流動金融債務利息,包括當期部分
|
5 434
|
464
|
845
|
686
|
3 439
|
||||||
|
租賃負債,非流動部分和流動部分
|
1 949
|
246
|
365
|
257
|
1 081
|
||||||
|
租賃負債利息,非流動部分和流動部分
|
1 536
|
49
|
83
|
66
|
1 338
|
||||||
|
資金不足的養卹金和其他離職後福利計劃
|
1 748
|
101
|
201
|
208
|
1 238
|
||||||
|
研發潛力里程碑承諾
|
4 404
|
809
|
761
|
891
|
1 943
|
||||||
|
或有對價負債
|
1 036
|
71
|
352
|
230
|
383
|
||||||
|
不動產、廠場和設備購置承付款
|
220
|
177
|
43
|
|
|
||||||
|
收購業務承諾 1
|
10 164
|
10 130
|
34
|
|
|
||||||
|
合同現金債務總額
|
48 846
|
14 049
|
7 334
|
6 798
|
20 665
|
||||||
|
1 有關收購業務承諾,請參閲“第18項。財務報表—附註2重大交易—重大待決交易"。
|
|||||||||||
項目6.董事、高級管理人員和僱員
6.董事和高級管理人員
6.B補償
薪酬一覽
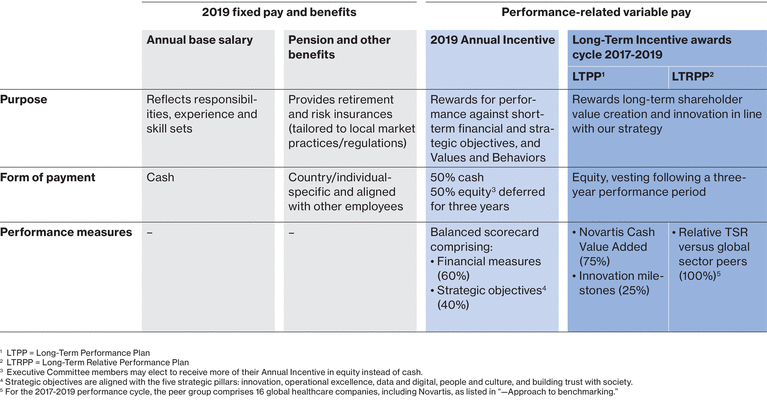
|
決定
|
決策權
|
||
|
董事會主席和其他成員的報酬
|
董事會
|
||
|
CEO薪酬
|
董事會
|
||
|
執行委員會其他成員的報酬
|
薪酬委員會
|
||
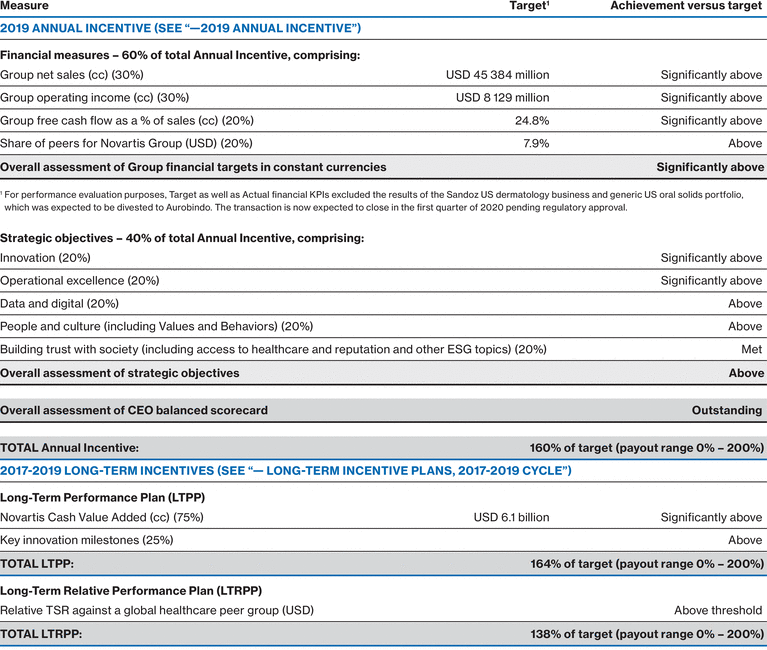
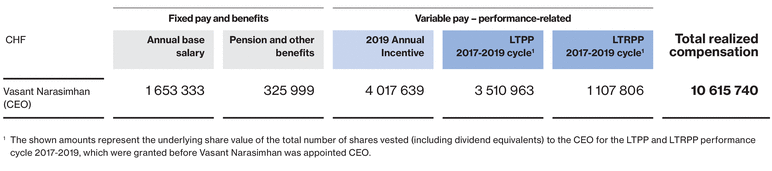
|
千瑞士法郎 |
2019-2020年度股東大會
年費 |
||
|
董事會主席
|
3 800
|
||
|
董事會成員
|
280
|
||
|
副主席
|
50
|
||
|
審計和合規委員會主席
|
130
|
||
|
薪酬委員會主席
|
90
|
||
|
以下委員會主席:
·治理、提名和企業責任委員會 ·研發委員會 ·風險委員會 |
70 |
||
|
審計和遵約委員會成員
|
70
|
||
|
下列委員會的成員:
·薪酬委員會 ·治理、提名和企業責任委員會 ·研發委員會 ·風險委員會 |
40 |
||
|
千瑞士法郎 |
2019
總薪酬 1 |
||
|
董事會主席
|
3 804
|
||
|
董事會其他12名成員
|
4 387
|
||
|
總計
|
8 191
|
||
|
1 包括諾華公司向政府社會保障體系支付的21 002瑞士法郎的強制性僱主繳款。這一數額是從僱主繳款總額413 '985瑞士法郎中扣除的,併為董事會成員提供了獲得未來最高保險政府養卹金福利的權利。
|
|||
執行委員會薪酬理念和原則
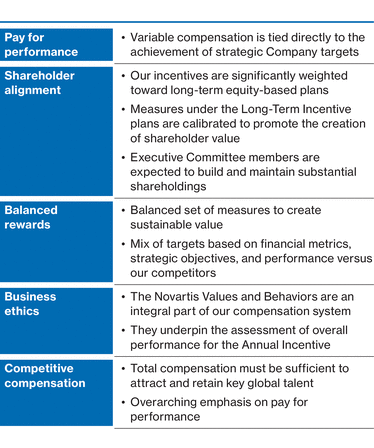
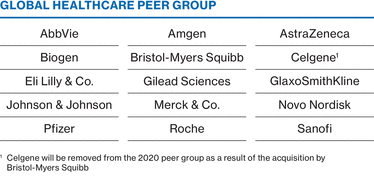
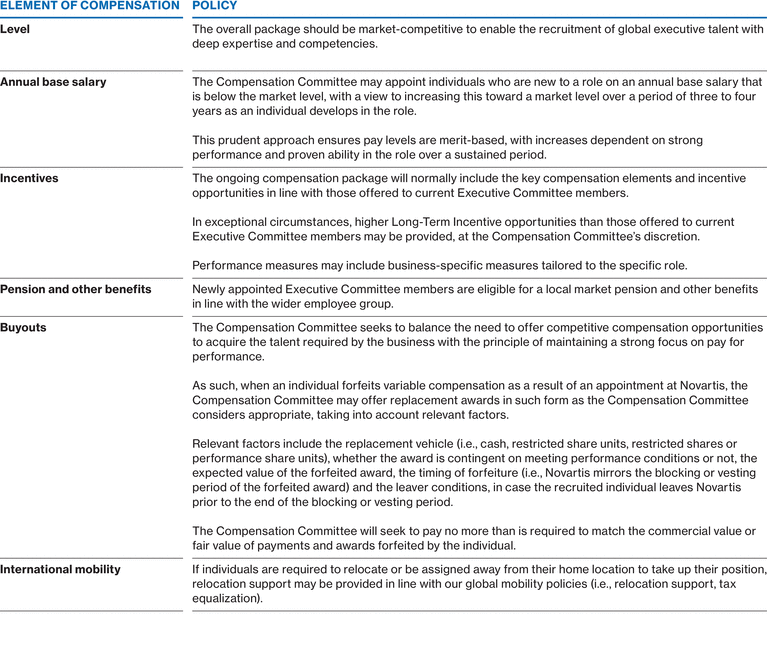
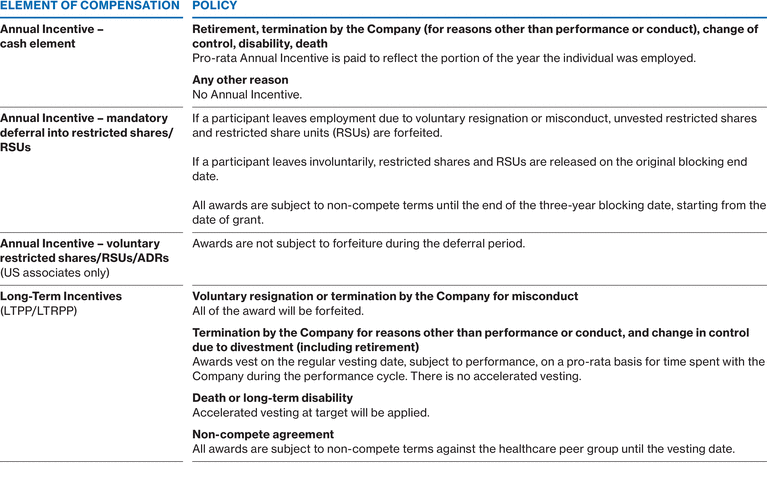

2019年執行委員會薪酬
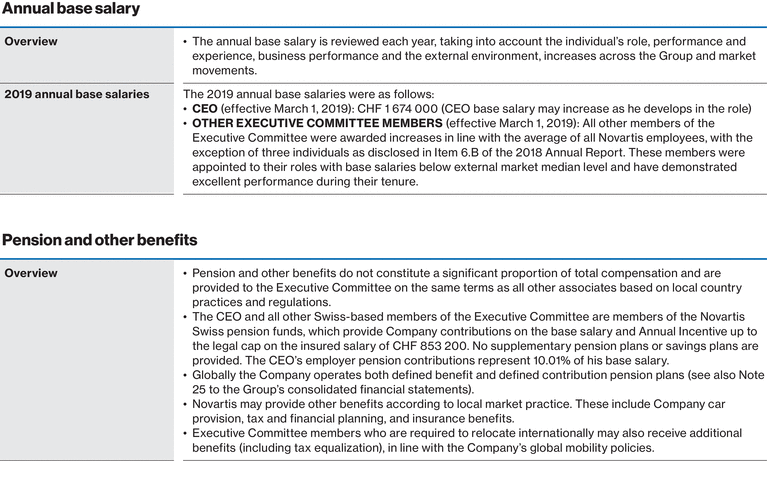
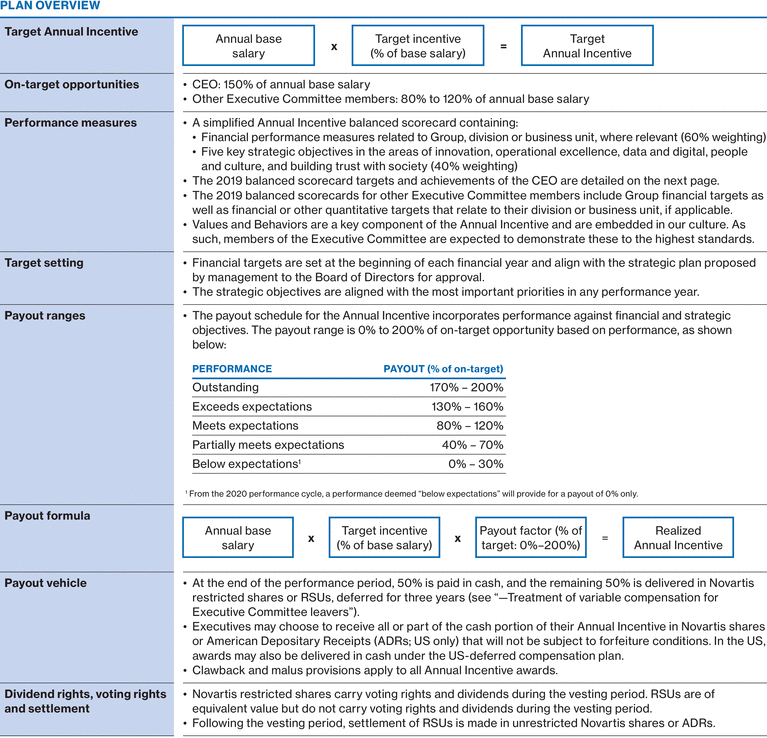
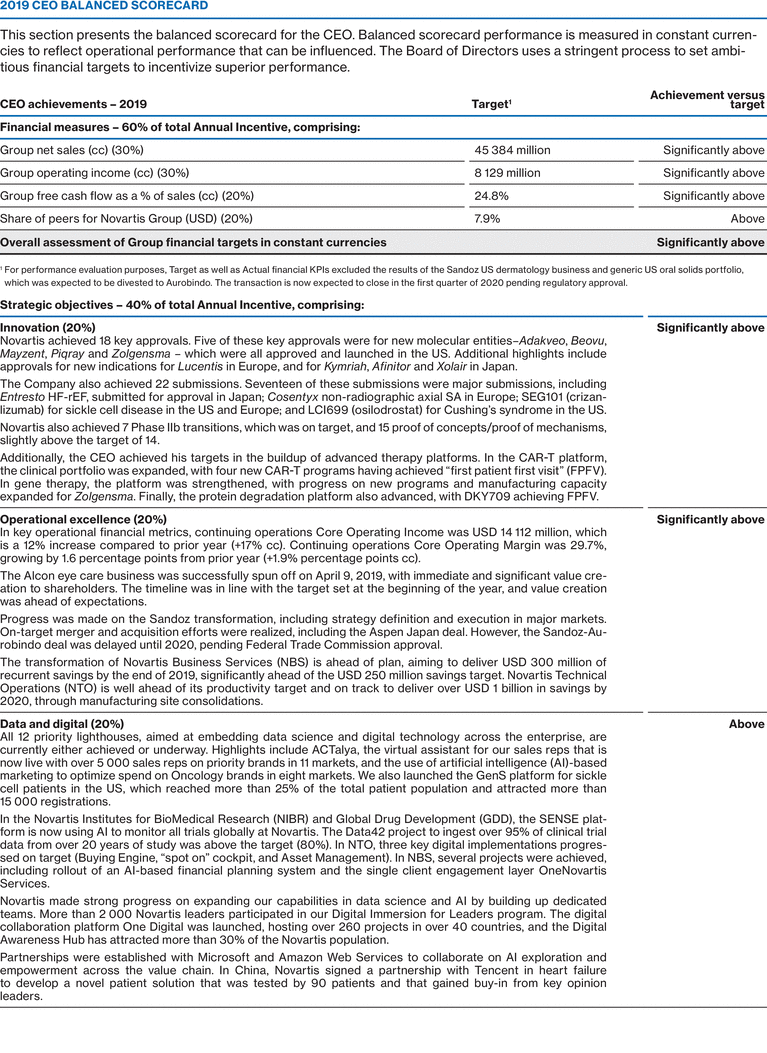

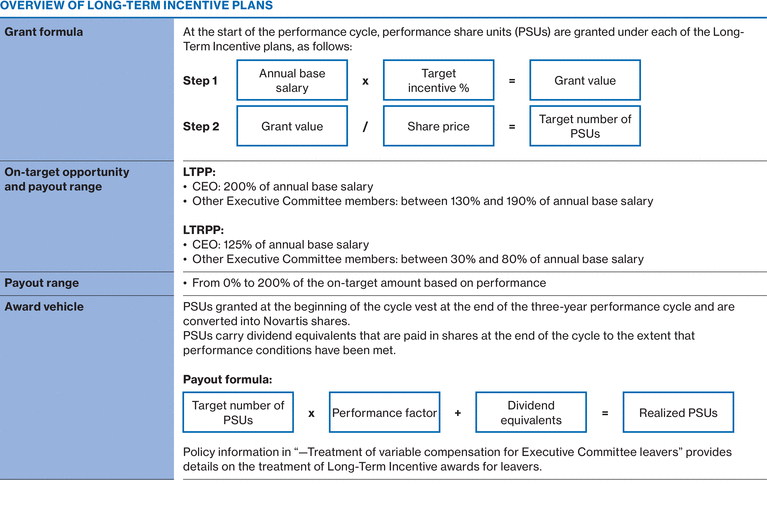

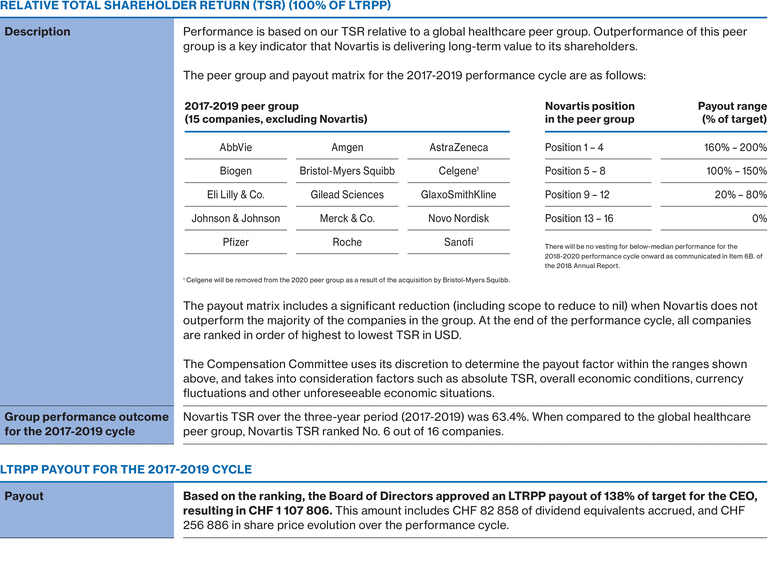
|
名字
|
任命之日
|
現金支付(瑞士法郎)
|
股權獎勵
|
授予時的總價值
|
||
|
理查德·塞諾
|
2019年7月15日
|
157 087
|
1 034 803
|
1 191 890
|
||
|
首席執行官,Sandoz
|
|
|
相當於4,172個PSU和7,280個RSU,在2020—2022年期間歸屬
|
|
||
|
|
||||||
|
|
2019年度基薪
|
2019年養老金福利1
|
2019年度獎勵
|
長期激勵
|
2019年其他補償
|
|
|||||||||||||
|
|
|
|
|
|
LTPP 2017—2019週期
|
LTRPP 2017—2019週期
|
|
|
|||||||||||
|
貨幣 |
現金(金額) |
金額 |
現金 |
權益2 |
價值(Value) (於歸屬日期)3 |
股權(價值 (於歸屬日期)3 |
金額2,4,5 |
已實現總收益
補償 (包括分享 價格變動)6 |
|||||||||||
|
執行委員會成員
|
|||||||||||||||||||
|
Yu Sheng(CEO)
|
CHF
|
1 653 333
|
165 547
|
2 008 800
|
2 008 839
|
3 510 963
|
1 107 806
|
160 452
|
10 615 740
|
||||||||||
|
其他14名執行委員會成員(包括在2019財政年度辭職的兩名成員)的實際薪酬總額 7, 8
|
CHF
|
9 370 547
|
2 131 905
|
5 809 455
|
7 013 842
|
17 932 704
|
6 383 700
|
7 233 594
|
55 875 748
|
||||||||||
|
總計
|
CHF
|
11 023 880
|
2 297 452
|
7 818 255
|
9 022 682
|
21 443 667
|
7 491 506
|
7 394 046
|
66 491 488
|
||||||||||
|
2018年的比較數字見“--CEO和其他執行委員會成員的2018年已實現薪酬”。
|
|||||||||||||||||||
|
1 包括諾華公司向政府社會保障體系支付的僱主強制性繳款:CEO 4'373瑞士法郎,執行委員會其他成員63'461瑞士法郎。該金額是2019年為所有執行委員會成員支付的僱主繳款總額3'923 '070瑞士法郎中的,併為執行委員會成員提供了獲得未來最高保險政府養老金福利的權利。
|
|||||||||||||||||||
|
2 以股權形式交付的年度獎勵部分按授予日期(2020年1月21日)每股諾華股份92. 89瑞士法郎和每股ADR 95. 19美元的收盤價四捨五入至最接近的股份。
|
|||||||||||||||||||
|
3 該金額指於2020年1月17日歸屬於首席執行官及其他執行委員會成員的232 '425個LTPP PSU及77'904個LTPP PSU的相關股份價值,包括三年週期的賺取股息等值(詳見“—2017—2019年績效週期LTPP和2017—2019年績效週期LTPP”)應課税價值採用諾華董事會批准LTPP和LTRPP最終業績因素當日的收盤股價確定(即,2020年1月21日)每股諾華股份92.89美元,每股ADR 95.19美元。Shannon Thyme Klinger、Stefan Lang、Susanne Schaffert及Marie—France Tschudin於2017—2019年業績期間獲晉升為執行委員會成員,因此,所披露的資料反映了彼等於2017—2019年LTPP及LTRPP的按比例支出。Bertrand Bodson、Klaus Moosmayer、John Tsai、Robert Weltevreden和Richard Saynor在2017年LTI頒獎後加入諾華,因此在2017—2019年的演出期間沒有獲得LTPP和LTRPP獎項。
|
|||||||||||||||||||
|
4 根據全球流動政策,包括任何其他津貼、實物福利、國際外派福利(例如,在退任日期後,該等權益包括住房、國際醫療保險、兒童學費、衡平税)以及LTPP及LTRP下的既得股份。
|
|||||||||||||||||||
|
5 包括5430個既得受限制股份單位2019年7月28日(502 003瑞士法郎),以代替他在離開前僱主時沒收的長期利息及1323個既得受限制單位(123 092瑞士法郎)和14470個PSU(1 346 289瑞士法郎)於2019年3月24日歸屬給Paul Hudson,以代替他離開前僱主時沒收的長期利息。PSU在2016—2018年績效週期中採用與LTPP相同的績效指標(NCVA和長期創新)。
|
|||||||||||||||||||
|
6 所有數額均在扣除執行委員會成員應繳的社會保障繳費和所得税之前。
|
|||||||||||||||||||
|
7 根據計劃規則,包括Sandoz前首席執行官Richard Francis的薪酬,包括其2017—2019績效週期的長期獎勵。Paul Hudson之未歸屬股份於彼離開本公司時被沒收。詳情見"執行委員會成員離職"。
|
|||||||||||||||||||
|
8 以美元支付的執行委員會成員款項按1. 00美元= 0. 9938瑞士法郎的匯率換算,與本集團2019年合併財務報表所用的平均匯率相同。
|
|||||||||||||||||||
|
贈款時的PSU
|
|
歸屬時交付的股份
|
|||||||||||||||
|
PSU (目標數量) |
PSU (目標值 授出日期) (瑞士法郎) 2 |
支出係數 對於LTPP (目標的百分比) |
業績股 在歸屬時交付 (數字) |
業績股 在歸屬時交付 (歸屬日期的價值) (瑞士法郎) 3 |
分紅 等值股份 在歸屬時交付 (數字) 4 |
分紅
等值股份 在歸屬時交付 (歸屬日期的價值) (瑞士法郎) |
總股份數
在歸屬時交付 (價值在 歸屬日期) (瑞士法郎) |
||||||||||
|
執行委員會成員 1
|
|
|
|
|
|
|
|
|
|||||||||
|
Vasant Narasimhan
|
21 323
|
1 980 693
|
164%
|
34 970
|
3 248 363
|
2 827
|
262 600
|
3 510 963
|
|||||||||
|
其他14名執行委員會成員,包括在2019財政年度辭職的兩名成員 5
|
109 616
|
10 247 244
|
164%
|
178 984
|
16 735 046
|
13 151
|
1 227 397
|
17 932 704
|
|||||||||
|
總計
|
130 939
|
12 227 938
|
|
213 954
|
19 983 409
|
15 978
|
1 489 997
|
21 443 667
|
|||||||||
|
1 Shannon Thyme Klinger、Stefan Lang、Susanne Schaffert和Marie—France Tschudin於2017—2019年業績期間加入執行委員會。因此,所披露的資料反映了他們作為執行委員會成員期間的按比例LTPP 2017—2019支出。Bertrand Bodson、Klaus Moosmayer、John Tsai、Robert Weltevreden和Richard Saynor在2017年LTPP頒獎典禮後加入諾華,因此在2017—2019年的演出期間沒有獲得LTPP獎項。
|
|||||||||||||||||
|
2 所示金額代表2017—2019年業績期間授予各執行委員會成員的PSU目標數量的基礎股份價值,基於授予日期(2017年1月17日)的收盤價每股諾華股份71. 35瑞士法郎和每股ADR 71. 99美元。
|
|||||||||||||||||
|
3 所示金額代表2017—2019年業績期間歸屬的目標數量PSU的相關股份價值,基於諾華董事會批准最終LTPP和LTRPP業績支付因素當日的最後收盤股價(即,2020年1月21日)每股諾華股份92.89瑞士法郎,每股ADR 95.19美元。
|
|||||||||||||||||
|
4 股息等值股份乃根據執行委員會各成員於二零一七年至二零一九年表現期末實際交付之股份數目而收取之股息計算。在歸屬時,股息等價物計入股份或美國存託憑證。
|
|||||||||||||||||
|
5 根據計劃規則,包括Sandoz前首席執行官Richard Francis在2017—2019年績效週期的LTPP歸屬。諾華製藥前首席執行官Paul Hudson的LTPP歸屬於2019年8月31日,他離開本公司時被沒收。更多詳情請參見"—LTPP績效結果"。
|
|||||||||||||||||
|
贈款時的PSU
|
|
歸屬時交付的股份
|
|||||||||||||||
|
PSU (目標數量) |
PSU (目標值 授出日期) (瑞士法郎) 2 |
支出係數 對於LTRPP (目標的百分比) |
業績股 在歸屬時交付 (數字) |
業績股 在歸屬時交付 (歸屬日期的價值) (瑞士法郎) 3 |
分紅 等值股份 在歸屬時交付 (數字) 4 |
分紅
等值股份 在歸屬時交付 (歸屬日期的價值) (瑞士法郎) |
總股份數
在歸屬時交付 (價值在 歸屬日期) (瑞士法郎) |
||||||||||
|
執行委員會成員 1
|
|
|
|
|
|
|
|
|
|||||||||
|
Vasant Narasimhan
|
7 996
|
742 748
|
138%
|
11 034
|
1 024 948
|
892
|
82 858
|
1 107 806
|
|||||||||
|
其他14名執行委員會成員,包括在2019財政年度辭職的兩名成員 5
|
45 858
|
4 290 344
|
138%
|
63 283
|
5 920 579
|
5 077
|
474 933
|
6 383 700
|
|||||||||
|
總計
|
53 854
|
5 033 093
|
|
74 317
|
6 945 527
|
5 969
|
557 791
|
7 491 506
|
|||||||||
|
1 Shannon Thyme Klinger、Stefan Lang、Susanne Schaffert和Marie—France Tschudin於2017—2019年業績期間加入執行委員會。因此,所披露的資料反映彼等擔任執行委員會成員期間的按比例於二零一七年至二零一九年長期發展與投資計劃支出。Bertrand Bodson、Klaus Moosmayer、John Tsai、Robert Weltevreden和Richard Saynor在2017年LTRPP頒獎典禮後加入諾華,因此在2017—2019年的演出期間沒有獲得LTRPP獎項。
|
|||||||||||||||||
|
2 所示金額代表2017—2019年業績期間授予各執行委員會成員的PSU目標數量的基礎股份價值,基於授予日期(2017年1月17日)的收盤價每股諾華股份71. 35瑞士法郎和每股ADR 71. 99美元。
|
|||||||||||||||||
|
3 所示金額代表2017—2019年業績期間歸屬的目標數量PSU的相關股份價值,基於諾華董事會批准最終LTPP和LTRPP業績支付因素當日的最後收盤股價(即,2020年1月21日)每股諾華股份92.89瑞士法郎,每股ADR 95.19美元。
|
|||||||||||||||||
|
4 股息等值股份乃根據執行委員會各成員於二零一七年至二零一九年表現期末實際交付之股份數目而收取之股息計算。在歸屬時,股息等價物計入股份或美國存託憑證。
|
|||||||||||||||||
|
5 根據計劃規則,包括Sandoz首席執行官2017—2019績效週期的LTRPP歸屬。Paul Hudson於二零一九年八月三十一日離開本公司時,其歸屬的LTRPP已被沒收。更多詳情請參見"—LTRPP績效結果"。
|
|||||||||||||||||
|
|
2018年年度基薪
|
2018年養老金福利1
|
2018年度獎勵
|
長期激勵
|
2018年其他補償
|
||||||||||||||
|
|
|
|
|
|
LTPP 2016—2018週期
|
LTRPP 2016—2018週期
|
|
|
|||||||||||
|
貨幣 |
現金(金額) |
金額 |
現金 |
權益2 |
價值(Value) (於歸屬日期)3 |
股權(價值 (於歸屬日期) |
金額2,4 |
已實現總收益
補償 (包括分享 價格變動)5 |
|||||||||||
|
執行委員會成員
|
|||||||||||||||||||
|
Vasant Narasimhan(2018年2月1日起擔任CEO)
|
CHF
|
1 491 667
|
168 233
|
1 594 801
|
1 594 805
|
1 796 381
|
0
|
34 401
|
6 680 288
|
||||||||||
|
執行委員會其他16名成員的實際薪酬總額,包括2018財政年度辭職的4名成員 6, 7
|
CHF
|
9 297 021
|
1 874 671
|
5 727 765
|
5 532 316
|
24 079 974
|
0
|
13 131 653
|
59 643 400
|
||||||||||
|
總計
|
CHF
|
10 788 688
|
2 042 904 1
|
7 322 566
|
7 127 121
|
25 876 355
|
0
|
13 166 054
|
66 323 688
|
||||||||||
|
1 包括首席執行官的強制性僱主繳費4336瑞士法郎,以及諾華公司向政府社會保障系統支付的執行委員會其他成員的強制性僱主繳費78403瑞士法郎。這一數額來自2018年為執行委員會所有成員支付的2 847 422瑞士法郎的僱主繳費總額,併為執行委員會成員提供了獲得未來最高保險政府養老金福利的權利。
|
|||||||||||||||||||
|
2 以股權形式交付的年度激勵部分將根據授予日(2019年1月22日)的收盤價(每股諾華股票88.14瑞士法郎,每股美國存託憑證88.32美元)向上舍入到最近的股票。
|
|||||||||||||||||||
|
3 這些金額代表於2019年1月22日歸屬首席執行官和其他執行委員會成員的294 971個PSU在2016-2018年度業績週期的基本股票價值,包括三年週期的賺取股息等價物。應税價值是根據諾華董事會批准最終LTPP和LTRPP業績因數當日(即2019年1月22日)的收盤價確定的,每股諾華股票88.14瑞士法郎,每股美國存託憑證88.32美元。Vasant Narasimhan、Shannon Thyme Klinger、Stefan Lang和AndréWyss於2016-2018年期間加入執行委員會,因此,披露的信息反映了他們在擔任執行委員會成員期間按比例支付的2016-2018年度LTPP股息。伊麗莎白·巴雷特、伯特蘭·博德森、保羅·哈德森、克勞斯·穆斯邁爾、約翰·蔡崇信和羅伯特·韋爾特夫雷登在2016年LTPP獎頒發後加入,因此沒有獲得2016-2018年的LTPP獎。
|
|||||||||||||||||||
|
4 包括任何其他福利、實物福利、全球流動政策規定的國際派任福利(例如住房、國際醫療保險、子女學費、税收均衡),以及在退役日期後長期合作伙伴關係下的既得股份。
|
|||||||||||||||||||
|
5 所有數額均在扣除執行委員會成員應繳的社會保障繳費和所得税之前。
|
|||||||||||||||||||
|
6 包括即將離任的首席執行官、總法律顧問、愛爾康首席執行官和諾華瑞士業務和國家總裁的總裁的薪酬,包括根據計劃規則授予他們在2016年至2018年業績週期的長期激勵。
|
|||||||||||||||||||
|
7 執行委員會成員以美元支付的金額按1.00美元=0.978瑞士法郎的匯率折算,這與集團2018年綜合財務報表使用的平均匯率相同。
|
|||||||||||||||||||
|
|
固定薪酬和養卹金福利
|
可變薪酬
|
|
||||||||||||||
|
|
2019年實際支付或批准的補償
|
2019—2021年長期激勵性週期贈款達到目標
|
|
|
|||||||||||||
|
|
2019年度基薪
|
2019年養老金福利
|
2019年度獎勵 (取得的業績)
|
ltpp 2019—2021週期
|
2019年其他補償
|
總 補償 支付、承諾或授予2019年
|
|||||||||||
|
貨幣 |
現金 (金額) |
金額 1 |
現金 (金額) |
權益
(價值在 授予日期) 2 |
PSU
(目標值 授出日期) 3 |
金額 4 |
金額 5 |
||||||||||
|
執行委員會成員活躍於2019年12月31日
|
|||||||||||||||||
|
Vasant Narasimhan
|
CHF
|
1 653 333
|
165 547
|
2 008 800
|
2 008 839
|
5 440 530
|
160 452
|
11 437 501
|
|||||||||
|
史蒂文·伯特
|
CHF
|
789 750
|
161 454
|
633 360
|
633 417
|
1 662 585
|
124 979
|
4 005 545
|
|||||||||
|
貝特朗·博德森
|
CHF
|
607 500
|
170 178
|
341 040
|
341 092
|
974 476
|
137 826
|
2 572 111
|
|||||||||
|
詹姆斯·布拉德納 6
|
美元
|
1 126 781
|
359 961
|
951 720
|
951 805
|
2 832 511
|
85 498
|
6 308 275
|
|||||||||
|
哈里·基爾希
|
CHF
|
1 053 000
|
164 467
|
1 045 044
|
1 045 105
|
2 744 591
|
27 658
|
6 079 865
|
|||||||||
|
香農百里香克林格
|
CHF
|
783 333
|
188 990
|
468 000
|
468 073
|
1 600 005
|
111 375
|
3 619 776
|
|||||||||
|
斯特芬·朗
|
CHF
|
745 000
|
167 815
|
408 000
|
612 145
|
1 200 026
|
9 810
|
3 142 796
|
|||||||||
|
克勞斯·莫斯邁爾
|
CHF
|
500 000
|
125 483
|
260 000
|
260 092
|
800 047
|
171 749
|
2 117 371
|
|||||||||
|
Richard Saynor(2019年7月15日) 7
|
CHF
|
356 021
|
87 118
|
179 315
|
179 371
|
–
|
1 950 908
|
2 752 732
|
|||||||||
|
蘇珊娜·沙弗特 7
|
CHF
|
850 000
|
167 096
|
459 000
|
1 071 115
|
1 870 066
|
160 252
|
4 577 528
|
|||||||||
|
蔡俊華
|
CHF
|
858 333
|
181 048
|
602 000
|
602 020
|
2 064 063
|
377 544
|
4 685 007
|
|||||||||
|
Marie—France Tschudin(2019年6月7日起) 7
|
CHF
|
481 667
|
92 090
|
290 630
|
290 653
|
968 249
|
–
|
2 123 289
|
|||||||||
|
羅伯特·韋爾特夫雷登
|
CHF
|
607 500
|
157 423
|
158 340
|
475 132
|
974 476
|
4 860
|
2 377 731
|
|||||||||
|
小計
|
|
10 405 223
|
2 186 434
|
7 799 341
|
8 932 950
|
23 114 040
|
3 322 378
|
55 760 366
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
2019年卸任的執行委員會成員
|
|||||||||||||||||
|
Richard Francis(至2019年3月19日) 8, 9
|
CHF
|
179 315
|
36 025
|
18 914
|
37 435
|
720 460
|
3 808 445
|
4 800 594
|
|||||||||
|
Paul Hudson(至2019年6月7日) 9, 10
|
CHF
|
439 342
|
74 994
|
–
|
–
|
270 451
|
2 885 164
|
3 669 950
|
|||||||||
|
小計
|
|
618 657
|
111 018
|
18 914
|
37 435
|
990 910
|
6 693 609
|
8 470 543
|
|||||||||
|
總計
|
|
11 023 880
|
2 297 452
|
7 818 255
|
8 970 384
|
24 104 951
|
10 015 988
|
64 230 910
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
基於假設100%的支出目標。實際支出(目標的0—200%)將於二零二二年一月三年週期結束時公佈。
|
|
|
|
||||
|
2018年的比較數據見下一頁。
|
|||||||||||||||||
|
1 包括諾華公司向政府社會保障體系支付的僱主強制性繳款:CEO 4'373瑞士法郎,執行委員會其他成員63'461瑞士法郎。該金額是2019年為所有執行委員會成員支付的僱主繳款總額3'923 '070瑞士法郎中的,併為執行委員會成員提供了獲得未來最高保險政府養老金福利的權利。
|
|||||||||||||||||
|
2 以股權形式交付的年度獎勵部分按授予日期(2020年1月21日)每股諾華股份92. 89瑞士法郎和每股ADR 95. 19美元的收盤價四捨五入至最接近的股份。
|
|||||||||||||||||
|
3 這些金額代表2019-2021年業績週期授予執行委員會成員的目標數量PSU的基本股票價值,基於授予日期(2019年1月22日)諾華股票每股88.14瑞士法郎和美國存託憑證每股88.32美元的收盤價,除Richard Saynor先生外,他在年度授予日期不是公司的一部分,因此沒有獲得LTPP獎勵。
|
|||||||||||||||||
|
4 根據全球流動政策,包括任何其他津貼、實物福利和國際外派福利(例如,住房、國際健康保險、兒童學費、衡平徵税)
|
|||||||||||||||||
|
5 所有數額均在扣除執行委員會成員應繳的社會保障繳費和所得税之前。
|
|||||||||||||||||
|
6 James Bradner的美元金額按1.00瑞士法郎=1.006美元的匯率轉換,這是本集團2019年合併財務報表使用的平均匯率。
|
|||||||||||||||||
|
7 對於那些於2019年加入執行委員會的成員,“2019年實際支付或發放的報酬”和“按目標計算的2019-2021年長期獎勵週期贈款”欄下的資料包括從他們加入執行委員會之日起至2019年12月31日止至業績週期結束時按比例計算的報酬,如果是“按目標計算的2019-2021年長期獎勵週期贈款”。
|
|||||||||||||||||
|
8 理查德·弗朗西斯於2019年3月19日辭去Sandoz首席執行官一職,並將根據合同通知期於2020年3月31日離開公司。在通知期結束之前,他將獲得進一步的合同補償,包括基本工資、年度獎勵和養老金福利。根據計劃規則,LTPP 2019-2021年週期贈款(21 217 PSU)全部包括在上表中,將根據業績週期內諾華公司的僱傭月數按比例在正常歸屬日期按比例授予。這筆贈款的授予取決於在期末評估的業績條件。
|
|||||||||||||||||
|
9 對於那些離開執行委員會的成員,“2019年實際支付或發放的報酬”和“按目標計算的2019-2021年週期贈款長期獎勵”一欄反映了他們擔任執行委員會成員期間按比例支付的報酬。“2019年其他報酬”一欄除其他外,包括他們從離開執行委員會之日起至2019年12月31日期間的按比例報酬,或在“按目標提供的2019-2021年長期獎勵週期贈款”的情況下,直至業績週期結束。詳情見“-2019年執行委員會成員離職”。
|
|||||||||||||||||
|
10 保羅·哈德森於2019年6月7日辭去諾華製藥首席執行官一職,並於2019年8月31日離開公司,這與他縮短的合同通知期一致(有關更多細節,請參閲《-2019年執行委員會成員離職》)。上表所列的2019-2021年年度獎勵和長期合作伙伴計劃週期補助金(31 553個PSU)在他離職後被全部沒收。
|
|||||||||||||||||
|
|
|||||||||||||||||
|
|
|||||||||||||||||
|
|
|||||||||||||||||
|
|
固定薪酬和養卹金福利
|
可變薪酬
|
|
|
||||||||||||||||
|
|
2018年實際支付或發放的賠償金
|
2018-2020年目標週期贈款長期激勵
|
|
|
||||||||||||||||
|
|
2018年年度基本工資
|
2018年養老金福利
|
2018年度激勵(績效達標)
|
LTPP 2018-2020週期
|
LTRPP 2018-2020週期
|
2018年其他薪酬
|
2018年已支付、承諾或授予的補償總額
|
|||||||||||||
|
貨幣 |
現金 (金額) |
金額 1 |
現金 (金額) |
權益
(價值在 授予日期) 2 |
PSU
(目標值 授出日期) 3 |
PSU
(目標值 授出日期) 3 |
金額 4 |
金額 5 |
||||||||||||
|
執行委員會成員活躍於2018年12月31日
|
||||||||||||||||||||
|
Vasant Narasimhan(2018年2月1日起擔任CEO) 6
|
CHF
|
1 491 667
|
168 233
|
1 594 801
|
1 594 805
|
3 100 046
|
1 937 539
|
34 401
|
9 921 491
|
|||||||||||
|
史蒂文·伯特
|
CHF
|
780 000
|
152 914
|
585 000
|
585 073
|
1 170 051
|
468 053
|
77 550
|
3 818 642
|
|||||||||||
|
Elizabeth Barrett(2018年2月1日至2018年12月31日) 7
|
CHF
|
779 167
|
174 274
|
0
|
0
|
1 360 040
|
510 057
|
2 747 859
|
5 571 397
|
|||||||||||
|
Bertrand Bodson(2018年4月1日起) 8
|
CHF
|
450 000
|
97 666
|
216 986
|
217 001
|
440 614
|
110 174
|
146 478
|
1 678 918
|
|||||||||||
|
詹姆斯·布拉德納 9
|
美元
|
1 094 462
|
257 018
|
924 000
|
924 004
|
1 870 085
|
880 086
|
63 313
|
6 012 967
|
|||||||||||
|
理查德·弗朗西斯
|
CHF
|
850 000
|
176 368
|
382 500
|
382 528
|
1 360 057
|
510 001
|
1 790 428
|
5 451 882
|
|||||||||||
|
保羅·哈德森
|
CHF
|
985 000
|
180 771
|
1 007 325
|
1 007 352
|
1 683 036
|
792 027
|
94 355
|
5 749 866
|
|||||||||||
|
哈里·基爾希
|
CHF
|
1 040 000
|
173 499
|
858 000
|
858 043
|
1 768 008
|
832 067
|
58 814
|
5 588 431
|
|||||||||||
|
Shannon Thyme Klinger(2018年4月1日起) 8
|
CHF
|
520 833
|
103 448
|
275 770
|
275 790
|
619 595
|
185 862
|
37 118
|
2 018 416
|
|||||||||||
|
Steffen Lang(2018年4月1日起) 8
|
CHF
|
540 000
|
99 535
|
260 384
|
260 454
|
596 631
|
179 064
|
8 595
|
1 944 663
|
|||||||||||
|
Klaus Moosmayer(2018年12月1日起)
|
CHF
|
41 667
|
9 704
|
16 986
|
17 011
|
0
|
0
|
808 821
|
894 189
|
|||||||||||
|
John Tsai(2018年5月1日起)
|
CHF
|
566 667
|
126 845
|
313 801
|
313 867
|
0
|
0
|
4 590 950
|
5 912 129
|
|||||||||||
|
Robert Weltevreden(2018年6月1日起)
|
CHF
|
350 000
|
70 950
|
77 392
|
232 337
|
671 702
|
155 003
|
3 715
|
1 561 099
|
|||||||||||
|
小計
|
|
9 464 855
|
1 785 446
|
6 492 171
|
6 647 490
|
14 597 819
|
6 540 145
|
10 460 974
|
55 988 900
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
2018年卸任的執行委員會成員 10
|
||||||||||||||||||||
|
Joseph Jimenez(CEO至2018年1月31日)
|
CHF
|
178 601
|
19 146
|
133 767
|
0
|
0
|
0
|
2 357 371
|
2 688 885
|
|||||||||||
|
F.邁克爾·鮑爾(至2018年6月30日) 9
|
美元
|
555 397
|
|
126 594
|
|
333 238
|
|
333 231
|
|
888 640
|
|
388 845
|
2 970 642
|
5 596 587
|
||||||
|
費利克斯河Ehrat(至2018年5月31日)
|
CHF
|
384 740
|
|
68 918
|
|
153 896
|
|
153 892
|
|
654 081
|
|
230 877
|
2 346 072
|
3 992 477
|
||||||
|
André Wéré(至2018年3月31日) 11
|
CHF
|
217 582
|
45 646
|
216 986
|
0
|
116 060
|
43 523
|
1 375 802
|
2 015 599
|
|||||||||||
|
小計
|
|
1 323 833
|
257 458
|
830 395
|
479 632
|
1 638 802
|
654 503
|
8 983 098
|
14 167 721
|
|||||||||||
|
總計
|
|
10 788 688
|
2 042 904
|
7 322 566
|
7 127 122
|
16 236 621
|
7 194 648
|
19 444 072
|
70 156 621
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
基於假設100%的支出目標。實際支出(目標的0—200%)將於二零二一年一月三年週期結束時公佈。
|
|
|
|
|
|
||||
|
1 包括首席執行官的強制性僱主繳費4336瑞士法郎,以及諾華公司向政府社會保障系統支付的執行委員會其他成員的強制性僱主繳費78403瑞士法郎。這一數額來自2018年為執行委員會所有成員支付的2 847 422瑞士法郎的僱主繳費總額,併為執行委員會成員提供了獲得未來最高保險政府養老金福利的權利。
|
||||||||||||||||||||
|
2 以股權形式交付的年度激勵部分將根據授予日(2019年1月22日)的收盤價(每股諾華股票88.14瑞士法郎,每股美國存託憑證88.32美元)向上舍入到最近的股票。
|
||||||||||||||||||||
|
3 該金額代表2018—2020年業績週期授予執行委員會成員的PSU目標數量的基礎股份價值,基於授予日期(2018年1月18日)的收盤股價每股諾華股份82. 90瑞士法郎和每股ADR 86. 41美元(除Elizabeth Barrett和Robert Weltevreden外)。對於Barrett女士和Weltevreden先生,授予日期的收盤價分別為每股諾華股份於2018年2月1日83.52瑞士法郎和2018年6月1日74.70瑞士法郎。
|
||||||||||||||||||||
|
4 根據全球流動政策,包括任何其他津貼、實物福利和國際外派福利(例如,住房、國際健康保險、兒童學費、衡平徵税)
|
||||||||||||||||||||
|
5 所有數額均在扣除執行委員會成員應繳的社會保障繳費和所得税之前。
|
||||||||||||||||||||
|
6 這些數據包括Vasant Narasimhan 2018年1月作為全球藥物開發負責人的薪酬。
|
||||||||||||||||||||
|
7 Elizabeth Barrett於2018年營業年度結束時辭去諾華腫瘤學首席執行官的職務和執行委員會的職務。2018—2020年表現週期的LTPP及LTRP補助金(分別為16284及6107個PSU),以及2018年21267股表現股份的買斷獎勵(反映在其他補償中),均載於上表,已於2018年12月31日離職時全數沒收。
|
||||||||||||||||||||
|
8 對於於2018年加入執行委員會的成員,“2018年年度基本工資”、“2018年退休金福利”、“2018年年度獎勵”、“LTPP”及“LTPP”欄下的資料包括他們自加入執行委員會之日起至2018年12月31日的按比例薪酬。
|
||||||||||||||||||||
|
9 美元為F。Michael Ball和James Bradner的匯率為1.00瑞士法郎= 0.978美元,與集團2018年合併財務報表中使用的平均匯率相同。
|
||||||||||||||||||||
|
10 對於於2018年離開執行委員會的成員,“2018年年度基本工資”、“2018年退休金福利”、“2018年年度獎勵”、“LTPP”和“LTPP”欄下的信息反映了他們於2018年擔任執行委員會成員期間的按比例薪酬。“其他2018年薪酬”一欄下的信息還包括,除其他外,他們從執行委員會卸任之日起至2018年12月31日的按比例薪酬。
|
||||||||||||||||||||
|
11 根據《2018—2020年長期發展計劃》和《2018—2020年長期發展計劃》,授予André Wendel的永久發展計劃總數分別為16985個和6370個。上表所列長期保護計劃及長期保護計劃下的金額乃按比例披露至其通知期結束時(即,2018年9月30日),根據他的合同協議並受計劃規則的約束。
|
||||||||||||||||||||
|
可變薪酬1
|
|||||||
|
2019年度獎勵(取得的業績)
|
LTPP 2019—2021週期
|
其他
|
|||||
|
權益
(數字) 2 |
PSU
(目標數量) 3 |
權益/PSU
(數字) |
|||||
|
執行委員會成員活躍於2019年12月31日
|
|||||||
|
Vasant Narasimhan
|
21 626
|
61 726
|
0
|
||||
|
史蒂文·伯特
|
6 819
|
18 863
|
0
|
||||
|
貝特朗·博德森
|
3 672
|
11 056
|
0
|
||||
|
詹姆斯·布拉德納
|
9 999
|
32 071
|
0
|
||||
|
哈里·基爾希
|
11 251
|
31 139
|
0
|
||||
|
香農百里香克林格
|
5 039
|
18 153
|
0
|
||||
|
斯特芬·朗
|
6 590
|
13 615
|
0
|
||||
|
克勞斯·莫斯邁爾
|
2 800
|
9 077
|
0
|
||||
|
Richard Saynor(2019年7月15日) 4
|
1 931
|
0
|
11 452
|
||||
|
蘇珊娜·沙弗特
|
11 531
|
21 217
|
0
|
||||
|
蔡俊華
|
6 481
|
23 418
|
0
|
||||
|
Marie—France Tschudin(2019年6月7日起) 4
|
3 129
|
11 085
|
0
|
||||
|
羅伯特·韋爾特夫雷登
|
5 115
|
11 056
|
0
|
||||
|
小計
|
95 983
|
262 476
|
11 452
|
||||
|
|
|
|
|||||
|
2019年卸任的執行委員會成員
|
|||||||
|
Richard Francis(至2019年3月19日) 5, 6
|
403
|
8 841
|
0
|
||||
|
Paul Hudson(至2019年6月7日) 5, 7
|
0
|
4 525
|
0
|
||||
|
小計
|
403
|
13 366
|
0
|
||||
|
總計
|
96 386
|
275 842
|
11 452
|
||||
|
2018年的比較數據見下一頁。
|
|||||||
|
1 獎勵價值載於表“首席執行官及其他執行委員會成員按授出價值計算的2019年薪酬”。”
|
|||||||
|
2 2019年業績期間根據年度獎勵授出的既得股份、受限制股份及╱或受限制股份單位
|
|||||||
|
3 2019—2021年績效週期,根據長期保障計劃授予的PSU目標數目(適用於2019—2021年)
|
|||||||
|
4 對於於2019年加入執行委員會的成員,“可變薪酬”一欄下的資料包括自彼等加入執行委員會之日起至2019年12月31日止,或如屬“LTPP 2019—2021週期”,則至業績週期結束時按比例持有的權益工具數目。
|
|||||||
|
5 對於離開執行委員會的成員,"可變薪酬"一欄反映了其擔任執行委員會成員期間按比例持有的股權工具數量。“其他”一欄包括從他們離開執行委員會之日起至2019年12月31日或“LTPP 2019—2021週期”至績效週期結束的按比例薪酬。詳見《—2019執委會委員離任情況》。
|
|||||||
|
6 Richard Francis於2019年3月19日辭去Sandoz首席執行官一職,並將於2020年3月31日根據合同通知期離開公司。根據計劃規則,LTPP 2019—2021年週期授出(21217個PSU)(全部列於上表)將於正常歸屬日期根據諾華在業績週期內的僱用月數按比例歸屬。該補助金的歸屬須受期末評估的表現條件所規限。
|
|||||||
|
7 Paul Hudson於2019年6月7日辭去諾華製藥首席執行官一職,並於2019年8月31日根據縮短的合同通知期離開公司(更多詳情請參見“—2019執行委員會成員離職”)。上表所載2019年度獎勵及LTPP 2019—2021週期補助金(31 553個總補助金)已於彼離職時全數沒收。
|
|||||||
|
|
|||||||
|
|
|||||||
|
可變薪酬1
|
|||||||||
|
2018年度獎勵(業績)
|
LTPP 2018—2020週期
|
LTRPP 2018—2020週期
|
其他
|
||||||
|
權益
(數字) 2 |
PSU
(目標數量) 3 |
PSU
(目標數量) 3 |
權益/PSU
(數字) |
||||||
|
執行委員會成員活躍於2018年12月31日
|
|||||||||
|
Vasant Narasimhan(2018年2月1日起擔任CEO)
|
18 094
|
37 395
|
23 372
|
0
|
|||||
|
史蒂文·伯特
|
6 638
|
14 114
|
5 646
|
0
|
|||||
|
Elizabeth Barrett(2018年2月1日至2018年12月31日) 4
|
0
|
16 284
|
6 107
|
21 267
|
|||||
|
Bertrand Bodson(2018年4月1日起)
|
2 462
|
5 315
|
1 329
|
0
|
|||||
|
詹姆斯·布拉德納
|
10 462
|
21 642
|
10 185
|
0
|
|||||
|
理查德·弗朗西斯
|
4 340
|
16 406
|
6 152
|
0
|
|||||
|
保羅·哈德森
|
11 429
|
20 302
|
9 554
|
0
|
|||||
|
哈里·基爾希
|
9 735
|
21 327
|
10 037
|
0
|
|||||
|
Shannon Thyme Klinger(2018年4月1日起)
|
3 129
|
7 474
|
2 242
|
0
|
|||||
|
Steffen Lang(2018年4月1日起)
|
2 955
|
7 197
|
2 160
|
0
|
|||||
|
Klaus Moosmayer(2018年12月1日起)
|
193
|
0
|
0
|
8 857
|
|||||
|
John Tsai(2018年5月1日起)
|
3 561
|
0
|
0
|
27 381
|
|||||
|
Robert Weltevreden(2018年6月1日起)
|
2 636
|
8 992
|
2 075
|
0
|
|||||
|
小計
|
75 634
|
176 448
|
78 859
|
57 505
|
|||||
|
|
|
|
|
||||||
|
2018年卸任的執行委員會成員
|
|||||||||
|
Joseph Jimenez(CEO至2018年1月31日) 5
|
0
|
0
|
0
|
0
|
|||||
|
F.邁克爾·鮑爾(至2018年6月30日)
|
7 609
|
10 284
|
4 500
|
18 865
|
|||||
|
費利克斯河Ehrat(至2018年5月31日)
|
4 221
|
7 890
|
2 785
|
17 603
|
|||||
|
André Wéré(至2018年3月31日) 6
|
0
|
1 400
|
525
|
3 915
|
|||||
|
小計
|
11 830
|
19 574
|
7 810
|
40 383
|
|||||
|
總計
|
87 464
|
196 022
|
86 669
|
97 888
|
|||||
|
1 獎勵價值載於“按補助價值計算的2018年首席執行官及執行委員會成員按補助價值計算的2018年薪酬計算的首席執行官及其他執行委員會成員按補助價值計算的2018年薪酬計算”。”
|
|||||||||
|
2 2018年業績期間根據年度獎勵授出的既得股份、受限制股份及╱或受限制股份單位
|
|||||||||
|
3 2018—2020年表現週期內,根據長期保障計劃及長期保障計劃批出的私營單位目標數目(如適用)
|
|||||||||
|
4 Elizabeth Barrett於2018年營業年度結束時辭去諾華腫瘤學首席執行官的職務和執行委員會的職務。2018—2020年表現週期的LTPP及LTRP補助金(分別為16284及6107個PSU),以及2018年21267股表現股份的買斷獎勵(反映在其他補償中),均載於上表,已於2018年12月31日離職時全數沒收。
|
|||||||||
|
5 Joseph Jimenez以100%現金獲得2018年度獎勵,但沒有獲得LTPP和LTRPP 2018—2020績效週期的獎勵。
|
|||||||||
|
6 André Wendel於2018年3月31日辭去執行委員會職務,並於2018年9月30日結束其通知期。彼按比例以現金100%獲得二零一八年度獎勵,而上表所載2018—2020年表現週期的長期發展計劃及長期發展計劃補助將於表現週期結束時根據其合約協議按比例歸屬,並受計劃規則規限。
|
|||||||||
|
功能
|
所有權水平
|
||
|
首席執行官
|
5倍基本補償
|
||
|
執行委員會其他成員
|
3倍基本補償
|
||
|
既得股份 和ADR 1 |
未歸屬股份 和其他股權 2 |
股權級別
作為的倍數 年基本工資 3 |
未授權的目標PSU (e.g.,LTPP/LTRPP) 4 |
相配股份 根據《本地退休計劃》 5 |
總計為 2019年12月31日 |
||||||||
|
Vasant Narasimhan
|
59 983
|
89 381
|
8x
|
115 896
|
4 657
|
269 917
|
|||||||
|
史蒂文·伯特
|
39 785
|
31 890
|
8x
|
64 538
|
0
|
136 213
|
|||||||
|
貝特朗·博德森
|
4 600
|
11 492
|
2x
|
15 037
|
0
|
31 129
|
|||||||
|
詹姆斯·布拉德納
|
21 794
|
46 531
|
5x
|
104 379
|
0
|
172 704
|
|||||||
|
哈里·基爾希
|
108 193
|
40 968
|
12x
|
102 484
|
0
|
251 645
|
|||||||
|
香農百里香克林格
|
12 193
|
22 028
|
3x
|
35 117
|
1 488
|
70 826
|
|||||||
|
斯特芬·朗
|
56 063
|
20 248
|
9x
|
26 782
|
4 535
|
107 628
|
|||||||
|
克勞斯·莫斯邁爾
|
0
|
3 016
|
0x
|
12 034
|
0
|
15 050
|
|||||||
|
Richard Saynor(2019年7月15日)
|
0
|
9 211
|
1x
|
1 790
|
0
|
11 001
|
|||||||
|
蘇珊娜·沙弗特
|
43 770
|
26 123
|
7x
|
36 224
|
1 735
|
107 852
|
|||||||
|
蔡俊華
|
11 859
|
29 570
|
4x
|
12 487
|
0
|
53 916
|
|||||||
|
Marie—France Tschudin(2019年6月7日起)
|
5 500
|
24 715
|
3x
|
45 078
|
0
|
75 293
|
|||||||
|
羅伯特·韋爾特夫雷登
|
150
|
7 751
|
1x
|
11 386
|
0
|
19 287
|
|||||||
|
總計 6
|
363 890
|
362 924
|
|
583 232
|
12 415
|
1 322 461
|
|||||||
|
1 包括與執行委員會成員"密切聯繫的人"持有的財產(見定義"—密切聯繫的人)。")
|
|||||||||||||
|
2 根據上述定義,包括未歸屬股份和美國存託憑證以及適用於確定股權金額的其他股權。還包括與Alcon分拆有關收到的未歸屬保留完整股份。
|
|||||||||||||
|
3 倍數乃根據全年基本薪金及二零一九年財政年度結算日之收市股價計算。於二零一九年十二月三十一日,二零一九年最後一個交易日的股價為91. 90瑞郎╱ 94. 69美元。
|
|||||||||||||
|
4 除非根據相關計劃規則,獎勵符合完全歸屬資格,否則優先認股單位的目標數目按比例披露至二零一九年十二月三十一日。
|
|||||||||||||
|
5 槓桿式股份儲蓄計劃(LSSP)項下的配對股份按比例披露至2019年12月31日,除非獎勵根據計劃規則符合完全歸屬資格。2014年,執行委員會成員停止參加LSP計劃,儘管一些現任成員在成為執行委員會成員之前根據該計劃獲得了後來的贈款。未償還的獎勵將於授出日期起計五年內歸屬,惟須遵守LSSP計劃規則。
|
|||||||||||||
|
6 Paul Hudson和Richard Francis於2019年退出執行委員會。在他們從執行委員會卸任時,哈德森先生擁有零歸屬股份、140121股未歸屬股份和其他股權,弗朗西斯先生擁有50615股已歸屬股份和86740股未歸屬股份和其他股權。
|
|||||||||||||
|
|
|||||||||||||
|
|
|||||||||||||
|
每年一次
基本工資 1 |
變量
補償 2 |
||||
|
Vasant Narasimhan
|
14.7%
|
85.3%
|
|||
|
史蒂文·伯特
|
20.5%
|
79.5%
|
|||
|
貝特朗·博德森
|
25.3%
|
74.7%
|
|||
|
詹姆斯·布拉德納
|
18.9%
|
81.1%
|
|||
|
哈里·基爾希
|
17.8%
|
82.2%
|
|||
|
香農百里香克林格
|
22.8%
|
77.2%
|
|||
|
斯特芬·朗
|
25.0%
|
75.0%
|
|||
|
克勞斯·莫斯邁爾
|
25.1%
|
74.9%
|
|||
|
理查德·塞諾
|
13.4%
|
86.6%
|
|||
|
蘇珊娜·沙弗特
|
19.3%
|
80.7%
|
|||
|
蔡俊華
|
19.1%
|
80.9%
|
|||
|
瑪麗-法國-舒丁
|
23.7%
|
76.3%
|
|||
|
羅伯特·韋爾特夫雷登
|
27.4%
|
72.6%
|
|||
|
總計 3
|
19.4%
|
80.6%
|
|||
|
1 不包括養卹金和其他福利
|
|||||
|
2 有關可變資產的披露原則,見表“2019年CEO及其他執行委員會成員按補助價值計算的薪酬”。
補償。 |
|||||
|
3 不包括2019年辭去執行委員會職務的Richard Francis和辭職的Paul Hudson。
|
|||||
|
績效衡量標準
|
跟蹤
|
||
|
LTPP NCVA(75%)
|
在目標前面
|
||
|
LTPP創新(25%)
|
在目標前面
|
||
|
LTRPP相對TSC(100%)
|
領先於同齡羣體中位數
|
||
2020年執行委員會薪酬制度
2020年執行委員會薪酬
2019年董事會薪酬
|
千瑞士法郎 |
2019-2020年度股東大會
年費 |
||
|
董事會主席
|
3 800
|
||
|
董事會成員
|
280
|
||
|
副主席
|
50
|
||
|
審計和合規委員會主席
|
130
|
||
|
薪酬委員會主席
|
90
|
||
|
以下委員會主席:
·治理、提名和 企業責任委員會 ·研發委員會 ·風險委員會 |
70 |
||
|
審計署的成員
和合規委員會 |
70 |
||
|
下列委員會的成員:
·薪酬委員會 ·治理、提名和 企業責任委員會 ·研發委員會 ·風險委員會 |
40 |
||
|
|
|||
|
董事會成員
|
審計和合規委員會
|
薪酬委員會
|
治理, 提名 和企業 責任 委員會
|
研究與發展委員會
|
風險委員會
|
股份(數量) 1
|
現金(瑞士法郎)(A)
|
股份(瑞士法郎)(B)
|
其他(瑞士法郎)(C) 2
|
總計(瑞士法郎)(A)+(B)+(C) 3
|
|||||||||||||
|
活躍於2019年12月31日的董事會成員
|
|||||||||||||||||||||||
|
約爾格·萊因哈特 4
|
椅子
|
|
|
|
椅子
|
|
21 498
|
1 900 000
|
1 900 000
|
4 373
|
3 804 373
|
||||||||||||
|
恩里科·瓦尼
|
副主席
|
•
|
椅子
|
•
|
|
|
4 494
|
220 833
|
309 166
|
3 512
|
533 511
|
||||||||||||
|
南希·安德魯斯
|
•
|
|
|
|
•
|
•
|
2 035
|
180 000
|
180 000
|
–
|
360 000
|
||||||||||||
|
唐·比希納
|
•
|
•
|
|
|
|
|
2 967
|
145 833
|
204 166
|
4 373
|
354 372
|
||||||||||||
|
帕特里斯·布拉 5
|
•
|
|
•
|
|
|
|
1 813
|
–
|
266 667
|
4 373
|
271 040
|
||||||||||||
|
Srikant Datar
|
•
|
•
|
•
|
|
|
椅子
|
2 602
|
230 000
|
230 000
|
–
|
460 000
|
||||||||||||
|
伊麗莎白·多爾蒂
|
•
|
椅子
|
|
|
|
•
|
2 544
|
225 000
|
225 000
|
–
|
450 000
|
||||||||||||
|
安·福吉
|
•
|
|
•
|
•
|
|
•
|
2 262
|
200 000
|
200 000
|
–
|
400 000
|
||||||||||||
|
Frans van Houten
|
•
|
|
|
|
•
|
|
2 716
|
26 667
|
293 334
|
–
|
320 001
|
||||||||||||
|
安德烈亞斯·馮·普蘭塔
|
•
|
•
|
|
椅子
|
|
•
|
2 602
|
230 000
|
230 000
|
4 373
|
464 373
|
||||||||||||
|
Charles L.索耶斯
|
•
|
|
|
•
|
•
|
|
2 035
|
180 000
|
180 000
|
–
|
360 000
|
||||||||||||
|
William T.温特斯
|
•
|
|
•
|
• 5
|
|
|
3 620
|
–
|
353 333
|
–
|
353 333
|
||||||||||||
|
小計
|
|
|
|
|
|
|
51 188
|
3 538 333
|
4 571 666
|
21 002
|
8 131 001
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
於2019年股東周年大會上卸任的董事會成員
|
|||||||||||||||||||||||
|
迪米特里·阿扎爾 6
|
•
|
|
|
•
|
•
|
|
1 016
|
30 000
|
30 000
|
–
|
60 000
|
||||||||||||
|
小計
|
|
|
|
|
|
|
1 016
|
30 000
|
30 000
|
–
|
60 000
|
||||||||||||
|
總計
|
|
|
|
|
|
|
52 204
|
3 568 333
|
4 601 666
|
21 002
|
8 191 001
|
||||||||||||
|
2018年的比較數據見下一頁。
|
|||||||||||||||||||||||
|
1 所示金額代表於二零一九年就各董事會成員服務期間交付予各董事會成員的股份總數。本欄所呈報之股份數目指:(i)於二零一九年二月就二零一八年股東周年大會至二零一九年股東周年大會之服務交付之第二期及最後一期股權分期付款,及(ii)於二零一九年八月就二零一九年股東周年大會至二零二零年股東周年大會之服務交付之兩期股權分期付款中的第一期。自二零一九年股東周年大會至二零二零年股東周年大會之服務之第二期及最後一期股權分期付款將於二零二零年二月進行。
|
|||||||||||||||||||||||
|
2 包括諾華公司向政府社會保障體系支付的21 002瑞士法郎的強制性僱主繳款。這一數額是從僱主繳款總額413 '985瑞士法郎中扣除的,併為董事會成員提供了獲得未來最高保險政府養卹金福利的權利。
|
|||||||||||||||||||||||
|
3 所有金額均未扣除董事會成員應付的社會保障繳款和所得税。
|
|||||||||||||||||||||||
|
4 Joerg Reinhardt沒有額外的委員會費用,以擔任研究與發展委員會主席。
|
|||||||||||||||||||||||
|
5 2019年2月28日起
|
|||||||||||||||||||||||
|
6 截止2019年2月28日
|
|||||||||||||||||||||||
|
|
|||||||||||||||||||||||
|
|
|||||||||||||||||||||||
|
董事會成員
|
審計和合規委員會
|
薪酬委員會
|
治理, 提名 和企業 責任 委員會
|
研究與發展委員會
|
風險委員會
|
股份(數量) 1
|
現金(瑞士法郎)(A)
|
股份(瑞士法郎)(B)
|
其他(瑞士法郎)(C) 2
|
總計(瑞士法郎)(A)+(B)+(C) 3
|
|||||||||||||
|
2018年12月31日活躍的董事會成員
|
|||||||||||||||||||||||
|
約爾格·萊因哈特 4
|
椅子
|
|
|
|
椅子
|
|
23 889
|
|
1 900 000
|
|
1 900 000
|
4 336
|
3 804 336
|
||||||||||
|
恩里科·瓦尼
|
副主席
|
•
|
椅子
|
•
|
|
|
4 854
|
41 667
|
483 334
|
3 475
|
528 476
|
||||||||||||
|
南希·安德魯斯
|
•
|
|
|
|
•
|
•
|
2 262
|
180 000
|
180 000
|
–
|
360 000
|
||||||||||||
|
迪米特里·阿扎爾
|
•
|
|
|
• 5
|
•
|
|
2 359
|
182 500
|
182 500
|
–
|
365 000
|
||||||||||||
|
唐·比希納
|
•
|
• 5
|
|
|
|
• 6
|
4 270
|
–
|
346 667
|
4 336
|
351 003
|
||||||||||||
|
Srikant Datar
|
•
|
•
|
•
|
|
|
椅子
|
2 859
|
229 167
|
229 167
|
–
|
458 334
|
||||||||||||
|
伊麗莎白·多爾蒂
|
•
|
椅子
|
|
|
|
•
|
2 828
|
225 000
|
225 000
|
–
|
450 000
|
||||||||||||
|
安·福吉
|
•
|
|
•
|
•
|
|
•
|
2 481
|
199 167
|
199 167
|
–
|
398 334
|
||||||||||||
|
Frans van Houten
|
•
|
|
|
|
• 5
|
|
2 334
|
148 333
|
168 333
|
–
|
316 666
|
||||||||||||
|
安德烈亞斯·馮·普蘭塔
|
•
|
•
|
|
椅子
|
|
•
|
2 859
|
229 167
|
229 167
|
4 336
|
462 670
|
||||||||||||
|
Charles L.索耶斯
|
•
|
|
|
•
|
•
|
|
2 262
|
180 000
|
180 000
|
–
|
360 000
|
||||||||||||
|
William T.温特斯
|
•
|
|
•
|
|
|
|
4 087
|
–
|
321 667
|
–
|
321 667
|
||||||||||||
|
小計
|
|
|
|
|
|
|
57 344
|
3 515 001
|
4 645 002
|
16 483
|
8 176 486
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
在2018年年度股東大會上辭職的董事會成員
|
|||||||||||||||||||||||
|
皮埃爾·蘭道特(至2018年3月2日) 7
|
•
|
|
|
• 6
|
|
|
2 131
|
–
|
55 000
|
3 475
|
58 475
|
||||||||||||
|
小計
|
|
|
|
|
|
|
2 131
|
–
|
55 000
|
3 475
|
58 475
|
||||||||||||
|
總計
|
|
|
|
|
|
|
59 475
|
3 515 001
|
4 700 002
|
19 958
|
8 234 961
|
||||||||||||
|
1 所示金額為2018年向每名董事會成員交付的各自董事會成員服務期間的股份總數。本欄報告的股份數量代表:(I)2018年2月就2017年股東周年大會至2018年股東周年大會的服務交付的第二期也是最後一期股權分期付款,及(Ii)2018年8月就2018年股東周年大會至2019年股東周年大會的服務交付的兩期股權分期付款中的第一期。從2018年年度股東大會到2019年年度股東大會的服務的第二次也是最後一次股權分期付款將於2019年2月進行。
|
|||||||||||||||||||||||
|
2 包括諾華公司向政府社會保障系統支付的所有董事會成員的強制性僱主繳費,金額為19958瑞士法郎。這一數額是僱主繳費總額383 864瑞士法郎中的一部分,為董事會成員提供了獲得未來最高保險政府養老金福利的權利。
|
|||||||||||||||||||||||
|
3 所有金額均未扣除董事會成員應付的社會保障繳款和所得税。
|
|||||||||||||||||||||||
|
4 Joerg Reinhardt沒有額外的委員會費用,以擔任研究與發展委員會主席。
|
|||||||||||||||||||||||
|
5 2018年3月2日起
|
|||||||||||||||||||||||
|
6 至2018年3月2日
|
|||||||||||||||||||||||
|
7 根據皮埃爾·蘭道特的説法,桑多斯家族基金會是這筆賠償的經濟受益者。
|
|||||||||||||||||||||||
|
股份數量
2019年12月31日 1,2 |
|||
|
約爾格·萊因哈特
|
563 697
|
||
|
恩里科·瓦尼
|
26 645
|
||
|
南希·安德魯斯
|
7 265
|
||
|
唐·比希納
|
10 950
|
||
|
帕特里斯·布拉
|
1 946
|
||
|
Srikant Datar
|
41 334
|
||
|
伊麗莎白·多爾蒂
|
6 765
|
||
|
安·福吉
|
14 114
|
||
|
Frans van Houten
|
4 764
|
||
|
安德烈亞斯·馮·普蘭塔
|
161 035
|
||
|
Charles L.索耶斯
|
10 986
|
||
|
William T.温特斯
|
18 170
|
||
|
總計 3
|
867 671
|
||
|
1 包括與董事會成員有“密切聯繫”的人的持有量(見定義“--密切聯繫的人”)
|
|||
|
2 每股股票提供了一票的權利。
|
|||
|
3 迪米特里·阿扎爾於2019年2月28日辭去董事會職務。2019年2月28日,阿扎爾先生持有18750股。他的股票不包括在總數中。
|
|||
薪酬治理

|
決定
|
決策權
|
||
|
董事會主席和其他成員的報酬
|
董事會
|
||
|
CEO薪酬
|
董事會
|
||
|
執行委員會其他成員的報酬
|
薪酬委員會
|
||
6.董事會慣例
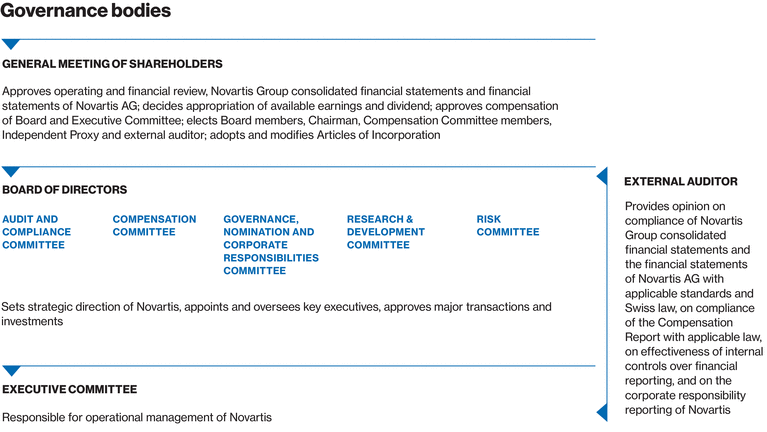
|
持股百分比
股本 2019年12月31日 |
|||
|
登記在自己賬户上的股東:
|
|
||
|
埃馬桑股份公司,巴塞爾
|
3.5
|
||
|
諾華員工參與基金會,巴塞爾
|
2.1
|
||
|
瑞銀基金管理(瑞士)股份公司,巴塞爾
|
2.1
|
||
|
持股百分比
股本 2019年12月31日 |
|||
|
登記為被提名人的股東:
|
|
||
|
大通提名者有限公司,倫敦
|
10.4
|
||
|
紐約梅隆銀行,紐約
|
3.8
|
||
|
通過紐約梅隆銀行,Everett
|
2.0
|
||
|
通過紐約梅隆銀行,紐約
|
1.2
|
||
|
通過紐約梅隆銀行,SA/NV,布魯塞爾
|
0.6
|
||
|
諾瑞信被提名人有限公司,倫敦
|
3.9
|
||
|
作為美國存托股份(美國存托股份)存託的股東:
|
|
||
|
摩根大通銀行,N.A.,紐約
|
12.5
|
||
|
截至2019年12月31日 1 |
數量
註冊 股東 |
註冊的百分比 股本 |
|||
|
1–100
|
25 442
|
0.06
|
|||
|
101–1 000
|
97 161
|
1.59
|
|||
|
1 001–10 000
|
34 884
|
3.84
|
|||
|
10 001–100 000
|
3 080
|
3.16
|
|||
|
100 001–1 000 000
|
451
|
5.45
|
|||
|
1 000 001–5 000 000
|
64
|
4.96
|
|||
|
5000至001人或更多 2
|
29
|
50.66
|
|||
|
登記股東/股份總數
|
161 111
|
69.72
|
|||
|
未登記股份
|
|
30.28
|
|||
|
總計
|
|
100.00
|
|||
|
1 於二零一九年股東周年大會(股東周年大會)的記錄日期,未登記股份佔15%。
|
|||||
|
2 包括上文所列的重要註冊股東
|
|||||
|
截至2019年12月31日
|
股東百分比
|
佔%的股份
|
|||
|
個人股東
|
96.43
|
12.99
|
|||
|
法人單位 1
|
3.52
|
32.77
|
|||
|
被提名人、受託人和美國存托股份託管機構
|
0.05
|
54.24
|
|||
|
總計
|
100.00
|
100.00
|
|||
|
1 不包括諾華公司或其全資附屬公司作為庫存股持有的5.7%股本
|
|||||
|
截至2019年12月31日
|
股東百分比
|
佔%的股份
|
|||
|
比利時
|
0.13
|
1.13
|
|||
|
法國
|
2.06
|
0.29
|
|||
|
德國
|
5.66
|
1.64
|
|||
|
日本
|
0.21
|
0.70
|
|||
|
盧森堡
|
0.05
|
0.42
|
|||
|
瑞士 2
|
87.68
|
42.38
|
|||
|
英國
|
0.56
|
26.15
|
|||
|
美國
|
0.32
|
25.41
|
|||
|
其他國家
|
3.33
|
1.88
|
|||
|
總計
|
100.00
|
100.00
|
|||
|
1 被提名者持有的記名股票顯示在作為股東登記在股份登記冊上的公司/關聯公司的登記所在地。
|
|||||
|
2 不包括諾華公司或其全資附屬公司作為庫存股持有的5.7%股本
|
|||||
|
年度股東大會 |
股東決定 |
已註銷的股份 |
平均回購
股價(瑞士法郎) 1 |
||||
|
2017
|
·資本減少510萬瑞士法郎(從1 313 557 410瑞士法郎減至1 308 422 410瑞士法郎)
|
10 270 000
|
74.67
|
||||
|
2018
|
·資本減少3311萬瑞士法郎(從1 308 422 410瑞士法郎減至1 275 312 410瑞士法郎)
|
66 220 000
|
78.34
|
||||
|
2019
|
·資本減少1,163萬瑞士法郎(從1 275 312 410瑞士法郎減至1 263 687 410瑞士法郎)
·授權董事會回購最多100億瑞士法郎的股份 根據第八次股票回購計劃, |
23 250 000
|
79.08
|
||||
|
|
|
|
|||||
|
年度股東大會 |
向股東提出的建議 |
待註銷股份 |
平均回購
股價(瑞士法郎) 1 |
||||
|
2020
|
·資本減少3,016萬瑞士法郎(從1 263 687 410瑞士法郎減至1 233 530 460瑞士法郎)
|
60 313 900
|
88.18
|
||||
|
1 所有股票都是在Six Swiss Exchange的第二個交易線上回購的。
|
|||||||
|
2019
|
2018
|
2017
|
|||||
|
已發行股份
|
2 527 374 820
|
2 550 624 820
|
2 616 844 820
|
||||
|
國庫股 1
|
262 366 332
|
239 453 391
|
299 388 321
|
||||
|
截至12月31日的流通股
|
2 265 008 488
|
2 311 171 429
|
2 317 456 499
|
||||
|
加權平均流通股數
|
2 290 792 782
|
2 319 322 369
|
2 345 783 843
|
||||
|
1 約1.18億股庫存股(2018年:1.22億股;2017年:1.31億股)由諾華實體持有,限制其使用。
|
|||||||
|
2019
|
2018
|
2017
|
|||||
|
持續經營基本每股收益(美元)
|
3.12
|
5.52
|
3.20
|
||||
|
非持續經營的基本每股收益(美元)
|
2.00
|
– 0.08
|
0.08
|
||||
|
每股基本收益合計(美元)
|
5.12
|
5.44
|
3.28
|
||||
|
持續運營攤薄後每股收益(美元)
|
3.08
|
5.46
|
3.17
|
||||
|
已終止經營業務之每股攤薄收益(美元)
|
1.98
|
– 0.08
|
0.08
|
||||
|
每股攤薄後總收益(美元)
|
5.06
|
5.38
|
3.25
|
||||
|
持續經營業務的經營活動現金流量淨額(美元)
|
5.91
|
5.63
|
4.87
|
||||
|
諾華製藥股東年終權益(美元)
|
24.49
|
34.01
|
32.00
|
||||
|
股息(瑞士法郎) 2
|
2.95
|
2.85
|
2.80
|
||||
|
1 按已發行股票的加權平均數計算,年終股本除外
|
|||||||
|
2 2019年:於2020年2月28日提交股東周年大會批准的提案
|
|||||||
|
2019
|
2018
|
2017
|
|||||
|
市盈率 1
|
18.5
|
15.7
|
25.7
|
||||
|
持續經營的市盈率 1
|
30.4
|
15.4
|
25.7
|
||||
|
股息率(%) 1
|
3.2
|
3.4
|
3.4
|
||||
|
1 基於諾華公司每年12月31日的股價
|
|||||||
|
2019 1
|
2018
|
2017
|
|||||
|
年終ADR價格(美元)
|
94.69
|
85.81
|
83.96
|
||||
|
高 2
|
96.14
|
93.91
|
86.65
|
||||
|
低 2
|
75.40
|
72.44
|
70.03
|
||||
|
未解決的不良反應數量 3
|
315 073 094
|
338 641 387
|
320 833 039
|
||||
|
|
|||||||
|
1 2019年不包括Alcon的業務,該業務於2019年4月分拆為獨立交易的獨立公司。
|
|||||||
|
2 以每日收盤價計算
|
|||||||
|
3 存託銀行摩根大通銀行每發行一份美國存託憑證,就會持有一股諾華製藥的股票。
|
|||||||
|
2019 1
|
2018
|
2017
|
|||||
|
年終股價
|
91.90
|
84.04
|
82.40
|
||||
|
高 2
|
96.04
|
91.84
|
85.15
|
||||
|
低 2
|
77.03
|
72.42
|
69.55
|
||||
|
年終市值(十億美元) 3
|
214.8
|
197.0
|
195.5
|
||||
|
年終市值(數十億瑞士法郎) 3
|
208.2
|
194.2
|
191.0
|
||||
|
1 2019年不包括Alcon的業務,該業務於2019年4月分拆為獨立交易的獨立公司。
|
|||||||
|
2 以每日收盤價計算
|
|||||||
|
3 市值是根據流通股(不包括庫存股)的數量計算的。美元市值是以年終瑞郎兑美元匯率換算的瑞郎市值為基礎。
|
|||||||
股東參與
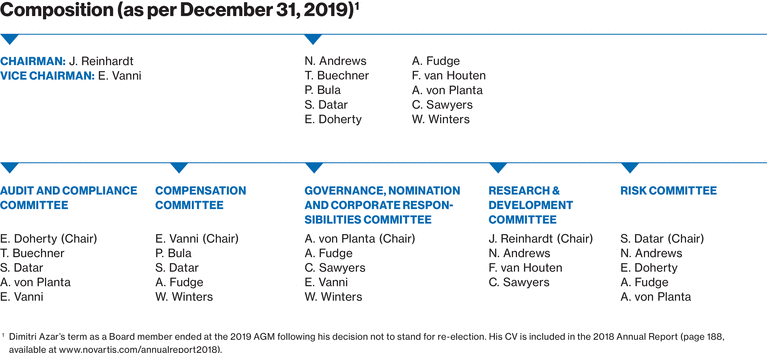
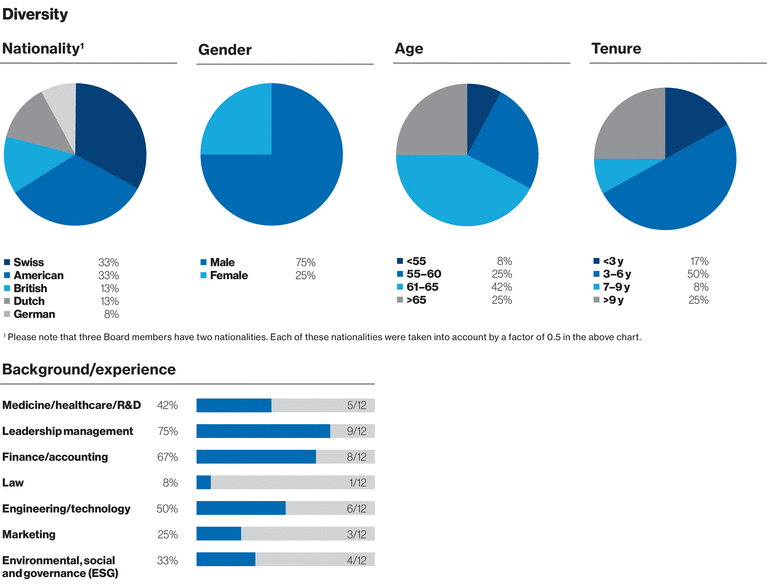
董事會成員

 醫藥/醫療保健/研發
醫藥/醫療保健/研發  領導力管理
領導力管理
 醫藥/醫療保健/研發
醫藥/醫療保健/研發  財務/會計
財務/會計  工程/技術
工程/技術
 醫藥/醫療保健/研發
醫藥/醫療保健/研發  領導管理
領導管理 
 領導管理
領導管理  財務/會計
財務/會計  環境、社會和治理(ESG)
環境、社會和治理(ESG)  工程/技術
工程/技術
 領導管理
領導管理  營銷
營銷  財務/會計
財務/會計  工程/技術
工程/技術
 *財務/會計
*財務/會計
 領導管理
領導管理  營銷
營銷  財務/會計
財務/會計  工程/技術
工程/技術
 領導管理
領導管理  營銷
營銷  環境、社會和治理(ESG)
環境、社會和治理(ESG)
 醫藥/醫療保健/研發
醫藥/醫療保健/研發  領導管理
領導管理  財務/會計
財務/會計  *工程/技術
*工程/技術
 財務/會計
財務/會計  法
法  環境、社會和治理(ESG)
環境、社會和治理(ESG)
 醫藥/醫療保健/研發
醫藥/醫療保健/研發  領導管理
領導管理  環境、社會和治理(ESG)
環境、社會和治理(ESG)
 領導管理
領導管理  財務/會計
財務/會計  工程/技術
工程/技術





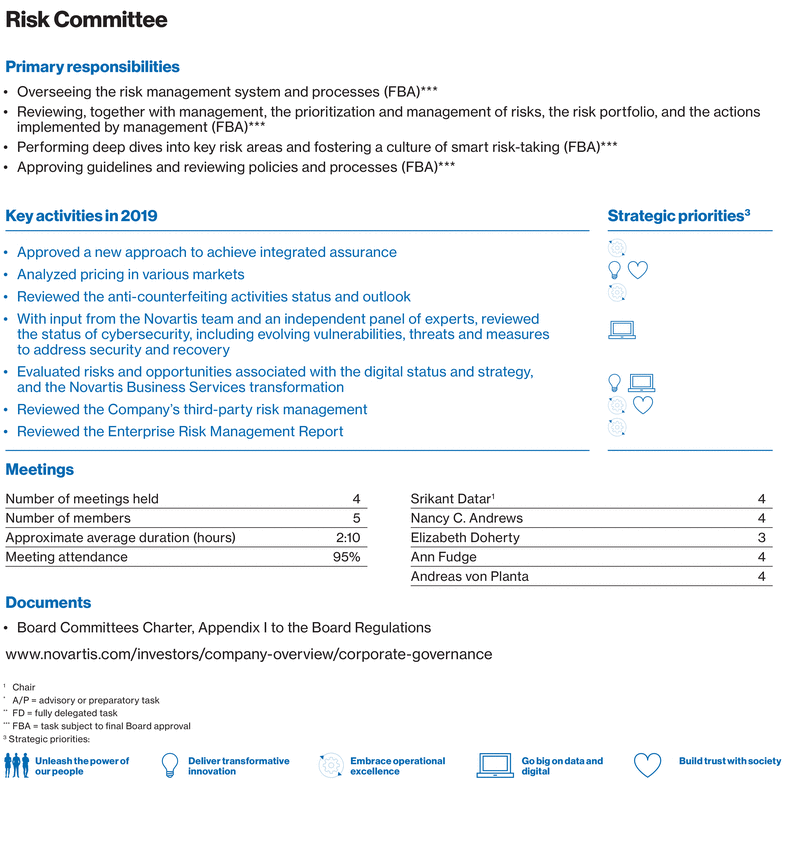
|
最大數量
任務清單 |
|||
|
任務規定
|
10
|
||
|
其他上市公司 1
|
4
|
||
|
1 其他上市公司的董事會主席被視為兩項授權。
|
|||
|
最大數量
任務清單 |
|||
|
諾華製藥控制的公司中的委託
|
沒有限制
|
||
|
應諾華製藥或其控制的公司的要求而持有的委託
|
5
|
||
|
協會、慈善組織、基金會、信託基金和僱員福利基金會的任務
|
10
|
||
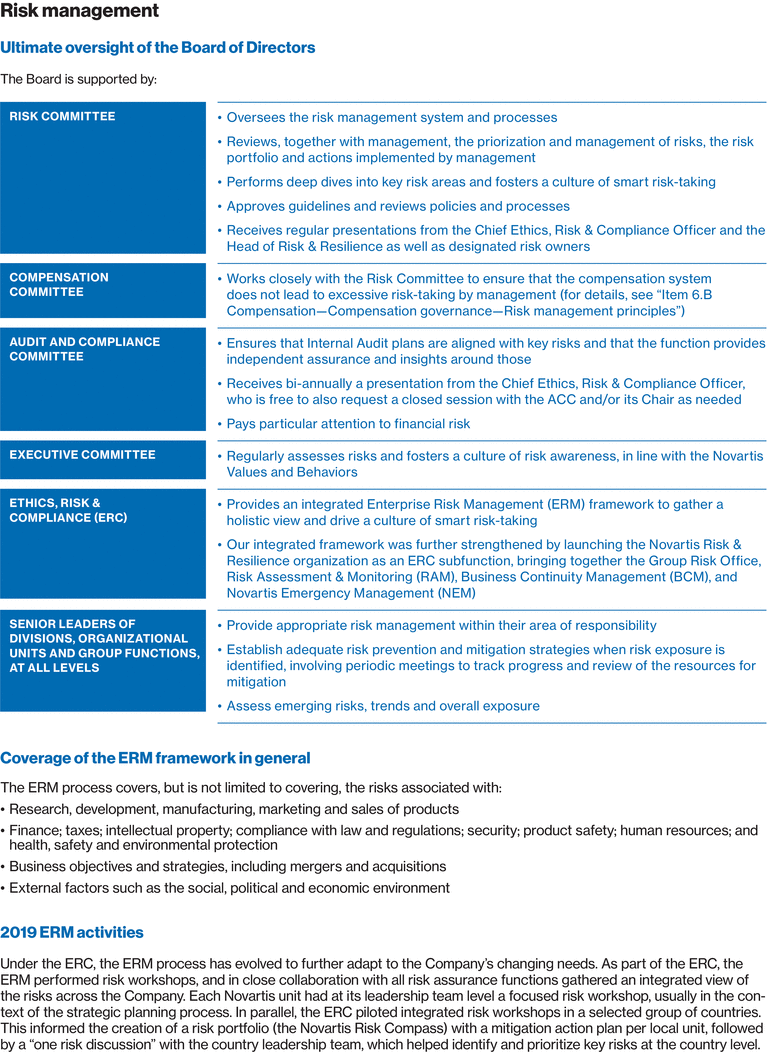

執行委員會

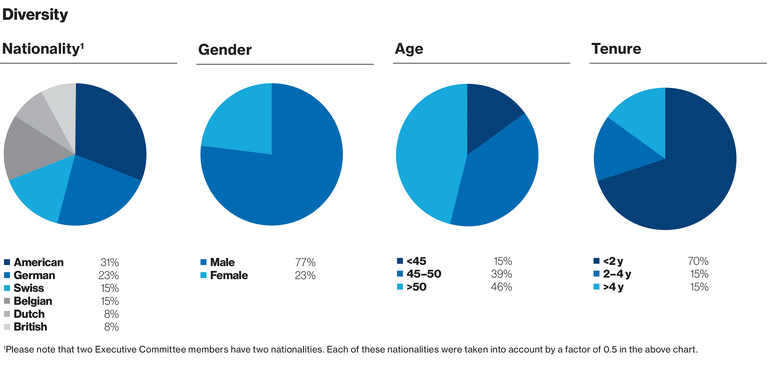
|
最大數量
任務清單 |
|||
|
任務規定
|
6
|
||
|
其他上市公司 1
|
2
|
||
|
1 其他上市公司不得擔任董事長。
|
|||
|
最大數量
任務清單 |
|||
|
諾華製藥控制的公司中的委託
|
沒有限制
|
||
|
應諾華製藥或其控制的公司的要求而持有的委託
|
5
|
||
|
協會、慈善組織、基金會、信託基金和僱員福利基金會的任務
|
10
|
||
執行委員會成員













審計師
|
2019
百萬美元 |
2018
百萬美元 |
||||
|
審計服務
|
21.2
|
25.6
|
|||
|
與審計相關的服務
|
1.0
|
13.4
|
|||
|
税務服務
|
0.7
|
0.7
|
|||
|
其他服務
|
1.4
|
2.4
|
|||
|
總計
|
24.3
|
42.1
|
|||
|
|
|||||
信息政策
|
主題
|
信息
|
||
|
股本
|
諾華製藥的公司章程
Www.novartis.com/investors/company-overview/corporate-governance 諾華的關鍵份額數據 Www.novartis.com/key-share-data |
||
|
股東權利
|
諾華製藥的公司章程
Www.novartis.com/investors/company-overview/corporate-governance |
||
|
股東周年大會
|
股東周年大會
Www.novartis.com/investors/shareholder-information/annual-general-meeting |
||
|
董事會規則
|
董事會規則
Www.novartis.com/investors/company-overview/corporate-governance |
||
|
諾華公司高級財務官代碼
|
諾華首席執行官和高級財務官道德行為準則
Www.novartis.com/investors/company-overview/corporate-governance |
||
|
諾華進軍社會ESG報告
|
諾華進軍社會ESG報告
Www.novartis.com/nisreport2019 |
||
|
諾華財務數據
|
諾華財務數據
Www.novartis.com/Investors/Financial-data |
||
|
新聞稿
|
新聞稿
Www.novartis.com/news/news-archive?type=press_release 免費電子郵件服務 Www.novartis.com/News/保持最新狀態 |
||
|
更多信息
(包括諾華投資者活動日曆,註冊辦事處, 聯繫和電子郵件地址、電話號碼等) |
諾華公司投資者關係
Www.novartis.com/Investors |
||
6.D級僱員
|
截至該年度為止
2019年12月31日 (相當於全日制職位) |
市場營銷和 銷售額 |
生產和銷售 供應 |
研究和 發展 |
國家統計局 1 |
一般和 行政管理 |
總計 |
|||||||
|
美國
|
5 360
|
2 830
|
5 412
|
614
|
763
|
14 979
|
|||||||
|
加拿大和拉丁美洲
|
3 396
|
838
|
480
|
864
|
397
|
5 975
|
|||||||
|
歐洲
|
16 395
|
19 386
|
9 988
|
4 352
|
2 666
|
52 787
|
|||||||
|
亞洲/非洲/澳大拉西亞
|
17 455
|
3 163
|
4 296
|
4 233
|
1 026
|
30 173
|
|||||||
|
總計
|
42 606
|
26 217
|
20 176
|
10 063
|
4 852
|
103 914
|
|||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||||||
|
截至該年度為止
2018年12月31日 (相當於全日制職位) |
市場營銷和 銷售額 |
生產和銷售 供應 |
研究和 發展 |
國家統計局 1 |
一般和 行政管理 |
總計 |
|||||||
|
美國
|
6 825
|
7 524
|
6 700
|
1 467
|
911
|
23 427
|
|||||||
|
加拿大和拉丁美洲
|
4 584
|
960
|
508
|
899
|
490
|
7 441
|
|||||||
|
歐洲
|
19 608
|
21 397
|
10 049
|
4 845
|
2 780
|
58 679
|
|||||||
|
亞洲/非洲/澳大拉西亞
|
20 099
|
6 636
|
3 977
|
3 613
|
1 289
|
35 614
|
|||||||
|
總計
|
51 116
|
36 517
|
21 234
|
10 824
|
5 470
|
125 161
|
|||||||
|
|
|
|
|
|
|
||||||||
|
其中繼續開展業務2
|
43 954
|
25 862
|
19 803
|
10 824
|
4 337
|
104 780
|
|||||||
|
其中已終止業務2
|
7 162
|
10 655
|
1 431
|
0
|
1 133
|
20 381
|
|||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
||||||||
|
截至該年度為止
2017年12月31日 (相當於全日制職位) |
市場營銷和 銷售額 |
生產和銷售 供應 |
研究和 發展 |
國家統計局 1 |
一般和 行政管理 |
總計 |
|||||||
|
美國
|
6 563
|
7 095
|
6 803
|
1 680
|
726
|
22 867
|
|||||||
|
加拿大和拉丁美洲
|
4 477
|
1 305
|
557
|
900
|
471
|
7 710
|
|||||||
|
歐洲
|
18 665
|
20 412
|
10 173
|
4 903
|
2 469
|
56 622
|
|||||||
|
亞洲/非洲/澳大拉西亞
|
19 005
|
6 970
|
3 883
|
3 386
|
1 154
|
34 398
|
|||||||
|
總計
|
48 710
|
35 782
|
21 416
|
10 869
|
4 820
|
121 597
|
|||||||
|
其中繼續開展業務2
|
42 115
|
25 564
|
20 060
|
10 869
|
3 859
|
102 467
|
|||||||
|
其中已終止業務2
|
6 595
|
10 218
|
1 356
|
0
|
961
|
19 130
|
|||||||
|
1 NBS指的是諾華商業服務組織部門的全職同等員工。
|
|||||||||||||
|
2 持續經營業務包括創新藥品和Sandoz部門的業務以及持續的企業活動,而已終止經營業務包括Alcon眼科護理設備業務以及分拆前Alcon應佔的若干企業活動。見"項目18.財務報表—附註2。2019年重大交易”。
|
|||||||||||||
6.E股所有權
項目7.大股東和關聯方交易
7.A大股東
|
|
在以下日期實益擁有的股本的百分比:
|
||||||||
|
普通股
實益擁有截至 2019年12月31日 |
2019年12月31日 |
2018年12月31日 |
2017年12月31日 |
||||||
|
登記在自己賬户上的股東:
|
|
|
|
||||||
|
瑞士巴塞爾Emasan AG
|
89 193 765
|
3.5
|
3.5
|
3.4
|
|||||
|
諾華員工參與基金會,瑞士巴塞爾 1
|
53 983 628
|
2.1
|
2.3
|
2.5
|
|||||
|
瑞士巴塞爾瑞銀基金管理(瑞士)股份公司
|
52 845 411
|
2.1
|
2.2
|
2.0
|
|||||
|
1 諾華員工參與基金會(以下簡稱“員工基金會”)是一個特殊目的實體,由諾華創立,但獨立於諾華。
|
|||||||||
|
|
截至以下日期各自持有的股本百分比:
|
||||||||
|
普通股
持有日期為 2019年12月31日 |
2019年12月31日 |
2018年12月31日 |
2017年12月31日 |
||||||
|
登記為被提名人的股東:
|
|
|
|||||||
|
大通提名有限公司,英國倫敦
|
264 073 363
|
10.4
|
9.8
|
7.8
|
|||||
|
紐約梅隆銀行,紐約
|
95 456 296
|
3.8
|
4.1
|
4.3
|
|||||
|
紐約梅隆銀行(Bank of New York Mellon,Everett,MA)
|
50 207 591
|
2.0
|
2.1
|
2.0
|
|||||
|
通過紐約銀行梅隆,紐約,NY
|
29 356 938
|
1.2
|
1.3
|
–
|
|||||
|
通過The Bank of New York Mellon,SA/NV,布魯塞爾,比利時
|
15 891 767
|
0.6
|
0.7
|
2.3
|
|||||
|
諾瑞信被提名者有限公司,英國倫敦
|
98 354 215
|
3.9
|
3.6
|
3.8
|
|||||
|
作為美國存托股份(美國存托股份)存託的股東:
|
|
|
|
|
|||||
|
摩根大通銀行,N.A.,紐約
|
314 717 099
|
12.5
|
13.3
|
12.3
|
|||||
7.關聯方交易
7.c專家和律師的利益
項目8.財務信息
8.a合併報表和其他財務資料
8.B重大變化
項目9.報價和清單
9.報價和掛牌細節
9.B分配方案
9.C街市
9.D出售股東
9.E稀釋
9.發行債券的開支
項目10.補充信息
10.A股本
10.B組織章程大綱及章程細則
10.C材料合同
10.外匯管制
10.電子課税
10.F派息及支付代理人
10.專家的發言
10.陳列的文件
10.一、附屬信息
項目11.關於市場風險的定量和定性披露
項目12. 股本證券以外的證券描述
12.A債務證券
12.B認股權證及權利
12.c.其他證券
12.D美國存托股份
|
類別
|
存託訴訟
|
連帶費用
|
|||
|
存放或替代
標的股份 |
接受交出的股份,併發行美國存託憑證作為交換,
包括就下列事項作出的交出及發出: -股份分配 -股票拆分 -權利 -合併 -交換股份或任何其他交易或事件或其他分發 影響美國存託憑證或存入股份 |
每100張美國存託憑證5美元
(or部分) 以新的, 交付的不良反應 |
|||
|
撤回
標的股份 |
接受為提取存放股份而交出的美國存託憑證
|
每100張美國存託憑證5美元
(or部分) 由ADR證明, 投降 |
|||
|
銷售或
行使權利 |
分發或出售股份,所收取的費用為
執行和交付本應收取費用的ADR 由於該等股份的存放 |
每100張美國存託憑證5美元
(或其部分) |
|||
|
轉移,
分裂或 分組收據 |
存託憑證的轉讓、合併或分組
|
每ADR 1.50美元
|
|||
|
該委員會的開支
託管人 |
代表持票人發生的與下列事項有關的費用:
-遵守外匯管理法規或任何法律或 關於外商投資的規定 -保管人或其託管人遵守適用法律的情況; 規章制度 -股票轉讓或其他税收和其他政府收費 -電報、電傳和傳真的傳輸和交付 -保管人與外國資產轉換有關的費用 貨幣兑換成美元(用這種外幣支付) -任何保管人或其代理人應支付的任何其他費用 |
應由獨資支付的費用
保管人的酌處權 按帳單持有人或按 從一項中扣除費用 或更多現金股息或 其他現金分配 |
|||
|
預支税額減免
|
為合格持有人提供税務減免/回收流程
|
託管服務費
每美國存托股份0.008美元 |
|||
第II部
項目13.拖欠股息和拖欠股息
項目14.對擔保持有人權利的實質性修改和收益的使用
項目15. 控制和程序
項目16A。審計委員會財務專家
項目16B。道德守則
項目16C。首席會計師費用及服務
項目16 D. 豁免審核委員會遵守上市準則
項目16E。發行人及關聯購買人購買股權證券
|
2019 |
總人數 購入的股份 (a) 1 |
平均價格 按股支付 以美元為單位 (b) |
總數 的股份 購得 作為.的一部分 公開 宣佈 計劃或 節目 (c) 2 |
極大值
近似值 的價值 分享 可能還會是 購得 在 計劃或 節目 (百萬瑞士法郎) (d) |
極大值
近似值 的價值 分享 可能還會是 購得 在 計劃或 節目 (百萬美元) (e) 3 |
||||||
|
1月1日至31日
|
1 913 205
|
87.38
|
830 000
|
2 137
|
2 152
|
||||||
|
2月1日至28日
|
203 399
|
88.31
|
0
|
10 000
|
10 027
|
||||||
|
3月1日至31日
|
81 551
|
92.09
|
0
|
10 000
|
10 042
|
||||||
|
4月1日至30日
|
3 687 215
|
80.82
|
3 452 000
|
9 716
|
9 539
|
||||||
|
5月1日至31日
|
15 719 319
|
83.55
|
15 695 000
|
8 392
|
8 338
|
||||||
|
6月1日至30日
|
12 852 939
|
90.27
|
12 840 000
|
7 247
|
7 433
|
||||||
|
7月1日至31日
|
23 550 117
|
92.10
|
23 538 500
|
5 106
|
5 156
|
||||||
|
8月1日至31日
|
3 966 974
|
91.76
|
3 958 400
|
4 752
|
4 809
|
||||||
|
9月1日至30日
|
36 197
|
89.69
|
0
|
4 752
|
4 790
|
||||||
|
10月1日至31日
|
2 031
|
84.92
|
0
|
4 752
|
4 811
|
||||||
|
11月1日至30日
|
16 065
|
87.12
|
0
|
4 752
|
4 758
|
||||||
|
12月1日至31日
|
18 567
|
90.12
|
0
|
4 752
|
4 903
|
||||||
|
|
|
|
|
|
|||||||
|
總計
|
62 047 579
|
88.70
|
60 313 900
|
|
|
|
|
|
|||
|
1 第(a)欄顯示了在瑞士證券交易所第二條交易線上回購的股份,加上我們從通過諾華員工所有權計劃獲得這些股份的員工手中購買的股份。見"項目18。財務報表—附註26聯營公司的股權參與計劃。”
|
|||||||||||
|
2 (c)欄顯示根據2016年股東周年大會(AGM)批准的第七次100億瑞士法郎股份回購授權在SIX瑞士交易所第二條交易線上回購的股份,以及根據2019年股東周年大會批准的第八次100億瑞士法郎股份回購授權在該日期之後的交易。見"項目6。董事、高級管理人員和僱員—項目6C。董事會慣例—我們的資本結構—資本變動。”
|
|||||||||||
|
3 (e)欄顯示截至月底將(d)欄中的瑞士法郎數額換算成美元,使用適用的月底瑞士法郎/美元匯率
|
|||||||||||
項目16F。更改註冊人的認證會計師
項目16G。公司治理
第16H項。煤礦安全信息披露
第三部分
項目17. 財務報表
項目18. 財務報表
項目19.展品
簽名
諾華集團合併財務報表
|
(除非另有説明,否則為百萬美元)
|
注意事項
|
2019
|
2018
|
2017
|
|||||
|
持續運營對第三方的淨銷售額
|
3
|
47 445
|
44 751
|
42 338
|
|||||
|
已終止經營分部的銷售額
|
|
53
|
82
|
43
|
|||||
|
持續經營的淨銷售額
|
|
47 498
|
44 833
|
42 381
|
|||||
|
其他收入
|
3
|
1 179
|
1 266
|
1 023
|
|||||
|
銷貨成本
|
|
– 14 425
|
– 14 510
|
– 13 633
|
|||||
|
持續經營毛利
|
|
34 252
|
31 589
|
29 771
|
|||||
|
銷售、一般和行政管理
|
|
– 14 369
|
– 13 717
|
– 12 465
|
|||||
|
研發
|
|
– 9 402
|
– 8 489
|
– 8 389
|
|||||
|
其他收入
|
|
2 031
|
1 629
|
1 922
|
|||||
|
其他費用
|
|
– 3 426
|
– 2 609
|
– 2 137
|
|||||
|
持續經營的營業收入
|
|
9 086
|
8 403
|
8 702
|
|||||
|
來自相聯公司的收入
|
4
|
659
|
6 438
|
1 108
|
|||||
|
利息支出
|
5
|
– 850
|
– 932
|
– 750
|
|||||
|
其他財務收支
|
5
|
45
|
186
|
42
|
|||||
|
持續經營的税前收入
|
|
8 940
|
14 095
|
9 102
|
|||||
|
税費
|
6
|
– 1 793
|
– 1 295
|
– 1 603
|
|||||
|
持續經營淨收益
|
|
7 147
|
12 800
|
7 499
|
|||||
|
來自已終止經營業務之淨(虧損)╱收入(扣除分派收益前)。諾華公司股東
|
30
|
– 101
|
– 186
|
204
|
|||||
|
Alcon Inc.諾華公司股東
|
2
|
4 691
|
|
|
|||||
|
非持續經營的淨收益/(虧損)
|
30
|
4 590
|
– 186
|
204
|
|||||
|
淨收入
|
|
11 737
|
12 614
|
7 703
|
|||||
|
歸因於:
|
|
|
|
|
|||||
|
諾華製藥的股東
|
|
11 732
|
12 611
|
7 703
|
|||||
|
非控制性權益
|
|
5
|
3
|
0
|
|||||
|
|
|
|
|
||||||
|
持續經營的基本每股收益(美元)
|
|
3.12
|
5.52
|
3.20
|
|||||
|
非持續經營的基本每股收益(美元)
|
|
2.00
|
– 0.08
|
0.08
|
|||||
|
每股基本收益合計(美元)
|
7
|
5.12
|
5.44
|
3.28
|
|||||
|
|
|
|
|
||||||
|
持續運營的稀釋後每股收益(美元)
|
|
3.08
|
5.46
|
3.17
|
|||||
|
非持續經營的攤薄後每股收益(美元)
|
|
1.98
|
– 0.08
|
0.08
|
|||||
|
每股攤薄後總收益(美元)
|
7
|
5.06
|
5.38
|
3.25
|
|||||
|
附註是綜合財務報表的組成部分。
|
|||||||||
|
(百萬美元)
|
注意事項
|
2019
|
2018
|
2017
|
|||||
|
淨收入
|
|
11 737
|
12 614
|
7 703
|
|||||
|
其他全面收益將最終撥回綜合收益表:
|
|
|
|
|
|||||
|
有價證券公允價值調整,扣除税項
|
8.1
|
|
|
39
|
|||||
|
債務證券公允價值調整,扣除税項
|
8.1
|
1
|
|
– 1
|
|||||
|
遞延現金流量對衝的公允價值調整,扣除税項
|
8.1
|
1
|
12
|
12
|
|||||
|
金融工具公允價值調整總額,扣除税項
|
|
2
|
12
|
50
|
|||||
|
諾華應佔聯營公司確認的其他綜合收益(扣除税項)
|
4
|
– 94
|
– 482
|
– 37
|
|||||
|
淨投資對衝
|
8
|
44
|
95
|
– 237
|
|||||
|
貨幣換算效應
|
8.2
|
352
|
315
|
2 210
|
|||||
|
最終要回收的項目總數
|
|
304
|
– 60
|
1 986
|
|||||
|
其他全面收益概不會重新撥回綜合收益表:
|
|
|
|
|
|||||
|
精算(虧損)/受益確定型福利計劃的收益,扣除税款
|
8.3
|
– 467
|
– 359
|
851
|
|||||
|
權益證券扣除税項後的公允價值調整
|
8.1
|
– 47
|
13
|
|
|||||
|
永遠不能回收的物品總數
|
|
– 514
|
– 346
|
851
|
|||||
|
綜合收益總額
|
|
11 527
|
12 208
|
10 540
|
|||||
|
歸因於:
|
|
|
|
|
|||||
|
諾華製藥的股東
|
|
11 525
|
12 210
|
10 538
|
|||||
|
持續運營
|
|
6 948
|
12 417
|
10 211
|
|||||
|
停產經營
|
|
4 577
|
– 207
|
327
|
|||||
|
非控制性權益
|
|
2
|
– 2
|
2
|
|||||
|
附註是綜合財務報表的組成部分。
|
|||||||||
|
(百萬美元)
|
注意事項
|
2019
|
2018
|
||||
|
資產
|
|
|
|
||||
|
非流動資產
|
|
|
|
||||
|
財產、廠房和設備
|
9
|
12 069
|
15 696
|
||||
|
使用權資產
|
10
|
1 677
|
|
||||
|
商譽
|
11
|
26 524
|
35 294
|
||||
|
商譽以外的無形資產
|
11
|
28 787
|
38 719
|
||||
|
對相聯公司的投資
|
4
|
8 644
|
8 352
|
||||
|
遞延税項資產
|
12
|
7 909
|
8 699
|
||||
|
金融資產
|
13
|
2 518
|
2 345
|
||||
|
其他非流動資產
|
13
|
738
|
895
|
||||
|
非流動資產總額
|
|
88 866
|
110 000
|
||||
|
流動資產
|
|
|
|
||||
|
盤存
|
14
|
5 982
|
6 956
|
||||
|
應收貿易賬款
|
15
|
8 301
|
8 727
|
||||
|
應收所得税
|
|
254
|
248
|
||||
|
有價證券、商品、定期存款和衍生金融工具
|
16
|
334
|
2 693
|
||||
|
現金和現金等價物
|
16
|
11 112
|
13 271
|
||||
|
其他流動資產
|
17
|
2 680
|
2 861
|
||||
|
未處置組的流動資產合計
|
|
28 663
|
34 756
|
||||
|
出售集團持有待售資產
|
2
|
841
|
807
|
||||
|
流動資產總額
|
|
29 504
|
35 563
|
||||
|
總資產
|
|
118 370
|
145 563
|
||||
|
|
|
|
|||||
|
權益和負債
|
|
|
|
||||
|
權益
|
|
|
|
||||
|
股本
|
18
|
936
|
944
|
||||
|
國庫股
|
18
|
– 80
|
– 69
|
||||
|
儲量
|
|
54 618
|
77 739
|
||||
|
諾華製藥股東應佔已發行股本和公積金
|
|
55 474
|
78 614
|
||||
|
非控制性權益
|
|
77
|
78
|
||||
|
總股本
|
|
55 551
|
78 692
|
||||
|
負債
|
|
|
|
||||
|
非流動負債
|
|
|
|
||||
|
金融債務
|
19
|
20 353
|
22 470
|
||||
|
租賃負債
|
10
|
1 703
|
|
||||
|
遞延税項負債
|
12
|
5 867
|
7 475
|
||||
|
準備金和其他非流動負債
|
20
|
6 632
|
7 319
|
||||
|
非流動負債總額
|
|
34 555
|
37 264
|
||||
|
流動負債
|
|
|
|
||||
|
貿易應付款
|
|
5 424
|
5 556
|
||||
|
金融債務和衍生金融工具
|
21
|
7 031
|
9 678
|
||||
|
租賃負債
|
10
|
246
|
|
||||
|
流動所得税負債
|
|
2 194
|
2 038
|
||||
|
準備金和其他流動負債
|
22
|
13 338
|
12 284
|
||||
|
未處置組的流動負債總額
|
|
28 233
|
29 556
|
||||
|
出售集團持有待售資產的負債
|
2
|
31
|
51
|
||||
|
流動負債總額
|
|
28 264
|
29 607
|
||||
|
總負債
|
|
62 819
|
66 871
|
||||
|
權益和負債總額
|
|
118 370
|
145 563
|
||||
|
附註是綜合財務報表的組成部分。
|
|||||||
|
(百萬美元) |
注意事項 |
分享 資本 |
財務處 股票 |
保留 收益 |
總價值 調整 |
已發行股份
資本和 儲量 可歸因性 致諾華製藥 股東 |
非- 控管 利益 |
總計 股權 |
|||||||||
|
2017年1月1日的總股本
|
|
972
|
– 76
|
81 148
|
– 7 212
|
74 832
|
59
|
74 891
|
|||||||||
|
淨收入
|
|
|
|
7 703
|
|
7 703
|
|
7 703
|
|||||||||
|
其他綜合收益
|
8
|
|
|
– 37
|
2 872
|
2 835
|
2
|
2 837
|
|||||||||
|
綜合收益總額
|
|
|
|
7 666
|
2 872
|
10 538
|
2
|
10 540
|
|||||||||
|
分紅
|
18.1
|
|
|
– 6 495
|
|
– 6 495
|
|
– 6 495
|
|||||||||
|
購買庫藏股
|
18.2
|
|
– 36
|
– 5 538
|
|
– 5 574
|
|
– 5 574
|
|||||||||
|
減少股本
|
18
|
– 3
|
5
|
– 2
|
|
|
|
|
|||||||||
|
行使期權和員工交易
|
18.2
|
|
2
|
253
|
|
255
|
|
255
|
|||||||||
|
基於股權的薪酬
|
18.2
|
|
5
|
607
|
|
612
|
|
612
|
|||||||||
|
非控股權益的變動
|
18.6
|
|
|
|
|
|
– 2
|
– 2
|
|||||||||
|
其他股票變動合計
|
|
– 3
|
– 24
|
– 11 175
|
|
– 11 202
|
– 2
|
– 11 204
|
|||||||||
|
截至2017年12月31日的總權益,如先前報告
|
|
969
|
– 100
|
77 639
|
– 4 340
|
74 168
|
59
|
74 227
|
|||||||||
|
會計政策變動的影響
|
1
|
|
|
237
|
– 177
|
60
|
|
60
|
|||||||||
|
2018年1月1日重列權益
|
|
969
|
– 100
|
77 876
|
– 4 517
|
74 228
|
59
|
74 287
|
|||||||||
|
淨收入
|
|
|
|
12 611
|
|
12 611
|
3
|
12 614
|
|||||||||
|
其他綜合收益
|
8
|
|
|
– 482
|
81
|
– 401
|
– 5
|
– 406
|
|||||||||
|
綜合收益總額
|
|
|
|
12 129
|
81
|
12 210
|
– 2
|
12 208
|
|||||||||
|
分紅
|
18.1
|
|
|
– 6 966
|
|
– 6 966
|
|
– 6 966
|
|||||||||
|
購買庫藏股
|
18.2
|
|
– 13
|
– 1 960
|
|
– 1 973
|
|
– 1 973
|
|||||||||
|
減少股本
|
18
|
– 25
|
34
|
– 9
|
|
|
|
|
|||||||||
|
行使期權和員工交易
|
18.2
|
|
4
|
430
|
|
434
|
|
434
|
|||||||||
|
其他股份銷售
|
18.2
|
|
2
|
261
|
|
263
|
|
263
|
|||||||||
|
基於股權的薪酬
|
18.2
|
|
4
|
752
|
|
756
|
|
756
|
|||||||||
|
根據股份回購交易計劃增加庫存股回購責任
|
18.3
|
|
|
– 284
|
|
– 284
|
|
– 284
|
|||||||||
|
交易成本,税後淨額
|
18.4
|
|
|
– 79
|
|
– 79
|
|
– 79
|
|||||||||
|
出售金融資產的公允價值調整
|
8
|
|
|
16
|
– 16
|
|
|
|
|||||||||
|
合併實體所有權變更的影響
|
18.5
|
|
|
– 13
|
|
– 13
|
22
|
9
|
|||||||||
|
非控股權益的變動
|
18.6
|
|
|
|
|
|
– 1
|
– 1
|
|||||||||
|
其他動作
|
18.7
|
|
|
38
|
|
38
|
|
38
|
|||||||||
|
其他股票變動合計
|
|
– 25
|
31
|
– 7 814
|
– 16
|
– 7 824
|
21
|
– 7 803
|
|||||||||
|
截至2018年12月31日的總權益,如先前報告
|
|
944
|
|
– 69
|
|
82 191
|
|
– 4 452
|
|
78 614
|
|
78
|
|
78 692
|
|||
|
會計政策變動的影響
|
1
|
|
|
|
|
3
|
|
|
|
3
|
|
|
|
3
|
|||
|
2019年1月1日重列權益
|
|
944
|
|
– 69
|
|
82 194
|
|
– 4 452
|
|
78 617
|
|
78
|
|
78 695
|
|||
|
淨收入
|
|
|
|
11 732
|
|
11 732
|
5
|
11 737
|
|||||||||
|
其他綜合收益
|
8
|
|
|
– 94
|
– 113
|
– 207
|
– 3
|
– 210
|
|||||||||
|
綜合收益總額
|
|
|
|
11 638
|
– 113
|
11 525
|
2
|
11 527
|
|||||||||
|
分紅
|
18.1
|
|
|
– 6 645
|
|
– 6 645
|
|
– 6 645
|
|||||||||
|
實物股息,以實現愛爾康公司的剝離。
|
2
|
|
|
– 23 434
|
|
– 23 434
|
|
– 23 434
|
|||||||||
|
購買庫藏股
|
18.2
|
|
– 31
|
– 5 480
|
|
– 5 511
|
|
– 5 511
|
|||||||||
|
減少股本
|
18
|
– 8
|
12
|
– 4
|
|
|
|
|
|||||||||
|
行使期權和員工交易
|
18.2
|
|
3
|
207
|
|
210
|
|
210
|
|||||||||
|
基於股權的薪酬
|
18.2
|
|
5
|
828
|
|
833
|
|
833
|
|||||||||
|
作為剝離愛爾康的結果,交付給愛爾康員工的股票
|
18.2
|
|
|
18
|
|
18
|
|
18
|
|||||||||
|
庫藏股交易税
|
|
|
|
– 189
|
|
– 189
|
|
– 189
|
|||||||||
|
減少股份回購交易計劃下的庫存股回購責任
|
18.3
|
|
|
284
|
|
284
|
|
284
|
|||||||||
|
交易成本,税後淨額
|
18.4
|
|
|
– 253
|
|
– 253
|
|
– 253
|
|||||||||
|
出售金融資產的公允價值調整
|
8
|
|
|
95
|
– 95
|
|
|
|
|||||||||
|
合併實體所有權變更的影響
|
18.5
|
|
|
– 3
|
|
– 3
|
– 2
|
– 5
|
|||||||||
|
非控股權益的變動
|
18.6
|
|
|
|
|
|
– 1
|
– 1
|
|||||||||
|
與剝離有關的公允價值調整
|
8
|
|
|
– 3
|
3
|
|
|
|
|||||||||
|
其他動作
|
18.7
|
|
|
22
|
|
22
|
|
22
|
|||||||||
|
其他股票變動合計
|
|
– 8
|
– 11
|
– 34 557
|
– 92
|
– 34 668
|
– 3
|
– 34 671
|
|||||||||
|
2019年12月31日的總權益
|
|
936
|
– 80
|
59 275
|
– 4 657
|
55 474
|
77
|
55 551
|
|||||||||
|
附註是綜合財務報表的組成部分。
|
|||||||||||||||||
|
(百萬美元)
|
注意事項
|
2019
|
2018
|
2017
|
|||||
|
持續經營淨收益
|
|
7 147
|
12 800
|
7 499
|
|||||
|
將持續業務的淨收入與持續業務的業務活動現金流量淨額進行調整
|
|
|
|
|
|||||
|
沖銷非現金項目和其他調整
|
23.1
|
9 122
|
1 486
|
5 787
|
|||||
|
從聯營公司及其他公司收取的股息
|
|
463
|
719
|
987
|
|||||
|
收到的利息
|
|
214
|
241
|
97
|
|||||
|
支付的利息
|
|
– 793
|
– 816
|
– 697
|
|||||
|
其他財務收入
|
|
28
|
218
|
|
|||||
|
其他財務付款
|
|
– 33
|
– 31
|
– 270
|
|||||
|
已繳納的税款
|
23.2
|
– 1 876
|
– 1 506
|
– 1 487
|
|||||
|
營運資金和撥備變動前持續經營活動產生的經營活動現金流量淨額
|
|
14 272
|
13 111
|
11 916
|
|||||
|
從準備金和非流動負債中的其他淨現金流動中支付
|
|
– 924
|
– 638
|
– 829
|
|||||
|
流動資產淨值和其他經營性現金流量項目變動
|
23.3
|
199
|
576
|
332
|
|||||
|
來自持續經營的經營活動現金流量淨額
|
|
13 547
|
13 049
|
11 419
|
|||||
|
來自非持續經營的經營活動的現金流量淨額
|
|
78
|
1 223
|
1 202
|
|||||
|
業務活動現金流量淨額共計
|
|
13 625
|
14 272
|
12 621
|
|||||
|
購置房產、廠房和設備
|
|
– 1 379
|
– 1 254
|
– 1 325
|
|||||
|
出售財產、廠房和設備所得收益
|
|
857
|
102
|
91
|
|||||
|
購買無形資產
|
|
– 878
|
– 1 394
|
– 969
|
|||||
|
出售無形資產所得款項
|
|
973
|
823
|
640
|
|||||
|
購買金融資產
|
|
– 302
|
– 205
|
– 354
|
|||||
|
出售金融資產所得收益
|
|
1 152
|
165
|
328
|
|||||
|
購買其他非流動資產
|
|
– 60
|
– 39
|
– 40
|
|||||
|
出售其他非流動資產所得款項
|
|
3
|
9
|
1
|
|||||
|
收購和撤資聯營公司的權益,淨額
|
23.4
|
– 6
|
12 854
|
29
|
|||||
|
企業收購和撤資,淨額
|
23.5
|
– 3 760
|
– 13 683
|
– 714
|
|||||
|
購買有價證券和商品
|
|
– 228
|
– 2 440
|
– 580
|
|||||
|
出售有價證券和商品所得
|
|
2 561
|
472
|
549
|
|||||
|
用於持續經營的投資活動的現金流量淨額
|
|
– 1 067
|
– 4 590
|
– 2 344
|
|||||
|
用於投資活動的非持續業務現金流量淨額
|
30
|
– 1 159
|
– 1 001
|
– 775
|
|||||
|
投資活動所用現金流量淨額共計
|
|
– 2 226
|
– 5 591
|
– 3 119
|
|||||
|
支付給諾華製藥股東的股息
|
|
– 6 645
|
– 6 966
|
– 6 495
|
|||||
|
收購庫藏股
|
|
– 5 533
|
– 2 036
|
– 5 490
|
|||||
|
行使期權及其他庫藏股交易所得收益
|
|
201
|
700
|
252
|
|||||
|
非流動金融債務增加
|
23.6
|
93
|
2 856
|
4 933
|
|||||
|
償還非流動金融債務
|
23.6
|
– 3 195
|
– 366
|
– 188
|
|||||
|
本期財政債務變動情況
|
23.6
|
– 1 582
|
1 687
|
– 644
|
|||||
|
支付租賃負債,淨額
|
23.6
|
– 273
|
|
|
|||||
|
合併實體所有權變更的影響
|
|
– 6
|
– 19
|
0
|
|||||
|
其他融資現金流,淨額
|
|
56
|
67
|
314
|
|||||
|
用於持續業務籌資活動的現金流量淨額
|
|
– 16 884
|
– 4 077
|
– 7 318
|
|||||
|
來自/用於已終止經營業務融資活動的現金流量淨額
|
30
|
3 257
|
– 167
|
– 415
|
|||||
|
用於籌資活動的現金流量淨額總額
|
|
– 13 627
|
– 4 244
|
– 7 733
|
|||||
|
匯率變動影響前的現金和現金等價物淨變化
|
|
– 2 228
|
4 437
|
1 769
|
|||||
|
匯率變動對現金及現金等價物的影響
|
|
69
|
– 26
|
84
|
|||||
|
現金和現金等價物淨變化總額
|
|
– 2 159
|
4 411
|
1 853
|
|||||
|
1月1日的現金和現金等價物
|
|
13 271
|
8 860
|
7 007
|
|||||
|
12月31日的現金和現金等價物
|
|
11 112
|
13 271
|
8 860
|
|||||
|
附註是綜合財務報表的組成部分。
|
|||||||||
|
|
|||||||||
諾華集團合併財務報表附註
|
使用壽命
|
|||
|
建築物
|
20到40年
|
||
|
機械及其他設備
|
|
||
|
機器和設備
|
7到20年
|
||
|
傢俱和車輛
|
5至10年
|
||
|
計算機硬件
|
3至7年
|
||
|
使用壽命 |
損益表位置
用於攤銷和 減值費用 |
||||
|
目前市場上銷售的產品
|
5到20年
|
“銷貨成本”
|
|||
|
營銷訣竅
|
25年
|
“銷貨成本”
|
|||
|
技術
|
10到20年
|
"銷售貨物成本" 或"研究 和發展"
|
|||
|
其他(包括計算機軟件)
|
3至7年
|
在相應的 功能費用
|
|||
|
愛爾康品牌名稱
|
未攤銷,無限期使用壽命
|
“其他費用”
|
|||
|
(百萬美元) |
4月8日,
2019 |
||
|
取消確認的淨資產 1
|
– 20 025
|
||
|
對分銷責任的不再確認
|
23 434
|
||
|
淨資產和分配負債之間的差額
|
3 409
|
||
|
關於Alcon Inc.通過合併基金會獲得的股份
|
1 273
|
||
|
貨幣換算收益循環至綜合收益表
|
123
|
||
|
在綜合收益表中確認的交易成本
|
– 114
|
||
|
Alcon Inc.諾華公司股東
|
4 691
|
||
|
1 更多信息見附註30。
|
|||
|
(百萬美元) |
十二月三十一日,
2019 |
十二月三十一日,
2018 |
|||
|
分類為持作出售的出售組別資產
|
|
|
|||
|
財產、廠房和設備
|
169
|
148
|
|||
|
商譽以外的無形資產
|
475
|
478
|
|||
|
遞延税項資產
|
11
|
8
|
|||
|
其他非流動資產
|
2
|
1
|
|||
|
盤存
|
181
|
165
|
|||
|
其他流動資產
|
3
|
7
|
|||
|
總計
|
841
|
807
|
|||
|
(百萬美元) |
十二月三十一日,
2019 |
十二月三十一日,
2018 |
|||
|
分類為持作出售之出售組別負債
|
|
|
|||
|
遞延税項負債
|
2
|
2
|
|||
|
準備金和其他非流動負債
|
4
|
4
|
|||
|
準備金和其他流動負債
|
25
|
45
|
|||
|
總計
|
31
|
51
|
|||
|
創新藥物
|
桑多茲
|
公司(包括淘汰)
|
集團化
|
||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
|||||||||
|
持續運營對第三方的淨銷售額
|
37 714
|
34 892
|
9 731
|
9 859
|
|
|
47 445
|
44 751
|
|||||||||
|
向持續經營及終止經營分部的銷售
|
783
|
741
|
141
|
177
|
– 871
|
– 836
|
53
|
82
|
|||||||||
|
持續經營的淨銷售額
|
38 497
|
35 633
|
9 872
|
10 036
|
– 871
|
– 836
|
47 498
|
44 833
|
|||||||||
|
其他收入
|
1 092
|
1 188
|
63
|
62
|
24
|
16
|
1 179
|
1 266
|
|||||||||
|
銷貨成本
|
– 10 050
|
– 9 870
|
– 5 334
|
– 5 530
|
959
|
890
|
– 14 425
|
– 14 510
|
|||||||||
|
持續經營毛利
|
29 539
|
26 951
|
4 601
|
4 568
|
112
|
70
|
34 252
|
31 589
|
|||||||||
|
銷售、一般和行政管理
|
– 11 617
|
– 10 907
|
– 2 218
|
– 2 305
|
– 534
|
– 505
|
– 14 369
|
– 13 717
|
|||||||||
|
研發
|
– 8 152
|
– 7 675
|
– 1 250
|
– 814
|
|
|
– 9 402
|
– 8 489
|
|||||||||
|
其他收入
|
1 586
|
977
|
167
|
505
|
278
|
147
|
2 031
|
1 629
|
|||||||||
|
其他費用
|
– 2 069
|
– 1 475
|
– 749
|
– 622
|
– 608
|
– 512
|
– 3 426
|
– 2 609
|
|||||||||
|
持續經營的營業收入
|
9 287
|
7 871
|
551
|
1 332
|
– 752
|
– 800
|
9 086
|
8 403
|
|||||||||
|
來自相聯公司的收入
|
1
|
1
|
2
|
5
|
656
|
6 432
|
659
|
6 438
|
|||||||||
|
利息支出
|
|
|
|
|
|
|
– 850
|
– 932
|
|||||||||
|
其他財務收支
|
|
|
|
|
|
|
45
|
186
|
|||||||||
|
持續經營的税前收入
|
|
|
|
|
|
|
8 940
|
14 095
|
|||||||||
|
税費
|
|
|
|
|
|
|
– 1 793
|
– 1 295
|
|||||||||
|
持續經營淨收益
|
|
|
|
|
|
|
7 147
|
12 800
|
|||||||||
|
停止經營的淨虧損扣除分配給諾華製藥股東的收益前的淨虧損
|
|
|
|
|
|
|
– 101
|
– 186
|
|||||||||
|
Alcon Inc.諾華公司股東
|
|
|
|
|
|
|
4 691
|
|
|||||||||
|
非持續經營的淨收益/(虧損)
|
|
|
|
|
|
|
4 590
|
– 186
|
|||||||||
|
淨收入
|
|
|
|
|
|
|
|
|
11 737
|
12 614
|
|
||||||
|
歸因於:
|
|
|
|
|
|
|
|
|
|||||||||
|
諾華製藥的股東
|
|
|
|
|
|
|
11 732
|
12 611
|
|||||||||
|
非控制性權益
|
|
|
|
|
|
|
5
|
3
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
持續經營的淨收入包括:
|
|
|
|
|
|
|
|
|
|||||||||
|
利息收入
|
|
|
|
|
|
|
245
|
292
|
|||||||||
|
財產、廠房和設備折舊
|
– 952
|
– 1 075
|
– 283
|
– 285
|
– 110
|
– 122
|
– 1 345
|
– 1 482
|
|||||||||
|
使用權資產折舊 1
|
– 247
|
|
– 41
|
|
– 17
|
|
– 305
|
|
|||||||||
|
無形資產攤銷
|
– 2 509
|
– 2 214
|
– 315
|
– 366
|
– 12
|
– 7
|
– 2 836
|
– 2 587
|
|||||||||
|
不動產、廠場和設備減值費用淨額
|
– 100
|
– 239
|
– 101
|
– 60
|
– 1
|
– 2
|
– 202
|
– 301
|
|||||||||
|
無形資產減值費用淨額
|
– 632
|
– 592
|
– 506
|
– 249
|
|
|
– 1 138
|
– 841
|
|||||||||
|
金融資產減值支出及公允價值變動淨額
|
18
|
107
|
|
|
20
|
– 113
|
38
|
– 6
|
|||||||||
|
對重組條款的補充
|
– 229
|
– 395
|
– 165
|
– 32
|
– 98
|
– 94
|
– 492
|
– 521
|
|||||||||
|
諾華股權計劃的股權補償
|
– 761
|
– 645
|
– 67
|
– 53
|
– 239
|
– 220
|
– 1 067
|
– 918
|
|||||||||
|
|
|||||||||||||||||
|
1 使用權資產折舊自二零一九年一月一日(國際財務報告準則第16號租賃的實施日期)起確認。附註1和10提供了額外披露。
|
|||||||||||||||||
|
|
|||||||||||||||||
|
創新藥物
|
桑多茲
|
公司(包括淘汰)
|
集團化
|
||||||||||||||
|
(百萬美元)
|
2018
|
2017
|
2018
|
2017
|
2018
|
2017
|
2018
|
2017
|
|||||||||
|
持續運營對第三方的淨銷售額
|
34 892
|
32 278
|
9 859
|
10 060
|
|
|
44 751
|
42 338
|
|||||||||
|
向持續經營及終止經營分部的銷售
|
741
|
668
|
177
|
118
|
– 836
|
– 743
|
82
|
43
|
|||||||||
|
持續經營的淨銷售額
|
35 633
|
32 946
|
10 036
|
10 178
|
– 836
|
– 743
|
44 833
|
42 381
|
|||||||||
|
其他收入
|
1 188
|
898
|
62
|
37
|
16
|
88
|
1 266
|
1 023
|
|||||||||
|
銷貨成本
|
– 9 870
|
– 8 650
|
– 5 530
|
– 5 800
|
890
|
817
|
– 14 510
|
– 13 633
|
|||||||||
|
持續經營毛利
|
26 951
|
25 194
|
4 568
|
4 415
|
70
|
162
|
31 589
|
29 771
|
|||||||||
|
銷售、一般和行政管理
|
– 10 907
|
– 9 887
|
– 2 305
|
– 2 126
|
– 505
|
– 452
|
– 13 717
|
– 12 465
|
|||||||||
|
研發
|
– 7 675
|
– 7 615
|
– 814
|
– 774
|
|
|
– 8 489
|
– 8 389
|
|||||||||
|
其他收入
|
977
|
1 027
|
505
|
204
|
147
|
691
|
1 629
|
1 922
|
|||||||||
|
其他費用
|
– 1 475
|
– 1 124
|
– 622
|
– 351
|
– 512
|
– 662
|
– 2 609
|
– 2 137
|
|||||||||
|
持續經營的營業收入
|
7 871
|
7 595
|
1 332
|
1 368
|
– 800
|
– 261
|
8 403
|
8 702
|
|||||||||
|
來自相聯公司的收入
|
1
|
– 1
|
5
|
23
|
6 432
|
1 086
|
6 438
|
1 108
|
|||||||||
|
利息支出
|
|
|
|
|
|
|
– 932
|
– 750
|
|||||||||
|
其他財務收支
|
|
|
|
|
|
|
186
|
42
|
|||||||||
|
持續經營的税前收入
|
|
|
|
|
|
|
14 095
|
9 102
|
|||||||||
|
税費
|
|
|
|
|
|
|
– 1 295
|
– 1 603
|
|||||||||
|
持續經營淨收益
|
|
|
|
|
|
|
12 800
|
7 499
|
|||||||||
|
淨(虧損)/非持續經營收入
|
|
|
|
|
|
|
– 186
|
204
|
|||||||||
|
淨收入
|
|
|
|
|
|
|
|
|
|
12 614
|
7 703
|
|
|||||
|
歸因於:
|
|
|
|
|
|
|
|
|
|||||||||
|
諾華製藥的股東
|
|
|
|
|
|
|
12 611
|
7 703
|
|||||||||
|
非控制性權益
|
|
|
|
|
|
|
3
|
0
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
持續經營的淨收入包括:
|
|
|
|
|
|
|
|
|
|||||||||
|
利息收入
|
|
|
|
|
|
|
292
|
110
|
|||||||||
|
財產、廠房和設備折舊
|
– 1 075
|
– 916
|
– 285
|
– 270
|
– 122
|
– 117
|
– 1 482
|
– 1 303
|
|||||||||
|
無形資產攤銷
|
– 2 214
|
– 2 167
|
– 366
|
– 447
|
– 7
|
– 10
|
– 2 587
|
– 2 624
|
|||||||||
|
不動產、廠場和設備減值費用淨額
|
– 239
|
– 84
|
– 60
|
– 73
|
– 2
|
|
– 301
|
– 157
|
|||||||||
|
無形資產減值費用淨額
|
– 592
|
– 591
|
– 249
|
– 61
|
|
|
– 841
|
– 652
|
|||||||||
|
金融資產減值支出及公允價值變動淨額
|
107
|
– 42
|
|
|
– 113
|
– 185
|
– 6
|
– 227
|
|||||||||
|
對重組條款的補充
|
– 395
|
– 122
|
– 32
|
– 61
|
– 94
|
– 3
|
– 521
|
– 186
|
|||||||||
|
諾華股權計劃的股權補償
|
– 645
|
– 593
|
– 53
|
– 52
|
– 220
|
– 208
|
– 918
|
– 853
|
|||||||||
|
|
|||||||||||||||||
|
|
|||||||||||||||||
|
創新藥物
|
桑多茲
|
阿爾康1
|
公司(包括淘汰)
|
集團化
|
|||||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
|||||||||||
|
總資產
|
71 225
|
67 055
|
16 468
|
17 328
|
|
25 971
|
30 677
|
35 209
|
118 370
|
145 563
|
|||||||||||
|
總負債
|
– 15 332
|
– 13 056
|
– 3 804
|
– 3 377
|
|
– 1 964
|
– 43 683
|
– 48 474
|
– 62 819
|
– 66 871
|
|||||||||||
|
總股本
|
|
|
|
|
|
|
|
|
55 551
|
78 692
|
|||||||||||
|
淨債務
|
|
|
|
|
|
|
|
|
15 938
|
16 184
|
|||||||||||
|
淨營業資產
|
55 893
|
53 999
|
12 664
|
13 951
|
|
24 007
|
|
|
71 489
|
94 876
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
資產及負債包括:
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
財產、廠房和設備合計
|
9 632
|
10 098
|
1 888
|
2 159
|
|
2 878
|
549
|
561
|
12 069
|
15 696
|
|||||||||||
|
不動產、廠場和設備的增加 2
|
1 114
|
822
|
217
|
294
|
|
519
|
143
|
139
|
1 474
|
1 774
|
|||||||||||
|
使用權資產總額 3
|
1 487
|
|
136
|
|
|
|
54
|
|
1 677
|
|
|||||||||||
|
對使用權資產的補充 2, 3
|
454
|
|
49
|
|
|
|
34
|
|
537
|
|
|||||||||||
|
商譽和無形資產總額
|
46 336
|
44 593
|
8 892
|
9 712
|
|
19 578
|
83
|
130
|
55 311
|
74 013
|
|||||||||||
|
商譽和無形資產的增加 2
|
647
|
1 265
|
68
|
107
|
|
196
|
52
|
24
|
767
|
1 592
|
|||||||||||
|
對聯營公司的總投資
|
128
|
81
|
7
|
7
|
|
|
8 509
|
8 264
|
8 644
|
8 352
|
|||||||||||
|
增加對相聯公司的投資
|
44
|
18
|
|
|
|
|
11
|
11
|
55
|
29
|
|||||||||||
|
現金及現金等價物、有價證券、商品、定期存款和衍生金融工具
|
|
|
|
|
|
|
11 446
|
15 964
|
11 446
|
15 964
|
|||||||||||
|
金融債務和衍生金融工具
|
|
|
|
|
|
|
27 384
|
32 148
|
27 384
|
32 148
|
|||||||||||
|
當期所得税和遞延税項負債
|
|
|
|
|
|
|
8 061
|
9 513
|
8 061
|
9 513
|
|||||||||||
|
1 據報告,自2019年2月28日起,阿爾孔司已停止運作(見附註1、2和30)。根據國際財務報告準則,2018年12月31日的綜合資產負債表包括愛爾康眼科護理設備業務的資產和負債,以及阿爾康業務應佔的某些公司資產和負債。附註30提供了關於停產業務的補充資料。
|
|||||||||||||||||||||
|
2 不包括企業合併的影響。
|
|||||||||||||||||||||
|
3 2019年1月1日實施IFRS 16租約後,2019年確認的總使用權資產和對使用權資產的增加。有關其他披露,請參閲附註1和10。
|
|||||||||||||||||||||
|
淨銷售額1
|
選定非流動資產合計2
|
||||||||||||||||||||
|
(百萬美元)
|
2019
|
%
|
2018
|
%
|
2017
|
%
|
2019
|
%
|
2018
|
%
|
|||||||||||
|
國家
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
瑞士
|
848
|
2
|
795
|
2
|
780
|
2
|
33 032
|
43
|
41 972
|
43
|
|||||||||||
|
美國
|
16 280
|
34
|
14 618
|
33
|
14 135
|
33
|
28 893
|
37
|
39 082
|
40
|
|||||||||||
|
法國
|
2 442
|
5
|
2 505
|
6
|
2 289
|
5
|
3 933
|
5
|
3 976
|
4
|
|||||||||||
|
德國
|
4 120
|
9
|
3 972
|
9
|
3 484
|
8
|
2 554
|
3
|
3 124
|
3
|
|||||||||||
|
日本
|
2 656
|
6
|
2 575
|
6
|
2 617
|
6
|
309
|
|
144
|
|
|||||||||||
|
其他
|
21 099
|
44
|
20 286
|
44
|
19 033
|
46
|
8 980
|
12
|
9 763
|
10
|
|||||||||||
|
集團化
|
47 445
|
100
|
44 751
|
100
|
42 338
|
100
|
77 701
|
100
|
98 061
|
100
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
區域
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
歐洲
|
17 933
|
38
|
17 259
|
39
|
15 760
|
37
|
46 103
|
59
|
55 913
|
57
|
|||||||||||
|
美洲
|
19 713
|
41
|
18 032
|
39
|
17 485
|
41
|
29 389
|
38
|
39 082
|
40
|
|||||||||||
|
亞洲/非洲/澳大拉西亞
|
9 799
|
21
|
9 460
|
22
|
9 093
|
22
|
2 209
|
3
|
3 066
|
3
|
|||||||||||
|
集團化
|
47 445
|
100
|
44 751
|
100
|
42 338
|
100
|
77 701
|
100
|
98 061
|
100
|
|||||||||||
|
|
|||||||||||||||||||||
|
1 按第三方客户所在地劃分的運營淨銷售額
|
|||||||||||||||||||||
|
2 物業、廠房及設備;商譽;無形資產;及於聯營公司的投資,以及於二零一九年的使用權資產總額於二零一九年一月一日實施國際財務報告準則第16號租賃時確認。其他披露見附註1和10。
|
|||||||||||||||||||||
|
2019 百萬美元 |
2018 百萬美元 |
變化
(2018 至2019年) 美元% |
2017 百萬美元 |
變化
(2017 至2018年) 美元% |
|||||||
|
創新藥物
|
|
|
|
|
|
||||||
|
歐洲
|
12 818
|
12 296
|
4
|
11 127
|
11
|
||||||
|
我們
|
13 789
|
11 864
|
16
|
10 857
|
9
|
||||||
|
亞洲/非洲/澳大拉西亞
|
8 458
|
8 097
|
4
|
7 702
|
5
|
||||||
|
加拿大和拉丁美洲
|
2 649
|
2 635
|
1
|
2 592
|
2
|
||||||
|
總計
|
37 714
|
34 892
|
8
|
32 278
|
8
|
||||||
|
其中在成熟市場
|
28 573
|
26 258
|
9
|
24 174
|
9
|
||||||
|
其中新興增長市場
|
9 141
|
8 634
|
6
|
8 104
|
7
|
||||||
|
|
|
|
|
|
|||||||
|
桑多茲
|
|
|
|
|
|
||||||
|
歐洲
|
5 115
|
4 963
|
3
|
4 633
|
7
|
||||||
|
我們
|
2 491
|
2 754
|
– 10
|
3 278
|
– 16
|
||||||
|
亞洲/非洲/澳大拉西亞
|
1 341
|
1 363
|
– 2
|
1 391
|
– 2
|
||||||
|
加拿大和拉丁美洲
|
784
|
779
|
1
|
758
|
3
|
||||||
|
總計
|
9 731
|
9 859
|
– 1
|
10 060
|
– 2
|
||||||
|
其中在成熟市場
|
7 111
|
7 233
|
– 2
|
7 383
|
– 2
|
||||||
|
其中新興增長市場
|
2 620
|
2 626
|
0
|
2 677
|
– 2
|
||||||
|
|
|
|
|
|
|||||||
|
集團化
|
|
|
|
|
|
||||||
|
歐洲
|
17 933
|
17 259
|
4
|
15 760
|
10
|
||||||
|
我們
|
16 280
|
14 618
|
11
|
14 135
|
3
|
||||||
|
亞洲/非洲/澳大拉西亞
|
9 799
|
9 460
|
4
|
9 093
|
4
|
||||||
|
加拿大和拉丁美洲
|
3 433
|
3 414
|
1
|
3 350
|
2
|
||||||
|
總計
|
47 445
|
44 751
|
6
|
42 338
|
6
|
||||||
|
其中在成熟市場
|
35 684
|
33 491
|
7
|
31 557
|
6
|
||||||
|
其中新興增長市場
|
11 761
|
11 260
|
4
|
10 781
|
4
|
||||||
|
1 按第三方客户所在地劃分的經營淨銷售額。新興增長市場包括除美國、加拿大、西歐、日本、澳大利亞和新西蘭的成熟市場以外的所有市場。
|
|||||||||||
|
|
|||||||||||
|
2019 百萬美元 |
2018 百萬美元 |
變化
(2018到 2019) 美元% |
2017 百萬美元 |
變化
(2017到 2018) 美元% |
|||||||
|
腫瘤學
|
|
|
|
|
|
||||||
|
塔西尼亞
|
1 880
|
1 874
|
0
|
1 841
|
2
|
||||||
|
善得定
|
1 585
|
1 587
|
0
|
1 612
|
– 2
|
||||||
|
Afinator/Votubia
|
1 539
|
1 556
|
– 1
|
1 525
|
2
|
||||||
|
Promacta/Revolade
|
1 416
|
1 174
|
21
|
867
|
35
|
||||||
|
塔芬拉爾 + 麥金主義者
|
1 338
|
1 155
|
16
|
873
|
32
|
||||||
|
Gleevec/Glivec
|
1 263
|
1 561
|
– 19
|
1 943
|
– 20
|
||||||
|
雅卡維
|
1 114
|
977
|
14
|
777
|
26
|
||||||
|
Exjade/Jadeu
|
975
|
1 099
|
– 11
|
1 059
|
4
|
||||||
|
Votrient
|
755
|
828
|
– 9
|
808
|
2
|
||||||
|
基斯卡利
|
480
|
235
|
104
|
76
|
NM
|
||||||
|
盧塔瑟羅島
|
441
|
167
|
164
|
0
|
NM
|
||||||
|
金利亞
|
278
|
76
|
NM
|
6
|
NM
|
||||||
|
皮克雷
|
116
|
|
NM
|
|
NM
|
||||||
|
其他
|
1 190
|
1 139
|
4
|
887
|
28
|
||||||
|
諾華腫瘤學業務部門總數
|
14 370
|
13 428
|
7
|
12 274
|
9
|
||||||
|
|
|
|
|
|
|||||||
|
眼科
|
|
|
|
|
|
||||||
|
盧森提斯
|
2 086
|
2 046
|
2
|
1 888
|
8
|
||||||
|
曲伏前列素組
|
433
|
517
|
– 16
|
589
|
– 12
|
||||||
|
西得拉
|
192
|
|
NM
|
|
NM
|
||||||
|
Beovu
|
35
|
|
NM
|
|
NM
|
||||||
|
其他
|
2 030
|
1 995
|
2
|
2 144
|
– 7
|
||||||
|
全眼科
|
4 776
|
4 558
|
5
|
4 621
|
– 1
|
||||||
|
|
|
|
|
|
|||||||
|
免疫學、肝病學和皮膚病學
|
|
|
|
|
|
||||||
|
科森提克斯
|
3 551
|
2 837
|
25
|
2 071
|
37
|
||||||
|
伊拉里斯
|
671
|
554
|
21
|
402
|
38
|
||||||
|
其他
|
|
1
|
NM
|
1
|
0
|
||||||
|
全免疫學、肝病學和皮膚科
|
4 222
|
3 392
|
24
|
2 474
|
37
|
||||||
|
|
|
|
|
|
|||||||
|
神經科學
|
|
|
|
|
|
||||||
|
吉倫亞
|
3 223
|
3 341
|
– 4
|
3 185
|
5
|
||||||
|
佐爾根斯馬
|
361
|
|
NM
|
|
NM
|
||||||
|
艾莫維格
|
103
|
8
|
NM
|
|
NM
|
||||||
|
梅曾特
|
26
|
|
NM
|
|
NM
|
||||||
|
其他
|
60
|
80
|
– 25
|
102
|
– 22
|
||||||
|
全神經科學
|
3 773
|
3 429
|
10
|
3 287
|
4
|
||||||
|
2019 百萬美元 |
2018 百萬美元 |
變化
(2018到 2019) 美元% |
2017 百萬美元 |
變化
(2017到 2018) 美元% |
|||||||
|
|
|
|
|
|
|||||||
|
呼吸性
|
|
|
|
|
|
||||||
|
Xolair 1
|
1 173
|
1 039
|
13
|
920
|
13
|
||||||
|
Ultibro Breezhaler
|
427
|
454
|
– 6
|
411
|
10
|
||||||
|
Seebri Breezhaler
|
121
|
148
|
– 18
|
151
|
– 2
|
||||||
|
Onbrez Breezhaler
|
82
|
101
|
– 19
|
112
|
– 10
|
||||||
|
其他
|
22
|
25
|
– 12
|
23
|
9
|
||||||
|
全呼吸
|
1 825
|
1 767
|
3
|
1 617
|
9
|
||||||
|
|
|
|
|
|
|||||||
|
心血管、腎臟和代謝
|
|
|
|
|
|
||||||
|
Entresto
|
1 726
|
1 028
|
68
|
507
|
103
|
||||||
|
其他
|
24
|
22
|
9
|
17
|
29
|
||||||
|
總心血管、腎臟和代謝
|
1 750
|
1 050
|
67
|
524
|
100
|
||||||
|
|
|
|
|
|
|||||||
|
已建立的藥物
|
|
|
|
|
|
||||||
|
加爾沃斯集團化
|
1 297
|
1 284
|
1
|
1 233
|
4
|
||||||
|
Diovan集團化
|
1 064
|
1 023
|
4
|
957
|
7
|
||||||
|
Exforge集團化
|
1 025
|
1 002
|
2
|
960
|
4
|
||||||
|
佐瑞斯/認證
|
485
|
464
|
5
|
414
|
12
|
||||||
|
Neoral/Sandimmun(e)
|
419
|
463
|
– 10
|
488
|
– 5
|
||||||
|
Voltaren/Cataflam
|
417
|
445
|
– 6
|
465
|
– 4
|
||||||
|
其他
|
2 291
|
2 587
|
– 11
|
2 964
|
– 13
|
||||||
|
已建立的藥品總數
|
6 998
|
7 268
|
– 4
|
7 481
|
– 3
|
||||||
|
|
|
|
|
|
|||||||
|
諾華製藥業務部門合計
|
23 344
|
21 464
|
9
|
20 004
|
7
|
||||||
|
|
|
|
|
|
|||||||
|
總事業部淨銷售額
|
37 714
|
34 892
|
8
|
32 278
|
8
|
||||||
|
1 淨銷售額反映Xolair所有適應症的銷售額。
|
|||||||||||
|
|
|||||||||||
|
NM=沒有意義
|
|||||||||||
|
品牌 |
商業特許經營權 |
指示 |
我們 百萬美元 |
其餘
世界 百萬美元 |
總計 百萬美元 |
||||||
|
科森提克斯
|
免疫學、肝病學和皮膚病學
|
銀屑病、強直性脊柱炎和銀屑病關節炎
|
2 220
|
1 331
|
3 551
|
||||||
|
吉倫亞
|
神經科學
|
複發性多發性硬化症
|
1 736
|
1 487
|
3 223
|
||||||
|
盧森提斯
|
眼科
|
老年性黃斑變性
|
|
2 086
|
2 086
|
||||||
|
塔西尼亞
|
腫瘤學
|
慢性髓系白血病
|
804
|
1 076
|
1 880
|
||||||
|
Entresto
|
心血管,腎臟 和代謝
|
慢性心力衰竭
|
925
|
801
|
1 726
|
||||||
|
善得定
|
腫瘤學
|
類癌和肢端肥大症
|
881
|
704
|
1 585
|
||||||
|
Afinator/Votubia
|
腫瘤學
|
乳腺癌/TSC
|
1 003
|
536
|
1 539
|
||||||
|
Promacta/Revolade
|
腫瘤學
|
免疫性血小板減少(ITP)、重型再生障礙性貧血(SAA)
|
691
|
725
|
1 416
|
||||||
|
塔芬拉爾 + 麥金主義者
|
腫瘤學
|
BRAF V600+轉移性和 晚期輔助性黑色素瘤 非小細胞肺癌
|
481
|
857
|
1 338
|
||||||
|
加爾沃斯集團化
|
已建立的藥物
|
糖尿病
|
|
1 297
|
1 297
|
||||||
|
Gleevec/Glivec
|
腫瘤學
|
慢性粒細胞白血病與胃腸道間質瘤
|
334
|
929
|
1 263
|
||||||
|
Xolair 1
|
呼吸性
|
重度過敏性哮喘(SAA) 慢性自發性蕁麻疹 (CSU)
|
|
1 173
|
1 173
|
||||||
|
雅卡維
|
腫瘤學
|
骨髓纖維化(MF), 單純性紅細胞增多症
|
|
1 114
|
1 114
|
||||||
|
Diovan集團化
|
已建立的藥物
|
高血壓
|
86
|
978
|
1 064
|
||||||
|
Exforge集團化
|
已建立的藥物
|
高血壓
|
13
|
1 012
|
1 025
|
||||||
|
Exjade/Jadeu
|
腫瘤學
|
慢性鐵超負荷
|
450
|
525
|
975
|
||||||
|
Votrient
|
腫瘤學
|
腎細胞癌
|
332
|
423
|
755
|
||||||
|
伊拉里斯
|
免疫學、肝病學和皮膚病學
|
自身炎症(CAPS, 陷阱,HIDS/MKD,FMF,SJIA, AOSD和痛風)
|
304
|
367
|
671
|
||||||
|
佐瑞斯/認證
|
已建立的藥物
|
移植
|
169
|
316
|
485
|
||||||
|
基斯卡利
|
腫瘤學
|
HR +/HER2—轉移性乳腺癌
|
250
|
230
|
480
|
||||||
|
前20名產品合計
|
|
|
10 679
|
17 967
|
28 646
|
||||||
|
投資組合的其餘部分
|
|
|
3 110
|
5 958
|
9 068
|
||||||
|
部門銷售總額
|
|
|
13 789
|
23 925
|
37 714
|
||||||
|
1 淨銷售額反映Xolair所有適應症的銷售額。
|
|||||||||||
|
品牌 |
商業特許經營權 |
指示 |
我們 百萬美元 |
其餘
世界 百萬美元 |
總計 百萬美元 |
||||||
|
吉倫亞
|
神經科學
|
複發性多發性硬化症
|
1 765
|
1 576
|
3 341
|
||||||
|
科森提克斯
|
免疫學、肝病學和皮膚病學
|
銀屑病、強直性脊柱炎和銀屑病關節炎
|
1 674
|
1 163
|
2 837
|
||||||
|
盧森提斯
|
眼科
|
老年性黃斑變性
|
|
2 046
|
2 046
|
||||||
|
塔西尼亞
|
腫瘤學
|
慢性髓系白血病
|
806
|
1 068
|
1 874
|
||||||
|
善得定
|
腫瘤學
|
類癌和肢端肥大症
|
817
|
770
|
1 587
|
||||||
|
Gleevec/Glivec
|
腫瘤學
|
慢性粒細胞白血病與胃腸道間質瘤
|
440
|
1 121
|
1 561
|
||||||
|
Afinator/Votubia
|
腫瘤學
|
乳腺癌/TSC
|
929
|
627
|
1 556
|
||||||
|
加爾沃斯集團化
|
已建立的藥物
|
糖尿病
|
|
1 284
|
1 284
|
||||||
|
Promacta/Revolade
|
腫瘤學
|
免疫性血小板減少(ITP)、重型再生障礙性貧血(SAA)
|
581
|
593
|
1 174
|
||||||
|
塔芬拉爾 + 麥金主義者
|
腫瘤學
|
BRAF V600+轉移性和 晚期輔助性黑色素瘤 非小細胞肺癌
|
457
|
698
|
1 155
|
||||||
|
Exjade/Jadeu
|
腫瘤學
|
慢性鐵超負荷
|
521
|
578
|
1 099
|
||||||
|
Xolair 1
|
呼吸性
|
重度過敏性哮喘(SAA) 慢性自發性蕁麻疹 (CSU)
|
|
1 039
|
1 039
|
||||||
|
Entresto
|
心血管,腎臟 和代謝
|
慢性心力衰竭
|
556
|
472
|
1 028
|
||||||
|
Diovan集團化
|
已建立的藥物
|
高血壓
|
84
|
939
|
1 023
|
||||||
|
Exforge集團化
|
已建立的藥物
|
高血壓
|
19
|
983
|
1 002
|
||||||
|
雅卡維
|
腫瘤學
|
骨髓纖維化(MF), 單純性紅細胞增多症
|
|
977
|
977
|
||||||
|
Votrient
|
腫瘤學
|
腎細胞癌
|
404
|
424
|
828
|
||||||
|
伊拉里斯
|
免疫學、肝病學和皮膚病學
|
自身炎症(CAPS, 陷阱,HIDS/MKD,FMF,SJIA, AOSD和痛風)
|
262
|
292
|
554
|
||||||
|
曲伏前列素組
|
眼科
|
眼內抬高復位術 壓力
|
194
|
323
|
517
|
||||||
|
佐瑞斯/認證
|
已建立的藥物
|
移植
|
145
|
319
|
464
|
||||||
|
前20名產品合計
|
|
|
9 654
|
17 292
|
26 946
|
||||||
|
投資組合的其餘部分
|
|
|
2 210
|
5 736
|
7 946
|
||||||
|
部門銷售總額
|
|
|
11 864
|
23 028
|
34 892
|
||||||
|
1 淨銷售額反映Xolair所有適應症的銷售額。
|
|||||||||||
|
|
|||||||||||
|
品牌 |
商業特許經營權 |
指示 |
我們 百萬美元 |
其餘
世界 百萬美元 |
總計 百萬美元 |
||||||
|
吉倫亞
|
神經科學
|
複發性多發性硬化症
|
1 709
|
1 476
|
3 185
|
||||||
|
科森提克斯
|
免疫學、肝病學和皮膚病學
|
銀屑病、強直性脊柱炎和銀屑病關節炎
|
1 275
|
796
|
2 071
|
||||||
|
Gleevec/Glivec
|
腫瘤學
|
慢性粒細胞白血病與胃腸道間質瘤
|
627
|
1 316
|
1 943
|
||||||
|
盧森提斯
|
眼科
|
老年性黃斑變性
|
|
1 888
|
1 888
|
||||||
|
塔西尼亞
|
腫瘤學
|
慢性髓系白血病
|
810
|
1 031
|
1 841
|
||||||
|
善得定
|
腫瘤學
|
類癌和肢端肥大症
|
832
|
780
|
1 612
|
||||||
|
Afinator/Votubia
|
腫瘤學
|
乳腺癌/TSC
|
819
|
706
|
1 525
|
||||||
|
加爾沃斯集團化
|
已建立的藥物
|
糖尿病
|
|
1 233
|
1 233
|
||||||
|
Exjade/Jadeu
|
腫瘤學
|
慢性鐵超負荷
|
515
|
544
|
1 059
|
||||||
|
Exforge集團化
|
已建立的藥物
|
高血壓
|
28
|
932
|
960
|
||||||
|
Diovan集團化
|
已建立的藥物
|
高血壓
|
87
|
870
|
957
|
||||||
|
Xolair 1
|
呼吸性
|
重度過敏性哮喘(SAA) 慢性自發性蕁麻疹 (CSU)
|
|
920
|
920
|
||||||
|
塔芬拉爾 + 麥金主義者
|
腫瘤學
|
BRAF V600+轉移性和 晚期輔助性黑色素瘤 非小細胞肺癌
|
339
|
534
|
873
|
||||||
|
Promacta/Revolade
|
腫瘤學
|
免疫性血小板減少(ITP)、重型再生障礙性貧血(SAA)
|
446
|
421
|
867
|
||||||
|
Votrient
|
腫瘤學
|
腎細胞癌
|
407
|
401
|
808
|
||||||
|
雅卡維
|
腫瘤學
|
骨髓纖維化(MF), 單純性紅細胞增多症
|
|
777
|
777
|
||||||
|
曲伏前列素組
|
眼科
|
降低升高的 眼壓
|
216
|
373
|
589
|
||||||
|
Entresto
|
心血管,腎臟 和代謝
|
慢性心力衰竭
|
297
|
210
|
507
|
||||||
|
Neoral/Sandimmun(e)
|
免疫學、肝病學和皮膚病學
|
移植
|
38
|
450
|
488
|
||||||
|
Voltaren/Cataflam
|
已建立的藥物
|
炎症/疼痛
|
|
465
|
465
|
||||||
|
前20名產品合計
|
|
|
8 445
|
16 123
|
24 568
|
||||||
|
投資組合的其餘部分
|
|
|
2 412
|
5 298
|
7 710
|
||||||
|
部門銷售總額
|
|
|
10 857
|
21 421
|
32 278
|
||||||
|
1 淨銷售額反映Xolair所有適應症的銷售額。
|
|||||||||||
|
|
|||||||||||
|
2019 百萬美元 |
2018 百萬美元 |
變化
(2018到 2019) 美元% |
2017 百萬美元 |
變化
(2017到 2018) 美元% |
|||||||
|
零售業泛型 1
|
7 590
|
7 880
|
– 4
|
8 409
|
– 6
|
||||||
|
生物製藥
|
1 607
|
1 436
|
12
|
1 135
|
27
|
||||||
|
抗感染
|
534
|
543
|
– 2
|
516
|
5
|
||||||
|
部門銷售淨額共計
|
9 731
|
9 859
|
– 1
|
10 060
|
– 2
|
||||||
|
1 其中7.84億美元(2018年:8.26億美元;2017年:8.8億美元)代表以Sandoz名義銷售的抗感染藥物
|
|||||||||||
|
創新藥物
|
桑多茲
|
公司(包括淘汰)
|
集團化
|
||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
|||||||||
|
利潤分享收入
|
732
|
874
|
2
|
3
|
|
|
734
|
877
|
|||||||||
|
特許使用費收入
|
104
|
162
|
19
|
10
|
24
|
16
|
147
|
188
|
|||||||||
|
里程碑式收入
|
201
|
128
|
30
|
45
|
|
|
231
|
173
|
|||||||||
|
其他 1
|
55
|
24
|
12
|
4
|
|
|
67
|
28
|
|||||||||
|
其他收入合計
|
1 092
|
1 188
|
63
|
62
|
24
|
16
|
1 179
|
1 266
|
|||||||||
|
1 其他包括製造或提供其他服務等活動的收入,但此類收入不計入淨銷售額。
|
|||||||||||||||||
|
創新藥物
|
桑多茲
|
公司(包括淘汰)
|
集團化
|
||||||||||||||
|
(百萬美元)
|
2018
|
2017
|
2018
|
2017
|
2018
|
2017
|
2018
|
2017
|
|||||||||
|
利潤分享收入
|
874
|
648
|
3
|
4
|
|
|
877
|
652
|
|||||||||
|
特許使用費收入
|
162
|
186
|
10
|
24
|
16
|
88
|
188
|
298
|
|||||||||
|
里程碑式收入
|
128
|
28
|
45
|
|
|
|
173
|
28
|
|||||||||
|
其他 1
|
24
|
36
|
4
|
9
|
|
|
28
|
45
|
|||||||||
|
其他收入合計
|
1 188
|
898
|
62
|
37
|
16
|
88
|
1 266
|
1 023
|
|||||||||
|
1 其他包括製造或提供其他服務等活動的收入,但此類收入不計入淨銷售額。
|
|||||||||||||||||
|
淨利潤表效應
|
其他綜合收益效應 1
|
總綜合收益效應
|
|||||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
2019
|
2018
|
2017
|
2019
|
2018
|
2017
|
||||||||||
|
瑞士羅氏控股公司
|
662
|
526
|
456
|
– 94
|
75
|
108
|
568
|
601
|
564
|
||||||||||
|
葛蘭素史克消費者醫療保健控股有限公司,英國
|
|
5 910
|
629
|
|
– 557
|
– 145
|
|
5 353
|
484
|
||||||||||
|
其他
|
– 3
|
2
|
23
|
|
|
|
– 3
|
2
|
23
|
||||||||||
|
與持續經營有關的聯營公司
|
659
|
6 438
|
1 108
|
– 94
|
– 482
|
– 37
|
565
|
5 956
|
1 071
|
||||||||||
|
1 2018年,由於剝離對GSK Consumer Healthcare Holdings Ltd.的投資,諾華在關聯公司確認的其他全面收益中的税後淨額5.11億美元被循環到綜合收益表中。2019年和2017年,沒有諾華份額的關聯公司確認的其他全面收益中的税後淨額被循環到綜合收益表中。
|
|||||||||||||||||||
|
資產負債表價值
|
|||||
|
(百萬美元) |
十二月三十一日,
2019 |
十二月三十一日,
2018 |
|||
|
瑞士羅氏控股公司
|
8 445
|
8 195
|
|||
|
其他
|
199
|
157
|
|||
|
總計
|
8 644
|
8 352
|
|||
|
(數十億瑞士法郎) |
流動資產 |
非當前
資產 |
當前
負債 |
非當前
負債 |
|||||
|
2018年12月31日
|
32.2
|
53.7
|
23.0
|
25.1
|
|||||
|
2019年6月30日
|
32.3
|
53.8
|
23.4
|
25.7
|
|||||
|
(數十億瑞士法郎) |
收入 |
淨收入 |
其他
明白-- 高收入 |
總計
明白-- 高收入 |
|||||
|
2018年12月31日
|
59.5
|
8.6
|
– 0.1
|
8.5
|
|||||
|
2019年6月30日
|
31.8
|
8.3
|
– 0.6
|
7.7
|
|||||
|
(百萬美元) |
十二月三十一日,
2019 |
||
|
諾華在羅氏估計淨資產中的份額
|
2 404
|
||
|
諾華在重新評估的無形資產中所佔份額
|
297
|
||
|
隱性諾華商譽
|
2 939
|
||
|
在可識別淨資產和商譽中份額的現值
|
5 640
|
||
|
累計權益會計調整及換算影響減已收股息
|
2 805
|
||
|
資產負債表價值
|
8 445
|
||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
諾華在羅氏本年度估計合併淨利潤中的份額
|
910
|
799
|
669
|
||||
|
上年度調整
|
– 129
|
– 125
|
– 67
|
||||
|
與無形資產有關的公允價值調整攤銷,税後淨額為2400萬美元(2018年:4000萬美元;2017年:4200萬美元)
|
– 162
|
– 148
|
– 146
|
||||
|
部分解除已確認的遞延税項負債
|
43
|
|
|
||||
|
淨收益效應
|
662
|
526
|
456
|
||||
|
(百萬美元)
|
2018
|
2017
|
|||
|
諾華佔GSK消費者醫療集團預計本年度合併淨利潤的份額
|
119
|
589
|
|||
|
上年度調整
|
4
|
47
|
|||
|
攤銷無形資產及存貨之公允價值調整,扣除税項100萬美元(二零一七年:100萬美元)
|
– 3
|
– 7
|
|||
|
剝離GSK Consumer Healthcare的税前收益
|
5 790
|
|
|||
|
淨收益效應
|
5 910
|
629
|
|||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
利息支出
|
– 714
|
– 877
|
– 741
|
||||
|
租賃負債利息支出
|
– 66
|
|
|
||||
|
貼現長期負債和資本化借款成本產生的費用
|
– 70
|
– 55
|
– 9
|
||||
|
持續經營的利息支出總額
|
– 850
|
– 932
|
– 750
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
利息收入
|
245
|
292
|
110
|
||||
|
其他財務收入
|
12
|
1
|
1
|
||||
|
財務費用
|
– 52
|
– 39
|
– 11
|
||||
|
貨幣結果,淨額
|
– 160
|
– 68
|
– 58
|
||||
|
持續經營的其他財務收入和支出總額
|
45
|
186
|
42
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
瑞士
|
8 097
|
11 887
|
5 385
|
||||
|
外國
|
843
|
2 208
|
3 717
|
||||
|
來自持續經營業務的税前收入
|
8 940
|
14 095
|
9 102
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
瑞士
|
– 1 186
|
– 615
|
– 462
|
||||
|
外國
|
– 961
|
– 988
|
– 1 451
|
||||
|
當期所得税支出
|
– 2 147
|
– 1 603
|
– 1 913
|
||||
|
瑞士
|
– 93
|
– 120
|
– 305
|
||||
|
外國
|
447
|
428
|
615
|
||||
|
遞延税項收入
|
354
|
308
|
310
|
||||
|
來自持續經營業務的所得税費用
|
– 1 793
|
– 1 295
|
– 1 603
|
||||
|
(As(百分比)
|
2019
|
2018
|
2017
|
||||
|
適用税率
|
11.7
|
14.3
|
14.3
|
||||
|
不準許開支的影響
|
4.8
|
1.7
|
3.1
|
||||
|
利用前期結轉的税務虧損的影響
|
– 0.1
|
– 0.1
|
– 0.1
|
||||
|
減税後入息課税的影響
|
– 0.7
|
– 0.4
|
– 0.2
|
||||
|
無須繳税的入息的影響 1
|
0.0
|
– 3.7
|
0.0
|
||||
|
税收抵免和免税額的影響
|
– 2.3
|
– 2.3
|
– 2.1
|
||||
|
解除或有對價負債的效果
|
– 0.5
|
– 0.2
|
– 1.3
|
||||
|
税率變動對流動和遞延税項資產負債的影響 2
|
– 1.4
|
– 0.1
|
4.8
|
||||
|
遞延税項資產核銷的影響 3
|
4.0
|
0.2
|
0.0
|
||||
|
附屬公司投資減記及回減記的影響
|
– 0.6
|
0.0
|
– 1.1
|
||||
|
2017年到期的税收優惠
|
0.0
|
0.0
|
– 0.9
|
||||
|
上一年度項目的影響
|
2.2
|
– 0.5
|
1.2
|
||||
|
其他項目的效果 4
|
3.0
|
0.3
|
– 0.1
|
||||
|
持續經營的有效税率
|
20.1
|
9.2
|
17.6
|
||||
|
|
|||||||
|
1 於2018年計入本集團出售於瑞士的GSK Consumer Healthcare Holdings Ltd.投資所產生的免税收入(-3.7%)的影響。
|
|||||||
|
2 2019年主要與瑞士於2019年實施的税務改革導致的遞延税項資產及負債重估有關,額外披露請參閲附註12。
於二零一七年包括與遞延税項資產及負債及部分即期應付税項重估有關的4. 8%影響。該重估乃由於於二零一七年十二月二十二日頒佈之美國税務改革法例所致,有關額外披露,請參閲附註12。 |
|||||||
|
3 2019年主要與因法人重組產生的遞延税項資產核銷的非現金一次性遞延税項開支有關。
|
|||||||
|
4 2019年其他項目(+3.0%)包括不確定税位變動(+2.6%)和其他項目(+0.4%)。
|
|||||||
|
2019
|
2018
|
2017
|
|||||
|
諾華製藥股東應佔淨收益(百萬美元)
|
|
|
|
||||
|
-持續運營
|
7 142
|
12 797
|
7 499
|
||||
|
-停產業務
|
4 590
|
– 186
|
204
|
||||
|
總計
|
11 732
|
12 611
|
7 703
|
||||
|
|
|
|
|||||
|
股份數量(單位:百萬)
|
|
|
|
||||
|
用於基本每股收益的加權平均流通股數量
|
2 291
|
2 319
|
2 346
|
||||
|
從期權中歸屬限制性股份、限制性股份單位和攤薄股份的調整
|
28
|
25
|
25
|
||||
|
稀釋後每股收益中的加權平均股數
|
2 319
|
2 344
|
2 371
|
||||
|
|
|
|
|||||
|
基本每股收益(美元)
|
|
|
|
||||
|
-持續運營
|
3.12
|
5.52
|
3.20
|
||||
|
-停產業務
|
2.00
|
– 0.08
|
0.08
|
||||
|
總計
|
5.12
|
5.44
|
3.28
|
||||
|
|
|
|
|||||
|
稀釋後每股收益(美元)
|
|
|
|
||||
|
-持續運營
|
3.08
|
5.46
|
3.17
|
||||
|
-停產業務
|
1.98
|
– 0.08
|
0.08
|
||||
|
總計
|
5.06
|
5.38
|
3.25
|
||||
|
(百萬美元) |
公允價值
調整 論適銷對路 證券 |
公允價值
調整 關於債務 證券 |
公允價值
調整 遞延現金 流動套期保值 |
公允價值
調整 股本 證券 |
精算
得/(失) 從已定義的 福利計劃 |
累計
貨幣 翻譯 效果 |
總價值 調整 |
||||||||
|
2017年1月1日的價值調整
|
349
|
– 1
|
– 3
|
|
– 5 915
|
– 1 642
|
– 7 212
|
||||||||
|
金融工具公允價值調整
|
39
|
– 1
|
12
|
|
|
|
50
|
||||||||
|
淨投資對衝
|
|
|
|
|
|
– 237
|
– 237
|
||||||||
|
福利確定型計劃精算淨損失
|
|
|
|
|
851
|
|
851
|
||||||||
|
貨幣換算效應
|
|
|
|
|
|
2 208
|
2 208
|
||||||||
|
2017年總價值調整數
|
39
|
– 1
|
12
|
|
851
|
1 971
|
2 872
|
||||||||
|
如先前報告所述,截至2017年12月31日的價值調整
|
388
|
– 2
|
9
|
|
– 5 064
|
329
|
– 4 340
|
||||||||
|
採用國際財務報告準則第9號對留存收益和保監局的影響 1
|
– 177
|
|
|
|
|
|
– 177
|
||||||||
|
重新分類為IFRS 9所要求的列報 1
|
– 211
|
|
|
211
|
|
|
|
||||||||
|
重述2018年1月1日的價值調整
|
|
– 2
|
9
|
211
|
– 5 064
|
329
|
– 4 517
|
||||||||
|
金融工具公允價值調整
|
|
|
12
|
13
|
|
|
25
|
||||||||
|
出售金融資產的公允價值調整
|
|
|
|
– 16
|
|
|
– 16
|
||||||||
|
淨投資對衝
|
|
|
|
|
|
95
|
95
|
||||||||
|
固定福利計劃的淨精算收益
|
|
|
|
|
– 359
|
|
– 359
|
||||||||
|
貨幣換算效應
|
|
|
|
|
|
320
|
320
|
||||||||
|
2018年總價值調整
|
|
|
12
|
– 3
|
– 359
|
415
|
65
|
||||||||
|
2018年12月31日的價值調整
|
|
– 2
|
21
|
208
|
– 5 423
|
744
|
– 4 452
|
||||||||
|
金融工具公允價值調整
|
|
1
|
1
|
– 47
|
|
|
– 45
|
||||||||
|
出售金融資產的公允價值調整
|
|
|
|
– 95
|
|
|
– 95
|
||||||||
|
淨投資對衝
|
|
|
|
|
|
44
|
44
|
||||||||
|
固定福利計劃的淨精算收益
|
|
|
|
|
– 466
|
|
– 466
|
||||||||
|
貨幣換算效應
|
|
|
|
|
|
354
|
354
|
||||||||
|
2019年總價值調整
|
|
1
|
1
|
– 142
|
– 466
|
398
|
– 208
|
||||||||
|
與剝離有關的公允價值調整
|
|
|
|
33
|
– 30
|
|
3
|
||||||||
|
2019年12月31日的價值調整
|
|
– 1
|
22
|
99
|
– 5 919
|
1 142
|
– 4 657
|
||||||||
|
1 附註1提供了與採用國際財務報告準則第9號金融工具的影響有關的額外披露。保監處:其他全面收入
|
|||||||||||||||
|
(百萬美元) |
公允價值
調整 論公平性 證券 1 |
公允價值
調整 關於債務 證券 |
公允價值
調整 遞延現金 流動套期保值 |
總計 |
|
||||||
|
2019年1月1日的公允價值調整
|
208
|
– 2
|
21
|
227
|
|||||||
|
公允價值變動:
|
|
|
|
|
|||||||
|
-出售的債務證券
|
|
1
|
|
1
|
|||||||
|
-股權證券
|
– 94
|
|
|
– 94
|
|||||||
|
轉入綜合損益表的現金流量對衝的攤銷淨虧損
|
|
|
1
|
1
|
|||||||
|
上述項目的遞延税金
|
47
|
|
|
47
|
|||||||
|
重新分類至保留盈利的已實現淨收益:
|
|
|
|
|
|||||||
|
—出售的其他金融資產
|
– 95
|
|
|
– 95
|
|||||||
|
年內公平值調整
|
– 142
|
1
|
1
|
– 140
|
|||||||
|
與剝離有關的公允價值調整
|
33
|
|
|
|
33
|
|
|||||
|
2019年12月31日的公允價值調整
|
99
|
– 1
|
22
|
120
|
|||||||
|
1 包括指定為金融資產的權益證券的公允價值調整,這些資產通過其他全面收益按公允價值估值,隨後不會再循環進入綜合損益表
|
|||||||||||
|
(百萬美元) |
公允價值
調整 從有價 證券 |
公允價值
調整 論公平性 證券 1 |
公允價值
調整 關於債務 證券 |
公允價值
調整 遞延現金 流動套期保值 |
總計 |
||||||
|
公允價值調整於2018年1月1日,如前所述
|
388
|
|
– 2
|
9
|
395
|
||||||
|
採用國際財務報告準則第9號對留存收益和其他全面收益的影響 2
|
– 177
|
|
|
|
– 177
|
||||||
|
重新分類為IFRS 9所要求的列報
|
– 211
|
211
|
|
|
|
||||||
|
於2018年1月1日重述公允價值調整
|
|
211
|
– 2
|
9
|
218
|
||||||
|
公允價值變動:
|
|
|
|
|
|
||||||
|
-股權證券
|
|
18
|
|
|
18
|
||||||
|
轉入綜合損益表的現金流量對衝的攤銷淨虧損
|
|
|
|
13
|
13
|
||||||
|
上述項目的遞延税金
|
|
– 5
|
|
– 1
|
– 6
|
||||||
|
重新分類至保留盈利的已實現淨收益:
|
|
|
|
|
|
||||||
|
—出售的其他金融資產
|
|
– 16
|
|
|
– 16
|
||||||
|
年內公平值調整
|
|
– 3
|
|
12
|
9
|
||||||
|
2018年12月31日的公允價值調整
|
|
208
|
– 2
|
21
|
227
|
||||||
|
1 包括指定為金融資產的權益證券的公允價值調整,這些資產通過其他全面收益按公允價值估值,隨後不會再循環進入綜合損益表
|
|||||||||||
|
2 附註1提供關於採用國際財務報告準則第9號金融工具的影響的補充披露。
|
|||||||||||
|
(百萬美元) |
公允價值
調整 論適銷對路 證券 |
公允價值
調整 關於債務 證券 |
公允價值
調整 遞延現金 流動套期保值 |
總計 |
|||||
|
2017年1月1日的公允價值調整
|
349
|
– 1
|
– 3
|
345
|
|||||
|
公允價值變動:
|
|
|
|
|
|||||
|
—可供出售的有價證券
|
12
|
– 1
|
|
11
|
|||||
|
—可供出售金融投資
|
47
|
|
|
47
|
|||||
|
已實現收益淨額轉撥至綜合收益表:
|
|
|
|
|
|||||
|
—出售的其他金融資產
|
– 109
|
|
|
– 109
|
|||||
|
轉入綜合損益表的現金流量對衝的攤銷淨虧損
|
|
|
13
|
13
|
|||||
|
轉撥至綜合收益表的減值金融資產
|
102
|
|
|
102
|
|||||
|
上述項目的遞延税金 1
|
– 13
|
|
– 1
|
– 14
|
|||||
|
年內公平值調整
|
39
|
– 1
|
12
|
50
|
|||||
|
2017年12月31日的公允價值調整
|
388
|
– 2
|
9
|
395
|
|||||
|
1 包括與美國持有的可供出售金融投資的遞延税項負債重估有關的1,800萬美元的影響,該影響先前通過與持續經營有關的其他全面收益確認。此次重估是由於美國於2017年12月22日頒佈的税務改革立法所致。有關額外披露,請參閲附註12。
|
|||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
税前固定福利養老金計劃
|
– 119
|
– 482
|
1 367
|
||||
|
其他税前離職後福利計劃
|
– 35
|
54
|
76
|
||||
|
上述項目的徵税 1
|
– 313
|
69
|
– 592
|
||||
|
税後共計
|
– 467
|
– 359
|
851
|
||||
|
歸因於:
|
|
|
|
||||
|
諾華製藥的股東
|
– 466
|
– 359
|
851
|
||||
|
非控制性權益
|
– 1
|
|
|
||||
|
|
|||||||
|
1 2019年包括與瑞士離職後福利遞延税項資產重估有關的—3.58億美元影響,該影響先前通過其他全面收益確認。這次重估是由於選民在2019年實施的瑞士税收改革。有關額外披露,請參閲附註12。
2017年包括與美國離職後福利遞延税項資產重估有關的影響—2.72億美元,該影響先前通過其他全面收益確認(持續經營業務—2.59億美元及已終止經營業務—1300萬美元)。此次重估是由於美國於2017年12月22日頒佈的税務改革立法所致。有關額外披露,請參閲附註12。 |
|||||||
|
(百萬美元) |
土地 |
建築物 |
施工 正在進行中 |
機械設備
及其他 裝備 |
總計 |
||||||
|
成本
|
|
|
|
|
|
||||||
|
2019年1月1日
|
696
|
14 135
|
2 042
|
17 155
|
34 028
|
||||||
|
與終止經營有關的資產成本 1
|
– 61
|
– 1 615
|
– 655
|
– 2 678
|
– 5 009
|
||||||
|
重新分類為使用權資產 2
|
– 122
|
– 3
|
|
– 2
|
– 127
|
||||||
|
與持作出售之出售組別有關之資產成本 3
|
|
– 3
|
– 12
|
– 8
|
– 23
|
||||||
|
企業合併的影響
|
10
|
24
|
1
|
9
|
44
|
||||||
|
重新分類 4
|
57
|
332
|
– 1 019
|
630
|
|
||||||
|
加法 5
|
6
|
112
|
1 001
|
355
|
1 474
|
||||||
|
處置和取消認可 6
|
– 75
|
– 1 551
|
– 9
|
– 1 774
|
– 3 409
|
||||||
|
貨幣換算效應
|
1
|
32
|
1
|
– 13
|
21
|
||||||
|
2019年12月31日
|
512
|
11 463
|
1 350
|
13 674
|
26 999
|
||||||
|
|
|
|
|
|
|||||||
|
累計折舊
|
|
|
|
|
|
||||||
|
2019年1月1日
|
– 43
|
– 6 328
|
– 37
|
– 11 924
|
– 18 332
|
||||||
|
與已終止業務有關的資產累計折舊 1
|
8
|
562
|
7
|
1 541
|
2 118
|
||||||
|
重新分類為使用權資產 2
|
26
|
|
|
|
26
|
||||||
|
與持作出售之出售組別相關之資產累計折舊 3
|
|
2
|
|
|
2
|
||||||
|
處置和解除確認的累計折舊 6
|
|
1 170
|
2
|
1 674
|
2 846
|
||||||
|
折舊費 7
|
|
– 447
|
|
– 898
|
– 1 345
|
||||||
|
減值費用 8
|
– 10
|
– 51
|
– 34
|
– 110
|
– 205
|
||||||
|
減值費用沖銷
|
|
1
|
2
|
|
3
|
||||||
|
貨幣換算效應
|
– 1
|
– 33
|
|
– 9
|
– 43
|
||||||
|
2019年12月31日
|
– 20
|
– 5 124
|
– 60
|
– 9 726
|
– 14 930
|
||||||
|
2019年12月31日的賬面淨值
|
492
|
6 339
|
1 290
|
3 948
|
12 069
|
||||||
|
購買房產、廠房和設備的承諾
|
|
|
|
|
220
|
||||||
|
資本化借款成本
|
|
|
|
|
4
|
||||||
|
1 指於二零一九年一月一日與報告為已終止經營業務的Alcon業務有關的資產成本及累計折舊。附註1、2和30提供了與已終止業務有關的資料。
|
|||||||||||
|
2 採納國際財務報告準則第16號租賃後,於二零一九年一月一日重新分類至使用權資產。有關額外披露,請參閲附註1及10。
|
|||||||||||
|
3 附註2提供有關持作出售之出售組別之額外披露。
|
|||||||||||
|
4 由於廠房和其他在建設備完工,各資產類別之間的重新分類
|
|||||||||||
|
5 2019年1月1日至2019年12月31日期間持作出售出售的出售組別的增加額為23百萬美元。
|
|||||||||||
|
6 終止確認不再使用且被視為不具有重大出售價值或其他替代用途的資產
|
|||||||||||
|
7 於二零一九年一月一日至二零一九年十二月三十一日期間,持作出售之出售組別並無錄得折舊開支。
|
|||||||||||
|
8 於二零一九年一月一日至二零一九年十二月三十一日期間,持作出售之出售組別之減值為200萬美元。
|
|||||||||||
|
(百萬美元) |
土地 |
建築物 |
施工 正在進行中 |
機械設備
及其他 裝備 |
總計 |
||||||
|
成本
|
|
|
|
|
|
||||||
|
2018年1月1日
|
720
|
14 064
|
2 368
|
16 858
|
34 010
|
||||||
|
與持作出售之出售組別有關之資產成本 1
|
– 11
|
– 114
|
– 24
|
– 160
|
– 309
|
||||||
|
企業合併的影響
|
2
|
40
|
15
|
80
|
137
|
||||||
|
重新分類 2
|
1
|
538
|
– 1 470
|
931
|
|
||||||
|
加法 3
|
7
|
110
|
1 250
|
407
|
1 774
|
||||||
|
處置和取消認可 4
|
– 7
|
– 212
|
– 21
|
– 457
|
– 697
|
||||||
|
貨幣換算效應
|
– 16
|
– 291
|
– 76
|
– 504
|
– 887
|
||||||
|
2018年12月31日
|
696
|
14 135
|
2 042
|
17 155
|
34 028
|
||||||
|
|
|
|
|
|
|||||||
|
累計折舊
|
|
|
|
|
|
||||||
|
2018年1月1日
|
– 40
|
– 5 983
|
– 38
|
– 11 485
|
– 17 546
|
||||||
|
與持作出售之出售組別相關之資產累計折舊 1
|
|
56
|
4
|
101
|
161
|
||||||
|
折舊費 5
|
– 3
|
– 574
|
|
– 1 140
|
– 1 717
|
||||||
|
處置和解除確認的累計折舊 4
|
|
180
|
3
|
412
|
595
|
||||||
|
減值費用
|
– 1
|
– 122
|
– 16
|
– 185
|
– 324
|
||||||
|
減值費用沖銷
|
|
|
8
|
12
|
20
|
||||||
|
貨幣換算效應
|
1
|
115
|
2
|
361
|
479
|
||||||
|
2018年12月31日
|
– 43
|
– 6 328
|
– 37
|
– 11 924
|
– 18 332
|
||||||
|
2018年12月31日的賬面淨值
|
653
|
7 807
|
2 005
|
5 231
|
15 696
|
||||||
|
融資租賃合同項下的不動產、廠場和設備賬面淨值
|
|
79
|
|
|
79
|
||||||
|
購買房產、廠房和設備的承諾
|
|
|
|
|
289
|
||||||
|
資本化借款成本
|
|
|
|
|
6
|
||||||
|
1 附註2提供有關持作出售之出售組別之額外披露。
|
|||||||||||
|
2 由於廠房和其他在建設備完工,各資產類別之間的重新分類
|
|||||||||||
|
3 持作出售的出售集團的新增金額為2100萬美元。
|
|||||||||||
|
4 終止確認不再使用且被視為不具有重大出售價值或其他替代用途的資產
|
|||||||||||
|
5 於二零一八年一月一日至重新分類至持作出售資產當日止期間,持作出售之出售組別之折舊支出為15百萬美元。有關已終止經營業務的折舊費用,請參閲附註30。
|
|||||||||||
|
(百萬美元)
|
|
||
|
經營租賃承諾2018年12月31日 1
|
3 612
|
||
|
經營租賃承諾2018年12月31日與已終止業務有關
|
– 222
|
||
|
經營租賃承諾2018年12月31日與持續經營有關
|
3 390
|
||
|
短期租賃的確認豁免
|
– 30
|
||
|
低價值租賃的確認例外
|
– 12
|
||
|
開始日期為2018年12月31日之後的租賃安排
|
– 65
|
||
|
截至2019年1月1日的未貼現未來租賃付款持續經營
|
3 283
|
||
|
貼現的效果
|
– 1 547
|
||
|
截至2019年1月1日確認的租賃負債 2
|
1 736
|
||
|
|
|||
|
1 如2018年年報附註27所述
|
|||
|
2 於二零一九年一月一日(即國際財務報告準則第16號租賃的實施日期)的加權平均增量借款利率為3. 5%。
|
|||
|
(百萬美元)
|
2019年1月1日
|
||
|
土地
|
536
|
||
|
建築物
|
848
|
||
|
車輛
|
147
|
||
|
機器設備及其他資產
|
23
|
||
|
使用權資產 1
|
1 554
|
||
|
|
|||
|
1 於國際財務報告準則第16號實施日期,使用權資產比租賃負債低1. 82億美元,原因是就確認分租應收款項、預付款項及應計租賃付款以及於二零一八年十二月三十一日記錄於物業、廠房及設備的租賃資產轉移作出調整。
|
|||
|
(百萬美元)
|
2019年1月1日
|
||
|
資產
|
|
||
|
非流動資產
|
|
||
|
財產、廠房和設備
|
– 101
|
||
|
使用權資產
|
1 554
|
||
|
其他非流動資產
|
74
|
||
|
非流動資產總額
|
1 527
|
||
|
總資產
|
1 527
|
||
|
|
|||
|
權益和負債
|
|
||
|
權益
|
|
||
|
儲量
|
3
|
||
|
總股本
|
3
|
||
|
|
|||
|
負債
|
|
||
|
非流動負債
|
|
||
|
金融債務
|
– 2
|
||
|
租賃負債
|
1 471
|
||
|
撥備和其他非流動負債
|
– 212
|
||
|
非流動負債總額
|
1 257
|
||
|
流動負債
|
|
||
|
金融債務和衍生金融工具
|
– 1
|
||
|
租賃負債
|
268
|
||
|
流動負債總額
|
267
|
||
|
總負債
|
1 524
|
||
|
權益和負債總額
|
1 527
|
||
|
(百萬美元)
|
|
||
|
2019年1月1日的使用權資產
|
1 554
|
||
|
加法
|
537
|
||
|
折舊費
|
– 305
|
||
|
租賃合同終止 1
|
– 98
|
||
|
跳水的影響
|
– 17
|
||
|
貨幣換算效應
|
6
|
||
|
於2019年12月31日的使用權資產總額
|
1 677
|
||
|
期內並無減值記錄。
|
|||
|
1 租賃合約終止亦包括導致使用權資產減少的現有租賃修訂及分租導致的減少。
|
|||
|
|
|||
|
(百萬美元) |
2019年12月31日 賬面價值 |
折舊
裝藥 2019 |
|||
|
土地
|
537
|
14
|
|||
|
建築物
|
990
|
194
|
|||
|
車輛
|
129
|
87
|
|||
|
機器設備及其他資產
|
21
|
10
|
|||
|
使用權資產總額
|
1 677
|
305
|
|||
|
|
|
||||
|
(百萬美元) |
租賃負債 2019 |
租賃負債
未打折 2019 |
||
|
不到一年
|
246
|
295
|
||
|
在一到兩年之間
|
202
|
246
|
||
|
兩到三年之間
|
163
|
202
|
||
|
在三到四年之間
|
138
|
173
|
||
|
在四到五年之間
|
119
|
150
|
||
|
五年後
|
1 081
|
2 419
|
||
|
租賃總負債
|
1 949
|
3 485
|
||
|
減去租賃負債的流動部分
|
– 246
|
– 295
|
||
|
租賃負債的非流動部分
|
1 703
|
3 190
|
||
|
(百萬美元)
|
2019
|
||
|
租賃負債利息支出 1
|
66
|
||
|
短期租賃費用
|
7
|
||
|
低價租賃費用
|
8
|
||
|
租賃現金流出總額
|
339
|
||
|
其中:
|
|
||
|
短期租賃和低價值租賃的現金流出 2
|
15
|
||
|
利息的支付 3
|
51
|
||
|
支付租賃負債 4
|
273
|
||
|
1 加權平均利率為3. 9%。
|
|||
|
2 短期及低價值租賃之現金流量計入經營活動現金流量淨額總額內。於二零一九年十二月三十一日,本集團承諾訂立的短期租賃組合與本集團於二零一九年訂立的短期租賃組合相似。
|
|||
|
3 包括在經營活動現金流量淨額總額內。
|
|||
|
4 報告為融資活動中使用的現金流出,扣除已收到的租賃獎勵3,300萬美元。
|
|||
|
商譽
|
商譽以外的無形資產
|
||||||||||||||||
|
(百萬美元) |
總計 |
正在進行中
研究和 發展 |
阿爾康 品牌名稱 |
技術 |
目前
銷售 產品 |
營銷 專有技術 |
其他
無形的 資產 |
總計 |
|||||||||
|
成本
|
|
|
|
|
|
|
|
|
|||||||||
|
2019年1月1日
|
35 700
|
16 167
|
2 980
|
6 253
|
35 412
|
5 960
|
2 253
|
69 025
|
|||||||||
|
與非連續性業務有關的資產成本 1
|
– 9 000
|
– 249
|
– 2 980
|
– 5 369
|
– 4 440
|
– 5 960
|
– 572
|
– 19 570
|
|||||||||
|
與出售集團有關的資產成本,淨額 2
|
|
– 1
|
|
|
4
|
|
|
3
|
|||||||||
|
企業合併的影響
|
186
|
342
|
|
|
3 550
|
|
22
|
3 914
|
|||||||||
|
重新分類 3
|
|
– 9 069
|
|
|
9 069
|
|
|
|
|||||||||
|
加法 4
|
|
265
|
|
|
243
|
|
259
|
767
|
|||||||||
|
處置和取消認可 5
|
|
– 75
|
|
|
– 544
|
|
– 436
|
– 1 055
|
|||||||||
|
貨幣換算效應
|
– 61
|
49
|
|
|
254
|
|
32
|
335
|
|||||||||
|
2019年12月31日
|
26 825
|
7 429
|
|
884
|
43 548
|
|
1 558
|
53 419
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
累計攤銷
|
|
|
|
|
|
|
|
|
|||||||||
|
2019年1月1日
|
– 406
|
– 1 120
|
|
– 4 758
|
– 21 218
|
– 1 906
|
– 1 304
|
– 30 306
|
|||||||||
|
與停產業務有關的資產累計攤銷/減值 1
|
101
|
3
|
|
4 184
|
|
2 592
|
1 906
|
128
|
8 813
|
||||||||
|
攤銷費用 6
|
|
|
|
– 42
|
|
– 2 657
|
|
– 137
|
– 2 836
|
||||||||
|
處置和解除確認的累計減值 5
|
|
70
|
|
|
494
|
|
419
|
983
|
|||||||||
|
減值費用 6
|
|
– 984
|
|
– 105
|
– 54
|
|
– 32
|
– 1 175
|
|||||||||
|
減值費用沖銷
|
|
37
|
|
|
|
|
|
37
|
|||||||||
|
貨幣換算效應
|
4
|
– 11
|
|
|
– 126
|
|
– 11
|
– 148
|
|||||||||
|
2019年12月31日
|
– 301
|
– 2 005
|
|
– 721
|
– 20 969
|
|
– 937
|
– 24 632
|
|||||||||
|
2019年12月31日的賬面淨值
|
26 524
|
5 424
|
|
163
|
22 579
|
|
621
|
28 787
|
|||||||||
|
1 指於2019年1月1日的資產成本和累計攤銷,與報告為已終止經營的Alcon業務有關。附註1、2和30提供了與已終止業務有關的資料。
|
|||||||||||||||||
|
2 附註2提供有關持作出售之出售組別資產之額外披露。
|
|||||||||||||||||
|
3 由於收購的正在進行的研究和開發的產品發佈以及軟件開發的完成,不同資產類別之間的重新分類
|
|||||||||||||||||
|
4 2019年1月1日至2019年12月31日期間持有待售的處置組無新增
|
|||||||||||||||||
|
5 對不再使用或正在開發且被認為不具有重大處置價值或其他替代用途的資產的取消確認
|
|||||||||||||||||
|
6 無與出售集團於2019年1月1日至2019年12月31日期間持有待售期間相關的攤銷或減值費用。
|
|||||||||||||||||
|
商譽
|
商譽以外的無形資產
|
||||||||||||||||
|
(百萬美元) |
總計 |
正在進行中
研究和 發展 |
阿爾康 品牌名稱 |
技術 |
目前
銷售 產品 |
營銷 專有技術 |
其他
無形的 資產 |
總計 |
|||||||||
|
成本
|
|
|
|
|
|
|
|
|
|||||||||
|
2018年1月1日
|
32 179
|
6 462
|
2 980
|
6 638
|
34 105
|
5 960
|
1 852
|
57 997
|
|||||||||
|
與持作出售之出售組別有關之資產成本 1
|
|
– 9
|
|
– 276
|
– 1 116
|
|
– 2
|
– 1 403
|
|||||||||
|
企業合併的影響
|
4 084
|
10 224
|
|
|
2 531
|
|
1
|
12 756
|
|||||||||
|
重新分類 2
|
|
– 697
|
|
|
479
|
|
218
|
|
|||||||||
|
加法 3
|
|
477
|
|
2
|
728
|
|
385
|
1 592
|
|||||||||
|
處置和取消認可 4
|
|
– 214
|
|
– 70
|
– 928
|
|
– 183
|
– 1 395
|
|||||||||
|
減值費用 5
|
– 183
|
|
|
|
|
|
|
|
|||||||||
|
貨幣換算效應
|
– 380
|
– 76
|
|
– 41
|
– 387
|
|
– 18
|
– 522
|
|||||||||
|
2018年12月31日
|
35 700
|
16 167
|
2 980
|
6 253
|
35 412
|
5 960
|
2 253
|
69 025
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
累計攤銷
|
|
|
|
|
|
|
|
|
|||||||||
|
2018年1月1日
|
– 429
|
– 1 170
|
|
– 4 268
|
– 19 631
|
– 1 668
|
– 1 263
|
– 28 000
|
|||||||||
|
出售集團持有待售資產的累計攤銷/減值 1
|
|
2
|
|
107
|
816
|
|
|
925
|
|||||||||
|
攤銷費用 6
|
|
|
|
– 570
|
– 2 521
|
– 238
|
– 310
|
– 3 639
|
|||||||||
|
處置和解除確認的累計減值4
|
|
209
|
|
|
791
|
|
257
|
1 257
|
|||||||||
|
減值費用 5
|
|
– 167
|
|
– 53
|
– 825
|
|
– 4
|
– 1 049
|
|||||||||
|
貨幣換算效應
|
23
|
6
|
|
26
|
152
|
|
16
|
200
|
|||||||||
|
2018年12月31日
|
– 406
|
– 1 120
|
|
– 4 758
|
– 21 218
|
– 1 906
|
– 1 304
|
– 30 306
|
|||||||||
|
2018年12月31日的賬面淨值
|
35 294
|
15 047
|
2 980
|
1 495
|
14 194
|
4 054
|
949
|
38 719
|
|||||||||
|
1 附註2提供有關持作出售之出售組別資產之額外披露。
|
|||||||||||||||||
|
2 由於收購的正在進行的研究和開發的產品發佈以及軟件開發的完成,不同資產類別之間的重新分類
|
|||||||||||||||||
|
3 自2018年1月1日起至重新分類為持有待售資產之日止的待出售處置集團內無新增
|
|||||||||||||||||
|
4 對不再使用或正在開發且被認為不具有重大處置價值或其他替代用途的資產的取消確認
|
|||||||||||||||||
|
5 與出售集團因減記已分配商譽而持有的減值費用相關的減值費用為1.83億美元,當前銷售的產品的減值費用為3700萬美元(其中900萬美元從2018年1月1日至重新分類為待出售資產之日確認)。有關與停產業務有關的攤銷,請參閲附註30。
|
|||||||||||||||||
|
6 自2018年1月1日至重新分類為持有待售資產之日為止,與出售集團持有待售資產相關之攤銷為4,500萬美元。
|
|||||||||||||||||
|
商譽
|
商譽以外的無形資產
|
||||||||||||
|
(百萬美元) |
總計 |
正在進行中
研究和 發展 |
技術 |
目前
銷售 產品 |
其他
無形的 資產 |
總計 |
|||||||
|
創新藥物
|
18 750
|
5 339
|
7
|
21 720
|
520
|
27 586
|
|||||||
|
桑多茲
|
7 767
|
85
|
156
|
859
|
25
|
1 125
|
|||||||
|
公司
|
7
|
|
|
|
76
|
76
|
|||||||
|
2019年12月31日的賬面淨值
|
26 524
|
5 424
|
163
|
22 579
|
621
|
28 787
|
|||||||
|
商譽
|
商譽以外的無形資產
|
||||||||||||||||
|
(百萬美元) |
總計 |
正在進行中
研究和 發展 |
阿爾康 品牌名稱 |
技術 |
目前
銷售 產品 |
營銷 專有技術 |
其他
無形的 資產 |
總計 |
|||||||||
|
創新藥物
|
18 551
|
14 377
|
|
6
|
11 228
|
|
431
|
26 042
|
|||||||||
|
桑多茲
|
7 837
|
419
|
|
304
|
1 115
|
|
37
|
1 875
|
|||||||||
|
阿爾康 1
|
8 899
|
246
|
2 980
|
1 185
|
1 851
|
4 054
|
363
|
10 679
|
|||||||||
|
公司
|
7
|
5
|
|
|
|
|
118
|
123
|
|||||||||
|
2018年12月31日的賬面淨值
|
35 294
|
15 047
|
2 980
|
1 495
|
14 194
|
4 054
|
949
|
38 719
|
|||||||||
|
1 據報告,自2019年2月28日起,阿爾孔司已停止運作(見附註1、2和30)。根據國際財務報告準則,2018年12月31日的綜合資產負債表包括愛爾康眼科護理設備業務的資產和負債,以及阿爾康業務應佔的某些公司資產和負債。附註30提供了關於停產業務的補充資料。
|
|||||||||||||||||
|
|
|||||||||||||||||
|
|
|||||||||||||||||
|
(As(百分比) |
創新
藥品 |
桑多茲 |
|||
|
終端增長率
|
1.5
|
2.0
|
|||
|
貼現率(税後)
|
6.5
|
6.5
|
|||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
創新藥物 1
|
– 669
|
– 592
|
– 591
|
||||
|
桑多茲 2
|
– 506
|
– 249
|
– 61
|
||||
|
總計
|
– 1 175
|
– 841
|
– 652
|
||||
|
1 2019年包括與通過2015年Spinifex Pharmaceuticals Inc.收購的知識產權& D減記有關的減值4.16億美元。收購和1.08億美元的減記,與停止特應性皮炎臨牀開發項目MOR106有關。
2018年包括與部分減記有關的4億美元減值Votrient目前銷售的產品。 2017年包括與Serelaxin知識產權& D減記相關的4.65億美元減值。 |
|||||||
|
2 2019年包括與停用通用Advair相關的知識產權& D相關的減值4.42億美元®發展計劃。
2018年包括與分配商譽(1.83億美元)減記相關的2.2億美元減值,以及與Sandoz美國皮膚科業務和仿製美國口服固體產品組合即將剝離有關的當前上市產品(3700萬美元)。見附註2。 |
|||||||
|
(百萬美元) |
財產, 植物和 裝備 |
無形的 資產 |
養老金和
其他好處 義務 聯營公司 |
盤存 |
税損 進位- 遠期 |
其他資產, 條文 和應計項目 |
總計 |
||||||||
|
截至2019年1月1日的遞延税項總資產
|
191
|
1 233
|
1 188
|
3 722
|
273
|
2 175
|
8 782
|
||||||||
|
截至2019年1月1日的遞延税項負債總額
|
– 622
|
– 5 384
|
– 273
|
– 474
|
|
– 805
|
– 7 558
|
||||||||
|
截至2019年1月1日的遞延税金淨餘額
|
– 431
|
– 4 151
|
915
|
3 248
|
273
|
1 370
|
1 224
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
2019年1月1日
|
– 431
|
– 4 151
|
915
|
3 248
|
273
|
1 370
|
1 224
|
||||||||
|
與停產業務有關的遞延税金淨餘額 1
|
82
|
1 403
|
– 123
|
– 248
|
– 39
|
– 217
|
858
|
||||||||
|
記入[記入]收入貸方
|
74
|
605
|
308
|
– 818
|
– 113
|
298
|
354
|
||||||||
|
記入股權
|
|
8
|
|
|
75
|
– 166
|
– 83
|
||||||||
|
記入其他全面收入
|
|
|
– 313
|
|
|
24
|
– 289
|
||||||||
|
企業合併的影響
|
3
|
– 45
|
|
|
21
|
– 26
|
– 47
|
||||||||
|
其他動作 2
|
– 10
|
39
|
|
– 23
|
31
|
– 12
|
25
|
||||||||
|
於2019年12月31日的遞延税項結餘淨額
|
– 282
|
– 2 141
|
787
|
2 159
|
248
|
1 271
|
2 042
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
截至2019年12月31日的遞延税項總資產
|
108
|
1 469
|
1 078
|
2 446
|
255
|
2 596
|
7 952
|
||||||||
|
於2019年12月31日的遞延税項負債總額
|
– 390
|
– 3 610
|
– 291
|
– 287
|
– 7
|
– 1 325
|
– 5 910
|
||||||||
|
於2019年12月31日的遞延税項結餘淨額
|
– 282
|
– 2 141
|
787
|
2 159
|
248
|
1 271
|
2 042
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
在同一税務管轄區內抵銷下列金額的遞延税項資產和負債後,餘額為:
|
|
|
|
|
|
|
|
|
|
|
|
|
43
|
||
|
截至2019年12月31日的遞延税項資產
|
|
|
|
|
|
|
7 909
|
||||||||
|
截至2019年12月31日的遞延税項負債
|
|
|
|
|
|
|
– 5 867
|
||||||||
|
於2019年12月31日的遞延税項結餘淨額
|
|
|
|
|
|
|
2 042
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||||||
|
2018年1月1日遞延税項資產總額
|
137
|
1 287
|
1 090
|
3 786
|
97
|
1 983
|
8 380
|
||||||||
|
2018年1月1日遞延税項負債總額
|
– 613
|
– 2 985
|
– 254
|
– 455
|
– 9
|
– 1 003
|
– 5 319
|
||||||||
|
2018年1月1日遞延税項淨額結餘
|
– 476
|
– 1 698
|
836
|
3 331
|
88
|
980
|
3 061
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
2018年1月1日
|
– 476
|
– 1 698
|
836
|
3 331
|
88
|
980
|
3 061
|
||||||||
|
與持作出售之出售組別有關之遞延税項結餘淨額
|
1
|
|
1
|
|
|
|
– 6
|
|
– 1
|
|
– 1
|
|
– 6
|
||
|
記入[記入]收入貸方
|
31
|
378
|
4
|
– 86
|
– 113
|
368
|
582
|
||||||||
|
記入股權
|
|
|
|
|
|
– 17
|
– 17
|
||||||||
|
記入其他全面收入
|
|
|
69
|
|
|
8
|
77
|
||||||||
|
企業合併的影響
|
|
– 2 874
|
|
|
298
|
83
|
– 2 493
|
||||||||
|
其他動作
|
13
|
42
|
6
|
9
|
1
|
– 51
|
20
|
||||||||
|
2018年12月31日的遞延税金淨餘額
|
– 431
|
– 4 151
|
915
|
3 248
|
273
|
1 370
|
1 224
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
截至2018年12月31日的遞延税項總資產
|
191
|
1 233
|
1 188
|
3 722
|
273
|
2 175
|
8 782
|
||||||||
|
2018年12月31日的遞延税項負債總額
|
– 622
|
– 5 384
|
– 273
|
– 474
|
|
– 805
|
– 7 558
|
||||||||
|
2018年12月31日的遞延税金淨餘額
|
– 431
|
– 4 151
|
915
|
3 248
|
273
|
1 370
|
1 224
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
在同一税務管轄區內抵銷下列金額的遞延税項資產和負債後,餘額為:
|
|
|
|
|
|
|
|
|
|
|
|
|
83
|
||
|
截至2018年12月31日的遞延税項資產
|
|
|
|
|
|
|
8 699
|
||||||||
|
截至2018年12月31日的遞延税項負債
|
|
|
|
|
|
|
– 7 475
|
||||||||
|
2018年12月31日的遞延税金淨餘額
|
|
|
|
|
|
|
1 224
|
||||||||
|
|
|||||||||||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||||||||||
|
2 包括與出售集團有關的300萬美元遞延税金淨額
|
|||||||||||||||
|
(數十億美元)
|
2019
|
2018
|
|||
|
預計將對超過12個月後的當前應繳税款產生影響
|
|
|
|||
|
-遞延税項資產
|
4.3
|
3.9
|
|||
|
-遞延納税義務
|
5.2
|
6.7
|
|||
|
(數十億美元)
|
2019
|
2018
|
|||
|
合併實體保留作再投資的未匯出盈利
|
61
|
73
|
|||
|
(數十億美元)
|
2019
|
2018
|
|||
|
對子公司的投資
|
3
|
3
|
|||
|
收購帶來的商譽
|
– 24
|
– 33
|
|||
|
(百萬美元)
|
不記作資本
|
大寫
|
2019年合計
|
||||
|
一年
|
14
|
0
|
14
|
||||
|
兩年
|
28
|
0
|
28
|
||||
|
三年
|
28
|
6
|
34
|
||||
|
四年
|
16
|
46
|
62
|
||||
|
五年
|
127
|
37
|
164
|
||||
|
五年多
|
435
|
2 249
|
2 684
|
||||
|
總計
|
648
|
2 338
|
2 986
|
||||
|
(百萬美元)
|
不記作資本
|
大寫
|
2018年總計
|
||||
|
一年
|
23
|
4
|
27
|
||||
|
兩年
|
14
|
0
|
14
|
||||
|
三年
|
27
|
12
|
39
|
||||
|
四年
|
65
|
5
|
70
|
||||
|
五年
|
345
|
36
|
381
|
||||
|
五年多
|
522
|
2 288
|
2 810
|
||||
|
總計
|
996
|
2 345
|
3 341
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
已到期結轉的税損
|
9
|
8
|
1
|
||||
|
(百萬美元) |
收入
陳述式 繼續 運營 |
權益 |
總計 |
||||
|
遞延税項資產及負債重估
|
|
|
|
||||
|
以前在綜合損益表中確認的項目
|
234
|
|
234
|
||||
|
以前在其他全面收益中確認的項目 1
|
|
– 358
|
– 358
|
||||
|
遞延税項資產及負債重估總額
|
234
|
– 358
|
– 124
|
||||
|
1 與離職後福利有關
|
|||||||
|
(百萬美元) |
收入
陳述式 繼續 運營 |
權益 |
總計 |
||||
|
遞延税項資產及負債重估
|
|
|
|
||||
|
以前在綜合損益表中確認的項目 1
|
– 440
|
|
– 440
|
||||
|
以前在其他全面收益中確認的項目 2
|
|
– 254
|
– 254
|
||||
|
以前在留存收益中確認的項目 3
|
|
– 71
|
– 71
|
||||
|
遞延税項資產及負債重估總額
|
– 440
|
– 325
|
– 765
|
||||
|
本期應付税款重估總額 4
|
– 34
|
|
– 34
|
||||
|
遞延所得税資產和負債及當期所得税負債的重估總額
|
– 474
|
– 325
|
– 799
|
||||
|
1 先前在已終止業務中確認的項目為4.16億美元
|
|||||||
|
2 與離職後福利和可供出售金融投資相關(歸屬於持續經營業務—2.41億美元,歸屬於已終止經營業務—1300萬美元)
|
|||||||
|
3 與股權補償計劃相關(歸屬於持續經營業務—6,600萬美元,歸屬於終止經營業務—500萬美元)
|
|||||||
|
4 已終止經營業務應佔本期應付税項重估為—300萬美元。
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
股權證券
|
1 524
|
1 155
|
|||
|
債務證券
|
33
|
31
|
|||
|
基金投資
|
233
|
251
|
|||
|
財務投資總額
|
1 790
|
1 437
|
|||
|
客户的長期應收賬款
|
|
164
|
|||
|
融資租賃協議的最低租賃付款 1
|
|
91
|
|||
|
融資轉租的長期應收賬款
|
66
|
|
|||
|
其他長期應收賬款
|
104
|
3
|
|||
|
或有代價應收賬款 2
|
399
|
396
|
|||
|
長期貸款、墊款和保證金
|
159
|
254
|
|||
|
金融資產總額
|
2 518
|
2 345
|
|||
|
1 附註30提供與已終止經營業務有關的融資租賃協議最低租賃付款的額外披露。
|
|||||
|
2 附註29提供有關或然代價的額外披露。
|
|||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
遞延補償計劃
|
414
|
468
|
|||
|
預付離職後福利計劃
|
148
|
137
|
|||
|
其他非流動資產
|
176
|
290
|
|||
|
其他非流動資產合計
|
738
|
895
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
原材料、消耗品
|
751
|
931
|
|||
|
正在進行的工作
|
3 024
|
3 087
|
|||
|
成品
|
2 207
|
2 938
|
|||
|
總庫存
|
5 982
|
6 956
|
|||
|
(數十億美元)
|
2019
|
2018
|
2017
|
||||
|
銷貨成本
|
– 8.5
|
– 8.3
|
– 8.2
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
存貨撥備
|
– 752
|
– 603
|
– 416
|
||||
|
庫存準備金的撤銷
|
218
|
216
|
172
|
||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
之應收貿易賬款總額為本
|
8 396
|
8 853
|
|||
|
可疑貿易應收賬款撥備
|
– 95
|
– 126
|
|||
|
應收貿易賬款總額,淨額
|
8 301
|
8 727
|
|||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
一月一日
|
– 126
|
– 190
|
– 162
|
||||
|
與停止經營有關的撥備 1
|
54
|
|
|
||||
|
跳水的影響
|
|
|
12
|
||||
|
企業合併的影響
|
|
– 1
|
|
||||
|
於綜合收益表扣除之呆賬應收賬款撥備 2
|
– 89
|
– 47
|
– 119
|
||||
|
可疑貿易應收賬款準備的使用
|
12
|
39
|
12
|
||||
|
撥回計入綜合收益表的呆賬應收賬款撥備 3
|
53
|
61
|
76
|
||||
|
貨幣換算效應
|
1
|
12
|
– 9
|
||||
|
12月31日
|
– 95
|
– 126
|
– 190
|
||||
|
|
|||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||
|
2 於二零一八年及二零一七年,自持續經營業務自綜合收益表扣除的撥備分別為3,000萬美元及9,400萬美元。
|
|||||||
|
3 2018年及2017年,來自持續經營業務的撥備撥回分別為4,400萬美元及6,000萬美元。
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
未逾期
|
7 763
|
7 916
|
|||
|
逾期不超過一個月
|
161
|
296
|
|||
|
逾期一個月以上三個月以下
|
123
|
194
|
|||
|
逾期三個月以上六個月以下
|
103
|
136
|
|||
|
逾期六個月以上一年以下
|
96
|
98
|
|||
|
逾期一年以上
|
150
|
213
|
|||
|
可疑貿易應收賬款撥備
|
– 95
|
– 126
|
|||
|
應收貿易賬款總額,淨額
|
8 301
|
8 727
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
來自密切監測國家的貿易應收款總額餘額
|
1 588
|
1 729
|
|||
|
逾期一年以上
|
61
|
97
|
|||
|
條文
|
24
|
44
|
|||
|
|
|||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
美元(U.S.)
|
3 466
|
3 510
|
|||
|
歐元(歐元)
|
1 384
|
1 551
|
|||
|
日元(JPY)
|
466
|
658
|
|||
|
俄羅斯盧布(盧布)
|
341
|
247
|
|||
|
人民幣(CNY)
|
279
|
282
|
|||
|
英鎊(GBP)
|
202
|
183
|
|||
|
巴西雷亞爾(BRL)
|
165
|
206
|
|||
|
加元(CAD)
|
129
|
136
|
|||
|
澳元(AUD)
|
125
|
161
|
|||
|
瑞士法郎(瑞士法郎)
|
89
|
100
|
|||
|
其他貨幣
|
1 655
|
1 693
|
|||
|
應收貿易賬款總額,淨額
|
8 301
|
8 727
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
債務證券
|
24
|
325
|
|||
|
基金投資
|
37
|
35
|
|||
|
有價證券總額
|
61
|
360
|
|||
|
商品
|
110
|
104
|
|||
|
原始期限在90天以上的定期存款和短期投資
|
61
|
2 087
|
|||
|
衍生金融工具
|
102
|
130
|
|||
|
債務證券、定期存款和短期投資的應計利息
|
|
12
|
|||
|
有價證券、商品、定期存款和衍生金融工具總額
|
334
|
2 693
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
美元(U.S.)
|
|
302
|
|||
|
歐元(歐元)
|
13
|
|
12
|
||
|
日元(JPY)
|
11
|
11
|
|||
|
債務證券總額
|
24
|
325
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
經常賬户
|
3 247
|
3 121
|
|||
|
原始到期日不足90天的定期存款和短期投資
|
7 865
|
10 150
|
|||
|
現金和現金等價物合計
|
11 112
|
13 271
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
增值税應收賬款
|
508
|
588
|
|||
|
可追回的預扣税
|
108
|
99
|
|||
|
預付費用
|
|
|
|||
|
-第三方
|
898
|
811
|
|||
|
-聯營公司
|
|
1
|
|||
|
關聯公司應收賬款
|
1
|
2
|
|||
|
其他應收款和流動資產
|
1 165
|
1 360
|
|||
|
其他流動資產總額
|
2 680
|
2 861
|
|||
|
(百萬美元) |
2017年1月1日 |
運動
以年計 |
2017年12月31日 |
運動
以年計 |
2018年12月31日 |
運動
以年計 |
2019年12月31日 |
||||||||
|
股本
|
972
|
– 3
|
969
|
– 25
|
944
|
– 8
|
936
|
||||||||
|
國庫股
|
– 76
|
– 24
|
– 100
|
31
|
– 69
|
– 11
|
– 80
|
||||||||
|
已發行股本
|
896
|
– 27
|
869
|
6
|
875
|
– 19
|
856
|
||||||||
|
|
2019
|
2018
|
2017
|
||||||||||||||||||
|
流通股數量 (單位:百萬) |
注意事項 |
總計
諾華公司 股票 |
總計
財政部 股票 1 |
總計
傑出的 股票 |
總計
諾華公司 股票 |
總計
財政部 股票 1 |
總計
傑出的 股票 |
總計
諾華公司 股票 |
總計
財政部 股票 1 |
總計
傑出的 股票 |
|||||||||||
|
年初餘額
|
|
2 550.6
|
– 239.4
|
2 311.2
|
2 616.8
|
– 299.3
|
2 317.5
|
2 627.1
|
– 253.0
|
2 374.1
|
|||||||||||
|
股票因減資而被註銷 2
|
|
– 23.3
|
23.3
|
|
– 66.2
|
66.2
|
|
– 10.3
|
10.3
|
|
|||||||||||
|
被收購的股份將被註銷 3
|
|
|
– 60.3
|
– 60.3
|
|
– 23.3
|
– 23.3
|
|
– 66.2
|
– 66.2
|
|||||||||||
|
其他股票購買 4
|
|
|
– 1.7
|
– 1.7
|
|
– 1.2
|
– 1.2
|
|
– 3.8
|
– 3.8
|
|||||||||||
|
行使期權和員工交易 5
|
18.8
|
|
5.5
|
5.5
|
|
7.8
|
7.8
|
|
4.6
|
4.6
|
|||||||||||
|
基於股權的薪酬 5
|
|
|
9.4
|
9.4
|
|
7.4
|
7.4
|
|
8.8
|
8.8
|
|||||||||||
|
派發給愛爾康員工的股票
|
|
|
0.9
|
0.9
|
|
|
|
|
|
|
|||||||||||
|
其他股份銷售
|
|
|
|
|
|
3.0
|
3.0
|
|
|
|
|||||||||||
|
總移動量
|
|
– 23.3
|
– 22.9
|
– 46.2
|
– 66.2
|
59.9
|
– 6.3
|
– 10.3
|
– 46.3
|
– 56.6
|
|||||||||||
|
年終餘額
|
|
2 527.3
|
– 262.3
|
2 265.0
|
2 550.6
|
– 239.4
|
2 311.2
|
2 616.8
|
– 299.3
|
2 317.5
|
|||||||||||
|
|
|||||||||||||||||||||
|
1 約1.176億股庫存股(2018年:1.216億股;2017年:1.313億股)由諾華實體持有,限制其使用。
|
|||||||||||||||||||||
|
2 諾華通過取消前幾年在瑞士證券交易所第二交易線回購的股票減少了股本。
|
|||||||||||||||||||||
|
3 根據2016年年度股東大會(AGM)批准的100億瑞士法郎股份回購授權,用於2019年2月28日之前的交易,以及根據2019年年度股東大會批准的100億瑞士法郎股份回購授權,用於該日期之後的交易
|
|||||||||||||||||||||
|
4 從僱員處獲得的股份,這些股份以前根據各自的計劃授予他們
|
|||||||||||||||||||||
|
5 因行使期權而交付的股票以及與基於股權的參與計劃相關的實物股票交付
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||
|
2019
|
2018
|
2017
|
|||||
|
每股股息(瑞士法郎)
|
2.85
|
2.80
|
2.75
|
||||
|
股息支付總額(十億美元)
|
6.6
|
7.0
|
6.5
|
||||
|
|
2019
|
2018
|
2017
|
||||||||||||
|
注意事項 |
數量
傑出的 股票 (單位:百萬) |
對股票的影響 百萬美元 |
數量
傑出的 股票 (單位:百萬) |
對股票的影響 百萬美元 |
數量
傑出的 股票 (單位:百萬) |
對股票的影響 百萬美元 |
|||||||||
|
被收購的股份將被註銷 1
|
|
– 60.3
|
– 5 351
|
– 23.3
|
– 1 859
|
– 66.2
|
– 5 270
|
||||||||
|
其他股票購買 2
|
|
– 1.7
|
– 160
|
– 1.2
|
– 114
|
– 3.8
|
– 304
|
||||||||
|
購買庫藏股
|
|
– 62.0
|
– 5 511
|
– 24.5
|
– 1 973
|
– 70.0
|
– 5 574
|
||||||||
|
行使期權和員工交易 3
|
18.8
|
5.5
|
210
|
7.8
|
434
|
4.6
|
255
|
||||||||
|
基於股權的薪酬 4,5
|
|
9.4
|
833
|
7.4
|
756
|
8.8
|
612
|
||||||||
|
派發給愛爾康員工的股票
|
|
0.9
|
18
|
|
|
|
|
||||||||
|
其他股份銷售
|
|
|
|
3.0
|
263
|
|
|
||||||||
|
總計
|
|
– 46.2
|
– 4 450
|
– 6.3
|
– 520
|
– 56.6
|
– 4 707
|
||||||||
|
|
|||||||||||||||
|
1 根據2016年股東大會批准的100億瑞士法郎股份回購授權,用於2019年2月28日之前的交易,以及根據2019年股東大會批准的100億瑞士法郎股份回購授權,用於該日期之後的交易
|
|||||||||||||||
|
2 從僱員處獲得的股份,這些股份以前根據各自的計劃授予他們
|
|||||||||||||||
|
3 因行使與股權參與計劃和庫存股交付有關的期權而交付的股份。所交付股份的平均股價顯著低於市場價格,反映了行使的期權的執行價。
|
|||||||||||||||
|
4 股權結算股份薪酬根據股份薪酬計劃的歸屬期間在綜合收益表中列支。已授出股份及購股權的價值於各自歸屬期間記入綜合股本。此外,超過損益表中確認的費用的可扣税金額所產生的税收優惠計入權益。
|
|||||||||||||||
|
5 2017年包括與先前通過保留收益確認的股權補償遞延税項資產重估有關的7100萬美元影響。此次重估是由於美國於2017年12月22日頒佈的税務改革立法所致。有關額外披露,請參閲附註12。
|
|||||||||||||||
|
|
|||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
直通債券
|
22 167
|
25 283
|
|||
|
對銀行和其他金融機構的負債 1
|
188
|
285
|
|||
|
融資租賃義務
|
|
92
|
|||
|
總額,包括非流動金融債務的當期部分
|
22 355
|
25 660
|
|||
|
非流動金融債務的較少流動部分
|
– 2 002
|
– 3 190
|
|||
|
非流動金融債務共計
|
20 353
|
22 470
|
|||
|
1 平均利率0. 2%(二零一八年:0. 3%)
|
|||||
|
息票 |
貨幣 |
名義上的 金額 |
發行 年 |
成熟性 年 |
發行人 |
發行價 |
2019
(美元 百萬美元) |
2018
(美元 百萬美元) |
|||||||||
|
5.125%
|
美元
|
3 000
|
2009
|
2019
|
諾華證券投資有限公司百慕大漢密爾頓
|
99.822%
|
|
3 000
|
|||||||||
|
4.400%
|
美元
|
1 000
|
2010
|
2020
|
諾華資本公司,紐約,美國
|
99.237%
|
1 000
|
998
|
|||||||||
|
2.400%
|
美元
|
1 500
|
2012
|
2022
|
諾華資本公司,紐約,美國
|
99.225%
|
1 495
|
1 493
|
|||||||||
|
3.700%
|
美元
|
500
|
2012
|
2042
|
諾華資本公司,紐約,美國
|
98.325%
|
489
|
489
|
|||||||||
|
3.400%
|
美元
|
2 150
|
2014
|
2024
|
諾華資本公司,紐約,美國
|
99.287%
|
2 139
|
2 137
|
|||||||||
|
4.400%
|
美元
|
1 850
|
2014
|
2044
|
諾華資本公司,紐約,美國
|
99.196%
|
1 825
|
1 825
|
|||||||||
|
0.750%
|
歐元
|
600
|
2014
|
2021
|
諾華金融公司盧森堡盧森堡
|
99.134%
|
670
|
683
|
|||||||||
|
1.625%
|
歐元
|
600
|
2014
|
2026
|
諾華金融公司盧森堡盧森堡
|
99.697%
|
670
|
684
|
|||||||||
|
0.250%
|
CHF
|
500
|
2015
|
2025
|
諾華製藥,瑞士巴塞爾
|
100.640%
|
517
|
508
|
|||||||||
|
0.625%
|
CHF
|
550
|
2015
|
2029
|
諾華製藥,瑞士巴塞爾
|
100.502%
|
568
|
558
|
|||||||||
|
1.050%
|
CHF
|
325
|
2015
|
2035
|
諾華製藥,瑞士巴塞爾
|
100.479%
|
336
|
330
|
|||||||||
|
3.000%
|
美元
|
1 750
|
2015
|
2025
|
諾華資本公司,紐約,美國
|
99.010%
|
1 735
|
1 732
|
|||||||||
|
4.000%
|
美元
|
1 250
|
2015
|
2045
|
諾華資本公司,紐約,美國
|
98.029%
|
1 219
|
1 219
|
|||||||||
|
0.125%
|
歐元
|
1 250
|
2016
|
2023
|
諾華金融公司盧森堡盧森堡
|
99.127%
|
1 392
|
1 419
|
|||||||||
|
0.625%
|
歐元
|
500
|
2016
|
2028
|
諾華金融公司盧森堡盧森堡
|
98.480%
|
553
|
563
|
|||||||||
|
1.800%
|
美元
|
1 000
|
2017
|
2020
|
諾華資本公司,紐約,美國
|
99.609%
|
1 000
|
998
|
|||||||||
|
2.400%
|
美元
|
1 000
|
2017
|
2022
|
諾華資本公司,紐約,美國
|
99.449%
|
996
|
995
|
|||||||||
|
3.100%
|
美元
|
1 000
|
2017
|
2027
|
諾華資本公司,紐約,美國
|
99.109%
|
990
|
989
|
|||||||||
|
0.000%
|
歐元
|
1 250
|
2017
|
2021
|
諾華金融公司盧森堡盧森堡
|
99.133%
|
1 396
|
1 421
|
|||||||||
|
1.125%
|
歐元
|
600
|
2017
|
2027
|
諾華金融公司盧森堡盧森堡
|
99.874%
|
670
|
684
|
|||||||||
|
0.500%
|
歐元
|
750
|
2018
|
2023
|
諾華金融公司盧森堡盧森堡
|
99.655%
|
837
|
853
|
|||||||||
|
1.375%
|
歐元
|
750
|
2018
|
2030
|
諾華金融公司盧森堡盧森堡
|
99.957%
|
838
|
856
|
|||||||||
|
1.700%
|
歐元
|
750
|
2018
|
2038
|
諾華金融公司盧森堡盧森堡
|
99.217%
|
832
|
849
|
|||||||||
|
全額直通債券
|
|
|
|
|
|
|
22 167
|
25 283
|
|||||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
2019
|
|
3 190
|
|||
|
2020
|
2 002
|
2 006
|
|||
|
2021
|
2 067
|
2 111
|
|||
|
2022
|
2 583
|
2 585
|
|||
|
2023
|
2 321
|
2 278
|
|||
|
2024
|
2 139
|
2 137
|
|||
|
2024年之後
|
11 243
|
11 353
|
|||
|
總計
|
22 355
|
25 660
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
美元(U.S.)
|
12 889
|
15 964
|
|||
|
歐元(歐元)
|
7 861
|
8 028
|
|||
|
日元(JPY)
|
184
|
272
|
|||
|
瑞士法郎(瑞士法郎)
|
1 421
|
1 396
|
|||
|
總計
|
22 355
|
25 660
|
|||
|
(百萬美元) |
2019
天平 板材 |
2019
公平 值 |
2018
天平 板材 |
2018
公平 值 |
|||||
|
直通債券
|
22 167
|
23 701
|
25 283
|
25 438
|
|||||
|
其他
|
188
|
188
|
377
|
377
|
|||||
|
總計
|
22 355
|
23 889
|
25 660
|
25 815
|
|||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
作為非流動金融債務抵押品的不動產、廠房及設備賬面淨值總額
|
3
|
96
|
|||
|
(百萬美元)
|
2019
|
2018
|
|||
|
員工福利的應計負債:
|
|
|
|||
|
固定收益養老金計劃 1
|
3 469
|
3 546
|
|||
|
其他長期僱員福利和遞延薪酬
|
546
|
600
|
|||
|
其他離職後福利 1
|
612
|
954
|
|||
|
環境補救規定
|
592
|
634
|
|||
|
關於產品責任、政府調查和其他法律事項的規定
|
200
|
214
|
|||
|
或有對價 2
|
958
|
874
|
|||
|
其他非流動負債
|
255
|
497
|
|||
|
準備金和其他非流動負債總額
|
6 632
|
7 319
|
|||
|
1 附註25提供了與離職後福利有關的補充披露。
|
|||||
|
2 附註29提供有關或然代價的額外披露。
|
|||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
一月一日
|
692
|
761
|
773
|
||||
|
現金支付
|
– 30
|
– 48
|
– 46
|
||||
|
釋放 1
|
– 83
|
– 21
|
– 153
|
||||
|
加法 2
|
124
|
7
|
154
|
||||
|
貨幣換算效應
|
11
|
– 7
|
33
|
||||
|
12月31日
|
714
|
692
|
761
|
||||
|
減去當期經費
|
– 122
|
– 58
|
– 55
|
||||
|
截至12月31日的非流動環境補救準備金
|
592
|
634
|
706
|
||||
|
|
|||||||
|
1 二零一八年及二零一七年,來自持續經營業務的撥備撥備分別為2,100萬美元及1. 53億美元。
|
|||||||
|
2 於二零一八年及二零一七年,自持續經營業務自綜合收益表扣除的撥備分別為700萬美元及154百萬美元。
|
|||||||
|
(百萬美元) |
預期
現金流出 |
||
|
在兩年內到期
|
141
|
||
|
逾期兩年但在五年內到期
|
210
|
||
|
應在5年後但在10年內支付
|
258
|
||
|
在10年後到期
|
105
|
||
|
環境補救責任規定總額
|
714
|
||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
一月一日
|
340
|
351
|
395
|
||||
|
與已終止業務有關的準備金 1
|
– 42
|
|
|
||||
|
企業合併的影響
|
10
|
|
|
||||
|
現金支付
|
– 116
|
– 118
|
– 69
|
||||
|
條文的發放 2
|
– 52
|
– 107
|
– 70
|
||||
|
對條文的增補 3
|
1 230
|
220
|
93
|
||||
|
貨幣換算效應
|
– 1
|
– 6
|
2
|
||||
|
12月31日
|
1 369
|
340
|
351
|
||||
|
較小電流部分
|
– 1 169
|
– 126
|
– 121
|
||||
|
12月31日非流動產品責任、政府調查和其他法律事項規定
|
200
|
214
|
230
|
||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||
|
2 來自持續經營業務的撥備於二零一八年及二零一七年分別為1. 07億美元及6,300萬美元。
|
|||||||
|
3 於二零一八年及二零一七年,自持續經營業務自綜合收益表扣除的撥備分別為2. 20億美元及4,700萬美元。
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
聯營公司應要求應付的應付賬款 1
|
1 836
|
1 778
|
|||
|
銀行和其他金融債務 2
|
719
|
701
|
|||
|
商業票據
|
2 289
|
3 951
|
|||
|
非流動金融債務的流動部分
|
2 002
|
3 190
|
|||
|
衍生金融工具的公允價值
|
185
|
58
|
|||
|
流動金融債務和衍生金融工具總額
|
7 031
|
9 678
|
|||
|
1 加權平均利率0. 5%(二零一八年:0. 5%)
|
|||||
|
2 加權平均利率12. 9%(二零一八年:9. 6%)
|
|||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
所得税以外的其他税種
|
471
|
528
|
|||
|
重組條文
|
438
|
507
|
|||
|
已收到但未開發票的貨物和服務的應計費用
|
1 046
|
970
|
|||
|
應計特許權使用費
|
653
|
651
|
|||
|
金融債務的應計利息
|
98
|
156
|
|||
|
從收入中扣除的準備金
|
5 595
|
5 262
|
|||
|
應計報酬和福利,包括社會保障
|
2 464
|
2 527
|
|||
|
環境修復責任
|
122
|
58
|
|||
|
遞延收入
|
114
|
236
|
|||
|
關於產品責任、政府調查和其他法律事項的規定 1
|
1 169
|
126
|
|||
|
應計股份支付
|
326
|
273
|
|||
|
或然代價 2
|
78
|
33
|
|||
|
回購自有股份的承諾 3
|
|
284
|
|||
|
其他應付款
|
764
|
673
|
|||
|
準備金總額和其他流動負債
|
13 338
|
12 284
|
|||
|
|
|||||
|
1 附註20提供了與法律規定有關的補充披露。
|
|||||
|
2 附註29提供有關或然代價的額外披露。
|
|||||
|
3 附註18提供有關購回本身股份承諾的額外披露。
|
|||||
|
|
|
|
|
|
損益表費用2
|
|
|
||||||||||
|
(百萬美元) |
收入 扣除額 條文 一月一日 |
收入
扣除額 條文 相關內容 停產 運營1 |
的效果 貨幣 翻譯 和商業 組合 |
付款/ 利用率 |
調整 前幾年的 |
本年度 |
更改中 條文 偏移量 總貿易額 應收賬款 |
收入 扣除額 條文 12月31日 |
|||||||||
|
2019
|
|
|
|
|
|
|
|
|
|||||||||
|
特定於美國的醫療保健計劃和計劃回扣
|
1 883
|
0
|
|
– 5 183
|
– 193
|
5 474
|
|
1 981
|
|||||||||
|
非特定於美國的醫療計劃和計劃回扣
|
1 625
|
– 28
|
– 19
|
– 2 467
|
– 2
|
2 659
|
1
|
1 769
|
|||||||||
|
非醫療保健計劃和計劃相關的回扣、退貨和其他扣除
|
1 754
|
– 166
|
9
|
– 11 698
|
– 25
|
11 868
|
103
|
1 845
|
|||||||||
|
2019年總計
|
5 262
|
– 194
|
– 10
|
– 19 348
|
– 220
|
20 001
|
104
|
5 595
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
2018
|
|
|
|
|
|
|
|
|
|||||||||
|
特定於美國的醫療保健計劃和計劃回扣
|
1 590
|
|
|
– 4 158
|
– 90
|
4 541
|
|
1 883
|
|||||||||
|
非特定於美國的醫療計劃和計劃回扣
|
1 356
|
|
– 78
|
– 2 182
|
83
|
2 555
|
– 109
|
1 625
|
|||||||||
|
非醫療保健計劃和計劃相關的回扣、退貨和其他扣除
|
1 726
|
|
– 51
|
– 12 227
|
– 91
|
11 956
|
441
|
1 754
|
|||||||||
|
2018年共計
|
4 672
|
|
– 129
|
– 18 567
|
– 98
|
19 052
|
332
|
5 262
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
2017
|
|
|
|
|
|
|
|
|
|||||||||
|
特定於美國的醫療保健計劃和計劃回扣
|
1 461
|
|
|
– 3 684
|
– 62
|
3 875
|
|
1 590
|
|||||||||
|
非特定於美國的醫療計劃和計劃回扣
|
1 020
|
|
131
|
– 1 954
|
80
|
2 186
|
– 107
|
1 356
|
|||||||||
|
非醫療保健計劃和計劃相關的回扣、退貨和其他扣除
|
1 702
|
|
65
|
– 11 814
|
– 127
|
12 045
|
– 145
|
1 726
|
|||||||||
|
2017年共計
|
4 183
|
|
196
|
– 17 452
|
– 109
|
18 106
|
– 252
|
4 672
|
|||||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||||||||||||
|
2 2018年,來自持續經營業務的綜合收益表的支出為182.48億美元,2017年為177.72億美元。
|
|||||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
一月一日
|
507
|
153
|
222
|
||||
|
與已終止業務有關的準備金 1
|
– 8
|
|
|
||||
|
加法 2
|
492
|
534
|
194
|
||||
|
現金支付
|
– 479
|
– 145
|
– 200
|
||||
|
釋放 3
|
– 72
|
– 33
|
– 64
|
||||
|
轉賬
|
|
|
– 7
|
||||
|
貨幣換算效應
|
– 2
|
– 2
|
8
|
||||
|
12月31日
|
438
|
507
|
153
|
||||
|
|
|||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||
|
2 自持續經營業務自綜合收益表扣除的撥備於二零一八年及二零一七年分別為5. 21億美元及1. 86億美元。
|
|||||||
|
3 2018年及2017年,來自持續經營業務的撥備撥回分別為3,100萬美元及5,900萬美元。
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
折舊、攤銷和減值:
|
|
|
|
||||
|
財產、廠房和設備
|
1 547
|
1 783
|
1 460
|
||||
|
使用權資產 1
|
305
|
|
|
||||
|
無形資產
|
3 974
|
3 428
|
3 276
|
||||
|
金融資產 2
|
– 38
|
6
|
227
|
||||
|
準備金和其他非流動負債的非現金變動
|
1 871
|
895
|
86
|
||||
|
財產、廠房和設備的處置和其他調整收益;無形資產;金融資產;以及其他非流動資產,淨額
|
– 1 234
|
– 902
|
– 1 077
|
||||
|
股權結算補償費用
|
758
|
673
|
612
|
||||
|
來自相聯公司的收入 3
|
– 659
|
– 6 438
|
– 1 108
|
||||
|
税費
|
1 793
|
1 295
|
1 603
|
||||
|
財務費用淨額
|
805
|
746
|
708
|
||||
|
總計
|
9 122
|
1 486
|
5 787
|
||||
|
1 使用權資產折舊自二零一九年一月一日(國際財務報告準則第16號租賃的實施日期)起確認。附註1和10提供了額外披露。
|
|||||||
|
2 包括公允價值調整
|
|||||||
|
3 2018年包括從剝離GSK Consumer Healthcare Holdings Ltd.的投資確認的税前收益(58億美元)的撥回(見附註2)。出售所得現金淨額130億美元已計入綜合現金流量表“收購及出售聯營公司權益淨額”。”
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
庫存(增加)
|
– 382
|
– 387
|
– 203
|
||||
|
貿易應收款(增加)
|
– 980
|
– 544
|
– 655
|
||||
|
貿易應付款增加
|
553
|
252
|
82
|
||||
|
其他流動資產變動
|
– 160
|
316
|
– 303
|
||||
|
其他流動負債變動
|
1 167
|
941
|
1 410
|
||||
|
其他調整,淨額
|
1
|
– 2
|
1
|
||||
|
總計
|
199
|
576
|
332
|
||||
|
(百萬美元)
|
注意事項
|
2019
|
2018
|
2017
|
|||||
|
確認為企業合併結果的淨資產
|
24
|
– 4 124
|
– 13 660
|
– 874
|
|||||
|
以前持有的股權的公允價值
|
|
33
|
|
|
|||||
|
或有代價,淨額
|
|
242
|
– 5
|
151
|
|||||
|
付款、遞延對價和其他調整,淨額
|
|
– 2
|
– 36
|
– 36
|
|||||
|
用於收購業務的現金流
|
|
– 3 851
|
– 13 701
|
– 759
|
|||||
|
業務剝離產生的現金流量淨額 1
|
|
91
|
18
|
45
|
|||||
|
用於收購和撤資業務的現金流,淨額
|
|
– 3 760
|
– 13 683
|
– 714
|
|||||
|
|
|||||||||
|
1 2019年,9100萬美元包括往年剝離產生的400萬美元淨現金流出和2019年業務剝離產生的9500萬美元淨現金流入。二零一九年已剝離業務的可識別資產淨值為1. 96億美元,包括非流動資產1. 59億美元、流動資產9,600萬美元(包括1,100萬美元現金及現金等價物)、非流動負債1,800萬美元及流動負債4,100萬美元。
2018年,1800萬美元代表往年撤資後的淨現金流入。 2017年,4500萬美元的淨現金流入與2017年剝離的可識別資產淨額有關。2017年剝離的業務總額為4800萬美元,包括非流動資產2900萬美元、流動資產3400萬美元和流動負債1500萬美元。 |
|||||||||
|
(百萬美元) |
非當前 金融 債務 |
當前
金融 債項及 導數 金融 儀器 |
非當前 租賃負債 |
當前租約 負債 |
|||||
|
2019年1月1日
|
22 470
|
9 678
|
|
|
|||||
|
採納國際財務報告準則第16號的影響 1
|
– 2
|
– 1
|
1 471
|
268
|
|||||
|
採納國際財務報告準則第16號的影響 2
|
– 89
|
|
246
|
40
|
|||||
|
與終止經營有關的金融債務和租賃負債 3
|
|
– 47
|
– 246
|
– 40
|
|||||
|
非流動金融債務增加
|
93
|
|
|
|
|||||
|
償還非流動金融債務
|
|
– 3 195
|
|
|
|||||
|
本期財政債務變動情況
|
|
– 1 582
|
|
|
|||||
|
支付租賃負債,淨額
|
|
|
|
– 273
|
|||||
|
租賃負債中列為經營活動現金流量的金額的利息支付
|
|
|
|
– 51
|
|||||
|
新租約
|
|
|
362
|
131
|
|||||
|
業務合併和剝離的影響
|
|
2
|
– 11
|
– 6
|
|||||
|
公允價值變動及其他變動淨額
|
|
129
|
33
|
20
|
|||||
|
債券攤銷折價
|
25
|
|
|
|
|||||
|
貨幣換算效應
|
– 141
|
44
|
4
|
1
|
|||||
|
從非流動重新分類為流動、淨額
|
– 2 003
|
2 003
|
– 156
|
156
|
|||||
|
2019年12月31日
|
20 353
|
7 031
|
1 703
|
246
|
|||||
|
1 租賃負債於二零一九年一月一日(國際財務報告準則第16號租賃的實施日期)確認。附註10提供了補充披露。
|
|||||||||
|
2 2018年,金融債務包括Alcon業務先前報告的融資租賃責任89百萬美元,該債務已於2019年1月1日重新分類至租賃負債,並採納國際財務報告準則第16號租賃。附註30提供額外披露。
|
|||||||||
|
3 指於2019年1月1日與報告為已終止經營業務的Alcon業務有關的金融債務及租賃負債。見注1、2和30。
|
|||||||||
|
(百萬美元) |
非當前 金融 債務 |
|
當前
金融 債項及 導數 金融 儀器 |
|
|
|
2018年1月1日
|
23 224
|
5 308
|
|||
|
非流動金融債務增加 1
|
2 856
|
|
|||
|
償還非流動金融債務 2
|
|
– 366
|
|||
|
本期財政債務變動情況 3
|
|
1 681
|
|||
|
企業合併的影響
|
10
|
4
|
|
||
|
公允價值變動及其他變動
|
5
|
– 48
|
|||
|
債券攤銷折價
|
27
|
2
|
|||
|
貨幣換算效應
|
– 462
|
– 93
|
|||
|
非流動金融債務的流動部分
|
– 3 190
|
3 190
|
|||
|
2018年12月31日
|
22 470
|
9 678
|
|||
|
1 非流動金融債務的增加僅記錄於持續經營業務現金流量綜合表。
|
|||||
|
2 償還非流動金融債務僅計入持續經營業務現金流量綜合表。
|
|||||
|
3 計入持續經營業務現金流量綜合表的流動金融債務變動為16.87億美元。
|
|||||
|
(百萬美元) |
非當前 金融 債務 |
|
當前
金融 債項及 導數 金融 儀器 |
|
|
|
2017年1月1日
|
17 897
|
5 905
|
|||
|
非流動金融債務增加 1
|
4 933
|
|
|||
|
償還非流動金融債務 2
|
– 1
|
– 187
|
|||
|
本期財政債務變動情況 3
|
|
– 755
|
|||
|
公允價值變動及其他變動
|
– 6
|
– 140
|
|||
|
債券攤銷折價
|
16
|
|
|||
|
貨幣換算效應
|
744
|
126
|
|||
|
非流動金融債務的流動部分
|
– 359
|
359
|
|||
|
2017年12月31日
|
23 224
|
5 308
|
|||
|
1 非流動金融債務的增加僅記錄於持續經營業務現金流量綜合表。
|
|||||
|
2 償還非流動金融債務僅計入持續經營業務現金流量綜合表。
|
|||||
|
3 計入持續經營業務現金流量綜合表的流動金融債務變動為6.44億美元。
|
|||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
財產、廠房和設備
|
44
|
137
|
|
||||
|
目前市場上銷售的產品
|
3 550
|
2 531
|
|
||||
|
獲得的研究和開發
|
342
|
10 224
|
1 223
|
||||
|
其他無形資產
|
22
|
1
|
|
||||
|
遞延税項資產
|
60
|
381
|
8
|
||||
|
財政資產和其他資產
|
8
|
19
|
|
||||
|
盤存
|
195
|
20
|
|
||||
|
應收貿易賬款和其他流動資產
|
4
|
90
|
|
||||
|
現金和現金等價物
|
|
1 112
|
20
|
||||
|
遞延税項負債
|
– 107
|
– 2 874
|
– 325
|
||||
|
經常和非流動金融債務
|
– 2
|
– 14
|
|
||||
|
應付貿易款項和其他負債
|
– 178
|
– 627
|
– 1
|
||||
|
取得的可確認淨資產
|
3 938
|
11 000
|
925
|
||||
|
現金和現金等價物
|
|
– 1 112
|
– 20
|
||||
|
非控制性權益
|
|
– 26
|
|
||||
|
商譽
|
186
|
4 084
|
94
|
||||
|
確認為企業合併結果的淨資產 1
|
4 124
|
13 946
|
999
|
||||
|
1 2018年,因持續經營業務合併而於合併資產負債表確認的淨資產為136.6億美元,2017年為8.74億美元。
|
|||||||
|
養老金計劃
|
其他離職後福利計劃
|
||||||||
|
(百萬美元)
|
2019
|
2018
|
2019
|
2018
|
|||||
|
1月1日的福利義務
|
22 179
|
23 210
|
1 073
|
1 115
|
|||||
|
與非持續經營有關的福利義務 1
|
– 662
|
|
– 385
|
|
|||||
|
當前服務成本
|
336
|
378
|
13
|
34
|
|||||
|
利息成本
|
330
|
321
|
29
|
39
|
|||||
|
過去的服務成本和結算
|
– 168
|
– 1
|
|
|
|||||
|
行政費用
|
24
|
26
|
|
|
|||||
|
財務假設變動引起的重新計量損失/(收益)
|
1 791
|
– 567
|
76
|
– 31
|
|||||
|
人口假設變化引起的重新計量(收益)/損失
|
– 193
|
5
|
– 9
|
1
|
|||||
|
與經驗相關的重新計量損失/(收益)
|
184
|
264
|
– 22
|
– 32
|
|||||
|
貨幣換算效應
|
283
|
– 374
|
|
– 7
|
|||||
|
福利支付
|
– 1 256
|
– 1 263
|
– 30
|
– 46
|
|||||
|
相聯者的供款
|
169
|
169
|
|
|
|||||
|
收購、撤資或轉讓的效果
|
49
|
11
|
1
|
|
|||||
|
12月31日的福利義務
|
23 066
|
22 179
|
746
|
1 073
|
|||||
|
1月1日計劃資產的公允價值
|
18 838
|
20 275
|
119
|
162
|
|||||
|
計劃與非持續運營相關的資產 1
|
– 424
|
|
– 40
|
|
|||||
|
利息收入
|
257
|
249
|
3
|
5
|
|||||
|
不含利息收入的計劃資產回報率
|
1 656
|
– 805
|
10
|
– 8
|
|||||
|
貨幣換算效應
|
304
|
– 310
|
|
|
|||||
|
諾華集團貢獻
|
420
|
520
|
74
|
6
|
|||||
|
相聯者的供款
|
169
|
169
|
|
|
|||||
|
聚落
|
– 193
|
– 3
|
|
|
|||||
|
福利支付
|
– 1 256
|
– 1 263
|
– 30
|
– 46
|
|||||
|
收購、撤資或轉讓的效果
|
39
|
6
|
– 2
|
|
|||||
|
12月31日計劃資產的公允價值
|
19 810
|
18 838
|
134
|
119
|
|||||
|
資金狀況
|
– 3 256
|
– 3 341
|
– 612
|
– 954
|
|||||
|
1月1日確認基金盈餘的限額
|
– 68
|
– 89
|
|
|
|||||
|
更改確認基金盈餘的限額(包括匯率差異)
|
7
|
25
|
|
|
|||||
|
限制基金盈餘的利息收入
|
– 4
|
– 4
|
|
|
|||||
|
12月31日確認基金盈餘的限額
|
– 65
|
– 68
|
|
|
|||||
|
資產負債表於12月31日的淨負債
|
– 3 321
|
– 3 409
|
– 612
|
– 954
|
|||||
|
|
|||||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||||
|
養老金計劃
|
其他離職後福利計劃
|
||||||||
|
(百萬美元)
|
2019
|
2018
|
2019
|
2018
|
|||||
|
1月1日的淨負債
|
– 3 409
|
– 3 024
|
– 954
|
– 953
|
|||||
|
減去:與停產業務有關的淨負債 1
|
238
|
|
345
|
|
|||||
|
當前服務成本
|
– 336
|
– 378
|
– 13
|
– 34
|
|||||
|
淨利息支出
|
– 77
|
– 76
|
– 26
|
– 34
|
|||||
|
行政費用
|
– 24
|
– 26
|
|
|
|||||
|
過去的服務成本和結算
|
– 25
|
– 2
|
|
|
|||||
|
重新測量
|
– 126
|
– 507
|
– 35
|
54
|
|||||
|
貨幣換算效應
|
21
|
64
|
|
7
|
|||||
|
諾華集團貢獻
|
420
|
520
|
74
|
6
|
|||||
|
收購、撤資或轉讓的效果
|
– 10
|
– 5
|
– 3
|
|
|||||
|
更改確認基金盈餘的限額
|
7
|
25
|
|
|
|||||
|
截至12月31日的負債淨額
|
– 3 321
|
– 3 409
|
– 612
|
– 954
|
|||||
|
|
|
|
|
||||||
|
在綜合資產負債表中確認的金額
|
|
||||||||
|
預付福利成本
|
148
|
137
|
|
|
|||||
|
應計福利負債
|
– 3 469
|
– 3 546
|
– 612
|
– 954
|
|||||
|
|
|||||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
|||||||||
|
2019
|
2018
|
||||||||||||||||
|
(百萬美元) |
瑞士 |
美聯航
州政府 |
其餘部分
世界 |
總計 |
瑞士 |
美聯航
州政府 |
其餘部分
世界 |
總計 |
|||||||||
|
12月31日的福利義務
|
15 106
|
3 552
|
4 408
|
23 066
|
14 263
|
3 348
|
4 568
|
22 179
|
|||||||||
|
其中無資金來源
|
|
670
|
466
|
1 136
|
|
649
|
491
|
1 140
|
|||||||||
|
按成員類型
|
|
|
|
|
|
|
|
|
|||||||||
|
主動型
|
6 167
|
630
|
1 400
|
8 197
|
5 618
|
653
|
1 616
|
7 887
|
|||||||||
|
延期領取養老金的人
|
|
1 205
|
1 517
|
2 722
|
|
1 131
|
1 531
|
2 662
|
|||||||||
|
領取養老金的人
|
8 939
|
1 717
|
1 491
|
12 147
|
8 645
|
1 564
|
1 421
|
11 630
|
|||||||||
|
12月31日計劃資產的公允價值
|
14 457
|
2 311
|
3 042
|
19 810
|
13 470
|
2 160
|
3 208
|
18 838
|
|||||||||
|
資金狀況
|
– 649
|
– 1 241
|
– 1 366
|
– 3 256
|
– 793
|
– 1 188
|
– 1 360
|
– 3 341
|
|||||||||
|
2019
|
2018
|
||||||||||||
|
(百萬美元) |
美聯航
州政府 |
其餘部分
世界 |
總計 |
美聯航
州政府 |
其餘部分
世界 |
總計 |
|||||||
|
12月31日的福利義務
|
658
|
88
|
746
|
1 001
|
72
|
1 073
|
|||||||
|
其中無資金來源
|
524
|
88
|
612
|
882
|
72
|
954
|
|||||||
|
按成員類型
|
|
|
|
|
|
|
|||||||
|
主動型
|
121
|
36
|
157
|
270
|
25
|
295
|
|||||||
|
延期領取養老金的人
|
15
|
0
|
15
|
18
|
0
|
18
|
|||||||
|
領取養老金的人
|
522
|
52
|
574
|
713
|
47
|
760
|
|||||||
|
12月31日計劃資產的公允價值
|
134
|
0
|
134
|
119
|
0
|
119
|
|||||||
|
資金狀況
|
– 524
|
– 88
|
– 612
|
– 882
|
– 72
|
– 954
|
|||||||
|
養老金計劃
|
其他離職後福利計劃
|
||||||||||||
|
2019
|
2018
|
2017
|
2019
|
2018
|
2017
|
||||||||
|
用於確定12月31日福利義務的加權平均假設
|
|
|
|
|
|
|
|||||||
|
貼現率
|
1.0%
|
1.6%
|
1.5%
|
3.6%
|
4.4%
|
3.7%
|
|||||||
|
養老金預期上升率
|
0.3%
|
0.4%
|
0.5%
|
|
|
|
|||||||
|
預期加薪幅度
|
2.8%
|
2.8%
|
2.8%
|
|
|
|
|||||||
|
儲蓄存款利息
|
0.3%
|
0.8%
|
0.6%
|
|
|
|
|||||||
|
65歲男性目前的平均預期壽命(以年為單位)
|
22
|
22
|
22
|
21
|
21
|
21
|
|||||||
|
65歲女性當前平均預期壽命(以年為單位)
|
24
|
24
|
24
|
23
|
23
|
23
|
|||||||
|
(百萬美元) |
2019年年底的變化
固定福利養卹金債務 |
||
|
貼現率上調25個基點
|
– 787
|
||
|
貼現率下調25個基點
|
837
|
||
|
預期壽命延長一年
|
848
|
||
|
養老金漲幅上調25個基點
|
546
|
||
|
養老金漲幅下調25個基點
|
– 135
|
||
|
儲蓄存款利息上調25個基點
|
62
|
||
|
儲蓄存款利息下調25個基點
|
– 60
|
||
|
加薪幅度上調25個基點
|
54
|
||
|
薪金增長率減少25個基點
|
– 55
|
||
|
2019
|
2018
|
2017
|
|||||
|
假設明年的醫療保健成本趨勢率
|
6.5%
|
7.0%
|
6.5%
|
||||
|
假定成本趨勢率將下降的比率
|
4.5%
|
4.5%
|
4.5%
|
||||
|
利率達到最終趨勢利率的年份
|
2028
|
2028
|
2025
|
||||
|
養老金計劃
|
|||||||||
|
(以百分比表示) |
長期的
目標 最小值 |
長期的
目標 最大值 |
2019 |
2018 |
|||||
|
股權證券
|
15
|
40
|
27
|
28
|
|||||
|
債務證券
|
20
|
60
|
36
|
35
|
|||||
|
房地產
|
5
|
20
|
17
|
17
|
|||||
|
另類投資
|
0
|
20
|
15
|
16
|
|||||
|
現金和其他投資
|
0
|
15
|
5
|
4
|
|||||
|
總計
|
|
|
100
|
100
|
|||||
|
十二月三十一日,
2019 |
十二月三十一日,
2018 |
||||
|
投資諾華製藥的股份
|
|
|
|||
|
股份數量(單位:百萬)
|
2.3
|
11.0
|
|||
|
市值(以十億美元為單位)
|
0.2
|
0.9
|
|||
|
(百萬美元) |
養老金計劃 |
其他職位-
就業 福利計劃 |
|||
|
諾華集團貢獻
|
|
|
|||
|
2020年(估計數)
|
410
|
46
|
|||
|
預期未來的福利支付
|
|
|
|||
|
2020
|
1 201
|
46
|
|||
|
2021
|
1 116
|
47
|
|||
|
2022
|
1 106
|
48
|
|||
|
2023
|
1 096
|
48
|
|||
|
2024
|
1 087
|
48
|
|||
|
2025–2029
|
5 270
|
231
|
|||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
固定繳款計劃持續業務的繳款
|
422
|
443
|
307
|
||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
與股權參與計劃相關的費用
|
1 067
|
918
|
853
|
||||
|
股權支付交易產生的負債
|
326
|
273
|
261
|
||||
|
2019
|
2018
|
||||||||
|
選項 (百萬) |
加權
平均值 鍛鍊 價格 (美元) |
選項 (百萬) |
加權
平均值 鍛鍊 價格 (美元) |
||||||
|
1月1日未平倉期權
|
5.6
|
59.9
|
7.4
|
59.5
|
|||||
|
出售或行使
|
– 2.2
|
58.4
|
– 1.8
|
58.2
|
|||||
|
截至12月31日的未償還款項
|
3.4
|
60.9
|
5.6
|
59.9
|
|||||
|
可於12月31日行使
|
3.4
|
60.9
|
5.6
|
59.9
|
|||||
|
未償還期權 |
|
|
|
|
共計/
加權 平均值 |
||||||
|
未繳數目(百萬)
|
0.3
|
0.7
|
0.9
|
1.5
|
3.4
|
||||||
|
剩餘合同期限(年)
|
0.0
|
1.0
|
2.0
|
3.0
|
2.1
|
||||||
|
行權價(美元)
|
54.5
|
57.0
|
57.6
|
66.0
|
60.9
|
||||||
|
2019
|
2018
|
||||||||
|
adr 選項 (百萬) |
加權
平均值 鍛鍊 價格 (美元) |
adr 選項 (百萬) |
加權
平均值 鍛鍊 價格 (美元) |
||||||
|
1月1日未平倉期權
|
15.2
|
60.7
|
20.3
|
59.9
|
|||||
|
出售或行使
|
– 5.6
|
58.6
|
– 5.1
|
57.4
|
|||||
|
截至12月31日的未償還款項
|
9.6
|
61.9
|
15.2
|
60.7
|
|||||
|
可於12月31日行使
|
9.6
|
61.9
|
15.2
|
60.7
|
|||||
|
未解決的ADR備選方案 |
|
|
|
|
共計/
加權 平均值 |
||||||
|
未繳數目(百萬)
|
0.4
|
1.2
|
2.9
|
5.1
|
9.6
|
||||||
|
剩餘合同期限(年)
|
0.0
|
1.0
|
2.0
|
3.0
|
2.3
|
||||||
|
行權價(美元)
|
54.5
|
57.0
|
57.6
|
66.0
|
61.9
|
||||||
|
2019
|
2018
|
||||||||||||
|
數 的股份 以百萬計 |
加權
平均公平 授予價值 日期(美元) |
公允價值在 授出日期, 數百萬美元 |
數 的股份 以百萬計 |
加權
平均公平 授予價值 日期(美元) |
公允價值在 授出日期, 數百萬美元 |
||||||||
|
1月1日的非既得股
|
25.7
|
77.1
|
1 981
|
23.9
|
80.6
|
1 926
|
|||||||
|
授與
|
|
|
|
|
|
|
|||||||
|
—年度獎勵
|
1.1
|
78.4
|
86
|
1.3
|
83.9
|
109
|
|||||||
|
—股票儲蓄計劃
|
4.2
|
83.0
|
349
|
4.1
|
84.9
|
348
|
|||||||
|
—選擇北美
|
5.3
|
64.0
|
339
|
3.9
|
77.8
|
303
|
|||||||
|
—選擇北美以外地區
|
2.6
|
67.4
|
175
|
2.1
|
79.7
|
167
|
|||||||
|
—長期績效計劃
|
2.5
|
68.9
|
172
|
1.5
|
85.8
|
129
|
|||||||
|
—長期相對績效計劃
|
0.1
|
0.0
|
0
|
0.3
|
52.0
|
16
|
|||||||
|
—其他股份獎勵
|
1.9
|
67.7
|
129
|
1.2
|
77.9
|
93
|
|||||||
|
既得
|
– 13.3
|
80.3
|
– 1 068
|
– 10.7
|
90.2
|
– 965
|
|||||||
|
被沒收
|
– 4.3
|
76.3
|
– 328
|
– 1.9
|
76.4
|
– 145
|
|||||||
|
截至12月31日的非既得股
|
25.8
|
71.1
|
1 835
|
25.7
|
77.1
|
1 981
|
|||||||
|
行政人員
|
非執行董事
|
總計
|
|||||||||||||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
2019
|
2018
|
2017
|
2019
|
2018
|
2017
|
||||||||||
|
現金和其他補償
|
20.7
|
22.5
|
18.4
|
4.1
|
4.0
|
4.0
|
24.8
|
26.5
|
22.4
|
||||||||||
|
離職後福利
|
2.6
|
2.5
|
2.0
|
|
|
|
2.6
|
2.5
|
2.0
|
||||||||||
|
基於股權的薪酬
|
40.6
|
42.5
|
49.9
|
4.6
|
4.8
|
4.8
|
45.2
|
47.3
|
54.7
|
||||||||||
|
總計
|
63.9
|
67.5
|
70.3
|
8.7
|
8.8
|
8.8
|
72.6
|
76.3
|
79.1
|
||||||||||
|
貨幣
|
2019
|
2018
|
2017
|
||||||
|
克勞爾醫生
|
CHF
|
60 000
|
60 000
|
60 000
|
|||||
|
瓦塞拉醫生
|
CHF
|
0
|
18 228
|
26 279
|
|||||
|
(百萬美元)
|
2019
|
||
|
2020
|
809
|
||
|
2021
|
442
|
||
|
2022
|
319
|
||
|
2023
|
724
|
||
|
2024
|
167
|
||
|
此後
|
1 943
|
||
|
總計
|
4 404
|
||
|
(百萬美元)
|
注意事項
|
2019 1
|
2018 1
|
||||
|
現金和現金等價物
|
16
|
11 112
|
13 271
|
||||
|
|
|
||||||
|
金融資產—按公平值計入其他全面收益計量
|
|
|
|
||||
|
有價證券
|
|
|
|
||||
|
債務證券
|
16
|
24
|
325
|
||||
|
|
|
||||||
|
長期財務投資
|
|
|
|
||||
|
股權證券
|
13
|
1 158
|
802
|
||||
|
債務證券
|
13
|
33
|
31
|
||||
|
長期金融投資總額—按公允價值計入其他全面收益
|
|
1 191
|
833
|
||||
|
|
|
|
|||||
|
金融資產總額—按公平值計入其他全面收益計量
|
|
1 215
|
1 158
|
||||
|
|
|
|
|||||
|
金融資產--按攤銷成本計量
|
|
|
|
||||
|
應收貿易賬款、應收所得税及其他流動資產(不包括預付款項)。
|
15/17
|
10 337
|
11 024
|
||||
|
債務證券、定期存款和短期投資的應計利息
|
16
|
|
12
|
||||
|
原始期限在90天以上的定期存款和短期投資
|
16
|
61
|
2 087
|
||||
|
長期貸款、墊款、保證金和其他長期應收款
|
13
|
329
|
512
|
||||
|
金融資產總額--按攤銷成本計量
|
|
10 727
|
13 635
|
||||
|
|
|
|
|||||
|
金融資產—按公平值計入綜合收益表計量
|
|
|
|
||||
|
股權證券
|
13
|
366
|
353
|
||||
|
基金投資
|
13/16
|
270
|
286
|
||||
|
相聯公司按公允價值計入損益
|
|
186
|
145
|
||||
|
衍生金融工具
|
16
|
102
|
130
|
||||
|
或有代價應收賬款
|
13
|
399
|
396
|
||||
|
金融資產總額—按公平值計入綜合收益表計量
|
|
1 323
|
1 310
|
||||
|
|
|
|
|||||
|
金融資產總額
|
|
24 377
|
29 374
|
||||
|
|
|
||||||
|
金融負債—按攤餘成本計量
|
|
|
|
||||
|
當前金融債務
|
|
|
|
||||
|
聯營公司的附息賬户須於即期付款
|
21
|
1 836
|
1 778
|
||||
|
銀行和其他金融債務
|
21
|
719
|
701
|
||||
|
商業票據
|
21
|
2 289
|
3 951
|
||||
|
非流動債務的流動部分
|
21
|
2 002
|
3 190
|
||||
|
流動金融債務總額
|
|
6 846
|
9 620
|
||||
|
|
|
||||||
|
非流動金融債務
|
|
|
|
||||
|
直通債券
|
19
|
22 167
|
25 283
|
||||
|
對銀行和其他金融機構的負債
|
19
|
188
|
285
|
||||
|
融資租賃義務
|
19
|
|
92
|
||||
|
非流動債務的流動部分
|
19
|
– 2 002
|
– 3 190
|
||||
|
非流動金融債務共計
|
|
20 353
|
22 470
|
||||
|
|
|
|
|||||
|
應付貿易賬款及購回自有股份承擔 2
|
|
5 424
|
5 840
|
||||
|
|
|
|
|||||
|
金融負債總額—按攤餘成本計量
|
|
32 623
|
37 930
|
||||
|
|
|
||||||
|
金融負債—按公平值計入綜合收益表計量
|
|
|
|
||||
|
或有代價(見附註20/22)和其他金融負債
|
|
1 065
|
917
|
||||
|
衍生金融工具
|
21
|
185
|
58
|
||||
|
金融負債總額—按公平值計入綜合收益表計量
|
|
1 250
|
975
|
||||
|
|
|
|
|||||
|
租賃負債
|
10
|
1 949
|
|
||||
|
|
|
|
|||||
|
財務負債總額
|
|
35 822
|
38 905
|
||||
|
|
|||||||
|
1 除直接債券(見附註19)外,賬面值與公平值合理相近。
|
|||||||
|
2 附註18及22提供有關購回本身股份承諾的額外披露。
|
|||||||
|
合同或基礎本金金額
|
正公允價值
|
負公允價值
|
|||||||||||
|
(百萬美元)
|
2019
|
2018
|
2019
|
2018
|
2019
|
2018
|
|||||||
|
遠期外匯匯率合約
|
10 779
|
10 823
|
96
|
130
|
– 75
|
– 58
|
|||||||
|
商品採購合同
|
9
|
|
6
|
|
|
|
|||||||
|
股權證券期權
|
269
|
|
|
|
– 110
|
|
|||||||
|
包括在有價證券和本期金融債務中的衍生金融工具總額
|
11 057
|
10 823
|
102
|
130
|
– 185
|
– 58
|
|||||||
|
2019
|
|||||||||
|
(百萬美元)
|
歐元
|
美元
|
其他
|
總計
|
|||||
|
遠期外匯匯率合約
|
1 373
|
7 760
|
1 646
|
10 779
|
|||||
|
商品採購合同
|
|
9
|
|
9
|
|||||
|
股權證券期權
|
|
250
|
19
|
269
|
|||||
|
衍生金融工具總額
|
1 373
|
8 019
|
1 665
|
11 057
|
|||||
|
2018
|
|||||||||
|
(百萬美元)
|
歐元
|
美元
|
其他
|
總計
|
|||||
|
遠期外匯匯率合約
|
2 989
|
6 558
|
1 276
|
10 823
|
|||||
|
衍生金融工具總額
|
2 989
|
6 558
|
1 276
|
10 823
|
|||||
|
2019
|
|||||||||||
|
(百萬美元) |
1級 |
2級 |
3級 |
價值
攤銷成本 |
總計 |
||||||
|
金融資產
|
|
|
|
|
|
||||||
|
債務證券
|
|
24
|
|
|
24
|
||||||
|
基金投資
|
37
|
|
|
|
37
|
||||||
|
有價證券總額
|
37
|
24
|
|
|
61
|
||||||
|
原到期日超過90天的定期存款和短期投資
|
|
|
|
61
|
61
|
||||||
|
衍生金融工具
|
|
102
|
|
|
102
|
||||||
|
有價證券、定期存款和衍生金融工具共計
|
37
|
126
|
|
61
|
224
|
||||||
|
債務證券和股權證券
|
976
|
|
581
|
|
1 557
|
||||||
|
基金投資
|
|
|
233
|
|
233
|
||||||
|
或有代價應收賬款
|
|
|
399
|
|
399
|
||||||
|
長期貸款、墊款、保證金和其他長期應收款
|
|
|
|
329
|
329
|
||||||
|
金融投資和長期貸款共計
|
976
|
|
1 213
|
329
|
2 518
|
||||||
|
相聯公司按公允價值計入損益
|
|
|
186
|
|
186
|
||||||
|
|
|
|
|
|
|||||||
|
金融負債
|
|
|
|
|
|
||||||
|
或有對價應付款
|
|
|
– 1 036
|
|
– 1 036
|
||||||
|
其他財務負債
|
|
|
– 29
|
|
– 29
|
||||||
|
衍生金融工具
|
|
– 185
|
|
|
– 185
|
||||||
|
按公允價值計算的財務負債總額
|
|
– 185
|
– 1 065
|
|
– 1 250
|
||||||
|
2018
|
|||||||||||
|
(百萬美元) |
1級 |
2級 |
3級 |
價值
攤銷成本 |
總計 |
||||||
|
金融資產
|
|
|
|
|
|
||||||
|
債務證券
|
302
|
23
|
|
|
325
|
||||||
|
基金投資
|
35
|
|
|
|
35
|
||||||
|
有價證券總額
|
337
|
23
|
|
|
360
|
||||||
|
原到期日超過90天的定期存款和短期投資
|
|
|
|
2 087
|
2 087
|
||||||
|
衍生金融工具
|
|
130
|
|
|
130
|
||||||
|
債務證券、定期存款和短期投資的應計利息
|
|
|
|
12
|
12
|
||||||
|
有價證券、定期存款和衍生金融工具共計
|
337
|
153
|
|
2 099
|
2 589
|
||||||
|
債務證券和股權證券
|
698
|
|
488
|
|
1 186
|
||||||
|
基金投資
|
|
|
251
|
|
251
|
||||||
|
或有代價應收賬款
|
|
|
396
|
|
396
|
||||||
|
長期借款、應收客户款項及融資租賃、墊款、保證金
|
|
|
|
512
|
512
|
||||||
|
金融投資和長期貸款共計
|
698
|
|
1 135
|
512
|
2 345
|
||||||
|
相聯公司按公允價值計入損益
|
|
|
145
|
|
145
|
||||||
|
|
|
|
|
|
|||||||
|
金融負債
|
|
|
|
|
|
||||||
|
或有對價應付款
|
|
|
– 907
|
|
– 907
|
||||||
|
其他財務負債
|
|
|
– 10
|
|
– 10
|
||||||
|
衍生金融工具
|
|
– 58
|
|
|
– 58
|
||||||
|
按公允價值計算的財務負債總額
|
|
– 58
|
– 917
|
|
– 975
|
||||||
|
2019
|
||||||||||||||
|
(百萬美元) |
關聯的
公司位於 公允價值至 損益 |
基金 投資 |
長期的 金融 投資 |
或有條件 考慮 應收賬款 |
或有條件 考慮 應付款 |
其他 金融 負債 |
||||||||
|
一月一日
|
145
|
251
|
488
|
396
|
– 907
|
– 10
|
||||||||
|
非連續性業務的影響 1
|
|
– 28
|
– 19
|
|
163
|
|
||||||||
|
公允價值收益及其他調整,包括在綜合收益表中確認的剝離
|
|
12
|
6
|
35
|
195
|
1
|
||||||||
|
公允價值虧損(包括減值, 其他調整 於綜合收益表
|
– 15
|
|
|
|
– 89
|
– 48
|
||||||||
|
綜合全面收益表確認的公允價值調整
|
|
|
– 6
|
|
|
|
||||||||
|
購買
|
49
|
28
|
229
|
|
– 401
|
– 5
|
||||||||
|
現金收支
|
|
|
|
– 32
|
3
|
33
|
||||||||
|
處置
|
– 3
|
– 30
|
– 53
|
|
|
|
||||||||
|
重新分類
|
10
|
|
– 64
|
|
|
|
||||||||
|
12月31日
|
186
|
233
|
581
|
399
|
– 1 036
|
– 29
|
||||||||
|
|
|
|
|
|
|
|||||||||
|
確認的公允價值損益總額 在綜合損益表中, 2019年12月31日持有的負債
|
– 15
|
12
|
6
|
35
|
106
|
– 47
|
||||||||
|
|
||||||||||||||
|
1 附註1、2和30提供了與已終止業務有關的資料。
|
||||||||||||||
|
2018
|
||||||||||||||
|
(百萬美元) |
關聯的
公司位於 公允價值至 損益 |
基金 投資 |
長期的 金融 投資 |
或有條件 考慮 應收賬款 |
或有條件 考慮 應付款 |
其他 金融 負債 |
||||||||
|
一月一日
|
188
|
166
|
437
|
844
|
– 852
|
– 72
|
||||||||
|
公平值收益及其他調整, 包括潛水員公認的 於綜合收益表
|
|
93
|
|
36
|
213
|
|
||||||||
|
公允價值虧損(包括減值, 其他調整 於綜合收益表
|
– 22
|
|
– 5
|
|
– 100
|
|
||||||||
|
綜合全面收益表確認的公允價值調整
|
|
|
– 10
|
|
|
|
||||||||
|
購買
|
24
|
22
|
123
|
|
– 182
|
|
||||||||
|
現金收支
|
|
|
|
– 484
|
11
|
62
|
||||||||
|
處置
|
– 6
|
– 30
|
– 25
|
|
|
|
||||||||
|
與出售集團持有待售有關的應付或有代價
|
|
|
|
|
3
|
|
||||||||
|
重新分類
|
– 39
|
|
– 32
|
|
|
|
||||||||
|
12月31日
|
145
|
251
|
488
|
396
|
– 907
|
– 10
|
||||||||
|
|
|
|
|
|
|
|||||||||
|
截至2018年12月31日的綜合資產負債損益表確認的公允價值損益合計
|
– 22
|
93
|
– 5
|
36
|
113
|
|
||||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
上市股權證券
|
843
|
597
|
|||
|
非上市股權證券
|
315
|
205
|
|||
|
總股本證券
|
1 158
|
802
|
|||
|
|
|||||
|
2019
|
|||||||||||||
|
(百萬美元) |
截止日期為 一個月 |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
截止日期晚於
一年 但不到 五年 |
截止日期為 五年 |
總計 |
|||||||
|
流動資產
|
|
|
|
|
|
|
|||||||
|
原到期日超過90天的有價證券、定期存款和短期投資
|
20
|
26
|
16
|
3
|
57
|
122
|
|||||||
|
商品
|
|
|
|
|
110
|
110
|
|||||||
|
衍生金融工具和應計利息
|
14
|
79
|
3
|
3
|
3
|
102
|
|||||||
|
現金和現金等價物
|
9 712
|
1 400
|
|
|
|
11 112
|
|||||||
|
流動金融資產總額
|
9 746
|
1 505
|
19
|
6
|
170
|
11 446
|
|||||||
|
|
|
|
|
|
|
||||||||
|
非流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
|
|
|
– 9 110
|
– 11 243
|
– 20 353
|
|||||||
|
金融債務--未貼現
|
|
|
|
– 9 150
|
– 11 355
|
– 20 505
|
|||||||
|
非流動金融債務共計
|
|
|
|
– 9 110
|
– 11 243
|
– 20 353
|
|||||||
|
|
|
|
|
|
|
||||||||
|
流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
– 4 243
|
– 1 373
|
– 1 230
|
|
|
– 6 846
|
|||||||
|
金融債務--未貼現
|
– 4 243
|
– 1 373
|
– 1 230
|
|
|
– 6 846
|
|||||||
|
衍生金融工具
|
– 130
|
– 29
|
– 26
|
|
|
– 185
|
|||||||
|
流動金融債務總額
|
– 4 373
|
– 1 402
|
– 1 256
|
|
|
– 7 031
|
|||||||
|
|
|
|
|
|
|
||||||||
|
淨債務
|
5 373
|
103
|
– 1 237
|
– 9 104
|
– 11 073
|
– 15 938
|
|||||||
|
2018
|
|||||||||||||
|
(百萬美元) |
截止日期為 一個月 |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
截止日期晚於
一年 但不到 五年 |
截止日期為 五年 |
總計 |
|||||||
|
流動資產
|
|
|
|
|
|
|
|||||||
|
原到期日超過90天的有價證券、定期存款和短期投資
|
39
|
56
|
2 091
|
198
|
63
|
2 447
|
|||||||
|
商品
|
|
|
|
|
104
|
104
|
|||||||
|
衍生金融工具和應計利息
|
40
|
75
|
27
|
|
|
142
|
|||||||
|
現金和現金等價物
|
3 571
|
9 700
|
|
|
|
13 271
|
|||||||
|
流動金融資產總額
|
3 650
|
9 831
|
2 118
|
198
|
167
|
15 964
|
|||||||
|
|
|
|
|
|
|
||||||||
|
非流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
|
|
|
– 8 980
|
– 13 490
|
– 22 470
|
|||||||
|
金融債務--未貼現
|
|
|
|
– 9 025
|
– 13 623
|
– 22 648
|
|||||||
|
非流動金融債務共計
|
|
|
|
– 8 980
|
– 13 490
|
– 22 470
|
|||||||
|
|
|
|
|
|
|
||||||||
|
流動負債
|
|
|
|
|
|
|
|||||||
|
金融債務
|
– 5 217
|
– 4 084
|
– 319
|
|
|
– 9 620
|
|||||||
|
金融債務--未貼現
|
– 5 217
|
– 4 084
|
– 319
|
|
|
– 9 620
|
|||||||
|
衍生金融工具
|
– 16
|
– 34
|
– 8
|
|
|
– 58
|
|||||||
|
流動金融債務總額
|
– 5 233
|
– 4 118
|
– 327
|
|
|
– 9 678
|
|||||||
|
|
|
|
|
|
|
||||||||
|
淨債務
|
– 1 583
|
5 713
|
1 791
|
– 8 782
|
– 13 323
|
– 16 184
|
|||||||
|
2019
|
|||||||||
|
(百萬美元) |
截止日期為 一個月 |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
|
總計 |
||||
|
衍生金融工具和衍生金融工具的應計利息
|
|
|
|
||||||
|
各種貨幣的潛在資金外流--金融衍生品負債
|
– 814
|
– 4 624
|
– 952
|
– 6 390
|
|||||
|
各種貨幣的潛在流入--來自金融衍生品資產
|
807
|
4 656
|
922
|
6 385
|
|||||
|
2018
|
|||||||||
|
(百萬美元) |
截止日期為 一個月 |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
|
總計 |
||||
|
衍生金融工具和衍生金融工具的應計利息
|
|
|
|
|
|||||
|
各種貨幣的潛在資金外流--金融衍生品負債
|
– 1 305
|
– 2 949
|
– 598
|
– 4 852
|
|||||
|
各種貨幣的潛在流入--來自金融衍生品資產
|
1 328
|
2 974
|
593
|
4 895
|
|||||
|
2019
|
|||||||||||
|
(百萬美元) |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
截止日期晚於
一年 但不到 五年 |
截止日期為 五年 |
總計 |
||||||
|
非流動負債的合同利息
|
– 36
|
– 428
|
– 1 531
|
– 3 439
|
– 5 434
|
||||||
|
租賃負債
|
– 65
|
– 181
|
– 622
|
– 1 081
|
– 1 949
|
||||||
|
貿易應付款
|
– 5 222
|
– 202
|
|
|
– 5 424
|
||||||
|
或有對價負債
|
– 62
|
– 9
|
– 582
|
– 383
|
– 1 036
|
||||||
|
2018
|
|||||||||||
|
(百萬美元) |
截止日期晚於
一個月 但不到 三個月 |
截止日期晚於
三個月 但不到 一年 |
截止日期晚於
一年 但不到 五年 |
截止日期為 五年 |
總計 |
||||||
|
非流動負債的合同利息
|
– 113
|
– 459
|
– 1 667
|
– 3 755
|
– 5 994
|
||||||
|
貿易應付款
|
– 5 556
|
|
|
|
– 5 556
|
||||||
|
或有對價負債
|
|
– 98
|
– 470
|
– 339
|
– 907
|
||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
所有金融工具
|
355
|
337
|
|||
|
按成分分析:
|
|
|
|||
|
對外幣匯率敏感的工具
|
89
|
217
|
|||
|
對股票市場波動敏感的工具
|
31
|
122
|
|||
|
對利率敏感的工具
|
187
|
221
|
|||
|
2019
|
|||||||
|
(百萬美元)
|
平均值
|
高
|
低
|
||||
|
所有金融工具
|
348
|
385
|
303
|
||||
|
按成分分析:
|
|
|
|
||||
|
對外幣匯率敏感的工具
|
143
|
195
|
86
|
||||
|
對股票市場波動敏感的工具
|
36
|
81
|
16
|
||||
|
對利率敏感的工具
|
233
|
303
|
187
|
||||
|
2018
|
|||||||
|
(百萬美元)
|
平均值
|
高
|
低
|
||||
|
所有金融工具
|
443
|
553
|
337
|
||||
|
按成分分析:
|
|
|
|
||||
|
對外幣匯率敏感的工具
|
324
|
473
|
217
|
||||
|
對股票市場波動敏感的工具
|
60
|
122
|
22
|
||||
|
對利率敏感的工具
|
253
|
361
|
169
|
||||
|
(百萬美元)
|
2019 1
|
2018
|
2017
|
||||
|
非持續經營對第三方的淨銷售額
|
1 777
|
7 149
|
6 771
|
||||
|
對持續經營分部的銷售
|
32
|
4
|
3
|
||||
|
來自已終止業務的淨銷售額
|
1 809
|
7 153
|
6 774
|
||||
|
其他收入
|
|
|
3
|
||||
|
銷貨成本
|
– 860
|
– 3 983
|
– 3 588
|
||||
|
非持續經營毛利
|
949
|
3 170
|
3 189
|
||||
|
銷售、一般和行政管理
|
– 638
|
– 2 754
|
– 2 532
|
||||
|
研發
|
– 142
|
– 585
|
– 583
|
||||
|
其他收入
|
15
|
61
|
47
|
||||
|
其他費用
|
– 113
|
– 126
|
– 194
|
||||
|
來自已終止經營業務的營業收入/(虧損)
|
71
|
– 234
|
– 73
|
||||
|
利息支出
|
– 10
|
– 25
|
– 27
|
||||
|
其他財務收支
|
– 3
|
– 1
|
– 3
|
||||
|
來自終止經營業務的税前收入/(虧損)
|
58
|
– 260
|
– 103
|
||||
|
税費
|
– 159
|
74
|
307
|
||||
|
來自已終止經營業務之淨(虧損)╱收入(扣除分派收益前)。 諾華公司股東
|
– 101
|
– 186
|
204
|
||||
|
愛爾康公司向諾華製藥股東分派的收益 2
|
4 691
|
|
|
||||
|
非持續經營的淨收益/(虧損)
|
4 590
|
– 186
|
204
|
||||
|
1 綜合損益表金額為2019年1月1日至分拆完成為止的期間。
|
|||||||
|
2 有關分派Alcon Inc.(“Alcon Inc.”)的不應課税非現金收益的進一步詳情,請參閲附註2。Novartis AG股東
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
利息收入
|
|
2
|
|
||||
|
財產、廠房和設備折舊
|
– 42
|
– 235
|
– 217
|
||||
|
使用權資產折舊 1
|
– 9
|
|
|
||||
|
無形資產攤銷
|
– 174
|
– 1 052
|
– 1 066
|
||||
|
財產、廠房和設備的減值費用
|
|
– 3
|
|
||||
|
無形資產減值準備 2
|
|
– 391
|
– 57
|
||||
|
對重組條款的補充
|
|
– 13
|
– 8
|
||||
|
諾華股權計劃的股權補償
|
– 9
|
– 93
|
– 71
|
||||
|
1 從2019年1月1日起確認的使用權資產折舊,也就是IFRS 16租賃的實施日期。有關其他披露,請參閲注1。
|
|||||||
|
2 2018年包括與CyPass目前上市產品的減記有關的減值3.37億美元,該產品是2016年Alcon Division收購Transcend Medical,Inc.。
|
|||||||
|
(百萬美元)
|
2019
|
2018
|
|||
|
物業、廠房和設備的附加費
|
113
|
519
|
|||
|
對使用權資產的補充 1
|
3
|
|
|||
|
商譽和無形資產的增加
|
36
|
196
|
|||
|
1 2019年1月1日實施IFRS 16租約後,2019年確認的使用權資產的增加。有關其他披露,請參閲注1。
|
|||||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
從可歸因於剝離愛爾康業務的交易費用撥備中支出
|
– 29
|
|
|
||||
|
已剝離現金和現金等價物
|
– 628
|
|
|
||||
|
分拆Alcon業務應佔的現金流量
|
– 657
|
|
|
||||
|
用於投資活動的其他現金流量,淨額
|
– 502
|
– 1 001
|
– 775
|
||||
|
已終止經營業務投資活動所用現金流量淨額
|
– 1 159
|
– 1 001
|
– 775
|
||||
|
2018
|
|||||||||||
|
(百萬美元) |
總計
未來 付款 |
不勞而獲
金融 收入 |
現在時 價值 |
規定 |
上網本 價值 |
||||||
|
不遲於一年 1
|
64
|
– 5
|
59
|
– 2
|
57
|
||||||
|
在一到五年之間
|
117
|
– 9
|
108
|
– 28
|
80
|
||||||
|
晚於五年
|
48
|
– 2
|
46
|
– 35
|
11
|
||||||
|
總計
|
229
|
– 16
|
213
|
– 65
|
148
|
||||||
|
1 最低租賃付款之流動部分記錄於應收貿易賬款或其他流動資產(以未開具發票為限)。
|
|||||||||||
|
(百萬美元)
|
2019
|
||
|
財產、廠房和設備
|
2 858
|
||
|
使用權資產
|
269
|
||
|
商譽
|
8 906
|
||
|
商譽以外的無形資產
|
11 121
|
||
|
遞延税項資產
|
732
|
||
|
金融資產和其他非流動資產
|
526
|
||
|
盤存
|
1 469
|
||
|
應收貿易賬款和其他流動資產
|
1 787
|
||
|
現金和現金等價物
|
628
|
||
|
遞延税項負債
|
– 1 713
|
||
|
流動和非流動租賃負債
|
– 269
|
||
|
經常和非流動金融債務
|
– 3 538
|
||
|
應付貿易賬款、撥備及其他負債
|
– 2 751
|
||
|
取消確認的淨資產
|
20 025
|
||
|
(百萬美元)
|
2019
|
2018
|
2017
|
||||
|
固定繳款計劃的繳款停止運作
|
33
|
104
|
99
|
||||
|
截至2019年12月31日 |
分享
資本 1 |
權益
利息 |
|||||||
|
阿爾及利亞
|
|||||||||
|
SANDOZ公司
|
阿爾及爾
|
DZD
|
650.0
|
m
|
100%
|
||||
|
阿根廷
|
|||||||||
|
諾華阿根廷公司
|
布宜諾斯艾利斯
|
阿爾斯
|
906.1
|
m
|
100%
|
||||
|
澳大利亞
|
|||||||||
|
諾華澳大利亞有限公司
|
麥格理公園,新南威爾士州
|
澳元
|
2
|
|
100%
|
||||
|
諾華製藥澳大利亞有限公司
|
麥格理公園,新南威爾士州
|
澳元
|
3.8
|
m
|
100%
|
||||
|
桑多茲私人有限公司
|
麥格理公園,新南威爾士州
|
澳元
|
11.6
|
m
|
100%
|
||||
|
奧地利
|
|||||||||
|
諾華奧地利有限公司
|
維也納
|
歐元
|
1.0
|
m
|
100%
|
||||
|
Novartis Pharma GmbH
|
維也納
|
歐元
|
1.1
|
m
|
100%
|
||||
|
Sandoz GmbH
|
Kundl
|
歐元
|
32.7
|
m
|
100%
|
||||
|
EBEWE Pharma Ges.m.b.H Nfg. kg
|
阿特湖河畔温特拉赫
|
歐元
|
1.0
|
m
|
100%
|
||||
|
孟加拉國
|
|||||||||
|
諾華(孟加拉國)有限公司
|
加茲浦爾
|
BDT
|
162.5
|
m
|
60%
|
||||
|
比利時
|
|||||||||
|
諾華製藥公司
|
Vilvoorde
|
歐元
|
7.1
|
m
|
100%
|
||||
|
Sandoz NV
|
Vilvoorde
|
歐元
|
19.2
|
m
|
100%
|
||||
|
Alcon - Couvreur NV
|
Puurs
|
歐元
|
110.6
|
m
|
100%
|
||||
|
百慕大羣島
|
|||||||||
|
諾華投資有限公司
|
哈密爾頓 3
|
美元
|
12 000
|
|
100%
|
||||
|
諾華證券投資有限公司
|
哈密爾頓
|
CHF
|
30 000
|
|
100%
|
||||
|
諾華金融服務有限公司
|
哈密爾頓
|
CHF
|
20 000
|
|
100%
|
||||
|
三角國際再保險有限公司
|
哈密爾頓
|
CHF
|
1.0
|
m
|
100%
|
||||
|
三一河保險有限公司。
|
哈密爾頓
|
美元
|
370 000
|
|
100%
|
||||
|
巴西
|
|||||||||
|
諾華生物科技股份有限公司
|
聖保羅
|
BRL
|
265.0
|
m
|
100%
|
||||
|
Sandoz do Brasil Indústria Farmacúutica Ltd.
|
賓夕法尼亞州坎貝
|
BRL
|
190.0
|
m
|
100%
|
||||
|
加拿大
|
|||||||||
|
諾華製藥加拿大公司。
|
魁北克省多瓦爾
|
計算機輔助設計
|
1.2
|
m
|
100%
|
||||
|
Sandoz加拿大公司
|
魁北克省布切維爾
|
計算機輔助設計
|
80.8
|
m
|
100%
|
||||
|
CIBA Vision Canada Inc.
|
安大略省密西索加
|
計算機輔助設計
|
82 886
|
|
100%
|
||||
|
智利
|
|||||||||
|
諾華智利公司
|
智利聖地亞哥
|
中電
|
2.0
|
BN
|
100%
|
||||
|
中國
|
|||||||||
|
北京諾華製藥有限公司公司
|
北京
|
美元
|
30.0
|
m
|
100%
|
||||
|
諾華製藥(香港)有限公司
|
香港
|
港幣
|
200
|
|
100%
|
||||
|
中國諾華生物醫學研究院有限公司公司
|
上海
|
美元
|
320.0
|
m
|
100%
|
||||
|
蘇州諾華科技發展有限公司公司
|
常熟
|
美元
|
12.0
|
m
|
100%
|
||||
|
上海諾華貿易有限公司
|
上海
|
美元
|
3.2
|
m
|
100%
|
||||
|
山德士(中國)製藥有限公司公司
|
中山
|
美元
|
57.6
|
m
|
100%
|
||||
|
哥倫比亞
|
|||||||||
|
哥倫比亞諾華公司
|
桑塔菲德·波哥大
|
科普
|
7.9
|
BN
|
100%
|
||||
|
克羅地亞
|
|||||||||
|
桑多茲·迪奧。印度農家樂
|
薩格勒布
|
HRK
|
25.6
|
m
|
100%
|
||||
|
捷克共和國
|
|||||||||
|
Novartis s.r.o.
|
布拉格
|
捷克ZK
|
51.5
|
m
|
100%
|
||||
|
桑多茲S.r.o。
|
布拉格
|
捷克ZK
|
44.7
|
m
|
100%
|
||||
|
丹麥
|
|||||||||
|
Novartis Healthcare A/S
|
哥本哈根
|
DKK
|
14.0
|
m
|
100%
|
||||
|
桑多茲A/S
|
哥本哈根
|
DKK
|
12.0
|
m
|
100%
|
||||
|
厄瓜多爾
|
|||||||||
|
Novartis Ecuador S.A.
|
基多
|
美元
|
4.0
|
m
|
100%
|
||||
|
埃及
|
|||||||||
|
諾華製藥有限公司
|
開羅
|
埃普
|
193.8
|
m
|
99.77%
|
||||
|
Sandoz Egypt Pharma S.A.E.
|
新開羅市
|
埃普
|
250 000
|
|
100%
|
||||
|
芬蘭
|
|||||||||
|
諾華芬蘭公司
|
埃斯波
|
歐元
|
459 000
|
|
100%
|
||||
|
截至2019年12月31日 |
分享
資本 1 |
權益
利息 |
|||||||
|
法國
|
|||||||||
|
諾華集團法國股份有限公司
|
Rueil-Malmaison
|
歐元
|
903.0
|
m
|
100%
|
||||
|
諾華製藥有限公司
|
Rueil-Malmaison
|
歐元
|
43.4
|
m
|
100%
|
||||
|
Advanced Accelerator Applications S.A.
|
聖熱尼斯-普利
|
歐元
|
9.6
|
m
|
99.2%
|
||||
|
CELLFORCURE
|
Les Ulis
|
歐元
|
4.2
|
m
|
100%
|
||||
|
山德士股份有限公司
|
Levallois—Perret
|
歐元
|
5.4
|
m
|
100%
|
||||
|
德國
|
|||||||||
|
諾華德國有限公司
|
紐倫堡
|
歐元
|
155.5
|
m
|
100%
|
||||
|
Novartis Pharma GmbH
|
紐倫堡
|
歐元
|
25.6
|
m
|
100%
|
||||
|
諾華製藥有限公司
|
韋爾
|
歐元
|
2.0
|
m
|
100%
|
||||
|
諾華製造有限公司
|
馬爾堡
|
歐元
|
25 000
|
|
100%
|
||||
|
Sandoz International GmbH
|
霍爾茨基興
|
歐元
|
100 000
|
|
100%
|
||||
|
1 A Pharma GmbH
|
奧伯哈興
|
歐元
|
26 000
|
|
100%
|
||||
|
HEXAL AG
|
霍爾茨基興
|
歐元
|
93.7
|
m
|
100%
|
||||
|
Salutas Pharma GmbH
|
巴勒本
|
歐元
|
42.1
|
m
|
100%
|
||||
|
Aeropharm GmbH
|
魯道夫施塔特
|
歐元
|
26 000
|
|
100%
|
||||
|
希臘
|
|||||||||
|
諾華(希臘)S.A.C.I.
|
《變形記》/雅典
|
歐元
|
23.4
|
m
|
100%
|
||||
|
匈牙利
|
|||||||||
|
諾華匈牙利醫療保健有限責任公司
|
布達佩斯
|
HUF
|
545.6
|
m
|
100%
|
||||
|
匈牙利山德士有限責任公司
|
布達佩斯
|
HUF
|
883.0
|
m
|
100%
|
||||
|
印度
|
|||||||||
|
諾華印度有限公司
|
孟買
|
INR
|
123.5
|
m
|
70.68%
|
||||
|
諾華醫療私人有限公司
|
孟買
|
INR
|
60.0
|
m
|
100%
|
||||
|
Sandoz Private Limited
|
孟買
|
INR
|
32.0
|
m
|
100%
|
||||
|
印度尼西亞
|
|||||||||
|
PT.諾華印尼公司
|
雅加達
|
IDR
|
7.7
|
BN
|
100%
|
||||
|
愛爾蘭
|
|||||||||
|
諾華愛爾蘭有限公司
|
都柏林
|
歐元
|
25 000
|
|
100%
|
||||
|
Novartis Ringaskiddy Limited
|
林加斯基迪
|
歐元
|
2.0
|
m
|
100%
|
||||
|
以色列
|
|||||||||
|
諾華以色列有限公司
|
特拉維夫
|
ILS
|
1 000
|
|
100%
|
||||
|
意大利
|
|||||||||
|
諾華製藥公司
|
奧利焦
|
歐元
|
18.2
|
m
|
100%
|
||||
|
Advanced Accelerator Applications(Italy)S.r.l.
|
波齊利
|
歐元
|
119 000
|
|
99.2%
|
||||
|
Sandoz S.p.A.
|
奧利焦
|
歐元
|
1.7
|
m
|
100%
|
||||
|
日本
|
|||||||||
|
諾華控股日本公司
|
東京
|
日元
|
10.0
|
m
|
100%
|
||||
|
諾華製藥公司
|
東京
|
日元
|
6.0
|
BN
|
100%
|
||||
|
汽巴-蓋基日本有限公司
|
東京
|
日元
|
8.5
|
m
|
100%
|
||||
|
山德士K.K.
|
東京
|
日元
|
100.0
|
m
|
100%
|
||||
|
拉脱維亞
|
|||||||||
|
諾華波羅的海新航
|
里加
|
歐元
|
3.0
|
m
|
100%
|
||||
|
盧森堡
|
|||||||||
|
諾華投資股份有限公司
|
盧森堡市
|
美元
|
100.0
|
m
|
100%
|
||||
|
諾華財務公司
|
盧森堡市
|
美元
|
100 000
|
|
100%
|
||||
|
馬來西亞
|
|||||||||
|
諾華公司(馬來西亞)有限公司巴赫德。
|
吉隆坡
|
麥爾
|
3.3
|
m
|
100%
|
||||
|
墨西哥
|
|||||||||
|
諾華公司,S.A.de C.V.
|
墨西哥城
|
MXN
|
205.0
|
m
|
100%
|
||||
|
Sandoz,S.A. de C.V.
|
墨西哥城
|
MXN
|
468.2
|
m
|
100%
|
||||
|
摩洛哥
|
|||||||||
|
諾華製藥公司Maroc SA
|
卡薩布蘭卡
|
瘋了
|
80.0
|
m
|
100%
|
||||
|
荷蘭
|
|||||||||
|
諾華荷蘭公司
|
阿姆斯特丹
|
歐元
|
1.4
|
m
|
100%
|
||||
|
諾華製藥公司
|
阿姆斯特丹
|
歐元
|
4.5
|
m
|
100%
|
||||
|
IDB荷蘭BV
|
巴勒-拿騷
|
歐元
|
18 000
|
|
99.2%
|
||||
|
山德士公司
|
阿爾梅勒
|
歐元
|
907 560
|
|
100%
|
||||
|
新西蘭
|
|||||||||
|
諾華新西蘭有限公司
|
奧克蘭
|
NZD
|
820 000
|
|
100%
|
||||
|
截至2019年12月31日 |
分享
資本 1 |
權益
利息 |
|||||||
|
挪威
|
|||||||||
|
諾華公司作為
|
奧斯陸
|
諾克
|
1.5
|
m
|
100%
|
||||
|
巴基斯坦
|
|||||||||
|
諾華製藥(巴基斯坦)有限公司
|
卡拉奇
|
PKR
|
6.7
|
BN
|
99.99%
|
||||
|
巴拿馬
|
|||||||||
|
諾華製藥(物流)公司
|
巴拿馬城
|
美元
|
10 000
|
|
100%
|
||||
|
祕魯
|
|||||||||
|
諾華生物科學祕魯有限公司
|
利馬
|
鋼筆
|
6.1
|
m
|
100%
|
||||
|
菲律賓
|
|||||||||
|
諾華菲律賓醫療保健公司。
|
馬卡蒂市
|
PHP
|
298.8
|
m
|
100%
|
||||
|
菲律賓山德士公司
|
馬卡蒂市
|
PHP
|
30.0
|
m
|
100%
|
||||
|
波蘭
|
|||||||||
|
諾華波蘭公司ZO.O。
|
華沙
|
PLN
|
44.2
|
m
|
100%
|
||||
|
Sandoz Polska Sp. z o.o.
|
華沙
|
PLN
|
25.6
|
m
|
100%
|
||||
|
Lek S.A.
|
斯特雷庫夫
|
PLN
|
11.4
|
m
|
100%
|
||||
|
葡萄牙
|
|||||||||
|
諾華葡萄牙SGPS Lda.
|
薩爾沃港
|
歐元
|
500 000
|
|
100%
|
||||
|
Novartis Farma—Produtos Farmacêuticos S.A.
|
薩爾沃港
|
歐元
|
2.4
|
m
|
100%
|
||||
|
桑多茲農場公司
|
薩爾沃港
|
歐元
|
499 900
|
|
100%
|
||||
|
羅馬尼亞
|
|||||||||
|
諾華製藥服務羅馬尼亞公司
|
布加勒斯特
|
羅恩
|
3.0
|
m
|
100%
|
||||
|
Sandoz S.R.L.
|
Targu-Mures
|
羅恩
|
105.2
|
m
|
100%
|
||||
|
俄羅斯聯邦
|
|||||||||
|
諾華製藥有限公司
|
莫斯科
|
擦,擦
|
20.0
|
m
|
100%
|
||||
|
諾華Neva有限責任公司
|
聖彼得堡
|
擦,擦
|
500.0
|
m
|
100%
|
||||
|
趙三都士
|
莫斯科
|
擦,擦
|
57.4
|
m
|
100%
|
||||
|
沙特阿拉伯
|
|||||||||
|
諾華沙特有限公司
|
利雅得
|
撒爾
|
26.8
|
m
|
75%
|
||||
|
新加坡
|
|||||||||
|
諾華(新加坡)私人有限公司
|
新加坡
|
SGD
|
100 000
|
|
100%
|
||||
|
諾華新加坡製藥私人有限公司
|
新加坡
|
SGD
|
45.0
|
m
|
100%
|
||||
|
諾華亞太製藥有限公司
|
新加坡
|
SGD
|
39.0
|
m
|
100%
|
||||
|
斯洛伐克
|
|||||||||
|
諾華公司斯洛伐克公司。
|
布拉迪斯拉發
|
歐元
|
2.0
|
m
|
100%
|
||||
|
斯洛文尼亞
|
|||||||||
|
Lek Pharmaceuticals d.d.
|
盧布爾雅那
|
歐元
|
48.4
|
m
|
100%
|
||||
|
Sandoz Pharmaceuticals d.d.
|
盧布爾雅那
|
歐元
|
1.5
|
m
|
100%
|
||||
|
南非
|
|||||||||
|
諾華南非(私人)有限公司
|
米德蘭德
|
扎爾
|
86.3
|
m
|
100%
|
||||
|
Sandoz南非(Pty)Ltd
|
Kempton Park
|
扎爾
|
3.0
|
m
|
100%
|
||||
|
韓國
|
|||||||||
|
諾華韓國有限公司
|
首爾
|
KRW
|
24.5
|
BN
|
98.55%
|
||||
|
西班牙
|
|||||||||
|
諾華FarmacéUtica,S.A.
|
巴塞羅那
|
歐元
|
63.0
|
m
|
100%
|
||||
|
高級加速器應用程序伊比利亞,S.L.U。
|
埃斯普古斯·德·洛貝雷加特
|
歐元
|
22.6
|
m
|
99.2%
|
||||
|
Sandoz Farmacéutica股份有限公司
|
馬德里
|
歐元
|
270 450
|
|
100%
|
||||
|
山德士工業產品有限公司
|
Les Franqueses del Vallés/巴塞羅那
|
歐元
|
9.3
|
m
|
100%
|
||||
|
Alcon Cusi S.A.
|
El Masnou/巴塞羅那
|
歐元
|
10.1
|
m
|
100%
|
||||
|
Abadia Retuerta S.A.
|
薩隆·德·杜埃羅/巴拉多利德
|
歐元
|
6.0
|
m
|
100%
|
||||
|
瑞典
|
|||||||||
|
諾華Sverige AB
|
斯德哥爾摩
|
塞克
|
5.0
|
m
|
100%
|
||||
|
瑞士
|
|||||||||
|
諾華國際公司
|
巴塞爾
|
CHF
|
10.0
|
m
|
100%
|
||||
|
諾華控股公司
|
巴塞爾 3
|
CHF
|
100.2
|
m
|
100%
|
||||
|
諾華國際製藥投資公司
|
巴塞爾
|
CHF
|
100 000
|
|
100%
|
||||
|
諾華生物風險投資公司
|
巴塞爾
|
CHF
|
100 000
|
|
100%
|
||||
|
諾華福爾施蒂夫通
|
巴塞爾
|
--
|
--
|
|
100%
|
||||
|
諾華Stiftung für Kaderosbildung
|
巴塞爾
|
--
|
--
|
|
100%
|
||||
|
諾華-米塔貝特公司
|
巴塞爾
|
--
|
--
|
|
100%
|
||||
|
諾華Stiftung für Mensch和Umwell
|
巴塞爾
|
--
|
--
|
|
100%
|
||||
|
Stiftung der Novartis AG für Erziehung,Ausbildung und Bildung
|
巴塞爾
|
--
|
--
|
|
100%
|
||||
|
諾華海外投資公司
|
巴塞爾
|
CHF
|
1.0
|
m
|
100%
|
||||
|
日本股份公司
|
巴塞爾
|
CHF
|
50 000
|
|
100%
|
||||
|
諾華製藥公司
|
巴塞爾 3
|
CHF
|
350.0
|
m
|
100%
|
||||
|
諾華國際製藥公司
|
巴塞爾 3
|
CHF
|
100 000
|
|
100%
|
||||
|
諾華製藥服務公司
|
巴塞爾
|
CHF
|
20.0
|
m
|
100%
|
||||
|
諾華製藥Schweizerhalle AG
|
穆滕茨
|
CHF
|
18.9
|
m
|
100%
|
||||
|
諾華製藥公司
|
斯坦
|
CHF
|
251 000
|
|
100%
|
||||
|
諾華製藥公司
|
裏希
|
CHF
|
5.0
|
m
|
100%
|
||||
|
諾華眼科公司
|
弗裏堡
|
CHF
|
100 000
|
|
100%
|
||||
|
高級加速器應用國際公司
|
日內瓦
|
CHF
|
9.3
|
m
|
99.2%
|
||||
|
Sandoz股份公司
|
巴塞爾
|
CHF
|
5.0
|
m
|
100%
|
||||
|
Sandoz製藥公司
|
裏希
|
CHF
|
100 000
|
|
100%
|
||||
|
羅氏控股公司
|
巴塞爾
|
CHF
|
160.0
|
m
|
33/6 2
|
||||
|
截至2019年12月31日 |
分享
資本 1 |
權益
利息 |
|||||||
|
臺灣
|
|||||||||
|
諾華(臺灣)有限公司
|
臺北
|
臺幣
|
170.0
|
m
|
100%
|
||||
|
泰國
|
|||||||||
|
諾華(泰國)有限公司
|
曼谷
|
THB
|
302.0
|
m
|
100%
|
||||
|
土耳其
|
|||||||||
|
Novartis Saglik,Gida ve Tarim Ürünleri Sanayi ve Ticaret A.S.
|
伊斯坦布爾
|
試試看
|
98.0
|
m
|
100%
|
||||
|
Farmanova Saglik Hizmetleri Ltd.STI.
|
伊斯坦布爾
|
試試看
|
6.7
|
m
|
100%
|
||||
|
Sandoz IlaçSanayi ve Ticaret A.S.
|
伊斯坦布爾
|
試試看
|
165.2
|
m
|
99.99%
|
||||
|
Sandoz Grup Saglik Ürünleri Ilaçlari Sanayi ve Ticaret A.S.
|
格布茲-科卡埃利
|
試試看
|
50.0
|
m
|
100%
|
||||
|
烏克蘭
|
|||||||||
|
Sandoz烏克蘭有限責任公司
|
基輔
|
UAH
|
8.0
|
m
|
100%
|
||||
|
阿拉伯聯合酋長國
|
|||||||||
|
諾華中東FZE
|
迪拜
|
AED
|
7.0
|
m
|
100%
|
||||
|
英國
|
|||||||||
|
諾華英國有限公司
|
倫敦
|
英鎊
|
25.5
|
m
|
100%
|
||||
|
諾華製藥英國有限公司
|
倫敦
|
英鎊
|
5.4
|
m
|
100%
|
||||
|
諾華格里姆斯比有限公司
|
倫敦
|
英鎊
|
250.0
|
m
|
100%
|
||||
|
影像設備有限公司
|
倫敦
|
英鎊
|
100
|
|
99.2%
|
||||
|
Vivacta Limited
|
弗裏姆利/坎伯利
|
英鎊
|
2.9
|
m
|
100.0%
|
||||
|
Ziarco Group Limited
|
倫敦
|
英鎊
|
3 904
|
|
100%
|
||||
|
Sandoz Limited
|
弗裏姆利/坎伯利
|
英鎊
|
2.0
|
m
|
100%
|
||||
|
美利堅合眾國
|
|||||||||
|
諾華公司
|
East Hanover,NJ
|
美元
|
72.2
|
m
|
100%
|
||||
|
諾華金融公司
|
East Hanover,NJ 3
|
美元
|
1 000
|
|
100%
|
||||
|
諾華資本公司
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
Novartis Services,Inc.
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
諾華美國基金會
|
East Hanover,NJ
|
--
|
--
|
|
100%
|
||||
|
諾華製藥公司
|
East Hanover,NJ
|
美元
|
650
|
|
100%
|
||||
|
Advanced Accelerator Applications USA,Inc.
|
新澤西州米爾本
|
美元
|
1
|
|
99.2%
|
||||
|
AveXis公司
|
Bannockburn,IL
|
美元
|
1
|
|
100%
|
||||
|
Novartis Inflamasome Research,Inc.
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
諾華技術有限責任公司
|
East Hanover,NJ
|
--
|
--
|
|
100%
|
||||
|
諾華生物醫學研究所
|
馬薩諸塞州劍橋
|
美元
|
1
|
|
100%
|
||||
|
CoStim Pharmaceuticals Inc
|
馬薩諸塞州劍橋
|
美元
|
1
|
|
100%
|
||||
|
Encore Vision,Inc.
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
Endocyte公司
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
導航生物製藥服務公司。
|
加利福尼亞州卡爾斯巴德
|
美元
|
1
|
|
100%
|
||||
|
Reprixys製藥公司
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
Spinifex製藥公司
|
East Hanover,NJ
|
美元
|
1
|
|
100%
|
||||
|
Novartis Institute for Functional Genomics,Inc.
|
加利福尼亞州聖地亞哥
|
美元
|
1 000
|
|
100%
|
||||
|
Sandoz Inc.
|
新澤西州普林斯頓
|
美元
|
25 000
|
|
100%
|
||||
|
Oriel Therapeutics公司
|
北卡羅來納州達勒姆
|
美元
|
1
|
|
100%
|
||||
|
富格拉制藥公司
|
紐約州梅爾維爾
|
美元
|
1
|
|
100%
|
||||
|
Eon Labs,Inc.
|
新澤西州普林斯頓
|
美元
|
1
|
|
100%
|
||||
|
Novartis Vaccines and Diagnostics,Inc.
|
East Hanover,NJ
|
美元
|
3
|
|
100%
|
||||
|
委內瑞拉
|
|||||||||
|
委內瑞拉諾華製藥公司
|
加拉加斯
|
VES
|
14
|
|
100%
|
||||
|
此外,本集團在以下國家的子公司和聯營公司的總資產或淨銷售額低於2500萬美元:波斯尼亞/黑塞哥維那、保加利亞、多米尼加共和國、危地馬拉、肯尼亞、北馬其頓、尼日利亞、波多黎各、烏拉圭和越南
|
|||||||||
|
1 股本可以不反映應納税股本,也不包括任何實收盈餘。
|
|||||||||
|
2 約33%的有表決權股份;約6%的淨收入和諾華應佔權益。
|
|||||||||
|
3 美國證券交易委員會規則下的重要附屬公司S-X規則1-02(W)
|
|||||||||
|
M=百萬;BN=十億
|
|||||||||
獨立註冊會計師事務所報告