附錄 99.1
附錄 99.1
 附錄 99.1
附錄 99.1
EyePoint Pharmaceuticals公佈了2023年第四季度和全年財務業績,並重點介紹了最近的公司發展
馬薩諸塞州沃特敦,2024年3月7日(環球新聞專線)——致力於開發和商業化改善嚴重視網膜疾病患者生活的療法的公司EyePoint製藥公司(納斯達克股票代碼:EYPT)今天公佈了截至2023年12月31日的第四季度和年度的財務業績,並重點介紹了最近的公司發展。
“對於EyePoint製藥而言,2023年是非凡的執行和業績。EyePoint Pharmicals總裁兼首席執行官傑伊·杜克醫學博士、醫學博士傑伊·杜克説,這些亮點包括我們在濕式AMD中進行的 EYP-1901 二期DAVIO 2期試驗的積極數據、我們正在進行的NPDR和DME的2期試驗的持續進展,以及12月的2.3億美元超額認購融資強化了我們的資產負債表,以及去年5月以8,250萬美元外加未來特許權使用費的價格出售了YUTIQ® 的版權。“EYP-1901 的 DAVIO 2 臨牀試驗實現了所有主要和次要終點,凸顯了其成為濕性 AMD 患者改變模式的維持治療的潛力。我們期待在計劃於今年4月結束的第二階段會議上與美國食品藥品監督管理局(FDA)討論我們的第三階段計劃,並在今年下半年啟動第一項關鍵試驗。”
杜克博士繼續説:“我們預計,針對中度重度至重度非增殖性糖尿病視網膜病變(NPDR)的 EYP-1901 二期 PAVIA 臨牀試驗的關鍵數據將在2024年第二季度公佈。我們對 EYP-1901 在 NPDR 中的潛力感到興奮。NPDR 是一種慢性病,目前超過 90% 的患者在出現威脅視力的併發症之前不接受任何療程。2024
 附錄 99.1
附錄 99.1
隨着我們繼續通過這三個非常重要的適應症的臨牀開發,推進 EYP-1901 的發展,這有望成為又一個變革性的一年。”
研發亮點和更新
近期企業要聞
截至2023年12月31日的第四季度業績回顧
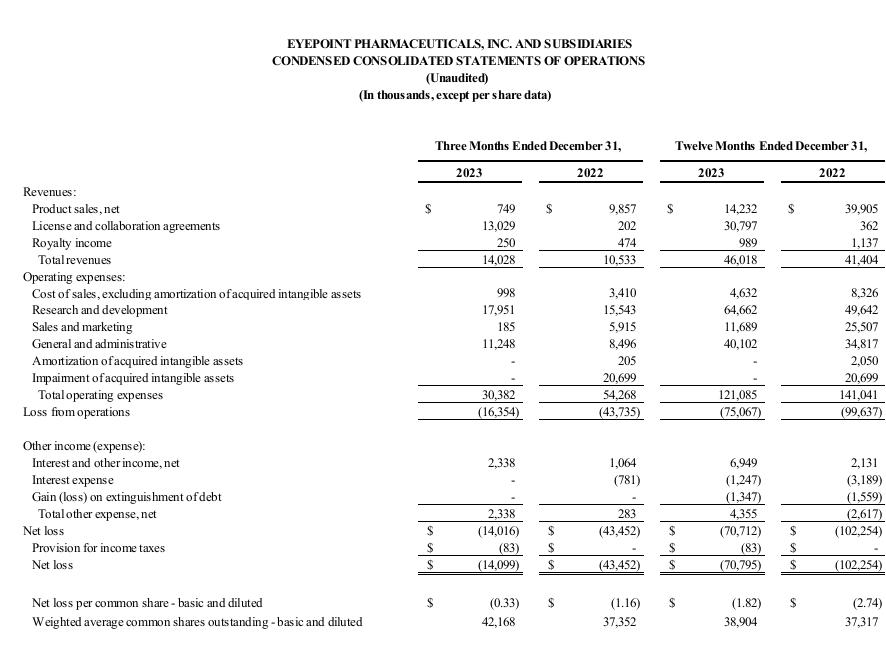
截至2023年12月31日的季度,總淨收入為1,400萬美元,而截至2022年12月31日的季度為1,050萬美元。截至2023年12月31日的季度淨產品收入為70萬美元,而截至2022年12月31日的季度淨產品收入為990萬美元。淨產品收入的下降是由於我們的商業業務在2023年上半年戰略退出所致。
截至2023年12月31日的季度,特許權使用費和合作淨收入總額為1,330萬美元,而2022年同期為70萬美元。增長的主要原因是部分確認了YUTIQ特許經營許可的遞延收入,從2023年第二季度開始,將在2年內確認與YUTIQ供應單位的交付相關的遞延收入。
 附錄 99.1
附錄 99.1
截至2023年12月31日的季度的運營支出總額為3,040萬美元,而去年同期為5,430萬美元。這一下降主要是由我們在2023年上半年從商業業務中戰略退出以及2022年第四季度的一次性無形資產減值費用推動的。
淨非營業收入總額為230萬美元,淨虧損為1,410萬美元,合每股虧損0.33美元,而去年同期的淨虧損為4,350萬美元,合每股虧損1.16美元。
截至2023年12月31日的全年業績回顧
截至2023年12月31日的全年總淨收入為4,600萬美元,而截至2022年12月31日的全年淨收入為4,140萬美元。截至2023年12月31日的全年淨產品收入為1,420萬美元,而截至2022年12月31日的全年淨產品收入為3,990萬美元。淨產品收入的下降是由於該公司在2023年上半年戰略退出其商業業務。
截至2023年12月31日的全年特許權使用費和合作淨收入總額為3180萬美元,而2022年同期為150萬美元。
截至2023年12月31日的全年運營支出總額為1.211億美元,而去年同期為1.41億美元。這一下降主要是由我們在2023年上半年從商業業務中戰略退出以及2022年第四季度的一次性無形資產減值費用推動的。
淨非營業支出總額為440萬美元,淨虧損為7,080萬美元,合每股虧損1.82美元,而去年同期的淨虧損為1.023億美元,合每股虧損2.74美元。
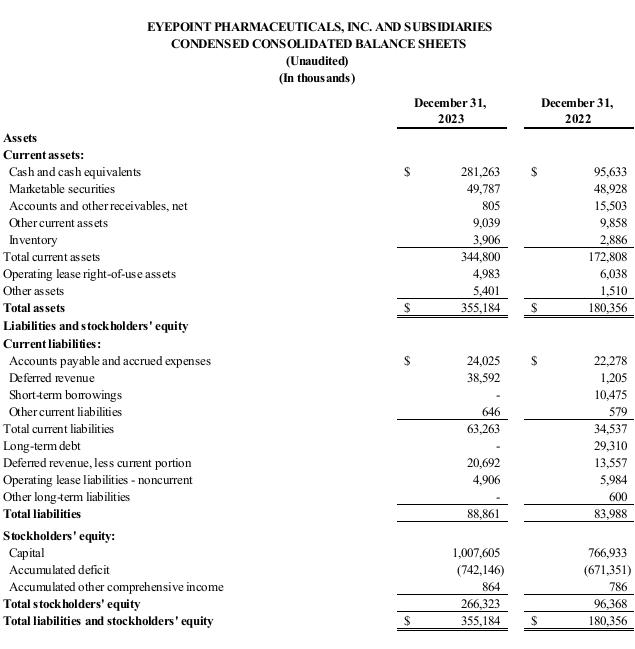
截至2023年12月31日,現金、現金等價物和有價證券投資總額為3.311億美元,而截至2022年12月31日為1.446億美元。
財務展望
我們預計,我們在2023年12月31日的現金、現金等價物和投資將使我們能夠通過計劃於2026年針對濕性AMD進行的 EYP-1901 3期臨牀試驗的收入數據為運營提供資金。
電話會議信息
EyePoint將於美國東部時間今天上午8點30分舉行電話會議,討論截至2023年12月31日的第四季度和年度的業績以及最近的公司發展。要觀看電話會議直播,請在以下地址註冊 https://register.vevent.com/register/BI91be5d0e320646e887cf4047c70fe73c。該活動的網絡直播可通過公司網站的 “投資者” 部分觀看 www.eyepointpharma.com。電話會議結束後,公司網站上還將提供網絡直播重播。
關於 EyePoint 制
EyePoint 製藥公司(納斯達克股票代碼:EYPT)是一家臨牀階段的生物製藥公司,致力於開發和商業化療法,以幫助改善嚴重視網膜疾病患者的生活。該公司的產品線利用其專有的可生物腐蝕的Durasert E技術實現持續的眼內藥物輸送。該公司的主要候選產品 EYP-1901 是一種研究性持續給藥療法,用於治療血管內皮生長因子介導的視網膜疾病,vorolanib(一種受專利保護的選擇性酪氨酸激酶抑制劑)與 Durasert E 結合使用。正在研發的項目包括 EYP-2301,一種前景看好的 TIE-2 激動劑,razuprotafib,f/k/a AKB-9778,採用杜拉塞特 E 配製,有可能改善嚴重視網膜疾病的預後。久經考驗的 Durasert® 藥物遞送技術
 附錄 99.1
附錄 99.1
已使用四種美國食品藥品管理局批准的產品安全地注射到數千名患者眼中。EyePoint 製藥公司總部位於馬薩諸塞州沃特敦。
Vorolanib由貝達製藥的子公司Equinox Sciences獨家授權給EyePoint,用於對中國、澳門、香港和臺灣以外的所有眼科疾病進行本地化治療。
EYEPOINT PHARMICALS根據1995年《私人證券訴訟法》發表的安全港聲明:如果本新聞稿中的任何陳述涉及非歷史信息,則這些陳述均為1995年《私人證券訴訟改革法》下的前瞻性陳述。此類聲明包括但不限於關於將收益用於發行的聲明以及其他以 “將”、“潛在”、“可以”、“可以”、“相信”、“打算”、“繼續”、“計劃”、“期望”、“預期”、“估計”、“可能” 等詞語標識的聲明,或使用未來日期。就其性質而言,前瞻性陳述涉及不同程度的不確定性問題。不確定性和風險可能導致EyePoint的實際業績與EyePoint的前瞻性陳述中表達或暗示的業績存在重大差異。對於 EyePoint 而言,這包括有關我們的候選產品(包括 EYP-1901 和 EYP-2301)的時機和臨牀開發的不確定性;EYP-1901 作為嚴重眼部疾病的新型持續療法的可能性,包括濕性年齡相關性黃斑變性(濕性 AMD)和非增殖性糖尿病視網膜病變(NPDR)和糖尿病黃斑水腫(DME);臨牀試驗的有效性和及時性以及數據的實用性;監管批准的及時性,包括潛在的美國食品藥品監督管理局(FDA)EYP-1901 和 EYP-2301 的監管批准;當前和未來許可協議的成功;我們對合同研究機構、聯合推廣合作伙伴以及其他外部供應商和服務提供商的依賴;Durasert® 作為藥物交付平臺在 FDA 批准產品中的成功;產品責任;行業整合;遵守環境法;國際業務運營的風險和成本;股價波動;可能的稀釋;沒有股息;總體商業和經濟狀況的影響;保護我們的知識產權和避免知識產權侵權;留住關鍵人員;製造風險;以及我們在向美國證券交易委員會提交的文件中描述的其他因素。我們無法保證任何前瞻性陳述中表達、預期或暗示的結果和其他預期能夠實現。包括這些風險在內的各種因素可能導致我們的實際業績和其他預期與前瞻性陳述中表達、預期或暗示的預期業績或其他預期存在重大差異。如果已知或未知風險出現,或者基本假設被證明不準確,則實際結果可能與過去的業績以及前瞻性陳述中的預期、估計或預測結果存在重大差異。在考慮任何前瞻性陳述時,應牢記這一點。我們的前瞻性陳述僅代表其發表之日。EyePoint沒有義務更新或修改任何前瞻性陳述,無論是由於新信息、未來事件還是其他原因。
投資者:
克里斯蒂娜·塔塔利亞
Stern IR
直接:212-698-8700
christina.tartaglia@sternir.com
 附錄 99.1
附錄 99.1
媒體聯繫人:
艾米菲利普
綠色房間通信
直播:412-327-9499
aphillips@greenroompr.com
 附錄 99.1
附錄 99.1
 附錄 99.1
附錄 99.1