

附錄 99.1 neffy 2024 年 3 月 7 日投資者日

前瞻性陳述本演示文稿中不純屬歷史性質的陳述是 1995 年《私人證券訴訟改革法》所指的 “前瞻性陳述”。本演示文稿中的前瞻性陳述包括但不限於以下方面的陳述: ARS Pharma計劃在2024年第二季度初提交保密協議,預計PDUFA的行動日期,如果獲得批准,將在2024年下半年推出neffy;EMA做出決定和向其他外國 監管機構提交報告的時機;neffy的潛在市場、需求和擴張機會;ARS Pharma的預期競爭地位;是否結果足以證明 neffy 至少與 neffy 一樣有效可注射的 腎上腺素;美國以外地區的潛在監管申請、批准和商業化的時間表;ARS Pharma的營銷和商業化戰略,包括在外國司法管轄區的潛在合作伙伴關係; 如果獲得批准,neffy的潛在好處,包括醫生開納菲處方以及過敏患者和護理人員選擇攜帶和服用neffy的劑量的可能性;預期的 neffy 獲得了 的保障,包括對 80% 的商業廣告的無限制上市後一年之內有效;ARS Pharma的預期現金、現金等價物和短期投資在將來獲得批准和推出neffy後;ARS Pharma銷售隊伍的預期規模、 構成和覆蓋範圍;NeffyExperience和NeffyConnect的可用性和功能;預期的定價和共付額收購;未來研究和商業化的預期時間和成本 及其對運營的影響;ARS Pharma的預計運營軌道;預期的知識產權保護;以及任何上述任何一項所依據的假設陳述。這些前瞻性陳述 受1995年《私人證券訴訟改革法》的安全港條款的約束。由於此類陳述受風險和不確定性的影響,因此實際結果可能與此類前瞻性 陳述所表達或暗示的結果存在重大差異。諸如 “預期”、“可能”、“演示”、“期望”、“表明”、“可能”、“計劃”、“潛力”、“將” 等詞語以及類似的 表述旨在識別前瞻性陳述。這些前瞻性陳述基於ARS Pharma當前的預期,涉及可能永遠無法實現或可能被證明不正確的假設。由於各種風險和不確定性,實際結果 和事件發生時間可能與此類前瞻性陳述中的預期存在重大差異,其中包括但不限於:由於 ARS Pharma無法控制的各種因素,PDUFA的目標行動日期可能會進一步推遲;neffy獲得和維持監管部門批准的能力;新臨牀試驗的結果可能不支持neffy的批准;臨牀試驗的結果可能不是表示將來可能觀察到的 結果;潛力neffy 的安全性和其他併發症;neffy 的標籤(如果獲得批准);neffy 開發和商業化的範圍、進展和擴展;付款人推遲、限制 或拒絕為 neffy 提供保險的可能性;市場規模和增長以及市場對肌肉注射劑產品的接受率和程度;ARS Pharma 保護其知識產權地位的能力; 相關的不確定性資本要求;以及政府法律法規的影響。ARS Pharma於2023年11月9日向美國證券交易委員會(“SEC”)提交的截至2023年9月30日的季度10-Q表季度報告中的 “風險因素” 標題下包含了可能導致實際結果和結果與前瞻性 陳述中設想的重大差異的其他風險和不確定性。也可以在ARS Pharma的網站ir.ars-pharma.com上單擊 “投資者與媒體” 選項卡下的 “財務與申報” 鏈接,訪問ARS Pharma向美國證券交易委員會提交的本文件和其他文件。 本演示文稿中包含的前瞻性陳述僅在發佈之日作出。除非法律要求,否則ARS Pharma不承擔任何義務,也不打算更新這些前瞻性陳述。

今天的演講嘉賓 ARS 管理層主要意見領袖理查德 Lowenthal,理學碩士,MSEL Jonathan Spergel,醫學博士,首席執行官,過敏項目聯合創始人帶領美國食品藥品管理局批准了多款費城兒童醫院鼻腔噴霧劑產品 25 年以上的經驗 Eric Karas Thomas B. Casale,醫學博士® 醫學和兒科教授領導納肯商業運營首席運營官過敏與免疫學應急/適應和輔助專業南佛羅裏達大學 25 年以上的經驗 3

改變I型過敏反應治療方法的潛力 • neffy®:第一種針對I型過敏反應的潛在的 “無針,不注射” 解決方案,以滿足未滿足的市場需求 • 註冊計劃顯示出可比的PK和PD,沒有與針頭相關的安全問題、恐懼和猶豫的風險 • 即使在給藥 neffy 1 分鐘後,也觀察到對PD替代品(SBP,HR)的快速且具有統計學意義的反應與注射相比 • 顛覆當前腎上腺素 注射劑市場的重大機遇 • 已完成重複美國食品藥品管理局於2023年9月要求進行劑量NAC研究 CRL • 保密協議有望在2024年第二季度初對FDA CRL做出迴應,美國食品藥品管理局的行動日期和2024年下半年可能在美國上市 • 受HCP和消費者偏好和採用的推動,潛在的數十億美元市場•至少在2038年之前具有類似NCE的知識產權獨家經營潛力 • 截至2023年12月31日,現金和短期投資為2.28億美元,預計為1.95億美元預計 FDA 將在 2024 年下半年採取行動 4

我們今天將涵蓋的內容 I 型過敏反應 中未滿足的需求 包括過敏反應 Jonathan Spergel neffy 博士臨牀概況、註冊研究 Richard Lowenthal neffy 包括過敏反應在內的益處-風險 Thomas Casale 博士美國市場機會和商業化戰略 Eric Karas 5

未滿足的需求/當前的挑戰絕大多數 I 型過敏患者 在當前的治療方案中面臨重大侷限性沒有治療拒絕延遲用户錯誤問題可用的治療在治療中只有 10%-20% ~ 40%-60% 的患者攜帶約 25%-60% 不是 23%-35% 不能 活性 2 7 ( 患者

2024 年 neffy 的重要催化劑 o 美國保密協議在 2024 年第二季度初對 CRL 作出迴應 FDA o PDUFA 的行動日期預計在 2024 年下半年 o EMA 決定(CHMP 意見)預計在 2024 年年中期提交 o 日本保密協議預計在 2024 年年提交 o 計劃在其他主要的除美國 地區提交申請 o 擴張機會 • 第二階段慢性烏爾都的積極數據 2024 年 2 月公佈的麻疹研究 • 2b 期門診蕁麻疹研究啟動 7

I 型過敏和未滿足的需求 Jonathan M. Spergel,醫學博士,博士 兒科教授費城兒童醫院過敏項目主任

I 型過敏反應:全身性超敏反應 每年有超過 500,000 次急診就診約 4,000 萬人由於全身 I 型過敏 1 2 反應,對過敏原的反應平均每次造成 1600 美元以上。其他 I 型過敏症狀顯著 合併症和症狀由暴露於特定過敏原(例如蕁麻疹發作)引起,最常見的是影響生活質量。食物、毒液、藥物參考文獻:1.卡里洛-馬丁一世等2020 年 J Allergy Clin Immunol Pract。2.BlueCross 美國的 BlueShield。2018 年美國兒童過敏症 9 圖片經許可轉載

粘膜呼吸道心臟胃腸道過敏反應診斷標準和 症狀 2-14 種症狀(> 2%)在美國過敏反應事件中報告的症狀(> 2%)0% 20% 40% 60% 100% 蕁麻疹或血管性水腫蕁麻疹潮紅瘙癢血管性水腫(例如面部、嘴脣、舌頭或喉)口腔內水腫或舌頭腫脹喉部水腫 咽喉瘙癢症 ophyarngeal 水腫呼吸困難/呼吸困難喉嚨緊張氣喘息支氣管痙攣聲音嘶啞咳嗽胸悶/胸痛呼吸衰竭 Stridor 鼻部症狀/鼻炎心動過速/驚厥/輕度 頭暈低血壓混亂/嗜睡意識喪失吞嚥困難嘔吐/嘔吐腹瀉 + 腹痛惡心腹痛或絞痛腹瀉參考文獻:1.Shaker MS 等J Allergy Clin Immunol。2020. 2.Pistiner M 等人J 《過敏臨牀免疫法》。2021. 3.Jalil M 等人AAAI 2020 虛擬會議摘要。4.Gonzelez-Estrada A 等人Ann Allergy 哮喘免疫學。10 2018。5.Lee S 等人J Allergy Clin Immunol。2017。6.Lee S 等人J Allergy Clin Immunol Pract。2014。7.Manivannan V 等人Am J Emerg Med. 2014. 8.Wood RA 等J Allergy Clin Immunol 2014. 9.Walsh KE 等藥物流行病學藥物 Saf 2013. 10.Decker WW 等人J Allergy Clin Immunol。2008。11.羅斯議員等J Allergy Clin Immunol。2008。12.Webb LM & Lieberman P. Ann 過敏哮喘免疫學。2006。13。同上 AM 等人。Ann 過敏哮喘免疫學。1996. 14。Rudders SA 等人兒科。2010。請注意,某些出版物未指定血管性水腫症狀亞型。 報告時彙總了血管性水腫亞型頻率。

最常報告的症狀是呼吸困難、血管性水腫 (面部、嘴脣、舌頭、喉)和蕁麻疹(蕁麻疹)參考文獻:1.Loverde D 等人胸部。2018. 2.經許可轉載的圖片 11

腎上腺素:眾所周知的作用機制腎上腺素藥理學 作用腎上腺素的臨牀作用受體 • 穩定肥大細胞和嗜鹼性粒細胞-• 逆轉病理組胺級聯抑制炎症介質 • 增加支氣管氣流 β 2 • 支氣管平滑肌鬆弛 • 增加骨骼肌血液舒張 • 骨骼血管舒張血管系統 β • 增加血壓和心率 • 緩解低血壓和休克 1 • 增加收縮壓 血壓 • 緩解低血壓和休克 • 原因血管收縮 α 1 • 緩解上呼吸道阻塞 • 降低粘膜水腫受體靈敏度 12
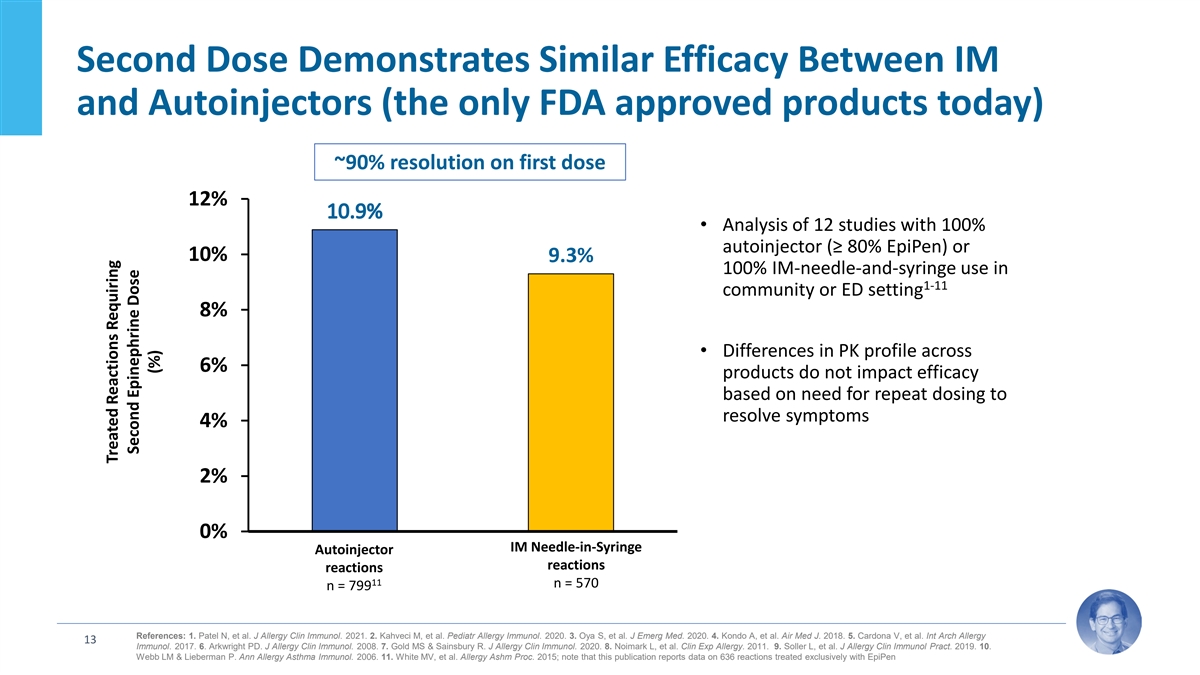
第二劑在 IM 和 AutoInjectors 之間表現出相似的功效 (當今唯一獲得 FDA 批准的產品)約 90% 的分辨率為 12% • 對 12 項研究的分析,使用 100% 自動注射器(≥ 80% EpiPen)或 10% 9.3% 在 1-11 社區使用注射針和注射器 100% 或急診室設置 8% • 6% 產品中 PK 分佈的差異不會影響療效,因為需要重複給藥才能緩解症狀 4% 2% IM 注射器自動注射器% r 需要第二劑量反應反應 11 n = 570 n = 799 參考文獻:1.Patel N 等人J Allergy Clin Immunol。2021. 2.Kahveci M 等人兒科過敏免疫學。2020. 3.Oya S 等人新興醫學雜誌 2020. 4.Kondo A 等人Air Med J. 2018. 5.Cardona V 等Int Arch Allergy 13 Immunol。2017. 6.Arkwright PD。J Allergy Clin Immunol 2008. 7.Gold MS & Sainsbury R.J Allergy Clin Immunol。2020. 8.Noimark L 等人Clin Exp Allergy。2011. 9.Soller L 等人J Allergy Clin Immunol Pract。2019。10。Webb LM & Lieberman P. Ann 過敏哮喘免疫學。2006。11。White MV 等 等Allergy Ashm Proc. 2015;請注意,本出版物報告了僅使用 EpiPen 治療的需要第二劑腎上腺素的反應治療的 636 種反應的數據(%)

及時使用腎上腺素治療是關鍵的抗原暴露 延遲治療的後果危險因素 1 生命體質異常(心率、SBP、呼吸)p
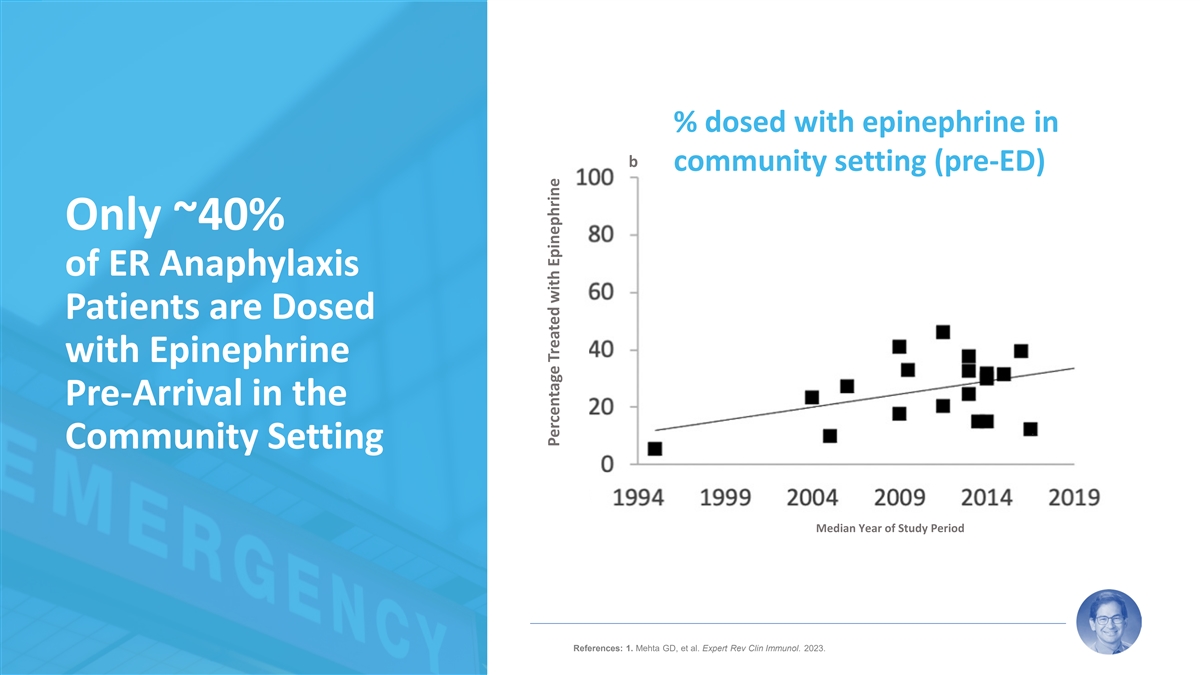
在 b 社區環境(Pre-ED)中服用腎上腺素的百分比只有大約 40% 的 ER 過敏反應患者在抵達社區前接受腎上腺素的劑量設置研究週期中位數 15 參考文獻:1.Mehta GD 等人專家 Rev Clin Immunol. 2023。用腎上腺素治療的百分比

腎上腺素治療延遲主要是由於 自動注射器的侷限性和陪護患者不情願 ~40% 的患者不願填充或補充腎上腺素 40% 2 1 40% 的所有腎上腺素處方都給予腎上腺素 > 50% 的父母害怕或 55%-60% 不太害怕給孩子服用 50% 2-4 60% 的腎上腺素 5 上腺素約 20% 的患者未接受培訓的患者約 70% 未經培訓的患者中 20% 70% 的患者正確給藥 7 參考文獻: 1。文件中的數據。ARS 製藥。2023. 2.Warren CM 等Ann 過敏哮喘免疫學。2018。3.布魯克斯 C 等Ann Allergy 哮喘免疫學。2017。4.柯蒂斯 C 等人Ann Allergy 哮喘免疫學。2014. 5.Chad L,16 等Eur J Allergy Clin Immunol。2013. 6.Sicherer SH 等人兒科。2000. 7.El Turki A 等Emerg Med J. 2017。

與針頭相關的安全風險和使用錯誤針頭相關風險 在所有自動注射器的標籤中定義 Ø 割傷和骨注射 Ø 靜脈注射(血管注射)— 可能導致最嚴重的病人或護理人員意外自我注射到四肢 1 Ø ~每年報告 3,500 起事件 Ø 需要立即就醫(通常在急診室進行治療)2 注射部位疼痛、感染和其他反應濕式注射打針(拔針過快)和其他給藥錯誤 3,4,5,6,7,8,9 用户 錯誤和設備故障參考文獻:1.Anshien M 等人Am J Ther. 2019. 2.嬌蘭 S 等人。Ann 過敏哮喘免疫學。2011。3.El Turki A 等人Emerg Med J. 2017. 4.Moss RB 等Ann Allergy 哮喘免疫學。2018。5. 17 賽諾菲。 Auvi-Q 召回。2015 年 10 月。6.食品和藥物管理局EpiPen 和 EpiPen Jr Recall。2017 年 3 月。7.食品和藥物管理局與設備故障和用户管理有關的 EpiPen 自動注射器錯誤。2020 年 3 月 8.食品和藥物管理局Amneal 和 Impax Laboratories 腎上腺素自動注射器 設備出現故障。2020 年 6 月 9.食品和藥物管理局因潛在的製造缺陷召回Symjepi(腎上腺素)注射劑。2022年3月。

2023 年 AAAAI 指南已更新, 90% 的事件無需激活 EMS 歷史指南建議在使用腎上腺素進行過敏反應後去看急診室,這可能會導致家庭不給予腎上腺素以避免急診就診根據急診室過敏反應的結果和 COVID-19 疫情,數據表明過敏反應的治療和監測可以在家中進行 Ø 如果體徵並且症狀會在給藥後幾分鐘內消退,在第一次給藥後在家中進行監測 Ø 如果體徵和症狀在給藥後的幾分鐘內有所改善,如果舒服,請在家進行監測,同時考慮激活EMS並可能服用第二劑腎上腺素 Ø 如果體徵和症狀無法緩解,請立即激活 EMS,並考慮服用第二劑腎上腺素。立即使用 腎上腺素並在家中進行監測會降低醫療保健的利用率 18

neffy(腎上腺素鼻腔噴霧劑)可以滿足 患者和護理人員尚未滿足的巨大醫療需求腎上腺素具有良好的療效和安全性 Ø 儘管存在藥效差異,但腎上腺素注射產品的療效相同。立即給予腎上腺素至關重要 不願使用或攜帶現有設備 Ø 對安全性的擔憂 Ø 攜帶未滿足的無針需求很麻煩,易於使用、易於攜帶、安全有效的腎上腺素選項 neffy 可以滿足我們 患者的需求 19

neffy 簡介 ARS Pharma 首席執行官理查德·洛文塔爾

neffy 是一種生物利用度高、劑量低 2 mg 的鹽基鼻腔 噴霧劑:經過驗證的 FDA 批准的三種成分生物利用度高、低劑量可最大限度地減少模仿過敏反應(胃腸道症狀)的副作用 > 9 個 FDA 批准過敏和過量給藥引起的心臟毒性風險(> 100 年的臨牀 經驗)Epinephrine 7 FDA 批准噴霧器 1 (> 55) 百萬雷亞爾,99.999% 可靠)3 項美國食品藥品管理局批准,包括 Intravail 1(> 100 萬 Rx)®® NARCAN VALTOCO NAYZILAM®® TOSYMRA VALTOCO Intravail®® TOSYMRA VALTOCO Intravail® Intravail 噴霧器 ®® ZAVZPRET 十二烷基麥芽糖苷:IMITREXTOSYMRA GRAS 吸收增強劑® OPVEE® OPVEE 21 參考文獻:1.IQVIA 處方數據和存檔的 ARS 公司數據

Intravail® 允許在低鼻內劑量下進行類似注射的 PK ,不會產生刺激或疼痛,Intravail 可實現 2038 年以上 nCE 的排他性 • 將腎上腺素放入水基溶液中時不能通過鼻子進行全身吸收 • Intravail 允許在已知的 N-十二烷基 beta-D-治療劑量窗口內全身吸收腎上腺素 Maltoside (Intravail®) 注射劑產品 • 被公認為安全 (GRAS) 吸收 • 無需吸入 — 吸收鼻腔粘膜增強劑 • 已發行美國物質專利的組成和 • 在全球範圍內鬆開緊密連接的生物表面活性劑® 1、2,涵蓋Intravail + 腎上腺素(旁細胞),以及 流化和 • 已發佈的治療方法專利可阻止其他低劑量細胞膜(跨細胞)滲透 3-7 種水性鼻腔噴霧劑 (

23 手機殼專為便於攜帶和便攜而設計,可容納兩臺 neffy 2mg 設備。

社區用途產品的批准依據 Ø 經批准的社區 用途產品包括 IM 和 SC 劑量(FDA 簡報)Ø 幾乎所有未獲得 PK 數據批准的 FDA 批准的路線器械藥代動力學(任何數據,包括文獻)Basis 和 Dose® EpiPen 的顯著差異(EpiPen 與 IM)僅在大約 10 年內已知的 IM & SC 無 PK 數據(1987 年)最近已知的血管注射風險(靜脈注射)0.15 和 0.3 mg® Twinject IM & SC 沒有 PK 數據迄今為止尚無已知 PK 數據(2003 年)0.15 和 0.3 mg® Adrenaclick IM & SC 沒有 PK 數據未知 PK 數據日期(2003)0.15 和 0.3 mg® Auvi-Q PK 比 IM 更快,但相對於 EpiPen IM 和 SC 單一 PK 研究(2012 年)(T = 20 分鐘對 10 分鐘)0.1、0.15 和 0.3 mg max® Symjepi IM & SC 無 PK 數據 ARS 研究顯示 PK 比 neffy 或其他自動注射器更慢 (2017) 0.15 和 0.3 mg® Teva EpiPen IM & SC 無 PK 數據 ARS 研究顯示 PK 比 neffy 或其他自動注射器更慢 (2017) 0.15 和 0.3 mg® Teva EpiPen IM & SC 暫無 PK 數據迄今為止無;針頭更短,活化力不同(2018 年)0.15 和 0.3 mg 24

儘管存在不同的 PK,但所有產品仍顯示出療效 Ø 儘管 PK 差異沒有已知的功效 Ø 所有產品的單劑量分辨率中位數或平均值 C 研究 T 範圍 1 最大治療來源 N 研究 T 最大值(pg/mL)(最小)(最小)EpiPen 0.3 mg 文獻和 ARS 507 288 — 869 5 至 40 1 — 240 IM 0.3 mg 文獻和 ARS 381 209 — 489 30 至 60 3 — 360 Auvi-Q 0.3 mg 文獻 96 486 — 646 20 到 30 5 — 60 Symjepi 0.3 mg ARS 數據 88 337 — 438 30 4 — 240 SC 0.3 mg ARS 36 246 45 4 — 180 總範圍 209 到 869 5 到 60 1 到 360參考文獻:1.Srisiwat C 等人。Asian Pac J 過敏免疫學雜誌。2022年 2.Aquestive Therapeutics 新聞稿。2022年9月 3.愛德華茲 ES 等。Ann 過敏哮喘免疫學。2013。4.Dworaczyk D & Hunt A. 摘要演示 25 AAAAI 2021(虛擬會議)。5.Aquestive Therapeutics 新聞稿。2023 年 5 月。

開發計劃側重於與 批准的腎上腺素產品PK的PK/PD特徵進行比較,以確保在批准的產品範圍內實現有效和安全的PD反應以支持效果-受體反應包圍方法 • 血壓(BP):α和β(β) 受體 1 1 2 • 最低暴露量 ≥ IM/SC(功效)• 心率(HR):β 受體 1 • 最大暴露量

註冊研究表明,兩種 PD Surrogates 的療效和藥效與 neffy PD 和 PK 數據安全數據具有可比性 • 2 mg neffy 符合所有臨牀終點 • 不良事件本質上通常是輕度的,在不超過 4 mg 劑量時沒有明顯的鼻腔刺激或疼痛 • PD 替代品的療效 與批准的產品相當(SBP/HR ≥ 獲得批准)• 最常見的不良事件(> 5%)是輕度鼻腔注射產品)不適(9.7%)和輕度頭痛(6%),鼻部不適與疼痛或刺激無關 • 反應迅速且顯著PD 替代品 • 即使在給藥 1 分鐘後也能觀察到療效,VAS 疼痛的平均分數介於 100 分中的 5 到 8 分之間 • 根據正式評估沒有刺激 • PK 由批准的產品括起來 (療效暴露量 ≥ IM/SC,

neffy 2 mg 研究的藥代動力學結果符合包圍療法 使用 FDA 450 neffy 2.0 mg (HCP) (n=78) * 400 neffy 2.0 mg(自我給藥)(n=42)安全性上限 350 IM 0.3 mg(n=178)EpiPen 0.3 mg(n=77)300 SC 0.3 mg(n=35)250 下級療效 200 150 100 50 0 60 90 120 150 180 210 240 270 300 330 360 時間(分鐘)*包括研究 EPI-15 和 EPI-16 28 平均腎上腺素濃度 (pg/mL)

neffy PK 被 EpiPen 研究(Cmax 或 tmax)平均值研究 C 中位數研究 T max 治療研究參考文獻 N(pg/mL)(最小)AQST-109 EPIPHAST II 結果(2022)22 869 22 ARS EPI-JP01 數據(2020)30 676 10 AQST-109 試點結果(2023)27 628 10 ARS EPI-15(2022)35 612 8 Tal 等人。EAACI (2022) 12 550 9 EpiPen (0.3 mg) ARS Epi-11b Data (2021) 9 537 6 Edwards 等人。NDA #201739 (2012) 67 520 10.2 Chen 等人。AAAAI (2019) 11 511 5 ARS EPI-12 數據 (2021) 36 493 8 ARS EPI-13 數據 (2022) 39 490 6 ARS EPI-16 數據 (2022) 36 491 20 ARS 綜合分析 (2022) — EPI-15/16 78 485 20.5 neffy (2.0 mg) ARS EPI-15 數據 (2022) 42 481 30 ARS EPI-17 數據 (2022) 42 421 30 Worm 等人。Clin Transl Allergy (2020) 12 390 至 530 9 至 30 Turner 等人。Clin Exp Allergy (2021) 37 386 40 Amphastar US2021/030502 (2021) 56 364-458 7-15 ARS EPI-07 數據 (2019) 35 375 24 Dworaczyk 等人。AAAI (2020) 55 308 到 440 10-16 EpiPen (0.3 mg) Oppenheimer 等人。AAAAI (2022) 10 341 22 ARS EPI-01 數據 (2018) 12 333 20 Aquestive R&D Day (2021) 9 300 10 Dworaczyk 等人。AAAI (2021) 25 288 10 Dworaczyk 等人。ACAAI (2023) 26 279 20 Dworaczyk 等人。ACAAI (2023) 25 228 21 29
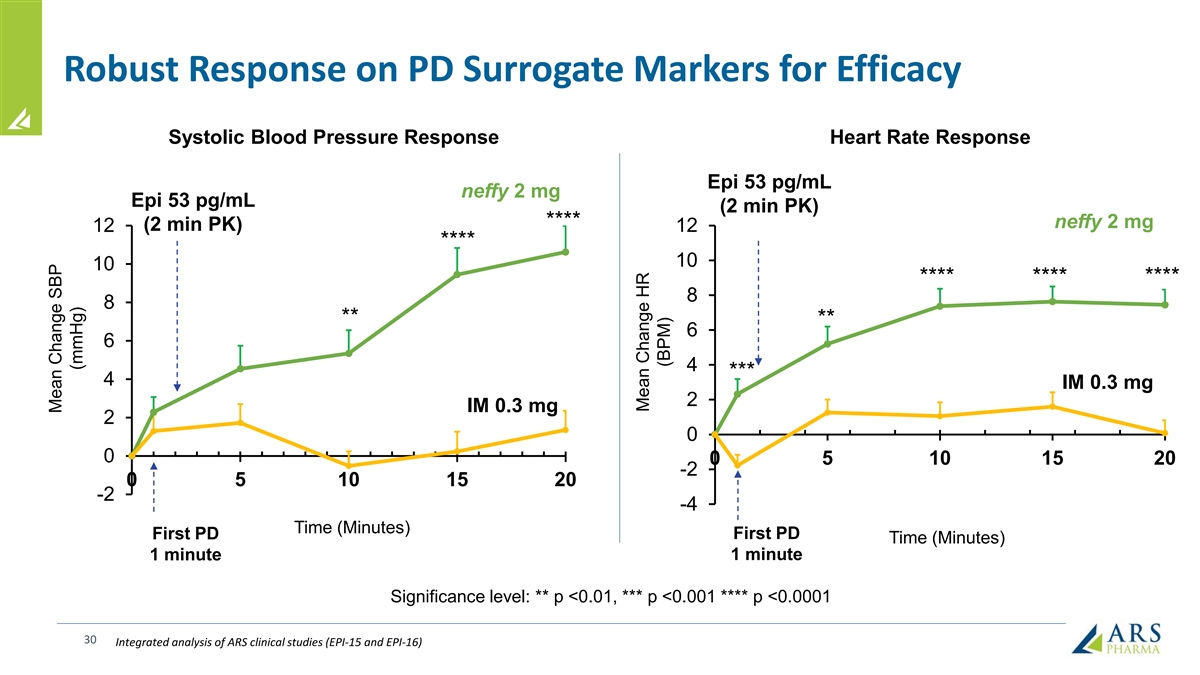
對收縮血功效的 PD 替代標誌物反應強勁 壓力反應心率反應 Epi 53 pg/mL neffy 2 mg Epi 53 pg/mL(2 分鐘 PK)**** neffy 2 mg(2 分鐘 PK)12 12 **** 10 **** 8 **** 6 6 4 *** 4 IM 0.3 mg 2 0 0 5 10 15 20 -2 0 5 15 20 -2 -2 分鐘() 首次 PD 首次 PD 時間(分鐘)1 分鐘 1 分鐘重要性等級:** p

FDA AdCom 的積極投票支持奈菲的益處風險 FDA 諮詢 委員會(2023 年 5 月)投票認為,neffy 的益處風險支持 FDA 批准 Ø 17:5 和 16:6 分別投票贊成在兒科和成人羣體中批准 Ø 投票反對批准的諮詢成員希望獲得過敏反應的臨牀療效比較 臨牀療效數據,這些數據不符合道德標準 FDA 諮詢委員會認為單劑量 NAC 研究數據 “令人鼓舞”” 和 “有利”,因為在臨牀時期 的濃度水平較高腎上腺素可觀察到反應 Ø 鼻腔過敏原挑戰後鼻塞(將純化抗原直接噴射到鼻子)與正常 狀態相比,在最初的 20 分鐘內加速奈菲的吸收 Ø 治療指南建議如果在給藥後的 5 到 15 分鐘內未觀察到任何反應,則給予第二劑 Ø 美國食品藥品管理局報告説,過敏反應患者的鼻粘膜症狀發生率在 2% 到 11% 之間(加權 根據對13種出版物的彙總分析,文獻中的平均頻率約為4%)沒有成員諮詢委員會要求將重複劑量鼻炎研究作為FDA批准的先決條件 31

根據 FDA 的 CRL 要求完成重複劑量 neffy NAC 研究 顯示 PK/PD 大於或相似 IM 注射 PD 反應(SBP、HR 的平均變化)PK 曲線(平均血漿濃度,pg/mL)neffy 2 mg 兩次(R/L)正常(N=42)心率(bpm)平均變化 0.3 mg 兩次 (R/L) L) 正常 (N=42) neffy 2 mg 兩次 (R/L) NA C (N=40) 16 20 neffy 2 mg 兩次 (R/R) NA C (N=41) 900 IM 腎上腺素 0.3 mg 兩次 (R/L) NA C (N=42) 18 14 14 16 800 12 700 14 10 600 12 800 10 400 8 6 300 4 2 0 0 0 0 0 0 0 0 15 30 60 0 0 0 0 15 30 60 0 0 30 60 0 30 60-2 時間(分鐘)時間(分鐘)時間(分鐘)預計在 2024 年第二季度初對 FDA 的 CRL 做出迴應,隨後將進行長達 6 個月的 FDA 審查 32 注:FDA 明確要求 IM 腎上腺素作為本研究的對照品,因為 IM 是腎上腺素產品療效的 基礎,儘管藥效不同,但各種批准的注射設備之間沒有已知的差異

南佛羅裏達大學過敏與免疫學系主任 醫學博士兼兒科主任 neffy Thomas B. Casale 的風險收益評估

腎上腺素輸送產品的理想特性它有效嗎? 安全嗎?患者會使用嗎?Ø 一致且可重複的 PK/PD Ø 無受傷風險和 Ø 副作用極小(無異常值)和最小的副作用 Ø 受 過敏反應症狀影響的可口 Ø 最大限度地降低過量服藥的風險 Ø 較小或先前存在的疾病或與腎上腺素髮病率共存 Ø 易於使用 Ø 避免具有強大而快速的 PD 效果的副作用過敏反應 症狀對嚴重的過敏反應尤其重要 34
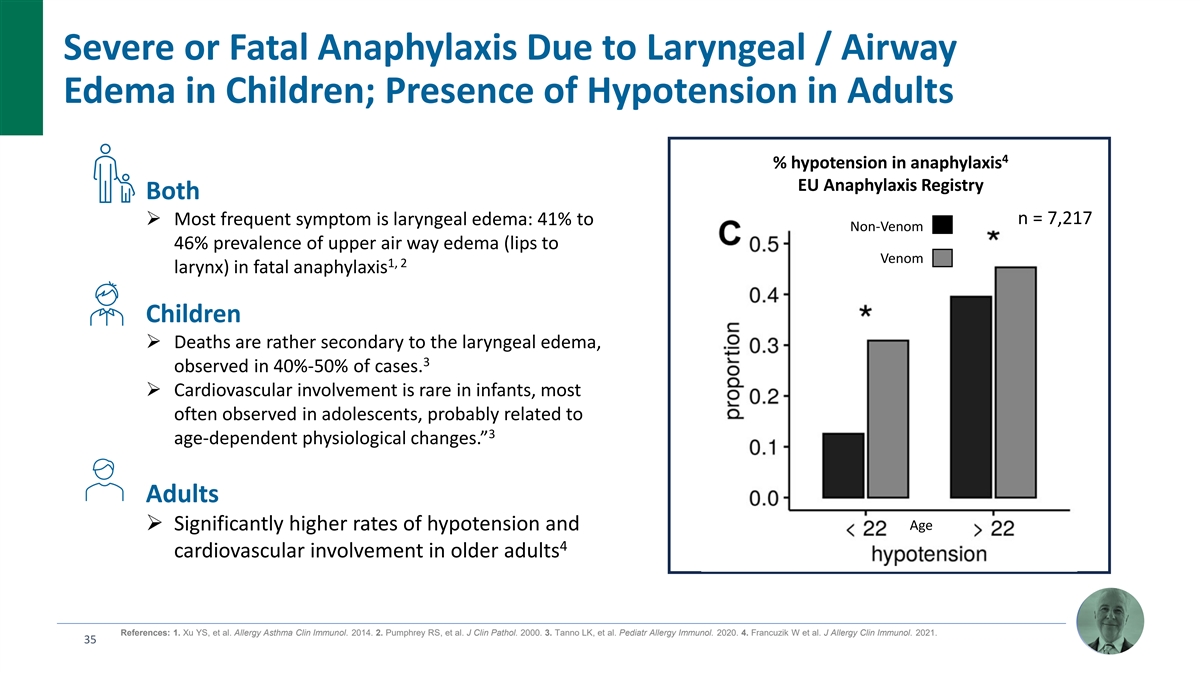
兒童因喉部/氣道水腫引起的嚴重或致命性過敏反應;成人存在低血壓 4% 過敏反應歐盟過敏反應登記處兩者 n = 7,217 Ø 最常見的症狀是喉部水腫:41% 至非毒液體 46% 的上氣道水腫(嘴脣到毒液 1、2 喉) 致命性過敏反應兒童 Ø 死亡相當繼發於喉部水腫,在 40%-50% 的病例中觀察到3例。Ø 心血管受累在嬰兒中很少見,最常見於青少年,可能與3種年齡相關的 生理變化有關。”成人年齡 Ø 老年人的低血壓和4%的心血管受累率明顯更高參考文獻:1.Xu YS 等過敏性哮喘臨牀免疫學。2014。2.Pumphrey RS 等人J Clin Pathol。2000. 3. Tanno LK 等人兒科過敏免疫學。2020. 4.Francuzik W 等人J Allergy Clin Immunol. 2021. 35

neffy 表現出快速而強勁的 PD 反應,顯示可逆轉過敏反應症狀的受體相互作用 收縮壓反應心率反應 neffy 2 mg Epi 53 pg/mL Epi 53 pg/mL(2 分鐘 PK)(2 分鐘 PK)**** 2 mg 12 12**** 10 **** 8 ** 6 6 4 *** 4 IM 0.3 mg 2 0 0 5 10 15 20 -2 0 5 10 15 20 -2 -4 時間(分鐘)時間(分鐘)第一警局第一警察 1 分鐘 1 分鐘重要性等級:** p
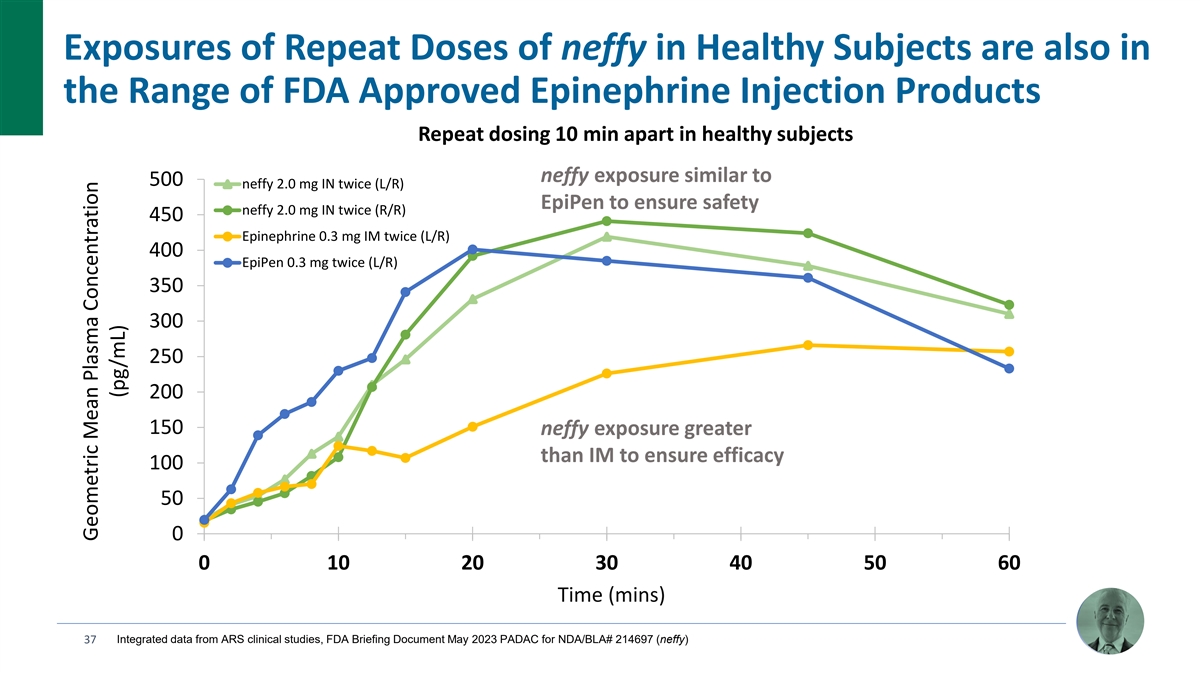
健康受試者重複劑量 neffy 的暴露量也在 FDA 批准的腎上腺素注射產品範圍內 健康受試者間隔 10 分鐘重複給藥 neffy 2.0 mg IN 兩次 (L/R) EpiPen 以確保安全 neffy 2.0 mg IM 兩次 (L/R) 450 腎上腺素 0.3 mg IM 兩次 (L/R) 400 EpiPen 0.3 mg 兩次 (L/R) 350 300 250 200 1.65x 150 neffy 暴露量大於 IM 以確保療效 100 50 0 0 10 20 30 40 50 60 時間(分鐘)37 來自 ARS 臨牀研究的綜合數據,FDA 2023 年 5 月簡報文件 NDA/BLA#214697 (neffy) 幾何平均血漿濃度 (pg/mL)

經證實 PD 反應至少與 EpiPen 一樣好,支持 受體參與逆轉過敏反應症狀單劑量 SBP 反應兩次劑量 SBP 反應 p = 0.947 (ns) 75 p

neffy 顯示口服食品挑戰賽 誘發的過敏反應症狀療效研究口服食品挑戰賽研究結果 1 誘發性過敏反應 (EPI-JP-03) 臨牀反應率 (%) 研究設計:單臂、開放標籤研究 neffy 100.0% 參與者:15 名兒科受試者(年齡 6 至 17 歲):(EPI-JP-03) Ø 9 名受試者 (30 kg+) Ø 6 名受試者 (15-15%) 30 kg) 出現 2 級(中度)或更高的患者 100% 的患者對 中的單劑量 neffy 3 過敏反應症狀(滿分 3 個等級)有反應前 15 分鐘,不需要進行第二次口服食物挑戰,根據治療指南,服用單劑量的腎上腺素 2 mg 或 1 mg neffy:Ø 粘膜:全身性蕁麻疹/出疹/小麥瘙癢,100% 的患者 的臉部腫脹完全消退,咽痛 2 Ø GI:中度腹痛,反覆嘔吐/腹瀉,麻疹單劑量 neffy 有呼吸道反應症狀:反覆咳嗽、胸悶/喘息 可通過聽診檢測到 16 分鐘完全消退 Ø 循環系統:臉色蒼白/輕度低血壓/心動過速(>15 次/分鐘)、頭暈目眩/ “單劑量 neffy doom 後有待出現過敏反應” 的感覺 /嗜睡/頭痛參考文獻:1.Ebisawa M 等人在 AAAI 2024(華盛頓特區)上的演講。2. 根據指南,100% 服用 neffy 的 EPI-JP-03 患者在前 15 分鐘內不需要接種第二劑,因為 未觀察到反應,100% 的患者症狀完全緩解。16 名受試者(6.7%)中有 1 名(6.7%)在服用單劑 neffy 2h 45 分鐘後出現雙相反應,達到完全的 } 症狀的緩解。這與食物誘發的過敏反應兒童中報告的雙相反應頻率為12.8%一致。(Gupta RS 等人。《過敏臨牀免疫學雜誌》,2021年)。
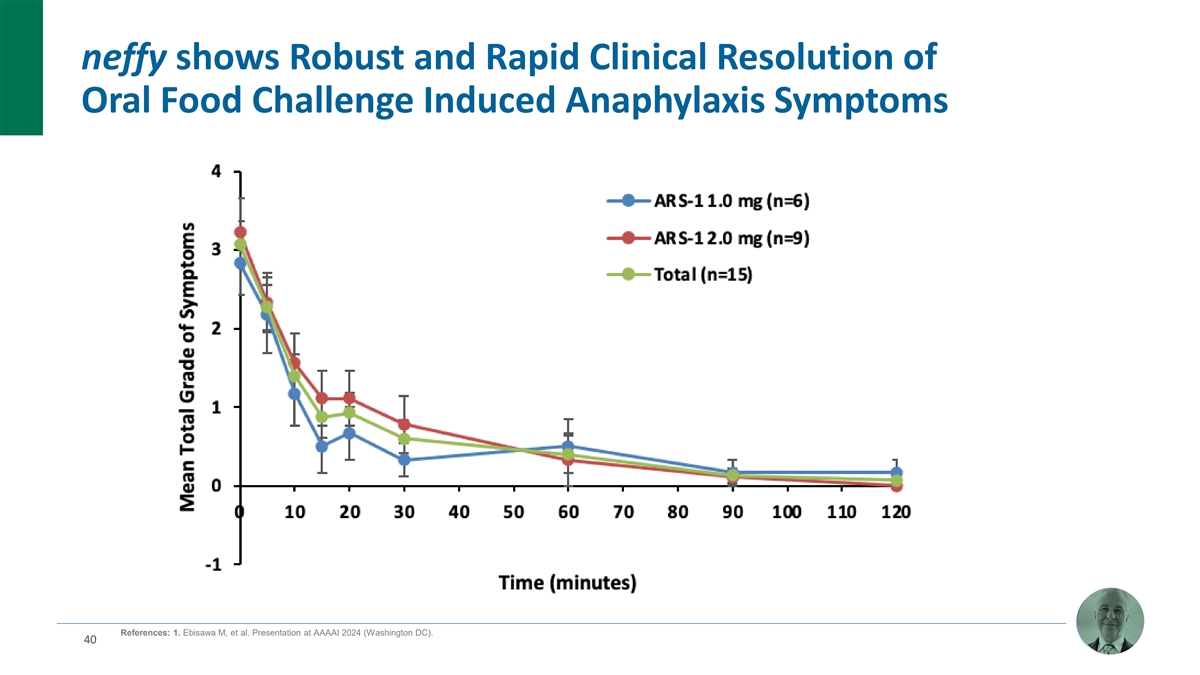
neffy 顯示口服食品挑戰賽 誘發的過敏反應症狀可靠、快速的臨牀緩解參考文獻:1.Ebisawa M 等人在 AAAI 2024(華盛頓特區)上的演講。40

neffy 在 1 項治療難治性慢性蕁麻疹 (EPI-U01) 研究設計隨機、安慰劑對照的交叉試驗研究中顯示出強勁而快速的臨牀反應 蕁麻疹(最常見的過敏反應症狀)的隨機、安慰劑對照的療效數據 • 18 名慢性蕁麻疹受試者 在接受慢性治療(抗組胺藥 +/-)期間每週至少出現兩次發作的慢性蕁麻疹受試者 Xolair) • 患者在出現發作時就診並使用 2 mg、1 mg 或安慰劑進行治療參考文獻:1.伯恩斯坦 D,等。 在 AAAI 2024(華盛頓特區)上的演講。41

實驗性 NAC 誘發的鼻炎不會產生負面影響 neffy 的 PK 簡介(過敏性鼻炎受試者)美國食品藥品管理局諮詢委員會認為 neffy NAC 數據 “令人鼓舞” 且 “有利” NAC 誘發的鼻炎可加速 對更嚴重的過敏反應劑量 neffy 的吸收,但在 neffy 注射範圍內 2 mg 兩次(R/L)正常(N=42)IM 腎上腺素 0.3 mg 兩次(R/L)正常(N=42)間隔 10 分鐘劑量 neffy 2.0 mg neffy 2.0 mg 鼻炎 ARS-1 2.0 mg 在 ARS-1 2.0 中mg IN 鼻炎 neffy 2 mg 兩次 (R/L) NA C (N=40) 900 IM 0.3 mg 腎上腺素 0.3 mg IM neffy 2 mg 兩次 (R/R) NA C (N=41) 300 800 IM 腎上腺素 0.3 mg 兩次 (R/L) NA C (N=42) 250 700 600 500 * 400 * * * 300 100 100 50 0 0 0 * * 300 100 50 0 0 0 * * 300 100 50 0 0 0 10 20 30 40 0 10 20 30 40 時間(分鐘)時間(分鐘)觀察臨牀反應的時間、觀察臨牀反應的時間、每個指南的再劑量和根據指南的再劑量 42 * 鼻炎奈菲與注射注射劑量之間具有統計學意義的 差異(p

實驗性 NAC 誘發的鼻炎不會對 neffy 的 PD 特徵產生負面影響(間隔 10 分鐘重複劑量)心率的平均變化(bpm)收縮壓的平均變化(mmHg)neffy 2 mg 兩次(R/L)正常(N=42)neffy 2 mg 兩次(R/L)NAC(N=40)) 16 neffy 2 mg 兩次 (R/R) NAC (N=41) 20 IM 腎上腺素 0.3 mg 兩次 (R/L) NAC (N=42) 14 18 16 12 14 10 8 8 6 6 6 4 4 2 2 0 0 0 30 60 -2 時間 (分鐘) 時間 (分鐘) 43

上呼吸道感染 (URTI) 誘發的鼻炎對 neffy 平均腎上腺素血漿的 PK/PD 分佈沒有臨牀意義的影響 18 500 n ne ef ff fy y 2.0 mg neffy y 2.0 mg neffy 2.0 mg neffy 2.0 mg neffy 2.0 mg neffy 2.0 mg 含 URTI 16 neffy neffy 2.0 mg neffy 2.0 mg neffy 2.0 mg 含 URTI 16 neffy 2.0 mg 2.0 mg 和 URTI 400 14 12 300 10 8 200 6 4 100 2 0 0 0 0 20 60 60 80 100 120 0 50 100 150 250 -2 時間(分鐘)時間(分鐘)44 N = 21 URTI/16 正常(返回)平均腎上腺素濃度(pg/mL)±SE 與基線相比平均SBP變化(mmHg)± SE

PK/PD 特徵和劑量能力可能會受到不同的 病症的影響,包括過敏反應本身頭痛心力衰竭/驟停口腔/齶部瘙癢/刺痛心律失常對劑量能力或吸收能力的潛在影響腎上腺素的理論給藥途徑/ 鼻炎 4.22% 意識喪失過敏反應症狀 US% 鼻內舌下口腔下口服症狀 * 吸入* 混亂/嗜睡過敏反應分析 Stridor 1-13 呼吸衰竭症狀頻率腹瀉鼻部症狀/鼻炎 4% X X 美國 (n= 4,805 名患者) 腹痛或絞痛胸悶/胸痛口咽水腫 10% X X 口咽水腫 9.66% 噁心嘔吐/嘔吐 20% X X 咳嗽低血壓吞嚥困難 23% X X 經尿前/眩暈/輕微頭痛 聲音嘶啞喉部水腫 24% X 腹瀉 + 腹痛嘔吐/Emesis 20.01% 咽喉瘙癢支氣管痙攣 24% X 吞嚥困難 23.32% 喉水腫 23.58% 口腔內水腫或 24% X X 支氣管痙攣 23.79% 舌腫口腔內水腫或 舌腫脹 24.38% 暈厥/經前血管性水腫(例如面部、心動過速)45% X X 喘息(嘴脣、舌頭或喉部)喉嚨緊張血管性水腫(未具體説明)45.12% 呼吸困難/瘙癢 55% X 潮紅性呼吸困難蕁麻疹 *由於快速結合和呼吸困難/呼吸困難, 口服和吸入全身吸收不足 55.23% 14 胃腸道氧化或難以攝入足夠的呼吸蕁麻疹/血管性水腫 0% 20% 40% 60% 80% 100% 參考文獻:1.Pistiner M 等人J 《過敏臨牀免疫法》。2021. 2.Jalil M 等人AAAI 2020 虛擬會議摘要。3.Gonzelez-Estrada A 等人Ann Allergy 哮喘免疫學。2018。4.Lee S 等人J Allergy Clin Immunol。2017。45 5.Lee S 等人J Allergy Clin Immunol Pract。2014。6.Manivannan V 等人Am J Emerg Med. 2014. 7.Wood RA 等J Allergy Clin Immunol 2014. 8.Walsh KE 等藥物流行病學藥物 Saf 2013. 9.Decker WW 等人J Allergy Clin Immunol。2008. 10。羅斯議員等J Allergy Clin Immunol。2008。11.Webb LM & Lieberman P. Ann 過敏哮喘免疫學。2006。12。同上 AM 等人。Ann Allergy 哮喘免疫學。1996. 13。Rudders SA 等人兒科。2010.14。Simons KJ 等J Allergy Clin Immunol。2004。請注意,某些 出版物未指定血管性水腫症狀亞型。報告時彙總了血管性水腫亞型頻率。

極佳的耐受性和適口性不良事件本質上通常為輕度 ,無明顯的鼻腔刺激或疼痛,劑量不超過 4 mg,任何臨牀研究均無嚴重不良事件無針頭相關損傷或血管注射 neffy 的風險最常見的不良事件(> 5%)為輕度鼻腔 不適(9.7%)和輕度頭痛(6%),鼻部不適與疼痛或刺激無關 Ø VAS 疼痛平均分數 100 箇中有 5 到 8 個(無刺痛或燒灼感)Ø 根據正式評估無刺激(無紅斑或 潰瘍)極佳的適口性 — neffy 1 Ø 沒有味道或氣味 “腎上腺素固有的苦味可能會影響患者,尤其是兒童的接受度” 46 參考文獻:1.Rachid O 等人AAPS PharmasciTech 2010。

不良事件概況與自動注射器相比良好 neffy、EpiPen 和 Auvi-Q 研究中 不良事件的發生率(頻率大於 5%)1 2 2 不良事件 2 mg neffy 0.3 mg EpiPen 0.3 mg Auvi-Q 注射現場紅斑 0% 32.6% 31.3% 注射部位疼痛 0% 24.4% 13.4% 震顫 0% 14.4% 13.4% 輕微鼻部不適 9.7% 0% 輕度頭痛 6.0%

低劑量是 neffy 的一個重要益處,它可以最大限度地降低 過量給藥的風險,並且難以監測臨牀反應。如果過量的藥物被全身吸收過快(例如靜脈注射),腎上腺素具有治療窗口,可能出現過量服用 1、2 — 文獻中報告了多種心臟事件和死亡 2 mg neffy 即使該事件中的生物利用度更高,過度暴露的風險基本上也微乎其微過敏反應期間的滲透性增加或種羣變異性(鼻腔異常、使用其他藥物的影響或 )鼻粘膜上的物質等)高劑量的腎上腺素還會導致吞嚥未被吸收的 5、6 腎上腺素和胃腸道副作用(嘔吐/腹痛)嘔吐/腹痛是食物引起的過敏反應(特別是 雙相)的常見症狀,7、8、9 會混淆對臨牀反應的監測,導致不必要的治療,重新給藥 neffy 幾乎沒有胃腸道副作用參考文獻:1.Casale TB 等Ann 過敏哮喘免疫學。2024. 2.Ebisawa M 等人J Allergy Clin Immunol Glob。2023. 3.Pumphrey RS 等人Clin Exp Allergy。2020. 4.Ring J 等人2018 年荷蘭阿茲泰寶國際賽。5.Schlegel C 等人J 48 荷蘭皮膚科雜誌 2009 年版。6.Dworaczyk D & Hunt A. 在 AAAI 2023(德克薩斯州聖安東尼奧, )上的演講,7.Francuzik W 等人J Allergy Clin Immunol. 2021. 8.Pflipsen MC & Colon KMV。我是家庭醫生。2020. 9.Gupta、RS 等。《過敏臨牀免疫學雜誌》,2021年。
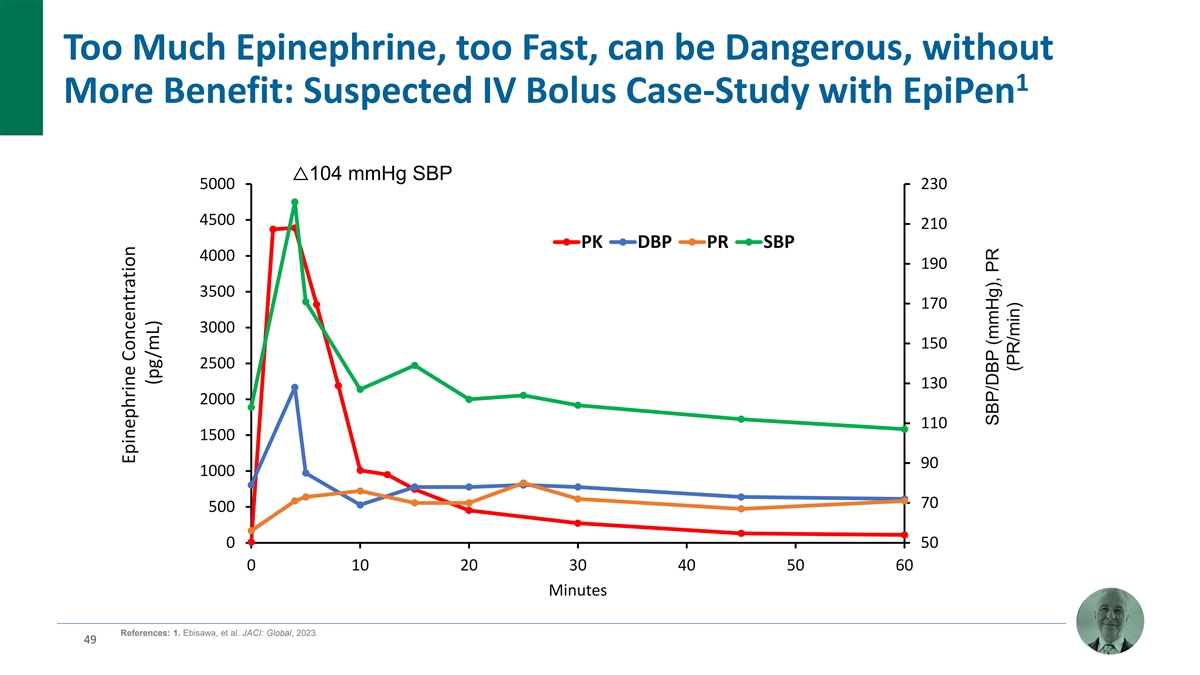
腎上腺素過多、速度過快可能很危險,如果沒有 1 個 益處:使用 EpiPen 的疑似靜脈注射病例研究 △104 mmHg SBP 5000 230 4500 210 PK DBP PR SBP 4000 190 3500 170 3000 150 2500 PK PR SBP 4000 190 3500 150 150 2500 310 PK 3500 50 60 分鐘參考文獻:1.惠比澤等JACI:全球, 2023。49 腎上腺素濃度 (pg/mL) SBP/DBP (mmHg),PR(PR/min)

與對非毒液過敏的成人 過敏反應患者相比,兒童更容易出現嘔吐和胃腸道症狀 ~ 40% 的兒科胃腸道症狀發生率 ~ 60% 的兒科胃腸道症狀發生率非毒液非毒液過敏反應毒液 n = 7,217 n = 7,217 年齡 監測臨牀結果(以及可能改變吸收的合併發病率)應避免的重要副作用口服劑量)參考文獻:1.Francuzik W 等人。J Allergy Clin Immunol. 2021。50 比例比例

人為因素研究和現實世界數據證明,neffy 易於患者攜帶且易於使用經驗證的易用性在人為因素研究和現實世界的緊急使用環境中 100% 的成人(包括沒有過敏症的路人)能夠成功使用 neffy 100% 的 兒童(約佔當前自動注射器處方的一半)無需培訓即可成功使用 neffy NARCAN 非處方藥中同樣的設備(無需培訓)51

使用 neffy 潛在的同類最佳腎上腺素產品簡介,患者應該儘快攜帶和給藥。它有效嗎?患者會使用嗎?它安全嗎?Ø PK/PD 反應顯示在 1 以內發作 Ø 良性安全特徵 — 輕度 Ø 良性安全特徵 — 給藥後一分鐘輕微鼻部不適(9.7%)和鼻部不適和頭痛輕微頭痛(6%)Ø OFC 過敏反應的快速療效 Ø 可口 — 無意義(前 15 分鐘內反應率為 100%),因為 Ø 無受傷風險(無針) 疼痛/刺激,無刺激 /氣味良好,耐藥性蕁麻疹,即使是 Ø Small — 裝在口袋裏 Ø 劑量成比例的 PK/PD 羣體變異性可預測(範圍內的高知名度)經批准的 Ø 易於使用 — 100% 的成人生物利用度,低劑量)注射產品,即使在真實環境下,兒童也可以在沒有世界合併症(例如鼻炎)的情況下使用 Ø 沒有副作用(胃腸道、訓練(甚至是路人);嘔吐, 紅斑)。Ø 只有能夠不阻塞的過敏反應症狀才會混淆臨牀改變 PK/劑量是鼻炎對於 neffy 來説,通過過敏反應、症狀監測和治療,不會對 PK/PD 52 產生負面影響

商業機會埃裏克·卡拉斯首席商務官

解決當前1美國重度 過敏反應市場(淨額約10億美元)未滿足需求的重大機遇。醫生流行病學流行病學流行率數據估計,2-10 1~4000萬名1型過敏反應患者自2010年以來複合年增長率+6.5%,2023年同比增長12.7% 促銷響應度比市場增長趨勢增長約50% 約2,000萬確診和接受醫生護理1,消費者促進(2010 年至 2015 年)11 以上在過去的3年中,約有320萬名患者在2023年填充了處方藥,但有11~330萬患者沒有定期補藥,約80-90%的患者沒有按指示服用 尚未重新填充或尚未填充約1350萬份確診的1型藥但是(1)不攜帶(約 50%),(2)不注射(25-60%),2022年有11份書面處方(3)等待注射(40-60%)或(4)劑量不正確(23-35%)未開處方(過去 3 年) 參考文獻:1.基於IQVIA處方數據(2023年售出約520萬支兩包藥物)和加權平均仿製/品牌腎上腺素自動注射器淨價格。2.Gupta RS 等人兒科。2011。4.Gupta RS 等人兒科學 2018. 54 5. McGowan EC 等《臨牀過敏免疫學雜誌》。2013. 6.Jackson KD 等NCHS 數據簡報。2013. 7.Black LI 等人美國疾病預防控制中心國家衞生統計中心數據簡報。2019 年。8.Gupta RS 等人JAMA 網絡公開賽。2019. 9.Verrill L 等人過敏 哮喘專業版。2015. 10.Bilo BM 等人當前 Opin Allergy Clin Immunol。2008。11.IQVIA 索賠數據,2023
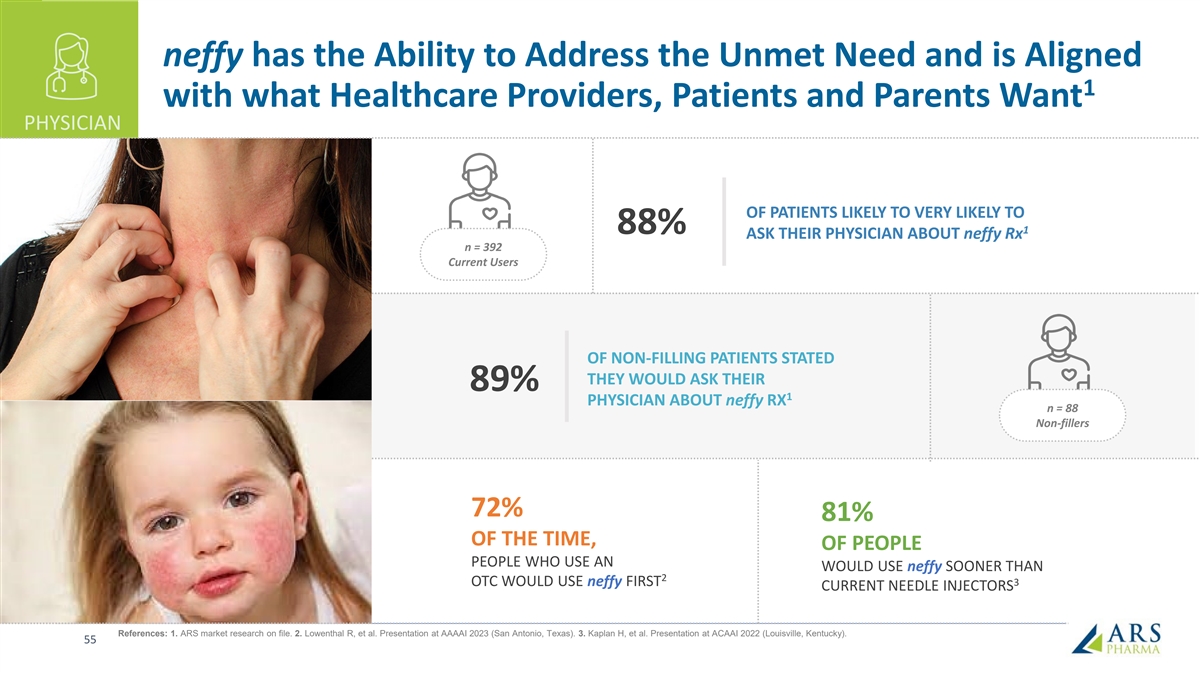
neffy 有能力解決未得到滿足的需求,並與 醫療保健提供者、患者和家長想要什麼 1 患者醫生很可能 88% 1 向醫生詢問 neffy n = 392 當前未填充患者的用户表示他們會向他們的 89% 的醫生詢問 neffy rx n = 88 非填充劑 72% 81% 的使用者會使用 neffy 早於 2 點 OTC 就會使用 neffy 前 3 台當前的針頭注射器參考文獻:1.ARS 市場研究存檔。2.Lowenthal R 等人在 AAAI 2023(德克薩斯州聖安東尼奧市)上的演講。3.Kaplan H 等人在 ACAAI 2022(肯塔基州路易斯維爾)上的演講。55
支持將 neffy 付諸實踐的醫生 PHICYSIONAL 1 8.5 分(滿分 10 分)被視為治療的重大進步 10 = 重大進步/1 = 根本不是進步 n = 75 醫生如果 99% 1 的患者要求開奈菲處方 n = 185 位醫生參考文獻:1。ARS 市場研究已存檔。 56

三分之二的過敏症專家和一半的全科醫生準備儘快給neffy開處方 ;大多數兒科醫生希望醫生在一年內開出neffy處方 — 醫生百分比儘快 68% 在批准後的一年內 54% 52% 43% 在 市場上市 1-3 年後 40% 30% 普通過敏症專家兒科醫生 5% 從業人員(n=98)(n=56)(n=48)參考文獻:存檔的ARS市場研究。57

neffy:使用 針頭注射器克服已知挑戰的創新療法 SAR 患者使用時間縮短 45% 平均攜帶時間(分鐘)從症狀開始到設備使用至少一 1 使用 2,3 腎上腺素設備無針 8.8 替代品解決主要未滿足需求的好處 9.3% 55 Ø 更多的過敏患者和 Patient Carry 5.1 護理人員可能會 N = 100 2 N = 917 與目前的 4.9 針刺選項相比,攜帶 neffy 8.3 Ø 使用護理人員 4.7 85 N = 100,患者服用 neffy 的劑量可能更快無針設備可攜帶 3 N = 150 N = 200 當前設備 neffy 市場研究參考文獻:1.Kaplan H 等人。在 ACAAI 2022(肯塔基州路易斯維爾)上的演講。2.Warren CM 等Ann 過敏哮喘免疫學。2018。3.ARS 市場 研究已存檔。58

約 72% 的受訪者會特別預約與 HCP 患者討論 neffy 採取行動與 HCP 討論 49% neffy 45% 40% 特別預約親自討論 neffy 27% 27% 26% 預約特別遠程醫療 22% 預約討論 neffy 18% 等着看我的醫生是否想和我討論 neffy 18% 等着看我的醫生是否想和我討論 neffy 總計患者(P)看護者(C)8月23日可能向HCP詢問neffy情況的受訪者:受訪者總數(n=476)、患者(n=244)、看護者(n=232)百分比受訪者參考文獻: ARS 市場研究已存檔。59

60
neffy 戰略目標教育處方者推動 專業和高十分之一處方者採用 neffy 引人注目的價值主張促進獲取 neffy 的獲取、可負擔性和支持服務激活患者提高認識並激勵患者和護理人員尋找 neffy 61

推動專業和高十分制處方者的採用率 EDUCATE 醫療保健提供商發佈目標 Ø 由 110 名銷售和虛擬代表以及區域銷售經理組成的商業力量 Ø 教育、宣傳和資源以推動採用率(neffy Experience)Ø 召集 12,500 名過敏 專家和高十分制處方者 • 達到所有 HCP 處方的 40-45% • 向過敏症專家和兒科醫生提供超過 80% 的處方 62

致力於確保所有患者都能獲得舒適的治療促進與主要支付方和 PBM 討論的關鍵 發現:• 對早期對話中的耐受性非常感興趣;在批准之前主動要求臨牀表現 • 腎上腺素作為 藥房福利保障,我們預計將在推出後的一年內實現對80%的商業生活的無限制保障 • ARS致力於提供可及性和可負擔性——我們將為商業患者提供25美元的自付額收購, 現金價格為199美元,以及針對未投保或投保不足的患者援助計劃 • neffyconnect將通過向患者、護理人員和醫療保健提供者提供有關支持計劃和 經濟援助的信息來幫助管理保險 “這改變了遊戲規則;實際上,“延遲准入沒有任何價值” 如果定價合理,則可以解決我們目前對此類產品未滿足的需求,而這不可能是 最先進的產品空間,特別是安全事先授權 (PA)。我們無法對患者進行'治療'。” 和耐受性問題。” 患者需要它。” — PBM — PAYER — PBM 63

提高認識並激勵患者和護理人員申請 neffy ACTIVATE 消費者發佈目標 Ø 提高認識,激勵患者和護理人員按名字申請 neffy Ø 讓患者和護理人員做好在潛在危機時刻採取行動的充分準備 Ø 激活 患者和護理人員分享他們的 neffy 故事以鼓勵同伴接受 64
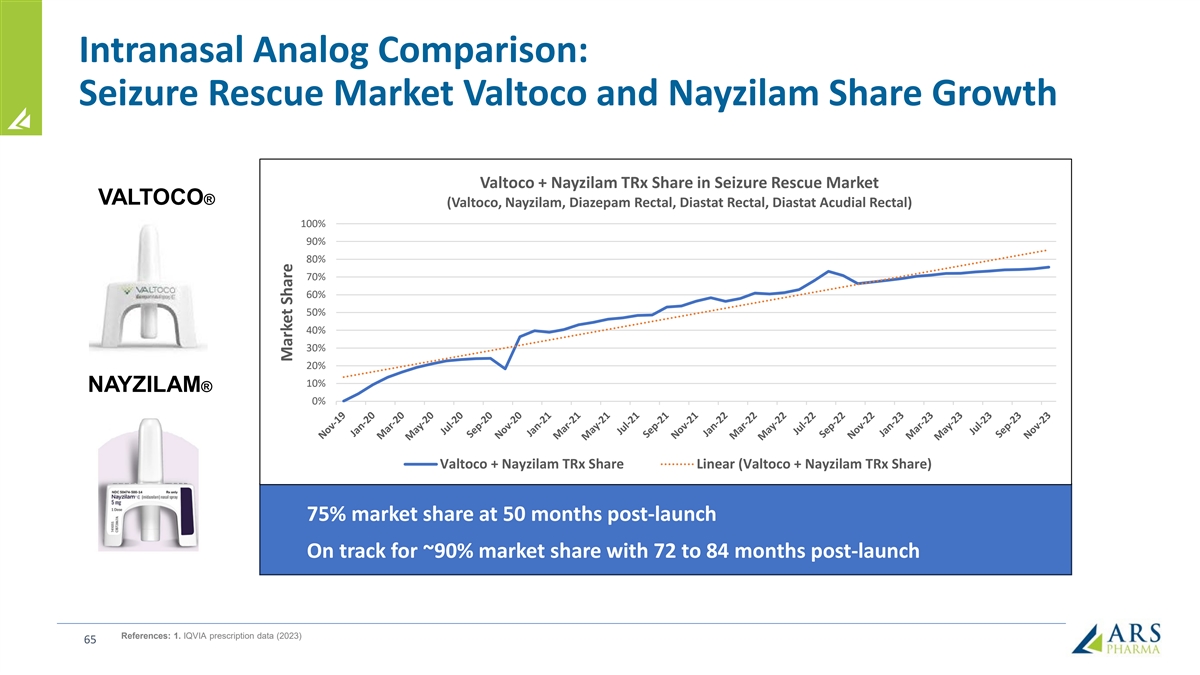
鼻內模擬比較:發作救援市場 Valtoco 和 Nayzilam 的份額增長 Valtoco + Nayzilam TRx 在癲癇發作救援市場的份額增長 Valtoco®(Valtoco、Nayzilam、Diazepam 直腸、Diastat Rectal、Diastat Rectal)100% 90% 70% 60% 40% 30% 20% 10% NAYZILAM® 0% Valtoco + Nayzilam TRx Share Linear(Valtoco + Nayzilam tRx Share)在發佈後50個月內佔有75%的市場份額有望在推出後的72至84個月內實現約90%的市場份額參考文獻:1.IQVIA 處方數據 (2023) 65 市場份額
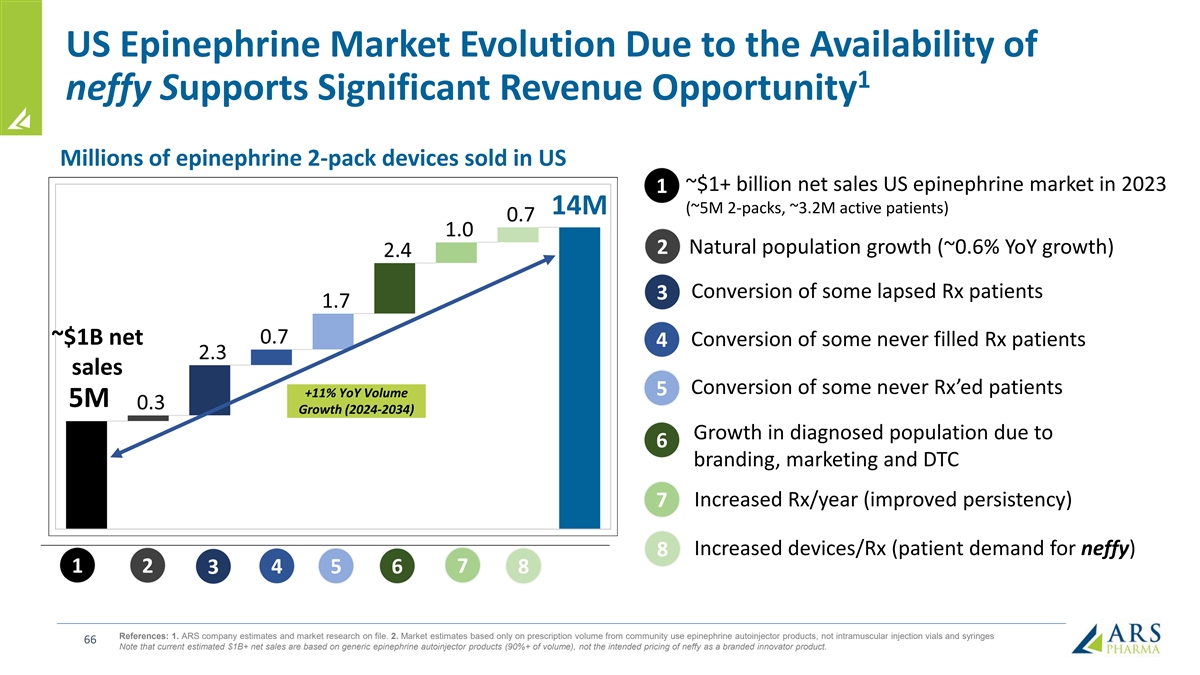
美國腎上腺素市場的演變由於 1 個 neffy 的上市為巨大的收入機會數百萬個腎上腺素 2 件裝設備售出約 10 億美元淨銷售額 2023 年美國腎上腺素市場 1(約 500 萬 2 包,約 320 萬活躍患者)1400 萬 2 自然人口增長(同比增長約 0.6%)轉化部分流失的 Rx 患者 3 ~10 億美元淨轉化率從未填補過處方藥患者 4 銷售額部分從未接受過治療的患者的轉化率 5 +11% 同比增長 5% 量 500萬增長(2024-2034)6個品牌推廣、營銷和DTC使診斷人羣的增長 增加Rx/Year(提高持續性)7 增加設備/Rx(患者對 neffy 的需求)8 1 2 7 3 4 5 6 8 參考文獻:1.ARS公司的估算和存檔的市場研究。2.市場估計僅基於社區使用 腎上腺素自動注射產品的處方量,而不是肌肉注射瓶和注射器 66 請注意,目前估計的10億美元以上的淨銷售額是基於仿製腎上腺素自動注射器產品(佔銷量的90%以上),而不是neffy作為品牌 創新產品的預期定價。

neffy:第一種無針施用腎上腺素的方法 Rapid, 可靠配送體積小巧便於攜帶位置和新聞管理在廣泛試驗中耐受性良好,可避免所有與針頭相關的不良事件

財務更新 *上市後要求/上市後 承諾
財務亮點現金和短期投資:2.28億美元債務:0萬美元 普通股:9640萬美元截至2023年12月31日預計至少有三年的運營期,包括neffy 69的預期推出和商業化

neffy 的重大出美機會

2024 年 neffy 的重要催化劑 o 美國保密協議在 2024 年第二季度初對 CRL 作出迴應 FDA o PDUFA 的行動日期預計在 2024 年下半年 o EMA 決定(CHMP 意見)預計在 2024 年年中期提交 o 日本保密協議預計在 2024 年年提交 o 計劃在其他主要的除美國 地區提交申請 o 擴張機會 • 第二階段慢性烏爾都的積極數據 2024 年 2 月公佈的麻疹研究 • 2b 期門診蕁麻疹研究啟動 71

問與答