
附錄 99.2

W: moonlaketx.com | E: info@moonlaketx.com © 2024 | 專有 | MoonLake TX MoonLake Immunotherapeutics 2024 年 3 月 10 日聖地亞哥研發日,AAD 期間
歡迎來到我們的研發日議程子主題演講嘉賓時間:2024 年 3 月 10 日時間:太平洋標準時間 09.00-11:30 地點:聖地亞哥灣景威斯汀酒店(也提供網絡直播)物流-歡迎和會議詳情簡介 Matthias Bodenstedt 5 分鐘-pSA,一項多領域挑戰-競爭背景下的 SLK-ARGO 數據讀出(24 周)-Ph 3 計劃的後續步驟 pSA 超越風濕病學教授 Joseph Merola Kristian Reich 40 分鐘——HS,一種毀滅性的疾病——背景下的 MIRA 數據來源:MoonLake Corporate © 2024 | 專有 | 德克薩斯州月湖2 HS A Derm 教授肯·戈登·克里斯蒂安·賴希·豪爾赫·桑托斯·達席爾瓦建築指示-監管反饋和第 3 期項目-市場規模和潛力 20 分鐘 Jorge Santos da Silva-解鎖 SLK 的價值-新跡象-前進道路催化劑 2024/2025 年 SLK 和 MLTX 的新前沿 5 分鐘 Matthias Bodenstedt-財務和後續步驟-MLTX 向前邁進的後續步驟結束問答環節 40 分鐘

免責聲明來源:MoonLake Corporate © 2024 | 專有聲明 | MoonLake TX 3 前瞻性陳述本演示文稿中的某些陳述可能構成美國所指的 “前瞻性陳述”。S。1995年《私人證券訴訟改革法》。前瞻性陳述包括但不限於關於我們對未來的預期、希望、信念、意圖或戰略的陳述,包括但不限於以下方面的陳述:臨牀前研究、臨牀試驗和研發計劃的計劃;這些研究和試驗結果的預期時間;潛在的市場機會、市場規模的估計和市場增長的估計;潛在跡象;監管會議的時機;市場的發生和時機參與度;對我們的資本資源足以為預期運營提供資金的時間段的預期;成功的時機和可能性、管理層對未來運營的計劃和目標以及預期產品開發工作的未來結果;以及對流動性和資本資源的影響,包括現金狀況。此外,任何涉及未來事件或情況的預測、預測或其他描述的陳述,包括任何基本假設,均為前瞻性陳述。“預期”、“相信”、“繼續”、“可能”、“估計”、“期望”、“打算”、“可能”、“計劃”、“可能”、“潛在”、“預測”、“項目”、“應該”、“努力”、“將” 等詞語以及類似的表述可以指向前瞻性的陳述,但這些詞語的缺乏並不意味着這種説法不是前瞻性的。前瞻性陳述基於當前的預期和假設,儘管我們和我們的管理層認為這些預期和假設是合理的,但本質上是不確定的。新的風險和不確定性可能會不時出現,因此不可能預測所有的風險和不確定性。可能導致實際業績與當前預期存在重大差異的因素包括但不限於管理層無法控制的各種因素,包括總體經濟狀況和其他風險、不確定性以及我們在向美國提交的10-K表年度報告中題為 “風險因素” 和 “關於前瞻性陳述的警示聲明” 部分中列出的因素。S。美國證券交易委員會(“SEC”)2024年2月29日,以及與在生物製藥行業運營的MoonLake Immunotherapeutics等公司相關的因素。本演示文稿中的任何內容都不應被視為任何人表示本文提出的前瞻性陳述將得到實現,也不得將實現此類前瞻性陳述的任何預期結果。你不應過分依賴本演示文稿中的前瞻性陳述,這些陳述僅代表其發表之日,並參照此處的警示性陳述對這些陳述進行了全面限定。我們既不承諾也不接受任何義務公開發布任何前瞻性陳述的任何更新或修訂,以反映我們的期望或任何此類聲明所依據的事件、條件或情況的任何變化。本演示文稿並不旨在總結MoonLake免疫療法的所有狀況、風險和其他屬性。行業和市場數據本演示文稿中包含的某些信息涉及或基於研究、出版物、調查以及我們自己的內部估計和研究。在本演示文稿中,我們依賴並參考了有關我們所競爭行業的市場參與者的公開信息和統計數據以及其他行業數據。將我們與任何其他實體進行任何比較都假定我們所獲得信息的可靠性。我們從第三方來源獲得了這些信息和統計數據,包括市場研究公司的報告和公司文件。此外,本演示文稿中包含的所有市場數據都涉及許多假設和侷限性,無法保證此類假設的準確性或可靠性。最後,儘管我們認為我們的內部研究是可靠的,但此類研究尚未得到任何獨立來源的證實,我們也沒有獨立驗證這些信息。商標本演示文稿可能包含其他公司的商標、服務標記、商品名稱和版權,這些是其各自所有者的財產。僅為方便起見,本演示文稿中提及的某些商標、服務標誌、商品名稱和版權可能不帶有 TM、SM © 或® 符號,但我們將在適用法律的最大範圍內主張適用所有者(如果有)對這些商標、服務標誌、商品名稱和版權的權利。

本次會議的説明請注意上一頁的免責聲明您可以通過問答功能提交問題——問題只有主持人才能看到——我們將在本次會議結束時回答儘可能多的問題。演示和重播將在我們的投資者關係網站上公佈。對於網絡直播期間出現的任何技術問題,也可以使用問答功能請求支持。其他請求應發送至 ir@moonlaketx.com 或 media@moonlaketx.com 來源:MoonLake Corporate © 2024 | 專有企業 | 德克薩斯州月湖 4

© 2024 | 專有 | MoonLake TX 來源:於 2021 年在瑞士成立 Nanobody® 技術已通過首次私人融資獲得許可 IL、三特異性 IL-17A 和 IL-17F Nanobody® 的獨特分子可提升400億美元以上的市場中的炎症治療,自2022年4月起在納斯達克上市,迄今已籌集了約7.5億美元臨牀階段公司成功完成了銀屑病的2b期研究(n=3)13)、HS(“MIRA”,n=234)和 pSA(“ARGO”,n=207)將於 2024 年開始第三階段項目,預計在 2027 年首次商業推出,由頂級團隊推動,目標是從2023年起解鎖涵蓋大型適應症的產品管道(僅HS和PsA就超過50億美元)MoonLake Corporate

差異化分子 — 你還是抗體嗎?Sonelokimab 是一種約 40kDa 的人源化納米體®,由三個由柔性間隔層共價連接的 VHH 結構域組成,大小約為傳統抗體的四分之一。具有 2 個結構域,它與 IL — 17A 和 IL-17F 高度結合 — 第三個結構域結合人白蛋白皮下給藥,Q4W IL-17A 和 IL-17F Nanobodies® 要小得多與傳統抗體相比,它們可以設計成具有多個不同的結合結構域來源:MoonLake Research © 2024 | 專有 | MoonLake TX 6

這完全取決於二聚體 IL-17A 和 IL-17F 通過激活 IL-17RA 和 RC 受體複合物起到二聚體的作用來驅動炎症。不同的 IL-17RA 和 RC 鏈結合形成複合物,它們對不同的二聚體具有不同的親和力 1,2 並非所有的 IL-17A/A、IL-17A/F 和 IL-17F/F 二聚體都能抑制 IL-17A/F 和 IL-17F/F 二聚體 A A/F F/F 受體的二聚體親和力示意圖 A/A F/F 1 Liu S 等人Nat Commun. 2013;4:1888;2 Goepfert A 等人免疫。2020 年 3 月 17 日;52 (3): 499-512 SLK 是唯一結合所有二聚體且具有相似親和力的資產來源:MoonLake Research © 2024 | 專有資產 | MoonLake TX 7

來源:© 2024 | 專有 | MoonLake TX psA 包括臨界綜合評分第 2b 期 (ARGO) 安慰劑——由Humira 207 IL-17A和F TNF和IL-17A x皮膚/關節反應最高,MoonLake Corporate 8 SLK迅速成為大型炎症性疾病試驗患者的領導者(n)SLK領先資產 psA ARGO 24-eek今天公佈的數據,以及其他領先適應症的信息 MoA HS 有史以來最高的主要終點安慰劑,反應深度第 2b 期 (MIRA) 安慰劑-由 Humira 234 x (HisCR75) 控制,IL最大的三角洲——17A和F TNF和伊利諾伊州-17A 其他 Rheum & Derm IL-17A 和 F 抑制效果最佳數據 AS,nr-axSPA,PPP... 待定 IL-17A 和 F 其他 pSO 第 2b 期安慰劑-使用 Cosentyx 313 與市場領導者相比,伊利諾伊州 BKZ-23 等 x Cosentyx 在 PASI100、17A 和 F IL-23 和 IL-23 和 IL-17A

© 2024 | 專有 | MoonLake TX pSa 在風濕病學領域超越自我 9

© 2024 | 機密和專有信息 | MoonLake TX 10 psA — 一項多領域挑戰賽 Joseph F. Merola 教授

11 © 2024 | 專有 | 德克薩斯州月亮湖教授梅羅拉是安進、勃林格英格海姆、布裏斯托爾的顧問和/或研究員-邁爾斯施貴寶、艾伯維、禮來、諾華、詹森、UCB、賽諾菲、Regeneron、Sun Pharma、Biogen、輝瑞、MoonLake 免疫療法披露

12 psA 是一種多領域疾病,涉及關節和皮膚 1 https://www.psoriasis.org/psoriasis-統計數據/ 2024 年 3 月訪問 2 Merola 等人 Dermatol Ther 2023;13:2635 — 2648 3 Luce 等人 AAD 2024;海報 50361 4 Coates 等人 Rev Rev Rheumatol 2022;18:465 — 479 | 指甲炎和指甲/皮膚圖片由 Proftylitis 提供. 分別是 Joseph F. Merola 和 Kristian Reich 教授(請不要複製)| 其他圖片轉載自 Mochizuki 等人 Case Rep Reumatol 2018:2018:4216938,Jurik Insights Imaging 2011;2:177 — 191,McQueen 等人關節炎研究所Ther 2006;8:207 5 Gossec 等人 J Rheumatol 2018;45:6 — 13 psA 是一種多領域疾病治療是使用臨牀和患者報告的跨領域療效關鍵臨牀終點關節和皮膚 4 其他臨牀領域 4 軸向附着炎指甲指炎患者——報告的結果 5 功能,例如 HAQ 疼痛,例如 VAS 疾病的嚴重程度,例如 PGA 多域複合結果 5 多域複合結局越來越突出同時評估跨領域治療影響的臨牀試驗 MDA 最低疾病活性 = ≥5在 7 種嚴格的多領域療效中,關節疼痛關節腫脹皮膚病變柔軟 HAQ 疼痛 PGA 合成 ACR + PASI 關節 + 皮膚的反應我們能否提升到 ACR70 + PASI 100?ACR50 PASI100 © 2024 | 專有 | MoonLake TX

41% 的人已經出現關節症狀,但在大多數情況下,他們沒有與醫生討論過如何治療這些症狀 6 13 psA 很常見,而且往往診斷不足,而且治療不足 1 約翰霍普金斯醫學 [https://www.hopkinsarthritis.org/arritis-info/銀屑病-關節炎 ]2024 年 3 月 2 日訪問美國國家牛皮癬基金會 [https://www.psoriasis.org/psoriasis-統計數據 ]訪問時間 2024 年 3 月 3 日 Merola 等人 Dermatol Ther 2023;13:2635 — 2648 4 Mease 等人。J • 據認為 150 萬美國人患有 psA 1 30% 的 PSO 患者轉為 psA 診斷 2 • 47% 的患者在 PSO 診斷時已出現肌肉骨骼症狀 3 psA 很常見在 AAD 2024 年進行的新研究在受訪的美國 PSO 患者中:在最近的一項國際調查中,約有五分之二的確診為 psA 的患者未服用生物製劑,每五名左右有 2 名的 psA 患者診斷不足 PREPARE 非介入性研究 4 但是,psA 通常診斷不足或治療不足 41% 41% Am Acad Dermatol。2013;69:729 — 35 5 Tillett 等人。Rheumatol Ther. 2020;7:617 — 37 6 Luce 等人 AAD 2024;海報 50361 © 2024 | 專有 | MoonLake TX

14 psA 的症狀負擔會導致嚴重的工作障礙使用能更好地解決症狀的治療將為患者和社會帶來廣泛——範圍廣泛的益處 A > 30% 和 25% 的焦慮和抑鬱症患病率 2 五分之四的患者報告疲勞,3 對身體活動有重大影響 1 Shadick 等人 ACR 2023;海報 0488 2 Vestergaard 等人 RMD 公開賽 2024;10:e003412 3 Gossec 等人 J Rheuuu 2022年;49:1221 — 8 4 Haugeberg 等人關節炎研究報告 2020;22:198 5 Gossec 等人 Ann 在 COPPAR 登記冊中 psA 患者出現工作障礙(N =113) 1 44% • 疲勞、疼痛、焦慮、抑鬱和睡眠障礙 1,5,6 是相互關聯的症狀 4 與工作障礙有關 • 多領域疾病 7 也與工作障礙有關,包括皮膚、多關節和內臟受累功能障礙焦慮疲勞疼痛抑鬱睡眠障礙 Rheum Dis 2020;79(補充 1): AB0821 6 Spindler 等人 J Am Acad Dermatol 2021; 85:910 — 922 7 Walsh 等人 Joint Bone Spine 2023;90:105534 © 2024 | 專有 | 德克薩斯州月湖

15 除關節外,皮膚的高臨牀反應對患者至關重要。圖片來源:皮膚——由克里斯蒂安·賴希教授提供,關節 — Mochizuki 等人 Case Rep Reumatol 2018:2018:4216938 1 402 名 psA 和中度至重度皮膚受累(≥ 3% BSA)患者的生活質量數據評估關節和皮膚的治療反應至關重要為了給患者帶來最大的改變,多域 psA 會導致更明顯的 QoL 損傷 2 • 更大的爆發風險 • 更嚴重的工作損傷 • 更高的發生率焦慮和抑鬱 • 總體生活質量評分較差關節 DAPSA 反應皮膚 PASI 反應最大的生活質量影響 1 — 10 0 10 20 30 QoL 情商變化-5D-VAS ACR + PASI 評估 SPIRIT 3 期臨牀研究項目中雙關節的反應 + 皮膚療法/安慰劑(經梅羅拉教授許可轉載)| Kavanaugh 等人關節炎類風濕醇 2017;69(suppl 10);AB2539 2 Tillett 等人 Rheumatol Ther 2020;7:617 — 37 © 2024 | 專有 | 德克薩斯州月湖

16 大多數患者目前仍無法達到 MDA,即使在 psA 中有生物製劑治療上限:psA 治療的進步在某些領域取得了成功,但使用生物製劑實現 MDA 仍然具有挑戰性,即使是新療法,在美國的真實世界研究中獲得 MDA 的患者百分比未達到 MDA 的患者的總體疾病負擔也可能更高,例如:2 身體機能惡化心理功能惡化生活質量影響 >4 名患者中有 3 名在生物學起始後 6 個月內未達到 MDA 1 77% 未達到 MDA從 CoreVitas 註冊機構獲得 MDA 1 數據(N=1,251);Ogdie 等人 ACR 2021;摘要 1344 2 Coates 等人 RMD 2019 年公開賽;5:e001002。© 2024 | 專有權 | MoonLake TX

影像學進展指甲指甲指炎軸向附着點炎 17 銀屑病外周關節炎首選生物製劑 1 IL-17i TnFi IL-12/23i IL-23i IL-23i IL-17i 是 psA 1 所有臨牀領域的唯一首選生物學類別首選生物學類別基於梅羅拉教授對臨牀研究結果的專家解讀、指甲炎和由約瑟夫·F. 教授提供的指甲/皮膚圖像分別是 Merola 和 Kristian Reich 教授(請勿複製)| 其他圖片 Skin Joints 其他域名轉載自 Mochizuki 等人 CaseRep Rheumatol 2018:2018:4216938,Jurik Insights Imaging 2011;2:177 — 191,McQueen 等人關節炎研究報告 2006;8:207 © 2024 | 專有 | 德克薩斯州月湖

49 62 46 67 周 16 ITT——NRI 第 48 周 ITT——僅限 NRI SEC A BKZ A+F SEC A 只有 BKZ A+F +13 改進 18 我們能否優化 IL-17 抑制?PASI 100 BE RADIANT Phase 3b H2H BKZ 與 SEC 1 IL-17A-唯一抑制劑 Secukinumab mab IL-17A+IL-17F 抑制劑 Bimekizumab 單抗 bimekizumab 單抗作為處理 psA 所有結構域的首選類別,MOA 的創新集中在優化 IL-17i 上,這是越來越多的證據表明 IL-17F 與 IL-17A 一起推動銀屑病炎症... 與抑制 IL-17A 相比,抑制 IL-17A+IL-17F 對皮膚有更大的益處——僅限 17A 一項針對中度至重度牛皮癬患者的研究;只有一部分參與者患有 psA,臨牀意義為研究結果尚不清楚(PsA 中沒有對這兩個 MOA 的正面研究);Reich 等人 N Engl J Med. 2021;385:142 — 52 P

3 41 PLC ADA 參考文獻 BKZ 10 46 44 PLC ADA 參考文獻 BKZ 19 IL-17A 和 IL-17F 雙重抑制劑是 psA Bimekizumab IL-17A 和 IL-17F 抑制劑(160 mg Q4W)中經過新驗證的 MOA | BEOPTIM(第 3 階段 psA)1 1 NRI,非應答者插入;McInnes 等人 Lancet 2023 401:25 — 37;2 Merola 等人 Lancet 2023;401:38 — 48 ▪ 參與該研究的患者是生物學——天真——腫瘤壞死因子-紅外研究 2 主要終點關鍵次要終點多域終點 ACR 50(關節)PASI 90(皮膚)MDA 61 13 45 ADA ref BKZ PLC 第 16 周 NRI-ITT在第 16 周,對 IL-17A 和 IL-17F 的抑制提供了高水平的皮膚 + 關節反應 © 2024 | 專有技術 | MoonLake TX

20 Sonelokimab 是一種新型的人源化納米體®,靶向 IL-17A+IL-17F Anti-IL-17A 抗白蛋白抗劑-IL-17A 或 IL-17F A A A F F F F 抑制 IL-17A/A、IL-17A/F 和 IL-17F/F 二聚體 Sonelokimab Nanobody® ~40 kDa 1,2 © 2024 | 專有 | MoonLake TX IL,白介素;mAb,單克隆抗體;PASI,牛皮癬面積和嚴重程度指數。1.Papp KA 等人,《柳葉刀》,2021;397:1564 — 1575;2.Svecova D 等人 J Am Acad Dermatol。2019;81:196 — 203。Sonelokimab 2b 期治療銀屑病 1 • 快速持久的皮膚清除(PASI 100),無意外安全發現作為納米體®,索內洛基單抗(SLK)旨在穿透難以到達的組織並直接靶向炎症部位:1,2 • 體積小(約 40 kDa,傳統單抗約為 150 kDa)• 白蛋白-結合結構以延長半衰期炎症的目標部位

21 SLK 在第 12 周實現了高水平的關節和皮膚反應 Sonelokimab IL-17A 和 IL-17F 抑制劑(納米體)| ARGO(第 2 期 psA)▪ 生物學天真和有經驗的患者都參與了該研究。使用納米抗體抑制 IL-17A 和 IL-17F 對兩個皮膚和關節均顯示出令人鼓舞的療效 12 周 NRI-ITT 15 50 77 20 43 46 PLC N=40 ADA ref N=42 SLK 60 mg N=41 主要終點 ACR 50(關節)關鍵次要終點 PASI 90(皮膚)PLC N=26 © 2024 | 專有 | MoonLake TX ADA 參考 N=32 SLK 60 mg N=26

22 SLK Nanobody® 在綜合評分中也顯示出令人鼓舞的反應 8 16 27 ADA 參考 SLK 60 mg PLC Sonelokimab ARGO 第 12 周 ITT——NRI SLK 治療在 ARGO 試驗中提供了滿足嚴格的高閾值終點,例如 MDA 和 ACR 70 + PASI 100 多域終點關節 + 皮膚複合材料 MDA ACR 50 + PASI 100 更高閾值 ACR 70 + PASI 100 8 22 31 PLC ADA 參考 SLK 60 mg 20 44 36 0 10 20 30 40 50 0 4 8 12% 參與者 Weeks SLK 60 mg ADA 參考安慰劑 © 2024 | 專有產品 | MoonLake TX

23 © 2024 | 專有 | ARGO試驗中的MoonLake TX摘要第12週數據對SLK治療的關鍵終點以及多域複合材料的持續增長設定了很高的期望 • 多個領域未滿足的需求需要新的psA療法 • MDA是特定的、嚴格的終點,為各個領域設定了很高的門檻,而ACR + PASI複合材料允許同時評估關鍵領域 • IL-17A + IL-17A+ IL-177 F 抑制有可能優化 psA 結構域(包括 MDA 和關節 + 皮膚複合材料)的結果 •Sonelokimab 旨在結合 “兩全其美”:IL-17A + IL-17F 抑制,由一種小白蛋白結合的 Nanobody® 介導 • 在 ARGO 2 期試驗中,使用 Nanobody® sonelokimab 抑制 IL-17A + IL-17F 導致第 12 周出現高水平的多域反應,沒有停滯的跡象

© 2024 | 機密和專有信息 | MoonLake TX 24 ARGO 試用版 24 週數據 Kristian Reich

Baarsen LG 等人的 1關節炎研究雜誌 2014;16:426-436;2 Schett G,等人《自然評論風濕病學》。2017;13:731-741;3 Prinz JC 等人J Exp Med. 2020 年 1 月 6 日;217 (1): e20191397;4 Sweet K 等人2021 年 RMD 公開賽;7e001679;5 Shao M 等Clin Immunol 2020;213:108374;6 Lories RJ 和 McInnes IB,《自然醫學》。2012;18:1018-1019;7 Reich K.J Eur Acad Acad Dermatol Venereol。2009;23 補充 1:15-21;臨牀圖片 K. Reich 來源:MoonLake Medical,臨牀圖片 K. Reich © 2024 | 專有技術 | MoonLake TX 25 pSA:IL-17F 依賴型多藥物-結構域疾病位於難以到達的組織中... 3x IL-17F vs IL-17A 1... IL-17A 1... IL-17A psA IL-17F pSa IL-17F psA 指甲銀屑病軸向性疾病指甲炎... 並造成毀滅性損害(psA 起始於 2 號附着點炎,IL-17F 在其中產生細胞相關斑塊 3 和軸向疾病 4-6,80% 的患者患有指甲牛皮癬 7) 斑塊指甲銀屑病關節和脊柱疾病 psA 是一種多域深層組織疾病... 疾病活動銀屑病 PASI 90 外周關節炎 ACR50 2030 年後銷售額 psA 患者皮膚受累達 10% — 嚴重皮膚病全球患病率 0.5% 10% 以上 80% 或更多具有多個疾病領域的患者 20% 仍是標準 ACR 水平改善的市場規模未滿足的需求

ARGO:2期試驗設計ARGO ▪ 全球研究的關鍵設計元素,約有50個研究點,207名患者隨機分組 ▪ 雙盲、安慰劑對照、主動參照組 ▪ 活性 pSA(TJC68 ≥3、SJC≥3、當前活性 psO 和/或確診的 pSO)▪ ACR50 作為主要終點,PASI90 作為關鍵次要終點 ▪ ITT-NRI 初步分析;按性別分層,先前的生物使用情況 ▪ SLK mg 和 SLK 60mg 在 12 周達到統計標誌 ▪ 第 3 組(“SLK 60mg NI”,未入職)在 wk 12 時尚未達到統計標誌 ▪ 有些跨界武器未單獨分析(小)樣本,5-7 pts/arm)注:1 按性別和先前接觸過的生物製劑進行隨機分層;2 在第 0 周/第 1 天,所有符合條件的參與者被隨機分組 1:1:1:1;3 在交叉週期中,從第 12 周開始,沒有達到足夠反應的參與者在第 24 周之前改用阿達木單抗 40 mg Q 2 W;服用 sonelokimab 60 mg(從基線 Q 2 W 或 Q 4 W 開始)但反應不夠的參與者直到第 24 周才改用索內洛基單抗 120 mg Q 4 W;沒有達到足夠反應的阿達木單抗參與者在第 24 周之前切換到 sonelokimab 120 mg Q 4 W 以獲得足夠的反應;適當的反應定義為將關節的刺痛和腫脹數量減少 ≥ 20%。第 12 周服用安慰劑的參與者在第 24 周之前改用索內洛基單抗 Q 4 W 今天的業績焦點 SLK 120mg ADA 40mg SLK 60mg PLC SLK 60mg NI 第 B 部分 2023 年 11 月 6 日的業績來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 26

處理意見:ARGO試驗在2024年2月7日B部分處置(A+B部分)B部分數據庫鎖定中下降了5%。AE = 不良事件,S 的 Wdw = 受試者戒斷;已完成的 A 部分 = 在第 10 周之前完成治療並完成了第 12 周的評估;3 名患者隨後沒有進入 B 部分;1:1x 未治療,1x Wdw by S 和 1 x 無效;2:1x 協議戒斷標準;3:1x AE(與治療無關)和 1x Wdw by S;4:1x Wdw by S;5:3 x AE; 6:1 1x Wdw by S;7:1 x AE 1x Wdw by S;8:1 x PD 1 x Wdw by S;9 1 x AE 1 x PD 265 篩查失敗 207 隨機 40 安慰劑 41 索內洛基單抗 (SLK) 60mg NI(無誘導)41 索內洛基單抗(SLK)60mg 42Adalimumab 40mg Q2W(參考臂)已停產(3)1 已停產(0)已停產(1)2 已停產(2)3 已完成的A部分:已完成的A部分:已完成的A部分:已完成的A部分:41 41 40 41 43 索內洛基單抗(SLK)120mg 停產(1)4 已完成的A部分:34 已停產(3)5 34 SLK 60mg 5 SLK 120mg 已停產 (0) 已停產 (1) 6 已完成的 B 部分:38 34 SLK 60mg 5 SLK 120mg 停產 (0) 已停產 (0) 已完成 B 部分:39 36 SLK 120mg 已完成 B 部分:39 已停產 (2) 7 已停產 (0) 5 阿達木單抗 34 阿達木單抗 347 SLK 120mg 來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 27 已停產 (2) 8 已停產 (2) 9 已完成 B 部分:37

46.3 61.0 0 0 0 2 4 6 8 10 12 14 16 18 20 22 24 周 ACR70 反應(次要終點)70 +15pp 29.3 25.6 43.2 0 2 4 6 8 10 12 14 16 18 20 22 24 0 50 +16pp 關節療效持續改善至第 24 周,高反應百分比(%)分數達到分數,NRI 1 交叉周交叉百分比(%)分數達到分數,NRI 1 ARGO (NRI 1) BE OPTIMIL 2 (NRI) 注意:不同試驗的比較存在固有的侷限性。沒有對頭試驗 1 ITT-NRI 直至第 24 周,唯一的不同是根據協議在第 12 周從原治療組重新分配的參與者的最後觀察結果是從 W12 W24 SLK 60 W12 W24 SLK 120 W12 W24 SLK 120 W12 W24 PLC-> SLK 120 W12 W24 ADA W16 W24 W24 W24 W24 W24 W24 W24 W24 W24 W24 W24 W12 W24 W24 W24 W12 W24 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 W24 W24 W12 WK 120 W12 W24 PLC-> SLK 120 W12 W24 ADA W16 W24 BKZ W16 W24 ADA PLC SLK 60mg ACR50 響應(主要終點)SLK 120mg PLC->SLK 120mg 交叉——與 BKZ 46 47 22 43 43 43 44 46 58 55 45 47 +6-2 29 26 24 28 39 42 43 36 14 29 2930 +6-1 第 12 周起;2 Ritchlin 等人Ann Rheum Dis 2023;82:1404 — 1414 處於最佳狀態;來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 28

皮膚預後繼續改善至第 24 周,超出競爭對手 PASI90 反應百分比 (%) 分數達到分數,NRI 1 57.7 63.0 0 4 8 12 16 20 24 周 0 90 15.4 48.1% (%) 分數達到分數,NRI 1 交叉反應 PASI100 反應與 SLK 的交叉 PASI 反應率持續提高至第 24 周——臨牀反應尚未停滯安慰劑交叉組達到 83% PASI90 而在短短 12 周的 SLK 治療後,PASI100 的發生率為 75% 的 Deltas 介於 SLK 劑量和阿達木單抗之間 24 周時 PASI90 為 27%,PASI100 SLK 60mg 和 120 mg 為 25%在第 24 周(以及 ACR)測試的每個 PASI 分數中都優於阿達木單抗 SLK 反應在數值上高於 BKZ 的觀測值,(第 24 周 BE OPTIMIL 中的 73% PASI90 和 56% PASI100)2 20 24 周 76.9 70.4 83.3 0 90 4 8 15.4 59.3 12 16 PLC 注意:不同試驗的比較存在固有的侷限性。沒有正對頭試驗 1 部分受試者基線 BSA >= 3%,ITT-NRI 直至第 24 周,唯一的不同是根據方案在第 12 周從原治療組重新分配的參與者,其最後一次觀察從第 12 周開始延期 2 2 Ritchlin 等人。Ann Rheum Dis 2023;82:1404 — 1414 BE 最佳來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 29 SLK 60 SLK 120 PLC->SLK 120

大多數患者同時達到關節和皮膚預後 — 差異化特徵 31 33 8 22 23 16 46 52 34 31 25 +18pp +6pp +11pp +7pp 同時達到 ACR50 和 PASI100 的患者得分百分比 (%) 分數,NRI 1% (%) 分達到分數 42 44 8 25 58 46 38 +22pp BE OPTIMIL 2 ARGO (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI) (NRI 1) 120mg W12 W24 W12 W12 W24 W12 W24 W12 W24 W12 W24 W12 W24 W24 W24 W12 W12 W12 W24 W12 W24 W12 W24 W12 W24 W24 W12 W24 ADA BKZ ADA PLC->SLK 120 SLK 60 Delta 在 SLK 和阿達木單抗之間從 11pp 增長到 18pp ACR50 PASI90到第 24 周,BKZ 在 BE OPTIMAL 中看不到這種模式注意:不同試驗的比較存在固有的侷限性。沒有正對頭試驗 1 部分受試者基線 BSA >= 3%,ITT-NRI 直至第 24 周,唯一的不同是根據方案在第 12 周從其原始治療組重新分配的參與者,其最後一次觀察從第 12 周開始延期;2 Ritchlin 等人。Ann Rheum Dis 2023;82:1404 — 1414 最佳來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 30

治療目標越高,SLK 的療效就進一步顯示出近 50% 的患者同時達到 ACR70 和 PASI100。在第 24 周,在該高杆綜合評分中 delta 與 adalimumab 2 相比療效提高的強烈信號 1 在較高的障礙終點上 BSA >= 3% 的受試者,ITT-NRI 截至第 24 周的受試者除外根據方案,他們最初在第 12 周的治療組將從第 12 周開始的最後一次觀察延期;患者同時達到 ACR70 和 PASI100得分百分比 (%) 分,NRI 1 27 22 8 16 35 48 19 +29pp 2 標稱 p 值,事後分析 (psLk 120)

1 來自 CoreVitas 註冊表的數據(N=1,251);Ogdie 等人。ACR 2021;摘要 1344;2 BSA,體表面積;HAQ-DI,健康評估問卷殘疾指數;PASI,牛皮癬面積和嚴重程度指數;PRO,患者——報告的結果;S/TJC,關節腫脹/壓痛;VAS,視覺模擬量表;Gossec 等人。J Rheumatol. 2018;45:6 — 13 來源:約瑟夫·梅羅拉教授 © 2024 | 專有 | MoonLake TX 32 MDA:由關節和皮膚中雄心勃勃的臨牀反應目標 23% 反應者 77% 非反應者 >4 名患者中有 3 名在生物學起始後 6 個月內未達到 MDA 1 使用任何生物製劑實現 MDA 臨牀反應低的 MDA 分解 2 MDA(最低疾病活性)deno是指達到以下 7 個標準中的 ≥5 個的患者:1.接頭:TJC ≤1 2。接頭:SJC ≤1 3。皮膚:PASI ≤1(或 BSA ≤ 3%)4。附錄:投標密封點數 ≤1 5。優點:患者疼痛 VAS ≤15 6.優點:患者全球活動 VAS ≤20 7.優點:HAQ-DI VAS ≤0.5% 的 MDA 應答患者

44 37 36 61 51 62 45 22 3 +16pp SLK 對 MDA 的影響顯而易見:60% 以上的患者達到了這個較高的目標。達到最低疾病活動 (MDA) 百分比 (%) pts 達到分數 42 41 48 48 0pp BE OPTIMIL 2 (NRI) 注意:不同試驗的比較存在固有的侷限性。沒有對頭試驗 1 ITT-NRI 直至第 24 周,唯一的不同是根據方案在第 12 周從原治療組重新分配的參與者的最後一次觀察從第 12 周開始延期;2 Ritchlin 等人。Ann Rheum Dis 2023;82:1404 — 1414 處於最佳狀態;3 與第 12 周的總體 PLC 率(20%)不同,因為這僅包括在 W12 時交叉使用 SLK 120mg 的參與者來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 33 W12 W24 W24 W24 W24 SLK 120 W12 W24 PLC — >SLK 120 ARGO (NRI 1) W12 PLC — >SLK 120 ARGO (NRI 1) W12 PLC W24 BKZ W12 W24 ADA SLK使超過50%的患者出現跨組MDA反應,高於先前的psA試驗中觀察到的對阿達木單抗的Delta(高達16pp),而在試驗中觀察到的對阿達木單抗的Delta(高達16pp),而BKZ的情況並非如此包括相同參照臂 W12 W24 的試驗

SLK 在 wk 24 73 65 50 61 56 SLK 60 SLK 120 PLC 處還顯示出更高的深層組織響應-> ADA SLK 120 BKZ n.d. ADA +12pp 67 86 100 60 SLK 60 SLK 120 PLC-> SLK 120 ADA +26pp 基線 LEI 2+ 的 pts 百分比 (%) 提高 2+ pt 利茲附着炎指數 (LEI) 指甲 psO 分辨率 (mnaPO) si=0) 基準時mnapsi>0的pt中達到mnapsi=0的百分比(%)注:不同試驗的比較存在固有的侷限性。沒有正面對頭試驗。1 所有缺失值的最後一次觀察延期;2 ITT——NRI 直至第 24 周,但根據協議在第 12 周從原治療組重新分配的參與者的最後一次觀察從第 12 周開始延期;3 Merola 等人,ACR Convergence 2023 海報 1433,根據圖 ARGO(Wk 24,NRI 2)BE OPTIMAL 3(Wk 24,NRI 2)BE OPTIMAL 3(Wk 24,NRI 2)BE OPTIMAL 3(Wk 24,NRI 2)估計)-9.3-10.0-8.3-13.2 SLK 120 SLK 60 與基線相比的平均變化 Nail pSO 嚴重程度 (mnapSI) PLC-> ADA SLK 120 ARGO(Wk 24,LOCF 1)ARGO(Wk 24,NRI 2)來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 34 Deltas to adalimumab 從第 12 周到第 24 周持續改善

B部分交叉信號在腫瘤壞死因子非反應者中SLK的潛力注意:不同試驗的比較存在固有的侷限性。沒有正對頭試驗 1 部分受試者基線 BSA >= 3%,ITT-NRI 直至第 24 周,唯一的不同是根據方案在第 12 周從原治療組重新分配的參與者的最後一次觀察從第 12 周開始延期;2 共有 7 名 ADA 不足的受試者交叉到了 SLK 120 W12 W24 SLK 60 SLK 60 K 120 ARGO 試驗設計 — 阿達木單抗組在第 12 周重新分配僅向來源曝光來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 35 SLK for 12第 2 周

關鍵亞組 120mg 的療效更高 39 33 62 33 42 86 63 57 所有 PASI >=10 全部 PASI >=10 +52pp +24pp +3pp +1pp ACR70 PASI100 1 ITT-NRI 至第 24 周,唯一的不同是根據方案在第 12 周從原治療組重新分配的參與者的上次觀察從第 12 周開始延期;第 24 周的反應率(亞組)百分比 (%) pts 中,NRI 1 SLK 60mg SLK 120mg 39 36 62 38 42 59 63 67 所有來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 36 hscrp>ULN 全部 hscrp>ULN +22pp +29pp +3pp +1pp 中度至嚴重牛皮癬炎症水平高 ▪ 關鍵亞組可通過120mg對比60mg進一步受益 ▪ 包括皮膚受累程度高(中度至重度 pSO)和高發炎率(高 CRP)的患者 ▪ 或具有高 psA 疾病活性(DAPSA≥28)且存在指甲病(mnapsi>0)的患者 ▪ 其他亞組在 wk12 時受益,但 60 毫克 “迎頭趕上” 許多患者處於第 24 周——向上滴定——可能是這些患者的逐案決定(例如,MTX 使用量高、體重高、預先使用 Bx)▪ 患者受益於更高的劑量(從一開始)或向上(滴定),估計佔試驗人羣的20-30%

A + B 部分 A 部分 Sonelokimab Sonelokimab 阿達木單抗索內洛基單抗 120mg 60mg(有效參考)120mg 含誘導 6 0 mg 含誘導安慰劑 97 82 43 41 39 39 有事件的患者,n 57 (58.8%) 37 (45.1%) 14 (39.5%) 14 (34.1%) 15 (38.1%) 15 (38.1%) 5%) 任何 TEAE 4 (4.1%) 2 1 (2.4%) 2 0 0 1 (2.4%) 0 任何 SAE 6 (6.2%) 4 0 0 0 1 (2.3%) 0 0 0 任何導致停藥的 TEAE 0 0 0 0 0 致命 TEAE 最常見的 TEAE 1 5 (5.2%) 5 (5.6%) 3 (7.1%) 0 1 (2.4%) 1 (2.6%) 1 (2.6%) 1 (2.6%) 1 (2.6%) 鼻咽炎 4 (4.1%) 5 (5.6%) 1 (2.4%) 1 (2.3%) 2 (4.9%) 1 (2.6%) 1 (2.6%) 上呼吸道感染 3 (3.1%) 3 (3.7%) 1 (2.4%) 3 (7.0%) 2 (4.9%) 0 注射部位紅斑(反應)特別關注的不良事件 0 0 0 0 0 IBD 2 (2.1%) 1 (1.2%) 1 (1.2%) 1 (2.4%) 1 (2.4%) 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 0 (2.4%) 0 (2.4%) 0 (2.4%) 0 0 (2.4%) 0 (2.4%) 0 0 (2.4%) 0 (2.4%) 0 0 (2.4%) 0 (2.4%) 0 0 0 0 0 0 0 0 0 口咽念珠菌病 0 0 0 0 0 0 0 食管念珠菌病 0 0 0 0 0 0 0 外陰****念珠菌病 0 0 0 0 0 0 0 0 0 0 0 皮膚念珠菌病 0 0 0 0 0 0 0 0 生殖器念珠菌病其他令人關注的不良事件 0 0 0 0 0 0 0 0 嚴重超敏反應 1 (1.0%) 2 1 (2.4%) 2 0 0 (2.4%) 2 0 0 (2.4%) 0 嚴重感染 0 0 0 0 0 0 0 MACE 0 00 0 0 0 肝臟 AST/ALT > 5x ULN 3 安全性:無明顯信號,獲益良好-pSA 風險概況來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 37 ALT、丙氨酸氨基轉移酶和 AST、天冬氨酸轉氨酶;IBD,炎症性腸病;MACE,重大心血管不良事件;SAE,嚴重不良事件;TEAE,治療——緊急不良事件;ULN,正常值的上限;1 SLK 組中最常見的 AE 前三名。注:MIRA試驗中使用的阿達木單抗療法是原藥(不含檸檬酸鹽的配方);2例未被判定為與治療相關的SAE;3 阿達木單抗組中轉氨酶升高> 3 x ULN的病例報告為AE;SLK 60 mg中一例轉氨酶和CK短暫升高同時發生運動相關肌肉炎症事件;4 TEAEs 領先者停藥包括 1 x 強直性陣攣發作、1 x Furuncle、1 x 咽膿腫和皮下肺氣腫、1 x 扁桃體炎症、1 x 附睾炎、1 x 附睾炎、1 x關節炎

PK 數據顯示 ARGO psA 劑量表現符合預期 0 2 4 6 24 周 0.01 1 10 100 3 μg/ml* 8 10 12 14 16 18 20 22 最後劑量 SLK 60mg SLK 120mg PLC SLK 120mg ADA-> SLK 120mg Sonelokimab 幾何平均槽濃度 (μg/mL) SLK 槽濃度通過交叉雙臂濃度複製前 12 周的數據,SLK 迅速突破了最佳血漿濃度(以減少大量靶點),並在患者轉向維持劑量時保持在水平以上 * 表明組織抗炎的最佳血漿濃度活動來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 38

沒有臨牀相關免疫原性的跡象 SLK 120mg 幾何平均槽濃度(μg/mL)按 ADA 狀態劃分 SLK 槽濃度未受治療影響——緊急 ADA 狀態 0.01 0.10 1 10 100 周 0 0 2 4 6 8 10 14 16 20 24 0 14 14 16 16 18 20 20 22 24 周 10 20 30 40 50 60 治療急診 ADA 是的(Y)此外,臨牀反應無明顯變化受抗藥抗體影響 1 No (N) SLK 120mg ACR50 反應率 (%) 受 ADA 狀態影響 60 毫克劑量相似來源:MoonLake Clinical © 2024 | 專有技術 | MoonLake TX 39

psA:通往第三階段(當前計劃)的明確途徑現在從ARGO ▪ 劑量——反應模式與斑塊型銀屑病(pSO,313名患者)和化膿性汗腺炎(HS,234名患者)的發現一致 ▪ 具有最佳益處的劑量-已確定psA的風險概況-60 mg和120mg(誘導)▪ 支持良好的安全性 ▪ 主要的ARGO研究設計要素將可在第 3 階段設計中複製 ▪ 更大的項目規模(可能約為 1,100-1400)將減少由小組驅動的變化 ▪ 具有向上滴定潛力的子組已確定 ▪ 第 3 階段的終點已確認 — ACR50 和 PASI90 — 但預計主要終點在第 16 周,重點是複合二次試驗 ▪ 目前正在計劃兩項試驗 ▪ 腫瘤壞死因子——紅外試驗 ▪ 生物——天真試驗 FDA EoP2 計劃時間表(與 EMA 平行):▪ FDA 會議申請:2024 年第一季度 ▪ 提交 FDA 簡報:2024 年第一季度 ▪ FDA 會議:預計 2024 年第二季度 ▪ 第 2 期完整的 TFL psA 試驗 (ARGO) 將於 2024 年第二季度到期來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 40

41 IL-17 預計將在未來幾年成為PSA中最大的藥物 1.1 1.6 2.2 5.5 7.3 7.9 2021 2031E 2035E 2 6.5 9.0 psA 市場規模估計 100 萬美元 ▪ IL-17 將成為未來幾年在 pSA 中最大的藥物類別(據估計在 2031 年佔市場份額的 35-40%)▪ 大多數數據來源,包括 DRG/Carivate 在內的 BKZ 最新估計是在完成之前發佈的(Ph 3) 業績 ▪ SLK尚未納入公開的總體估計,儘管所有分析師都認為,到2031年,pSa的銷量將高於轟動一時的水平l ▪ BKZ約佔伊利諾伊州17類的18%致DRG/Clarivate,與美國證券交易委員會或IXE相比,這可能被低估 ▪ 大多數分析師認為,僅SLK的市場份額很小(約1-15%)——與任何領先免疫學市場的生物製劑相比,這可能是低估了4 Bio Non-Bio 1基於DRG/Clarivate數據(“Bio” 包括TNF,伊利諾伊州-12/23,伊利諾伊州-17和伊利諾伊州-23相關資產;“非生物” 包括所有資產)DMARDs、JAK抑制劑和精選共刺激調節劑);2 基於使用5年曆史複合年增長率(2027-2031年)將銷售額延長至2035年;3 分析師顯示的區間上限涵蓋MLTX的報告(如果有);4 考慮來自16種免疫學適應症的DRG數據:psA、RA、哮喘、中度成人 AD、重度成人 AD、nr-axSPA、AS、CU、LN、SLE、psO、慢性阻塞性肺病、維持性UC(其中每個適應症的平均生物學份額約為13%,第二大生物藥物的份額約為23%,佔比約為23%,佔比約為23%,佔比約為23%,佔比約為23% 領先的 Biologic 為 36% 來源:MoonLake,DRG/Clarivate,分析師報告 © 2024 | 專有 | MoonLake TX ~15 3 主要筆記 ~10 3

來源:© 2024 | 專有 | MoonLake TX 42 psA:ARGO 的結果證實 SLK 是 psA MoonLake Corporate 前所未有的多域反應的潛在領導者,約 60% 的患者在第 24 周達到了 MDA,約 60% 的患者達到了 ACR50+PASI90,證實了 SLK 的持續多域影響。更大的反應深度到第 24 周達到 ACR70,60% 以上的患者達到 PASI100,約 50% 的患者達到 ACR70+PASI90 PASI100 複合材料 — 效果持久,尚未達到最大限度的疾病控制效果更快(ACR50,27% wk 8),同時在 24 周(ACR50,61% wk 24)時療效提高 —還反映在深層組織(70% 的指甲清除率)和患者報告的預後靈活劑量 60 毫克已證實足以在大多數領域取得領先效果,120 毫克增加了特定亞組的益處 — 非常便捷的治療方案(每月維護)除了目前的生物製劑之外,在所有臨界評分中,患者對 SLK 和 ADA 的反應更好,也高於其他 Bx ——這是一個差異化的舉措。良好的安全性沒有新信號,如ISR率,念珠菌(如果存在)是短暫的,沒有停藥

© 2024 | 專有 | 德克薩斯州月亮湖 HS 特許經營大樓指示 43

© 2024 | 機密和專有信息 | MoonLake TX 44 HS — 一種毀滅性的疾病 Kenneth B. Gordon 教授

45 © 2024 | 專有 | 德克薩斯州MoonLake Gordon教授已獲得以下製藥公司的酬金和/或研究支持:艾伯維、安進、Arcutis、布裏斯托爾——邁爾斯施貴寶、勃林格英格海姆、德馬萬、DICE、Incyte、禮來、楊森、LEO Pharma、MoonLake 免疫療法、諾華、輝瑞、Protagonist、Union Disonist、Union Disonist 封閉

... 我們需要在開發時考慮到所有患者的 HS 療法 —— 反映數百萬人... 我們需要能夠持續顯著改善患者生活的 HS 療法... 我們需要能夠治療所有類型病變、有機會實現炎症緩解的 HS 療法 HS 是漸進的,隨着時間的推移會導致不可逆轉的組織破壞... 1 46 化膿性汗腺炎:挑戰和機遇引流隧道 T 膿腫 T 潰瘍伴有大量疤痕和潰瘍的晚期疾病 4 1 Sabat 等人 Nat Rev DisPrimers 2020;6:18 2 Krueger 等人 Br J Dermatol 2024;190:149 — 162 3 Ingram 等人 EADV 2023;海報 P0046 4 T,隧道 | 圖片由肯尼思·戈登教授和 Gretchen M. Roth 博士提供。延遲和治療不足是疾病管理中的關鍵空白... 2 延遲(及低於)的診斷推動了保守的患病率估計... 2,3% 全球晚期深度膿腫患病率還有隧道 4 © 2024 | 專有 | MoonLake TX

47 HS 的特點是給患者和社會帶來沉重負擔 NIS,全國住院患者樣本症狀 1 主要症狀包括... • 疼痛 • 惡臭引流 • 情緒低落/抑鬱... 對於有排水隧道的患者來説,住院和急診室就診很常見 2 • 在涵蓋2016 — 2019 年的美國索賠數據庫中,30% 的 HS 患者作為住院次數≥1次 2 • 6 根據NIS的數據,住院天數和3.3萬美元的費用代表了HS患者的典型住院時間 3工作和就業負擔在美國,與對照組相比,HS導致失業天數超過2倍和傷殘天數接近3倍 4 18 8 8 4 0 5 10 15 20 觀察到的年率 HS 對照組患者失業總天數醫療相關缺勤天數 N=6020 N=1204 >2x ~3x 2x 1 Ingram 等人 EHSF 2023;海報 P139 2 Chopra 等人 SID 2022 海報;343 3 Bhattaru 等人 AAD 2023;海報 43666 4 Tzellos 等人 Br J Dermatol 2019;181:147 — 154 5 Schneider——Burrus 等人 Br J Dermatol 2023;188:122 — 130 © 2024 | 專有 | MoonLake TX A 同樣嚴重對工作和就業的影響見於歐洲 5
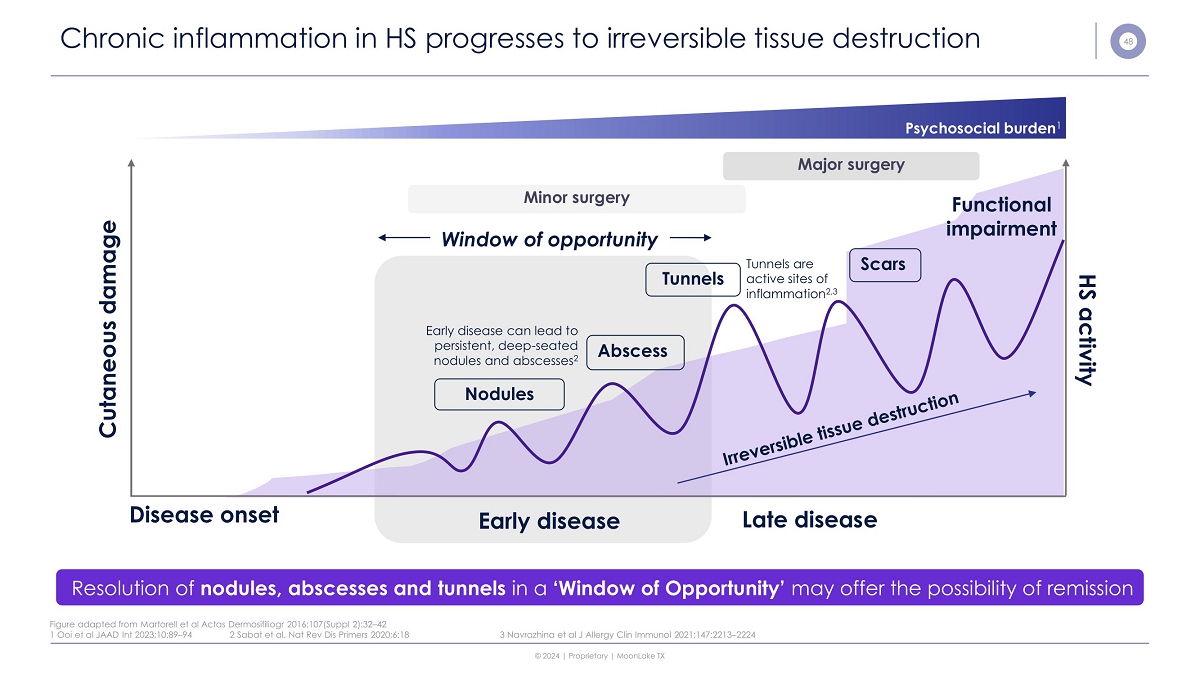
48 HS 中的慢性炎症發展為不可逆轉的組織破壞在 “機會之窗” 中消退結節、膿腫和隧道可能為緩解提供可能性圖改編自 Martorell 等人 Actas Dermosifiliogr 2016; 107 (Suppl 2): 32 — 42 皮膚損傷 HS 活動隧道疤痕膿腫結節疾病發作早期疾病晚期疾病功能障礙隧道是炎症的活性部位 2,3 早期疾病可能導致持續的深層結節和膿腫 2 小手術機會之窗心理負擔1 大手術 1 Ooi 等人 JAAD Int 2023;10:89 — 94 2 Sabat 等人。Nat Rev Dis Primers 2020;6:18 3 Navrazhina 等人 J Allergy Clin Immunol 2021;147:2213 — 2224 © 2024 | 專有 | MoonLake TX

© 2024 | 專有 | MoonLake TX 2 我們能否在 “機會之窗” 中更有效地治療 HS?我們需要 • 更多的治療選擇 • 更好的療法 • 更短的治療時間,使衞生系統能夠更快地將患者轉向治療,並使他們持續接受治療 49 HS 牛皮癬 12 只有 2 種生物製劑獲批 HS FDA-批准的生物療法 1 1 藥物 @ FDA:HS — 阿達木單抗、secukinumab。牛皮癬 — 依那西普、英夫利昔單抗、阿達木單抗、ustekinumab、certolizumab pegol、secukinumab、ixekizumab、brodalumab、brodalumab、bimekizumab、guselkumab、tildakizumab、risankizumab

50 目前使用阿達木單抗的療法停藥率很高

51 HS 的有效療法需要什麼?不受控制的 HS 會對患者生活和社會的方方面面造成嚴重後果 1 Ingram 等人 EHSF 2023;T6-O-15 2 Ring 等人 Br J Dermatol 2024;doi: 10.1093/bjd/ljae042 5 Schneider——Burrus 等人 Br J Dermatol 2023;188:122 — 130 6 Willems 等人 2023;16:153 — 164 3 Garg 等人 J Am Acol 2020 年 82:366 — 376 4 Krueger 等人 Br J Dermatol 2024;190:149 — 162 既定的安全概況 1,6 — 發生嚴重不良事件的風險是皮膚和患者的另一個重要考慮因素持續療效對皮膚和患者 1,2 是其他治療目標的核心住院 3,4 • 減輕住院和急診室就診的負擔 • 減少手術幹預 © 2024 | 專有技術 | MoonLake TX 工作和就業負擔 5 • 促進就業 • 提高個人幸福感和社會融合症狀 6 通過解決包括隧道在內的所有炎症病變類型來緩解症狀負擔
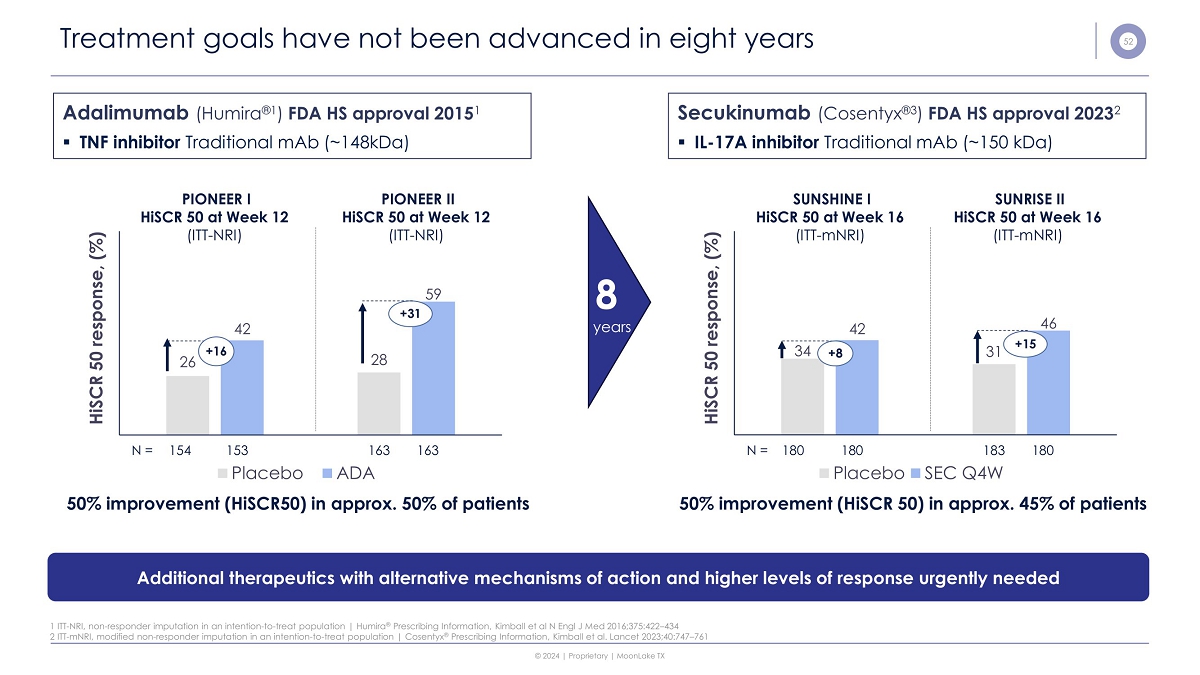
52 治療目標八年來未取得進展其他具有替代作用機制和更高反應水平的療法迫切需要 26 28 42 59 HiSCR 50 反應,(%)180 183 180 N = 180 163 163 154 N = SEC Q4W 安慰劑 ADA 安慰劑 +16 +31 阿達木單抗(Humira® 1)2015 年 FDA HS 批准 1 ▪ 腫瘤壞死因子抑制劑傳統單抗(~148kDa)PIONEER I HiSCR 50 在第 12 周(ITT-NRI)PIONEER II HiSCR 50 在第 12 周(ITT-NRI),大約 50% 的患者改善了 50%(HisCR50)1 ITT——NRI,非應答者歸咎意在——治療人羣 | Humira® 處方信息,Kimball 等人 N Engl J Med 2016;375:422 — 434 31 42 46 HiSCR 50 反應,(%) +8 +15 Secukinumab (Cosentyx® 3) FDA HS 批准 2023 2 ▪ IL-17A 抑制劑傳統單抗(~150 kDa)SUNSINE I HiSCR 50 在第 16 周(ITT-mnRI)SUNRISE II 第 16 周 HiSCR 50(ITT-mnRI)大約 45% 的患者 8 年改善 50%(HisCR 50)2 ITT——mnRI,修改了非反應者歸因,意圖——治療人羣 | Cosentyx® 處方信息,Kimball 等人《柳葉刀》2023;40:747 — 761 © 2024 | 專有 | 德克薩斯州月湖

29 45 48 32 54 52 BKZ 安慰劑 BKZ BKZ 安慰劑 BKZ BKZ 安慰劑 BKZ BKZ 安慰劑 BKZ BKZ 安慰劑 Q2W Q2W Q2W Q2W Q2W Q2W Q4W Q4W Q2W Q2W Q2W 第 16 周(ITT-mnRI)的主要終點 HiSCR 50 我被聽見 II PBO N=~73,BKZ N=~73,BKZ N=~~~~~~~ 每隻手臂 290 53 能否在 HS 中瞄準 IL-17A + IL-17F 的預先治療目標?+19 Bimekizumab (Bimzelx®) ▪ IL-17A 和 IL-F 抑制劑傳統單抗(約 150kDa)• 安全概況:無意外發現(如 MOA 預期的那樣出現口腔念珠菌病)• 維持反應:第 3 期數據顯示持續療效至第 48 周 +16 +22 +20 +20 +20 第 16 周 +22 +20 18 25 33 34 36 +15 +7 +18 +20 次要終點 HiSCR 75(ITT-mnRI) BE HEARD I BE BE HEARD IE BE HEARD II PBO N=~73,BKZ N=~290 每隻手臂 Kimball 等人 AAD 2023;最新演示 © 2024 | 專有技術 | MoonLake TX mnRI;修改後的非響應者歸因,由於不良事件或缺乏療效,以及全身性抗生素的啟動或強化,被歸咎為非反應提升試驗終點 • 主要終點反應在早期 HS 試驗的報告範圍內 • HisCR 75 數據表明,HisCR 75 數據表明,HISCR 50 的閾值反應可能高於 HisCR 50

54 HS 中 IL-17A + IL-17F 升高:靶向兩種細胞因子的理由 IL-17A 和 IL-17F 在 HS 病變,包括炎性結節和排水隧道 1 10 100 IL-17F (pg/mL) 0.1 1 10 100 IL-17A (pg/mL) * P

55 納米抗體® 能否改善 HS 的結果?白蛋白-結合結構域靶向炎症較小的生物製劑較高的組織吸收 1 納米抗體® 的積累 2 抗腫瘤壞死因子納米抗體® +/-白蛋白-結合位點的分佈 24 小時後膠原蛋白誘發的關節炎 100 90 70 60 50 40 30 20 10 0 0 50 150 150 生物分子量 (kDa) 生物分佈係數 1 (%)-50%-50% 較小的生物製劑諸如 Nanobodies® 之類的藥物可能包含白蛋白-結合結構域以靶向炎症並延長半衰期 2 不含白蛋白的 Nanobody®-結合位點 Nanobody® 與白蛋白結合位點抗腫瘤壞死因子抗腫瘤壞死因子抗腫瘤壞死因子抗白蛋白關節炎僅在左爪中誘發性關節炎 1 生物分佈係數,按肌肉中的組織濃度/血漿濃度計算(其他組織分子量變化在 14 到 41 kDa 之間,組織穿透率差異為 50%);Li 等人 mAbs 2016;8:113 — 9 組織穿透率每約 35 kDa 可降低 50% Nanobodies® 旨在直接靶向難以觸及的炎症部位組織,例如 HS 3 2 Coppieters 等人中的深層真皮隧道Arthritis Rheum 2006;54:1856 — 66 3 Krueger 等人 Br J Dermatol 2024;190:149 — 162 © 2024 | 專有 | 德克薩斯州月湖

27.9 65.7 53.0 安慰劑 N=68 SLK 120 mg N=67 SLK 240 mg N=66 14.7 43.3 34.8 0 20 40 60 80 安慰劑 N=68 SLK 120 mg N=67 SLK 240 mg N=66 參與者獲得緩解 (%) 56 在 MIRA 試驗中,索內洛基單抗的反應水平很高 SLK 在第 12 周的療效 SLK 在較高的閾值下實現了疼痛反應 NRS 50 同行評審的第 24 週數據將於太平洋標準時間 14:00 在 AAD Late 突破性研究會議上公佈,索內洛基單抗耐受性良好,沒有意想不到的安全發現 4.3 0 20 40 60 80 安慰劑 N=47 SLK 120 mg N=50 SLK 240 mg N=46參與者在 HS 試驗中首次達到 NRS 50 (%) *** 32.0 *** 41.3 疼痛 NRS 50 (ITT-NRI) 主要終點 hisCR 75 (ITT-NRI) 關鍵次要終點 hiSCR 50 (ITT-NRI) +29 +20 +38 +25 Kimball 等人 EADV 2023;最新演示 D1T01.1H © 2024 | 專有 | MoonLake TX 最高等級的安慰劑——迄今為止報告的調整後的 HisCR 反應的疼痛閾值高於先前的 HS 研究

57 一項探索性超聲子研究測量了排水隧道變化的直接證據,皮膚下方的 SLK 成像病變顯示對隧道有直接影響基線第 12 周 • 對隨機分配到索內洛基單抗 240 mg 治療組的參與者的案例研究 • 第 12 周 32.7 30 23.8 20 * .1 0 10 40 50 安慰劑 (n=63) Sonelokimab 120 mg (n=63) Sonelokimab 120 mg (n=63) 56) Sonelokimab 240 mg (n=52) 參與者在第 12 周 (NRI) 第 3 階段達到 DT 100 (%) 排水隧道 (DT 100) 的完全分辨率至關重要為了更好地瞭解SLK作為納米體改善臨牀療效的潛力,超聲圖像顯示基線和第12周的排水隧道相同(白色箭頭);彩色陰影區域表示活動性炎症(隧道周圍血流量增加的雙重信號;灰色箭頭)| Kirby等人ISDS 2023;P260 © 2024 | 專有產品 | MoonLake TX

58 第三階段的關鍵目標將是保持與第二階段的一致性,同時在 MIRA 之後始終保持以患者為中心的關注點:我希望在 3 期計劃中看到的終點選擇高級終點,例如 HiSCR 75、DT 100、IHS4-100 查看高水平終點並將重症患者包括在內反映臨牀實踐中的患者維持反應評估治療效果的持續時間至關重要患者羣體基線疾病嚴重程度是解釋的關鍵結果基於風險的最佳劑量—收益監管機構提供的證據 SIMPLE PROTOCOL 與 MIRA 一致的協議,對皮膚有吸引力隊列規模招收足夠數量的患者以滿足監管機構的要求 Kenneth B. Gordon 教授的專家意見 © 2024 | 專有 | MoonLake TX 第 3 階段

© 2024 | 機密和專有 | MoonLake TX 59 SLK 差異化和第 3 階段計劃 Kristian Reich

注意:這是一項跨試驗的比較,但存在固有的侷限性。沒有對頭試驗。1 POV 使用平均氨基酸數量減少作為主要終點 2 使用第 12 周 PLC 劑量的 2 個交叉組的平均反應(從 PLC 到 SLK 劑量從第 8 周開始)以及 120 mg 組的 wk 16 反應;PLC、安慰劑;SLK、Sonelokimab(MIRA 研究);BK,Sonelokimab(MIRA 研究);BK,BK,Sonelokimab(MIRA 研究);BK Bimekizumab(合併為 BE HEAR I/II);ADA、Adalimumab(合併為 PIONEER I/II);POV,Povorcitinhib(NCT 04476043);UPA,Upadacitinib(NCT 04430855);SEC,Secukinumab(合併日出/陽光)來源:MoonLake Clinical(2023 年 6 月 27 日研發日)© 2024 | 專有 | MoonLake TX 60 回顧:為主要終端設定 HS 的新標準 19 24 17 15 11 SLK BKZ ADA POV UPA SEC 18 16 13 POV 16 75mg (mnRI) n.d. SEC Wk 16 75mg (mnRI) n.d. UPA Wk 12 30mg (mnRI) SLK BKZ ADA Wk 12 Wk Wk 12 Wk 16 Wk 12 120 mg 320mg 40mg (NRI) (mnRI,All-Abx) (NRI) HisCr50 delta 到 PLC(其他人的主要終點 1)最佳劑量的增量百分比,初步分析 * p

HS:SLK的反應持續到第24周增加,月劑量HisCr90反應百分比(%)分數達到分數週通過便捷的每月注射達到Hiscr75的患者人數顯著增加通過每月維持劑量加深反應,在第24周之前有近40%的患者達到Hiscr90 1 ITT——NRI數據截至第12周(A部分)2從第14-24周(B部分)觀察到的數據43.3 53.3 6.9 0 10 20 30 40 50 Hiscr75 響應(主要終點)達到分數的百分比(%)分數 60 0 2 4 6 8 10 12 14 16 18 20 22 24 PLC SLK 120mg SLK 240mg 14。7 A 部分 1 第 B 部分 2 22.4 37.9 7.4 部分 A 1 0 10 30 40 0 2 4 6 8 10 12 14 16 18 20 22 24 部分 B 2 Hiscr100 = 29.3% (W24,SLK 120mg) 10 ppt + 40 ppt + 14 ppt + 30 ppt + 30 ppt + 來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 61

十分之四分 1 分 HS:SLK 允許患者和醫生瞄準炎症緩解每月 SLK 加深 IHS4 反應(例如,IHS4-90 和 IHS4-100)大約四分之一的 HS 患者每月服用 SLK 120mg 達到炎症緩解(IHS4-100)1 ITT——NRI 數據高達 12 周;如第 12 周之後的觀測數據 10.3 23.9 39.7 18.2 22.4 SLK 120mg SLK 120mg PLC SLK 240mg SLK 240mg IHS4-90 回覆百分比(%)得分 1 周 12(A 部分)第 12 周(B 部分)第 12 周(A 部分)第 24 周(B 部分)第 12 周(B 部分)第 12 周(A 部分)第 12 周(B 部分)周24(B 部分)SLK 120mg SLK 120mg PLC SLK 240mg SLK 240mg IHS4-100 響應百分比(%)分數達到分數 1 ~12 ppt 5.9 來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 62 11.9 24.1 9.1 15.5

來源:© 2024 | 專有 | MoonLake TX 63 HS:結果令人震驚,證實了 SLK 是潛在的領導者 MoonLake Corporate 更高 Hiscr75,第四季度劑量 57% 的患者在 24 周達到 HisCR75,反應深度增加 40% 的患者達到 HisCR90 和 IHS4-90 個(14ppt +)每4名炎症緩解患者中就有1名疾病控制(IHS4-100) 和 40% 以上報告疾病活性不存在或微乎其微 (PGI-S) 經證實的最佳劑量 120 mg 是全面表現最佳劑量,劑量行為可複製第 12 周的劑量對腫瘤壞死因子患者的影響第 24 周患者對 SLK 的反應比 ADA 的反應更好;非反應者在 12 周內達到類似 SLK 的反應良好的安全性概況沒有新信號、沒有 IBD 或惡性腫瘤、單克隆抗體(如 ISR 率)、念珠菌(如果有)是短暫的,沒有停藥

1 按赫利階段狀態(II 與 III)和先前的生物製劑用途(是/N)進行分層的隨機分層。Hurley III 期患者限制在 40% 左右;2 名受試者:連續兩次就診 Hiscr75,間隔 4 周來源:MoonLake 臨牀開發 © 2024 | 專有 | MoonLake TX HS:美國食品和藥物管理局 EoP2 會議非常積極,Hiscr75 次安慰劑篩查(2 至 4 周)安慰劑——對照安慰劑交叉索內洛基單抗 120mg:第 0、2、4、6、8 周,然後 Q4W Sonelokimab 120mg:第 16、18、20、22、24 周,然後是 Q4W 第 1 組(n=266)R 1 組 2(n = 133)OLE(最多 2 年)第 0 周 4 16 1 增 EP vs PLC 52 2 △ EP 8 24 ▪ 單劑量階段 3 — 美國食品藥品管理局同意 HS 的劑量非常嚴格清除(120mg)▪ 僅限 800 名患者(與諾華、UCB 等相比)— FDA 將 Ph 2 視為註冊狀態,並考慮其他適應症的患者數據 ▪ 所有其他領域,包括統計數據、分析等,均清晰且風險低 ▪ 允許在 2025 年中期推出主要終點,於 2027 年(BKZ 推出後 18 至 24 個月內)推出 ▪ HS 試驗的手頭現金,與其他試驗無風險 ▪ 方案相比進入第 2 階段,其統計數據可能有利於 PLC 的 delta(例如,mnRI 與 NRI)在 FDA eOp2 會議之後的 3 階段協議詳細與 FDA 和 EMA 的相互作用對應可用可比較的第 2 階段和第 3 階段協議重複協議 2x(n=800 分)— VELA I 和 II(均遵循相同的協議)

來源:© 2024 | 專有 | 德克薩斯州月湖 MoonLake ClinDev 65 2.HS:VELA 建立在 MIRA 成功的基礎上宣佈第三階段 HS 計劃:VELA I VELA II MoonLake HS 臨牀試驗仍然是唯一以 HisCR75 為主要終點的臨牀試驗

來源:MoonLake Clinical © 2024 | 專有 | MoonLake TX 66 HS:Pivotal——與其他試驗 1 Glatt 等人相比,Ph3 中複製了 MIRA 的設計。JAMA Dermatol 2021;157:1279 — 88;2 NCT03248531;3 Kimball 等人。AAD 2023;口頭陳述;4 NCT04242498;5 靈敏度分析作為主要數據在主要出版物中提供;6 沒有先前的 TnFi 或 IL-17i 根據協議 — 研究出版物中未闡明先前的其他生物學經驗 7 無主要失敗或不適合治療的患者 8 Q2W 組的平均值 AN #17.2,Q2W 組為 14.7,先前的 IL-17A/F 不包括在內,沒有主要失敗-17i 注意:不同試驗的比較,存在固有的侷限性。不是正面試驗。並非所有的試驗細節都可能被完整記錄下來。VELA 設計尚待監管部門最終批准試驗結構統計分析隊列特徵 BKZ Ph2 1,2 n=90 BKZ Ph3 (BH II) 3,4 n=509 MLTX Ph2 (MIRA) n=234 MLTX Ph3 (VELA) n=800 PPS 沒有明確的 Abx Tx 規則 NRI,如觀察到的 5 貝葉斯增強 +40 PBO,ADA 9% 安慰劑 HisCR 75 12% 停藥初級週期僅測試了一劑負荷劑量 21 名患者接受了安慰劑雙盲/安慰劑-對照組 0% 之前的生物製劑使用 6 強制性局部防腐劑 ≥3 AN 病變平均值 AN # 14.5 BKZ vs 22.1 PBO 49% Hurley II 伴發 Abx 沒有限制(未報告百分比)1 分層因子(Hurley)已測試兩劑量無負荷劑量 74 名患者接受安慰劑 13% 之前使用過生物製劑沒有強制性防腐劑 ≥5 AN 病變平均值 AN # 17.7 BKZ Q4W 8 vs 14.4 PBO 61% Hurley II 伴隨Abx限值未報告(總人羣中基線為9%)2 分層因素(Hurley,ABX)雙盲法 /安慰劑——按照 Abx Tx 規則控制 ITT mnRI 無貝葉斯增強 16% 安慰劑 HiSCR 75 ~ 8% 停藥初級期 ITT 採用 Abx Tx 規則 NRI 無貝葉斯增強 15% 安慰劑 HiSCR 75 ~ 5%停藥初級週期兩劑測試無負荷劑量 68 名患者接受了安慰劑雙盲/安慰劑-對照 18% 之前的生物製劑 7 上限為 30% 無強制性防腐劑 ≥5 AN 病變平均值 AN # 平衡 14.6 SLK 120 與 14.5 PBO 64% Hurley II 伴隨的 Abx 限值為 30%(總人羣中基線為 11%)2 個分層因素(Hurley,之前的 Bx ITT)按照 Abx Tx 規則 mnRI 無貝葉斯增強 pHiI 預計會複製 PhiI 預期停藥量低一劑測試無負荷劑量 266 名患者接受安慰劑雙盲/安慰劑——對照 30% 先前生物製劑上限 9 無強制性防腐劑 ≥5 AN 病變平衡均值預期 40% Hurley III 上限 30% 伴隨的 Abx 3 分層因子(Hurley,之前的 Bx,區域)

© 2024 | 機密和專有信息 | MoonLake TX 67 HS 是 Derm Jorge Santos da Silva 的下一個重要指標

來源:MoonLake Commercial、DRG/Clarivate、學術期刊、CBO;Komodo Health © 2024 | 專有 | MoonLake TX 回顧:預計到2035年,美國市場將增長至100億美元以上 2035年未來腫瘤壞死因子α(mAb)艾伯維只有大約 50% 的患者在第12周達到Hiscr50——17 A(mAb)諾華略有下降與 Humira 相比功效但反應持久安全性有限反應耐久性 (

市場:龐大的市場規模得到了真實世界數據的證實。注:生物製劑(Bx)包括其他靶向療法(例如JAKs、PDE4i);1.2016-2023年診斷為HS且年齡在18歲以上的患者;根據約75%的索賠覆蓋率(美國索賠數據)推斷;2. 根據約75%的覆蓋率(美國索賠數據)推斷;2. 2016-2023年每年新診斷的HS患者的歷史平均值,基於約75%的覆蓋率;3.在 2023 年有 HS 相關的 Bx 處方並在 2016-2023 年被診斷為 HS 的患者;4.基於給定年份持有 HS 相關 Bx 處方的患者的歷史增長情況以及之前的 HS 診斷關鍵見解(推斷為 100% 的美國人口)▪ 來自處方索賠數據的獨一無二的美國患者 ▪ 約2.5億名美國患者生活(覆蓋率約 75%)▪ 診斷和治療的患者 HS 診斷(ICD-10 L73.2)約 200 萬名在 2016-2023 年診斷和治療的獨特患者 1 證實了大量現有 HS 人羣 ~ 25% 的增長 p.a. 生物製劑——2016 年至 2023 年處理過的藥物 4 證實了高未滿足的需求和 Bx 市場增長潛力約 30%處方不是——2023年阿達木單抗3確認對新療法的高未滿足需求和需求每年約24萬名新診斷和治療患者(以前未確診)2 確認診斷不足和未來增長潛力索賠方法 2023年約40k/56k 阿達木單抗/生物製劑治療患者 3 確認當前Bx市場規模估計 1 2 名美國成人 HS 患者來源:MoonLake Commercial,© 2023 Komodo Health, Inc. 版權所有。© 2024 | 專有權 | MoonLake TX 69

市場:僅索賠就顯示約200萬名HS患者——不包括未確診的2.0 2.9 0.9 1.9 4.8 1。包括在2016年至2023年期間被診斷為HS的18歲以上的患者;根據約75%的索賠覆蓋率推斷——顯示有0.8%的美國人口被診斷和治療了HS;2.將200萬名患者(0.8%)的患病率擴大到2.1%(根據文獻——見腳註4);3.基於2024-2027年每年淨新診斷的HS患者的歷史平均水平推斷;基於約75%的美國索賠承保範圍;4.Prens L. 等人Br J Dermatol. 2022年患病率每年淨新增患者24萬——預計美國成年HS患者歷史平均水平今天已確診1可能在發佈前確診3在峯值之前有額外的增長機會索賠證實了HS市場的重要今天我們已經看到約1%的被診斷和治療人口的市場規模基於峯值(2035年)的市場規模(2027年)3 24萬淨新增患者—預計歷史平均水平1 ~ 1% ~ 2% 文獻估計 4 已診斷和治療 1 ~5.5 2 來源:MoonLake Commercial,© 2023 Komodo Health, Inc. All版權所有。© 2024 | 專有權 | MoonLake TX 70
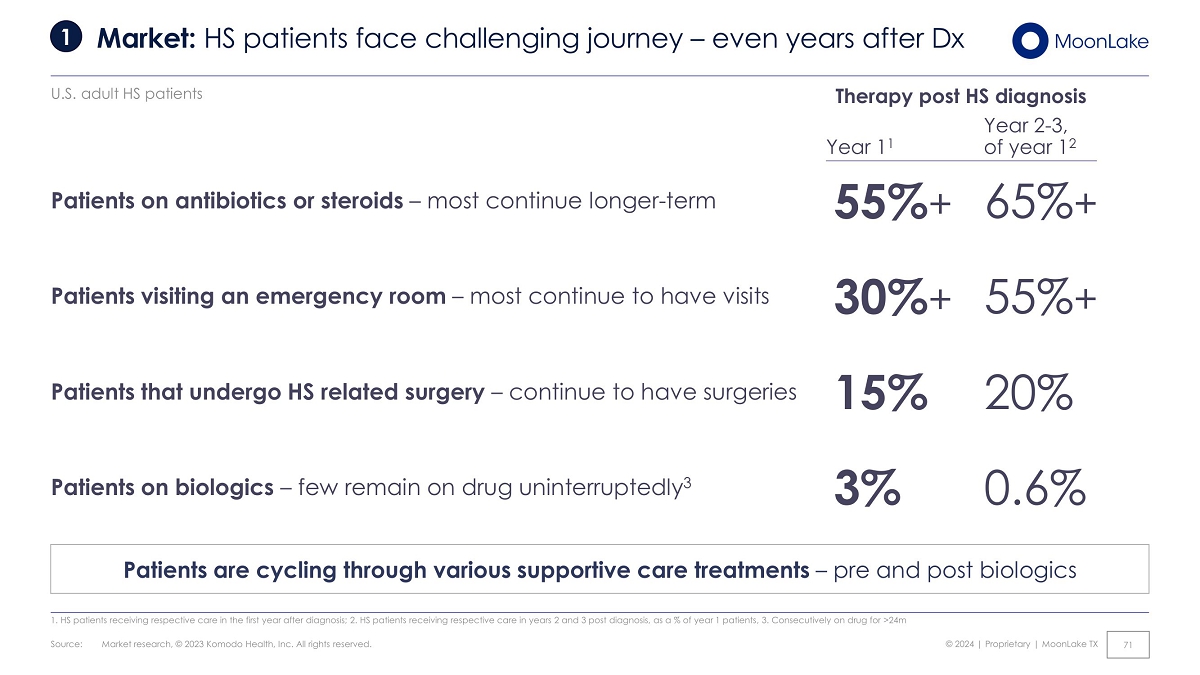
1。HS 患者在診斷後的第一年內接受相應的治療;2.HS 患者在診斷後第 2 年和第 3 年分別接受治療,佔第 1 年患者的百分比,3。連續服藥價格超過2400萬美元來源:市場研究,© 2023 Komodo Health, Inc. 版權所有。© 2024 | 專有 | MoonLake TX 市場:HS 患者面臨着艱難的旅程——即使在 Dx 美國成人 HS 患者治療後 2 年到第 3 年、第 1 年第 1 年、第 1 年 2 年患者仍在循環接受各種支持性護理治療——生物製劑前後 71 1 患者——大多數持續時間更長-學期 55% + 65% + 30% + 55% + 15% 20% 3% 0.6% 接受 HS 相關手術的患者 — 繼續接受手術患者去急診室看病——大多數人繼續去看病人服用生物製劑——很少有人不間斷地服藥 3

來源:MoonLake Commercial,© 2023 Komodo Health, Inc. 版權所有...N Engl J Med 2016;375:422-434;JAMA Dermatol。2022 年 2 月;158 (2):1 — 5。© 2024 | 專有 | MoonLake TX 試驗結果:9m 後反應維持不變 ~ 35% ~ 55% ~ 30% 的患者按接受治療的月數(處方填充間隔時間大於 3 個月作為新療法)xx 索賠療法數據中位持續時間 (m) 在現實世界的患者中,阿達木單抗的治療時間有限(中位數約為1100萬次),使他們沒有有效的 HS 治療選擇索賠:治療時間(n=53k)1 2 ~11m 中位持續時間治療與美國的准入和負擔能力障礙無關,9 15 ~ 70% 29 11 鑑於歐洲的研究顯示了相似的結果 2 市場:阿達木單抗在現實世界中反應時間有限 1.2016至2023年期間,有處方的HS相關阿達木單抗患者的平均治療時間從2022年開始至2022年;2.例如,Prens L.M. 等人Br J Dermatol. 2021 年 7 月;185 (1): 177-184. doi: 10.1111/bjd.19863,Ring H.C. 等人。JAMA Dermatol. 2022 年 2 月 1 日;158 (2): 184-188. doi: 10.1001/jamadermatol.2021.4805. 72 1

17 21 12 11 25 15 32 17 17 7 13 6 19 22 29 32 50 56 240-310 9 39 13 10 9 40 +24% 1.在相應年份和之前有 HS 相關生物製劑處方的患者;包括 JAK 和 PDE4i;2.2017-2023年,之前被診斷為AD的患者的Bx的年增長率;3.相應年份持有HS相關生物製劑處方的患者佔每年接受HS治療人口的百分比(約65%);4.2023 年持有 psO/axSPA/psA 相關生物製劑處方的患者佔2016-2023 年診斷為 psO/axSPA/psA 的患者總數的百分比 Bx 佔每年接受治療患者的百分比 3: ▪ 從 2016 年到 2023 年 Bx 治療強勁增長至每年 25% 左右 ▪ 由於 Bx 療效有限和 Adalimumamai 耐久性低,今天的 Bx 份額從很小的基數開始 b(約佔每年接受治療的患者的3%)▪ 約佔Humira以外的Bx治療(例如ixekizumab)的30%,這進一步凸顯了美國市場對新穎有效的治療選擇的需求: 預計增長和未得到滿足的需求將保持在較高水平 HS 生物製劑和靶向治療患者 (k) 1 3% 8-10% 100% 的現有淨新類似物(pSO、axSPA、pSA、AD)自Bx推出以來每年增長4~40% 2016 2017 2018 2023 2023 2023 2023 2035 2023年聲稱不假設歷史性增長,峯值2的Bx份額為8-10%: MoonLake 商業、市場研究,© 2023 Komodo Health, Inc. 版權所有。© 2024 | 專有 | MoonLake TX 73

0.5 0.5 0.3 0.5 市場:Humira佔當前20億美元以上的生物製劑市場的大部分競爭對手接受治療的患者(k)2023年1份索賠尚未100%獲得(時差)美國市場(2023年—第四季度索賠未完全保障)X 2023年填充率(年)2 X淨價格(美元)3 =收入(十億美元)總額1。包括在 2023 年有相應藥物處方和相應的 HS 診斷(美國索賠數據)的患者;2.基於2023年所有患者使用相應藥物的平均供應天數(2023年所有有處方的患者的平均填充率);3.按年化WAC(用於維持治療)計算,減去總GTN,包括服務費、法定和保密的全權退税等(基於市場研究);4.包括 JAK 和 PDE4i 41 4 4 12 1.6 0.1

1。在相應年份開過生物製劑處方且之前有過PSo診斷的患者;來源:市場研究,© 2023 Komodo Health, Inc. 版權所有。© 2024 | 專有 | MoonLake TX 35% 9% 32% 11% 13% 2% 23% 13% 5% 23% 5% 11% 9% 10% 12% 9% 19% 154 262 305 419 447 573 +21% ▪ 更好臨牀概況最重要:在分別推出之後,Cosentyx和Skyrizi佔據了很大的市場份額 ▪ 新進入者正在發展市場:生物製劑市場一經推出,就大幅增長(Skyrizi)佔市場增長的40%)▪ 儘管稍後推出,但仍可以建立疾病領域的領導地位:在20多個生物製劑競爭對手中,Skyrizi是pSO的市場領導者(2023年約佔19%的份額)市場:pSO顯示出臨牀差異化對市場的勝利。(k)1 2 新進入者在pSO中佔據相當大的份額,並通過提高療效和設定新的治療結果標準來提高市場增長率(例如,PASI100),儘管不是第一個進入市場的其他股票 delta '23 vs 16'-2pt Humira(2005)Cosentyx(2015)Skyrizi(2019)藥物:(上市)-18pt +2pt +19pt 自推出以來總市場增長的40%包括20多種產品Cosentyx市場份額快速增長——發佈後上升,高達13% 2016 2017 2018 2019 2021 2021 2022 2023

根據索賠推斷,美國成人HS生物製劑市場估計為480萬份 1 ~ 10% 類似物 ~ 15%(psA、axSPA 3)~ 8% 診斷患病率生物製劑採用率 1.2016-2023年診斷為HS的患者年齡在18歲以上的患者;根據約75%的索賠覆蓋率進行推斷,進一步保守地推斷出2024-2027年每年淨新診斷的HS患者的歷史平均值和2028年至2035年每年淨新診斷的HS患者歷史平均水平的約70%;假設基於約75%的索賠覆蓋率,2。2023 年持有 psO/axSPA/pSA 相關處方的患者佔2016-2023年診斷為 psO/axSPA/psA 的患者總數的百分比;3. 根據 SLK 機會和 Humira(類似 Humira)的價格推斷出來來源:MoonLake Commercial,© 2023 Komodo Health, Inc. 版權所有。© 2024 | 專有 | MoonLake TX 市場:美國市場可能比 Hus 還要大 2035年100億美元通過最近的索賠分析,我們不僅可以證實預計的2035年美國100億美元市場,而且我們認為美國真正的HS市場有潛力變成 150 億美元以上 150 億美元+ 2035 2035 美元以上 100 億美元以上 500 萬美元以上可能僅限於已診斷和治療的索賠 2 更高的 HS 意識提高了診斷和治療率更有效的治療選擇將 Bx 的採用率提高到類似物的水平根據對歷史增長非常有説服力的推斷 76

1。根據科莫多健康索賠數據:包括2022年持有Bx處方和2015-2022年HS診斷的患者來源:市場研究,© 2023 Komodo Health, Inc. 版權所有,MoonLake Commercial © 2024 | 專有 | MoonLake TX 0 20 40 60% 的美國 pts 的百分比涵蓋了大約 70% 的生物製劑治療患者 1 12% 的 HCoS 覆蓋約 70% 的生物製劑患者 1(在前 15 個州內)有針對性的 Go-To-Market 方法可以解鎖 SLK 在集中的 HS 格局中大放異彩的地位 5% 12%(約 210 個)的 HCoS 覆蓋了 Bx 分數的 50% 100 80約 12%(約 520)的 HCO 覆蓋了 70% 的 Bx pts 按州分佈 HCO 在前 15 個州的分佈目標:實現 SLK 在集中格局中的轟動地位 CA/TX 前五大城市覆蓋 60-70% 的 Bx 患者高度集中度也受成熟的 HS-CoE(65)(根據 HS 基金會的説法)服用生物製劑的美國成人 HS 患者 77

注意:各試驗間的比較,存在固有的侷限性。沒有正對頭試驗。1 Warren 等人,EADV 2021,P0353 來源:MoonLake Commercial、IQVIA、巴克萊研究、RAPID 每週審計,2023 年 11 月至 2023 年 12 月(版權所有 IQVIA),公司聲明 © 2024 | 專有 | 德克薩斯州月亮湖聖誕周(12月25日至31日)Bimzelx憑藉快速的市場吸收和良好的臨牀數據(斑塊狀牛皮癬)證實 A&F 贏得了 MoA SLK在多項試驗和臨牀結果中表現出差異化特徵 ▪ SLK在HS(MIRA試驗)的所有相關結果中,在第12周和第24周均顯示出領先的反應,包括成為第一個使用HisCR75作為主要終點的患者,在不同的HiSCR中顯示安慰劑的增量最大,使四分之一的患者實現炎症緩解,顯示出對隧道的影響等。▪ SLK在第12周和第24周的psA(ARGO試驗)的所有相關結果中均顯示出領先的反應,尤其是在其他藥物似乎表現不佳的多域評分中 ▪ 銀屑病(pSO)的原始數據表明 SLK在皮膚炎症方面也具有領先的反應,可以維持長期的反應 Bimzelx在皮膚炎症方面處於領先地位伊利諾伊州17級的動態市場份額,份額達到約40%競爭:Bimzelx超出預期— SLK進一步脱穎而出 78

來源:產品宣傳單、公司信息、MoonLake Commercial © 2024 | 專有 | MoonLake TX 79 HS:SLK 最方便維護注射時間表每 1 毫升注射器 15 秒注射時間 1 次 1 次 1 次注射時間大幅減少、速度更快(注射速度快 5 倍)注意:Bimzelx 為 320 mg,Cosentyx 為 300 mg,每次使用 2 個注射器,然後每兩週注射一次 [Q2W]已應用 1.試驗包括Q2W和Q4W給藥方案(均需要注射2次)——待實際標籤注射)和300mg/2ml的注射筆;標準劑量為Q4W,但可能改為300mg Q2W。每個 1 毫升注射器 2 個 150 毫克(4 個 SLK),注射時間為 15 秒 2

© 2024 | 專有 | 德克薩斯州MoonLake 來源:回顧:HS提供了一個龐大的市場,未得到滿足的需求 MoonLake Commercial 80 ▪ 規模龐大、診斷不足的市場:如今有200萬名患者,每年超過24萬名新診斷患者 ▪ 儘管起步基礎很小(2016年約為1.3萬人),但生物製劑市場仍在快速增長(每年25%):軌跡與pSO、AD等其他市場相似 ▪ 嚴重的未滿足需求當前的選擇:患者在沒有疾病控制的情況下循環 ▪ HS 會給患者和衞生系統帶來巨大負擔(急診室就診、手術、藥物治療)▪ SLK有可能成為差異化最大的患者:ADA患者約1,100萬人,SEC患者需要約4倍才能獲得SLK預後(HisCR50),關鍵分數高出10-20個百分點,而BKZ市場可能是炎症領域最大的市場(超過150億),並且能夠容納不同的參與者:SLK被定位為潛在的領導者

© 2024 | 專有 | MoonLake TX 新適應症 SLK 和 MLTX 81 的新前沿

1 Liu S 等人Nat Commun. 2013;4:1888;2 Goepfert A 等。免疫。2020 年 3 月 17 日;52 (3): 499-512 來源:MoonLake Research © 2024 | 專利 | MoonLake TX 82 SLK 是一種獨特的分子:靶向 IL-17 A 和 F IL-17A 和 IL-17F 的納米體® 通過激活 IL-17RA 和 RC 受體複合物起到二聚體的作用,通過激活 IL-17RA 和 RC 受體複合物不同的 IL-17RA 和 RC 鏈結合形成不同的 IL-17RA 和 RC 鏈對不同二聚體的親和力 1,2 並非所有 IL-17-靶向療法都能抑制 IL-17A/A、IL-17A/F 和 IL-17F/F 二聚體 A/A A/F F/F 二聚體 A/A A/F F/F 説明受體 A/A F/F SLK 的二聚體親和力是唯一能結合所有二聚體且具有相似親和力的資產

來源:© 2024 | 專有 | MoonLake TX 自適應 T 細胞 Th、Tc 細胞先天淋巴細胞 T 細胞、ILC3、MAIT 中性粒細胞 IL-23 IL-1 IL-1 IL-18 IL-6 TGF TCR 激活 TNF IL-12 c5a 差異激活差異產生 IL-17A IL-19 IL-36 CXCL1 CXCL8 CCL20 MoonLake Clinical 83 Key MoA: IL-IL-12 c5a 差異激活差異化產生 IL-17A IL-19 IL-36 MoonLake Clinical 83 Key MoA: IL-IL-IL-12 C517A 和 F 是許多炎症途徑的癥結所在。不同的細胞類型優先產生 IL-17 A 和/或 F 多種刺激誘導免疫細胞亞羣產生 IL-17A 和 F IL-17A 和 F 誘導多種促炎性效應因子,例如激活角質細胞 IL-17A 和 F 作為許多病理的 “瓶頸”。靶向 IL-17A 和 F 的上游或下游途徑,由於路徑宂餘,已導致多次失敗

84 除了 HS 和 psA MLTX 核心適應症以外,許多疾病都將 IL-17A&F 作為關鍵途徑(Onco、CV)其他適應症(Onco、CV)潛在市場規模 NSCLC Nr-axSPA PM DM GCA Takayasu SLE LN ssc Behcet 的 PPP GP 糠疹 (PG) BC RCC GC OC OC AIC AIC H UC CD SC PBC (PSC) MIR gvHD GBS COPD RA NIU AS HS psA Plaque Plus psO Plaque Plus psO 排除的適應症(示例)Derm Rheum Auto 43 37 150+ JIA(RF-)Juv HS 縮寫:HS(化膿性汗腺炎)、psA(銀屑病關節炎)、AS(強直性脊柱炎或放射學軸向性脊柱關節炎)、nr-axSPA(非射線照相軸向脊柱關節炎)、pSO(銀屑病)、AIH(自身免疫性肝炎)、PSC(原發性硬化性膽管炎)、PBC(原發性膽汁性膽管炎)、gvHD(移植物與宿主病)、GBS(吉蘭-巴雷綜合徵)、PM(多肌炎)SLE)、DM(皮肌炎)、GCA(鉅細胞動脈炎)、NIU(非傳染性葡萄膜炎)、SLE(系統性紅斑狼瘡)、LN(狼瘡腎炎)、ssC(系統性硬化)、JIA(幼年特發性關節炎)、PPP(棕櫚-足底膿皰病)、GPP(全身性膿皰病)牛皮癬)、BC(乳腺癌、NSCLC(非小細胞肺癌)、GC(胃癌)、RCC(腎細胞癌)、A-HCC(酒精相關肝細胞癌)、MIR(心肌缺血和再灌注)來源:臨牀和科學出版物,MoonLake © 2024 | 專有 | MoonLake TX
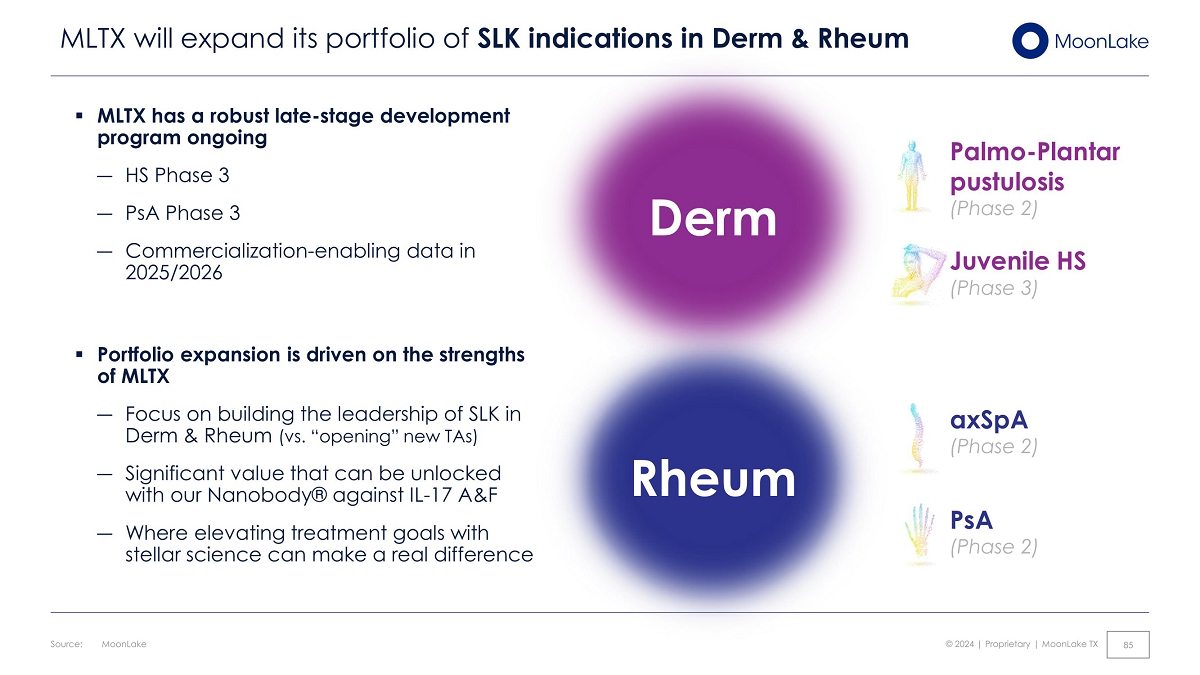
▪ MLTX 正在進行一項強有力的後期開發計劃 ― HS 第 3 階段 ― pSA 第 3 階段 ― 商業化 — 2025/2026 年的支持數據 ▪ 投資組合擴張由 MLTX 的優勢推動——專注於建立 SLK 在 Derm & Rheum 領域的領導地位(與 “開啟” 新協議)——我們的Nanobody® 對抗 IL-17 A&F — 提升治療目標在哪裏科學可以帶來真正的改變 MLTX 將擴大其在 Derm & Rheum Derm Palmo-足底膿皰病(第 2 期)幼兒 HS(第 3 期)中的 SLK 適應症組合axSpa(第 2 階段)pSA(第 2 階段)Rheum 來源:MoonLake © 2024 | 專有 | MoonLake TX 85

新適應症如何推動MLTX 1的價值 Merola J. 等人(2018)。皮膚病療法;31:e12589。doi.org/10.1111/dth.12589 和 Chimenti 等人(2020 年)。生物製劑;14:53-75. doi:10.2147/BTT;2 Passeron 等人(2023 年)。JAMA Dermatol. doi: 10.1001/jamadermatol.2023.5051;3 疾病控制有限 — 即使處於較低水平:根據 ATLAS 試驗數據,大約 40% 的 Humira pts 在 w12 時無法達到 ASAS20;4 基於 BE MOBILE 的試驗結果 PPP(第 2 階段)▪ “類似 HS” 的疾病,皮膚的關鍵優先事項,大量未得到滿足的需求 ▪ 高達 10-15% 的 pSO 患者有手足麻痺症 BKZ 案例系列 2 Derm Rheum 顯示了 IL17 A&F 的相關性。來源:MoonLake © 2024 | 專有 | MoonLake TX 86 ▪

1。帕瑟隆等人(2023)。JAMA Dermatol. doi: 10.1001/jamadermatol.2023.5051;2 Brunasso A. & Massone C (2021)。Fac Rev.;Twelves 等人(2019.J Allergy Clin Immunol,143 (3): 1021-1026。以及 Misiak-Galazka,M.(2020)。Am J Clin Dermatol 21、355 — 370。;3 Merola J. 等人(2018 年)。皮膚病療法;31:e12589。doi.org/10.1111/dth.12589 和 Chimenti 等人(2020 年)。生物製劑;14:53-75。doi:10.2147/BTT 來源:MoonLake 團隊 © 2024 | 專有 | MoonLake TX PPP:提升作為 Derm 87 SLK 領先創新者的地位可以實現高度差異... 在沒有有效治療的嚴重疾病中... 通過開闢新天地,其他人放棄將PPPasi作為主要終點來提高門檻以建立更廣泛的治療方法客觀炎症終點作為額外分數目標具有競爭力的試驗患者數量,主要PPP場所的設計極具吸引力,被認為足以轉移到第三階段甚至獲得批准,成功讀出2037年以後的銷售額為10億美元在掌足受累的pSO患者中 3 0.3% 4+ ~10-15% 全球患病率 0 批准或有效的治療方案 IL-17 A&F 是最有希望的 MoA 考慮到 BKZ 病例 1,此前考慮到病變的深層組織位置(類似於 HS 隧道、深層皮膚膿皰等),A&F 是最有希望的 MoA) 有可能在美國和美國率先上市,併為皮膚市場規模增加另一種獨特的療法慢性炎症:Crops of膿皰導致疼痛和出血 2 未獲批准的治療多個 MOA 失敗(例如,伊利諾伊州-1,伊利諾伊州-12/23s,伊利諾伊州-36,伊利諾伊州-17)未滿足的需求

新適應症如何推動MLTX PPP(第 2 階段)的價值 ▪ “類似 HS” 的疾病,皮膚的重中之重,大量未得到滿足的需求 ▪ 高達 10-15% 的 pSO 患者有掌瓣受累 1 ▪ IL17 A&F 的相關性 BKZ 案例系列 2 Derm Rheum ▪ 首次針對青少年 HS 的臨牀試驗,解決真皮的關鍵缺口 ▪ 有機會控制進展性疾病在不可逆損傷之前的損傷 ▪ 與成人 HS Ph 3 平行,可以作為 “高中領導者” Juv HS(第 3 階段)1 Merola J. 等人(2018 年)進一步脱穎而出。皮膚病療法;31:e12589。doi.org/10.1111/dth.12589 和 Chimenti 等人(2020 年)。生物製劑;14:53-75. doi:10.2147/BTT;2 Passeron 等人(2023 年)。JAMA Dermatol。doi: 10.1001/jamadermatol.2023.5051;3 疾病控制有限 — 即使處於較低水平:根據 ATLAS 試驗數據,大約 40% 的 Humira pts 在 w12 時仍無法達到 ASAS20;4 基於 BE MOBILE 試驗結果來源:MoonLake © 2024 | 專有 | MoonLake TX 88

新適應症如何推動MLTX PPP(第二階段)的價值 ▪ “類似 HS” 的疾病,皮膚的重中之重,大量未得到滿足的需求 ▪ 高達約 10-15% 的 pSO 患者有掌瓣受累 1 ▪ IL17 A&F 相關性,通過BKZ 案例系列 2 axSPA(第 2 階段)顯示 ▪ 多億市場(r/nr-axSPA),當前的 SoC 3 ▪ 使用效果有限 SA 允許 MLTX 在血清陰性脊柱關節炎方面進一步處於領先地位 ▪ BKZ 病例 4 顯示了 IL17 A&F 的相關性,體積小是一種優勢 Derm Rheum ▪ 在幼兒 HS 中進行的首次臨牀試驗,解決了皮膚的關鍵差距 ▪有機會控制漸進性疾病的不可逆轉損傷 ▪ 與成人 HS Ph 3 相似,可以作為 “HS 領導者” Juv HS(第 3 階段)1 Merola J. 等人(2018)進一步脱穎而出。皮膚病療法;31:e12589。doi.org/10.1111/dth.12589 和 Chimenti 等人(2020 年)。生物製劑;14:53-75. doi:10.2147/BTT;2 Passeron 等人(2023 年)。JAMA Dermatol。doi: 10.1001/jamadermatol.2023.5051;3 疾病控制有限 — 即使處於較低水平:根據 ATLAS 試驗數據,大約 40% 的 Humira pts 在 w12 時仍無法達到 ASAS20;4 基於 BE MOBILE 試驗結果來源:MoonLake © 2024 | 專有 | MoonLake TX 89

1。根據BE MOBILE試驗結果,BKZ具有持久的療效,可有效治療合併疾病(即葡萄膜炎);2.根據美國對 AS 的索賠數據和估計:在 2015 年至 2023 年間診斷出的獨特患者(ICD-10 代碼:M45.*),並假設 AS 和 nr-axSPA 之間分成 50:50;3. 根據 ATLAS 試驗數據,大約 40% 的 Humira pts 在 w12 時未達到 ASAS20;4.Ruderman E. 等人(2013)。類風濕性關節炎。2013;65:S1052 — S1053。資料來源:MoonLake團隊;Lubrano(E.)(2018)。Clin Rev Allergy Immunol;9298。;Tahir H. 等人(2021 年)。J Exp Pharmacol. 2;13:627-635;myAS;© 2024 Komodo Health, Inc. 版權所有 © 2024 | 專有權 | MoonLake TX axSPA:通過將 axSPA 90 SLK 的護理提升到新的療效水平,擴大在 Rheum 領域的領導地位... 在需求未得到滿足的疾病中... 通過創新成像來重新定義結果衡量標準,未來10年市場潛力10億美元以上 40% 的受試者在當前療法下未達到相關改善 3 全球患病率的 1.5% 30% 作為目前進展到r的nr-axSPA患者的上限——axSPA 4的市場規模與目前一樣軸骨上部慢性炎症大量未得到滿足的需求,2015-2023年至少有150萬美國患者被診斷和治療 2 SoC 的疾病控制有限 — 即使處於較低水平 3 未得到滿足的需求 SLK 有充分的理由提高 axSPA 的護理水平 − 獲勝 MoA,IL-17A&F 抑制顯示出最持久的反應 − 關節和指甲中強勁的 SLK pSa 數據可作為脊柱炎症的代名詞 − 納米抗體難以獲益-治療深部炎症和併發症 1 使用 pSa 可讓 MLTX 在血清陰性脊柱關節炎方面進一步處於領先地位創新設計包括 PET 和 MRI 成像並行進行臨牀讀數,加速進入第 3 階段的臨牀試驗患者數量具有競爭力,保留了專科部位的精美設計。經許可轉載。

新適應症如何推動MLTX 1的價值 Merola J. 等人(2018)。皮膚病療法;31:e12589。doi.org/10.1111/dth.12589 和 Chimenti 等人(2020 年)。生物製劑;14:53-75. doi:10.2147/BTT;2 Passeron 等人(2023 年)。JAMA Dermatol. doi: 10.1001/jamadermatol.2023.5051;3 疾病控制有限 — 即使處於較低水平:根據 ATLAS 試驗數據,大約 40% 的 Humira pts 在 w12 時無法達到 ASAS20;4 基於 BE MOBILE 的試驗結果 PPP(第 2 階段)▪ “類似 HS” 的疾病,皮膚的關鍵優先事項,大量未得到滿足的需求 ▪ 高達 10-15% 的 pSO 患者有手足麻痺症足底受累 1 ▪ BKZ 病例系列 2 axSPA(第 2 期)顯示了 IL17 A&F 的相關性 ▪ 多億市場(r/nr-axSPA),但當前 SoC 的療效有限 ▪ 使用 pSA 可以讓 MLTX 在血清陰性脊柱關節炎領域進一步處於領先地位▪ BKZ 病例 4 顯示了 IL17 A&F 的相關性,體積小就是優勢 psA(第 2 階段)▪ 通過提高療效門檻來加倍研究 pSA(和脊柱關節炎)▪ 創新衡量疾病——關節、附着點炎、指關節炎的改變 ▪ 與當前的 Ph 3 平行,進一步推動商業成功 Derm Rheum ▪ 首次針對青少年 HS 的臨牀試驗,填補了皮膚的關鍵差距 ▪ 機會在不可逆轉之前控制漸進性疾病 ▪ 與成人 HS Ph 3 相似,可以進一步區分為 “HS 領導者” Juv HS(第 3 階段)來源:MoonLake © 2024 | 專有 | MoonLake TX 91

來源:MoonLake 內部機會模型,© 2024 Komodo Health, Inc. 版權所有。經許可轉載。© 2024 | 專有 | MoonLake TX 92 新適應症為數十億美元市場提供了巨大的機會 1 參見 Bimekizumab 案例系列:Passeron 等人(2023 年)。JAMA Dermatol. doi: 10.1001/jamadermatol.2023.5051;2 基於BE MOBILE的試驗結果;3 基於文獻和美國索賠數據的患病率/基於預測患病率歷史增長的全球市場規模估計,以及對關鍵假設(例如淨價格、依從性等)的MLTX研究 4.根據其他適應症的安全數據,在青少年中使用 Humira 標籤;根據 ATLAS 試驗數據,有 5 ~ 40% 的 Humira pts 在 w12 時未達到 ASAS20 PPP(第 2 階段)Juv HS(第 3 階段)axSPA(第 2 階段)psA(第 2 階段)關鍵挑戰市場規模(美元,2035)流行率(%)領先的 MoA IL-17A&F 1 IL-17A&F TNF(無試驗)伊利諾伊州-17A&F 2 TNF & IL-17A 伊利諾伊州-17A&F TNF & IL-17A 0.3% 1% 1% 3% 35-40 億美元(比 22 年增長 12%)10-20 億美元(比 22 年增長 9%)100-120 億美元(比 22 年增長 6%)150 億美元(比 22 年增長 5%)沒有批准或有效的療法沒有經過臨牀研究的產品 4SOC 5 效果不理想(例如 ACR)Derm Rheum 的功效有限

1 假設當前的第三階段計劃已與監管機構達成一致(+/-6 個月)來源:MoonLake 團隊 © 2024 | 專有 | MoonLake TX 新適應症進一步豐富了 2024 年 6 月 25 日的潛在催化劑日曆-23 日:pH2b 2023 年第二季度第三季度 2023 年第 1 季度 2025 年 3 月-24 日:PsA ph2b 24-周讀數 10 月 23 日:HS pH2b 24-週數據本週讀出 HS HS 2024 年上半年 HS 第 3 季度/第 4 季度——24:啟動 psA psA psA pSO pSO Ph3 準備就緒(2022年)2025年下半年第四季度——25/Q1——26:Ph3 第 1 個終點(16 周)1 psA x x 新研究向 SLK 增加 150-200 名患者和 25 個以上的受試地點總體計劃 PPP H2-24:研究開始(FPI)H1/H2-25:完整讀數 H1-25:最後一次患者出院(LPO)axSPA H1-25:最後一次出院(LPO)H2-25:完整讀數 H2-24:完整讀數 H2-24:研究開始(FPI)pSa H2-25:最後一次出院(LPO)H2-25:完整讀數 H2-24:研究開始(FPI)H2-24:研究開始(FPI)H1-26:完整讀數 H1-26:最後一次出院(LPO)青少年 HS 93 Q3-25:Ph3 第 1 個終點(16 周)11 月 1 日至 23 日:psA ph2b 第 1 個終點(12 周)HS x x Q1/Q2-24:啟動 Ph3 試驗

來源:© 2024 | 專有資產 | MoonLake TX MoonLake Corporate 94 潛在的新適應症可能會進一步增強SLK的潛在80億美元以上(2035年)MoonLake繼續解決炎症性疾病領域最緊迫的未得到滿足的需求。額外計劃帶來了超過30億美元的收入,繼續推動SLK作為炎症領域領先藥物的潛力。由於數據支持投資組合擴張,運營規模可以輕鬆地從當前結構的MLTX中擴大支持開發計劃和增長,直至市場推出 AxSPAPPP pSa HS Juv HS

來源:© 2024 | 專有 | MoonLake TX Moonlake Clinical 95 退後一步:MLTX 第 3 階段(啟用 BLA)psA 第 3 階段(2025/26)HS 第 3 階段(2025/26)Juv HS 第 3 階段(2026 年)下一波(第 3 期啟用)PPP 第 2 階段(2025 年)pSA 第 2 階段(2025 年)深層組織研究(包括合作)深層組織研究(包括合作)基於臨牀抽樣的 SLK 滲透率(2025-26)基於人體模型的新 TaS 產品組合擴展(2024/25)生物——知識產權——賦能 Derm & markers Rheum 項目(2024-25 年)

© 2024 | 專有 | MoonLake TX 向前邁進 96

注意:各試驗間的比較,存在固有的侷限性。沒有正對頭試驗。1 根據對2023年11種適應症(psO、RA、哮喘、AD、axSPA、CU、SLE、psA、COPD、CD、UC)的銷售情況的分析,2030 年的範圍甚至更高來源:DRG,MoonLake Corporate © 2024 | 專有資產 | MoNLake TX 97 SLK 結合了其他資產所沒有的特性一種有前途的 MoA... 和差異化分子 ▪ 高性能 SLK 顯示出最高的反應在較高的治療目標下,Hiscr75、IHS4-100、psO PASI100、psA MDA、ACR50/70+PASI90/100 和關鍵患者預後 ▪ 更高的目標相比之下將更高的主要臨牀終點組合在一起金牌——Humira®(或Cosentyx®)等標準 ▪ 提高了便利性每月 1 毫升保養注射劑並帶來了領先的益處——風險概況 ▪ 最高反應 IL-17A 和 F 抑制顯示出最高、最持久的反應(BKZ 和 SLK)▪ 良好的安全性長期以來,念珠菌(“鵝口瘡”)是主要的不良事件,與結核病、ISR、癌症、感染相比,心血管事件、死亡...(使用腫瘤壞死因子α或JAK1)▪ 潛在領導者通常獲得適應症生物銷售額的2/3(平均40億美元以上)1

前進的戰略道路保持不變當前所有者來源:MoonLake © 2024 | 專有 | MoonLake TX 98 更好的所有者

以強勁的狀況運營:B/S 現金、現金等價物和短期有價債務證券的現金超過5億美元,以百萬美元計 2023年9月30日 16 2023年第四季度至2023年第四季度至2023年12月自動櫃員機現金消耗收益2023年31日31日(不包括ATM) 31 53 期後自動櫃員機收益預估現金 496 511 包括-2025 年製造業預付款 840 萬美元預計在 2026 年底之前有足夠的現金流道,涵蓋來源:MoonLake © 2024 | 專有 | MoonLake TX 99 ▪ HS 的 Ph3 計劃 ▪ PSA 的 Ph3 項目 ▪ 其他指標工作提交 ▪ 所有其他基本支出低現金消耗繼續顯示出成本效益的設置和重點 MLTX通過自動櫃員機以最低的稀釋量增加了8,500萬美元,以加倍投資SLK的開發——目前沒有進一步籌資的計劃 ▪

來源:MoonLake Corporate © 2024 | 專有 | MoonLake TX 中性粒細胞 Th17 Th22 ILC3 IL-17 IL-22 IL-23 100 重點強化 SLK 作為 3 型疾病領導者的故事 Th2 細胞 ILC2 肥大細胞 T fh Basophil 伊利諾伊州嗜酸粒細胞-4 IL-13 IL-5 IL-31 類型 2 巨噬細胞 Th1 ILC1 NK IL-12 IL-12 IL IL-2 IL-6 TNF 1 型原代免疫細胞 1,2 關鍵細胞因子 1-3 與免疫失調相關的疾病(示例)4,6 炎症途徑 UC、CD SL E、其他 C TD 類風濕關節炎特應性皮炎過敏性哮喘 crsWNP 嗜酸性食管炎食道炎食物過敏、BP pSO、psA、HS、NR & R Ax-sP、GPP、PG、GCA、SSC、肌炎、AIH、膽管炎、腎小球病、A-HCC 等。B 細胞 B 細胞佔主導地位的天皰瘡、ITP 自發性其他 IL-1 IL-36 CAPS,DIRA 注意:根據已發佈的關鍵信息進行簡化描述,不適合本質上是詳盡無遺的。AD,特應性皮炎;IFNγ幹擾素 gamma;IL,白介素;ILC,先天淋巴樣細胞;NK,自然殺手;Tfh,濾泡助手;Th,T 助手。1 Kaiko GE 等免疫學。2008;123:326-338 2 Eyerich K,Eyerich S. J Eur Acad Dermatol Venereol。2018;32:692-703 3 3 Raphael I 等細胞因子。2015;74:5-17 4 Nakayama T 等人Annu Rev Immunol. 2017;35:53-84 5 Coates LC 等人Semin Arthrities Rheum。2016;46:291-304 6 Gandhi NA 等人Expert Rev Clin Immunol。2017;13 (5): 425-437。例如,αTL1A 例如,Dupixent 例如,Sonelokimab Type 3

© 2024 | 專有 | MoonLake TX 問答 101

W: moonlaketx.com | E: info@moonlaketx.com