
推進藥品發展。解決問題。改善生活。推進藥品發展。解決問題。改善生活。2023 年第三季度收益補充材料 2023 年 11 月 6 日 1

推進藥品發展。解決問題。改善生活。2® 免責聲明本演示文稿中的某些陳述包括1995年《私人證券訴訟改革法》所指的 “前瞻性陳述”。諸如 “相信”、“預測”、“計劃”、“期望”、“估計”、“打算”、“可能”、“將” 或這些術語的否定詞等詞語以及類似的表述旨在識別前瞻性陳述。這些前瞻性陳述包括但不限於關於我們的候選產品Anaphylm™(腎上腺素)舌下薄膜的進展和相關時機的陳述,該薄膜用於緊急治療嚴重過敏反應,包括通過臨牀開發和美國食品藥品監督管理局(FDA)的批准進行過敏反應,包括為Anaphylm提交關鍵藥代動力學(PK)臨牀試驗和其他支持性臨牀研究;關於通過臨牀開發和批准取得進展並確定時機美國食品藥品管理局對我們的候選產品Libervant™(地西泮)口腔膠片的新藥申請(NDA)與美國食品藥品管理局合作的急性治療頻繁發作活動(即發作集羣、急性重複性發作)的間歇性陳規定型發作(即發作集羣、急性重複性發作)的美國食品和藥物管理局;關於批准Libervant的美國市場準入這些年齡在12歲及以上的癲癇患者,克服了美國食品藥品管理局批准的孤兒藥市場排他性另一家公司針對該年齡組患者羣體的鼻腔噴霧劑產品延長至2027年1月;關於向美國以外的第三方許可Anaphylm的可能性;關於擴大公司製造能力和支持美國和其他國家對現有和未來潛在許可產品的需求增長的潛在和相關時機;關於公司2023年的財務前景及其增長以及未來的財務和經營業績和財務狀況;以及其他聲明那不是歷史事實。這些前瞻性陳述受到 COVID-19 全球疫情對公司業務的不確定影響,包括臨牀試驗的啟動、註冊和臨牀試驗的時間和充足性;對Anaphylm和Libervant、藥物成分和其他原材料供應鏈、製造和分銷的監管申報和監管審查及批准;以及適當勞動力和熟練專業人員的持續供應。這些前瞻性陳述基於公司當前的預期和信念,存在許多風險和不確定性,這些風險和不確定性可能導致實際業績與前瞻性陳述中描述的結果存在重大差異。此類風險和不確定性包括但不限於與公司開發工作相關的風險,包括產品開發活動和Anaphylm、Libervant和其他候選產品的臨牀試驗的時機、成本和成功的任何延遲或變化;公司在臨牀試驗中生成足夠數據以供美國食品藥品管理局批准2至5歲患者的Anaphylm和Libervant的風險;公司迴應美國食品藥品管理局對公司關鍵藥物研究方案的評論的能力,以及美國食品藥品管理局在Anaphylm第二階段末會議上確定的其他問題;美國食品藥品管理局可能需要額外的臨牀研究才能批准2至5歲患者的Anaphylm和Libervant的風險;Anaphylm和Libervant延遲或未能獲得美國食品藥品管理局批准的風險;美國食品藥品管理局克服孤兒藥七年的市場排他性而不批准Libervant進入美國市場的風險美國食品藥品管理局批准的鼻腔噴霧劑產品有效期至2027年1月,無法保證該公司將在以下方面取得成功Anaphylm和Libervant獲得上述任何美國食品藥品管理局的批准,包括任何年齡組患者的Libervant的美國市場準入;在公司獲得美國食品藥品管理局對這些2至5歲癲癇患者的Libervant保密協議的批准之前,Libervant的競爭性兒科癲癇產品將獲得美國食品藥品管理局批准的風險;與美國食品藥品管理局孤兒藥排除決定的不可預測性相關的風險性;第三方因克服 FDA 孤兒藥獨家經營權而提起訴訟的風險獲批的產品應經美國食品藥品管理局批准Libervant為該癲癇患者羣體中的任何年齡組提供美國市場準入;出於其他原因獲得Libervant市場準入的風險;與公司開發工作相關的風險,包括公司產品開發活動的時機、成本和成功的任何延遲或變化;任何競爭產品的成功風險;新產品商業化所固有的風險(包括技術風險、財務風險、市場風險和實施風險),以及監管限制);我們的候選產品(包括Anaphylm和Libervant)以及我們在美國和國外的許可產品的市場接受率和程度的風險;資本和現金資源不足的風險,包括獲得可用債務和股權融資及運營收入的渠道不足,無法滿足公司的所有短期和長期流動性和現金需求以及其他現金需求,包括為未來的臨牀開發活動提供資金 Anaphylm、Libervant 和我們的其他產品候選人;我們的製造能力足以支持美國和其他國家對現有和未來潛在許可產品的需求的風險;我們的基礎業務實現增長的風險;任何競爭產品的成功風險;Suboxone® 市場份額下降的風險以及作為佔我們當前營業收入很大一部分的產品衰退的風險;產品市場規模和增長的風險;遵守所有FDA和其他產品的風險政府和客户對我們的要求製造設施;與公司產品相關的知識產權和侵權索賠的相關風險;意想不到的專利開發風險;與總體經濟、政治(包括戰爭和恐怖主義行為)、商業、行業、監管、金融和市場狀況以及其他不尋常事項相關的不確定性;以及 “風險因素” 部分和公司2022年10-K表年度報告、10-Q表季度報告中所述的影響公司的其他風險和不確定性,以及向美國證券交易委員會提交的 8-K 表最新報告。鑑於這些不確定性,您不應過分依賴這些前瞻性陳述,這些陳述僅代表截至發佈之日。本警示聲明明確規定了隨後歸因於公司或任何代表公司行事的人的所有前瞻性陳述。除非適用法律要求,否則在本演示文稿發佈之日之後,無論是由於新信息、未來事件還是其他原因,公司均沒有義務更新前瞻性陳述、展望或指導。本演示文稿中包含的與截至2023年9月30日的九個月有關的財務信息是初步的,未經審計,可能隨時變動。因此,公司的獨立審計師沒有對此類初步信息進行審計、研究、審查或執行任何程序,因此,他們沒有就此發表意見或提供任何其他形式的保證。我們截至2023年9月30日的九個月的財務結算程序尚未完成,因此,無法保證此類初步業績表明公司的未來業績,實際業績可能存在重大差異。PharmFilm® 和 Aquestive 徽標是 Aquestive Therapeutics, Inc. 的註冊商標。AQST-109 “Anaphylm” 的商品名稱已獲得美國食品藥品管理局的有條件批准。Anaphylm™ 專有名稱的最終批准取決於美國食品藥品管理局對候選產品 AQST-109 的批准。此處提及的所有其他註冊商標均為其各自所有者的財產。© 2023 Aquestive Therapeutics, Inc.的財產

推進藥品發展。解決問題。改善生活。3 2023 年第三季度收益:關鍵信息 AnaphylmTM(腎上腺素)語言下影片收到美國食品藥品管理局對關鍵研究協議的積極反饋將於 2023 年第四季度開始關鍵研究繼續積極尋求美國境外許可機會 Anaphylm 財務業績於 11 月完成債務再融資,截至 2025 年 6 月,FY2023 年初至今收入與 FY2022 同期相比增長了 25%(調整後)用於 Sympazan®(clobazam)口服薄膜的許可外(非公認會計準則調整後的息税折舊攤銷前利潤)不包括調整後的研發支出連續第二季度為正數。截至2023年第三季度,現金和現金等價物為2,490萬美元* 美國食品藥品管理局接受了針對2至5歲年齡組的LibervantTM(地西泮)口腔膠片Libervant保密協議,PDUFA的目標行動日期為2024年4月28日。繼續積極為Libervant尋求美國的許可機會*本金和債務支付是於 2023 年 10 月 2 日製作,到期日。

推進藥品發展。解決問題。改善生活。4 第三季度持續執行在全球食物過敏預防峯會和阿斯彭過敏會議上公佈了 Anaphylm 的標題數據公佈了 AQ109103 研究中Anaphylm的積極標題結果 8 月向美國食品藥品管理局提交了 Anaphylm Pivotal PK 協議供美國食品藥品管理局審查 Emylif®(利魯唑)口服膠片由我們的被許可方贊汶七月 Libervant 2 至 5 歲年齡組的申請被接受供美國食品藥品管理局審查 Emylif®(利魯唑)口服薄膜將於9月份擴大到德國和法國

推進藥品發展。解決問題。改善生活。Anaphylm 關鍵研究 5
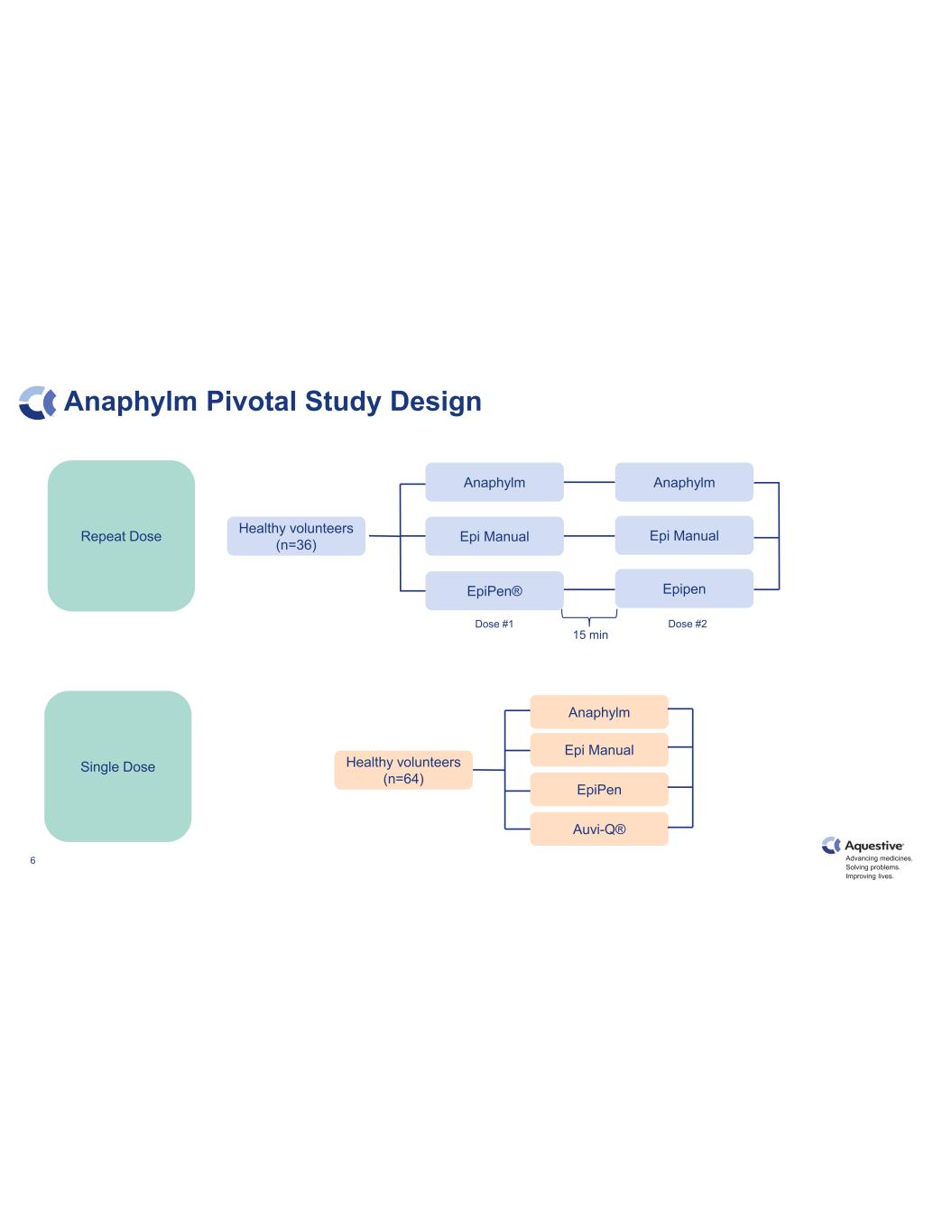
推進藥品發展。解決問題。改善生活。Anaphylm 關鍵研究設計 6 名健康志願者 (n=36) Anaphylm Epi 手冊 EpiPen® Anaphylm Epi 手冊 Epipen 15 分鐘劑量 #1 重複劑量 #2 單劑量健康志願者 (n=64) Anaphylm Epi 手冊 Auvi-Q® EpiPen

推進藥品發展。解決問題。改善生活。關鍵終點 7 藥代動力學 (PK) 藥效學 (PD) • 最大血漿濃度 (Cmax) • 達到最大血漿濃度的時間 (Tmax) • 曲線下方的局部區域位於 10、20、30 和 45 分鐘 • 收縮壓變化 • 舒張壓變化 • 心率變化

推進藥品發展。解決問題。改善生活。財務業績 8

推進藥品發展。解決問題。改善生活。債務再融資亮點9描述新債務融資先前債務融資票據持有人管理資金超過100億美元的領先機構貸款機構銀團固定利率 13.5% 12.5% 簽訂時扣除聯邦基金利率後的固定利率 8.0% 10.2% 認股權證無 2,000,000 收入、息税折舊攤銷前利潤、現金契約無僅利息期 32 個月 36 個月管道資產有限特許權使用費是否

推進藥品發展。解決問題。改善生活。10 繼續管理我們的現金狀況 18.6 27.3 26.9 22.4 24.9 0 5 10 15 20 25 30 截至2022年第三季度2023年第一季度2023年第一季度2023年第二季度第三季度末現金期末現金*所有數字均為百萬美元*本金和利息債務的償還是在2023年10月2日到期時支付的。
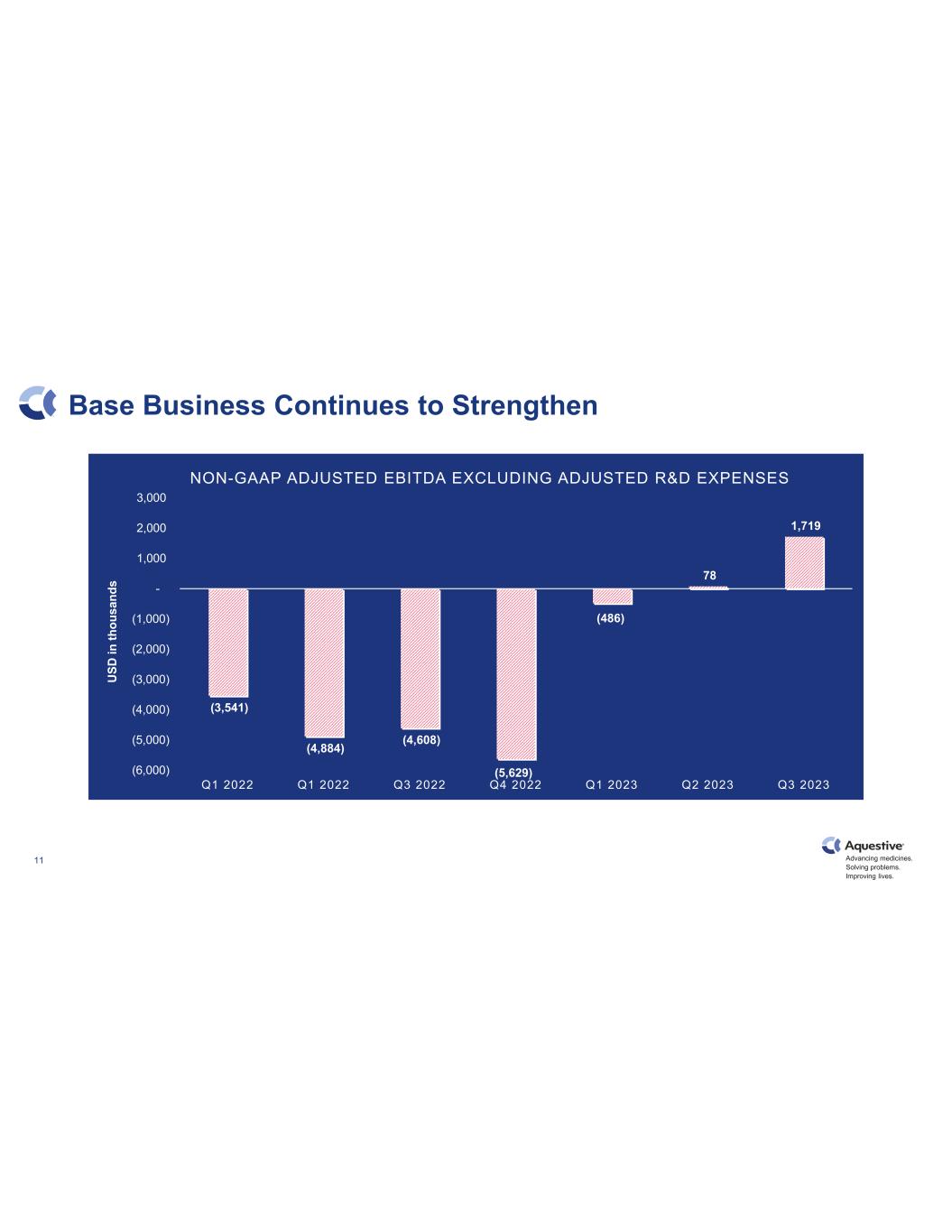
推進藥品發展。解決問題。改善生活。11 基礎業務持續增強 (3,541) (4,884) (4,608) (5,629) (486) 78 1,719 (6,000) (4,000) (3,000) (2,000) (1,000)-1,000 2,000 2022年第一季度2022年第一季度2023年第四季度2023年第二季度美國境內的美元和非公認會計準則調整後的息税折舊攤銷前利潤不包括調整後的研發費用

推進藥品發展。解決問題。改善生活。12 個製造量達到預期併產生現金流 47,505 36,413 42,182 47,041 41,041 41,097 36,863 33,458 47,458 47,241-10,000 30,000 40,000 000,000 ,000 ,000 ,000 ,000 ,000 ,000 2021 年第四季度 2021 年第一季度 2023 年第一季度 2023 年第二季度 2023 年第三季度 PharmFilm® 成交量(千人)
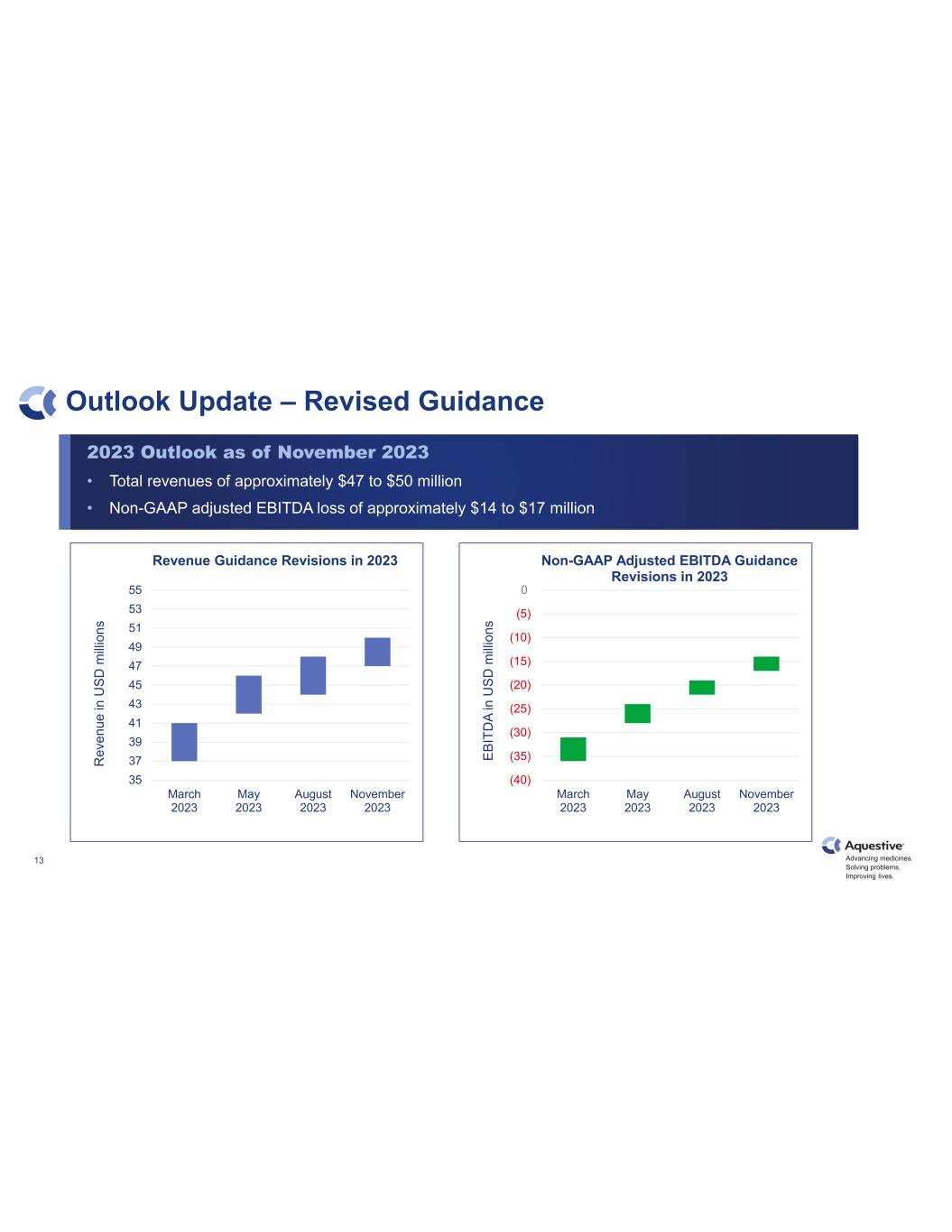
推進藥品發展。解決問題。改善生活。13 展望更新——修訂後的指導方針 35 37 39 43 45 47 49 51 53 53 55 2023 年 5 月 2023 年 8 月 2023 年 11 月 R ev en ev en ue ssd milli 在 2023 年 3 月 (40) (35) (30) (25) (20) (15) (10) (5) 2023 年 5 月 2023 年 8 月 2023 年 11 月 EB IT D A 在非公認會計準則調整後的 EB IT D A 2023年展望中的2023年修訂指南•總收入約為4700萬至5000萬美元•非公認會計準則調整後的息税折舊攤銷前利潤虧損約為1,400萬美元至1,700萬美元

推進藥品發展。解決問題。改善生活。謝謝