

將創新與目標聯繫起來 2024 年 2 月 2 日企業演示納斯達克:CRBP CorbusPharma.com @CorbusPharma 附錄 99.1

前瞻性陳述本演示文稿包含1933年《證券法》第27A條和1934年《證券交易法》第21E條和經修訂的《私人證券訴訟改革法》所指的某些前瞻性陳述,包括與公司的重組、試驗結果、產品開發、臨牀和監管時間表、市場機會、競爭地位、可能或假定的未來經營業績、業務戰略、潛在增長機會和其他陳述有關的前瞻性陳述本質上是預測性的。這些前瞻性陳述基於當前對我們運營所在行業和市場的預期、估計、預測和預測以及管理層當前的信念和假設。這些陳述可以通過使用前瞻性表達來識別,包括但不限於 “期望”、“預期”、“打算”、“計劃”、“相信”、“估計”、“潛力”、“預測”、“項目”、“應該”、“將” 以及類似的表達方式以及這些術語的否定詞。這些陳述與未來事件或我們的財務業績有關,涉及已知和未知的風險、不確定性和其他因素,包括最近 COVID-19 疫情的潛在影響以及持續保持社交距離的努力對我們的運營、臨牀開發計劃和時間表的潛在影響,這些影響可能導致實際業績、業績或成就與前瞻性陳述所表達或暗示的任何未來業績、業績或成就存在重大差異。這些因素包括公司向美國證券交易委員會提交的文件中列出的因素。提醒潛在投資者不要過分依賴此類前瞻性陳述,這些陳述僅代表截至本陳述之日。公司沒有義務公開更新任何前瞻性陳述,無論是由於新信息、未來事件還是其他原因。所有產品名稱、標識、品牌和公司名稱均為其各自所有者的商標或註冊商標。它們的使用並不意味着這些公司的隸屬關係或認可。
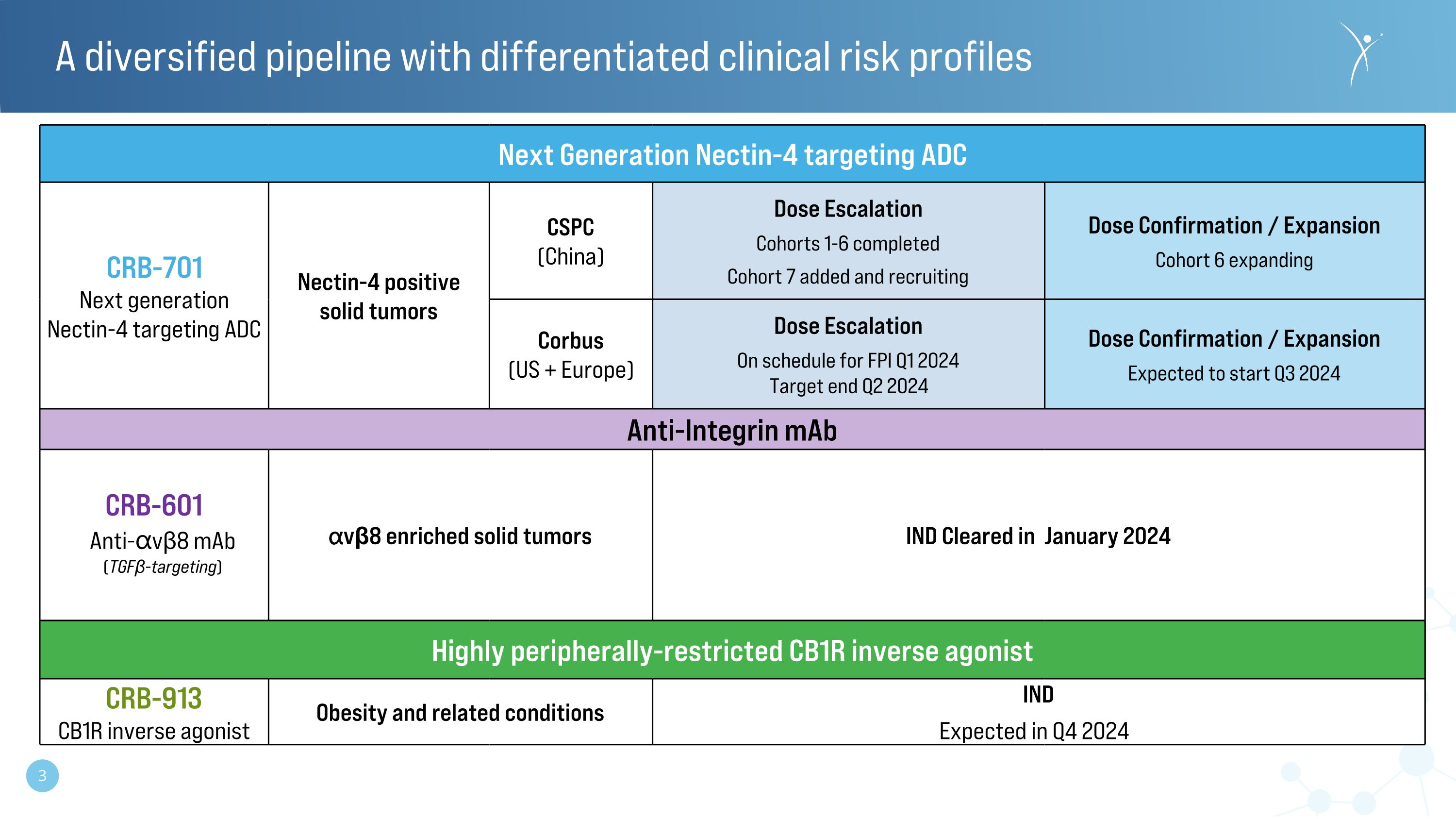
下一代 Nectin-4 靶向 ADC CRB-701 下一代 Nectin-4 靶向 ADC Nectin-4 陽性固體腫瘤 CSPC(中國)劑量遞增隊列 1-6 已完成添加並招募劑量確認/擴展隊列 6 正在擴大 Corbus(美國 + 歐洲)劑量升級計劃於 2024 年第一季度結束 2024 年第二季度劑量確認/擴張預計於 2024 年第三季度開始 Anti-Integrin maB CRB-60b 1抗-vβ8 單抗(靶向 TGFβ)vβ8 富集實體瘤於 2024 年 1 月獲批高度外周受限 CB1R 反向激動劑 CRB-913 CB1R 反向激動劑 CB1R 逆向激動劑激動劑肥胖及相關疾病(IND)(預計在2024年第四季度推出)具有差異化臨牀風險特徵的多元化產品線

crb-701Next Gen Nectin-4 瞄準 ADC

CRB-701 摘要與 Padcev® Ph1 相比,Nectin-4 腫瘤的治療指數持續增加,2024 年第一季度首次發佈數據新興臨牀數據支持差異化 ADC 特徵
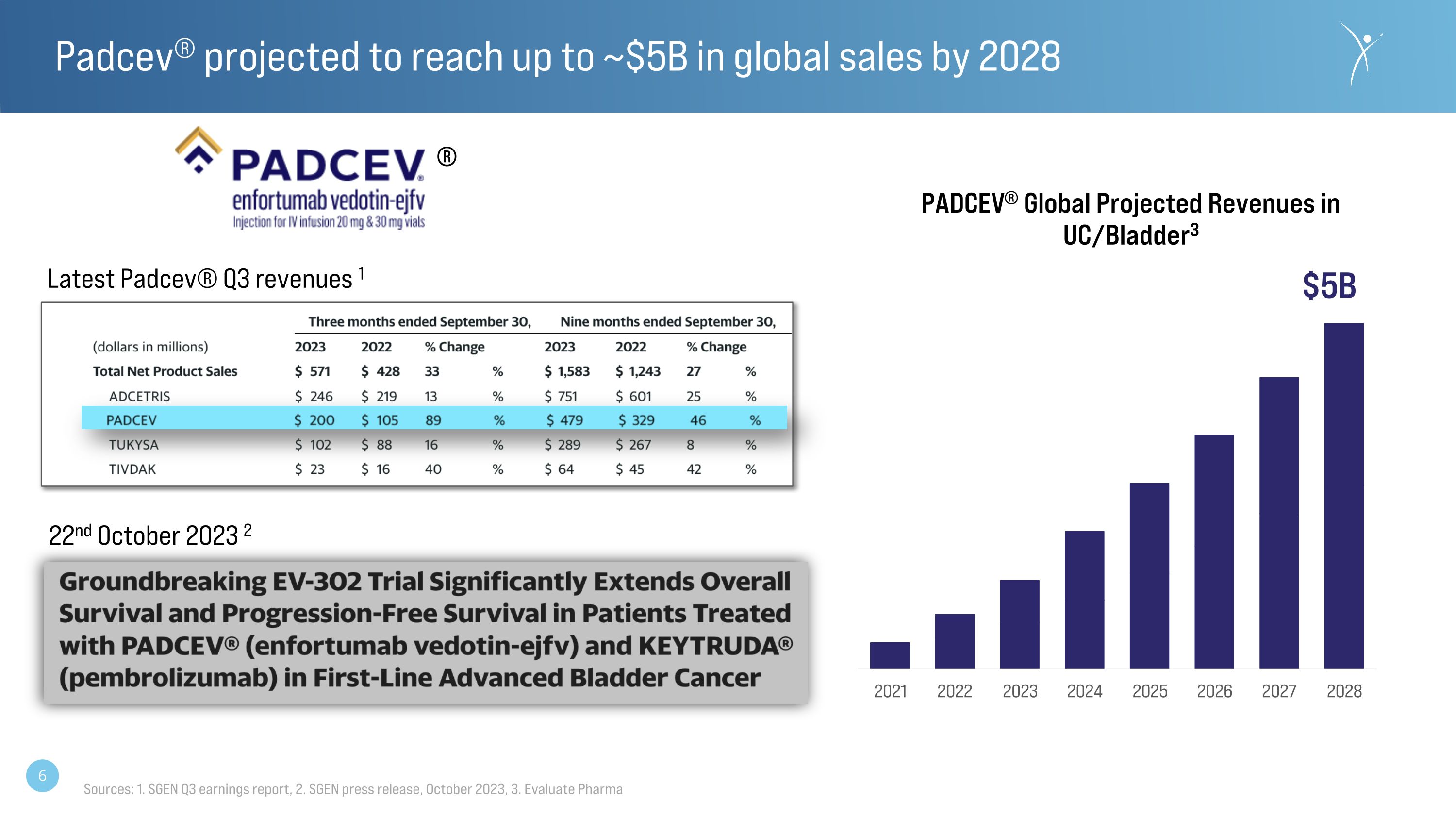
Padcev® 預計到2028年全球銷售額將達到約50億美元® 最新的Padcev® 第三季度收入 1 2023 年 10 月 22 日 2 來源:1.SGEN 第三季度收益報告,2.SGEN 新聞稿,2023 年 10 月,3.評估製藥
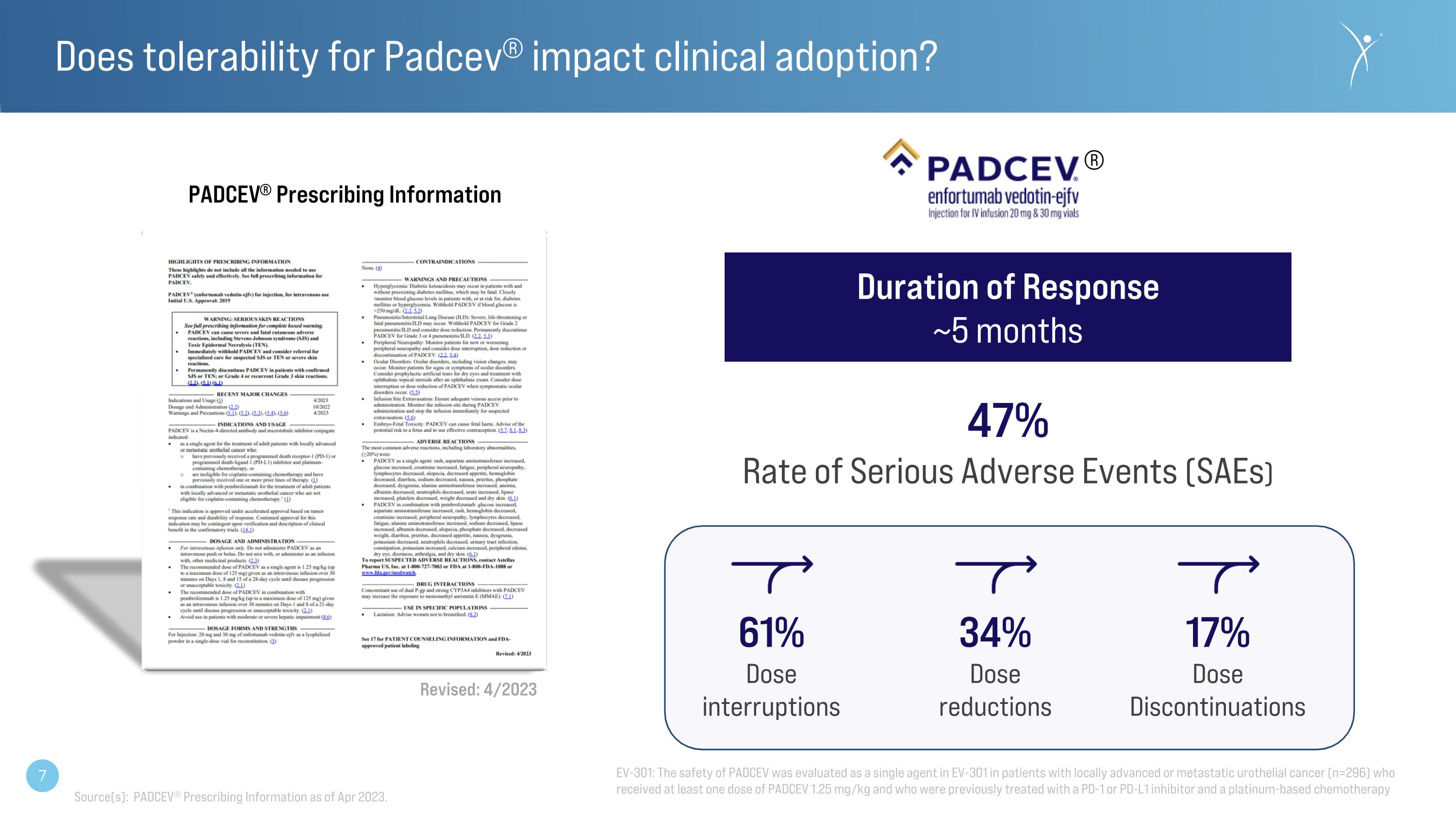
Padcev® 的耐受性會影響臨牀採用嗎?® 緩解持續時間約 5 個月 47% 嚴重不良事件 (SAE) 61% 劑量中斷 34% 劑量減少 17% 劑量停藥修訂版:2023 年 4 月 PADCEV® 處方信息來源:截至 2023 年 4 月 PADCEV® 處方信息。EV-301:PADCEV 的安全性被評估為 EV-301 中的單一藥物,用於局部晚期或轉移性尿路上皮癌(n=296)患者,這些患者接受了至少一劑量的 PADCEV 1.25 mg/kg,並且之前接受過 PD-1 或 PD-L1 抑制劑和鉑類化療的治療

Padcev® 與皮膚毒性和周圍神經病變有關 PADCEV® 單一療法1 PADCEV® + Keytruda1 所有年級 ≥ Gr 3 所有年級 ≥ Gr 3 SkinReactions 58% 14% 70% 17% 周圍神經病變 53% 5% 67% 不良事件(患者百分比)來源:1。PADCEV® 處方信息 2023 年 12 月。2...Rosenberg 等人,2020® A Black Box 警告 1 NR = 未報告 PADCEV® 停藥中超過 25% 與周圍神經病變有關 2 PADCEV + Keytruda 患者:13% 完全解決率 87% 的患者有殘留神經病變(45% 的患者等級≥2)1
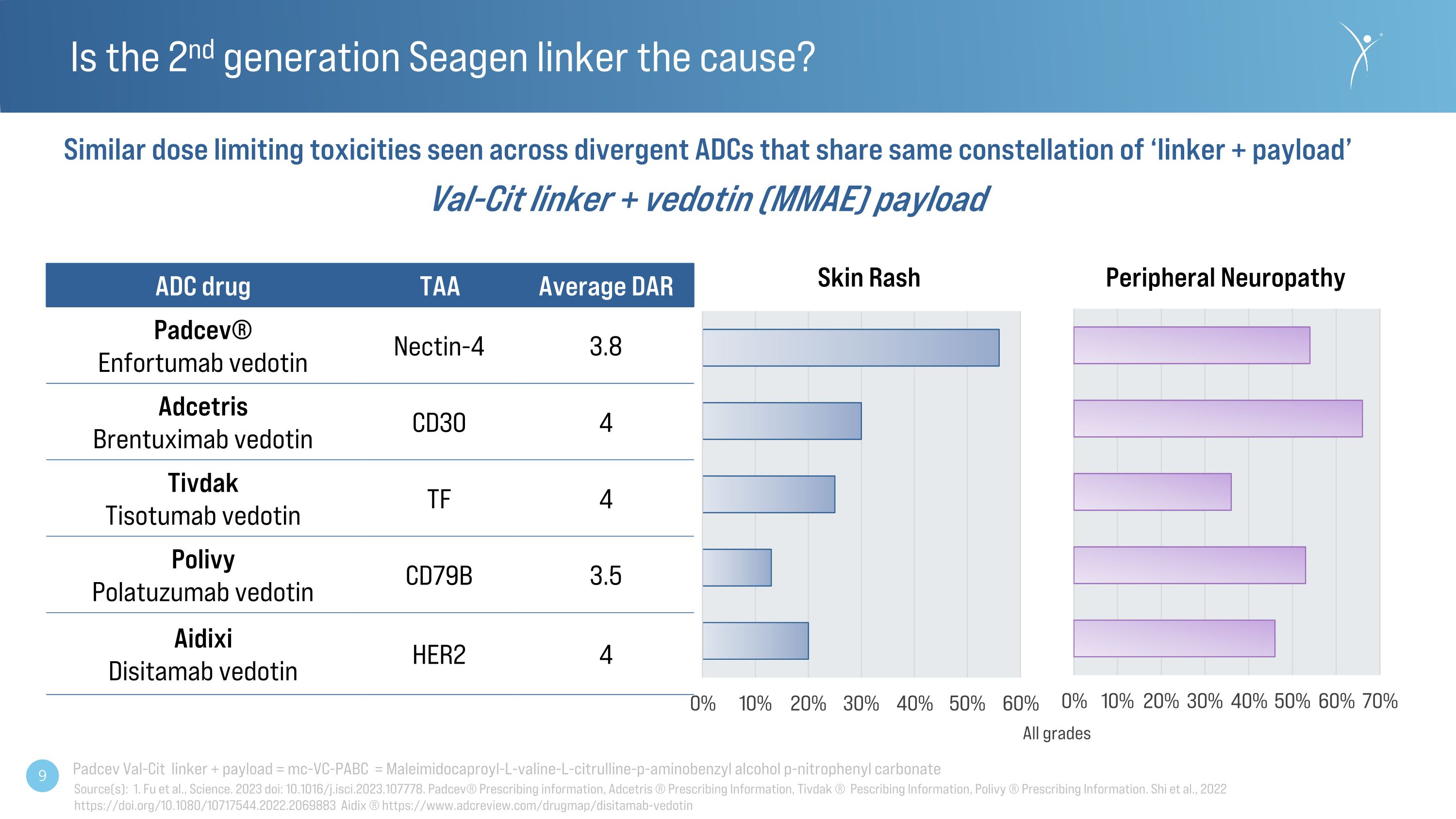
第二代希根鏈接器是原因嗎?皮疹周圍神經病變 Val-Cit 連接劑 + 有效載荷組合的不同 ADC 中存在類似的劑量限制毒性 Val-Cit 連接劑 + vedotin (MMAE) 有效載荷所有等級 ADC 藥物 TAA 平均值 DAR Padcev® Enfortumab vedotin nectin-4 3.8 adcetrisbrentuximab vedotin vedotin vedotin vedotin Vedotin TF 4 vedotin TF 4 Polivy Polatuzumab vedotin CD79B 3.5 aidixidisitamab vedotin vedotin HER2 4 來源:1。傅等人,《科學》。2023 doi:10.1016/j.isci.2023.107778。Padcev® 處方信息、Adcetris® 處方信息、Tivdak® 處方信息、Polivy® 處方信息。Shi 等人,2022 https://doi.org/10.1080/10717544.2022.2069883 Aidix® https://www.adcreview.com/drugmap/disitamab-vedotin Padcev Val-Cit 連接器 + 有效載荷 = mc-vc-PABC = 馬來酰亞胺己酰-L-纈氨酸-L-瓜氨酸-p-氨基苯甲醇 p-硝基苯基碳酸酯
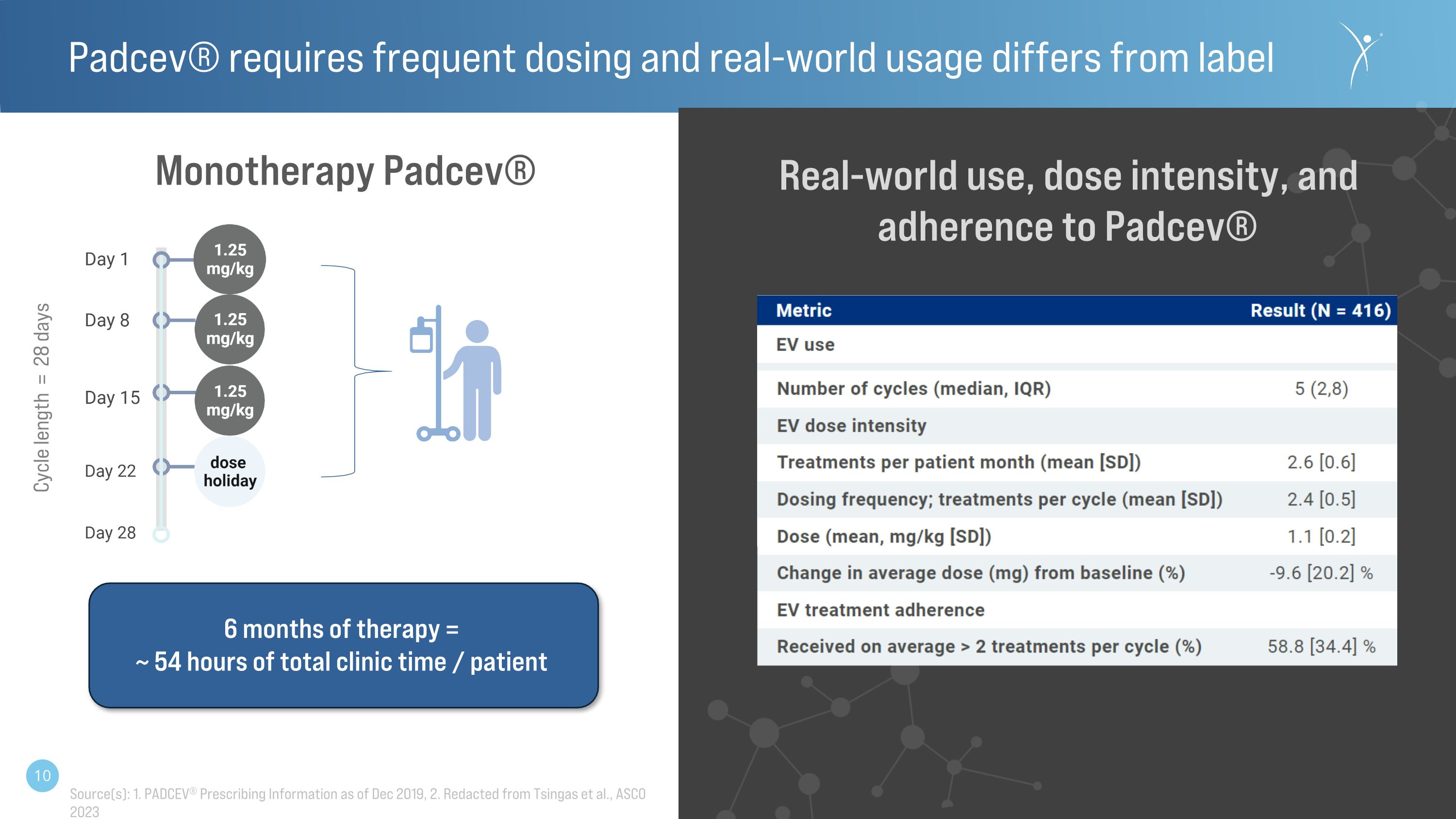
單一療法 Padcev® 來源:1.截至2019年12月的PADCEV® 處方信息,2.摘自 Tsingas 等人,ASCO 2023 6 個月的治療 = 約 54 小時的總臨牀時間/患者的實際使用情況、劑量強度和對 Padcev® Padcev® 的依從性需要頻繁給藥,實際使用與標籤不同。週期長度 = 28 天
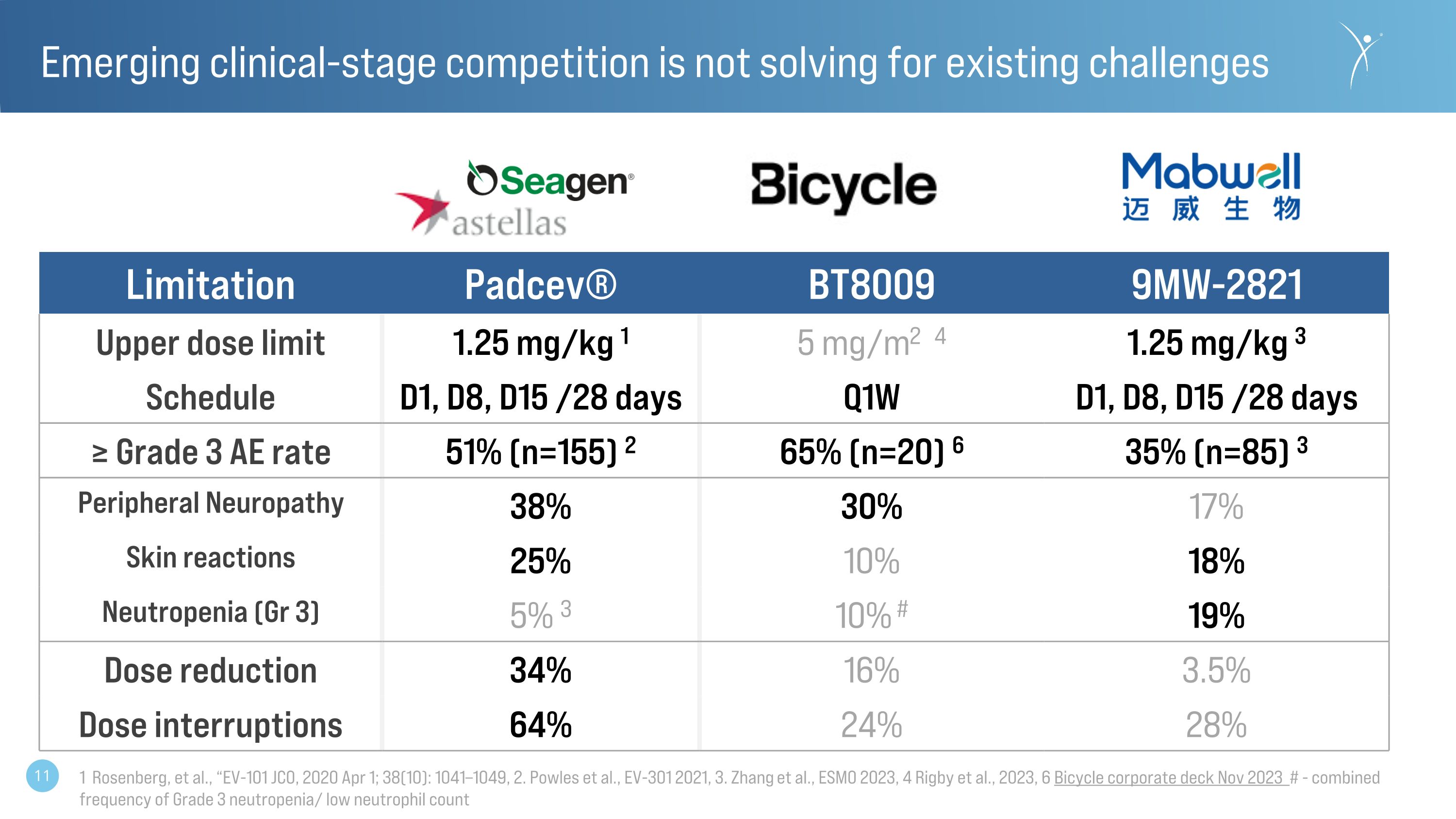
新興的臨牀階段競爭並不能解決現有挑戰侷限性 Padcev® BT8009 9MW-2821 劑量上限 1.25 mg/kg 1 5 mg/m2 4 1.25 mg/kg 3 附表 D1、D8、D15 /28 天 Q1W D1、D8、D15 /28 天 ≥ 3 級 AE 率 51% (n=155) 2 65% (n=20) 6 35% (n=85) 3 外圍設備神經病 38% 30% 17% 皮膚反應 25% 10% 18% 中性粒細胞減少(Gr 3)5% 3 10% # 19% 劑量減少 34% 16% 3.5% 劑量中斷 64% 24% 28% 1 羅森伯格等人,“EV-101 JCO,2020 年 4 月 1 日;38 (10):1041—1049,2。Powles 等人,EV-301 2021,3。張等人,ESMO 2023,4 Rigby 等人,2023 年,6 自行車公司套牌 2023 年 11 月 #-3 級中性粒細胞減少/中性粒細胞計數低的合併頻率

設計旨在解決 Padcev® 未滿足需求的 Nectin-4 ADC 毒性:具有穩定連接器的第三代 ADC 減少自由循環 MMAE 合規性:延長 ADC 半衰期降低給藥頻率功效:更低 DAR + 更長半衰期劑量高於 Padcev®
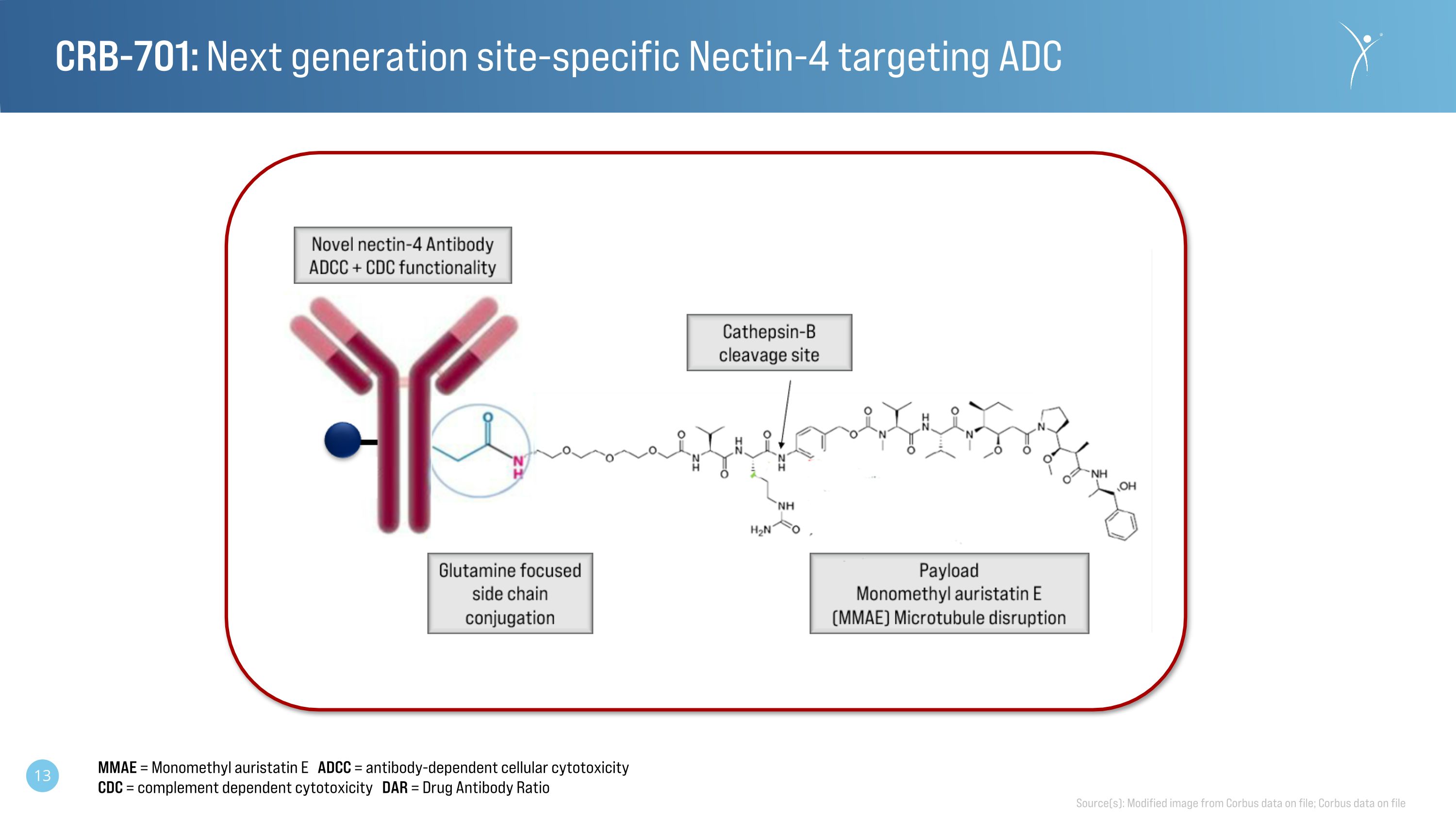
CRB-701:靶向 ADC 的下一代位點特異性 Nectin-4 來源:來自存檔 Corbus 數據的修改圖像;存檔 Corbus 數據 MMAE = 單甲基奧瑞他汀 E ADCC = 抗體依賴性細胞毒性 CDC = 補體依賴性細胞毒性 DAR = 藥物抗體比率
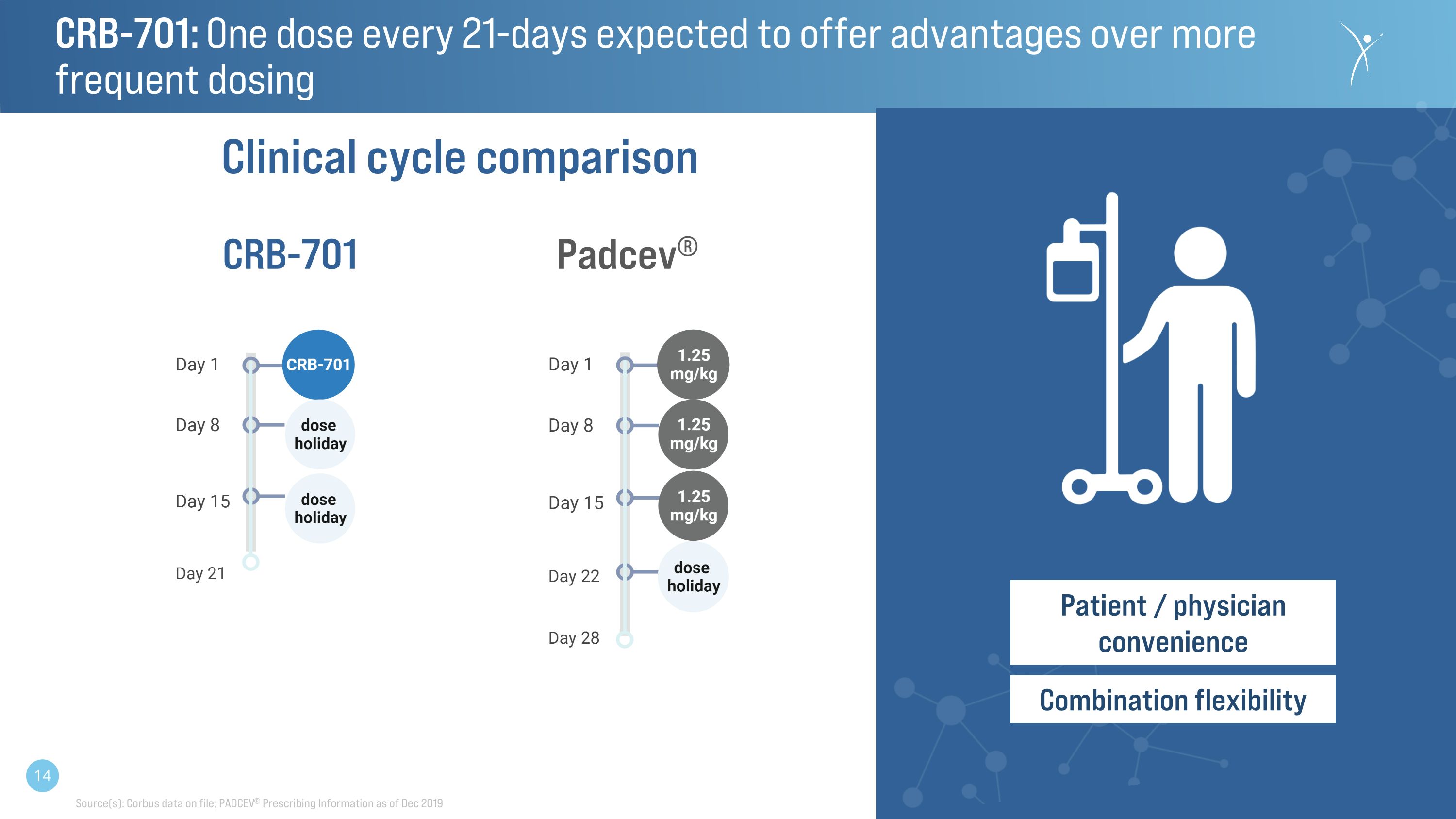
CRB-701:與更頻繁的給藥相比,預計每 21 天一劑有優勢 Padcev® CRB-701 患者/醫生的便利性組合靈活性臨牀週期比較來源:Corbus 存檔數據;截至 2019 年 12 月的 PADCEV® 處方信息

第一階段劑量遞增研究(中國):ASCO-GU 2024
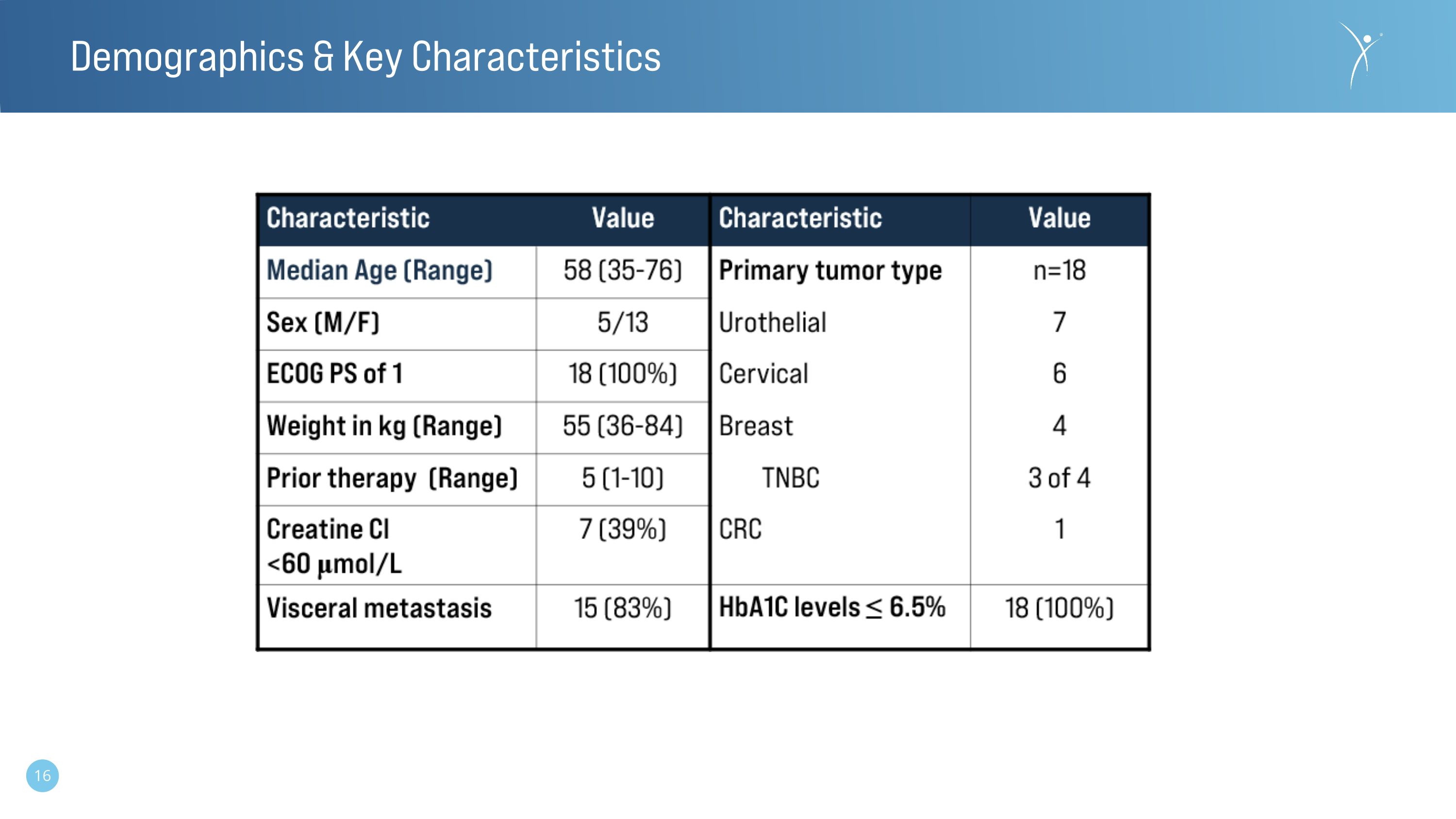
人口統計和關鍵特徵
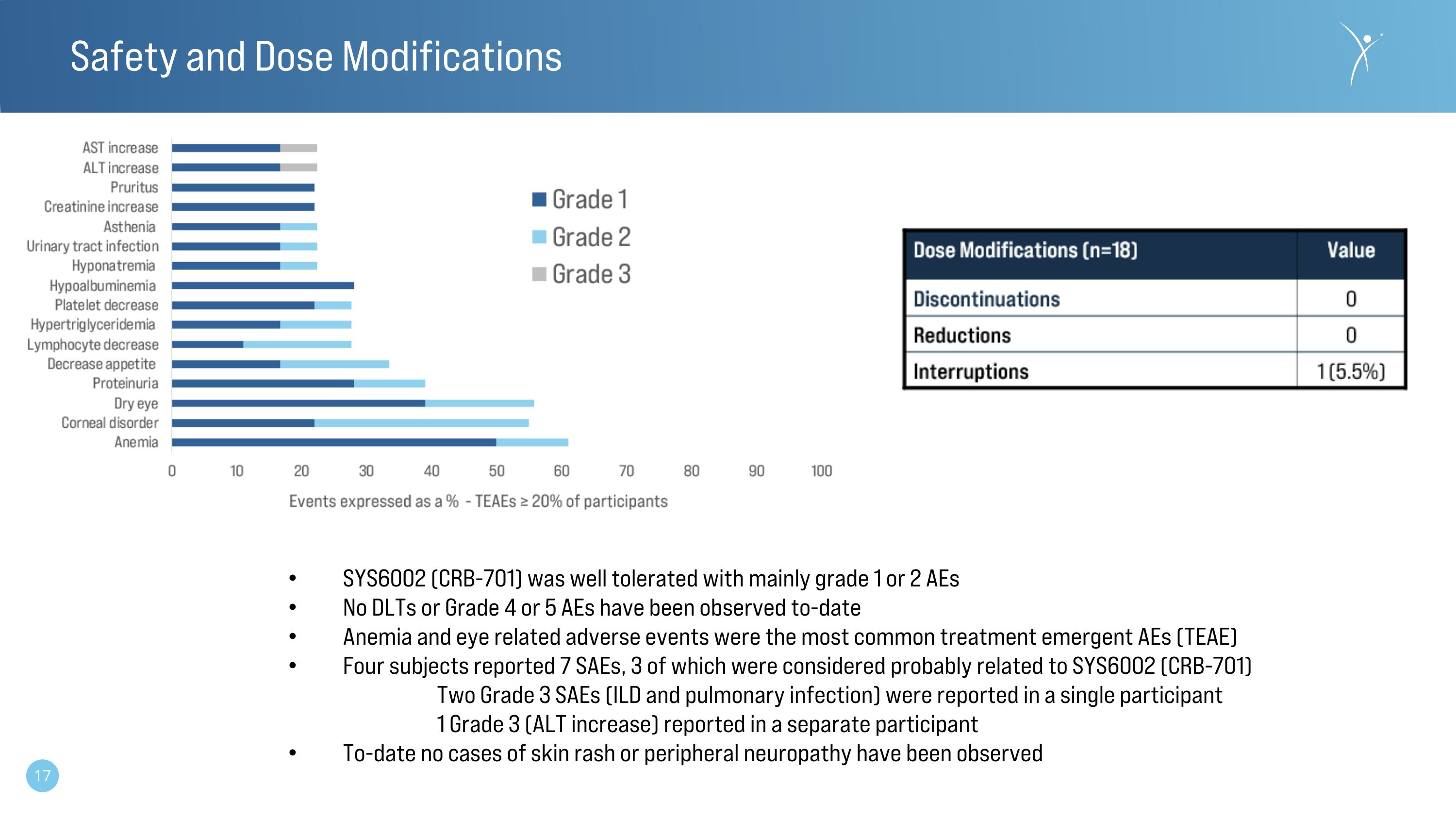
安全性和劑量修改 SYS6002 (CRB-701) 耐受性良好,主要為 1 級或 2 級 AE 迄今未觀察到 DLT 或 4 級或 5 級不良事件貧血和眼部相關不良事件是最常見的治療緊急不良事件 (TEAE) 四名受試者報告了 7 個 SAE,其中 3 個被認為可能與 SYS6002 (CRB-701) 有關,在單個參與者中報告了兩個 3 級 SAE(ILD 和肺部感染)1 級 3 級(ALT 增加)在另一位參與者中:迄今為止,尚未觀察到皮疹或周圍神經病變的病例
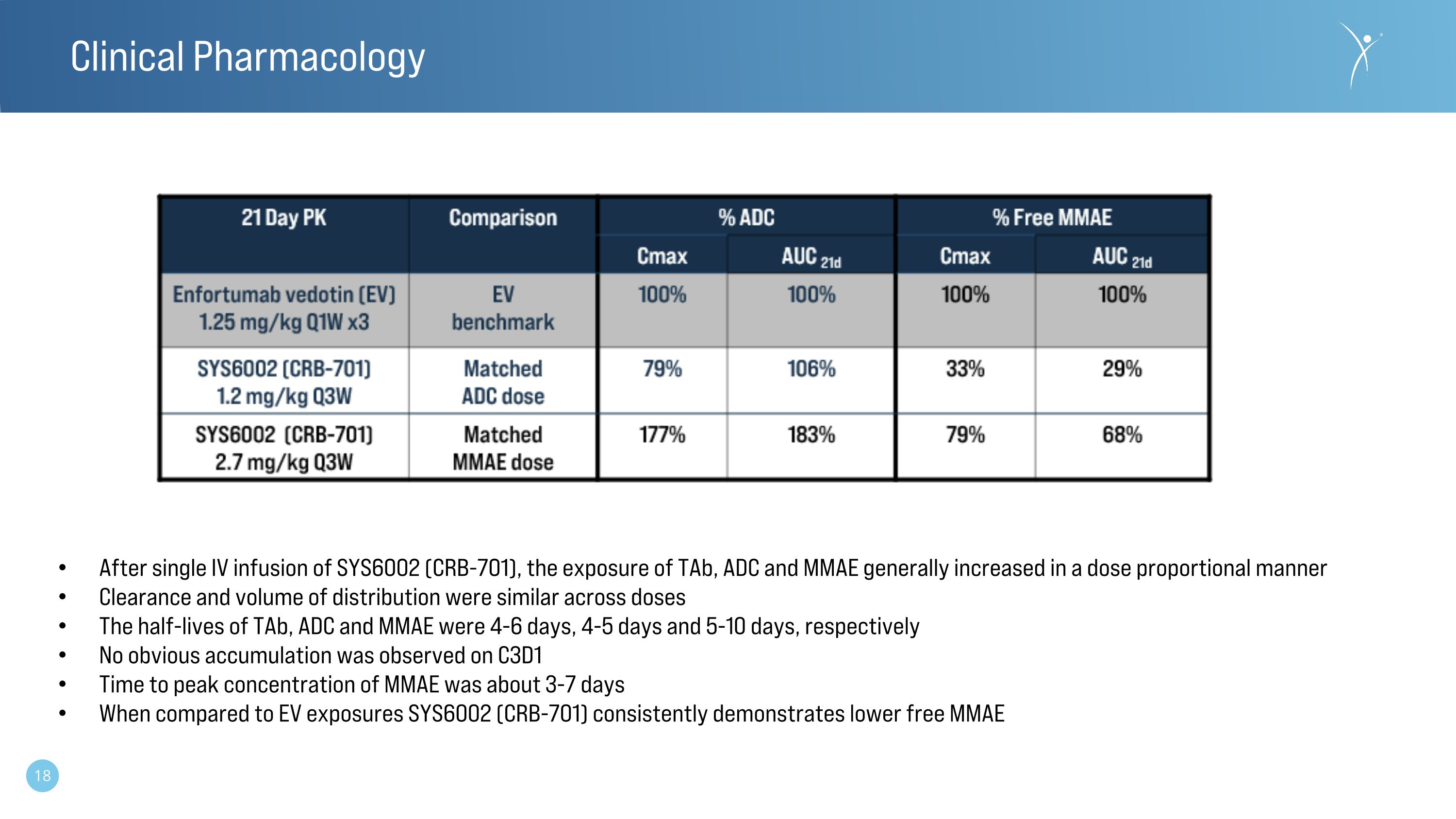
臨牀藥理學 SYS6002 (CRB-701) 單次靜脈輸注後,TaB、ADC 和 MMAE 的暴露量通常以劑量成比例的方式增加。TaB、ADC 和 MMAE 的半衰期分別為 4-6 天、4-5 天和 5-10 天,在 C3D1 上未觀察到明顯的累積 MMAE 達到峯值濃度的時間約為 3-7 天,與電動汽車暴露相比 SYS6002 (CRB-701) 的半衰期分別為 4-6 天、4-5 天和 5-10 天免費降低 MMAE
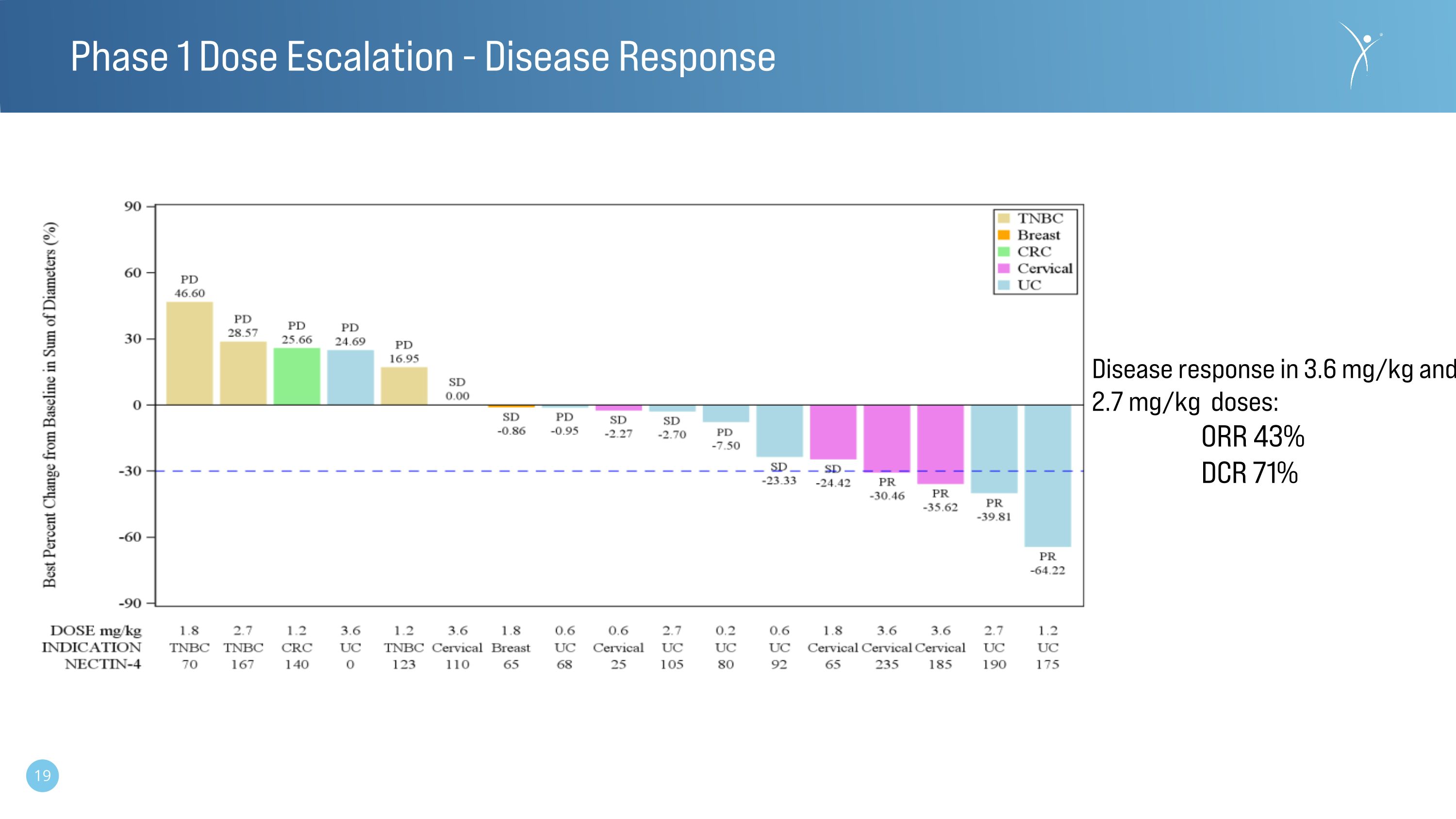
第 1 階段劑量遞增——疾病反應在 3.6 mg/kg 和 2.7 mg/kg 劑量下的疾病反應:ORR 43% DCR 71%
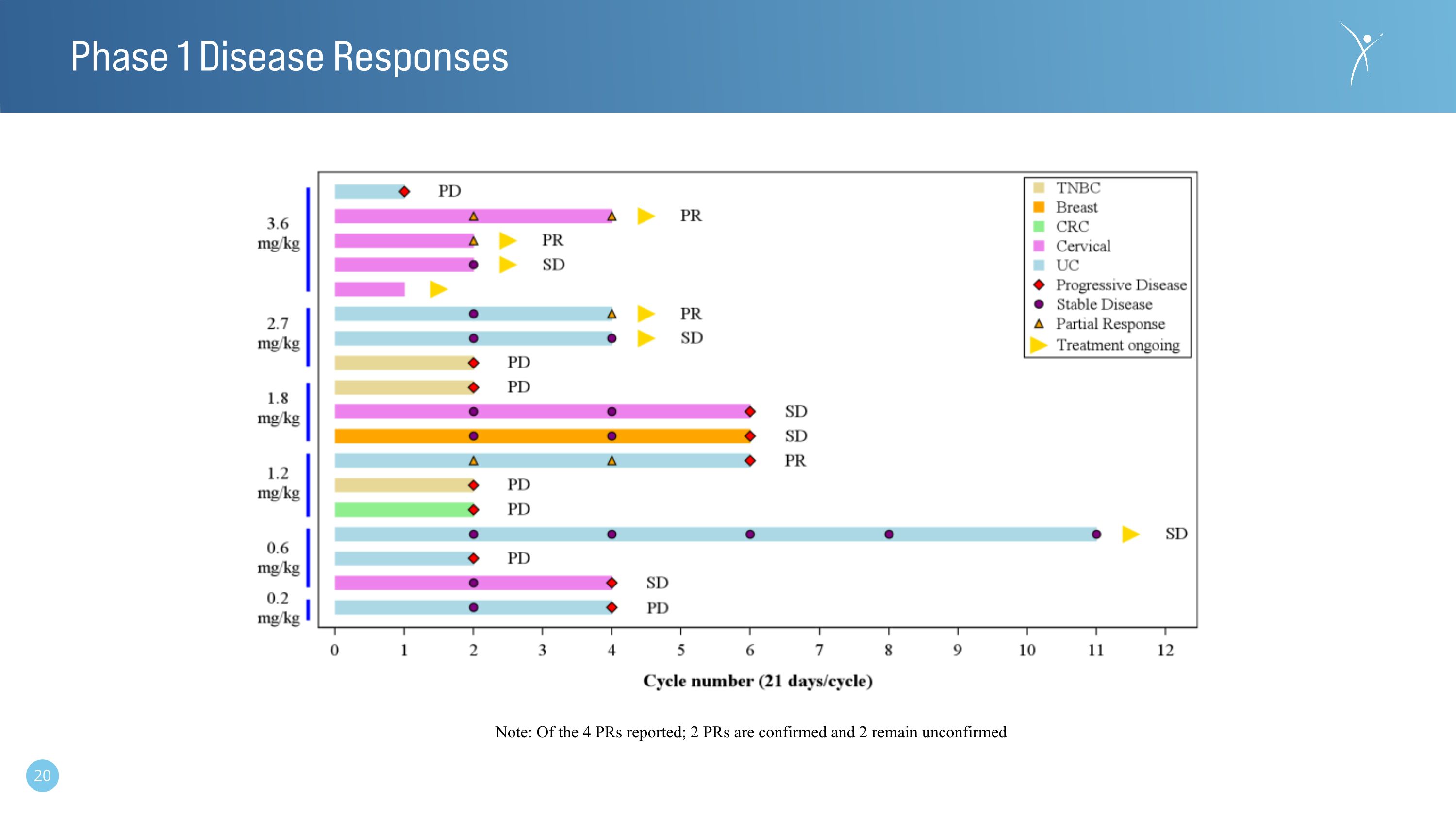
第 1 階段疾病反應注:在報告的四個 PR 中;2 個 PR 已確認,2 個仍未確認
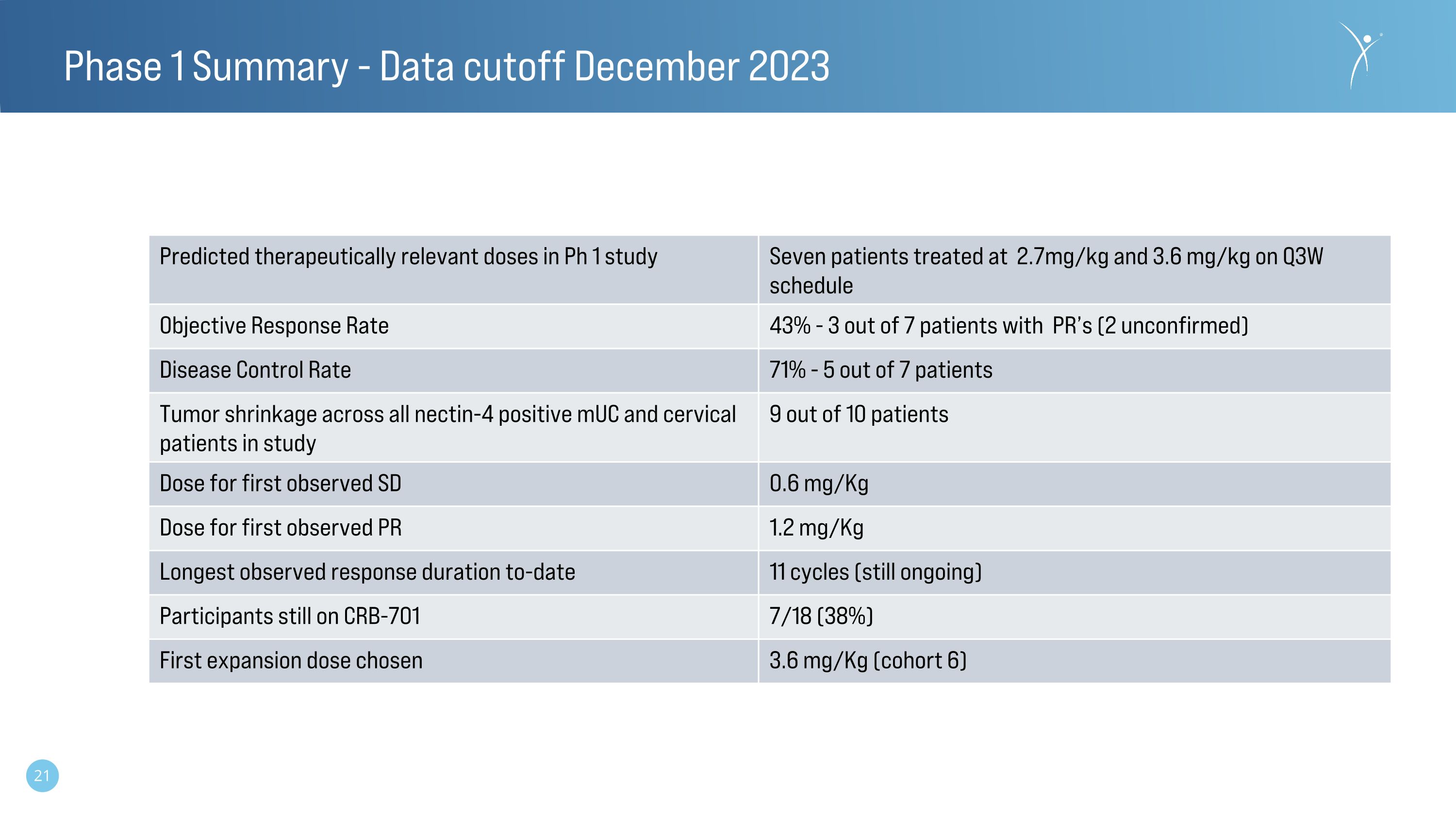
第 1 階段摘要-2023 年 12 月截止數據在 Ph 1 研究中預計的治療相關劑量按照第三季度計劃進行的 7 名患者以 2.7 mg/kg 和 3.6 mg/kg 的治療目標反應率 43%-7 名 PR 患者中有 3 名(2 名未經證實)疾病控制率 71%-7 名患者中有 5 名在研究中 nectin-4 陽性 mUC 和宮頸患者的腫瘤收縮率 10 名患者中有 9 名首次觀察到 SD 的劑量 0.6 首次觀察 PR 的 mg/kg 劑量 1.2 mg/kg 迄今為止觀察到的最長反應時間 11 個週期(仍在進行中)參與者仍在服用 CRB-701 7/18(38%)) 選擇的第一個擴展劑量 3.6 mg/kg(隊列 6)
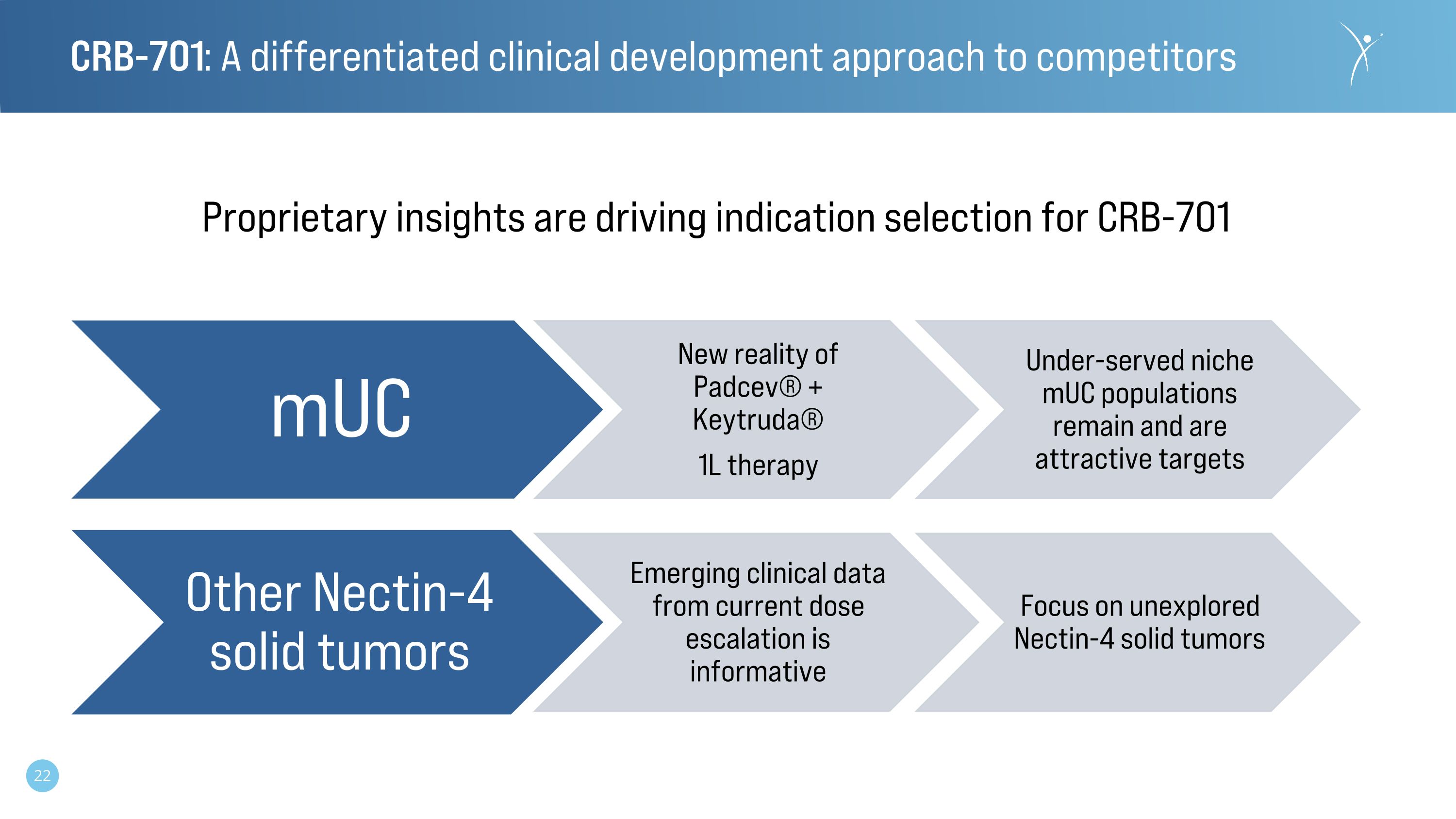
CRB-701:針對競爭對手的差異化臨牀開發方法 muC Padcev® + Keytruda® 1L 療法服務不足的利基 muC 人羣仍然存在並且是有吸引力的靶標其他 Nectin-4 實體瘤當前劑量增加的新興臨牀數據信息聚焦未開發的 Nectin-4 實體瘤專有見解正在推動 CRB-701 的適應症選擇
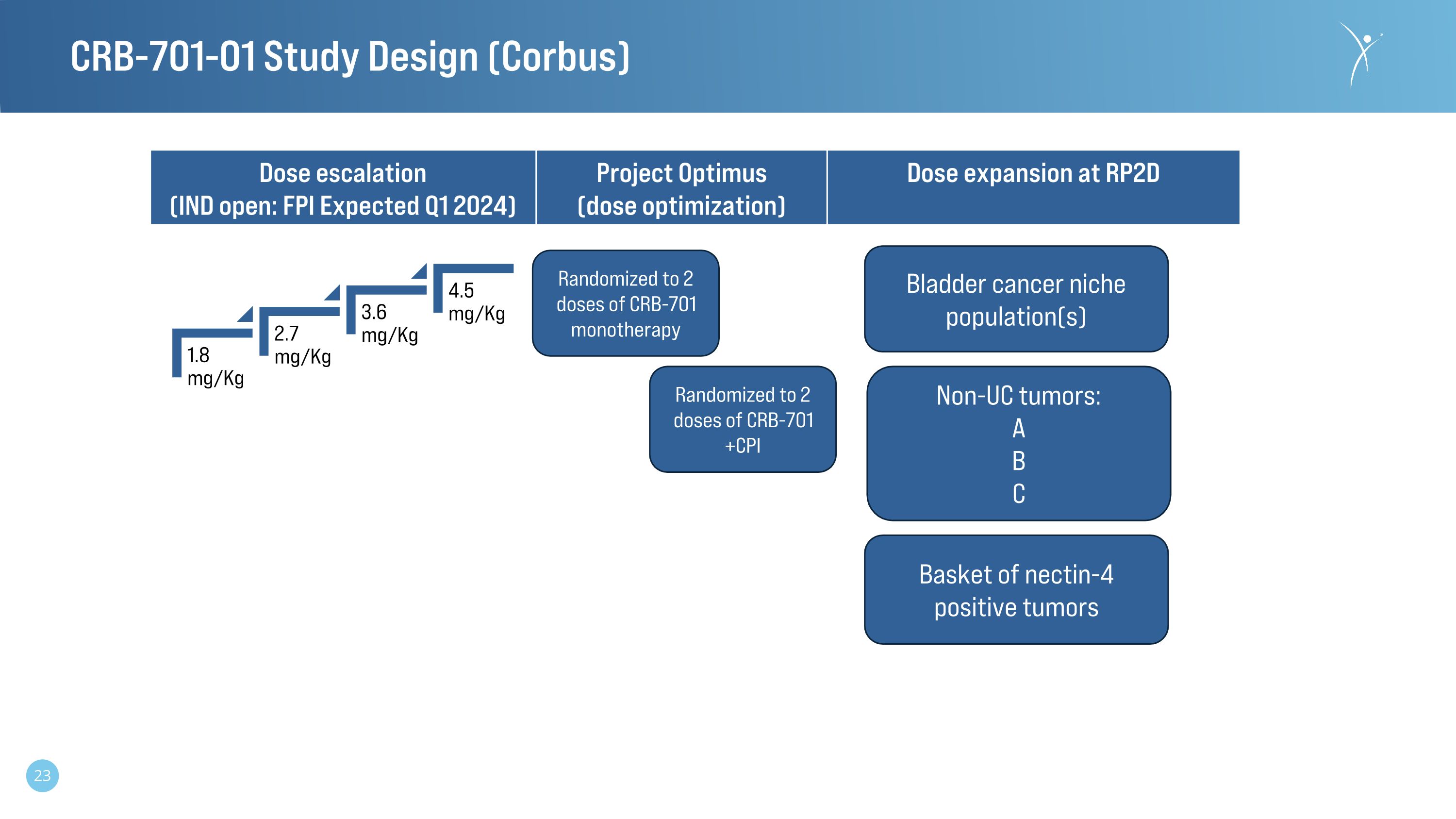
CRB-701-01 研究設計(Corbus)1.8 mg/kg 2.7 mg/kg 3.6 mg/kg 4.5 mg/kg 劑量遞增(印度公開賽:FPI 預計 2024 年第一季度)Optimus 項目(劑量優化)RP2D 的劑量擴大 2 劑隨機分配給 CRB-701 +CPI 膀胱癌利基人羣非 UC 腫瘤:Nectin-4 陽性腫瘤的 B C 籃子 CRB-701
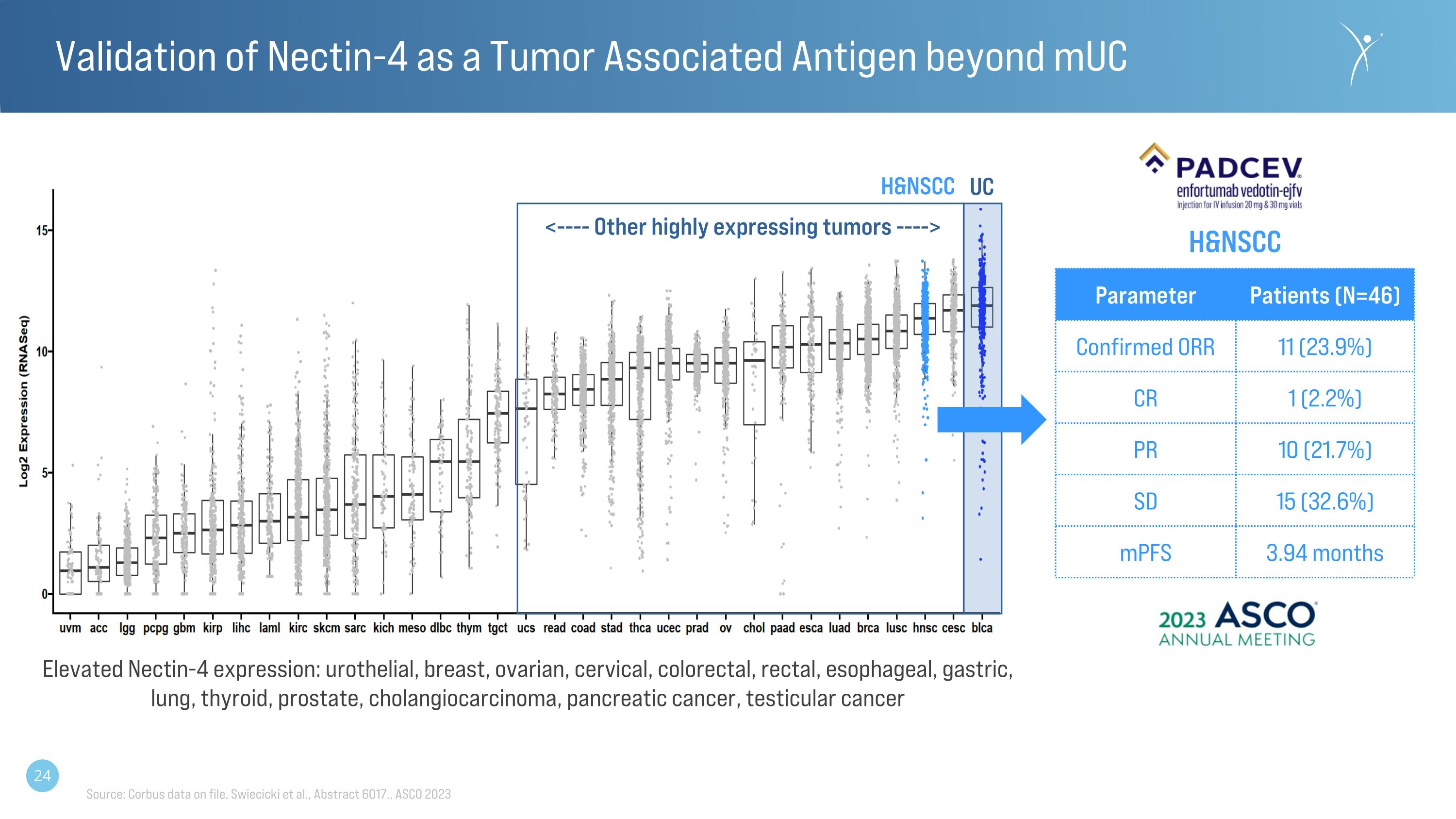
確認 Nectin-4 是超出 muC 參數患者的腫瘤相關抗原 (N=46) 證實 ORR 11 (23.9%) CR 1 (2.2%) PR 10 (21.7%) SD 15 (32.6%) mpfs 3.94 個月來源:Corbus 存檔數據,Swiecicki 等人,摘要 6017。,ASCO 2023 Nectin-4 表達升高:尿路上皮、乳房、卵巢、宮頸,結直腸癌、直腸癌、食管癌、胃癌、肺癌、甲狀腺、前列腺、膽管癌、胰腺癌、****癌 UC H&NSCC H&NSCC
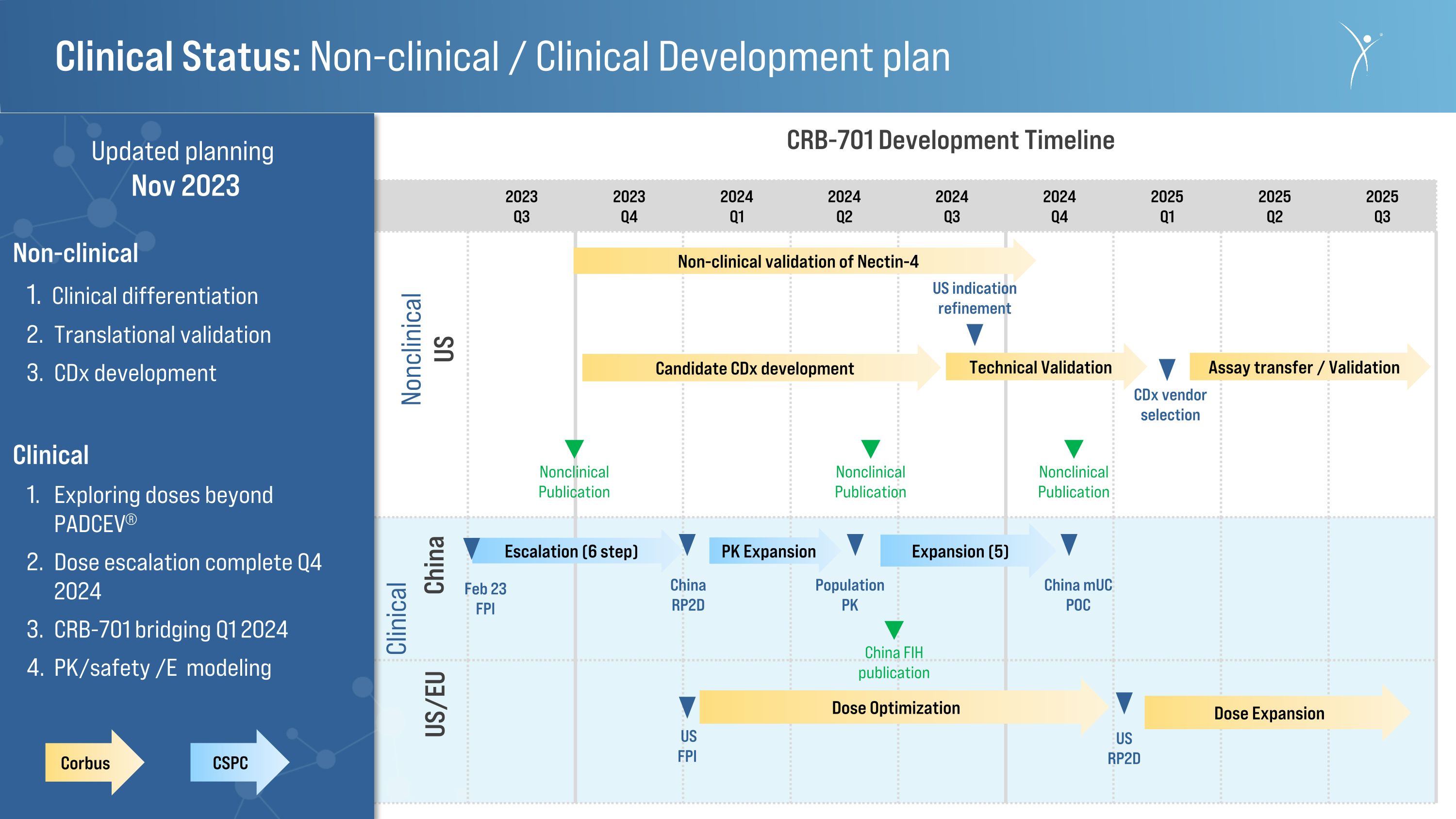
臨牀狀態:非臨牀/臨牀開發計劃 2023 年第 1 季度 2023 年第 2 季度 2023 年第 4 季度 2024Q1 2024 年第 2 季度 2024Q4 2025 年第一季度 Q2 2025Q3 CRB-701 開發時間表中國 Nectin-4 的非臨牀驗證美國 RP2D 升級(6 步)非臨牀美國 CDx 供應商選擇擴展(5)2 月 23 日 FPI 人羣 PK 中國 RP2D 中國 muC POC 分析轉移/驗證非臨牀出版物美國適應症完善 Corbus CSPC 劑量優化非臨牀出版物技術驗證臨牀美國 FPI 更新計劃 2023 年 11 月非臨牀臨牀差異化翻譯驗證 CDx 開發臨牀探索 PADCEV® 以外的劑量遞增已完成 2024 年第 4 季度 CRB-701 橋接 2024 年第一季度 pk/安全性/E 建模 PK 擴展非臨牀出版物候選出版物 CDx 開發中國 FIH 出版物劑量擴展

CRB-701:摘要新興的臨牀安全性和卓越治療指數的潛力劑量擴大已經開始(中國);美國 2024 年第一季度第三代 ADC 的劑量增加,連接劑穩定性得到改善,降低了循環中的 MMAE

CRB-913:口服大麻素1型反向激動劑可改善肥胖症的腸促素納斯達克:CRBP CorbusPharma.com @CorbusPharma
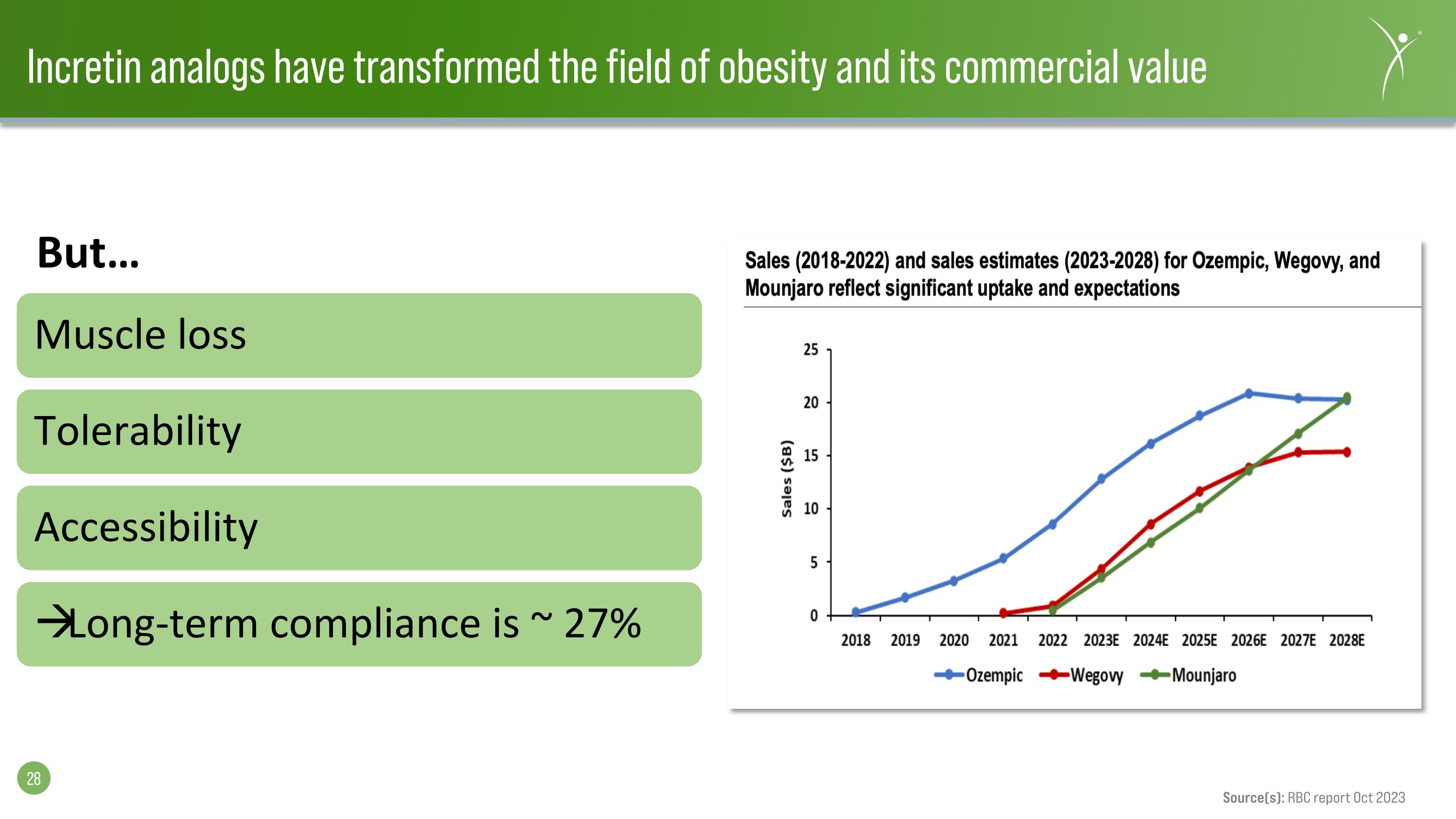
增量素類似物已經改變了肥胖領域及其商業價值肌肉流失耐受性可及性長期依從性約為 27% 來源:加拿大皇家銀行 2023 年 10 月報告但是

肥胖格局正在演變以解決這些問題肌肉流失:減肥程度減肥質量耐受性:單一MOA 多種正交 MOA 可及性:注射劑口服小分子來源:加拿大皇家銀行 2023 年 10 月報告

CB1 反向激動作用:經臨牀驗證的 30 類肥胖藥物的迴歸
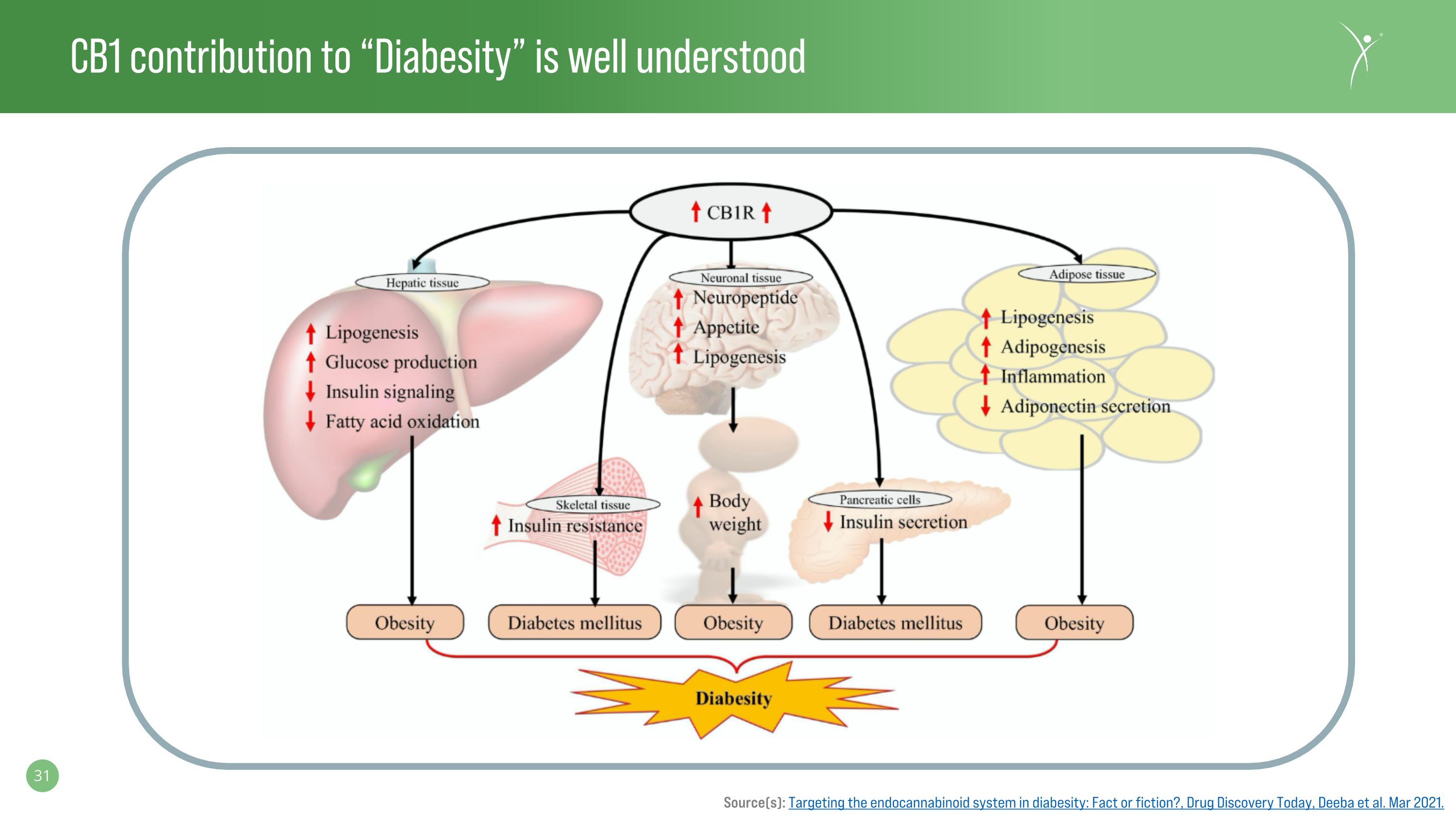
CB1 對 “糖尿病” 的貢獻眾所周知來源:針對糖尿病中的內源性大麻素系統:事實還是虛構?,《今日藥物發現》,Deeba等人。2021 年 3 月。
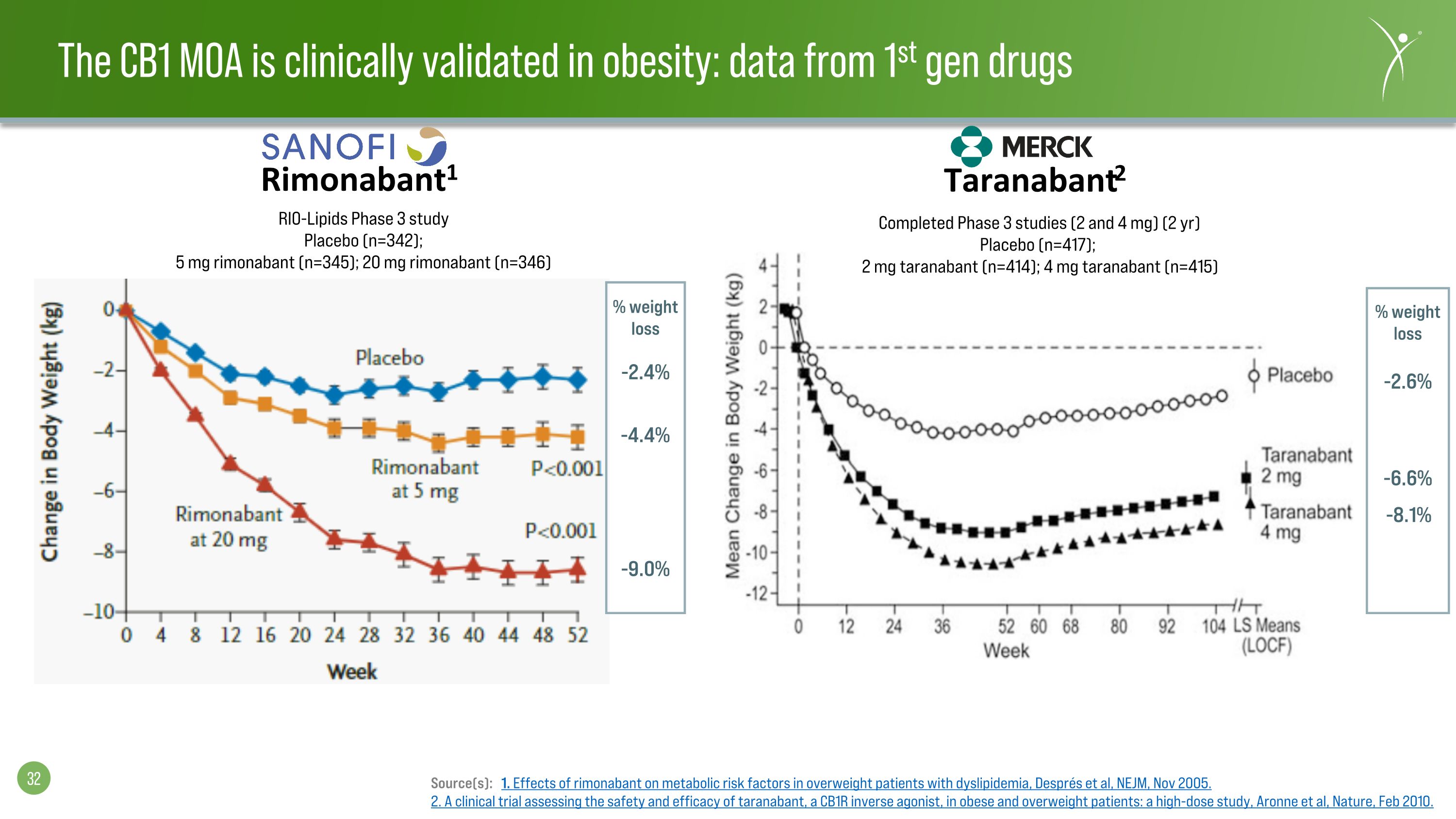
-9.0% -4.4% -2.4% 減肥 rio-Lipids 3 期研究安慰劑(n=342);5 mg 利莫那班(n=345);20 mg 利莫那班(n=346)已完成 3 期研究(2 和 4 mg)(2 年)安慰劑(n=417);2 mg taranabant(n=414);4 mg taranabant 減肥% (n=415)% 減肥 -8.1% -6.6% -2.6% Rimonabant1 Taranabant2 來源:1。利莫那班對血脂異常超重患者代謝危險因素的影響,Després等人,NEJM,2005年11月。2.一項評估CB1R反向激動劑塔拉那班在肥胖和超重患者中的安全性和有效性的臨牀試驗:一項高劑量研究,Aronne等人,《自然》雜誌,2010年2月。CB1 MOA 已在肥胖方面得到臨牀驗證:來自第一代藥物的數據

利莫那班減肥與肥胖患者瘦肉質量減少無關在 RIO Lipids 中使用體內 DEXA 測量了一部分患者的身體成分。觀察到與安慰劑相比,利莫那班20 mg組的總體重有所下降(p
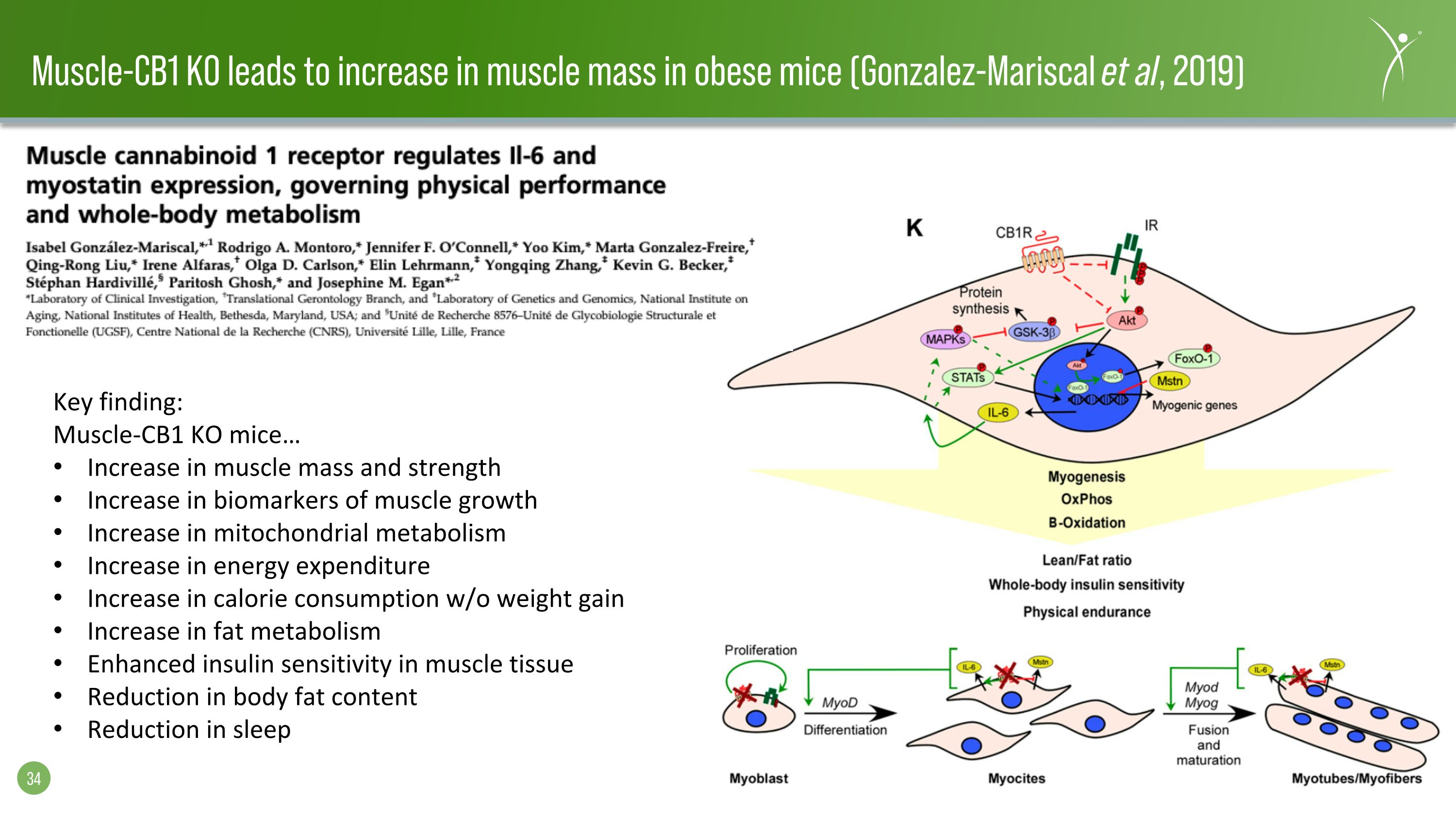
Muscle-cb1 KO 導致肥胖小鼠的肌肉質量增加(Gonzalez-Mariscal 等人,2019 年)關鍵發現:Muscle-cb1 KO 小鼠 增加肌肉質量和力量增加肌肉生長的生物標誌物增加線粒體代謝增加能量消耗增加不增加體重增加卡路里消耗量增加脂肪代謝增加肌肉組織中的胰島素敏感性減少體內脂肪含量減少睡眠
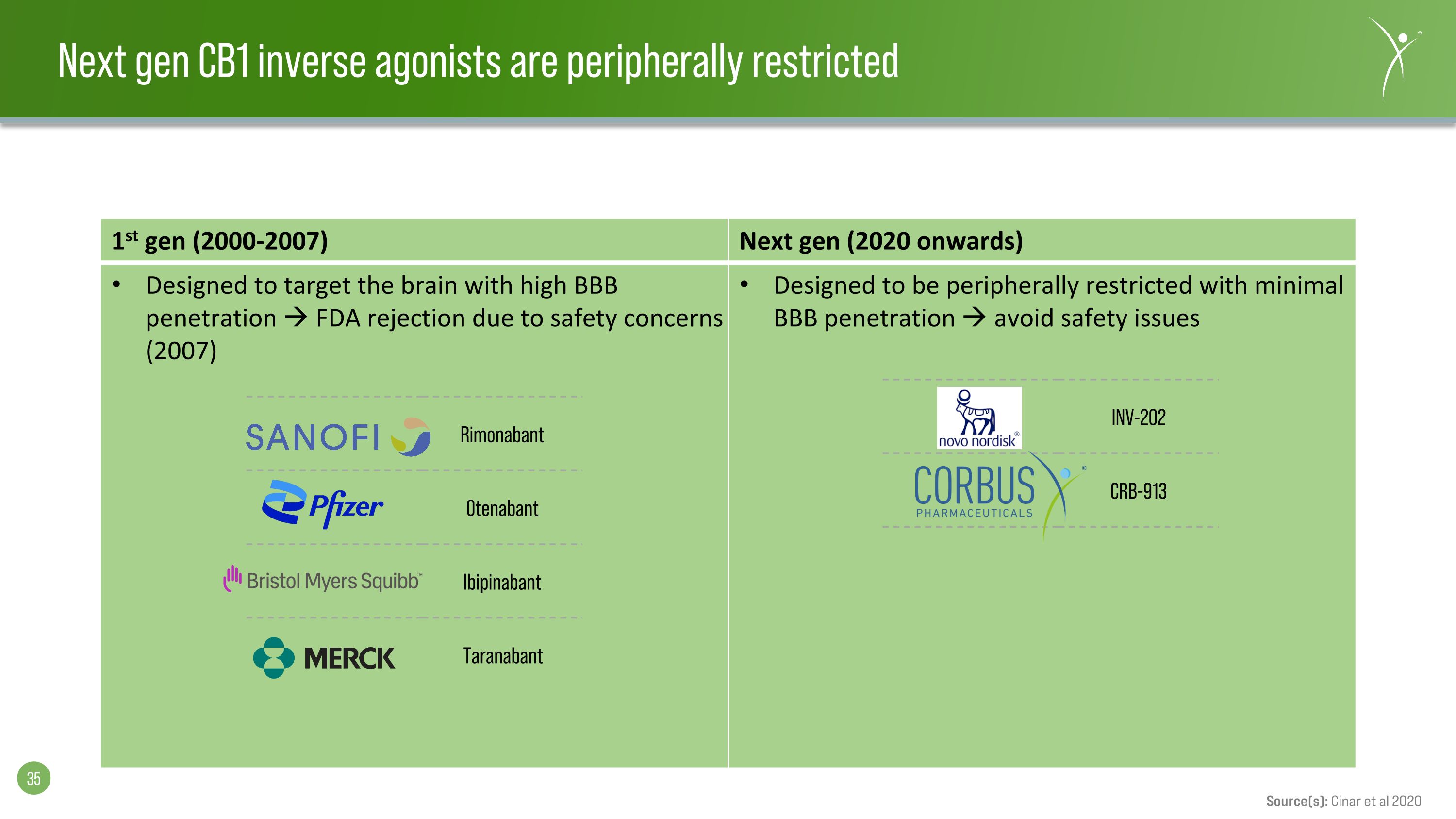
下一代 CB1 反向激動劑受外周限制第一代(2000-2007 年)下一代(2020 年起)專為靶向 BBB 滲透率高的大腦而設計,出於安全考慮,FDA 拒絕(2007 年)專為外周限制而將 BBB 穿透率降至最低可避免安全問題 Rimonabant Otenabant Ibipinabant Taranabant INV-202 CRB-913 來源:Cinar 等人 2020
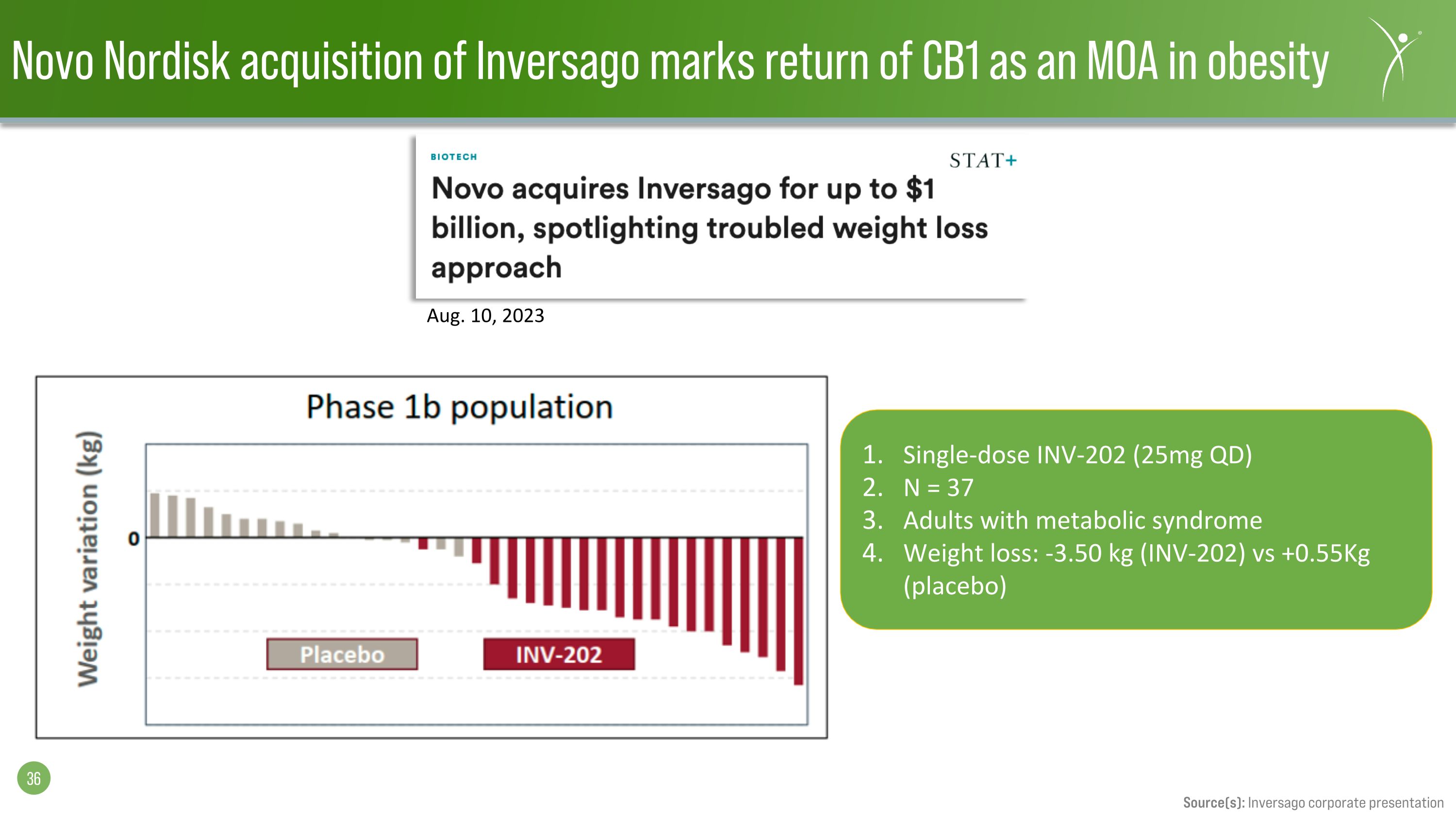
Novo Nordisk 收購 Inversago 標誌着 CB1 作為肥胖領域的 MOA 迴歸單劑量 INV-202(25mg QD)N = 37 名患有代謝綜合徵的成年減肥:-3.50 kg(INV-202)與 +0.55 Kg(安慰劑)2023 年 8 月 10 日來源:Inversago 公司介紹

CRB-913:口服 CB1 反向激動劑,用於腸促胰島素聯合治療 2023 年 11 月 37 日

CRB-913:旨在成為一流的下一代 CB1 逆向激動劑設計目標:一流的外周限制保護精益質量(肌肉)保持第一代功效增強腸促胰島素類似物的功效

Ibipinabant(2004-2008)JD-5037(2012-2018)/CRB-4001(2018-2021 年)已完成 Iib 期(Solvay/BMS)小脂溶性分子 BBB 滲透率高 2018 年獲得詹林的許可進行了大量的臨牀前研究 PK 不支持 TPP 口服 CRB-913 新知識產權發佈——專利覆蓋面已優化 TPP 有利於多物種生物利用度(> 50%)降低製造量成本與口服增生素的對比 CRB-913 是一項為期多年的藥物化學活動的結果 CRB-4001 JD5037
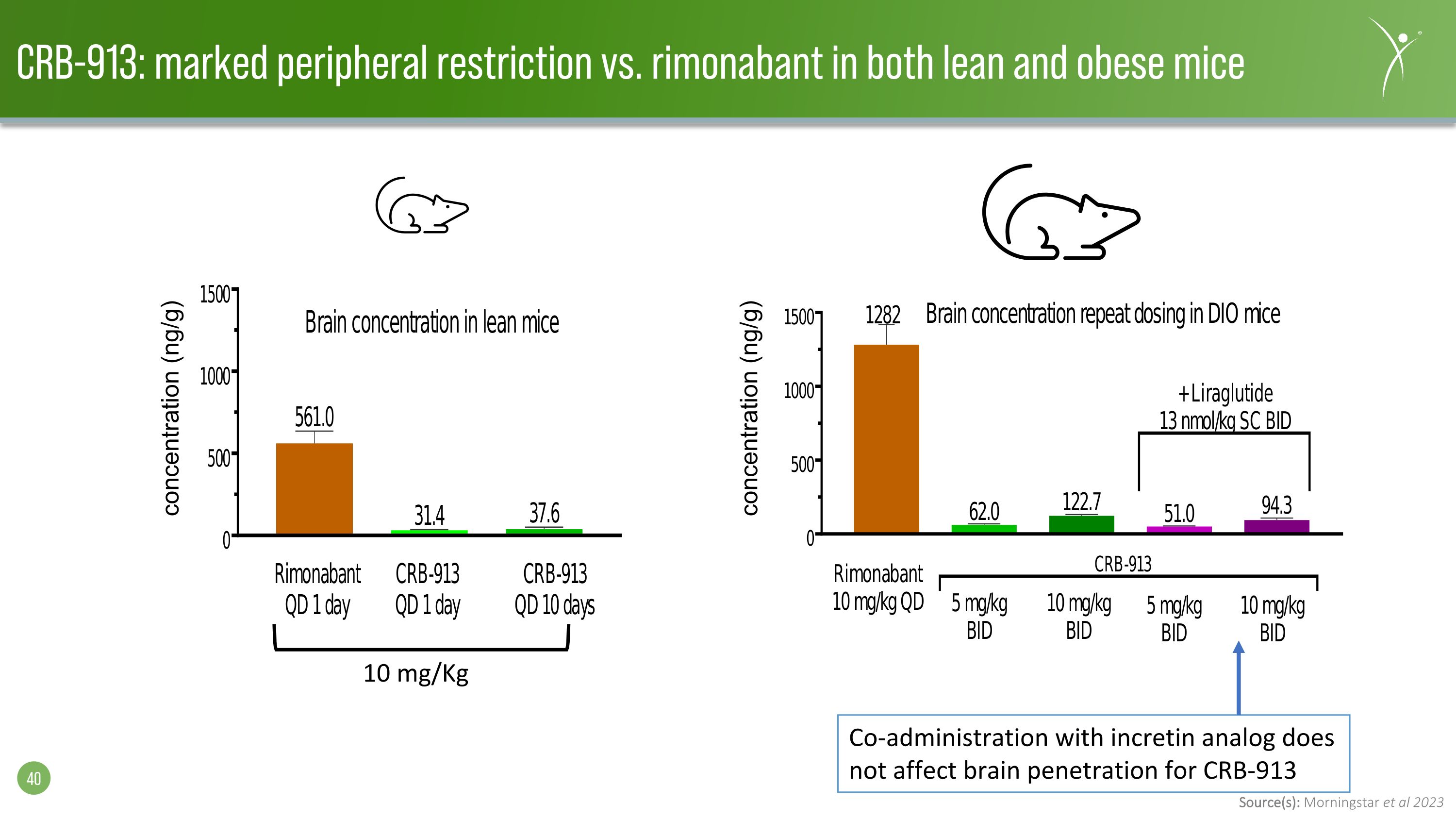
來源:晨星等人 2023 CRB-913:與利莫那班相比,在瘦小鼠和肥胖小鼠濃度 (ng/g) 濃度 (ng/g) 濃度 (ng/g) 10 mg/kg 與腸促胰島素類似物共同給藥不會影響 CRB-913 的大腦穿透

來源:*Morningstar 等人 2023 和 **Liu 等人 2021 年 CRB-913:外周限制程度高於 INV-202 大腦濃度(ng/g)單一急性劑量 CRB-913(瘦小鼠)INV-202(瘦小鼠)Rimonabant(瘦小鼠)10 mg/kG 26* 319** 561* 1:12 1:21
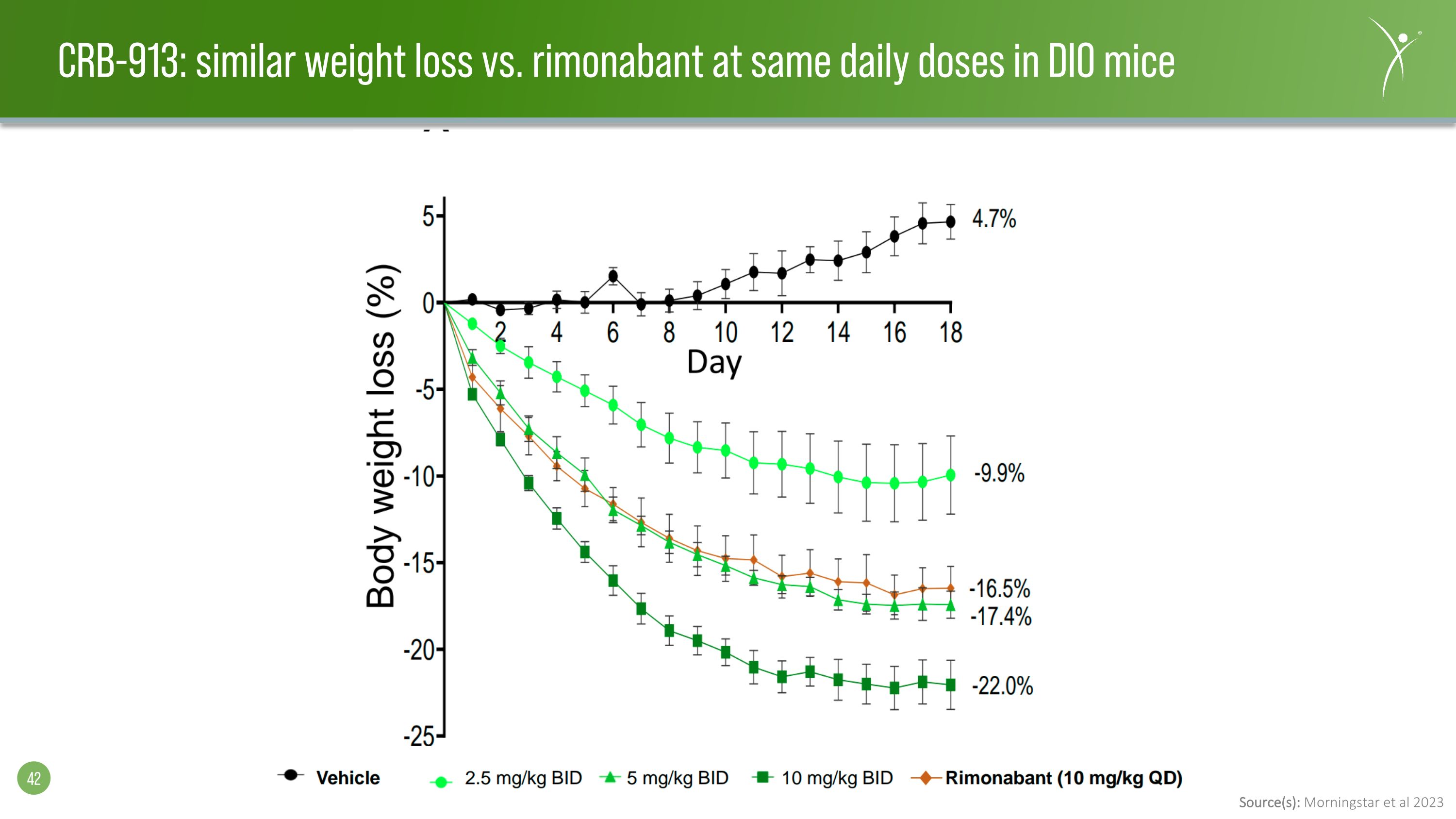
來源:晨星等人 2023 CRB-913:DIO 小鼠每日相同劑量的利莫那班減肥效果與利莫那班相似
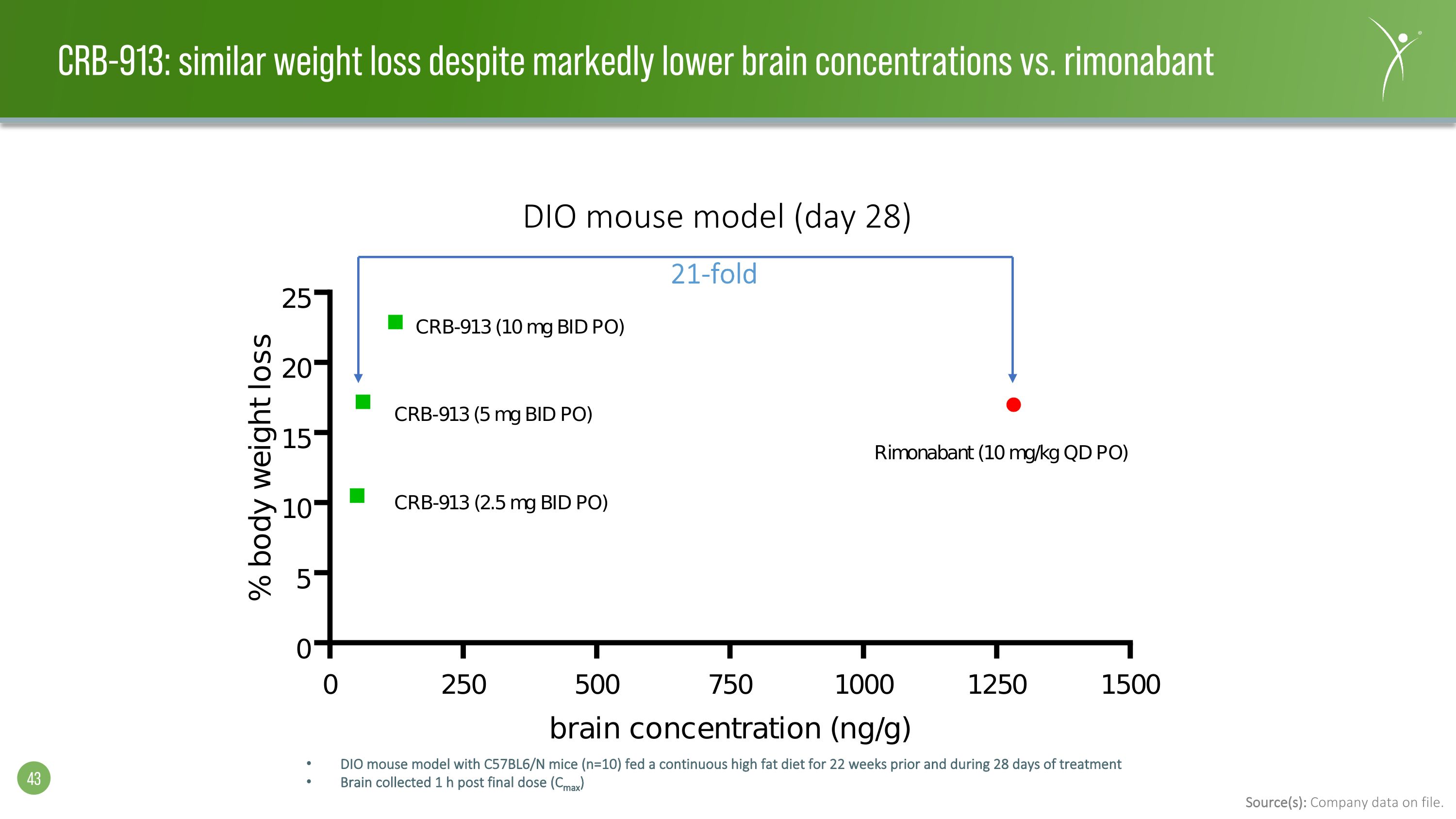
21 倍 DIO 小鼠模型(第 28 天)使用 C57BL6/N 小鼠(n=10)的 DIO 小鼠模型,在治療前 22 周和治療 28 天內,大腦在最終劑量(Cmax)後的 1 小時內收集了持續的高脂飲食。來源:公司存檔數據。CRB-913:儘管與利莫那班相比,大腦濃度明顯降低,但體重仍有類似的減輕
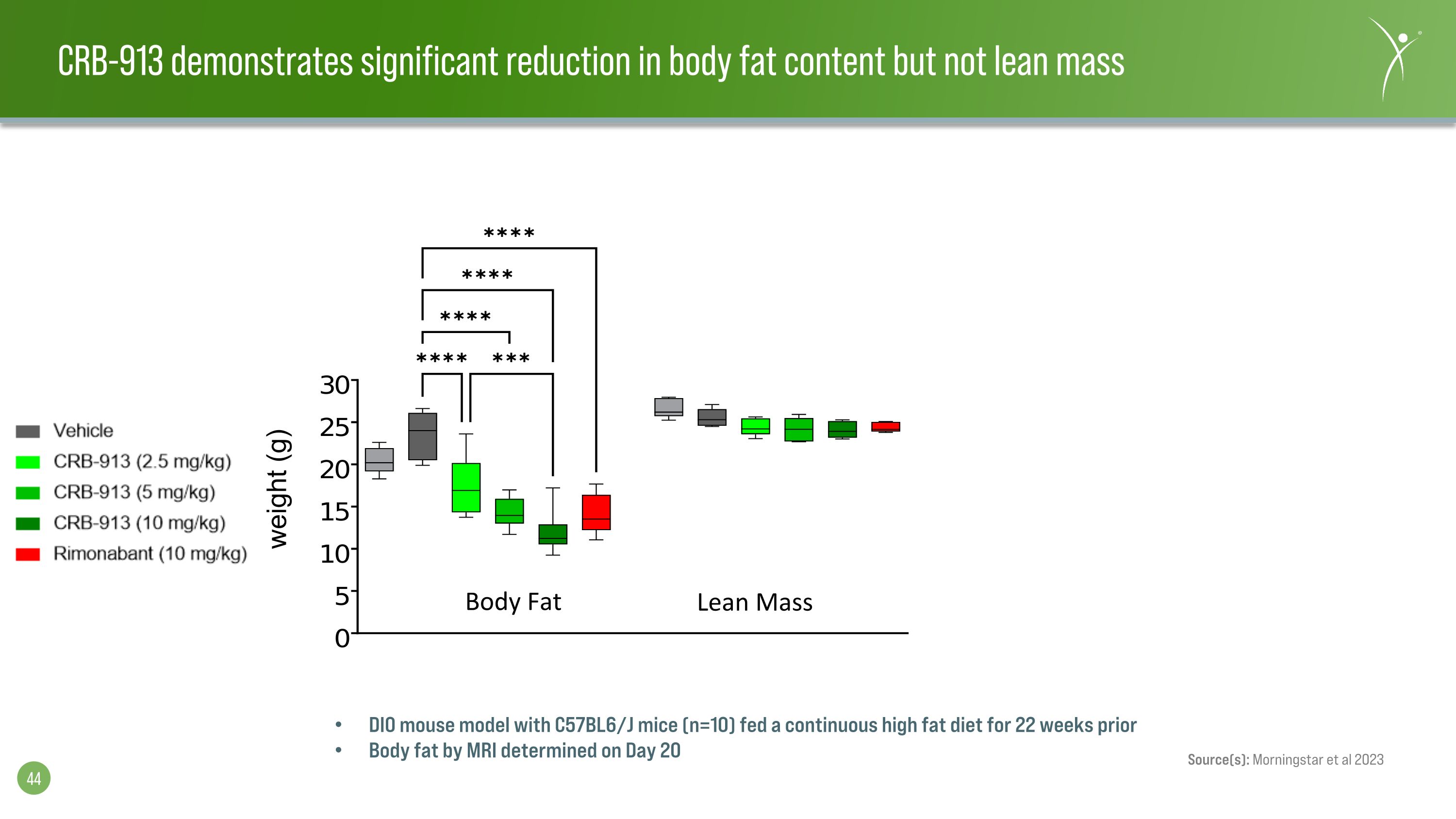
DIO 小鼠模型採用 C57BL6/J 小鼠(n=10)在第 20 天通過磁共振成像測定的 22 周內持續餵食高脂飲食體脂來源:Morningstar 等人 2023 CRB-913 顯示體內脂肪含量顯著降低,但瘦體重沒有明顯降低 (g) 體脂精益質量
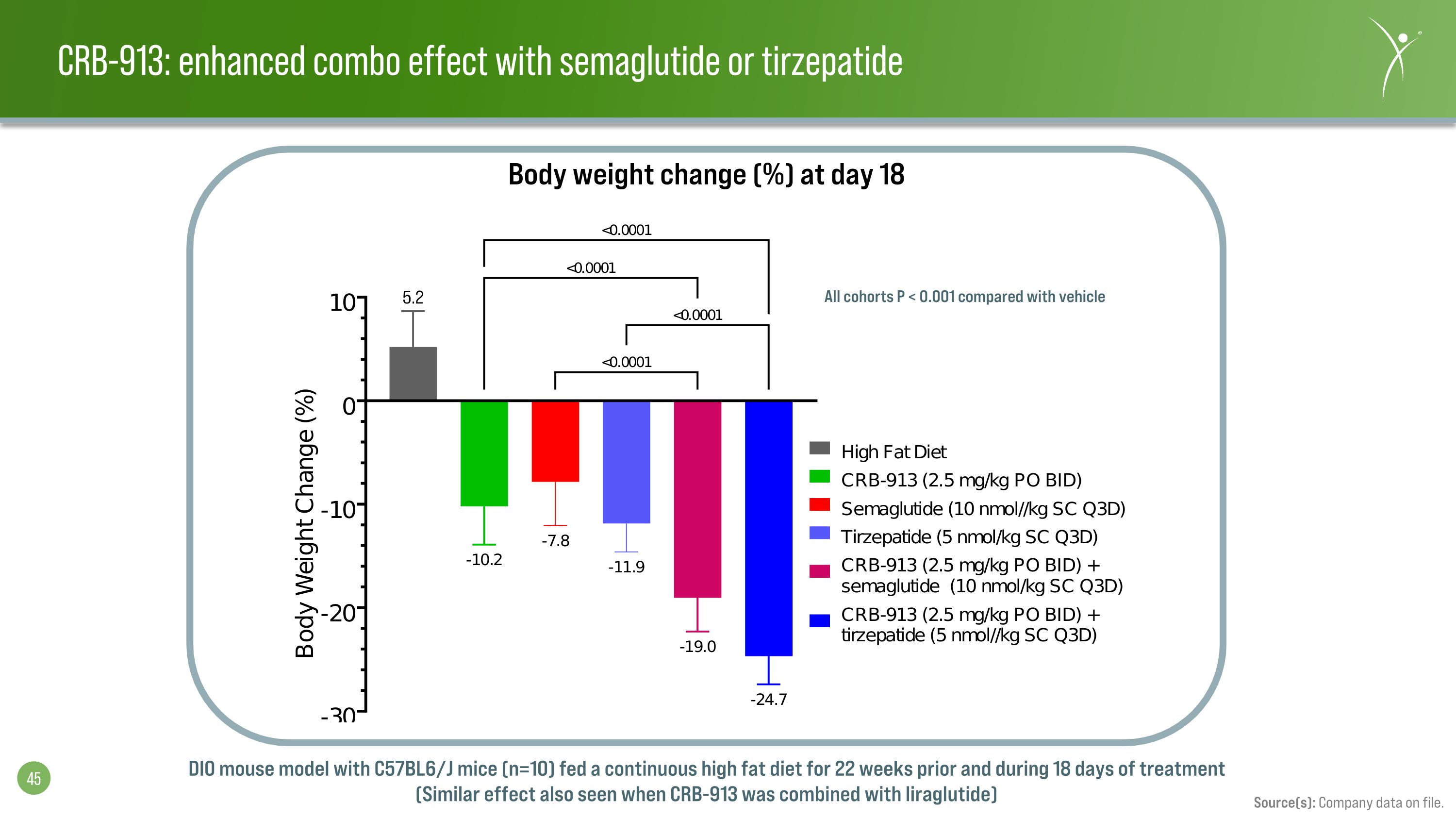
CRB-913:使用semaglutide或tirzepatide增強組合效果來源:公司數據存檔。使用 C57BL6/J 小鼠的 DIO 小鼠模型(n=10)在治療前 22 周和治療期間 18 天持續餵食高脂飲食(CRB-913 與利拉魯肽聯合使用時也會出現類似的效果)第 18 天體重變化(%)所有隊列 P
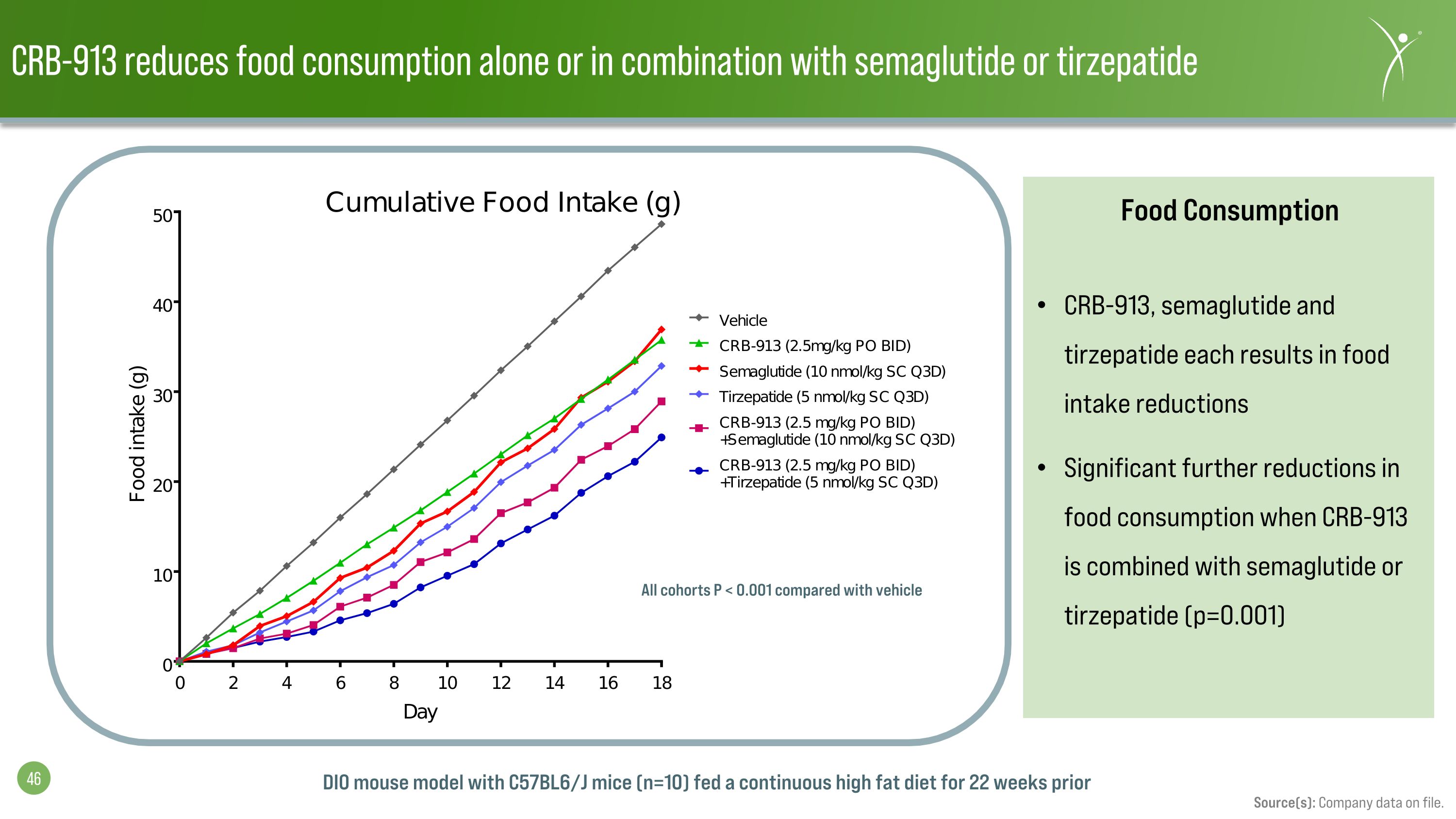
CRB-913 單獨或與西瑪魯肽或替西塞帕肽聯合使用可減少食物消耗量來源:公司存檔數據。食物消費 CRB-913、semaglutide 和 tirzepatide 各導致食物攝入量減少當 CRB-913 與西瑪魯肽或替西西帕肽合用時,食物消耗量將進一步顯著減少(p=0.001)所有隊列 P
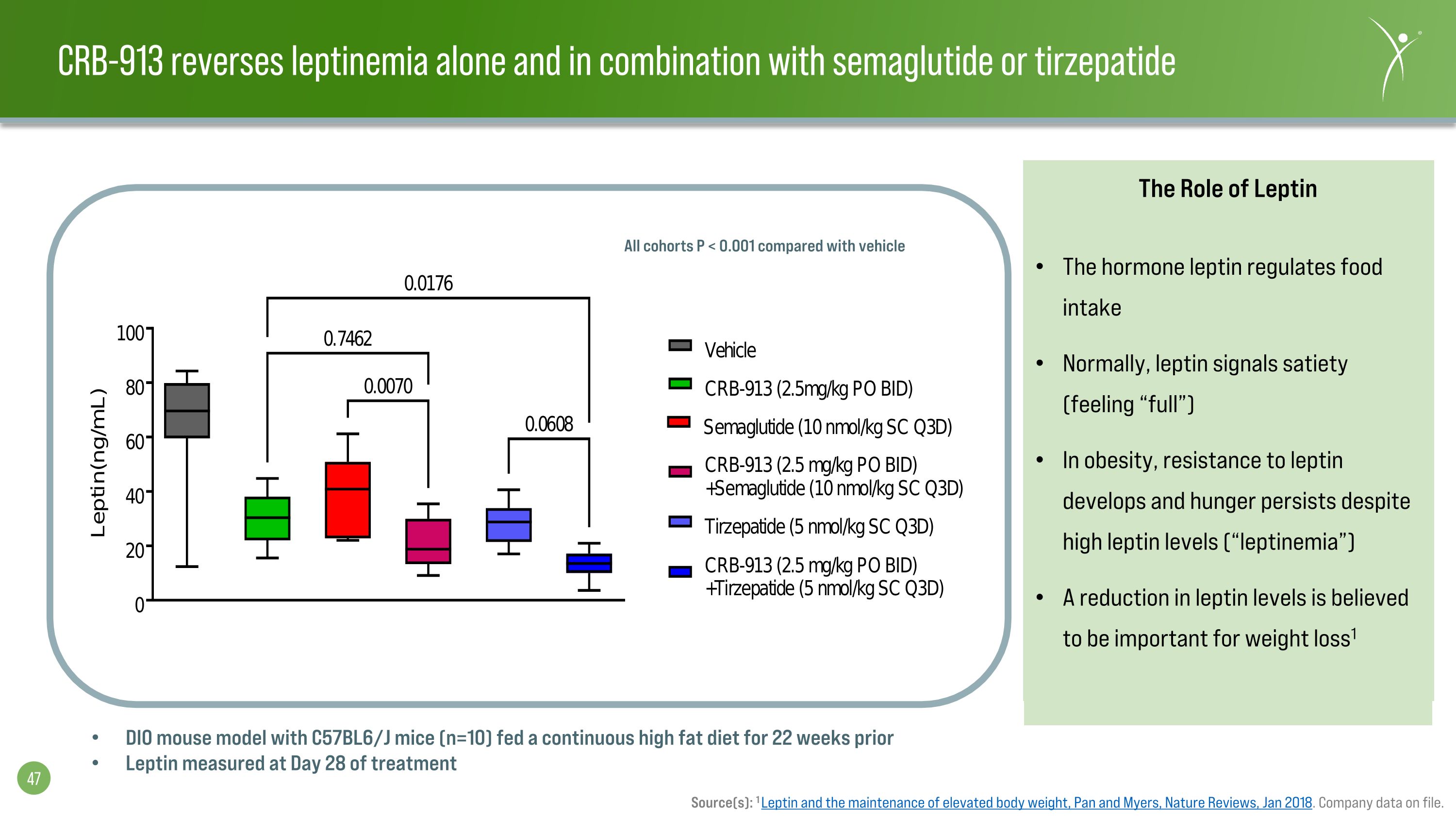
CRB-913 單獨或與西瑪魯肽或替西西帕肽聯合使用可逆轉瘦素血癥來源:1 瘦素和維持體重升高,Pan and Myers,《自然評論》,2018 年 1 月。存檔的公司數據。瘦素的作用瘦素調節食物攝入量通常,瘦素會發出飽腹感(感覺 “飽腹感”)在肥胖中,儘管瘦素水平很高,但對瘦素的抵抗力仍然存在(“瘦血癥”)瘦素水平降低被認為對減肥很重要1 DIO小鼠模型,C57BL6/J小鼠(n=10)持續餵養22周的高脂飲食先前在治療第 28 天測得的瘦素所有隊列 P
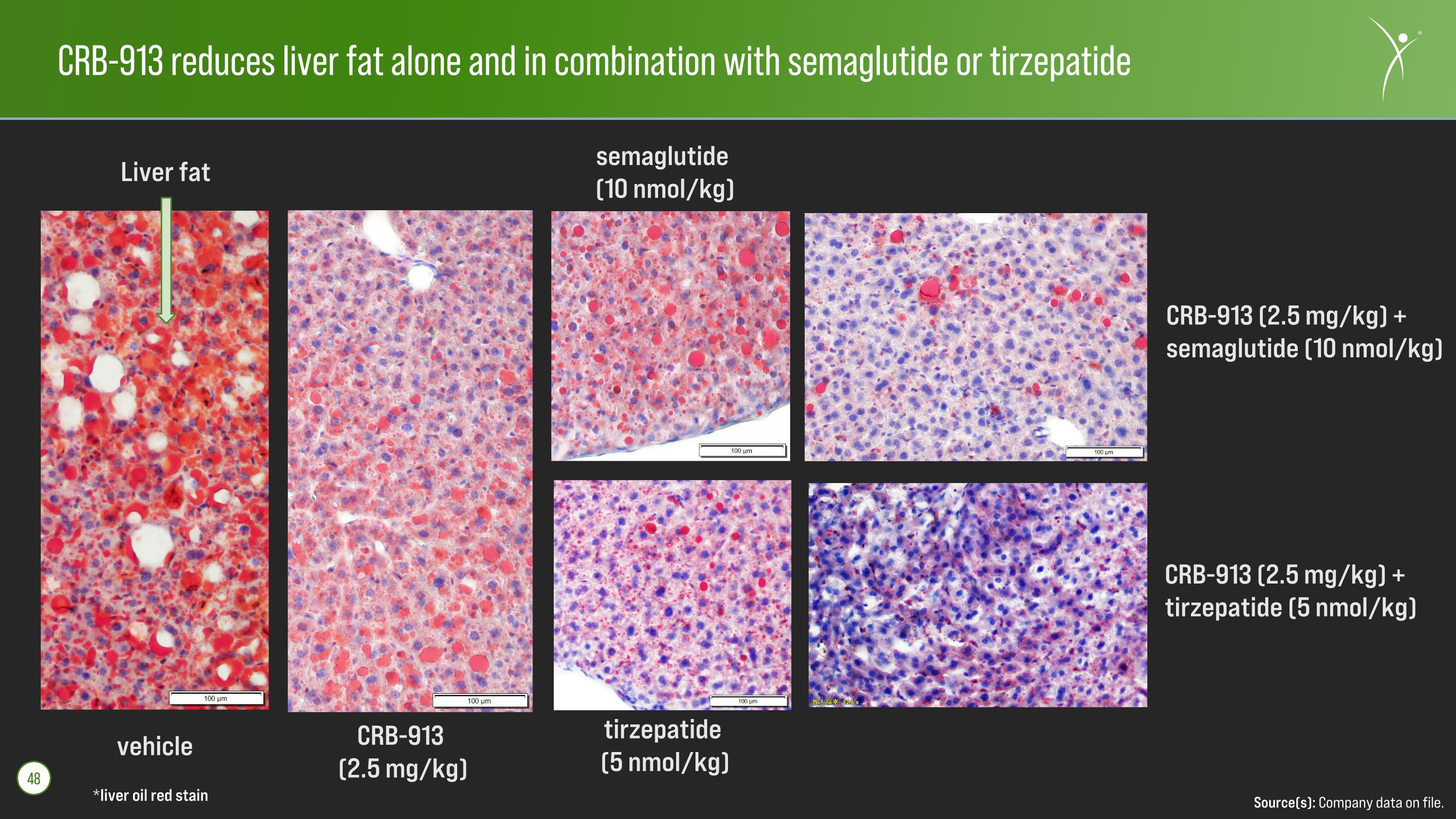
CRB-913 單獨使用以及與索瑪魯肽或替塞帕肽聯合使用可減少肝脂肪 *肝油紅色污漬來源:公司存檔數據。48 輛車 CRB-913(2.5 mg/kg)semaglutide(10 nmol/kg)CRB-913(2.5 mg/kg)+ semaglutide(10 nmol/kg)+ semaglutide(10 nmol/kg)+ semaglutide(10 nmol/kg)+ semaglutide(10 nmol/kg)+ 替塞帕肽(10 nmol/kg)(5 nmol/kg) 肝臟脂肪 CRB-913
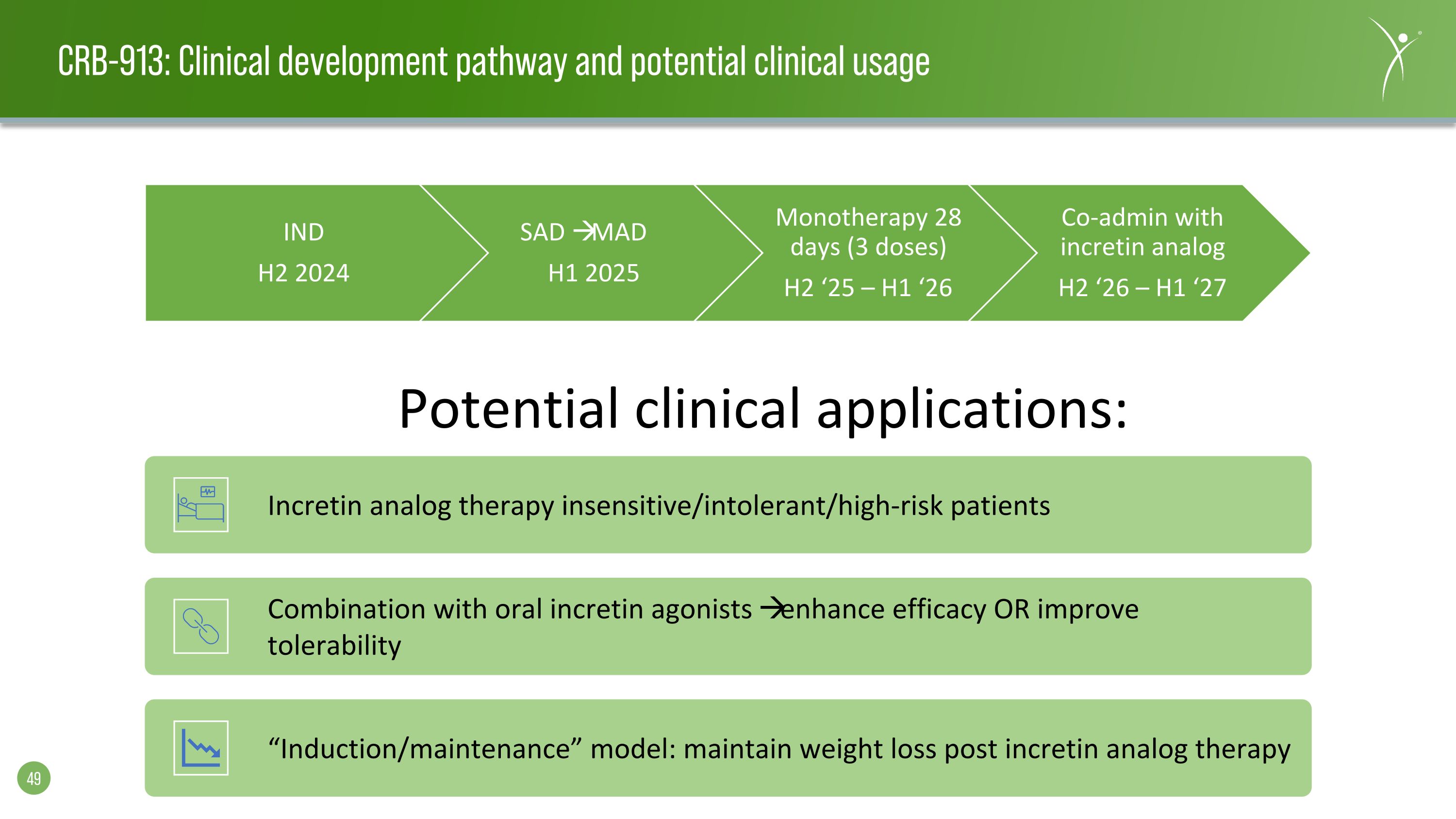
CRB-913:臨牀開發路徑和潛在臨牀用途 IND H2 2024 SAD MAD H1 2025 單一療法 28 天(3 劑)H2 '25 — H1 '26 共同管理與增量素類似物 H2 '26 — H1 '27 潛在的臨牀應用:腸促胰島素類似療法不敏感/不耐受/高危患者與口服促胰島素激動劑聯合使用可增強療效或提高耐受性 “誘導/維持” 模型:腸促胰島素模擬療法不敏感/不耐受/高危患者聯合使用可增強療效或提高耐受性 “誘導/維持” 模型:腸促胰島素模擬療法不敏感/不耐受性/高危患者聯合使用可增強療效或提高耐受性 “誘導/維持” 模式模擬療法

CRB-913:設計為一流的下一代 CB1 逆向激動劑一流的外周限制保護精益質量(肌肉)保持第一代功效增強腸促胰島素類似物的功效

領導力即將到來的催化劑財務

管理團隊尤瓦爾·科恩博士自2014年起擔任首席執行官兼董事Corbus聯合創始人兼首席執行官。自2005年起擔任Celsus Therapeutics的總裁兼聯合創始人。肖恩·莫蘭自2014年起擔任註冊會計師、工商管理碩士首席財務官Corbus聯合創始人兼首席財務官。曾在新興生物技術和醫療器械公司擔任高級財務管理經驗。Rachael Brake,博士首席科學官專家,曾在多家領先製藥公司開發和執行創新藥物發現和臨牀開發腫瘤學項目。克里斯蒂娜·伯奇(Christina Bertsch)人力資源主管資深人力資源主管為各行各業的大型和小型企業提供戰略人力資源諮詢服務。

董事會大使艾倫·霍爾默退休董事會主席在華盛頓特區從事公共服務超過二十年,包括駐華特使;phRMA 前首席執行官。Avery W. (Chip) Catlin 董事在生命科學公司擁有超過 25 年的高級財務領導經驗;曾任 Celldex Therapeutics 首席財務官兼祕書。尤瓦爾·科恩,博士,首席執行官,自2014年起擔任Corbus聯合創始人兼首席執行官。自2005年起擔任Celsus Therapeutics的總裁兼聯合創始人。Rachelle Jacques 董事超過25年的職業生涯,在美國和全球生物製藥商業領導領域擁有豐富的經驗,包括在罕見病領域發佈多款備受矚目的產品;Akari Therapeutics首席執行官。納斯達克股票代碼:AKTX)John K. Jenkins,醫學博士傑出職業生涯,在美國食品藥品管理局任職25年,包括在CDER和OND擔任高級領導職務15年。Pete Salzmann,醫學博士,工商管理碩士,擁有20年的行業經驗,目前擔任Immunovant(納斯達克股票代碼:IMVT)首席執行官。Immunovant 是一家專注於為自身免疫性疾病患者開發療法的生物製藥公司。Anne Altmeyer,博士、工商管理碩士、mphDirector 在推進腫瘤學研發項目和領導有影響力的企業發展交易方面擁有20年的經驗;現任TigaTX總裁兼首席執行官。Yong (Ben) Ben,醫學博士,工商管理碩士總監,在行業和學術界擁有25年的腫瘤學研發經驗。曾擔任過兩個行業首席營銷官職位,最近一次是在百濟神州(BGNE)。
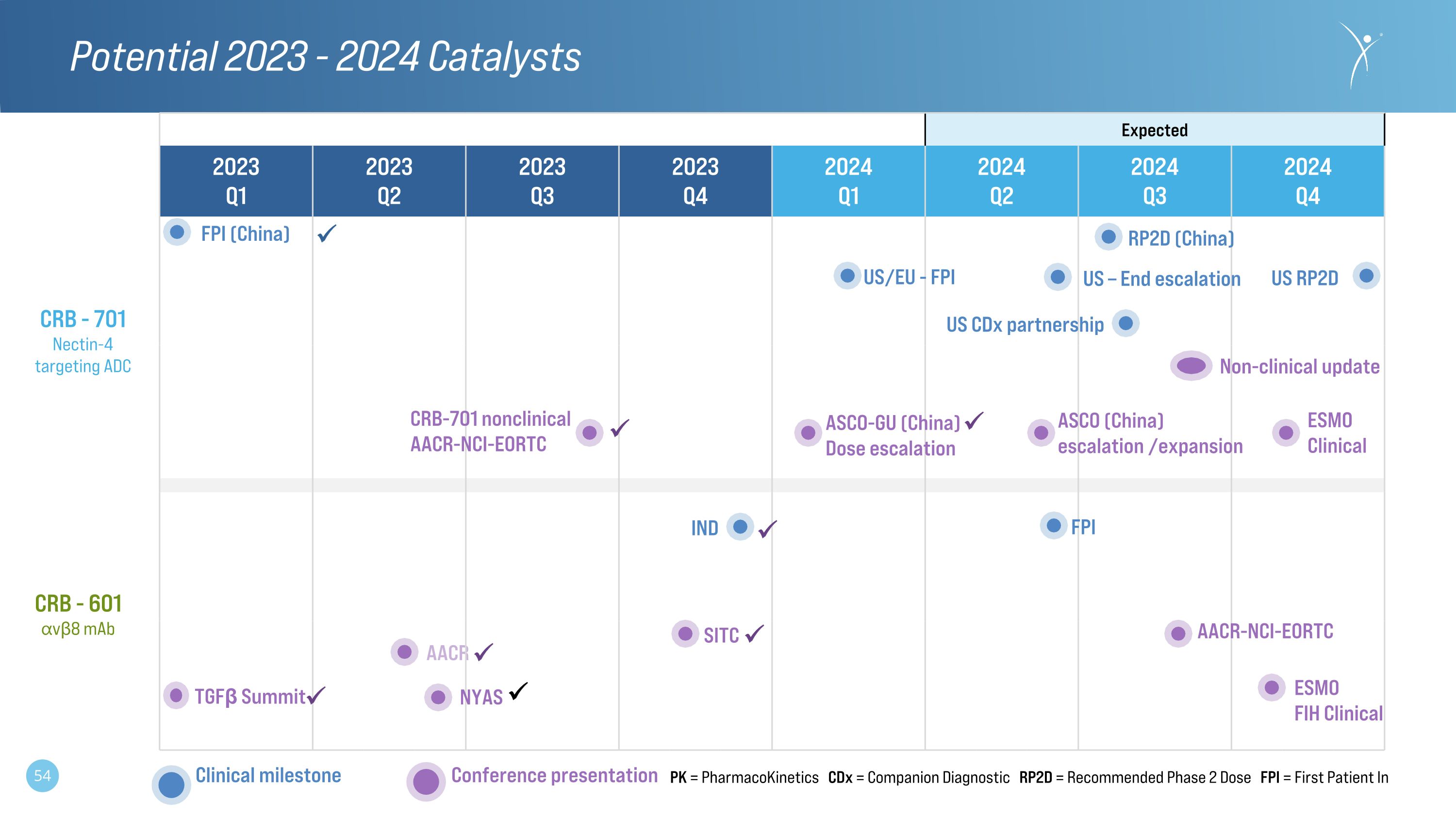
AACR 2023-2024 年潛力催化劑預計於 2023 年第一季度第二季度第 2023 季度第四季度 2024Q1 2024 年第二季度第三季度 2024Q4 CRB-601vβ8 mAb CRB-701Nectin-4 靶向 ADC IND FPI AACR-NCI-EORTC TGFβ 峯會 NYAS 會議演示臨牀里程碑 SITC PK = 藥代動力學 CDx = 伴隨診斷 RP2D = 推薦的第 2 階段 FPI 劑量 = ESMO FIH Clinical 美國 CDx 合作伙伴關係中的第一位患者 CRB-701 非臨牀 AACR-NCI-EORTC 非臨牀更新 ASCO(中國)升級/擴展 FPI(中國)RP2D(中國)ASCO-GU(中國)劑量遞增美國/歐盟-FPI 美國 — 結束升級美國 RP2D ESMO 臨牀

投資摘要將抗vβ8整合素計劃推進到Clinic-IND已通過CRBPticker 1.27億美元專注於開發精準腫瘤學 + 差異化資產臨牀開發下一代Nectin-4截至2024年2月2日的目標為ADC現金和投資以及1,030萬股已發行普通股(全面攤薄後的1110萬股)預計將在2024年下半年通過IND將 CRB-913 推向臨牀

附錄

crb-601 潛力 “同類最佳” vβ8 單抗體

CRB-601 具有增強檢查點抑制的潛力專注於採用精確靶向方法腫瘤微環境中靶向 tgfB 的新機制如果 POC 得到驗證則機會潛力巨大
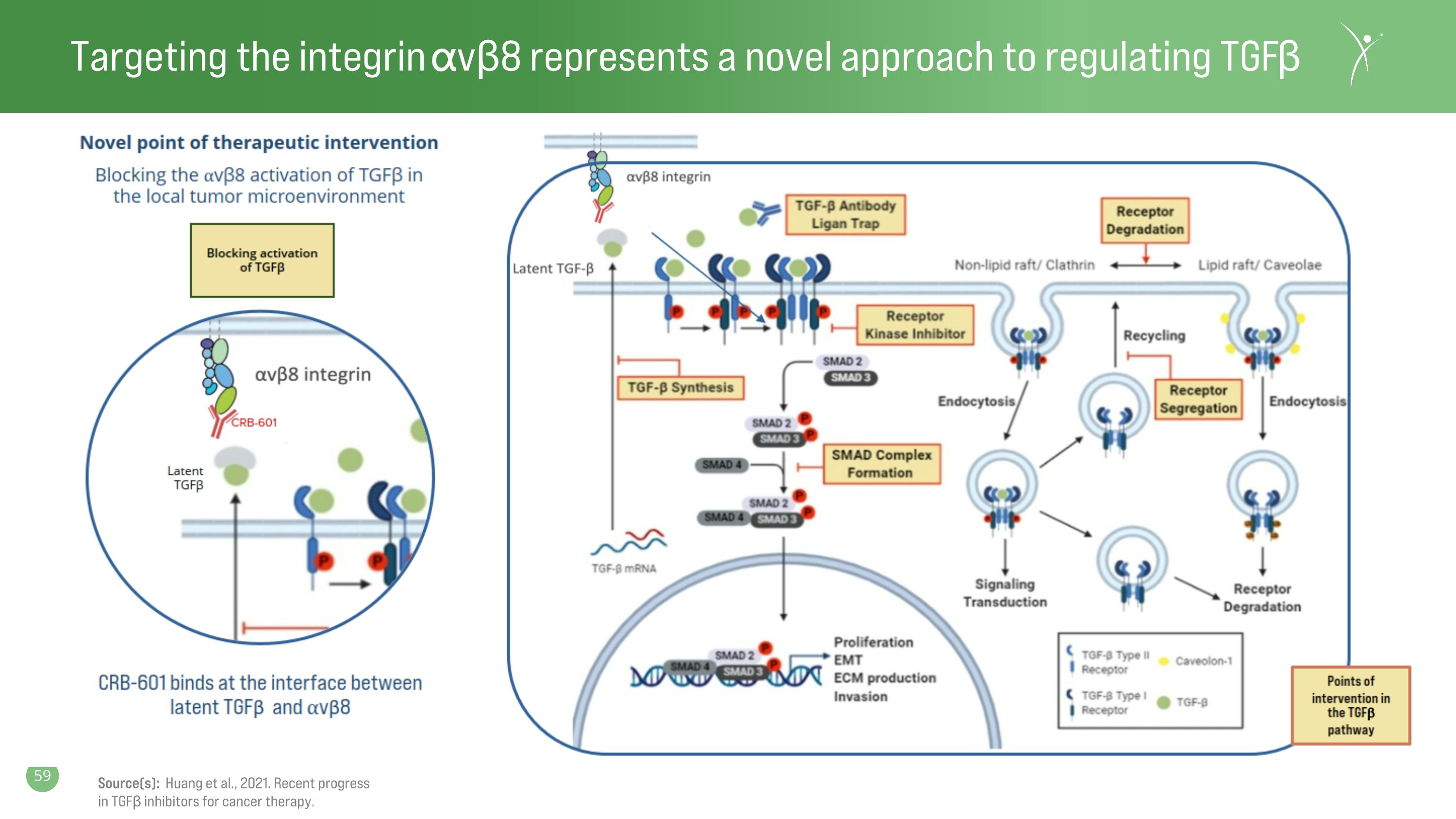
靶向整合素 vβ8 代表了一種調節 TGFβ 的新方法來源:Huang 等人,2021 年。用於癌症治療的轉化生長因子β抑制劑的最新進展。
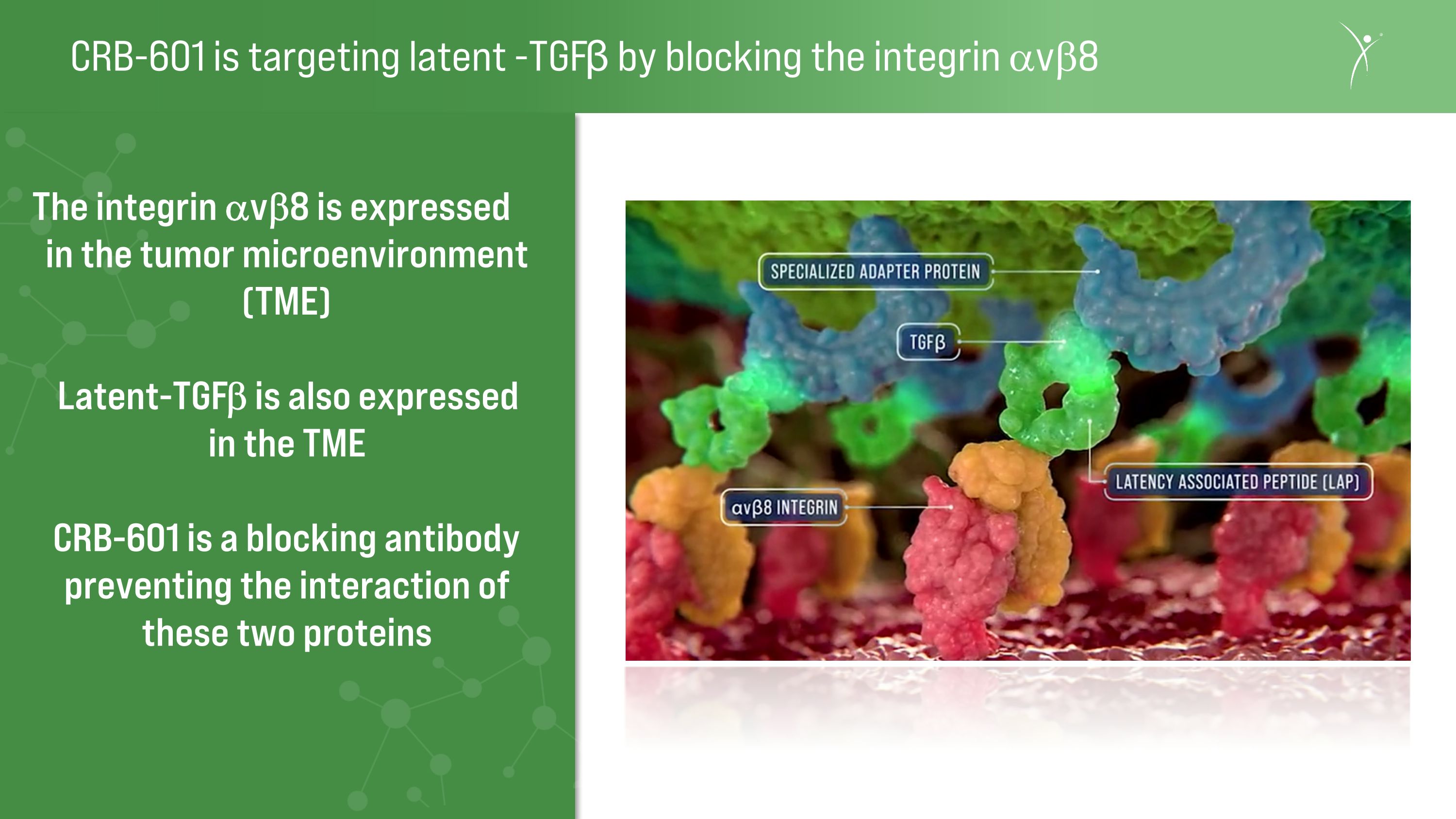
CRB-601 通過阻斷整合素 avb8 來靶向潛伏-tgfβ 整合素 avb8 在腫瘤微環境 (TME) 中表達 latent-tgfb 也在 TME 中表達 CRB-601 是一種阻斷抗體,可以防止這兩種蛋白質的相互作用
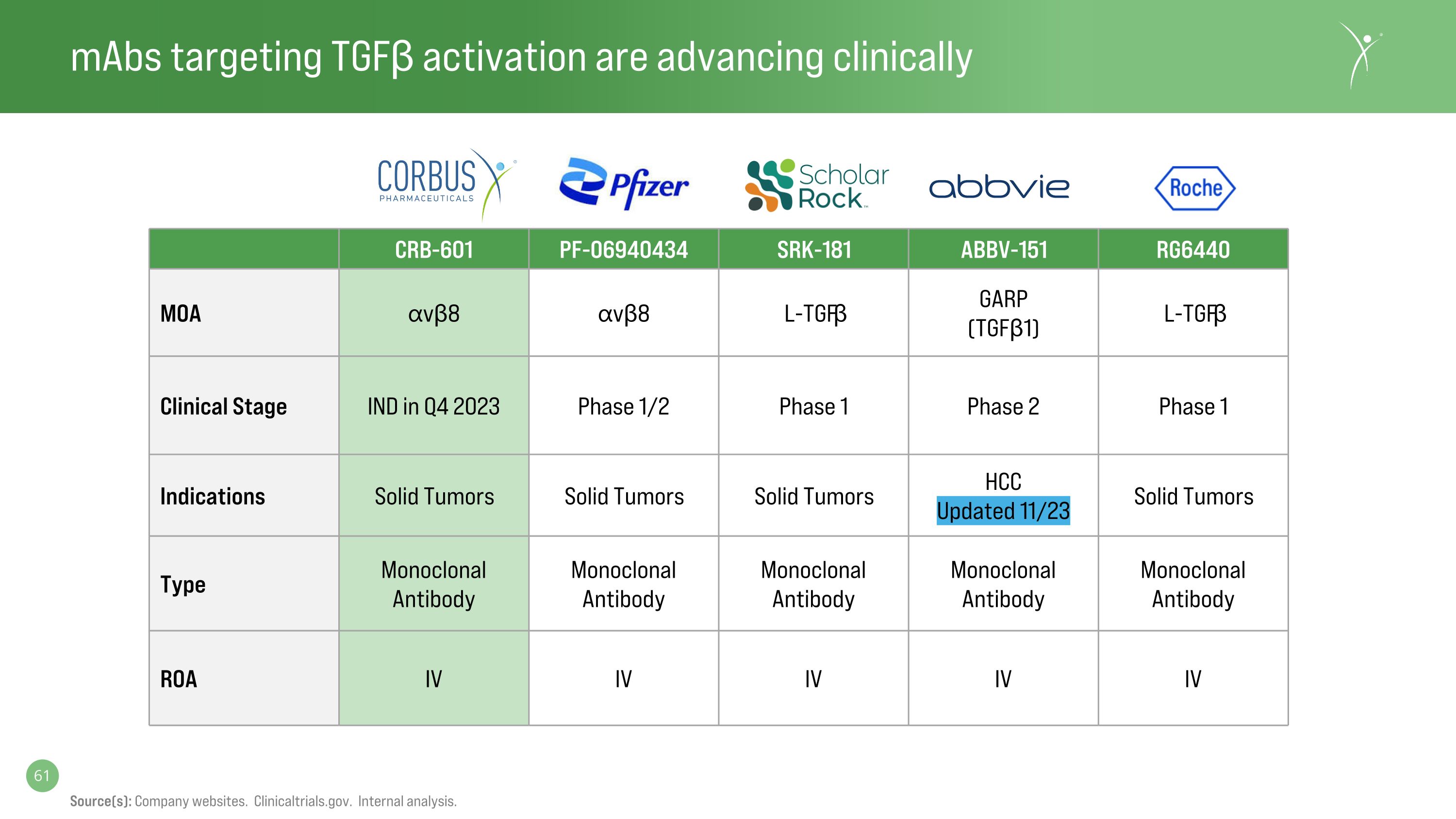
靶向轉化生長因子β激活的單克隆抗體正在臨牀上取得進展來源:公司網站。ClinicalTrials.gov。內部分析。CRB-601 PF-06940434 SRK-181 ABBV-151 RG6440 MOA vβ8 vβ8 L-TGFβ GARP (TGFβ1) L-TGFβ 臨牀階段 2023 年第四季度臨牀階段 IND 1/2 階段 1 期 1 期適應症實體瘤實體瘤實體瘤 HCC 更新於 11/23 實體瘤類型單克隆抗體單克隆抗體單克隆抗體 ROA IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV IV
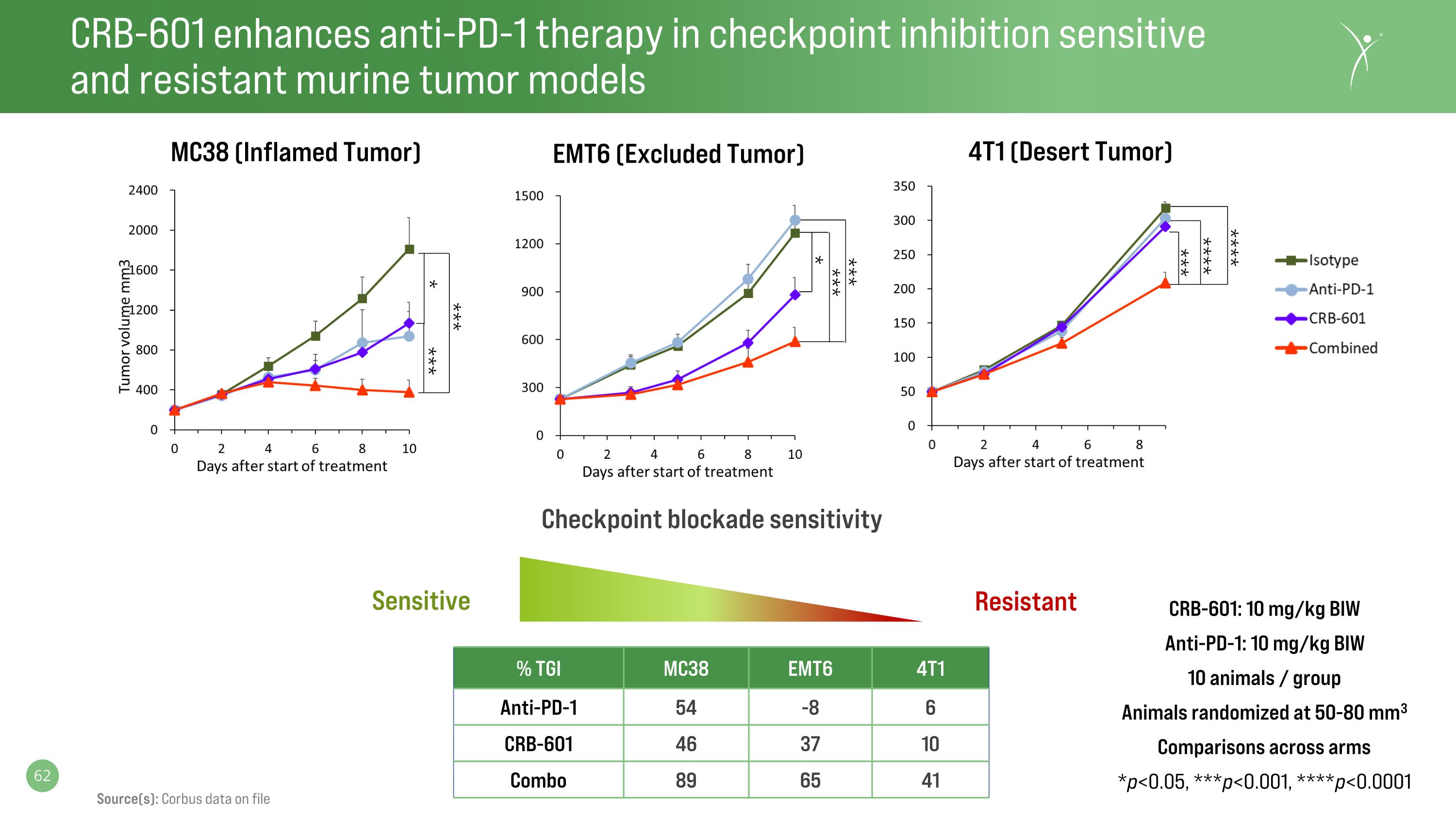
CRB-601 在檢查點抑制敏感和耐藥小鼠腫瘤模型中增強抗 PD-1 療法 CRB-601:10 mg/kg BIW 抗 PD-1:10 mg/kg BIW 10 只動物/羣組動物隨機分組 50-80 mm3 跨臂比較 *p
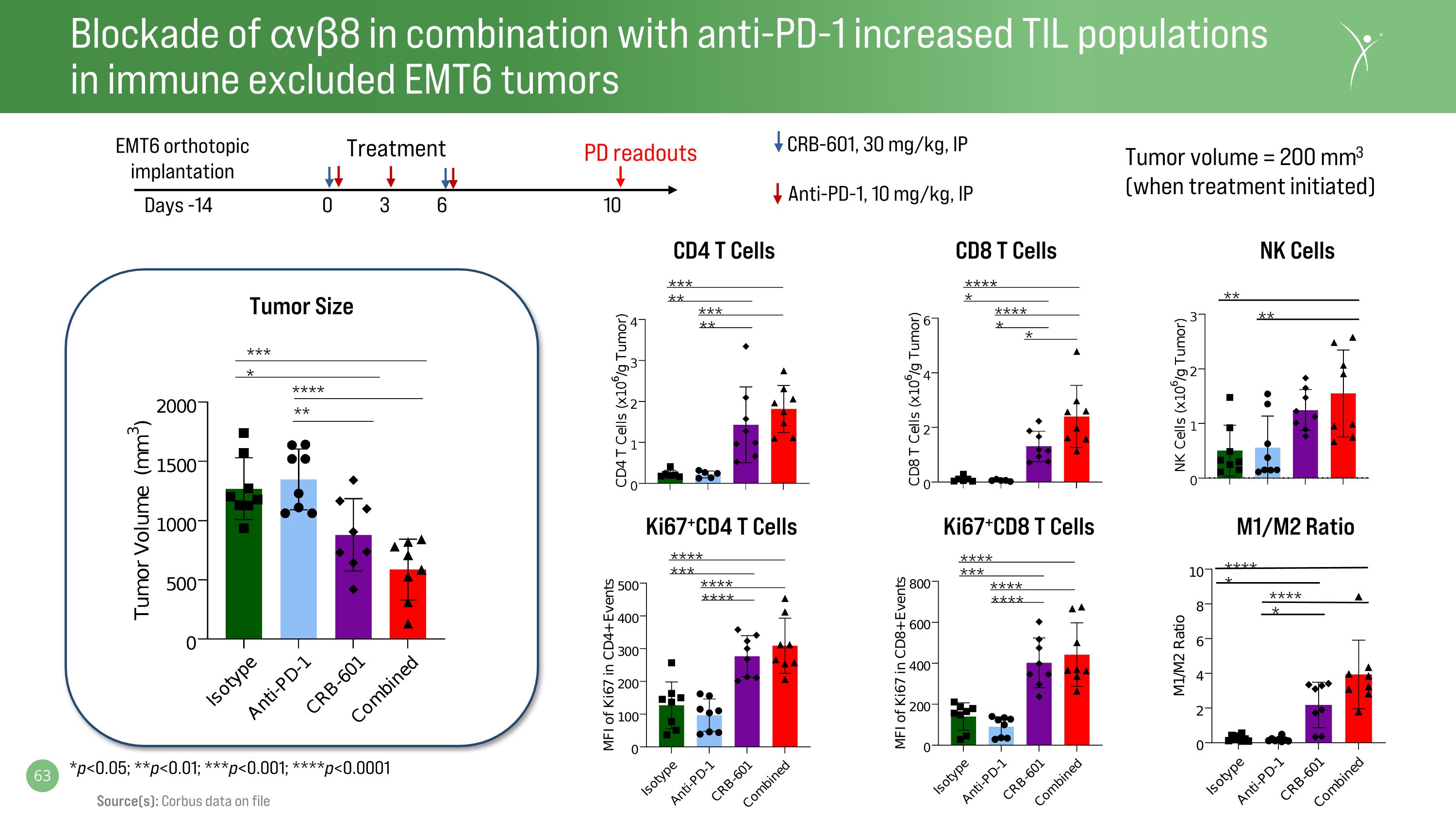
阻斷 vβ8 與抗PD-1結合抗PD-1增加免疫排除外的 EMT6 腫瘤種羣********************************** **** ki67+cd4 T 細胞 CD4 T 細胞 CD8 T 細胞腫瘤大小**** ***** ** ** ** ** ** ** ** ** ** ** ** ** ** *** * 治療天數 -14 0 3 6 10 抗 PD-1,10 mg/kg,IP CRB-601,30 mg/kg,IP EMT6 原位植入 PD 讀數腫瘤體積 = 200 mm3(治療開始時)*p
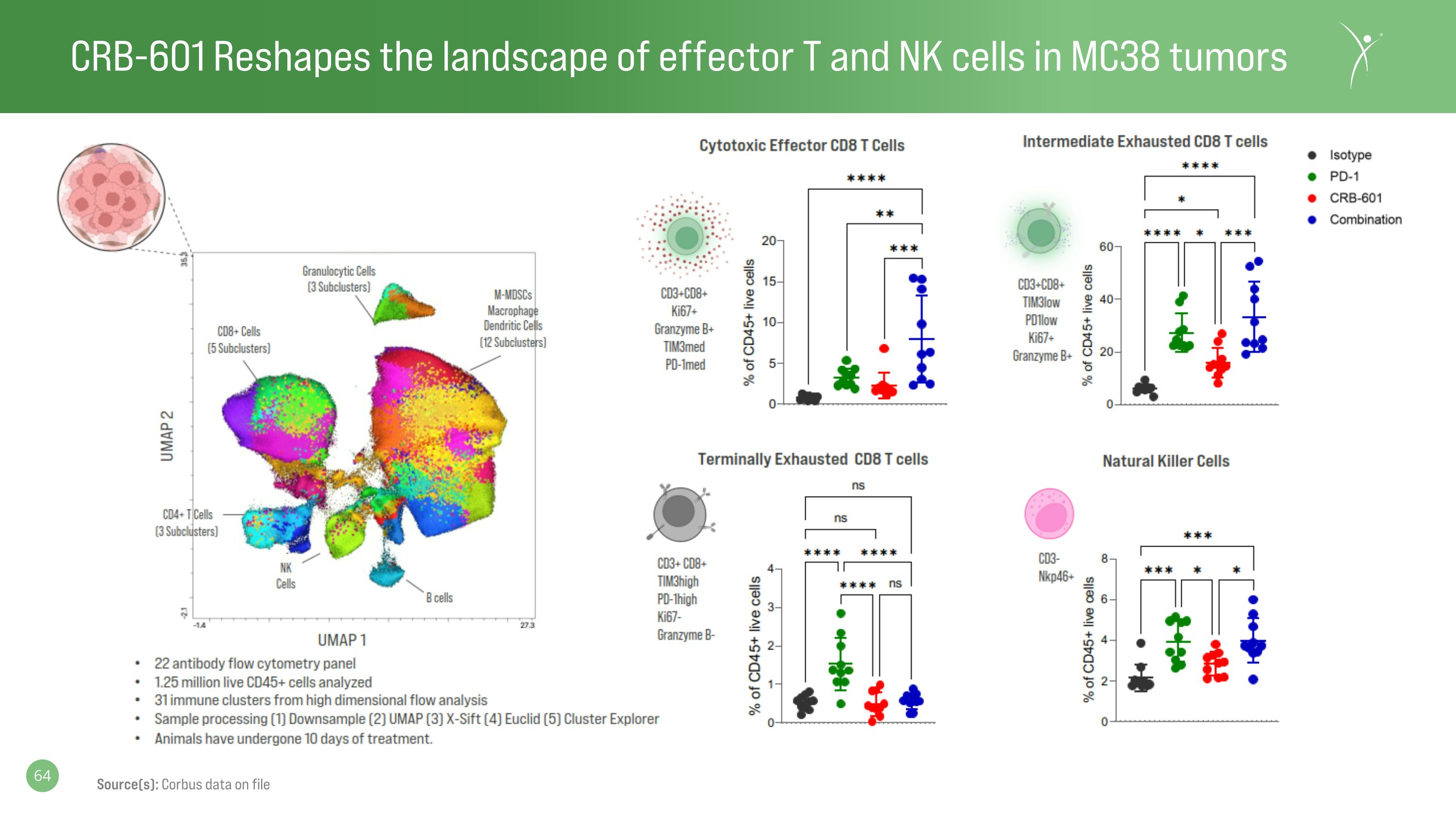
CRB-601 重塑了 MC38 腫瘤中效應 T 和 NK 細胞的格局來源:Corbus 存檔數據
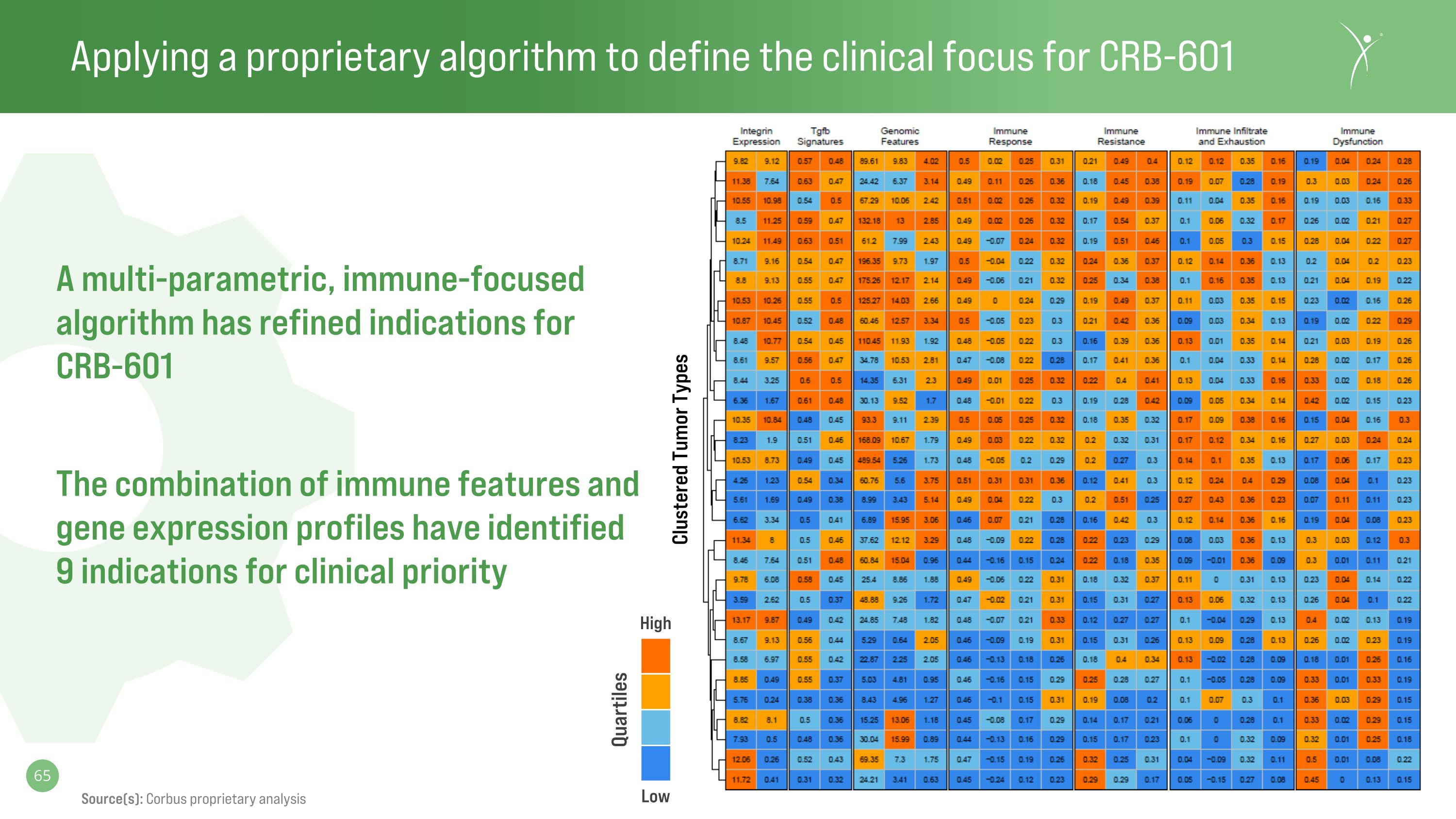
應用專有算法定義 CRB-601 的臨牀重點多參數、以免疫為中心的算法完善了 CRB-601 的適應症。免疫特徵和基因表達譜相結合,確定了9種臨牀優先適應症 High Low Quartiles 來源:Corbus 專有分析聚類腫瘤類型
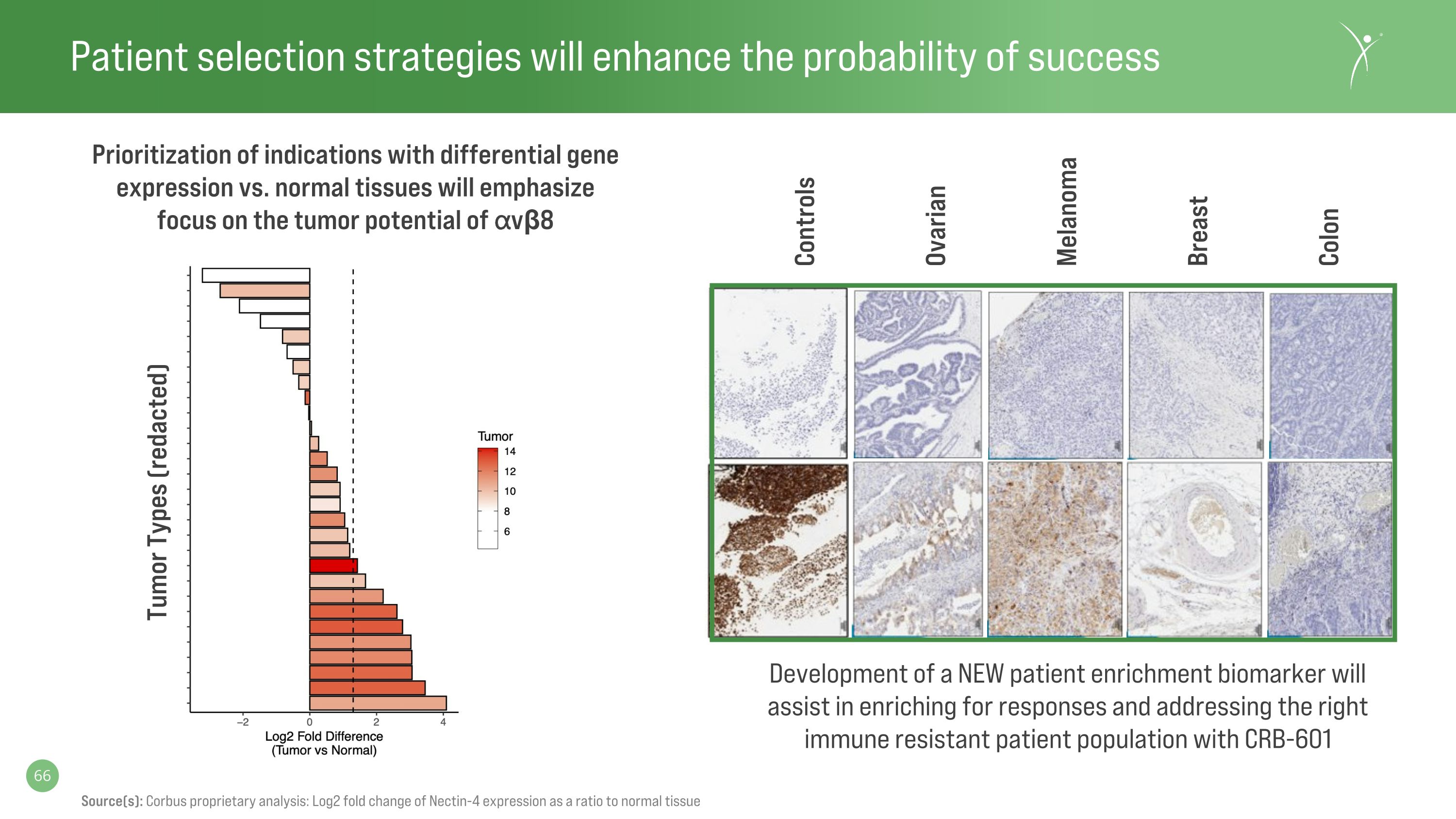
患者選擇策略將提高成功概率來源:Corbus 專有分析:Nectin-4 表達與正常組織之比的 Log2 倍變化控制卵巢黑色素瘤乳腺結腸優先考慮基因表達與正常組織差異的適應症將強調關注腫瘤潛力 vβ8 開發新的患者富集生物標誌物將有助於豐富反應並解決正確的 CRB-601 腫瘤類型免疫耐藥患者羣體(已編輯)

CRB-601 Next Steps IND 於 2024 年 1 月獲得批准 FPI 預計 H1-2024 在 2023 年對潛在患者選擇生物標誌物的非臨牀驗證劑量遞增和確認將是 2024 年的重點