

按設計劃分的癌症免疫療法納斯達克:ITOS 2024 年 1 月

前瞻性陳述本演示文稿包含前瞻性陳述。任何不只是歷史事實陳述的陳述都是前瞻性陳述。諸如 “相信”、“預測”、“計劃”、“期望”、“將”、“可能”、“打算”、“準備”、“看”、“潛在”、“可能” 等詞語以及類似的表述旨在識別前瞻性陳述。這些前瞻性陳述包括與我們的候選產品和組合的潛在益處有關的陳述,包括belrestotug有可能成為該領域最高質量的TIGIT,EOS-984 的機制作為單一療法或聯合療法可能產生深遠影響,以及衝動可能增強化療治療反應;預計2024年將是ITEOS的決定性一年;我們的2024年臨牀和數據生成計劃,包括啟動 TIGIT 第 3 期註冊研究,有來自 GALAXIES Lung-201 和 TIG-006 HNSCC 的臨牀數據,包括 2024 年底來自 A2A-005 劑量遞增部分的臨牀數據,提供了 2024 年第二季度來自 EOS-984 的臨牀前作用機制數據,以及來自 2024 年底晚期惡性腫瘤的 1 期劑量遞增試驗的主要數據;我們的目標是在 1L NSCLC 中獲得 belrestotug 的商業批准,並分支到早期的產品線,甚至可能擴展到各種各樣的 IO 適宜的腫瘤;我們的 TIGIT 生物標誌物在識別靶向適應症方面的潛力亞羣;我們的市場機會和可能有資格獲得候選產品的患者數量;我們與葛蘭素史克合作的潛在好處,以及預計2024年將是這種合作勢頭強勁的一年;以及我們預計到2026年的現金流,其中考慮啟動多項TIGIT 3期試驗。這些前瞻性陳述涉及風險和不確定性,其中許多是ITEOS無法控制的。由於此類風險和不確定性,實際結果可能與這些前瞻性陳述所陳述或暗示的結果存在重大差異。已知的風險因素包括:臨牀前測試和早期臨牀試驗的成功並不能確保以後的臨牀試驗取得成功,臨牀試驗的早期結果不一定能預測最終結果;我們的候選產品的數據可能不足以支持監管部門的批准;由於產品研發和生物製劑製造固有的挑戰和不確定性,ITEO可能會遇到意想不到的成本,或者現金支出可能比目前預期的更快或更慢;預期由於各種原因,包括雙方無法履行協議下的承諾和義務、產品研發和製造限制中固有的挑戰和不確定性,與ITEOS和葛蘭素史克之間的協議相關的利益和機會可能無法實現,也可能需要比預期更長的時間才能實現;ITEOS可能無法執行其業務計劃,包括實現其預期或計劃的監管里程碑和時間表、研究和臨牀開發計劃以及制定其候選產品上市的原因多種多樣,其中一些原因可能不在ITEOS的控制範圍內,包括公司財務和其他資源可能受到限制、無法預期或無法及時解決的生產限制、免疫腫瘤學領域的負面發展,例如不良事件或令人失望的結果,包括與競爭對手療法有關的結果,以及監管、法院或機構的裁決,例如美國專利和商標局對所涉專利的裁決我們的候選產品;以及iTEOS向美國證券交易委員會(SEC)提交的截至2023年9月30日的九個月的10-Q表季度報告中在 “風險因素” 標題下確定的風險,以及公司向美國證券交易委員會提交的其他文件,鼓勵您審查這些文件。關於公司現金流的聲明並未表明公司何時可以進入資本市場。上述任何風險都可能對ITEOS的業務、經營業績和ITEOS普通股的交易價格產生重大不利影響。我們提醒投資者不要過分依賴本新聞稿中包含的前瞻性陳述。ITEOS沒有義務根據本新聞稿發佈之日之後的事件或情況公開更新其前瞻性陳述。2

2024 年是 iTEOS 的決定性一年 TIGIT: PD-1 Doublet 1 預計在 2024 年讀出兩次數據解鎖腺苷途徑 2 預計在 2024 年發佈兩次數據讀出截至 2026 年第三季度已獲資助 3 6.45 億美元的現金
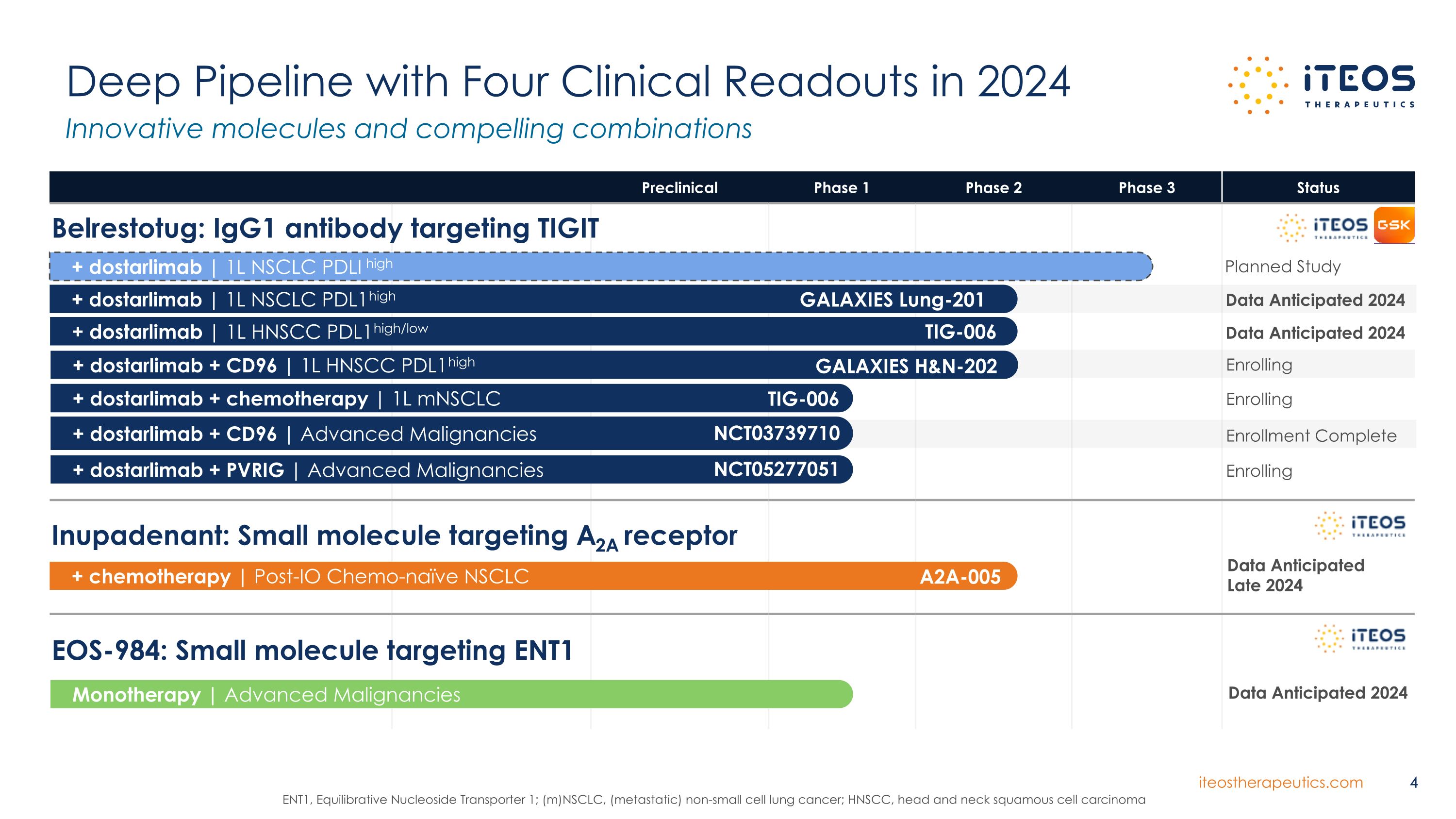
臨牀前 1 期 2 期 3 期深度研發管道,將於 2024 年推出四次臨牀讀數創新分子和引人注目的組合 4 ENT1,平衡核苷轉運蛋白 1;(m)非小細胞肺癌,(轉移性)非小細胞肺癌;HNSCC、頭頸部鱗狀細胞癌 Inupadenant:靶向 A2A 受體 + 化療的小分子 | Post-IO Chemo-naive NASCLC A2A-005 數據預計 2024 年末單一療法 | 晚期惡性腫瘤 EOS-984:靶向 ENT1 的小分子數據預計在 2024 年+ dostarlimab | 1L NSCLC PDL1High + dostarlimab | 1L HNSCCPDL1High/Low + dostarlimab | 1L NSCLC PDLI 高 Belrestotug:靶向 TIGIT GALAXIES Lung-201 TIG-006 + dostarlimab + 化療 | 1L mnsCLC TIG-006 + dostarlimab + CD96 | 晚期惡性腫瘤 NCT03739710 + dostarlimab + PVRIG | 晚期惡性腫瘤 NCT05277051 + dostarlimab + CD96 96 | 1L HNSCC PDL1High GALAXIES H&N-202 數據 2024 年預計數據 2024 年註冊入學人數完成註冊計劃研究

BelrestoTugeos-448/GSK4428859A iTeos 和 GSK 在利用 TIGIT/CD226 軸方面處於獨特的地位
我們在領域佔據優勢2023年勢頭強勁將TIGIT作為目標組件質量很重要指示選擇重要優化試驗設計的重要性
經過驗證的 TIGIT 和 FcγR TIGIT 單一療法活性靶標參與度 Pembrolizumab 對比 Pembrolizumab 需要變革性的 TIGIT: PD-1 Doublet 高品質 PD-1 高品質 TIGIT 7 我們相信我們的 TIGIT: PD-1 Doublet 在關鍵領域具有差異性

POC,概念驗證;Pembro、pembrolizumab 需要變革性的 TIGIT: PD-1 Doublet Belrestotug + dostarlimab 代表差異化的高質量療法 TIGIT PD-1 Dostarlimab PERLA Data4 市場領先的 PD-1 第一階段單一療法活動1 有限數據未披露與 SKY-012 的強大 POC 沒有 Pembro 對比 Fc Silent No Pembro 對比 Fc Silent No Pembro 對比對比 3 負數 ESMO 讀數3 1. iTeOS AACR 2021 2.基因泰克 3 期 Skyscraper-01 研究-2023 年 8 月 22 日發佈 3.ESMO 2023-Advantig-203、Advantig-206、Advantig-202 4.ESMO 2023 — 葛蘭素史克贊助的針對 1L 非小細胞肺癌的 PERLA 第 2 期研究
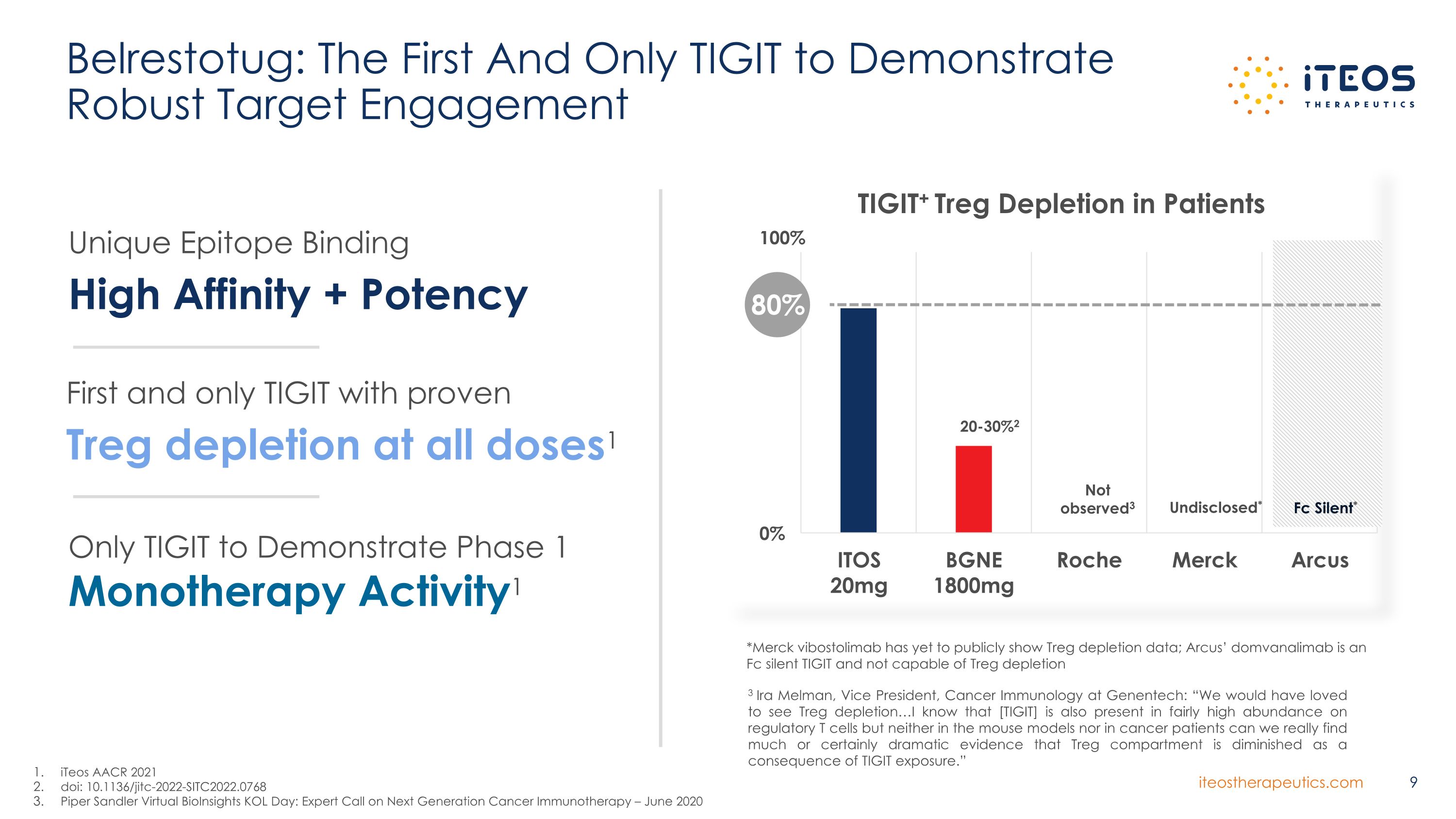
Belrestotug:第一個也是唯一一個表現出強勁靶向參與度的TIGIT iTeos AACR 2021 doi:10.1136/JITC-2022-SITC2022.0768 派珀·桑德勒虛擬生物洞察關鍵人物日:下一代癌症免疫療法專家電話會議 — 2020年6月 *默克維博斯托利單抗尚未公開顯示Treg消耗數據;Arcus的domvanalimab是Fc的沉默TIGIT和無法消耗 Treg 消耗 Fc Silent* 未披露* 100% 3 基因泰克癌症免疫學副總裁 Ira Melman:“我們本來希望看到 Treg 消耗 我知道 [TIGIT]調節性 T 細胞的丰度也相當高,但無論是在小鼠模型中還是在癌症患者中,我們都無法真正找到太多或肯定是戲劇性的證據,表明 TIGIT 暴露導致 Treg 隔室縮小。” 20-30% 2 未觀察到3 獨特的表位結合高親和力 + 效力首先也是唯一一個經證實在所有劑量均可消耗 Treg 的 TIGIT 1 只有 TIGIT 表現出 1 期單一療法活性1 80%
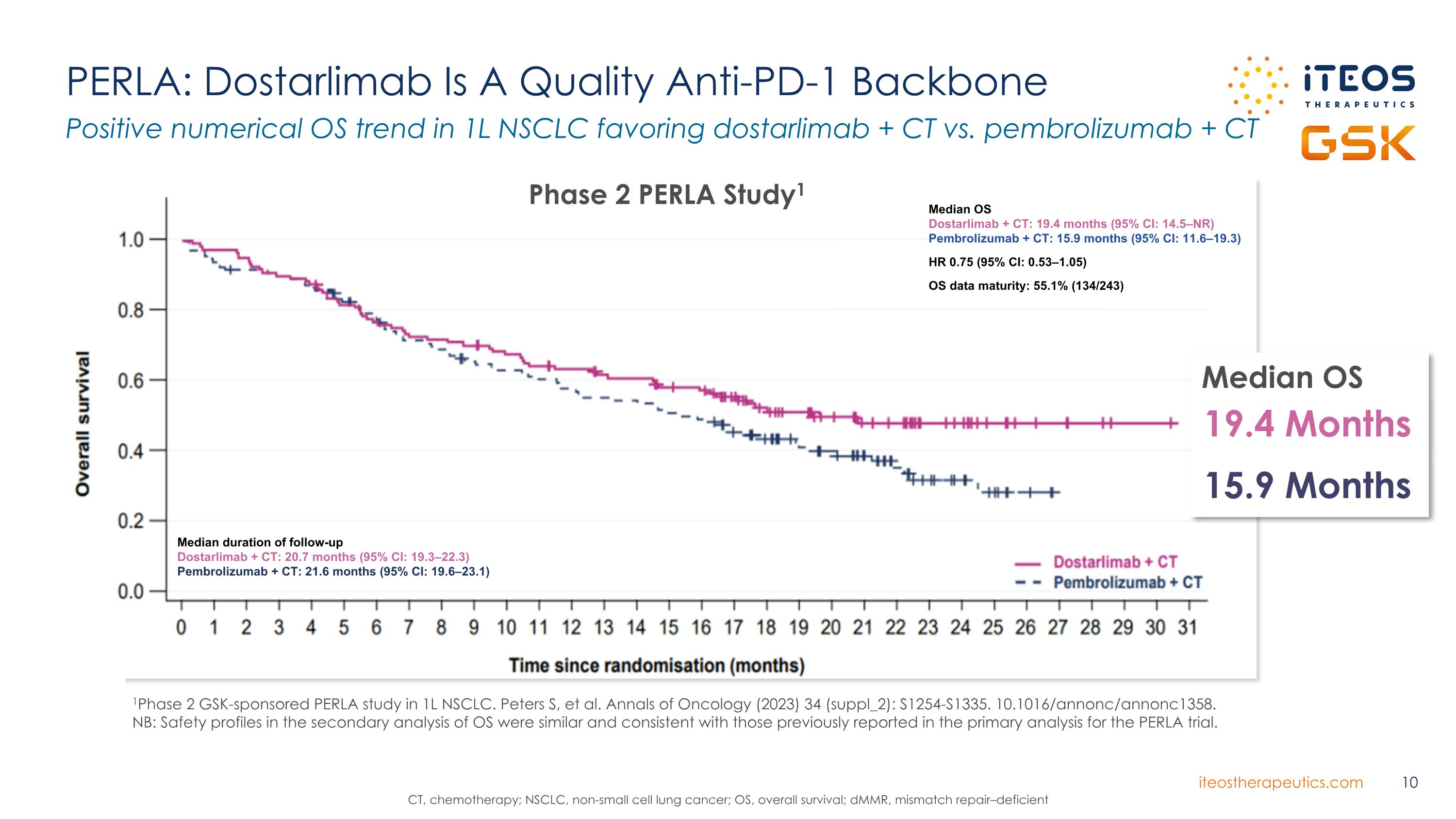
PERLA:Dostarlimab 是抗PD-1的優質骨幹 1L NSCLC 的正數值操作系統趨勢有利於 dostarlimab + CT 與 pembrolizumab + CT、化療;NSCLC,非小細胞肺癌;操作系統,總存活率;dmMR,失配修復——缺乏的 Dostarlimab + CT Pembrolizumab + CT Pembrolizumab + CT 2 期 PERLA Stuybrolizumab + CT Pembrolizumab + CT 2 期 PERLA Stuylamab + CT dy1 操作系統中位數 Dostarlimab + CT:19.4 個月(95% 置信區間:14.5—NR)Pembrolizumab + CT:15.9 個月(95% 置信區間:11.6—19.3)HR 0.75(95% 置信區間:0.53—1.05)操作系統數據成熟度:55.1%(134/243)中位隨訪時長 Dostarlimab + CT:20.7 個月(95% 置信區間:19.3—1.05)操作系統數據成熟度:55.1%(134/243)中位隨訪時間:20.7 個月(95% 置信區間:19.3—22.3) Pembrolizumab +CT:21.6 個月(95% 置信區間:19.6—23.1)操作系統中位數 19.4 個月 15.9 個月 1GSK 贊助的 1L 非小細胞肺癌第 2 階段 PERLA 研究。Peters S 等人《腫瘤學年鑑》(2023)34(suppl_2):S1254-S1335。10.1016/annonc/annonc1358。注意:操作系統二次分析中的安全概況與先前在PERLA試驗初步分析中報告的相似且一致。
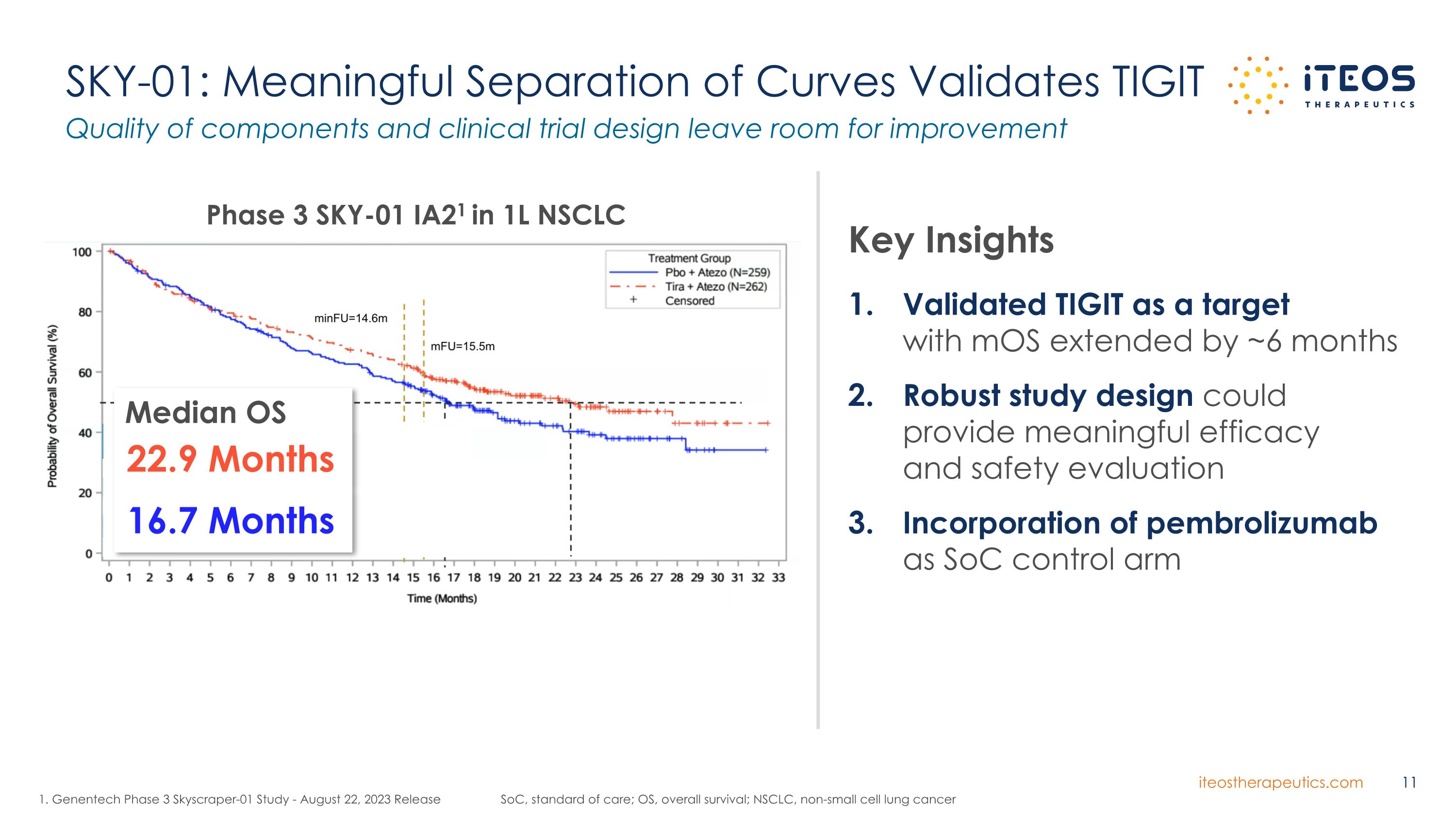
SKY-01:有意義的曲線分離驗證了TIGIT SoC、護理標準;操作系統,總體存活率;NSCLC,非小細胞肺癌成分質量和臨牀試驗設計仍有改進餘地。經過驗證的TIGIT作為靶標的MoS延長了約6個月穩健的研究設計可以提供有意義的療效和安全性評估將pembrolizumab作為SoC控制部門Key Insights 1.基因泰克 3 期 Skyscraper-01 研究——2023 年 8 月 22 日發佈第 3 階段 SKY-01 IA21 在 1L NSCLC 操作系統中位數 22.9 個月 16.7 個月
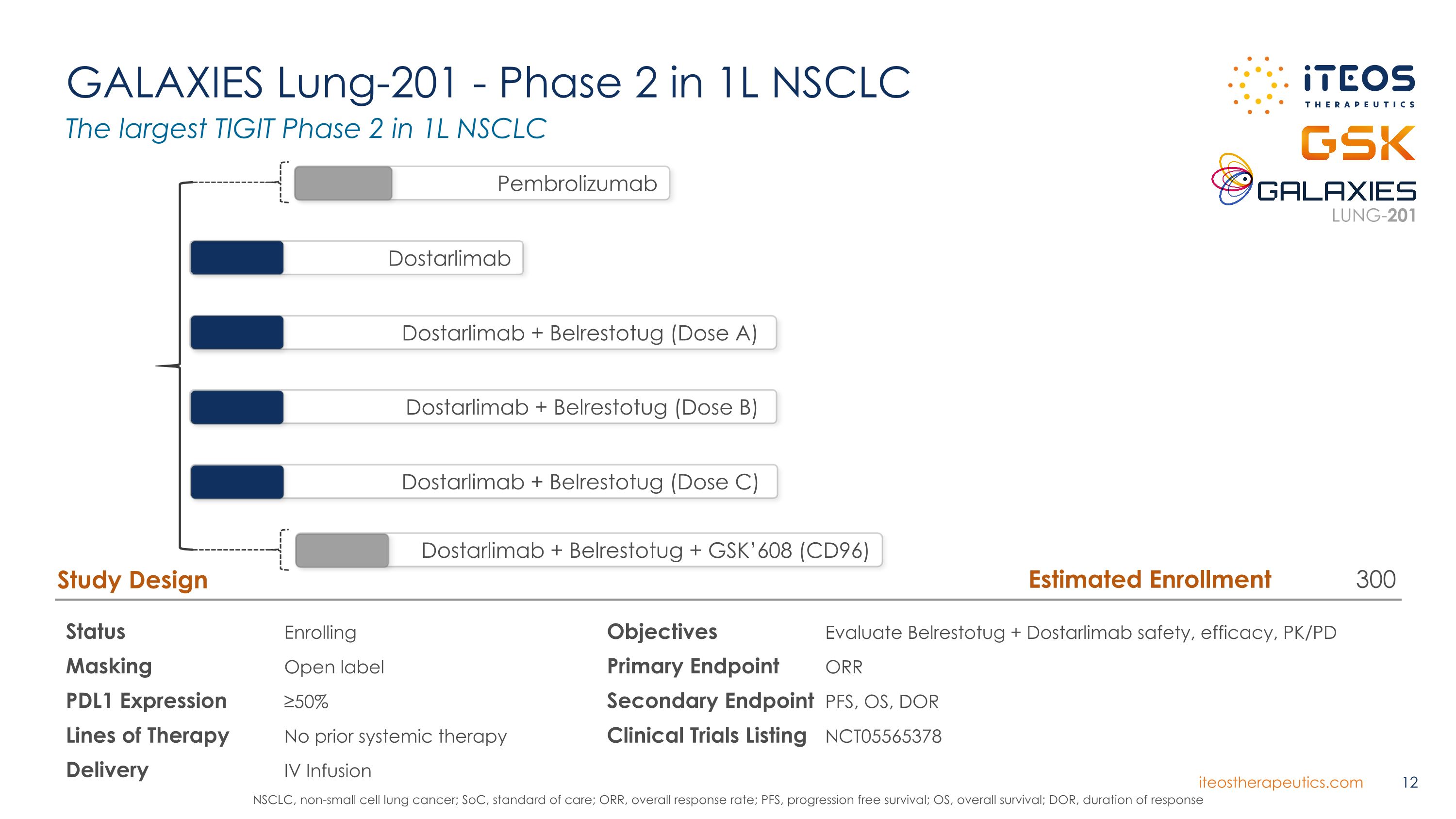
GALAXIES Lung-201-1L NSCLC 狀態第 2 期註冊掩蓋開放標籤 PDL1 表達 ≥ 50% 先前沒有全身療法交付 IV 輸液研究設計目標評估 Belrestotug + Dostarlimab 安全性、療效、PK/PD 主要終點 ORR 次要終點 PFS、OS、DOR 臨牀試驗清單 NCT05565378 Dostarlimab + Belrestotug + GSK'608 (CD96) Pembrolizumab Dostarlimab Dostarlimab Dostarlimab + Belrestotug(劑量 A)Dostarlimab + Belrestotug(劑量 B)Dostarlimab + Belrestotug(劑量 C)1L NSCLC 中最大的 TIGIT 第 2 期,非小細胞肺癌;SoC,護理標準;ORR,總體緩解率;PFS,無進展存活率;OS,總存活率;DOR,緩解持續時間 LUNG-201 估計入學人數 300

1L NSCLC:建立有意義的地位不斷變化的競爭格局有利於高質量的 TIGIT: PD-1 雙胞胎非小細胞肺癌;IO,免疫腫瘤學;POC,概念驗證 31k 患者可能有資格獲得 Belrestotug 有力的科學依據,TIGIT+ Tregs 含量高,T 細胞浸潤率高,非常適合 IO 療法。正確劑量的正確的 3 期策略,對組合、正確的試驗設計和正確的商業方法 1L NSCLC 發射點和臨牀 POC 為未來對其他 NSCLC 的探索提供了可能肺部以外的設置和適應症來源:Kantar,iTeos內部分析

GALAXIES H&N-202:1L HNSCC 狀態註冊掩蓋開放標籤 PDL1 表達 PDL1+ 線路之前沒有全身療法交付 IV 輸液研究設計目標評估抗腫瘤活性、安全性 + 新型 iOS 主要終點 ORR 次要終點 PFS、OS、DOR 臨牀試驗清單 NCT06062420 Dostarlimab + Belrestotug Dostarlimab + GSK'608 (CD96) Dostarlimab + Belrestotug + GSK'608 (CD96) HNSCC,頭頸部鱗狀細胞癌;ORR,總緩解率;PFS,無進展存活率;操作系統,總體存活率;DOR,反應持續時間預計入學人數 360 H&N-202

TIG-006 — 1L HNSCC PDL1高/低狀態註冊屏蔽打開標籤 PDL1 表達 PDL1+ 治療系先前未進行全身療法交付 IV 輸液研究設計目標評估兩個 CPS 人羣中的 Belrestotug + Dostarlimab 主要終點 ORR 次要終點 PFS、OS、DOR 臨牀試驗清單 NCT05060432 CPS 高 ≥ 20 Dostarlimab + Belrestotug(劑量 B)) CPS 低

1L HNSCC:潛在的首次上市機會未得到充分服務的人羣尋求進展 HNSCC、頭頸部鱗狀細胞癌;MoS,總存活率中位數 17,000 名患者可能有資格獲得 Belrestotug 來源:Kantar,iTEOS 內部分析 TIGIT+ Tregs 含量高,T 細胞浸潤率高,適應症適合 PD-1 治療的適應症有充分的科學依據沒有正在進行的第三階段研究,有可能率先進入市場,並且有機會擴展到本地高級設置
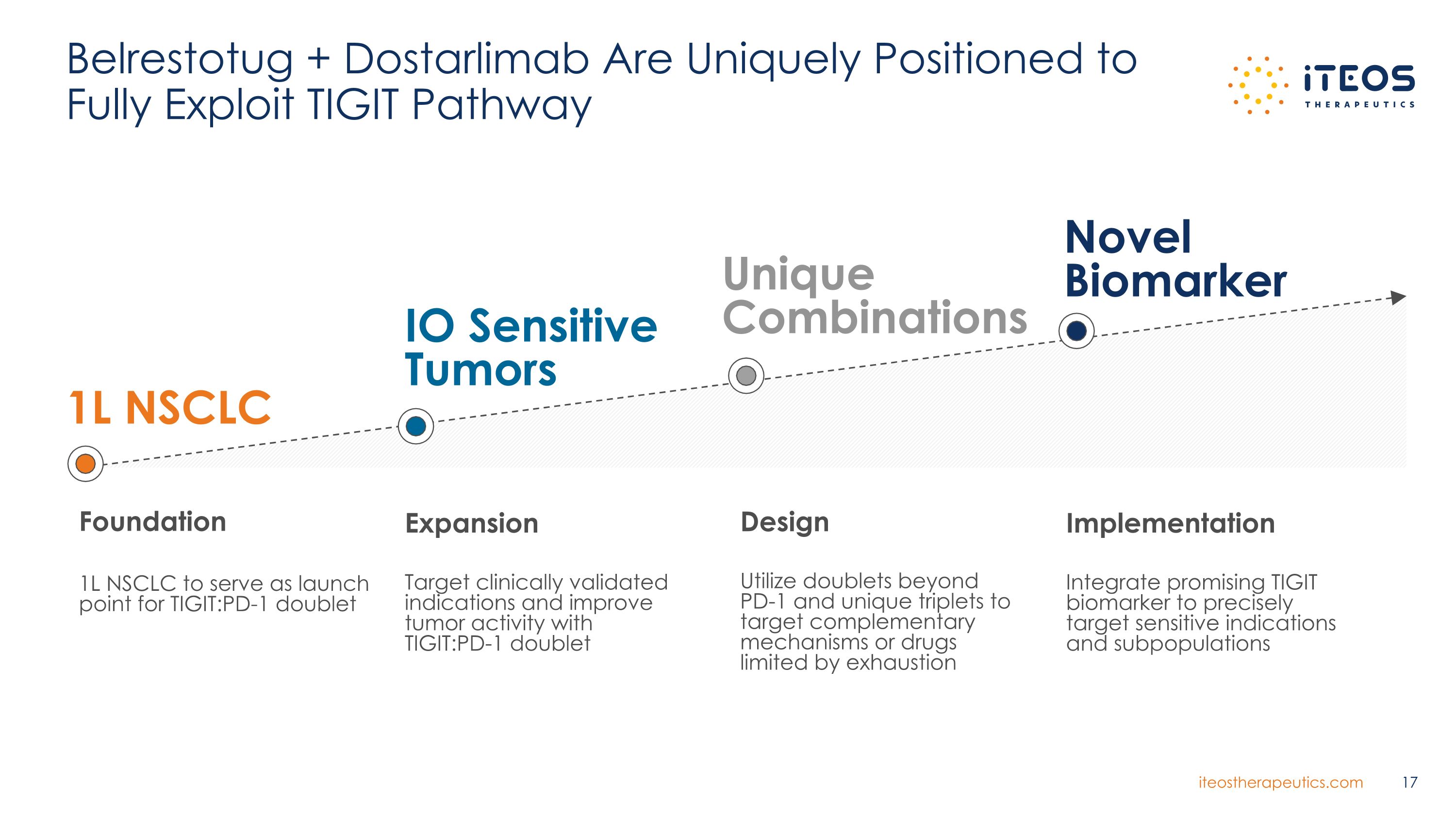
Belrestotug + Dostarlimab 具有獨特的優勢,可以充分利用 TIGIT 途徑 1L NSCLC 基金會 1L NSCLC 作為 TIGIT: PD-1 雙胞胎IO 敏感腫瘤獨特組合擴展靶向臨牀驗證適應症,提高腫瘤活性,利用 TIGIT: PD-1 雙胞胎設計利用超越 PD-1 和獨特的三胞胎來靶向互補機制或受衰竭限制的藥物實施整合有前景的 TIGIT 生物標誌物可精確靶向敏感適應症和亞羣 Novel Biomarker
正確的交易和正確的合作伙伴數據驅動的方法可釋放高質量療法的潛力經過驗證的 PD-1 正確的合作伙伴質量 TIGIT PFS,無進展存活;操作系統,總體存活率;DMMR,不匹配修復缺陷成功因素戰略方針預付款 6.25 億美元,高達 14.5 億美元里程碑開發費用 40% iTeos/60% GSK 美國地區:共同商業化和 50/50 的利潤分成(美國除外):兩位數的特許權使用費高達 20%

腺苷途徑解鎖負責免疫抑制的最有前途的靶標之一
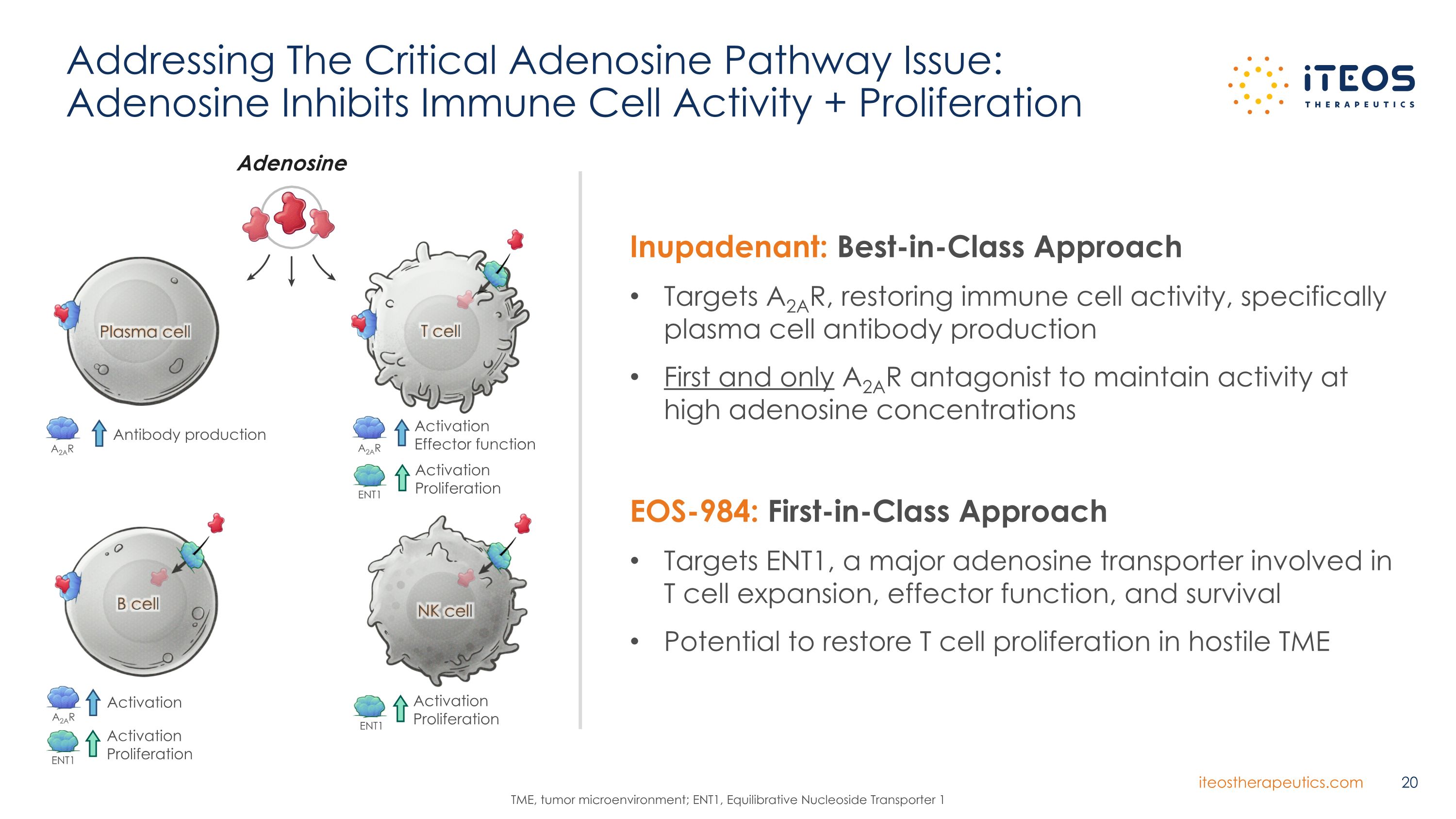
解決關鍵的腺苷途徑問題:腺苷抑制免疫細胞活性 + 增殖 TME、腫瘤微環境;ENT1,平衡核苷轉運蛋白 1 Inupadenant:一流的方法靶向 A2AR,恢復免疫細胞活性,特別是漿細胞抗體的產生第一種也是唯一一種在高腺苷濃度下保持活性的 A2AR 拮抗劑 EOS-984:同類首創的方法靶向 ENT1,一種主要的腺苷參與T細胞擴張、效應器功能和存活的轉運蛋白恢復T細胞的潛力敵對 TME 漿細胞中的增殖抗體產生 A2AR T 細胞激活效應器功能 A2AR 激活增殖 ENT1 B 細胞 ENT1 激活增殖激活 A2AR NK 細胞激活增殖 ENT1 腺苷
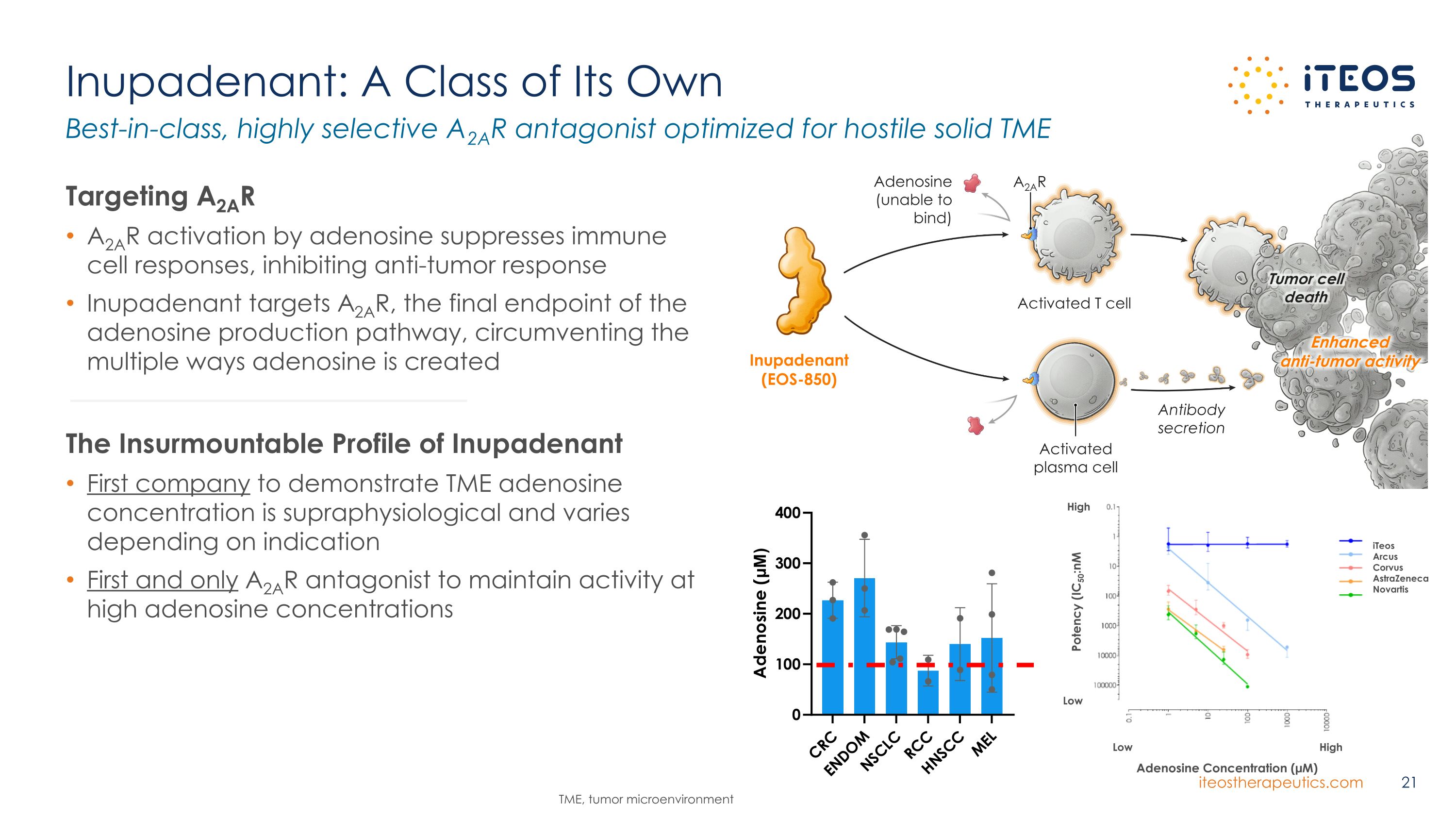
低高腺苷濃度 (µM) 效力 (IC50: nm) 低高 iTEOS Arcus Corvus AstraZeneca Novartis Inupadenant:一類自己的靶向 A2AR A2AR 通過腺苷激活抑制免疫細胞反應,抑制抗腫瘤反應 Inupadenant 靶標 A2AR,這是腺苷產生途徑的最終終點,避開腺苷的多種方式是創建的 Inupadenant 的不可逾越概況第一家證明 TME 腺苷濃度的公司是超生理學的,因適應症而異。第一個也是唯一的 A2AR 拮抗劑在高腺苷濃度下保持活性最佳的高選擇性 A2AR 拮抗劑針對敵對固體 TME TME、腫瘤微環境 A2AR 腫瘤細胞死亡活化 T 細胞活化漿細胞抗體分泌增強的抗腫瘤活性腺苷(無法結合)Inupadenant (EOS-850)
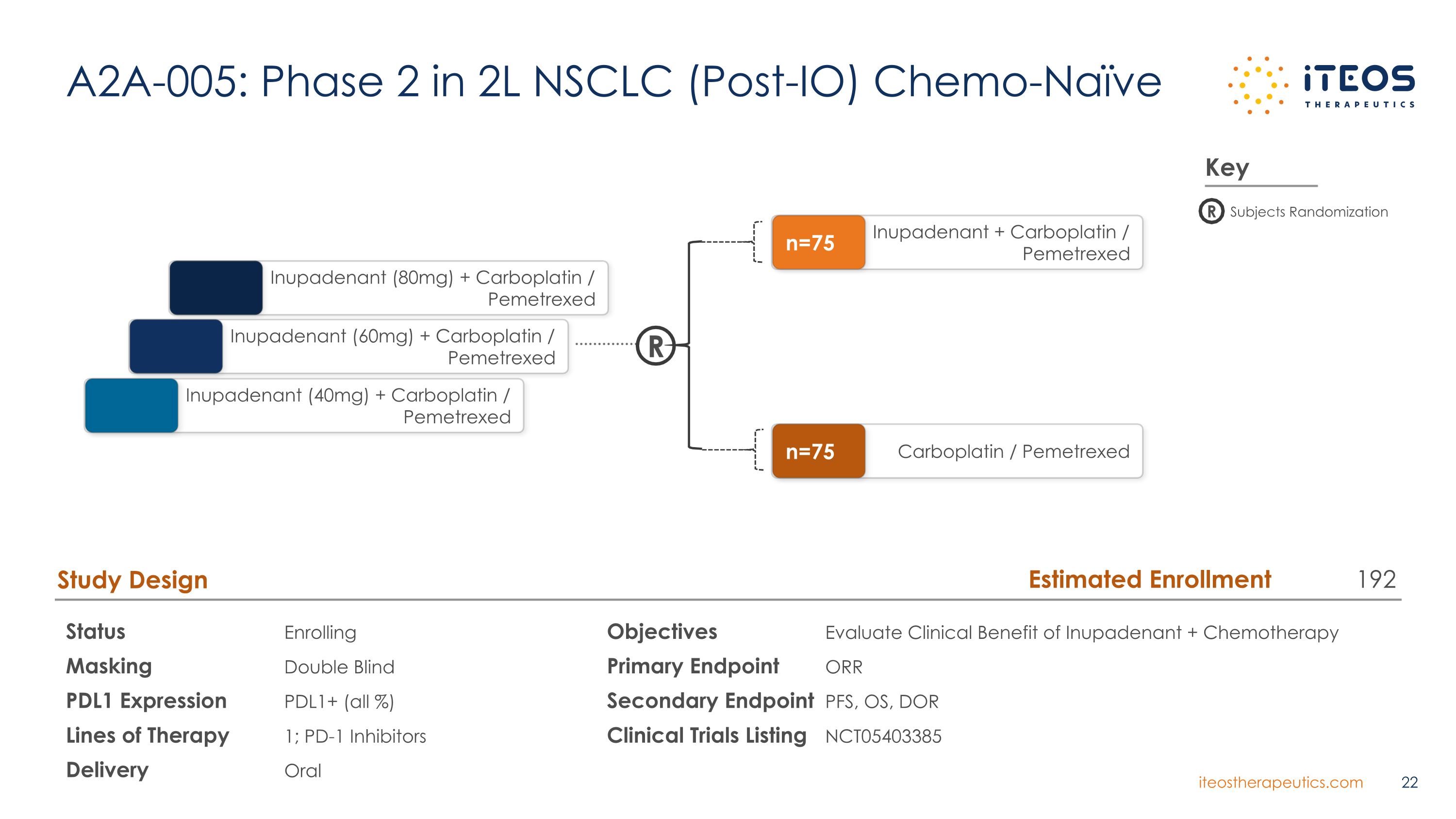
A2A-005:2L 非小細胞肺癌(IO 後)化療初始狀態註冊掩蓋雙盲 PDL1 表達 PDL1+(所有百分比)療法 1;PD-1 抑制劑交付口服研究設計目標評估 inupadenant + 化療主要終點 ORR 次要終點 PFS、OS、DOR 臨牀試驗清單 NCT05403385 R Inupadenant (60 mg) + 卡鉑/培美曲侖的臨牀益處 Inupadenant (40 mg) + 卡鉑/培美曲塞 inupadenant (80 mg) + 卡鉑/培美曲塞 inupadenant + 卡鉑/培美曲塞 n=75 卡鉑/培美曲塞 n=75 卡鉑/培美曲塞 n=75 關鍵 R 受試者隨機化估計入學人數 192

Inupadenant 抵消了化療的關鍵缺點來源:Kantar,iTeos 內部分析化療通過細胞死亡增加腺苷水平,阻礙免疫系統和漿細胞活性 Inupadenant 在高腺苷水平下保持效力和功能,有可能增強化療的治療反應目前僅有 2L NSCLC 的臨牀試驗是具有充分生物學依據的服務不足的人羣尋求進展 NSCLC,非小細胞肺癌;TME,腫瘤微環境,可能有 15k 名患者有資格獲得 Inupadenant
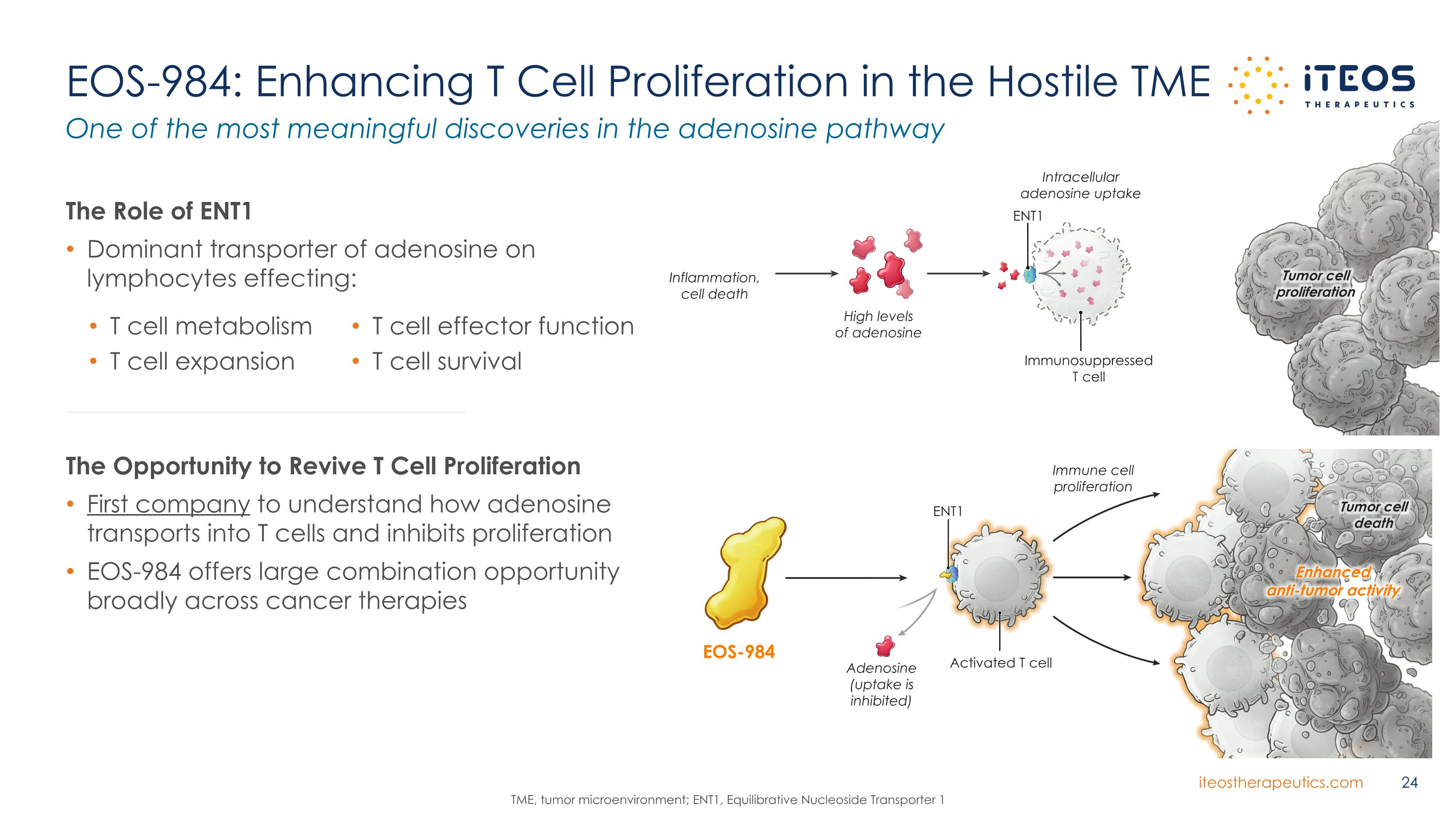
EOS-984:在敵對的 TME 中增強 T 細胞增殖復甦 T 細胞增殖的機會第一家瞭解腺苷如何轉運到 T 細胞並抑制增殖的公司 EOS-984 為癌症療法提供了廣泛的組合機會腺苷途徑中最有意義的發現之一 TME,腫瘤微環境;ENT1,平衡核苷轉運蛋白 1 T 細胞效應器功能 T 細胞存活 ENT1 腺苷顯性轉運蛋白的作用淋巴細胞影響:T 細胞代謝 T 細胞擴張 ENT1 炎症、細胞死亡腫瘤細胞增殖高水平的腺苷免疫抑制 T 細胞細胞內腺苷攝取 ENT1 腫瘤細胞死亡腺苷(吸收受到抑制)激活 T 細胞免疫細胞增殖增強的抗腫瘤活性 EOS-984
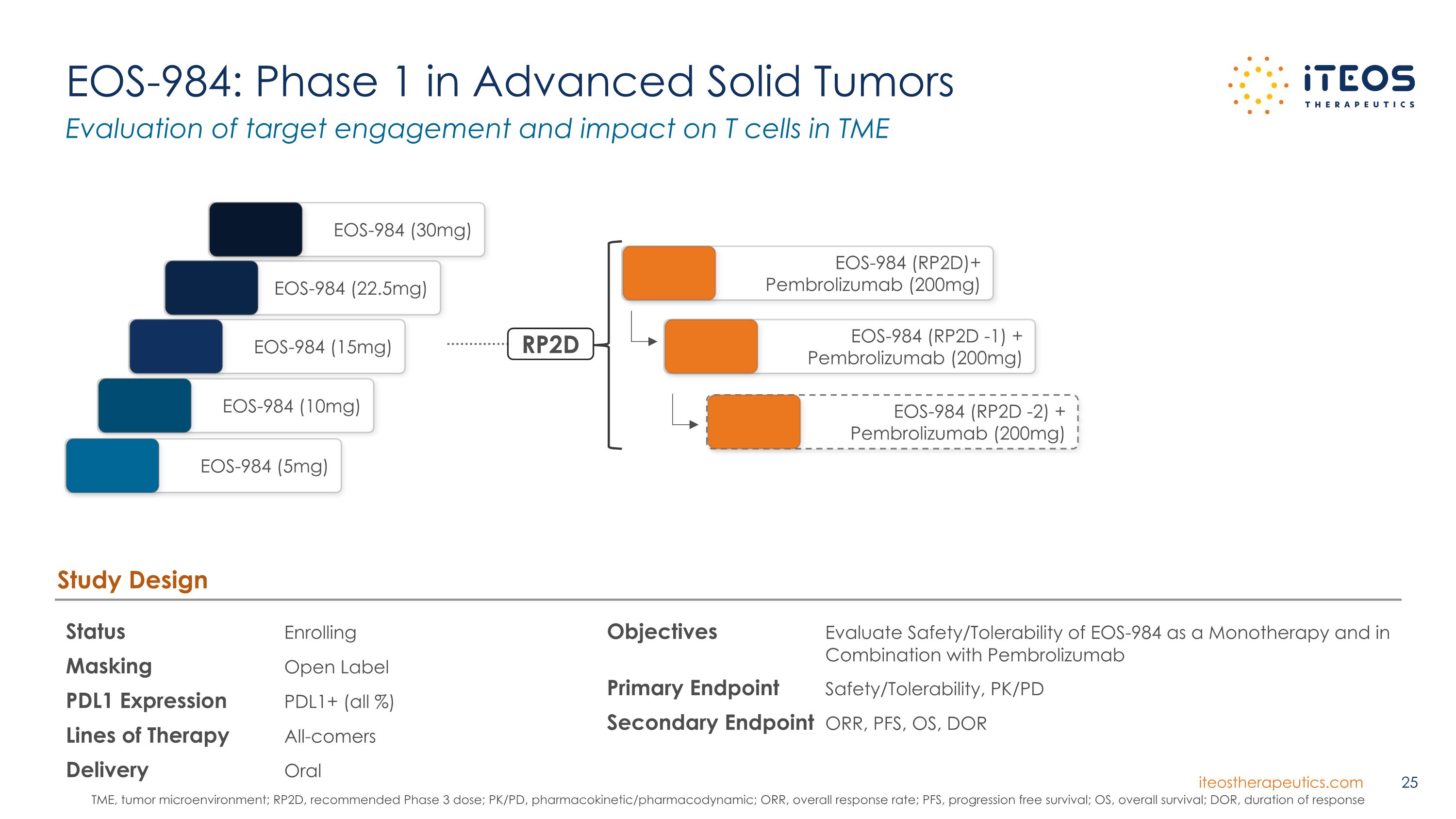
EOS-984:進入晚期實體瘤狀態的第 1 期註冊屏蔽開放標籤 PDL1 表達 PDL1+(所有百分比)治療線所有來者提供口服研究設計目標評估 EOS-984 作為單一療法以及與派姆羅利珠單抗聯合應用的安全性/耐受性、PK/PD 次要終點 ORR、PFS、OS、DOR EOS-984 (15mg) EOS-984 (10mg) EOS-984 (2mg) (2mg) 2.5mg) EOS-984 (RP2D -1) + Pembrolizumab (200 mg) EOS-984 (5mg) EOS-984 (30mg) RP2D EOS-984 (RP2D) + Pembrolizumab (200 mg) EOS-984 (RP2D -2) + Pembrolizumab (200 mg) 評估TME TME、腫瘤微環境中的靶向作用和對T細胞的影響;RP2D,推薦的3期劑量;PK/PD,藥代動力學/藥效學;ORR,總體反應率;PFS,無進展存活率;OS,總存活率;DOR,反應持續時間

2024 年:數據生成的關鍵年份利用深層腫瘤免疫學專業知識的創新投資組合 TIGIT 6.45 億美元截至 2026 年第三季度現金、現金等價物和投資腺苷途徑 1L NSCLC(第 2 期 GALAXIES LUNG-201)1L HNSCC(第 2 期 TIG-006)A2AR-2L NSCLC(第 2 期 A2A-005)ENT1-MOA(臨牀前)ENT1-晚期惡性腫瘤(EOS-984 第一階段)通過重要里程碑資助 NSCLC,非小細胞肺癌;HNSCC,頭頸部鱗狀細胞癌;ENT1,平衡核苷轉運蛋白 1;MoA,機制 EOS-984行動

按設計劃分的癌症免疫療法納斯達克:ITOS 2024 年 1 月