

附錄 99.1 納斯達克:CRGX 工程下一代汽車 T-CELL 療法將提供更多治療方法 2024 年摩根大通醫療保健會議

前瞻性陳述/免責聲明 ⚫ 本演示文稿 包含1995年《私人證券訴訟改革法》所指的前瞻性陳述。這些陳述可能包括 “相信”、“期望”、“預期”、“打算”、 “計劃”、“估計”、“項目”、“將”、“可能”、“目標” 等類似表述,以及除歷史事實陳述以外的陳述,包括但不限於 與公司管理層的業務戰略、計劃、預計里程碑和目標有關的陳述。此類前瞻性陳述反映了公司當前對未來事件的看法,受已知和 未知風險的影響,包括業務、監管、經濟和競爭風險、不確定性、突發事件和對公司的假設,包括但不限於開發 CRG-022 或 CRG-023 所固有的風險、 公司正在進行和計劃中的臨牀試驗的未來結果、公司獲得足夠資金以資助其計劃臨牀試驗的能力以及其他支出趨勢,在行業中,法律以及該行業和未來 支出的監管框架。鑑於這些風險和不確定性,前瞻性陳述中提及的事件或情況可能不會發生。實際結果可能與預期結果有所不同,並且差異可能是重大的。這些 前瞻性陳述不應被視為預測或承諾,也不應被視為暗示任何跡象、保證或保證,表明此類前瞻性陳述所依據的假設是正確的, 詳盡無遺,或者就假設而言,在演示文稿中已充分陳述。提醒您不要過分依賴這些前瞻性陳述,這些陳述僅代表截至本演示文稿發表之日。 在CARGO向美國證券交易委員會(SEC)提交的文件中,包括其於2023年10月10日向美國證券交易委員會提交的S-1表格註冊聲明(以及隨後經過修訂)或CARGO 隨後向美國證券交易委員會提交或提供的其他文件中詳細描述了這些風險和其他風險。CARGO沒有義務或義務因新信息、未來事件或預期變化而更新任何前瞻性陳述。⚫ 本演示文稿中的信息 (包括市場數據和統計信息)來自各種來源(包括第三方來源),公司不保證此類信息的準確性或完整性。所有預測、估值和 統計分析僅供參考。它們可能基於主觀評估和假設,可能使用產生不同結果的眾多替代方法中的一種,如果它們基於 歷史信息,則不應將它們作為對未來表現的準確預測,並提醒您不要過度考慮它們。⚫ 本演示文稿討論了正在臨牀研究的候選產品和尚未獲得美國食品藥品監督管理局批准上市的 。對於這些候選產品的安全性或有效性, 未作任何陳述。⚫ 此處提及的 CRG-022 一期臨牀試驗由斯坦福大學使用其 CRG-022 配方進行。該公司對斯坦福工藝進行了額外的工藝和分析改進,為 CRG-022 創建了 預期的商業製造工藝,以提高製造產量和效率。2

CARGO — 開發具有潛在治療作用的細胞療法 ⚫ 自體 CAR T 收入預計到 2030 年將達到33億美元。變革性且不斷增長的 CAR T 市場 ⚫ 隨着越來越多的治療中心提供 CAR T (1),患者的可及性正在擴大 ⚫ CRG-022 可能會解決大約 60% 的 LBCL 患者使用 CD19 CAR T 細胞療法無法獲得持久反應嚴重未得到滿足的需求 (2) ⚫ 到 2030 年,在 CD19 CAR T 之後,僅在美國/歐盟/英國,就有約 7,600 名患者在 CD19 CAR T 治療後需要治療 ⚫ 1 期陽性結果 CD19 CAR T R/R LBCL — 53% CR具有令人印象深刻的耐久性和安全性 CRG-022:靶向在多項臨牀試驗中給藥的 ⚫ 120 多名患者,CRG-022 的耐受性普遍良好 CD22,有可能 ⚫ 啟動了潛在的關鍵性 2 期臨牀試驗;迄今為止,已成功製造出多名患者,處於關鍵階段,利用我們預期的商業化且易於轉移的製造工藝 ⚫ 斯坦福獲得 FDA 的突破性療法 稱號 ⚫ 利用專有的細胞工程平臺技術開發一系列項目incorplatform technologies 旨在解決 耐藥機制的多種轉基因治療 “貨物” 和三特異性 ⚫ CRG-023(一種靶向 CD19、CD20 和 CD22 的 IND 支持階段的三特異性階段)整合了第一個平臺,該項目集成了新型 CD2 共刺激結構域以對抗 CD58 ⚫ 由全球公認的腫瘤學和細胞療法的先驅和領導者世界級團隊和 ⚫ 經驗豐富的強大領導團隊於 2021 年共同創立擁有深厚的細胞療法和腫瘤學經驗,資本充足 ⚫ 2023 年 11 月首次公開募股 籌集了約3.2億美元的總收益,納斯達克股票代碼:CRGX 來源:Yi-Jiun Su等ASH 2023,2023 年 11 月數據截止 (1) (2) 來源:ZUMA-1 試驗的五年隨訪;2017 年 N Engl J. Med;377:2531-44 DOI:10.1056/nejmoa1707447;Clarivate 2023 年疾病與景觀預測(NHL、CLL);美國/歐盟4/英國和貨運公司分析 3
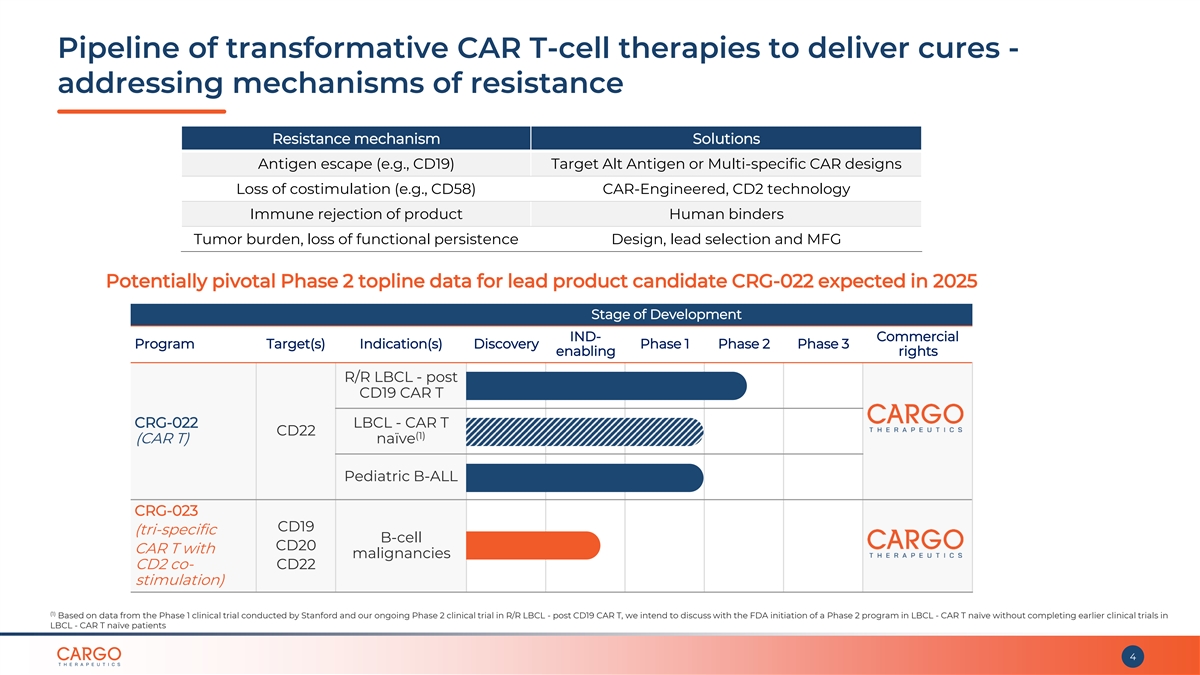
提供治療的變革性 CAR T 細胞療法管道- 解決耐藥機制抗原逃逸(例如 CD19)靶向替代抗原或多特異性 CAR 設計喪失共刺激(例如 CD58)CAR工程的 CD2 技術對產品的免疫排斥人類 粘合劑腫瘤負擔、功能持久性喪失設計、先導選擇和 MFG 預計潛在的關鍵候選產品 CRG-022 的 2 期頂線數據 2025 年發展階段 IND-商業計劃目標指標 Discovery 第 1 階段 2 期 3 期授權權 R/R LBCL-CD19 後 CAR T CRG-022 LBCL-CAR T CD22 (1) (CAR T) 天真兒科 B-ALL CRG-023 CD19(三特異性 B 細胞 CD20 CAR T 伴惡性腫瘤 CD2 共同 CD22 刺激)(1) 基於斯坦福大學進行的 1 期臨牀試驗和我們正在進行的復/R 二期臨牀試驗的數據 LBCL——CD19 CAR T之後,我們打算與美國食品藥品管理局討論在LBCL-CAR T天真患者中啟動2期計劃,但沒有完成先前針對LBCL-CAR T天真患者 的臨牀試驗 4
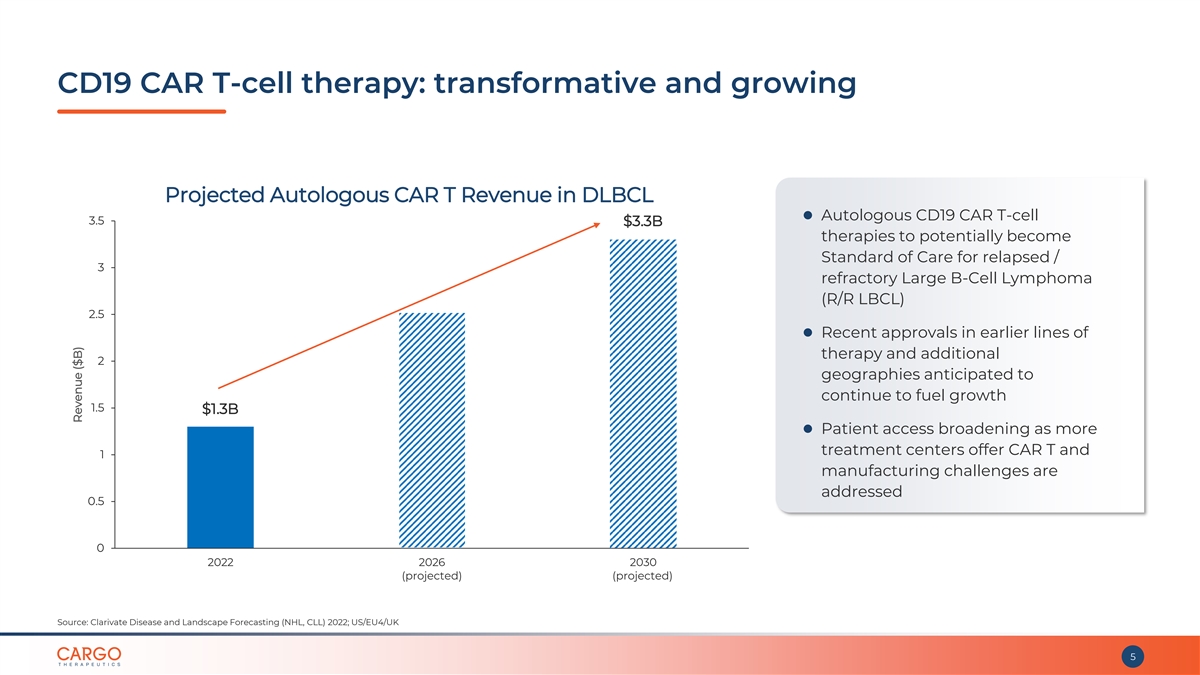
CD19 CAR T 細胞療法:DLBCL ⚫ 自體 CD19 CAR T 細胞療法的預計自體 CAR T 收入將具有變革性且不斷增長的 3.5 美元33億美元,有可能成為復發/3 種難治性大 B 細胞淋巴瘤 (R/R LBCL) 的護理標準 2.5 ⚫ 早期療法和其他 2 地區的批准預計將繼續推動增長 1.5 13億美元 ⚫ 隨着越來越多的治療中心提供 CAR T 和 1 的製造難題得到解決,患者獲得的機會不斷擴大 0.5 0 2022 2026 2030(預計)(預計)來源:Clarivate 疾病和2022年景觀預測(NHL、CLL);美國/歐盟4/英國 5 收入(B 美元)
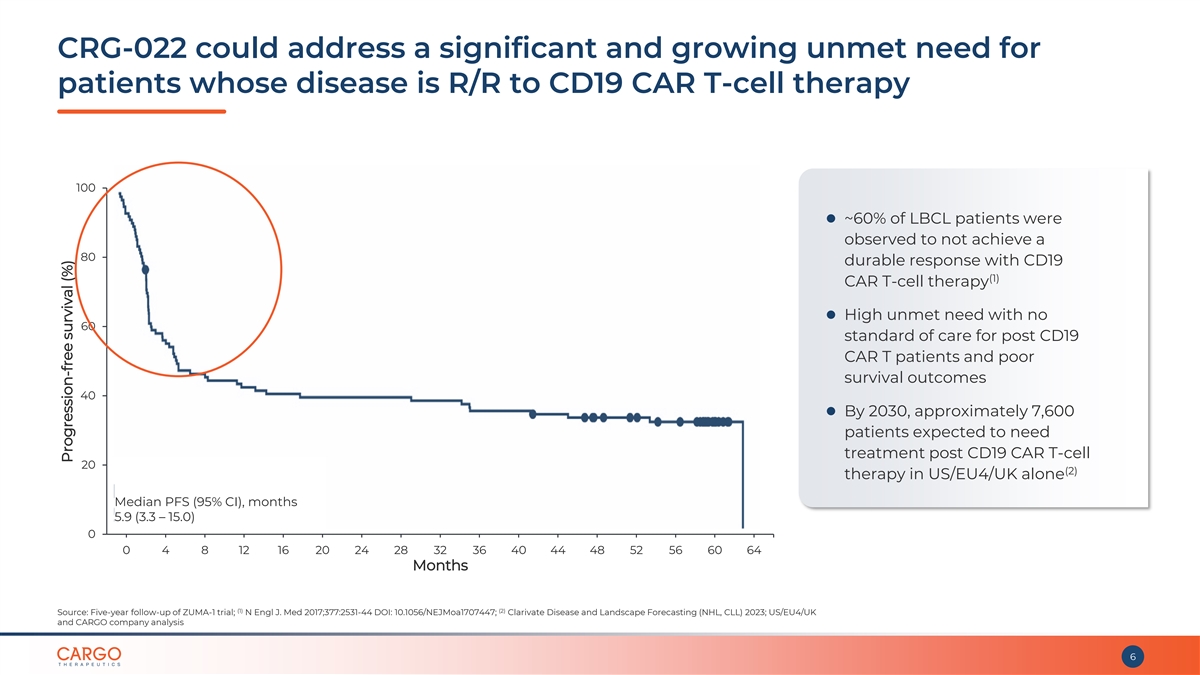
CRG-022 可以解決疾病為 CD19 復發/復發的患者 大量且不斷增長的未得到滿足的需求 CAR T 細胞療法 100 ⚫ ~ 60% 的 LBCL 患者被觀察到 CD19 (1) CAR T 細胞療法無法達到 80% 的持久反應 ⚫ CD19 後 CAR T 患者沒有達到 60 個標準的護理且存活效果不佳 40 ⚫ 到 2030 年,大約 7,600 名 CD患者預計需要接受後治療 19 僅在美國/歐盟4/英國進行的 CAR T 細胞 20 (2) 治療中位數 PFS(95% 置信區間),5.9 個月(3.3 — 15.0)0 4 8 12 16 20 24 28 32 36 40 44 48 52 56 60 64 個月 (1)(2) 來源:ZUMA-1 試驗的五年隨訪;2017 年 N Engl J. Med;377:2531-44 DOI:10.1056/nejmoa1707447;2023 年 Clarivate 疾病與景觀預測(NHL、CLL);美國/歐盟4/英國和 CARGO 公司分析 6 無進展 存活率(%)

CRG-022
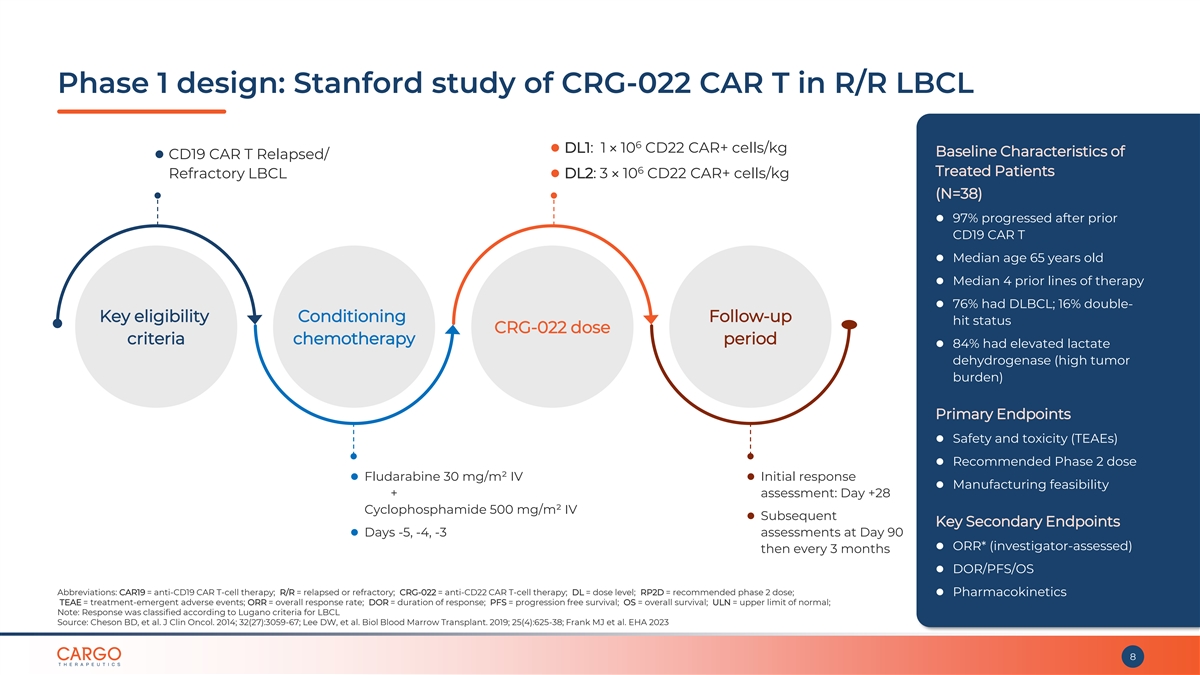
第 1 階段設計:斯坦福對復發/R 中 CRG-022 CAR T 的研究 LBCL 6 ⚫ DL1:1 × 10 個 CD22 CAR+ 細胞/kg ⚫ CD19 CAR T 復發/6 名接受治療的患者的基線特徵難治性 LBCL ⚫ DL2:3 × 10 CD22 CAR+ 細胞/kg (N=38) ⚫ 在先前的 CD19 CAR T ⚫ 年齡 65 歲中位數 ⚫ 之前的係數之後進展了 97% 的療法 ⚫ 76% 有 DLBCL;16% 的雙重關鍵資格條件隨訪命中狀態 CRG-022 劑量標準化療期 ⚫ 84% 的乳酸脱氫酶升高(腫瘤負擔過高) 主要終點 ⚫ 安全性和毒性 (TEAE) ⚫ 推薦第 2 階段劑量 ⚫ 氟達拉濱 30 mg/m² IV ⚫ 初步反應 ⚫ 製造可行性 + 評估:第 +28 天環磷酰胺 500 mg/m² IV ⚫ 後續的關鍵次要終點 ⚫ 第 90 天 -5、-4、3 天 ⚫ ORR*(研究者評估)然後每 3 個月進行一次 ⚫ DOR/PFS/OS 縮寫:CAR19 = 抗 CD19 CAR T 細胞療法;R/R = 復發或難治性;CRG-022 = 抗 CD22 CAR T 細胞療法;DL = 劑量水平;RP2D = 推薦的 2 期劑量;⚫ 藥代動力學 TEAE = 治療緊急不良事件;ORR = 總體緩解率;DOR = 持續時間反應;PFS = 無進展存活率;OS = 總存活率 ;ULN = 正常值上限;注意:反應根據盧加諾的 LBCL 標準進行分類來源:Cheson BD 等人J Clin Oncol. 2014;32 (27): 3059-67;Lee DW 等人Biol 血髓移植。2019;25 (4): 625-38;Frank MJ 等人 EHA 2023 8

第 1 階段結果:對於疾病為復發至 CD19 的 LBCL 患者,CRG-022 有可能成為有效的 療法 CAR T 細胞療法無進展存活率 (PFS) 總體存活率 (OS) 關鍵要點 • CR 率:53% • ORR 率:68% • CR 通常持久,獲得 CR 的 20 個受試者中只有 4 個復發 LBCL DL1 (n=29) DL2 (n=9) 總計 (n=38) • 製造成功率:95% • 劑量等級 1 中位隨訪時間,月 [範圍] 27.3 [12.0 – 48.9] 39.8 [35.1 – 43.9] 28.9 [12.0 – 48.9]• 100 萬 CAR+ 細胞/kg 總體反應率 (ORR) *,n (%) 19 (66%) 7 (78%) 26 (68%) • 劑量 2 級 CR 率 15 (52%) 5 (56%) 20 (53%) • 300 萬 CAR+ 細胞/kg 1 12 個月 CR 11/15 (73%) 4/5 (80%) 15/20 (75%) 操作系統中位數,月 [95% 置信區]NR (8.4 — NR) 14.1 (1.2 — NR) 14.1 (8.4 — NR) 來源:斯坦福大學在 ASH 研究者會議上發佈的第 1 階段數據;蘇怡軍等ASH 2023;2023 年 11 月數據截止五名死於非復發原因的患者在死亡時 處於 CR;5 名患者中有 2 名處於劑量級別 1,5 名患者中有 3 名處於劑量級別 2。1) 2 名患者復發。3 名患者死亡(1 名相關,2 名無關);NR:未達到 9
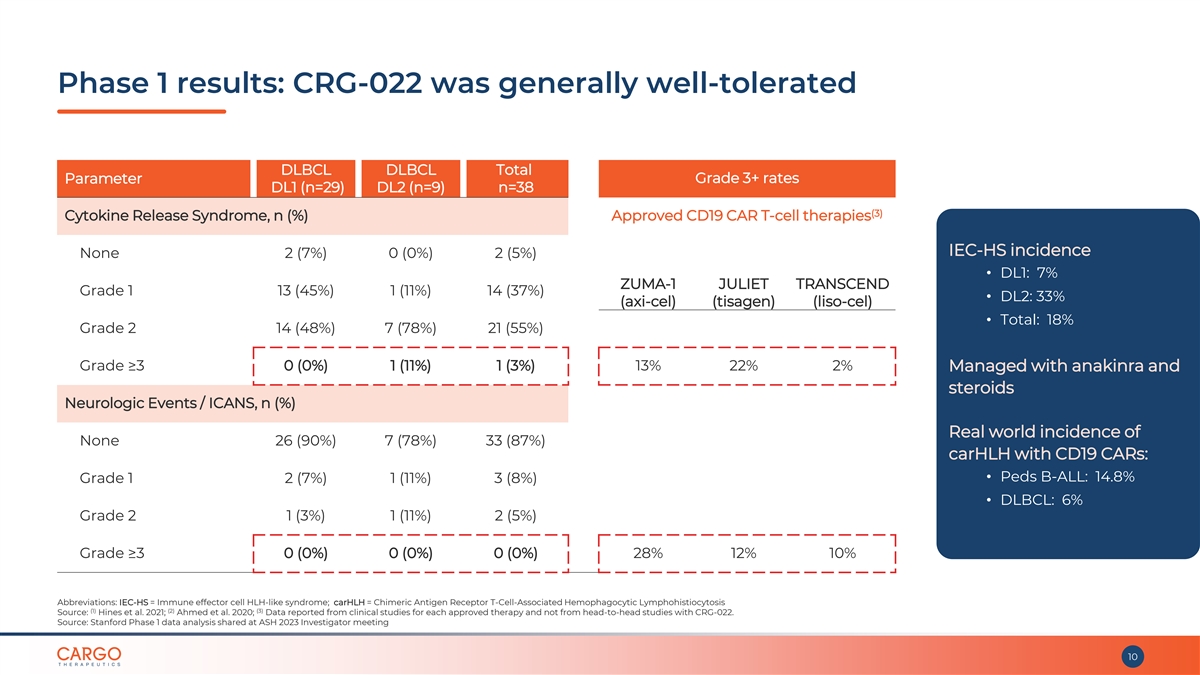
第 1 階段結果:CRG-022 總體耐受性良好 DLBCL DLBCL 總計 參數等級 3+ 率 DL1 (n=29) DL2 (n=9) n=38 (3) 細胞因子釋放綜合症,n (%) 批准的 CD19 CAR T 細胞療法 IEC-HS 發病率無 2 (7%) 0 (0%) 2 (5%) • DL1:7% ZUMA-1 JULIET TRANSCEND 1 級 13 (45%)) 1 (11%) 14 (37%) • DL2:33% (axi-cel) (tisagen) (liso-cel) • 總計:18% 2 級 14 (48%) 7 (78%) 21 (55%) 等級 ≥3 0 (0%) 1 (11%) 1 (3%) 13% 22% 使用阿那金拉和類固醇治療神經系統事件/ICANS,n (%) 現實世界中無 26 (90%) 7 (78%) 33 (87%)carHLH 搭配 CD19 CAR:• Peds B-ALL:14.8% 1 級 2 (7%) 1 (11%) 3 (8%) • DLBCL:6% 2 級 1 (3%) 1 (11%) 2 (5%) ≥3 0 (0%) 0 (0%) 28% 12% 10% 縮寫:IEC-HS = 免疫效應細胞 HLH 樣 綜合徵;carHLH = 嵌合抗原受體 T 細胞相關噬血細胞淋巴組織細胞增多症 (1) (2) (3) 來源:Hines 等人,2021 年;Ahmed 等人,2020 年;數據來自每種批准療法的臨牀研究,而不是來自 CRG-022 的正面交鋒 研究。來源:斯坦福大學在 ASH 2023 研究者第 10 次會議上分享的第 1 階段數據分析
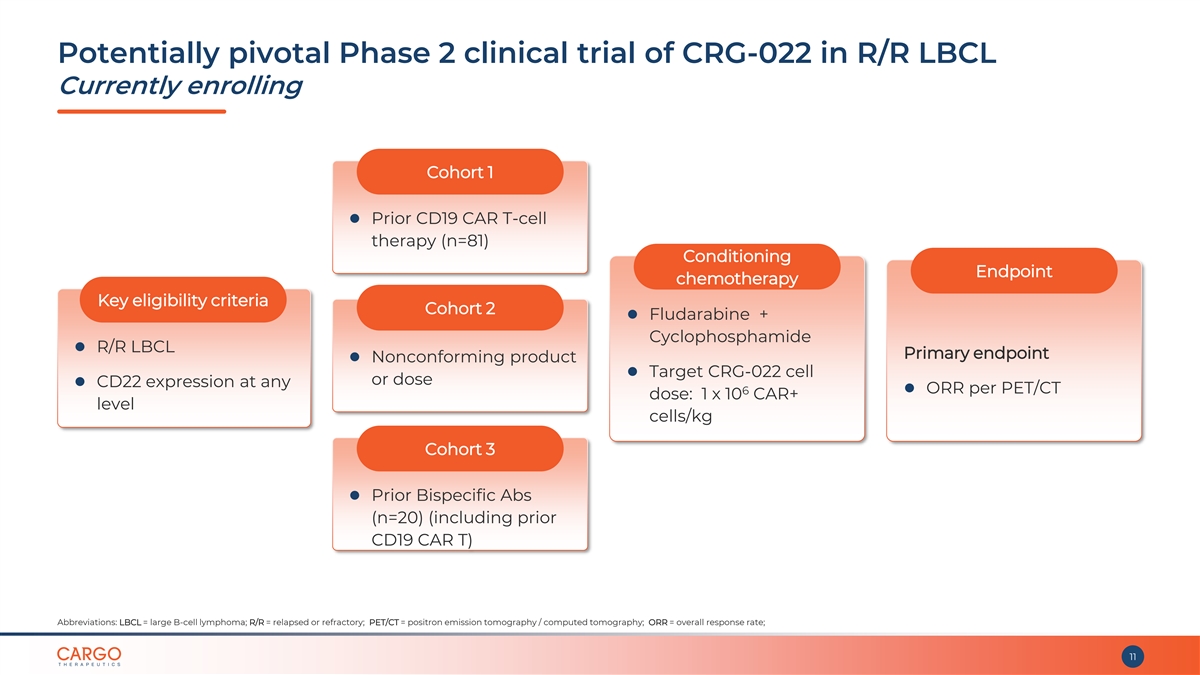
CRG-022 在 R/R 中的潛在關鍵性 2 期臨牀試驗 LBCL 目前正在註冊隊列 1 ⚫ 之前的 CD19 CAR T 細胞療法(n=81)調節終點化療關鍵資格標準隊列 2 ⚫ 氟達拉濱 + 環磷酰胺 ⚫ R/R LBCL 主要終點 ⚫ 不合格產品 靶向 CRG-022 細胞或劑量 ⚫ CD22 表達 ⚫ ORR 每 PET/CT 6 劑量:1 x 10 個 CAR+ 水平細胞/kg 隊列 3 ⚫ 先前的雙特異性 Abs (n=20)(包括之前的 CD19 CAR T)縮寫:LBCL = 大 B 細胞淋巴瘤;R/R = 復發或難治性;PET/CT = 正電子 ⚫發射斷層掃描/計算機斷層掃描;ORR = 總響應率;11
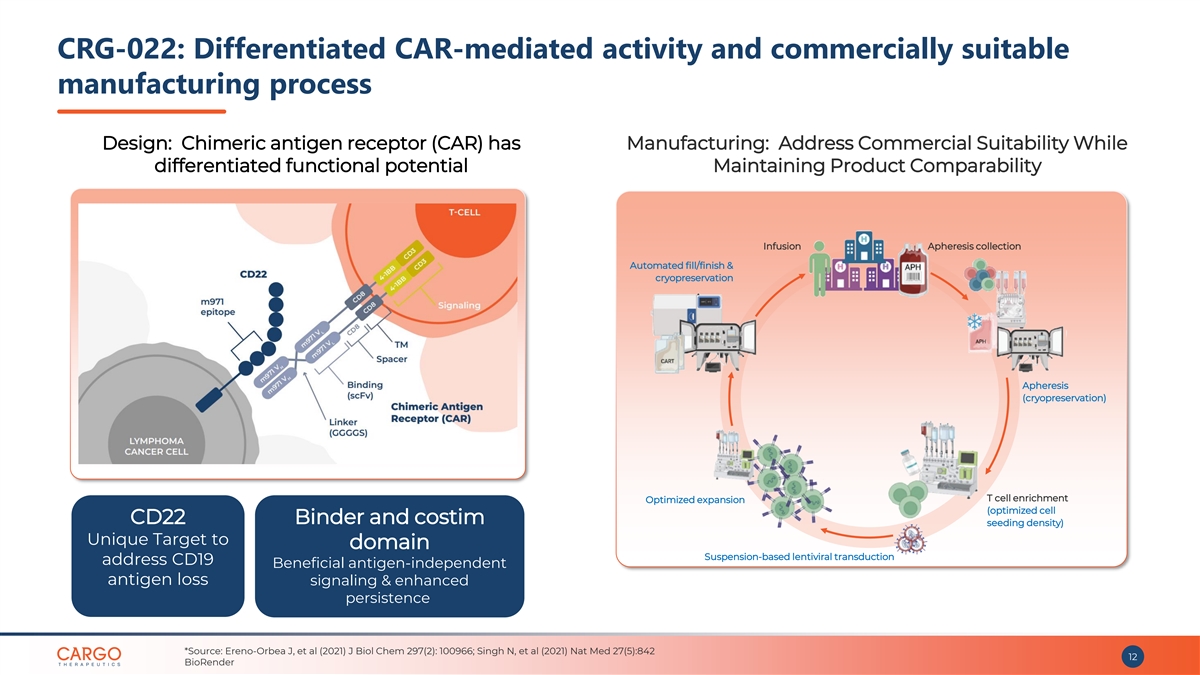
CRG-022:差異化CAR介導活性和商業上合適的 製造工藝設計:嵌合抗原受體(CAR)具有製造能力:解決商業適用性同時實現差異化功能潛力保持產品可比性輸液分離收集自動填充/完成和 冷凍保存血液分離術(冷凍保存)T 細胞富集優化擴展(優化細胞 CD22 粘合劑和 costim 播種密度)基於懸浮液的獨特靶向結構的慢病毒轉導地址 CD19 有益抗原無關 抗原丟失信號傳導和持久性增強 *來源:Ereno-Orbea J 等人(2021)J Biol Chem 297(2):100966;Singh N 等人(2021)Nat Med 27 (5): 842 12 BioRender

管道和平臺概述
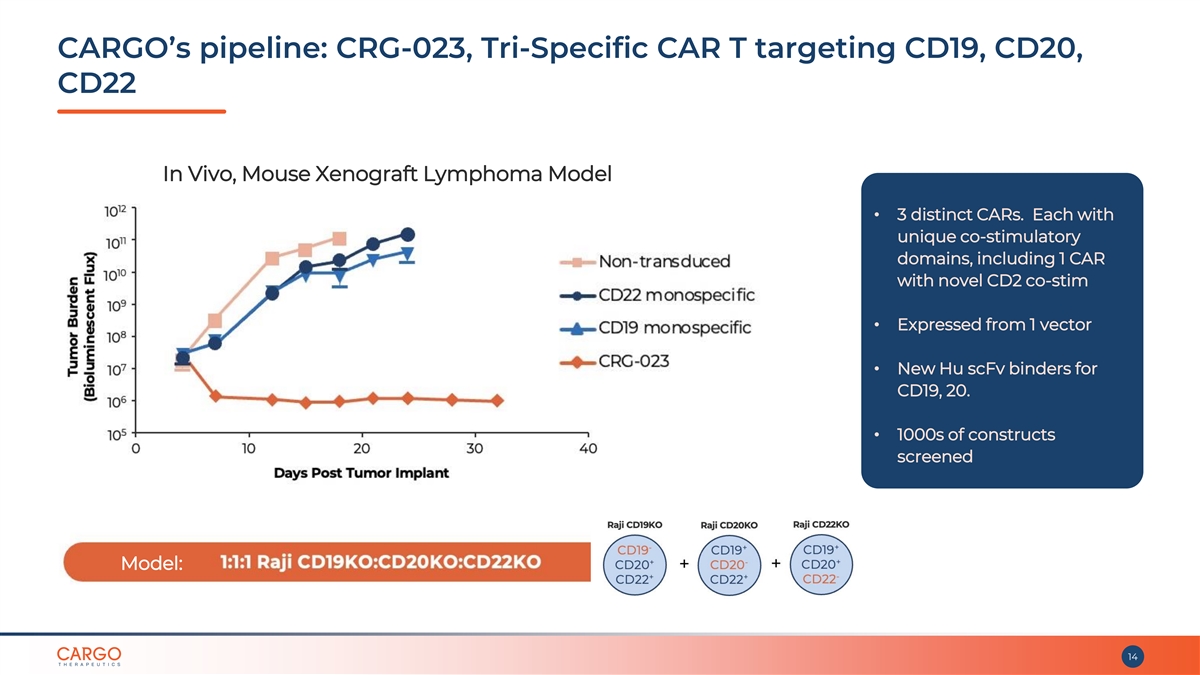
CARGO 的產品線:CRG-023、靶向 CD19 的三特異性 CAR T、 CD20、CD22 體內、小鼠異種移植淋巴瘤模型 • 3 種不同的 CAR。每種都有獨特的共刺激域,包括 1 個帶有新型 CD2 共刺激結構的 CAR • 由 1 個載體表達 • 用於 CD19 的新 Hu scfV 粘合劑,20。• 篩選了 1000 個 種結構模型:14

經驗豐富的領導團隊擁有豐富的腫瘤學和細胞療法 經驗 Gina Chapman Anup Radhakrishnan Ginna Laport,醫學博士總裁兼首席執行官首席財務官兼首席醫學官首席技術官邁克爾·波特斯博士 Kari Leetch Halley Gilbert,JD Bethany Rogers首席科學官首席人事官首席法務官產品戰略與商業化高級副總裁 15

CARGO — 專注於開發和提供具有潛在療效的 細胞療法強勁的財務狀況和可觀的價值關鍵收穫轉折點 ⚫ 2023 年 11 月籌集了 3.2 億美元的總收益 ⚫ 首次公開募股後,CD19 CAR T R/R P LBCL 的 CRG-022 第 1 階段業績令人印象深刻 ⚫ 2023 年 8 月啟動 CRG-022 的第二階段 ⚫ 目前正在註冊潛在的關鍵性 2 期臨牀試驗,P 的頂線數據預計將於 2025 年在 LBCL R/R CD19 ⚫ 2025年第二階段中期業績(預期)⚫ 開發了 強勁的商業化且易於轉讓LBCL R/R CD19 中所有臨牀試驗 CRG-022 的製造流程 ⚫ 利用專有的細胞工程平臺技術開發一系列項目 ⚫ 經驗豐富、強大的 領導團隊 ⚫ 手頭現金總額(截至 2023 年 12 月 31 日):4.06 億美元 *包括 A 輪第 3 批註:截至 2023 年 5 月 3 日數據截止日期 16

謝謝