
1 月 2 日 0 2 4 公司概述 Onvansertib 機遇


首創 PLK1 抑制劑 • Onvansertib • FDA • FDA 2L Kras-Mut mCRC 的可靠臨牀數據 • 73% ~ 25% • 15 個月約 8 個月輝瑞 • 輝瑞 • 輝瑞我們預計 2024 年中期 Ras-Mut mCRC 一線試驗的臨牀數據將延續至 2025 年

小鼠體內生長的人轉移性結直腸癌 (mCRC) 腫瘤 (KRAS G12V) • • onvansertib 和 bevacizumab 的組合顯示腫瘤大小和血管形成顯著減小

具有致癌基因改變的靶點* ROS1估計符合條件的患者出現在Turning Point Therapeutics2022年5月的公司報告幻燈片6中(美國14萬非小細胞肺癌的發病率,其中 2% 的患者患有ROS1易位)。RET估計了Loxo Oncology在8-K表格(2018年1月8日)上披露的2018年1月公司簡報中列出的符合條件的患者。KRAS G12C估計的合格患者包括來自SEER網站的患者人數和米拉蒂公司報告中的G12C百分比。BMS 宣佈打算於 2023 年 8 月 10 日以 48 億美元的股權價值收購 MRTX。mCRC 的估計人羣包括一線癌症、KRAS 和 NRAS 突變癌症。53 50 48 年度符合資格的美國患者('000 人)* 29 宣佈被 BMS 5 以 48 億美元的價格收購
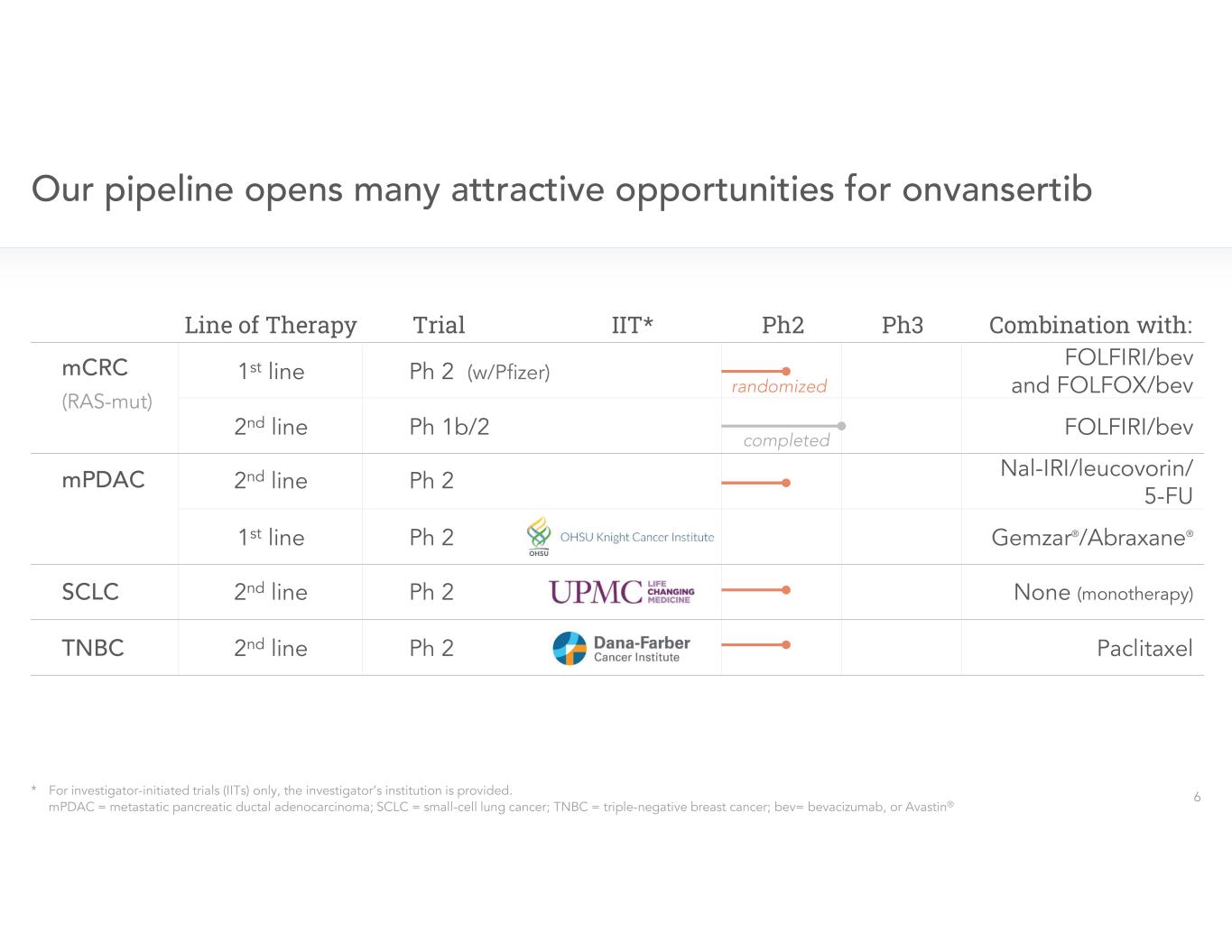
治療系列 Ph2 Ph3 與:Trial IIT* 組合療法

通過 PLK1 抑制對抗 mCRC 領先的 mCRC 項目中的可靠數據:加快批准的路徑

onvansertib 特異性屬性 • • •
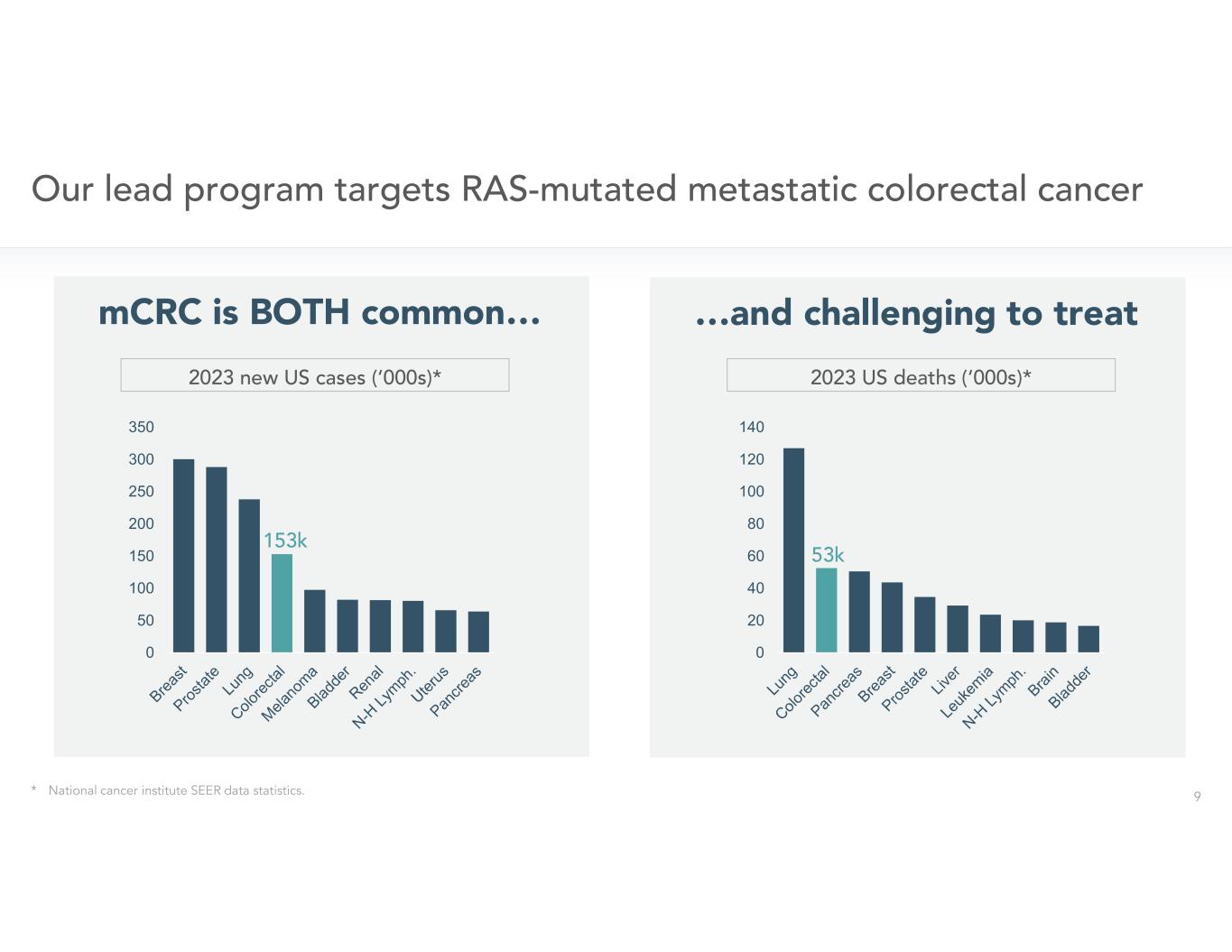
0 50 100 150 200 250 300 350 0 20 40 60 80 100 120 140

護理標準
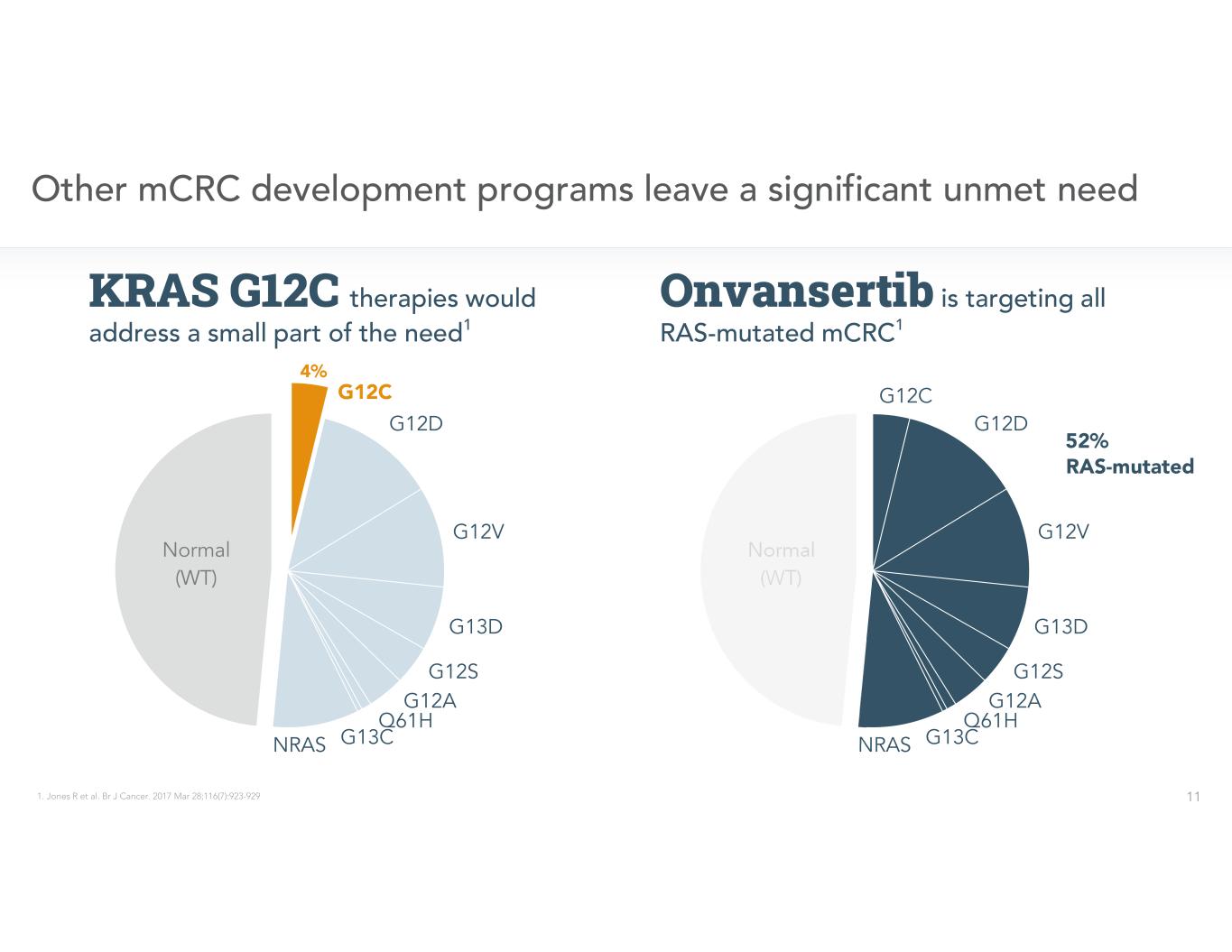
KRAS G12C Onvansertib
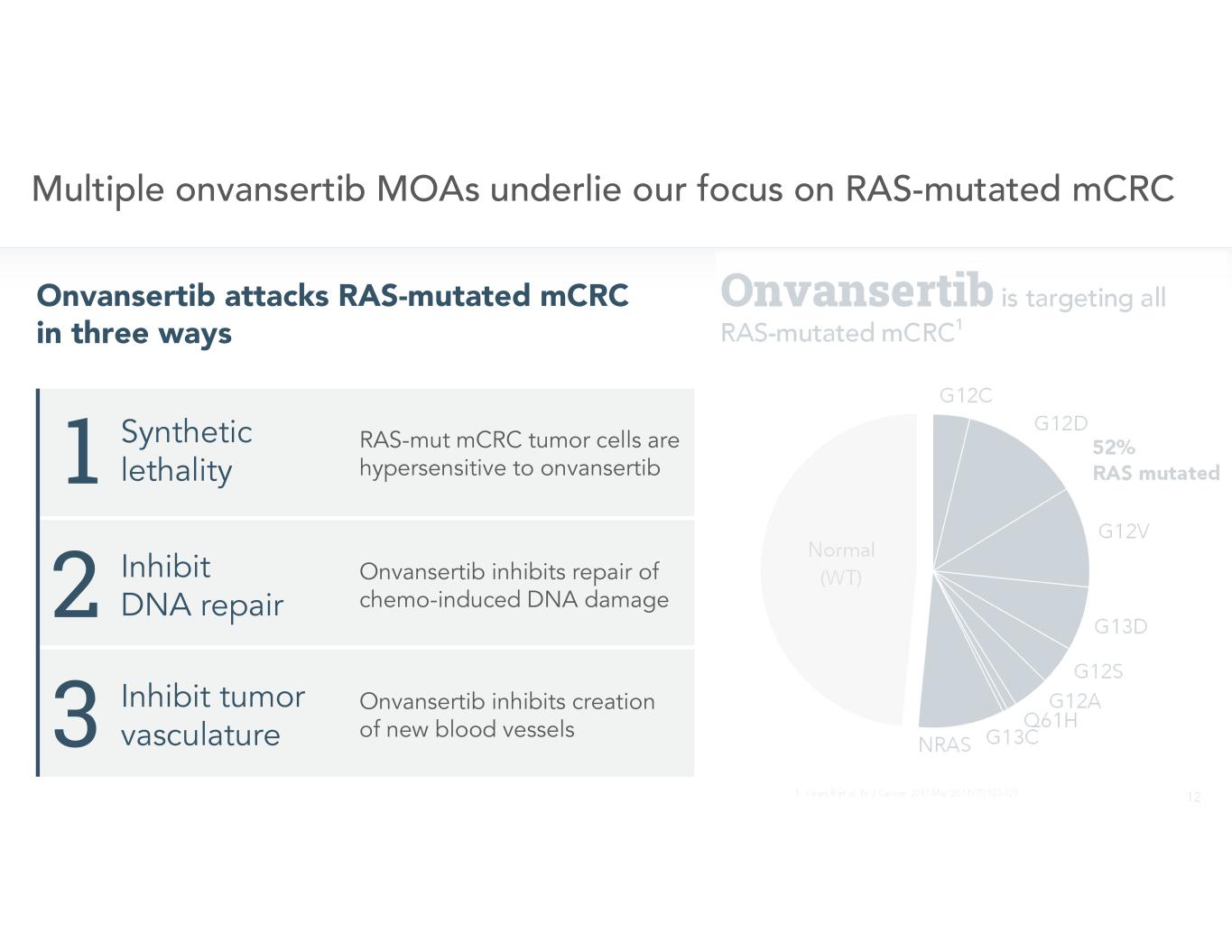
Onvansertib 2 1 3

具有致癌基因改變的靶點* ROS1估計符合條件的患者出現在Turning Point Therapeutics2022年5月的公司報告幻燈片6中(美國14萬非小細胞肺癌的發病率,其中 2% 的患者患有ROS1易位)。RET估計的符合條件的患者在Loxo Oncology的2018年1月公司報告中,在表格8-K中披露(2018年1月8日)。mCRC的估計人羣包括一線、KRAS和NRAS突變的癌症。mpDAC的估計人羣包括一線PDAC患者。SCLC 估計的人羣中包括 SCLC 救助患者。TNBC 的估計人羣包括侵入性二線 TNBC 患者。53 15 12 5050 48 年度符合條件的美國患者('000 人)*

通過 PLK1 抑制對抗 mCRC 領先的 mCRC 項目中的可靠數據:加快批准的路徑

第一行第二行正常 RAS 突變
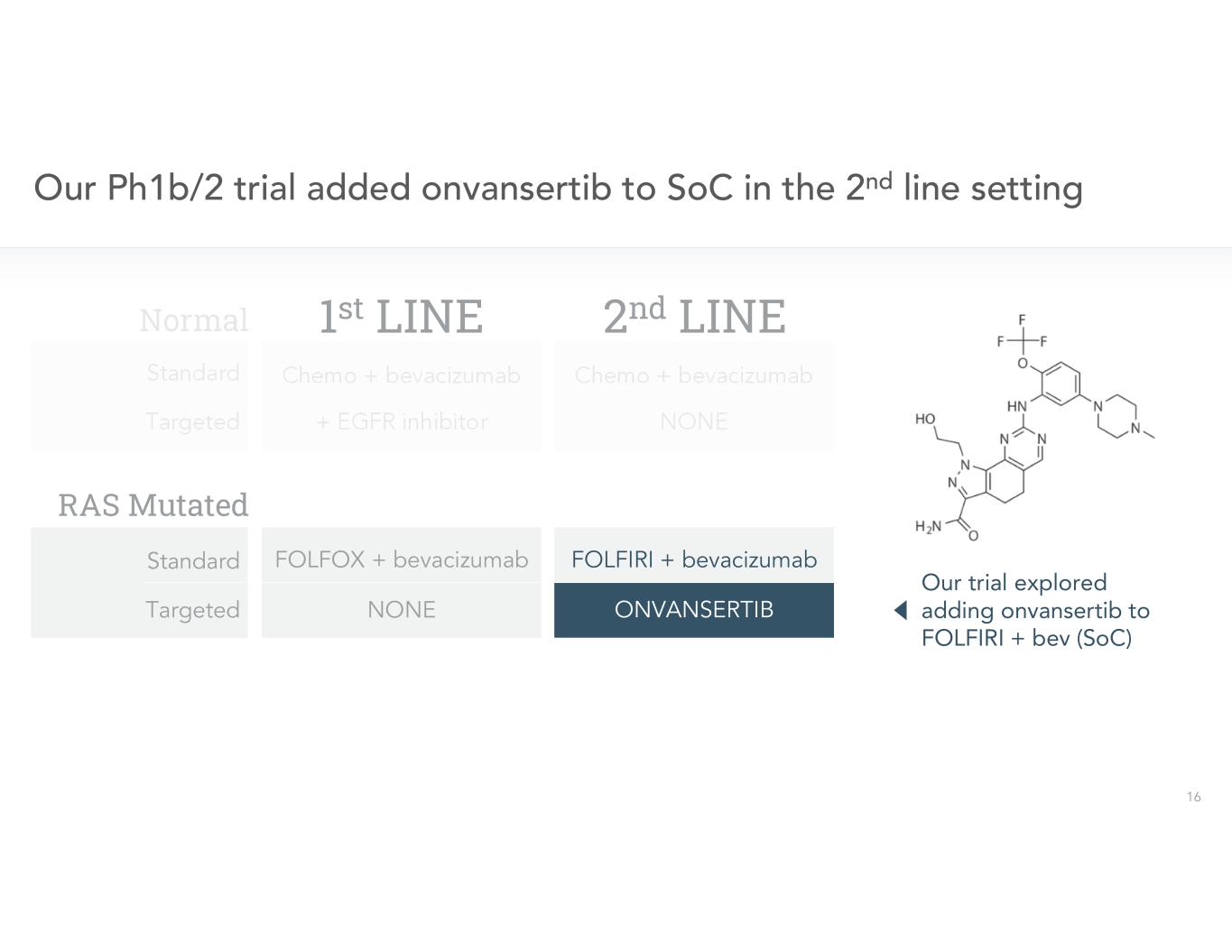
第 2 行第 1 行正常 RAS 突變

28 天週期註冊標準療效終點 1 2 3

第一行第二行 lineBev 暴露於 bev 天真的患者
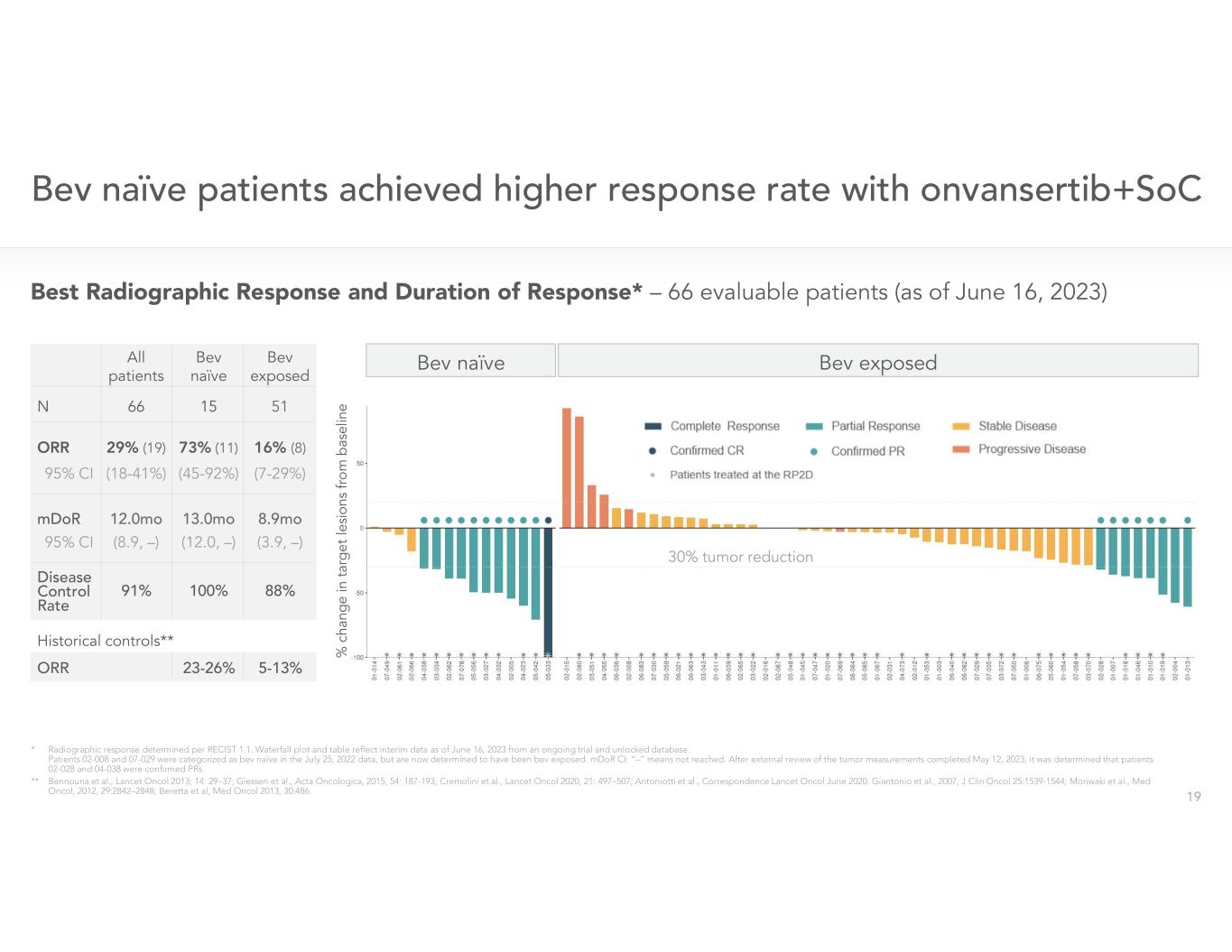
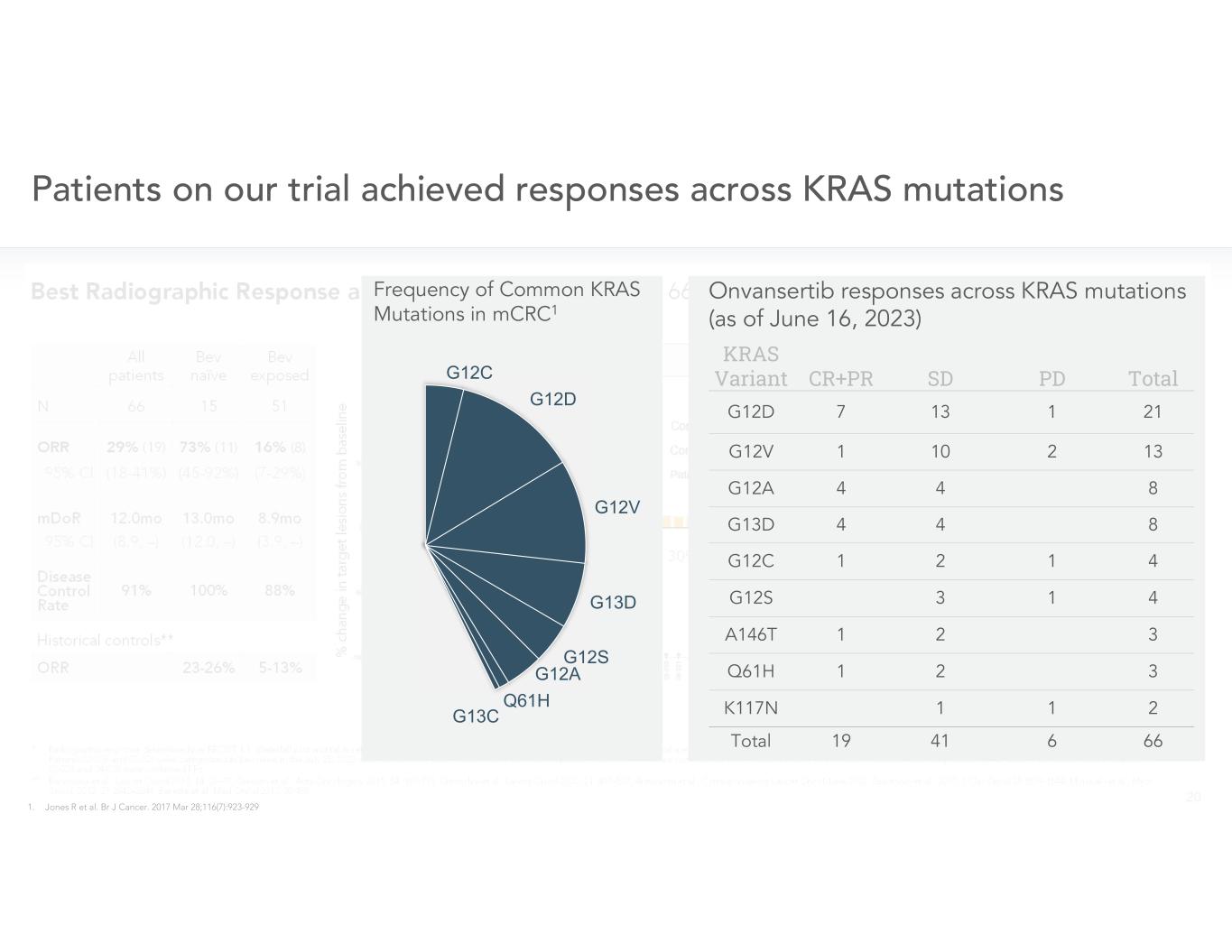
TotalPDSDCR+PR KRAS VariantG12C G12D G12V G13D G12S G12S G12A Q61H G13C


臨牀發現的科學依據

T um 或 v ol um e (m m 3) 0 10 20 30 0 500 1000 1500 2000 2500 SW620 (KRAS G12V) 與單一藥物相比,該組合具有顯著優異的抗腫瘤活性
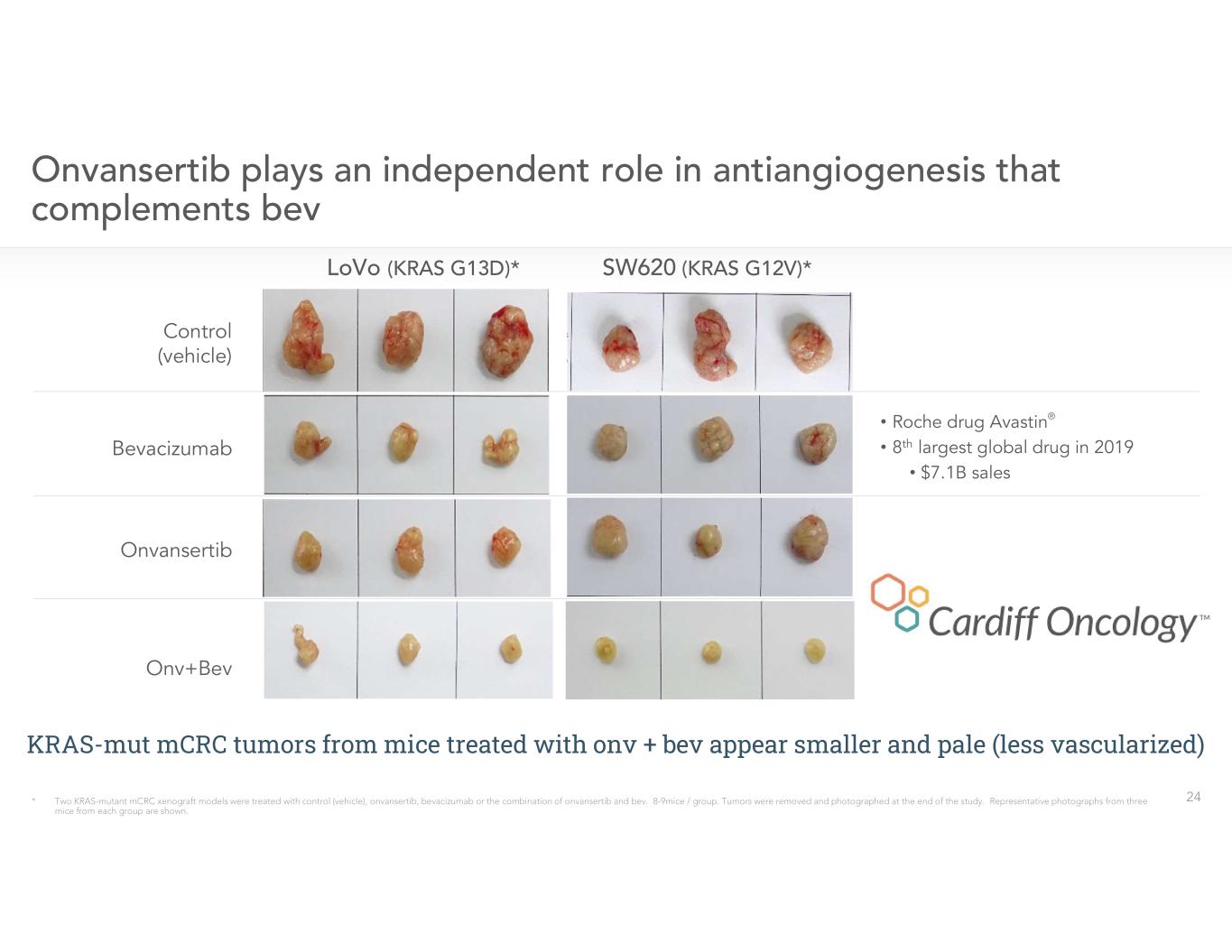
使用 onv + bev 治療的小鼠身上的 Kras-Mut mCRC 腫瘤顯得更小更蒼白(血管化程度較低)• •
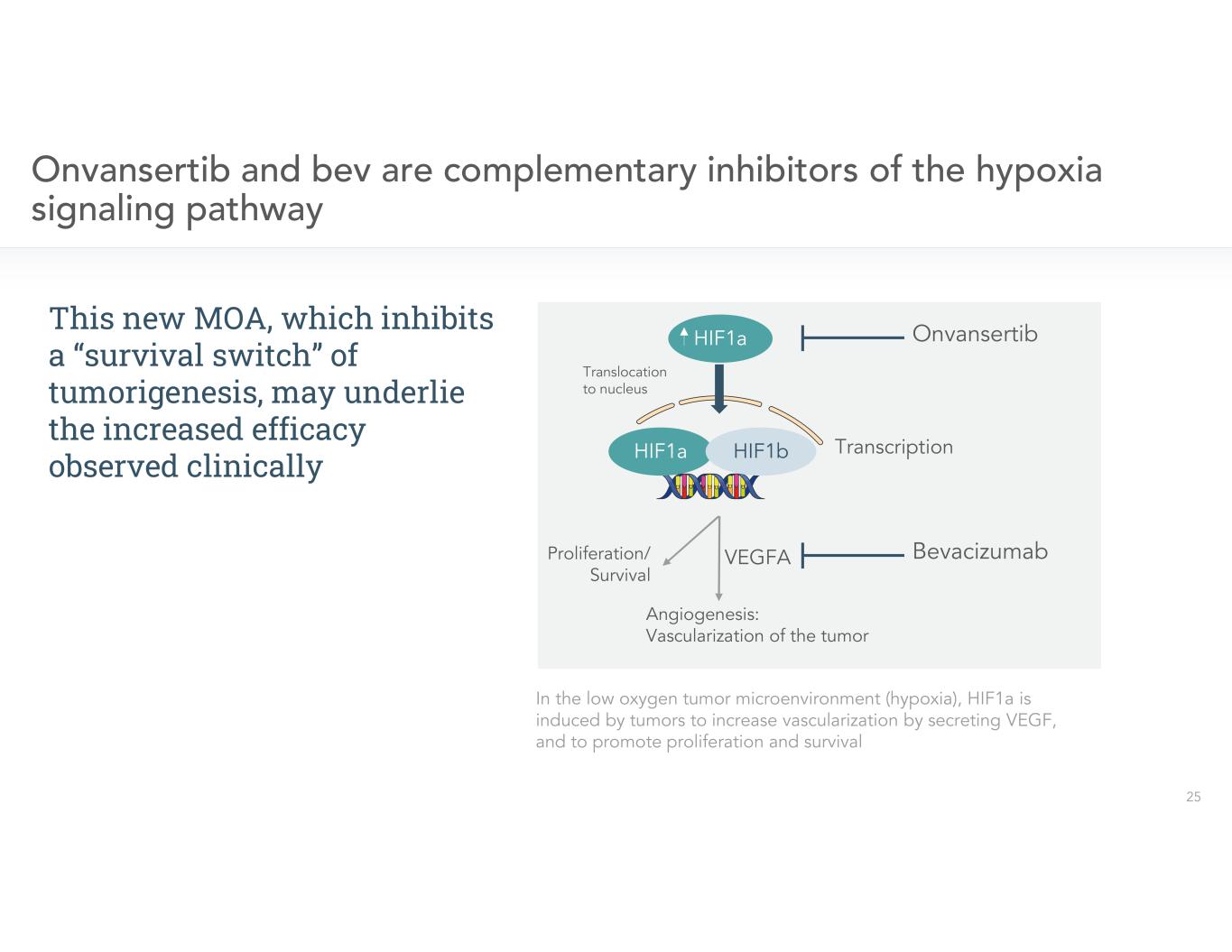
這種新的MOA抑制了腫瘤發生的 “生存轉換”,可能為臨牀觀察到的療效提高奠定了基礎

通過 PLK1 抑制對抗 mCRC 領先的 mCRC 項目中的可靠數據:加快批准的路徑

mCRC 臨牀開發計劃在 2023 年 6 月 C 型會議上與 FDA 達成協議 • • • • • •

入學標準終點小學中學成功基準 PFIZER IGNITE
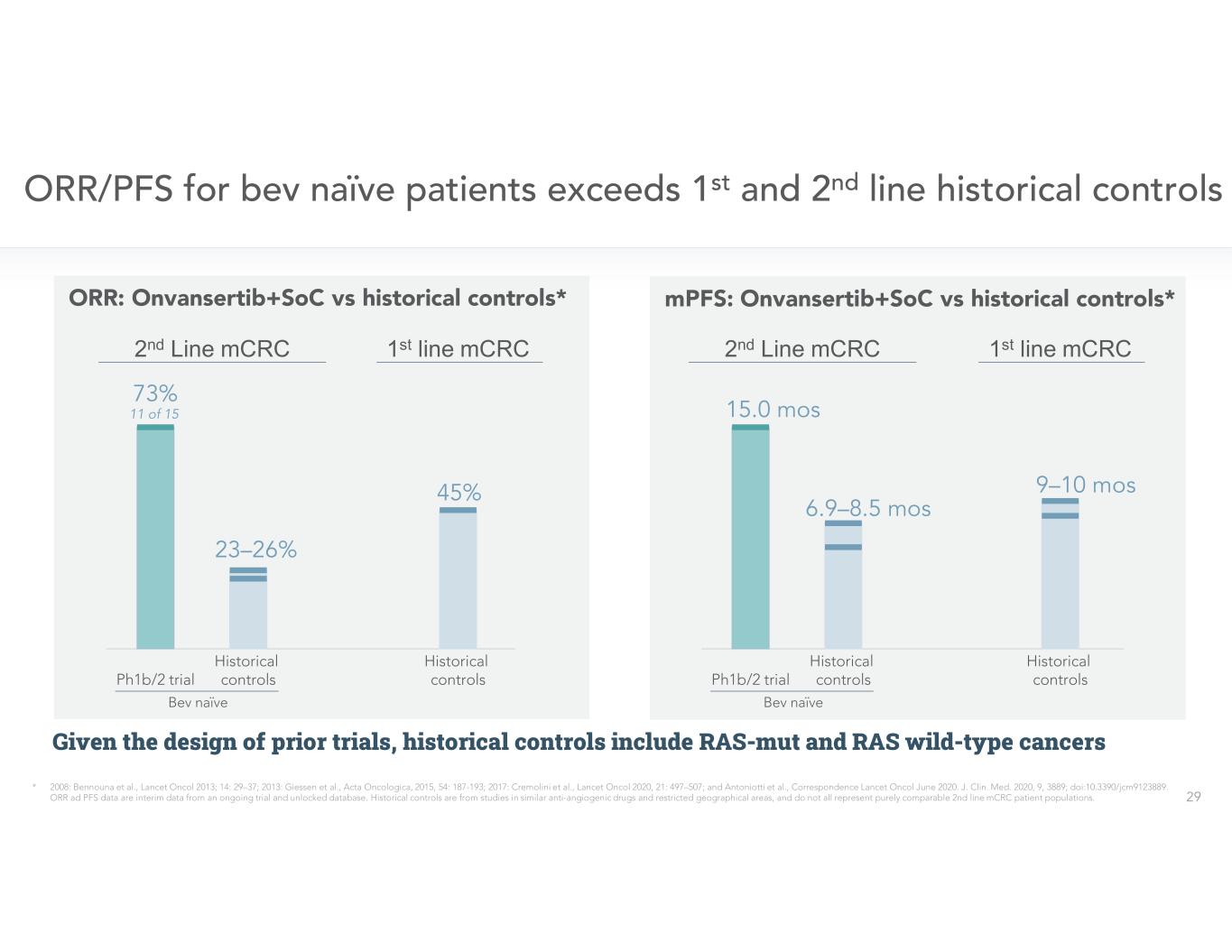
二線 mCRC 一線 mCRC 二線 mCRC 一線 mCRC 第一線 mCRC 鑑於先前試驗的設計,歷史對照包括 ras-Mut 和 RAS 野生型癌症

突破性增長計劃 • • • 輝瑞輝瑞點火 • •

同類首創 PLK1 抑制劑 • Onvansertib • FDA • FDA 2L Kras-Mut mCRC 的可靠臨牀數據 • 73% ~ 25% • 15 個月~8 個月輝瑞 • 輝瑞 • 輝瑞我們預計我們的一線 ras-mut mCRC 試驗的臨牀數據將在 2024 年中期

附錄其他 mCRC 數據
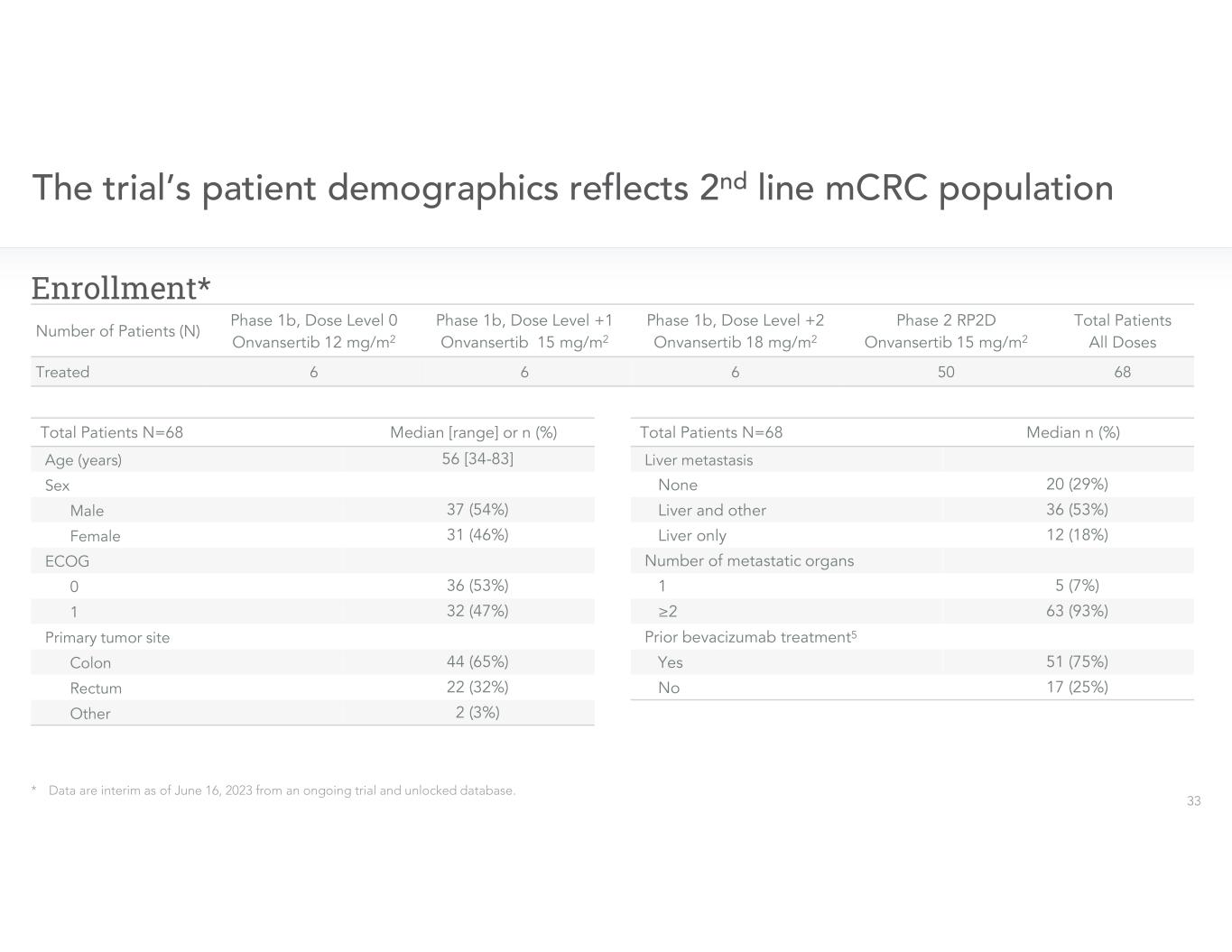
註冊*
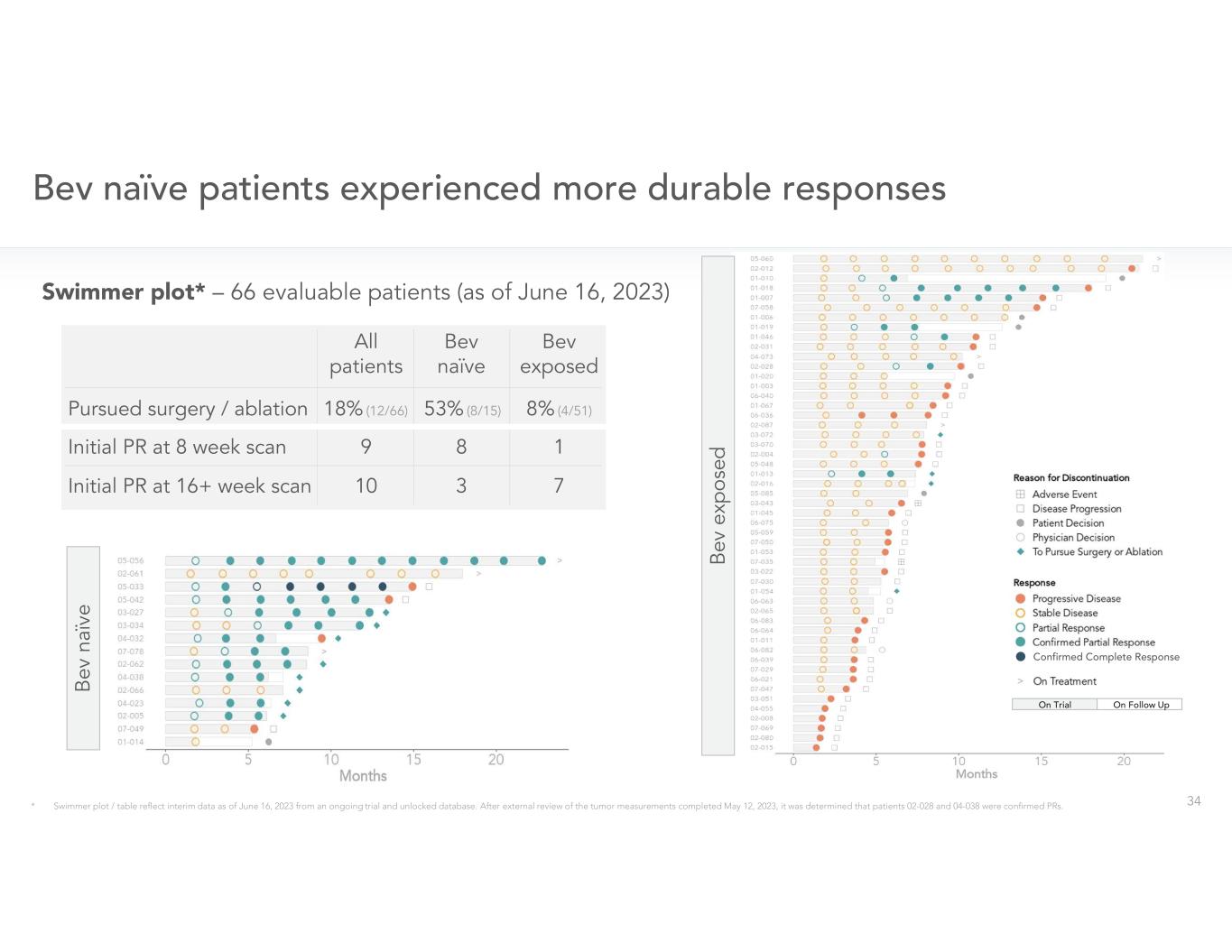

沒有任何單一患者特徵可以解釋先前 bev 狀態下反應率的差異

TOTALGR4GR3GR2GR1TEAETOTALGR4GR3GR2GR1TEAE 11 16% 00011Cough53 78% 072224疲勞 10 15% 0118Pyrexia49 72% 723181中性粒細胞減少 10 15% 0037Dyspnea46 68% 041329噁心 10 15% 0127AST 增加38 56% 041321腹瀉 9 13% 0072淋巴細胞減少29 43% 15149白細胞減少症 9 13% 0009Dyspepsia29 43% 02522貧血 9 13% 0108ALT 增加25 37% 00520脱髮 9 13% 0009低鈣血癥25 37% 03814腹痛 9 13% 0009Insomnia24 35% 03615口炎 8 12% 0251脱水 23 34% 09104 高血壓 8 12% 0026低鉀血癥23 34% 01517血小板減少症 8 12% 0026Arthralgia20 29% 01217便祕 7 10% 0025手部/足Syndrome20 29% 03611嘔吐 7 10% 0025痔瘡15 22% 00015Epistaxis 7 10% 0016非心臟性胸痛13 19% 00013頭痛 7 10% 0115ALP 增加12 18% 0264食慾下降 12 18% 00210背痛 • • • •

• • • • • •

使用 siRNA 對 PLK1 (SIPLK1) 2 進行抑制 α PLK1 抑制可防止缺氧誘導的 HIF1α 表達 α αα 在 4 個 RAS 突變 CRC 細胞系中 1,onvansertib 抑制了缺氧誘導的 HIF1α 表達 β α
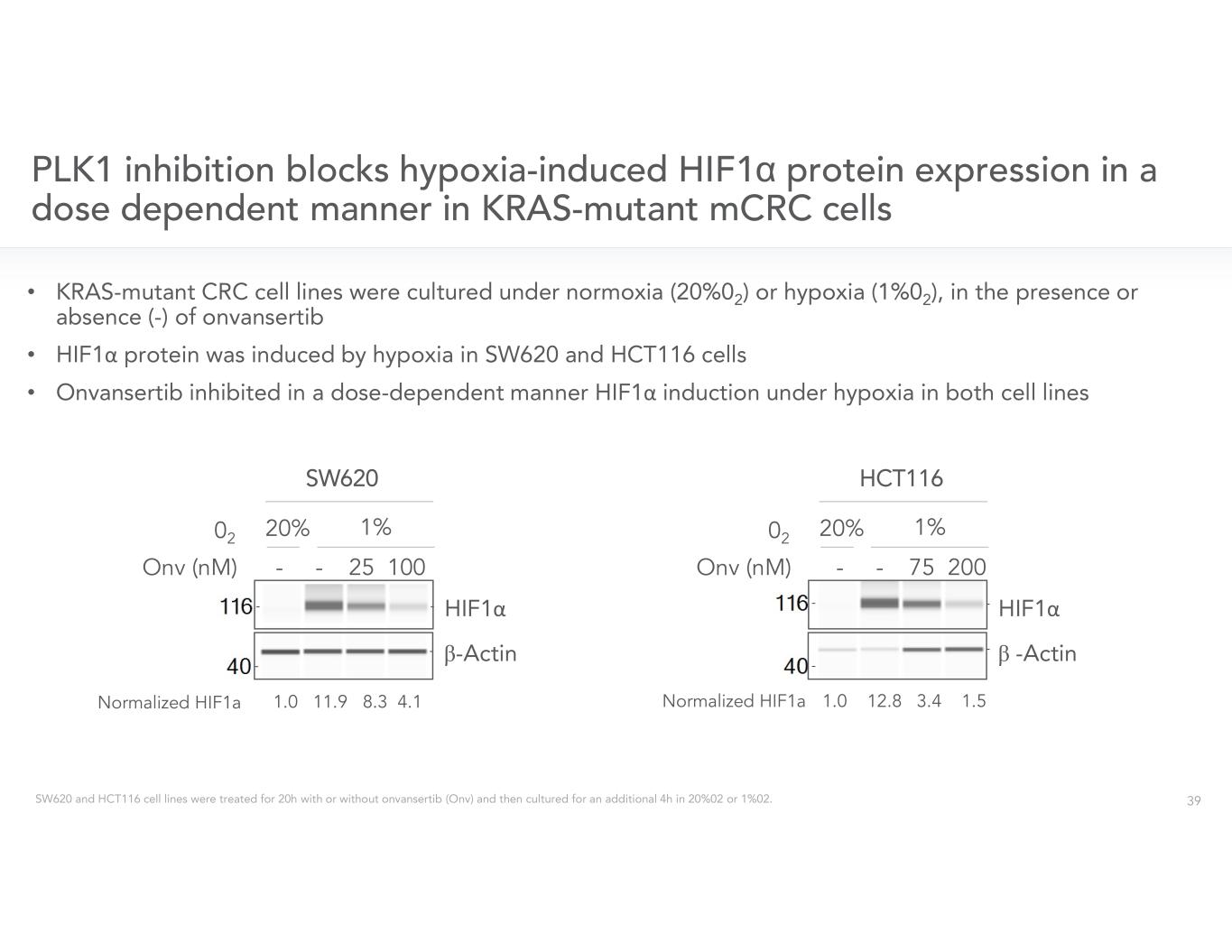
α • • α • α α β α β
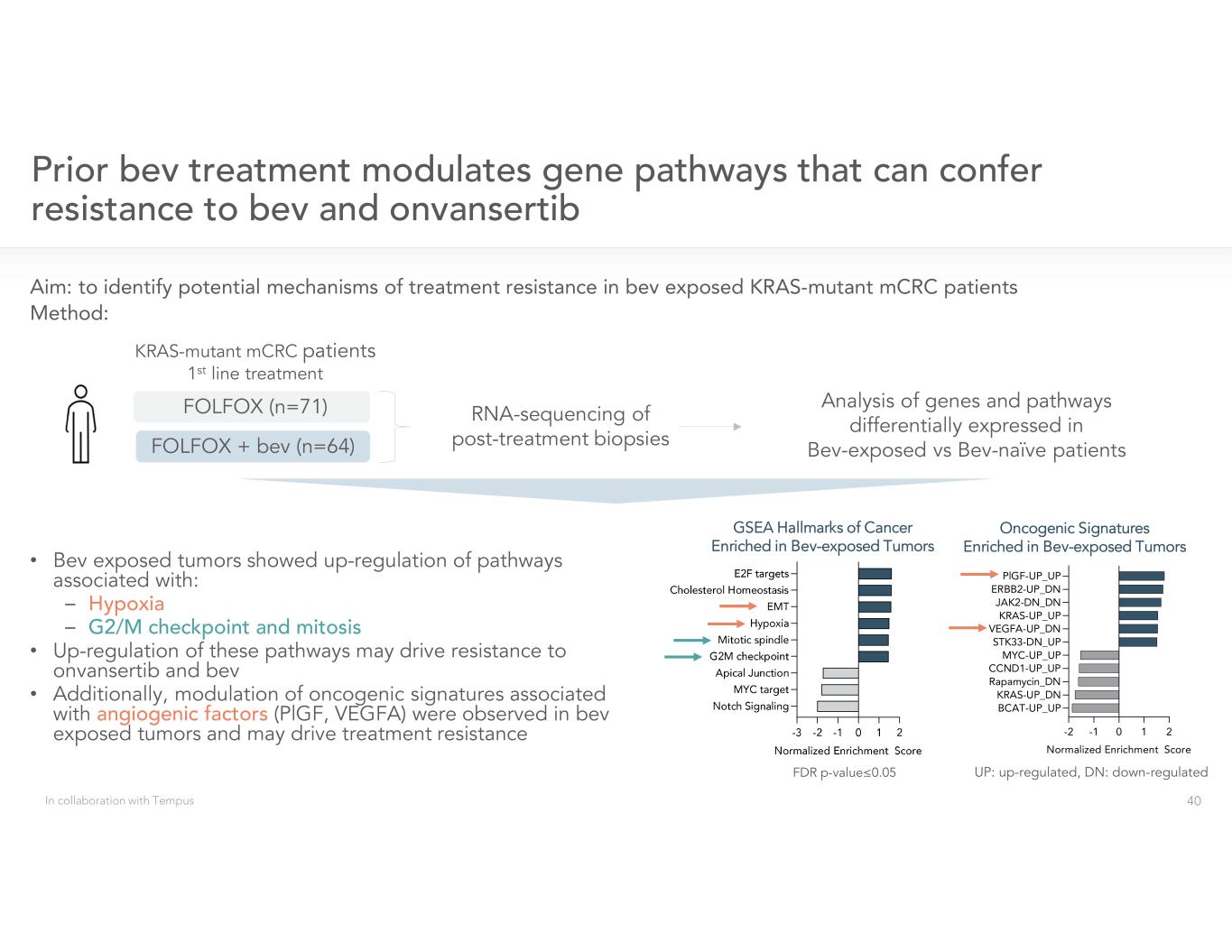
• – – • •
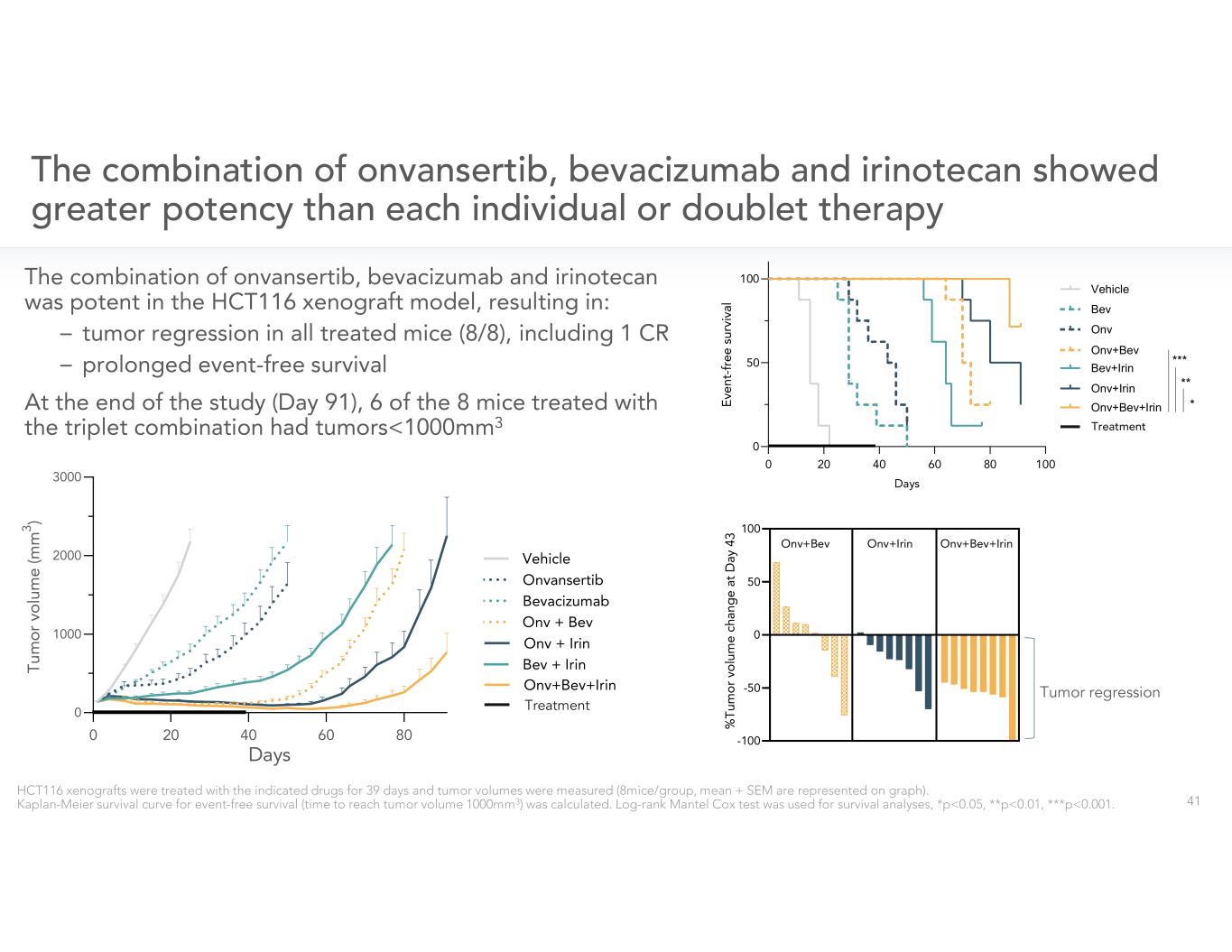
— — Onv+Bev+Irin Vehicle Bev Onv Bev+Irin Onv+Bev Onv+Bev Onv+Irin Vec Onv+Irin *** *
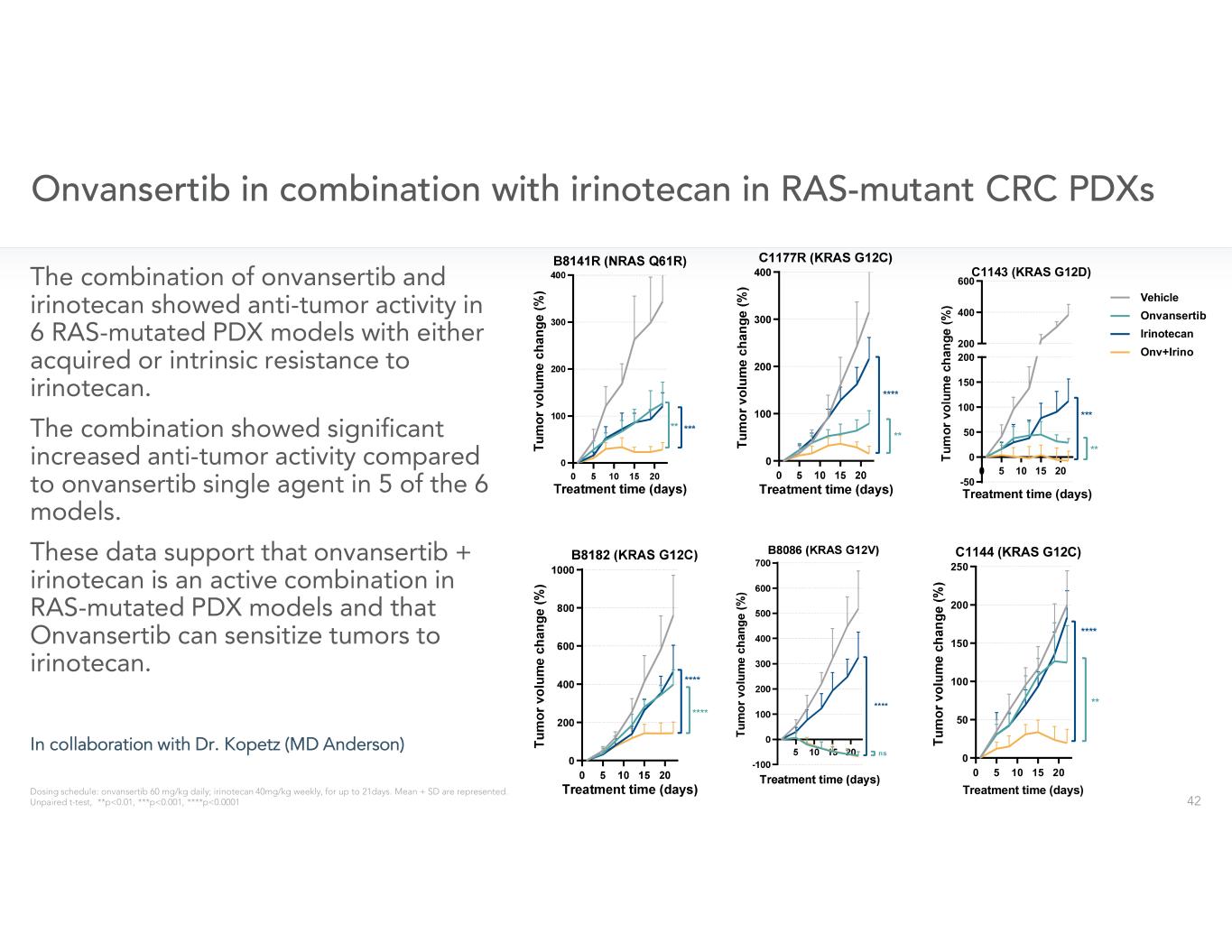
0 5 10 15 20 -50 0 50 100 150 200 200 400 600 治療時間(天)C1143(KRAS G12D)** *** *** 0 5 10 15 20 0 50 100 150 150 150 200 250 250 250 250 250 治療時間(天)C1144 (KRAS G12C) ****** Vehicle Onvansertib Irinotecan

0 5 10 15 20 0 0 100 200 300 治療時間(天)C1138(KRAS G13D)***** 0 5 10 15 20 0 200 400 600 800 800 治療時間(天)B8239 (KRAS G12C) *** *** 5 10 15 20 0 100 200 300 300 治療時間(天)C1143 (KRAS G12D) ***
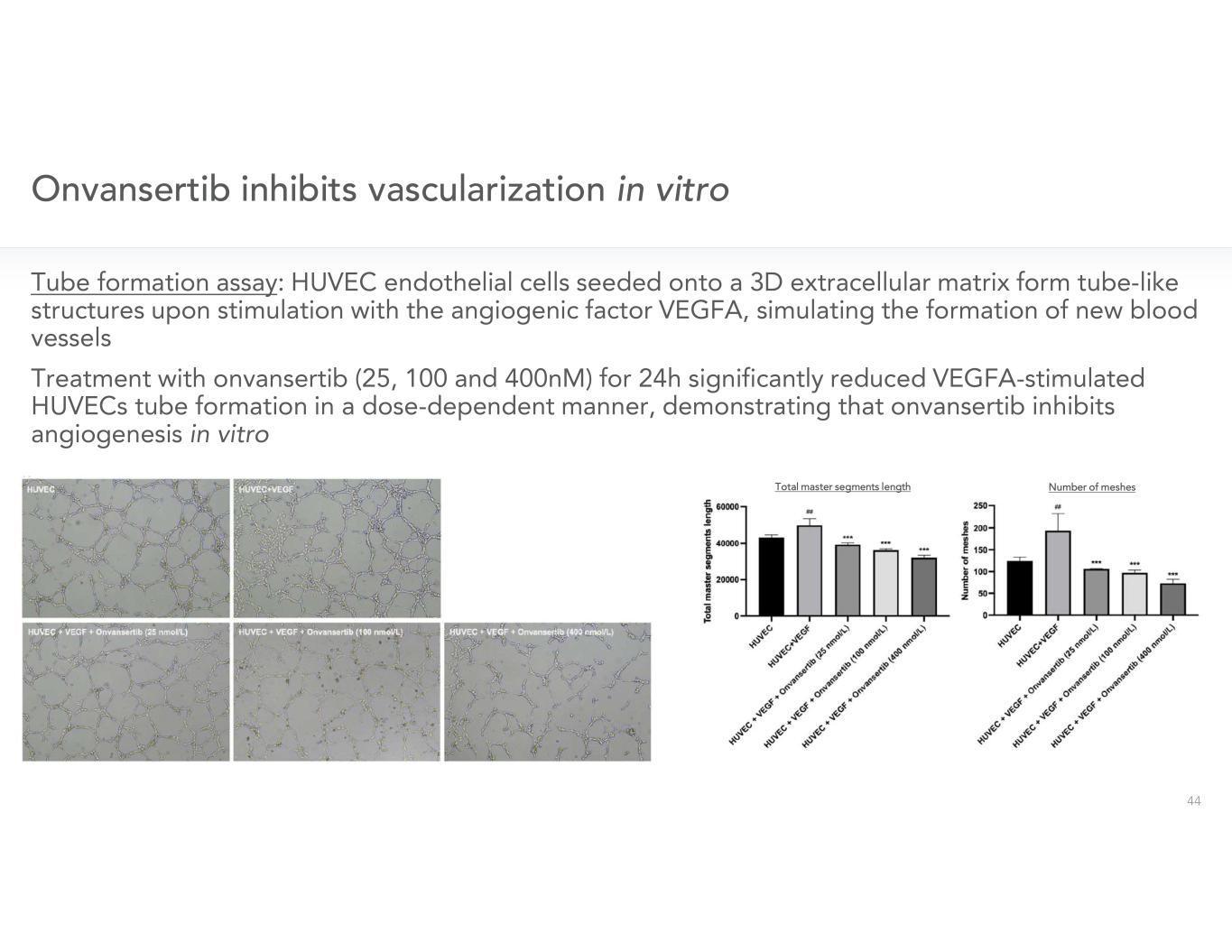

附錄:轉移性胰腺腺癌 (mpDAC)

mpDAC CRDF-001 Ph 2 二線試驗 • mpDAC 生物標誌物發現試驗 (IIT) • 前進之路:轉向一線 mpDAC •

mpDAC CRDF-001 Ph 2 二線試驗 • mpDAC 生物標誌物發現試驗 (IIT) • 前進之路:轉向一線 mpDAC •

14 天週期註冊標準目標主要終點次要終點

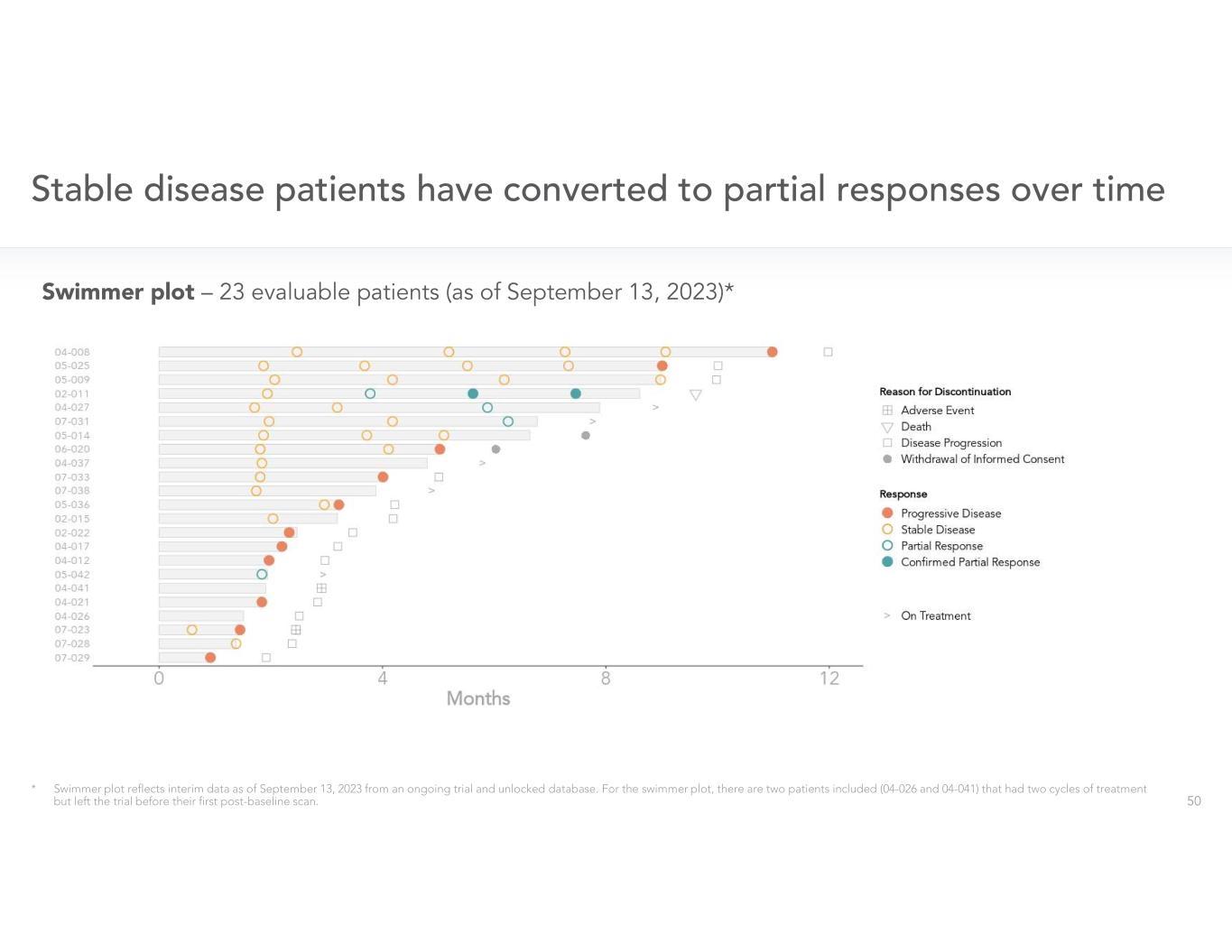
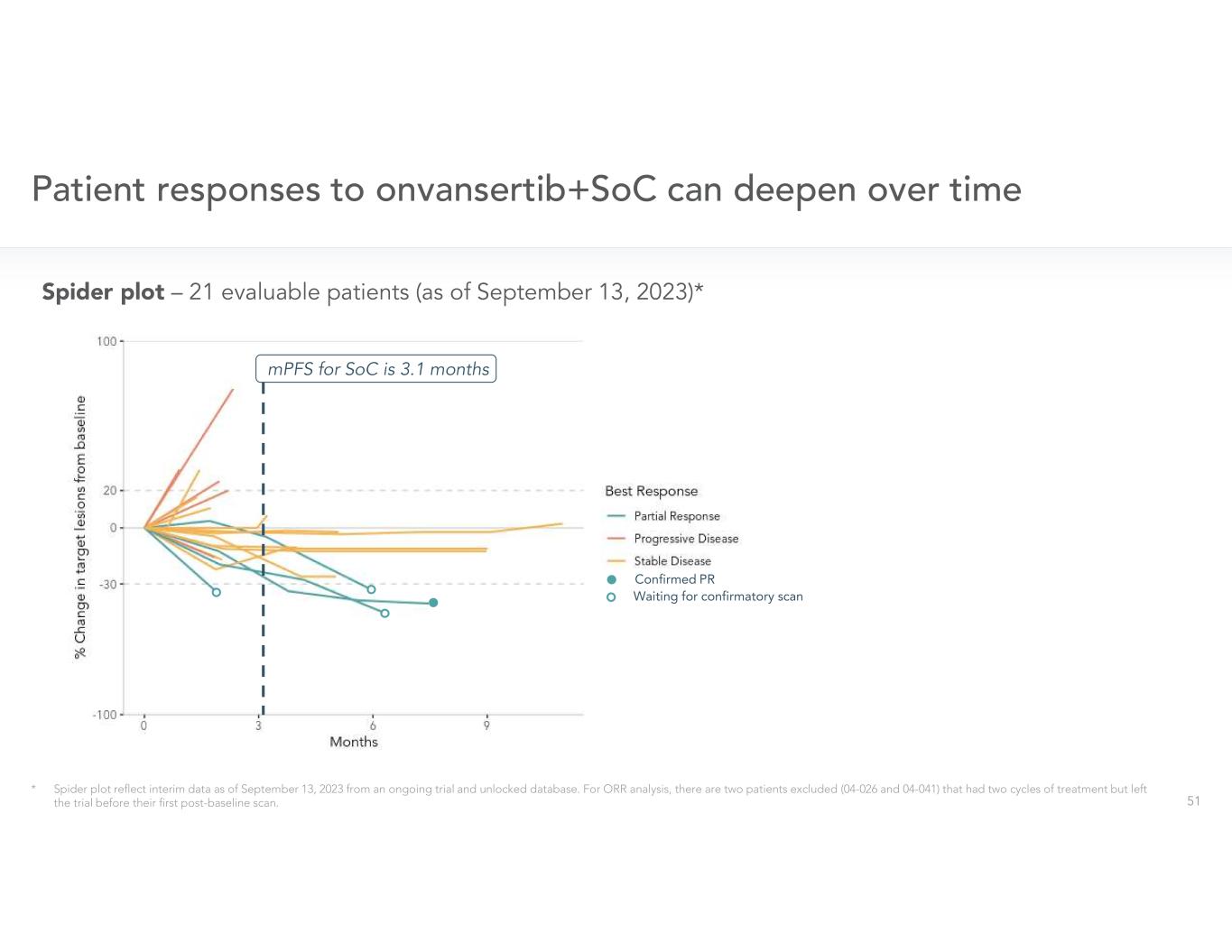


mpDAC CRDF-001 Ph 2 二線試驗 • mpDAC 生物標誌物發現試驗 (IIT) • 前進之路:轉向一線 mpDAC •
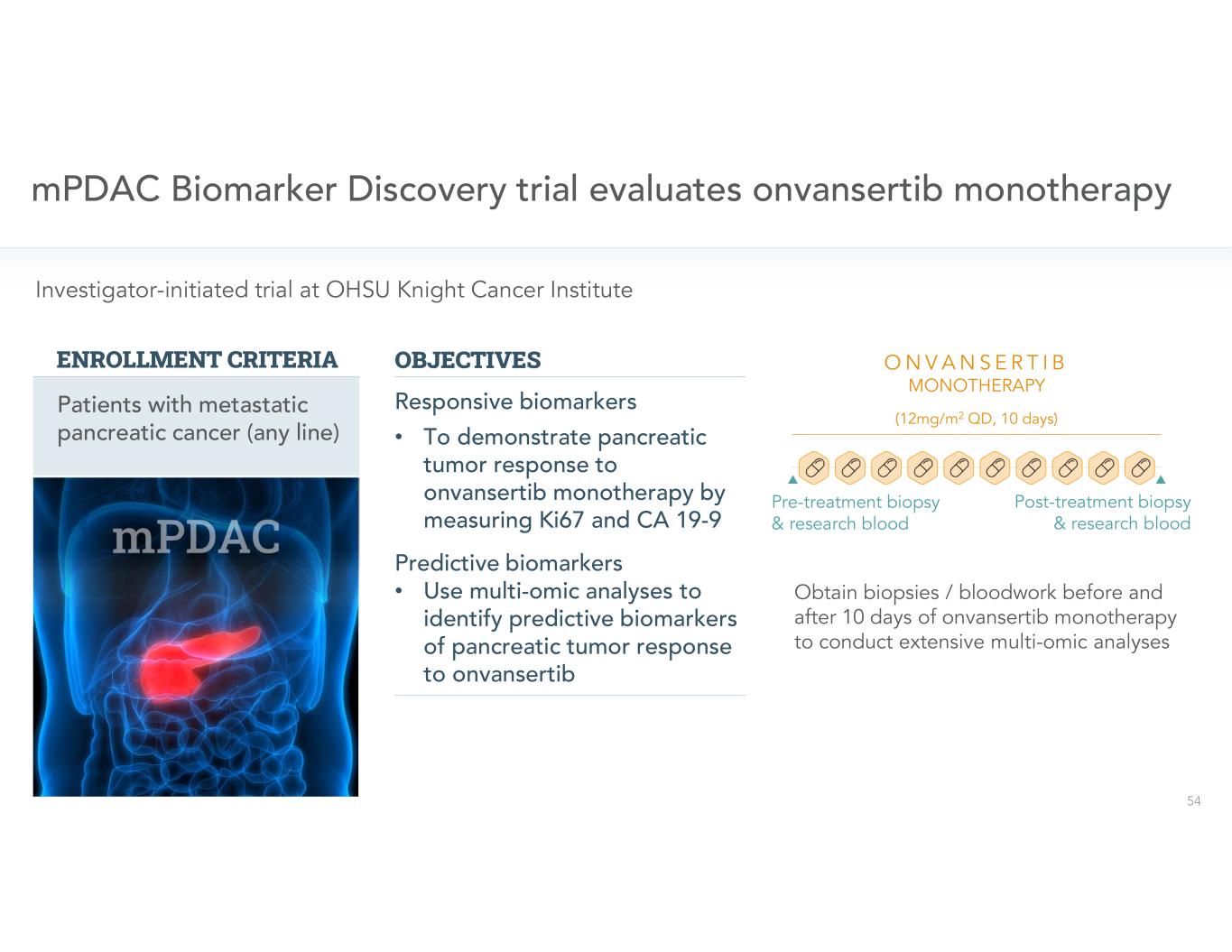
• • 目標/註冊標準
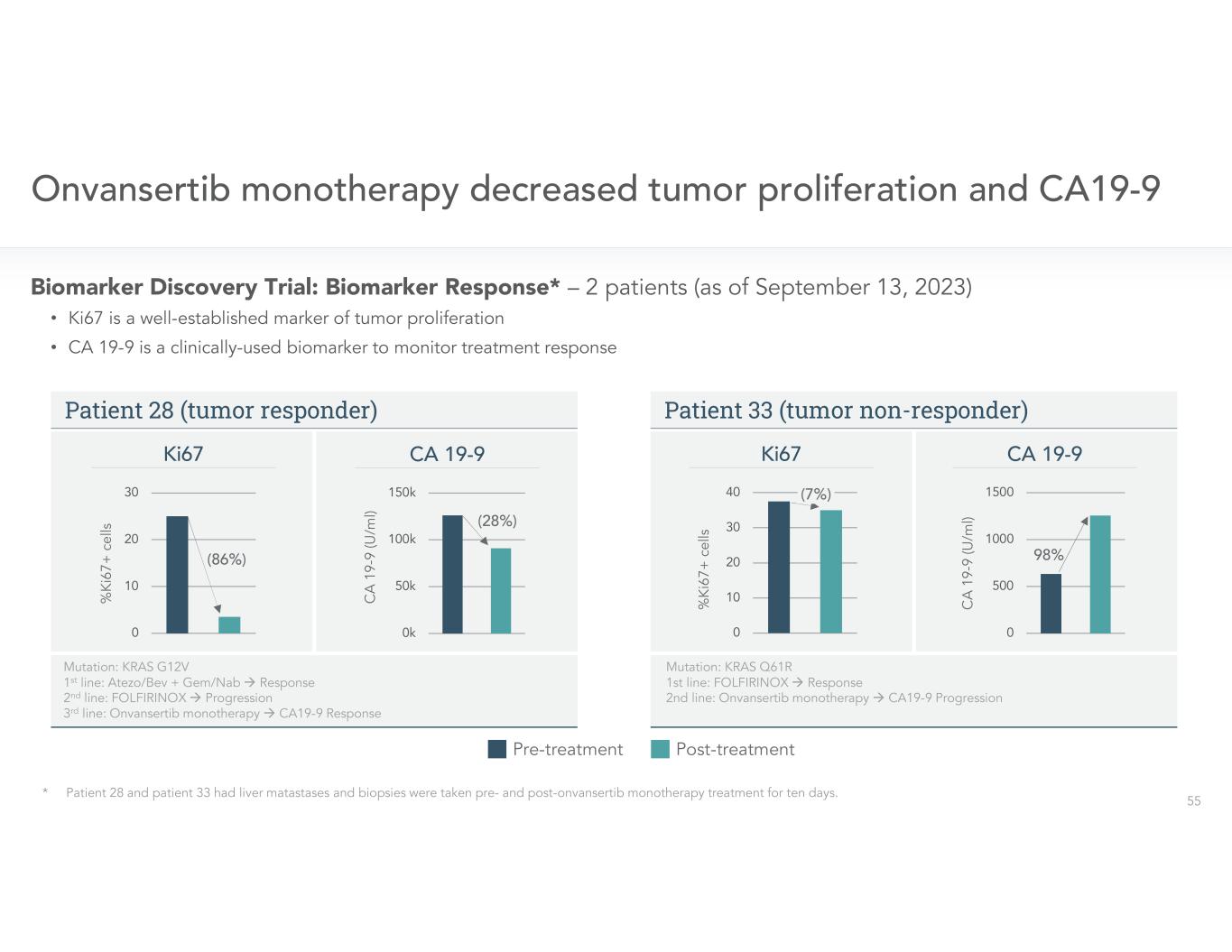
患者 28(腫瘤反應者)患者 33(腫瘤無反應者)•

mpDAC CRDF-001 Ph 2 二線試驗 • mpDAC 生物標誌物發現試驗 (IIT) • 前進之路:轉向一線 mpDAC •

入組標準 28 天週期兩個先導隊列後續化療 + ONVANSERTIB 治療* • • 主要終點次要終點
附錄:研究者發起的小細胞肺癌(SCLC)試驗

審判理由

註冊標準 21 天週期主要終點次要終點目標

附錄:研究者發起的三陰性乳腺癌(TNBC)試驗

審判理由

− 註冊標準主要終點 28 天週期

註冊標準 28 天週期主要終點次要終點 −