
1 第42屆摩根大通醫療保健年度會議開發和提供改善癌症患者生活的下一代療法(太平洋時間1月10日星期三下午 1:30)

2 本演示文稿包含1995年《私人證券訴訟改革法》所指的前瞻性陳述。諸如 “可能”、“將”、“期望”、“計劃”、“預測”、“估計”、“打算”、“可以”、“相信”、“目標”、“預測”、“表明”、“潛力”、“機會” 等詞語和類似表達(以及其他提及未來事件、條件或情況的詞語或表達)旨在識別前瞻性陳述。本演示中的前瞻性陳述包括但不限於對COSELA®(trilaciclib)商業成功的預期、我們進一步開發和擴大COSELA在廣泛期小細胞肺癌治療中的用途的能力、曲拉西利布在三陰性乳腺癌治療中的治療潛力,以及與ADC相關的前瞻性陳述,曲拉西利布的最大影響是對包括操作系統在內的長期終點,曲拉西利布可以改善長期免疫監測,從而在治療後獲得更多益處,預計在正在進行的PRESERVE 2三期臨牀試驗中實現操作系統終點有望在2024年及以後實現全球監管機構申報,G1的現金流預計將延續到2025年,鉑基化療短缺的影響已開始減弱,全球擴張,在3期TNBC試驗中實現操作系統主要終點可能會成為全球擴張計劃的催化劑。此外,COSELA可能無法達到市場對商業成功的接受程度,證明trilaciclib + gem/carbo作為1L TNBC標準護理的潛力,以及 COVID-19(冠狀病毒)等流行病的影響,均基於我們截至本次演講之日的預期和假設。這些前瞻性陳述都涉及風險和不確定性,可能導致我們的實際業績與此類陳述中表達或暗示的業績存在重大差異。投資者、潛在投資者和其他人應仔細考慮這些風險和不確定性。我們在向美國證券交易委員會提交的文件中討論了適用的風險和不確定性,包括其中包含的 “風險因素” 部分,包括但不限於我們成功商業化COSELA的能力;對COSELA商業成功的依賴;我們完成COSELA和除COSELA以外的任何候選產品的臨牀試驗、獲得批准和商業化的能力;我們最初的成功在臨牀試驗中可能不表示在以下情況下獲得的結果這些試驗已完成或處於後期試驗階段;與開發新產品或技術以及作為商業階段公司運營相關的固有不確定性;化療短缺和市場狀況。除非法律要求,否則即使有新的信息,我們也沒有義務更新此處包含的任何前瞻性陳述以反映預期的任何變化。前瞻性陳述 G1Therapeutics® 和 G1Therapeutics 徽標以及 COSELA® 和 COSELA 徽標是 G1 Therapeutics, Inc. 的商標 ©2024 G1 Therapeutics, Inc.

3 G1 Therapeutics:顯著增長的機會 • 通過短暫的G1抑制HSPC和T細胞為患者帶來有意義的好處的新產品 • 美國建立了商業基礎設施,初始ES-SCLC適應症的收入不斷增長 • 3期讀數提供了重要的短期全球潛在商業機會(第一季度中期分析)• 隨機第二階段觀察到的強大操作系統,後續療法持續改善 • sacituzumab govitecan的2期研究提供了重要的潛在全球商業機會(第一季度中期分析)在 TROP2 ADC 組合中用作 trilaciclib 的概念驗證• 觀察安全性和耐受性的強勁改善以及潛在的生存益處 • 評估更多後期研究並對下一代產品進行研究 • 在成功發佈1L TNBC後,計劃尋找全球擴張的合作伙伴 • 預計到2025年的現金流美國上市的獨特產品具有不斷增長的收入潛力將轉化1L TNBC治療有機會提高面向全球擴張和未來增長的領先ADC的安全性和有效性注:HSPC的:造血術幹細胞和祖細胞,ES-SCLC:廣泛期小細胞肺癌,TNBC:三陰性乳腺癌;ADC” 抗體藥物偶聯物

4 Agenda 在美國上市的獨特產品,收入潛力不斷增長,將改變1L TNBC治療的機會,以提高領先ADC的安全性和有效性,為全球擴張和未來增長做好準備
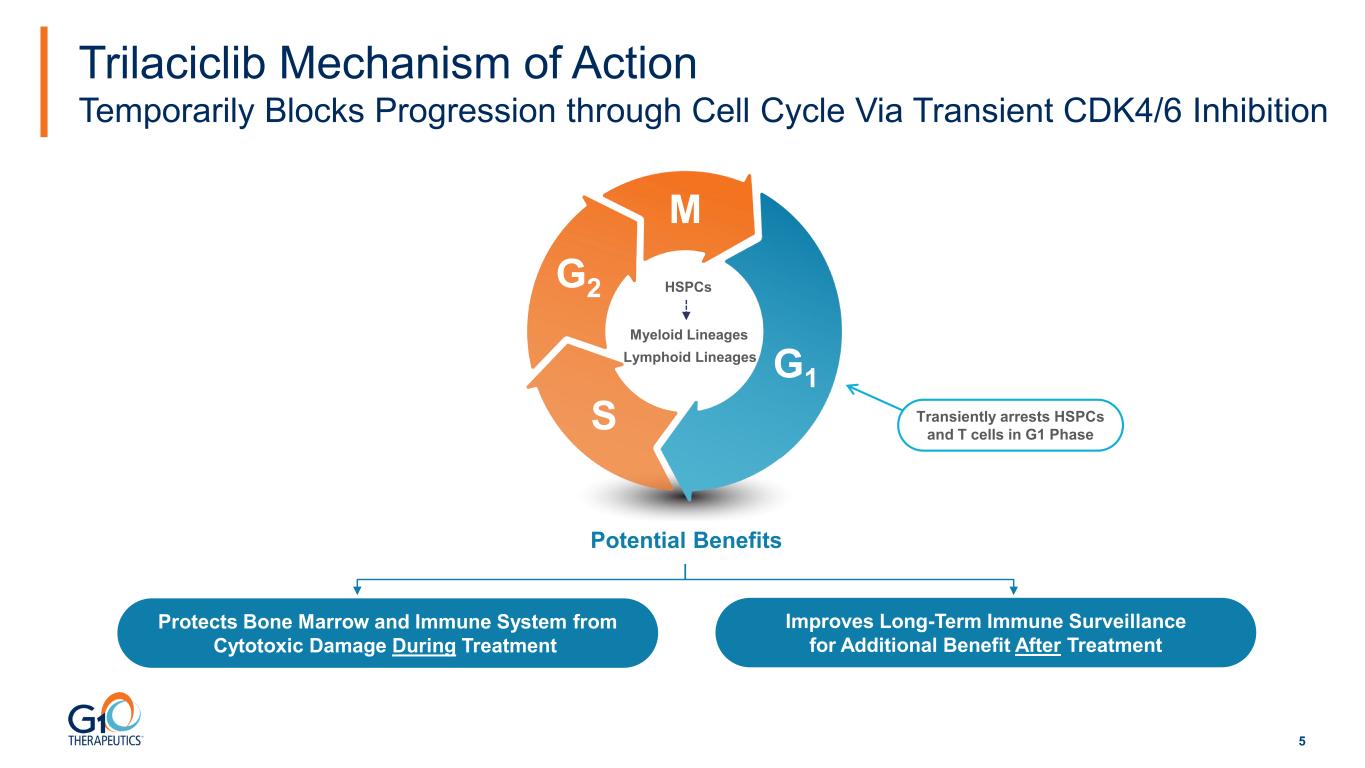
5 Trilaciclib 的作用機制通過瞬時的 CDK4/6 抑制暫時阻斷細胞週期進展主要優點 M G2 S G1 髓系淋巴譜系 HSPC 在治療期間保護骨髓和免疫系統免受細胞毒性損傷改善長期免疫監測以獲得額外益處在 G1 階段暫時抑制 HSPC 和 T 細胞潛在益處

6 強效的選擇性CDK4和CDK6抑制作用穩健的瞬態G1抑制IV給藥的獨特產品屬性Trilaciclib的半衰期短的關鍵特性可實現穩定的瞬態G1抑制這些特性對於最大限度地發揮瞬態CDK4/6抑制的優勢至關重要,通過快速靜脈注射獲得精確的定時效果通過靶向活性抑制G1可優化T細胞的增殖能力
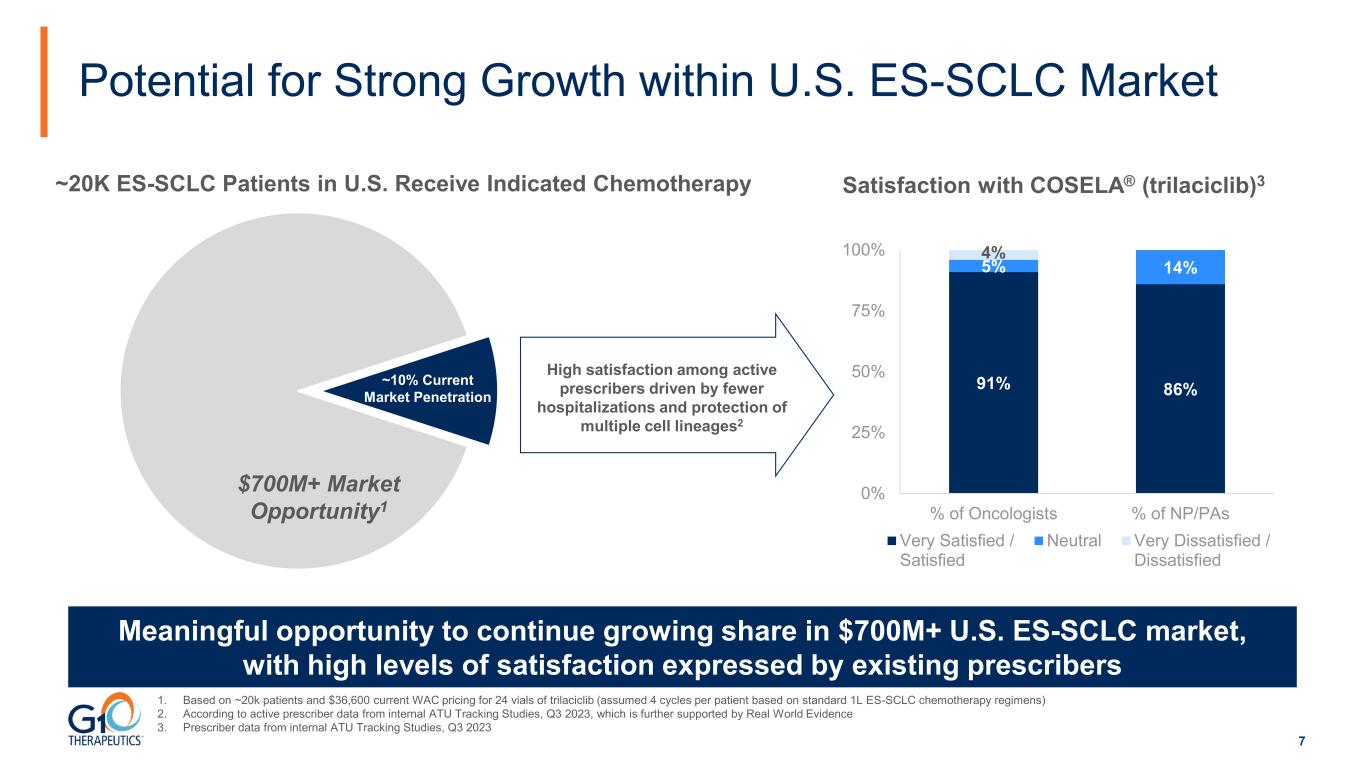
7 1.基於約2萬名患者和目前WAC對24瓶曲拉西利布的36,600美元定價(根據標準的1L ES-SCLC化療方案,假設每位患者有4個週期)2。根據2023年第三季度ATU內部跟蹤研究的活躍處方數據,該數據得到了真實世界證據 3 的進一步支持。來自ATU內部跟蹤研究的處方者數據,2023年第三季度在超過7億美元的美國ES-SCLC市場中繼續增長份額的有意義的機會,現有處方者表示了很高的滿意度。美國約2萬名ES-SCLC患者接受了7億美元以上的指定化療市場機會1對COSELA®(曲拉西布)3 的滿意度 91% 86% 5% 14% 4% 0% 25% 50% 75% 的腫瘤百分比醫生百分比NP/PA非常滿意/滿意中立非常不滿意/不滿意 ~ 10% 當前市場滲透率受較少驅使活躍處方者滿意度高住院治療和多細胞譜系保護2 美國ES-SCLC市場有強勁增長的潛力
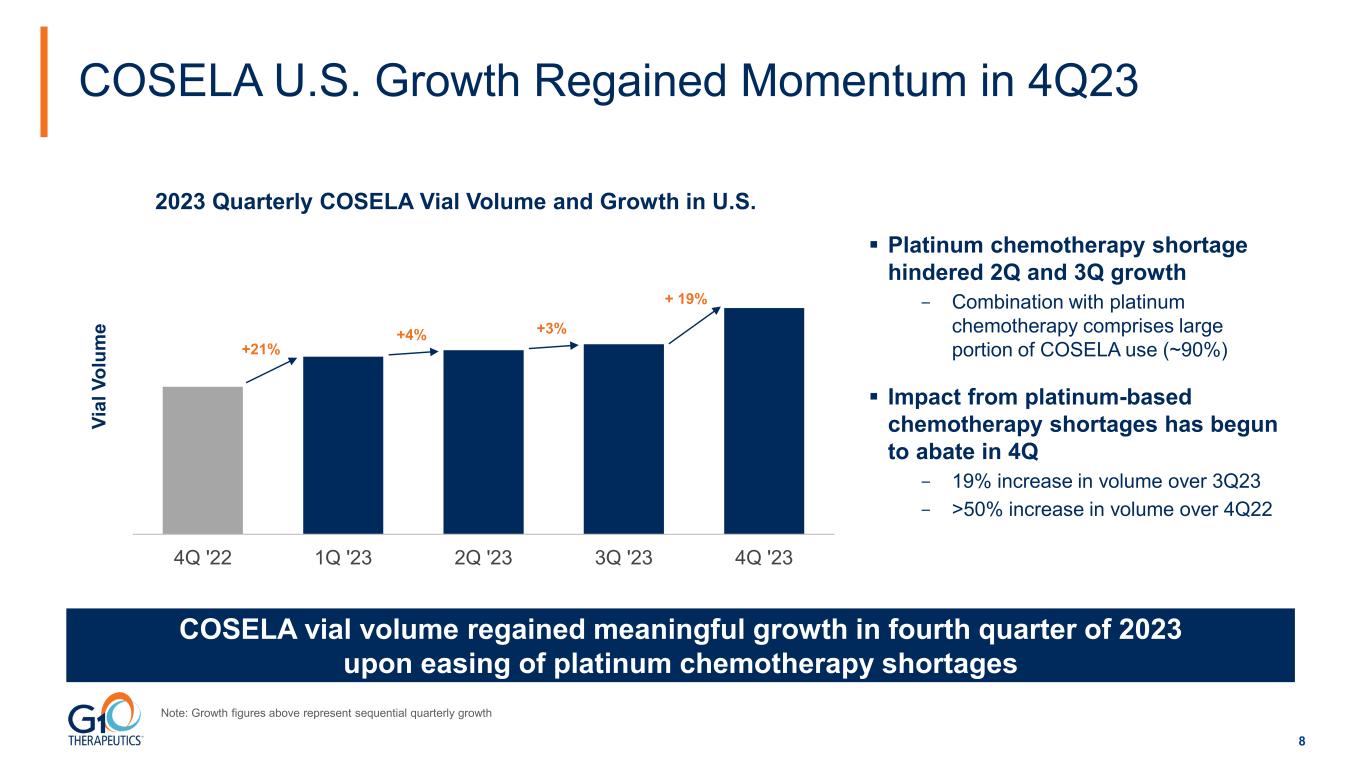
8 2022年第四季度第一季度23季度23年第三季度2023年第四季度Vi al V ol um e 2023年第四季度COSELA藥瓶數量和美國增長COSELA美國增長在2023年第四季度恢復勢頭 COSELA藥瓶數量在鉑金化療短缺緩解後於2023年第四季度恢復了有意義的增長注意:上面的增長數據代表連續季度增長 +3% + 19% 鉑金化療短缺阻礙了第二季度和第三季度增長-與鉑化療聯合使用佔COSELA使用量的很大一部分(約90%),鉑類化療短缺的影響已在第四季度開始減弱-交易量比 23 年第 3 季度增長 19%-交易量比 22 年第 4 季度增長超過 50% +21% +4%
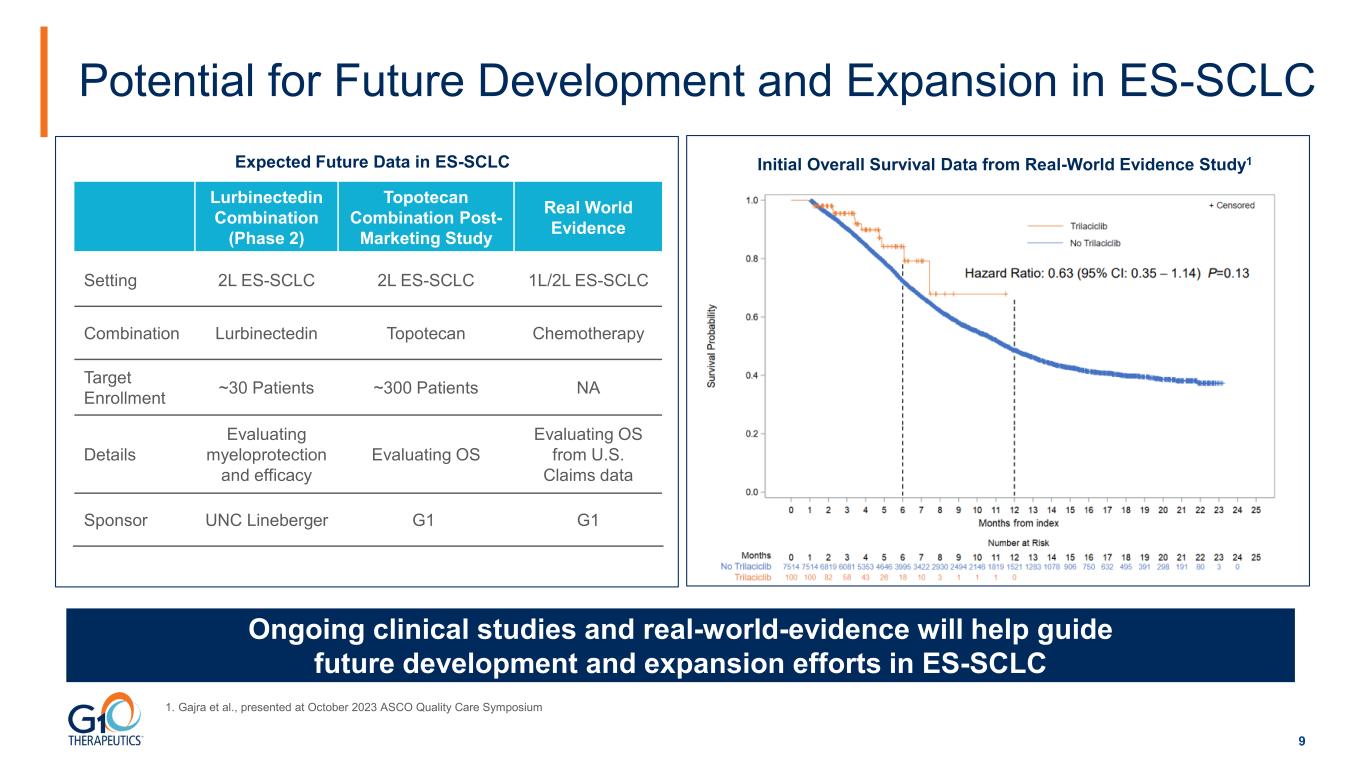
9 ES-SCLC 未來發展和擴張的潛力正在進行的臨牀研究和真實證據將有助於指導 ES-SCLC Lurbinectedin 組合(第 2 期)拓撲替康組合上市後研究真實世界證據設置 2L ES-SCLC 2L ES-SCLC 1L/2L ES-SCLC 組合 Lurbinectedin 拓撲替康化療目標入組 ~30 名患者 ~300 名患者北美詳情評估骨髓保護和功效評估操作系統根據美國索賠數據評估操作系統贊助商 UNC Lineberger G1 G1 初始總存活率來自真實世界證據研究的數據1ES-SCLC中的預期未來數據 1.Gajra 等人,在 2023 年 10 月 ASCO 質量護理研討會上發表

10項議程:美國獨一無二的上市產品,收入潛力不斷增長,將改變1L TNBC治療的機會,以提高面向全球擴張和未來增長的領先ADC的安全性和有效性

11 轉移性 TNBC:未得到滿足的高需求領域曲拉西利布有可能改變轉移性 TNBC 的治療方案 Metastatic TNBC 是一種侵襲性癌症,治療選擇有限 SoC(基於亞羣的+/-免疫療法)Trilaciclib 在 1L/2L/3L TNBC 隨機分組 2 期中表現出廣泛益處——在 PD-L1+ 和 PD-L1-亞羣中觀察到獲益——獲得 Fast Track 稱號由美國食品藥品管理局批准用於局部晚期或轉移性 TNBC 1。基於Clarivate DRG數據、主要市場研究和內部分析,估算2024年美國潛在人口 2.市場規模估算基於目前WAC對32瓶曲拉西利布的48,700美元(在之前的mtnBC第二期研究中接受的約8個週期的曲拉西布的平均值)美國患者羣體(美國市場規模估計)1 3L TNBC 5K可治療患者(約2.5億美元的市場機會)2L TNBC 7K可治療患者(約3.5億美元的市場機會)1L TNBC 9K 可治療的患者(約4.5億美元的市場機會)
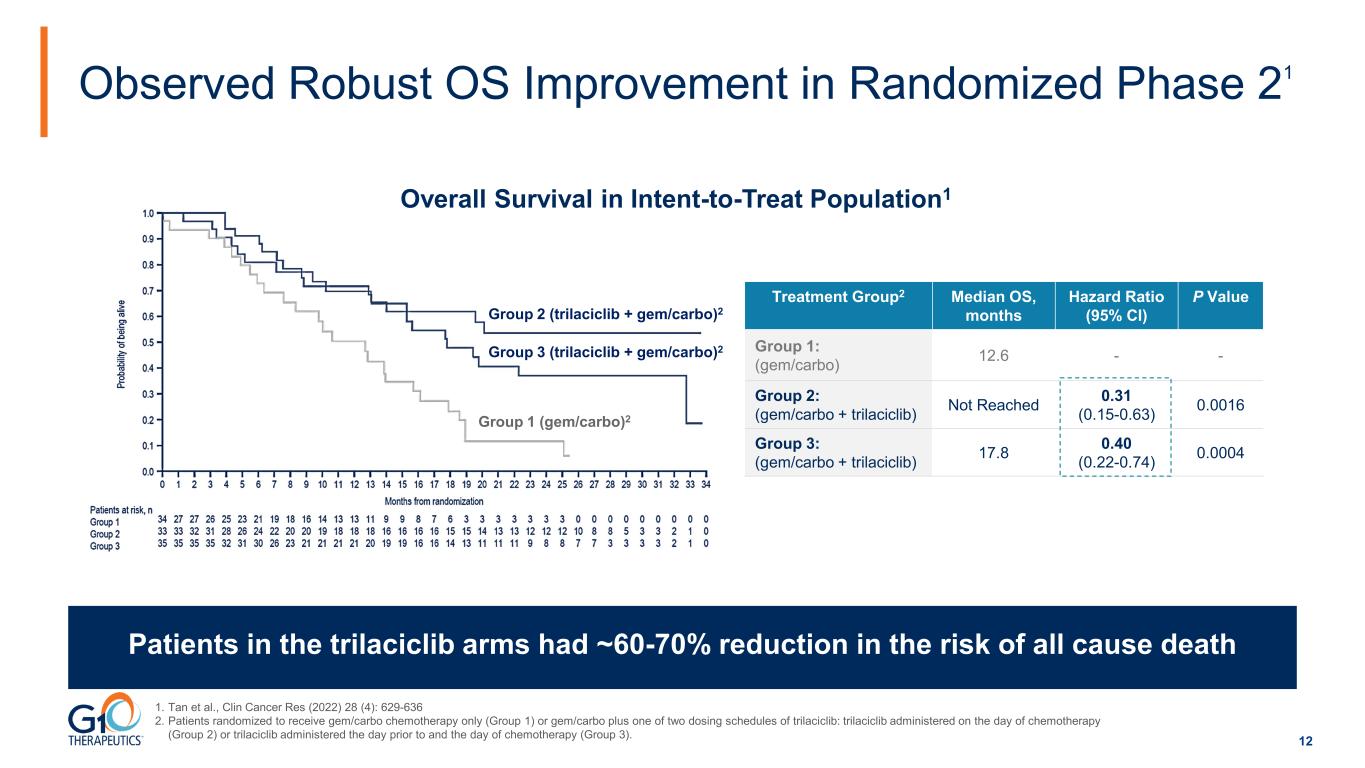
12 觀察到隨機階段 21 中操作系統的強勁改進 1.陳等人,《臨牀癌症研究》(2022年)28(4):629-636 2。患者隨機分配僅接受gem/carbo化療(第1組)或gem/carbo加上曲拉西利布的兩種給藥計劃之一:在化療當天給藥(第2組)或在化療前一天和化療當天給藥(第3組)的曲拉西布。曲拉西利布組的患者全因死亡風險降低了約 60-70% 治療組2 操作系統中位數,月份危險比(95% CI)P 值組 1:(gem/carbo)12.6--第 2 組:(gem/carbo + trilaciclib)未達到 0.31(0.15-0.63)0.0016 組 3:(gem/carbo + trilaciclib)17.8 0.40(0.22-0.63)0.0016 組 3:(gem/carbo + trilaciclib)17.8 0.40(0.22-22-lib)0.0.74) 0.0004 意向治療人羣的總存活率1 組 1(寶石/碳水化合物)2 組 3(trilaciclib + gem/carbo)2 第 2 組(trilaciclib + gem/carbo)2

13 總體存活率最顯著的效果 1.陳等人,《臨牀癌症研究》(2022年)28(4):629-636 2。患者隨機分配僅接受gem/carbo化療(第1組)或gem/carbo加上曲拉西利布的兩種給藥計劃之一:在化療當天給藥(第2組)或在化療前一天和化療當天給藥(第3組)的曲拉西布。

14 在 PD-L1 亞羣中觀察到操作系統改善 PD-L1 陽性腫瘤患者的總存活率 PD-L1 陰性腫瘤患者的總存活率 1.Tan 等人,《臨牀癌症研究》(2022年)28(4):無論患者的腫瘤狀態如何,均觀察到629-636 操作系統改善 Chemo(第 1 組)Trilaciclib(第 2 組/3 組)患者(n)17 32 操作系統中位數(月)10.5 32.7 HR 0.34 P 值 0.004 Chemo(第 1 組)Trilaciclib(第 2 組/3 組)患者(n)17 32 操作系統中位數(月)10.5 32.7 HR 0.34 P 值 0.004 Chemo(第 1 組)Trilaciclib(第 2 組/3 組)患者(n)10 26 操作系統中位數(月)月) 13.9 17.8 小時 0.48 P 值 0.093 PD-L1

隨着時間的推移,隨着後續治療患者接受後續療法,15 操作系統增加1 具有統計學意義;p=0.001 未接受後續治療的患者1 隨着患者接受後續治療,曲拉西利布組的操作系統益處持續增加 20 20 18 14 11 8 5 3 3 0 3 3 0 39 35 34 30 26 17 14 6 2 0 高危患者,n 化療(第 1 組):任何 SACT Trila(組 2/3):任何 SACT 高危患者,化療(第 1 組):無 SACT 試驗(第 2/3 組):無 SACT 14 6 3 2 2 1 1 0 25 23 15 6 5 5 3 3 3 1 0 Trila(第 2/3 組):任何 SACT 中位數 OS = 32.7化療(第 1 組):任何 SACT 中位數操作系統 = 12.8 Pr ob ili i i i f o ve ve ra ll su rv iv 自隨機化以來的時間(月)0 3 6 9 12 15 18 21 24 27 30 33 36 0 3 6 9 12 15 18 21 24 27 30 0.8 0.6 0.2 0.2 pr ob ab ili ty ra ll su rv iv all 0.8 0.6 0.2 Trv iv al 0.8 0.6 0.2 Trv iv al 0.8 0.6 0.2 Trv iv al 0.8 0.6 0.2 Trv iv al 0.8 0.6 ILA(第 2/3 組):無 SACT 中位數 OS = 9.4 Chemo(第 1 組):無 SACT 中位數 OS = 5.4 注意:SACT:後續抗癌治療。1.Goel S,《在細胞毒性化療之前接受曲拉西利布治療的轉移性三陰性乳腺癌患者,在接受後續抗癌治療後,存活率有所提高,聖安東尼奧乳腺癌研討會(SABCS),2023年12月5日至9日,PO2-06-12。
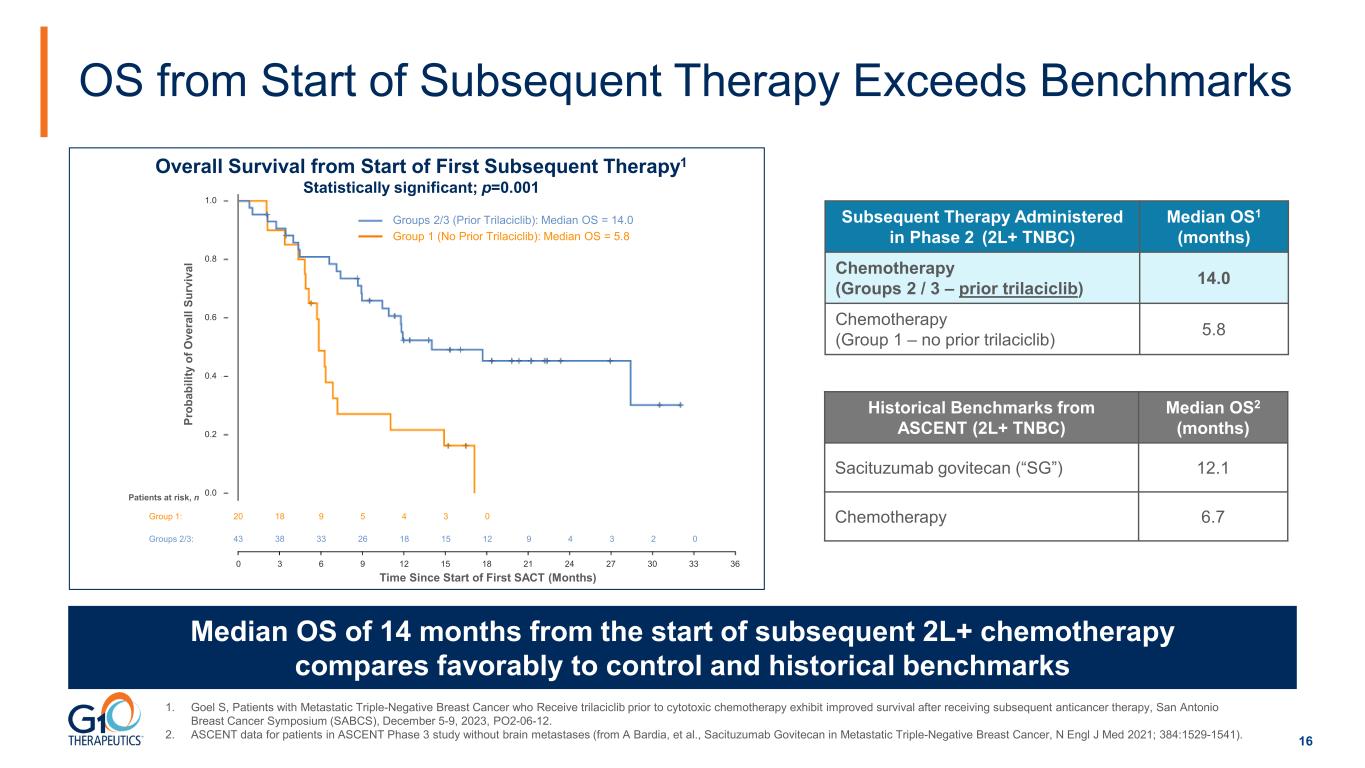
16 種操作系統從後續治療開始算起 14 個月的操作系統中位數超過基準 2L+ 化療開始後 14 個月的中位操作系統與對照組和歷史基準相比效果較好 2 期(2L+ TNBC)中位數 OS1(月)化療(第 2 組/3 組 — 之前的曲拉西布)14.0 化療(第 1 組 — 之前沒有曲拉西布)5.8 來自 OSCENT 的歷史基準(2L+ TNBC 中位數)2(月)Sacituzumab govitecan(“SG”)12.1 化療 6.7 1.Goel S,《在細胞毒性化療之前接受曲拉西利布治療的轉移性三陰性乳腺癌患者,在接受後續抗癌治療後存活率有所提高,聖安東尼奧乳腺癌研討會(SABCS),2023年12月5日至9日,PO2-06-12。2.ASCENT 3期研究中沒有腦轉移的患者的ASCENT數據(來自A Bardia等人,Sacituzumab Govitecan在轉移性三陰性乳腺癌中的應用,N Engl J Med 2021;384:1529-1541)。第 2/3 組(之前的 Trilaciclib):操作系統中位數 = 14.0 組 1(無之前的 Trilaciclib):操作系統中位數 = 5.8 20 18 9 5 4 3 0 38 33 26 18 15 12 9 4 3 0 Pr ob ab ili i f o ve ll su rv iv iv iv 所有處於危險中的患者,n 組 2/3:自第一次 SACT 開始以來的時間(月)0 3 6 9 12 15 18 21 24 27 30 33 36 1.0 0.8 0.6 0.4 0.2 0.0 自首次後續治療開始以來的總存活率1 具有統計學意義;p=0.001

17 隨着後續療法的顯著改善,trilaciclib + gem/carbo 作為 1L TNBC 護理標準的可能性持續提高 1L TNBC 第 3 期建立在評估 1L TNBC 患者 PD-L1 陽性和陰性腫瘤患者的結果基礎上 P R I M A R Y E N D P O I N T:總體存活次要終點:PFS、ORR、PRO、骨髓保護措施狀態:麻省理工學院入組的174名患者 2024 年第一季度的 T1 中期操作系統分析 1. miTT 是調整後的治療意向人羣,用於移除參與該研究的 13 名患者來自烏克蘭。安慰劑 + gem/carbo 在第 1 天和第 8 天每 21 天進行一次 trilaciclib + gem/carbo 每隔 21 天進展一次 trilaciclib + gem/carbo 每 21 天進展一次 TNBC R and do m 處於 io n 1:1 治療階段每 3 個月存活一次

18 Agenda在美國上市的獨特產品,收入潛力不斷增長,將改變1L TNBC治療的機會,以提高領先ADC的安全性和有效性,為全球擴張和未來增長做好準備

19 將 Trilaciclib 與 ADC 聯合使用的臨牀依據提高安全性和耐受性改善長期免疫監測保護免疫系統功能 1 2 3 提高免疫系統識別和消滅腫瘤細胞的能力(增強正在進行和後續療法後的長期療效)最大限度地減少細胞毒性有效載荷對免疫系統的長期損害(維持負責長期抗腫瘤免疫的 T 細胞羣)減少與主要 TROP2 ADC 相關的骨髓毒性和腹瀉(改善耐受性狀況並啟用擴展到早期階段)曲拉西利布有可能顯著提高領先ADC的療效和安全性
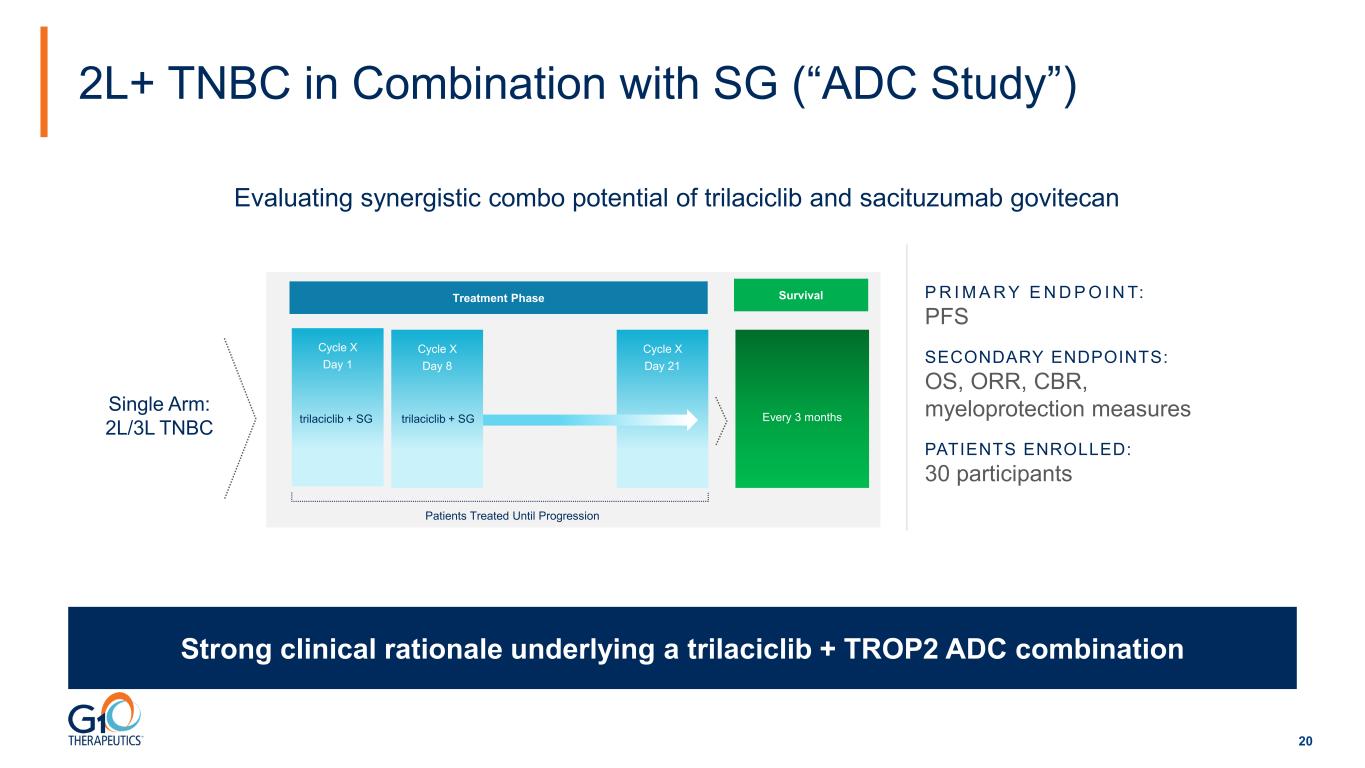
trilaciclib + TROP2 ADC 組合 2L+ TNBC 與 SG 聯合使用(“ADC 研究”)週期 X 第 8 天週期 X 第 1 天週期 X 第 21 天治療階段 trilaciclib + SG trilaciclib + SG 患者治療直至進展 P R I M A R Y E N D P O I N T:PFS 次要終點:OS、ORR、CBR、骨髓保護措施入組患者:30 參與者評估曲拉西利布和沙西妥珠單抗的協同組合潛力 govitecan 每 3 個月生存單臂:2L/3L TNBC
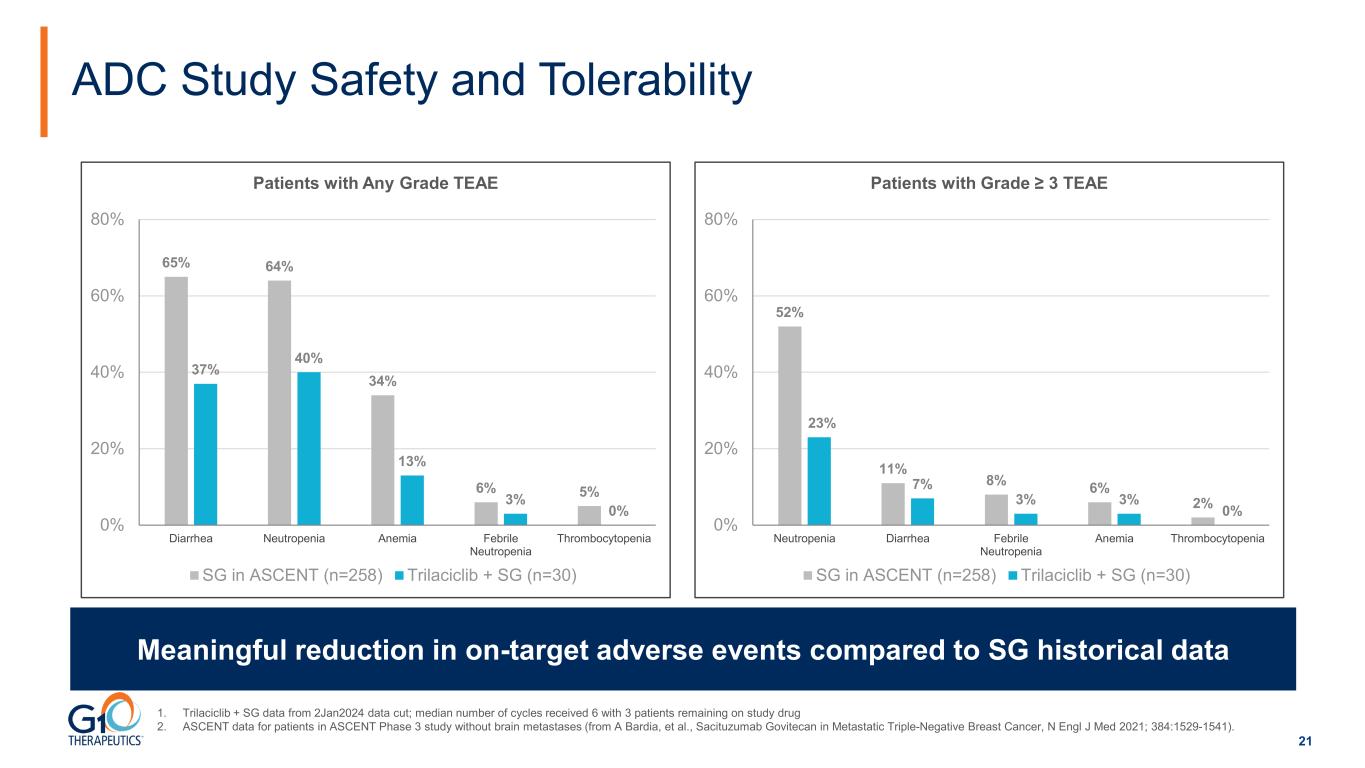
21 ADC 研究安全性和耐受性與 SG 歷史數據相比,靶向不良事件顯著減少 1.Trilaciclib + SG數據截取自2024年1月2日的數據;接受的週期中位數為6次,還有3名患者仍在服用研究藥物2。ASCENT 三期研究中無腦轉移患者的ASCENT數據(來自A Bardia等人,Sacituzumab Govitecan在轉移性三陰性乳腺癌中的應用,N Engl J Med 2021;384:1529-1541)。65% 64% 34% 64% 6% 5% 37% 40% 0% 20% 60% 80% 腹瀉中性粒細胞減少性貧血發熱性中性粒細胞減少血栓症 ASCENT 中任何等級 TEAE SG 的細胞減少患者 (n=258) Trilaciclib + SG (n=30) 52% 11% 8% 6% 2% 23% 3% 3% 0% 20% 40% 60% 80% 80% 中性粒細胞減少腹瀉發熱性中性粒細胞減少貧血血小板減少症 ≥ 3 級 TEAE SG 的患者(n=258)Trilaciclib + SG (n=30)
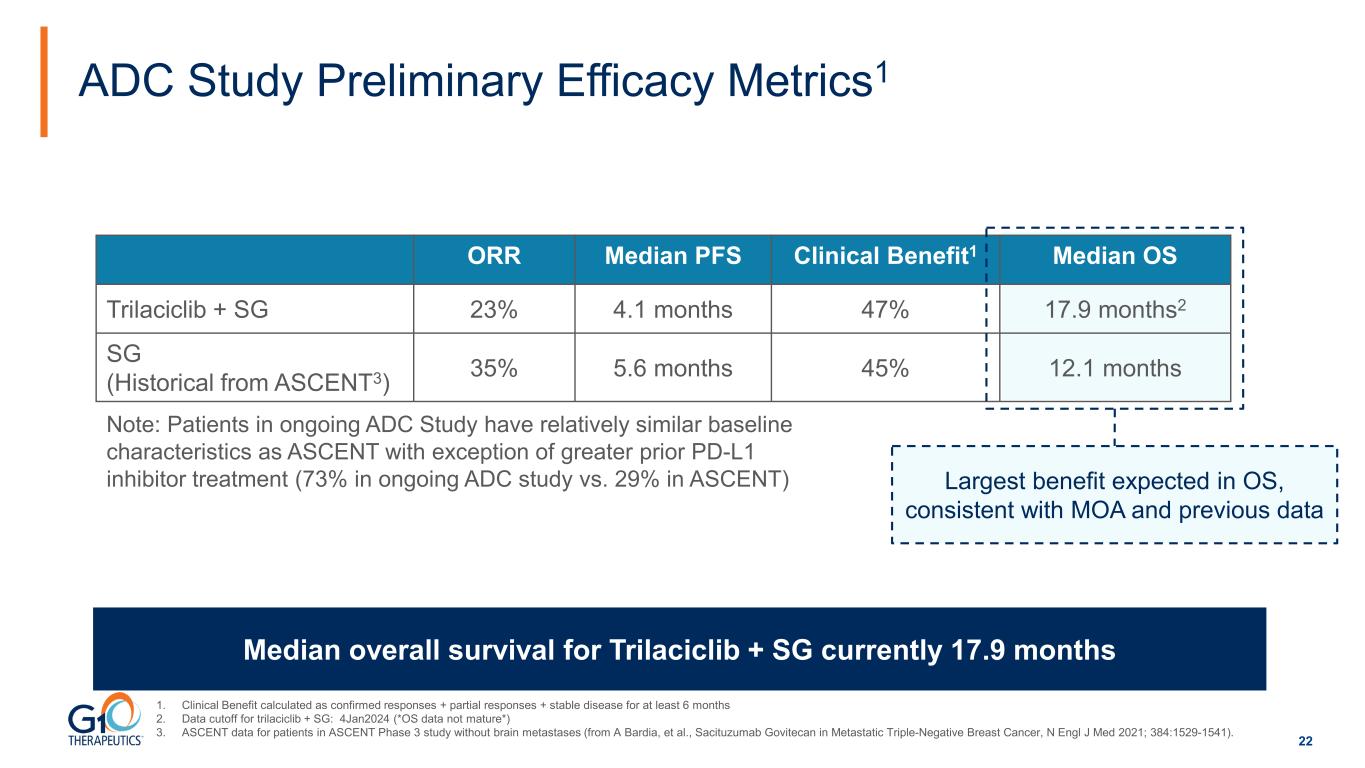
22 ADC 研究初步療效指標1 ORR 中位數 PFS 臨牀效益1 中位數 OS Trilaciclib + SG 23% 4.1 個月 47% 17.9 個月2 SG(來自 ASCENT3 的歷史)35% 5.6 個月 45% 12.1 個月曲拉西布 + SG 的總存活率中位數目前為 17.9 個月操作系統中預期的最大益處,與 MOA 和先前的數據一致。注意:正在進行的 ADC 研究中的患者的基線特徵與 ASCENT 相對相似,但先前較大除外 PD-L1 抑制劑治療(正在進行的 ADC 研究為 73%,ASCENT 為 29%)1。臨牀益處按已確認的反應 + 部分反應 + 至少 6 個月的穩定疾病計算得出 2.trilaciclib + SG 的數據截止日期:2024 年 1 月 4 日(*操作系統數據未成熟*)3.ASCENT 3期研究中沒有腦轉移的患者的ASCENT數據(來自A Bardia等人,Sacituzumab Govitecan在轉移性三陰性乳腺癌中的應用,N Engl J Med 2021;384:1529-1541)。
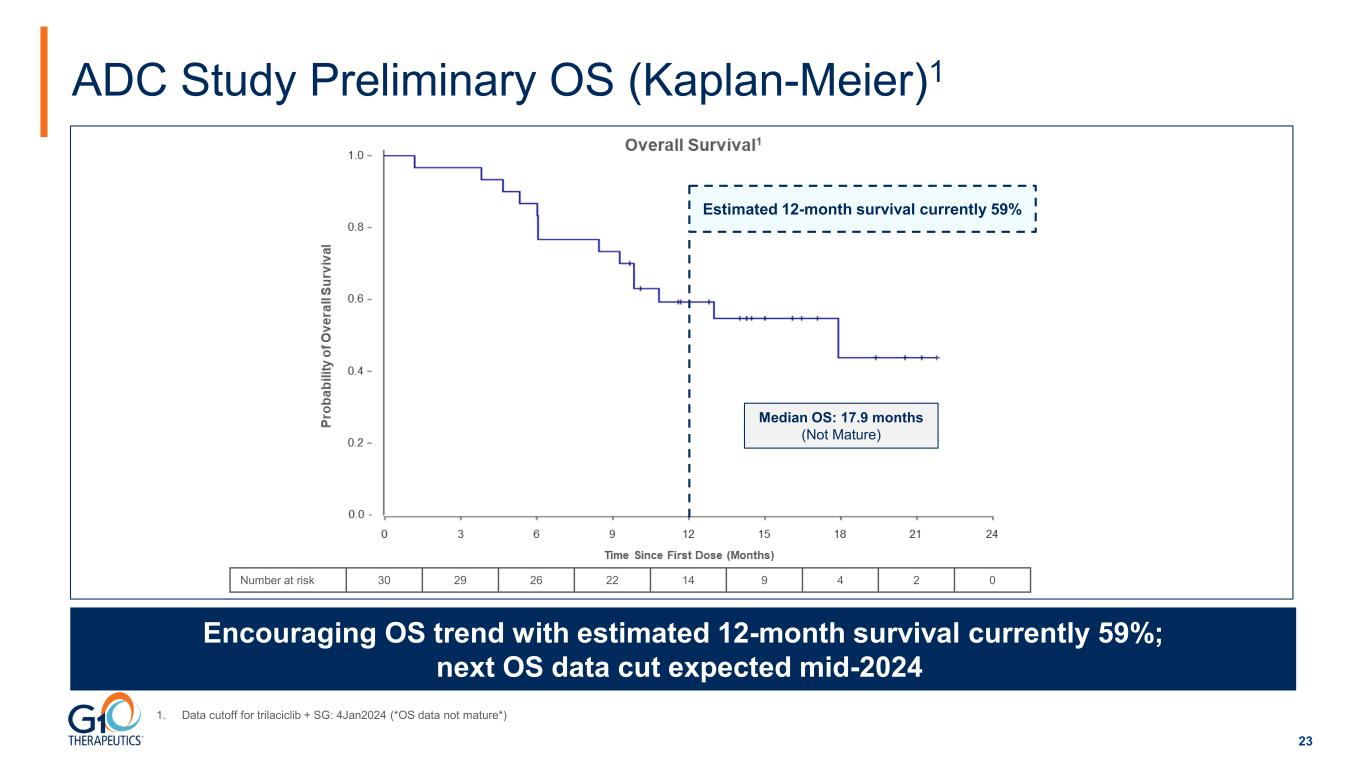
23 1.trilaciclib + SG 的數據截止日期:2024 年 1 月 4 日(*操作系統數據尚未成熟*)ADC 研究初步操作系統(Kaplan-Meier)1 操作系統趨勢令人鼓舞,目前估計 12 個月的存活率為 59%;下一次操作系統數據預計在 2024 年中期下調風險人數 30 29 26 22 14 9 4 2 0 目前估計 59% 操作系統中位數:17.9 個月(未成熟)

24 Agenda 在美國上市的獨特產品,收入潛力不斷增長,將改變1L TNBC治療的機會,以提高領先ADC的安全性和有效性,為全球擴張和未來增長做好準備
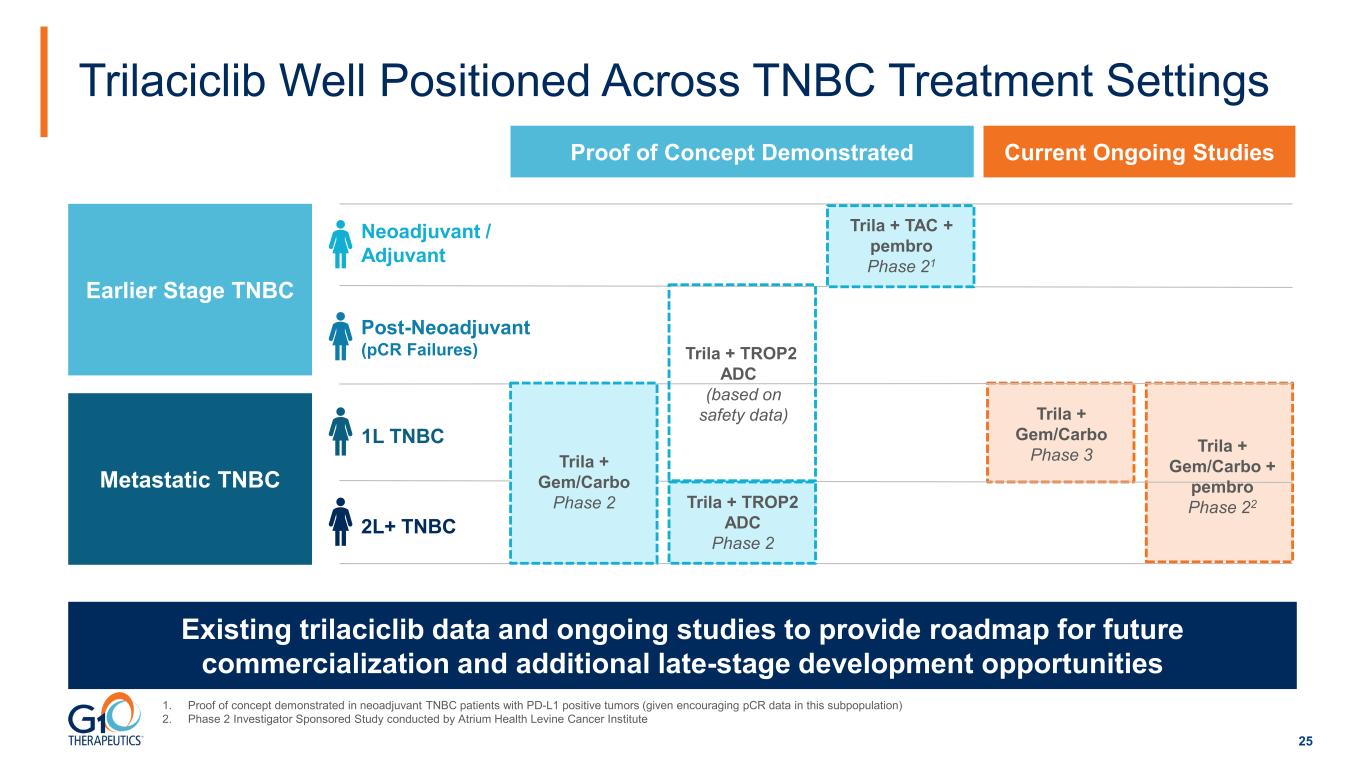
25 Trilaciclib 在 TNBC 治療環境中處於有利地位現有的 trilaciclib 數據和正在進行的研究為未來的商業化提供了路線圖和額外的後期開發機會 Neozuvant /輔助後期新輔助劑(pcR 失敗)早期階段 TNBC 轉移性 TNBC 1L TNBC 2L+ TNBC Trila + Gembro + pembro 第 22 階段概念驗證演示了 Trila + TAC + pembro 第 21 階段 Trila + TROP2 ADC 第 2 階段 1.PD-L1 陽性腫瘤的新輔助TNBC患者得到了概念驗證(鑑於該亞羣中令人鼓舞的聚合酶鏈反應數據)2。2 期研究者贊助的研究由 Atrium Health Levine 癌症研究所進行當前正在進行的研究 Trila + Gem/Carbo 第 2 期 Trila + Gem/Carbo 第 3 期 Trila + TROP2 ADC(基於安全數據)
26. 在獲得療效數據之前,故意不向美國和中國境外提交申報 TNBC數據有望在其他地區實現報銷 Ph3 成功發佈後規劃夥伴關係討論通過合作伙伴關係追求全球機遇預計成功的 1L TNBC 數據將成為全球擴張計劃的催化劑

27 通過現金流有效管理資本到2025年預計現金流將加強資產負債表提高財務靈活性減少運營開支——減少員工人數/確定儲蓄——2023年開支比2022年減少30%——通過出售大中華區特許權使用費獲得淨收益2,700萬美元1-與中國TNBC的保密協議申請/批准相關的潛在資金2,800萬美元2——將現有未償債務從7500萬美元減少至5000萬美元——經修訂的貸款協議至緩解更嚴格的現金契約3 已採取的關鍵資本分配行動在 2023 年 1.從中國合作伙伴(Simcere)獲得2700萬美元扣除地方預扣税後的淨收益,以換取他們未來在大中華區銷售的特許權使用費減免。2.在中國申請保密協議和批准TNBC的曲拉西利布適應證之前,有可能從先聲醫療獲得額外的1800萬美元里程碑獎勵。3.修訂了與Hercules Capital的現有貸款協議,降低了最低現金契約並取消了現有的收入協議(以換取有條件的借款基準限額),年底增加了靈活性,現金、現金等價物和有價證券約為8200萬美元
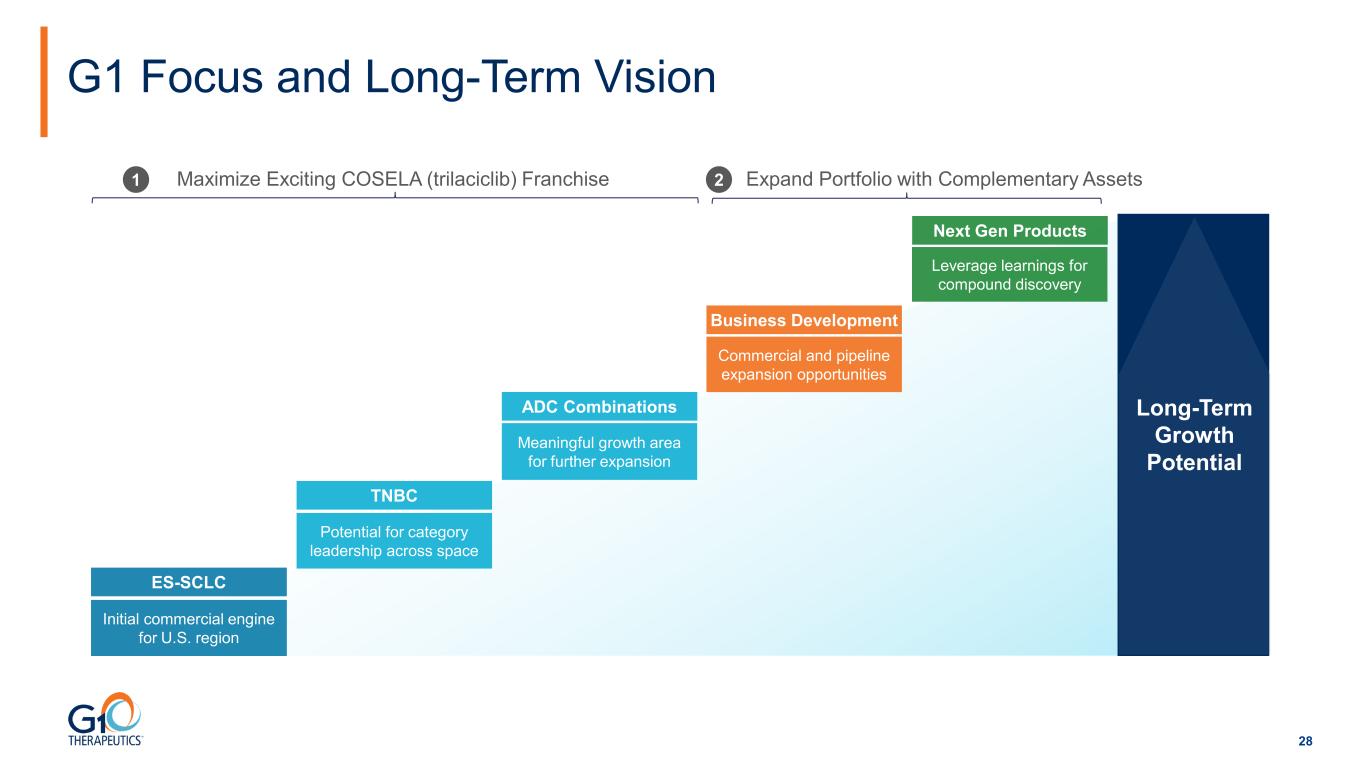
28 長期增長潛力 G1 重點和長期願景美國地區的初始商業引擎跨領域類別領先地位的潛在增長領域進一步擴張的有意義的增長領域下一代產品商業和管道擴張機會最大化令人興奮的 COSELA (trilaciclib) 特許經營權利用互補資產擴大投資組合1 2 ES-SCLC TNBC ADC 組合業務開發利用經驗進行化合物發現
29 附錄

2023年近期的30場演講重點介紹Trilaciclib醫學會議演講的好處增強了Trilaciclib的巨大潛力美國臨牀腫瘤學會(ASCO)• 減少與ADC相關的不良事件 • 免疫介導的MOA保護免疫系統免受ADC損傷歐洲腫瘤內科學會(ESMO)• MOA可能會改善免疫監測聖安東尼奧乳腺癌研討會(SABCS)• 重點介紹曲拉西利布 MOA 的臨牀影響 • 接受曲拉西利布的患者 + 在隨後的抗癌經歷之前進行化療可以提高存活率與單獨使用化療相比 ASCO 質量護理研討會 (ASCO QC) • 提高小細胞肺癌患者的存活率 (HR 0.63) • 嚴重骨髓抑制的機率降低了超過 70% • 住院率降低了國際藥物經濟學與結果研究學會 (ISPOR) • 小細胞肺癌患者化療後骨髓抑制的風險持續存在
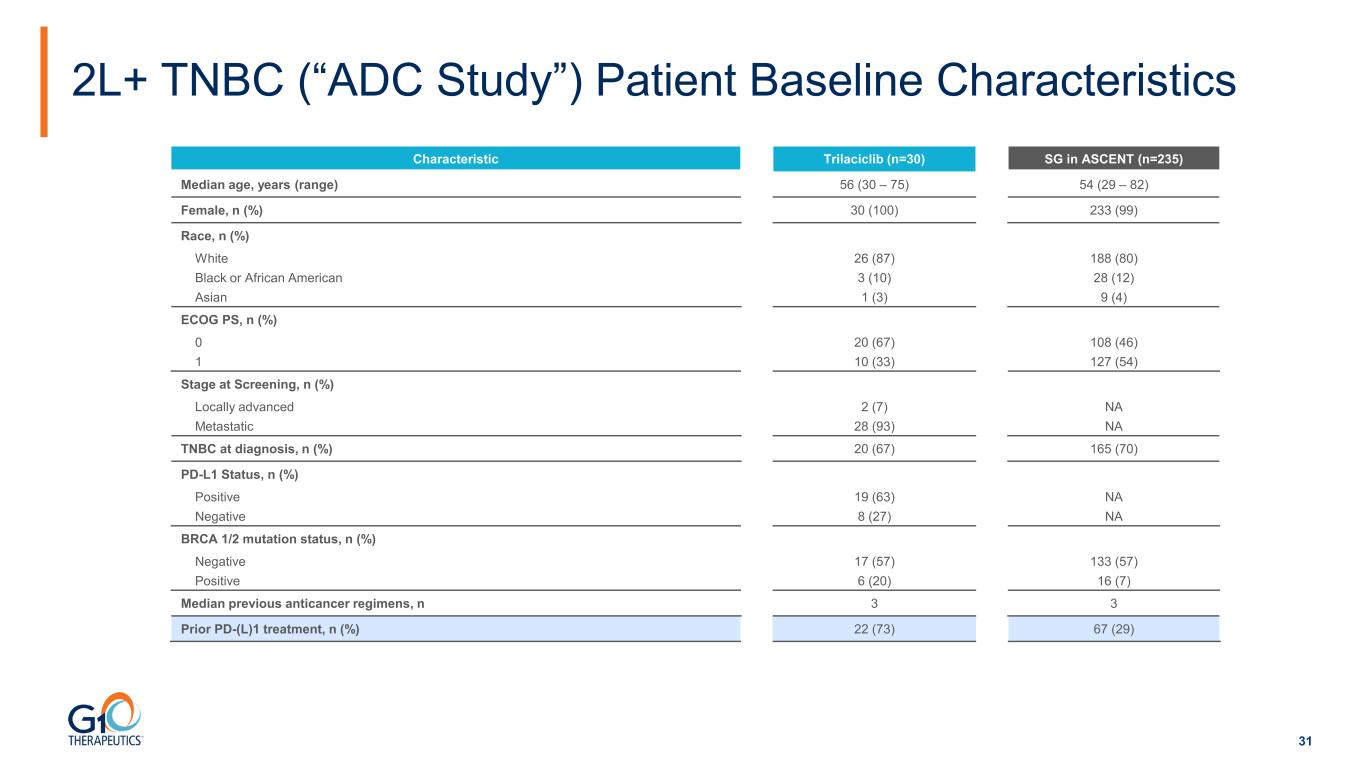
31 2L+ TNBC(“ADC 研究”)患者基線特徵 Trilaciclib(n=30)ASCENT 中的 SG(n=235)中位年齡、年齡(範圍)56(30 — 75)54(29 — 82)女性,n(%)30(100)233(99)種族,n(%)白人 26(87)188(80)黑人或非裔美國人 3(10)28(12)亞裔 1 (3) 9 (4) ECOG PS,n (%) 0 20 (67) 108 (46) 1 10 (33) 127 (54) 篩查階段,n (%) 局部晚期 2 (7) NA 轉移 28 (93) 診斷時的 NA TNBC,n (%) 20 (67) 165 (70) PD-L1 狀態,n (%) 陽性 19 (63) NA 陰性 8 (27) NA BRCA 1/2 突變狀態,n (%) 陰性 17 (57)133 (57) 陽性 6 (20) 16 (7) 先前的抗癌方案中位數,n 3 3 之前的 PD-(L) 1 次治療,n (%) 22 (73) 67 (29)