
附錄 99.2

將我們的使命變為現實摩根大通首席執行官凱特·哈維蘭德醫療會議2024年1月8日艾德里安·克林頓患有系統性肥大細胞增多症的患者

前瞻性陳述本演示文稿包含經修訂的1995年《私人證券訴訟改革法》所指的前瞻性陳述,包括但不限於關於公司未來業務增長的計劃、戰略、時間表和預期的聲明,包括其2024年的增長戰略;AYVAKIT在SM抓住重磅市場機會的潛力;BLU-808是否有藥丸潛力;是否有該公司的產品候選人將講述的未滿足的醫療需求;2024年公司現金消耗的減少;有關公司當前或未來批准的藥物和候選藥物的計劃和預期的聲明;公司當前或未來批准的任何藥物或候選藥物在治療患者方面的潛在益處;以及公司的財務業績、戰略、目標和預期里程碑、業務計劃和重點。“目標”、“可能”、“將”、“可以”、“應該”、“計劃”、“預測”、“打算”、“相信”、“估計”、“預測”、“項目”、“潛力”、“繼續”、“目標” 等類似表述旨在識別前瞻性陳述,儘管並非所有前瞻性陳述都包含這些識別詞。本演示文稿中的任何前瞻性陳述均基於管理層當前的預期和信念,受許多風險、不確定性和重要因素的影響,這些風險和不確定性可能導致實際事件或結果與本演示文稿中任何前瞻性陳述所表達或暗示的重大差異,包括但不限於公司繼續擴大商業基礎設施、成功推出、營銷和銷售當前或未來批准產品的能力和計劃;公司的能夠成功擴大AYVAKIT/AYVAKYT的批准適應症或將來在其他地區獲得AYVAKIT/AYVAKYT的上市許可;推遲任何當前或計劃中的臨牀試驗或公司當前或未來的候選藥物的開發;公司推進多項早期階段工作;公司成功證明其候選藥物的安全性和有效性並獲得候選藥物批准的能力及時提供依據(如果有的話);臨牀前和臨牀結果公司的候選藥物,可能不支持單一療法或與其他藥物聯合使用等候選藥物的進一步開發,也可能影響數據或監管機構提交的預期時間;在臨牀試驗場所啟動臨牀試驗和試驗羣組的時間以及患者入組率;監管機構的行動,可能影響臨牀試驗的啟動、時間和進展;公司獲得、維持和執行專利和其他知識產權保護的能力適用於 AYVAKIT/AYVAKYT或其正在開發的任何候選藥物;公司為AYVAKIT/AYVAKYT或其當前和未來的任何候選藥物開發和商業化伴隨診斷測試的能力;公司成功擴大其業務、研究平臺和候選藥物組合及其時機和成本的能力;以及公司當前和未來合作、融資安排、合作伙伴關係或許可安排的成功;以及風險和相關不確定性考慮到COVID-19大流行對世界的影響公司的業務、運營、戰略、目標和預期里程碑,包括公司正在進行和計劃中的研究和發現活動、進行正在進行和計劃中的臨牀試驗的能力、當前或未來候選藥物的臨牀供應、當前或未來批准產品的商業供應,以及當前或未來批准產品的上市、營銷和銷售。公司向美國證券交易委員會(SEC)提交的文件中標題為 “風險因素” 的部分對這些風險和不確定性進行了更詳細的描述,包括該公司最新的10-K表年度報告,並輔之以其最新的10-Q表季度報告以及該公司已經或將來可能向美國證券交易委員會提交的任何其他文件。本演示文稿中的前瞻性陳述僅在發佈之日作出,除非法律要求,否則公司沒有義務根據新信息、未來事件或其他原因更新本演示文稿中包含的任何前瞻性陳述。因此,提醒讀者不要過分依賴這些前瞻性陳述。本演示文稿還包含獨立各方和公司就市場規模和增長做出的估計、預測和其他統計數據,以及有關公司行業的其他數據。這些數據涉及許多假設和侷限性,提醒您不要過分重視此類估計。此外,對公司未來業績的預測、假設和估計以及公司經營所在市場的未來表現必然受到高度的不確定性和風險的影響。Blueprint Medicines、AYVAKIT、AYVAKYT 和相關徽標是藍圖藥品公司的商標。2

Blueprint Medicines 的加速增長概況 3 在SM中樹立領導地位加速增長孵化創新通過專有研究平臺有機建立廣泛的產品組合在美國和歐盟批准和推出AdvSM和ISM的AYVAKIT®(阿伐替尼)重磅機遇,專注於引人入勝的增長機會以及盈利之路 2011 — 2021 — 2023 — 2024 — FUTURE Avritapinib 獲得批准,商品名為 AYVAKYT® 在歐洲。advSM,晚期系統性肥大細胞增多症;ISM,惰性系統性肥大細胞增多症;SM,系統性肥大細胞增多症一家完全整合、商業化的全球生物製藥公司,增長速度加快

在 2024 年及以後實現業務增長 4 項成就 2024 年增長戰略在 ISM 中啟動 AYVAKIT 交付了四個第一階段臨牀數據集為未來投資提供信息提名的 3 個發展中國家,包括口服野生型 KIT 抑制劑 BLU-808 運營費用持續下降隨着AYVAKIT在SM的推出實現收入大幅增長專注於具有重要價值驅動力的引人注目的增長機會持久的資本狀況可以獨立於資本市場 DC,開發候選者

2024年的三個關鍵增長驅動力 5 過敏/免疫學腫瘤學/血液學投資可持續創新保持財務實力強勁穩定的全球上市在未來十年實現增長抓住重大機遇

AYVAKIT 擁有獨特的多維價值主張 6 重磅市場機遇引人注目的臨牀概況多種增長機會積極的接受能力推動需求

AYVAKIT 在 SM 7 中抓住了重大的機會 $28.6 $30.1 $39.9 $39.9 54.2 2023年第一季度第二季度2023年第二季度AYVAKIT 淨產品收入(百萬美元)+36% 2023年5月22日:美國食品藥品管理局批准ISM的人羣明顯增加,有可能接受長期治療的高利潤率特種藥物具有可操作的治療潛在驅動因素的療法由於長期的知識產權保護、知識產權、知識產權,預計未來十年將持續增長

AYVAKIT 提供持久的症狀控制和耐受性良好的每日一次藥丸 8 廣泛而持久的療效改善涵蓋廣泛的皮膚、胃腸道、神經認知和其他症狀安全配置支持在 PIONEER 1 中長達 4 年以上的慢性治療治療;長期安全數據將於 2024 年公佈劑量範圍多劑量滿足各種 SM 患者的醫療需求 1.藍圖藥品數據存檔。截至2023年11月,PIONEER(n = 251)的平均治療時間為25.1個月(運行年齡:0.2-52.9個月)。8

強勁的資金比率和執行廣度推動了短期增長軌跡 9 1.藍圖藥品數據存檔。百分比基於SP/HUB頻道中可見的2023年第三季度新增SM患者開診情況,該頻道反映了AYVAKIT的大部分交易量。不同提供商類型和渠道的廣泛需求量受新開處方者與現有處方者的驅動量約60/ 40% 學術與社區賬户推動的交易量 ~50/ 50% 商業和醫療執行推動知名度與推出之前相比 AYVAKIT 意識的增長 3.5X 患者可能會向醫生詢問 AYVAKIT ~ 65% SM 出版物 70+ 教育演講者項目 230 多個區域 SM 會議 300+ 易於獲取從處方到發貨的轉化率 ~ 95% 可填充大多數患者 95%

隨着SM市場的增長,有很大的上行空間 10 • 擴大醫療保健提供商對AYVAKIT(符合條件的患者)的視角,使其與我們的廣泛標籤保持一致 • 通過更有效的診斷建立市場 •進入美國以外的新市場美國約9,500例確診和不受控制的ISM 1 ~32,000例美國SM患病率2>同比增長約21,000例 1 1.藍圖藥品數據存檔,基於美國索賠數據中獨特患者的可見性。2.Cohen 等人 2014 年。

抓住重磅機遇 2024年的三個關鍵增長動力 11 過敏/免疫學腫瘤學/血液學投資可持續創新保持財務實力重點投資推動長期增長

BLU-222 CDK2 正在進行的合作討論 BLU-956(下一代)CDK2 靶向蛋白降解劑 CDK2 全球靶向蛋白降解劑未公開的 AYVAKIT®(阿伐替尼)1 試劑盒 D816V 全球不包括大中華區 4 埃萊尼斯替尼(下一代)試劑盒 D816V Global BLU-808 野生型試劑盒其他未公開的肥大細胞靶標/模式在兩個重點和令人興奮的科學領域建立規模 12 Inn Dolent SM 2 Advanced SM 3 Indolent SM 慢性蕁麻疹 HR+/HER2-乳腺癌其他 CDK2 脆弱癌症 HR+/HER2-乳腺癌項目 TARGET DISCOVERY臨牀商業權利 HR+/HER2-乳腺癌肥大細胞疾病過敏/炎症重點:實體瘤腫瘤腫瘤學重點:1.美國還批准用於攜帶 PDGFRA 外顯子 18 突變的不可切除或轉移性 GIST 的成年人,包括 P DGF RA D842V 突變。歐洲(AYVAKYT®)獲批准,用於攜帶 PDGFRA D842V 突變的不可切除或轉移性 GIST 的成年人。2.在美國獲準用於患有惰性 SM 的成年人。在歐洲(AYVAKYT)獲批,用於對症治療無法充分控制的惰性 SM 的成年人,其發生率為中等至嚴重症狀。在美國獲準用於晚期SM(包括侵襲性SM(ASM)、伴有相關血液學腫瘤(SM-AHN)的SM和肥大細胞白血病(MCL)的成年人。在歐洲(AYV AKYT®)獲得批准,適用於至少經過一次全身治療後患有 ASM、SM-AHN 或 MCL 的成年人。4.基石製藥擁有在大中華區開發和商業化阿伐替尼的獨家權利。更新於 2024 年 1 月 8 日。其他項目未公開全球

肥大細胞是一系列炎症性疾病生物學的核心驅動力 13 • KIT-介導的信號傳導在肥大細胞的存活、增殖和激活中起着核心作用 • 當脱顆粒發生時,炎症分子的釋放會產生廣泛的生理影響 KIT 是一種經臨牀驗證的肥大細胞靶向前列腺素 KIT 組胺細胞因子胰蛋白酶脱顆粒 MCAS、肥大細胞激活綜合徵;GI,胃腸道

Elenestinib,一種正在研究的下一代強效選擇性 KIT D816V 抑制劑 14 — 22.2 — 28.5 — 31.8 — 33.6 — 40.0 — 35.0 — 30.0 — 25.0 — 20.0 — 15.0 — 10.0 — 5.0 0.0 0.0 安慰劑(n=10)埃萊內斯替尼 25 mg QD(n=10)Elenestinib 50 mg QD(n =10)Elenestinib 50 mg QD(n =10)Elenestinib 50 mg QD(n = 10)Elenestinib 100 mg QD(n=8)與基線相比的平均變化百分比依來替尼在ISM中的降低-SAF總症狀評分為1。Tashi T. 等人在 ASH 2023 上展出。耐受性良好,沒有因不良反應而中斷治療;經驗證的ISM-SAF評估的大多數AE的1/2級改善疾病相關症狀減少了肥大細胞負擔的多種生物標誌物在不同劑量下觀察到穩健的臨牀活性和良好的耐受性 HARBOR 第 1 部分試驗結果在 ASH 2023 1 上公佈:

野生型 KIT 抑制劑 BLU-808 在藥丸中處於首位、也是同類最佳的管道中,計劃於 2024 年第二季度提交 15 款車輛 IND 屬性理想候選藥物 BLU-808 PKit /增殖 IC 50 50x/> 50x >300/>9600 激酶選擇性;S (10)

通過口服療法靶向試劑盒以滿足大量未得到滿足的醫療需求 16 蕁麻疹或蕁麻疹的典型表現,這是慢性蕁麻疹的常見症狀 1 由肥大細胞驅動的疾病生物學靶向驗證 WTKit 抑制已為慢性蕁麻疹方法建立了臨牀概念驗證小分子 TKI;有機會通過口服療法推動市場擴張由於瘙癢、蕁麻疹、腫脹和相關焦慮導致的重大疾病負擔和生活質量影響,睡眠不足美國和歐盟4國約有68萬名患者對口服治療的需求未得到滿足核心生物學機會 TKI,酪氨酸激酶抑制劑;QoL,生活質量;EU4 包括法國、德國、意大利、西班牙 1。抗組胺耐藥物,聲稱——在美國和歐盟4國已確定患有CU的患者

BLU-222 CDK2 正在進行的合作討論 BLU-956(下一代)CDK2 靶向蛋白降解劑 CDK2 全球靶向蛋白降解劑未公開的 AYVAKIT®(阿伐替尼)1 試劑盒 D816V 全球不包括大中華區 4 埃萊尼斯替尼(下一代)試劑盒 D816V Global BLU-808 野生型試劑盒其他未公開的肥大細胞靶標/模式在兩個重點和令人興奮的科學領域建立規模 17 Dolent SM 2 Advanced SM 3 Indolent SM 慢性蕁麻疹 HR+/HER2-乳腺癌其他 CDK2 脆弱癌症 HR+/HER2-乳腺癌項目 TARGET DISCOVERY臨牀商業權利 HR+/HER2-乳腺癌肥大細胞疾病過敏/炎症重點:實體瘤腫瘤腫瘤學重點:1.美國還批准用於攜帶 PDGFRA 外顯子 18 突變的不可切除或轉移性 GIST 的成年人,包括 P DGF RA D842V 突變。歐洲(AYVAKYT®)獲批准,用於攜帶 PDGFRA D842V 突變的不可切除或轉移性 GIST 的成年人。2.在美國獲準用於患有惰性 SM 的成年人。在歐洲(AYVAKYT)獲批,用於對症治療無法充分控制的惰性 SM 的成年人,其發生率為中等至嚴重症狀。在美國獲準用於晚期SM(包括侵襲性SM(ASM)、伴有相關血液學腫瘤(SM-AHN)的SM和肥大細胞白血病(MCL)的成年人。在歐洲(AYV AKYT®)獲得批准,適用於至少經過一次全身治療後患有 ASM、SM-AHN 或 MCL 的成年人。4.基石製藥擁有在大中華區開發和商業化阿伐替尼的獨家權利。更新於 2024 年 1 月 8 日。其他項目未公開全球

藉助BLU-222,我們解決了CDK2抑制的選擇性挑戰 18 CDK2是經過臨牀驗證的細胞週期靶標大型市場仍有大量未得到滿足的需求的全面計劃將2023年用於HR+/HER2乳腺癌的CDK4/6抑制劑的全球銷售價值提高和解決CDK4/6耐藥性作為聯合療法的支柱高度選擇性方法最大限度地減少靶向毒性,使聯合合作伙伴成為首選的藥物下一頁-實現長期價值最大化的發電資產 CDK、細胞週期蛋白依賴激酶;HR+,激素受體陽性;HER2-,人類表皮生長因子受體 2 陰性;SOC,標準護理標準選擇性 CDK2 抑制歷來難以實現

BLU-222 有可能成為首款也是最佳的 CDK2 同類選擇性抑制劑 19 BLU-222 1 PF-4091 2 臨牀前概況選擇性評分/SI (10) 0.045 0.127 CDK2 效力/CDK2 酶 IC 50 (nM) 2.6 7.2 1 期單一療法劑量遞增數據患者 27 名患者 35 名患者劑量範圍 50 mg — 800 mg BID(MTD 未確定)75 mg — 500 mg BID(MTD:300 mg BID)PK(平均有效半衰期)~12 小時 ~2-3 小時治療緊急不良事件 (TEAE) 無 Gr5;1 Gr4(低鉀血癥;無關)1 Gr5(無關);1 Gr4(中性粒細胞減少)血液學 TEAE s ALL GR3 GR4 ALL GR3 GR4 • 貧血 29.6% 3.7% 45.7% 8.6% • 中性粒細胞減少症 3.7% 28.6% 14.3% 2.9% • 血小板減少症 3.7% 3.7% 20.0% 2.9% 1.Patel、M.R. 等人、ASCO 2023 和存檔的藍圖數據。數據已於 2023 年 4 月 25 日發佈。2.是的,T.A. 等人,ASCO 2023

抓住重大的機遇 f 2024 年的三大增長驅動力 20 過敏/免疫學腫瘤學/血液學投資可持續創新保持財務實力持久的資本狀況有明確的盈利路徑

21 美元 53 美元 111 美元 2020 年 2021 年 2022 2023 2024 2026 2026 2027+ AYVAKIT 正在抓住一個重大的機會 SM AYVAKIT 將在 2023 財年第四季度財報電話會議上提供 2023 財年財務狀況和 2024 年 AYVAKIT 產品收入指導。估計超過15億美元的全球小企業峯值收入21 AYVAKIT年度淨產品收入(百萬美元)數字以圖形形式提供,不作為財務指導。
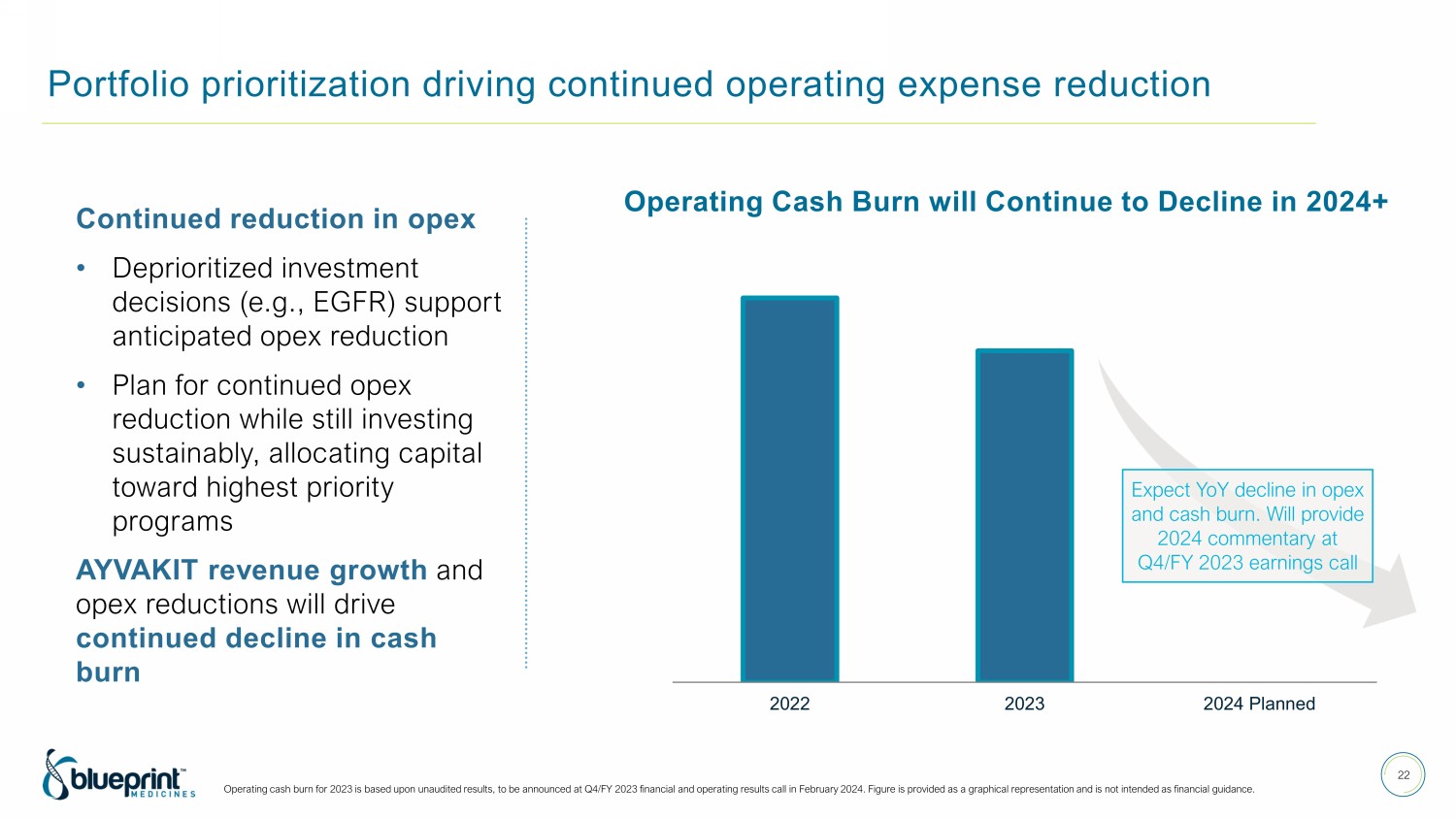
投資組合優先順序推動運營支出持續減少 22 運營支出持續減少 • 非優先級投資決策(例如EGFR)支持預期的運營支出減少 • 計劃在持續投資的同時繼續減少運營支出,將資本分配給最優先項目 AYVAKIT 收入增長和運營支出的減少將推動現金消耗的持續下降 2024 年以上的運營現金消耗將繼續下降 2023 年的運營現金消耗基於未經審計的業績,將在上公佈 2023 財年第四季度財務和運營結果全部在 2024 年 2 月。該數字以圖形形式提供,不作為財務指導。2022-2023年計劃預計運營支出和現金消耗同比下降。將在 2023 財年第四季度財報電話會議上提供 2024 年評論

2024 年的主要預期產品組合里程碑 23 個區域項目里程碑計時肥大細胞疾病 AYVAKIT 目前在 ISM 1H 2024 年 BLU-808 IND 提交的長期安全性和有效性數據 Elenestinib 啟動註冊——啟用 2024 年下半年的 HARBOR 試驗第 2 部分實體瘤 BLU-222 與 ribociclib 和 fulvestrant 聯合用於 HR+/HER2 的數據-乳腺癌 2024 年上半年提供HR+/HER2-2024年下半年乳腺癌註冊計劃的最新情況除AYVAKIT收入增長外,Blueprint預計還會出現以下情況2024 年與數據相關的里程碑:

藍圖有望在2024年及以後加速我們的業務增長。AYVAKIT正在SM中抓住一個重大的機遇。SM 中的 AYVAKIT 是當今發佈的最激動人心的罕見疾病之一。利用我們的專業知識,重點投資增長機會。在我們對核心生物學和業務戰略的深刻理解的基礎上,追求令人興奮的科學領域,通過槓桿和規模推動增長。走上盈利之路。通過增加收入和有針對性的支出計劃,我們保持了持久的資本狀況,同時還投資於長期增長的機會。

BLU-222 CDK2 正在進行的合作討論 BLU-956(下一代)CDK2 靶向蛋白降解劑 CDK2 全球靶向蛋白降解劑未公開的 AYVAKIT®(阿伐替尼)1 試劑盒 D816V 全球不包括大中華區 4 埃來斯替尼(下一代)試劑盒 D816V Global BLU-808 野生型試劑盒其他未公開的肥大細胞靶標/模式藍圖藥品管線 25 Indolent SM 2 Advanced SM 3 Indolent SM 慢性蕁麻疹 HR+/HER2-乳腺癌其他 CDK2 脆弱癌症 HR+/HER2-乳腺癌項目 TARGET DISCOVERY 臨牀商業權利 HR+/HER2-乳腺癌肥大細胞疾病過敏/炎症重點:實體瘤腫瘤學重點:1.美國還批准用於攜帶 PDGFRA 外顯子 18 突變的不可切除或轉移性 GIST 的成年人,包括 P DGF RA D842V 突變。歐洲(AYVAKYT®)獲批准,用於攜帶 PDGFRA D842V 突變的不可切除或轉移性 GIST 的成年人。2.在美國獲準用於患有惰性 SM 的成年人。在歐洲(AYVAKYT)獲批,用於對症治療無法充分控制的惰性 SM 的成年人,其發生率為中等至嚴重症狀。在美國獲準用於晚期SM(包括侵襲性SM(ASM)、伴有相關血液學腫瘤(SM-AHN)的SM和肥大細胞白血病(MCL)的成年人。在歐洲(AYV AKYT®)獲得批准,適用於至少經過一次全身治療後患有 ASM、SM-AHN 或 MCL 的成年人。4.基石製藥擁有在大中華區開發和商業化阿伐替尼的獨家權利。更新於 2024 年 1 月 8 日。其他項目未披露的全球