| 納斯達克:PASG © 2024 Passage Bio。版權所有。 公司介紹 2024 年 1 月 |
| 2 前瞻性陳述 本演示文稿包括根據1995年《私人證券 訴訟改革法》的安全港條款作出的 “前瞻性陳述”,包括但不限於:我們對預期里程碑的時間和執行的預期,包括 臨牀試驗的進展和此類試驗的臨牀數據的可用性;我們對合作者和合作夥伴執行關鍵舉措能力的期望;我們的 } 對製造計劃的期望和策略;我們對現金跑道的期望;我們對與 PBGM01、PBKR03 和 PBML04 相關的潛在合作伙伴關係的期望,以及我們的主要候選產品治療各自靶向單基因中樞神經系統疾病的能力的預期。這些前瞻性陳述可能伴隨着諸如 “目標”、“預測”、“相信”、“可能”、“估計”、“預期”、“預測”、“目標”、“打算”、“可能”、“可能”、“計劃”、“潛在”、“可能”、“將” 等詞語以及其他具有類似含義的詞語和術語。這些陳述涉及風險和不確定性, 可能導致實際結果與此類陳述中反映的結果存在重大差異,包括:我們開發 候選產品並獲得監管部門批准的能力;臨牀前研究和臨牀試驗的時間和結果;與臨牀試驗相關的風險,包括我們充分 管理臨牀活動的能力、臨牀試驗期間獲得的其他數據或分析可能產生的意外問題,監管機構可能需要 額外信息或進一步研究,或可能無法批准或可能延遲批准我們的候選藥物;不良安全 事件的發生;臨牀前研究或臨牀試驗的陽性結果可能無法在後續試驗中複製或在早期臨牀試驗中取得成功的風險 可能無法預測後期臨牀試驗的結果;未能保護和執行我們的知識產權和其他專有權利;我們對合作者和其他所有權的依賴 開發和製造產品的第三方候選人和我們 無法完全控制的業務的其他方面;與當前和潛在延誤、停工或供應鏈中斷相關的風險;以及公司不時向美國證券交易委員會 (SEC) 提交的文件中 “風險因素” 部分描述的其他風險和不確定性,以及向美國證券交易委員會 (SEC) 提交的其他 報告。Passage Bio沒有義務公開更新 可能不時發表的任何前瞻性陳述,無論是書面還是口頭陳述,無論是由於新信息、未來發展還是其他原因。 |
| 3 我們的願景 通過提供可永久重新定義 病程的 基因藥物,改善患有神經退行性 疾病的患者的生活。 潛在的同類最佳計劃籌資 FTD-GRN 基因療法計劃 建立了製造和工藝 分析能力 強勁的現金狀況,預計 將投資組合擴展到其他成人 神經退行性疾病 * 基於截至2023年9月30日的現金、現金等價物和有價證券 |
| 4 種有可能解決多種 神經退行性疾病 項目適應症美國/歐盟 患病率發現臨牀前1/2期關鍵 PBFT02 額膜痴呆- GRN 18,0001-3 額瞼痴呆- c9orf72 21,0002-4 肌萎縮側索硬化 72,6005-6 阿爾茨海默氏病伴有 rs5848 SNP 3.9M48 7-8 未命名的亨廷頓氏病 60,0009 PBGM01 GM1 神經節苷脂症 PBKR03 Krabbe 病 PBML04 異色性白質營養不良症 追求潛在的 合作伙伴關係 來源: [1]格里夫斯簡歷等J Neurol 2019;266:2075-2086, [2]Galvin JE 等人。神經病學 2017; 89:2049-2056, [3]Onyike CU 等。2013 年精神病學國際修訂版;25:130-137, [4]Moore KM, 等Lancet Neurol 2020;19:145—156, [5]布朗等Neuroepi 2021;55:342-353, [6]CDC ALS 註冊表板, [7]Sheng J 等基因 2014; 141-145, [8]Alz Assoc. 2023 年阿爾茨海默氏病事實與數據。阿爾茨海默氏痴呆症 2023; 19, [9]克羅威爾等Neuroepi. 2021; 55:361-368 |
| 5 • 一次性療法 • 經久耐用的超生理學腦脊液 PGRN 水平 • 通過非手術注射直接給腦脊液 主要臨牀項目:PBFT02 在 FTD-GRN 中表現出同類最佳潛力 差異化、潛力 最佳產品概況 來自前 3 名接受治療 患者的初始數據 • 治療後 30 天 (n=3) 所有患者的超生理腦脊液 PGRN 水平高於基線 4x-7 倍 (n=3) • 超生理學腦脊液 PGRN 水平 在 治療 (n=1) 後維持長達 6 個月 全球劑量-FTD-GRN 中 PBFT02 的升級研究 |
| 6 Discovery uPenn GTP 研究分析 和矢量 工程 過程/分析 開發 Passage CMC 研發實驗室 成熟的分析 綜合流程 開發 GMP 質量控制能力 強大的監管 CMC 科學專業知識 擴大規模 GMP 製造業 與 Catalent 的長期合作關係 端到端臨牀 供應鏈 通過混合方法領先 CMC 能力 外部 製造 合作伙伴關係和 端到端 供應鏈 關鍵戰略 夥伴關係 內部最先進的 CMC 能力 內部合作伙伴關係 內部維護的關鍵分析和開發能力 |
| PBFT02 額室痴呆 — GRN |
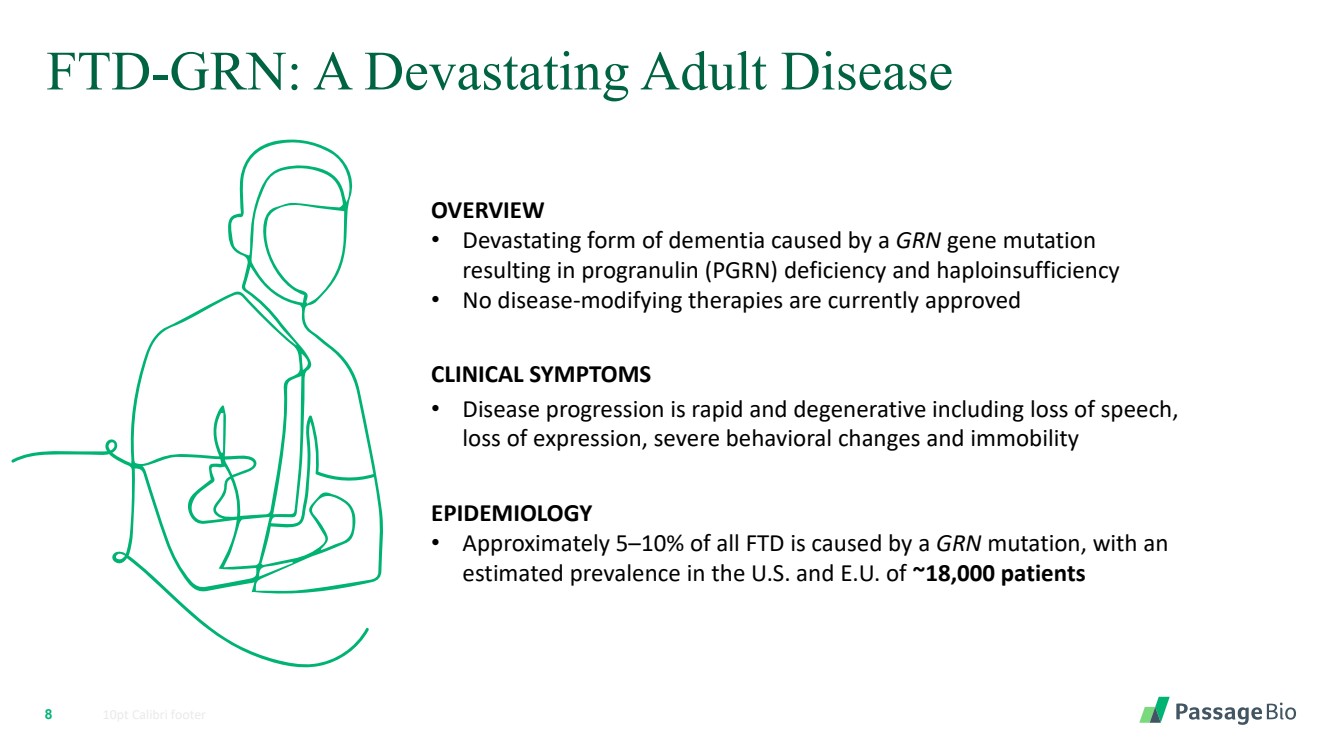
| 8 FTD-GRN:一種毀滅性的成人病 10pt Calibri footer 概述 • 由 GRN 基因突變 引起的毀滅性痴呆 導致前列腺素 (PGRN) 缺乏和單倍功能不全 • 目前沒有批准任何改善疾病的療法 流行病學 • 所有 FTD 中大約 5-10% 由 GRN mun 引起,在美國和歐盟, 估計患病率約為18,000名患者 臨牀症狀 • 疾病進展迅速且具有退行性,包括言語喪失、 表達喪失、嚴重的行為改變以及靜止不動的 |
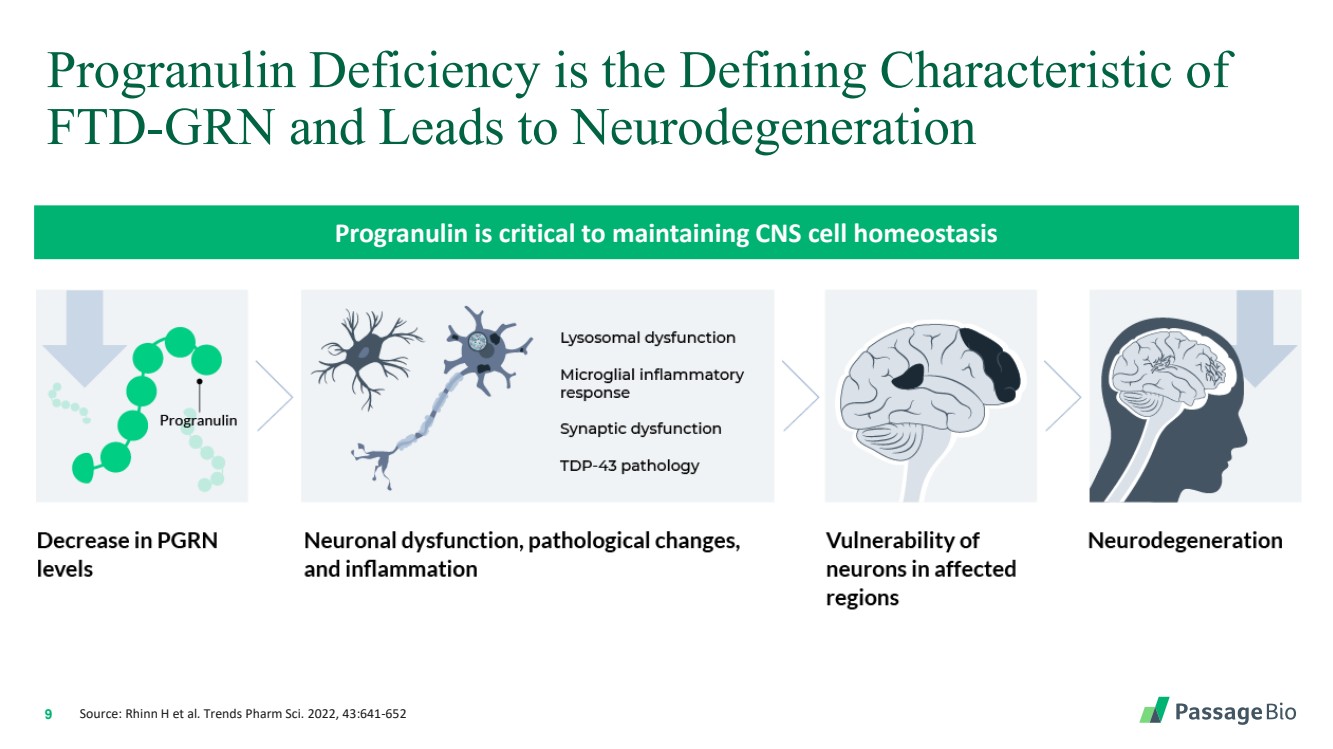
| 9 Progranulin 缺乏是 FTD-GRN 的決定性特徵,會導致神經變性 Progranulin 對維持中樞神經系統細胞動態平衡至關重要 來源:Rhinn H 等人。Trends Pharm Sci.2022,43:641-652 |
| 10 PBFT02 • 專有的 AAV1 結構提供功能性 GRN 基因編碼 progranulin (PGRN) • 一次性療法的潛在治療益處 • 通過單次水箱內注射 (ICM) 直接輸送到腦脊液: — 允許廣泛的中樞神經系統生物分佈 —與靜脈注射相比,劑量更低 —減少中性影響抗體 • 基於 臨牀前和初步臨牀證據,能夠達到腦脊液progranulin的超生理水平 • 獲得美國食品和藥物管理局的孤兒藥和快速通道認定歐共體 認定為孤兒 潛在的變革療法 |
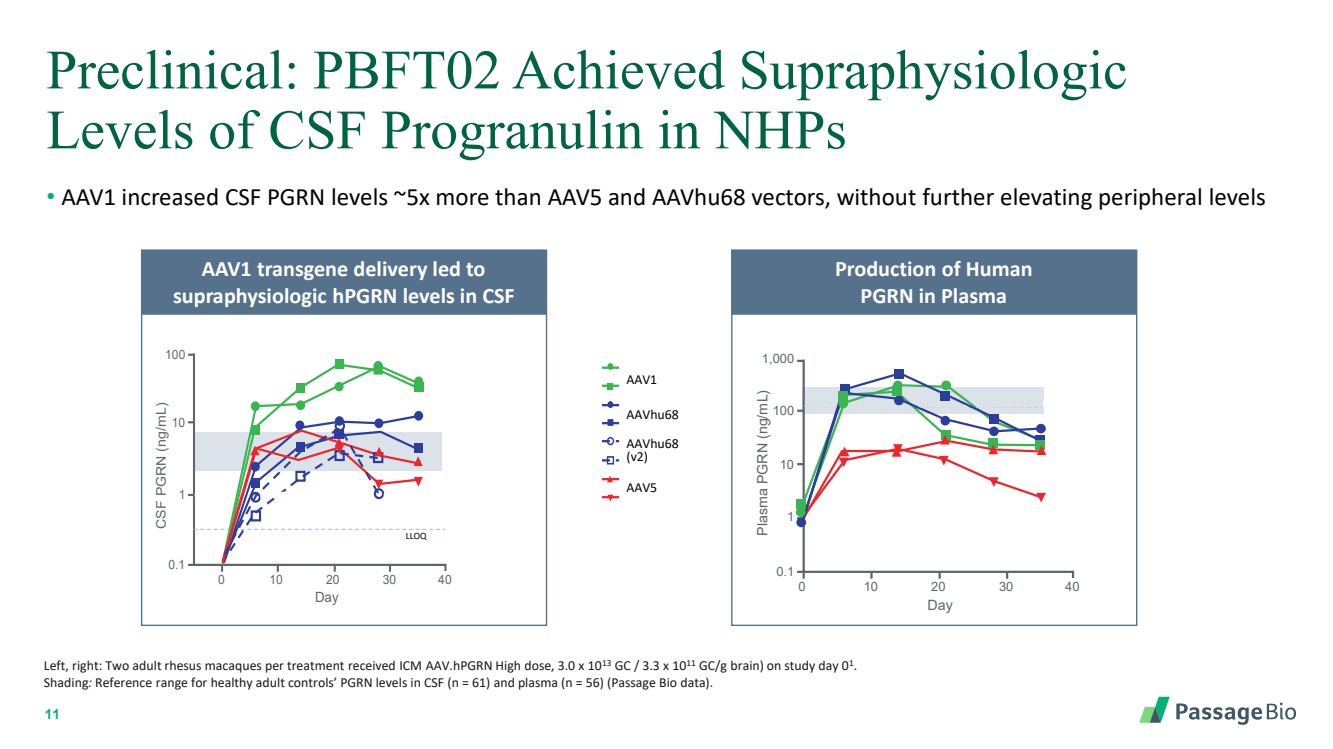
| 11 臨牀前:PBFT02 在 NHP 中達到超生理學 的腦脊液預聚素水平 • AAV1 使腦脊液 PGRN 水平提高了約 5 倍,但沒有進一步升高外周水平 左,右:每次接受治療有兩隻成年恆河猴 ICM AAV.HPGRN 高劑量,3.0 x 1013 GC/3.3 x 1011 gc/g(大腦)(第 01 天)。 陰影:健康成人對照組腦脊液(n = 61)和血漿(n = 56)中的PGRN水平的參考範圍(Passage Bio數據)。 血漿中人類 PGRN 的產生 AAV1 轉基因輸送導致腦脊液 腦脊液 PGRN (ng/mL) 0 10 20 30 40 CSF 0.1 1 10 100 LLOQ 正常 日 RA2981 RA2982 RA3027 RA3153 RA3151 RA3170 RA3155 RA3160 aavHu68 aavHu68 (v2) AAV1 AAV5 RA2981 RA2982 RA3027 RA3153 RA3151 RA3160 RA2981 aavHu68 aavHu68 (v2) AAV1 AAV5 (v2) AAV1 AAV1 AAV5 (v2) RA3151 RA3170 RA3155 RA3155 RA3160 AAVHu68 (v2) AAV1 AavHu68 AAV5 AAV5 AAV5 AAvHu68 (v2) AAV1 AavHu68 AAV5 AAV5 v2) AAV5 AAV1 正常 LLOQ 等離子 血漿 PGRN (ng/mL) 0 10 20 30 40 0.1 RA3170 RA3155 RA2982 RA3027 RA31531 10 100 普通 日 1,000 |
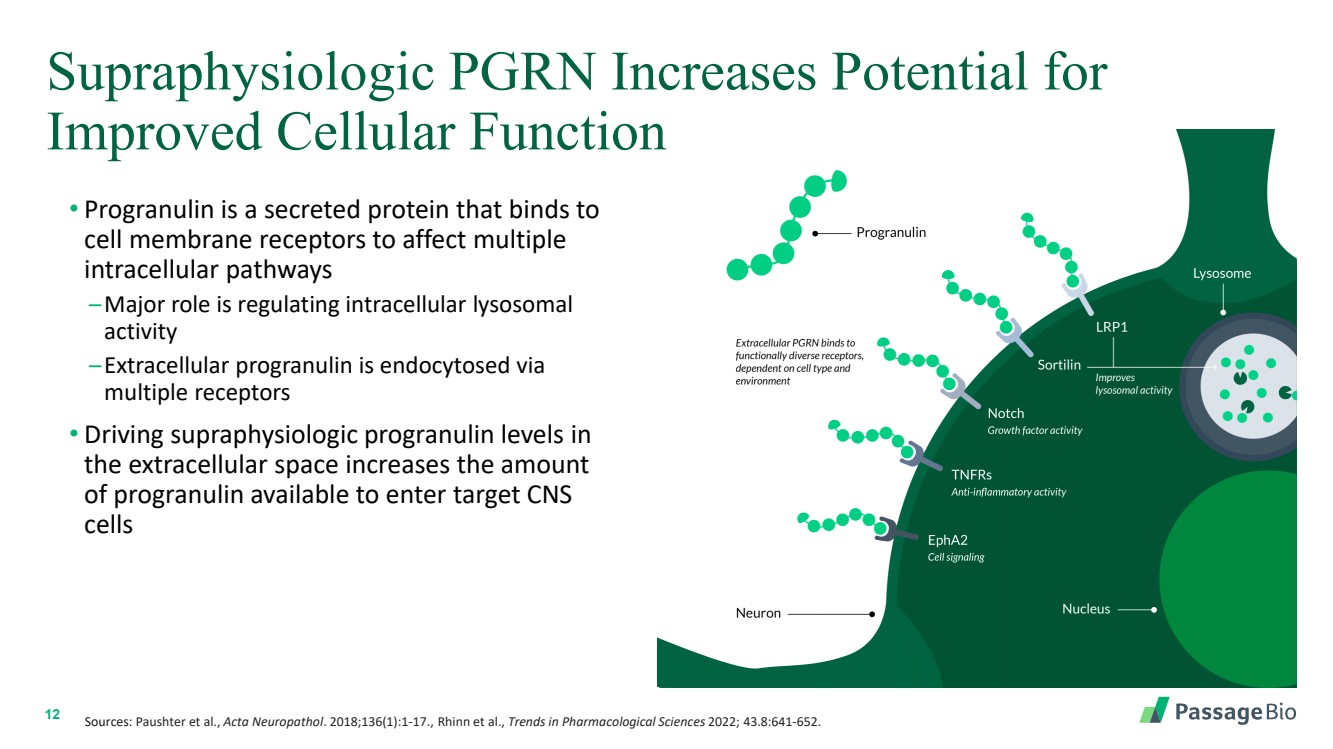
| 12 超生理學 PGRN 增加了 改善細胞功能的可能性 • Progranulin 是一種分泌蛋白,可與 細胞膜受體結合,影響多個 細胞內通路 — 主要作用是調節細胞內溶酶體 活性 — 細胞外程序通過 多重內吞細胞受體 • 推動 細胞外空間的超生理程序蛋白水平會增加 可用於進入靶中樞神經系統 細胞 細胞的程序蛋白量 來源:Paushter 等人,Acta Neuropathol。2018;136 (1): 1-17.,Rhinn等人,《2022年藥理科學趨勢》;43. 8:641-652。 |
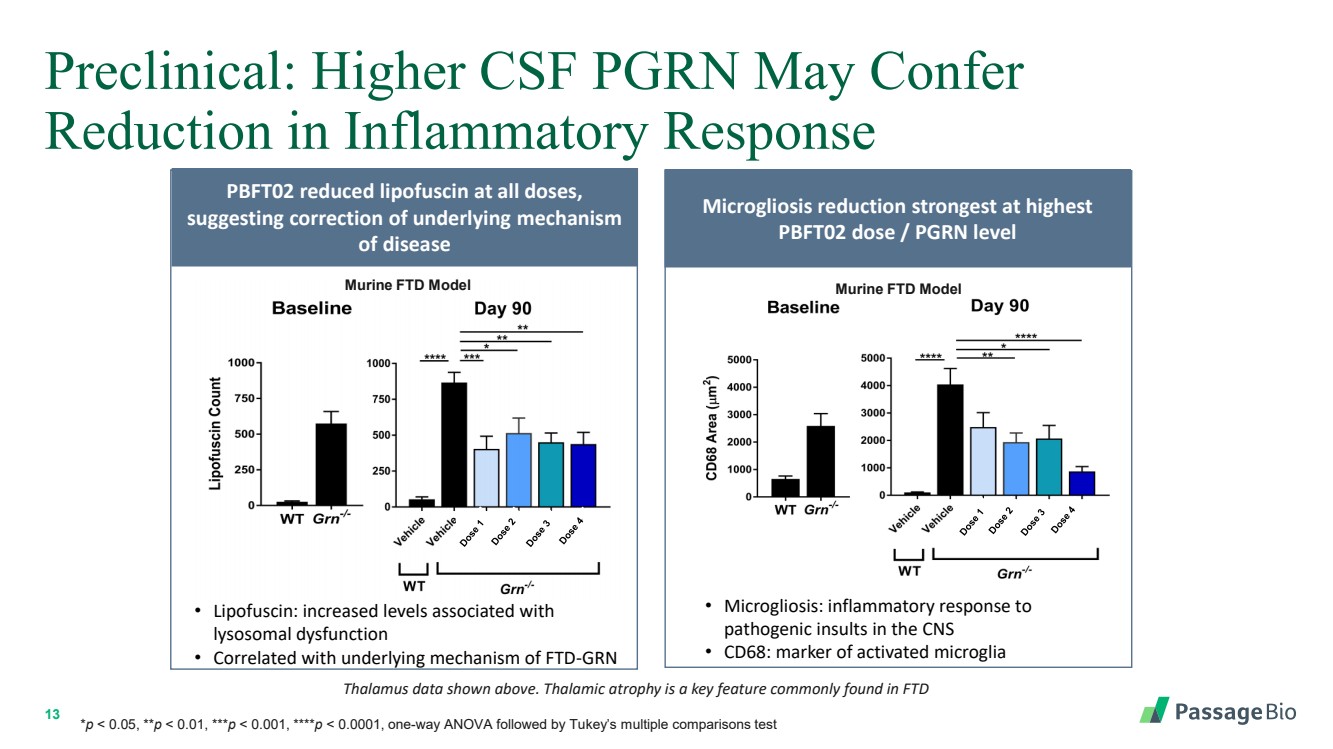
| 13 臨牀前:較高的腦脊液 PGRN 可能使 炎症反應降低 上面顯示的丘腦數據。丘腦萎縮是常見於 FTD PBFT02 降低所有劑量的脂褐素中的一個關鍵特徵, 提示糾正疾病的潛在機制 • 脂褐素:與 溶酶體功能障礙相關的水平升高 • 與 FTD-GRN 的潛在機制相關 *p |
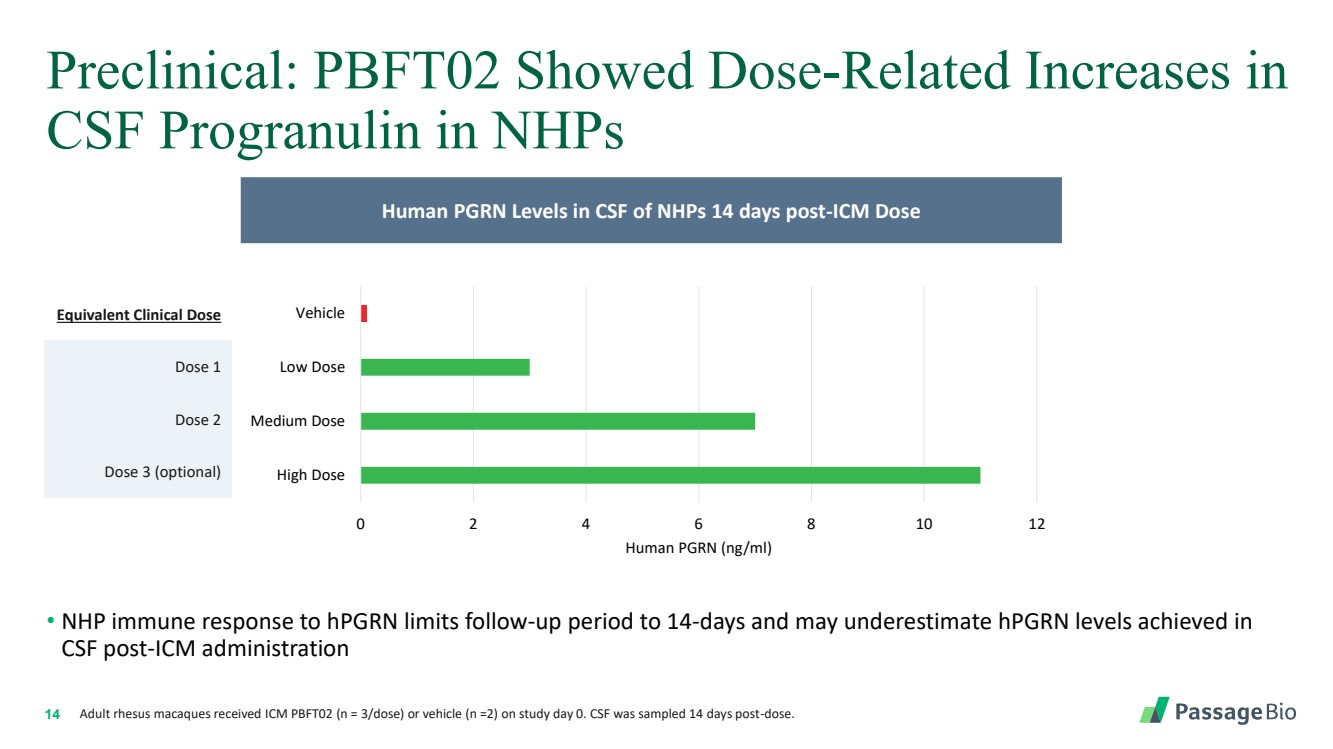
| 14 臨牀前:PBFT02 在研究第 0 天接受了 ICM PBFT02(n = 3 次劑量)或載體(n =2)的 nHP 成年恆河猴中 腦脊液中丙氨酸的劑量相關增加。在給藥 14 天后,對腦脊液進行了採樣。 ICM 劑量 14 天后 NHP 腦脊液中人類 PGRN 水平 0 2 4 6 8 10 12 高劑量 中劑量 低劑量 載體 人類 PGRN (ng/ml) 等效臨牀劑量 劑量 1 劑量 3(可選) • NHP 對 hpGRN 的免疫反應將隨訪期限制為 14 天和可能低估了 CSF 後 ICM 管理中達到的 hpGRN 水平 |
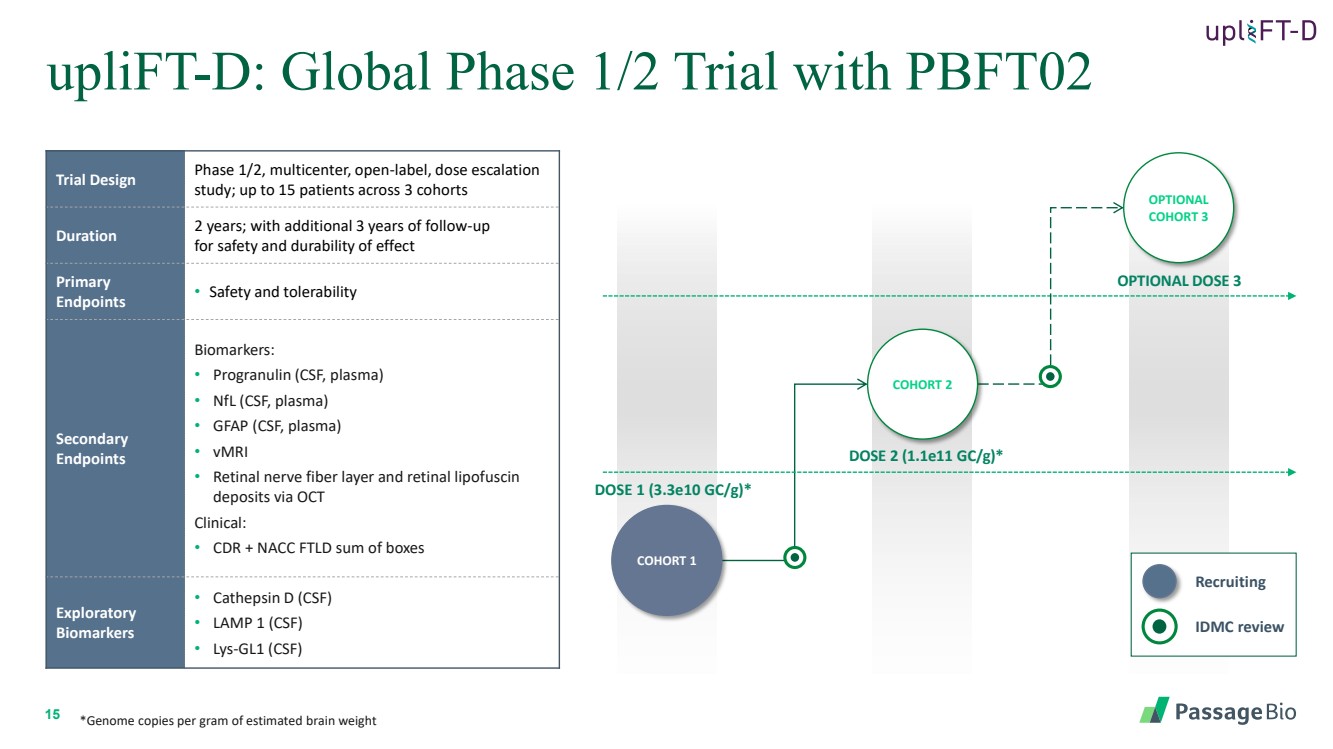
| 15 uplift-D:全球 1/2 期試驗,包括 PBFT02 可選劑量 3 劑量 2 (1.1e11 gc/g) * 劑量 1 (3.3e10 gc/g) * 隊列 1 隊列 2 可選 隊列 3 試驗設計 1/2 期,多中心、開放標籤、劑量遞增 研究;3 個隊列中最多 15 名患者 持續兩年;另加 2 年 3 年隨訪 檢查效果的安全性和耐久性 主要 終點 • 安全性和耐受性 次要 終點 生物標誌物: • Progranulin(腦脊液、血漿) • nFL(腦脊液、血漿) • 視網膜神經纖維層以及通過 OCT 臨牀研究的視網膜脂褐素 沉積物: • CDR + NACC FTLD 盒子總和 探索性 • Catepsin D (CSF) • LAMP 1 (CSF) • lys-gL1 (CSF) *每克估計腦重量的基因組拷貝 IDMC 評論 招聘 |
| 16 uplift-D:來自前 3 名接受治療患者的中期數據 • 患者 1 經歷了兩次與免疫反應一致的 SAE;對 方案進行了修訂,增加了類固醇治療方案 • 患者 2 和患者 3 接受了更高水平的類固醇免疫抑制,且 沒有出現 SAE;僅報告了輕度至中度治療的緊急不良反應 • 沒有證據 DRG 毒性,經測量通過神經傳導研究 • 未觀察到與 ICM 給藥相關的併發症 SAE:嚴重不良事件;AE:不良事件;DRG:背根神經節;ICM:intracisterna magna;NHP:非人類靈長類動物 *截至 2024 年 1 月 3 日數據截止日期,患者隨訪時間介於 2 至 6 個月之間。安全* 療效/目標 • 中期數據顯示,PBFT02 在低劑量 下有可能獲得同類最佳療效。• 在所有患者中,1 劑量達到了超生理學腦脊液 PFS 第 30 天的 GRN 水平:基線 4-7 倍 • 腦脊液 PGRN 水平超過了 NHP 中觀察到的水平 |
| 17 在更新了增加類固醇的協議後,患者 2 和 3 沒有 SAE 或明顯免疫反應的證據 患者 1 患者 2 患者 3 免疫抑制1 天 -1-60:60 mg 口服潑尼鬆第 1-3 天:1,000 mg 靜脈注射甲潑尼鬆 第 4-60 天:60 mg 口服潑尼鬆 LFTs 第 14-21 天和第 51-55 天:升高無症狀與基線 影像學檢查結果與基線沒有顯著變化 無症狀無 DRG 毒性無 ICM 併發症無 ICM 併發症無 隨訪時長 (截至 2024 年 1 月 3 日) 2 個月 (受試者在第 10 周退出研究)6 個月 3 個月 摘要 • 2 個 SAE:均無症狀且 與免疫反應一致 1。肝毒性(用 甲基潑尼鬆龍解決) 2.靜脈竇血栓形成 • 無 SAE • 與基線相比無肝毒性或顯著的 LFT 變化 • 核磁共振成像 無靜脈竇血栓形成或炎症 • 無臨牀顯著免疫反應需要調整 免疫抑制方案 • 所有急診急性輕度至中度 LFT:肝功能試驗;嚴重不良事件 1 天減去一是指給藥的前一天。 2 第 14-21 天 LFT 升高為輕度且可自行解決;第 51-55 天 LFT 升高:ALT 16x 正常上限 (ULN),AST 4x ULN,鹼性 磷酸酶 2x ULN,GGT 10x ULN;總膽紅素正常。在患者撤回研究時使用甲基潑尼鬆龍解決。 |
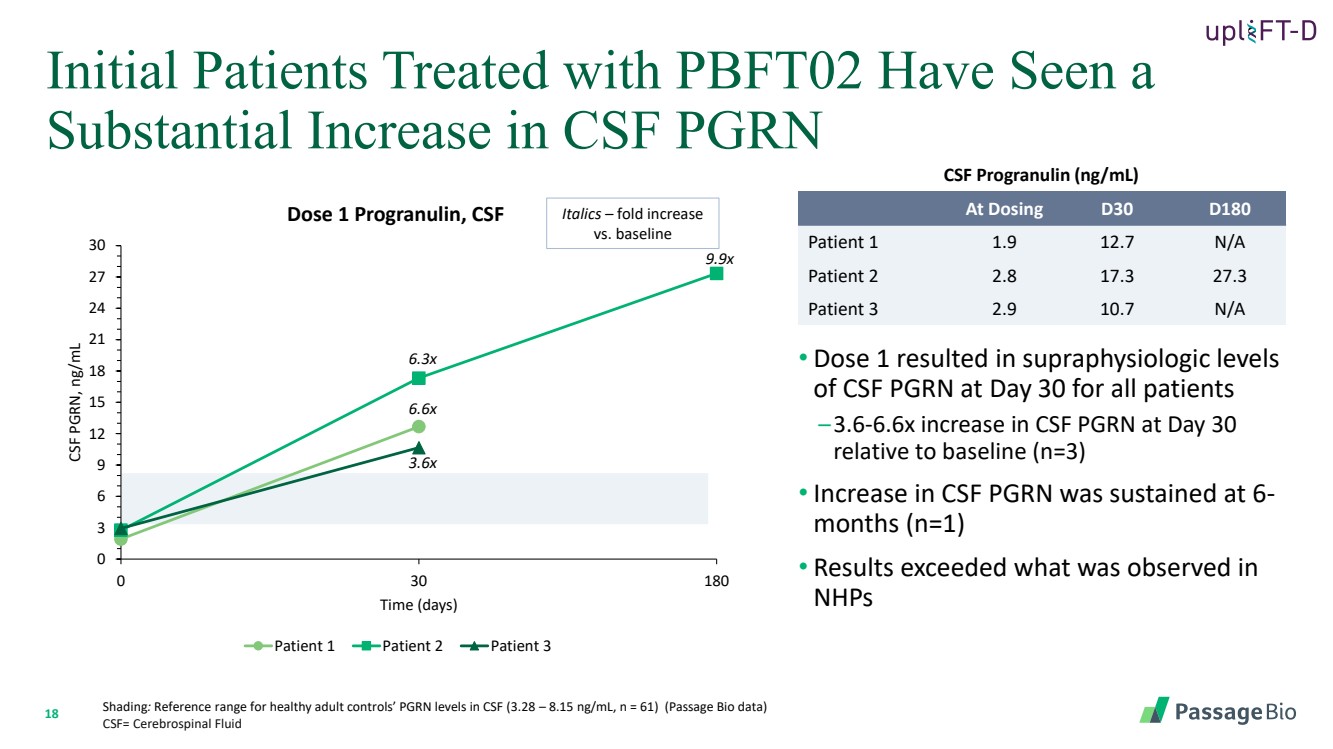
| 18 • 劑量 1 導致所有患者在第 30 天腦脊液 PGRN 的超生理水平 —第 30 天腦脊液 PGRN 相對於基線 (n=3) 增加了 3.6-6.6 倍 • 腦脊液 PGRN 在 6- 個月 (n=1) 時持續升高 • 結果超過 nHP 中觀察到的水平 陰影:健康成人對照組腦脊液中 PGRN 水平的參考範圍(3.28 — 8.15 ng/mL,n = 61)(通道生物數據) CSF= 腦脊液 最初接受 PBFT02 治療的患者的腦脊液 PGRN 0 3 6 9 12 15 18 21 24 27 30 0 30 180 CSF PGRN,nbr} 0 3 6 9 12 15 18 21 24 27 30 0 30 180 CSF PGRN,nGRN g/mL 時間(天) 劑量 1 Progranulin,CSF 患者 1 患者 2 患者 3 在給藥時 D30 D180 患者 1 1.9 12.7 N/A 患者 2 2.8 17.3 27.3 患者 3 2.9 10.7 N/A 6.3x 6.6x 3.6x 斜體 — 摺疊增加 與基線 腦脊液程序輸入 (ng/mL) 9.9x |
| 19 陰影:健康成人對照組血漿中 PGRN 水平參考範圍的下限(91.6 — 372.4 ng/mL,n = 56)(Passage Bio 數據) • 在給藥後長達 6 個月內,血漿 PGRN 水平保持在 正常水平以下 • PGRN 僅在腦脊液中增加,其 有可能糾正與神經變性相關的缺陷 血漿 PGRN 水平仍低於正常水平 劑量後 0 10 20 30 40 50 60 70 80 90 100 0 0 7 14 30 90 180 血漿 PGRN,ng/mL 時間(天) 劑量 1 progranulin,血漿 患者 1 患者 2 患者 3 |
| 20 摘要 AES=不良事件;ICM=intra-cisterna magna * 截至2024年1月3日數據截止日期,患者隨訪時間在給藥後2至6個月不等。 SAFETY* PBFT02 迄今為止,第 1 劑量對患者 2 和 3 的耐受性總體良好,他們在 協議修正後接受了修訂的 類固醇方案 • 所有 AE 的 強度均為輕度至中度 • 沒有證據表明臨牀 有顯著的免疫反應、 肝毒性或靜脈竇 血栓 sis • 沒有證據 DRG 毒性 • 沒有觀察到與 ICM 注射 相關的併發症 生物標誌物 有證據表明 在第 30 天所有參與者中 靶向 參與的腦脊液progranulin 增加 3.6-6.6 倍 治療 • 在 此劑量水平 表現優於 NHP 數據 至第 180 天血漿 PGRN 水平不升高超生理腦脊液 PGRN 水平維持在 6 個月 (n=1) 預期 後續步驟 •在 2024 年上半年開始對隊列 2 患者進行給藥 • 其他 6 個月的數據 來自 2024 年下半年的隊列 1 • 來自 2025 年上半年 1 組患者的 12 個月隨訪數據 •來自 2025 年上半年 第 2 組的初始數據 |
| 展望未來 |
| 22 PBFT02 有可能糾正 FTD-GRN、FTD-c9orf72 和 ALS 中的基礎病理 提升 TDP-43 模型中的 PGRN 結果: • 歸一化細胞質 TDP-43 累積 • 提高存活率 臨牀前模型中的 TDP-43 病理學 1Rhinn 他等人。Trends Pharm Sci.2022,43:641-652;2Beel S 等人。Mol Neurodeg. 2018,13:55。 TDP-43 病理學是多種 神經退行性疾病的標誌1 • TDP-43 從細胞核錯定位到細胞質 • 形成與 神經變性相關的包涵體 |
| 23 PBFT02 有可能調節阿爾茨海默氏病 • GRN SNP rs5848 攜帶者降低了 PGRN 水平,增加了 AD 的風險 • GRN SNP rs5848 的 AD 患者表現出 PGRN 水平降低和 CSF tau 遺傳風險1 SNP:單核苷酸多態性 第三方臨牀前數據。資料來源:1Chen Y等人。J Neurol. 2015,262:814-22;Takahashi H 等人。Acta Neuropathol。2017,133:785-807。2Fenoglio C 等人。J Alzheimers Dis. 2009, 18:603-612。3Hosokawa M 等人。J Neuropath Exp Neurol. 2015,74:158-65;Minami SS 等人。Nat Med. 2014,20:1157-64;Van Kampen JM & Kay DG。PLOs ONE 2017,12:e0182896 支持 臨牀前 Evidence3 患病率 • PGRN 消融會加劇小鼠的 AD 病理 • PGRN 過度表達減輕了 AD 模型的病理負擔 • GRN SNP rs5848 估計發生在 30% 的普通人羣中,AD 患者的患病率與 相似2 |
| 24 TIMING MILESTONE FTD-GRN 2024 年上半年啟動隊列 2 患者的給藥 2024 年下半年 隊列 1 患者 6 個月的安全性和生物標誌物數據 2025 年上半年來自隊列 1 患者的初始安全和生物標誌物數據 2024 年下半年獲取監管反饋 治療 FTD-c9orf72 和 ALS 患者的臨牀路徑 即將到來的里程碑和企業 更新 PIPELINE • 尋求潛在的合作伙伴關係,以 推進兒科臨牀階段 項目 (GM1, PBFT02Krabbe & MLD) • 優先通過GTP合作伙伴關係推進 亨廷頓氏病計劃 資產負債表 • 截至9月30日的 現金餘額為1.33億美元* • 截至2023年9月30日的現金預計將為 運營提供資金至2025年第四季度* * 現金、現金等價物和有價證券 |
| 25 我們的願景 通過提供可永久重新定義 病程的 基因藥物,改善患有神經退行性 疾病的患者的生活 。 潛在的同類最佳計劃籌資 FTD-GRN 基因療法計劃 建立了製造和工藝 分析能力 強勁的現金狀況,預計 將投資組合擴展到多種成人 神經退行性疾病 * 基於截至2023年9月30日的現金、現金等價物和有價證券 |
| 謝謝 passagebio.com | 納斯達克:PASG |
| 27 Demonstrated Leadership LEADERSHIP TEAM Deep experience in rare disease, CNS disorders and genetic medicines Chip Cale General Counsel & Corporate Secretary Eden Fucci SVP Technical Operations BOARD OF DIRECTORS Maxine Gowen, Ph.D. Chairwoman Athena Countouriotis, M.D. Avenzo Therapeutics Derrell Porter, M.D. cTRL Therapeutics Dolan Sondhi, Ph.D. Weill Cornell Medicine Sandip Kapadia Harmony Biosciences Saqib Islam, J.D. SpringWorks William Chou, M.D. President & Chief Executive Officer William Chou, M.D. President & Chief Executive Officer Stuart Henderson SVP Corporate Development & Investor Relations Kathleen Borthwick SVP Finance & Interim CFO Mark Forman, M.D., Ph.D. Chief Medical Officer |
| 28 Intra-Cisterna Magna (ICM) Administration • Directly deliver vector into the CSF via a single injection to reach both CNS and peripheral tissues* –Allows for broad CNS biodistribution –Lower doses compared to IV systemic delivery –Reduced impact of neutralizing antibodies • Administered under anesthesia using modern neuroimaging to allow for precise delivery • Currently being used in several clinical studies in both pediatric and adult populations Cisterna magna *Hinderer et. al, Human Gene Therapy. 2018 Jan; 29(1):15-24 |