
附錄 99.1

Belite Bio報告2023年第三季度運營 亮點和財務業績
| · | 完成了針對青少年 Stargardt 病(“STGD1”)的Tinlarebant關鍵3期 “DRAGON” 試驗的入組,在全球 11 個國家招收了 104 名受試者 | |
| · | 在《地理萎縮》(“GA”)的關鍵全球三期 “PHOENIX” 試驗中,首位受試者服用了丁拉瑞班特 | |
| · | 口服,每日一次 Tinlarebant 仍然安全且耐受性良好,可減緩自體熒光的擴展, 可降低發病性視網膜萎縮性病變的生長速度,並在 2 期 STGD1 試驗(“LBS-008-CT02”)中將視力穩定長達 24 個月 | |
| · | 關鍵 “DRAGON” 試驗的中期3期安全性和有效性數據預計將於2024年下半年發佈 | |
| · | 電話會議和網絡直播,美國東部時間 2023 年 11 月 14 日星期二下午 4:30 |
聖地亞哥,2023年11月13日——Belite Bio, Inc(納斯達克股票代碼: BLTE)(“Belite” 或 “公司”)是一家臨牀階段的生物製藥藥物開發公司,專注於推進針對醫療需求未得到滿足的退行性視網膜疾病的 新療法,今天公佈了截至2023年9月30日的三個月的財務業績 ,並提供了總體業務最新情況。
Belite Bio董事長兼首席執行官湯姆·林博士説:“我們在本季度取得了有意義的進展, 推進了Tinlarebant的臨牀試驗,並對我們的結果感到興奮。”“在一項為期24個月的自然史研究中,我們對Tinlarebant治療兒童期Stargardt病的2期試驗結果 顯示,與患者 相比,亭拉雷班特降低了視網膜病變的生長,視力得到了穩定,同時保持了安全和良好的耐受性。此外,在 季度,我們完成了 DRAGON 試驗的註冊,給了我們的第一個受試者,並在 PHOENIX 試驗中取得了實質性進展。我們 仍然專注於為患有退行性視網膜疾病的患者提供新療法的願景。”
悉尼大學眼科專業主任、韋斯特米德和悉尼眼科醫院悉尼兒童醫院網絡顧問眼科醫生約翰·格里格教授 在本月初的美國眼科學會 年會上介紹了Tinlarebant針對青少年斯塔加特病患者的2期試驗結果,並評論説:“為期24個月的2期研究的結果的青少年 Tinlarebant 前景樂觀。Stargardt是一種使人衰弱的疾病,可能會對被診斷患有該疾病的人產生改變生活的影響。這種疾病 通常進展迅速,視力在很小的時候就會迅速惡化。2期數據繼續顯示,研究隊列中的疾病進展減緩 ,多個結構和功能參數趨於穩定,包括視力穩定 。這些結果以及可能影響患有目前尚無美國食品藥品管理局批准的治療方法的疾病 的患者的生活令我們深受鼓舞。”
2023 年第三季度業務亮點和即將到來的里程碑:
臨牀亮點
Tinlarebant(LBS-008)被設計為一種口服、強效、 每日一次的視黃醇結合蛋白 4(RBP4)拮抗劑,可在不中斷系統性視黃醇向其他組織的輸送的情況下降低血液中的 RBP4 水平並減少向眼睛輸送的維生素 A(視黃醇) 。維生素 A 對正常視力至關重要,但會作為 毒副產物積累,導致視網膜細胞死亡和視力喪失疾病,例如 STGD1 和 GA,乾性年齡相關性黃斑 變性(乾性 AMD)的晚期形式。
| · | Stargardt 病(STGD1):細胞毒性雙維甲酸的積累與 STGD1 的發作 和進展有關。Tinlarebant 已被美國食品藥品監督管理局 (FDA) 授予快速通道和罕見兒科疾病 (RPD) 稱號,並被美國和歐洲授予 STGD1 孤兒藥稱號 (ODD)。目前尚無美國食品藥品管理局批准的針對 STGD1 的治療方法 。 |
| o | LBS-008-CT02 試驗:針對青少年 STGD1 受試者的持續、開放標籤、為期 2 年的 1b/2 期試驗 |
| § | 在Tinlarebant的2期研究中,共有12名年齡在12-18歲之間的青少年 STGD1 受試者完成了24個月的治療。 的關鍵研究結果如下: |
| · | Tinlarebant 安全且耐受性良好,沒有因不良事件而停藥。 |
| · | 視網膜成像顯示,12名受試者中有5名在Tinlarebant治療24個月後仍未出現萎縮性視網膜病變(稱為自體熒光明顯降低 或 DDAF)。 | |
| · | 對接受丁拉瑞班特治療的受試者和具有相似 基線特徵(年齡≤18歲)的ProgStar參與者之間24個月的DDAF病變增長進行比較顯示,在24個月的 治療期內,接受丁拉瑞班特治療的受試者的DDAF病變生長持續降低(p | |
| · | 在研究期間,大多數受試者的視力穩定下來, 治療24個月後,平均丟失了五個字母(損失了 |

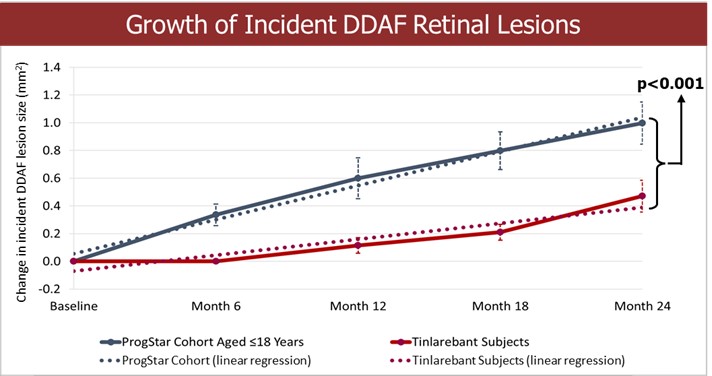
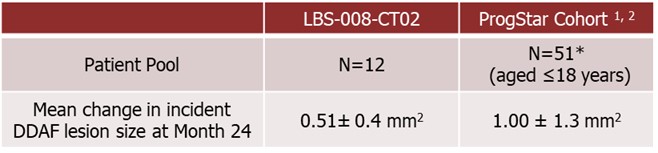
*由於一位受試者的篩查FAF數據不可分級,因此只有來自ProgStar 隊列(年齡≤18)的50名患者被納入分析。
| 1. | Strauss RW、Ho A、Munoz B 等。ProgStar 第 1 號報告。眼科學。2016;123 (4): 817-28。 |
| 2. | Strauss RW、Muñoz B、Ho A 等。ProgStar 第 9 號報告。JAMA Othalmol。2017;135 (11): 1232-1241。 |
| o | Pivotal DRAGON 試驗:2 年、隨機、雙面罩、安慰劑對照、全球、多中心、pivotal 3 期試驗,針對 12-20 歲的 STGD1 受試者: |
| § | 註冊已完成,在全球 11 個國家/地區共有 104 個科目,包括美國、英國、德國、 比利時、法國、瑞士、中國、香港、臺灣、澳大利亞和荷蘭的分校。 |
| § | 主要療效終點是減緩病變生長速度;還將評估安全性和耐受性。 |
| § | 2024 年下半年:預計將獲得中期療效和安全性數據。 |
| · | 地理萎縮(GA):GA 是乾性 AMD 的晚期形式,是一種視網膜 的慢性退行性疾病,會導致老年人失明。有毒維生素 A 副產物(雙維甲酸)的積累與 GA 的 進展有關。目前尚無美國食品藥品管理局批准的GA口服治療藥物。 |
| o | Pivotal PHOENIX 試驗:2 年前瞻性、隨機(2:1、活性:安慰劑,n ~430)、雙面罩、安慰劑對照、 全球、多中心、以 GA 受試者為對象的 3 期試驗。 |
| § | 主要療效終點是減緩病變生長速度;還將評估安全性和耐受性。 |
| § | 第一個受試者已經給藥。 |
| § | 預計將在試驗中期進行中期分析。 |
企業要聞
| · | 在截至2023年9月30日的三個月中, 該公司通過行使2023年5月承保 後續發行中授予的認股權證獲得的總收益為500萬美元,從而加強了資產負債表。 | |
| · | 在截至2023年9月30日的三個月中,該公司從其於2023年6月設立的 上市發行計劃中籌集了64萬美元的淨收益。 |

風險和不確定性
根據當前的業務計劃和財務預期, 公司預計,它將成為經修訂的1986年《美國 國税法》(“PFIC”)第1297條(“PFIC”)所指的 “被動外國投資公司”,並可能在未來一個或多個納税年度成為PFIC,這可能會對美國證券持有人產生不利的美國聯邦所得税影響。
如果公司在美國納税人 持有公司存款證或普通股期間的任何年份是PFIC,則該美國納税人通常需要將處置公司的存款證、普通股或認股權證或此類存款證、普通股或認股權證上收到的任何所謂 “超額分配” 視為普通收入,並支付利息此類收益或分配的一部分。 在某些情況下,税收和利息費用總額可能超過美國納税人處置時實現的收益總額 或獲得的超額分配金額。在遵守某些限制的前提下,如果美國納税人按照《守則》第1295條 的含義進行及時有效的 “合格選擇基金”(“QEF”)選擇(“QEF”)或《守則》第1296條所指的 “按市值計價選舉”(“按市值計價選舉”),則可以減輕這些税收後果。在這些認股權證 被行使之前,QEF 選舉不適用於認股權證。認股權證中的每位投資者(尤其是持有認股權證但不持有美國存託憑證或普通股的任何此類投資者) ,如果是美國納税人,則應就PFIC規則的税收後果以及認股權證的所有權和處置 諮詢自己的税務顧問。按市值計價選擇僅適用於在 合格交易所或市場上定期交易的ADS、普通股或權證。在遵守某些額外限制的前提下,可以針對公司的 ADS或普通股(對於按市值計價選舉,認股權證)進行此類選擇。進行及時有效的 QEF 選舉的美國納税人通常必須按時報告其在公司為PFIC的任何 年度的淨資本收益和普通收益中所佔的份額,無論公司是否分配與ADS或普通股有關的任何金額。 但是,美國納税人應意識到,如果公司是PFIC且美國納税人希望進行QEF選擇,則無法保證公司會滿足適用於QEF的記錄保存要求 ,也無法保證公司會向美國納税人提供此類美國納税人根據 QEF選舉規則要求申報的信息。因此,美國納税人 可能無法就其ADS或普通股進行QEF選舉。進行按市值計價選舉 的美國納税人通常每年必須將ADS或普通股的公允市場價值超過納税人 基礎的部分列為普通收入。每位身為美國納税人的潛在投資者都應諮詢自己的税務顧問,瞭解 PFIC規則的税收後果以及ADS或普通股的所有權和處置,包括QEF 選舉或按市值計價選舉的可用性和程序。
2023 年第三季度財務業績:
現金:截至2023年9月30日,該公司擁有5,450萬美元 的現金。
研發費用:
在截至2023年9月30日的三個月中,研究和 開發費用為870萬美元,而2022年同期為120萬美元。增長主要是由於在2023年第三季度向我們的 研發團隊發放基於股份的薪酬, 的(x)費用增加,以及(y)工資和薪金的增加。在截至2023年9月30日的九個月中,研發費用為2,000萬美元,而2022年同期為360萬美元。研發費用的增加主要歸因於 ,(i) 與進行 DRAGON 和 PHOENIX 試驗相關的費用增加,以及 (ii) 由於我們的研發團隊 擴張和2023年第三季度發放的基於股份的薪酬,以及 (ii) 工資和薪水的增加。
G&A 費用:
在截至2023年9月30日的三個月中,一般費用和 管理費用為220萬美元,而2022年同期為140萬美元。這一增長主要是由於2023年第三季度發放的基於股份的薪酬 增加。在截至2023年9月30日的九個月中,一般和行政費用 為470萬美元,而2022年同期為250萬美元。這一增長還主要源於2023年第三季度發放的基於股份的薪酬 的增加以及專業服務費的增加。

淨虧損:
在截至2023年9月30日的三個月中,該公司 報告的淨虧損為1,090萬美元,合每股虧損0.40美元,而2022年同期為240萬美元或每股虧損0.10美元。 截至2023年9月30日的九個月中,該公司報告淨虧損2460萬美元,合每股虧損0.95美元,而2022年同期淨虧損 為590萬美元,合每股虧損0.32美元。
網絡直播信息
Belite Bio將於美國東部時間2023年11月14日(星期二)下午 4:30 舉辦網絡直播,討論公司的財務業績並提供業務最新情況。要加入 網絡直播,請訪問 https://wsw.com/webcast/cc/blte/1366794。重播將在活動結束後的大約 90 天內提供。
關於 Belite Bio
Belite Bio是一家臨牀階段的生物製藥藥物開發 公司,專注於開發針對醫療需求嚴重未得到滿足的退行性視網膜疾病的新療法,例如晚期乾性 AMD 中的 STGD1 和 GA,以及特定的代謝性疾病。欲瞭解更多信息,請在推特、Instagram、 LinkedIn、Facebook 上關注我們或訪問我們的 www.belitebio.com。
關於前瞻性陳述的重要注意事項
本新聞稿包含有關未來 預期、計劃和前景的前瞻性陳述,以及與非歷史事實有關的任何其他陳述。這些陳述 包括但不限於有關臨牀數據對患者的潛在影響、臨牀開發、其候選產品的監管 里程碑的陳述,以及包含 “期望”、“將”、“相信”、 和其他類似表達方式的任何其他陳述。由於各種重要因素 ,實際結果可能與前瞻性陳述中顯示的結果存在重大差異,包括但不限於Belite Bio證明其候選藥物 安全性和有效性的能力;其候選藥物的臨牀結果,可能不支持進一步的開發或監管批准;對啟動、註冊和完成時間的預期 以及與其臨牀試驗相關的數據;相關監管機構做出的決定 關於Belite Bio候選藥物的監管批准;DRAGON或PHOENIX的研究是否可能需要根據各自的數據進行額外的臨牀 試驗;Tinlarebant的潛在療效以及 這些風險在Belite Bio向美國證券和 交易委員會提交的文件的 “風險因素” 部分中進行了更全面的討論。所有前瞻性陳述均基於Belite Bio目前獲得的信息,除非法律要求,否則Belite Bio沒有義務公開更新或修改任何前瞻性陳述, 無論是由於新信息、未來事件還是其他原因。

BELITE BIO, INC
未經審計的運營和綜合虧損簡明合併報表
(金額以千美元計, 份額和每股金額除外)
| 在這三個月裏 | 九個月來 | |||||||||||||||
| 9月30日結束, | 9月30日結束, | |||||||||||||||
| 2022 | 2023 | 2022 | 2023 | |||||||||||||
| 開支 | ||||||||||||||||
| 研究和開發 | 1,185 | 8,743 | 3,643 | 19,982 | ||||||||||||
| 一般和行政 | 1,355 | 2,218 | 2,457 | 4,731 | ||||||||||||
| 運營費用總額 | 2,540 | 10,961 | 6,100 | 24,713 | ||||||||||||
| 運營損失 | (2,540 | ) | (10,961 | ) | (6,100 | ) | (24,713 | ) | ||||||||
| 其他收入(支出): | ||||||||||||||||
| 其他收入總額,淨額 | 137 | 27 | 236 | 81 | ||||||||||||
| 所得税前虧損 | (2,403 | ) | (10,934 | ) | (5,864 | ) | (24,632 | ) | ||||||||
| 所得税支出 | - | 1 | - | 10 | ||||||||||||
| 淨虧損 | (2,403 | ) | (10,935 | ) | (5,864 | ) | (24,642 | ) | ||||||||
| 其他綜合收益(虧損) | ||||||||||||||||
| 扣除零税後的外幣折算調整 | (166 | ) | (55 | ) | (323 | ) | (115 | ) | ||||||||
| 綜合損失總額 | (2,569 | ) | (10,990 | ) | (6,187 | ) | (24,757 | ) | ||||||||
| 每股計算中使用的加權平均普通股數量: | ||||||||||||||||
| -基礎版和稀釋版 | 24,869,038 | 27,315,550 | 18,321,088 | 26,013,012 | ||||||||||||
| 每股普通股淨虧損 | ||||||||||||||||
| -基礎版和稀釋版 | $ | (0.10 | ) | $ | (0.40 | ) | $ | (0.32 | ) | $ | (0.95 | ) | ||||

BELITE BIO, INC
未經審計的簡明合併資產負債表
(金額以千美元計, 份額除外)
| 十二月三十一日 | 9月30日 | |||||||
| 2022 | 2023 | |||||||
| 流動資產 | $ | 42,807 | $ | 56,135 | ||||
| 其他資產 | 1,466 | 1,463 | ||||||
| 總資產 | $ | 44,273 | $ | 57,598 | ||||
| 負債總額 | $ | 2,772 | $ | 4,804 | ||||
| 股東權益總額 | 41,501 | 52,794 | ||||||
| 負債總額和股東權益 | $ | 44,273 | $ | 57,598 | ||||
| 授權的普通股 | 492,179,086 | 400,000,000 | ||||||
| 已發行和流通的普通股 | 24,898,908 | 27,599,244 | ||||||
媒體和投資者關係聯繫人:
詹妮弗·吳/ir@belitebio.com
Argot Partners belitebio@argotpartners.com