

附錄 99.2 INVIVYD 2023 年第三季度財務業績和業務亮點 2023 年 11 月 9 日 © 2023 Invivyd, Inc. Invivyd 和 Invivyd 徽標是 Invivyd, Inc.的商標。本演示文稿中的所有商標均為其各自所有者的財產。

關於前瞻性陳述的警示説明本演示文稿 包含1995年《美國私人證券訴訟改革法》所指的前瞻性陳述。本演示文稿中不是歷史事實陳述的陳述是前瞻性陳述。諸如 “可能”、“將”、“應該”、“預期”、“預期”、“尋找”、“可以”、“打算”、“目標”、“目標”、“目標”、 “項目”、“設計”、“估計”、“相信”、“預測”、“潛力” 或 “繼續” 之類的詞語或這些術語的否定或其他類似表述意在 識別前瞻性陳述,儘管並非所有前瞻性陳述都包含這些識別性詞語。前瞻性陳述包括有關我們正在進行的研究和 臨牀開發活動的進展和時間等的陳述,包括與 VYD222 有關的陳述;我們的 CANOPY 3 期關鍵臨牀試驗的預期初始主要終點數據的發佈時間;我們對快速生成可能提交的 VYD222 緊急使用許可 (EUA) 的臨牀數據的期望;我們計劃儘快在美國提交 EUA 申請;我們是否能夠成功提交未來的 EUA,以及EUA 提交的任何此類抗體的結果; 公司對目標患者羣體規模及其候選產品的潛在市場機會的預期;該公司的 INVYMAB 平臺方法在快速、連續生產新的 抗體以應對病毒威脅方面的潛力;我們對免疫功能低下的人羣需要更多治療選擇以防止 COVID-19 的信念;COVID-19 格局的未來;我們對靶標規模的期望 患者羣體和潛在市場我們的候選產品的機會以及我們的市場地位;CANOPY 臨牀試驗的設計;如果獲得批准,VYD222 可能在美國商業化;我們認為我們現有的 現金資源將足以支撐到2024年第四季度的預期現金流;以及其他非歷史事實的陳述。實際上,我們可能無法實現 前瞻性陳述中披露的計劃、意圖或預期,您不應過分依賴我們的前瞻性陳述。這些前瞻性陳述涉及風險和不確定性,可能導致我們的實際結果與前瞻性陳述中描述或暗示的結果 存在重大差異,包括但不限於:我們的發現、臨牀前和臨牀開發活動的時間和進展;我們從CANOPY 臨牀試驗中快速生成所需數據以支持 EUA 可能提交 VYD222 的能力;我們未來能否成功提交 EUA,以及任何此類EUA提交的結果;在臨牀前研究或 臨牀試驗中觀察到的意想不到的安全性或有效性數據;基於臨牀前研究的中和活性,VYD222 或其他候選產品的臨牀成功的可預測性;在不同檢測 中測試的候選產品的中和活性的潛在差異;臨牀前研究或臨牀試驗的結果可能無法預測與當前或未來臨牀試驗相關的未來結果的風險;所用模型中結果的可變性 預測針對值得關注的 SARS-CoV-2 變體的活性;預期或現有競爭的變化;監管環境的變化;監管審批程序的不確定性和時機;我們的平臺方法是否使我們 能夠快速、連續地產生新的抗體以應對病毒威脅;VYD222 或任何其他候選產品是否能夠證明並維持對主要的 SARS-CoV-2 變異體的中和活性,尤其是在病毒面前 br} 演變;以及我們是否有足夠的資金來應對未來的運營費用和資本支出需求。可能導致我們的實際業績與本演示文稿中前瞻性 陳述中表達或暗示的業績存在重大差異的其他因素,在我們向美國證券交易委員會(SEC)提交的最新10-K表年度報告、向美國證券交易委員會(SEC)提交的其他 文件中,以及我們未來向美國證券交易委員會提交的報告中,網址為www.sec.sec.gov。本演示文稿中包含的前瞻性陳述自該日期起作出,除非適用法律要求,否則我們沒有義務更新此類信息,無論是 新信息、未來事件或其他結果。© 2023 Invivyd, Inc. Invivyd、Invymab 和 Invivyd 徽標是 Invivyd, Inc.的商標。本演示文稿中的所有商標均為 其各自所有者的財產。2

議程 1.簡介/概述 − Dave Hering,首席執行官 官員 2.CANOPY 試驗和最新的 VYD222 體外中和數據-Pete Schmidt,醫學博士,首席醫學官 3.市場機會和商業準備-傑裏米·高勒,首席運營官兼商務官 4.第三季度財務回顧-比爾·杜克,首席財務官 5.問答 3

最近的業務亮點和主要成就已完成 CANOPY 3 期關鍵臨牀試驗 正在研究 VYD222 以預防出現症狀 COVID-19 公司預計將在 2023 年底或 2024 年第一季度初獲得初始 CANOPY 主要終點數據公司的目標是在切實可行的情況下儘快在美國提交緊急 使用授權 (EUA) 申請 TM 公司繼續推進 INVYMAB,這是其專有平臺方法,專為快速、連續生成新抗體而設計應對病毒威脅 4

保護免疫功能低下的人免受 COVID-19 感染的需求顯而易見 而且迫切需要評估 COVID-19 的風險和成本在 Omicron 時代 COVID-19 對大量美國人羣中免疫功能低下人羣的影響:來自 2 1 商業保險健康計劃的見解: EPOCH-US 研究基於人羣的觀察性信息研究 • 在英格蘭約 1200 萬人的樣本中,3.9% 是 • 在大約 1700 萬人的樣本中在美國大型商業免疫功能低下(IC)健康保險計劃中,2.7%是IC • 儘管只有 3.9% 的人口,IC 患者 • 大約 14% 的 IC 患者被診斷患有 COVID-19 佔住院人數的 22%,其中 24% 住院,佔死亡人數的 24% ——儘管超過 80% 的 人住院時間長,費用高昂的人羣接種了 ≥3 支 COVID-19 與 COVID-19 相關的疫苗,平均費用為 • 某些 IC 患者(例如,實體器官和幹細胞移植)6美元每位 名患者4,029人(以及接受者以及最近接受血液癌治療的患者的平均時長),住院時間為15天 COVID-19 COVID-19與沒有這些疾病的人相比,風險增加了 10 倍以上儘管有疫苗, 免疫功能低下的人出現嚴重 COVID-19 結果的風險仍然更高,需要額外的治療選擇來防止 COVID-19 1。Evans Lancet Reg 2023;2.Ketkar Curr Med Res Opin 2023 5

VYD222 已對各種前歐密克龍和 OMICRON 變體 1 變體亞系 VYD222 WT (D614G) WT (D614G) ✓ Delta B.1.617.2 ✓ BA.1 ✓ BA.4/5 ✓ BA.4.6 ✓ BF.7 ✓ Omicron XBB.BB.1 ✓ XBB.1.5 ✓ XBB.1.5.10 和 EG.5(一個 )中的主要變體,表現出廣泛的體外中和活性美國) 是 XBB 變體,其 XBB.1.16 ✓ 的刺突糖蛋白序列相同,包括在 XBB.1.5.10/EG.5 2-3 的約 80% 中發現的 F456L 突變體參考文獻:1. ✓CRO 使用偽病毒 SARS-CoV-2 中和 ✓ 標準化體外測定抗體測定中和活性生成的 VYD222 數據;2. https://covid.cdc.gov/covid-data-tracker/#variant-proportions(2023 年 10 月 30 日訪問);3. covspectrum.org 6
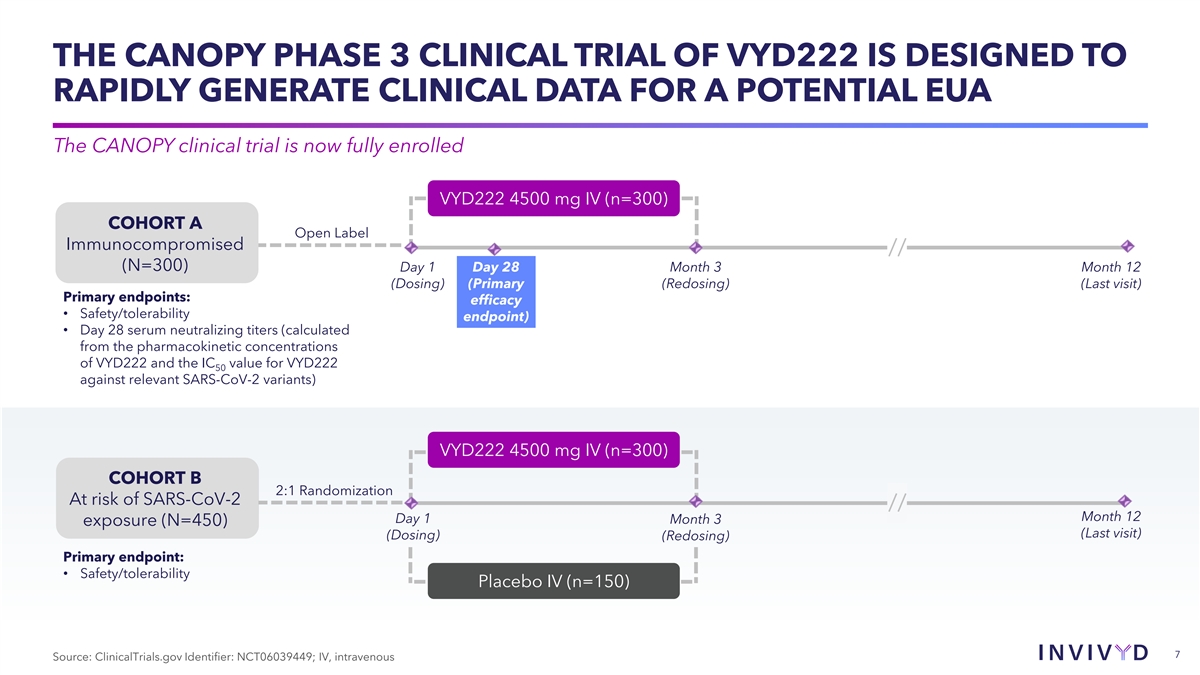
VYD222 的 CANOPY 3 期臨牀試驗旨在為潛在的 EUA 快速 生成臨牀數據 CANOPY 臨牀試驗現已全面註冊 VYD222 4500 mg IV (n=300) 隊列 A 開放標籤免疫受損者//(N=300) 第 1 天 28 個月 3 個月 12 日(給藥)(主要(再給藥)(最後一次就診)主要的 終點:療效 • 安全性/耐受性終點)• 天 28 個血清中和滴度(根據 VYD222 的藥代動力學濃度和 VYD222 50 對照相關 SARS-CoV-2 變體的 IC 值計算)VYD222 4500 mg IV (n=300)隊列 B 2:1 隨機分組 SARS-CoV-2 風險//月 12 天 1 月 3 日暴露(N=450)(最後一次就診)(給藥)(再給藥)主要終點:• 安全性/耐受性 IV(n=150)7 來源:ClinicalTrials.gov 標識符: NCT06039449;靜脈注射
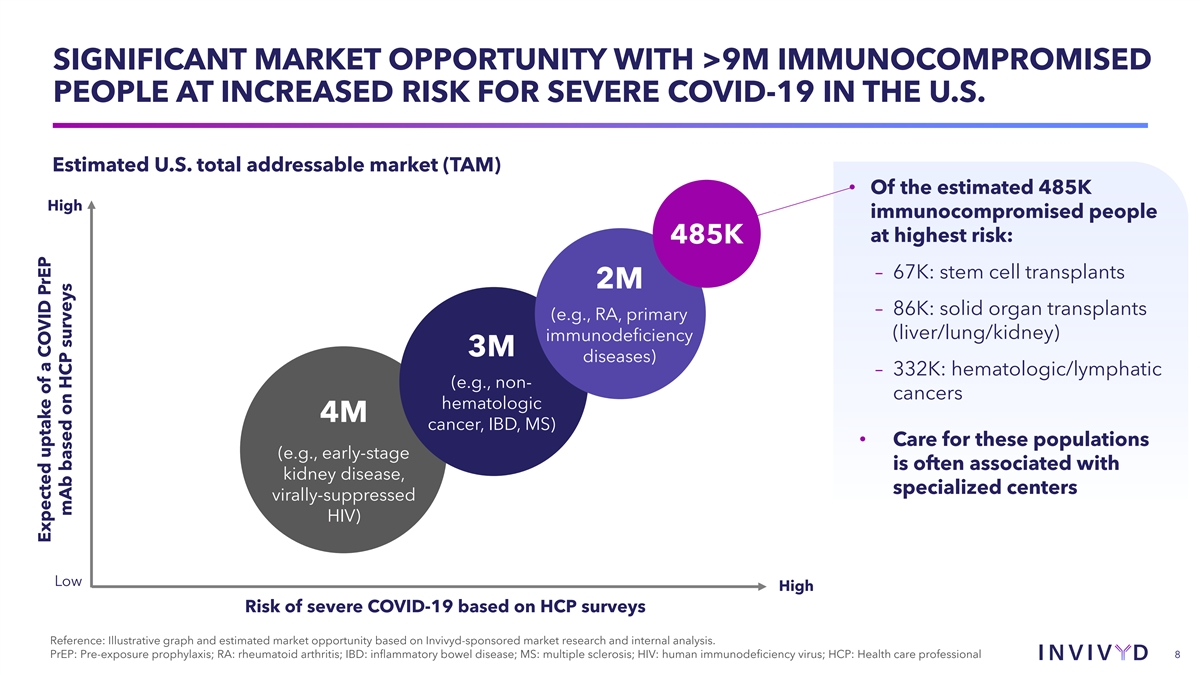
巨大的市場機會,美國超過 900 萬免疫功能低下的人患重度 COVID-19 的風險增加。估計的美國潛在市場總數 (TAM) • 在估計的 485 萬高免疫功能低下人羣中,風險最高:485K — 67K:幹細胞移植 2M — 86K:實體器官移植 (例如 RA、原發性(肝/肺/腎)免疫缺陷 3M 疾病)— 332K:血液學 /淋巴管(例如,非癌症,血液學 4M 癌、IBD、MS)• 對這些人羣的護理(例如,早期階段通常與腎臟 疾病有關,專業中心病毒抑制 HIV)基於 HCP 的調查顯示,重度 COVID-19 的低高風險參考:基於 Invivyd 贊助的市場研究和內部分析得出的説明性圖表和估計的市場機會。PrEP: 暴露前預防;RA:類風濕性關節炎;IBD:炎症性腸病;MS:多發性硬化症;HIV:人類免疫缺陷病毒;HCP:醫療保健專業人員 8 根據 HCP 的調查,COVID PrEP 單抗的預期攝取量

如果獲得授權,可能在美國推出 VYD222 的商業化準備工作正在進行中,前提是獲得授權的進入市場規劃(例如市場研究、市場規模/細分市場、品牌戰略、實地部隊規模)市場準入活動(例如付款人/定價研究、分銷渠道)製造初始商業 庫存建立必要的內部系統和技術以支持向商業階段過渡商業化由經驗豐富的團隊領導,成功地在 傳染病空間,例如:9

2023 年第三季度財務預期現金流道將持續到 2024 年第四季度,如果單克隆抗體候選藥物是 2023 年 9 月 30 日獲得授權或批准的 mAb:單克隆抗體 10,則截至產品收入中,現金、 現金等價物和有價商品收入為2.649億美元

謝謝