

附錄 99.1 Arash Mostaghimi 博士與分析師和投資者日 2023 年 10 月 16 日

前瞻性陳述本演示文稿包含有關Equillium, Inc. 的前瞻性 陳述(實際業績或事件可能與計劃、意圖和 “公司” 存在重大差異)。在某些情況下,您可以通過 前瞻性陳述中披露或暗示的預期來識別前瞻性陳述,這些陳述包括 “將”、“期望”、“打算”、“計劃”、“目標”、“相信”、“估計” 等字樣,因為公司 “潛在”、“繼續” 和 “持續”,或者這些條款的負面影響,或其他業務,包括但不限於,公司文件中描述的風險與 術語類似,旨在識別有關未來的陳述。與證券交易所委員會(“SEC”)。請注意,不要這些陳述基於公司管理層當前的信念,也不要過分依賴這些代表預期的前瞻性陳述 。這些陳述包括但不限於截至本演示之日的公司觀點的陳述。公司關於公司的業務戰略, 公司的發展計劃預計,隨後的事件和發展將引起其對候選產品、變更的安全性和有效性的看法和商業化。但是,儘管公司可能會選擇在未來的某個時候更新這些 遠期公司的候選產品、公司的計劃和預期的時機陳述,但除非適用法律要求,否則公司目前尚不瞭解監管文件和批准、 打算這樣做的規模和增長潛力。這些是公司候選產品和現金跑道的市場。這些以及其他風險和不確定性在標題中更全面地描述了這些風險和不確定性 涉及已知和未知的風險、不確定性和其他因素 “風險因素” 以及公司文件和報告中的其他地方,這可能會導致公司的實際業績、活動水平、業績 通過訪問美國證券交易委員會網站www.sec.gov上的EDGAR免費獲得,或者成就與所表達的信息存在重大差異標題為 “投資者” 的公司網站。 這些前瞻性陳述均為前瞻性陳述。本警示聲明實際上可能不會完全限定公司看待的陳述。實現其前瞻性聲明中披露的計劃、意圖或預期。這種謹慎態度是根據報表第21E條的 “安全港” 條款提出的,您不應過分依賴經修訂的1934年《公司證券交易法》。前瞻性陳述。商標本演示文稿可能包含其他公司的商標、服務標記、商品名稱和版權,這些都是其各自所有者的財產。僅為方便起見,本 演示文稿中提及的某些商標、服務商標、商品名稱和版權可能不帶商標、SM © 或® 符號,但是 Equillium 將在適用法律允許的最大範圍內維護適用所有者對這些商標、服務標記、商品名稱和 版權的權利(如果有)。2

歡迎今天的議程發言者:管道概述演講嘉賓 Bruce Steel、首席執行官 Arash Mostaghimi、醫學博士、M.P.A.、M.P.H. 皮膚病學副教授哈佛醫學院強效多細胞因子平臺史蒂夫·康納利、皮膚科住院諮詢服務首席科學官布里格姆和 婦女醫院 EQ101:一流的 IL-2 三特異性抑制劑,9 & IL-15 Equillium Management Steve Connelly,首席科學官 EQ101:針對斑禿的臨牀項目 Bruce Steel,CFA 首席執行官 Maple Fung,首席營銷官 ArashMostaghimi,哈佛大學和布里格姆婦女醫院閉幕詞 Steve Connelly 博士 Bruce Steel,首席科學官 Q&A Maple Fung,醫學博士首席醫學官 3

Equillium Snapshot & Investment 亮點一流的免疫學 資產抑制劑免疫生物學新型多細胞因子合作領域的領導者 Itolizumab 為多種多重治療開發高影響力的新型療法自身免疫和臨牀階段短期項目催化劑炎症性疾病 預計到2025年的現金流 4

多元化的一流免疫學資產管線藥物 適應症臨牀前 1 期 2 期 3 期合作伙伴預期里程碑 EQ101 2023 年第四季度初步數據 PoC 數據和 FDA/EMA Orphan 全球 IL-2/9/15 斑禿權 CTCL 的藥物名稱 2024 年中期 topline 數據抑制劑 2023 年第四季度 SAD/MAD 數據潛力 EQ102 全球 IL-15/21 乳糜瀉抑制劑擴展到 2024 年其他 2024 年乳糜瀉權利 or GI 適應症患者數據自身免疫領域的多重機會,全球細胞因子炎症和腫瘤學權利平臺 急性移植-versus-host FDA Fast Track 和 2024 年中期審查疾病孤兒藥名稱 EQ001 FDA Fast Track 系統性紅斑狼瘡 itolizumab 2024 年初頭線數據 (SLE) /狼瘡腎炎 (LN) LN 和抗 CD6 潰瘍性結腸炎的指定由 Biocon 在印度進行 5

預期里程碑 EQ101 — 2 期臨牀研究 Alopecia Areata — 初始數據 2023 年第四季度斑禿——Topline 數據 2024 年中期 EQ102 — 1 期臨牀研究 SAD/MAD(健康志願者)— 2023 年第四季度乳糜瀉 — 數據 2024 年伊託珠單抗 — 1b 期/3 期臨牀研究狼瘡腎炎均衡研究(1b 期)— Toplise 2024 年初數據 AgvHD EQUATOR 研究(第 3 階段)— 2024 年中期回顧 6

伊託珠單抗靶向 CD6-ALCAM 信號通路 7 的同類首創免疫修飾單抗體

小野製藥:高價值戰略合作伙伴關係 Equillium 獲得 伊託珠單抗研發的預付款和全額資金,以換取小野購買伊託珠單抗權的獨家選擇權收盤款*:3,820萬美元期權行權**:3510萬美元里程碑付款:1.014億美元期權期 到期三個 Equillium 開發和融資:交付後幾個月:• Illium 將繼續進行所有伊託珠單抗的研發 • 來自 EQUALISE 的頭條數據 • 小野將為 2022 年 7 月 1 日狼瘡腎炎研究 以及直到 2022 年 7 月 1 日的所有研發費用提供資金期權期 • 來自 EQUATOR 的中期數據 • 研發預算每季度約 800 萬美元 GVHD 里程碑研究高達 1.014 億美元:• 臨牀 • 監管 • 首次銷售 * 包括2640萬美元的預付款和2022年7月1日至12月31日期間的研發費用報銷。8** 50億日元視付款時的匯率而定(以上美元金額基於匯率)截至 2023 年 8 月 8 日);里程碑付款和研發報銷以美元為單位。

多細胞因子平臺和候選治療藥物 9

多細胞因子問題細胞因子利用共享受體 表現出重疊或協同生物活性,這在治療疾病時會帶來獨特的藥物開發挑戰細胞因子經常表現出... 細胞因子信號通過... 上游共享受體 “重疊 信號” 信號中心重疊生物靶標包括 Dupixent™ 活性下游分歧的 “協同信號” 激酶級聯結合產生生物活性靶標包括 JAK 抑制劑 10

靶向細胞因子信號傳導的挑戰理想的治療方法 maB JAK 抑制劑選擇性抑制疾病驅動細胞因子僅抑制一種細胞因子抑制 50+ 細胞因子抑制信號細胞因子的正確上游組合是獲得最佳治療效果的關鍵,平衡下游 的強效活性和信號傳導潛在毒性抑制太窄抑制過於廣泛最佳治療效果涉及其他細胞因子,非選擇性細胞因子靶嚮導致活性不足,導致廣泛免疫抑制還有 安全風險 11

Multi-Cytokine Platform 模塊化平臺生成的產品可調節細胞因子的自然生物學宂餘或協同作用,從而提供更大的治療益處驗證疾病 • 技術源自 • 產品可以靈活地靶向美國國立衞生研究院 優化計算功能治療特徵和組織生物學融合 • 獨特的靶向上遊靶向特性共享受體,以選擇性地調節多種細胞因子 • 廣泛的知識產權組合涵蓋產品 途徑中的產品 單本小説平臺、產品處理方法和成分結構硅內物質設計活性關係 • 靜脈、皮下和口服給藥蛋白質工程 12
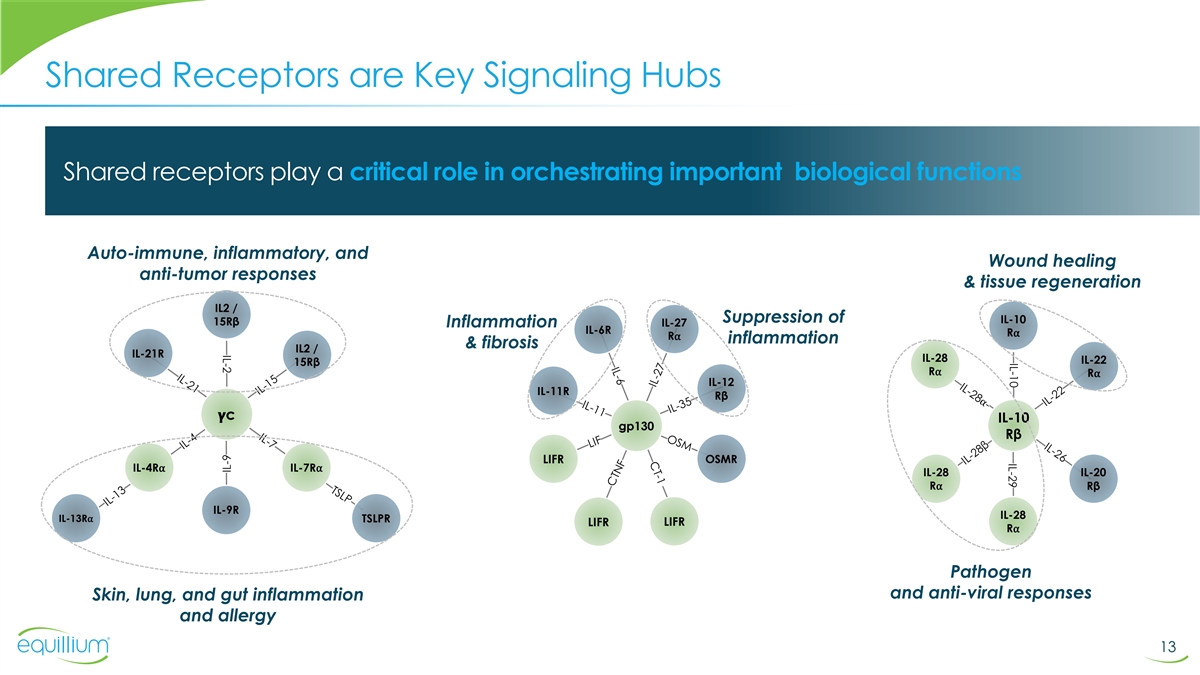
IL-10 IL-29 IL-2 共享受體是關鍵信號傳導中心共享 受體在協調重要的生物學功能中起着至關重要的作用自身免疫、炎症和傷口癒合抗腫瘤反應和組織再生 IL2 /抑制 IL-10 15Rβ IL-27 IL-6R 炎症 Rber R2 炎症和纖維化 IL2/IL-21R IL-28 15Rβ Rbeta Rbeta OSMR IL-4RIL-7Rlick rβ LIFR LIFR LIFR LIFR R病原體和抗病毒反應皮膚、肺部和腸道炎症和過敏 13 IL-9 IL-22 IL-12 IL-11R IL-10 IL-28 IL-20 IL-9R IL-28

多細胞因子平臺的產品共享受體為 提供了更有效的機會 •多細胞因子激活劑 (mcA) 調節生物學利用多種信號通路來調節生物學功能的工程蛋白 •多細胞因子抑制劑 (mcI) 阻斷多種信號通路以調節生物功能的工程肽或蛋白質 14

γC 受體:一個關鍵的共享細胞因子信號傳導中心 γC 受體的細胞因子是免疫反應的關鍵調節劑,因此,它成為調節 T、NK 和 B 細胞的有吸引力的藥物靶標協同信號傳導 CD8 和 NK T 細胞上 CD8 細胞毒性 T 細胞上的重疊信號 αα γαααγα β 私人共享受體 15

IL-15 處於組織特異性免疫炎症方法的頂端 靶向 IL-15 EQ101 和 EQ102 • 在腫瘤壞死因子α和其他關鍵細胞因子的表達之前啟動促炎級聯 • IL-15 在各種器官特異性自身免疫性疾病中起着致病作用 • IL-15 刺激 NK、NK-T、γΔ、ILC1 和記憶 CD8 T 細胞的生成 • 阻斷 16 Waldmann 等多種方法正在開發中 al.,JEM.,2019 IL-15

選擇性多細胞因子抑制劑 (mcI) 的產生 •細胞因子受體複合物 •CYTOKINE D-HELICES •功能融合細胞因子共享 PK 延伸策略受體私有 pegyLation 受體脂化 FC 融合肽原生序列口服給藥肽裝訂 多特異性分子專有複合序列 Fc-fusions — bi/tri-fusions — bi/tri-fusions 特異性 Helices A 和 C A 與私有受體 D 相互作用,而 helix D C 與共享受體相互作用 •優化 mcI 治療工程多細胞因子抑制劑 17

mcI moA:破壞受體複合物的組裝選擇性 抑制細胞因子 A、D 和 F 細胞因子 E A D C F 多細胞因子 B A 抑制劑 (mcI) A 無信號私有共享受體受體 A B C D E F 細胞因子 E Controls E Controlines E Control +mcI 細胞因子首先與私有受體結合 mcI 與 γc 受體 br} 結合親和力,然後在較低的親和力下與γc共享受體短暫二聚化並選擇性阻斷,只有選定的信號傳導才會導致信號傳導細胞因子,例如 A、D 和 F 信號傳導 18% 抑制

多細胞因子抑制劑的優勢通過選擇性地抑制那些導致疾病的細胞因子來解決 單靶點生物製劑和廣泛免疫抑制激酶抑制劑的侷限性 mcI 改進的治療特徵抑制一個細胞因子抑制 50+ 細胞因子抑制選定的 細胞因子 ü靶向上遊優化靶向——不是信號太窄/不太寬 u 比 jaKi 更高的選擇性可以改善安全狀況 下游 ü更大通過信號傳導抑制靶向細胞因子的下游信號傳導來發揮效力 19 活性不足安全責任最佳治療效果

一流的多細胞因子藥物的差異化產品線 EQ101 EQ102 EQ302 EQ400 系列 2/3 期 1 期臨牀前 pegyLated 肽抑制劑:聚乙二醇化肽抑制:穩定的肽抑制劑:蛋白質激活:IL-X + IL-Y IL-15 + IL-21 IL-2 + IL-9 + IL-15 IL-15 + Celiac 疾病腫瘤皮膚 T 細胞乳糜瀉淋巴瘤炎症性腸病疫苗輔助劑炎症性腸病斑禿1型糖尿病可能與檢查點抑制劑聯合口服給藥、白癜風 SLE IL-21局部作用的肽 ADC 或細胞療法類風濕性關節炎肝病同時接近體內和體外肌炎通過間質性肺病 sub-Q 注射液靜脈注射和 Sub-Q 靜脈注射 開發中 20 SLE = 系統性紅斑狼瘡;ADC = 抗體藥物偶聯物

EQ101 同類首創 IL-2/IL-9/IL-15 三特異性抑制劑 21

EQ101:一流的三特異性細胞因子抑制劑 EQ101 抑制 關鍵細胞因子 IL-2、IL-9 和 IL-15 可以從臨牀前模型轉化為人類 IL-9 IL-15 IL-2 • IL-2 和 IL-15 很重要 • 聚乙二醇化肽 • 與魯索利替尼一樣有效 • CD8 和 NK 細胞(基於 d-Helix)在抑制 >100 生物學方面的多種經驗方面具有重要臨牀意義,IL-9 有助於選擇性抑制 IL-2、淋巴增生或受試者,皮膚中有 1 2,3 個炎症 IL-9 和 IL-15 信號傳導 白血病 T 細胞繫有利於安全性還有 5,6 耐受性 • 抑制兩者都很重要 • 低劑量給藥 • 由於靜脈注射量,ruxolitinib 在小鼠身上比 IL-2 和 IL-15 更有效 • 在介導的脱髮中獲得細胞毒性 CD8 T 細胞配方/皮膚 T 細胞 4 6 發育斑禿淋巴瘤患者的皮下免疫模型在信號傳導中實現了積極的證明- 宂餘 22 1) Nata 等人,J. Biol。化學。, 2015;2) Massoud 等人,PNAS,2015;3) Wang 等人,白血病,2018 年;4) Azimi 等人,AHRS,佛羅裏達州奧蘭多,20185)Frohna 等人,J. ClinPharm.,2019 6) Querfeld 等人,Blood,2019

EQ101:與 jaki 相比 jaki 更完整的下游信號抑制 jaKi 對細胞因子信號傳導的抑制尚不完整,而 EQ101 抑制了完全抑制細胞因子信號傳導的多種下游途徑 ruxolitinib 阻斷 EQ101 僅阻斷所有 JAK/STAT 途徑主要途徑 α +IL-2 + IL-2-+ IL-2-+ rux β γ+ γ-3 pstat-3 pstat-3 pstat-3 stat-1 pstat-1 pstat-5 pstat-5 perk perk pi3k ppi3k Vinculin Vinculin 23 內部數據和 Frohna 等人,Alopecia Areata 研究峯會,紐約,紐約,2018 年 EQ101

EQ101 的表現與 IL-15 驅動的 ATL 模型中的 JAK 抑制類似 IL-2、IL-9 和 IL-15 在成人 T 細胞白血病 (ATL) 和皮膚 T 細胞淋巴瘤 1,2,3,4,5 (CTCL) 中過度表達,它們會推動癌細胞增殖和皮膚炎症增加單獨阻斷 IL-2 或 IL-15 在 治療大顆粒淋巴細胞 6 7 白血病 (LGLL) 時無效 ATL 對照 PBS EQ101 EQ101 ruxolitinib 40mg/kg,IV,BIW,連續給藥 4 周魯索利替尼,50mg/kg/d 24 1) Dobbeling 等人,Blood,1998;2) Mishra 等人,Clin。《癌症報告》, 2014;3) Qin 等人,2001 年;4) Garcia 等人,2016 年;5) Waldmann 等人,1993 年;6) Waldmann 等人,2013;7) Berkowitz 等人,2014;8) Wang 等人,2018

EQ101:迄今為止的歷史研究摘要 BNZ-CT-101,健康志願者的第一階段研究(n=18)首次調查單次上升劑量 BNZ132-1-40 的安全性、耐受性和 PK 的人體研究 • 每個治療組 3 名受試者 • 單次靜脈注射劑量為 0.2 mg/kg、0.4 mg/kg、1.6 mg/kg、3.2 mg/kg、6.4 mg/kg 研究 BNZ-CT-102,健康志願者 1 期研究(n = 25,已治療)單一中心,隨機、單盲、安慰劑對照、多劑量研究,以表徵靜脈注射的安全性、耐受性和 PK/PD BNZ132-1-40 • 受試者每週給藥 (QW),持續 4 劑量,或每隔一週 (QOW) 一次,持續 3 劑量 • 3 個 QW 隊列,分別為 0.5 mg/kg、1.0 mg/kg 和 1.5 mg/kg • 2 個 QOW 隊列分別為 2 mg/kg 和 3.0 mg/kg 研究 BNZ1-CT-201,1/2 期劑量 LGL或CTCL(n = 50)開放標籤、多中心研究,以表徵安全性、耐受性、初步性通過靜脈輸液給藥 QW 最多四劑量的 BNZ-1 的療效和 PK/PD • 在 1、8、15 和 22 天進行治療,然後延長 3 個月,在此期間,受試者最多接種 13 劑每週最多 17 劑量 BNZ-1 • 4 個隊列給藥劑量在 0.5 mg/kg 到 4 mg/kg 之間 25 Froha 等人,《2020年臨牀藥理學雜誌》;Querfeld 等人,在 2020 年 ASH 上的演講;Brammer 等人 Blood 2023 BNZ-1 = EQ101,PK = 藥代動力學,PD = 藥效學,IV = 靜脈注射,LGLL = 大顆粒淋巴細胞白血病,CTCL = 皮膚 T 細胞 淋巴瘤

EQ101:正常健康志願者的經驗摘要 üü{ br} ü沒有 AE >= 3 級,最常見的 AE 劑量成正比 PK,觀察到安全且 • SAD:18 名受試者中有 3 名受試者出現輕度頭痛(17%)耐受性良好、沒有 DLT 和 • MAD:24 天中有 4 天喉嚨痛和頭痛大約 5 天沒有臨牀意義的實驗室受試者(16%)異常 üü劑量依賴性變化多劑量 EQ101 ≥ 1.5mg/kg 無可檢測到的抗藥 IL-2/IL-15 依賴細胞會導致長時間的 PD 效應 >7 天抗體提示 QW 服用 QOW 劑量 26Froha 等人,《2020年臨牀藥理學雜誌》QW = 每週給藥 QOW = 每隔一週給藥一次

EQ101:CTCL 中的 1/2 期概念驗證研究臨牀驗證和 有利的安全特徵 EQ101 有待進一步研究 1 皮膚 T 細胞淋巴瘤患者的 1/2 期 MAD 研究(n=30)• 預先接受過大量治療的人羣(先前 5 次全身治療的中位數)• 關鍵細胞標誌物中的劑量依賴性 PK/PD 關係 • 觀察到安全且耐受性良好,沒有藥物相關的 SAE,沒有 DLT,也沒有臨牀意義實驗室異常 • IL-2 和 IL-15 依賴細胞的劑量依賴性減少以及 msWat 的改善 • 2mg/kg選擇擴大劑量研究持續時間長達 18 個月研究持續時間長達 8 個月* 27 (1) Querfeld 等人,ASH 2020;* 研究已結束,為EOP2會議做準備

EQ101:為 CTCL 的後期進展做好準備 EQ101 可減少 IL-2 和 IL-15 依賴細胞和炎症,皮膚病變和 ORR 得到改善,與基準藥物相比,評估 mogamulizumab 和 vorinostat 的 MAVORIC 3 期試驗為 基準 EQ-101 CTCL 疾病 IB/II 期 Mogamulizumab (n=68) vorinostat (n=72) 提供了最新、最可靠的 1 個估計值 基準 CTCL 疾病 IB/II 期 Mogamulizumab (n=68) vorinostat (n=72) EQ101 (n=19) 迴應率 2 27.9% 19.4% 42.1%(msWat,CR + PR)EQ101,2mg/kg 基線第 16 周基線第 16 周第 31 周 28 1) Kim 等人 2018。2) 另外兩名 患者已獲得 PR 但未包括在內,因為由於研究終止,他們沒有達到 4 周的答覆。包括這些患者的反應率 = 52.6% 3) 顯示的患者進入了 BNZ1-CT-201 的長期延期部分,並持續給藥 70 多周。msWat = 修改後的嚴重程度加權評估工具

EQ101:積極的概念驗證開啟適應症擴展 u üu >100 名受試者給藥,令人信服的臨牀活動有吸引力的靶產品在皮膚 T 細胞特徵中顯示出有利於治療淋巴瘤 (CTCL) 患者 CTCL 患者的安全性和耐受性 ü{ br} üIND 開放並在醫學皮膚病學中使用 jaKi 現在正在進行中 2/3 期為概念驗證研究開闢了機會 areecia areata 29

EQ101:有價值的醫學皮膚科特許經營權 EQ101 在醫學皮膚病學領域存在數十億美元 市場機會 660 萬美元 250,000 美元 25,000 美元 24,000 名成人 150 萬以上美國中度至重度中度-1 3 名美國患者患者 2 4 名患者嚴重患者皮膚 T 細胞脱髮 Areata 白癜風特應性皮炎淋巴瘤 PoC 已實現第 2 階段研究正在進行未來機會 2/3 階段準備就緒 • 只有兩項美國食品藥品管理局批准:jaKi • 只有一項美國食品藥品管理局批准:jaKi • 3 FDA 批准的 jaKi Open IND • 後期階段行業管線 • 後期行業管線 • 大型難治藥物 • 對需要安全的、主要是JaKi的人羣和有效的療法安全治療替代方案的需求未得到滿足 1) Kx Advisors 2) Benigno,Clin Cosmet Investig Dermatol,2020 3) Bergqvist C,Ezzedine K. Vitiligo:綜述。皮膚病學。2020 30 4) Chiesa Fuxench ZC,J Invest Dermatol。2019

EQ101:斑禿的靶向治療方法 IL-2、IL-9 和 IL-15 是斑禿疾病的關鍵驅動因素,它促進了毛囊中幹擾素γ生成增加和免疫細胞攻擊的循環 ifn-γ CD4 IL-2 驅動炎症 IL-15 和脱髮 IL-9 NK CD8 IL-15 31 Xing 等人,Nat.Med.,2014;Bertolini 等人,PLOS,2014 年;Suarez-Farinas 等人,J Allery Clin Immunol,2015;Dai 等人,JCI Insight,2021

EQ101 逆轉小鼠免疫介導的脱髮 EQ101 在人源化脱髮模型中在頭髮再生和抑制細胞毒性 CD8+ T 細胞方面比 ruxolitinib 更有效 EQ101 降低 CD8+ 細胞毒性 EQ101 改善頭髮再生 T 細胞激活標誌物 NKG2D 140 EQ101 2 mg/kg 120 IV 2x/week 100 80 第 0 天 14 天 21 60 40 Ruxolitinib 30 mg/kg 20 2x/day 0 PBS Ruxolitinib EQ101 第 0 天第 14 天 21 32 內部數據和 Azimi 等人,AHRS,佛羅裏達州奧蘭多 2018;Frohna 等人,脱髮研究峯會,紐約,紐約,2018 年 Fold over 控制

EQ101:斑禿臨牀綜述
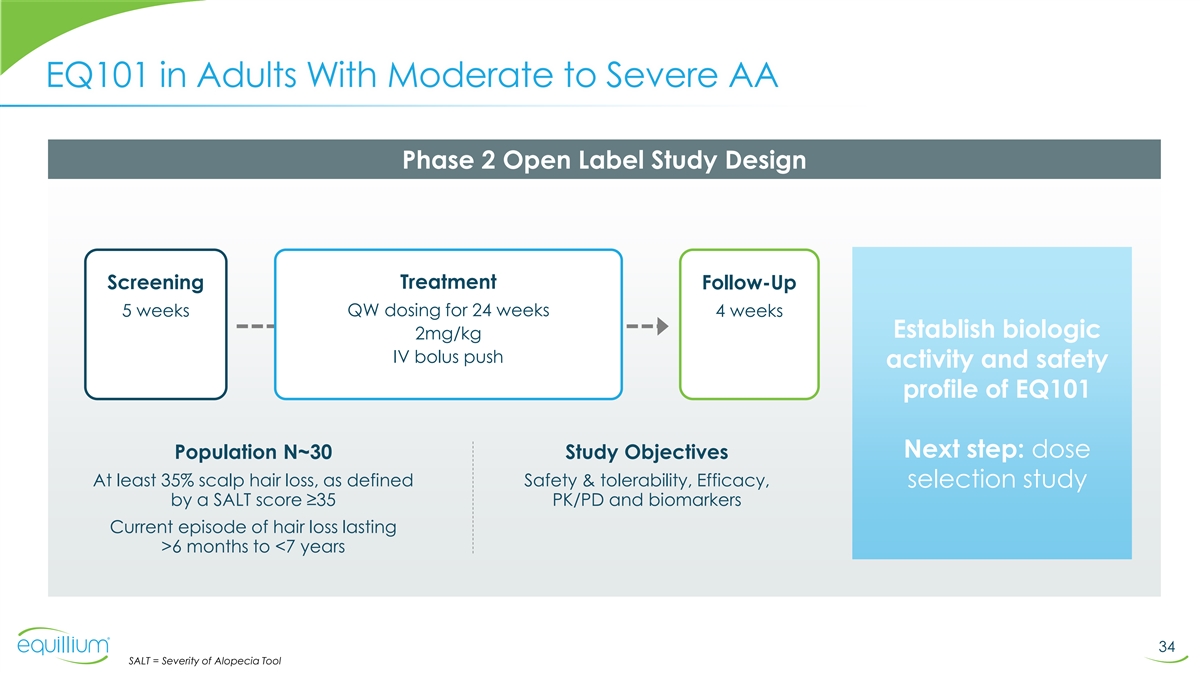
EQ101 在患有中度至重度的成人 AA 2 期開放標籤研究 設計治療篩查隨訪 5 周 QW 劑量 24 周 4 周建立生物 2mg/kg 靜脈注射推注活性和安全性概況下一步:劑量人羣 N~30 研究目標頭皮脱髮至少 35%,根據定義安全性 和耐受性、療效、SALT 評分 ≥ 35 PK/PD 的選擇研究以及生物標誌物當前脱髮發作持續 >6 個月到 EQ101

斑禿試驗説明療效棒和低安慰劑率 Ritlecitinib 來自 Ph 2 和 Allegro-2b/3 研究的結果:安慰劑受試者在 24 周時的 SALT 分數下降不到 6% SALT 評分較基線變化不到 6% baricitinib deuruxolitinib deuruxolitinib deuruxolitinib deuruxolitinib deuruxolitinib 來自 THRIVE AA1 的結果 Deuruxolitinib SALT = 脱髮工具的嚴重程度巴瑞替尼對嚴重斑禿患者的療效和安全性來源:禮來公司和康康特製藥公司和輝瑞 35 King 等人 J Am Acad Dermatol 2021;King 等人 Lancet2023 年 SALT 分數的平均百分比相對變化平均值 SALT 分數的相對變化百分比

巴瑞替尼研究中基於基線嚴重程度的 SALT 反應 SALT 分數 ≤20 反應率 SALT 評分 ≤20 反應率 baricitinib 2-mg baricitinib 4-mg EQ101 研究 EQ101 研究 24 周治療 24 周治療斑禿患者的安慰劑反應率非常低:治療 36 周時 95 36 Taylor 等人 2022 JAAD,P35766

Alopecia Areata Pipeline:後期資產®® OLUMIANT LITFULO SOTYKTU LY3009104 PF-06651600 CTP-543 SHR0302 BMS-986165 ASLAN003 ADX-914 HXN-7734 baracitinib ritlecitinib deuruxolitinib jaktinib ivarmacitinib deucravacitinib etrasimod deucravacitinib etrasimod farudostat bempikibart daxdilimab 批准的 P3 數據: 關鍵日期 NDA:2023 年上半年 P3 數據:2024 年 P2 數據:2024 年第三季度 P2 數據:2023 年第四季度 P2 數據:2024 年第一季度 P2 數據:2023 年第三季度 2022 年 6 月 2023 年 7 月 2024 年 7 月 MoA JAK1/2 JAK1/2 JAK1 TYK2 S1P 拮抗劑 DHODH anti-il7ra mab phase 3 第三階段第三階段Status MARKETED MARKETED 第二階段第二階段第二階段已完成(僅限中國)(僅限中國)美國批准 AA、RA、COVID AA 無無無牛皮癬無無無 P2/3(n=764、2 年 4 P3(n=706、1 年月、75 個地點)p2b/3(n=718)5mo,72 個地點)試驗/規模 P3(n=44 20) P3 (n=330) P2 (n=90) P2 (n=80) P2 (n=60) P2 (n=40) P2 (n=40) P2 (n=30) P3 (=546,1 年 6mo,P3 LT 正在進行中 P3(n=517,1 年 98 個地點)1 個月,63 個地點)鹽 ≥ 50 鹽 ≥ 50 鹽 ≥ 50 鹽 ≥ 50 SALT ≥ 50 鹽 ≥ 50 鹽 ≥ 25 到

目前對斑禿治療格局的擔憂 EQ101 完全有能力成為 JAK 抑制劑耐受性更好、更有效的替代品 ** 目前已獲批准且處於後期階段的 Blackbox 警告 “我很擔心警告:嚴重感染、死亡、在線藥物都是 JAK 抑制劑關於惡性腫瘤、重大心血管不良事件 (MACE) 和血栓形成口服 JAK 抑制劑的安全性 抑制劑查看完整的處方信息以獲取完整的盒裝警告。如果沒有包括結核病(TB)在內的安全慢性治療,仍然存在慢性需求,* • 如果沒有包括結核病(TB)在內的安全慢性治療,患嚴重細菌、真菌、 病毒以及我的 AA 患者機會性感染導致住院或死亡的風險增加。如果發生嚴重感染,請中斷OLUMIANT的治療,直到感染率達到 受訪者的百分比,n = 101 對照。皮膚科醫生認為安全性結核病患者不應服用 OLUMIANT。在治療前和治療期間進行潛伏性結核病檢測,COVID-19 除外;使用前先治療潛伏性結核病。在治療期間監測所有患者 是否存在活動性結核病,甚至擔心的是主要障礙 13% 的患者最初的潛伏性結核病檢測呈陰性。(5.1) • 全因死亡率更高,包括在 AA 患者中突然使用 jaKi 使用另一種Janus激酶抑制劑 (JAK) 與類風濕關節炎 (RA) 患者的腫瘤壞死因受體阻滯劑相比。(5.2) 21% • 接受治療的患者出現惡性腫瘤用 OLUMIANT。在接受調查的醫生中,淋巴瘤和肺癌的發病率更高,在關節炎患者中, 另一種JAK抑制劑與腫瘤壞死因子阻滯劑相比。(5.3) • 關節炎患者的MACE(定義為心血管死亡,66% 的人認為另一種JAK抑制劑的心肌梗死和中風發生率極高)與腫瘤壞死因子受體阻滯劑相比。(5.4) * 未滿足的醫療需求較高 79 • Thrombobogo 阻滯劑接受OLUMIANT治療的患者出現了這種情況。與腫瘤壞死因子受體阻滯劑相比,使用另一種 JAK 抑制劑會增加肺栓塞、靜脈和動脈血栓形成的發生率。(5.5) n 不同意 n Neutral n 同意 38 * Spherix Global Insights;** Olumiant 包裝説明書

Arash Mostaghimi 博士 Alopecia Areata 爐邊聊天 Arash Mostaghimi, 醫學博士、M.P.A.、M.P.H.。皮膚病學副教授哈佛醫學院皮膚病學副教授布里格姆婦女醫院皮膚科住院諮詢服務主任

問題 1 你如何治療 不同嚴重程度的斑禿患者(SALT 評分),特別是鑑於 JaKi 在去年 AA 中獲得批准?患者更喜歡什麼治療方法?40

斑禿治療 • 主要問題:安全、有效、 持續給藥 • 疾病有限(95% 的患者)• 沒有治療 • 局部療法(療效非常有限)• 可注射類固醇 • 廣泛疾病 • 全身免疫抑制劑 (抗代謝藥、潑尼鬆)• 某些生物製劑(dupilumab)的潛在作用 • JINIAK 抑制劑(baricity)b、ritlecitinib、deuruxolitinib)來自哈佛醫學院副教授 Arash Mostaghimi 博士的 41 張幻燈片

對當前療法深感不滿 DOI: 10.4103/ijt.ijt_53_17 42 來自哈佛醫學院副教授 Arash Mostaghimi 博士的幻燈片

患者影響 • 對生活質量的影響各不相同,但往往是深遠的 • 抑鬱、焦慮、情緒行為、急性壓力的發生率更高 • 影響學校、工作和人際關係的表現 • 創傷性、不可預測的疾病,1/3 符合創傷後應激障礙標準來源:DOI: 10.1007/s13555-021-00512-0 43 哈佛醫學院副教授 Arash Mostaghimi 博士的幻燈片

問題 2 經過 JaKi 的批准,在治療斑禿方面是否還有未滿足的需求?有人擔心長期使用 JaKi 嗎?44

我們今天的位置哈佛醫學院副教授 Arash Mostaghimi 博士的 45 張幻燈片

下一步:靶向療法 • JAK 抑制劑取得了巨大的進步 ,但還不夠 • 專為 AA 設計的靶向療法至關重要 • 更好的療效 • 提高治療的風險/益處 • 局部治療是一個未解決的問題!• 滿足 95% 未接受美國食品藥品管理局批准治療的人的需求 • 可用作輔助療法 • 風險/益處更好 46 張來自哈佛醫學院副教授 Arash Mostaghimi 博士的幻燈片

皮膚科醫生正在尋找更安全的 JAKI 替代品 FOR AA 聲明協議:對新治療方案的需求未得到滿足的受訪者百分比(n=103)我擔心口服 JAK 抑制劑對我的 AA 患者的安全性受訪者百分比(n=101)6.4 8.1 9.0 3.8 未滿足的 AA 治療選項需求% 受訪者 (n=103) 輕度中度重度 47 Spherix Global Insights,Market Dynamix Alimix Opecia Areata(美國)2022

問題 3 你能否分享一下你對 EQ101 的 MOA 以及 在 AA 患者中的潛在用途的看法?作為一名臨牀醫生,你希望在這項研究中觀察到什麼?48

我們應該如何衡量成功?• 對於概念驗證研究, 希望看到早期活動,然後繼續研究以優化劑量和給藥 • 不用擔心接受注射治療,但能夠持續長出頭髮並感到自信 • 速度可能不那麼重要 • 我們希望患者過上充實而幸福的生活 49 張來自哈佛醫學院副教授 Arash Mostaghimi 博士的幻燈片

最後的想法 • AA 作為一種疾病具有獨特的特性 — 我們 不能像牛皮癬和特應性皮炎那樣治療它 • 需要安全的慢性長期治療,醫生和患者將目光投向了 JAKI 之外 • 系統性治療還處於早期階段——請在這個領域進行創新 50 張來自哈佛醫學院副教授 Arash Mostaghimi 博士的幻燈片

謝謝 MOSTAGHIMI 博士可供問答 Arash Mostaghimi,醫學博士, M.P.A.,M.P.H.。皮膚病學副教授哈佛醫學院皮膚病學副教授布里格姆婦女醫院皮膚科住院諮詢服務主任

Equillium:短期預測 1.來自脱髮 areata 研究的 EQ101 初始數據預計將在年底之前公佈,其次是預計在 2024 年中期的頂線數據 2。EQ102 SAD/MAD 數據預計將在第三年年底之前公佈。伊託珠單抗:• 來自EQUALISE研究的狼瘡性腎炎數據將於11月在ASN和ACR上公佈, 隨後預計將於明年初公佈頂線數據 • 預計將於2024年對EQUATOR研究的AgvHD數據進行中期審查 • 小野行使決定和可能的期權支付 52

謝謝 www.equilliumbio.com