
EMERALD-1 完整數據演示文稿 2023 年 10 月 12 日

本演示文稿包含1995年《私人證券訴訟改革法》“安全港” 條款所指的 “前瞻性” 陳述,包括但不限於有關Morphic正在進行的臨牀試驗的時機和成功以及相關數據、Morphic臨牀試驗的最新和結果以及 MORF-057 的潛在治療益處的陳述。本演示文稿中的某些數據基於交叉研究比較,而不是基於任何正面交鋒的臨牀試驗。跨研究比較本質上是有限的,可能暗示誤導性的相似之處和不同之處。交叉研究比較中顯示的值是方向性的,可能無法直接比較。包括諸如 “相信”、“計劃”、“繼續”、“期望”、“將”、“發展”、“信號”、“潛在” 或 “正在進行” 之類的詞語的陳述以及將來時態的陳述均為前瞻性陳述。這些前瞻性陳述涉及風險和不確定性以及假設,如果這些假設沒有完全實現或被證明是不正確的,則可能導致我們的業績與此類前瞻性陳述所表達或暗示的結果存在重大差異。前瞻性陳述存在風險和不確定性,這些風險和不確定性可能導致Morphic的實際活動或業績與任何前瞻性陳述中表達或暗示的活動或業績存在顯著差異,包括與本演示文稿中的前瞻性陳述相關的風險和不確定性,以及我們在向美國證券交易委員會(SEC)提交的文件中列出的其他風險,包括2023年2月23日向美國證券交易委員會提交的截至2022年12月31日財年的10-K表年度報告和季度報告 10-Q 表格截至2023年6月30日的財季已於2023年8月3日向美國證券交易委員會提交。這些前瞻性陳述僅代表截至本文發佈之日,除非法律要求,否則Morphic明確否認任何義務更新這些前瞻性陳述或實際結果可能存在差異的原因,無論是由於新信息、未來事件還是其他原因。商標註意事項:本演示文稿中提及的所有第三方商標,包括名稱、徽標和品牌,均為其各自所有者的財產。所有提及第三方商標僅用於識別目的,根據商標法,應被視為名義上的合理使用。2 前瞻性陳述

• 主要終點已達到,關鍵指標均出現一致和預期的臨牀改善 • 患者的 PK 與健康志願者一致 • RO 和 T 細胞亞羣與健康志願者一致 • 總體耐受性良好,未觀察到安全信號 • 患者在第 12 周之後繼續治療,尤其是難治性患者 3 2a 期研究旨在確認療效信號:結果超出預期

• 歡迎和介紹 — Chris Erdman,投資者與企業傳播高級副總裁 • 試驗設計、患者處置、安全、PK/PD — Brihad Abhyankar 博士,形態療法臨牀開發高級副總裁 • 詳細的臨牀療效結果 — 形態治療總裁布魯斯·羅傑斯博士 • 結論性想法和公司最新消息 — Marc Schegerin博士,形態治療首席運營官兼首席財務官 • 問答 — Brian Feagan 博士 — Morphic Team 4 議程

EMERALD-1 試驗設計和患者處置
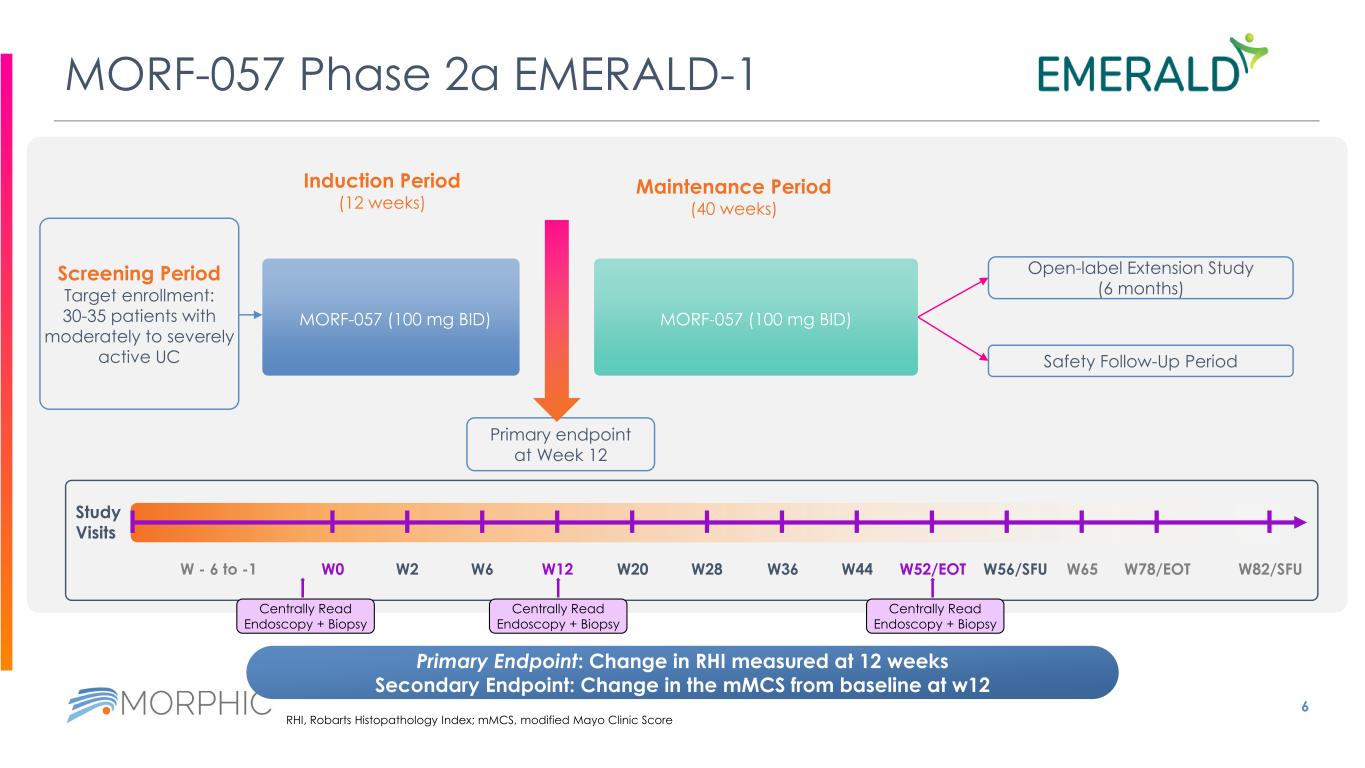
6 MORF-057 2a 期 EMERALD-1 誘導期(12 周)維持期(40 周)主要終點:12 周時測得的 RHI 變化次要終點:w12 開放標籤擴展研究(6 個月)MMC 與基線相比的變化安全隨訪期篩查期目標入組:第 12 周有 30-35 名中度至重度活躍的 UC 主要終點患者 MORF-057(100 mg BID)RHI,修改後的 MMC,Mayo Clinic Score 研究訪問量 W0 W2 W6 W12 W20 W28 W36 W44 W52/EOT W82/SFUW56/SFU W65 W78/EOTW-中央 6 比 -1閲讀內窺鏡檢查 + 活檢集中閲讀內窺鏡檢查 + 活檢集中閲讀內窺鏡檢查 + 活組織檢查 MORF-057(100 mg BID)
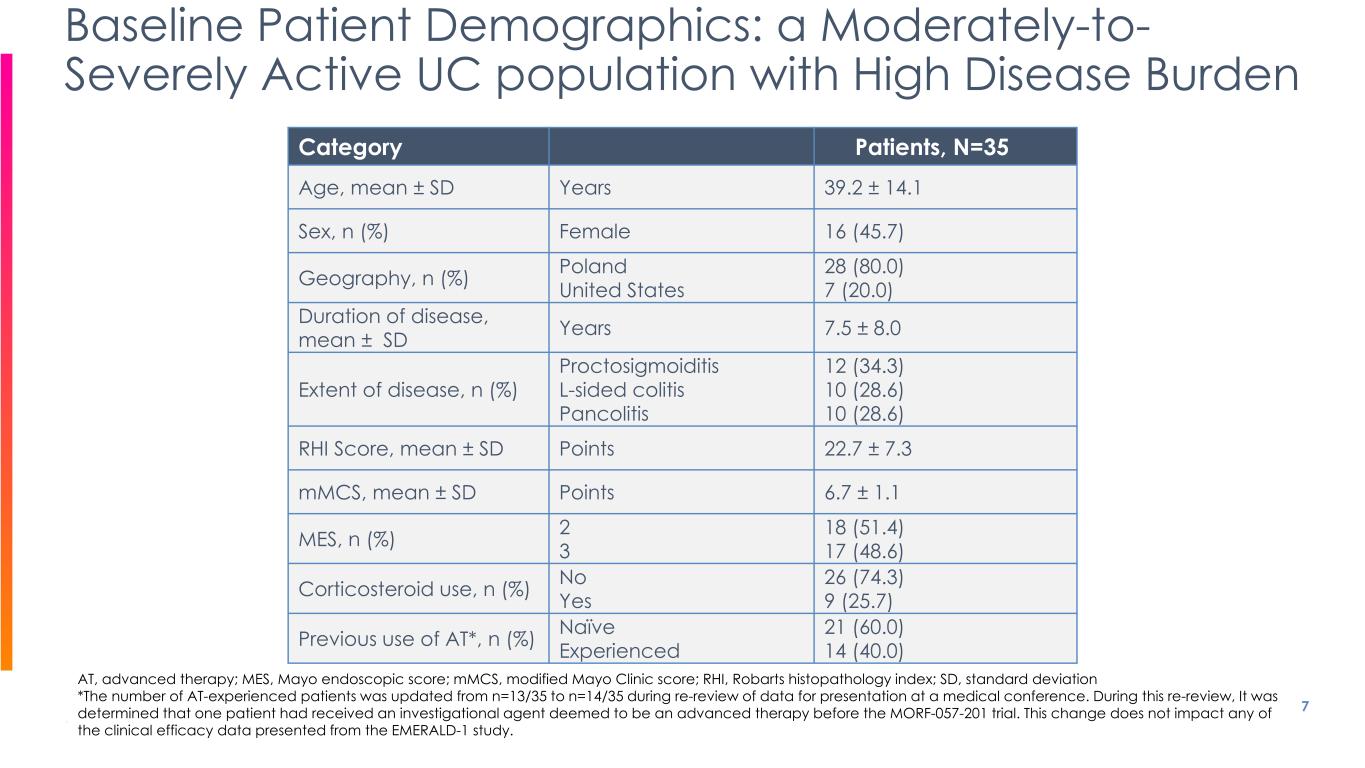
類別患者,N=35 年齡,平均值 ± SD 年份 39.2 ± 14.1 性別,n (%) 女性 16 (45.7) 地理,n (%) 波蘭美國 28 (80.0) 7 (20.0) 疾病持續時間,平均值 ± SD 年份 7.5 ± 8.0 疾病程度,n (%) 直腸乙狀結腸炎 L 側結腸炎 12 (34.3) 10 (28.6) 10 (28.6) 10 (28.6) RHI 分數,平均值 ± SD 分數 22.7 ± 7.3 mmcS,平均值 ± SD 分數 6.7 ± 1.1 MES,n (%) 2 3 18 (51.4) 17 (48.6) 皮質類固醇的使用,n (%) 否是 26 (74.3) 9 (25.7) 之前使用過 AT*,n (%) Naive Experience 21 (60.0) 14 (40.0) 7 基線患者人口統計:中度至-重度活躍的加州大學人羣,疾病負擔高 AT,高級治療;MES,梅奧內窺鏡評分;MMC,修改後的梅奧診所評分;RHI,Robarts 組織病理學指數;SD,標準差 *在重新審查供在醫學會議上公佈的數據時,有AT經驗的患者人數從n=13/35更新為n=14/35。在這次重新審查中,確定一名患者在 MORF-057-201 試驗之前接受了一種被視為高級療法的研究藥物。這一變化不會影響 EMERALD-1 研究中提供的任何臨牀療效數據。
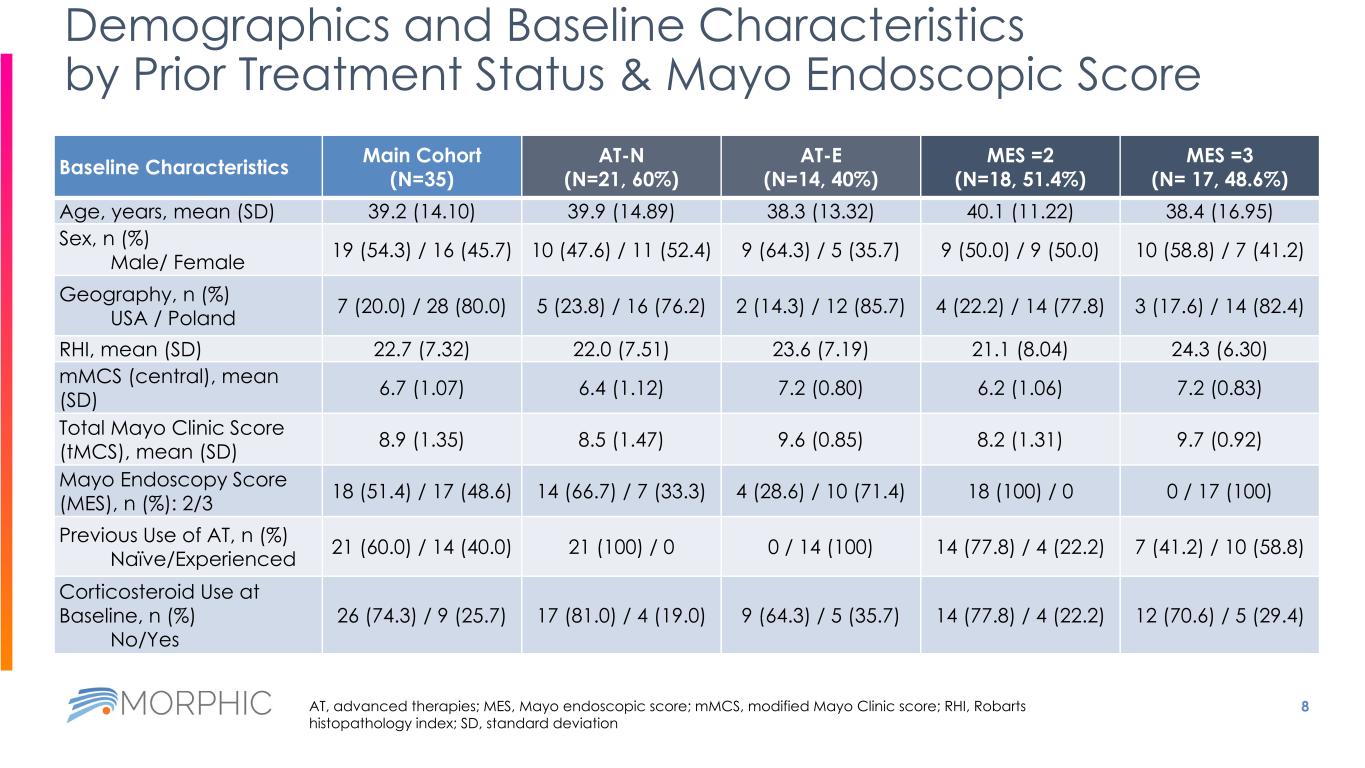
8 按先前治療狀況和梅奧內窺鏡評分劃分的人口統計學和基線特徵基線特徵主隊列(N=35)AT-N(N=21,60%)AT-E(N=14,40%)MES =2(N=18,51.4%)MES =3(N= 17,48.6%)年齡、年份、平均值(SD)39.2(14.10)39.9(14.89)38.3(13.32)48.3(13.32)48.3(13.32)48.3(13.32)48.3(13.32)48.3(13.32)48.3(13.32)48.3(13.32)48.3(13.32)0.1 (11.22) 38.4 (16.95) 性別,n (%) 男/女 19 (54.3)/16 (45.7) 10 (47.6)/11 (52.4) 9 (64.3)/5 (35.7) 9 (50.0) /9 (50.0) 10 (58.8) /7 (41.2) 地理,n (%) 美國/波蘭 7 (20.0))/28 (80.0) 5 (23.8) /16 (76.2) 2 (14.3) /12 (85.7) 4 (22.2) /14 (77.8) 3 (17.6) /14 (82.4) RHI,平均值 (SD) 22.7 (7.32) 22.0 (7.51) 23.6 (7.19) 21.1 (8.04) 24.3 (6.30) mmc(中央),平均值(SD)6.7(1.07)6.4(1.12)7.2(0.80)6.2(1.06)7.2(0.83)梅奧診所總分(TMC),平均值(SD)8.9(1.35)8.5(1.47)9.9(1.35)9.4(1.47)9.6 (0.85) 8.2 (1.31) 9.7 (0.92) Mayo 內窺鏡檢查分數 (MES),n (%):2/3 18 (51.4)/17 (48.6) 14 (66.7)/7 (33.3) 4 (28.6)/10 (71.4) 18 (100)/0 0/17 (100) 以前使用過自動變速器,n (%) 天真/經驗豐富 21 (60.6) 0)/14 (40.0) 21 (100)/0 0/ 14 (100) 14 (77.8)/4 (22.2) 7 (41.2)/10 (58.8) 基線使用皮質類固醇,n (%) 否/是 26 (74.3)/9(25.7) 17 (81.0)/4 (19.0) 9 (64.3) /5 (35.7) 14 (77.8) /4 (22.2) 12 (70.6)/5 (29.4) AT,高級療法;MES,梅奧內窺鏡評分;MMC,修改後的梅奧診所分數;RHI,Robarts 組織病理學指數;SD,標準差

安全性和耐受性

終點患者,N = 35 名 TEAE ≥ 1 的患者,n (%) 12 (34.3) 嚴重 TEAE,n (%) 0 AE 導致死亡,n (%) 0 患有 3 級 TEAE 的患者,n (%) UC 惡化 a 2 (5.7) 常見 TEAE (> 5%),n (%) UC 惡化 Anemiab,c 4 (11.4) 3 (8.6) 治療與 MENT 相關的 TEAE,n (%) 2 (5.7) 10 MORF-057:EMERALD-1 中總體耐受性良好未觀察到安全信號(截至 23 年 10 月 10 日)a. UC 加重一次導致提前停藥 b. 所有貧血事件都發生在基線時患有貧血並繼續研究鐵補充劑的患者。c. A.三分之一的炎症性腸病患者患有缺鐵性貧血 TEAE,即急需治療的不良事件;UC,潰瘍性結腸炎 *數據顯示 12 周的誘導期;截至 2013 年 10 月 10 日,患者已在 12 周的誘導期之後繼續接受 EMERALD-1 研究,沒有其他安全信號或 SAE 的報告。

PK/PD 和生物標誌物數據
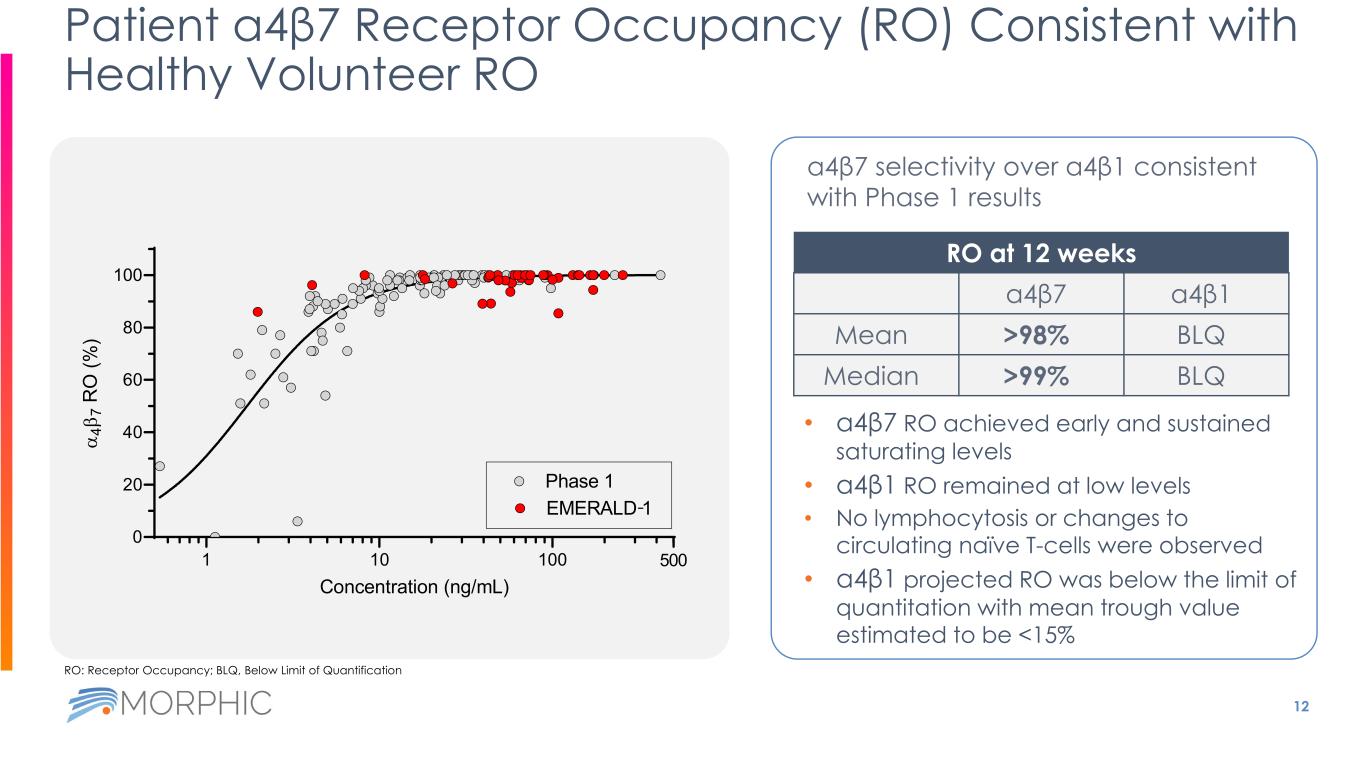
• a4β7 RO 早期達到持續飽和水平 • a4β1 RO 保持在較低水平 • 未觀察到淋巴細胞增多或循環的天真 T 細胞發生變化 • a4β1 預計反滲透低於定量極限,平均低谷值估計為 98% BLQ 中位數 > 99% BLQ 1 10 100 0 20 40 60 100 500 濃度 (ng/mL) 4β 7 R O (%) 第 1 階段 EMERALD 1-RO:受體佔用率;BLQ,低於定量極限
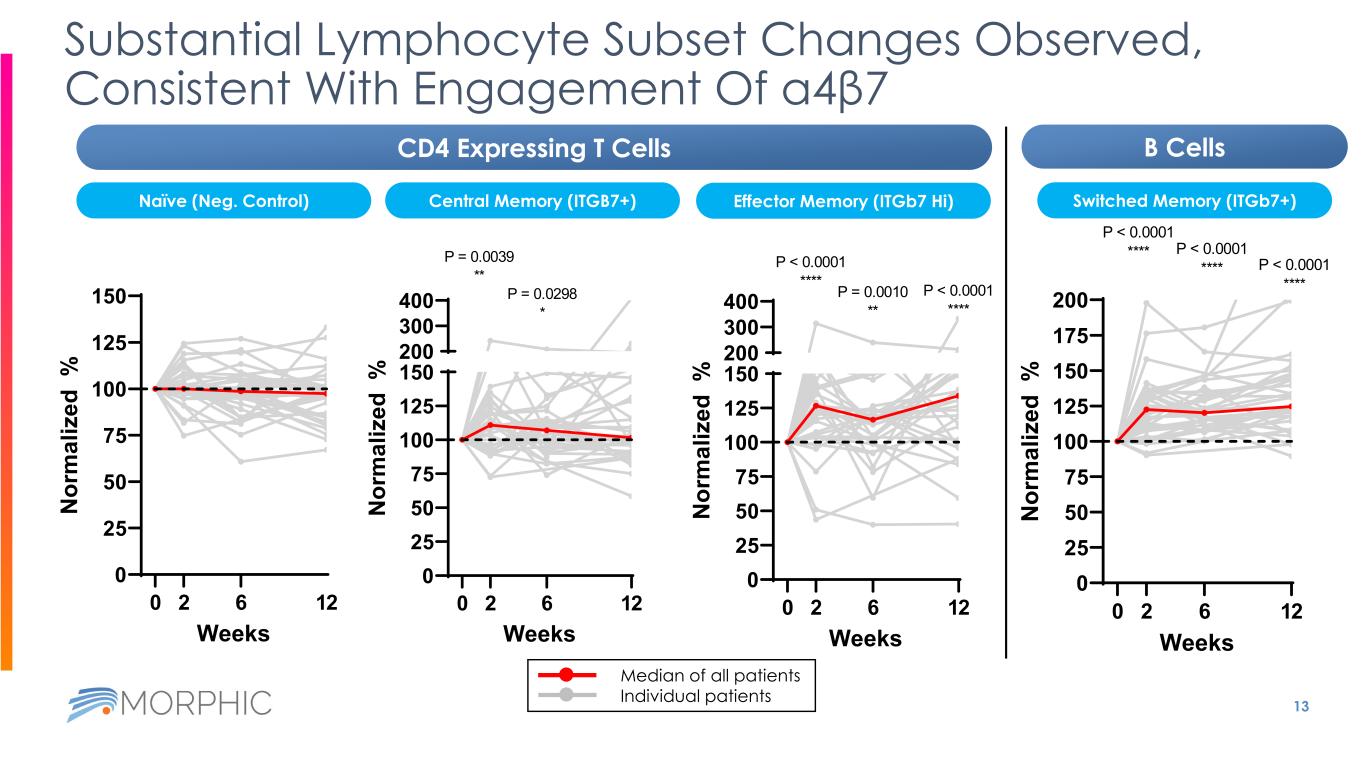
13 觀察到淋巴細胞子集的顯著變化,與 α4β7 的參與度一致 0 25 50 75 100 125 150 周 N 或 m al iz ed% 0 2 6 12 0 25 50 75 100 125 150 300 400 周 N 或 m al iz% P = 0.0039 ** 0 2 6 12 P = 0.0298 * 0 25 50 75 100 150 300 400 Weeks n or m al iz% 0 2 6 12 P = 0.039 * 0 2 6 12 P = 0.0298 * 0 25 50 75 100 150 300 weeks n or m al iz% 0 2 6 12 P
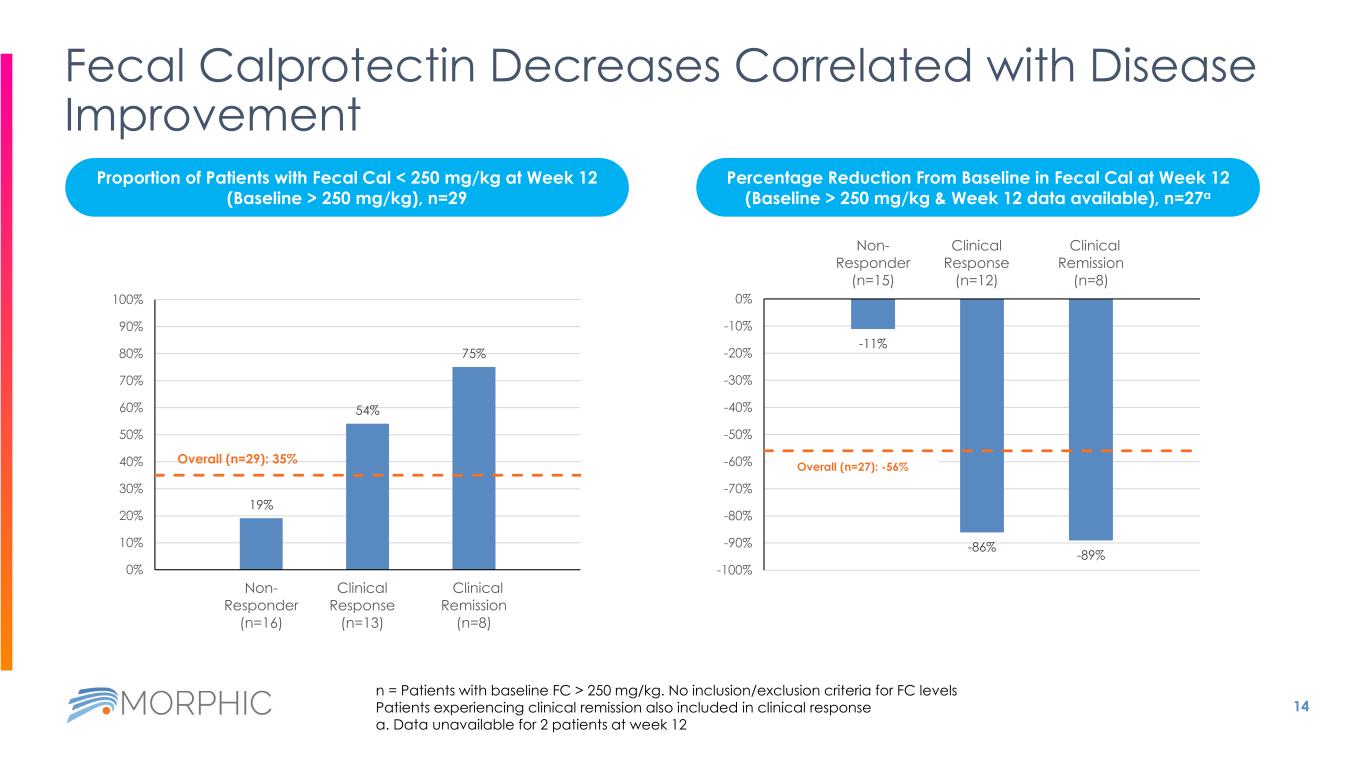
14 糞便鈣保護素降低與疾病改善相關 19% 54% 75% 總體(n=29):35% 0% 10% 20% 30% 40% 50% 60% 70% 90% 100% 非應答者 (n=16) 臨牀反應 (n=13) 臨牀緩解 (n=8) -11% -86% -89% 總體 (n=27):-56% -100% -90% -80% -60% -40% -30% -20% -10% 0% 非反應者 (n=15) 臨牀反應 (n=12) 臨牀緩解 (n=8) n = 基線 FC > 250 mg/kg 的患者。FC 水平沒有納入/排除標準臨牀反應中也包括臨牀緩解的患者 a. 第 12 周未提供 2 名患者的數據(糞便 Cal 250 mg/kg 患者的比例),n=29 第 12 周糞便鈣含量較基線降低百分比(基線 > 250 mg/kg,第 12 週數據可用),n=27a
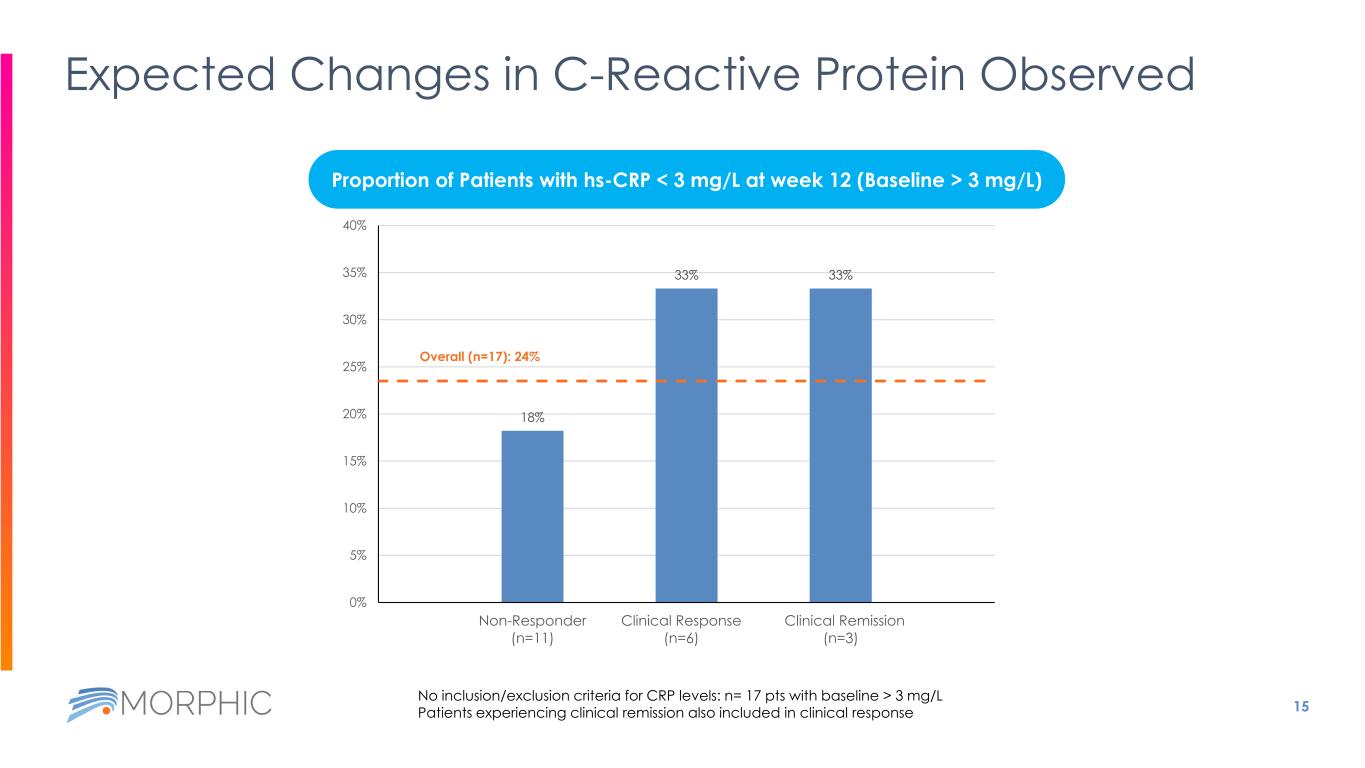
15 觀察到 C 反應蛋白的預期變化 18% 33% 33% 總體(n=17):24% 0% 5% 10% 15% 25% 30% 35% 40% 無反應者(n=11)臨牀反應(n=6)臨牀緩解(n=3)CRP 水平沒有納入/排除標準:n= 17 pts 基線 > 3 mg/L 臨牀緩解患者也包括在臨牀反應中 hs-CRP 患者比例 3 mg/L L)

臨牀療效結果
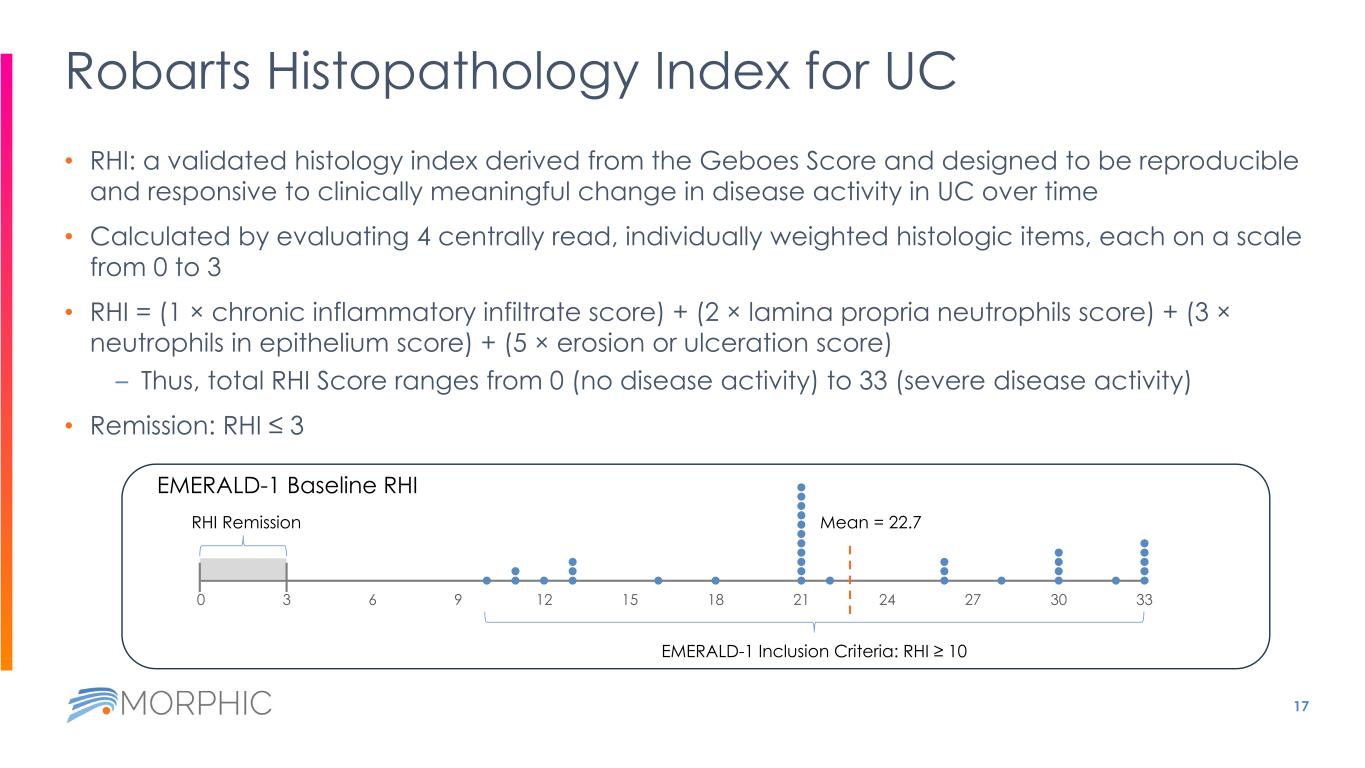
• RHI:一種源自 Geboes Score 的經過驗證的組織學指數,旨在可重複且對加州大學中疾病活動隨時間推移發生的有臨牀意義的變化做出反應 • 通過評估 4 個集中讀取、單獨加權的組織學項目計算得出,每個項目從 0 到 3 • RHI =(1 × 慢性炎性浸潤分數)+(2 × 中性粒細胞固有層評分)+(3 × 中性粒細胞分數)+(3 × 中性粒細胞分數)+(3 × 中性粒細胞)上皮細胞評分)+(5 × 侵蝕或潰瘍評分)— 因此,RHI 總分從 0(無疾病活動)到 33(嚴重疾病活動)• 緩解:RHI≤ 3 17 Robarts 加州大學組織病理學指數 0 3 6 9 12 15 18 21 24 27 30 33 Mean = 22.7RHI 緩解 EMERALD-1 基線 RHI EMERALD-1 納入標準:RHI ≥ 10

18 修改後的加州大學梅奧診所分數 • 修改後的梅奧診所分數 (MMC) — 三部分分數 — 0 到 9 量表,中度至重度 UC 5 到 9 — 臨牀緩解 • SFS ≤ 1 • RBS = 0 • MES ≤ 1 無脆性 — 內窺鏡反應/改善:MES ≤ 1 — 症狀緩解:SFS = 0(或 = 1,比基線降低 ≥ 1 分)和 RBS = 0 — PRO2:SFS + 蘇格蘭皇家銀行

19 Endpoint @ 第 12 周總體 (N=35) RHI 變化,平均值 (SD) -6.4 (11.18) p=0.0019 RHI 緩解率,n (%) 8 (22.9%) 臨牀反應 (mmcS) 1、n (%) 16 (45.7%) 臨牀緩解 (mmcS) 2、n (%) 9 (25.7%) 內窺鏡反應/改善3、n (%) 9、n (%) 9 (25.7%) 內窺鏡反應/改善3、n (%) 9、n (%) 9 (25.7%) (25.7%) 修改後的MCS中從基線到第12周的變化,平均值 (SD) -2.3 (2.14) 主要終點具有很高的統計學顯著性在所有探索性測量中觀察到的一致效應 1.臨牀反應 (MMC):MMCs比基線降低≥2分,較基線≥ 30%,再加上直腸出血分數降低 ≥ 1 或直腸絕對出血分數 ≤1 2。臨牀緩解 (MMC):直腸出血分數為 0;大便頻率分數為 ≤1;MES 為 ≤1,無脆性 3。內窺鏡反應/改善:MES ≤1

20 按 AT 狀態和 MES 端點劃分的 EMERALD-1 療效結果 @ 第 12 周總體 N=35 at-naíve n=21 AT-experience n=14 MES =2 n=18 MES =3 n= 17 RHI 變化,平均值 ± 6.4 ± 11.2 -7.4 ± 11.9 -6.9 ± 12.1 -5.8 ± 10.4 RHI 變化 ≥ 7 個百分點,n (%) 17 (48.6) 12 (57.1) 5 (35.7) 10 (55.6) 7 (41.2) RHI 減免 1、n (%) 8 (22.9) 6 (28.6) 2 (14.3) 6 (33.3) 2 (11.8) RHI 降低 ≥ 50%,n (%) 12 (34.3) 9 (42.9) 3 (21.4) 9 (50.0) 3 (17.6) MMC 的變化,平均值 ± SD -2.3 ± 2.1 -2.9 ± 2.4 -1.6 ± 1.5 -2.7 ± 2.3 -1.9 ± 1.9 臨牀反應 (mmcS) 2、n (%) 16 (45.7)11 (52.4) 5 (35.7) 9 (50) 7 (41.2) 臨牀緩解 (mmcS) 3、n (%) 9 (25.7) 9 (25.7) 9 (42.9) 0 6 (33.3) 3 (17.6) 症狀緩解4、n (%) 11 (31.4) 10 (47.6) 1 (7.1) 7 (38.9) 4 (23.5) 內窺鏡反應/改善 ment5,n (%) 9 (25.7) 9 (42.9) 0 6 (33.3) 3 (17.6) SF 的變化,平均值 ± SD -0.8 ± 1.1 ± 1.0 ± 1.2 -0.5 ± 0.7 ± 0.9 ± 0.6 ± 0.8 ± 0.8 ± 0.7 ± 0.8 ± 0.7 ± 0.7 AT,高級療法;MCS,梅奧診所評分;MCS,Mayo Clinic 分數;MMC,修改後的 MCS;RHI,Robarts 組織病理學指數;SF,大便頻率;RB,直腸出血;SD,標準差 1.RHI 緩解:RHI ≤ 2 2。臨牀反應 (MMC):MMCs比基線降低≥2分,較基線≥ 30%,再加上直腸出血分數降低 ≥ 1 或直腸絕對出血分數 ≤1 3。臨牀緩解 (MMC):直腸出血分數為 0;大便頻率分數為 ≤1;MES 為 ≤1,無脆性 4。症狀緩解:SFS = 0(或 = 1,比基線降低 ≥ 1 個百分點)和 RBS = 0 5。內窺鏡反應/改善:MES ≤1

21 觀察到一致的 “全方位” 療效信號亞組經驗者是 (n=14) 否 (n=21) 基線使用皮質類固醇是 (n=9) 否 (n=26) 基線 MES 3 (n=17) 2 (n=18) 平均變化 (95% 置信區間) -4.8 (-10.7, 1.1) -7.4 (-12.8, -2.0) -5.2 (-11.1, 0.7) -5.2 (-11.1, 0.7)) -6.8 (-11.7, -1.8) -5.8 (-11.1, -0.4) -6.9 (-13.0, -0.9) -26 -24 -22 -20 -18 -16 -14 -12 -10 -8 -6 -4 -2 0 2 2 2 羅伯茨組織病理學指數 (RHI) 修改後的梅奧臨牀評分 (mmcS) 亞組經驗者是 (n=14) 否 (n=14) 否 (n=14) 21) 基線使用皮質類固醇是 (n=9) 否 (n=26) Baseline MES 3 (n=17) 2 (n=18)均值變化 (95% 置信區間) -1.6 (-2.4, -0.7) -2.9 (-3.9, -1.8) -1.4 (-2.3, -0.6) -2.7 (-3.6, -1.7) -1.9 (-2.9, -1.0) -2.7 (-3.9, -1.6) -8 -7 -6 -4 -3 -2 -1 0 1 均值 = -2.3
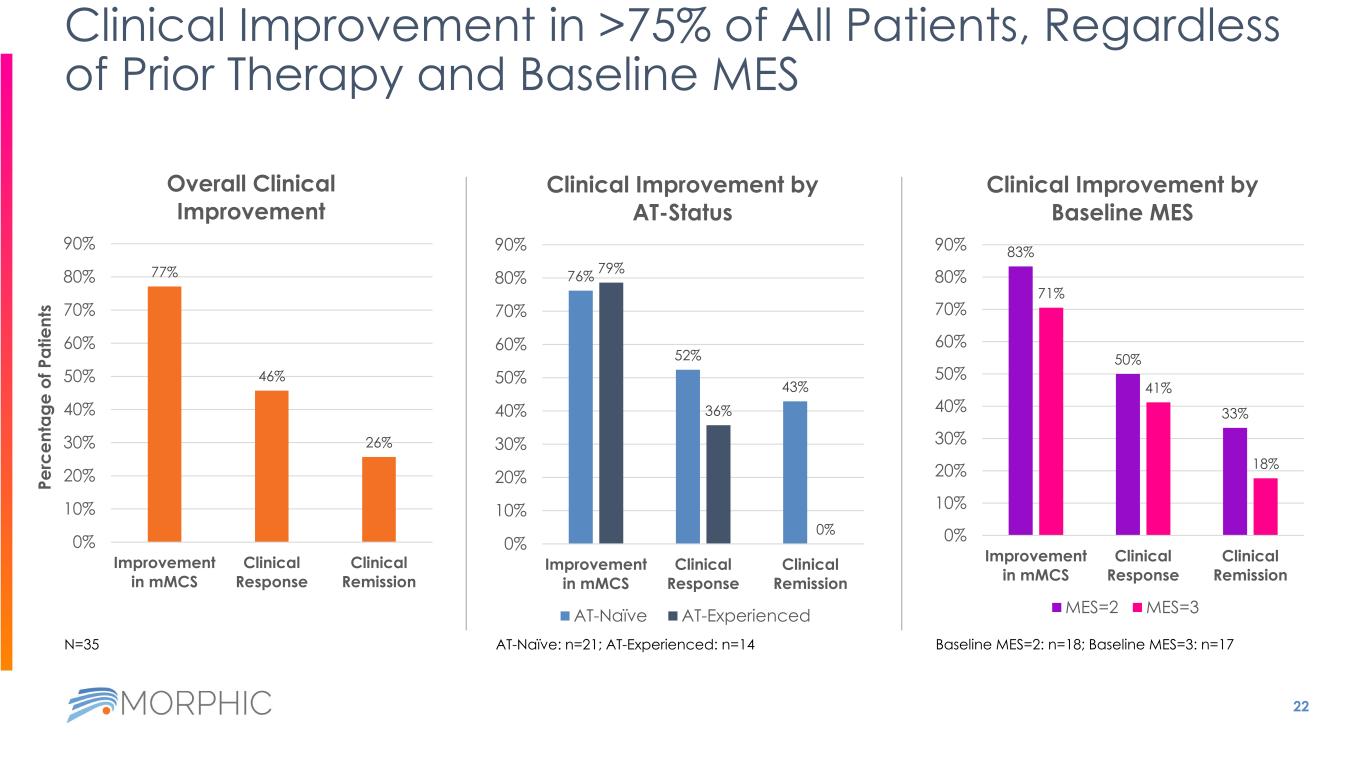
22 所有患者中超過 75% 的臨牀改善,無論之前的治療和基線如何 MES 77% 46% 26% 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% MMC 臨牀反應改善臨牀緩解總體臨牀緩解情況天真:n=21;AT 經驗:n=14 76% 52% 43% 79% 36% 0% 0% 10% 20% 40% 60% 70% 80% 90% mmC 臨牀反應改善按狀態劃分臨牀緩解率 90% at-naive AT 經驗豐富 83% 50% 33% 71% 41% 18% 0% 10% 20% 40% 50% 60% 70% 80% 90% MMC 臨牀反應臨牀緩解改善臨牀緩解基線臨牀改善 MES=2 MES=3 基線 MES=2:n=18;基線 MES=3:n=17n=35 Pe rc en ta ge o f P at ie nt s
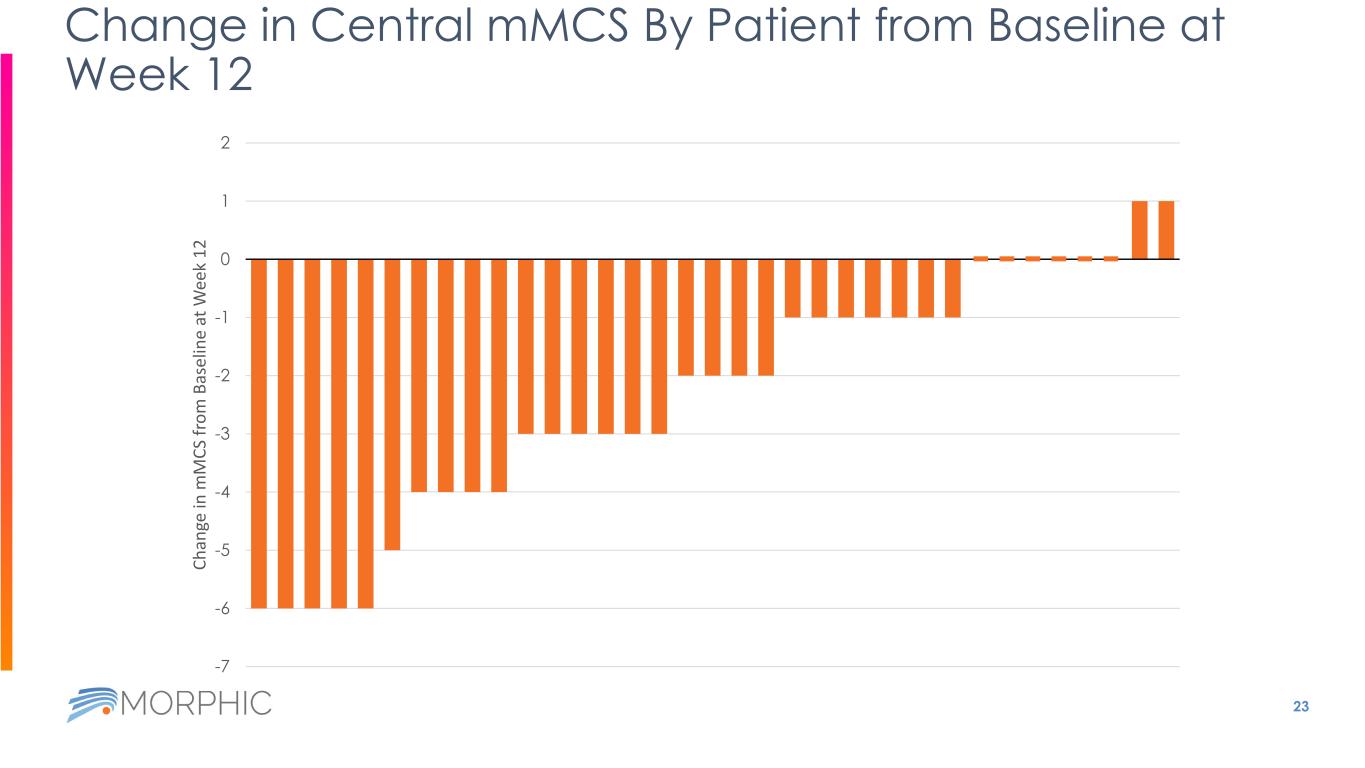
23 第 12 周患者中央 mmC 與基線相比的變化 -7 -6 -5 -4 -3 -2 -1 0 1 2 Ch 和 m M CS 中有 ge as el in e 在 W ee k 12

24 按子組劃分的中央 MMC 與基線相比的變化第 12 周 -7 -6 -5 -4 -3 -2 -1 0 1 2 Ch ang ge 在 m m CS 中為 e 在 W ee k 12 at naíve 基線 MES = 3 個有經驗的基線 MES = 3 有經驗的基線 MES = 2 反應緩解 RHI 比基線降低 ≥ 7 類固醇使用量 N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N Y N Y N Y Y Y N N N N Y N N N Y N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N N Baseline MES 2 2 2 2 2 2 2 2 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 1 1 1 AT,高級療法;RHI,Robarts 組織病理學指數;MES,Mayo 內窺鏡評分

超過 12 周的數據
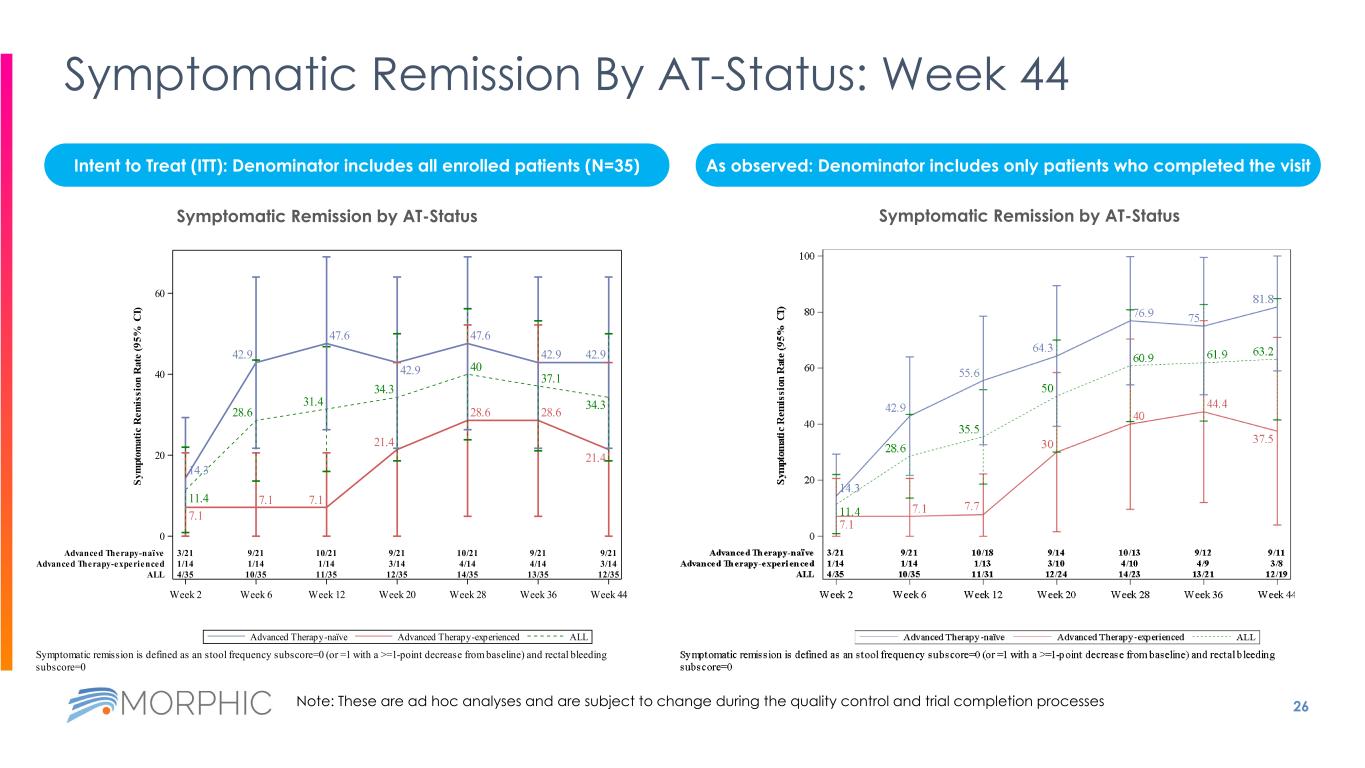
26 按狀態劃分的症狀緩解:第 44 周的治療意向 (ITT):分母包括所有入組患者(N=35)正如觀察到的那樣:分母僅包括完成就診的患者 14.3 7.1 11.4 42.9 7.1 28.6 71 31.4 42.9 21.4 34.3 42.9 28.6 37.1 42.9 34.3 9/21 10/21 9/21 10/21 9/21 9/21 1/14 1/14 1/14 3/14 4/14 4/14 4/14 3/14 4/35 10/35 11/35 12/35 14/35 13/35 12/35 第 2 周第 6 周第 12 周 20 周 28 周 36 周 44 0 20 40 60 Sy m pt om 在 ic R em 上是 si on R at e(9 5% C I)高級治療天真的高級療法經驗豐富所有 AllAdvanced Therapy-Experience Advanced Therapy-naive 症狀緩解定義為大便頻率 subscore=0 subscore=0 大便頻率 subscore=0 按狀態進行症狀緩解注意:這些是臨時分析,在質量控制和試驗完成過程中可能會發生變化
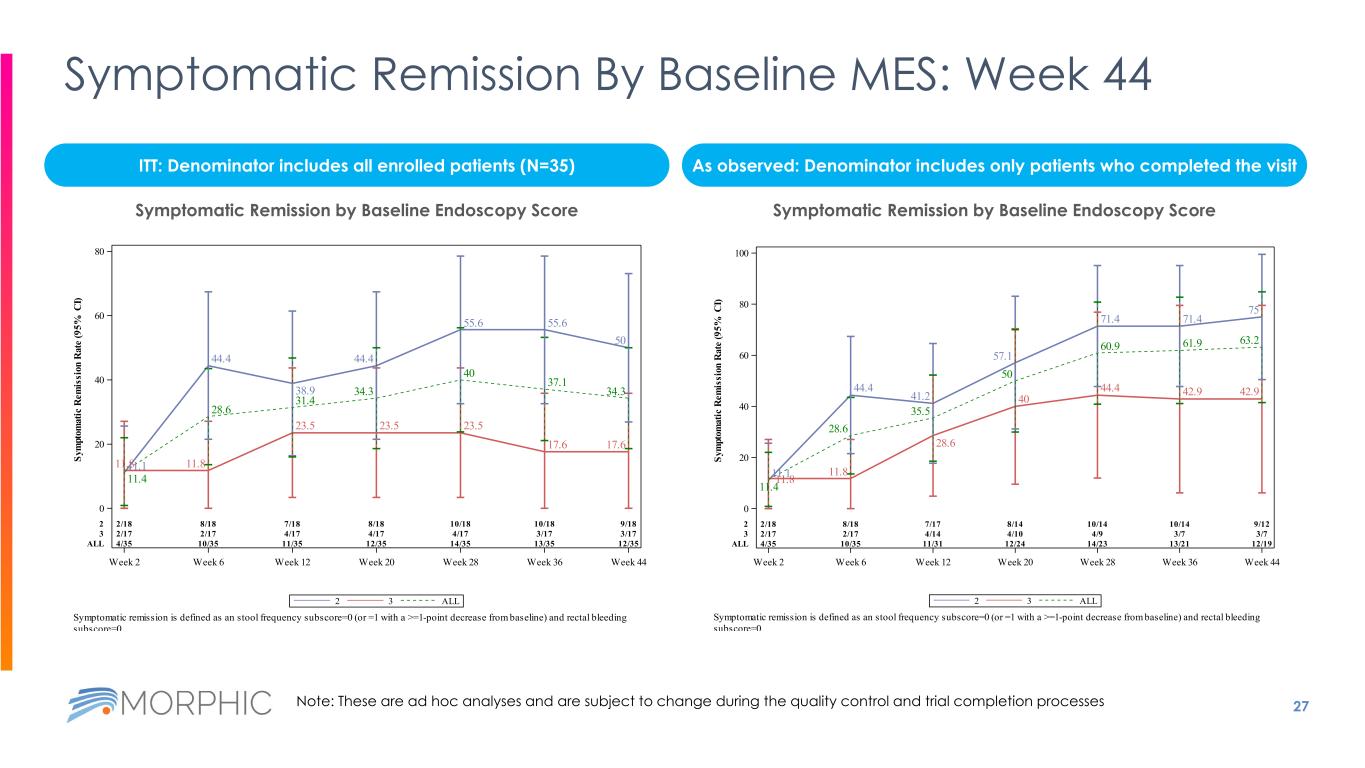
27 按基線劃分的症狀緩解 MES:第 44 周 ITT:分母包括所有入組患者(N=35)如觀察:分母僅包括完成就診的患者 11.11.8 11.4 44.4 28.6 33.5 31.4 44.4 23.5 55.6 45.6 45.6 37.1 50 17.6 34.3 2/18 8/18 7/18 9/18 10/18 9/18 2/17 23.5 33.5 55.6 55.6 37.1 50 17.6 34.3 2/18 8/18 7/18 9/18 2/18 10/18 9/18 2/17 17 4/17 4/17 4/17 3/17 3/17 4/35 10/35 11/35 12/35 12/35 12/35 第 2 周第 6 周 12 周 20 周 28 周 36 周 44 0 20 40 60 80 Sy m pt om at ic R em 是 si 在 R at e(9 5% C I)2 3 所有 ALL32 症狀緩解定義為糞便頻率 subscore=0(或=1,比基線降低 >=1)和直腸出血子分數 =0 11.11.8 11.4 44.4 11.8 28.6 41.2 28.6 35.5 57.1 40 50 71.4 44.4 61.9 75 42.9 75 42.9 63.2 2/18 8/17 8/17 8/14 9/12 2/17 4/9 3/7 3/7 4/35 10/35 11/31 12/23 13/21 12/19 第 2 周第 6 周 12 周 20 周 28 周 36 周 44 0 20 40 60 80 100 Sy m pt om at ic r em 是 R 上的 si at e(9 5% C I)2 3 所有 ALL32 y p y py py 症狀緩解定義為大便頻率 subscore=0(或 =1,比基線降低 >=1)和直腸出血 subscore=0 基線內窺鏡檢查分數症狀緩解按基線內窺鏡檢查分數計算症狀緩解注意:這些是臨時分析,在質量控制和試驗完成過程中可能會發生變化
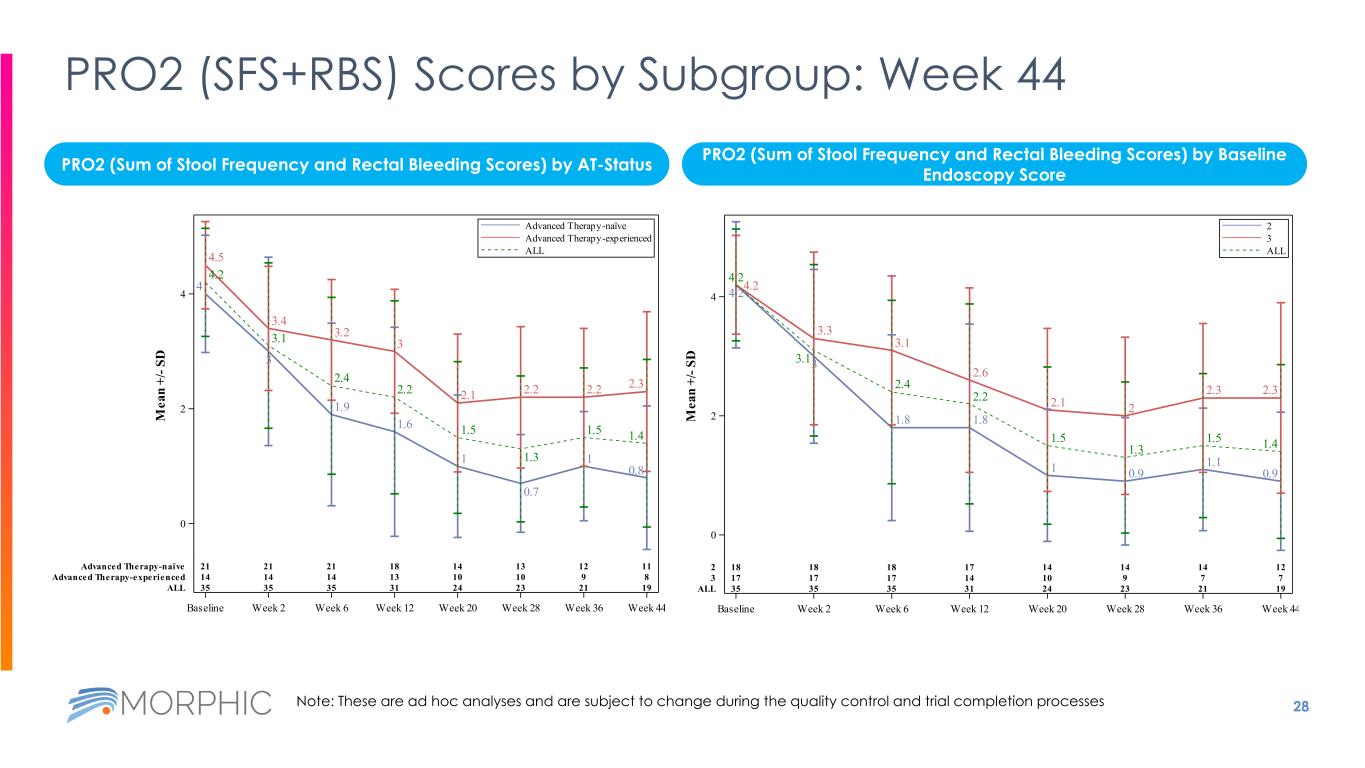
28 按子組劃分的 PRO2(SFS+RBS)分數:第 44 周 PRO2(大便頻率和直腸出血分數之和)按基線內窺鏡檢查分數劃分的 AT-Status PRO2(大便頻率和直腸出血分數之和)4.2 3.1 2.4 2.1 2 2.3 1.3 1.3 1.3 1.5 1.4 18 18 18 17 14 14 14 14 17 10 1.8 1.8 1.8 1.8 1 0.9 1.9 3.1 3.1 2.4 2.1 2.1 2.3 2.1 1.5 2.3 1.5 1.3 1.3 1.5 1.4 18 18 18 18 17 14 9 7 35 35 31 31 24 23 21 19 基準第 2 周第 6 周 12 周 20 周 28 周 36 周 44 0 2 4 M ea n +/-S D 2 3 全部 3 全部 3 2 q y g y py 4 3 1.9 1.6 1 0.7 1 0.8 4.5 3.2 3.2 2.2 2.2 2.2 3.2 3.2 3.2 3.2 2.2 3.2 2.2 2.2 3.1 2.2 2.4 1.5 1.4 1.4 21 21 1814 13 12 11 14 14 14 13 10 9 8 35 35 31 24 23 21 19 基線第 2 周第 6 周第 12 周 20 周 28 周 36 周 44 0 2 4 M ea n +/-S D 高級療法-天真高級療法經驗所有高級治療經驗過高級療法-天真注意:這些是臨時分析,在質量控制和試驗完成過程中可能會發生變化

• 主要終點已達到,關鍵指標均出現一致和預期的臨牀改善 • 患者的 PK 與健康志願者一致 • RO 和 T 細胞亞羣與健康志願者一致 • 總體耐受性良好,未觀察到安全信號 • 患者在第 12 周之後繼續治療,尤其是難治性患者 29 2a 期研究旨在確認療效信號:結果超出預期

公司最新消息
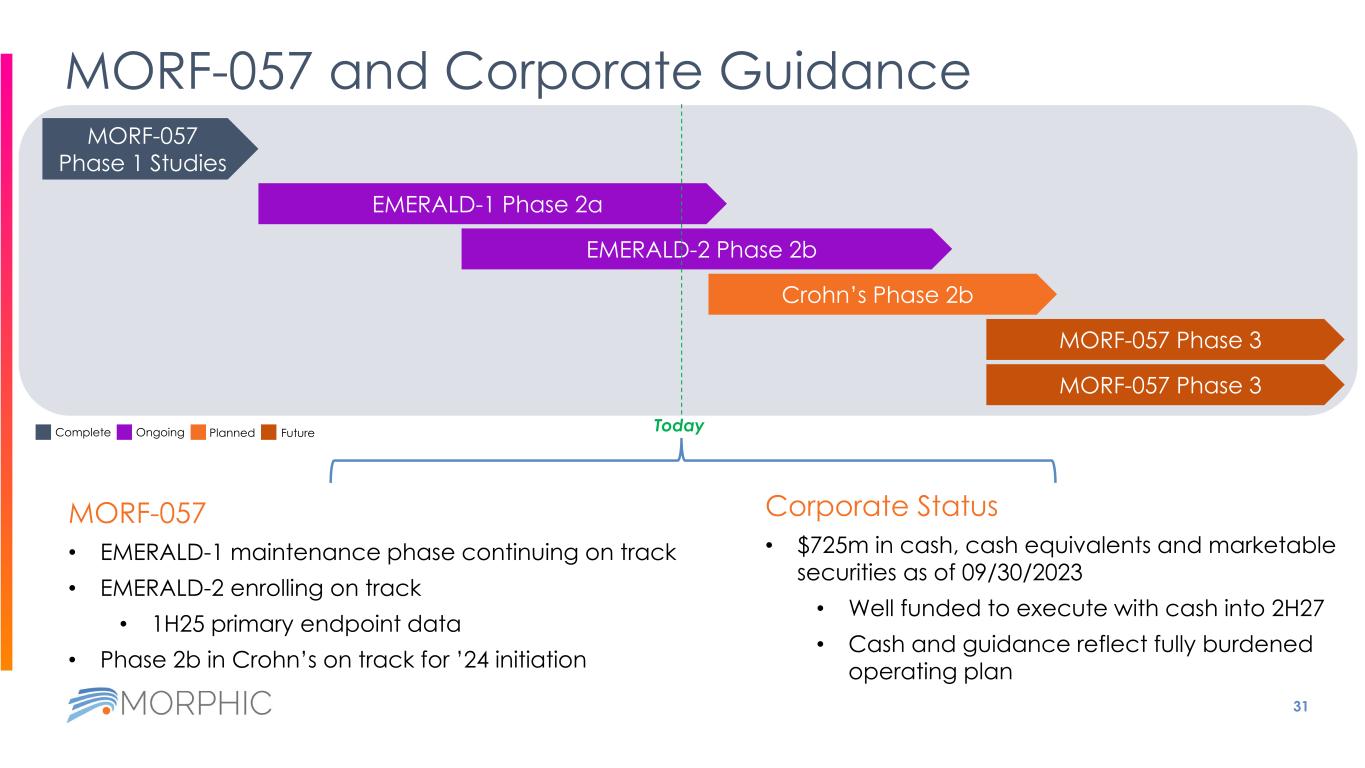
31 MORF-057 和企業指導方針 MORF-057 • EMERALD-1 維護階段繼續步入正軌 • EMERALD-2 報名步入正軌 • 1H25 年主要終點數據 • 克羅恩的 2b 階段有望在 24 年啟動 EMERALD-1 2a 階段 EMERALD-2 2b 階段克羅恩第 2b 階段 MORF-057 第 3 階段第 3 階段第 1 階段研究公司地位 • 截至 2023 年 9 月 30 日有7.25億美元的現金、現金等價物和有價證券 • 資金充足,可以用現金執行進入下半年 • 現金和指導反映了負擔沉重的運營計劃完成正在進行的計劃今天的未來 MORF-057 MORF-057

32 Brian Feagan博士是一名胃腸病學家,接受過臨牀流行病學和生物統計學方面的培訓。他的研究重點是設計、開展和執行克羅恩病(CD)和潰瘍性結腸炎(UC)的大規模隨機對照試驗(RCT),在過去的30年中,他一直是140多項多中心隨機對照試驗的首席研究員。他的研究一直致力於開發、驗證和優化結果衡量標準,以評估新型療法在CD和UC中的療效。Feagan 博士是舒利希醫學院和牙科學院的醫學教授、倫敦健康科學中心的胃腸病學家和 Alimentiv Inc. 的高級科學總監。問答參與者 Brian G. Feagan,醫學博士 • Brian G. Feagan,醫學博士 • Briad G. Feagan,FRCS • Bruce Rogers,博士 • Marc Schegerin,醫學博士 • Chris Erdman,MPH