

進化智能生物技術 2023 年 9 月附錄 99.1

前瞻性陳述以下幻燈片和任何隨附的口頭陳述均包含1995年《私人證券訴訟改革法》和其他聯邦證券法所指的前瞻性陳述。使用諸如 “可能”、“可能”、“將”、“應該”、“期望”、“計劃”、“預期”、“相信”、“估計”、“項目”、“打算”、“未來”、“潛在”、“機會” 或 “繼續” 之類的詞語以及其他類似的表達方式旨在識別前瞻性陳述。例如,所有關於以下內容的陳述:源自 tRNA 合成酶基因的蛋白質的潛在治療益處以及我們的候選產品和開發計劃;成功推進我們的候選產品和開展某些開發活動(例如啟動臨牀試驗、臨牀試驗註冊、開展臨牀試驗和宣佈臨牀結果)以及實現某些開發目標的能力,以及此類事件發生的時機;我們的候選產品的潛在市場機會;我們的能力我們的候選產品獲得監管部門的批准並實現其商業化;我們識別和發現其他候選產品的能力;合作協議下的潛在活動和付款;以及我們的知識產權組合提供保護的能力,均為前瞻性陳述。所有前瞻性陳述均基於我們管理層的估計和假設,儘管我們認為這些估計和假設是合理的,但本質上是不確定的。所有前瞻性陳述都受到風險和不確定性的影響,這些風險和不確定性可能導致實際結果與我們預期存在重大差異。這些風險、不確定性和其他因素在我們向美國證券交易委員會提交的文件中得到了更全面的描述,包括我們的10-K表年度報告、我們隨後提交的10-Q表季度報告以及我們的其他文件。本演示文稿中的前瞻性陳述僅代表截至本演示文稿發佈之日,我們和任何其他人均不對任何前瞻性陳述的準確性和完整性承擔責任。除非法律要求,否則我們沒有義務公開更新或修改任何前瞻性陳述,無論是由於新信息、未來事件還是其他原因。我們擁有各種美國聯邦商標申請和未註冊商標,包括我們的公司名稱。本演示文稿中提及的所有其他商標或商品名稱均為其各自所有者的財產。僅為方便起見,本演示文稿中提及的商標和商品名稱不帶符號®,但不應將此類提法解釋為其各自所有者不會在適用法律的最大範圍內主張其權利。本演示文稿討論了正在進行臨牀研究且尚未獲得美國食品藥品監督管理局批准上市的候選產品。對於這些候選產品的研究用途,沒有説明其安全性或有效性。本演示文稿還包含獨立各方和我們做出的與市場規模和增長有關的估計值和其他統計數據,以及有關我們行業的其他數據。這些數據涉及許多假設和侷限性,提醒您不要過分重視此類估計。此外,對我們未來業績以及我們運營所在市場的未來表現的預測、假設和估計必然會受到高度的不確定性和風險的影響。
將 tRNA 合成酶轉化為治療纖維化和炎症的新療法通過進化智力獲得的新型細胞外功能潛在的新藥物 IP 定向到所有 20 個 tRNA 合成酶基因的蛋白質成分臨牀概念驗證已建立肺結節病的 3 期 EFZO-FIT ️ 研究報名參加 SSC-ILD 發起的 Efzo-CONNECT ️ 研究:同類首創的生物免疫調節劑 ILD 專有 tRNA 合成酶平臺巨大的治療潛力差異化方法多款重磅炸彈機會治療重點:截至2023年6月30日,炎症和纖維化約1.12億美元的現金、限制性現金、現金等價物和投資公司預計到2026年將有現金跑道
進化智能:tRNA 合成酶進化為調節複雜系統結構域從全長蛋白質中局部釋放,使其能夠起到細胞外信號分子的作用。越來越多的證據表明,結構域通過跨多個器官系統的新治療幹預點起到恢復穩態的作用。隨着生物學變得更加複雜,新的tRNA合成酶結構域在進化壓力下持續存在,這表明了生物學的重要性

在同行評審期刊中越來越多地驗證 atYr Science “Efzofitimod:一種治療結節病的新型抗炎藥” ——依佐非替莫的第一篇主要評論文章 (https://doi.org/10.36141/svdld.v40i1.14396);“Efzofitimod用於治療肺結節病” — 1b/2a 期數據公佈 (https://doi.org/10.1016/j.chest.2022.10.037);ATYR2810 的靶標 NRP2 生物學登上了《科學轉化醫學》的封面 (https://www.science.org/doi/10.1126/scitranslmed.adf1128)

越來越多的同類首創 tRNA 合成酶衍生生物製劑項目靶標/MOA 適應症研究臨牀前 1 期 2 期 3 期 tRNA 合成酶項目 Efzofitimod NRP2 調節劑肺結節病 (1) SSC-ILD 其他 ILD(CTD-ILD;CHP)ATYR0101 LTBP1 調節劑纖維化 ATYR0750 FGFR4 調節劑肝臟疾病單克隆抗體計劃 ATYR2810 NRP2/VEGF 拮抗劑實體腫瘤 ATYR4010 NRP2/CCR7 拮抗劑自身免疫性疾病 ODD、Fast Track ODD、Fast Track 與 Kyorin Pharmaceutical Co., Ltd. 合作開發和日本用於ILD的依佐非替莫的商業化 ODD = 孤兒藥名稱;SSC-ILD = 硬皮病相關的 ILD;CTD-ILD = 結締組織病-ILD;CHP = 慢性超敏性肺炎

Efzofitimod 一流的間質性肺病 (ILD) 生物免疫調節劑
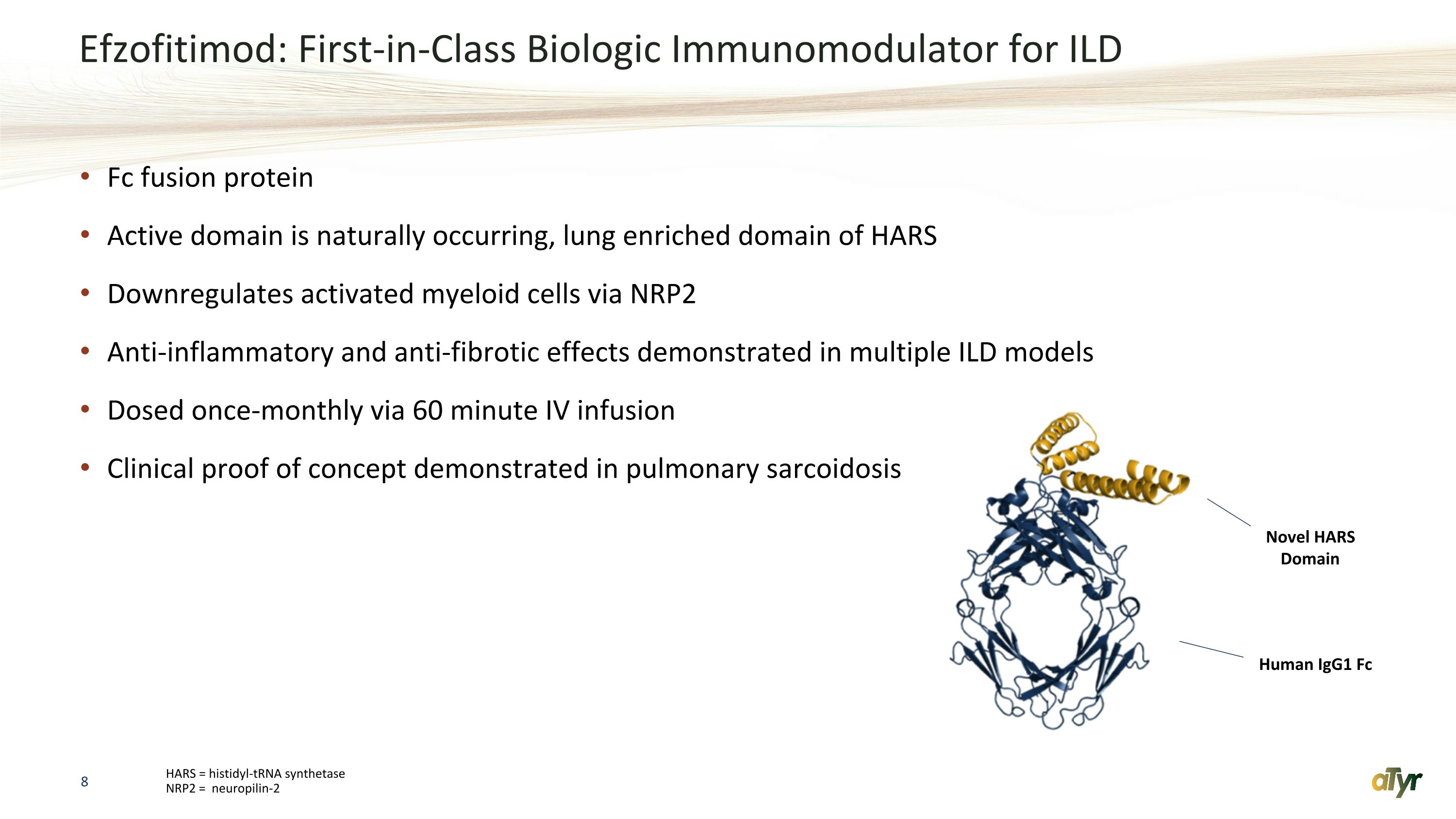
Efzofitimod:用於ILD Fc融合蛋白的同類首創生物免疫調節劑活性結構域是天然存在的,HARS的肺富集域通過NRP2向下調節活化的髓細胞抗炎和抗纖維化作用在多個ILD模型中顯示出抗炎和抗纖維化作用通過靜脈輸注60分鐘給藥一次肺結節病臨牀概念證明 HARS = histidyl-tRNA 合成酶 NRP2 = neuropilpild in-2 小説 HARS Domain Human igG1 Fc
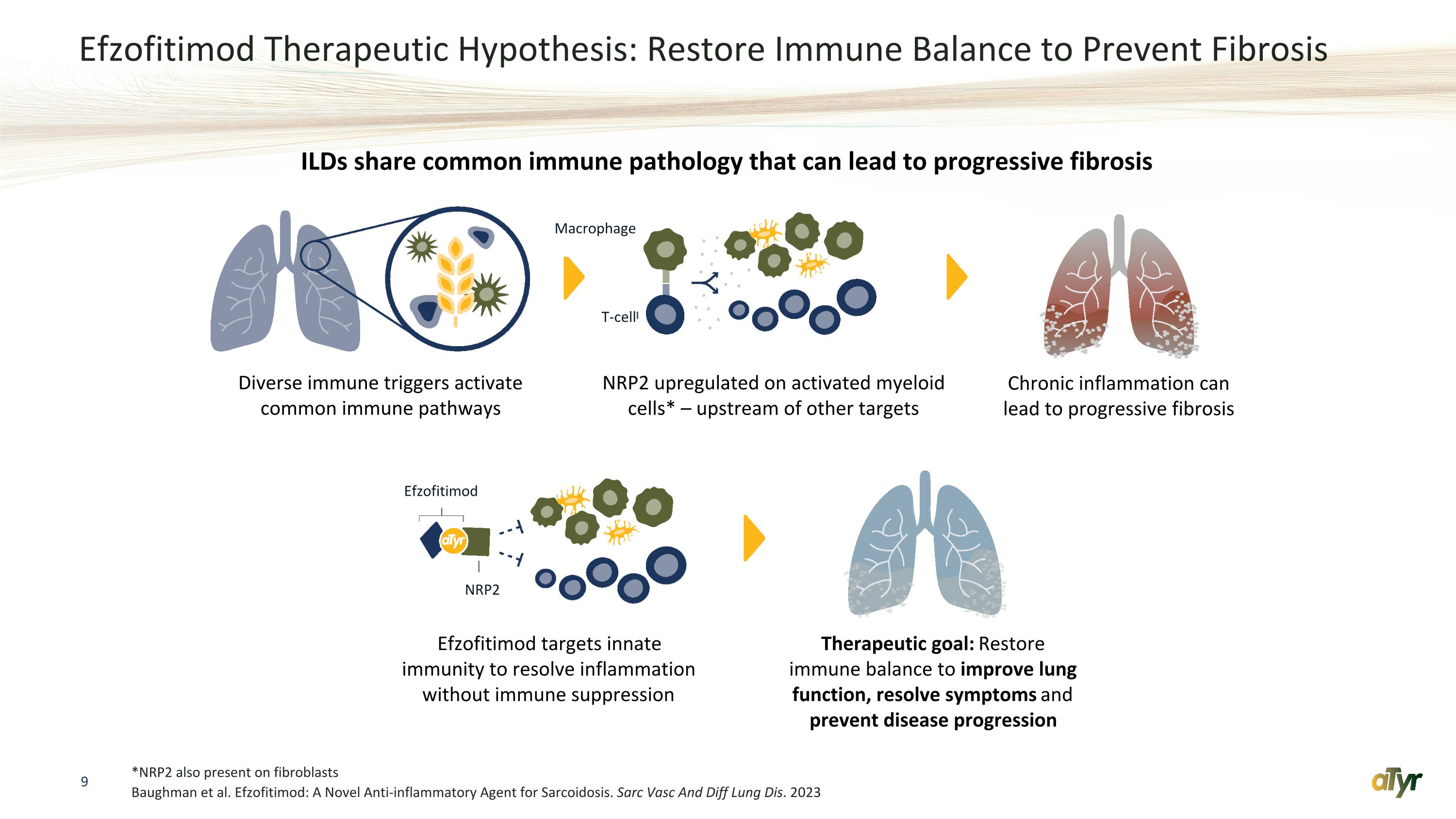
Efzofitimod 治療假設:恢復免疫平衡以防止纖維化 *NRP2 也存在於成纖維細胞中 Baughman 等人Efzofitimod:一種治療結節病的新型抗炎劑。Sarc Vasc And Diff Lung Diff Diff Lung Dis. 2023 多種免疫誘因激活的骨髓細胞激活了常見的免疫通路 NRP2 上調* — 其他靶標的上游慢性炎症可導致進行性纖維化 Efzofitimod 靶向先天免疫以在不抑制免疫的情況下解決炎症 ILD 具有共同的免疫病理學可能導致進行性纖維化治療目標:恢復免疫平衡以改善肺功能、緩解症狀並預防疾病進展 Efzofitimod 具有共同的免疫病理學可能導致進行性纖維化治療目標:恢復免疫平衡以改善肺功能、緩解症狀並預防疾病進展 Efzofitimod Timod Macrophage T 細胞 NRP2
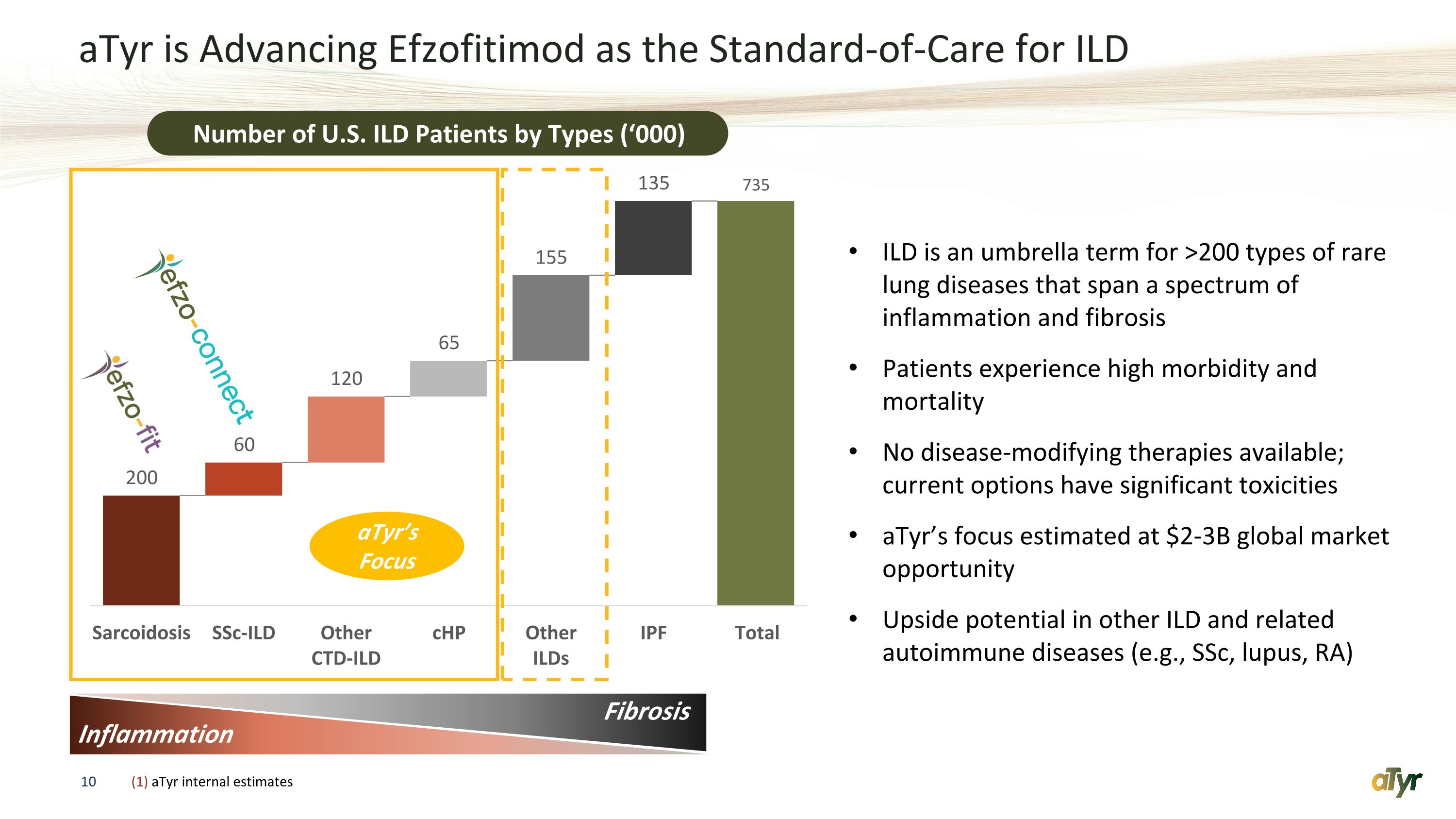
aTyr正在將Efzofitimod提升為ILD的護理標準。按類型劃分的美國ILD患者人數('000)ILD是涵蓋各種炎症和纖維化的超過200種罕見肺部疾病的總稱。患者的發病率和死亡率都很高沒有疾病改善療法可用;目前的選擇具有顯著的毒性 aTyr的重點估計為20億至30億美元的全球市場機會其他ILD和相關的自身免疫性疾病的上行潛力(例如,ssC、lupus、RA)炎症纖維化 aTyr's Focus (1) aTyR 內部估計
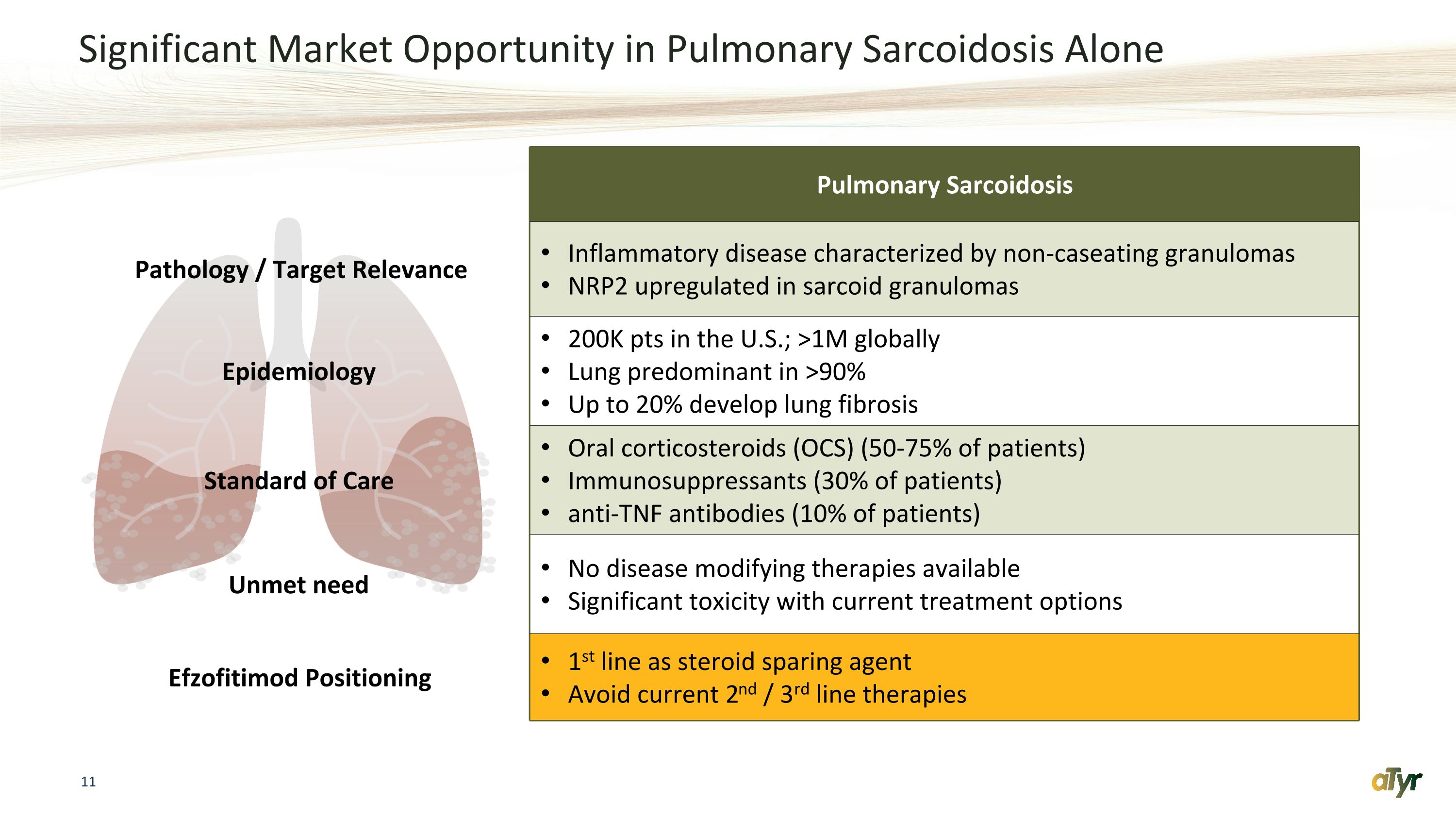
僅肺結節病的巨大市場機會肺結節病理學/目標相關性炎症性疾病以非囊性肉芽腫為特徵的炎症性疾病 NRP2 在美國肉芽腫中上調流行病學 20萬分;全球>100萬肺佔主導地位 > 90% 多達 20% 的人患上肺纖維化治療標準口服皮質類固醇 (OCS)(50-75% 的患者)免疫抑制劑(30% 的患者)抗腫瘤壞死因子抗體(10% 的患者)未得到滿足的需求沒有可用的疾病改善療法目前的治療方案毒性很大Efzofitimod 將第一線定位為類固醇保護劑避免目前的二線/三線療法
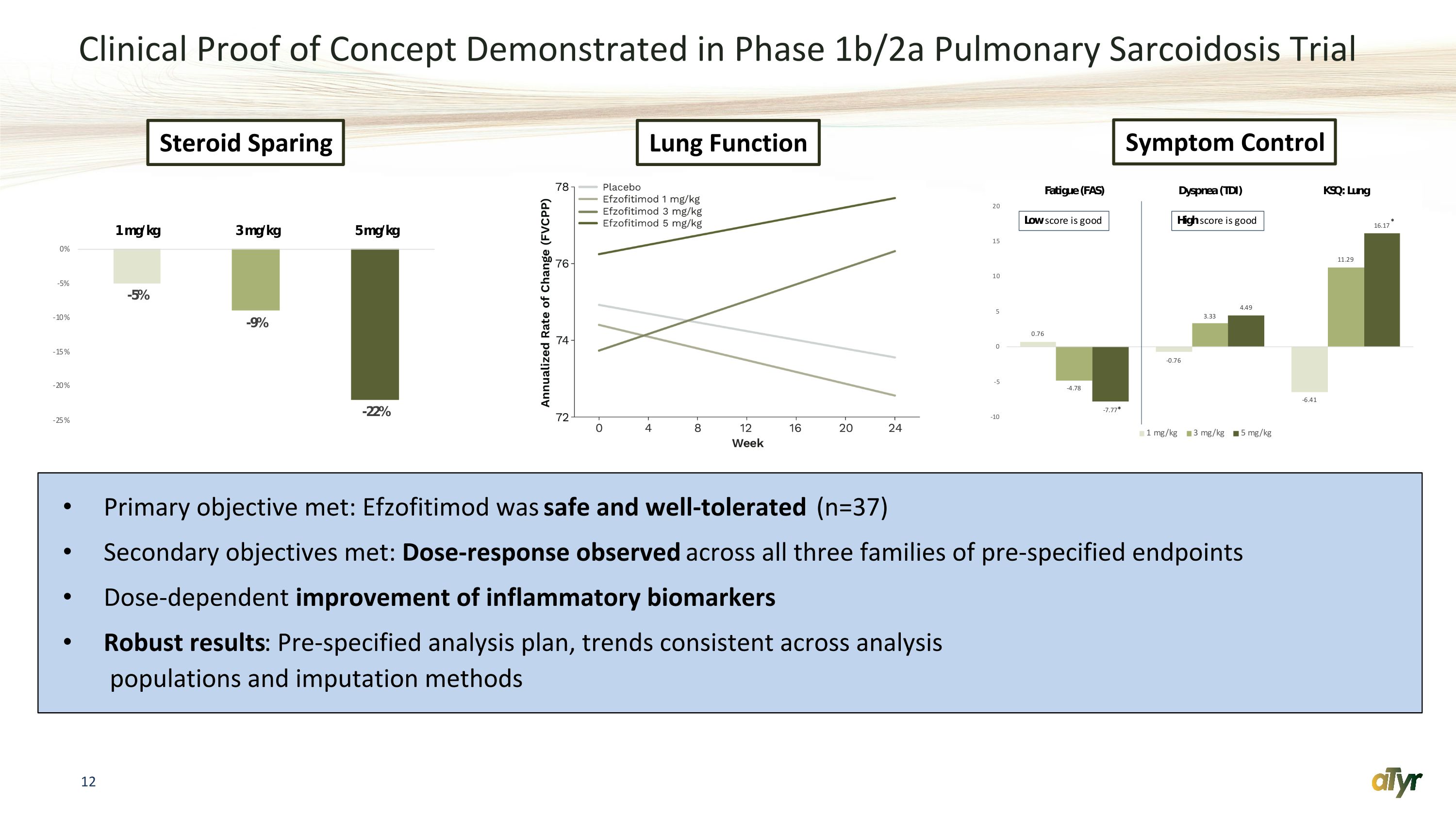
臨牀概念驗證已在1b/2a期肺結節病試驗中得到證實主要目標達到:依佐非替莫安全且耐受性良好(n=37)次要目標達到:在所有三個預先設定的終點家族中觀察到劑量反應炎症生物標誌物的劑量依賴性改善穩健的結果:預先設定的分析計劃、不同分析人羣和歸因方法保持一致的類固醇緩解肺功能症狀控制
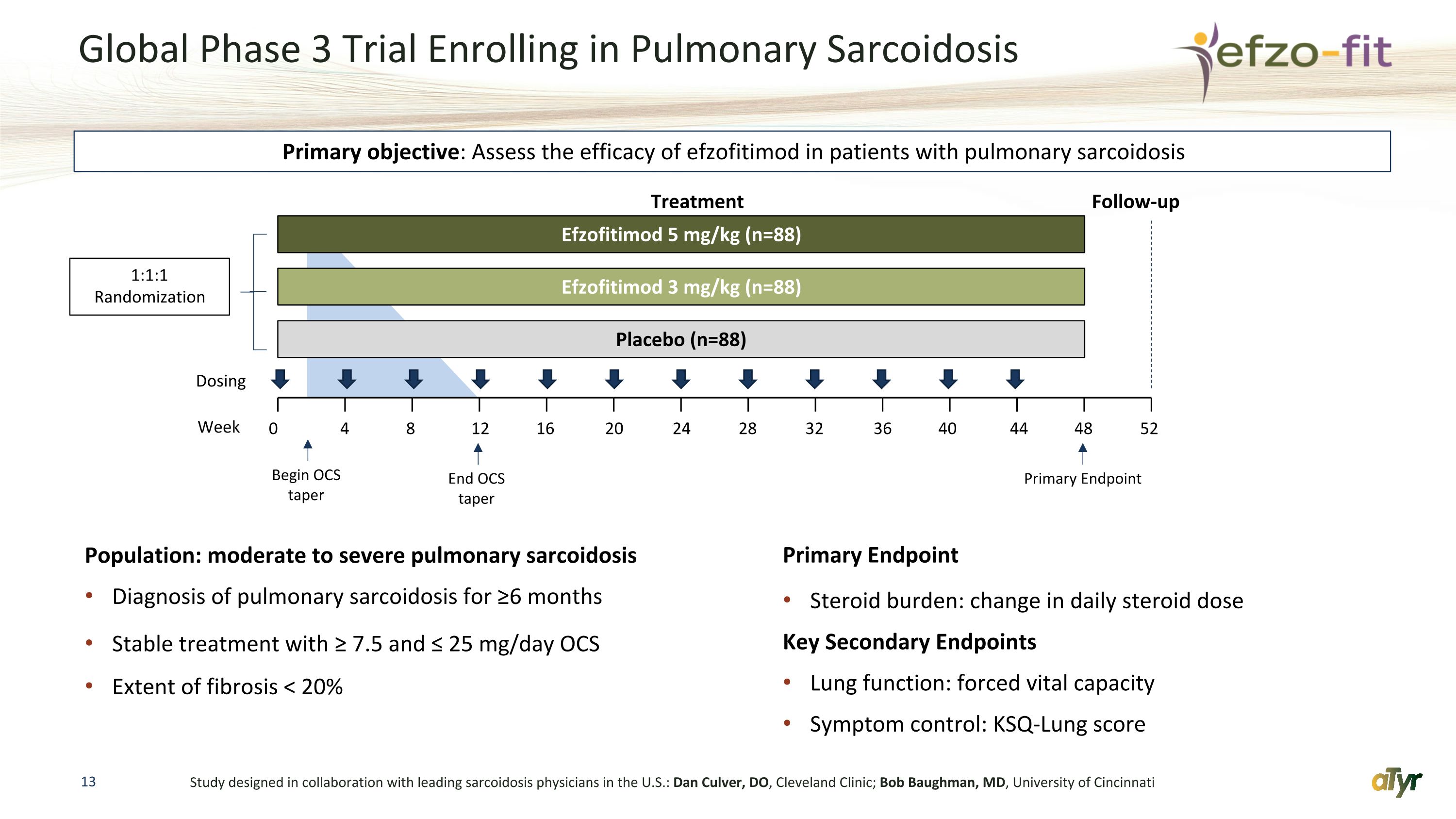
全球3期臨牀試驗在肺結節病人羣中報名:中度至重度肺結節病診斷肺結節病6個月以上穩定治療含量≥ 7.5 且≤ 25 mg/day OCS 纖維化程度
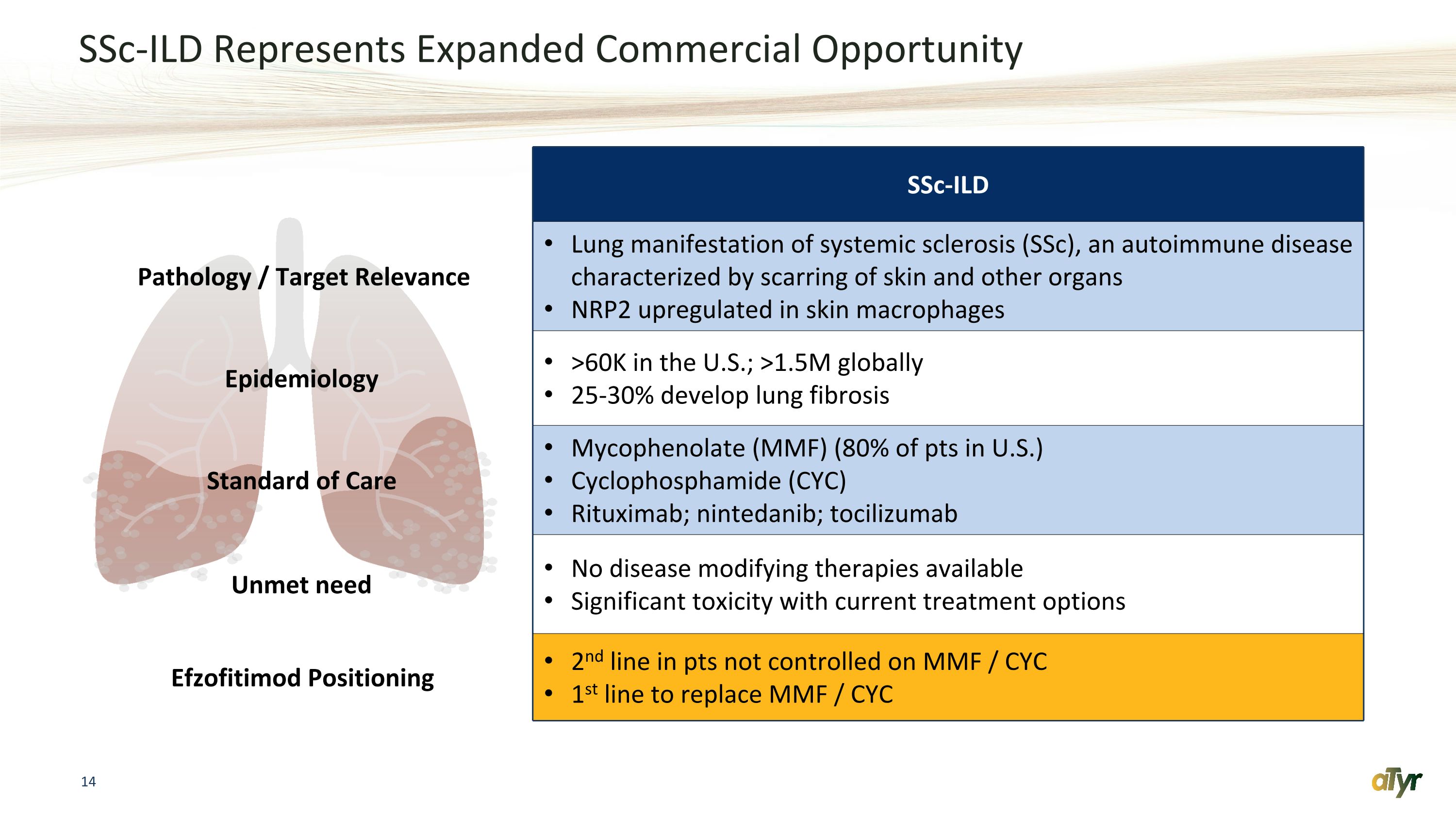
SSC-iLD 代表着更大的商業機會 SSC-iLD 病理學/靶點相關性系統性硬化症(SSC)的肺部表現系統性硬化症(SSC)是一種以皮膚和其他器官疤痕為特徵的自身免疫性疾病 NRP2 在皮膚巨噬細胞中上調流行病學 >6萬;全球>150萬 25-30% 開發肺纖維化治療標準黴酚酯(MMF)(美國80%的pts)環磷酰胺(CYC)利妥昔單抗;nintedanib;tocilizumab 未滿足需要沒有疾病改善療法可用的疾病改善療法目前的治療方案毒性顯著依佐非替莫德定位第 2 行 pts 不受控制在 MMF /CYC 第一線以取代 MMF /CYC

在 SSC-iLD 人羣中啟動的 2 期 POC 試驗:ssC 針對進展性 ILD 患者 SSC(ACR/EULAR 標準)和 ILD(基線 HRCT)進行性疾病(近期發作、炎症證據、瀰漫性皮膚 SSC)背景黴酚酸鹽治療主要終點肺功能:強制肺活量關鍵次要終點症狀控制:ProS 皮膚:組織病理學、基因分析、生物標誌物、mrSS 研究設計與美國領先的 SSC-iLD 醫生合作:克利夫蘭診所醫學博士克里斯汀·海蘭德;謝爾文·阿斯西,醫學博士,克利夫蘭大學得克薩斯州,休斯頓 -4 0 4 8 12 16 20 24 28 Efzofitimod 450 mg(n=10)Efzofitimod 270 mg(n=10)安慰劑(n=5)中期皮膚評估主要療效分析安全隨訪周給藥穩定背景方案篩查治療隨訪主要目標:評估依佐非替莫對肺部、皮膚和全身表現的療效 SSC-iLD POC = 概念驗證
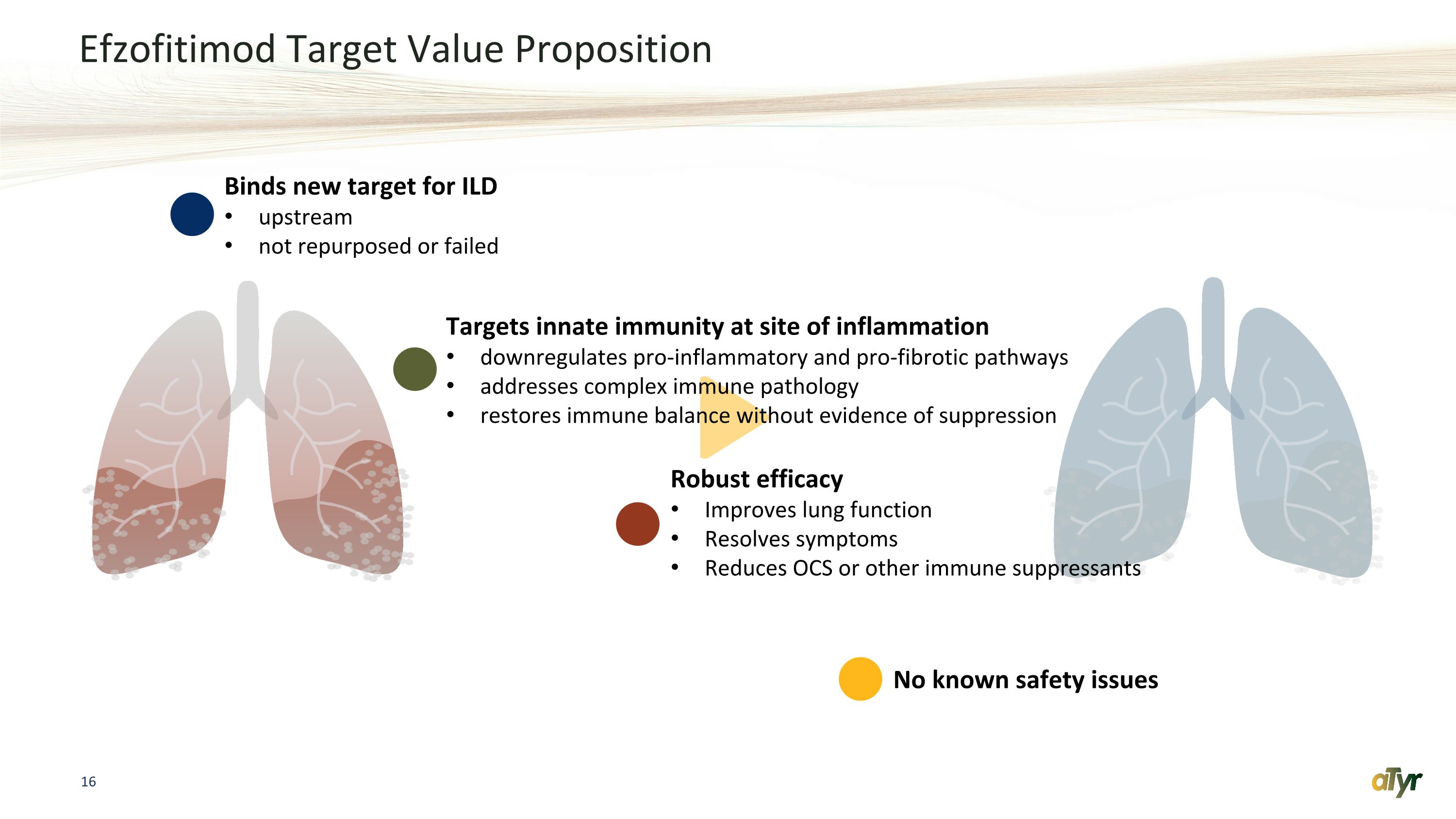
Efzofitimod 靶標價值主張為上游的 ILD 綁定新靶點未重新利用或失敗靶點炎症部位的先天免疫向下調節促炎和促纖維化途徑解決複雜的免疫病理學在沒有抑制證據的情況下恢復免疫平衡強大的療效改善肺功能解決症狀減少 OCS 或其他免疫抑制劑沒有已知的安全問題

為炎症和纖維化開發新療法的臨牀前管線

tRNA 合成酶平臺方法通過 efzofitimod 臨牀 POC HARS 衍生的 NRP2 調節劑 efzofitimod 目前處於肺結節病第 3 期的獨特藥物發現平臺利用進化情報的獨特藥物發現平臺細胞外 tRNA 合成酶可以解鎖新的靶點和/或信號通路對生物學或適應症的低偏見針對高價值市場的候選藥物管道差異化 MOA 可能帶來更好的結果選擇性激活的靶點差異化 MOA 可能帶來更好的結果系統具有專有分子的深厚研究能力針對所有 20 個 tRNA 合成酶基因的蛋白質成分的文庫 IP 與 Dualsystems Biotech AG 的研究合作旨在鑑定 tRNA 合成酶的靶受體

將 tRNA 合成酶生物學轉化為炎症和纖維化的新療法

將 tRNA 合成酶轉化為炎症和纖維化新療法進化情報藥物發現平臺細胞外 tRNA 合成酶代表了潛在的新藥物 aTyR 擁有的面向全類知識產權的潛在新藥物 aTyr 擁有的針對未開發的重磅市場的關鍵開發領導項目在肺結節病中建立臨牀POC 全球第 3 期 EFZO-FIT ️ 研究註冊肺結節病隨着 2 期的啟動擴展到第二適應症 EFZO-CONNECT ️ 在 ssc-iLD 中研究 tRNA 合成酶衍生候選藥物的生長管線多個針對炎症和纖維化的下一代項目解鎖新的治療幹預點截至2023年6月30日,通過多個轉折點實現穩健的財務狀況約為1.12億美元的現金、限制性現金、現金等價物和投資公司預計2026年將有現金流入日本與杏林藥業的依佐非替莫合作

謝謝