

附錄 99.1 公司概述 2023 年 9 月 © 2023 Invivyd, Inc. Invivyd 和 Invivyd 徽標是 Invivyd, Inc. 的商標。本演示文稿中的所有商標均為其各自所有者的財產。

關於前瞻性陳述的警示性説明本演示文稿 包含1995年《美國私人證券訴訟改革法》所指的前瞻性陳述。本演示文稿中不是歷史事實陳述的陳述均為前瞻性陳述。諸如 “可能”、“將”、“應該”、“期望”、“計劃”、“預期”、“尋求”、“可以”、“打算”、“目標”、“目標”、 “項目”、“設計”、“估計”、“相信”、“預測”、“潛在” 或 “繼續” 之類的詞語或這些術語或其他類似表達方式中的否定詞都旨在 確定前瞻性陳述,儘管並非所有前瞻性陳述都包含這些識別詞。前瞻性陳述包括以下方面的陳述:我們快速提供保護 弱勢羣體免受病毒威脅的抗體的使命;COVID-19 格局的未來;我們對目標患者羣體規模和候選產品的潛在市場機會的期望,以及我們的市場地位;我們 對抗 SARS-CoV-2 單克隆抗體 (mAB) 和候選產品的臨牀效用的信念;我們基於平臺的潛力持續接近發現和優化可以永久保護 弱勢羣體免受嚴重病毒威脅的單克隆抗候選藥物;VYD222 的預期廣泛活性和長期效用;我們正在進行的研究和臨牀開發計劃及其時機,包括與 VYD222 有關的研究和臨牀開發計劃及其時機;通過血清中和滴度進行免疫橋接的單克隆抗體在美國可能獲得緊急使用授權 (EUA) 的可能性;預期的 CANOPY 臨牀試驗設計,包括我們使用免疫橋接方法的計劃將 CANOPY 臨牀試驗中獲得的 數據與某些歷史adintrevimab數據進行比較;我們期望在CANOPY臨牀試驗中為可能提交的 VYD222 EUA 快速生成臨牀數據,以及CANOPY臨牀試驗的預期初始 終點數據的時間;我們計劃開發一個強大的候選產品陣容,如果獲得授權或批准,可以用於預防或治療嚴重病毒性疾病,首先是 COVID-19 並將 擴展到流感和其他急需適應症;我們的認為我們現有的現金資源將足以支持直至2024年第四季度的運營;以及其他非歷史事實的報表。實際上 我們可能無法實現前瞻性陳述中披露的計劃、意圖或預期,您不應過分依賴我們的前瞻性陳述。這些前瞻性陳述涉及風險和不確定性,可能導致 我們的實際結果與前瞻性陳述中描述或暗示的結果存在重大差異,包括但不限於:我們的發現、臨牀前和臨牀開發活動的時間和進展;我們 快速生成CANOPY臨牀試驗所需的臨牀數據以支持可能提交的 VYD222;臨牀試驗站點激活或入組率低於預期;意想不到的安全性或臨牀前研究或臨牀試驗期間觀察到的療效數據 ;根據臨牀前研究中和活性,VYD222 或其他候選產品臨牀成功的可預測性;臨牀前研究或臨牀 試驗的結果可能無法預測當前或未來臨牀試驗的未來結果的風險;用於預測對抗令人擔憂的 SARS-CoV-2 變異體的活性的模型結果的差異;預期或現有競爭的變化; 監管環境的變化;不確定性以及監管部門批准程序的時機;我們基於平臺的方法是否使我們能夠持續發現和優化能夠永久保護弱勢羣體 免受嚴重病毒威脅的單克隆抗候選藥物;VYD222 或任何其他候選產品是否能夠證明並維持對主要的 SARS-CoV-2 變異體的中和活性,尤其是在病毒進化面前;我們將來能否成功提交 EUA,以及任何此類變體的結果 EUA 提交;我們是否在研發方面做出了努力將為 COVID-19 以外的傳染病確定並制定安全有效的治療方案;以及 我們是否有足夠的資金來滿足未來的運營費用和資本支出需求。其他可能導致我們的實際業績與本 演示文稿中前瞻性陳述中表達或暗示的存在重大差異的因素在我們向美國證券交易委員會(SEC)提交的截至2022年12月31日的年度10-K表年度報告、我們向 SEC提交的其他文件以及我們未來向美國證券交易委員會提交的報告中,在 www.sec.上的 “風險因素” 標題下進行了描述 gov。本演示文稿中包含的前瞻性陳述自該日期起作出,除非適用法律要求,否則我們不承擔更新此類信息的責任,無論是新的 信息、未來事件還是其他原因。© 2023 Invivyd, Inc. Invivyd 和 Invivyd 徽標是 Invivyd, Inc. 的商標。本演示文稿中的所有商標均為其各自所有者的財產。 2
INVIVYD 的使命是快速提供保護 弱勢羣體免受病毒威脅的抗體,從 COVID-19 開始 8-18M 獲得授權或批准的 EUA 途徑為零免疫功能低下的人提供了在美國可能沒有單克隆抗體的機會 對急需的治療方法做出充分反應,以 1-4 COVID-19 疫苗接種預防有症狀的免疫功能低下的人 COVID-19 參考文獻:1.Harpaz JAMA 2016;2.Patel Emerg Infect Dis 2020;3.美國 2020 年人口普查局 數據;4.Lee BMJ 2022 3
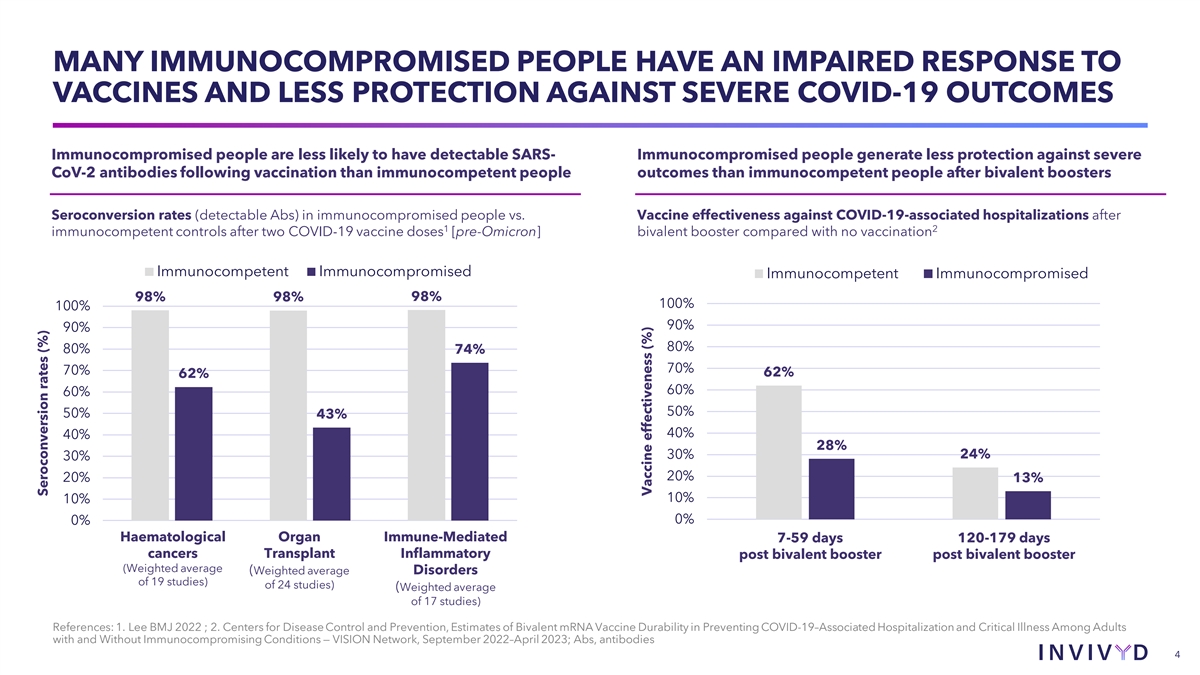
許多免疫功能低下的人對疫苗的反應受損,對嚴重 COVID-19 後果的保護也較差免疫功能低下的人不太可能患上可檢測到的 SARS — 免疫功能低下的人在接種疫苗後對嚴重 Cov-2 抗體的保護力低於免疫功能正常的人 ,免疫功能低下的人羣的血清轉化率(可檢測到的 Abs)與免疫功能正常的人在兩次之後接種疫苗對 COVID-19 相關住院的有效性相比 。br} COVID-19 疫苗劑量 [之前的 omicron]二價加強劑與未接種疫苗的比較免疫功能低下免疫功能低下免疫功能低下 98% 98% 100% 90% 90% 80% 74% 70% 62% 62% 60% 60% 50% 50% 43% 40% 40% 28% 24% 30% 20% 13% 10% 0% 0% 血液器官免疫介導 7-59 天 120-179 天癌症移植炎症後二價加強劑(加權平均值為 19 研究)24項研究) (17項研究的加權平均值)參考文獻:1.Lee BMJ 2022;2.美國疾病控制與預防中心,二價 mRNA 疫苗在預防有和不伴有免疫功能低下疾病的成年人中與COVID-19相關的住院和危重疾病方面的耐久性估計 — VISION Network,2022 年 9 月至 2023 年 4 月;Abs,抗體 4 血清轉化率 (%) 疫苗有效性 (%)

即使在免疫功能正常的人羣中,COVID-19 疫苗 的有效性 (VE) 也有所減弱單價加強劑對有症狀的二價加強劑提供 90% 的 VE 對抗最近的 Omicron 變異體 Delta 感染,對抗有症狀的 Omicron 感染 VE 為 46%,在主要免疫功能正常的 VE 中對抗SARS-CoV-2 感染,從單價增強劑開始超過 10 周內,VE 對抗有症狀的 COVID-19,主要免疫功能正常的 VE 對抗 SARS-CoV-2 感染在接種兩劑單價 疫苗後,單價 (bnt162b2) 二價加強劑最長可達 26 周) 二價增強劑 Omicron BA.4/5 顯性期 29% Delta B.1.617.2 90% Omicron BQ 顯性期 20% Omicron B.1.1.529 46% Omicron XBB 顯性期 4% 對當前變異提供更強有力保護的單克隆抗藥將是 COVID-19 藥櫃的重要補充,特別是對於弱勢人羣參考文獻:1.Andrews N Engl J Med 2022;2.Shrestha 公開論壇傳染病 2023 5
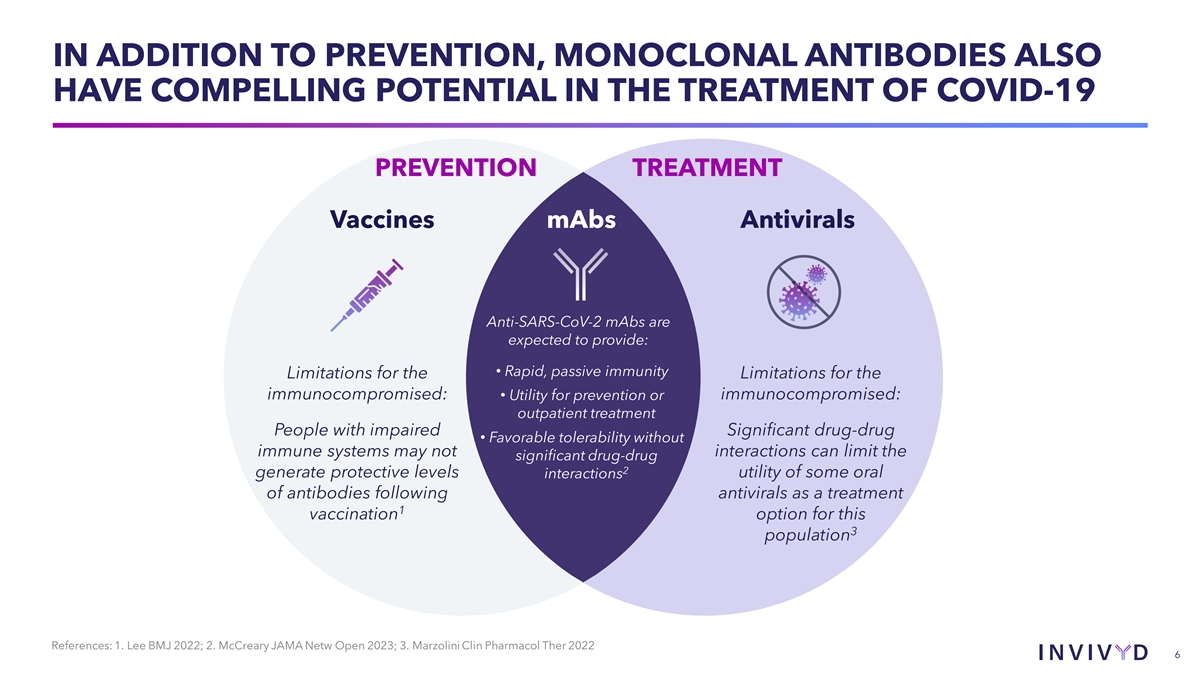
除了預防外,單克隆抗體在治療 COVID-19 預防治療疫苗方面也具有令人信服的 潛力 maB 抗病毒藥物抗 SARS-CoV-2 單克隆抗體預計將提供:• 免疫功能低下者的快速被動免疫侷限性限制:• 用於 預防或免疫功能低下的效用:門診治療嚴重藥物受損的人 • 沒有免疫系統的良好耐受性可能無法限制顯著的藥物相互作用 2 產生保護水平 一些口服的效用抗病毒藥物治療後抗體的相互作用這3個人羣有1種疫苗接種選擇參考文獻:1.Lee BMJ 2022;2.2023 年 McCreary JAMA 網絡公開賽;3.Marzolini Clin Pharmacol Ther 2022 6

在弱勢人羣中預防 COVID-19 提出了令人信服的 潛在長期價值主張 Evusheld® 2022 年的總收入為 22億美元,該單抗此前獲準保護弱勢羣體免受 COVID-19 的侵害 140 美元 12.7 億美元 1,200 美元在 2023 年對治療 免疫功能低下患者 1,000 美元 9.14 億美元的美國醫生的調查中,76% 的人表示,他們使用 Evusheld® 的費用為 800 美元 “極有可能” 或 “有點可能” Held® 如果還有 600 美元且與 2 種流通的 SARS-CoV-2 菌株有關 400 美元 200 美元 1.35 億美元 2021 年下半年 2022 年下半年 2022 年下半年參考文獻:1.阿斯利康公開公佈的結果;2.Invivyd贊助的對美國HCP的調查(N=197)(2023)7 總收入(百萬)

健康保險公司Humana審查的數據顯示,夏季的上漲預示着秋季和冬季的潛在浪潮,並凸顯了對 COVID-19 療法的持續需求 在過去的幾周裏,越來越多的老年人因Covid-19住院。2023 年 8 月 28 日 2023 年 9 月 6 日 2023 年 8 月 17 日 2023 年 7 月 27 日 8
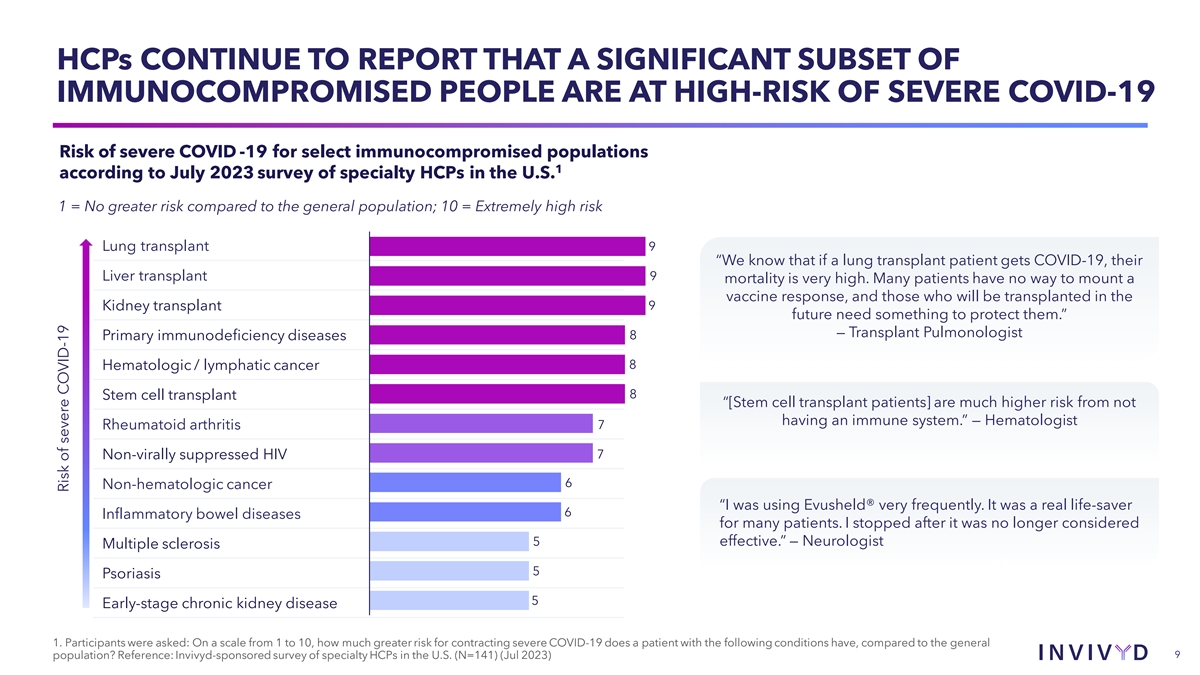
HCP 繼續報告説,很大一部分免疫功能低下 人羣面臨嚴重 COVID-19 風險特定免疫功能低下人羣患重度 COVID-19 的風險 1 根據 2023 年 7 月對美國特種醫護人員的調查 1 = 與普通人羣相比風險不大;10 = 極高 肺移植風險 9 “我們知道,如果肺移植患者得了 COVID-19,他們的 9 肝移植死亡率非常高。許多患者無法產生疫苗反應,而那些將來要移植腎臟 移植的患者需要一些東西來保護他們。” — 移植肺科醫生原發性免疫缺陷疾病 8 8 血液/淋巴癌 8 幹細胞移植”[幹細胞移植患者] 沒有免疫系統的風險要高得多。” — 血液學家 7 類風濕性關節炎 7 非病毒抑制 HIV 6 非血液學癌症 “我經常使用 Evusheld®。對於許多 患者來説,這確實是拯救生命的 6 種炎性腸病。在它不再被認為有效 5 之後我停了下來。” — 神經科醫生多發性硬化症 5 牛皮癬” 5 早期慢性腎臟病 1.參與者被問及:按照 1 到 10 的等級,與普通人羣相比,患有以下疾病的患者 感染重度 COVID-19 的風險要高多少?參考:Invivyd 贊助的對美國專業 HCP 的調查(N=141)(2023 年 7 月)9 出現嚴重 COVID-19 的風險

我們的平臺和 VYD222 © 2023 Invivyd, Inc. Invivyd 和 Invivyd 徽標是 Invivyd, Inc. 的商標。本演示文稿中的所有商標均為其各自所有者的財產。
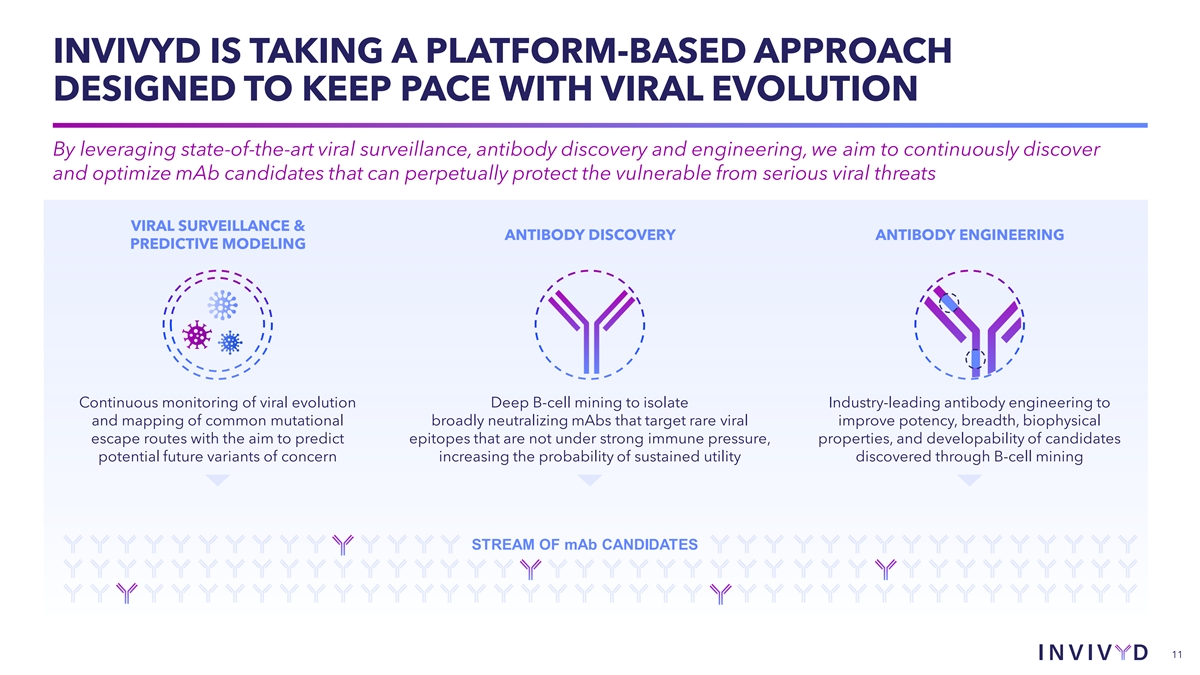
INVIVYD 正在採取一種基於平臺的方法,旨在跟上 病毒進化的步伐通過利用最先進的病毒監測、抗體發現和工程,我們的目標是不斷髮現和優化能夠永久保護弱勢羣體免受嚴重病毒威脅的單抗候選單克隆抗體 監測和抗體發現抗體工程預測建模持續監測病毒進化深度 B 細胞挖掘以分離行業領先的抗體工程並繪製常見突變廣泛中和單克隆抗體的地圖 靶向稀有病毒可改善效力、廣度、生物物理逃生途徑,目的是預測未承受強免疫壓力的表位、特性和候選人的發育能力潛在的未來可能令人擔憂的變異會增加 通過單抗候選單克隆抗體 B 細胞挖掘流發現持續效用的可能性 11
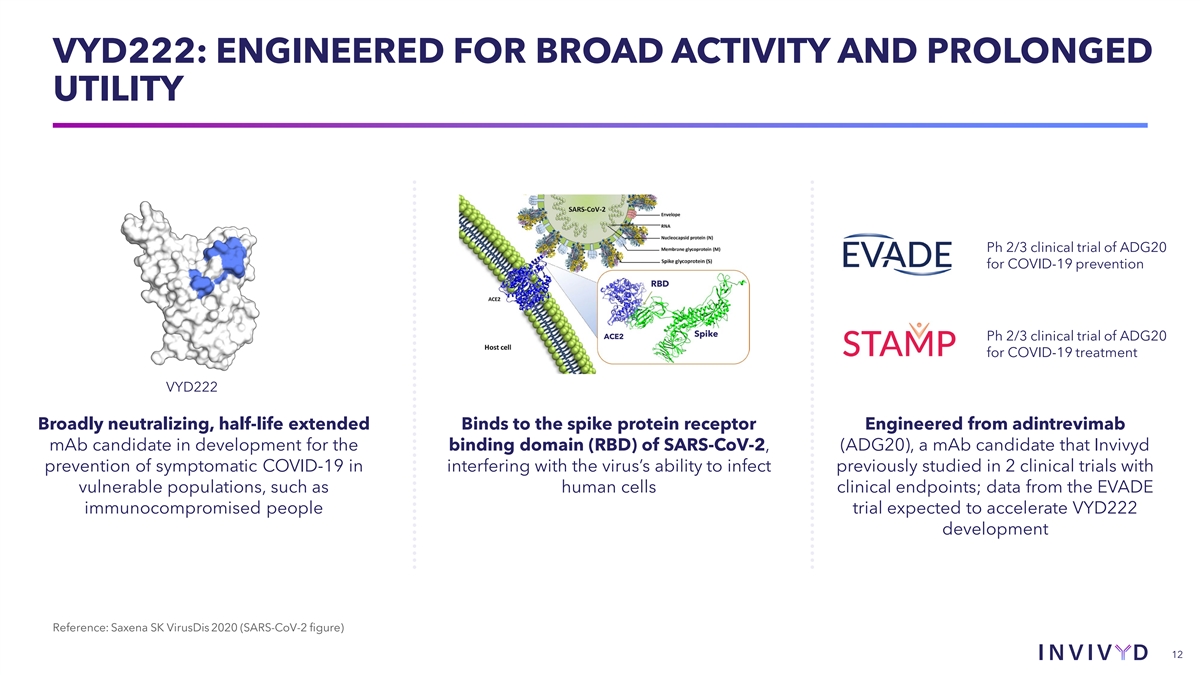
VYD222:專為廣泛活性和長效用而設計 ADG20 用於預防 COVID-19 的 Ph 2/3 臨牀試驗 RBD Spike ACE2 Ph 2/3 ADG20 用於 COVID-19 治療的臨牀試驗 VYD222 廣泛中和、延長半衰期結合刺突蛋白受體 在 SARS-CoV-2 結合域 (RBD) 開發中由 adintrevimab 候選藥物設計而成,(ADG20),Invivyd 預防的單抗候選單抗症狀會干擾病毒的感染能力,此前在兩項針對脆弱 人羣的臨牀試驗中進行了研究,COVID-19例如人體細胞臨牀終點;來自 EVADE 免疫功能低下的人羣試驗的數據預計將加速 VYD222 的開發參考文獻:Saxena SK Virusdis 2020(SARS-CoV-2 圖)12
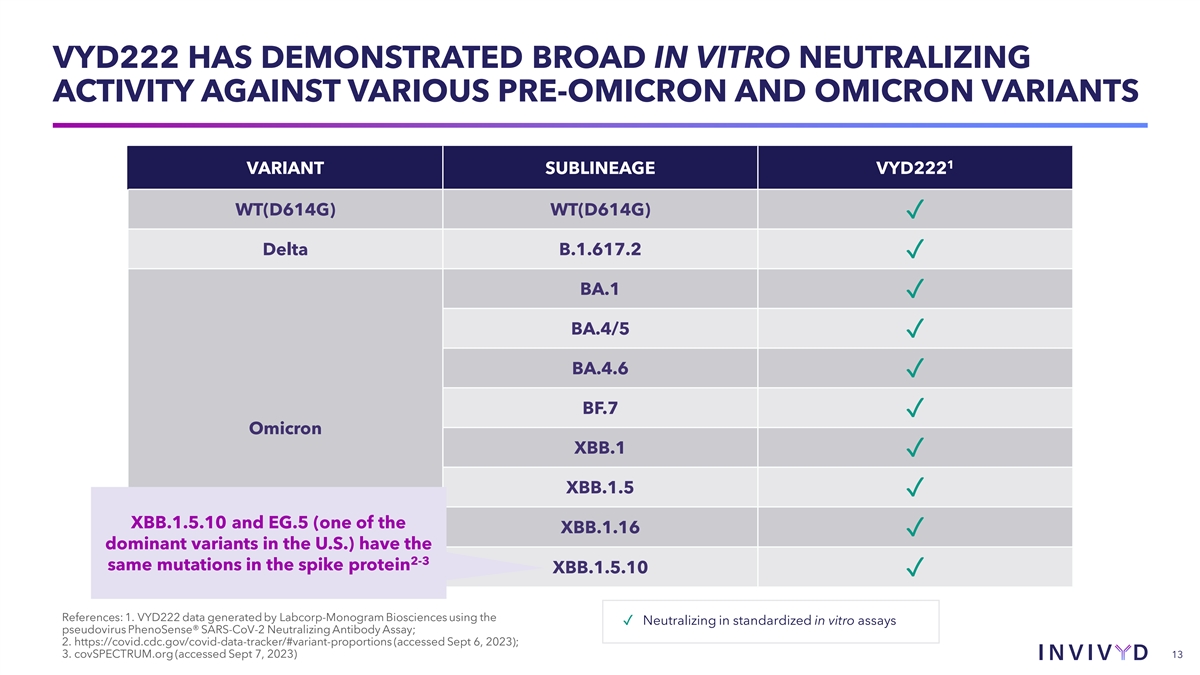
VYD222 對於 OMICRON 和 OMICRON 之前的各種變體 1 變體 sublineage VYD222 WT (D614G) WT (D614G) ✓ Delta B.1.617.2 ✓ BA.4 ✓ BA.4/5 ✓ BA.4.6 ✓ BF.7 ✓ Omicron XBB.1 ✓ XBB.1.5 XBB.1.5 ✓ XBB.1.5 XBB.1.5 和 EG.5(XBB.1.1 中的一個 16 ✓ 在美國佔主導地位的變體)在刺突蛋白中有 2-3 個相同的突變 XBB.1.5.10 ✓ 參考文獻:1.Labcorp-Monogram Biosciences 使用 ✓ 中和 體外測定假病毒 PhenoSense® SARS-CoV-2 中和抗體測定生成的 VYD222 數據;2. https://covid.cdc.gov/covid-data-tracker/#variant-proportions(2023 年 9 月 6 日訪問);3. covSpectrum.org(2023 年 9 月 7 日訪問)13
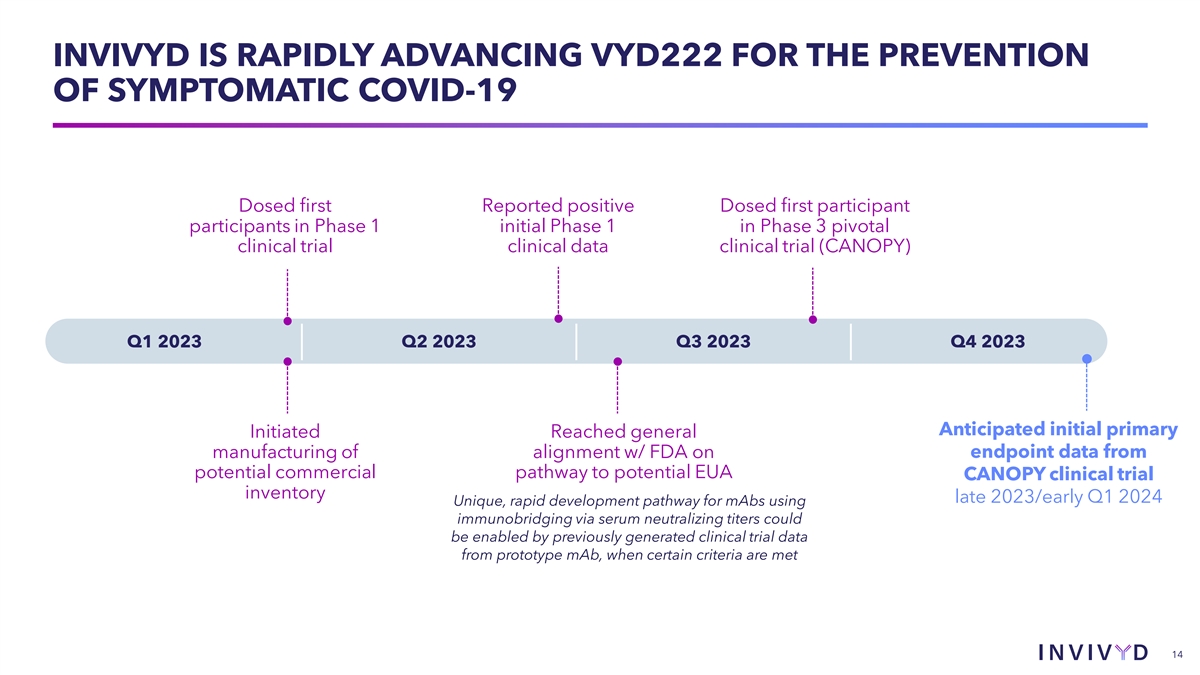
INVIVYD 正在迅速推進 VYD222 以預防症狀 COVID-19 首次被報告為陽性 1 期初始 1 期參與者 3 期關鍵臨牀試驗臨牀數據臨牀試驗 (CANOPY) 2023 年第一季度第 2023 季度第 3 季度預計 2023 年第 3 季度初始初始初始初發 已在 2023 年底/季度初與 FDA 就潛在的 EUA CANOPY 臨牀試驗庫存達成一致的總體終點數據 1 2024 使用血清進行免疫橋接的單克隆抗體獨特、快速的發育途徑 當滿足某些標準時,先前從原型單克隆抗生成的臨牀試驗數據可以啟用中和滴度 14
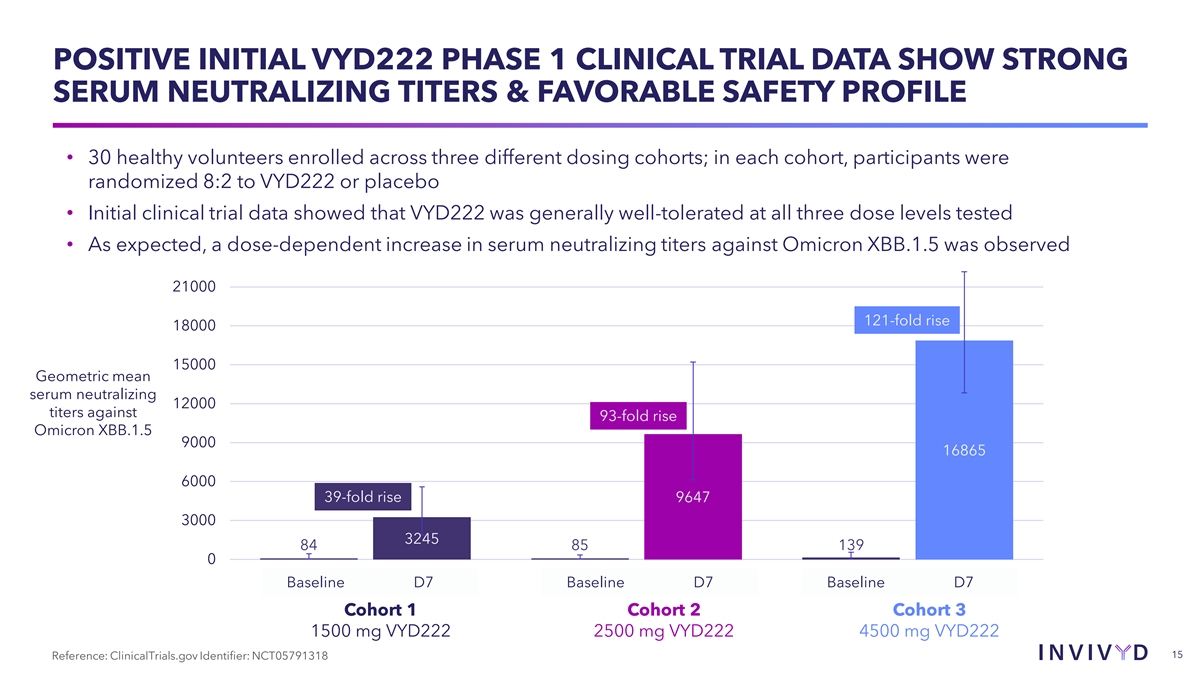
VYD222 1 期臨牀試驗初始數據呈陽性 中和滴度強且安全性良好 • 30 名健康志願者分為三個不同的給藥隊列;在每個隊列中,參與者以 8:2 隨機分配到 VYD222 或安慰劑 • 初步臨牀試驗數據顯示, VYD222 在所有三個測試劑量水平上總體耐受性良好 • 正如預期的那樣,血清中和滴度與 Omicron XBBON 相比呈劑量依賴性增加觀察到.1.5 21000 上升 121 倍 18000 15000 幾何平均血清中和 12000 滴度對抗 93 倍的增長 Omicron XBB.1.5 9000 16865 6000 39 947 3000 3245 84 139 0 基線 D7 基線 D7 基線 D7 隊列 1 隊列 2 隊列 3 1500 mg VYD222 2500 mg VYD222 4500 mg VYD222 15 參考文獻:clinicalTrials.gov 標識符:NCT05791318
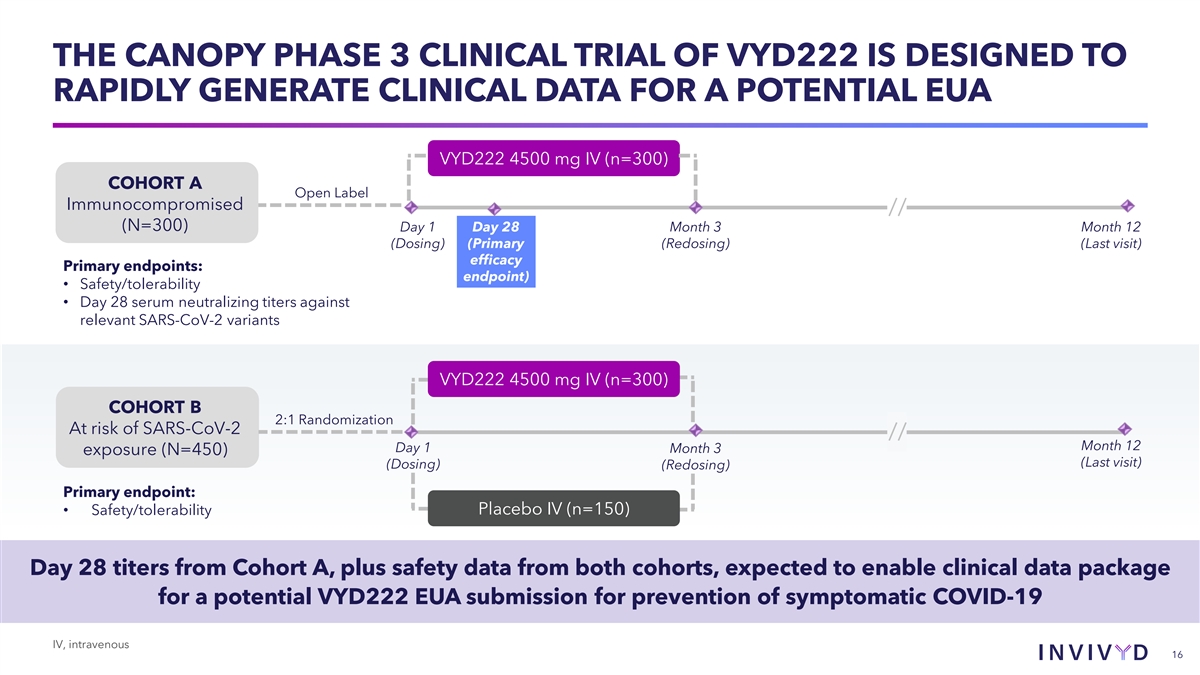
VYD222 的 CANOPY 3 期臨牀試驗旨在快速 生成潛在的 EUA VYD222 4500 mg IV (n=300) 隊列的臨牀數據 A 開放標籤免疫功能低下//(N=300) 第 1 天 28 個月 3 月 12(劑量)(原發性(再給藥)(最後一次就診)療效主要終點:終點)• 安全性/耐受性 • 第 28 天血清中和滴度與相關對比 SARS-CoV-2 變體 VYD222 4500 mg IV (n=300) 隊列 B 2:1 隨機化有 SARS-CoV-2 的風險//第 12 個月 1 個月第 3 個月暴露 (N=450)(最後一次訪問)(給藥)(劑量)(再給藥) 主要終點:•安全性/耐受性安慰劑 IV(n=150)來自隊列 A 的第 28 天滴度,加上兩個隊列的安全數據,預計將為可能提交的 VYD222 EUA 用於預防有症狀的 COVID-19 IV 靜脈注射、靜脈注射 16 提供臨牀數據包
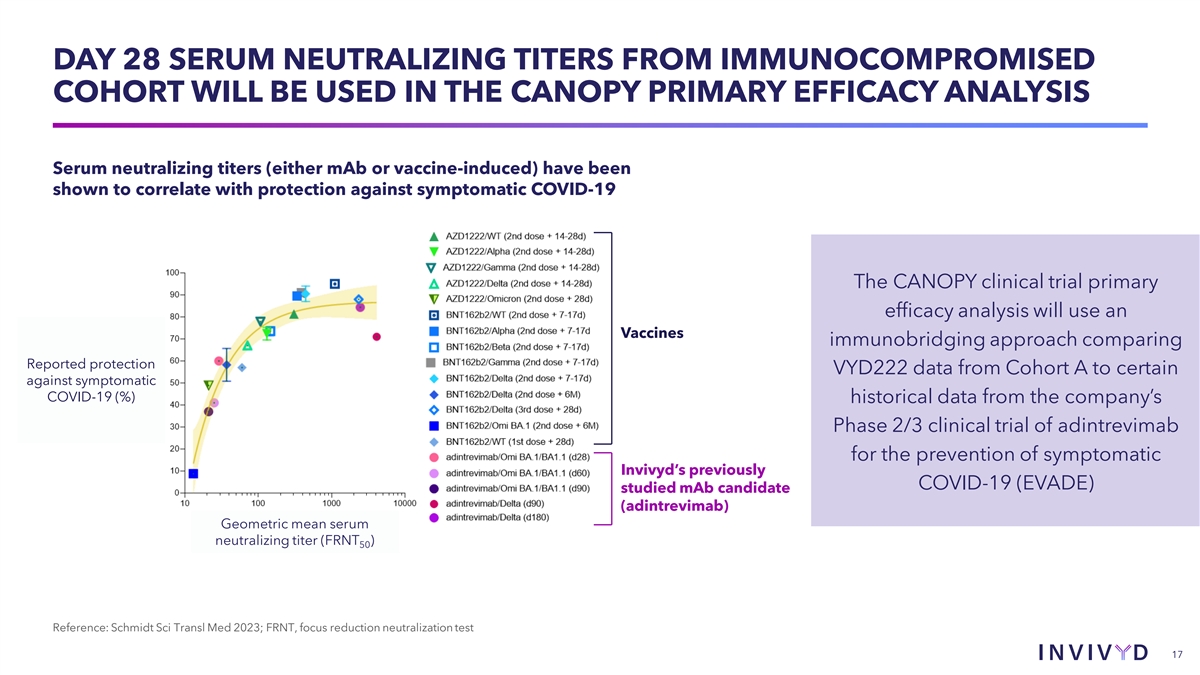
第 28 天免疫功能低下隊列的血清中和滴度將用於 CANOPY 主要功效分析血清中和滴度(單抗或疫苗誘導)已被證明與預防症狀 COVID-19 相關 CANOPY 臨牀試驗的主要療效分析將使用疫苗 免疫橋接方法,將隊列 A 報告的保護 VYD222 數據與該公司有症狀的 COVID-19 (%) 歷史數據進行比較 adintrevimab 預防有症狀的 2/3 期臨牀試驗 Invivyd 之前的 COVID-19(EVADE)研究了單克隆抗候選藥物(adintrevimab)幾何平均血清中和滴度(FRNT)50 參考文獻:Schmidt Sci Transl Med 2023;FRNT,減焦中和試驗 17
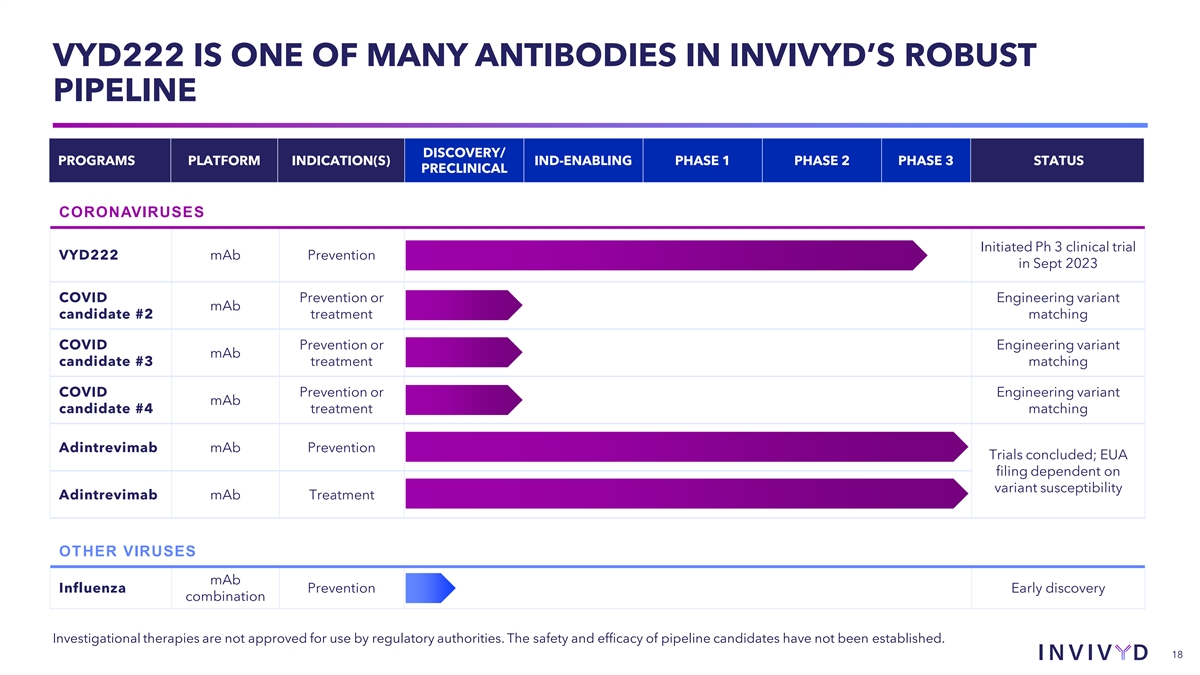
VYD222 是 INVIVYD 強大的產品線中的眾多抗體之一 DISCOVERY/ PROGRAMS 平臺適應症支持 IND 的 1 期 2 期 3 期現狀臨牀前冠狀病毒於 2023 年 9 月啟動 Ph 3 臨牀試驗 VYD222 單抗預防 COVID 預防或工程變異單抗候選藥物 #2 治療 匹配COVID預防或工程變異單抗候選藥物 #3 治療匹配COVID預防或工程變異單抗候選藥物 #4 治療匹配 Adintrevib 單克隆抗體預防試驗結束;EUA申請取決於變體 的易感性Adintrevimab 單抗治療其他病毒單抗流感預防早期發現組合研究性療法未獲監管機構批准使用。候選產品的安全性和有效性尚未確定 。18

具有傳染病專業知識和成功記錄的管理團隊 Peter C. Schmidt,醫學博士,史黛西·普萊斯理學碩士,M.S. William Duke,M.B.A. Dave Hering,工商管理碩士首席醫學官首席技術與製造官首席財務官兼董事吉爾·安德森,法學博士 Jeremy Gowler Robert Allen 博士,首席法務官兼公司首席運營祕書兼商務官首席科學官 19

INVIVYD 有望進入轉型期,短期 有機會提供急需的治療方法為免疫功能低下的人羣提供保護,使其免受 COVID-19 侵害,這是一項令人信服的、潛在的長期價值主張 Invivyd 正在迅速執行其 VYD222 臨牀開發計劃,2023 年第二季度公佈了積極的 1 期臨牀數據,CANOPY 3 期臨牀試驗的初始主要終點數據預計將於 2023 年底/第一季度初 2024 現金、現金等價物和有價物品 截至2023年6月30日,2.984億美元的證券預計將支持2024年第四季度的運營跑道,其中不包括對商業產品收入的潛在貢獻 20

謝謝!