| 投資者 演示文稿 2023 年 8 月 |
| 免責聲明 除本演示文稿中包含的歷史事實陳述外,涉及我們預期、認為或 預計將來將發生或可能發生的活動、事件或事態發展的所有陳述均為前瞻性陳述。這些陳述基於管理層當前的預期、假設、 的估計和信念。儘管我們認為此處包含的前瞻性陳述有合理的依據,但我們提醒您,這些陳述基於 當前對影響我們的未來事件的預期,並且受與我們的運營和業務環境相關的風險、不確定性和因素的影響,所有這些因素都難以預測,其中許多是我們無法控制的,這可能會導致我們的實際業績與本演示文稿中 前瞻性陳述所表達或暗示的結果存在重大差異。這些可能導致實際業績與 前瞻性陳述中描述的結果存在重大差異的潛在風險和不確定性包括但不限於 COVID-19 疫情的持續時間和嚴重程度及其對我們的業務或 經濟的影響的不確定性;包括外匯波動在內的總體宏觀經濟狀況的影響;CMS 為使用公司 iStent 系列產品的程序最終確定的 2022 年和 2023 年降低的醫生費和 ASC 設施費報銷 費率以及它的對我們在美國的組合型白內障青光眼收入的影響; 我們繼續銷售商業化產品以及開發和商業化更多產品的能力;我們的產品組件依賴數量有限的 第三方供應商,其中一些供應商是單一來源的;我們的主要工廠發生嚴重事故、自然災害、疫情或其他 中斷,這可能會對我們的製造能力產生重大影響和運營;確保或維持足夠的保險或 由政府報銷或使用iStent®、iStent inject® W、iAccess、iPrime、iStent infinite、我們的角膜交聯 產品或其他正在開發的產品進行手術的第三方付款人;我們有能力在競爭激烈且瞬息萬變的醫療器械行業中與當前和未來的技術進行有效競爭(包括 MIGS technologies);我們遵守聯邦、州和外國法律法規以獲得批准以及我們的產品和製造流程的銷售和營銷 ;漫長而昂貴的臨牀試驗過程以及任何特定的臨牀試驗或監管部門批准流程的時間和結果的不確定性 ;我們的產品出現召回或嚴重安全問題的風險以及患者預後的不確定性;我們保護我們的知識產權免受第三方和競爭對手侵害的費用和耗時性以及針對我們的任何侵權索賠的影響或 挪用第三方知識產權和任何相關訴訟;以及我們償還債務的能力。 這些和其他已知的風險、不確定性和因素在 “風險因素” 標題下以及我們向美國證券和 交易委員會(SEC)提交的文件的其他地方進行了詳細描述,包括我們於2023年8月2日向美國證券交易委員會提交的截至2023年6月30日的季度10-Q表季度報告。我們向美國證券交易委員會提交的 文件可在我們網站的投資者欄目www.glaukos.com或www.sec.gov上查閲。此外,有關我們產品的風險和收益的信息,請訪問我們的網站 www.glaukos.com。 上述警示陳述明確限定了本演示文稿中包含的所有前瞻性陳述。提醒您不要過分依賴本演示文稿中的前瞻性陳述,這些陳述僅代表截至本文發佈日期 。除非適用的證券法另有要求,否則我們不承擔任何義務更新、修改或澄清這些前瞻性陳述,無論是由於新信息、未來事件 還是其他原因。 © 2023 Glaukos 公司 2 |
| 我們會先走 創新是我們所做一切的核心。在Glaukos,我們 突破科學和技術的極限,以解決慢性眼病中未得到滿足的需求 。 © 2023 Glaukos 公司 3 |
| 我們的核心戰略 1.大創意 2.顯著的臨牀需求 3.專業的研發團隊 4.經驗豐富的銷售組織 5.久經考驗的市場建設者 6.高效的全球運營 旨在推動長期增長和價值創造 © 2023 Glaukos Corporation 4 |
| 自 2018 年以來投資研發 5 個不同的平臺 在 3 個特許經營中產生顛覆性的 無滴創新 4 億美元 14 2023 年披露的管線 項目,自 2018 年以來有 4 個投資於研發。我們的大創意 開發新的 pless 療法來 顛覆受困擾的傳統 局部滴眼液 療法 猖獗患者 非 -依從性 © 2023 Glaukos Corporation 5 |
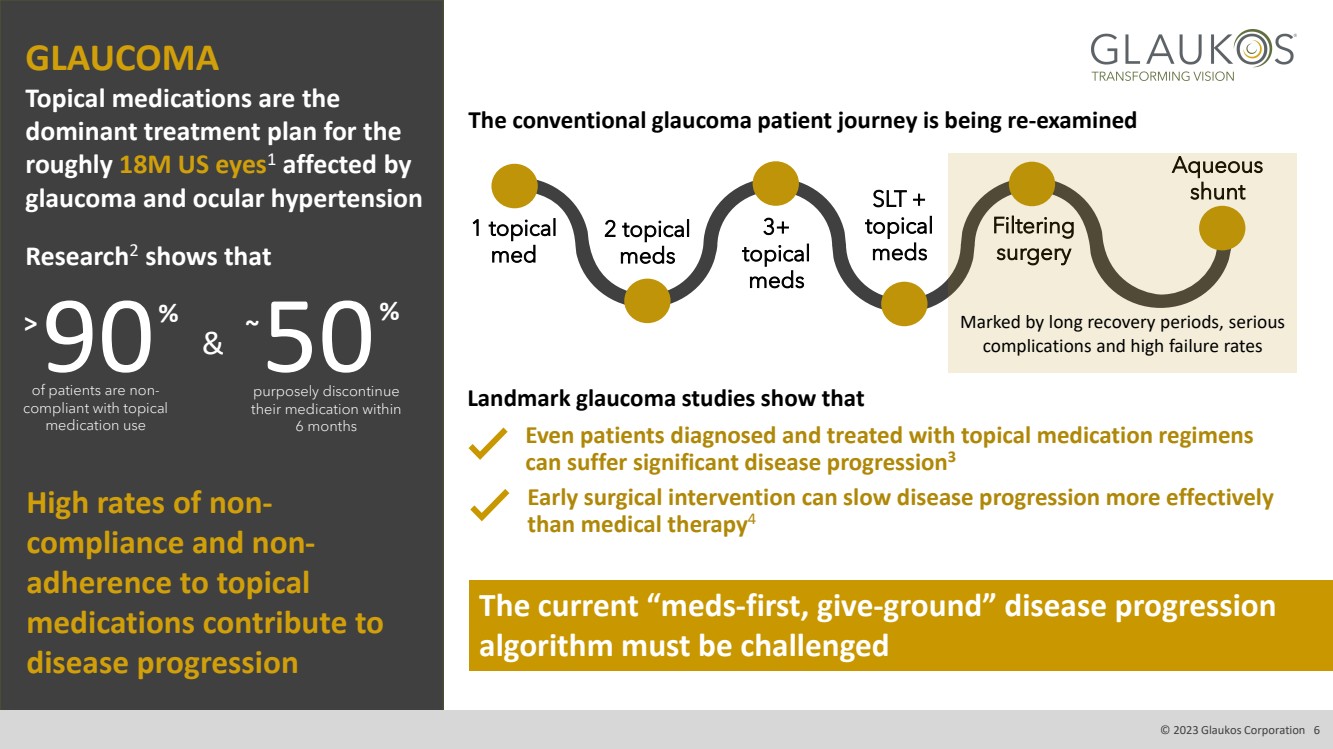
| 青光眼 局部用藥是 受青光眼和高眼壓影響的大約1800萬美國眼睛1的主導治療計劃 Research2 表明 >90% & 50 ~ % 的患者不符合局部用藥 使用 故意在 內停藥 br} 6 個月 外用 藥物的不合規率和不依從率高導致 疾病進展 即使是接受局部藥物治療和診斷的患者 也可能出現明顯的疾病進展3 Landmark青光眼研究表明 早期手術幹預可以比藥物治療更有效地減緩疾病進展 4 必須挑戰當前的 “藥物優先、讓步” 的疾病進展 算法 正在重新審視傳統的青光眼患者旅程 1 外用 med 2 外用 藥物 slt + topical meds 3+ 外用 meds meds 過濾 手術 Aqueous 分流術 以恢復期長、嚴重的 併發症和高失敗率為標誌 © 2023 Glaukos Corporation 6 |
| 介入性青光眼 青光眼 通過預測性 診斷、積極的患者 監測和程序性 幹預 在 治療模式的早期進行積極的青光眼 管理,以: • 改善患者管理 • 保持視覺功能 • 減緩疾病進展 • 減少或消除 對局部藥物和/或 侵入性切口手術的需求 } 介入性青光眼代表了 Glaukos 的創始承諾,即從根本上改變 傳統的治療算法 MIGS 療法,安全有效地減緩 青光眼進展並減輕藥物負擔 目標是全天候基礎眼壓控制,副作用或缺點最小 1 2 MIGS 療法的良性質迫使外科醫生 儘早考慮介入性青光眼治療 3 改善青光眼患者的生活質量 © 2023 Glaukos Corporation 7 |
| 介入性 青光眼 小樑旁路術 持續釋放 Viscodelivery 淋巴切開術 結膜下切開術 憑藉唯一全面的 青光眼產品組合 Glaukos 在解決這一重要未得到滿足的 需求並引領 介入性青光眼機會的開發方面處於獨特的地位 br} C o m b o-C a t a r a c t s t a n d a l o n e 為高達 240° 的液體流出覆蓋範圍創建 3 條路徑 流出覆蓋範圍;之前的醫療和 手術治療失敗 為液體 流出創建 2 條通路;更寬的法蘭可增強 的易用性和能見度 C o m b o-C a t a c t o r s t a n d a l o n e 精確刀片專為切割 小樑網狀組織而設計 粘彈性輸送系統 旨在提供卓越的 手術控制和精度 旨在提供全天候的、持續的 直接釋放 進入前房 ab-externo 3 期(已提交保密協議) 結膜下設備 基於疾病分期嚴重程度的定製療法 iDose TR 和 PreserFlo 未獲得美國食品藥品管理局的批准;iAccess 和 iPrime 尚未獲得美國食品藥品管理局的批准美國食品藥品管理局將在青光眼治療中減少眼壓值 © 2023 Glaukos Corporation 8 |
| 12 個月臨牀試驗 RESULTS5 76 ≥ % 的受試者在相同或 較低的藥物負擔下 平均眼壓降低 20% 或更多 50% 的受試者實現了 30% 或更大的降低 平均眼壓 有史以來第一臺用於獨立青光眼治療的微創植入設備 • 三個微型支架旨在提供高達 240° 的青光眼治療 • 三個微型支架旨在提供高達 240° 的青光眼持續、全天候流出 • Pivotal 試驗結果證實了非常有利的療效和安全性 • FDA 於 2022 年獲準用於先前 藥物和手術治療中無法控制的 OAG 患者;美國正在分階段上市 • 在長達數十年的iStent技術成功使用組合型白內障手術記錄的支持下 最難治療的基線平均降低 3.1 iOP 藥物且之前平均有 2 次 青光眼手術失敗的患者 20+ iStent 臨牀 經驗 br} 250+ 關於 iSent 技術的同行評審出版物 全球植入了 100 萬多臺 iStent 設備 © 2023 Glaukos Corporation 9 |
| 提供全天候長期治療,旨在解決 無處不在的患者對局部用藥 藥物的不依從性和 慢性副作用 。 介入性青光眼武器庫的下一個重要補充 • 旨在提供長期的 院內藥物;安全且 錨定設計;易於植入和 } 交易所 • 膜洗脱了特殊配方的 曲伏前列腺素,一種常用的外用處方 前列腺素,提供 100% 的合規性 • 2023 年 2 月提交了保密協議;PDUFA 日期定為2023 年 12 月 22 日 • 據估計,美國每年有 3M eyes6 旨在提供曲伏前列素 專有 配方的微創 植入物 iDose TR 尚未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 10 |
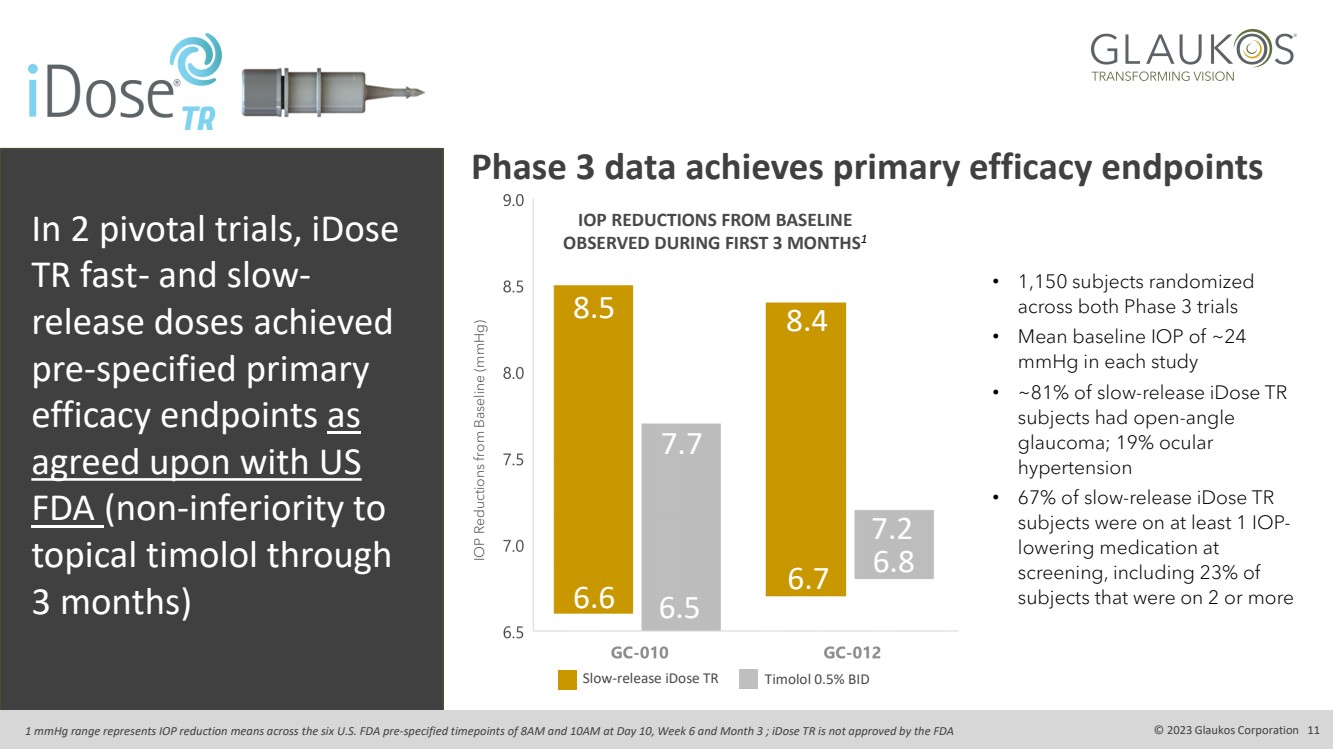
| 在兩項關鍵試驗中,iDose TR 快釋和緩釋劑量達到了 預先指定的主要 療效終點 與美國 FDA 達成的協議(在 3 個月內不遜於 局部噻嗎洛爾) IOP 比基線 (mmHg) 8.5 6.6 7.7 6.7 6.7 8.4 6.8 7.2 慢釋iDose TR 哈哈 0.5% BID 在前 3 個 MONTHS1 中觀察到 IOP 比基線降低 • 在兩項第 3 階段試驗中,有 1,150 名受試者隨機分組 • 每項研究的平均基線 IOP 約為 24 mmHg • 大約 81% 的緩釋iDose TR 受試者有開角度 青光眼;19% 眼部 高血壓 • 67% 的緩釋iDose TR 受試者在 篩查中至少服用了一種降低 IOP 的藥物,包括 23% 服用 2 個或更多 3 期數據達到主要療效終點 1 mmHg 範圍代表美國食品藥品管理局預先指定的上午 8 點和 10 點這六個時間點的 IOP 降低平均值上午在第 10 天、第 6 周和第 3 個月;iDose TR 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 11 |
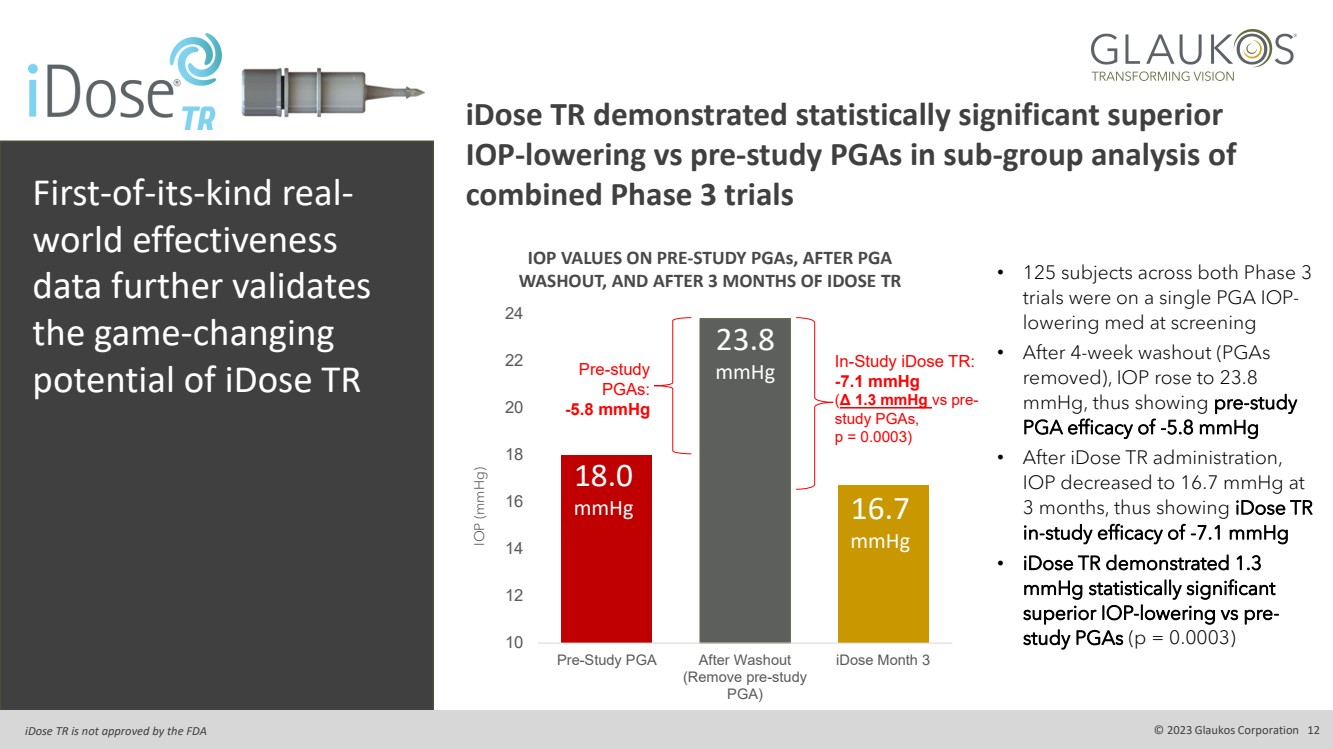
| 同類首創的現實世界有效性 數據進一步驗證了 iDose TR IOP (mmHg) 改變遊戲規則的潛力 10 12 14 16 18 20 22 24 PGA 沖洗後 (移除研究前 PGA) iDose 第三月 18.0 mmHg 16.7 mmHg 23.8 mmHg 研究前 PGA、PGA 沖洗後和 IDOSE TR 3 個月後 • 兩項 3 期試驗的 125 名受試者在篩查時都在服用一種降低 PGA IOP 的藥物 • 經過4周的沖洗(去除 PGA ),IOP 升至 23.8 mmHg,因此顯示研究前 PGA 療效為 -5.8 mmHg •iDose TR 給藥後, IOP 在 3 個月時降至 16.7 mmHg,因此顯示 iDose TR 在研究中的療效為-7.1 mmHg • iDose TR 與研究前 PGA 相比,iDose TR 的降低 IOP 優於研究前 PGA(p = 0.0003) iDose TR 在統計學上顯著優於研究前 PGA (p = 0.0003) iDose TR 的降低 iOP 在統計學上顯著優於研究前 PGA 在 組合 3 期試驗的亞組分析中 iDose TR 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 12 預研究 pGA: -5.8 mmHg 在研究 iDose TR: -7.1 mmHg (Δ1.3 mmHg vs 研究前 PGA, p = 0.0003) |
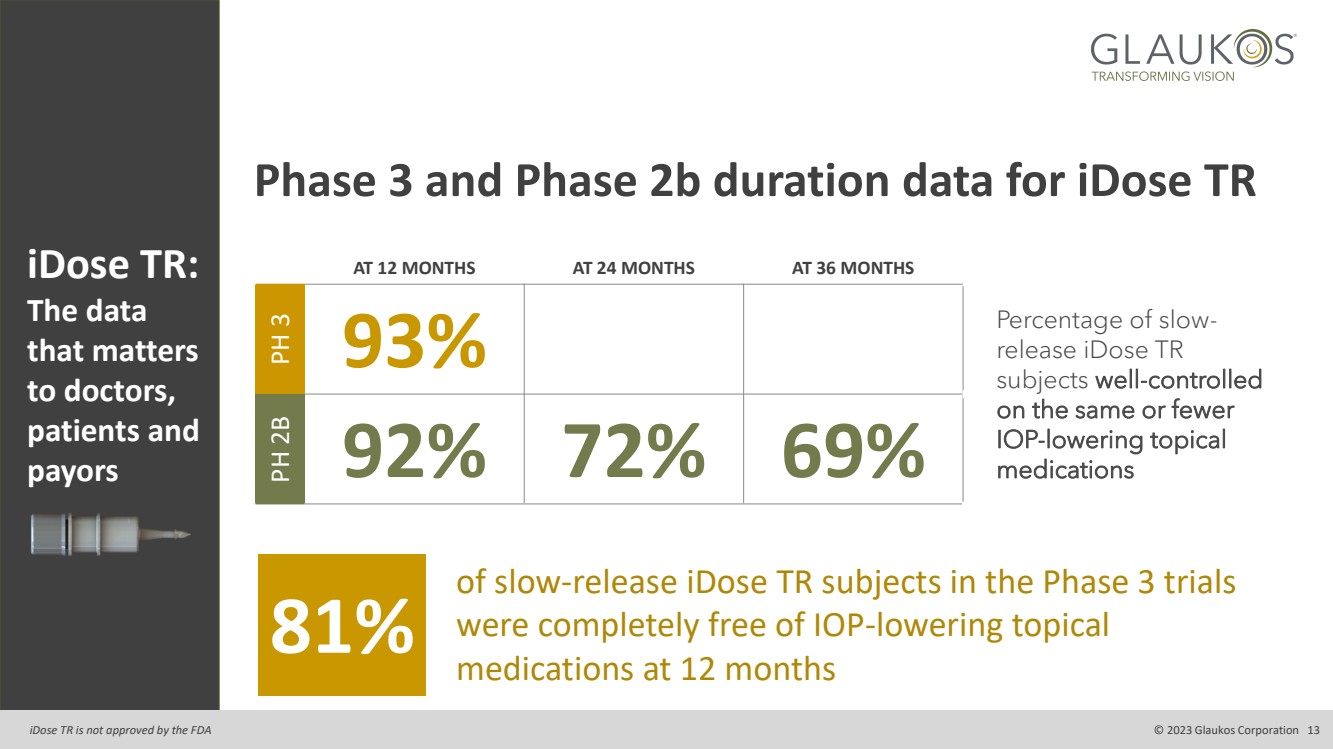
| iDose TR 的 3 期和 2b 期持續時間數據 iDose TR: 對醫生、 患者和 付款人很重要的數據 在 12 個月時為 24 個月和 36 個月 PH 3 93% 緩釋iDose TR 受試者中控制得當 使用相同或更少 降低 iOP 的局部藥物的百分比 br} PH 2B 92% 72% 69% 的藥物 在第三階段試驗中緩釋的 iDose TR 受試者 在 12 個月時完全沒有降低 IOP 的局部藥物 81% iDose TR 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 13 |
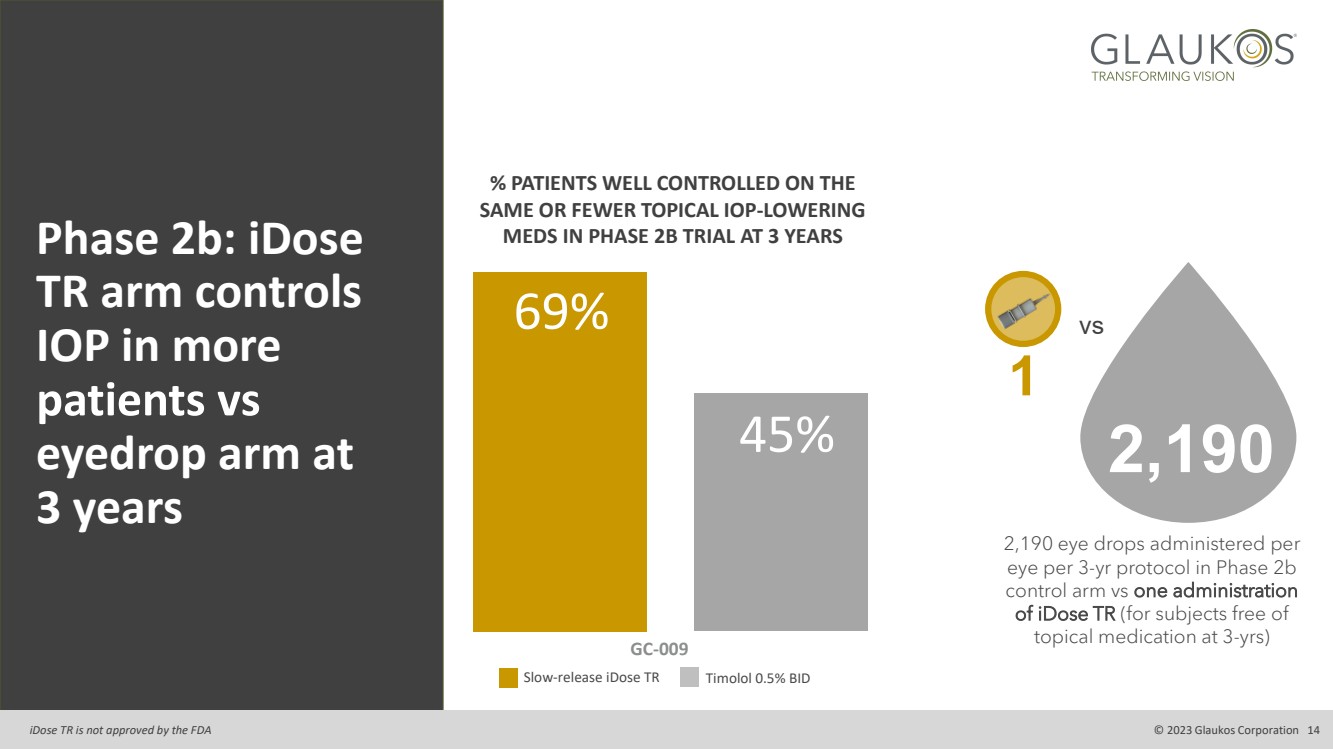
| GC-009 緩釋型 iDose TR 噻嗎洛爾 0.5% BID % 患者控制良好 相同或更少的局部降低 IOP 2b 期:iDose 藥物在 3 年內進行 2B 期試驗 TR arm 控制更多 患者的 IOP vs 3 年 69% 45% 2,190 在 2b 期 對照組中,每 3 年每個 眼藥水與一次給藥 iDose TR(適用於 3 歲時沒有 局部用藥的受試者) vs 2,190 1 iDose TR 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 14 |
| iDose TR 的 3 期和 2b 期安全數據 iDose TR: 對醫生、 患者和 付款人很重要的數據 Topical Ph 3 試驗 1 年 Ph 2b 試驗 3 年 沒有軌周脂肪萎縮的不良事件發病率至 70% 結膜非常低或沒有結膜 充血發病率 30%-50% 沒有角膜 內皮細胞流失的不良事件 虹膜變色發生率非常低或沒有 發病率 20% iDose TR 未獲美國食品藥品管理局批准 © 2023 Glaukos Corporation 15 |
| • 評估交換手術安全性的前瞻性多中心試驗 • 該研究招收了之前植入 iDose TR 2b 期研究的 33 名受試者 • 受試者的研究眼睛接受了慢釋放 iDose TR 模型的手術 交換,隨訪 12 個月 • 平均總體延期評估期為 5 年以上 Exchange 研究的陽性 數據套裝包含在 NDA 提交中以啟用 重複給藥 在 5 年以上的時間內角膜 內皮細胞計數沒有具有臨牀意義的變化 交換研究中沒有患者在延長的評估期內表現出 內皮細胞流失(流失 ≥ 30%)的不良事件 對重新給藥 iDose TR 0 500 1000 1500 2000 2500 2500 ph2b baseline ph2b 3 年重劑量 基線(4.2 年) 第二劑 1 年 (5.2 年) 角膜內皮細胞 (5.2 年) 角膜內皮細胞 密度 (cells/mm2) iDose TR 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 16 |
| iDose TR 有 潛力 解決 患者不遵守 局部青光眼 藥物的猖獗問題 iDose TR 未獲得美國食品藥品管理局的批准 作為第三階段試驗的一部分,在多個地點對不同受試者使用了 iDose TR,結果與第 3 期試驗一致 } 辦公室內給藥 臨牀試驗療效數據 在 3 期試驗中,93% 的受試者控制良好,81% 的受試者在 12 個月時完全沒有服用降低 IOP 的藥物;階段2b 試驗顯示 69% 的受試者在 36 個月時仍能得到很好的控制 Exchange 試驗數據 臨牀試驗安全數據 局部降低 IOP 的藥物常見的副作用發生率低或沒有;沒有與角膜內皮細胞流失相關的不良事件 前瞻性、多中心交換試驗,包括 33 名 2b 期受試者在 12 個月時表現出安全性 iP Dose TR 未獲美國食品藥品管理局批准 © 2023 Glaukos Corporation 17 |
| 產品患者狀態 COMBO-白內障 iStent/iStent 注射/ iStent 注射輕度至中度青光眼並伴有白內障批准 (2012 /2018/2020) istent 無限青光眼 (標籤擴展)IDE 已打開 istent 無限青光眼 istent 無限青光眼 } PreserFlo 高級難治性青光眼 OUS 批准 美國 IDE 計劃 iDose TR OHT-Glaucoma NDA 已提交 PDUFA 日期:12 月 22 日 iDose TREX OHT-Glaucoma 臨牀前 iDose ROCK OHT-Glaucoma 臨牀前 iDose ROCK OHT-Glaucoma 臨牀前 iLution Travoprost oht-GlaucomaIND open iAccess Precision Corporation FDelivery 美國食品藥品管理局批准 iPrime Viscodelivery FDelivery FDA 批准 青光眼組合 青光眼全方位進展 iAccess 和 iPrime 尚未獲美國食品藥品管理局批准減少青光眼治療中的 IOP © 2023 Glaukos Corportion 18 |
| iLink PLATFORM 針對圓錐角膜的生物活化角膜交聯 療法,圓錐角膜是一種危及視力、改變生命的疾病 ,通常發病於青春期 第一個也是唯一一個經美國食品藥品管理局批准的生物活化藥物 療法被證明可以減緩或阻止圓錐角膜的進展。 如果沒有有效的治療,五分之一的進展性圓錐角膜患者可能需要角膜移植。7,8 73 98% 的角膜移植術分別在 20 年和 30 年內失敗 和 30 年內失效 7,8 和 % % % Photrexa (epioff) Keratoconus 獲批 (2016) % % Photrexa (epioff) Keratoconus 獲批 (2016) Epioxa (epi-on) 圓錐角膜 第 1 期 3 期試驗已完成; 第 2 期 3 期確認性 試驗註冊已完成 iLink 第三代圓錐角膜第 2 期 iVeena Keratoconus 第 1 期商業產品和已披露的管線計劃 © 2023 Glaukos Corporation 19 |
| -1.0D 通過證明 耐受性良好的手術的 Kmax 治療效果實現了主要療效 結果 (大多數不良事件本質上是輕微和短暫的;在試驗過程中,角膜內皮細胞計數沒有 變化) 確定為 中與基線相比的最小 平方均值 Kmax 變化 與安慰劑組 6 個月時對比安慰劑組 (p = 0.0004) 0.2D 在治療組中,與安慰劑 Kmax 惡化0.8D 相比,Kmax 有所改善 ,這表明 Epi-on 的 有能力停止或減少 br} 疾病進展 98% 在最初的 6 個月隨訪後, 的安慰劑隨機化 患者選擇跨界接受Epi-on治療; 這些患者的數據 顯示治療後 6 個月的 Kmax 改善平均值為 0.3D 顯示出阻止或減少圓錐角膜進展的能力 (n=27br} 9 eyes) Epi-On 旨在縮短治療時間 和複雜性, 改善患者 的舒適度和康復率 時間 Kmax 是 角膜曲率的最高點,用屈光度 (D) 測量 Epioxa (epi-on) } 第 1 項第 3 階段試驗 已達到 主要 終點 epi-on 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 20 |
| iLution PLATFORM 透皮無滴療法 有可能治療各種 慢性眼部疾病和疾病 產品/項目患者狀態 iLution 乾眼乾眼症第 2 期 iLution 老花眼老花眼 2 期 iLution 瞼緣炎臨牀前 iLution 曲伏前列素 OHT-Glution 老花眼 2 期 iLution 眼瞼炎蠕形蟎眼瞼炎臨牀前 iLution 曲伏前列素 OHT-Gt 青光眼 IND open 已披露管道程序 Lacrimal Function Unit:集成系統 包括淚腺、眼 表面(角膜、結膜和 瞼板)和眼瞼以及 感覺和運動神經連接 他們。 與用於治療乾眼病和 其他疾病的處方眼藥水相比,iLution 配方的潛在靶點 眼皮給藥可能更容易, 起效更快,副作用和其他益處更少 ,有助於提高依從性。 © 2023 Glakos Corporation 21 |
| -8.5 -8.2 試驗顯示出良好的安全性和耐受性 • 98% 的患者完成了試驗 • 在 5% 或更高發生率時沒有發生眼部不良事件 淚膜質量(淚分裂 時間標誌)的改善以及視力質量 的相應改善(視力模糊症狀減輕) 早期 讀出 iLution 無滴療法治療乾眼病的潛在差異療效 iLution Dry Eye (GLK-301) 2a 期試驗: 218 dry對眼科患者 進行了為期 28 天的研究,並額外進行了 14- 天的安全隨訪 ~55 名患者/手臂在 3 劑 GLK-301 對比安慰劑 GLK-301 2a 期首次進入人體的結果顯示 GLK-301A 安慰劑 43% 22% TEAR 分手時間,百分比 第 28 天基線的變化 GLK-301A 安慰劑 VAS 中的視力模糊改善 第 28 天與基線的變化 27 19 iLution Dry Eye 未獲得美國食品藥品管理局的批准 © 2023 Glaukos Corporation 22 |
| RETINA XR PLATFORM 解決視網膜疾病傳統 療法的顯著 缺點 產品/項目患者狀態 IVT 多激酶抑制劑 AMD、DME、RVO 臨牀前 IVT 曲安西龍 DME 臨牀前 披露的管線計劃 靶向具有 持續療效的可生物降解的小分子植入物,旨在解決 持續療效 傳統注射的缺點會給患者帶來巨大的 治療負擔,並導致 依從性不足 2800 萬人 89% AMD 和 Diabetic Eye Eye疾病 在美國,視網膜疾病 影響大約 2800 萬 人;AMD 和糖尿病 眼病佔該患者羣體的 89% 10 每月或每兩個月注射一次抗 VEGF 是 AMD、DME 和 RVO 的標準護理方法,但研究 表明 39% 的患者因隨訪而流失 br} 2 年9 © 2023 Glaukos Corporation 23 |
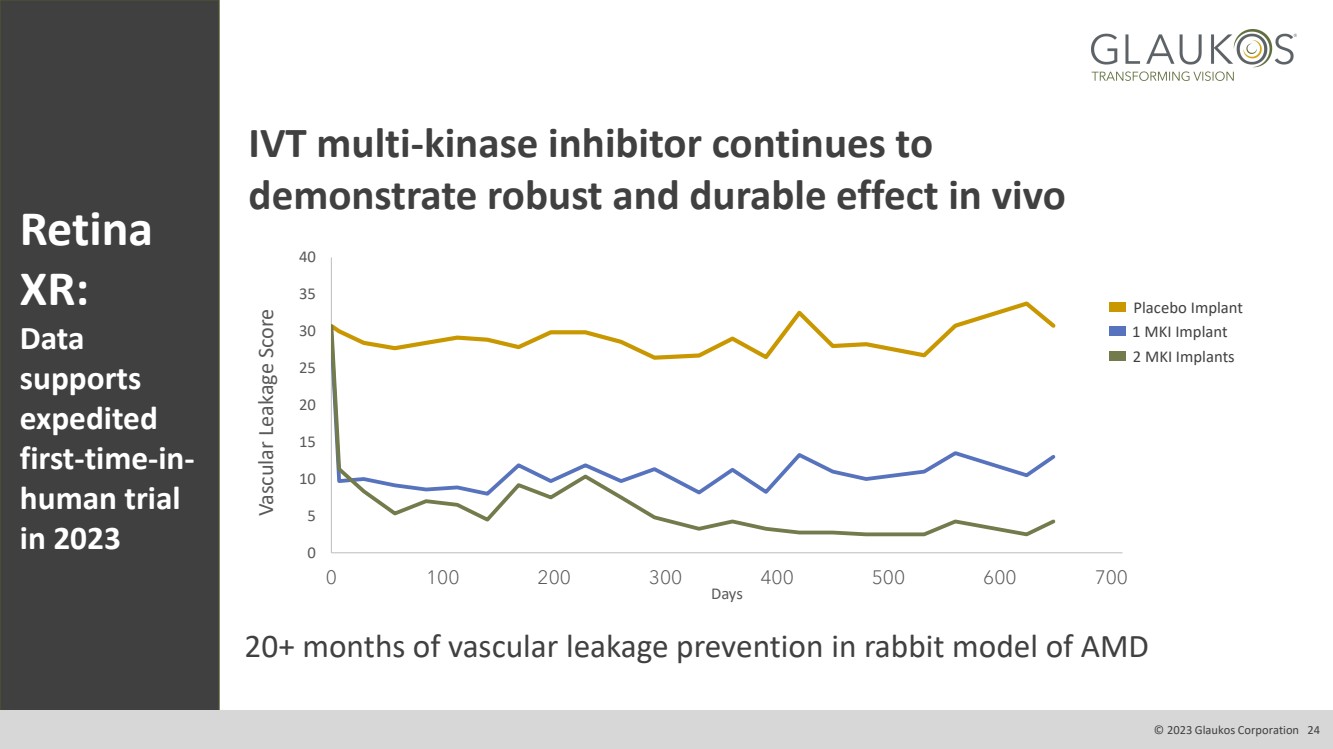
| -8.5 -8.2 視網膜 XR: 數據 支持 2023 年加快 首次人體試驗 在 AMD 的兔子模型中預防 20 多個月的血管滲漏 IVT 多激酶抑制劑繼續在體內表現出強大而持久的效果 0 5 10 10 20 25 30 40 0 100 300 500 700 血管泄漏評分 Days 安慰劑植入物 2 MKI 植入物 1 MKI 植入物 © 2023 Glaukos Corporation 24 |
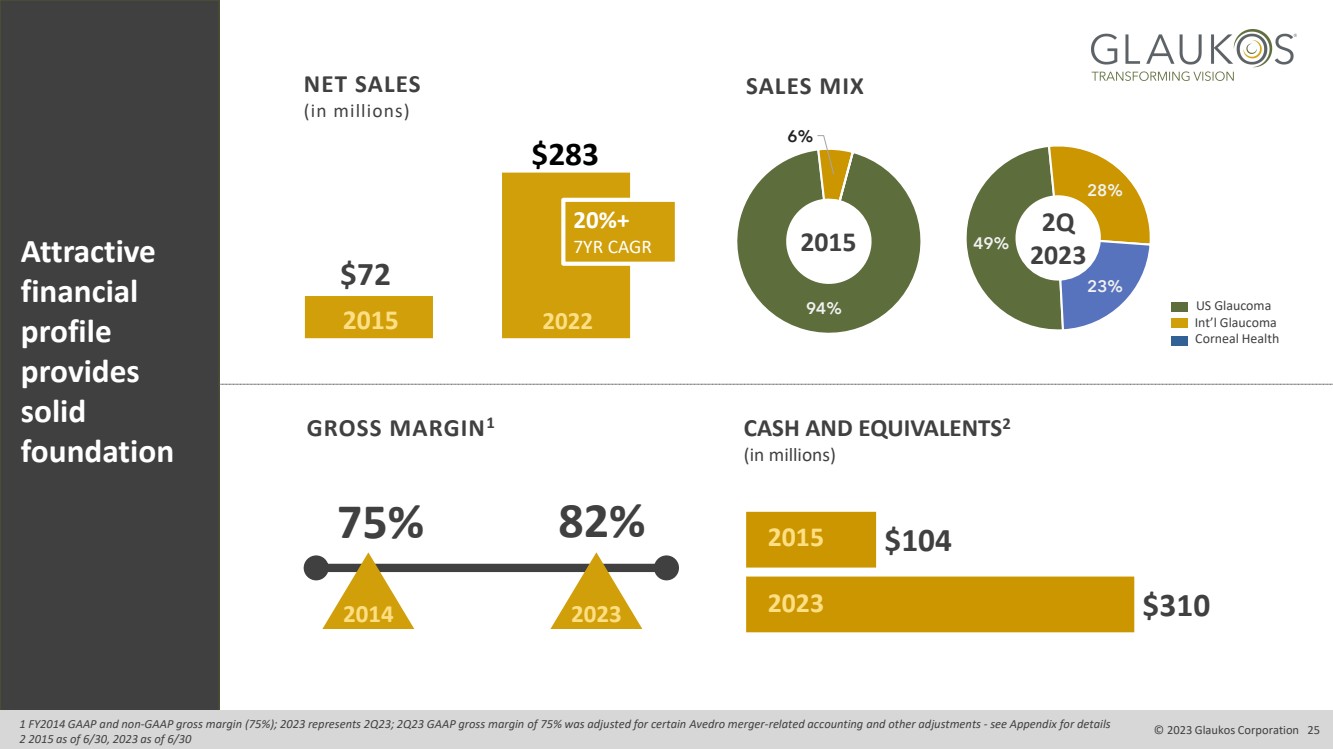
| 有吸引力的 financial 簡介 提供堅實的 基礎 淨銷售額 (百萬美元) 2015 年 2022 美元 283 美元利潤率 75% 82% 2014 年總收入 MARGIN1 2023 年310 美元 2023 年現金和 EQUIVALENTS2(百萬美元) 20% + 7 年複合增長率 2023 年銷售組合 © 2023 Glaukos Corporation 25 1 FY2014 GAAP 和非 GAAP 毛利率 (75%);2023 年代表 23 年第二季度;根據某些與 Avedro 合併相關的會計和其他調整調整調整了 23 年第二季度 GAAP 毛利率為 75% ——詳情見附錄 2 截至2023年6月30日 49% 28% 23% 2023 年第二季度 94% br} 6% 2015 美國青光眼 Corneal Health Int'l Glaucoma |
| 高效、 可擴展的 全球 平臺 支持 增長 2015 2023 65 275+ 全球商業 人員 直接銷售的國家 2014 2 2023 17 輔之以另外 35 個國家的 分銷商和 混合動力車型 全新最先進的混合製藥工廠 © 2023 Glaukos Corporation 26 |
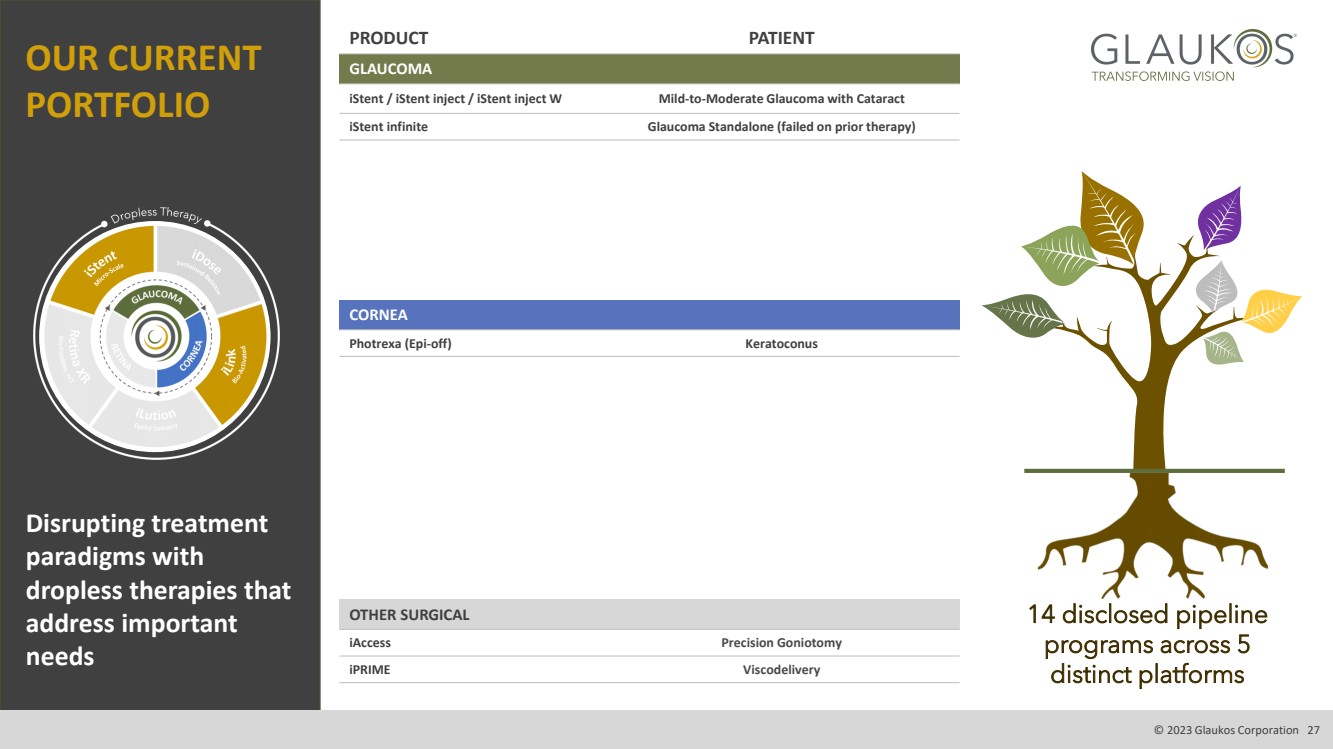
| MARGINS 我們當前的 投資組合 PORTFOLIOS 顛覆治療 範式 解決重要 需求 14 個在 5 個不同平臺上披露的管線 © 2023 Glaukos Corporation 27 產品患者 青光眼 istent/iStent注射/iStent注射了輕度至中度青光眼並伴有白內障 iStent infinite Glaucoma 獨立版(之前的治療失敗) CORNEA Photrexa (epiOFF) 圓錐角膜 其他外科手術 iAccess 精準角膜切開術 iPrime Viscodelivery |
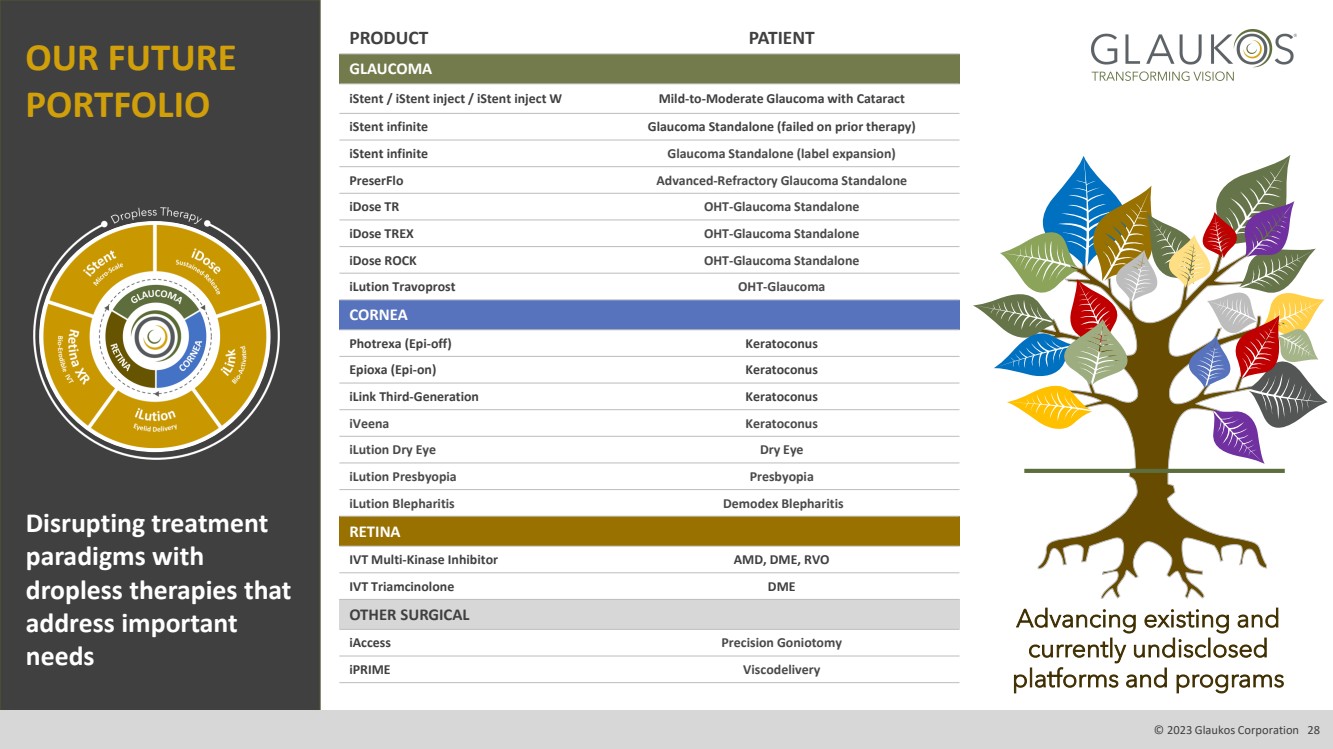
| MARGINS 產品患者 青光眼 iStent/iStent 注射/iStent 注射 W 輕度至中度青光眼伴白內障 iDose 無限青光眼獨立(之前的治療失敗) iStent 無限青光眼獨立版(標籤擴展) preserFlo 高級難治性青光眼獨立版 iDose TR ot-Glaucoma 獨立版 iDose TREX oht-Glaucoma 獨立版 iDose ROCK ot-Glaucoma 獨立版 iLution 曲伏前列素 ot-Glaucoma CORNEA Photrexa (epioff) Keratoconus Epioxa (epi-on) Keratoconus iLink 第三代 Keratoconus iVeena圓錐角膜 iLution 乾眼症 iLution 老花眼老花眼 iLution 瞼緣炎蠕形蟎眼瞼炎 視網膜 IVT 多激酶抑制劑 AMD、DME、RVO IVT 曲安西龍 DME 其他外科 iAccess 精準角膜切開術 {} iPrime Viscodelivery OUR FUTURE PORTFOLIO 使用 無滴療法顛覆治療 範式 滿足重要 需求 推進現有和 目前未公開的 平臺和計劃 © 2023 Glaukos Corporation 28 |
|
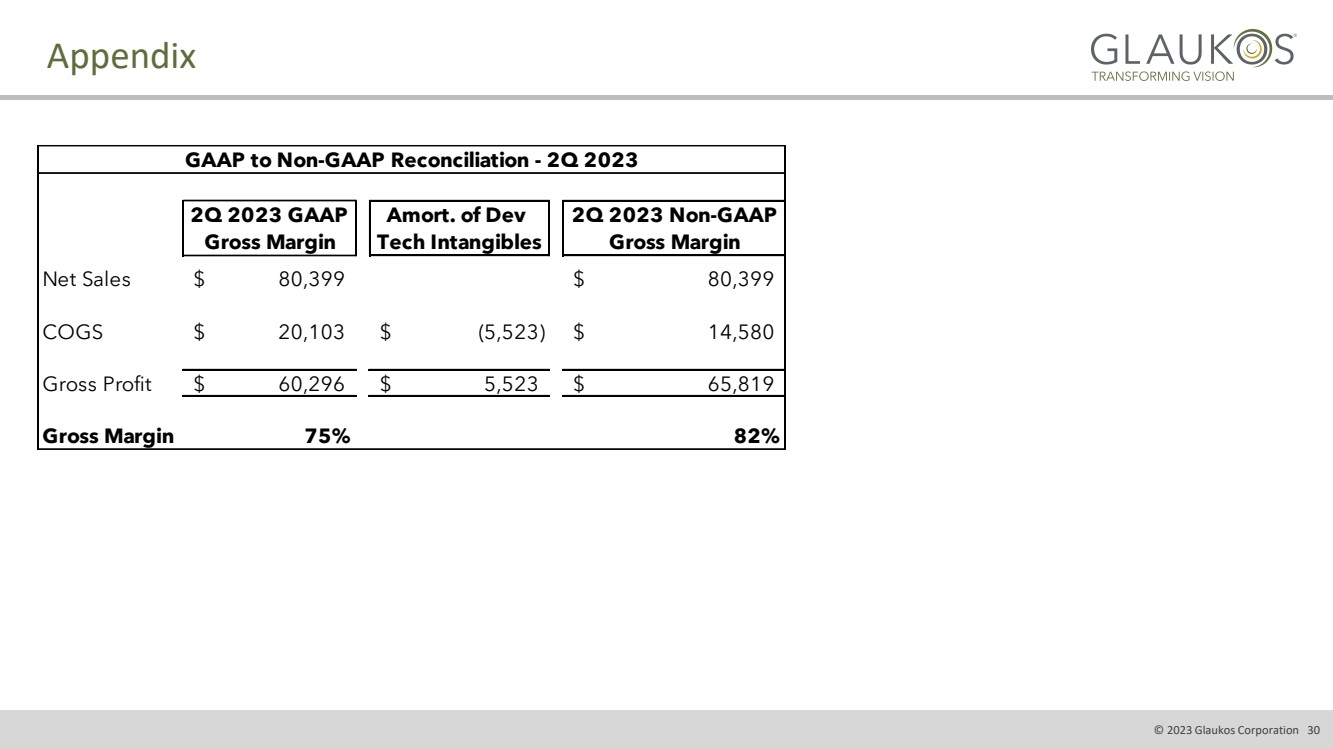
| 附錄 © 2023 Glaukos Corporation 30 2023 年第二季度 GAAP 2023 年第二季度發展分攤額非 GAAP 毛利率科技無形資產毛利率 淨銷售額 80,399 美元 80,399 美元 COGS 20,103 美元 (5,523) 美元 14,580 美元毛利率 60,296 美元 65,819 美元毛利率 75% 82% GAA 2023年第二季度與非公認會計準則的對賬 |
| References 1 Based on company analysis of Market Scope, Medicare Claims and IMS Health Compliance data 2 Nordstrom BL, Friedman DS, Mozaffari E, Quigley H, Walker AM. Persistence and adherence with topical glaucoma therapy. Am J Ophthalmol. 2005;140(4): 598-606 3 Malihi M, Moura, Filho ER, Hodge DO, Sit AJ. Long-term trends in glaucoma-related blindness in Olmsted County, MN Ophthalmology. 2014;121(1):134–41 4 Lichter PR, Musch DC, Gillespie BW, et al. Interim clinical outcomes in the Collaborative Initial Glaucoma Treatment Study comparing initial treatment randomized to medications or surgery. Ophthalmology. 2001;108(11):1943-1953 5 US IDE open-label, single-arm study in a standalone procedure; 72 subjects, including 61 with OAG uncontrolled by prior surgery and 11 uncontrolled by maximally tolerated medical therapy 6 Market opportunity estimates based on Glaukos algorithm of physician preference and combination therapy, utilization; assumes full product portfolio availability to physician, except pre-clinical products (iDose TREX, iDose Rock, etc) 7 Pramanik S, Musch DC, Sutphin JE, Farjo AA. Extended long-term outcomes of penetrating keratoplasty for keratoconus. Ophthalmology. 2006;113(9):1633-1638 8 Maharana PK, Agarwal K, Jhanji V, Vajpayee RB. Deep anterior lamellar keratoplasty for keratoconus: a review. Eye Contact Lens. 2014;40(6):382-389 9 Long-term Experience With Intravitreal Anti-VDGF Treatment in Patients with AMD: Analysis of IRIS Registry Database (presented at 39th Annual Meeting of the American Society of Retina Specialists by Theodore Leng, MD) 10 Market Scope, 2019 . © 2023 Glaukos Corporation 31 |