
1 Prime Medicine 202

2 本演示文稿包含1995年《私人證券訴訟改革法》所指的Prime Medicine, Inc.(“Prime”、“我們” 或 “我們的”)的前瞻性陳述。這些前瞻性陳述包含有關我們當前和未來前景以及我們的運營和財務業績的信息,這些信息基於當前可用信息。除本演示文稿中包含的歷史事實陳述外,所有陳述,包括有關我們的戰略、未來財務狀況、未來運營、預計成本、前景、計劃、管理目標和預期市場增長的陳述,均為前瞻性陳述。在某些情況下,你可以通過諸如 “目標”、“預期”、“假設”、“相信”、“考慮”、“繼續”、“可以”、“設計”、“到期”、“估計”、“預期”、“目標”、“打算”、“可能”、“目標”、“機會”、“預測”、“定位”、“潛力”、“潛力” 等術語來識別前瞻性陳述尋找”、“應該”、“目標”、“將” 和其他類似的表達方式,即預測或表明未來事件和未來趨勢,或者這些術語或其他類似術語的否定詞。這些前瞻性陳述包括但不限於關於Prime在以下方面的信念和期望的明示或暗示陳述:我們的研發計劃、臨牀前研究和未來臨牀試驗的啟動、時機、進展和結果,包括啟動針對慢性肉芽腫病(CGD)的研究性新藥支持研究以及我們的弗裏德賴希共濟失調和囊性纖維化項目;我們的 PASSIGE 技術在以下方面的應用能力細胞療法;我們的展示能力,以及時機多個項目的臨牀前體內概念驗證;我們追求戰略適應症類別的能力:即時靶向適應症、重複擴張障礙適應症和其他分化靶適應症;我們提交監管申請的時機,包括我們提交的研究性新藥申請,包括我們預計最早在2024年提交的首次IND申請,預計將在2025年提交更多申請;我們展示Prime Editing項目卓越的偏離目標特徵的能力;我們的開發和優化各種非病毒和病毒傳遞系統;我們使用專有的重組酶和/或逆轉座子以及其他專有技術擴展 Prime Editing;我們能夠為涵蓋我們的 Prime Editing 技術的知識產權建立和維護的保護範圍;結合我們和 Cimeio 各自技術的研究合作,包括我們的 Prime Editing 平臺和 Cimeio 的 SCIP 平臺,以及此類合作的目標、此類合作的潛在好處,包括能夠治癒各種疾病和取代移植等現有治療方法,以及行使獨家選擇權和支付經濟學費用;實施我們的業務、計劃和技術戰略計劃,包括我們確定和簽訂未來許可協議和合作的能力;以及我們對2025年之前的支出、資本要求和額外融資需求以及現金流量的估計。由於存在許多風險和不確定性,實際業績或事件可能與我們在前瞻性陳述中披露的計劃、意圖和預期存在重大差異。這些風險和其他風險、不確定性和重要因素在我們最新的10-Q表季度報告中標題為 “風險因素” 的部分以及隨後向美國證券交易委員會提交的任何文件中進行了描述。任何前瞻性陳述僅代表截至本演示文稿發佈之日的觀點,我們沒有義務更新或修改任何前瞻性陳述,無論是由於新信息、某些事件的發生還是其他原因。我們實際上可能無法實現前瞻性陳述中披露的計劃、意圖或預期,您不應過分依賴我們的前瞻性陳述。對任何此類前瞻性陳述的準確性不作任何陳述或擔保(明示或暗示)。本演示文稿中包含的某些信息涉及或基於從第三方來源獲得的研究、出版物、調查和其他數據以及我們自己的內部估計和研究。儘管我們認為截至本演示文稿發佈之日,這些第三方研究、出版物、調查和其他數據是可靠的,但我們尚未對從第三方來源獲得的任何信息的充分性、公平性、準確性或完整性進行獨立驗證,也沒有做出任何陳述。此外,沒有獨立來源評估過我們內部估計或研究的合理性或準確性,也不得依賴本演示文稿中與此類內部估計和研究有關或基於此類內部估計和研究的任何信息或陳述。前瞻性陳述

3 Prime Medicine 在正確的時間彙集了合適的人才和正確的技術,旨在兑現一次性治療性遺傳療法的承諾,以解決最廣泛的疾病。在第一位患者接受基因療法治療30年後,基因編輯才剛剛開始顯示出臨牀益處。現在是革命的時候了。

5 實現基因編輯的全部承諾需要一項極其強大的技術 Prime Editing (PE) 作為一流的遺傳醫學方法脱穎而出多功能性:只有具有編輯、更正、插入和刪除能力的基因編輯技術才能執行和糾正插入、刪除和所有十二種類型的單鹼基對校正精確的靶標插入或刪除千鹼基大小的DNA 可輕鬆編程到獨特的目標位置並進行廣泛的編輯恢復多種突變的基因功能使用單一產品(即 “熱點”)精度:儘量減少或不進行偏離目標的編輯可能會安全得多不會產生雙鏈中斷:目標編輯部位的索引率低,特異性高,不會產生雙鏈中斷:目標位點 “旁觀者編輯” 的潛力有限效率:Prime Medicine 產品組合中展示的持久高效編輯傳遞給子細胞的永久編輯原位校正基因,保持原生基因基因控制單劑量,可能野生型序列的治療性校正廣度:能夠解決多種組織類型和細胞中大約 90% 的致病突變糾正分裂和非分裂人體細胞中的突變 Prime Editing 工具箱中已有 100 種潛在適應症

6 Prime Medicine 完全有能力最大限度地發揮 Prime Editing 的廣泛治療潛力自公司成立以來的大約 2.5 年內:建立並推進了由 18 個項目組成的戰略產品組合 • 專注於展示技術成功的最快、最直接途徑的適應症,以及無法使用其他基因編輯方法治療的疾病 • 多個項目正在向開發候選藥物邁進,最早可能在 2024 年提交首次IND 申請展示的 Prime 編輯能力:成熟的臨牀前概念驗證和安全性 • 長期植入用於慢性肉芽腫病的 Prime Edited 造血幹細胞療法 • 有效去除弗裏德賴希共濟失調(一種重複擴張病)的病理重複,對患者類器官進行表型校正 • 高效編輯囊性纖維化患者類器官的表型校正高效 CMC 和遞送能力 • 齧齒動物肝臟和中樞神經系統的體內 Prime 編輯優化和擴展的 Prime Editing 平臺、功能和 IP • 使用 PASSIGE 技術一步非病毒精確地將全基因插入原代人類細胞的基因組 • 工業化和自動化 Prime Editor 篩選能力 • 先進且大幅改進的 Prime Edition • 建立了強大的企業地位由世界一流、多元化的研究人員和藥物開發人員團隊領導;公司發展到約 200 名員工 A/B 輪融資約 3.15 億美元,首次公開募股(22 年 10 月),來自一羣藍籌股投資者利用與創始人 David Liu 和 Andrew Anzalone 的密切關係,為 Prime Medicine 快速帶來新的創新,目標是在 2023 年通過BD和合作創造額外價值並擴大影響力
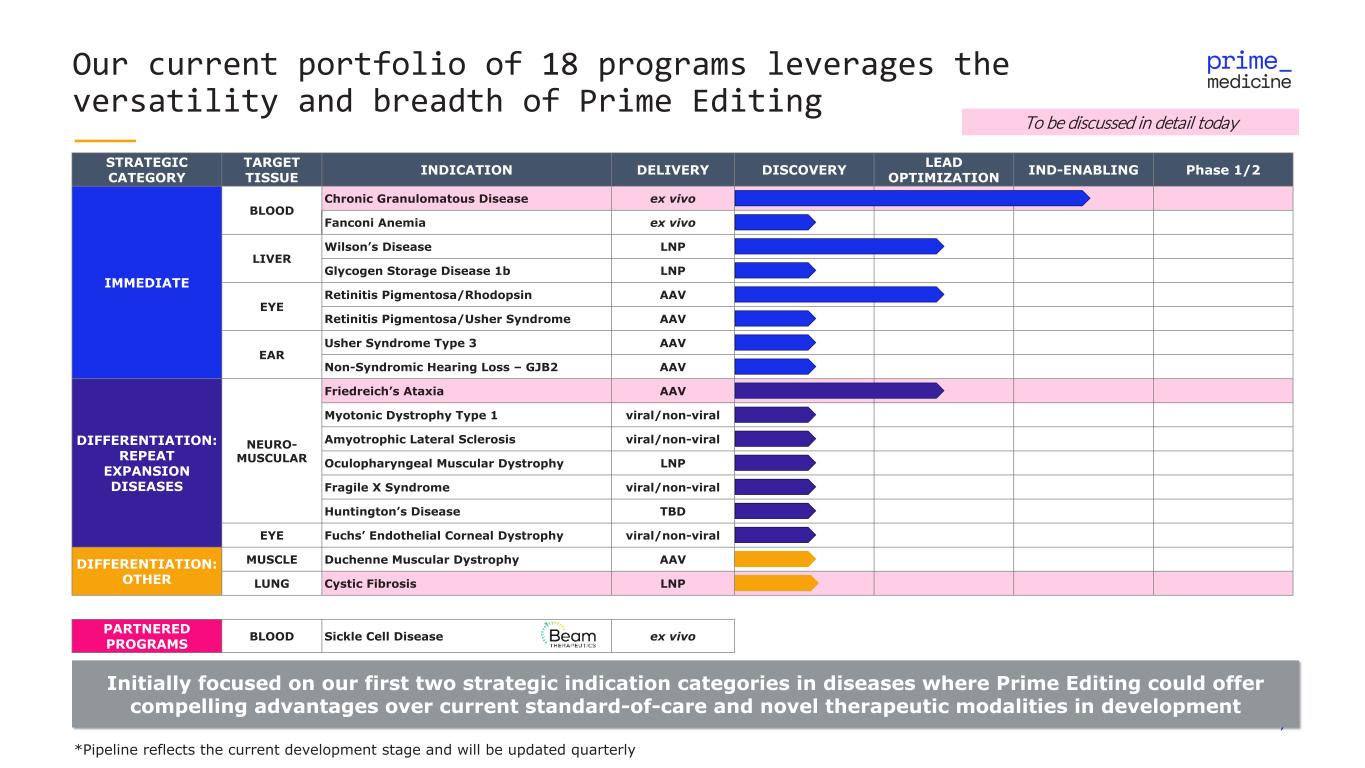
7 我們目前的18個項目組合利用了Prime Editing的多功能性和廣度,最初側重於我們的前兩個戰略適應症類別,在這些疾病中,Prime Editing可以比當前的護理標準和正在開發的新型治療模式具有引人注目的優勢。今天將詳細討論戰略類別靶組織適應症交付先導優化 IND-支持第一階段血液慢性肉芽腫病體外 Fanconi 貧血體外 LNP 肝臟威爾遜氏病 LNP 糖原儲存病1b LNP 眼部色素性視網膜炎/視紫素 AAV 色素性視網膜炎/厄舍爾綜合徵 AAV EAR Usher 綜合徵 3 型 AAV 非綜合徵性聽力損失 — GJB2 AAV 分化:重複擴張疾病 NEURO-MUSCIA Friedreich 的共濟失調 AAV 肌強直性營養不良症 1 型病毒/非病毒性肌萎縮性側索硬化症病毒/非病毒性眼咽硬化症肌萎縮性肌萎縮性肌萎縮性肌萎縮性肌萎縮性肌萎縮性肌萎縮性肌萎縮性肌萎縮性肌萎縮症 LNP Fragile X Syndrome 病毒/非病毒性亨廷頓舞蹈症待定 EYE Fuchs 內皮角膜營養不良病毒/非病毒分化:OTHER MUSCLE Duchenne 肌肉萎縮症 AAV 肺囊性纖維化 LNP合作項目 BLOOD Sickle Cell Disease 體外 *Pipeline 反映了當前的開發階段,將每季度更新一次
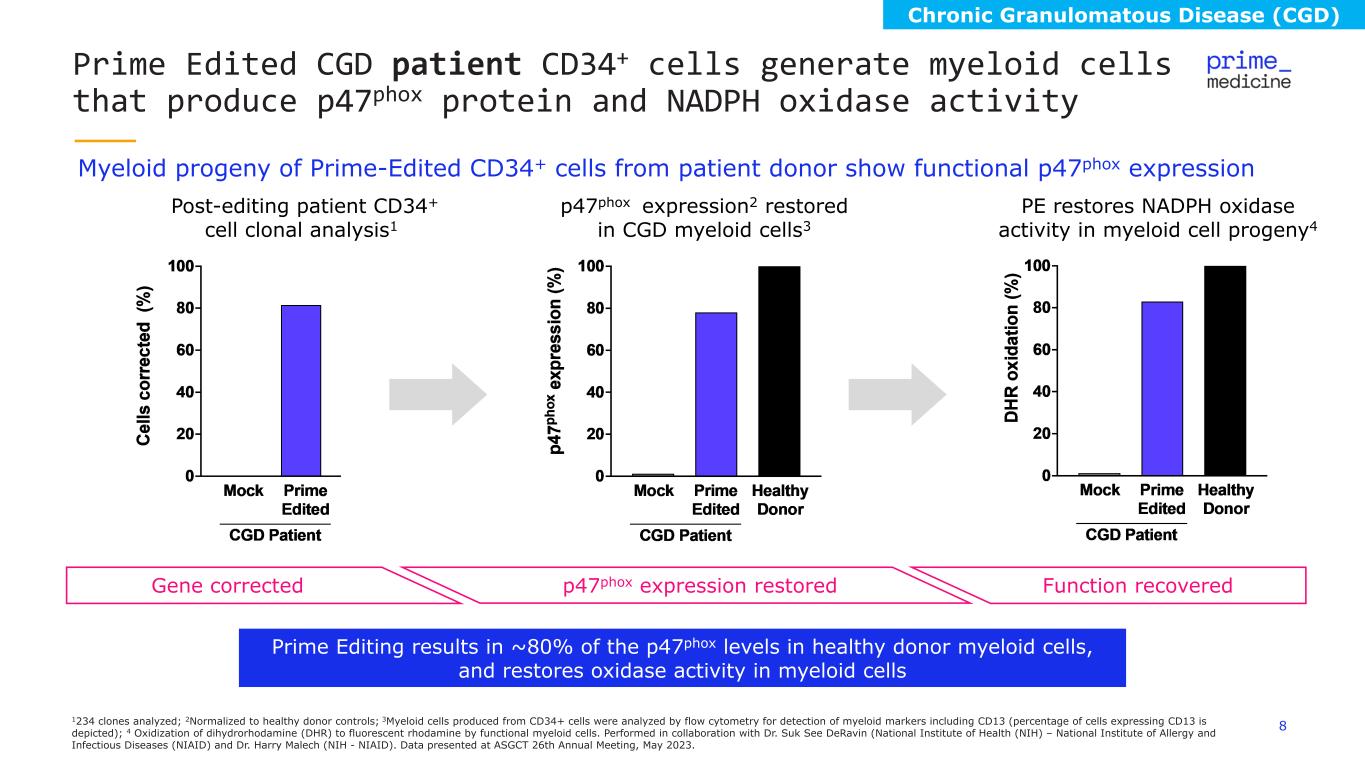
分析了81234個克隆;2歸一化為健康捐贈者對照組;通過流式細胞術分析了由CD34+細胞產生的3髓系細胞,以檢測包括CD13在內的髓系標誌物(描繪了表達CD13的細胞百分比);4 功能性髓系細胞將二氫羅達明(DHR)氧化為熒光羅丹明。與Suk See DeRavin博士(美國國立衞生研究院(NIH)——美國國家過敏和傳染病研究所(NIAID)和哈里·馬萊赫博士(NIH-NIAID)合作演出。數據在2023年5月舉行的ASGCT第26屆年會上公佈。Prime Edited CGD 患者 CD34+ 細胞會產生產生 p47phox 蛋白和 NADPH 氧化酶活性的髓系細胞來自患者捐贈者 Prime Edited CD34+ 細胞的髓系後代顯示功能性 p47phox 表達 Prime Edition 導致健康捐贈者髓系細胞中大約 80% 的 p47phox 水平,並恢復髓系細胞中的氧化酶活性 Function recoveredpho47 x 表達 restoredGene 校正的 PE 可恢復 CGD 髓系細胞後代 4 p47phox 表達2 中恢復的 NADPH 氧化酶活性 3 編輯後患者 CD34+ 細胞克隆分析1慢性肉芽腫病 (CGD)

9 在長期 HSC 種羣中植入 16 周後維持超過 92% 的長期造血幹細胞成功編輯:體內植入 Prime Edited CD34+ 細胞 NBSGW:nod.cg-kitw41J Tyr + prkdcscid il2rgtm1WJL/THOMJ 高度免疫缺陷小鼠,無需輻照即可支持人類 CD34+ 細胞植入。HSC:造血幹細胞。PE:Prime 已編輯。Naive CD34+Prime Editor cryopreserve/Thaw 0hr 24 小時編輯通過電穿孔進行高效率、非常精確的編輯高水平、長期植入導致健康 Prime 編輯的長期 HSC 恢復對抗感染的關鍵骨髓功能生成所有譜系小鼠在 16 周時身體健康,無毒性概述預期的臨牀研究設計 NBSGW miceEdited CD34+ 0 第 16 周長期移植的 CD34+ HSC 可以精確校正 NCF1 對於 PE 編輯的 HSC 的植入沒有區別與對照組患者受益的最低閾值 CGD-Ex-Vivo HSC

10 對來自單一捐贈者(捐贈者 2)的細胞的長期研究顯示,LT-HSC 校正率約為 90%(與上一張幻燈片中的捐贈者 1 結果類似)1 在長期 HSC 人羣中成功進行 Prime 編輯:Prime Edition 具有很高的可重複性 1長期植入在 CD34+ 細胞輸注後 16 周。2Data for for difor 1,3,4 非常相似 3Mock 和 PE 組的植入沒有顯著差異。通過雙向方差分析進行統計分析。數據在2023年5月舉行的ASGCT第26屆年會上公佈。CGD-Ex-Ex-Vivo HSC 體外 > 90% 的細胞校正(捐贈者 2-4)體內分析顯示:(僅限捐贈者 2)2 > 95% 的人體細胞植入3 > 90% 在 lt-HSCs 中觀察到的編輯效率、植入和保存長期造血幹細胞的效果相似
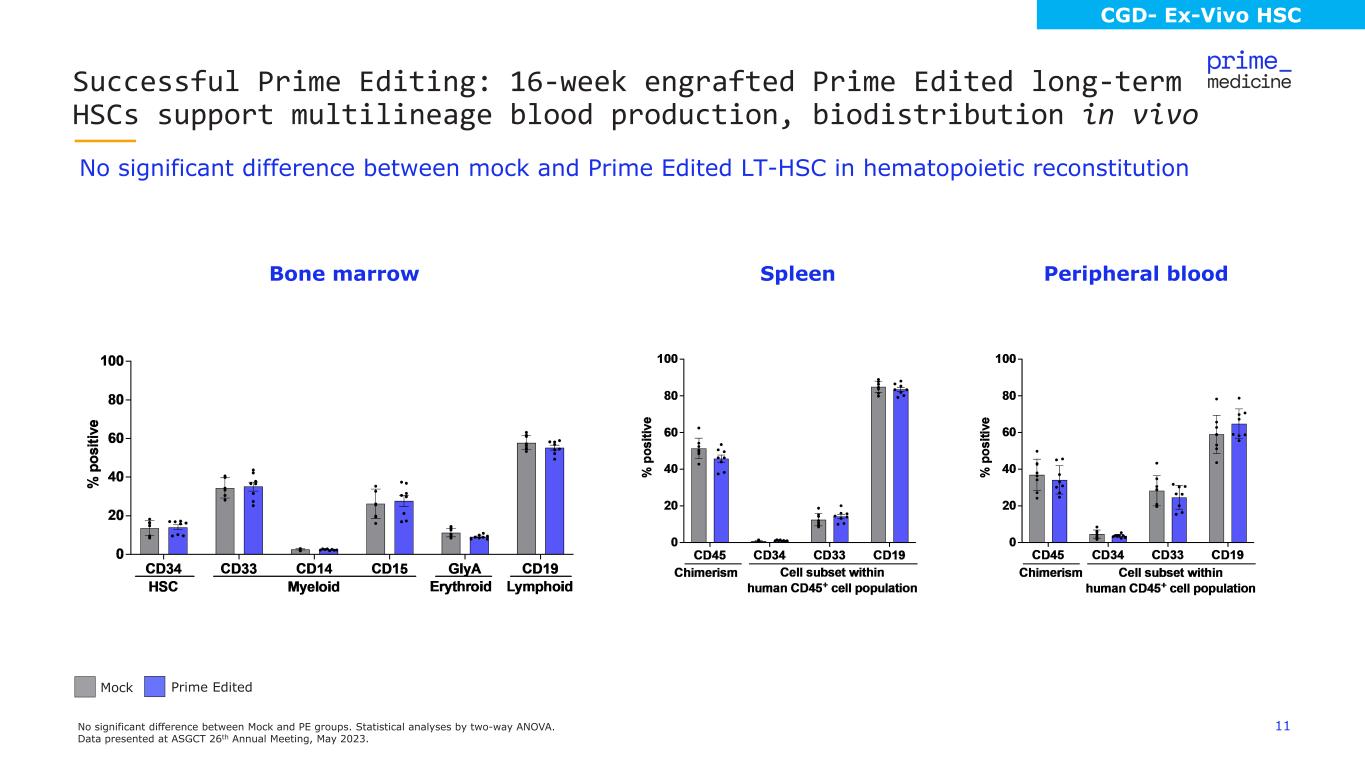
11 mock 和 Prime Edited LT-HSC 在造血重組方面沒有顯著差異成功的 Prime 編輯:16 周植入 Prime Edited 的長期 HSC 支持多譜系血液產生、體內生物分佈 Mock 和 PE 組之間沒有顯著差異。通過雙向方差分析進行統計分析。數據在2023年5月舉行的ASGCT第26屆年會上公佈。CGD-Ex-Vivo HSC Mock Prime 編輯脾臟外周血骨髓

12 高效的 Prime Editing 去除 Friedreich 共濟失調患者細胞中 Frataxin (FXN) 基因的 GAA 病理重複和超甲基化成功的 Prime Edition 去除致病重複:弗裏德賴希的共濟失調去甲基化恢復 FXN 啟動子的 mRNA 轉錄超甲基化阻止 FXN 啟動子的 mRNA 轉錄 Intron 1 X Prime 編輯啟動子 Intron 1 Prime Edited Exon 1 FRDA ipscs*% p re ci se c or re ct io n 高效、非常精確地編輯患者細胞,無需雙鏈斷裂恢復 FXN 基因 M 乙基化的正常甲基化 (%) 啟動子 Intron 1 Healthy Patient Patient Patient Patient Patient Patient patione Prime 編輯去除高甲基化1 重複擴張疾病許多重複擴張疾病表現出高甲基化是潛在發病機制的關鍵特徵 FXN:frataxin 基因:FRDA:Friedreich 共濟失調;iPSC:誘導的多能幹細胞。1 甲基化通過亞硫酸氫鹽測序量化
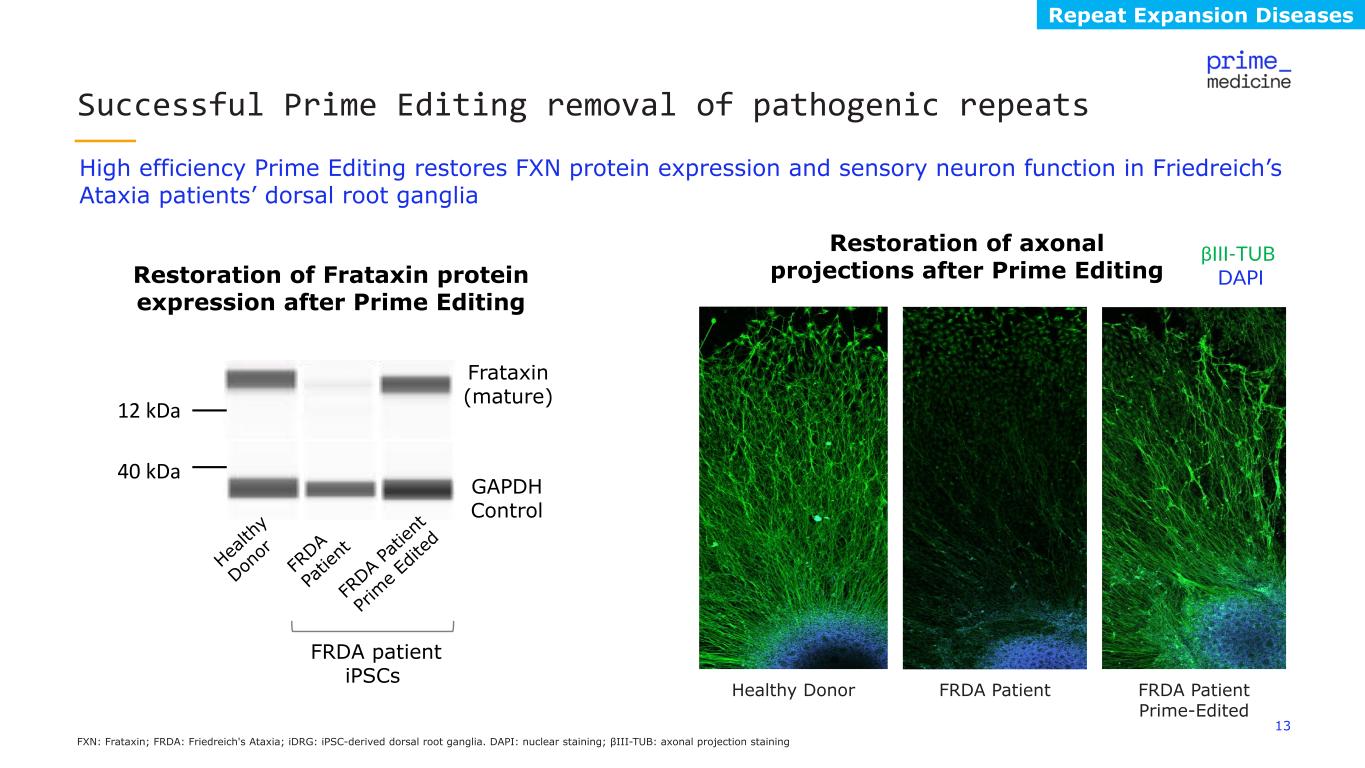
13 FXN:Frataxin;FRDA:Friedreich 的共濟失調;iDRG:源自 iPSC 的背根神經節。DAPI:核染色;βIII-TUB:軸突投影染色高效的 Prime Edition 恢復弗裏德賴希共濟失調患者背根神經節中的 FXN 蛋白表達和感覺神經元功能成功 Prime 編輯去除致病重複 FRDA 患者 prime 編輯 Frataxin(成熟)GAPDH 控制恢復後的軸突投影 Prime Edition 後的 Frataxin 蛋白表達 12 kDa 40 kDa 重複擴張疾病
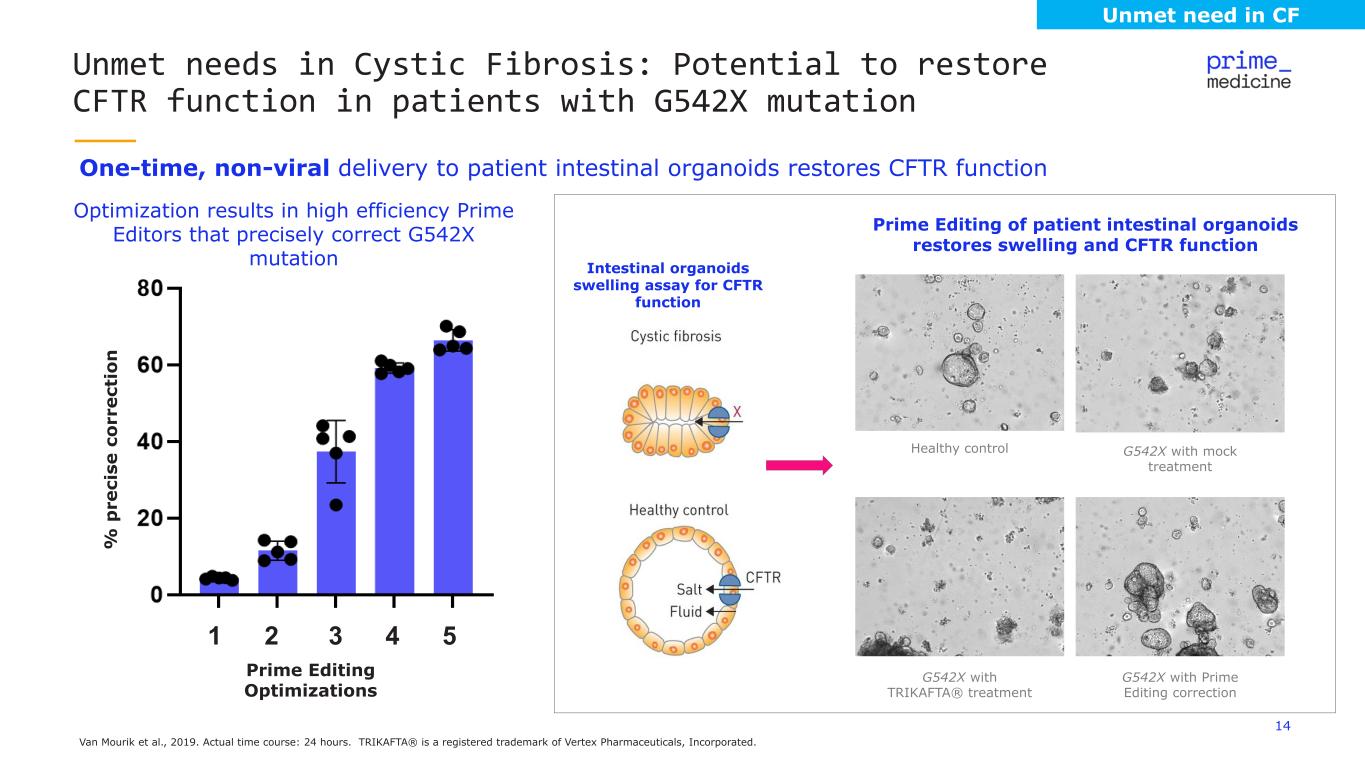
14 Van Mourik 等人,2019 年。實際時間課程:24 小時。TRIKAFTA® 是 Vertex 製藥公司的註冊商標。向患者一次性非病毒性腸道器官輸送可恢復 CFTR 功能囊性纖維化中未滿足的需求:G542X 突變患者可能恢復 CFTR 功能 1 2 3 4 5 患者腸道類器官的主要編輯可恢復腫脹和 CFTR 功能 CFTR 功能腸道類器官腫脹試驗 CFTR 功能使用模擬治療 G542X 帶有 Prime Edition 的健康控制使用 TRIKAFTA® 治療優化可實現高效的 Prime 編輯器精確糾正 G542X mutation Prime 編輯優化% p re ci se G542X G542Xc 或 rect io n CF 中未滿足的需求
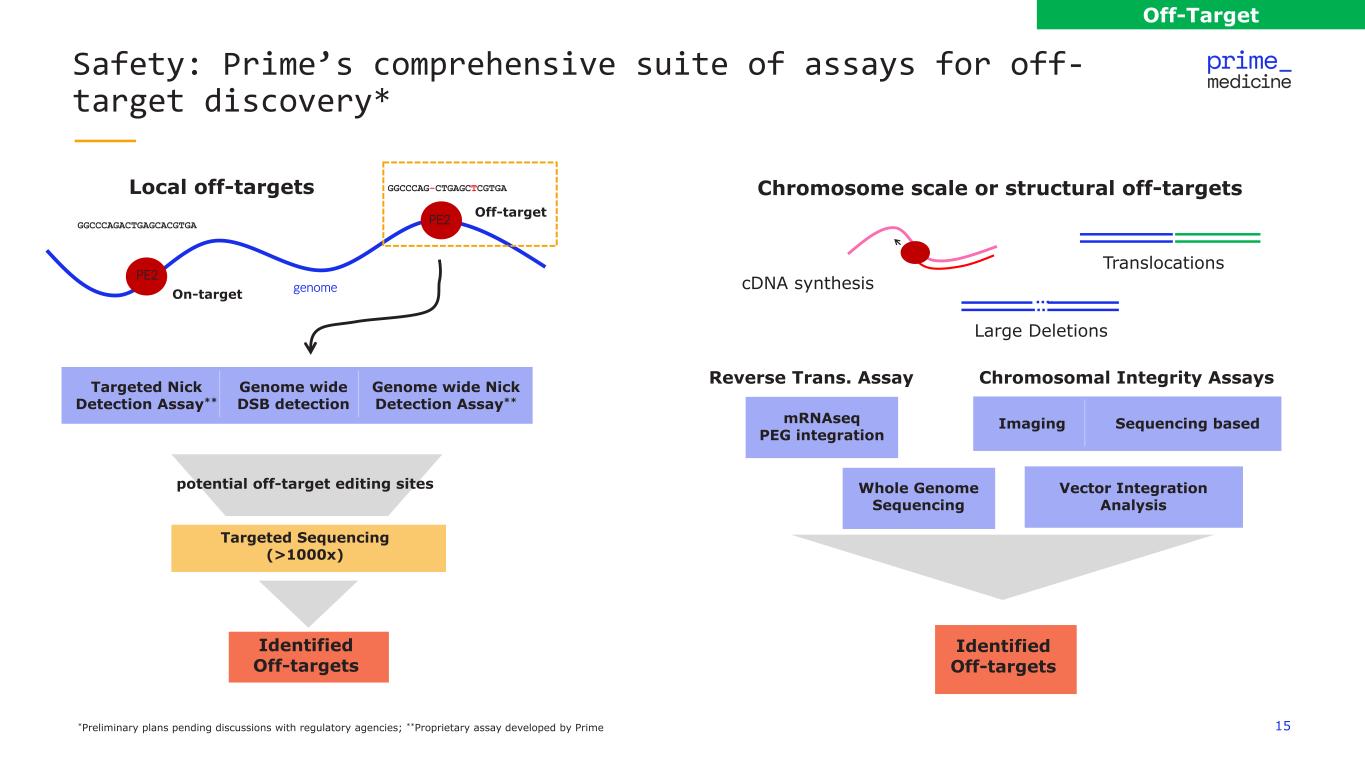
15 Safety:Prime 針對脱靶發現的全面檢測套件* 靶向偏離靶的 pe2 基因組 GGCCCAGACTGAGCGTGA GGCAGTGA GGCAGTGA 靶向測序 (>1000x) 已確定偏離目標的基因組全劃痕檢測測定** 局部脱靶染色體尺度或結構偏離靶位點 cdna 合成 mrnaSeq PEG 整合染色體完整性檢測識別偏離靶點成像測序的全基因組測序向量積分分析反向轉換Assay Off-Target *初步計劃有待與監管機構討論;**專有分析由 Prime 開發

16 安全:初步的偏離靶標的分析表明,最少或根本沒有偏離目標的編輯數據擴展了在多個主要編輯的細胞類型中未檢測到偏離靶標的編輯的演示。靶向測序全基因組和靶向檢測潛在的偏離靶標的潛在偏離靶點的閾值 0.5% 目標上 (ATP7B) CGD 計劃:CD34+ Cells1 威爾遜病計劃:Hepatocytes2 Off-Target 1分析來自編輯的 CD34+ 細胞 CGD 計劃:對 550 個潛在的偏離目標的地點進行有針對性的分析靶點編輯。2分析威爾遜氏病項目中經過編輯的iHEP(iPsG hepatocyte)細胞:靶向分析 170 個潛在的脱靶位點。SNP:單核苷酸多態性
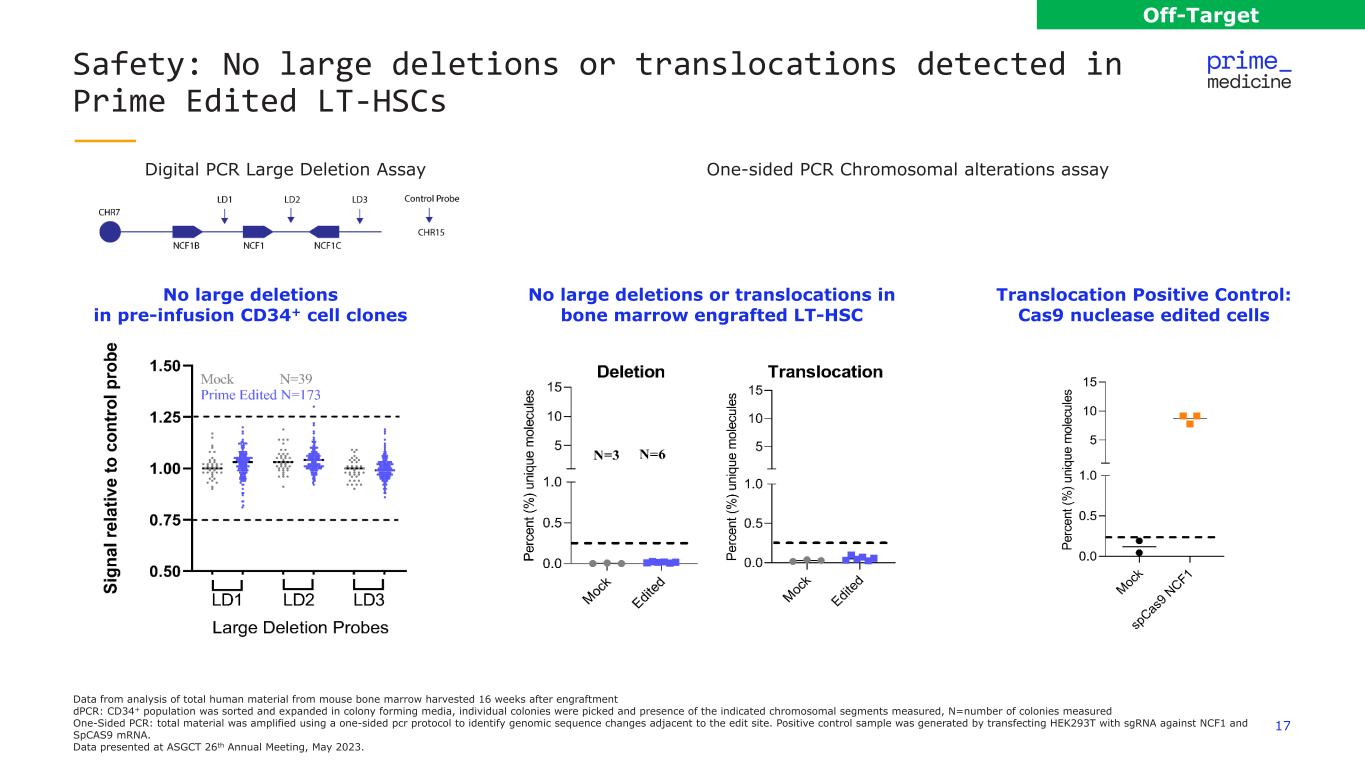
17 安全性:在 Prime Edited lt-hscs Off-Target 數據中未檢測到大量缺失或易位,這些數據來自植入 16 周後採集的小鼠骨髓中的總人類物質 dPCR:在菌落形成介質中對CD34+ 種羣進行了分類和擴展,採集了單個菌落並測量了指定染色體片段的存在,n=測量菌落數單面聚合酶鏈反應:使用單面聚合酶鏈反應協議對總材料進行擴增識別編輯站點附近的基因組序列變化。陽性對照樣本是用 sgRNA 對 NCF1 和 spcas9 mRNA 轉染 HEK293T 生成的。數據在2023年5月舉行的ASGCT第26屆年會上公佈。易位陽性對照:Cas9 核酸酶編輯的細胞移植骨髓中沒有大量缺失或易位 LT-HSC 輸液前 CD34+ 細胞克隆沒有大量缺失片面 PCR 染色體改變 assayDigital PCR 大缺失測定
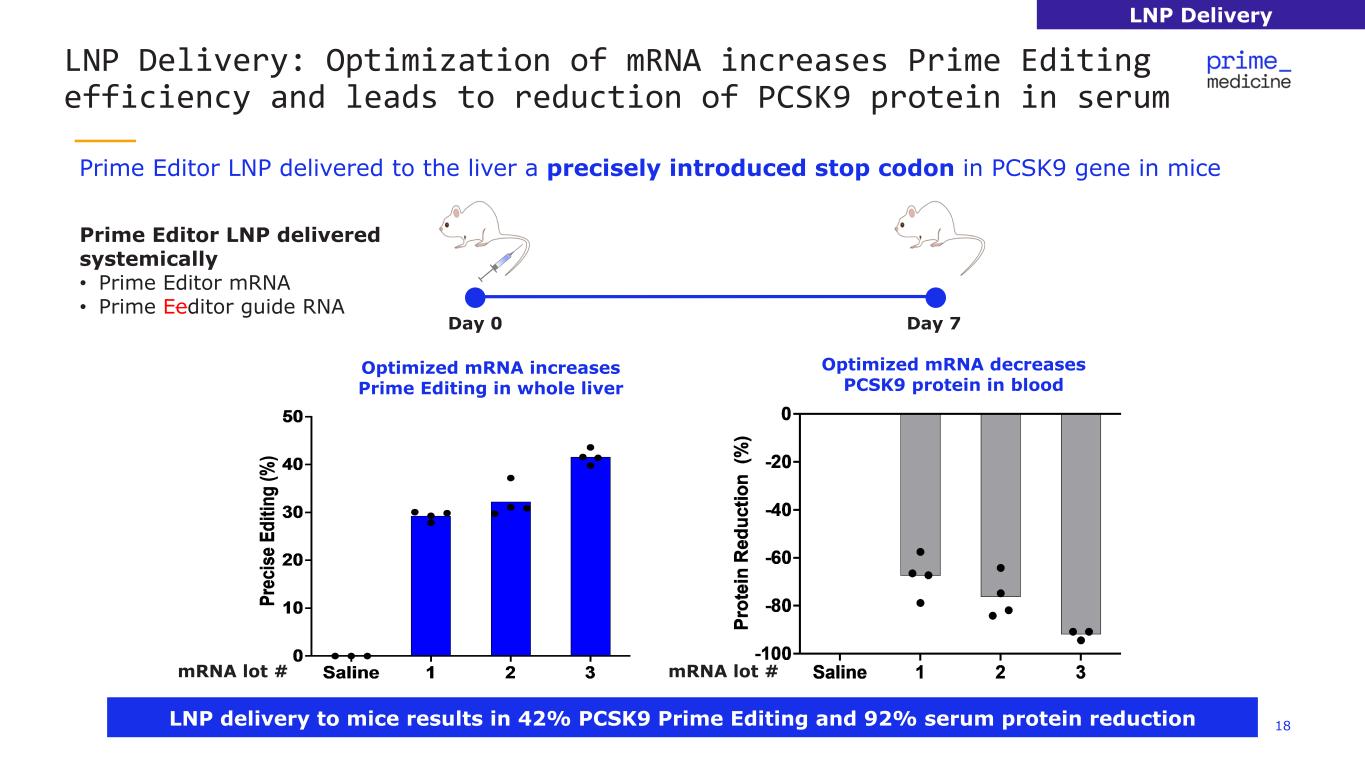
18 LNP 交付:優化 mRNA 可提高 Prime 編輯效率並減少系統交付的血清 Prime Editor LNP 中的 PCSK9 蛋白 • Prime Editor mRNA • Prime Editor 指南 RNA 優化的 mRNA 可增加全肝的 Prime 編輯第 0 天第 7 天優化 mRNA 批量減少 LNP Prime Editor 批次 # LNP Delivery 向肝臟輸送了小鼠 PCSK9 基因中精確引入的終止密碼子 PCSK9 PCSK9
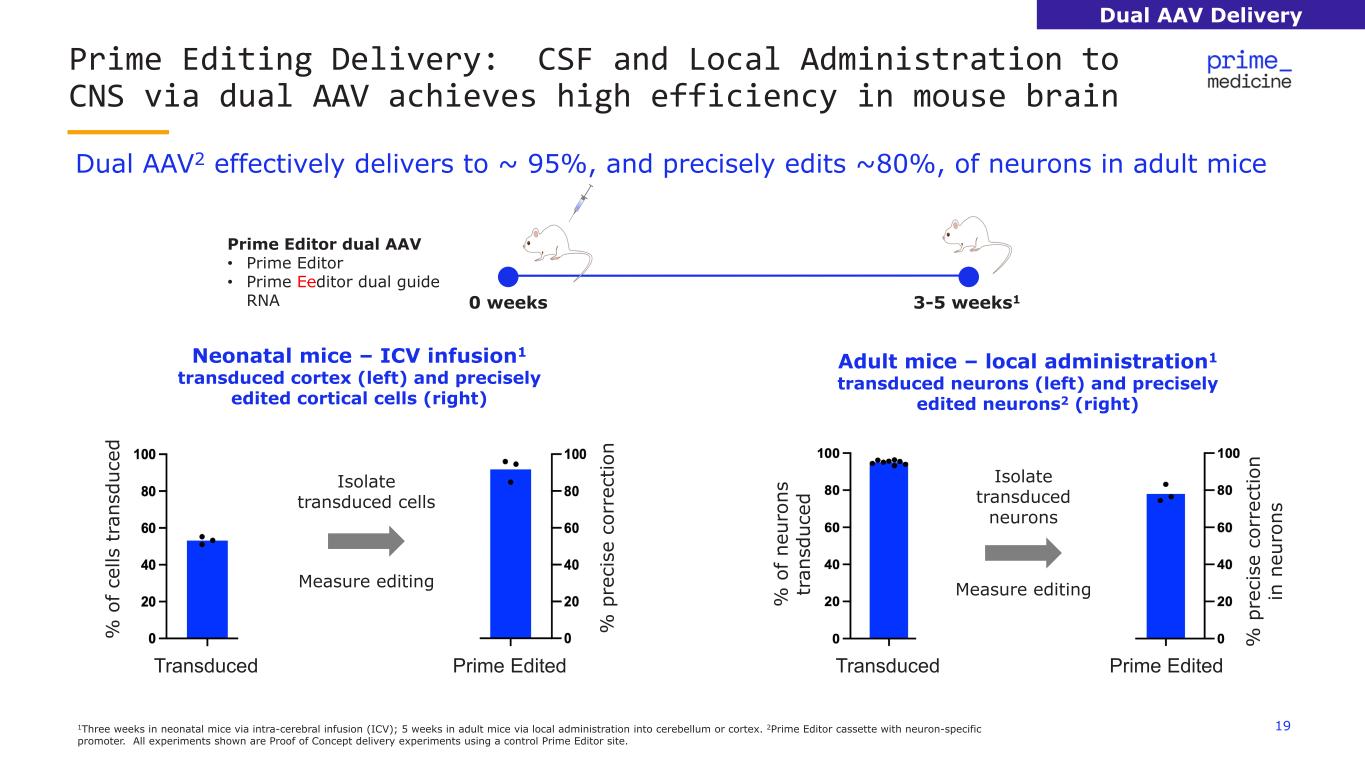
191通過腦內輸注(ICV)在新生小鼠身上注射三週;通過局部給藥進入小腦或皮層,在成年小鼠身上注射 5 周。2Prime Editor 盒式帶有神經元特異性啟動子。顯示的所有實驗都是使用控件 Prime Editor 網站進行的概念驗證交付實驗。Prime 編輯交付:通過雙 AAV 對中樞神經系統進行腦脊液和局部給藥可實現高效 Dual AAV2 可有效傳遞大約 95% 的成年小鼠神經元,並精確編輯大約 80% 的神經元 Prime Editor 雙 AAV • Prime Eeditor 雙指南 RNA 0 周 3-5 周1 新生兒小鼠 — ICV 輸液1 轉導皮層(左)和精確編輯的皮質細胞(右)成年小鼠 — 局部給藥 ation1 轉導了神經元(左)和精確編輯的 neurons2(右)% p re ci se c or re ct io n prime editedTendoned% o f ce ls t ra ns du ce d隔離轉導細胞測量編輯 tnorded% of ne ur on s tr and sd uc ed% p re ci se c or re ct io n n n eu ro ns Prime 編輯隔離轉導神經元測量編輯雙 AAV 交付
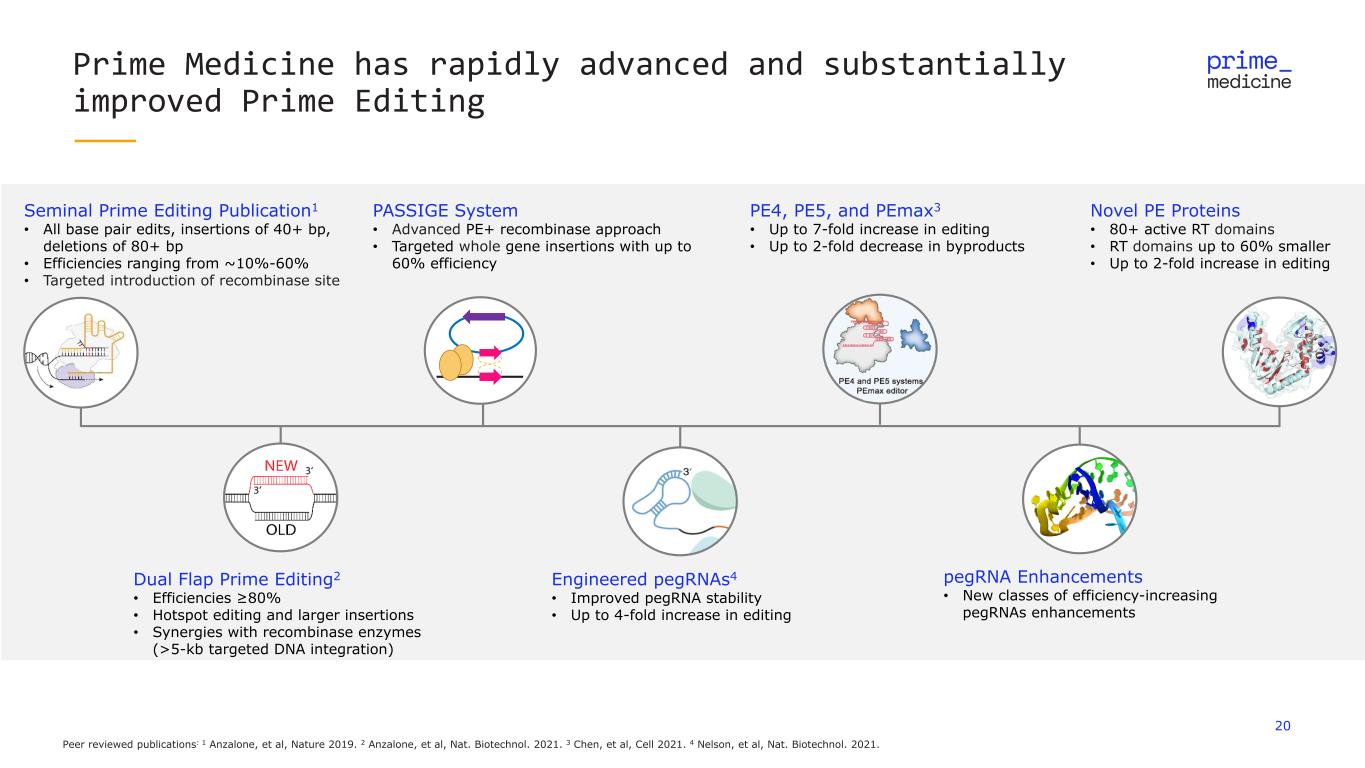
20 Prime Medicine 快速發展並大幅改善了 Prime 編輯工程 pegrnas4 • 提高了 pegRNA 穩定性 • 編輯新型 PE 蛋白的數量增加了多達 4 倍 • 80 多個活性 RT 結構域 • 編輯 pegRNA 增強功能增加了 2 倍 • 所有鹼基對編輯,插入 40 bp 以上,刪除 80 多個 bp • 效率介於大約 10%-60% 之間 • 有針對性地引入重組酶位點 Dual Flap Prime Editing2 •效率 ≥ 80% • 熱點編輯和更大的插入 • 與重組酶的協同作用(>5 kb 靶向 DNA 整合)PASSIGE System • 高級 PE+ 重組酶方法 • 效率高達 60% 的靶向全基因插入同行評審出版物:1 Anzalone 等人,Nat.Biotechnol。2021。3 Chen 等人,Cell 2021。4 Nelson 等人,Nat.Biotechnol。2021。PE4、PE5 和 peMax3 • 編輯量最多可增加 7 倍 • 副產品減少多達 2 倍

21 項專利組合包括:• 美國專利 11,447,770,涵蓋使用 Prime Editor 的方法 • 美國專利 11,643,652,涵蓋了 Prime 編輯指南 RNA (pegRNA) 的物質成分 • 美國允許申請 17/751,599,涵蓋包括 pegRNA、Prime Editor 蛋白和(可選)重組酶(預計於 2023 年第三季度發佈)的 Prime 編輯系統 Prime Medicine 已申請額外的技術知識產權保護 advancements Prime Medicine 擁有 Prime 編輯的基礎知識產權致力於為平臺技術確保最廣泛的知識產權保護,計劃和進步

22 PASSIGETM:應用 Prime Editing 將基因大小的序列精確插入基因組中 Prime Assisted 位點特異性整合酶基因組特異性重組 DNA 捐贈者重組酶基因組 DNA 在基因組 DNA 中的精確位置編程插入帶有重組酶靶序列的基因組 DNA(紫色)在精確位置整合 DNA 一步非病毒 kilobase size 基因編輯方法 — 無雙鏈中斷被動

23 Multiplex 編輯的 CAR-T CAR 模型:嵌合抗原受體;TRAC:T 細胞受體 alpha 常數;PASSIGE:Prime 輔助位點特異性整合酶基因編輯 PASSIGE 和異基因現成 CAR-T 細胞產品的多路複用 Prime 編輯方法支持 Prime Editing 開發同類最佳同種異體 CAR-T 細胞產品 X PASSIGE 在 T 細胞受體 (TRAC) 位點整合 CAR 的潛力細胞腫瘤特異性 T 細胞受體 KO 可阻止 gvHD 成分在不使用病毒的情況下一起交付的所有編輯使用 Prime Editing 對 KO B2M 進行多路複用,移除 MHC I 類逃避患者免疫系統允許在需要時重複給藥

24PASSIGE:Prime 輔助位點特異性整合酶基因編輯;n = 2 次技術重複;最右側面板:n = 4 個技術重複;測試後使用 Bonferroni 進行雙向方差分析 *** P = 0.0002;**** P

25數據在2023年5月舉行的ASGCT第26屆年會上公佈。PASSIGE:在 95% 的 Prime-Editid T 細胞中可以實現 B2M 的敲除,PRIME Editig 的 Prime Edition 可以減輕體內腫瘤負擔,在 T 細胞中高效且可以在多路複用 PASSIGE Prime 編輯技術中引入多種基因組修飾 β2 微球蛋白是通過在 PASSIGE show 生成的 b2M 基因中精確引入終止密碼子來擊倒減輕體內腫瘤負擔 NSG 小鼠移植腫瘤細胞用 Control 或 PASSIGE CAR-T 細胞測量小鼠生物發光造成的腫瘤負擔
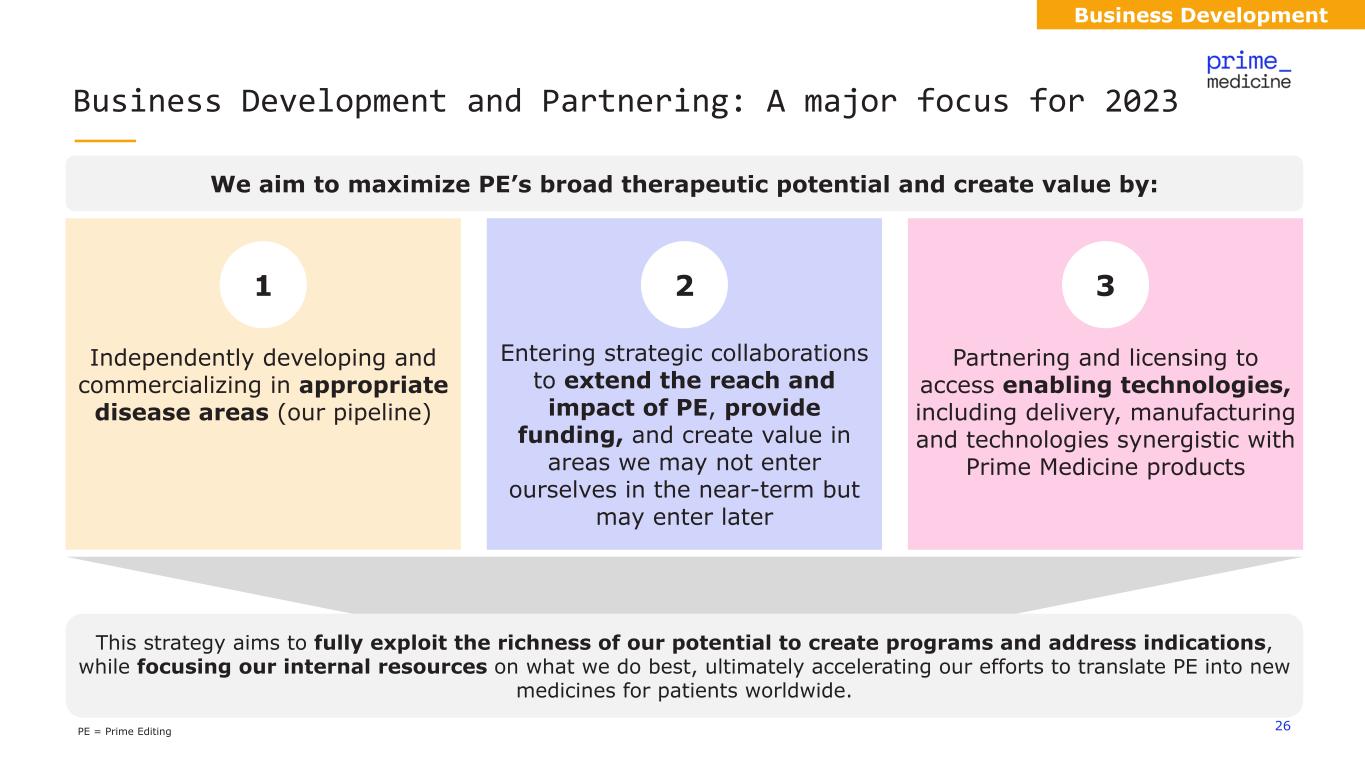
26PE = Prime Editing 業務發展與合作:2023 年的主要重點我們的目標是通過以下方式最大限度地發揮私募股權廣泛的治療潛力並創造價值:在適當的疾病領域獨立開發和商業化(我們的管道)進入戰略合作以擴大私募股權的影響力和影響力,提供資金,並在我們可能不會進入但稍後可能進入的領域合作和許可,以獲得支持技術,包括交付、製造和與 Prime 協同的技術醫學products 1 2 3 該戰略旨在充分利用我們創建項目和應對適應症的豐富潛力,同時將我們的內部資源集中在我們最擅長的事情上,最終加快我們將PE轉化為全球患者的新藥的努力。業務發展

27 HSC = 造血幹細胞;AML/MDS = 急性髓系白血病/骨髓增生異常綜合徵;SCIP = 屏蔽細胞和免疫療法配對 Prime Medicine 和 Cimeio:研究合作實現一流的 HSC 藥物目標:降低調理方案的毒性,引入新的治療選擇以擴大 HSC 移植和體內基因療法的效用 HSCT 市場規模龐大且不斷增長,但調理毒性是主要瓶頸 • HSC 移植可以治癒許多疾病,但效用因需求而受到限制骨髓消融調理方案 • 毒性較小的方案可以將潛在市場擴大到當前規模的倍數將 Prime Edition 與 Cimeio 的 SCIP 平臺相結合,可以:• 提高 HSC 移植的安全性和有效性,顯著提高可及性、資格和結果 • 允許選擇體內編輯的 HSC,無需移植即可治療遺傳性疾病戰略理由為 Cimeio 的 CD117 屏蔽變異體開發 Prime Editor • CD117 是一種細胞表面受體在生存、擴散中起着至關重要的作用以及 HSC 的分化;阻斷或消融導致 HSC 死亡的 CD117 信號傳導可編輯 CD117 表位以減少抗體結合,同時保持受體功能。這可以清除野生型 CD117 表達細胞,同時使用經過編輯的表位保護細胞 • Prime Edition 似乎是編輯 Cimeio 抗 CD117 結合表位的有效方法合作詳情如果成功,各公司將互相授予獨家許可選項:• Prime 將獲得許可 SCIP 技術的獨家選擇權,用於遺傳性疾病 CD117 屏蔽 HSC 移植 • Cimeio 將獲得 CD117 屏蔽的同種異體 HSC 的 Prime Editing 許可的獨家選擇權用於 AML/MDS 的產品,以及可能用於反洗錢/MDS 的第二種屏蔽蛋白 • 如果行使期權,兩家公司都有資格從許可產品的淨銷售額中獲得經濟效益
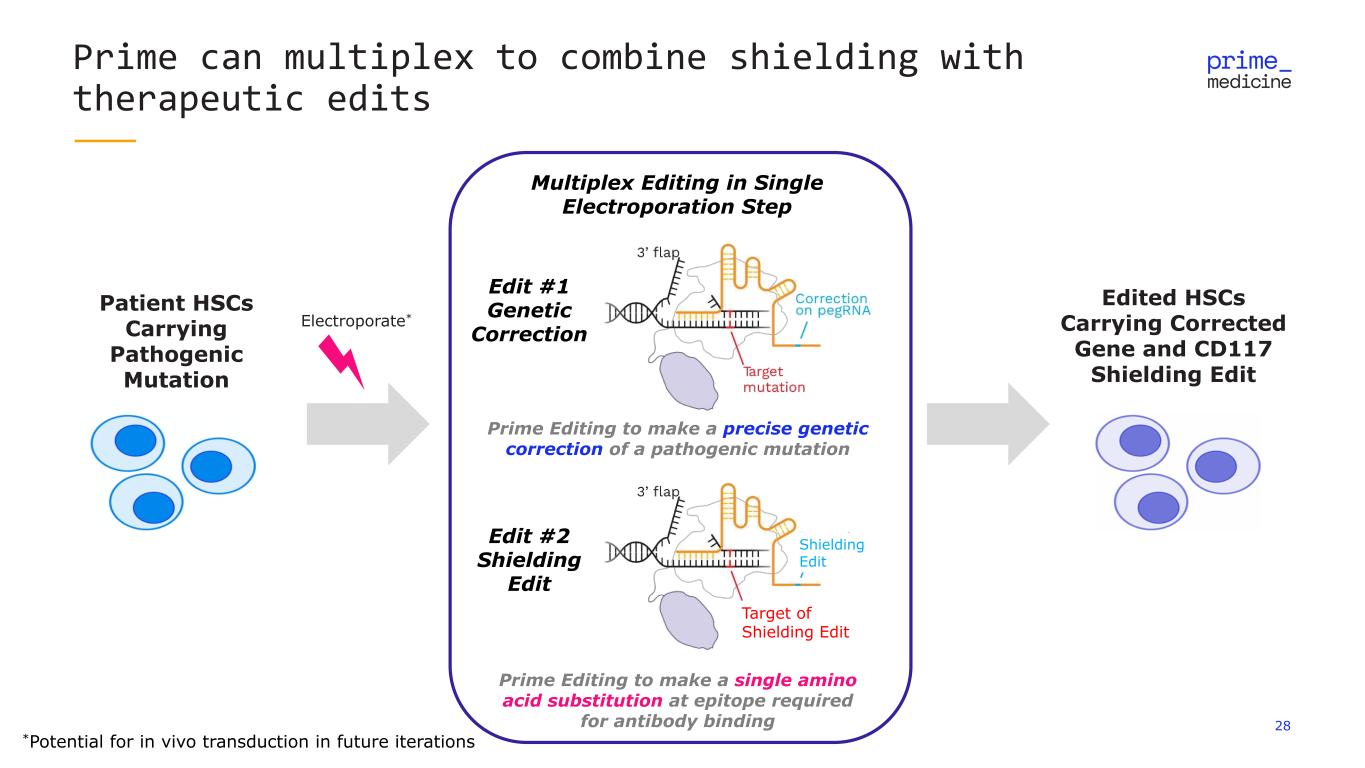
28 Prime 可以多路複用,將屏蔽與治療編輯相結合,攜帶致病突變的患者 HSC 編輯攜帶校正基因和 CD117 屏蔽編輯 Prime 編輯在抗體結合所需的表位進行單一氨基酸替代屏蔽編輯屏蔽編輯對致病突變進行精確的遺傳校正編輯 #1 基因校正編輯 #2 屏蔽編輯單一電穿孔步驟電穿孔中的多路複用編輯*活體轉導的潛力未來的迭代

29 目前 • 約有 200 名員工;研究與技術開發部門約有 85% • 組織所有部門的主要領導層和員工到位 • 在公司範圍內建立了核心能力,從知識產權戰略到自動化,從人工智能到 RNA 技術 • 建立了牢固的外部關係 • 位於馬薩諸塞州劍橋的 3 個分支機構,在劍橋增建一座化學工廠,目標於 2024 年 10 月成功上市 • 於 2022 年 10 月成功首次公開募股,迄今已籌集超過5億美元建立公司 2019 年 9 月 1.15 億美元 A 輪 2019 年 10 月 Prime 編輯開創性的 Nature1 論文 2020 年 7 月開始公司運營 2021 年 4 月 2 億美元 B 輪 4 45 2020 年 7 月 2021 年 7 月 2022 年 7 月 2022 年 7 月 2022 年 7 月實現人才成功增長關鍵里程碑 184+ 2022 年 10 月首次公開募股約 2 億美元

30 Prime Medicine 精選正在進行的活動和後續措施摘要即將舉行的活動將繼續推動 Prime Medicine 平臺在 2023 年第一季度向前推進 Prime Medicine 平臺被提名為慢性肉芽腫病 (CGD) 的首個開發候選藥物。• 在 2023 年下半年在 CGD 中啟動臨牀前概念驗證,包括在多個項目中共享體內齧齒動物研究和大型動物研究的數據。• 在其他肝臟、眼部和神經肌肉項目中共享體外臨牀前數據。• 預計最早將在2024年提交首次IND申請,預計將在2025年提交更多IND申請。平臺 • 繼續開發和優化非病毒和病毒傳送系統,並在 2023 年下半年分享來自體內齧齒動物和大型動物研究的更多概念驗證數據。• 進一步證明 Prime 編輯計劃的卓越的 “偏離目標” 特徵。• 使用專有的重組酶和/或逆轉座子技術為新項目和現有項目擴展 Prime Editing。強勁的現金狀況:截至2023年3月31日的現金、現金等價物和投資足以為2025年之前的預期運營費用和資本支出需求提供資金。

31 備份
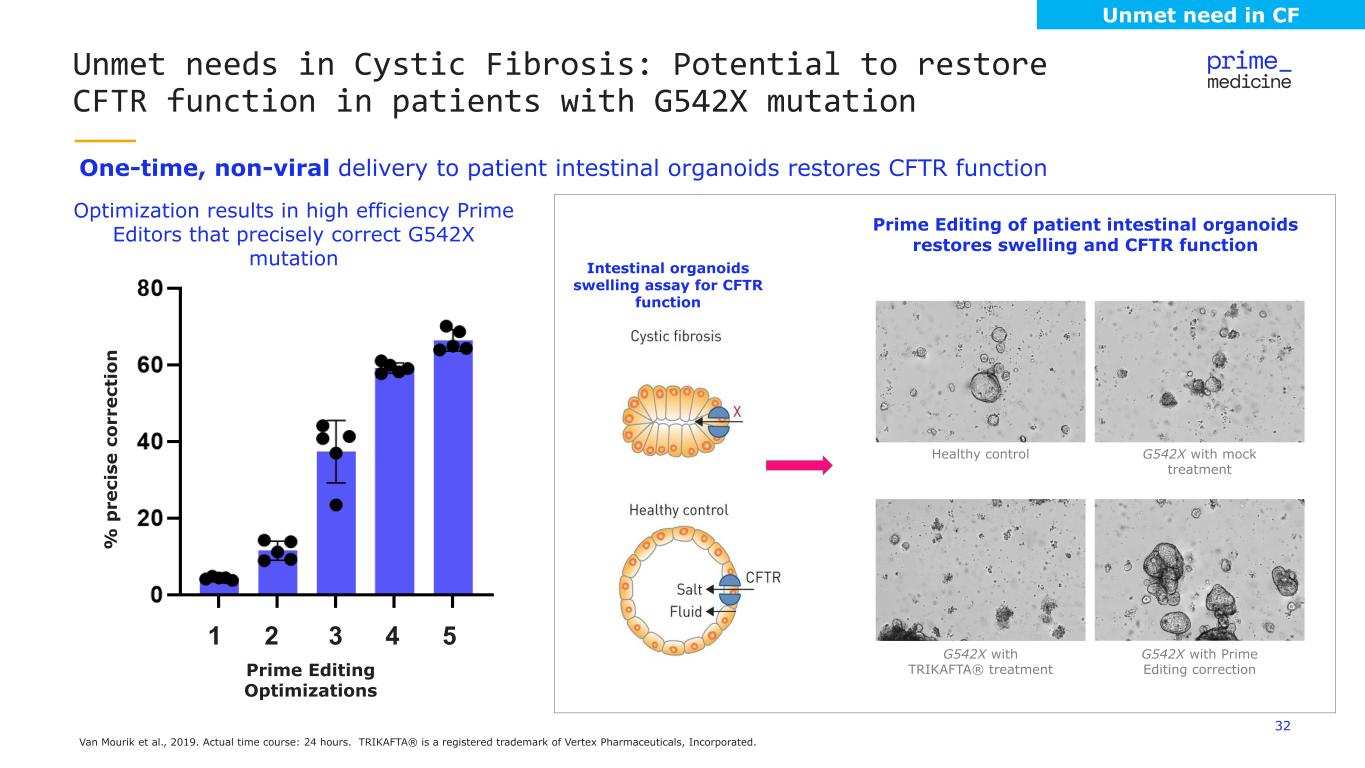
32 Van Mourik 等人,2019 年。實際時間課程:24 小時。TRIKAFTA® 是 Vertex 製藥公司的註冊商標。向患者一次性非病毒性腸道器官輸送可恢復 CFTR 功能囊性纖維化中未滿足的需求:G542X 突變患者可能恢復 CFTR 功能 1 2 3 4 5 患者腸道類器官的主要編輯可恢復腫脹和 CFTR 功能 CFTR 功能腸道類器官腫脹試驗 CFTR 功能使用模擬治療 G542X 帶有 Prime Edition 的健康控制使用 TRIKAFTA® 治療優化可實現高效的 Prime 編輯器精確糾正 G542X mutation Prime 編輯優化% p re ci se G542X G542Xc 或 rect io n CF 中未滿足的需求
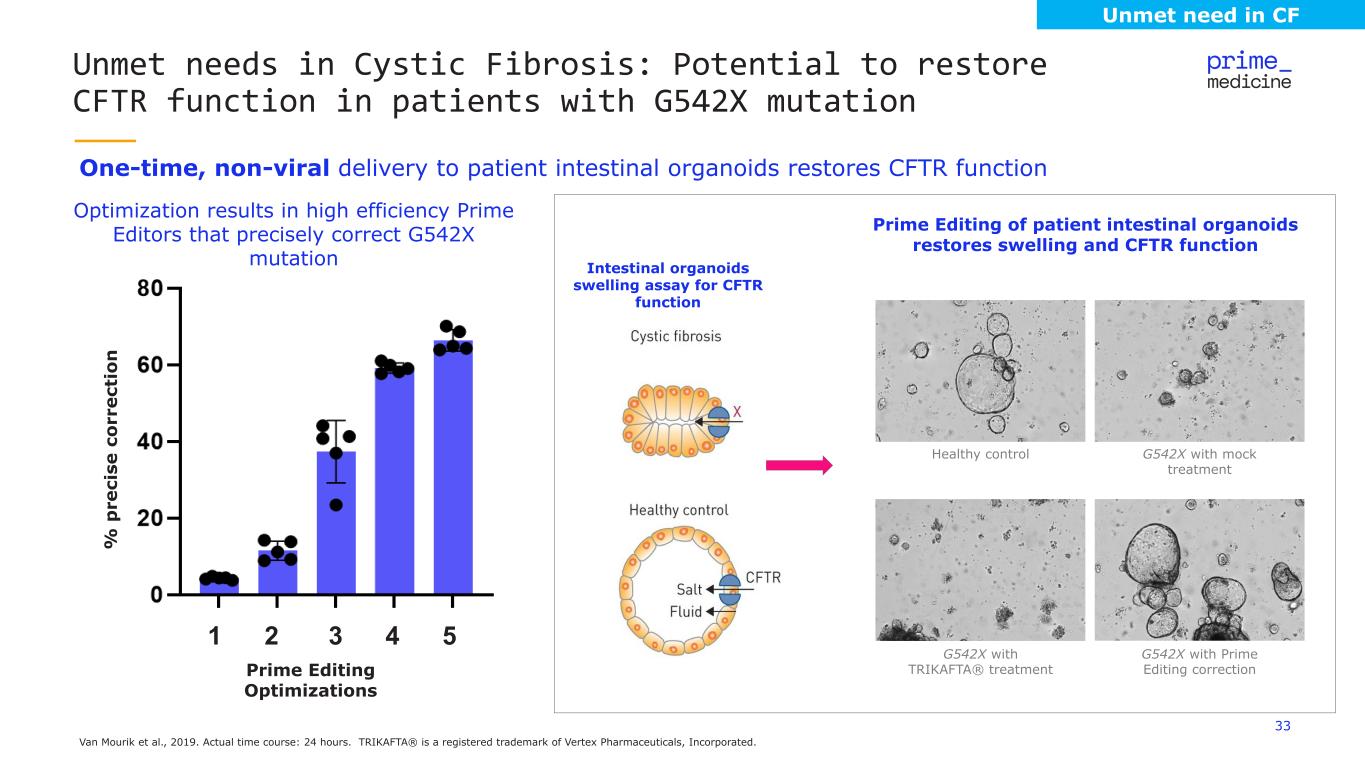
33 Van Mourik 等人,2019 年。實際時間課程:24 小時。TRIKAFTA® 是 Vertex 製藥公司的註冊商標。向患者一次性非病毒性腸道器官輸送可恢復 CFTR 功能囊性纖維化中未滿足的需求:G542X 突變患者可能恢復 CFTR 功能 1 2 3 4 5 患者腸道類器官的主要編輯可恢復腫脹和 CFTR 功能 CFTR 功能腸道類器官腫脹試驗 CFTR 功能使用模擬治療 G542X 帶有 Prime Edition 的健康控制使用 TRIKAFTA® 治療優化可實現高效的 Prime 編輯器精確糾正 G542X mutation Prime 編輯優化% p re ci se G542X G542Xc 或 rect io n CF 中未滿足的需求