
附錄 99.2

UniQure 宣佈 美國 AMT-130 I/II 期臨牀試驗的最新情況
用於治療亨廷頓舞蹈病的基因療法
~ AMT-130 繼續 在兩個劑量組中總體上耐受性良好 ~
~ 與基線相比,接受 AMT-130 治療的患者顯示出功能保持不變,相對於疾病自然史的臨牀益處 ~
~ 在接受低劑量 AMT-130 治療的患者中,腦脊液 (CSF) 中的 Neurofilament Light chain (nFl) 在 24 個月時低於基線;在接受高劑量 AMT-130 治療的患者中,在 12 個月時降至基線
~ 在低劑量隊列中抑制 CSF mhTT 支持 AMT-130 靶點參與;在高劑量隊列中觀察到的變異性更大 ~
~ 前景光明的數據 支持 AMT-130 的持續臨牀開發和尋求監管互動以討論後期開發 ~
~ 投資者會議 電話會議和網絡直播將於美國東部時間今天上午 8:30 舉行 ~
馬薩諸塞州列剋星敦 和荷蘭阿姆斯特丹,2023 年 6 月 21 日 — 為有嚴重醫療需求的患者推進 變革療法的領先基因療法公司 Uniqure N.V.(納斯達克股票代碼:QURE)今天公佈了來自正在進行的 AMT-130 治療亨廷頓 病的 26 名患者的令人鼓舞的中期數據,包括長達 24 個月的 隨訪。
Uniqure研發總裁Ricardo Dolmetsch博士表示:“我們對我們對 AMT-130 的美國 I/II 期臨牀試驗的中期分析數據非常滿意。” Uniqure研發總裁裏卡多·多爾梅奇博士説。 “AMT-130 的耐受性總體上仍然良好,兩種劑量的安全性均可控制。重要的是,這兩劑都顯示出 臨牀和功能益處的初步證據,包括總運動評分、總功能容量 和綜合統一亨廷頓氏病評級量表與自然史相比呈現出良好的趨勢。隨着我們從這些患者和歐洲研究中收集更多數據,我們計劃與監管機構合作,推進 這項前景光明的臨牀計劃。”
醫學博士、FRCP、博士、臨牀神經病學教授、倫敦大學學院 (UCL) 亨廷頓病中心主任 Sarah Tabrizi 表示:“今天令人鼓舞的中期更新顯示 AMT-130 具有潛在臨牀益處的早期跡象以及神經絲光 鏈的支持趨勢,這是神經元損傷的關鍵標誌,已被證明可用於多種神經退行性疾病 同時也是倫敦大學學院神經退行性疾病系的聯合主董事“儘管患者人數很少,但我感到鼓舞的是 看到,接受任一劑量 AMT-130 治療的患者似乎在很大程度上保持了功能,並且在長達 24 個月後傾向於自然的 病程。這些中期結果為患有這種毀滅性疾病的患者帶來了早期希望, 我期待更多的臨牀更新以及對 AMT-130 作為 亨廷頓病患者的潛在重要治療選擇的進一步研究。”
數據摘要 來自美國 AMT-130 亨廷頓舞蹈病 I/II 期試驗
共有 26 名 患有早期表現的亨廷頓病患者 已入組 AMT-130 的美國多中心 I/II 期臨牀試驗, 包括一個 10 名患者的低劑量隊列(6 名已接受治療,4 名對照組)和一個 16 名患者的高劑量隊列(10 名已接受治療,6 名對照組)。 患者被隨機分配接受治療,接受 AMT-130 或模仿(虛假)手術。該研究包括為期12個月的失明核心研究期,然後是 對接受治療的患者進行為期五年的非盲長期隨訪。迄今為止,高劑量隊列 中的六名對照患者中有四名已交叉接受治療。來自交叉患者的療效和生物標誌物數據未包含在下面的摘要中。
安全性和耐受性
AMT-130 通常耐受性良好,在接受較低劑量 6x10 治療的患者中,其安全性可控12載體基因組和 6x10 的 更高劑量13載體基因組。治療組中最常見的不良事件與外科 手術有關。沒有治療緊急不良事件 (TEAE) 導致患者隨訪停止。
正如先前報道的那樣,低劑量隊列中有兩起與 AMT-130(術後妄想和重度抑鬱症)無關的 嚴重不良事件 (SAE), 高劑量隊列中有一起 SAE(背部疼痛),對照組中有一起 SAE(深靜脈血栓形成)。此外,在高劑量隊列中出現了兩起疑似意外的 嚴重不良事件(劇烈頭痛、中樞神經系統炎症)。所有事件都已解決。
所有四名交叉 患者(3 名高劑量,1 名低劑量)在服用 AMT-130 的同時接受了短期免疫抑制治療。 在對中期數據分析進行審查後,美國 I/II 期臨牀試驗的數據安全監測委員會 (DSMB) 得出結論 兩種劑量均不存在安全問題,建議繼續進行 AMT-130 的臨牀開發。
探索性 功效數據
將每個劑量隊列中接受治療的患者的臨牀和功能 測量值與基線測量值、對照患者(長達 12 個月)和 自然史隊列進行了比較。自然史隊列由UniQure與治癒亨廷頓舞蹈病倡議(CHDI)合作開發,使用對早期亨廷頓舞蹈病患者的TRACK-HD自然史研究。該隊列包括31名符合UniQure臨牀試驗納入標準的患者,包括CAG長度、年齡、總功能容量、診斷分類 水平和最小紋狀體體積。
| ● | 早期 臨牀數據表明,趨勢與 AMT-130 在兩種劑量 AMT-130 下的潛在臨牀益處一致。 |
| ● | 將 與基線測量值相比,低劑量隊列中患者 的臨牀功能通常保持在 24 個月,高劑量隊列中的患者的臨牀功能通常保持在 12 個月。 |
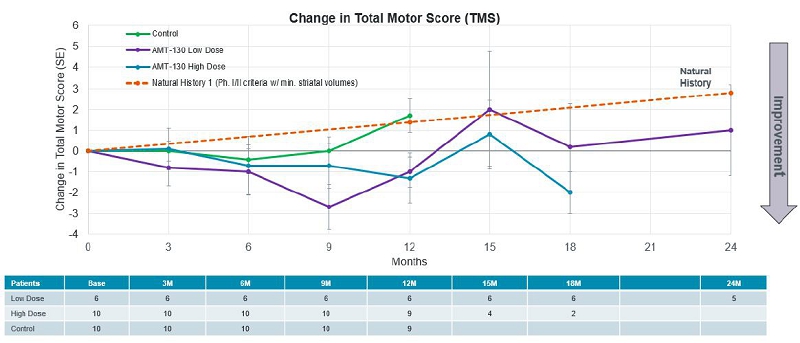
| ● | 將 與自然史相比,兩個劑量組的患者在總 運動分數、總功能容量和綜合統一亨廷頓氏病 評級量表中均顯示出益處。 |
| o | 總運動得分 (TMS):與自然史相比,低劑量患者在24個月時TMS平均改善了1.8分 ,高劑量患者在12個月時平均改善了2.7個百分點 。 |
| o | 總功能容量 (TFC):與自然史相比,低劑量患者在24個月時TFC平均改善了0.8個百分點 ,高劑量患者在12個月時平均改善了0.5個百分點 。 |
| o | 複合 統一亨廷頓舞蹈病評級量表 (cuHDR):與自然史相比,低劑量患者在24個月時顯示出 cuHDR平均改善了0.9個百分點,高劑量 患者在12個月時平均改善了1.0個百分點。 |
| ● | 與 基線和自然史相比,對照組中的患者 在 12 個月時出現總運動評分惡化。對照組患者在 12 個月時保留了 TFC 和 cuHDR。 |
| 生物標誌物 |
神經絲輕鏈 (nFl)
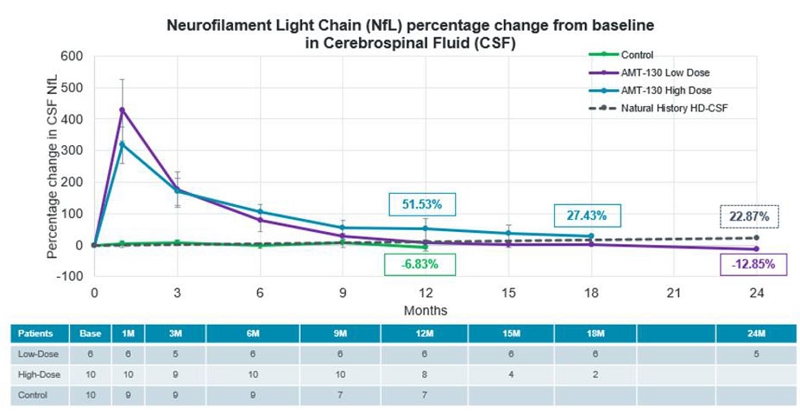
| ● | 正如 所預期和先前報道的那樣,接受 AMT-130 治療的患者經歷了與手術相關的腦脊液短暫增加 ,在 給藥後大約一個月達到峯值。這些短暫性增加不是劑量依賴性的,所有患者的腦脊液nFl隨後都出現了 下降。 |
| ● | 低劑量隊列的平均CSF nFl比基線低12.9%,而自然史上預計將增加22.9% ,五名低劑量患者中有四名CSF nFl水平低於 基線。 |
| ● | 在12個月內,高劑量隊列中的CSF nFl水平變化更大,與基線相比,平均增加了 51.5%。在八名接受了至少 12 個月 隨訪的高劑量患者中,有四名的 nFl 水平低於基線。兩名接受了18個月隨訪的大劑量患者 顯示CSF nFl持續下降至比基線高出27.4%。 |
| ● | 在 對照組中,平均腦脊液nFl相對穩定,在12個月時比基線低6.83%。 |
突變亨廷頓 蛋白 (mhTT)
| ● | 低劑量隊列的CSF mhTT 仍低於基線,24 個月時平均降低 8.1%。高劑量隊列的CSF mhTT變異要大得多,在12個月時平均比基線增加 為39.7%,而對照組的平均增幅為4.7%。在高劑量隊列的九名可評估患者中,有三名 在上次測量時腦脊液mhTT降至基線以下 。 |
大腦總容量
| ● | 對照組、低劑量組和高劑量組的 平均大腦總容量在12個月時分別下降了 0.74%、1.02% 和 1.23%,彼此之間沒有顯著差異 ,也與自然歷史沒有顯著差異。 |
後續步驟
基於本次中期分析中令人鼓舞的 數據,UniQure 將推進 AMT-130 的臨牀開發,並預計接下來將採取以下步驟:
| ● | 在2023年第三季度初 ,UniQure預計將完成歐洲臨牀試驗的高劑量 隊列的患者入組。 |
| ● | 在2023年下半年 ,UniQure預計將在正在進行的美國 臨牀試驗中啟動第三個隊列,以進一步研究這兩種劑量與圍手術期免疫抑制 聯合使用,重點是評估短期安全性。第三組將招收多達 10 名患者, 他們都將使用目前既定的立體定向神經外科 分娩程序接種 AMT-130。 |
| ● | 在 2023年第四季度,UniQure預計將公佈來自 AMT-130 I/II 期 研究的新臨牀數據,包括 美國試驗中接受治療的患者的更多隨訪數據以及來自歐盟試驗中低劑量患者 12 個月的隨訪數據。 |
| ● | 到2024年第一季度 ,UniQure預計將舉行監管交流會,討論來自美國和歐盟研究的 數據以及進一步推進 AMT-130 臨牀開發 的途徑。 |
投資者會議 電話會議和網絡直播信息
UniQure管理層 將於今天,即2023年6月21日星期三在以下地點舉辦投資者電話會議和網絡直播
美國東部時間上午 8:30 該活動將在UniQure網站的 “活動與演示” 部分進行網絡直播,活動結束後的重播將存檔 90 天。https://www.uniqure.com/investors-media/events-presentations通過電話參與的感興趣的人士需要使用 此在線表格進行註冊。註冊撥入詳細信息後,所有電話參與者將收到一封自動生成的電子郵件,其中包含撥入號碼的鏈接 以及用於通過電話訪問活動的個人 PIN 碼。如果您要加入電話會議,請在開始時間 15 分鐘前 撥號。
關於 AMT-130 的 I/II 期臨牀計劃
用於治療亨廷頓舞蹈病的 AMT-130 的美國 I/II 期臨牀試驗正在探索總共 26 名患者的安全性、耐受性和有效性信號 ,分為 10 名患者、低劑量隊列,然後是 16 名患者, 高劑量隊列;患者被隨機分配接受治療 AMT-130 或模仿(虛擬)手術。多中心試驗包括 為期12個月的失明核心研究期,然後是為期五年的非盲長期隨訪。在臨牀 試驗中,共有 16 名患者被隨機分配接受治療,並通過核磁共振成像引導、對流增強的立體定向 神經外科直接輸送到紋狀體(尾狀體和外殼)中接受了單次給藥 AMT-130。大劑量隊列 中另有四名對照患者交叉接受治療。更多詳情可在 www.clinicaltrials.gov (NCT04120493) 上查閲。
這項針對 AMT-130 的歐洲開放標籤 ib/II 期研究將在兩個劑量隊列中招收 15 名早期表現為亨廷頓氏病的患者。由六名患者組成的低劑量 隊列已完成入組,其餘的高劑量隊列預計將在2023年中期完成入組。 與美國的研究一起,歐洲研究旨在確立 AMT-130 的安全性、概念驗證和最佳劑量,以便在加速註冊途徑可行的情況下推進 III 期開發或進入確認性研究。
AMT-130 是 UniQure 首個整合其專有的 miQure 的專注於中樞神經系統 (CNS) 的臨牀項目®平臺。
關於亨廷頓氏病
亨廷頓氏病 是一種罕見的遺傳性神經退行性疾病,會導致包括舞蹈症在內的運動症狀,行為異常和 認知能力下降導致身心逐漸惡化。本病是一種常染色體顯性疾病,亨廷頓基因的第一個外顯子出現致病的 CAG 重複擴張,導致 大腦中異常蛋白質的產生和聚集。儘管亨廷頓舞蹈病的病因很明確,但目前尚無經批准的延緩發作或減緩 疾病進展的療法。
關於 Uniqure
UniQure正在兑現 的基因療法——具有潛在治癒效果的單一療法。UniQure最近批准了B型血友病基因 療法,這是一項基於十多年的研究和臨牀開發的歷史性成就,代表着 在基因組醫學領域的一個重要里程碑,為血友病患者開闢了新的治療方法。Uniqure 現在正在利用其模塊化和經過驗證的技術平臺推進一系列專有基因療法,用於治療 患者伴有亨廷頓氏病、難治性顳葉癲癇、ALS、Fabry 病和其他嚴重疾病。www.uniqure.com
UniQure 前瞻性 陳述
本新聞稿 包含經修訂的1933年《證券法》第27A條和經修訂的1934年《證券交易法》第21E 條所指的前瞻性陳述。除歷史事實陳述以外的所有陳述都是前瞻性陳述, 通常由 “預期”、“相信”、“可以”、“建立”、“估計”、“期望”、“目標”、“打算”、“展望”、“可能”、“計劃”、“潛力”、“預測”、“項目”、“尋求”、“應該” 等術語表示 “意志”、“將” 和類似的表達式 以及這些術語的否定詞。前瞻性陳述基於管理層的信念和假設以及截至本新聞稿發佈之日管理層可獲得的信息 。這些前瞻性陳述包括但不限於 AMT-130 潛在的 臨牀和功能影響,包括作為亨廷頓舞蹈病患者的重要治療選擇, 歐洲開放標籤的 AMT-130 ib/II 期研究的入組預計完成,以及正在進行的美國 I/II 期臨牀中啟動第三個隊列 。uniQure的實際結果可能與預期的結果存在重大差異這些前瞻性 陳述有多種原因,包括與進行臨牀相關的風險亨廷頓舞蹈病試驗、金融 和地緣政治事件對UniQure以及整個經濟和醫療保健系統的影響、Uniqure的臨牀開發活動、臨牀 結果、合作安排、監管監督、產品商業化和知識產權索賠,以及UniQure定期證券申報(包括其年度報告)中 “風險因素” 標題下描述的 風險、不確定性和其他因素 2023 年 2 月 27 日向美國證券交易委員會提交的 10-K 表報告及其季度報告10-Q 表格於 2023 年 5 月 9 日向美國證券交易委員會提交。鑑於這些風險、不確定性和其他因素,您不應過分依賴這些 前瞻性陳述,即使將來有新信息 可用,UniQure也沒有義務更新這些前瞻性陳述。
Uniqure 聯繫人:
| 對於投資者: | 對於媒體: | |||
| 瑪麗亞·E·坎託 | 基婭拉·魯索 | 湯姆·馬龍 | ||
| 直接:339-970-7536 | 直播:617-306-9137 | 直播:339-970-7558 | ||
| 手機:617-680-9452 | 手機:617-306-9137 | 手機:339-223-8541 | ||
| m.cantor@uniQure.com | c.russo@uniQure.com | t.malone@uniQure.com |