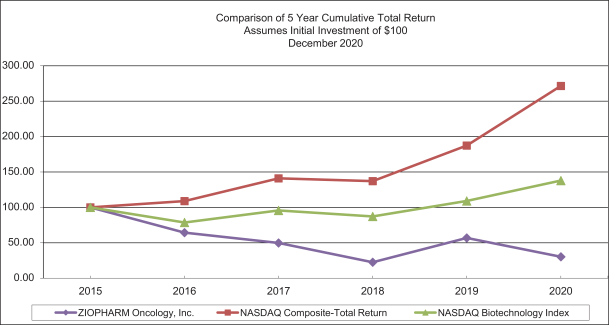
第6項:精選財務數據
我們已選擇遵守2021年2月10日修訂的S-K條例第301項,並依賴於此而省略本披露。
項目七、財務狀況和經營成果的管理研討與分析
以下對本公司財務狀況和經營結果的討論和分析應與本年度報告中其他部分的綜合財務報表和相關附註一併閲讀。
表格10-K.輸入
除了歷史財務信息之外,下面的討論還包含反映我們的計劃、估計和信念的前瞻性陳述。我們的實際結果可能與任何前瞻性陳述中包含或暗示的結果大不相同。可能導致或導致這些差異的因素包括第I部分第1A項所列“風險因素”項下和“關於前瞻性陳述的特別説明”項下或本年度報告其他部分中的那些因素。表格10-K
概述
我們是一家臨牀階段的生物製藥公司,專注於發現、開發和商業化下一代免疫腫瘤學平臺,利用基於細胞和基因的療法治療癌症患者。我們正在開發利用免疫系統的平臺技術,採用創新的細胞工程和新穎的受控基因表達技術,旨在為多種癌症類型的治療提供安全有效的細胞和基因療法。我們的主要平臺和優先事項被稱為睡美人,基於使用轉座子/轉座酶系統的免疫細胞的非病毒基因工程,該系統旨在穩定地設計體外T細胞,以便隨後進行輸注。我們的第二個平臺被稱為受控IL-12,旨在刺激白細胞介素12的表達,或
IL-12,
免疫系統的主要調節者,以受控的方式集中患者的免疫系統,以更有效地攻擊癌細胞。利用我們的睡美人平臺,我們正在開發T細胞受體或TCR T細胞療法,以針對實體腫瘤中的新抗原,使用兩種方法,我們稱之為“圖書館TCR-T方法”和“我們的個性化TCR-T方法”。庫TCR-T方法使用具有以下特性的第三方(同種)TCR
74