
G1 Treateutics公司提供2022年第四季度和全年的財務業績和經營亮點--2022年全年COSELA®(曲拉西利)的銷售淨收入達到3,130萬美元,比2021年增長182%;提供了2023年COSELA 5000萬至6000萬美元的淨收入指導--宣佈了接受FOLFOXIRI+Bevacizumab治療轉移性結直腸癌(CRC)患者的Trilaciclib關鍵第三階段試驗的主要結果(PREVER1)--提供了兩項針對三陰性乳腺癌(TNBC)的第二階段試驗的初步結果,表明Trilaciclib有潛力降低(>50%)與抗體藥物結合(ADC)相關的不良事件發生率,並有利地改變腫瘤微環境--宣佈的執行繼任計劃:首席財務官詹妮弗·摩西將於2023年3月15日辭職,並繼續擔任高級顧問;G1首席財務官約翰·W·烏姆斯特德五世被任命為首席財務官--管理層將於美國東部時間2023年3月1日上午8:30主持網絡廣播和電話會議--商業階段的腫瘤學公司G1治療公司(納斯達克代碼:GTHX)今天提供了截至2022年12月31日的第四季度和全年的公司和財務最新情況。G1治療公司首席執行官傑克·貝利表示:“自2022年初以來,G1團隊已經實現了我們在年初提出的里程碑,並懷着一家專注於我們尋求治療的癌症患者需求的公司的決心做到了這一點。”自從上個月宣佈PERVE 1的結果以來,我們在其他業務上已經迫不及待地向前推進。首先,我們對小細胞肺癌業務保持信心,並在2023年2月之前恢復了COSELA銷售額的增長。其次,我們正在積極執行我們正在進行的臨牀試驗,包括TNBC的第二階段ADC和MOA試驗, 其中每一項都在2022年底提供了令人信服的初步結果,預計今年第二季度還會有更多讀數。第三,我們已經迅速採取行動,對組織和我們的開支進行了必要的削減,以在我們正在進行的每一項臨牀試驗中擴大我們的現金跑道。“貝利繼續説道:“我還想代表G1團隊向Jen Mosse表示感謝,感謝她為我們的公司、我們的願景和我們尋求治療的患者所做的奉獻。任自2015年以來一直在G1工作,並於2019年成為我們的首席財務官;在此期間,她的財務領導能力一直不同尋常。我們祝願她在她的下一個職業篇章中繼續取得成功。2022年第四季度和最近的亮點財務·實現了2022年第四季度和全年COSELA淨收入890萬美元和3130萬美元:與2021年同期相比,業績分別增長了102%和182%。G1確認2022年第四季度和全年的總收入分別為1030萬美元和5130萬美元。·完成公開發行,淨收益為5200萬美元:2022年11月,G1完成了普通股的承銷公開發行,公開發行價為每股6.50美元。·截至2022年第四季度,現金、現金等價物和有價證券為1.451億美元。1

臨牀·宣佈接受FOLFOXIRI+Bevacizumab治療轉移性結直腸癌(CRC)患者的Trilaciclib關鍵3期試驗的頂線結果(PREVER1):G1宣佈其關鍵3期PREVE 1試驗的頂線結果表明,該試驗實現了與嚴重中性粒細胞減少症有關的共同主要終點,具有統計學意義(p50%),與先前發表的saituzumab單藥安全性簡介相比,與ADC saituzumab GOGITECHZIY相關的不良事件的發生率,包括骨髓抑制和腹瀉。該公司預計將在2023年第二季度的一次醫學會議上披露更全面的數據集,包括安全性和初步療效結果。(這裏發佈的新聞稿)·確認了包括Trilaciclib(PREVERE 3)的膀胱癌第二階段試驗的主要進展終點無進展存活的初步結果預計將於2023年年中公佈:G1重申,預計從2023年年中開始將有更多的安全性和有效性結果,包括無進展生存的主要終點的結果。(此處新聞稿)Medical·在聖安東尼奧乳腺癌研討會(SABCS)上公佈的第二階段作用機制試驗結果顯示,Trilaciclib有利地改變了腫瘤微環境:G1提供了24名患者進行的第二階段作用機制(MOA)試驗的初步結果,該結果顯示,單劑Triaciclib單藥治療後,腫瘤微環境發生了有利的變化,指標是早期三陰性乳腺癌(TNBC)患者CD8+T細胞與T調節細胞(Tregs)的比例增加。(新聞稿請點擊此處)2

·在2022年癌症免疫治療學會(SITC)會議上介紹了Trilaciclib的非臨牀研究結果,闡明瞭Trilaciclib的免疫效應:新的非臨牀數據顯示,Trilaciclib上調了癌症免疫循環中的關鍵過程,包括Trilaciclib促進CD8+T細胞分化為效應記憶和中樞記憶T細胞羣。此外,Triaciclib還可以通過上調HMC I和II類分子來增加腫瘤細胞的抗原提呈,並促進T細胞向腫瘤細胞的募集。(此處新聞稿)公司·減少員工人數和相關費用,以將Cash Runway擴展到臨牀試驗讀數之外:G1完成了約30%的有效裁員,但COSELA銷售團隊保持不變。由於這一點以及其他方面的支出削減,G1目前預計其2023年的運營費用將比2022年下降20%至30%。通過對運營費用的這些調整、提供的營收指導以及有關合作夥伴收入的其他假設,該公司相信,這將擴大其現金跑道,使其即將從正在進行的臨牀試驗中讀出數據。·宣佈的高管繼任計劃:G1首席財務官簡·摩西將於2023年3月15日辭職,並將繼續擔任該組織的高級顧問一年。自她離職之日起,G1的財務總監約翰·W·烏姆斯特德五世將被任命為首席財務官。烏姆斯特德自2018年以來一直在該公司工作。在加入本公司之前,Umstead先生曾在普華永道會計師事務所工作,為從小型非上市公司到大型上市公司等不同行業的客户提供服務,承擔着越來越多的責任。2022年第四季度和全年財務業績截至2022年12月31日,現金和現金等價物以及有價證券總額為1.451億美元, 相比之下,截至2021年12月31日,這一數字為2.212億美元。這包括2022年第四季度以每股6.50美元的公開發行價承銷的普通股公開發行的淨收益5200萬美元。考恩和雷蒙德·詹姆斯擔任此次發行的聯合簿記管理人。Needham&Company和韋德布什PacGrow擔任此次發行的牽頭經辦人。2022年第四季度的總收入為1030萬美元,其中COSELA的產品淨銷售額為890萬美元,許可證收入為140萬美元,主要與EQRx和Simcere的臨牀試驗報銷有關,而2021年第四季度的總收入為580萬美元。2022年全年總收入為5130萬美元,其中銷售COSELA的淨產品收入為3130萬美元,許可證收入為2000萬美元,而前一年的總收入為3150萬美元。2022年第四季度的運營費用為4110萬美元,而2021年第四季度為4340萬美元。GAAP運營費用包括2022年第四季度基於股票的薪酬支出440萬美元,而2021年第四季度為520萬美元。2022年全年的運營費用為1.875億美元,而前一年為1.739億美元。2022年全年的基於股票的薪酬支出為2060萬美元,而前一年為2230萬美元。2022年第四季度的商品銷售成本支出為100萬美元,而2021年第四季度為40萬美元,這主要是由於產品銷售額的增加。2022年全年的商品銷售成本支出為370萬美元,而前一年為200萬美元。2022年第四季度的研發(R&D)費用為1660萬美元, 相比之下,2021年第四季度的收入為1980萬美元。研發費用的減少主要是由於公司的臨牀計劃成本降低。2022年全年的研發費用為8330萬美元,而前一年為7620萬美元。3.

2022年第四季度的銷售、一般和行政(SG&A)支出為2360萬美元,而2021年第四季度為2320萬美元。SG&A費用的增加是由於人員費用增加,但被付給勃林格-英格爾海姆的款項減少以及專業和行政費用減少所抵消。2022年全年的SG&A費用為1.004億美元,而前一年為9570萬美元。2022年第四季度的淨虧損為3360萬美元,而2021年第四季度的淨虧損為4000萬美元。2022年全年淨虧損為1.476億美元,而前一年淨虧損為1.484億美元。2022年第四季度的基本和稀釋後每股淨虧損為0.73美元,而2021年第四季度為0.94美元。2022年全年的基本和稀釋後每股淨虧損為3.38美元,而上年為3.54美元。2023年財務指引G1今天提供了2023年全年財務指引。該公司預計2023年將產生5,000萬至6,000萬美元的COSELA淨收入。G1的產品收入指引是基於對COSELA在美國的銷售業績繼續加速的預期。網絡廣播和電話會議G1將在上午8:30主持網絡廣播和電話會議。美國東部時間今天提供截至2022年12月31日的第四季度和全年的企業和財務最新情況。請注意,有一個通過電話訪問呼叫的新流程。要註冊和接收撥入號碼和唯一PIN以訪問實時電話會議,請單擊此鏈接進行在線註冊。雖然不是必需的, 建議您在活動開始前10分鐘參加。該公司網站的活動和演示頁面將提供現場直播和存檔網絡直播,網址為:www.g1Treatutics.com。活動結束後,網絡直播將在同一頁面上存檔90天。注射用®(Triaciclib)於2021年2月12日獲得美國食品和藥物管理局的批准。適應症COSELA®(Triaciclib)在治療廣泛期小細胞肺癌之前使用含鉑/依託泊苷或含拓撲替康的方案,可減少成人患者化療引起的骨髓抑制的發生率。重要安全信息COSELA禁忌用於對曲拉西利有嚴重過敏反應史的患者。警告和預防措施包括注射部位反應(包括靜脈炎和血栓性靜脈炎)、急性藥物過敏反應、間質性肺部疾病(肺炎)和胚胎-胎兒毒性。最常見的不良反應(>10%)為乏力、低鈣血癥、低鉀血癥、低磷血癥、天冬氨酸轉氨酶升高、頭痛和肺炎。這些信息並不全面。請點擊此處查看完整的預售信息。Http://www.g1Treateutics.com/Cosela/pi/4

如需報告疑似不良反應,請致電1-800-790-G1TX與G1治療公司聯繫,或致電FDA電話1-800-FDA-1088或訪問www.fda.gov/medwatch。G1治療公司簡介G1治療公司是一家商業階段的生物製藥公司,專注於下一代療法的開發和商業化,以改善癌症患者的生活,其中包括該公司的第一種商業產品COSELA®(Triaciclib)。G1有一個深入的臨牀流程,並正在執行一項開發計劃,評估Triaciclib在各種實體腫瘤中的應用,包括乳腺癌、肺癌和膀胱癌。G1 Treateutics的總部設在北卡羅來納州的研究三角園區。如需更多信息,請訪問www.g1Treateutics.com,並在Twitter@G1 Treateutics上關注我們。G1 Treateutics®和G1 Treateutics標識以及COSELA®和COSELA標識是G1治療公司的商標。本新聞稿包含符合1995年私人證券訴訟改革法的前瞻性陳述。“可能”、“將”、“預期”、“計劃”、“預期”、“估計”、“打算”等詞語和類似的表述(以及涉及未來事件、條件或情況的其他詞語或表述)旨在識別前瞻性表述。本新聞稿中的前瞻性陳述包括但不限於對COSELA(Triaciclib)商業銷售的預期、COSELA(Triaciclib)的治療潛力、我們2023年全年的財務指導、我們產生數據以最大限度地提高Triaciclib對未來治療範例的適用性的能力、我們獲得批准COSELA(Triaciclib)其他適應症並將其商業化的能力, 以及我們對合作夥伴開發授權產品的依賴。如果我們不遵守每月淨收入契約或債務安排的最低現金契約,我們可能會受到貸款協議中的加速條款的約束,貸款人可能會收回債務,導致我們迫切需要額外資金。此外,COSELA(Triaciclib)可能無法達到市場對商業成功的接受程度,以及新冠肺炎(冠狀病毒)等流行病的影響。這些前瞻性陳述中的每一項都是基於公司截至本新聞稿發佈之日的預期和假設,涉及風險和不確定性。公司在提交給美國證券交易委員會的文件中討論了可能導致公司的實際結果與本新聞稿的前瞻性陳述中明示或暗示的結果不同的因素,包括其中包含的“風險因素”部分,包括但不限於,公司成功完成COSELA(Triaciclib)商業化的能力;該公司完成COSELA(Triaciclib)其他適應症的臨牀試驗、獲得批准並將其商業化的能力;該公司在正在進行的臨牀試驗中取得的初步成功可能不代表這些試驗完成或在後期試驗中取得的結果;與開發新產品或技術以及作為商業階段公司運營相關的內在不確定性;以及市場狀況。除非法律另有要求,否則公司沒有義務更新本文中包含的任何前瞻性陳述,以反映預期的任何變化,即使有新的信息可用。#G1治療公司聯繫人:Jen Mosse首席財務官919-930-8506, 投資者關係和企業溝通5

919-907-1944電子郵件:wroberts@g1Treateutics.com
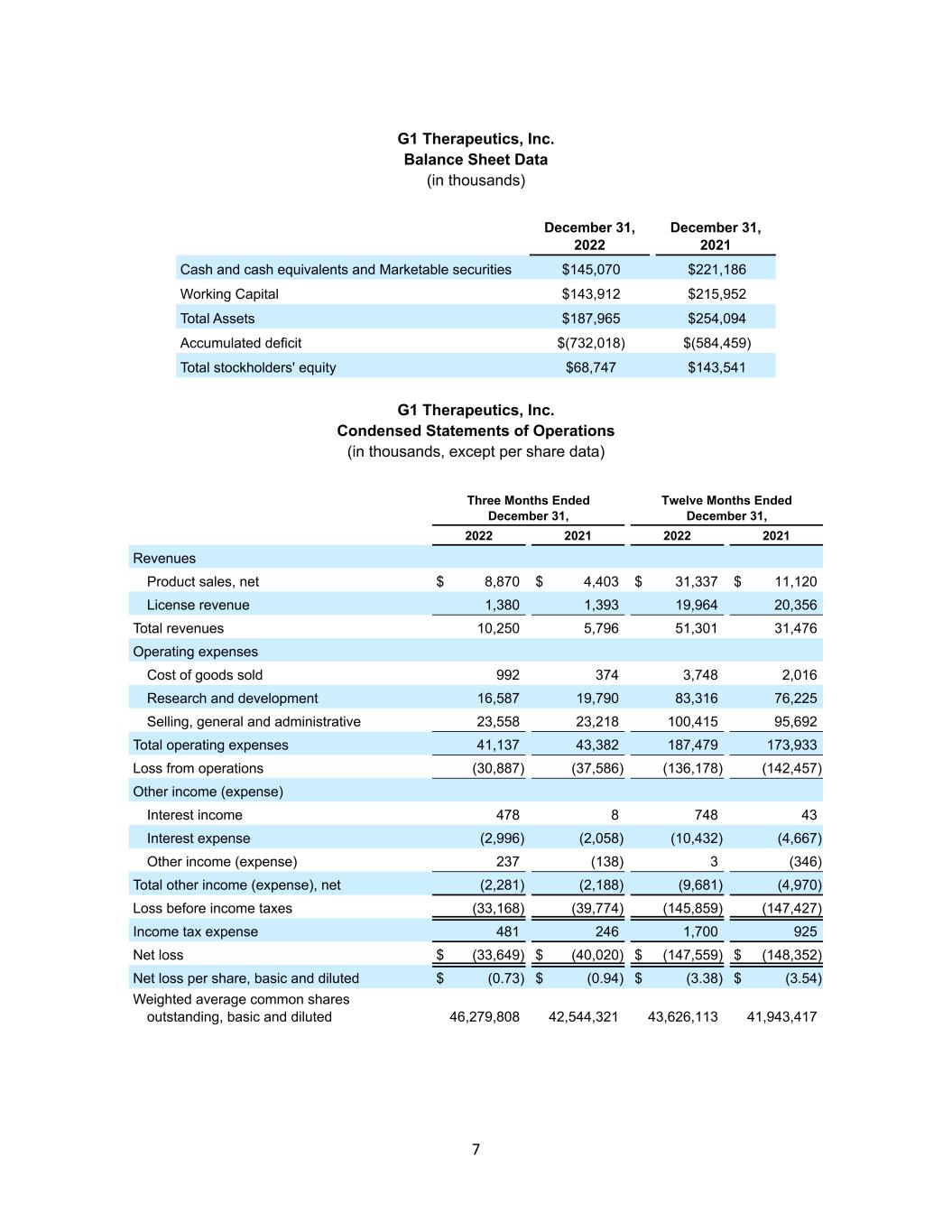
G1治療公司資產負債表數據(千)2021年12月31日現金及現金等價物和有價證券$145,070$221,186營運資本$143,912$215,952總資產$187,965$254,094累計虧損$(732,018)$(584,459)總股東權益$68,747$143,541 G1治療公司簡明運營報表(以千為單位,每股數據除外)截至2021年12月31日的三個月淨額$8,870$4,403$31,337$11,120許可收入1,380 1,393 19,964 20,356總收入10,250 5,796 51,301 31,476商品銷售成本992 374 3,748 2,016研發16,587 19,790 83,316 76,225銷售、一般和管理23,558 23,218 100,415 95,692總運營費用41,137 43,382 187,479 173,933(30,887)(37,586)(136,178)(142,457)其他收入(費用)利息收入478 8 743(2,058)(10,432)(4,237)其他收入(費用)(138)3(346)(2,281)(2,188)(9,681)(4,970)所得税前淨虧損(33,168)(39,774)(145,859)(147,427)所得税支出481 246 1,700 925淨虧損$(33,649)$(40,020)$(147,559)$(148,352)每股淨虧損,基本和稀釋後每股淨虧損(0.73)$(0.94)$(3.38)$(3.54)加權平均流通股,基本和稀釋後普通股46,279,808 42,544,321 43,626,113 41,943,417 7