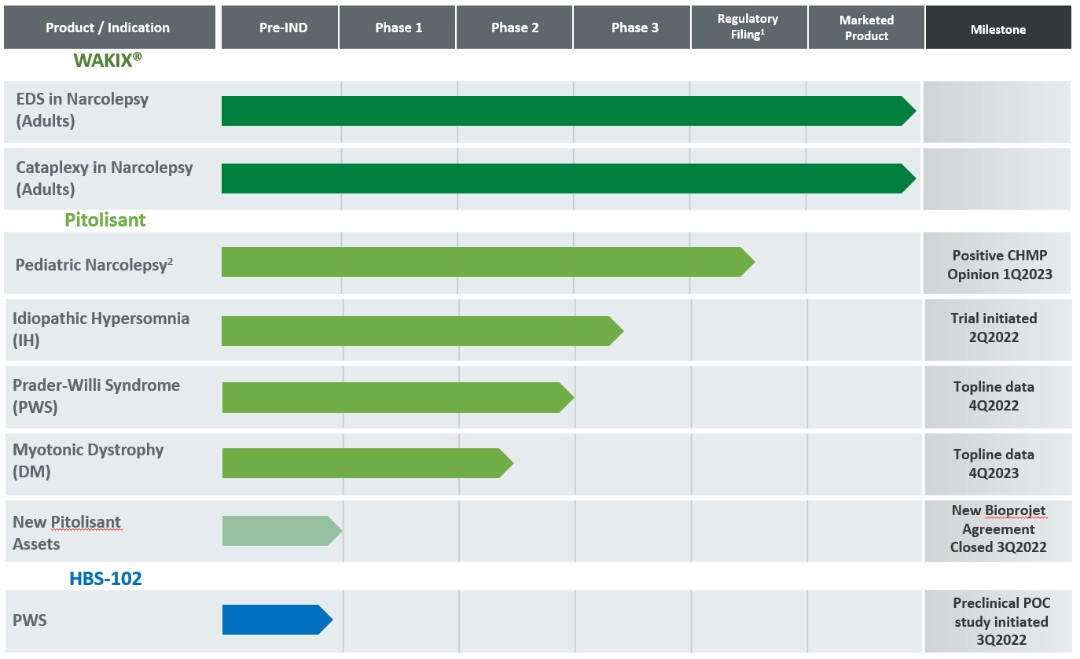
2022年LCA於2022年9月28日結束,3000萬美元的許可費在截至2022年12月31日的年度綜合運營和全面收益(虧損)報表中記錄在研發費用中。
2022年LCA將持續到為每個新產品支付版税的義務到期。任何一方都可以終止2022年LCA,因為另一方的重大違約在90天內仍未治癒。如果我們或我們的分被許可人對許可的專利提出質疑,BioProjet可能會完全終止2022年的LCA。此外,我們和BioProjet有權在對方破產時終止2022年LCA。
知識產權
知識產權,包括專利、商業祕密、商標和版權,對我們的業務非常重要。我們的商業成功在一定程度上取決於我們是否有能力為我們的WAKIX產品和未來潛在的基於瀝青劑的產品以及未來的候選產品和新發現、產品開發技術和專有技術獲得和維護專有知識產權保護。我們的商業成功在一定程度上還取決於我們在不侵犯他人所有權的情況下運營的能力,以及防止他人侵犯我們的所有權的能力。我們的政策是通過許可或提交與我們的技術、發明和改進有關的美國和外國專利和申請等方法,發展和保持對我們的專有地位的保護,這些專利和申請對我們的業務的發展和實施非常重要。
我們的WAKIX專利組合由三項美國專利組成,這三項專利是Bioprojet根據2017年LCA獨家授權給我們的。一項美國專利,第8,207,197號,其權利要求涉及一種多晶型,即一種特定的結晶形式,以及製備該多晶型的腦脂劑的方法,該專利預計將於2030年3月到期,這是基於一項被批准的延長專利期限的請求,但沒有考慮任何可能的兒科排他性。另一項美國專利,第8,486,947號,要求通過使用腦脊液治療日間過度嗜睡的方法,預計將於2029年9月到期,不考慮任何可能的專利期限延長。
我們的HBS-102專利組合包括三個專利系列。第一個專利系列包括美國專利第8,637,501號,該專利要求將某些黑色素濃縮激素(MCH-1)受體拮抗劑作為物質的組合物,以及製造該拮抗劑的方法,用於治療肥胖、焦慮和抑鬱的方法,以及製備化合物的方法,該專利預計將於2031年4月到期,不考慮任何可能的專利期延長。第二個專利系列包括三項已獲授權的美國專利(編號8,716,308;9,296,743;和9,650,378),並在澳大利亞、巴西、加拿大、中國、德國、西班牙、法國、英國、以色列、意大利、日本、韓國、墨西哥和新西蘭獲得專利。這些專利要求將某些人類MCH-1受體選擇性拮抗劑作為物質的組合物,預計將於2031年6月(‘308專利)和2029年1月(’743和‘378專利,以及國際專利)到期。第三個專利系列包括一項正在進行的PCT申請(WO2021/142395),並要求提供包含三重單胺再攝取抑制劑、MCH受體1(MCHR1)拮抗劑和二氮嗪的藥物的治療組合或配方,以及治療或預防過度吞噬、中到重度暴食障礙、神經性暴食症和肥胖管理的方法。
我們產品組合中單個專利的期限取決於獲得這些專利的國家/地區的專利法律期限。在美國,專利期是自提交非臨時專利申請的最早日期起20年。美國專利的期限可能符合專利期限調整的條件,這允許恢復專利期限,作為對美國專利商標局(USPTO)在專利起訴過程中發生的延遲的補償。此外,對於涵蓋FDA批准的藥物的專利,1984年的《藥品價格競爭和專利期限恢復法》(“哈奇-瓦克斯曼法案”)允許專利期限在專利到期後最多延長五年。雖然專利期限延長的長度與藥物接受監管審查的時間長短有關,但專利期限延長不能將專利的剩餘期限從產品批准之日起總共延長14年,而且根據哈奇-瓦克斯曼法案,每種批准的藥物只能延長一項專利。
像我們這樣的公司的專利地位通常是不確定的,涉及複雜的法律和事實問題。美國專利法或其解釋的變化可能會削弱我們保護我們的技術或候選產品的能力,並可能影響此類知識產權的價值。特別是,我們阻止第三方製造、使用、銷售、提供銷售或進口侵犯我們知識產權的產品的能力,在一定程度上將取決於我們能否成功地執行涵蓋我們的技術、發明和改進的專利主張。我們不能保證就我們將來可能提交的任何專利申請授予專利,也不能保證未來可能授予我們的任何專利在保護我們的產品、使用方法或