第一部分
關於這份年報
除文意另有所指外,本年度報告10-K表格中使用的術語“Benitec”、“公司”、“我們”、“我們”以及類似的術語指(I)在重新註冊(如本文定義)之前的Benitec Biophma Limited(BBL)及其子公司,以及(Ii)在重新註冊之後,指的是位於特拉華州的Benitec Biophma Inc.及其子公司(包括Benitec Limited)。凡提及“Benitec Limited”或“BBL”時,均指Benitec Biophma Limited,一家澳大利亞公司。2020年8月14日,BBL重組為一傢俬有有限公司,並更名為Benitec Biophma Property Limited。
本年度報告中所提及的“$”均指美元。本年度報告中提及的“澳元”均指澳元。截至2022年6月30日,美元兑澳元匯率為1.4512澳元。
我們的財政年度結束日期是6月30日。凡提及某一“財政年度”,即指截至該財政年度6月30日止的財政年度。
行業和市場數據
本年度報告包括來自第三方來源的有關市場和行業狀況以及市場份額的信息,或基於使用此類來源的估計(如果有)。我們認為,這些信息和估計是合理和可靠的。我們還認為,從第三方來源的出版物中摘錄的信息已被準確轉載。然而,我們尚未獨立核實來自第三方來源的任何數據。同樣,我們的內部研究是基於我們對行業狀況的瞭解,這些信息沒有得到任何獨立消息來源的核實。
商標和商號
我們擁有本年度報告中使用的商標的專有權和許可權,這些商標對我們的業務非常重要,其中許多商標是根據適用的知識產權法律註冊的。我們的商標包括:
| • | 貝尼特克生物製藥公司 ® |
| • | 貝尼特克 ® |
| • | 默默地治療疾病 ® |
| • | 讓生命沉默的基因 ® |
僅為方便起見,本年度報告中提及的商標和商號在出現時未使用
®
“或”™“符號,但此類引用並不以任何方式表明,我們不會在適用法律下最大限度地主張我們或適用許可人對這些商標和商號的權利。我們不打算使用或展示其他公司的商標、商標或服務標誌,以暗示我們與任何其他公司的關係,或我們的背書或贊助。本年度報告中出現的任何其他公司的每個商標、商號或服務標誌均為其各自持有人的財產。1
目錄表
關於前瞻性陳述的特別説明
本年度報告包含受許多風險和不確定性影響的前瞻性陳述,其中許多風險和不確定性是我們無法控制的。除本年度報告中包含的有關歷史事實的陳述外,所有有關本公司戰略、未來業務、財務狀況、預計成本、前景、計劃和管理目標的陳述均為前瞻性陳述。在本年度報告中使用的“可能”、“相信”、“預期”、“打算”、“估計”、“預期”、“可能”、“繼續”、“預測”、“潛在”、“項目”或這些術語的否定,以及類似的表述旨在識別前瞻性表述,儘管並不是所有的前瞻性表述都包含這樣的識別詞語。這些表述涉及已知和未知的風險、不確定性和其他重要因素,可能導致我們的實際結果、活動水平、業績或成就與這些前瞻性表述中明示或暗示的信息大不相同。這些風險、不確定因素和因素包括:
| • | 我們開發候選產品並可能將其商業化的計劃是否成功; |
| • | 啟動和完成臨牀前研究和臨牀試驗的時間; |
| • | 在任何未來的臨牀試驗中患者登記和劑量的時機和充分性; |
| • | 臨牀試驗數據的可獲得性; |
| • | 監管備案和批准的時間和結果; |
| • | 意想不到的延誤; |
| • | 銷售、營銷、製造和分銷要求; |
| • | 市場競爭和我們的產品在市場上的接受度; |
| • | 美國、法國和加拿大的監管動態; |
| • | 新型AAV載體的開發; |
| • | 我們的技術被許可方的計劃; |
| • | DdRNAi和我們的候選產品的臨牀用途、潛在屬性和益處,包括潛在的治療效果持續時間和“一針”治癒的可能性; |
| • | 我們對與合作者和其他第三方的關係的依賴; |
| • | 費用、持續虧損、未來收入、資本需求和額外融資需求,以及我們在市場條件和其他因素(包括我們的資本結構)下獲得額外融資的能力; |
| • | 我們作為一個持續經營的企業繼續存在的能力; |
| • | 我們預計我們的現金和現金等價物足以執行我們的商業計劃的時間長度; |
| • | 我們的知識產權狀況和我們的專利組合的期限; |
| • | 地方、區域、國家和國際經濟狀況和事件的影響;以及 |
| • | 當前新冠肺炎大流行的影響,由SARS-CoV-2病毒引起的疾病,可能對我們的業務以及臨牀前和未來的臨牀試驗產生不利影響; |
以及在本年度報告和提交給美國證券交易委員會的其他報告中在“風險因素”標題下詳細説明的其他風險。儘管我們相信本年度報告中包含的每一項前瞻性陳述都有合理的基礎,但我們提醒您,這些陳述是基於我們目前已知的事實和重要因素以及我們對未來的預期,而我們不能確定這些事實和因素。
本年度報告中包含的前瞻性陳述是基於我們在本年度報告日期或其日期所獲得的信息而作出的。除非法律要求,否則我們沒有義務修改或更新任何前瞻性陳述,無論是由於新信息、未來事件或
2
目錄表
否則的話。我們建議您參考我們可能直接向您作出的任何其他披露,或我們未來可能向美國證券交易委員會提交的報告,包括Form 10-K的年度報告、Form 10-Q的季度報告以及當前的Form 8-K報告。
本文中包含的所有前瞻性陳述或通過引用併入本文的文件中的所有前瞻性陳述都明確地受到本年度報告中其他地方包含或提及的警告性陳述的限制。
第1項。 |
公事。 |
公司概述
我們努力成為治療藥物的發現、開發和商業化的領導者,這些藥物能夠通過應用沉默和替代方法治療遺傳疾病來解決重大的未得到滿足的醫療需求。
Benitec Biophma Inc.(“Benitec”或“公司”或第三人稱“我們”或“我們的”)是一家發展階段的生物技術公司,專注於推動新型基因藥物的發展,總部設在加利福尼亞州海沃德。這個專利平臺名為DNA定向RNA幹擾,或ddRNAi,將RNA幹擾或RNAi與基因治療相結合,創造出有助於在一次給藥後持續沉默致病基因的藥物。該公司正在開發基於ddRNAi的療法,用於治療慢性和危及生命的臨牀適應症,包括眼嚥肌營養不良症(OPMD),這是一種慢性、危及生命的遺傳病。
BB-301是Benitec目前正在開發的最先進的基於ddRNAi的遺傳藥物。BB-301是一種基於AAV的基因療法,旨在沉默突變的致病基因的表達(減緩或停止疾病進展的潛在機制),同時用正常的“野生型”基因取代突變基因(以推動疾病細胞功能的恢復)。這種疾病管理的基本治療方法被稱為“沉默和替換”。沉默和替換機制提供了恢復病變細胞和組織的標準生理學的潛力,並改善了患有OPMD慢性和潛在致命影響的患者的治療結果。BB-301已在美國和歐盟獲得孤兒藥物稱號。
RNAi的靶向基因沉默效應,與通過使用修改的病毒載體實現的持久轉基因表達相結合,使沉默和替換方法具有產生長期沉默致病基因的潛力,同時在單次注射專利基因藥物後替換野生型基因功能。我們相信,Benitec開發的當前和未來研究藥物的這種新的機械性特徵可以促進實現強大和持久的臨牀活動,同時大大減少傳統上用於治療慢性病的藥物的給藥頻率。此外,實現長期的基因沉默和基因替換可能會顯著降低在潛在致命臨牀疾病的醫療處理過程中患者不依從性的風險。
我們將需要額外的資金來繼續開發我們的候選產品,度過關鍵的轉折點,並繼續執行我們的商業計劃。見“風險因素--我們的審計報告對我們作為持續經營企業的持續經營能力表示懷疑。”
我們的專有技術平臺被指定為DNA定向RNA幹擾或“ddRNAi”,以及“沉默和取代”。DdRNAi的設計目的是通過將RNA幹擾或RNAi與通常與基因治療領域相關的病毒遞送劑(即病毒載體)相結合,產生致病基因的長期沉默。修飾的AAV載體被用來傳遞編碼短髮夾狀RNA的基因構建體,然後,在轉導細胞內連續表達和處理以在靶細胞的生命週期內產生siRNA分子。這些新引入的siRNA分子驅動
3
目錄表
長期的,可能是永久性的,致病基因表達的沉默。沉默和替換方法進一步支持了長期沉默致病基因的生物學益處,方法是在改進的AAV載體中整合多功能基因構建體,以創建基於AAV的基因治療劑,該基因治療劑旨在沉默突變的致病基因的表達(減緩或阻止疾病進展的潛在機制),同時用正常的“野生型”基因取代突變基因(以推動疾病細胞功能的恢復)。這種完全不同的疾病管理治療方法提供了恢復治療組織的基本生理的潛力,並在此過程中,改善了患有眼嚥肌營養不良(OPMD)等疾病的慢性和潛在致命影響的患者的治療結果。
傳統的基因治療的定義是引入一種工程轉基因來糾正由突變或功能失常的基因引起的病理生理紊亂。突變的基因可以促進細胞內致病蛋白質的產生,也可以阻礙關鍵的、維持生命的蛋白質的產生。引入新的轉基因可以促進疾病細胞內正常蛋白質的產生,從而恢復自然的生物功能。關鍵是,這種傳統的基因治療方法的實施不能消除潛在突變基因的表達或潛在的有害影響(因為突變蛋白可能會持續表達,並聚集或推動其他天然蛋白在疾病細胞內的聚集)。在這方面,專有的沉默和替換方法的雙重能力,即通過ddRNAi沉默致病基因,同時通過交付工程轉基因來取代突變基因的野生型活性,可以促進針對一系列遺傳疾病的不同有效治療方法的開發。
RNAi和siRNA方法概述
單個基因的突變可通過導致致病蛋白(即目標蛋白的異常形式)的細胞內產生而導致慢性疾病,許多慢性和/或致命的疾病已知是由於單個基因或多個基因的不適當表達造成的。在某些情況下,這種類型的遺傳疾病可以通過RNA幹擾(“RNAi”)等得到充分驗證的生物學方法,通過“沉默”致病蛋白的細胞內產生來專門治療。RNAi使用小的核酸分子來激活細胞內的酶複合體,這一生物途徑暫時減少了致病蛋白的產生。在沒有致病蛋白的情況下,正常的細胞功能得到恢復,最初由於突變蛋白的存在而導致的慢性疾病部分或完全得到解決。RNAi可能適用於20,000多個人類基因和大量致病微生物特異性基因。
4
目錄表
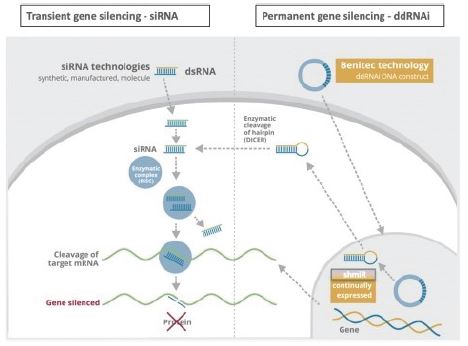
圖1
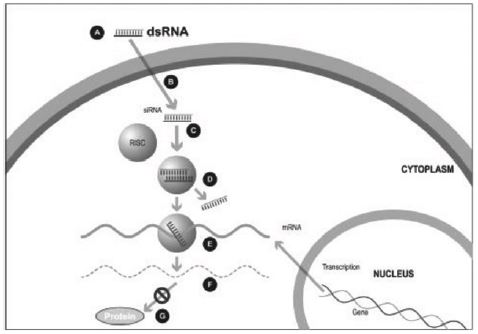
在實驗室合成了一種小的雙鏈RNA或dsRNA分子(A,圖1),由一條稱為正義鏈的鏈和另一條稱為反義鏈的鏈組成,這兩條鏈相互補充。這些小的dsRNA被稱為小幹擾RNA,或siRNA。正義鏈的序列對應於靶基因mRNA的一小段區域。SiRNA被傳遞到靶細胞(B,圖1),在那裏,一組被稱為RNA誘導沉默複合體(RISC)的酶處理siRNA(C,圖1),其中一條鏈(通常是正義鏈)被釋放(D,圖1)。RISC使用反義鏈來尋找具有互補序列(E,圖1)的mRNA,從而導致目標mRNA(F,圖1)的切割。因此,不會產生信使核糖核酸(蛋白質生產)的輸出(G,圖1)。包括Alnylam製藥公司(“Alnylam”)和Arbutus Biophma Corp.(“Arbutus”)在內的幾家公司在他們的RNAi產品候選中使用了這種方法。
重要的是,許多遺傳疾病不符合圖1中概述的傳統基因沉默方法,因為患病細胞可能產生感興趣的野生型蛋白質和致病蛋白質的突變變體的混合物,潛在的基因突變可能太小,無法通過專門使用基於siRNA的方法選擇性地靶向致病蛋白質變體。在這些情況下,在不同時沉默對正常細胞功能至關重要的野生型細胞內蛋白的情況下,選擇性地沉默致病蛋白是非常困難的。
我們專有的沉默和替換技術利用了RNAi獨特的特異性和強大的基因沉默能力,同時克服了基於siRNA的疾病管理方法的許多關鍵限制。
在標準的RNAi方法中,合成雙鏈siRNA,然後通過對RNA的化學修飾或替代遞送方法將其引入靶細胞。雖然通過使用這種方法已經在幾個臨牀適應症中證明瞭有效性,但基於siRNA的方法仍然存在一些侷限性,包括:
5
目錄表
| • | 臨牀治療需要重複給予以siRNA為基礎的治療劑多個週期以維持療效; |
| • | 由於給藥頻率和治療持續時間的原因,患者的長期依從性挑戰; |
| • | SiRNA的治療濃度並不穩定,因為靶細胞中合成的siRNA水平隨着時間的推移而下降; |
| • | 將siRNA引入靶細胞通常需要新的化學修飾或新的遞送材料,這使得開發廣泛的治療劑變得複雜; |
| • | 潛在的免疫不良反應,導致嚴重不良反應; |
| • | 要求為多基因突變引起的遺傳性疾病提供專門的分娩配方;以及 |
| • | SiRNA只起到沉默基因的作用,不能用來用正常功能的基因取代有缺陷的基因。 |
我們的遺傳病治療方法--ddRNAi和沉默與替代
我們專有的沉默和替換方法用於治療遺傳性疾病,將RNAi與野生型基因替換相結合,以推動致病基因的持續沉默,並在單次注射治療劑後恢復功能的野生型基因。Benitec將ddRNAi與經典的基因治療(即通過病毒載體進行轉基因傳遞)相結合,以克服RNAi的幾個基本侷限性。
治療遺傳性疾病的沉默和替換方法使用腺相關病毒載體(“AAVs”)來傳遞基因構建物,該基因構建體在給藥一次後可以:
| • | 在目標、患病的細胞內長期表達RNAi分子(以連續沉默突變的、致病的蛋白質和感興趣的野生型蛋白質的細胞內生產); |
| • | 同時驅動目標蛋白的野生型變體的表達(以恢復天然的細胞內生物學過程);以及 |
| • | AAV載體可以容納含有野生型轉基因工程基因和編碼短髮夾狀RNA/microRNA分子(shRNA/miRNA)的新基因的多功能DNA表達盒,這些基因是支持能夠實現沉默和替代治療方法目標的治療藥物的開發所必需的。 |
我們的沉默和替換技術利用專有的DNA表達盒來促進基因沉默shRNA和野生型蛋白的持續生產(通過表達野生型轉基因)。一系列病毒和非病毒基因治療載體可用於將DNA構建物運送到靶細胞的細胞核中,在運送時,shRNA分子被表達,隨後由細胞內的酶處理成siRNA分子,從而沉默突變的致病蛋白的表達(圖2)。
在靜默和替換方法中(圖2):
| • | 通過諸如AAV載體的基因治療載體(A)將DNA構建物遞送到靶細胞的核; |
| • | 一旦進入細胞核,DNA結構就會驅動shRNA分子(B)的持續產生,這些分子被一種名為DICER的酶處理成siRNA(C); |
6
目錄表
| • | 經過處理的siRNA被結合到RISC中,並使用圖1所示的相同機制沉默目標基因;以及 |
| • | 當DNA表達盒還包括野生型轉基因時,當DNA構建物通過AAV載體進入靶細胞的核時,DNA構建物也驅動野生型蛋白的連續生產(以恢復自然的細胞內生物學過程)。 |
圖2
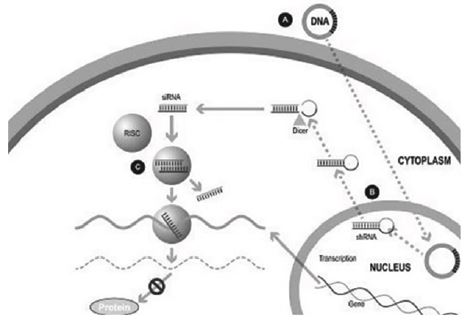
我們的戰略是發現、開發和商業化利用ddRNAi能力和沉默並取代疾病管理方法的治療方法。
對於選定的候選產品,在適當的階段,我們可能會與大型生物製藥公司合作,進一步共同開發,如果獲得批准,我們基於ddRNAi和靜音和替換的產品將商業化,以實現廣泛的臨牀和商業分銷。對於我們認為不在我們直接關注領域之外的特定臨牀適應症,我們將繼續在適當的情況下,超過我們ddRNAi和Silet的應用許可,以促進差異化療法的開發,這可能會進一步驗證我們的專有技術和疾病管理方法。
我們的現金和現金等價物將用於推進我們的OPMD候選產品BB-301,包括自然歷史引入研究和1b/2a階段BB 301治療研究,用於繼續推進其他現有和新產品候選產品的開發活動,用於一般企業用途和戰略增長機會。
眼嚥肌營養不良症(OPMD)
OPMD是一種隱匿性、常染色體顯性、起病晚的退行性肌肉疾病,通常出現在40至50歲的患者中。這種疾病的特點是進行性吞嚥困難(吞嚥困難)。
7
目錄表
和眼皮下垂(上瞼下垂)。OPMD是由聚(A)結合蛋白核1基因或PABPN1基因的特定突變引起的。OPMD是一種罕見的疾病;然而,至少有33個國家的患者被診斷出患有OPMD。患有OPMD的患者羣體得到了很好的識別,並注意到這種疾病患者的顯著地理聚集性,這可以簡化臨牀開發和全球商業化努力。
BB-301是一種基於AAV的基因療法,旨在沉默突變的致病基因的表達(減緩或停止疾病進展的潛在機制),同時用正常的“野生型”基因取代突變基因(以推動疾病細胞功能的恢復)。這種疾病管理的基本治療方法被稱為“沉默和替換”,這種生物機制提供了恢復治療組織的基本生理的可能性,並在這個過程中,改善了患有眼嚥肌營養不良(OPMD)的慢性和潛在致命影響的患者的治療結果。BB-301已在美國和歐盟獲得孤兒藥物稱號。
2018年7月9日,公司與Axovant簽訂了許可和合作協議。根據該協議,該公司授予Axovant全球獨家許可證,用於開發、製造和商業化含有該公司產品BB-301的產品,該產品是為潛在治療眼嚥肌營養不良症而設計的。截至2019年9月3日,與Axovant的許可和合作協議終止。因此,Benitec授予Axovant開發和商業化BB-301及相關基因治療產品候選產品的所有權利和許可證都終止了。我們現在完全負責與BB-301候選產品的開發和商業化相關的成本。
我們的優勢
我們相信,將我們的專利ddRNAi技術與我們在基因藥物設計和開發方面的深厚專業知識相結合,特別是基於ddRNAi的療法,將使我們能夠在用於治療人類疾病的基因沉默和基因療法方面實現並保持領先地位。我們的主要優勢包括:
| • | 基於ddRNAi的專有沉默和替換技術平臺,可能潛在地實現一次給藥療法的系列開發,能夠促進致病基因的持續、長期沉默和伴隨的野生型基因功能的替換; |
| • | 一種專有的AAV載體技術,它使用桿狀病毒系統提高昆蟲細胞中產生的病毒的內體逃逸能力。這項技術在以AAV為基礎的基因治療中有廣泛的應用; |
| • | 有能力推動一系列方案的發展,這些方案側重於患者人數較多的慢性疾病或罕見疾病,這可能會支持獲得包括OPMD在內的孤兒藥物指定;以及 |
8
目錄表
| • | 不斷增長的專利組合保護我們ddRNAi的改進,以及沉默和替換,候選技術和產品至少到2036年,預計額外的專利壽命至少到2040年。 |
我們的戰略
我們努力成為治療藥物的發現、開發和商業化的領導者,這些藥物能夠通過應用沉默和替代方法治療遺傳疾病來解決重大的未得到滿足的醫療需求。我們採用以下總體戰略來推動公司實現這些目標:
| • | 有選擇地開發專有和合作的程序;以及 |
| • | 繼續探索並確保與全球生物製藥公司的研發合作伙伴關係,以支持我們的科學平臺和知識產權組合的差異化性質。 |
我們的高級領導團隊將繼續探索與全球生物製藥公司的合作機會,因為我們預計,專利ddRNAi和沉默和替換方法的獨特屬性,以及適用於我們專利方法的廣泛潛在臨牀適應症,將支持在具有重大未滿足醫療需求的廣泛疾病上形成合作。
我們尋求積極保護我們的知識產權和專有技術。這些努力是我們業務增長的核心,包括:
| • | 尋求和維護要求我們的ddRNAi的專利,並沉默和取代與我們正在開發的特定產品有關的或對我們的業務發展具有商業和/或戰略重要性的技術和其他發明; |
| • | 保護和執行我們的知識產權;以及 |
| • | 戰略性地從第三方獲得知識產權許可,以推進我們候選產品的開發。 |
我們的管道
下表列出了我們目前的候選產品和開發狀況:
表1.流水線:眼嚥肌營養不良

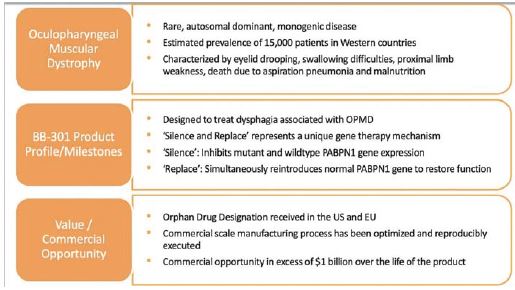
BB-301正在開發中,用於治療眼嚥肌營養不良症,目前正在進行臨牀試驗應用(CTA)使能和研究新藥(IND)使能研究中的評估。BB-301是Benitec的主要管道項目,BB-301的主要屬性如圖3所示。
9
目錄表
圖3
內部發展計劃
BB-301治療眼嚥肌營養不良症
OPMD是一種潛伏的、常染色體顯性的、起病晚的退行性肌肉疾病,通常出現在40至50歲的患者中。該病的特點是進行性吞嚥困難(吞嚥困難)和眼皮下垂(上瞼下垂)。OPMD是由聚(A)結合蛋白核1基因或PABPN1基因的特定突變引起的。OPMD是一種罕見的疾病,然而,至少有33個國家的患者被診斷出患有OPMD。患有OPMD的患者羣體得到了很好的識別,並注意到這種疾病患者的顯著地理聚集性,這可以簡化臨牀開發和全球商業化努力。
PABPN1是一種普遍存在的因子,它促進聚(A)聚合酶和CPSF(切割和聚腺苷酸化特異性因子)之間的相互作用,從而控制mRNA聚(A)尾部的長度、核中的mRNA輸出以及替代的聚(A)位點的使用。OPMD特有的基因突變導致PABPN1外顯子1內的三核苷酸重複序列擴張,並導致PABPN1 N末端的多聚丙氨酸鏈擴大。該突變產生一種蛋白質,其N端擴展的聚丙氨酸束最多由18個連續的丙氨酸殘基組成,容易形成稱為核內包涵體(INI)的聚集體。INIS隔離野生型PABPN1也可能導致與OPMD相關的功能表型喪失。
目前OPMD的治療方法和正在開發中的研究治療藥物
目前還沒有針對OPMD患者的根治或改善疾病的療法。手術幹預可用於姑息目的,包括使用環嚥肌切開術。
10
目錄表