

展品99.1 3Q 2022|業務介紹神經退行性疾病和癌症的疾病修飾療法的臨牀進展 Inhibikase.com:IKT

免責聲明本演示文稿不應構成出售要約或徵求購買任何證券的要約,也不得在任何州或司法管轄區出售此類證券,在這些州或司法管轄區,此類要約、招攬或出售在根據任何此類州或司法管轄區的證券法註冊或資格之前是非法的 。本報告包含的信息可能構成證券法第27A節和修訂後的1934年證券交易法第21E節所指的“前瞻性陳述”。Inhibikase Treateutics,Inc.(以下簡稱“公司”或“我們”)打算將前瞻性陳述納入這些章節中前瞻性陳述的安全港條款。一般來説,我們通過使用“相信”、“預期”、“打算”、“估計”、“預期”、“項目”、“目標”、“預測”、“ ”、“目的”、“應該”、“將”、“可能”、“繼續”以及類似的表述來識別此類前瞻性陳述。此類陳述受許多假設、風險和不確定因素的影響,這些假設、風險和不確定性可能會導致實際結果、業績或成就與這些前瞻性陳述中預期的大不相同。您應該仔細閲讀包含這些詞語的聲明,因為它們討論了未來的預期和計劃,其中包含對未來臨牀研究、監管批准、候選產品開發、運營結果或財務狀況的預測,或陳述其他前瞻性信息。然而,沒有這些詞語或類似的表達並不意味着一項陳述不具有前瞻性。前瞻性陳述不是歷史事實,而只是代表公司對未來事件的信念,其中許多事件的性質, 本質上是不確定的,不在公司的控制範圍內。公司的實際結果和財務狀況可能與這些前瞻性陳述中顯示的預期結果和財務狀況大不相同。管理層認為, 截至目前,這些前瞻性陳述是合理的。但是,應當注意的是,不要過度依賴任何此類前瞻性陳述,因為此類陳述只能説明發表之日的情況。除法律要求外,公司不承擔公開更新或修改任何前瞻性陳述的義務,無論是由於新信息、未來事件還是其他原因。此外,前瞻性陳述會受到某些風險和不確定性的影響,這些風險和不確定性可能會導致實際結果與公司的歷史經驗以及我們目前的預期或預測大相徑庭。可能導致實際結果與前瞻性陳述大不相同的重要因素在公司提交給美國證券交易委員會的文件中陳述,包括其10-K表格的年度報告和10-Q表格的季度報告,包括在“風險因素”標題下。我們 無意使用或展示其他實體的名稱、商號、商標或服務標誌,以暗示與任何其他實體之間的關係,或由任何其他實體背書或贊助我們。Inhibikase.com·:IKT 2

激酶抑制劑治療的多治療流水線開發治療光譜的創新藥物·專注於開發包括神經退行性變、腫瘤學和傳染病在內的廣泛治療範圍的新療法。·目的通過使用該公司使用代謝保留(RAMP)藥物化學平臺的重新工程方法模擬人類疾病來發現新的治療方法·IKT-148009:Lead Abelson Tyroine Kinase(c-Abl)抑制劑計劃有可能成為 帕金森氏病(PD)和相關疾病的疾病修正治療方法。2a期“201”課程開放招生。·IKT-001Pro:第一個腫瘤學產品是一種bcr-abl抑制劑,與治療白血病和胃腸道癌症的標準甲磺酸伊馬替尼相比,其安全性可能有所改善。提交慢性髓系白血病的IND申請。·強大的專利組合,保護到2033年(腫瘤學)和2036年(神經退行性變)。·來自美國國立衞生研究院、美國國防部、邁克爾·J·福克斯基金會和佐治亞州研究聯盟的2080萬美元贈款和合同,均經同行審查;2021年投資者資本毛收入6300萬美元·經驗豐富的管理團隊、顧問、董事會和科學顧問委員會Inhibikase.com·:IKT 3
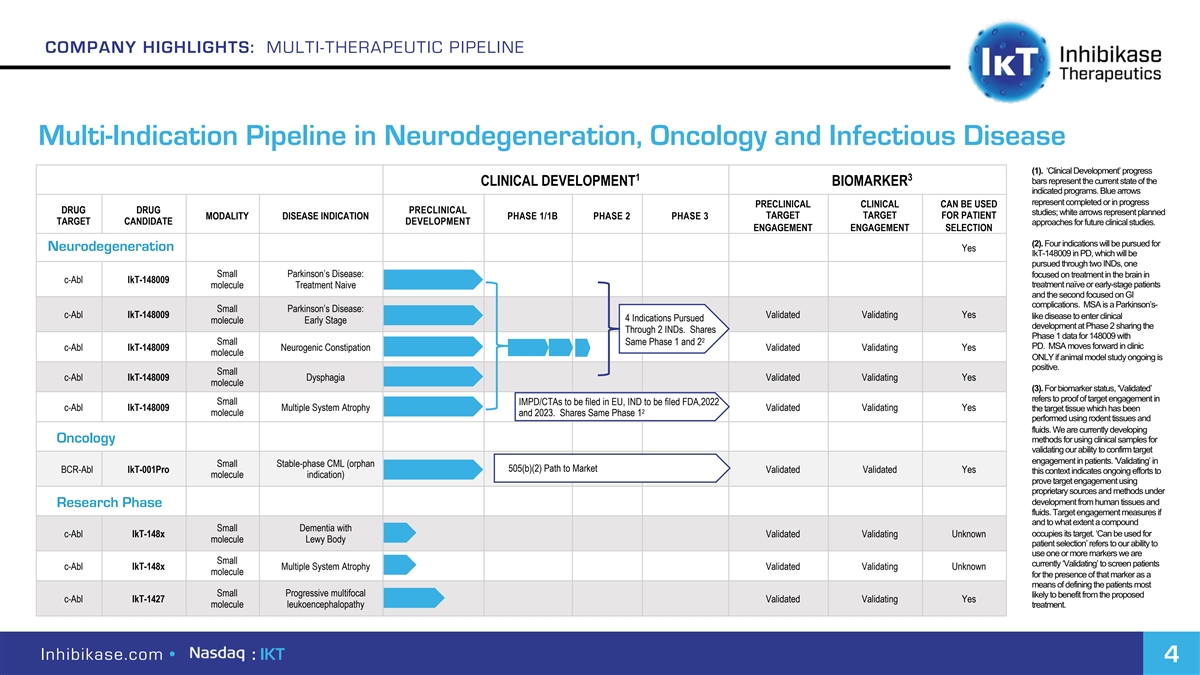
公司亮點:神經退行性疾病、腫瘤和傳染病的多治療流水線多適應症流水線(1)。‘臨牀開發’進展1-3條代表了臨牀開發生物標記物所指示的項目的當前狀態。藍色箭頭表示已完成或正在進行的 臨牀前藥物可用於藥物臨牀前研究;白色箭頭表示患者形態疾病適應症階段1/1B階段2階段3目標候選開發方法的計劃目標。 參與選擇(2)。神經退行性變將尋求四種適應症是IKT-148009治療帕金森氏症,將通過兩種IND來進行,一種是小型帕金森氏症:專注於大腦中的治療,c-Abl IKT-148009 治療幼稚或早期患者的分子治療樸素,第二種側重於胃腸道併發症。MSA是一種帕金森氏症-小型帕金森氏症:C-Abl IKT-148009驗證驗證是樣病進入臨牀4 共享通過2個IND的第二階段分子早期開發。與2個相同的小1期和2個PD共享148009的1期數據。MSA在臨牀上取得了進展,c-Abl IKT-148009神經源性便祕驗證驗證 只有在正在進行的動物模型研究呈陽性的情況下才驗證是分子。小c-Abl IKT-148009吞嚥困難驗證是分子(3)。對於生物標記物狀態,“有效”是指目標參與小型IMPD/CTA的證明將提交給歐盟,IND提交給FDA, 2022年c-Abl IKT-148009多系統萎縮驗證是的,驗證的目標組織已經是2個分子和2023年。共享使用齧齒動物組織和液體執行的相同階段1。我們目前正在開發腫瘤學 方法,使用臨牀樣本來驗證我們確認患者目標參與的能力。在小型穩定相CML(孤兒505(B)(2)上市之路BCR-ABL IKT-001Pro驗證是此上下文 指示正在進行的分子適應症的努力)使用來自人體組織和研究相液的專有來源和方法證明靶向參與。目標參與度衡量複合小規模痴呆症是否以及在多大程度上佔據目標。‘可用於c-Abl IKT-148x驗證未知分子路易體患者選擇’指的是我們使用一個或多個我們目前較小的標誌物的能力,以篩查c-Abl IKT-148x多系統萎縮驗證的患者c-Abl IKT-148x多系統萎縮驗證未知分子的存在,以此作為定義最小進展性多焦點可能從擬議的c-Abl IKT-1427 驗證白質腦病治療中受益的患者的一種手段。Inhibikase.com·:IKT 4

帕金森病市場和帕金森病市場 &戰略戰略Inhibikase.com·:IKT 5
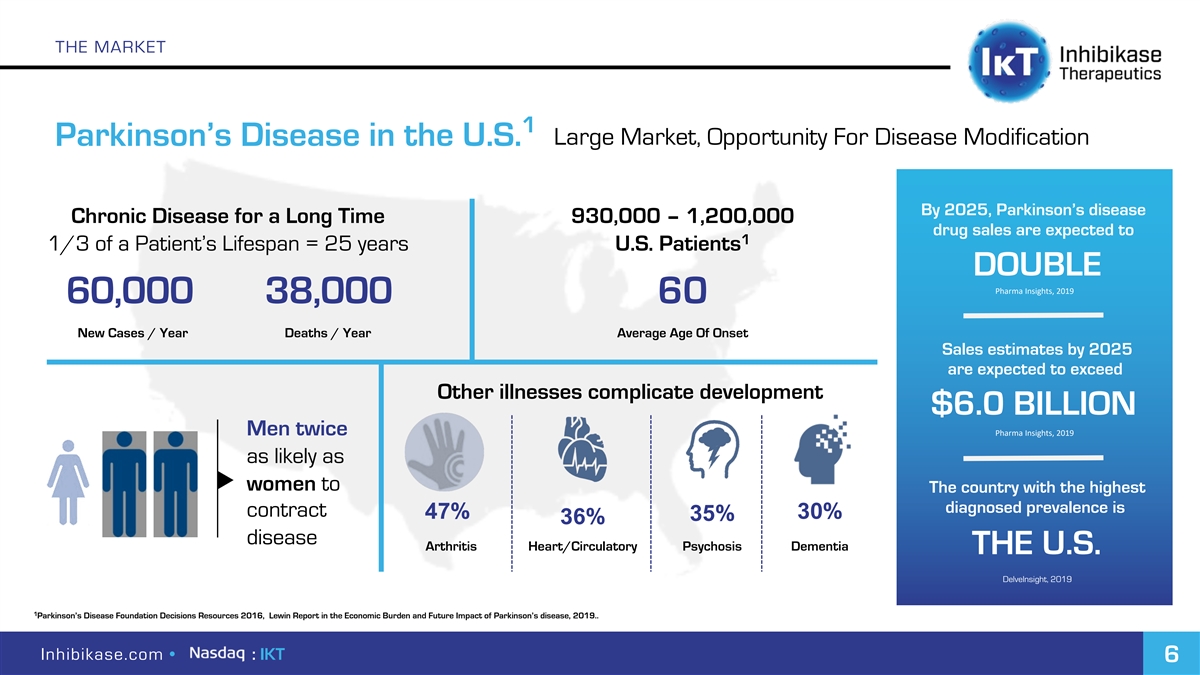
市場1大市場,疾病改良的機會 帕金森氏症在美國。到2025年,帕金森氏症慢性疾病長期存在93,000-1,200,000種藥物的銷售量預計將達到患者壽命的1/3=25年。美國患者加倍Pharma Insights,2019年 60,000 38,000新病例/年60例/年60例/年平均發病年齡銷售估計到2025年將超過其他疾病複雜化發展60億美元男性Pharma Insights,2019年與女性一樣,確診患病率最高的國家是合同47%30%35%36%疾病關節炎心臟/循環性精神病痴呆美國DelveInsight,2019年1帕金森氏病基金會決定資源2016,勒文在經濟負擔和 帕金森病的未來影響,2019年。Inhibikase.com·:IKT 6
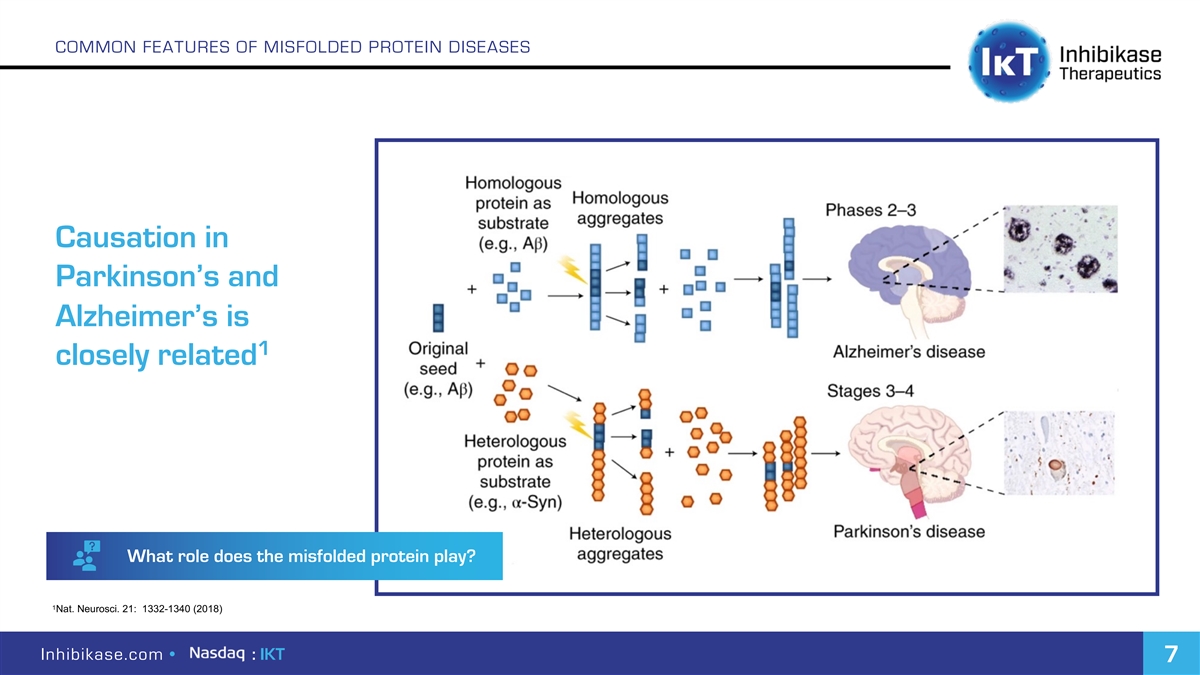
錯誤摺疊的蛋白質疾病的共同特徵在帕金森氏症和阿爾茨海默病的病因中密切相關,錯誤摺疊的蛋白質扮演什麼角色?神經科。21:1332-1340(2018)Inhibikase.com·:IKT 7
帕金森氏症c-Abl中錯誤摺疊的‘種子’蛋白導致神經變性的原因評估視頻>Inhibikase.com·:ikt 8
抑制酶將如何改變帕金森病:用IKT-148009抑制C-Abl激酶 :iKT 9
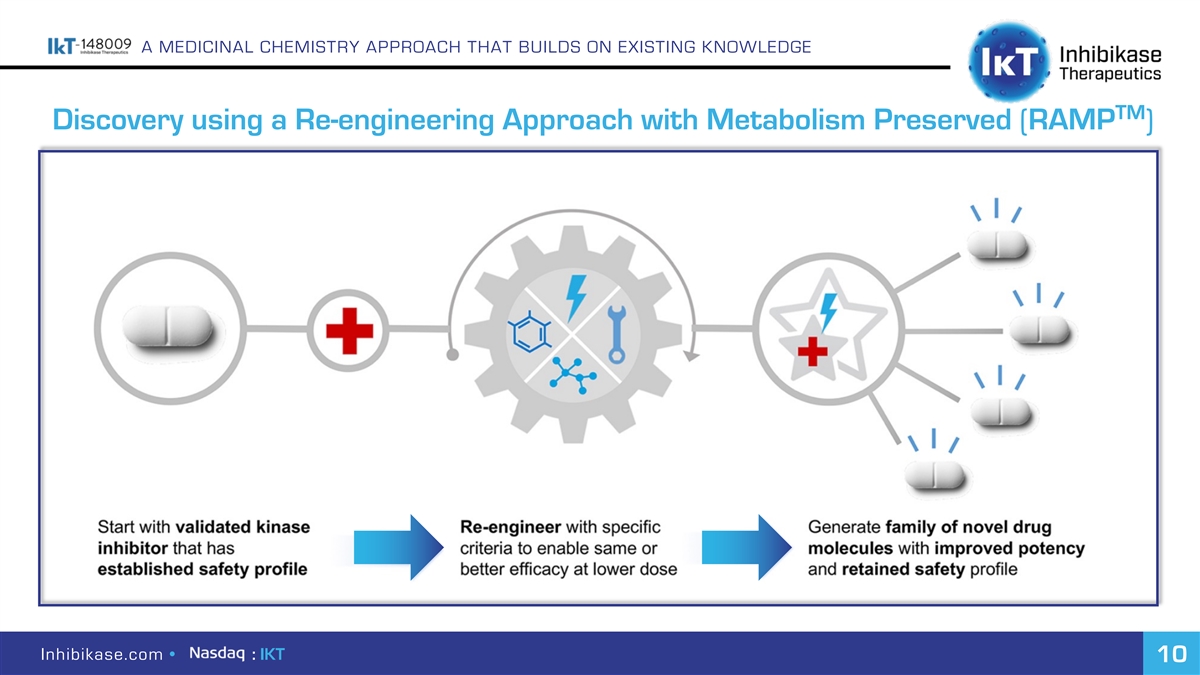
建立在現有知識基礎上的藥物化學方法TM 使用代謝保留(RAMP)Inhibikase.com·:IKT 10的重新工程方法發現

是一種小分子c-abl抑制劑IKT-148009,毒性低,選擇性強,腦滲透劑1c-Abl抑制劑在臨牀開發中的毒理學人類等量劑量伊馬替尼達沙替尼IKT-148009心血管無120腎無肝無100骨髓無· 選擇性80胸骨抑制劑無c-abl和載脂蛋白2/Arg血液無60個PBMCs略有增加·設計抑制中性粒細胞對癌症的毒性40種正常限量藥物對原代20或成熟細胞無細胞毒性在當前持續腦內低或無明顯器官毒性>1微摩爾0知識水平c-ab1 c-abl/Arg c-Kit PDGFRb1第13周和第39周的毒理學數據顯示,IKT-148009·高腦外顯率 抑制這些酶導致的毒性隨着劑量的延長具有更有利的毒性分佈:IKT 11 IC(Nm)50 0.6 48 33 1 41 14 31 5 100 28 72 100 28 72 28 72
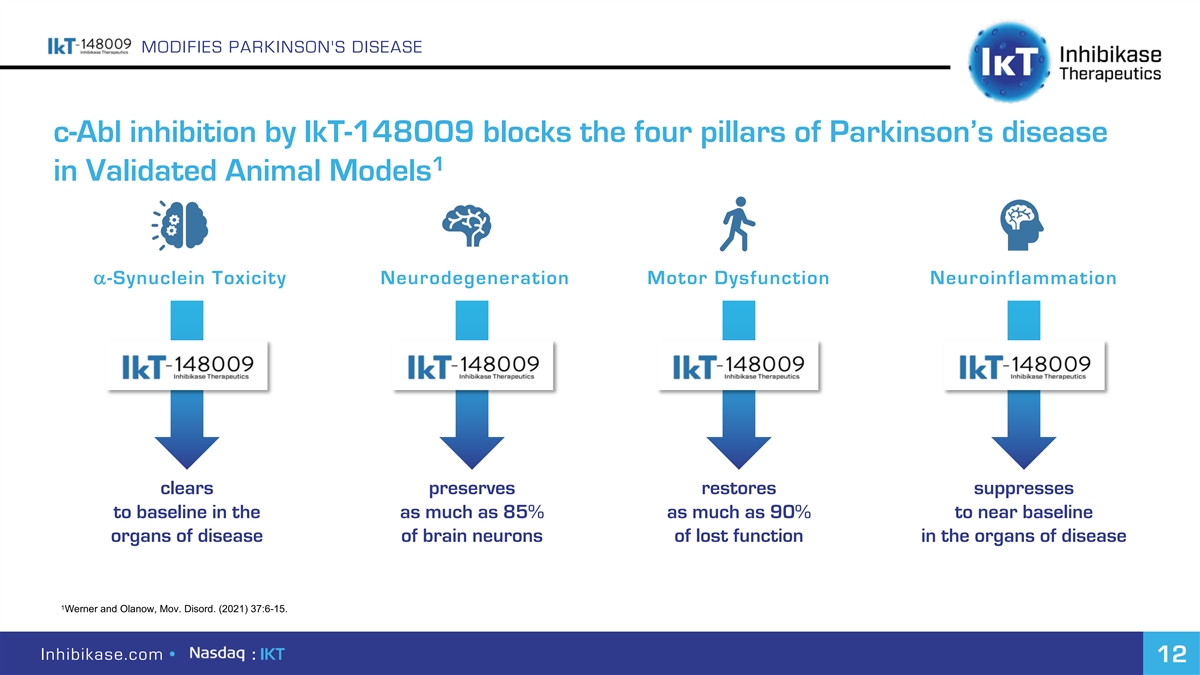
通過IKT-148009修飾帕金森病c-Abl抑制在經過驗證的動物模型中阻斷帕金森病1的四大支柱a-突觸核蛋白毒性神經變性運動功能障礙神經炎症清除保留恢復抑制到基線高達85%到接近基線 疾病器官中喪失功能的腦神經元在沃納和奧蘭諾,Mov的器官中。迪諾德。(2021)37:6-15。Inhibikase.com·:IKT 12

IKT-148009 Inhibikase.com·:iKT的臨牀開發 13

安全和劑量1/1B階段的第一階段試驗:劑量比例 臨牀藥代動力學和無臨牀顯著不良事件健康受試者評估帕金森患者價值類別人口學(佔總數的百分比N=88)(佔總數的百分比,N=13)性別女性34(38.6)6(42.8)男性54(61.4)7(57.2)平均年齡 (SD)57.9(5.72)62.5中位數58.0 62 IKT-148009不在45,69,57,70導致典型的c-Abl種族拉美裔或拉丁裔13(14.8)3(23.1)抑制劑不良事件:非西班牙裔或拉丁裔75(85.2)10(76.9)無GI種族黑人或非洲人 美國人54(61.4)2(15.4)無心血管白種33(37.5)11(84.6)無血液學其他1(1.1)0(0)不良反應7(7.9),所有臨牀意義不大5(38.5)Inhibikase.com

安全性和劑量方面的第一階段試驗第一階段:劑量比例臨牀 藥代動力學和沒有臨牀顯著不良事件IKT-148009-SAD Cmax AUC線性(Cmax)線性(Auc)200000 R²=0.9977 6000 180000 R²=0.9905 160000 5,000 140000臨牀4000藥代動力學120000 100000 3000低劑量口服劑量120000 100000 3000高暴露劑量;線性劑量2000年比例高達175 mg。60000次暴露於75 mg IKT-40000 148009相當於1000 1 20000 500 mg伊馬替尼治療劑量範圍1 00 FDA摘要 批准數據21-335 0 20 40 60 100 120 140 160 180口服劑量(Mg)Inhibikase.com·:IKT 15平均Cmax(Ng)平均AUC0-∞(ng-h/mL

評估帕金森氏症患者安全性的1B期試驗:1B期:與具有相似T和1/2暴露(C和AUC)的老年健康受試者相似的患者的藥物動力學。最大0-inf§PD評估未顯示疾病惡化Inhibikase.com·:IKT 16
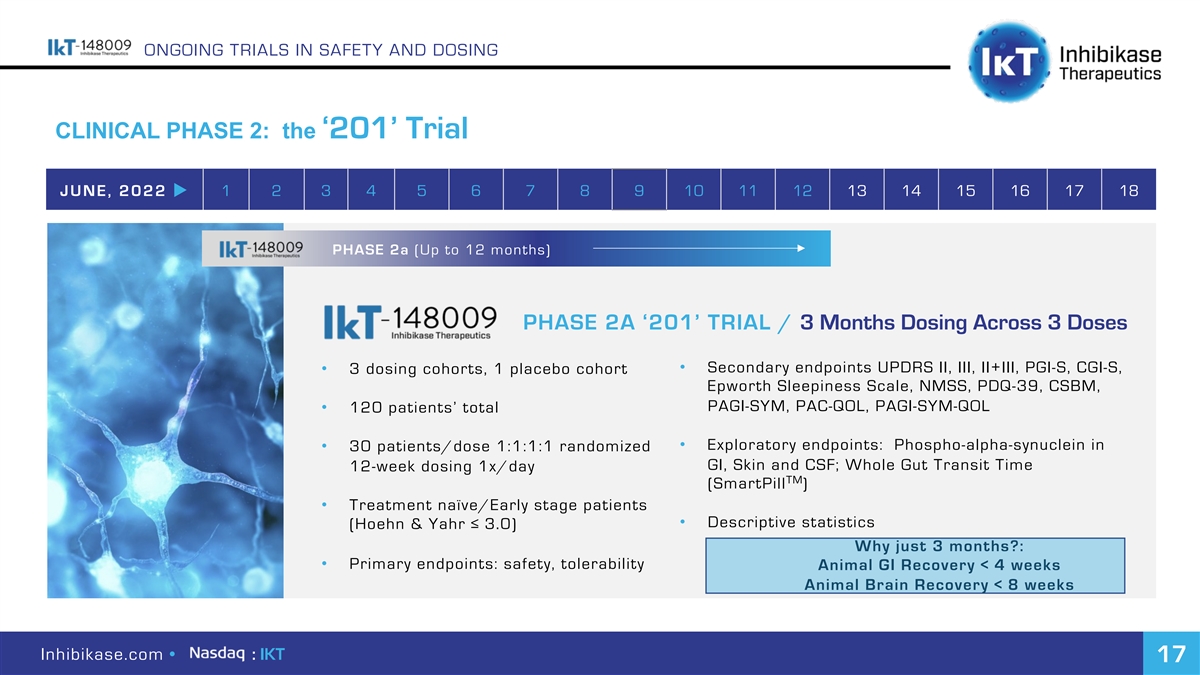
正在進行的安全性和劑量臨牀試驗第二階段:2022年6月1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18階段2a(長達12個月)進行中的‘201’試驗/3個月劑量·次級終點UPDR II、III、II+III、PGI-S、CGI-S、·3個劑量隊列、1個安慰劑隊列、Epworth嗜睡量表、NMSS、PDQ-39、CSBM、PAGI-SYM、PAC-QOL、PAGI-SYM-QOL·120例患者的總·探索終點:30例·磷酸-α-突觸核蛋白/劑量1:1:1:1隨機分為胃腸道、皮膚和腦脊液;全腸道轉運時間12周1次/天TM(智能避孕藥)·治療幼稚/早期患者·描述性統計(Hoehn&Yahr≤3.0)為什麼只有3個月?:·主要終點:安全, 耐受性動物GI恢復
穩定期慢性粒細胞白血病市場及策略 Inhibikase.com·:IKT 18
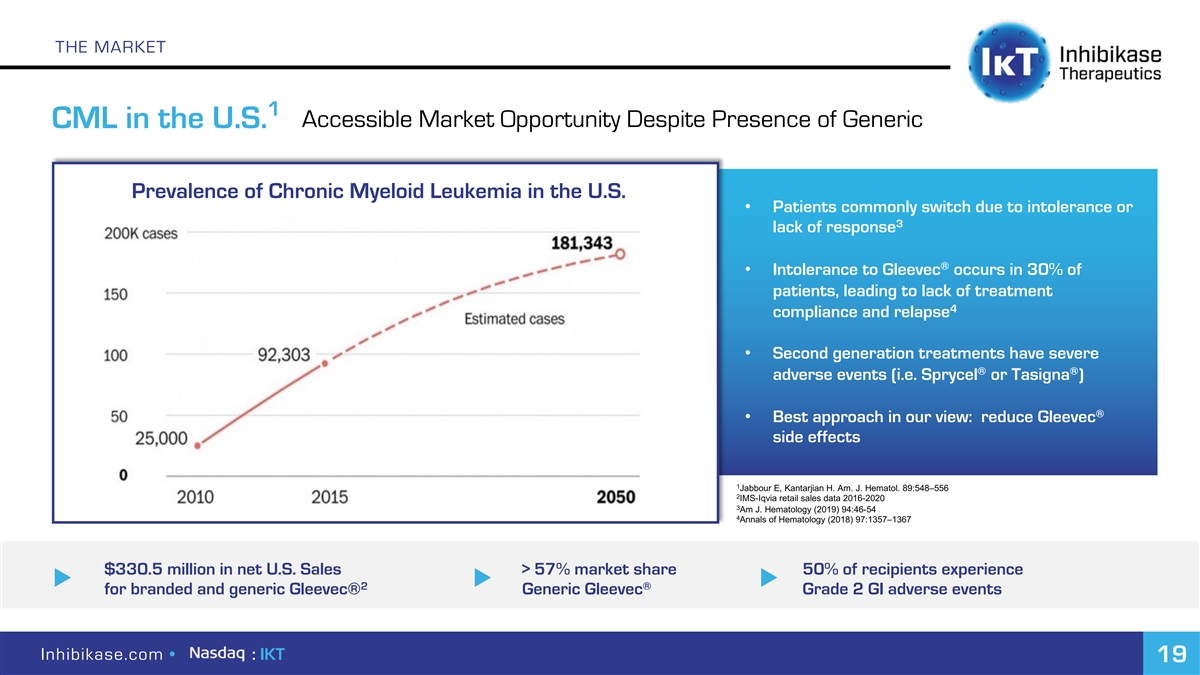
市場1可進入的市場機會,儘管美國存在非專利CML 慢性粒細胞白血病在美國的流行率·患者通常由於不耐受或3缺乏反應而轉而使用®·30%的患者對格列衞不耐受,導致缺乏治療依從性 並復發·第二代治療有嚴重的®®不良事件(即Sprycel或Tasigna)®·我們認為的最佳方法:減少格列衞副作用1 Jabbour E,Kantarkin H.AmJ.血醇。血液學年鑑(2019)94:46-54 4美國血液學年鑑(2018)97:13 57-13 67美國淨銷售額3.305億美元>57%市場份額50%的接受者經歷了品牌和仿製藥的u 2® 格列衞®通用Gleevec 2級GI不良事件Inhibikase.com
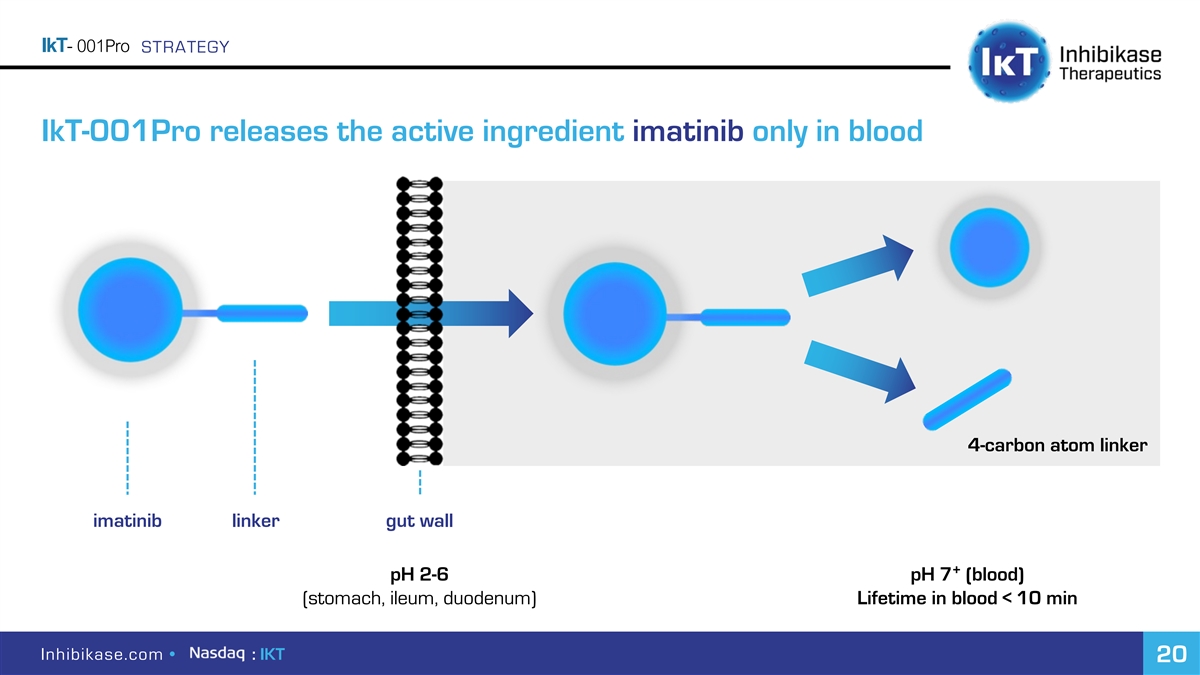
IKT-001Pro策略IKT-001Pro僅在血液中釋放活性成分伊馬替尼 4碳原子接頭伊馬替尼接頭腸壁+pH 2-6 pH 7(血液)(胃、迴腸、十二指腸)在血液中的壽命

IKT-001Pro是一種小分子bcr-abl抑制劑IKT-001Pro:® 替代普通格列衞的胃腸道毒性較低的IKT-001Pro在非人類靈長類動物中的測試結果表明:沒有不良事件水平Cmax Tmax AUC0-T(mg/kg)ü實現劑量彈性,(Mean,ng/mL)(Mean,h)(Mean,h)Ng-h/mL)NOAEL 包括由於AEs較低而使用較高劑量的Imatinib 176/206 4/3 1540/1960 15 1(第91天)(男/女)(男/女)ü抑制胃腸道感染和其他與依從性相關的不良反應IKT-001Pro 400/318 5.3/3.75220/3890 75事件(第28天)(男/女)1 FDA 供批准的彙總數據21-335▲▲無不良事件3倍3倍增加暴露劑量更高劑量的伊馬替尼作為001Pro Inhibikase.com·:IKT 21

IKT-001Pro的生物等效性和優越性臨牀開發試驗2022年6月1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18生物等效性IKT-001Pro(最長3個月)單劑兩部分生物等效性試驗·第1部分:3個劑量隊列,10名受試者每人發現劑量相當於400毫克甲磺酸伊馬替尼IKT-001Pro,測量96小時藥代動力學生物等效性·第2部分:在32名受試者中進行驗證性單劑量測量,證實96小時藥代動力學‘501’試驗·將根據 505(B)(2)法規在NDA路徑上與FDA磋商,遵循CML IKT-001Pro中501試驗優於護理標準的501試驗優勢·等待名單交叉設計,比較001Pro和400 mg伊馬替尼6個月·98名患者服用1x/天計劃·主要 終點是患者報告的胃腸道紊亂和腹瀉頻率的結果衡量指標。·計劃根據505(B)(2)法規Inhibikase.com. :IKT 22進行與追求保密協議同時進行的‘502’審判

Inh Hiib BIIK ka中的精選股票和財務數據作為Se E.C.co om m·::IKT 23 23

表2022年6月30日未償還普通股25,227,051流動資產:期權(WAEP:2.25)4,238,056現金$32,212,276認股權證(WAEP:5.21)1,561,913應收贈款$6,552完全稀釋 未償還的30,622,020股研究和開發$919,053美元IPO前的非稀釋授予收入(NIH,DoD,州政府)預付費用和其他811,482美元流動資產總流動資產33,949,363總流動負債$4,490,305營運資金29,459,058美國財政部持有的賬户中可用的主動贈款資金314,228美元營運資本總額29,773,286 Inhibikase.com

公司重點介紹即將到來的里程碑:2022年第三季度IKT-001Pro· 第一個在IKT-148009 2a期研究中的隨機患者·開始生物等效性臨牀研究·在治療樸素帕金森患者後開始生物等效性臨牀研究·FDA對IND的審查或研究的接收可能繼續進行·設計PK橋研究以 評估字母IKT-148009的藥片配方和食物對PD患者PK的影響·設計和開發優勢研究·完成IKT-001Pro相對於CML的兩個動物模型驗證研究中的第一個·IKT-148009在MSA中完成商業開發工作·在美國為MSA的IKT-148009文件IND;在美國尋求孤兒合作藥物指定·開始表徵新化合物作為 IKT-148009 Inhibikase.com·:IKT 25的後續產品

關於在藥物開發和商業化方面擁有豐富經驗的美國高管管理團隊 米爾頓·沃納、約瑟夫·弗拉塔羅利博士、註冊會計師C.沃倫·奧蘭諾醫學博士、總裁&首席財務官、CLINTREX臨時首席醫療官兼首席執行官。此前,沃納博士曾擔任弗拉塔羅利先生的董事 凱爾塔羅利先生是Celaxsys認證的公共研究人員。從1996年9月至2007年6月擔任Henry P.and Georgette Goldschmidt教授和2007年6月董事長之前,Werner博士一直擔任Henry P.and Georgette Goldschmidt教授和2007年6月董事長一職,在處理上市公司文件和西奈山醫學院神經病學系方面具有豐富的經驗。在加入西奈山分子生物學實驗室之前,他曾在麥吉爾大學、杜克大學和紐約市洛克菲勒大學分子生物物理系任職。在整個公司中。此前,他向南佛羅裏達州首席執行官提供了。他是運動障礙協會的前總裁,國際運動障礙協會的前總裁,美國運動障礙協會的前財務主管。他的科學生涯,一直是神經病學協會的財務主管和諮詢服務。他曾在Michael J.Fox的創新者執行委員會任職,該委員會整合了化學、物理和生物學幾個新興的生物製藥和基金會科學顧問委員會,他是科學委員會的前主席,並與巴赫曼-施特勞斯·帕金森基金會和Dystonia in Medicine的顧問委員會一起,致力於全面解決醫療器械公司的問題。沃納博士是《責任包括資本基金會》一書的作者或合著者。奧蘭諾博士是《運動障礙》雜誌的前聯合主編。70多篇研究文章、評論, Olanow博士在多倫多大學獲得醫學學位,完成了他的章節,並在哥倫比亞長老會醫療工作的紐約神經學研究所向神經學培訓過渡的私人公司的研究中發表了演講。成為公開交易的美國證券交易委員會註冊商。 哥倫比亞大學中心,並在哥倫比亞大學進行神經解剖學研究生學習,撰寫了600多篇神經退行性疾病領域的文章。Inhibikase.com·:IKT 26
關於美國/董事會丹尼斯·伯曼先生羅伊·弗里曼博士,醫學博士保羅·格林特,醫學博士伊麗莎白·奧法雷爾·聯合創始人、董事會成員和/或·哈佛大學神經病學教授·20年以上生物製藥經驗和·25年在禮來公司工作,是許多私立 醫學院和小分子研究與公司董事的種子投資者,最後擔任自主和外圍設備開發的首席生物技術和技術中心,包括成功的公司採購官和領導者,在公共共享服務全球負責人的審批和商業化部門中,已有5人神經紊亂。貝絲以色列女執事神經學,·曾在禮來公司擔任高級管理人員 ·目前擔任醫學中心免疫學和腫瘤治療學總裁,包括高級副總裁,政策莫利諾風險投資公司董事會·前世界地區主席。和金融;高級副總裁,諮詢和風險投資公司,神經學研究聯合會·董事,安培製藥金融;首席財務官,禮來公司,自主神經和Synedgen聯合創始人兼執行副總裁。美國;企業發展系統首席財務官禮來公司總裁,曾在加拿大擔任高級管理職務的·總裁;以及總審計師。在託卡根之前。美國自主學會和Cerexa,森林實驗室, 加入禮來公司,·種子投資人,輝瑞公司的種子投資人,聯合創始人和/或前董事長,PDL BioPharma的IDEC·董事,Intervu的Geron董事會成員,Kintera,美國藥物學會分部,以及先靈公司和LENSAR Inc.,gensia, 卡拉布裏亞神經科。犁公司。·會計學學士,榮譽和·Autonomic主編·皇家學院MBA管理信息研究員 神經科學:印第安納大學的基礎、臨牀和病理學家以及醫學學位體系。在聖巴塞洛繆醫院疼痛雜誌:倫敦大學臨牀學院的《臨牀》的編輯委員會上。 更新,和臨牀自主研究。·在疼痛和神經退行性疾病領域的幾家公司的連續創始人,並是許多大小製藥和生物技術公司的科學顧問委員會成員。Inhibikase.com ·:IKT 27

美國/業界領先的顧問瓦琳娜·道森博士,醫學博士卡爾·基伯茨,公共衞生碩士羅伯特·豪澤,醫學博士神經變性和幹細胞計劃,細胞研究所羅伯特·J·喬因特神經病學教授,工程大學神經病學系神經病學高級副院長和生理學臨牀研究,董事,南佛羅裏達大學醫學院臨牀與翻譯科學學院,約翰霍普金斯大學醫學院研究所,人類實驗治療中心創始人董事美國帕金森氏症和(CHET)-羅切斯特大學醫學中心運動障礙研究中心總裁博士,醫學博士,醫學博士FRCPC Henry P.和Georgette Goldschmidt教授兼主席Jeffrey Kordower,西奈山醫學院榮譽博士Jay Pasricha,MBBS,MD榮休,創建董事ASU-Banner神經退行性疾病首席執行官,Clintrex研究公司董事,約翰霍普金斯大學神經胃腸病研究中心(NDRC)醫學教授Charlene和J.Orin Edson在生命科學生物設計研究所授予董事傑出教授,亞利桑那州立大學神經退行性疾病研究所教授Ken Marek總裁和高級科學家Ted Dawson博士,MD,神經退行性疾病和幹細胞方案博士,細胞工程研究所神經、生理、藥理學、幹細胞系和分子科學-約翰霍普金斯大學醫學院Inhibikase.com·:IKT 28

喬治亞州Riverwood Parkway Suite1900 Atlanta,GA 30339,Massachusetts Office 1 Cranberry Hill Suite 200 Lexington,MA 02421 Inhibikase.com