
2022年第二季度財務結果和公司更新2022年8月8日附件99.2

本演示文稿包含經修訂的1995年《私人證券訴訟改革法案》所定義的前瞻性陳述,包括但不限於以下陳述:我們與新冠肺炎疫苗銷售相關的預期收入和淨利潤,在獲得完全或有條件營銷授權的情況下,被批准在我們合作伙伴控制的地區使用,特別是那些根據我們合作伙伴提供的初步估計得出的數字;我們在向各國政府首次銷售新冠肺炎疫苗後,與政府當局、私人健康保險公司和其他第三方付款人進行的定價和承保範圍談判;未來對新冠肺炎疫苗初始劑量或增強劑量的商業需求和醫療需求;來自其他新冠肺炎疫苗的競爭或與我們其他候選產品有關的競爭,包括那些具有不同作用機制和不同製造和分銷限制的產品,其基礎是療效、成本、儲存和分銷的便利性、批准的用途範圍、副作用概況和免疫反應的持久性;我們的新冠肺炎疫苗以及如果獲得批准的研究藥物被市場接受的速度和程度;我們研究和開發計劃的啟動、時間、進度、結果和成本,包括與新冠肺炎疫苗的其他配方有關的計劃,以及我們當前和未來的臨牀前研究和臨牀試驗,包括關於研究或試驗和相關準備工作開始和完成時間的聲明, 試驗結果公佈的期間以及我們的研發計劃;我們獲得和維持對我們的候選產品進行監管批准的時間和能力;BNT162b2預防由新出現的病毒變異引起的新冠肺炎的能力;我們和我們的交易對手管理和採購必要的能源資源的能力;我們發現研究機會和發現和開發研究藥物的能力;我們的第三方合作者繼續進行與我們的開發候選藥物和研究藥物相關的研發活動的能力和意願;新冠肺炎大流行對我們的發展計劃、供應鏈、合作者和財務業績的影響;由於使用我們的新冠肺炎疫苗和其他由我們開發或製造的產品和候選產品而導致的不可預見的安全問題和索賠;我們推進瘧疾、結核病和艾滋病毒計劃的能力,包括為這些計劃選擇臨牀候選人的時間和臨牀試驗的開始時間,以及任何數據讀數;世界衞生組織、歐盟委員會和其他組織支持的性質和持續時間,以及建立基礎設施的情況;在非洲大陸(包括我們的BioNTainers)開發可持續的疫苗生產和供應解決方案的情況,以及這些解決方案的性質和可行性;我們對研發收入、商業收入、銷售成本、研發費用、銷售和營銷費用、一般和行政費用、資本支出、所得税、流通股的估計;如果獲得批准,我們和我們的合作伙伴將我們的候選產品商業化和營銷的能力, 包括我們的新冠肺炎疫苗;我們管理我們開發和擴張的能力;美國和外國的監管發展;我們有效地擴大我們的生產能力和生產產品的能力,包括我們的新冠肺炎疫苗的目標生產水平和候選產品;以及其他我們目前未知的因素。在某些情況下,前瞻性表述可以通過“將”、“可能”、“應該”、“預期”、“打算”、“計劃”、“目標”、“預期”、“相信”、“估計”、“預測”、“潛在”、“繼續”或這些術語的否定或其他類似術語來識別,儘管並不是所有的前瞻性表述都包含這些詞語。本演示文稿中的前瞻性陳述既不是承諾,也不是保證,您不應過度依賴這些前瞻性陳述,因為它們涉及已知和未知的風險、不確定性和其他因素,其中許多因素不在BioNTech的控制範圍之內,可能導致實際結果與這些前瞻性陳述中明示或暗示的結果大不相同。你應該在我們截至2022年6月30日的三個月的季度報告中以及在生物技術公司提交給美國證券交易委員會的後續文件中(這些文件可在美國證券交易委員會的網站https://www.sec.gov/.上獲得)中審查在“風險因素”標題下描述的風險和不確定因素除法律另有規定外,在出現新信息、未來發展或其他情況時,BioNTech對更新或修改本演示文稿中包含的任何前瞻性陳述不承擔任何意圖或責任。這些前瞻性陳述是基於BioNTech目前的預期,僅代表截至本文發佈之日的情況。本幻燈片演示文稿包括前瞻性陳述2

COMIRATY®▼(輝瑞-生物科技新冠肺炎疫苗)已獲得歐盟委員會的有條件營銷授權,可以預防5歲以下人羣的冠狀病毒病2019年(新冠肺炎)。該疫苗以兩劑為一系列,間隔3周接種。此外,CMA已擴大到包括18歲及以上個人在第二次接種後至少6個月的加強劑量(第三次接種)。對於免疫功能低下的人,第三次接種可能在第二次接種後至少28天給予。歐洲藥品管理局的人類藥物委員會已經完成了對COMIRATY®的嚴格評估,一致認為關於疫苗質量、安全性和有效性的足夠有力的數據現在已經可用。重要安全信息:·已報告過敏反應事件。在接種疫苗後出現過敏反應的情況下,應隨時提供適當的治療和監督。·在接種Comirnaty疫苗後觀察到非常罕見的心肌炎和心包炎病例。這些病例主要發生在接種疫苗後14天內,更多發生在第二次接種之後,更多發生在年輕男子身上。現有數據表明,接種疫苗後的心肌炎和心包炎的病程與一般的心肌炎或心包炎沒有什麼不同。·與焦慮有關的反應,包括血管迷走神經反應(暈厥)、過度換氣或與壓力有關的反應(如頭暈、心悸、心率加快、血壓改變, 刺痛感和出汗)可能與接種過程本身有關。與壓力相關的反應是暫時的,並自行解決。應建議個人將症狀提請疫苗接種提供者進行評估。重要的是要採取預防措施,避免因暈倒而受傷。·疫苗的有效性、安全性和免疫原性尚未在包括接受免疫抑制治療在內的免疫功能受損的個人身上進行評估。在免疫抑制的個體中,COMIRATY®的療效可能較低。·與任何疫苗一樣,使用COMIRATY®接種疫苗可能不會保護所有疫苗接受者。個人可能要在第二次接種疫苗後7天才能獲得完全保護。·在臨牀研究中,16歲及以上參與者的不良反應為注射部位疼痛(>80%)、疲勞(>60%)、頭痛(>50%)、肌肉疼痛和寒戰(>30%)、關節痛(>20%)、發熱和注射部位腫脹(>10%),通常是輕度或中度,並在接種疫苗後幾天內消失。較低的反應性事件發生頻率與較大的年齡相關。·COMIRATY®在5至15歲參與者中的總體安全概況與16歲及以上參與者中看到的相似。·5至11歲兒童最常見的不良反應是注射部位疼痛(>80%)、疲勞(>50%)、頭痛(>30%)、注射部位紅腫(>20%)、肌肉疼痛和寒戰(>10%)。·12至15歲的臨牀試驗參與者最常見的不良反應是注射部位疼痛(>90%)、疲勞和頭痛(>70%)、肌肉痛和寒戰(>40%), 關節痛、發熱(>20%)。·在孕婦中使用COMIRATY®的經驗有限。只有在對母親和胎兒的潛在益處超過任何潛在風險的情況下,才應考慮在懷孕期間使用COMIRNatY®。·尚不清楚COMIRATY®是否會從母乳中排泄出來。·尚未研究與其他醫藥產品的相互作用或與其他疫苗同時使用COMIRATY®的情況。·有關COMIRATY®安全性的完整信息,請始終參考EMA網站上以歐盟所有語言提供的經批准的產品特性摘要和包裝傳單。黑色等邊三角形▼表示需要額外監測以捕獲任何不良反應。這將允許快速識別新的安全信息。個人可以通過報告他們可能獲得的任何副作用來提供幫助。副作用可以報告給EudraVigilance,或通過電子郵件Medinfo@biontech.de、電話+49 6131 9084 0或通過網站www.biontech.de安全信息3直接向BioNTech報告。

安全信息授權在美國使用·新冠肺炎疫苗是美國食品和藥物管理局批准的新冠肺炎疫苗,用於主動免疫,以預防由嚴重急性呼吸綜合徵冠狀病毒2(SARS-CoV-2)引起的12歲及12歲以上個人患上2019年冠狀病毒病(新冠肺炎)。根據歐盟法案,它還被授權向6個月至4歲的個人提供3劑初級系列,向5歲及5歲以上的個人提供2劑初級系列,向已被確定患有某種免疫損害的5歲及5歲以上的個人提供第三次初級系列劑量,向5歲至11歲及以上已完成輝瑞-生物科技新冠肺炎疫苗或COMIRNAY®初級系列接種的個人提供單劑加強劑,向12歲及12歲以上的具有某些免疫損害的個人提供第三次初級系列劑量。為12歲及以上完成輝瑞-生物科技新冠肺炎疫苗或COMIRATY®初級系列接種的個人提供第一劑加強疫苗,為18歲及以上使用不同授權新冠肺炎疫苗完成初步接種的個人提供第一劑加強劑, 第二次加強接種對象為50歲及以上已接種任何授權新冠肺炎疫苗第一劑加強接種的個人;第二次加強接種對象為12歲及以上已確定患有某些免疫損害並已接種第一劑授權新冠肺炎疫苗的個人。加強劑時間表基於用於初級系列的疫苗的標籤信息。重要安全信息個人不應接種以下情況:·在前一劑疫苗後出現嚴重過敏反應·對該疫苗的任何成分有嚴重過敏反應個人應將其所有醫療狀況告知疫苗接種提供者,包括如果他們:·有任何過敏·有心肌炎(心肌炎症)或心包炎(心臟外膜炎症)·發燒·有出血障礙或正在服用血液稀釋劑·免疫功能受損或正在服用影響免疫系統的藥物·懷孕,計劃懷孕,或者正在哺乳·接種了另一種新冠肺炎疫苗·曾因注射而暈倒疫苗可能並不能保護所有人。據報道,疫苗的副作用包括:·疫苗引起嚴重過敏反應的可能性很小,嚴重過敏反應通常在接種疫苗後幾分鐘至1小時內發生。因此,疫苗接種提供者可能會要求個人在接種疫苗後留在接種疫苗的地方進行監測。嚴重過敏反應的跡象可能包括呼吸困難、面部和喉嚨腫脹、心跳加快、全身出現嚴重皮疹、頭暈和虛弱。, 他們應該撥打911或去最近的醫院4

·一些接種疫苗的人發生心肌炎(心肌炎)和心包炎(心臟外襯裏的炎症),40歲以下的男性比女性和老年男性更常見。在這些人中,大多數人在接種第二劑疫苗後幾天內開始出現症狀。發生這種情況的可能性非常低。個別人士在接種疫苗後如有下列任何病徵,應立即求醫:o胸痛o呼吸急促o感覺心跳急促、撲騰, O嚴重的過敏反應;非嚴重的過敏反應,如注射部位疼痛;疲倦;頭痛;肌肉疼痛;寒戰;關節疼痛;發燒;注射部位腫脹;注射部位發紅;噁心;感覺不適;淋巴結腫大(淋巴結病);食慾減退;腹瀉;嘔吐;手臂疼痛;以及與注射疫苗相關的暈厥·這些可能不是疫苗接種的全部副作用。可能會出現嚴重的、意想不到的副作用。疫苗可能的副作用仍在臨牀試驗中研究。致電疫苗接種提供商或醫療保健提供商,瞭解令人煩惱的副作用或副作用不會消失,因為其他疫苗尚未提交給FDA,因此有關接種該疫苗的數據尚未提交給FDA。考慮與其他疫苗一起接種這種疫苗的個人應該與他們的醫療保健提供者討論他們的選擇。患者應該總是向他們的醫療保健提供者尋求關於不良事件的醫療建議。鼓勵個人向美國食品和藥物管理局(FDA)和疾病控制和預防中心(CDC)報告疫苗的負面副作用。請訪問https://www.vaers.hhs.gov或致電1-800-822-7967。此外,副作用可報告給輝瑞公司,網址為www.pfizerSafetyreport。或致電1-800-438-1985。5安全資訊

公司展望Ryan Richardson,首席戰略官Jens Holstein財務業績,CFO管道更新Özlem Türeci,CMO 2022年第二季度亮點Ugur Sahin,CEO 6
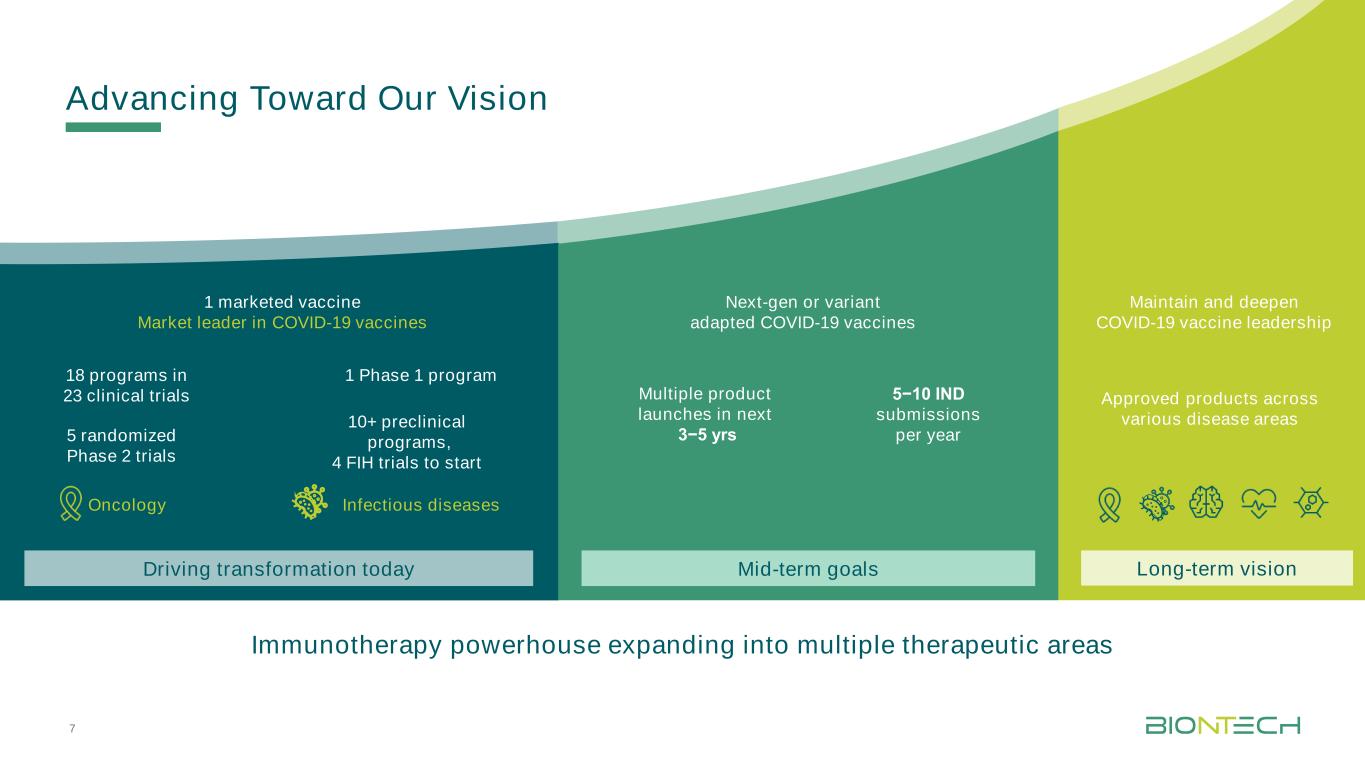
邁向我們的願景腫瘤學傳染病5隨機第二階段試驗1上市疫苗市場領先者新冠肺炎疫苗10+臨牀前計劃,4項FIH試驗將啟動1階段1計劃23項臨牀試驗中的18項計劃保持並深化新冠肺炎疫苗的領先地位未來3−5年中期目標推動轉型今天推動轉型長期願景5−每年10次提交新一代或變種新冠肺炎疫苗批准的產品跨不同疾病領域免疫治療強者擴展到多個治療領域7

第二季度的亮點:企業和腫瘤學流水線·報告的第二季度總收入為3.2BN1歐元,今年迄今的收入為9.6BN1歐元·開始在非洲建設第一個BioNTainer mRNA疫苗製造設施·與Genmab簽署新的等額成本/利潤合作協議,共同開發針對CD27的抗體·BNT122(INeST):胰腺癌切除患者的第一階段試驗的陽性數據顯示良好的安全性和令人鼓舞的臨牀活動跡象2·BNT116(FixVac):晚期NSCLC的FPD處於第一階段試驗·BNT142(Ribomab):FPD處於第一階段試驗在CLDN6陽性實體腫瘤·BNT211(CLDN6 CAR-T細胞療法):用於第三或更晚一線治療睾丸癌的EMA優先藥物(PRIME)公司更新腫瘤學:Produced Advantage 1 BioNTech的利潤份額是根據輝瑞公司和BioNTech公司共享的初步數據估計的,在截至12月31日的Form 20-F年度報告中進一步描述,2021年以及截至2022年6月30日的三個月和六個月的季度報告,作為BioNTech於2022年8月8日提交的當前Form 6-K報告的證物。協作合作伙伴毛利潤的估計份額的任何變化都將被前瞻性地確認。2調查員發起的試驗8

第二季度亮點:新冠肺炎疫苗/COMIRNAY·FDA批准EUA用於6個月至4歲兒童的初級系列,並用於5至11歲兒童的加強劑量,兒科標籤現在包括1:·6個月。至
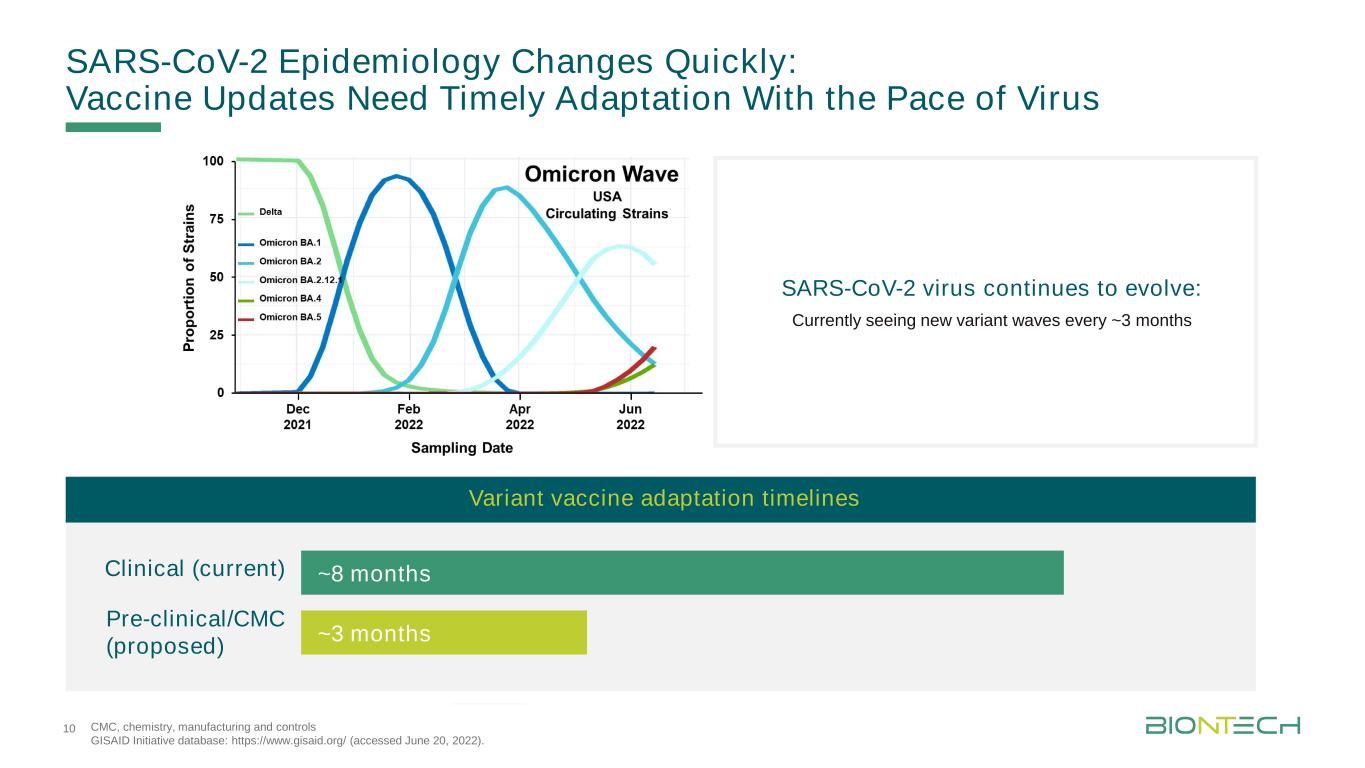
SARS-CoV-2流行病學變化迅速:疫苗更新需要及時適應病毒CMC、化學、製造和控制的步伐。GISAID倡議數據庫:https://www.gisaid.org/(2022年6月20日訪問)。~8個月~3個月臨牀(當前)臨牀前/CMC(建議)變異疫苗適應時間表SARS-CoV-2病毒繼續演變:目前每~3個月出現新的變異浪潮10

FDA、EMA和其他監管機構建議在全球範圍內為BA.1和BA.4/5適應二價疫苗提交正在進行的奧密克戎適應二價疫苗提交·FDA:為編碼奧密克戎BA.4/5刺突蛋白的二價疫苗提供指導·EMA:奧密克戎BA.1適應二價疫苗提交最終完成;準備提交奧密克戎BA.4/5二價疫苗的臨牀前和CMC數據包為2022年10月初推出奧密克戎二價疫苗做準備CMC、化學、製造和控制第一批發貨量預計最早將於10月獲得監管部門的批准計劃啟動·奧密克戎BA.4/5二價疫苗的臨牀試驗預計將於8月啟動·BA.1-和BA.4/5-二價疫苗生產已啟動·計劃在秋季助推活動之前及時供應這兩種疫苗監管參與臨牀開發生產規模擴大11

公司展望首席戰略官Ryan Richardson 04 03財務業績Jens Holstein,CFO管道更新Özlem Türeci,CMO 01 2022年第二季度亮點Ugur Sahin,CEO 12
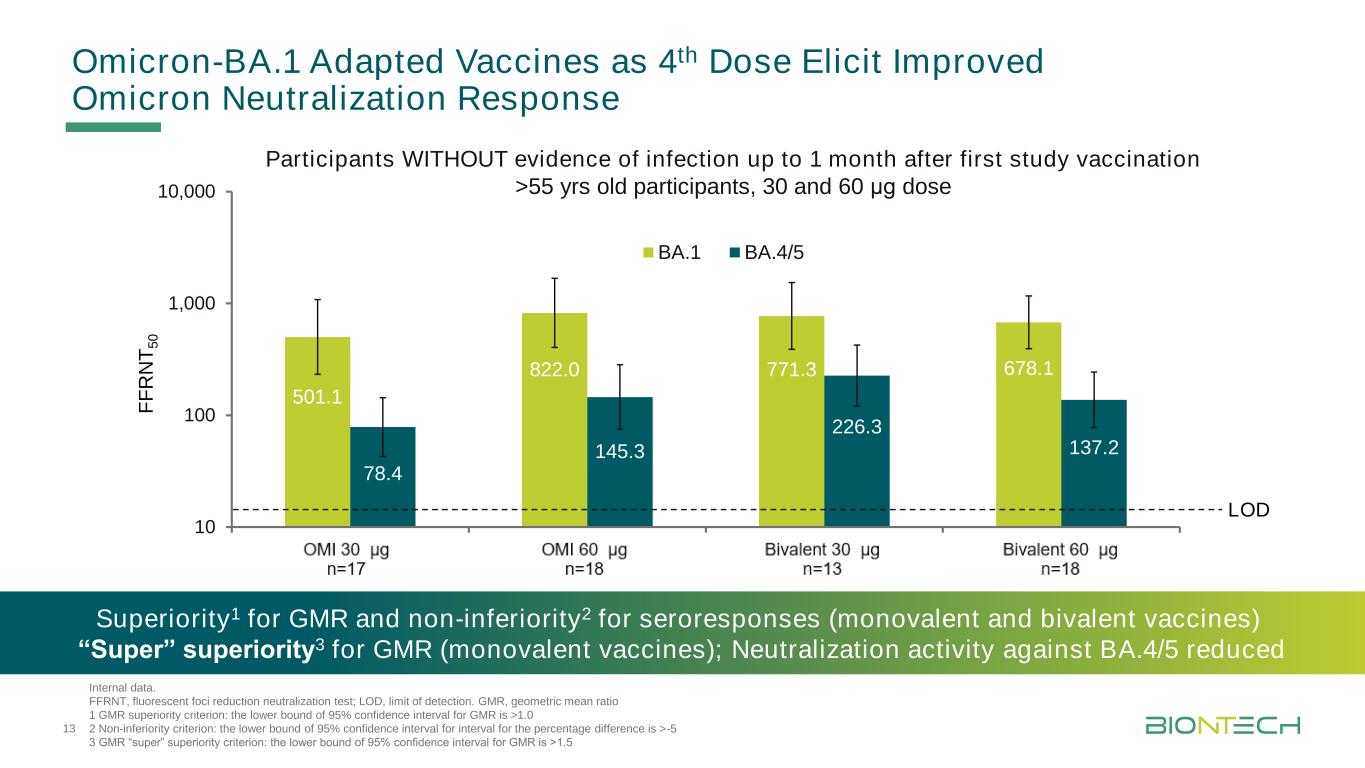
F F R N T 5 0 501.1 822.0 771.3 678.1 78.4 145.3 226.3 137.2 10 100 1,000,000 OMI 30μg…Omi 60μg…二價30μg…二價60μg…BA.1 BA.4/5 LOD奧密克戎-BA.1適應疫苗第4劑誘導改善奧密克戎中和反應內部數據。FRNT,熒光減灶中和試驗;LOD,檢出限。GMR,幾何平均比率1 GMR優勢標準:GMR的95%可信區間下限>1.0 2非劣勢標準:百分比差異區間的95%可信區間下限>-5 3 GMR“超級”優勢標準:首次研究接種後1個月內無感染證據的GMR的95%可信區間下限>1.5>55歲的參與者,30和60μg劑量13優勢1,血清應答(單價和雙價疫苗)“超”優勢2 GMR(單價和雙價疫苗)“超級”優勢3
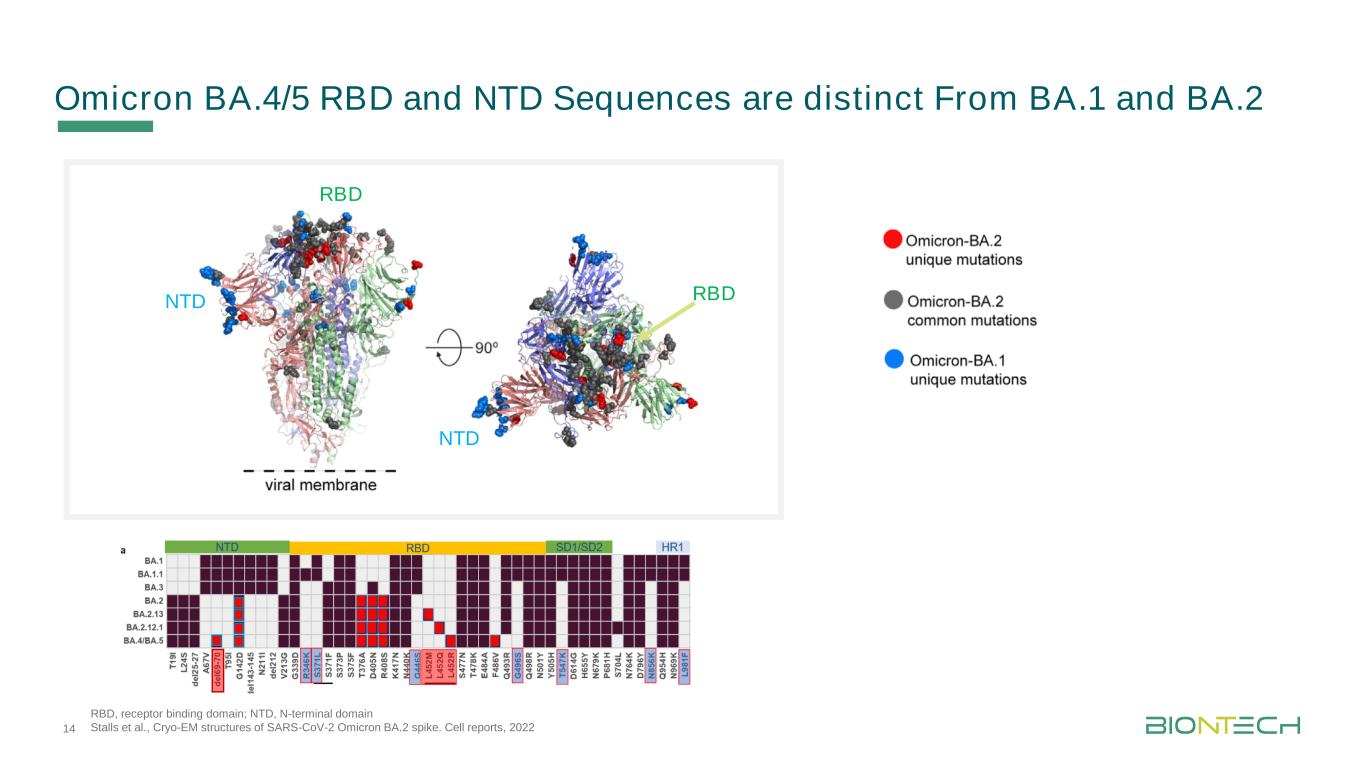
NTD RBDNTD RBD奧密克戎BA.4/5 RBD和NTD序列不同於BA.1和BA.2的14個RBD受體結合域,NTD,N-末端結構域STALS等,以及SARS-CoV-2奧密克戎BA.2棘突的冷凍-EM結構。《2022年細胞報告》
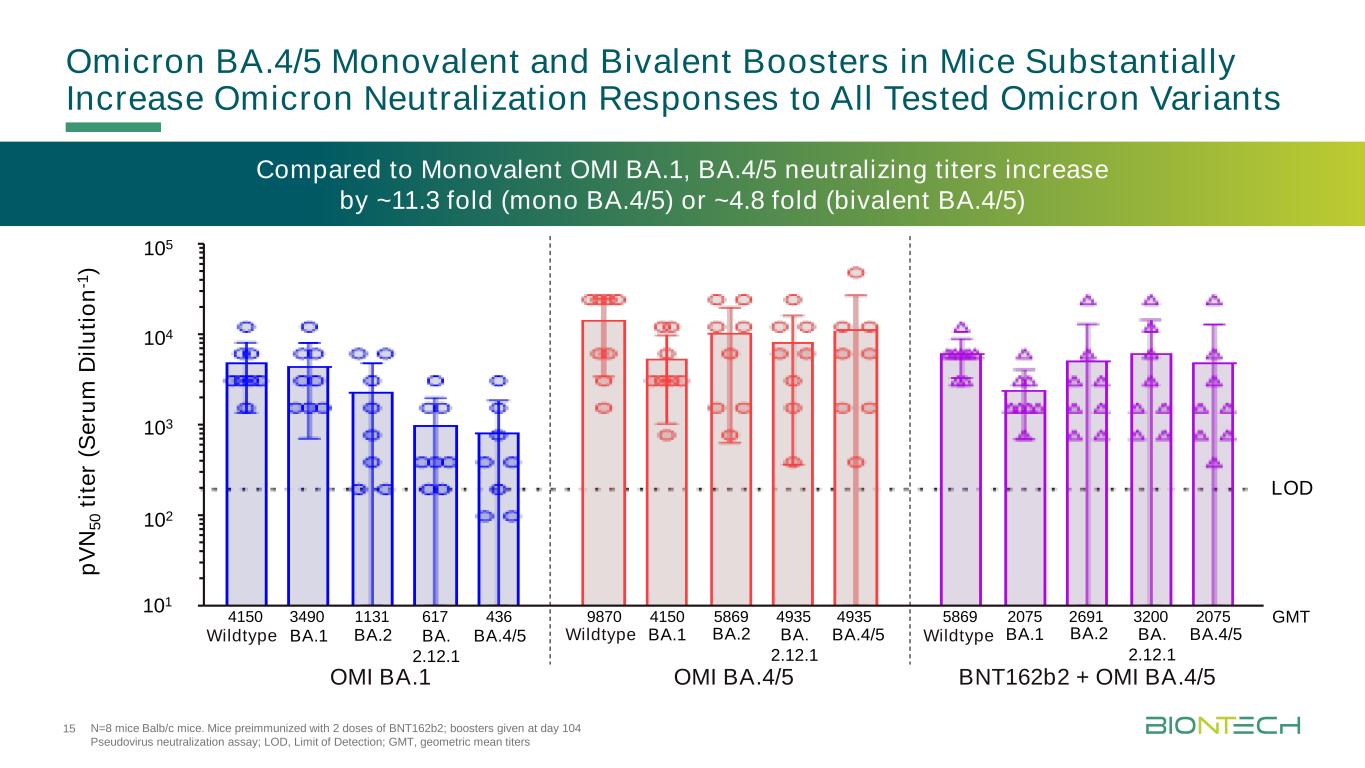
與單價OMI BA.1相比,BA.4/5中和效價增加了~11.3倍(單價BA.4/5)或~4.8倍(二價BA.4/5)OMI BA.1 OMI BA.1 OMI BA.4/5 BNT162b2+OMI BA.4/5 101 102 103 105 p V N 5 0 te r(S e ru m D il u ti o n-1)武漢BA.1 BA.2 BA。2.12.1BA.4/5 LOD 4150 436 9870 4935 5869 2075GMT3490 4150 20751131 617 5869 4935 2691 3200 N=8只Balb/c小鼠。用2劑BNT162b2預免疫小鼠;第104天給予加強免疫;假病毒中和試驗;LOD,檢測限;GMT,武漢BA.1 BA2 BA幾何平均滴度。2.12.1 BA.4/5武漢BA.1 BA.2 BA2.12.1BA.4/5野生型野生型15

尋求多種新的新冠肺炎疫苗方法,提供持久和高水平的保護,對抗不斷演變的變種T細胞增強型疫苗候選設計,旨在刺激和增強T細胞免疫泛SARS-CoV-2疫苗候選潛力更大,更持久的保護以管理未來令人擔憂的變異臨牀試驗開始預計2022年下半年:下一代疫苗接近為優化免疫原性而設計的下一代SARS-CoV-2尖峯抗原·提高預輸血穩定性·暴露更多中和敏感表位BNT162b5:二價疫苗候選增強的SARS-CoV-2祖先株和奧密克戎BA2亞型第二階段:7月份的FPD長期戰略包括多管齊下設計和測試多種結構,目的是接觸免疫系統的不同部分,包括抗體和T細胞-概念驗證試驗預計2H 2022年16

SMIM,小分子免疫調節劑。1名研究人員發起的第1階段試驗;2名與Genentech合作;3名與賽諾菲合作;4名與Genmab合作。腫瘤方面的重大進展和擴展2022藥物類別平臺候選產品適應症(目標)臨牀前1期2期3期里程碑mRNA修復Vac BNT111晚期和R/R黑色素瘤BNT112前列腺癌BNT113 HPV16+頭頸癌BNT1151卵巢癌BNT116 NSCLC FPD 2022年7月iNeST Autogene cevumeran(BNT122)2 1L黑色素瘤數據更新:1H 2023輔助直腸癌實體瘤輔助胰腺導管腺癌1(BNT131)3實體瘤(IL-12sc,IL15-sushi,GM-CSF,GM-CSF)2022年1月的FPD BNT142多實體腫瘤(CD3×CLDN6)2022年7月的FPD核細胞因子BNT151多實體腫瘤(優化的IL-2)BNT152,BNT153多實體腫瘤(IL-7,IL-2)細胞治療CAR T細胞+CARVac BNT211多實體腫瘤(CLDN6)數據更新:2H 2022 BNT212胰腺,α其他腫瘤(CLDN18.2)基於新抗原的T細胞BNT221(NEO-PTC-01)多實體腫瘤TCR工程T細胞將被選為所有腫瘤抗體下一代免疫檢查點調節劑GEN1046(BNT311)4轉移性非小細胞肺癌(PD-L1×4-1BB)多實體腫瘤(PD-L1×4-1BB)GEN1042(BNT312)4多實體腫瘤(CD40×4-1BB)GEN1053(BNT313)4惡性實體腫瘤(CD27)啟動階段:2H 2022靶向腫瘤抗體BNT321(MVT-5873)胰腺癌(SLEA)SMTL樣受體結合BNT411實體瘤(TLR7)✓✓17✓
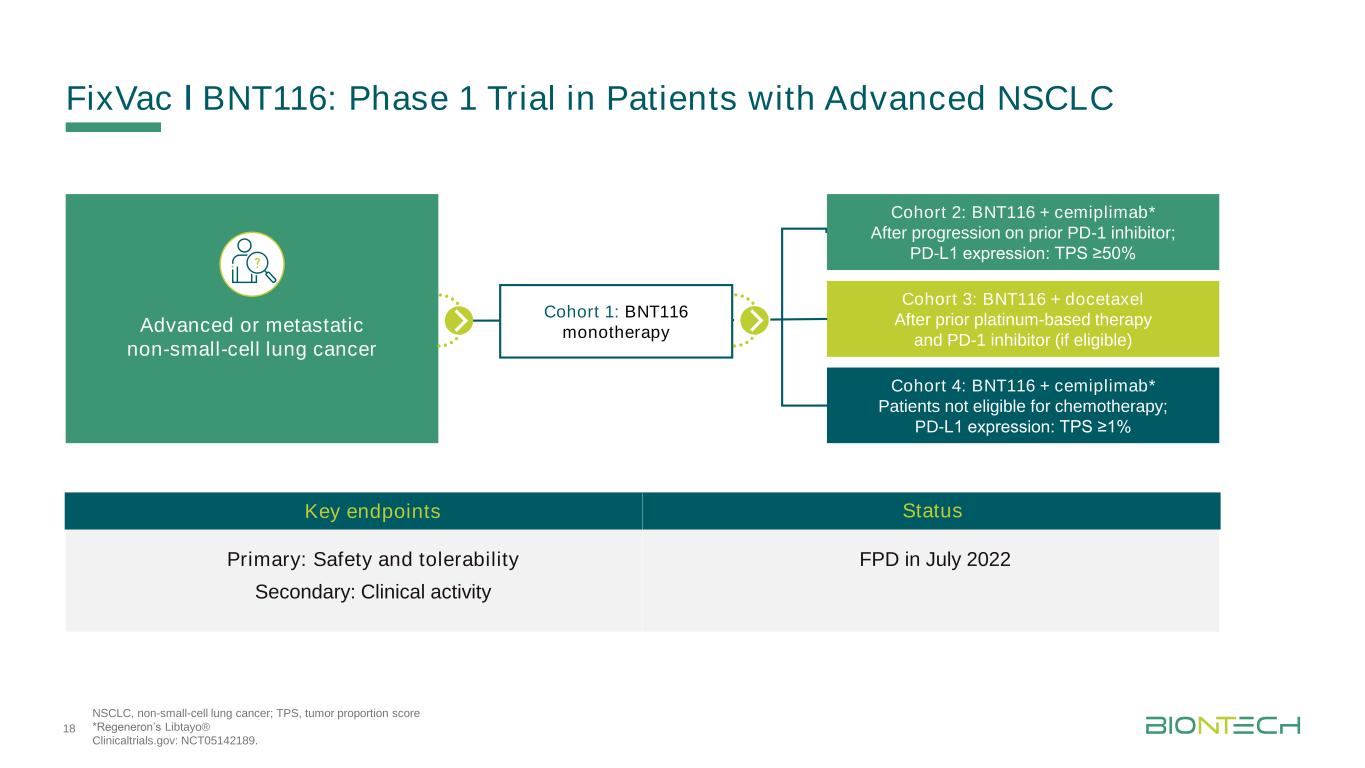
修復Vac非小細胞肺癌BNT116:晚期非小細胞肺癌患者的1期試驗;TPS,腫瘤比例評分*Regeneron的Libtayo®ǀ臨牀試驗。2022年7月晚期或轉移性非小細胞肺癌:安全性和耐受性繼發:臨牀活動隊列2:BNT116+西米普利單抗*在使用PD-1抑制劑後進展;PD-L1表達:Tps≥50%隊列4:BNT116+西米普單抗*不符合化療條件的患者;PD-L1表達:Tps≥1%隊列1:BNT116單一治療隊列3:BNT116+多西紫杉醇在之前基於鉑的治療和PD-1抑制劑(如果符合條件)後
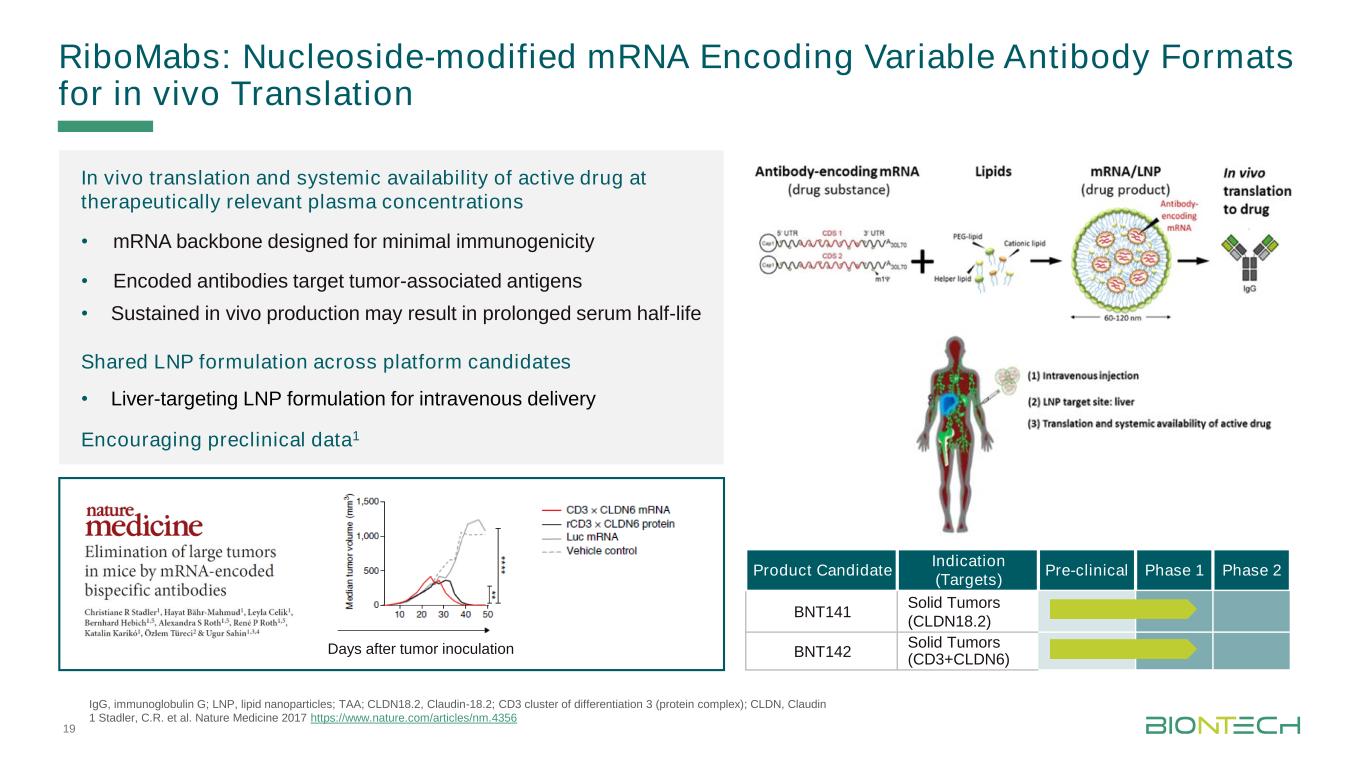
Ticelmaster Format Durch Klken BearbeitenRiboMabs:核苷修飾的mRNA編碼可變抗體格式在體內翻譯和有效藥物在治療相關血漿濃度的系統可利用性·為最低免疫原性設計的mRNA主幹·編碼的抗體針對腫瘤相關抗原·體內持續生產可能導致延長血清半衰期共享跨平臺候選LNP配方·肝臟靶向LNP配方用於靜脈注射鼓勵臨牀前數據1免疫球蛋白G;LNP,脂質納米顆粒;TAA;CLDN18.2,Claudin-18.2;CD3分化簇3(蛋白質複合體);CLDN,Claudin 1 Stadler,C.R.等人。自然醫學2017年https://www.nature.com/articles/nm.4356產品候選適應症(目標)臨牀前1期2 BNT141實體瘤(CLDN18.2)BNT142實體瘤(CD3+CLDN6)腫瘤接種後19天
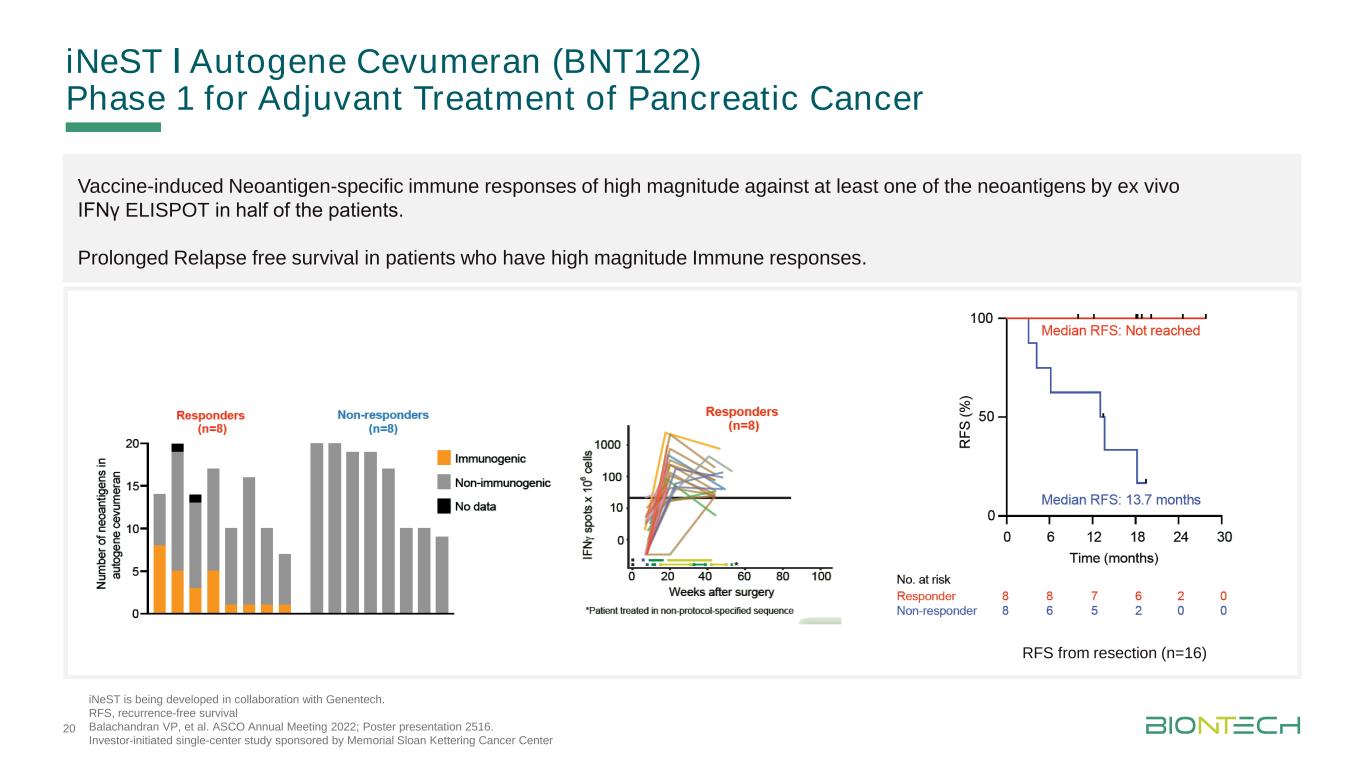
INeSTǀ自體基因Cevumeran(BNT122)用於胰腺癌輔助治療的第一階段正在與基因技術公司合作開發。RFS,無復發生存期,Balachandran VP,等。2022年ASCO年會;海報展示2516。投資者發起的單中心研究,由紀念斯隆-凱特琳癌症中心切除(n=16)疫苗通過體外幹擾素γELISPOT在半數患者體內誘導針對至少一種新抗原的高強度的新抗原特異性免疫反應。免疫反應強度高的患者的無復發生存期延長。20個
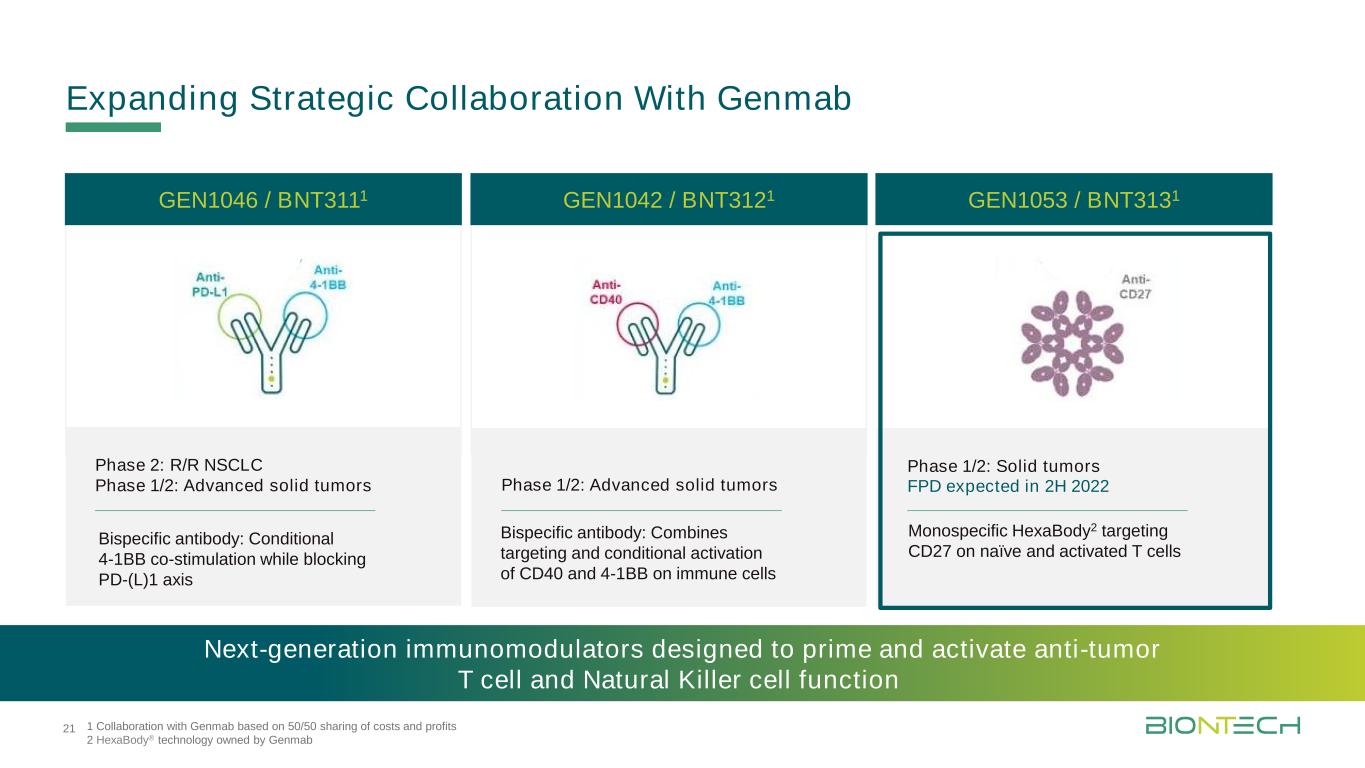
擴大與Genmab的戰略合作1在成本和利潤各佔一半的基礎上與Genmab合作2由Genmab下一代免疫調節劑擁有的HexaBody®技術旨在啟動和激活抗腫瘤T細胞和自然殺傷細胞功能1/2階段:晚期實體腫瘤GEN1042/BNT3121階段2:R/R非小細胞肺癌階段1/2:晚期實體腫瘤GEN1046/BNT3111階段1/2:實體腫瘤FPD預計在2022年下半年GEN1053/BNT3131雙特異性抗體:有條件的4-1BB共刺激同時阻斷PD-(L)1雙特異性抗體:結合靶向和有條件激活CD40和4-雙特異性抗體針對幼稚和活化T細胞21上的CD27的免疫細胞上的單特異性HexaBody2

公司展望首席戰略官Ryan Richardson 04財務業績Jens Holstein,CFO 02管道更新Özlem Türeci,CMO 01 2022年第二季度亮點Ugur Sahin,CEO 22
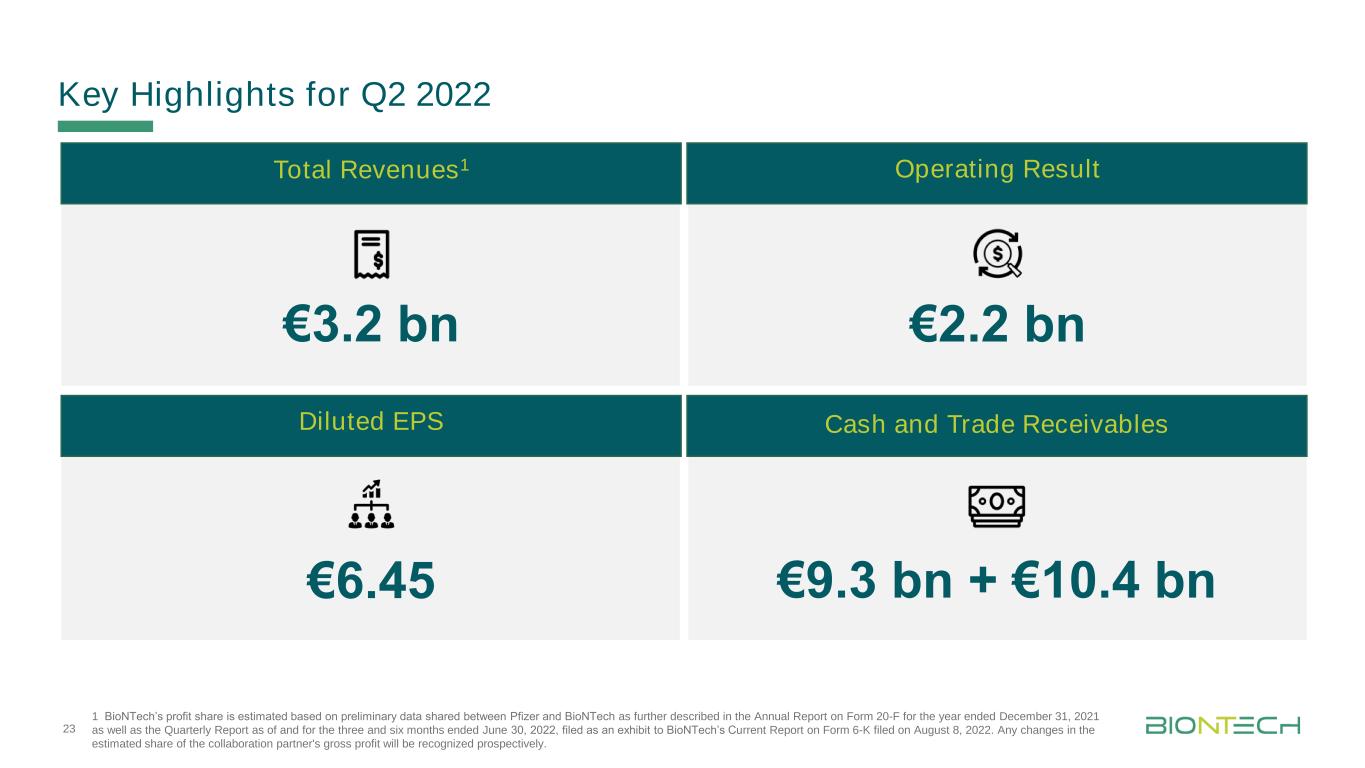
歐元32億歐元22億歐元93億歐元+104億歐元1 BioNTech的利潤份額是根據輝瑞和BioNTech共享的初步數據估計的,具體描述見截至2021年12月31日的Form 20-F年度報告以及截至2022年6月30日的三個月和六個月的季度報告,這些報告作為BioNTech於2022年8月8日提交的當前Form 6-K報告的證物。協作合作伙伴毛利潤的估計份額的任何變化都將被前瞻性地確認。2022年第二季度總收入1營業業績攤薄每股現金和應收貿易賬款6.45歐元23
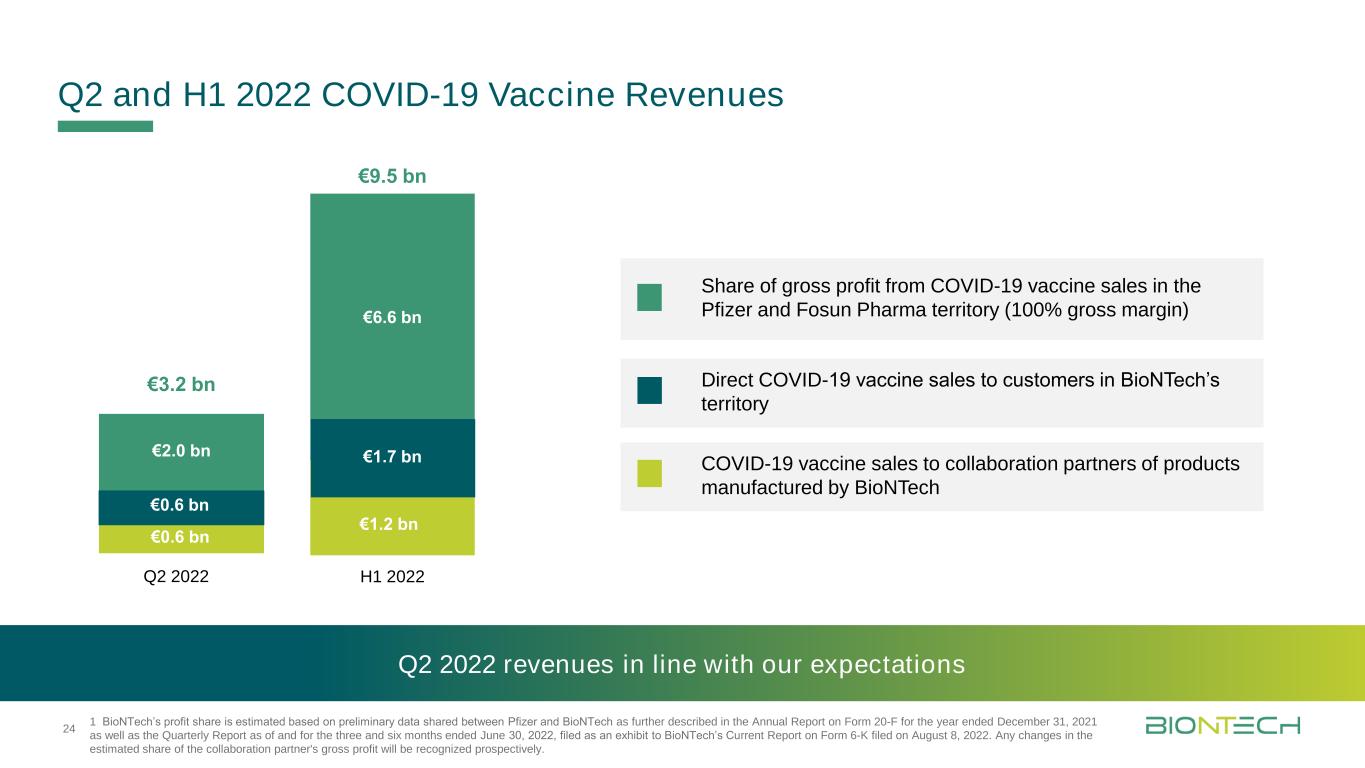
2022年第二季度和上半年新冠肺炎疫苗收入1 BioNTech的利潤份額是根據輝瑞與BioNTech共享的初步數據估計的,具體描述見截至2021年12月31日的Form 20-F年度報告以及截至2022年6月30日的三個月和六個月的季度報告,這些報告作為BioNTech於2022年8月8日提交的當前Form 6-K報告的證物。協作合作伙伴毛利潤的估計份額的任何變化都將被前瞻性地確認。2022年第2季度收入符合我們的預期2022年第2季度收入32億歐元6億歐元95億歐元2022年上半年66億歐元66億歐元17億歐元12億24新冠肺炎直接銷售疫苗在輝瑞和復星國際製藥地區的毛利潤份額新冠肺炎疫苗銷售給合作伙伴生物科技公司生產的產品
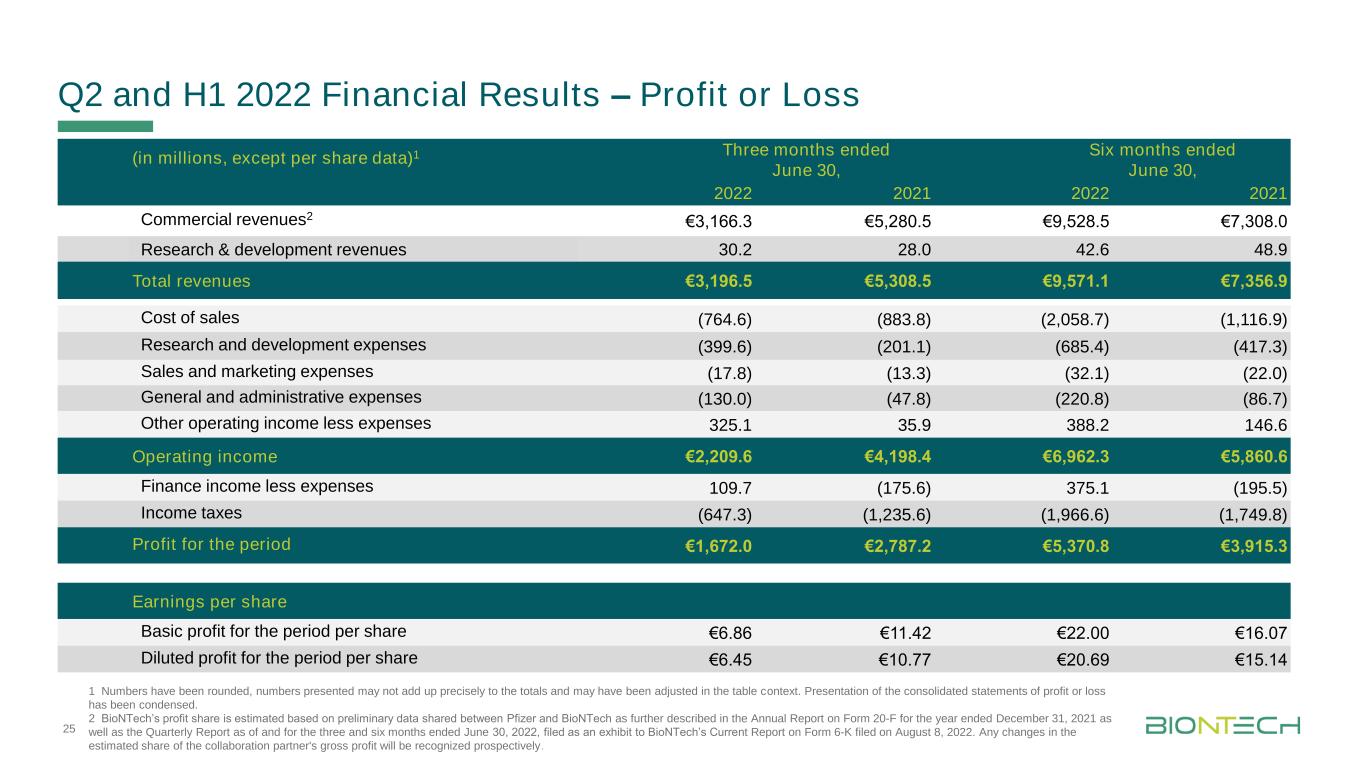
2022年第二季度和上半年財務業績-利潤或虧損(百萬美元,每股數據除外)1截至6月30日的三個月,截至6月30日的六個月,商業收入2歐元3,166.3歐元5,280.5歐元9,528.5歐元7,308.0研發收入30.2 28.0 42.6 48.9總收入3,196.5歐元5,308.5歐元9,571.1歐元7,356.9銷售成本(764.6)(883.8)(2,058.7)(1,116.9)研發費用(399.6)(201.1)(685.4)(417.3)銷售和營銷費用(17.8)其他營業收入減去支出325.1 35.9 388.2 146.6營業收入歐元2,209.6歐元4 198.4歐元6,962.3歐元5,860.6財務收入減去支出109.7(175.6)375.1(195.5)所得税(647.3)(1,235.6)(1,966.6)(1,749.8)該期間的利潤歐元1,672.0歐元2,787.2歐元5,370.8歐元3,915.3該期間的基本每股利潤歐元6.86歐元11.42歐元22.00歐元16.07稀釋後的每股利潤歐元6.45歐元10.77歐元20.69歐元15.14 1數字已四捨五入,所列數字的總和可能與總數不符,可能已在表格中進行了調整。綜合損益表的列報已精簡。2 BioNTech的利潤份額是根據輝瑞和BioNTech共享的初步數據估計的,在截至2021年12月31日的Form 20-F年度報告以及截至2022年6月30日的三個月和六個月的季度報告中有進一步描述,該季度報告作為BioNTech於2022年8月8日提交的當前Form 6-K報告的證物。協作合作伙伴毛利潤的估計份額的任何變化都將被前瞻性地確認。25個

2022財年指導重申1範圍反映了當前的基本情況預測,不包括額外合作或潛在併購交易造成或推動的潛在影響。2 BioNTech Group估計,由於平均貿易税率下降,年有效所得税税率從2021財年的31.6%降至2022財年的約28%。新冠肺炎疫苗收入20221財年預計生物科技新冠肺炎疫苗收入130億至170億歐元2022年計劃支出和Capex1研發支出1400至15億歐元SG&A支出4.5億至5.5億歐元資本支出4.5億至5.5億歐元2022財年估計税收假設生物科技集團估計年度有效所得税税率~28%2 26

公司展望Ryan Richardson,首席戰略官03財務業績Jens Holstein,CFO 02管道更新Özlem Türeci,CMO 01第二季度2022年第二季度亮點Ugur Sahin,CEO 27

截至2022年7月初全球新冠肺炎疫苗特許經營1的強勁地位和前景2輝瑞和BioNTech運營的市場上2022年1月1日至2022年7月20日疫苗的累計份額,報告的市場份額數據3包括。發達市場(4)和新興市場(阿根廷、智利、厄瓜多爾、香港、尼泊爾、祕魯、南非、烏拉圭)的所有市場4包括美國、歐盟/歐洲經濟區、其他國際發達市場(日本、韓國、瑞士、烏克蘭)5從1月1日開始,此數據集的2022年數據來自2022年第一季度收益報告5等待監管部門批准與輝瑞公司合作分銷新冠病毒-10疫苗自產品推出以來已運往180個國家或地區超過36億劑1自20222年1月以來市場份額增加3:從52%增加到63%·發達市場4:從59%增加到68%2022年訂單:約25億劑·美國政府額外訂購1.05億劑,價值32億美元·再訂購1.95億劑·EC訂單6.5億劑,2022年交付·修改了重新交付的合同2022年第4季度28隨着奧密克戎變異疫苗計劃在秋季晚些時候推出,出貨量預計將增加5

履行提供公平獲得藥品的承諾·端到端信使核糖核酸生產單位,能力高達5000萬劑/年·第一個製造設施成為分散和強大的非洲端到端製造網絡的節點·在盧旺達破土動工後正在建設設施·2020年12月至2022年7月17日期間通過雙邊和捐贈協議為塞內加爾和南非增加潛在地點1通過雙邊和捐贈協議BioNTainer於2022年6月在非洲塞內加爾、盧旺達和南非啟動>15億劑新冠肺炎疫苗運往中低收入國家承諾20億劑在非洲1個潛在的製造地點29

標題母版格式持續Klken Bearbeiten精選2022年流水線里程碑預期計時新冠肺炎疫苗:後續和下一代疫苗奧密克戎BA 4/5改編的二價疫苗試驗開始2022年8月BNT162b5:下一代雙價疫苗,編碼祖先和BA2的增強型SARS-CoV-2刺突抗原第二階段:FPD 2022年7月T細胞增強疫苗試驗開始2022年下半年額外的下一代疫苗試驗開始,包括泛SARS-CoV-2疫苗2H 2022多數據更新2022 4傳染病首例人類試驗開始帶狀皰疹疫苗1 2H 2022 BNT163 HSV2疫苗2H 2022 BNT164結核病疫苗2 2H 2022/2023 BNT165瘧疾疫苗2H 2022/2023年初4腫瘤學首例人類試驗於2022年1月開始BNT141實體腫瘤核單抗(CLDN18.2)FPD實體腫瘤BNT142核單抗(CD3×CLDN6)FPD 2022 BNT116 Vac與Cplimab聯合用於NSCLC FNT313(GEN1053)2022年7月BNT313(GEN1053)INeST聯合pbro治療一線黑色素瘤目前處於2023年上半年BNT211期1/2CAR-T/CLDN6+多發性實體瘤2H 2022✓✓✓HSV2,單純皰疹病毒2型;FPD,首例給藥患者;CLDN,克勞丁;非小細胞肺癌,非小細胞肺癌1與輝瑞合作;2與輝瑞合作;3與Genmab合作4與基因泰克✓30合作
展望2022年及以後新冠肺炎疫苗的進一步開發加快晚期腫瘤學計劃推進傳染病投資組合尋求互補性收購改造和擴大全球組織一代人一次的機會改變醫學為患者、股東和社會帶來長期價值31

謝謝你32