目錄表
項目2.管理層對財務狀況和經營成果的討論和分析
您應閲讀以下對我們的財務狀況和經營結果的討論和分析,以及我們的財務報表和本季度報告10-Q表中其他部分包含的相關附註和其他財務信息。除了歷史財務信息外,本討論和分析還包含基於當前預期的涉及風險和不確定性的前瞻性陳述,例如我們的計劃、目標、預期、意圖和信念的陳述。由於各種因素的影響,我們的實際結果可能與這些前瞻性陳述中預期的結果大不相同,其中包括下文第二部分第1A項下題為“風險因素”的章節中所述的那些因素。
概述和管道
我們是一家臨牀階段的基因藥物公司,專注於開發針對中樞神經系統(CNS)疾病的變革性療法,這些疾病的治療方案有限或沒有批准的治療方案。我們的願景是通過開發突破性的療法來改變中樞神經系統疾病患者的生活,最終實現基因療法的承諾。基因醫學領域正在迅速擴大,我們相信,我們有一種差異化的方法來開發中樞神經系統疾病的治療方法,使我們能夠以更高的技術和監管成功概率選擇和推進候選產品。我們已經與賓夕法尼亞大學或賓夕法尼亞大學的基因治療計劃或GTP的受託人進行了戰略研究合作,該計劃由基因藥物領域的領先者詹姆斯·威爾遜博士領導。我們還利用我們與賓夕法尼亞孤兒疾病中心(ODC)的密切合作關係,開發歷史和預期的可比較的自然病史患者檔案,以便與介入試驗的參與者進行比較。通過這一合作,我們彙集了一系列基因藥物候選產品的深度組合,我們保留這些產品的全球權利,其細節如下表所示:
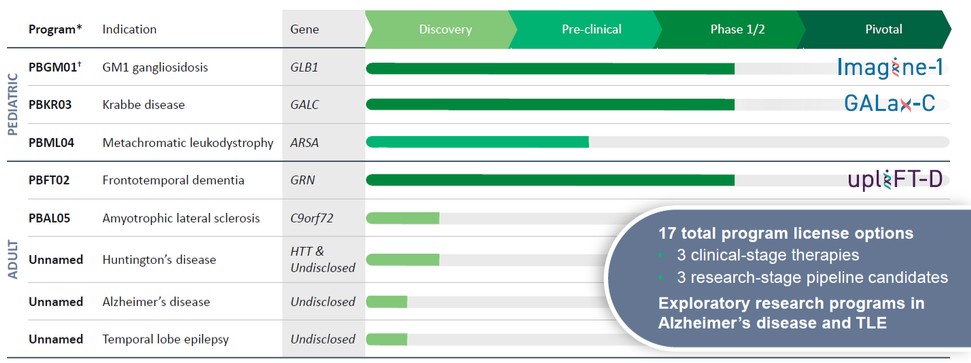
*8個額外的CNS管道許可證選項;之前行使了3個許可證選項,權利隨後歸還給賓夕法尼亞大學。
†計劃包括正在進行的對嬰兒和青少年神經節苷脂沉積症患者的自然病史研究。
23