
展品99.4

Valneva報告2022年第1季度業績並提供公司更新分析師演示文稿2022年5月5日

免責聲明Valneva 2022年第一季度分析師演示文稿2022年5月5日2本演示文稿不包含或構成向美國或任何司法管轄區的任何人發出的購買或認購Valneva SE股票的要約,或該要約或要約對其是非法的。Valneva是一家歐洲公司。發佈的信息受到歐洲與美國不同的披露要求的約束。財務報表和信息可能是根據會計準則編制的,而這些準則可能無法與美國公司普遍使用的會計準則相比較。本演示文稿僅包括截至本演示文稿之日提供的摘要信息,並不自稱是全面的。本演示文稿中的任何信息純屬指示性信息,可隨時修改,恕不另行通知。Valneva不保證本演示文稿中包含的信息或觀點的完整性、準確性或正確性。Valneva或其任何附屬公司、董事、高級管理人員、顧問和員工均無義務更新此類信息,也不對因使用本演示文稿而造成的任何損失承擔任何責任。這些信息未經獨立核實,並受Valneva根據巴黎泛歐交易所和納斯達克全球精選市場上市公司適用的規則、法規和實踐要求公佈的商業、財務和其他信息的完整限定,尤其包括Valneva於2022年3月23日提交給法國金融市場管理局的全球註冊文件和提交給美國的20-F表格中描述的風險因素。S.美國證券交易委員會(美國證券交易委員會),2022年3月24日, 以及任何其他定期報告和任何其他新聞稿中的信息,這些信息可在Valneva的網站(www.Valneva)免費獲得。瓦爾內瓦。Com)和/或AMF(WWW.AMF-法國。Org)和美國證券交易委員會(WWW美國證券交易委員會。Gov)。本報告中包含的某些信息和陳述不是歷史事實,而是前瞻性陳述,包括有關收入指引、進展、時機、候選產品的研究、開發和臨牀試驗的完成結果以及對未來業績的估計的陳述。前瞻性表述(A)基於當前的信念、預期和假設,包括但不限於對當前和未來業務戰略以及Valneva運營環境的假設,涉及已知和未知的風險、不確定性和其他因素,可能導致實際結果、業績或成就與這些前瞻性表述中明示或暗示的結果、業績或成就大不相同,(B)僅在本演示文稿發佈之日發表,(C)僅供説明之用。請投資者注意,前瞻性信息和陳述不是對未來業績的保證,會受到各種風險和不確定因素的影響,其中許多風險和不確定因素很難預測,而且通常不在Valneva的控制範圍之內。

議程Valneva 2022年第1季度分析師演示文稿2022年5月5日3簡介業務更新財務報告2022年第1季度新聞流問答財務展望

▪報告2022年第一季度的總收入為2,180萬歐元來自旅遊市場和第一個新冠肺炎銷售的積極信號截至2022年3月31日的現金狀況為3.113億歐元▪報告2022年第一季度的業績並提供公司最新情況臨牀計劃的出色進展▪萊姆病:報告的進一步積極的第二階段結果,包括第一個兒科數據▪新冠肺炎:MHRA條件營銷授權收到NHRA緊急使用授權,巴林的首個疫苗接種確認EMA滾動審查正在進行▪基孔肯亞:最終積極的關鍵3期結果報告提交前與美國食品和藥物管理局發起的討論首個新冠肺炎疫苗銷售和強勁的現金狀況2022年第1季度Valneva分析師演示文稿2022年5月5日4

議程Valneva 2022年第1季度分析師演示文稿2022年5月5日簡介業務更新財務報告2022年第2季度新聞流問答財務展望

第2階段試驗1、2、3報告陽性結果,包括。第一個兒科數據和助推器反應4;第三階段時間表選擇的多價疫苗(6個血清型)在美國和歐洲幫助預防萊姆病在美國和歐洲獨家全球合作伙伴輝瑞VLA15-多價萊姆病候選疫苗僅適用於高級臨牀開發萊姆病計劃今天1 FDA快速通道指定被授予2 4 5遵循萊姆病疫苗的已證明的作用機制3 Valneva Q1 2022分析師演示文稿2 Valneva宣佈萊姆病候選疫苗第二階段研究的陽性初步結果;2 Valneva宣佈萊姆病候選疫苗第二階段研究的陽性初步結果。3 Valneva和輝瑞報告了萊姆病候選疫苗第二階段的進一步陽性數據;4 Valneva和輝瑞報告了萊姆病候選疫苗的進一步陽性第二階段結果,包括增強反應

VLA15:成人1、2、3、4和兒科參與者的發展進展和展望積極的第二階段結果5報告Valneva Q1 2022分析師演示文稿2022年5月5日第二階段試驗VLA15-221招募了625名隨機參與者,年齡為5至65歲2▪分別於2022年2月3日和4月報告了成人和兒童參與者的強免疫原性5.▪發現,在兒科參與者(5-17歲)中,VLA15的免疫原性比同時接受兩劑或三劑疫苗接種計劃的成年人更強。根據最新的第二階段免疫原性和安全性數據,▪計劃於2022年第三季度開始第三階段臨牀試驗,Valneva和輝瑞公司計劃繼續為成人和兒童參與者進行三劑初級系列疫苗接種計劃5▪臨牀讀數,基於一個滴答季節,預計到2023年底▪將向Valneva支付2500萬美元的里程碑付款,因為Valneva和輝瑞宣佈啟動萊姆病候選疫苗的第二階段研究。,2 Valneva和輝瑞完成萊姆病候選疫苗第二階段試驗的招募;3 Valneva和輝瑞報告萊姆病候選疫苗第二階段進一步陽性數據;4 Valneva和輝瑞報告萊姆病候選疫苗第二階段結果進一步陽性,包括加強反應,5 Valneva和輝瑞報告萊姆病候選疫苗第二階段兒科數據陽性
VLA1553:單針基孔肯雅疫苗候選全球最先進的基孔肯雅疫苗計劃注:圖片來源:詹姆斯·加薩尼。1 Valneva宣佈其單針基孔肯雅候選疫苗的第三階段關鍵結果呈陽性;2 Valneva宣佈其單針基孔肯雅候選疫苗的批次對批次一致性試驗結果呈陽性;3 Valneva宣佈其單針基孔肯雅候選疫苗啟動青少年第三階段試驗;4 Valneva授予食品和藥物管理局對其單針基孔肯雅候選疫苗的突破稱號;5 Valneva授予FDA對基孔肯雅候選疫苗的快速通道稱號;6 https://www.fda.gov/about-fda/中心-藥物評估和研究/熱帶疾病優先審查-代金券計劃;7 Valneva的基孔肯雅候選疫苗獲得EMA優質稱號;8 CHIKV LR2006-OPY1感染性克隆通過刪除編碼NSP3(甲型病毒複製酶)的大部分基因而減弱;9 Valneva與巴坦坦研究所合作為低收入和中等收入國家提供單針基孔肯雅疫苗;10 VacZineAnalytics基孔肯雅病毒疫苗全球需求分析。2020年2月。最終積極的關鍵3期結果1和TOPLINE批量數據2報告;2022年1月啟動的青少年階段3試驗獲得FDA突破性治療4、Fast Track 5和EMA Prime 7稱號;可能有資格獲得優先審查憑單6;FDA預提交過程啟動單針活減毒預防疫苗8針對基孔肯雅病毒中和作用CEPI授予Valneva最高2,340萬美元用於研發;與布坦坦研究所合作開發LMICs 9非常適合現有的商業和製造能力1 2 4 5 3全球市場,包括流行地區, 預計到2032 10 6 Valneva 2022年第1季度分析師演示文稿2022年5月5日

VLA1553:發展展望提交前討論與美國FDA發起的Valneva Q1 2022分析師演示文稿2022年5月5日9 1 Valneva成功完成單針基孔肯雅候選疫苗的關鍵第三階段試驗;2 Valneva宣佈其單針基孔肯雅候選疫苗的批次對批次一致性試驗結果呈陽性;3 Valneva宣佈啟動其單針基孔肯雅候選疫苗的青少年第三階段試驗;第一個也是唯一一個在全球範圍內報告3期陽性結果的項目完成了6個月的隨訪-所有3期免疫原性和安全終點滿足-98.9%的參與者在1個月後出現血清應答,66.3%的參與者在6個月後出現血清應答-良好的安全性和耐受性概況確認了▪陽性的背線批次對批次一致性試驗結果報告(VLA1553-302)2,預計在2022年第二季度進行的最終數據▪抗體持久性後續試驗(VLA1553-303)正在進行:將每年對來自VLA1553-301試驗的375名志願者進行為期5年的跟蹤調查,以支持潛在的標籤擴展,▪青少年階段3試驗於2022年1月啟動由防疫創新聯盟(CEPI)資助3

英國MHRA條件營銷授權2和巴林NHRA緊急使用授權收到3;EMA滾動審查正在進行的2個關鍵階段3試驗顯示出優於阿斯利康的Vaxzevria,並且顯著更有利的耐受性6;陽性topline同源增強數據報告7;實驗室研究中顯示中和奧密克戎和達美航空的變體8 4與歐盟委員會4簽訂的4份預先購買協議,與巴林5 3 VLA2001:新冠肺炎滅活全病毒疫苗候選藥物僅在歐洲的診所滅活新冠肺炎疫苗計劃注:圖片:CDC/Alissa Eckert,MSMI;Dan Higgins,MAM。1 Valneva和Dyavax宣佈其新冠肺炎滅活疫苗和佐劑滅活疫苗的商業供應協議;2 Valneva獲得英國衞生部有條件營銷授權的滅活新冠肺炎疫苗VLA2001;3 Valneva獲得巴林緊急使用授權的滅活新冠肺炎疫苗VLA2001;4 Valneva與歐盟委員會簽署的2001年新冠肺炎滅活疫苗VLA2001採購協議;5 Valneva與巴林簽署預購協議以獲得滅活新冠肺炎佐劑疫苗VLA2001;6 Valneva報告滅活新冠肺炎佐劑候選疫苗VLA2001的第三階段陽性結果;7 Valneva宣佈滅活新冠肺炎候選疫苗VLA2001的陽性同源強化數據, 佐劑新冠肺炎候選疫苗VLA2001--Valneva;8 Valneva的滅活新冠肺炎候選疫苗被證明中和了奧密克戎變體;9 Valneva和IDT Biologika宣佈合作生產滅活新冠肺炎疫苗VLA2001;10基於內部產能和外部/合同製造。建立在Valneva的IXIARO®製造技術和dynavax的CpG1018佐劑1 1的基礎上,利用Valneva在蘇格蘭和瑞典的製造基地;正在擴大產能,包括CMO 9目標>每年1億劑10 6 5正在進行的臨牀試驗,旨在逐步擴大目標產品範圍(標籤)Valneva Q1 2022分析師演示文稿2022年5月5日10
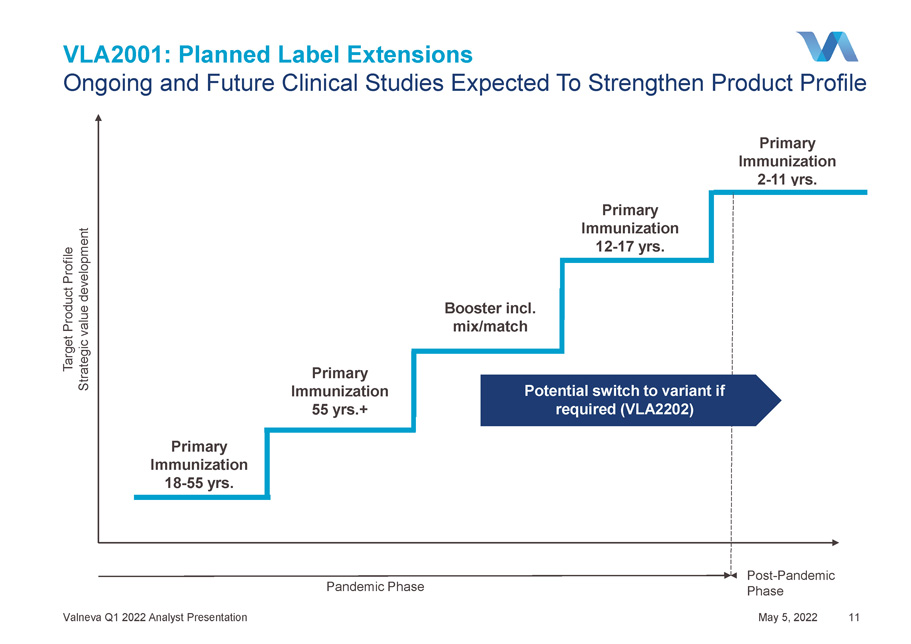
VLA2001年:計劃中的標籤擴展正在進行中,未來的臨牀研究預計將在18-55年內加強初級免疫的產品概況。目標產品簡介、戰略價值開發、大流行階段、大流行後階段、初級免疫接種2-11年。初級免疫12-17年。助推器包括混合/匹配初級免疫接種55年+可能根據需要轉換為變體(VLA2202)Valneva Q1 2022分析師演示文稿2022年5月5日11

議程Valneva 2022年第1季度分析師演示文稿2022年5月5日12簡介業務更新財務報告2022年第2季度新聞流問答財務展望
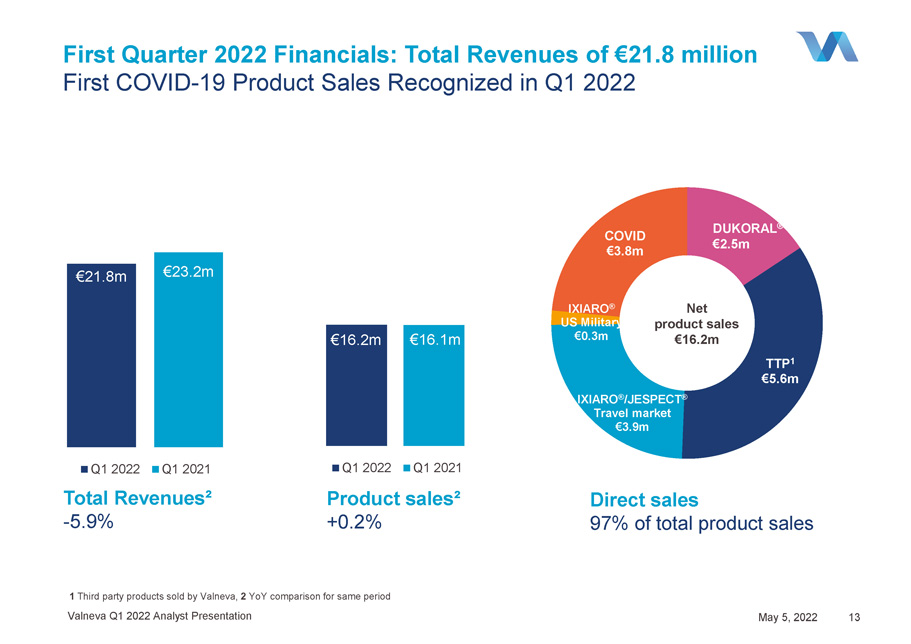
Ixiaro®美國軍方30萬歐元TTP 1歐元560萬歐元Ixiaro®/JESPECT®旅遊市場歐元390萬歐元COVID歐元380萬歐元2022年第一季度財務:總收入2,180萬歐元2022年第一季度確認的第一個新冠肺炎產品銷售杜科拉爾®250萬歐元直接銷售額250萬歐元佔產品總銷售額的97%2同期產品淨銷售額1,620萬歐元2,180萬歐元2,320萬歐元2022年第一季度2,320萬歐元2021年第一季度總收入1-5.9%1,620萬歐元1,610萬歐元2021年第一季度產品銷售額+0.2%Valneva 2022年第1季度分析師演示文稿2022年5月5日13

2022年第一季度財務:私人旅遊市場產品銷售額1620萬歐元,顯示出顯著復甦,Valneva 2022年第一季度分析師演示文稿,5月5日2022年14歐元(未經審計)2022年第一季度2021年第一季度2021年第一季度與2021年第一季度對比IXIARO®/JESPECT®4.2 13.3 14.2-70.5%杜科拉®2.5 0.1 0.1>2000%第三方產品5.6 2.7+110.9%COVID 3.8---產品總銷售額16.2 16.1 17.0-4.8%IXIARO®/JESPECT®(不包括美國軍方)3.9 1.0 1.0>3500%*2021年第一季度按實際平均匯率重新計算
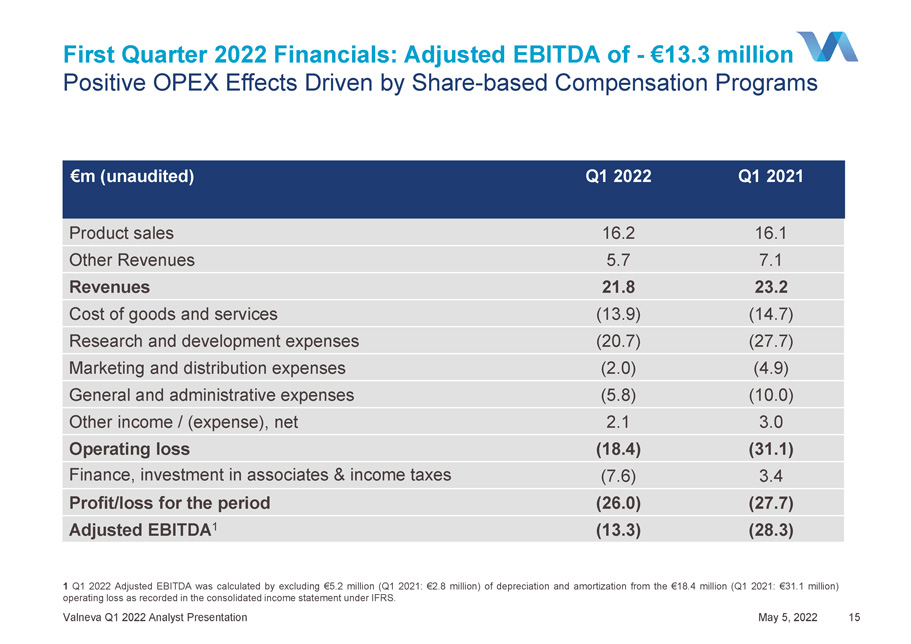
2022年第一季度財務:調整後的EBITDA為-1330萬歐元,由基於股票的薪酬計劃推動的積極運營支出影響Valneva 2022年第一季度分析師演示文稿2022年5月5日1 2022年第一季度調整後的EBITDA是通過從1840萬歐元(2021年第一季度:3110萬歐元)的綜合收益表中記錄的1840萬歐元(2021年第一季度:3110萬歐元)營業虧損中扣除520萬歐元(2021年第一季度:280萬歐元)計算的。2022年第一季度產品銷售額16.2 16.1其他收入5.7 7.1收入21.8 23.2商品和服務成本(13.9)(14.7)研發費用(20.7)(27.7)營銷和分銷費用(2.0)(4.9)一般和行政費用(5.8)(10.0)其他收入/(費用),淨2.1 3.0營業虧損(18.4)(31.1)財務,聯營公司投資及所得税(7.6)3.4當期損益(26.0)(27.7)調整後EBITDA 1(13.3)(28.3)
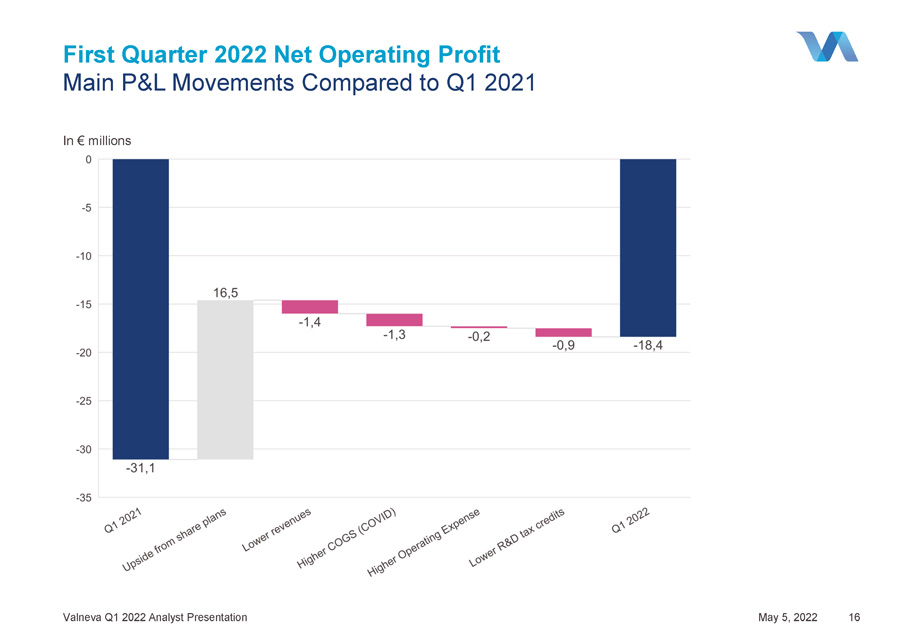
2022年第一季度淨營業利潤與2021年第一季度的主要損益變動(百萬歐元)Valneva 2022年第一季度分析師演示文稿2022年5月5日16
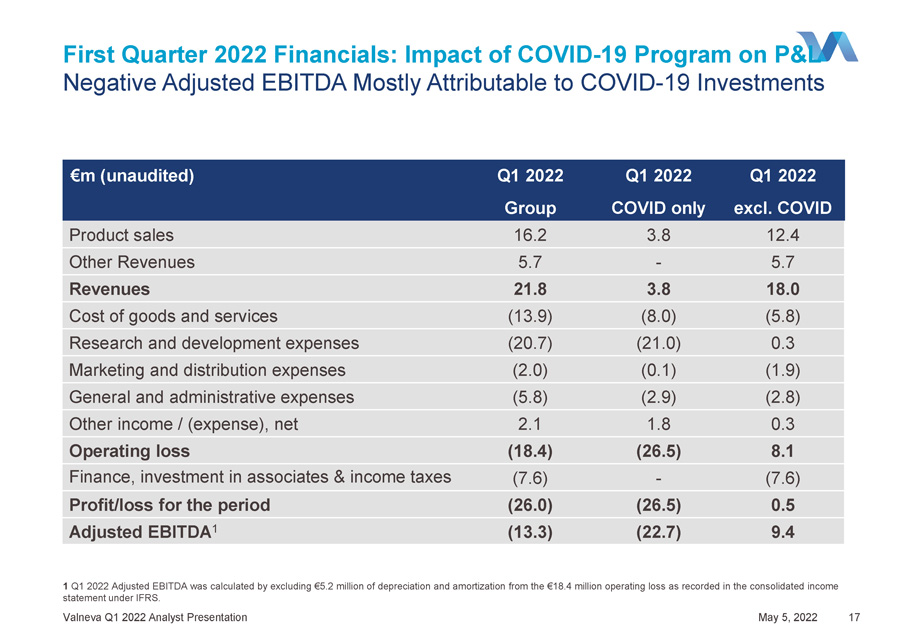
2022年第一季度財務:新冠肺炎計劃對損益的影響調整後的EBITDA主要歸因於新冠肺炎投資Valneva 2022年第一季度分析師演示文稿2022年5月5日17年第一季度調整後的EBITDA是通過從國際財務報告準則下的綜合收益表中記錄的1840萬歐元的營業虧損中剔除520萬歐元的折舊和攤銷來計算的。歐元(未經審計)2022年第1季度集團2022年第1季度COVID僅2022年第1季度不包括COVID產品銷售16.2 3.8 12.4其他收入5.7-5.7收入21.8 3.8 18.0商品和服務成本(13.9)(8.0)(5.8)研發費用(20.7)(21.0)0.3營銷和分銷費用(2.0)(0.1)(1.9)一般和行政費用(5.8)(2.9)(2.8)其他收入/(支出),淨額2.1 1.8 0.3營業虧損(18.4)(26.5)8.1財務、聯營公司投資及所得税(7.6)-(7.6)當期損益(26.0)(26.5)0.5調整後EBITDA 1(13.3)(22.7)9.4

議程Valneva 2022年第1季度分析師演示文稿2022年5月5日18簡介業務更新財務報告2022年第1季度新聞流問答財務展望

Valneva 2022年財務指導確認了Valneva 2022年第一季度分析師演示文稿2022年5月19日▪總收入預計將在2022年2月宣佈的範圍內(4.3億歐元至5.9億歐元)。考慮到產品交付時間的不確定性,▪按類別劃分的總收入分佈可能與2月份公佈的數字不同

議程Valneva 2022年第1季度分析師演示文稿2022年5月5日20簡介業務更新財務報告2022年第2季度新聞流問答財務展望

2022年即將到來的關鍵催化劑和新聞流2022年第1季度分析師演示文稿2022年5月5日21萊姆病候選疫苗VLA15▪第三階段試驗預計於2022年第三季度啟動候選基孔肯雅疫苗▪最終批次到批次第三階段數據預計2022年第二季度▪生物製品許可證申請預計2022年下半年新冠肺炎候選疫苗VLA2001▪潛在的額外法規批准▪供應和潛在的進一步採購協議▪進一步的臨牀試驗和數據預計

謝謝你,謝謝你,丹克大頭針