任何已發佈專利的權利要求都將提供足夠的專有保護,使其免受競爭對手的侵害。我們持有的任何專利都可能被第三方挑戰、規避或宣佈無效。
由於美國和某些其他司法管轄區的專利申請通常保密18個月,而且科學或專利文獻中發現的發佈往往落後於實際發現,我們無法確定我們已發佈的專利和未決專利申請所涵蓋的發明的專利權。此外,我們可能不得不參與美國專利商標局(USPTO)宣佈的幹擾程序,以確定發明的優先權,或者參與USPTO或外國專利局的授權後挑戰程序,如異議、重新審查、各方之間的審查、授權後審查或派生程序,挑戰我們對一項發明的權利或我們專利申請或已頒發專利中一項或多項權利要求的可專利性。即使最終結果對我們有利,這樣的訴訟也可能導致巨大的成本。
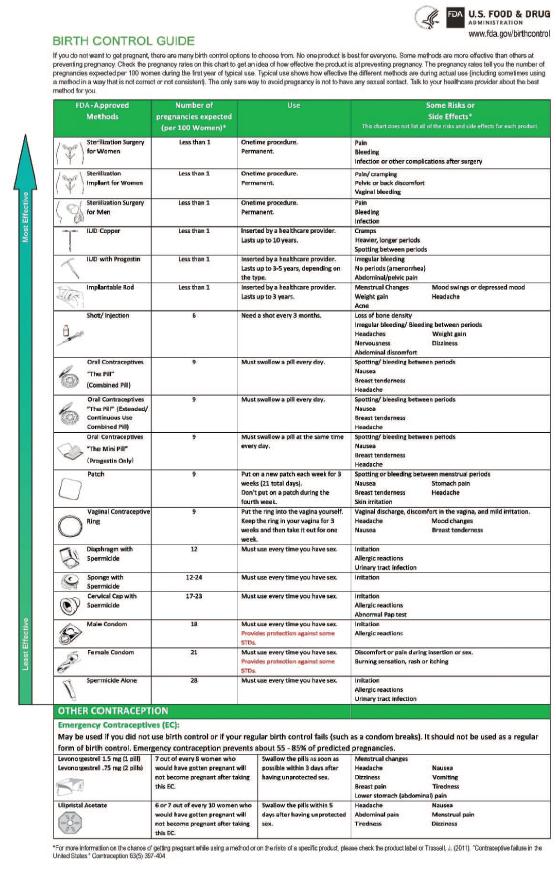
更具體地説,Twirla®是一種經皮避孕激素釋放系統。該系統是一種適用於皮膚的貼片,包含兩種原料藥,荷爾蒙LNG和EE,前者是一種合成孕激素,後者是一種合成雌激素。原料藥的配方與皮膚滲透促進劑的組合,促進透過真皮和血液滲透,從而達到有效的血液活性物質水平,以抑制排卵,從而防止懷孕。
在我們的Twirla候選產品線中,活性膠粘劑系統由聚丙烯酸酯膠粘劑聚合物基質中的活性成分組成,其中包括滲透促進劑二甲基亞碸、乳酸乙酯、戊酸和乳酸月桂酯。將活性混合物塗覆在離型襯墊上,並在活性混合物的頂部添加襯墊層。將包括三層的外圍粘合劑系統(也稱為覆蓋層)添加到背襯層上。所述貼麪包括聚異丁烯粘合層、丙烯酸酯粘合層和貼面覆蓋物。覆蓋層是市面上可買到的仿絲綢滌綸織物。覆蓋層的粘合組件,除了其粘合功能外,還創建了原位封口通過一次性離型襯墊,可將揮發性溶劑阻隔在活性混合物中,從而延長候選產品的可用貨架期,並有助於透皮系統在使用過程中的舒適性和有效性。在使用我們的任何潛在候選產品之前,用户會移除釋放襯墊並將其丟棄。然後將貼片貼在皮膚上。
FDA的橙皮書中列出了來自兩個專利家族的八項美國專利。這些專利包括針對具有活性粘合劑基質的透皮遞送系統的權利要求,以及針對通過應用這種經皮遞送系統並且在所有情況下包括皮膚滲透促進劑來控制生育的方法的權利要求。我們已頒發的八項美國專利中有一項於2020年11月22日到期。還有四款將於2021年3月14日到期。其中兩項將於2028年7月10日到期。第八期將於2028年8月26日到期。
到期的美國專利號7,045,145,7,384,650,8,221,784,8,221,785和8,883,196涉及Twirla中使用的透皮給藥系統與Twirla中使用的乾燥最終產品配方的粘合劑基質以及給藥方法。其中某些專利的外國同行已經獲得授權,並在中國、香港、印度、以色列和墨西哥繼續有效。
美國專利第8,246,978、8,747,888和9,050,348號專利針對的是Twirla貼片設計中用於激素或其他藥物經皮給藥的經皮給藥系統的結構特徵。因此,這些專利保護了一種用於輸送液化天然氣、EE、其他激素和其他藥物的平臺技術。這些專利將於2028年7月和8月到期。外國同行已在澳大利亞、巴西、加拿大、歐亞大陸、瑞士、德國、西班牙、法國、英國、香港、愛爾蘭、印度、意大利、日本、荷蘭、新西蘭和日本獲得批准。
美國專利號9,198,876、9,192,614、9,198,919、9,198,920、9,775,847和9,782,419以及相關專利和專利申請涉及各種新型給藥方案,其中每一種方案都在“治療間隔”期間採用避孕劑量的EE和LNG的透皮給藥,並在“停藥間隔”期間採用低劑量的EE和低劑量LNG的透皮給藥。外國同行在歐洲和加拿大獲得許可。我們預計這些專利將與我們正在開發的兩款產品AG200-SP和AG200-SP相關。呃,還有其他潛在的新的養生法。這些專利將於2029年10月到期。