附件99.1
Adverum BioTechnologies報告2021年第四季度和全年財務業績
加利福尼亞州雷德伍德城,2022年3月29日-Adverum BioTechnologies,Inc.(納斯達克股票代碼:ADVM),一家針對眼科和罕見疾病未得到滿足的醫療需求的臨牀階段基因治療公司,今天公佈了截至2021年12月31日的第四季度和全年的財務業績,並提供了最新業務情況。
Adverum生物技術公司總裁兼首席執行官Laurent Fischer醫學博士説:“2022年對Adverum來説將是重要的一年,因為我們計劃啟動一項第二階段試驗,評估兩劑ADVM-022對濕性老年性黃斑變性患者的療效。鑑於我們對使用ADVM-022治療的所有55名患者進行了強有力的安全性審查,以及我們在濕性老年性黃斑變性和進入2024年的現金跑道的光學研究中產生的有希望的臨牀療效數據,我們能夠滿懷信心地啟動ADVM-022的第二階段試驗。我們期待着在2022年第三季度給第一名患者開藥。
此外,我們繼續通過聘用多名高級管理層和任命董事會成員來加強我們的領導團隊,所有這些人都是各自領域的資深人士,並擁護Adverum的願景,“Fischer繼續説,”我們共同致力於推進ADVM-022的開發及其潛力,提供旨在防止濕性老年性黃斑變性患者視力喪失的一次性辦公室治療,並提供一種替代當今需要頻繁注射抗血管內皮生長因子的治療標準的方法。“
ADVM-022用於濕性老年性黃斑變性(Wet AMD)
Adverum計劃啟動一項第二階段試驗,以評估兩種劑量水平的ADVM-022,2×10^11 Vg/眼(2E11)和新的較低劑量6 X 10^10 Vg/眼(6E10),以及新的增強型預防性類固醇療法,預計將包括局部類固醇和局部和全身類固醇的組合。Adverum預計,這項研究將評估類似於濕性AMD第一階段光學試驗的終點。該公司預計將在2022年第三季度為第二階段試驗中的第一名患者提供劑量。
Adverum在2021年10月舉行的視網膜學會第54屆年度科學會議上公佈了其在濕性AMD患者中進行的ADVM-022第一階段光學試驗的兩年隨訪數據。提供的數據顯示,在2E11 VG/EY ADVM-022玻璃體內注射(IVT)後,每年的抗VEGF注射減少了80%以上。此外,在濕性AMD患者中,ADVM-022耐受性良好,眼部炎症輕微,對類固醇滴眼液有反應。
其他近期亮點
·Adverum被FDA授予ADVM-062(AAV/7M8-L-opsin)孤兒藥物稱號(ODD),這是一種新的基因治療候選產品,通過提供OPN1LW基因的功能副本,被開發為潛在的單一IVT用藥,用於治療藍色錐體單色症。
·主要高管領導層成員包括首席財務官魯珀特·德蘇扎(Rupert D‘Souza)博士、醫學博士斯塔·塞德卡澤米(Star Seyedkazemi)和首席醫療官理查德·貝克曼(Richard Beckman)。2021年8月加入該公司的吉姆·王(Jim Wang)博士、工商管理碩士,最近被提升為首席監管官。
·董事會增加了兩名成員,任命了醫學博士Rabia Gurses Ozden和M.B.A.Soo J.Hong。奧茲登博士在眼科、臨牀開發和手術、藥物警戒、監管事務和基因治療方面擁有20年的經驗。洪女士在人力資本管理、高管和領導力發展以及高管和董事會薪酬設計和治理方面擁有深厚的專業知識,在轉型期間為快速增長的組織提供服務。
預計2022年的里程碑
·2022年第2季度--於2022年5月1日在科羅拉多州丹佛市舉行的視覺與眼科研究協會(ARVO)年會上發表題為“ADVM-022玻璃體內(IVT)基因治療新生血管性AMD的第1階段研究(光學試驗):中和抗體(NAB)的作用”
·2022年第二季度-打算提供非人類靈長類蛋白質表達數據,支持人類相當劑量的ADVM-022 6 X 10^10 Vg/眼(6E10)
·2022年年中-完成IND修訂程序,以啟動ADVM-022在濕性AMD中的第二階段試驗
·2022年第三季度-計劃在濕性AMD的ADVM-022第二階段試驗中為第一名患者提供劑量
截至2021年12月31日的三個月的財務業績
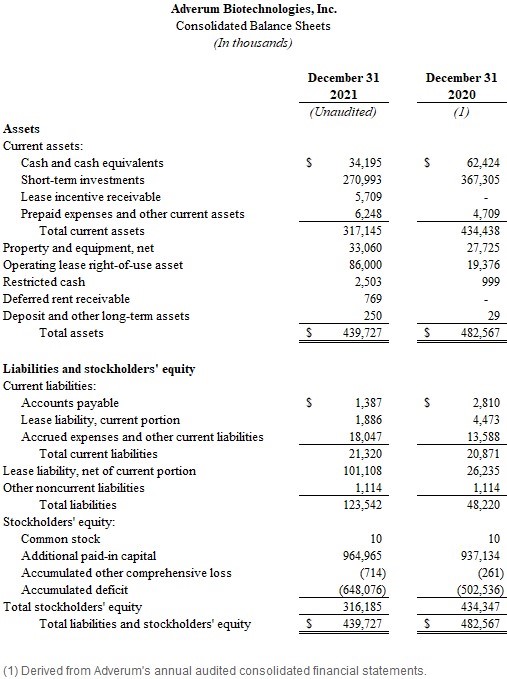
·截至2021年12月31日,現金、現金等價物和短期投資為3.052億美元,而截至2021年9月30日為3.327億美元,截至2020年12月31日為4.297億美元。Adverum預計,年底的現金狀況將為2024年的運營提供資金。
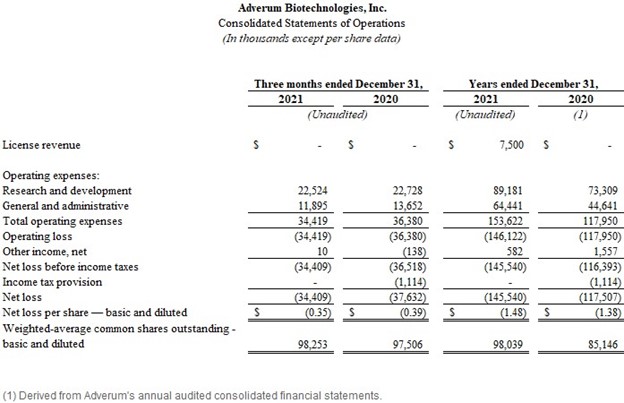
·截至2021年12月31日的三個月,研發支出為2250萬美元,而2020年同期為2270萬美元。研究和開發費用相對持平,主要是由於臨牀試驗成本較低,但實驗室和諮詢費用略有上升。2021年第四季度,包括在研發費用中的股票薪酬支出為180萬美元。
·截至2021年12月31日的三個月,一般和行政費用為1190萬美元,而2020年同期為1370萬美元。一般和行政費用減少的主要原因是與人員相關的和專業服務費用下降,但被Adverum新總部的保險和租賃費用增加部分抵消。2021年第四季度,包括在一般和行政費用中的基於股票的薪酬支出為270萬美元。
·截至2021年12月31日的三個月,淨虧損為3440萬美元,或每股基本攤薄虧損0.35美元,而2020年同期為3760萬美元,或每股基本攤薄虧損0.39美元。
關於Adverum生物技術公司
Adverum生物技術公司(納斯達克代碼:ADVM)是一家臨牀階段的基因治療公司,目標是治療嚴重的眼科和罕見疾病,滿足未得到滿足的醫療需求。Adverum正在評估其新的基因治療候選藥物ADVM-022,作為一次性玻璃體內注射,用於治療新生血管或濕性老年性黃斑變性患者。ADVM-062是一種基因治療候選藥物,專門為患有藍色錐體單色症的患者設計。ADVM-062利用Adverum的適當載體衣殼AAV.7m8。欲瞭解更多信息,請訪問www.Adverum.com。
前瞻性陳述
本新聞稿中包含的有關未來可能發生的事件或結果的陳述屬於“1995年私人證券訴訟改革法”所指的“前瞻性陳述”。這些陳述包括但不限於關於2024年的預期當前現金跑道的陳述,以及標題為“預期的2022年裏程碑”和標題為“ADVM-022用於濕性老年性黃斑變性(Wet AMD)”的陳述。由於各種風險和不確定性,實際結果可能與前瞻性聲明中預期的結果有實質性差異,這些風險和不確定性包括但不限於:Adverum的新技術使其難以預測候選產品開發和獲得監管批准的時間和成本;早期臨牀試驗的結果並不總是能預測未來的結果;以及與使用ADVM-022相關的任何未來併發症或副作用,以推遲或阻止ADVM-022的監管推進或批准。Adverum面臨的其他風險和不確定因素在Adverum公司提交給美國證券交易委員會的文件和報告中以“風險因素”為標題列出,這些文件和報告包括Adverum公司截至2021年9月30日的10-Q表格季度報告,以及Adverum公司未來的文件和報告,包括Adverum公司截至2021年12月31日的10-K表格年度報告。本新聞稿中包含的所有前瞻性陳述僅在發表之日發表。Adverum沒有義務更新這些聲明,以反映在聲明發表之日之後發生的事件或存在的情況。
問詢
阿南德·雷迪
副總裁,公司戰略和對外事務及接洽負責人
Adverum生物技術公司
T: 650-649-1358
或
投資者:
勞倫斯·瓦茨
吉爾馬丁集團
T: 619-916-7620
電子郵件:laurence@gilmartinir.com
媒體:
詹妮弗·阿庫爾運河通信公司
T: 917-603-0681
電子郵件:jennifer.Arure@canalecomm.com
來源:Adverum BioTechnologies,Inc.