目錄
第二項。管理層對財務狀況和經營成果的討論與分析。
管理層對截至2021年9月30日的財務狀況以及截至2021年9月30日的三個月和九個月的經營業績的討論和分析,應與管理層對截至2020年12月31日的年度10-K表格中包括的財務狀況和經營結果的討論和分析一併閲讀,該年度報告於2021年2月25日提交給美國證券交易委員會(SEC)或美國證券交易委員會。我們的討論包括基於當前預期的前瞻性陳述,這些預期涉及風險和不確定性,例如我們的計劃、目標、期望和意圖。由於多種因素的影響,實際結果和事件發生的時間可能與這些前瞻性陳述中預期的大不相同,這些因素包括我們提交給證券交易委員會的10-K表格年度報告“業務”部分和本報告其他部分以及我們提交給證券交易委員會的其他報告。我們使用諸如“可能”、“將會”、“可能”、“可能”、“將會”、“應該”、“期望”、“打算”、“計劃”、“預期”、“相信”、“估計”、“預測”、“項目”、“目標”、“潛力”、“繼續”、“正在進行”、“目標”、“預測”、“指導,“展望”或這些術語的否定或其他類似表述來識別前瞻性表述,儘管並不是所有前瞻性表述都包含這些詞語。本報告中包含的所有前瞻性陳述均基於我們在本報告發布之日獲得的信息,除非法律另有要求,否則我們不承擔更新任何此類前瞻性陳述的義務。除文意另有所指外,本季度報告中10-Q表格中提及的“Iovance”、“我們”、“我們”和“我們”均指Iovance BioTreateutics,Inc.及其子公司。
概述
我們是一家臨牀階段的生物製藥公司,專注於細胞療法的開發和商業化,這些細胞療法是新型癌症免疫療法產品,旨在利用患者自身免疫系統的力量來根除癌細胞。腫瘤浸潤性淋巴細胞(TIL)療法是一種自體多克隆細胞治療平臺技術,最初由美國國家癌症研究所(NCI)開發,該研究所對轉移性黑色素瘤和宮頸癌等疾病進行了這種療法的初步臨牀試驗。我們已經開發了一種新的、更短的TIL製造工藝,稱為Gen 2,它可以生產低温保存的TIL產品。這種集中的、專有的和可擴展的製造方法正在多個適應症中進行研究。我們的主要候選產品包括治療轉移性黑色素瘤和轉移性宮頸癌的脂質體。除了轉移性黑色素瘤和轉移性宮頸癌,我們正在研究TIL療法治療頭頸部鱗狀細胞癌(HNSCC)、非小細胞肺癌(NSCLC)的有效性和安全性。我們正在通過我們贊助的試驗,研究外周血淋巴細胞(PBL)對復發或難治性慢性淋巴細胞白血病(CLL)和小淋巴細胞性淋巴瘤(SLL)患者的治療。我們還在通過與領先的癌症研究中心的學術合作,研究TIL治療在其他腫瘤學適應症中的潛力。
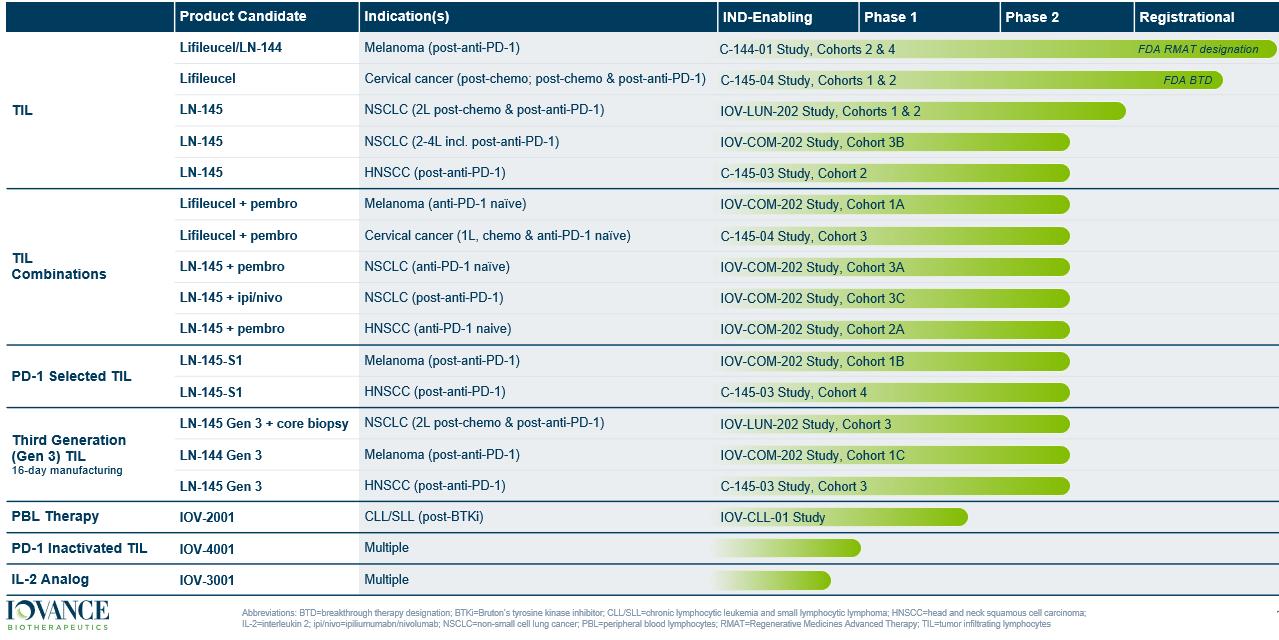
我們目前的候選產品渠道彙總如下圖所示:
30