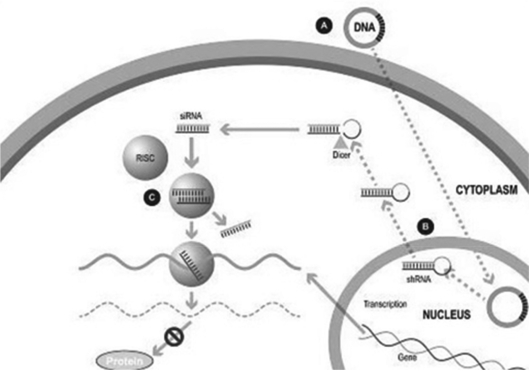
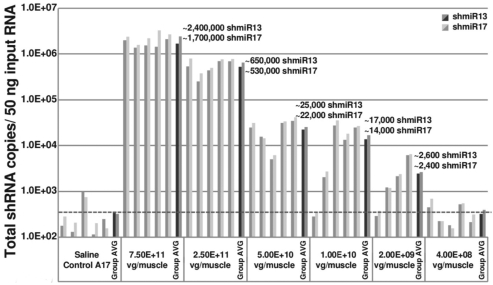
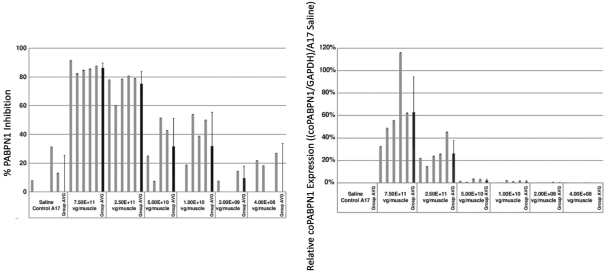
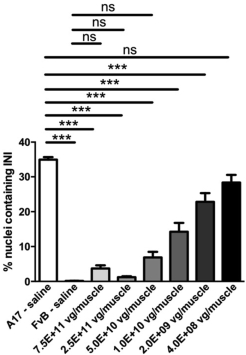
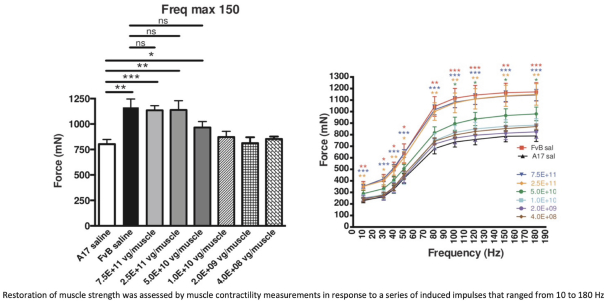
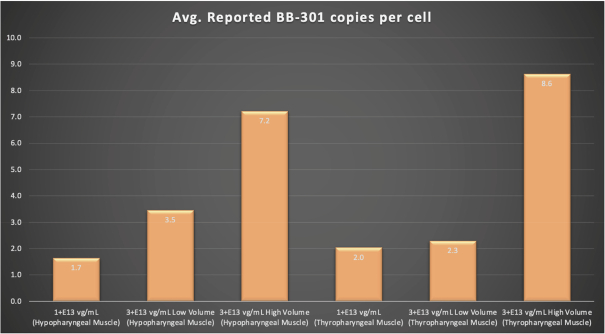
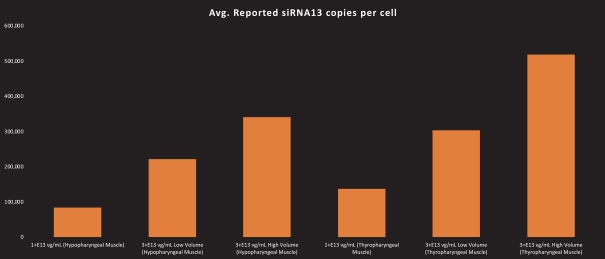
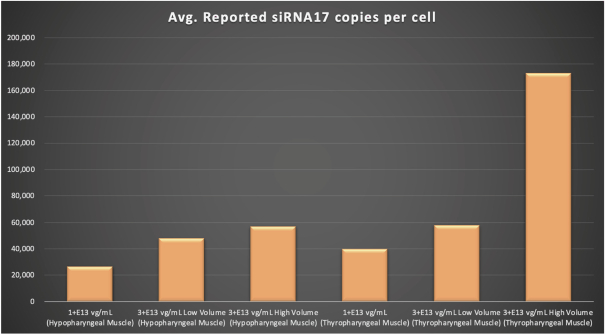
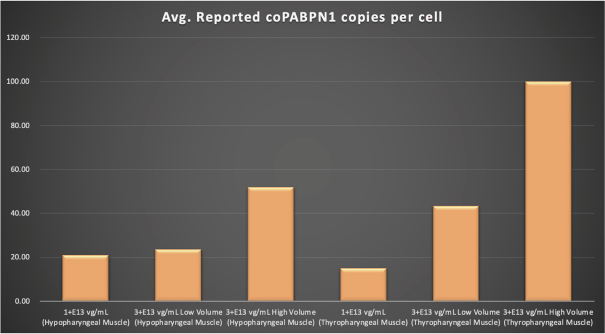
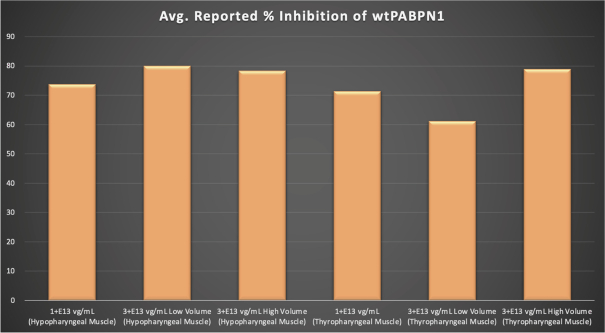
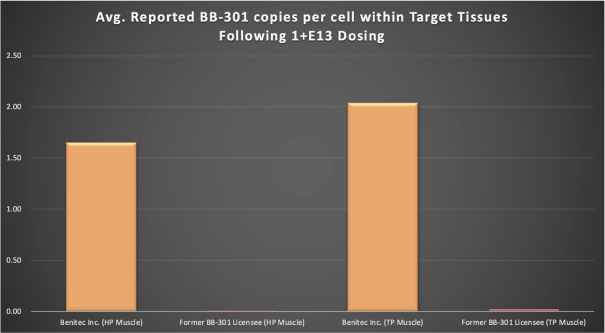
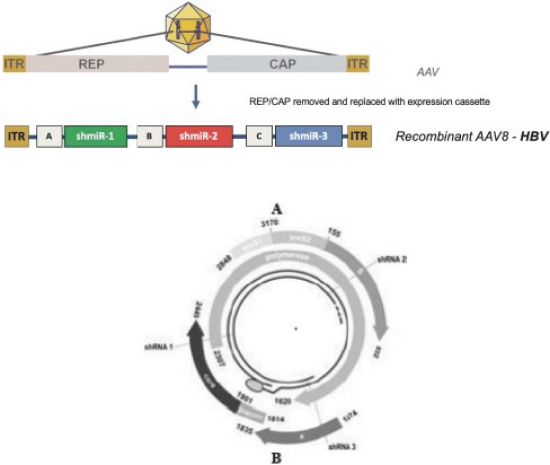
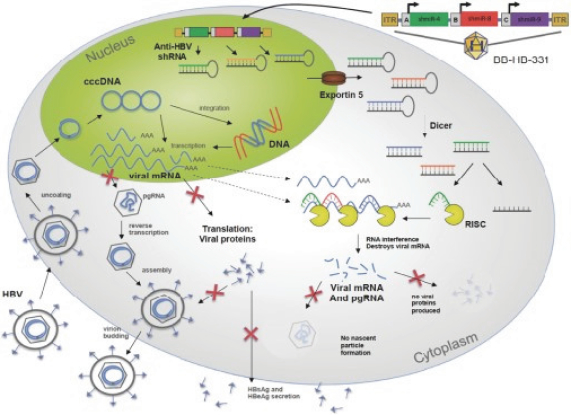
圖1
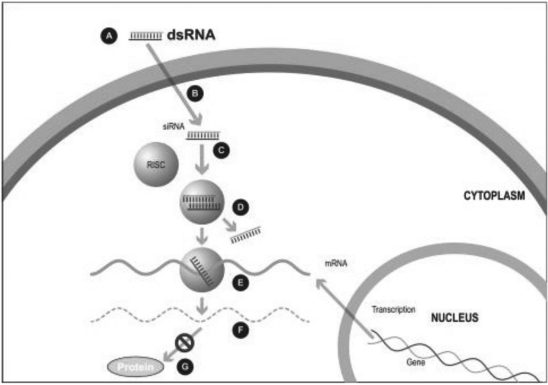
在實驗室合成了一種小的雙鏈RNA或dsRNA分子(A,圖1),由一條稱為正義鏈的鏈和另一條稱為反義鏈的鏈組成,這兩條鏈相互補充。這些小dsRNA被稱為小幹擾RNA,或siRNA。正義鏈序列對應於靶基因mRNA的一小段區域。SiRNA被傳遞到靶細胞(B,圖1),在那裏有一組酶,稱為
RNA誘導
沉默複合體或RISC處理siRNA(C,圖1),其中一條鏈(通常是正義鏈)被釋放(D,圖1)。RISC使用反義鏈來尋找具有互補序列(E,圖1)的mRNA,從而導致靶mRNA的切割(F,圖1)。因此,mRNA(蛋白質生產)的輸出不會發生(G,圖1)。包括Alnylam製藥公司(“Alnylam”)、Arbutus Biophma Corp.(“Arbutus”)和Dicerna製藥公司(“Dicerna”)在內的幾家公司在他們的RNAi產品候選中使用這種方法。重要的是,許多遺傳疾病不符合圖1中概述的傳統基因沉默方法,因為患病細胞可能產生感興趣的野生型蛋白和致病蛋白的突變變體的混合物,潛在的基因突變可能太小,無法通過專門使用基於siRNA的方法選擇性地靶向致病蛋白的突變變體。在這些情況下,要選擇性地沉默致病蛋白而不同時沉默感興趣的野生型細胞內蛋白是非常困難的,因為野生型細胞內蛋白的存在對正常細胞功能的進行至關重要。
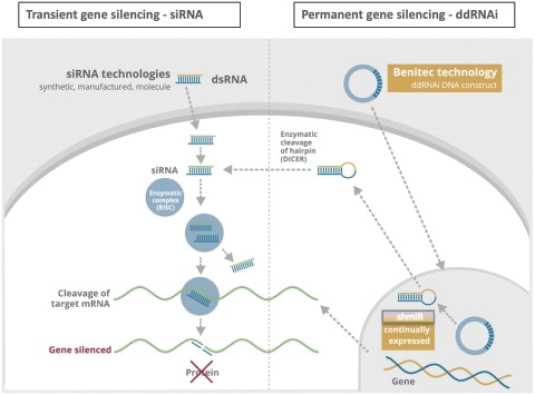
我們專有的沉默和替換技術利用了RNAi獨特的特異性和強大的基因沉默能力,同時克服了基於siRNA的疾病管理方法的許多關鍵限制。
在標準的RNAi方法中,合成雙鏈siRNA,然後通過對RNA的化學修飾或其他遞送方法將其導入靶細胞。雖然功效有
5