依據第424(B)(4)條提交
註冊號碼333-256997
註冊號碼333-258772
2,571,428個單位,包括
2,571,428股普通股和
認股權證將購買最多2,571,428股普通股

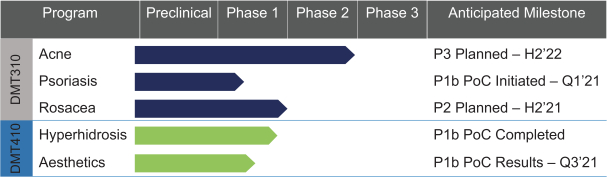
皮瑪塔治療公司(Dermata Treateutics,Inc.)
Dermata Treateutics,Inc.正在發售單位,每個單位包括一股我們的普通股和一個認股權證,用於在首次公開募股(IPO)中購買一股我們的普通股,或每個認股權證。我們的普通股或組成這些單位的認股權證目前還沒有公開市場。這些單位沒有獨立權利,也不會作為獨立證券進行認證或發行 。普通股和認股權證可以立即分開,並將在此次發行中單獨發行。本公司發行的每份認股權證於發行日起立即行使,行使價為每股普通股7.00美元,自發行之日起5年期滿。
我們的普通股和權證將分別在納斯達克資本市場(Nasdaq Capital Market)或納斯達克(Nasdaq)交易,代碼分別為DRMA和DRMAW。
根據2012年的Jumpstart Our Business Startups Act 或JOBS Act,我們是一家新興的成長型公司,因此,我們已選擇遵守本招股説明書和未來備案文件中某些降低的上市公司報告要求。
投資我們的證券 具有高度的投機性和高度的風險。請參見?風險因素?從本招股説明書的第12頁開始,討論在投資我們的證券時應考慮的信息 。
美國證券交易委員會(Securities And Exchange Commission)和任何州證券委員會都沒有批准或不批准這些證券,也沒有就本招股説明書的準確性或充分性發表意見。任何相反的陳述都是刑事犯罪。
| 人均 單位 |
總計 | |||||||
| 首次公開發行(IPO)價格 |
$ | 7.00 | $ | 17,999,996 | ||||
| 承保折扣和佣金(1) |
$ | 0.56 | $ | 1,440,000 | ||||
| 未扣除費用的收益給我們 |
$ | 6.44 | $ | 16,559,996 | ||||
| (1) | 不包括保險人某些費用的報銷。我們建議您訪問 \f25 \f25包銷?從第151頁開始,瞭解有關承銷商賠償的更多信息。 |
我們已 授予承銷商代表可在本招股説明書發佈之日起45天內行使的選擇權,可按每股6.99美元的價格向我們額外購買最多385,714股普通股和/或最多額外 385,714股認股權證,以購買最多385,714股普通股,每份認股權證的價格為0.01美元,每種情況下均減去承銷折扣和佣金,以彌補超額配售(如果有)。如果承銷商代表全面行使選擇權,則應支付的承保折扣和佣金總額為1,656,000美元,扣除費用前給我們的總收益為19,043,994美元。
我們的某些現有股東及其附屬實體與我們的創始人兼首席執行官以及我們的某些現任 董事(包括Proehl Investment Ventures,LLC和Hale BioPharma Ventures,LLC)在此次發行中以首次公開募股(IPO)價格購買了總計約125萬美元的單位。承銷商將 從這些股東購買的任何單位獲得與他們在此次發行中向公眾出售的任何其他單位相同的承銷折扣和佣金。
承銷商預計在2021年8月17日左右交付組成這些單位的證券。
| 唯一圖書運行經理 Maxim Group LLC |
| 聯席經理 布魯克林資本市場 阿卡迪亞證券有限責任公司的一個部門 |
本招股説明書的日期為2021年8月12日。