美國
證券交易委員會
華盛頓特區20549
表格10-q
根據1934年證券交易所第13或15(D)節提交的季度報告
截至2019年11月30日止的季度
O根據1934年證券交易所ACT第13或15(D)節提交的過渡報告
佣金檔案號碼:000-50298
奧拉梅德製藥公司
( 其約章所指明的註冊人的確切名稱)
| 特拉華州 | 98-0376008 | |
| ( 註冊或組織的州或其他管轄範圍) | (I.R.S.僱主) 識別號) | |
| 美洲大道1185號,紐約228號套房,紐約 | 10036 | |
| (首席行政辦公室地址) | (郵政編碼) |
844-967-2633
(登記人的電話號碼,包括 區號)
根據該法第12(B)條登記的證券:
| 每一班的職稱 | 交易符號 | 註冊的每個交易所的名稱 | ||
| 普通股票面價值0.012美元 | ORMP | 納斯達克資本市場,特拉維夫證券交易所 |
(1)已提交1934年“證券交易法”第13條或第15(D)節要求在過去12個月內提交的所有報告(或要求登記人提交此類報告的時間較短的 );(2)在過去90天中一直受到這種申報要求的限制。
是 x No o
通過檢查標記,説明註冊人是否以電子方式提交了每一份交互數據文件,這些文件必須按照本章第405條(本章第232.405節)的規定在過去12個月內提交(或在較短的時間內要求註冊人提交此類文件)。
是x否o
通過檢查標記指示註冊人是大型加速 備案者、加速備案者、非加速備案者、較小的報告公司還是新興的增長公司。參見“Exchange Act”規則12b-2中“大型加速篩選器”、“加速篩選器”、“小型報告公司”和“新興 增長公司”的定義 。
| 大型加速濾波器 | 加速濾波器 |
| 非加速濾波器x |
小型報告公司x 新興成長公司o |
如果是新興成長型公司,請用支票標記表明註冊人是否選擇不使用延長的過渡期來遵守“外匯法”第13(A)條規定的任何新的或經修訂的財務會計準則。☐
通過複選標記指示註冊人是否為shell公司 (如“交易法”第12b-2條所定義)。
是的 o No x
截至2020年1月9日,發行人普通股共有17735775股,每股票面價值0.012美元,已發行。
奧雷德製藥公司
表格10-q
目錄
| 第一部分-財務資料 | 1 |
| 項目1-財務報表 | 1 |
| 項目2-管理層對財務狀況和業務結果的討論和分析 | 17 |
| 項目3-市場風險的定量和定性披露 | 24 |
| 項目4-管制和程序 | 24 |
| 第二部分-其他資料 | 25 |
| 第2項-股本證券的未登記出售及收益的使用 | 25 |
| 項目6-展品 | 25 |
如本季度報告中所用的表格 10-Q,術語“we”、“us”、“our”和“Company”指的是Oramed製藥公司。以及我們的全資子公司,除非另有説明。除 另有説明外,所有美元金額均指美元。
2019年11月30日,以色列銀行引用的新以色列謝克爾(或稱新謝克爾)與美元之間的匯率為3.476至1.00美元。除非上下文另有説明,本季度報告表10-Q中提供新謝克爾金額美元等值或 提供新謝克爾等值美元數額的報表均以這種匯率為基礎。
i
第一部分-財務 資料
項目1-財務報表
奧雷德製藥公司
精簡合併財務報表
截至2019年11月30日
目錄
| 頁 | |
| 精簡的合併財務報表: | |
| 資產負債表 | 2 |
| 綜合損失表 | 3 |
| 股東權益變動表 | 4 |
| 現金流量表 | 5 |
| 財務 報表附註 | 6-16 |
1
Oramed製藥公司
壓縮合並資產負債表
美元(千美元)(除股票 和每股數據外)
(未經審計)
| 十一月三十日, | 八月三十一日, | |||||||
| 2019 | 2019 | |||||||
| 資產 | ||||||||
| 流動資產: | ||||||||
| 現金和現金等價物 | 3,171 | 3,329 | ||||||
| 短期存款 | 23,755 | 25,252 | ||||||
| 有價證券 | 3,207 | 3,701 | ||||||
| 預付費用和其他流動資產 | 609 | 1,042 | ||||||
| 流動資產總額 | 30,742 | 33,324 | ||||||
| 長期資產: | ||||||||
| 長期存款 | 1 | 1 | ||||||
| 有價證券 | 250 | 1,295 | ||||||
| 退休時為僱員權利提供資金的數額 | 16 | 19 | ||||||
| 財產和設備,淨額 | 27 | 24 | ||||||
| 經營租賃使用權資產 | 106 | - | ||||||
| 長期資產總額 | 400 | 1,339 | ||||||
| 總資產 | 31,142 | 34,663 | ||||||
| 負債和股東權益 | ||||||||
| 流動負債: | ||||||||
| 應付帳款和應計費用 | 1,796 | 2,541 | ||||||
| 遞延收入 | 2,703 | 2,703 | ||||||
| 應付關聯方的款項 | 96 | 64 | ||||||
| 經營租賃負債 | 46 | - | ||||||
| 流動負債總額 | 4,641 | 5,308 | ||||||
| 長期負債: | ||||||||
| 遞延收入 | 8,983 | 9,658 | ||||||
| 僱員退休後的權利 | 17 | 22 | ||||||
| 對不確定税收狀況的備抵 | 11 | 11 | ||||||
| 經營租賃負債 | 60 | - | ||||||
| 其他負債 | 270 | 271 | ||||||
| 長期負債總額 | 9,341 | 9,962 | ||||||
| 承諾(附註2) | ||||||||
| 股東權益: | ||||||||
| 普通股,票面價值0.012美元(截至2019年11月30日和2019年8月31日,分別為30,000,000股;17,400,612股和17,383,359股) | 209 | 208 | ||||||
| 額外已付資本 | 100,597 | 100,288 | ||||||
| 累積赤字 | (83,646 | ) | (81,103 | ) | ||||
| 股東權益總額 | 17,160 | 19,393 | ||||||
| 負債和股東權益共計 | 31,142 | 34,663 | ||||||
所附附註是精簡合併財務報表的組成部分。
2
奧雷德製藥公司
綜合損失合併報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
| 三個月結束 | ||||||||
| 十一月三十日, | 十一月三十日, | |||||||
| 2019 | 2018 | |||||||
| 收入 | $ | 674 | $ | 674 | ||||
| 收入成本 | 35 | |||||||
| 研發費用 | 2,022 | 4,347 | ||||||
| 一般和行政費用 | 1,081 | 932 | ||||||
| 營運損失 | 2,429 | 4,640 | ||||||
| 財政收入 | 209 | 286 | ||||||
| 財務費用 | 20 | 8 | ||||||
| 投資公允價值變動的收入(損失) | (303 | ) | 60 | |||||
| 這一期間的淨虧損 | $ | 2,543 | $ | 4,302 | ||||
| 普通股每股虧損: | ||||||||
| 普通股每股基本損失和稀釋損失 | $ | 0.15 | $ | 0.25 | ||||
| 用於計算普通股每股基本損失和稀釋損失的普通股加權平均數量 | 17,472,315 | 17,448,744 | ||||||
所附附註是精簡合併財務報表的組成部分。
3
奧雷德製藥公司
股東權益變動的合併合併報表
美元(千美元)
(未經審計)
| 累積 | ||||||||||||||||||||||||
| 額外 | 其他 | 共計 | ||||||||||||||||||||||
| 普通股 | 已付 | 綜合 | 累積 | 股東‘ | ||||||||||||||||||||
| 股份 | $ | 資本 | 收入 | 赤字 | 衡平法 | |||||||||||||||||||
| 以千計 | ||||||||||||||||||||||||
| 截至2019年8月31日的餘額 | 17,383 | $ | 208 | $ | 100,288 | - | $ | (81,103 | ) | $ | 19,393 | |||||||||||||
| 截至2019年11月30日的三個月期間的變化情況: | ||||||||||||||||||||||||
| 為服務發行的股份 | 5 | * | 17 | - | - | 17 | ||||||||||||||||||
| 認股權證及期權的行使 | 12 | 1 | 12 | - | - | 13 | ||||||||||||||||||
| 股票補償 | - | * | 280 | - | - | 280 | ||||||||||||||||||
| 淨損失 | - | - | - | - | (2,543 | ) | (2,543 | ) | ||||||||||||||||
| 截至2019年11月30日的結餘 | 17,400 | $ | 209 | $ | 100,597 | - | $ | (83,646 | ) | $ | 17,160 | |||||||||||||
| 累積 | ||||||||||||||||||||||||
| 額外 | 其他 | 共計 | ||||||||||||||||||||||
| 普通股 | 已付 | 綜合 | 累積 | 股東‘ | ||||||||||||||||||||
| 股份 | $ | 資本 | 收入 | 赤字 | 衡平法 | |||||||||||||||||||
| 以千計 | ||||||||||||||||||||||||
| 截至2018年8月31日的餘額 | 17,369 | $ | 207 | $ | 99,426 | $ | 702 | $ | (69,223 | ) | $ | 31,112 | ||||||||||||
| ASC 606的初步通過 | 1,773 | 1,773 | ||||||||||||||||||||||
| ASU 2016-01初步通過 | (702 | ) | 702 | - | ||||||||||||||||||||
| 2018年11月30日終了的三個月期間的變化: | ||||||||||||||||||||||||
| 為服務發行的股份 | 8 | * | 36 | - | - | 36 | ||||||||||||||||||
| 股票補償 | - | * | 239 | - | - | 239 | ||||||||||||||||||
| 淨損失 | - | - | - | - | (4,302 | ) | (4,302 | ) | ||||||||||||||||
| 截至2018年11月30日餘額 | 17,377 | $ | 207 | $ | 99,701 | - | $ | (71,050 | ) | $ | 28,858 | |||||||||||||
| * | 表示小於$1的金額。 |
所附附註是精簡合併財務報表的組成部分。
4
奧雷德製藥公司
合併現金流量表
千美元
(未經審計)
| 三個月結束 | ||||||||
| 十一月三十日, | ||||||||
| 2019 | 2018 | |||||||
| 業務活動現金流量: | ||||||||
| 淨損失 | $ | (2,543 | ) | $ | (4,302 | ) | ||
| 將淨虧損與用於業務活動的現金淨額對賬所需的調整數: | ||||||||
| 折舊 | - | 2 | ||||||
| 存款和到期日債券的匯兑差額和利息 | (92 | ) | (116 | ) | ||||
| 投資公允價值的變化 | 303 | (60 | ) | |||||
| 股票補償 | 280 | 239 | ||||||
| 為服務發行的股份 | 17 | 36 | ||||||
| 經營資產和負債的變化: | ||||||||
| 預付費用和其他流動資產 | 433 | (153 | ) | |||||
| 應付帳款、應計費用和關聯方 | (714 | ) | 929 | |||||
| 合同負債 | (675 | ) | (674 | ) | ||||
| 退休時僱員權利的法律責任 | (5 | ) | - | |||||
| 其他負債 | - | (32 | ) | |||||
| 用於業務活動的現金淨額共計 | (2,996 | ) | (4,131 | ) | ||||
| 投資活動的現金流量: | ||||||||
| 購買短期存款 | (3,000 | ) | - | |||||
| 購買持有至到期證券 | - | (397 | ) | |||||
| 出售短期存款所得收益 | 4,600 | 3,000 | ||||||
| 持有至到期證券的到期日收益 | 1,225 | 400 | ||||||
| 退休時僱員權利基金 | 3 | - | ||||||
| 購置財產和設備 | (3 | ) | (8 | ) | ||||
| 投資活動提供的現金淨額共計 | 2,825 | 2,995 | ||||||
| 來自籌資活動的現金流量: | ||||||||
| 發行普通股的收益,扣除發行成本 | 1 | - | ||||||
| 行使選擇權所得收益 | 12 | - | ||||||
| 籌資活動提供的現金淨額共計 | 13 | - | ||||||
| 匯率變動對現金的影響 | 0 | 1 | ||||||
| 現金和現金等價物減少 | (158 | ) | (1,135 | ) | ||||
| 期初現金及現金等價物 | 3,329 | 4,996 | ||||||
| 期末現金及現金等價物 | $ | 3,171 | $ | 3,861 | ||||
| 現金流量補充披露- | ||||||||
| 收到的利息 | $ | 112 | $ | 159 | ||||
所附附註是精簡的合併財務報表的組成部分。
5
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
注 1-重要會計政策:
| a. | 一般情況: |
| 1) | 成立及運作 |
奧拉梅德製藥公司(與其子公司“公司”合併,除非上下文另有説明)是根據內華達州的法律於2002年4月12日成立的。從公司成立到2006年3月3日,該公司是一家從事礦產資產收購和勘探的勘探階段公司。2006年2月17日,該公司與Hadasit醫療服務和發展有限公司簽訂了一項協議,獲得用於治療糖尿病患者的口服胰島素膠囊的臨時專利。
2007年5月14日,該公司在以色列成立了一家全資子公司Oramed Ltd.(“子公司”),從事研究和開發。
2011年3月11日,該公司從內華達州恢復到特拉華州。
2019年7月30日,該附屬公司在香港成立了全資子公司Oramed HK Limited.截至2019年11月30日,OramedHK有限公司沒有業務。
2015年11月30日,公司與合肥天輝科技有限公司簽訂技術許可證協議。(“HTIT”) 和2015年12月21日,雙方簽署了一項經修正和恢復的技術許可協議,並於2016年6月3日和2016年7月24日(“許可協議”)進一步修正了 。根據許可證協議, 公司授予HTIT在中華人民共和國、澳門和香港(“領土”)境內的獨家商業化許可證,涉及該公司的口服胰島素膠囊ORMD-0801(“產品”)。根據許可證協議 ,HTIT將自費就子公司的技術和ORMD-0801膠囊開展某些商業化前和管制活動,並將向附屬公司支付10%的特許使用費,用於HTIT在該領土銷售的相關商業化產品(“特許權使用費”), 和(Ii)總計37,500美元,其中3,000美元應立即支付,其中8,000美元將由公司與某些第三方簽訂某些協議,在實現某些里程碑和條件後,將支付26 500美元。如果公司不符合某些條件,可以將特許權使用費降低到至少8%。在2033年該公司關於該技術的專利最終到期後,在某些情況下可將 特許權使用費降低到5%。
特許權使用費支付義務應在下列期間適用:自該產品在領土內第一次商業銷售起至(1)在該領土上最後到期的許可專利的最後一次過期;和(2)該產品在領土內首次商業銷售後15年(“皇家條款”)之後的一段時間內。
“許可協議”將一直有效,直到王室任期屆滿時為止。“許可證協定”載有習慣上的終止條款。
6
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
注 1-重大會計政策(續):
除其他外,該公司通過 參與產品提交日期將包括為該領土的商業化前活動提供諮詢,以及不斷向技術創新技術提供諮詢服務。
截至2019年11月30日,該公司共收到20 500美元的里程碑付款,總額如下:首次付款3 000美元已於2016年1月收到。在實現某些里程碑之後,2016年7月分別收到第二次和第三次付款6 500美元和第三次付款4 000美元,2016年10月收到第四次里程碑付款4 000美元,2019年1月收到第五次里程碑付款3 000美元。
此外,2015年11月30日,該公司與HTIT簽訂了股票購買協議(“SPA”)。根據SPA,該公司以12,000美元向HTIT發行了1,155,367股 普通股。交易於2015年12月28日結束。
2015年7月,根據雙方或其附屬公司簽署的意向書 ,HTIT的附屬公司向子公司支付了不可退還的500美元的非商店 費用。沒有商店的費用被推遲,相關的收入在許可證協議的估計期限內被確認。
收入確認政策見附註1c。
| 2) | 發展和流動性風險 |
該公司在生物技術領域從事創新藥物解決方案的研究和開發,包括用於治療糖尿病患者的口服胰島素膠囊,以及使用口服可吸收膠囊運送其他多肽,而且沒有從其業務中獲得可觀的收入。根據公司目前的現金資源和承付款項,公司認為至少在今後12個月及以後能夠維持目前計劃的開發活動 和相應的支出水平,但不能保證公司在此之前不需要額外資金。如果業務費用意外增加, 公司可能需要在今後12個月內尋求額外資金。該公司成功完成開發 項目和向正常運作過渡取決於在美國境內銷售其產品、獲得外國監管機構批准在國際上銷售其產品或與第三方簽訂許可協議之前,必須獲得美國食品和藥品管理局的必要監管批准。不能保證 公司將獲得其任何產品候選方的監管批准,而且在 公司達到足以支持其業務的收入水平之前,可能需要相當長的時間。, 如果有的話。該公司還期望在其每個產品候選人各自開發期間的管理審批過程中產生大量的 支出。獲得營銷批准將直接取決於公司是否有能力執行在美國和其他國家獲得營銷批准所需的必要的管理步驟。公司無法預測這些活動的結果。
7
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註1-重大會計政策(續):
| b. | 普通股虧損 |
每普通股的基本淨虧損和稀釋淨虧損是通過將該期間的淨虧損除以每一期間已發行普通股的加權平均股份數來計算的。未償還的股票期權、認股權證和限制性股票單位(“RSU”)已被排除在攤薄的每股 損失的計算之外,因為所有這類證券在提出的所有期間都是反稀釋的。在截至11月30日、2019年和2018年的三個月期間,不計算稀釋淨損失的普通股(認股權證)、認股權證和RSU的加權平均數分別為4,366,806和4,352,798。
| c. | 收入確認 |
許可協議和SPA被認為是具有多個交付品的 單一安排。該公司根據許可證協議 和SPA之間的公允價值分配了49,500美元的總審議額,具體如下:10,617美元用於發行普通股(減去發行費用 $23),根據該公司在2015年12月28日SPA截止日期的股票報價,分配給許可證協議的是38,883美元。
根據會計準則編纂(“ASC”) 605(這是2018年9月1日前所有期間適用的權威性收入確認指南),鑑於該公司通過在2023年6月提交預期產品而繼續參與,在該公司有權獲得相應付款的期間內確認了與許可證協議 有關的金額,並在賺取費用期間採用基於時間的模式方法確認了預期提交的產品 日期。
2018年9月1日,該公司採用修正的回顧性採用方法,通過了會計準則更新(“ASU”)“2014-09年與客户的合同收入(主題606)”(“ASC 606”)。根據這一方法,該公司在通過日期 將ASC 606應用於許可證協議,並被要求對2018年9月1日開始累積赤字餘額進行調整,所有以前的 期繼續列在ASC 605項下。採用ASC 606最重要的影響是確認與里程碑付款相關的收入的時間(br})的影響。根據ASC 605(這是2018年9月1日之前所有時期適用的權威收入確認 指南),鑑於該公司通過2023年6月提交的預期產品 繼續參與,在公司有權獲得相應付款的期間內確認了與許可證協議有關的金額,並在賺取費用的期間內使用基於時間的模式方法確定了預期的產品提交日期。然而,根據ASC 606,公司必須確認交易總價格(包括在滿足識別標準後與里程碑相關的 考慮),在此期間,公司必須使用輸入法確認交易價格(包括與里程碑相關的 考慮)-履行了履約義務。因此,一旦在交易 價格中包含了與里程碑相關的考慮因素,就會立即根據完全滿足執行義務 的時間來確認增量收入。這種方法比ASC 605早確認收入,由此產生的影響 記錄為2018年9月1日累積赤字期初餘額的減少,詳見下文。
8
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註1-重大會計政策(續):
根據ASC 606,該公司在協議中確定了一個單一的執行 義務,並確定許可證和服務並不不同,因為許可證和服務彼此高度依賴。換句話説,如果沒有相關服務,HTIT就不能從許可證中獲益,反之亦然。
由於客户隨着 實體的執行而從服務中受益,收入將通過2023年6月的預期產品提交日期(使用輸入法)來確認。 公司使用輸入方法來衡量此過程,以識別收入,這與直接的 線屬性接近。公司在確定產品提交日期時使用了重要的判斷。
根據ASC 606,公司在實現合同里程碑(視未來事件的發生而定)時有權獲得的考慮是一種可變的考慮形式。在評估將包含在交易價格 中的此類里程碑相關考慮的部分(如果有的話)時,公司首先評估每個里程碑的最可能結果,並排除與發生的事件不被視為最可能的結果的與里程碑相關的考慮因素( )。
然後,公司評價在第一步中確定的任何可變代價 是否受到限制,在交易價格變量中列入考慮因素,使其 有可能在隨後解決與可變代價相關聯的不確定性時,不發生所確認的累積收入數額的重大逆轉。公司在確定可變考慮的第一步時使用了重要的判斷。
潛在的未來版權費考慮也被認為是ASC 606下可變考慮的一種形式,因為它基於公司產品未來潛在銷售的百分比。 但是,公司適用基於銷售的版權費例外情況,因此在相關銷售發生時將確認基於銷售的版權費金額。到目前為止,本公司尚未確認任何與特許權使用費有關的收入.
截至收養日,由於可變考慮的影響,公司將其累計 赤字從合同負債中調整了1,773美元。
截至2019年11月30日,分配給許可證協議 的金額共計22 382美元,所有這些都是通過資產負債表日期收到的。截至2019年11月30日,公司確認了與該協議有關的收入總額為10 696美元(其中674美元在2019年11月30日終了的季度中被確認為 ),並推遲了其餘的11 686美元,後者作為合併資產負債表上的遞延收入列報。
9
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註1-重大會計政策(續):
| d. | 金融工具 |
2016年1月,財務會計準則委員會(“FASB”)發佈了指南,更新了確認、計量、列報 和披露金融資產和金融負債的某些方面(“ASU 2016-01”)。該指南要求各實體確認公允價值在淨收入中的變化,而不是在累積的其他綜合收入中的變化。該公司在2019年財政年度第一季度採用了 這一更新的規定。自2018年9月1日起,該公司將可出售證券的 歸類為按公允價值通過損益計量的金融資產。這一收養對公司截至收養日累計虧損的影響為702美元。
| e. | 合併財務報表的編制 |
此處包括 在內的精簡合併財務報表是按照美國普遍接受的會計原則(“美國公認會計原則”)和附註1f所述的情況編制的,其基礎與公司2019年8月31日終了會計年度10-K表的審定合併財務報表(“2019表10-K”)相同。這些精簡的合併的 財務報表反映了所有的調整,這些調整具有正常的經常性性質,並被認為是公平的所列期間結果的 報表所必需的。通常列入年度合併財務報表的某些信息和披露已根據證券和交易委員會的規則和條例在本中期報告中省略。由於精簡的合併中期財務報表沒有包括美國公認會計準則對年度財務報表所要求的所有信息和 披露,因此應結合2019年表格10-K所載經審計的合併的 財務報表和附註一併閲讀。中期的結果不一定表示整個財政年度的結果。
| f. | 最近採用的標準 |
2016年2月,FASB發佈了題為“租賃 (主題842)”的ASU第2016-02號,取代了現有的租賃會計準則-租約(主題840)。新標準要求 a承租人在其資產負債表上記錄所有12個月以上租約的資產和負債。租賃將被歸類為融資或經營,分類影響到承租人的 收益表中的費用確認模式。該公司從2019年9月1日起在修訂的追溯基礎上採用了這一標準,並且不會重新聲明比較期。該公司選出了在 過渡指導下允許的一攬子實際權宜之計,該新標準除其他外,允許公司進行歷史租賃分類。公司進行了會計政策選擇,將最初期限為12個月或更短的租約保留在資產負債表之外。公司 在租賃期內直線業務報表中確認了這些租賃付款。
截至通過之日,截至2019年9月1日,公司在其資產負債表上確認經營 租賃資產和負債分別為113美元和113美元。
10
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
説明2-承諾:
| a. | 2011年3月,該子公司將其被投資公司Entera的股份出售給D.N.A,保留了117 000股普通股(在2018年7月實施了Entera公司的股票分割之後)。在考慮出售給D.N.A的股份時,除其他付款外,公司還收到了D.N.A的普通股(另見注 4)。 |
作為該協議的一部分,該附屬公司簽訂了一項專利轉讓協議(“專利轉讓協定”),根據該協議,指定給Entera 的附屬公司在與口頭管理自2010年8月以來已向Entera發放的蛋白質有關的某項專利申請中擁有所有權利、所有權和權益。根據這一協議,附屬公司有權從Entera特許使用費 收取Entera 3%的淨收入(如協議所定義),並獲得該專利申請的許可證,用於糖尿病和流感的 。截至2019年11月30日,Entera尚未實現任何收入,也未向該子公司支付任何特許權使用費。2018年12月11日,Entera宣佈與Amgen簽訂了研究合作和許可協議 (“Amgen許可證”),涉及炎症性疾病和其他嚴重疾病的研究。據報告,根據Amgen許可證的條款,Entera將從Amgen收取少量的初步技術訪問費,並將負責安進的臨牀前發展。如果 Amgen決定將所有這些項目向前推進,Entera將有資格獲得高達27萬美元的總計 付款,以及高達中個位數的分級版税。安進是負責臨牀發展,製造和商業化 的任何結果項目。如果安進許可證產生專利轉讓協議所界定的淨收入,則該子公司將有權獲得上述特許權使用費。
此外,作為2011年2月15日與第三方 的諮詢協議的一部分,附屬公司有義務支付2011年3月出售給Entera的專利淨使用費 的8%。
| b. | 2017年1月3日,該子公司就其在以色列的辦公設施簽訂了租賃協議。租約有效期為60個月,自2016年10月1日起生效。 |
從2016年10月至2018年9月,年度租賃付款為新以色列謝克爾119 000(32美元),2018年10月至2021年9月為132 000新謝克爾(38美元),並與以色列消費價格指數(“CPI”)的上漲掛鈎(截至2019年11月30日,根據2019年11月30日的匯率計算,未來租賃付款總額為70美元)。
作為對這一租賃協議義務的擔保,該公司提供了相當於三個月租賃付款的銀行擔保。
11
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
説明2-承諾(續):
| c. | 2017年12月18日,該子公司與一家供應商達成協議,開發和生產其一種口服膠囊成分,金額為2 905美元,將在訂婚期間支付,並以實現某些發展里程碑為基礎,其中1 542美元已在截至2019年11月30日的研發費用中得到確認。 |
| d. | 2018年2月14日,該附屬公司與第三方簽訂了“臨牀研究組織服務協議”,自2017年11月1日起生效,以保留其作為臨牀研究組織(“CRO”)的地位,用於該公司為2型糖尿病患者口服胰島素膠囊的三個月劑量範圍的臨牀試驗,並於2019年5月20日對該協議進行了修正。作為對其服務的考慮,該子公司將在聘用期間並根據某些里程碑的實現情況,向CRO支付總額為10,206美元的款項,其中8,003美元在截至2019年11月30日的研發費用中得到確認。 |
| e. | 2018年5月21日,該子公司與第三方簽訂了CRO服務協議,將其保留為CRO,用於其口服胰島素膠囊的食品效應臨牀試驗。作為對其服務的考慮,該附屬公司將在聘用期間並根據某些里程碑的實現情況,向CRO支付總額為1 166美元的款項,其中1 141美元在截至2019年11月30日的研發費用中得到確認。 |
| f. | 2019年7月29日,該子公司與第三方簽訂了CRO服務協議,將其保留為CRO,用於其口服胰島素的劑量範圍廣泛的臨牀試驗。作為對其服務的考慮,該子公司將在聘用期間並根據某些里程碑的實現情況,向CRO支付總額658美元的款項,其中313美元在截至2019年11月30日的研發費用中得到確認。 |
| g. | 以色列創新管理局(IIA)的贈款 |
根據該公司從 IIA提供的資金條件,從如此供資的項目開發的產品的銷售應支付3%的特許權使用費,最高數額相當於所收到贈款的100%-150%(與美元掛鈎),並按倫敦銀行同業拆借利率增加利息。
在收到贈款時,有關項目的成功開發沒有得到保證。截至2019年11月30日收到的總額為2,207美元。
與已供資的 項目有關的特許權使用費費用在2019年11月30日終了的季度和以前各期的收入成本中得到確認。
| h. | 歐洲聯盟委員會(“歐共體”)的贈款 |
2019年11月26日,該公司收到歐共體根據“2020年歐洲創新方案地平線”的中小企業工具支付的初步付款17.50歐元。
作為贈款條款的一部分,公司必須在歐洲使用贈款的收益。該公司打算利用這筆贈款,探討在歐洲進行臨牀 試驗的可能性。
12
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註3-公允價值:
公司計量公允價值,公開金融資產公允 價值計量。公允價值是基於在計量日市場參與者之間有秩序的 交易中出售資產所收到的價格。為了提高公允價值 計量的一致性和可比性,指南建立了一個公允價值等級,將用於衡量 公允價值的可觀測和不可觀測的投入分為三大層次,其描述如下:
| 第1級: | 在資產或負債的計量日,活躍市場的報價(未經調整)。公允價值層次結構給予1級輸入最高優先級。 |
| 2級: | 根據不包括在一級內的報價以外的投入而直接或間接觀察到的資產或負債的可觀測價格的可觀察價格。 |
| 第3級: | 當很少或根本沒有市場數據時,使用不可觀測的輸入。公允價值層次結構給予3級輸入最低優先級。 |
截至2019年11月30日,按 公允價值計量的資產由股票證券(一級)構成。附註4所列持有至到期債券的公允價值是基於第2級計量的 。
截至2019年11月30日,由於這些票據的短期期限, 現金等價物、短期存款和應付賬款的賬面價值接近其公允價值。
截至2019年11月30日,由於市場利率的規定,長期存款的賬面金額接近其公允價值。
為僱員權利提供資金的數額 按現金退還價值列報,接近其公允價值。
在截至2019年11月30日和2018年11月30日的三個月 期內,沒有第三級項目。
13
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註4:有價證券:
公司的有價證券包括對D.N.A和Entera的股票證券和持有至到期債券的投資。
| a. | 組成: |
十一月三十日, 2019 | 八月三十一日 | |||||||
| 短期: | ||||||||
| D.N.A(見下文b) | $ | 296 | $ | 557 | ||||
| Entera(見下文c) | 263 | 304 | ||||||
| 持有到期日債券(見下文d) | 2,648 | 2,840 | ||||||
| $ | 3,207 | $ | 3,701 | |||||
| 長期: | ||||||||
| 持有到期日債券(見下文d) | $ | 250 | $ | 1,295 | ||||
| b. | D.N.A |
D.N.A普通股在特拉維夫證券交易所交易。這些證券的公允價值按計量日的證券報價計算。
截至2019年11月30日,該公司擁有D.N.A公司流通股的6.9%左右。
截至2019年11月30日和2019年8月31日的證券成本為595美元。
| c. | 腸 |
Entera普通股自2018年6月28日以來一直在納斯達克資本市場交易。公司從該日起按公允價值計量投資,因為它有一個易於確定的 公允價值(在此日期之前,該投資被記為成本法投資(共計1美元))。
14
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註4-有價證券(續):
| d. | 持有至到期證券 |
截至2019年11月30日,持有至到期日證券的攤銷成本和估計公允價值如下:
| (2019年11月30日) | ||||||||||||
| 攤銷成本 | 未實現損失毛額 | 估計公允價值 | ||||||||||
| 短期: | ||||||||||||
| 商業債券 | $ | 2,624 | $ | (16 | ) | $ | 2,608 | |||||
| 應計利息 | 24 | - | 24 | |||||||||
| 長期 | 250 | - | 250 | |||||||||
| $ | 2,898 | $ | (16 | ) | $ | 2,882 | ||||||
截至2019年11月30日,被歸類為持有到期日的債務證券的合同期限 如下:一年至兩年後,250美元,到期收益率為2.77%。
截至2019年8月31日,持有至到期日證券的攤銷成本和估計公允價值如下:
| 八月三十一日 | ||||||||||||
| 攤銷成本 | 未實現損失毛額 | 估計公允價值 | ||||||||||
| 短期: | ||||||||||||
| 商業債券 | $ | 2,808 | $ | 6 | $ | 2,814 | ||||||
| 應計利息 | 32 | - | 32 | |||||||||
| 長期 | 1,295 | 4 | 1,299 | |||||||||
| $ | 4,135 | $ | 10 | $ | 4,145 | |||||||
截至2019年8月31日,被歸類為持有至到期的債務證券的合同期限 如下:一年至兩年後,1,295美元和到期收益率(br}利率介於2.55%至3.20%之間。
持有至到期的證券,在 期間到期,自資產負債表日期起計的12個月,包括在短期可買賣證券中。持有到期日超過一年的到期日被認為是長期有價證券。
15
奧拉梅德製藥公司
附註 精簡合併財務報表
美元(千美元)(除股票 和每股數據外)
(未經審計)
附註5-股東權益:
2019年9月5日,公司根據 訂立了一項股權分配協議(“銷售協議”),公司可根據公司的選擇不時發行和出售公司普通股的股份,其總髮行價最高可達15,000美元,但須符合某些條款和條件。任何出售的股份都將按照公司S-3表格上的有效貨架登記聲明出售,包括一份日期為2017年2月2日的招股説明書,並輔以2019年9月5日的招股説明書補充説明。本公司將向銷售代理支付現金佣金(Br}為銷售協議下通過銷售代理出售的股票收益總額的3.0%。截至2019年11月30日,沒有根據銷售協議出售股票。截至2020年1月9日,根據銷售協議{Br}發行了335,163股,淨收益總額為1,785美元。
附註6-相關各方-交易:
2008年7月1日,該子公司與KNRY有限公司簽訂了兩項諮詢協議。(“KNRY”),一家以色列公司,由首席科學幹事(“CSO”)擁有, 據此首席執行官(“首席執行官”)和民間社會組織通過KNRY向該公司提供服務(“諮詢協議”)。諮詢協議在書面通知前140天由任何一方終止。經修訂的諮詢協議規定,KNRY將得到補償,以支付與執行諮詢協議有關的合理費用,每月付給首席執行幹事和CSO的諮詢費分別為127,570新謝克爾(37美元)和80,454新謝克爾(23美元), 。
除了諮詢協議之外,該公司還根據ORI-組織資源國際有限公司編寫的搬遷成本分析報告,支付因首席執行官遷至紐約而產生的某些直接費用、相關税收和費用。在截至2019年11月30日的三個月期間,此類搬遷費用共計86美元,而截至2018年11月30日的3個月為131美元。
16
項目2-管理層對財務狀況和經營結果的討論和分析
以下對我們財務狀況和業務結果的討論和分析,應與本報告其他地方所載的合併財務報表(br}和相關附註以及我們的合併財務報表、所附附註和“管理部門對財務狀況和業務結果的討論和分析”一併閲讀,這些説明和分析載於我們的年度報告(見下文)。
前瞻性陳述
本季度報告中關於表10-Q的陳述不是歷史事實,是1995年“私人證券訴訟改革法”和其他聯邦證券法意義上的“前瞻性陳述”。“預期”、“預期”、“打算”、“計劃”、“計劃支出”、“認為”、“尋求”、“估計” 等詞以及類似的詞語或變體,都是為了識別前瞻性語句,但不認為 代表一種包括識別前瞻性報表的所有手段,如本季度表10-Q報告中所指的前瞻性報表。此外,關於未來事項的 聲明是前瞻性聲明.我們提醒讀者,前瞻性聲明僅僅是 預測,因此必然受不確定因素和其他因素的影響,涉及已知和未知的風險,這些風險可能導致實際結果、績效、活動水平、或我們的成就或行業成果與任何未來的結果、業績、活動水平、或我們的成就或行業成果(這些前瞻性陳述所表達或暗示的)大不相同。這些前瞻性發言除其他外,包括關於下列方面的發言:
| ● | 我們的 產品在治療糖尿病方面的預期發展和潛在利益; |
| ● | 與其他公司或醫療機構簽訂更多許可證協議或其他夥伴關係或合作形式的前景; |
| ● | 與合肥天輝科技有限公司簽訂的許可協議下的未來里程碑、條件和特許權使用費, 或HTIT; |
| ● | 我們的研究和發展計劃,包括臨牀前和臨牀試驗計劃和註冊時間,取得 結果和試驗結論,包括但不限於,我們對我們將開始第三階段臨牀 試驗的期望,以及我們以後提出一項新的藥物應用的期望; |
| ● | 我們相信,我們的技術有潛力口頭提供藥物和疫苗,而今天只能通過注射才能提供藥物和疫苗; |
| ● | 以技術為基礎的產品效能、安全性、病人方便性、可靠性、價值和專利地位的競爭能力; |
| ● | 潛在的市場需求,我們的產品; |
| ● | 我們期望在未來的一年裏,我們的研發開支淨額將繼續成為我們的主要支出; |
| ● | 我們對短期和長期資本需求的期望; |
| ● | 我們對未來幾個月和未來時期的展望,包括但不限於我們對未來收入和支出的預期;以及 |
| ● | 有關我們業務的任何其他計劃和策略的信息。 |
17
儘管這個 季度的前瞻性語句 表格10-Q的報告反映了我們管理層的誠信判斷,這樣的陳述只能基於我們目前所知道的事實和因素。因此,前瞻性陳述本身就受制於風險和不確定性 ,實際結果和結果可能與前瞻性 語句中討論或預期的結果和結果大不相同。可能導致或促成這種成果和結果差異的因素包括(但不限於)在標題1A下具體述及的 因素。風險因素“在截至2019年8月31日的 財政年度的表10-K的年度報告中,或我們於2019年11月27日向證券交易委員會或證券交易委員會提交的年度報告中,以及在我們的年度報告其他地方討論並不時在我們向 SEC提交的其他文件中表達的風險因素。此外,科學研究、臨牀和臨牀前試驗的歷史性成果並不能保證未來研究或試驗的 結論不會提出不同的結論。此外,根據額外的研究、臨牀及臨牀前試驗結果,本季刊(br}表格10-q報告所提及的歷史性結果,可根據額外的研究、臨牀及臨牀前試驗結果而作出不同的解釋。 表格10-Q報告 。除法律規定外,我們沒有義務修改或更新任何前瞻性陳述,以便 反映本季度報告表10-Q之後可能出現的任何事件或情況。我們促請讀者仔細檢討及考慮整季所作的各種披露。 報告表格 10-Q試圖就可能影響我們的業務、財務狀況、經營結果和前景的風險和因素向有關各方提出建議。
業務概覽
我們是一家制藥公司,目前正在研究和開發創新的藥物解決方案,包括用於治療糖尿病患者的口服胰島素膠囊,以及使用口服可攝取的膠囊運送其他多肽。我們利用臨牀研究組織(CROS)來進行我們的臨牀研究。
最近的業務發展
產品候選
口服胰島素我們正在尋求通過我們的專利旗艦產品ORMD-0801改變對糖尿病的治療,我們的技術允許胰島素從胃腸道經由門靜脈進入血液,徹底改變胰島素的傳遞方式。它能以比目前給藥方法更生理的方式通過 胰島素。我們的技術是一個平臺,有可能口頭提供藥物和疫苗,而今天只能通過注射來提供藥物和疫苗。
FDA指南:2017年8月,在與美國食品和藥物管理局(FDA)的電話中,我們被告知,提交ORMD-0801 的監管途徑將是生物製劑許可證申請(BLA)。如果獲得批准,BLA途徑將允許我們從批准之日起為ORMD-0801提供12年的營銷專賣權,如果該產品也獲得用於兒科病人的 批准,我們還可以獲得6個月的獨家銷售許可。FDA證實,非臨牀毒理學、化學制造 控制和輔料鑑定的方法將由其公佈的指導文件驅動。
階段 IIb研究:2018年5月,我們啟動了ORMD-0801的三個月劑量範圍II期臨牀試驗.這一安慰劑對照, 隨機,90天的治療臨牀試驗是在美國全國多箇中心的269名2型糖尿病患者進行的,依據的是FDA的調查新藥物應用程序(Ind)。試驗的主要終點是評估ORMD-0801在90天治療期間對HbA1c水平的影響。試驗的次要終點 包括在混合餐耐受性試驗中測定空腹血糖或FPG、餐後血糖或ppg水平、 或mmmtd和體重。在2019年5月,我們開始對大約75名2型糖尿病患者延長這一方案,他們使用較低劑量的 劑量。我們期望在2020年曆年第一季度收到這項研究的最後報告。
18
在2019年11月,我們宣佈了第IIb階段試驗的初步結果。隨機進入每日ORMD-0801的患者平均HbA1c比基線降低0.60%,或經安慰劑調整後減少0.54%(p值=0.036)。這0.54%的減少HbA1c 被認為是有臨牀意義的。與安慰劑相比,ORMD-0801的治療顯示出很好的安全性,沒有嚴重的與藥物相關的 不良事件,也沒有增加低血糖發作的頻率。此外,在這90天的試驗中,沒有觀察到體重增加.在最初的隊列中,269名以美國為基礎的患者接受了劑量遞增的 方法治療:16毫克初始劑量,滴定至24毫克/劑量,然後滴定至32毫克/劑量。將患者隨機分為三組,分別為每日一次(32 mg/d)、每日兩次(64 mg/d)、每日三次(96 mg/d)。每個治療臂都有相應的安慰劑。209例患者完成治療至12周終點 ,並納入數據分析(24名受試者未完成整個12周的治療)。此外,由於證據 的治療中心相互作用,兩個位點(36名患者(佔在冊受試者的13.4%)被排除在統計分析 ,因為他們顯示的結果與其他有統計學意義的結果相反。我們仍在調查造成這一差異的原因。
每日一次和兩天兩次的武器分別比A1C的基線 減少0.60%(安慰劑調整為0.54%)和0.59%(安慰劑調整為0.53%)(p值分別為0.036和0.042)。每日三次臂 不符合統計學意義(p-值0.093).
FDA同意於2020年2月4日舉行第二階段會議的初步結束,以審查化學制造和控制(CMC)的各個方面。第二階段會議的第二次會議將側重於臨牀方面,預計在2b階段試驗的低劑量組 公佈數據之後。
我們預計將開始對1型和2型糖尿病患者進行第三階段臨牀試驗,預計將在2020年曆年的下半年開始。在這些試驗之後,我們希望在2024年的日曆結束前提交一份可能獲得FDA批准的BLA。
夾鉗研究:2018年6月,我們發起了一項葡萄糖鉗夾研究,該研究應該量化使用ORMD-0801治療的糖尿病患者的胰島素吸收。葡萄糖鉗是一種定量胰島素吸收的方法,用於測量病人的胰島素敏感性和病人代謝葡萄糖的情況。這項探索性的、隨機的、雙盲的葡萄糖鉗夾研究正在評估使用ORMD-0801治療的1型糖尿病患者的暴露-反應譜。6名A1C水平在10%或10%以下的患者,年齡在18-50歲之間,參加了這項研究。我們期望在2020年第一季度收到這項研究的最後報告。
食物效應研究:2018年6月,我們啟動了ORMD-0801食品效應試驗。這一單盲、五週期、隨機、安慰劑對照的交叉試驗正在評估在不同時間服用的ORMD-0801與健康志願者和1型糖尿病患者膳食關係中的藥代動力學(PK)和藥效學。48(48)名患者,包括24名健康志願者和24名1型糖尿病患者.我們期望在2020年的第一季度收到這項研究的最後報告。
納什研究:2018年10月,我們開始了一項關於非酒精性脂肪性肝炎(NASH)2型患者ORMD-0801的探索性臨牀研究。由以色列衞生部批准的為期三個月的治療研究將評估ORMD-0801對30例NASH患者降低肝臟脂肪含量、炎症和纖維化的效果。應以色列衞生部的要求,這項研究的第一部分將對10名參加者進行,預計將在2020年曆年第一季度完成。
毒理學研究(6個月):在2019年3月,我們完成了為期6個月的ORMD-0801劑量毒理學研究,該研究是在FDA的請求下於2018年9月啟動的。我們期望在2020年曆年第一季度收到這項研究的最後報告。
第一類研究:在2019年11月,我們發起了一項1型糖尿病患者的交叉研究,以比較每日一次的ORMD-0801與每日三次的ORMD-0801的效果。這項研究預計將包括26個主題,預計將於2020年第一季度完成。
19
口服胰高血糖素樣肽-1胰高血糖素樣肽-1(GLP-1)是一種促分泌胰島素的內分泌激素.此外,還發現 GLP-1可抑制胰高血糖素的釋放(一種參與調節葡萄糖的激素),減緩胃 排空,以減少營養物質在血液中的吸收速度,增加飽腹感。GLP-1的其他重要有益屬性 是其增加胰腺β細胞(製造和釋放胰島素的細胞)數量的作用,也可能是保護心臟的作用。除了我們的旗艦產品ORMD-0801胰島素膠囊,我們正在使用我們的技術 口服可食用的GLP-1膠囊,或ORMD-0901。
在2019年2月,我們完成了一項 第一階段PK試驗,以評價ORMD-0901與安慰劑相比的安全性和藥動學。我們期望在2020年的第一季度收到這項研究的最後報告。這項研究是根據IND進行的,我們預計隨後將進行進一步的生物利用度研究(預期結果在歷年 2020),並對2型糖尿病患者進行第二階段試驗,該試驗很可能將在美國根據IND進行。
其他產品
我們最近開始開發一種新的藥物 候選,以口服瘦素膠囊的形式進行減肥治療。我們預計在2020年的第一季度,我們的口服瘦素藥物候選藥物的概念、單劑量 研究將對10例1型糖尿病成人患者的藥效學和藥效學(胰高血糖素減少)進行評估。我們期望在2020年曆年的上半年收到這項研究的最後報告。
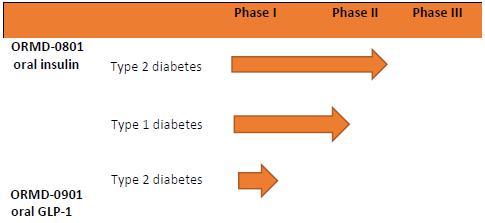
下表概述了我們的 初級產品管道:

無牌技術
2015年11月30日,我們與我們的以色列子公司 和HTIT簽訂了一項技術許可協議,2015年12月21日,這些締約方簽訂了一項經修正和恢復的技術許可協議,該協議於2016年6月3日和2016年7月24日或許可協議中被雙方進一步修正。 根據許可協議,我們在中華人民共和國、澳門和香港或該領土的領土內授予了HTIT獨家商業化許可證,涉及我們的口服胰島素膠囊ORMD-0801,或者產品。根據 許可證協議,HTIT將自費對我們子公司的技術和ORMD-0801膠囊進行某些商業化前和監管活動,並將支付(I)將由HTIT在該領土銷售的相關商業化 產品淨銷售額10%的版税,或版税;(Ii)總計3750萬美元,其中300萬美元應立即支付 ,800萬美元將由我們與某些第三方簽訂某些協議,在實現某些里程碑和條件後,將支付2 650萬美元。如果我們不能滿足某些條件,可以將 版税率降低到至少8%。在2033年,我們的專利涉及 地區的專利最終到期後,在某些情況下,特許權使用費可能會降低到5%。特許權使用費支付義務應在下列期間內適用:自該產品在領土內首次商業銷售之日起,至其後(I)在該領土上最後到期的特許專利屆滿之時止;及(Ii)該產品在領土內首次商業銷售後15年內。, 或者皇室術語。許可證協議將繼續有效,直到 皇家任期屆滿。“許可證協定”載有習慣上的終止條款。截至2019年11月30日,在3750萬美元的總額中,我們總共收到了2050萬美元的里程碑付款。
20
2015年11月30日,我們還與HTIT(SPA)簽訂了一份單獨的證券採購協議,根據該協議,我們於2015年12月向HTIT發行了1,155,367股我們的普通股 股票,總價為1,200萬美元。關於許可證協議和SPA,我們收到了一筆500,000美元的非商店費用。
業務結果
2019和2018年11月30日終了三個月期間的比較
下表彙總了公司截至2019年11月30日和2018年11月30日三個月期間業務數據的某些報表(除 股和每股數據外,以千美元計):
| 三個月結束 | ||||||||
| 十一月三十日, | ||||||||
| 2019 | 2018 | |||||||
| 收入 | $ | 674 | $ | 674 | ||||
| 收入成本 | - | 35 | ||||||
| 研發費用 | 2,022 | 4,347 | ||||||
| 一般和行政費用 | 1,081 | 932 | ||||||
| 財務收入淨額 | 114 | 338 | ||||||
| 這一期間的淨虧損 | $ | 2,543 | $ | 4,302 | ||||
| 普通股虧損-基本損失和稀釋損失 | $ | 0.15 | $ | 0.25 | ||||
| 加權平均普通股 | 17,472,315 | 17,448,744 | ||||||
收入
收入包括與許可證協議 有關的收益,這些收益是在可能不會通過使用輸入法的預期產品提交日期2023年6月實現確認的 累積收入的情況下累計確認的。
在截至2019年11月30日和2018年11月30日的三個月期間,每個月的收入都是67.4萬美元。
收入成本
收入成本包括與許可證協議有關的特許權使用費,這些使用費將根據收入確認會計和1984年“鼓勵工業研究、發展和技術創新法”(經修訂)在許可證協定的期限內支付,包括根據該協定頒佈的任何條例或軌道。
截至2019年11月30日的三個月期間沒有收入成本,而2018年11月30日終了的三個月期間的收入為3.5萬美元。減少的原因是,在截至2018年11月30日的三個月內,將許可證協議下的額外里程碑付款列入交易價格,作為ASC 606實施 的一部分。
21
研發費用
研究和開發費用包括直接歸因於進行研究和開發方案的費用,包括工資、僱員福利、材料、用品的費用、外部承包商提供的服務的費用,包括與我們的臨牀 試驗有關的服務、臨牀試驗費用、製造用於研究和臨牀前開發的藥品的全部費用。與研究和開發有關的所有 費用均按已發生的費用計算。
臨牀試驗費用是研究和開發費用的重要組成部分,包括與第三方承包商有關的費用。我們將我們的臨牀試驗活動的很大一部分外包出去,利用外部實體,如合同研究機構或CRO、獨立的臨牀 調查人員和其他第三方服務提供商來協助我們進行臨牀研究。
臨牀活動主要涉及臨牀地點和其他管理職能,以管理我們的臨牀試驗主要是由CRO執行。CRO通常為我們的試驗執行大部分的啟動活動,包括文件準備、站點識別、篩選和準備、 學習前訪問、培訓和項目管理。
臨牀試驗和臨牀前試驗費用包括管理和科學顧問的薪酬和費用、研究費用、材料採購、膠囊製造費用、病人招募和治療費用以及研究和開發工作人員的工資和相關費用。
截至2019年11月30日的三個月期間的研究和開發費用減少了53%,從2018年11月30日終了的三個月期間的4 347 000美元降至2 022 000美元。這一減少主要是由於我們的IIb階段三個月臨牀試驗的費用減少,並被與監管諮詢有關的費用增加部分抵消。截至2019年11月30日的三個月期間,以股票為基礎的補償費用共計95,000美元,而2018年11月30日終了的三個月期間為39,000美元,增加的主要原因是在截至2019年11月30日的三個月內增加了新的贈款。
政府贈款
在截至11月30日、2019年和2018年的三個月期間,我們沒有承認任何研究和開發贈款。截至2019年11月30日,我們向以色列經濟和工業部以色列創新管理局支付了354 000美元的使用費。
一般和行政費用
一般費用和行政費用包括我們的管理人員的薪金和有關費用、諮詢費用、法律和專業費用、旅費、業務發展費用、保險費用和其他一般費用。
截至2019年11月30日的三個月期間的一般開支和行政費用從2018年11月30日終了的三個月期間的932 000美元增加到1 081 000美元,增加了16%。與一般活動和行政活動有關的費用增加的主要原因是法律 費用增加。截至2019年11月30日的三個月期間,股票補償費總額為184,000美元,而2018年11月30日終了的三個月期間為199,000美元( )。減少的主要原因是2020財政年度向僱員和董事發放的 獎勵的攤銷進展,並因2019年財政年度頒發的獎勵增加而部分抵消。
22
財務收入淨額
淨財務收入減少66%,從2018年11月30日終了的三個月期間的338,000美元下降到2019年11月30日終了的三個月期間的114,000美元。減少的主要原因是,由於現金投資減少,銀行存款和持有到期日 債券的收入減少,D.N.A生物醫學解決方案有限公司和Entera Bio有限公司普通股的公允價值下降。
流動性和資本資源
從成立到2019年11月30日,我們總共遭受了83,646,000美元的損失。在此期間,到2020年1月9日,我們通過幾次私募普通股以及公開發行普通股為我們的業務提供資金,除交易費用外,共籌集了79 521 000美元。在此期間,我們還收到 行使認股權證和期權的現金5 889 000美元。到2019年11月30日,我們有3,171,000美元的可用現金,23,755,000美元的短期銀行存款和3,457,000美元的可流通證券。
管理層繼續評價各種籌資備選辦法,以資助今後的研究和開發活動,並通過在公共或私人股本市場籌資籌措 的一般和行政開支。雖然沒有保證我們將在這些倡議中取得成功,但管理部門 認為,由於今後的第三方投資,它將能夠獲得必要的資金。根據我們目前的現金資源和承諾,我們認為我們將能夠至少在今後12個月及以後維持我們目前計劃的發展活動和相應的支出水平。
截至2019年11月30日,我們的流動資產總額為30,742,000美元,流動負債總額為4,641,000美元。2019年11月30日,我們的營運資本盈餘為26,101,000美元,累計虧損83,646,000美元。截至2019年8月31日,我們的流動資產總額為33,324,000美元,流動負債總額為5,308,000美元。2019年8月31日,我們的營運資本盈餘為28,016,000美元,累計虧損為81,103,000美元。流動資金從2019年8月31日至2019年11月30日的減少主要是由於業務活動中使用的現金。
在截至2019年11月30日的三個月期間,現金和現金等價物從截至2019年8月31日報告的3 329 000美元減少到3 171 000美元,原因如下:
在2019年11月30日終了的三個月期間,業務活動使用的現金為2 996 000美元,而2018年11月30日終了的三個月期間使用的現金為4 131 000美元。用於業務活動的現金主要包括研究和開發以及一般和 行政費用造成的淨損失,以及由於許可證協議而引起的合同負債的變化,並由應付帳款和應計費用的變化部分抵銷。
在2019年11月30日終了的三個月期間,投資活動提供了2 825 000美元的現金,而2018年11月30日終了的三個月期間提供的現金為2 995 000美元。投資活動提供的現金主要包括短期存款的到期日和持有至到期的 證券,並被購買短期存款部分抵銷。
供資活動在2019年11月30日終了的三個月期間提供了13 000美元的現金,而在2018年11月30日終了的三個月期間沒有提供現金。2019年11月30日終了的三個月期間的籌資活動包括由於行使期權而發行12 253股普通股的淨收益總額12 253美元。
2019年9月5日,我們簽訂了“銷售協議”,根據該協議,我們可以根據自己的選擇,不時發行和出售我們普通股的股票,其總髮行價最高可達15,000,000美元,通過銷售代理,但須遵守某些條款和條件。任何出售的股票將根據我們在表格S-3上的有效貨架登記聲明出售,包括一份日期為2017年2月2日的招股説明書,並由2019年9月5日的招股説明書補充 。根據銷售協議,我們將向銷售代理支付銷售總收益的3.0%的現金佣金。截至2019年8月31日和2020年1月9日,沒有根據“銷售協議”出售 股和335 163股,淨收益總額分別為零和1785362美元。
23
表外安排
截至2019年11月30日,我們沒有任何表外安排已經或我們預期有可能對我們的財務狀況、財務狀況的變化、收入或支出、經營結果、流動資金、資本支出或資本資源產生重大影響。
關鍵會計政策和估計數
我們的重要會計政策在截至2019年8月31日的合併財務報表附註中作了説明,並在本季度報告(表10-Q)所載的合併財務報表附註中作了説明。
計劃支出
我們在研究和開發上投入了大量資金,我們預計在今後的幾年裏,我們的研究和開發費用將繼續成為我們的主要經營費用。
項目3-關於 市場風險的定量和定性披露
在截至2019年11月30日的季度內, 我們的市場風險敞口沒有顯著變化。有關我們面對市場風險的討論,請參閲年報第II部第7A項“市場風險的定量及定性披露”。
項目4-管制和程序
披露控制和程序
截至2019年11月30日,我們的管理層,包括我們的首席執行官(首席執行官)和首席財務官(首席財務官),評估了我們的披露控制和程序的有效性。基於這一評估,我們的首席執行官和首席財務官得出結論,我們的披露控制和程序是有效的。
財務報告內部控制的變化
在截至2019年11月30日的季度內,我們對財務報告的內部控制 沒有發生重大影響,也沒有可能對財務報告的內部控制產生重大影響。
24
第二部分-其他資料
第二項-未登記的股本證券出售及收益使用
2019年9月10日,我們向公司簡介(LLC)或公司簡介發行了2,500股普通股(Br},用於支付根據我們與公司概況(2018年4月8日)和公司簡介({BR}或信函協議)欠公司簡介的投資者關係服務諮詢費的一部分。
在2019年11月1日,我們發行了2500股我們的普通股到公司簡介,以支付部分投資者關係服務顧問費,根據書面協議欠 公司簡介。
我們根據1933年“證券法”第4(A)(2)節所載的豁免註冊發行這些股份。
項目6-展品
| 數 | 陳列品 | |
| 10.1* | 日期為2019年12月19日的“就業協定”第一修正案於2019年5月16日由Oramed有限公司和Avraham Gabay公司和Avraham Gabay公司簽署。 | |
| 10.2* | Oramed製藥公司賠償協議的代表形式。以及我們的每一位董事和官員。 | |
| 31.1* | 根據經修訂的1934年“證券交易法”第13a-14(A)條和第15d-14(A)條認證首席執行官。 | |
| 31.2* | 根據經修訂的1934年“證券交易法”第13a-14(A)條和第15d-14(A)條認證首席財務官。 | |
| 32.1** | 根據“美國法典”第1350條認證首席執行官。 | |
| 32.2** | 根據“美國法典”第1350條認證首席財務官。 | |
| 101.1* | 以下是公司截至2019年11月30日的第10-Q號季度財務報告中以XBRL格式編制的財務報表:(1)精簡的綜合資產負債表;(Ii)精簡的綜合虧損綜合報表;(Iii)股東權益變動彙總表;(Iv)現金流動合併報表;及(V)精簡的綜合財務報表附註。 |
| * | 隨函提交 |
| ** | 隨函提供 |
25
簽名
根據1934年“證券交易法”的要求,登記人已正式安排由下列簽署人代表其簽署本報告,並經正式授權。
| 奧雷德製藥公司 | ||
| 日期:2020年1月9日 | 通過: | S/Nadav Kidron |
| 納達夫·基隆 | ||
| 總裁兼首席執行官 | ||
| 日期:2020年1月9日 | 通過: | /s/Avraham Gabay |
| 阿夫拉姆·加貝 | ||
| 首席財務官 | ||
| (首席財務及會計主任) | ||
26