
別紙99.1

JPモルガン第42回年次ヘルスケアカンファレンス 1 © 2024 NOVAVAX。全著作権所有。ナスダック:NVAX | 2024年1月

このプレゼンテーションには、将来の見通しに関する記述が含まれています。これらの将来の見通しに関する記述は、一般的に「予想する」、「期待する」、「計画する」、「かもしれない」、「するだろう」、「意志」、「信じる」、「見積もる」、「予測」、「目標」、「プロジェクト」、その他の同様の意味の言葉を使用することで識別できます。これらの将来の見通しに関する記述は、Novavaxの将来、支出率の引き下げ、キャッシュフローの管理、規模と構造の進化などの短期的な優先事項、グローバルなリストラとコスト削減計画の金額と影響、事業計画、目標と展望、2023年と2024年の通年の財務ガイダンス、将来の財務または事業実績、条件または戦略、CZ製造施設の売却の可能性など、さまざまな事項を扱っています、会社のパートナーシップ(とのパートナーシップを含む)R 21/Matrix-Mマラリアワクチンの発売、最新のCOVID-19ワクチン、COVID-19-インフルエンザ併用(CIC)治験用ワクチン候補およびインフルエンザワクチン候補の継続的な開発、ワクチンの提供と配布のタイミング、将来および保留中の規制当局への提出および結果(予想されるUを含む)について。S。更新されたCOVID-19ワクチンの生物製剤ライセンス申請(BLA)、CICワクチン候補をフェーズ3に進めるタイミングとその商業的発売の可能性、予想されるラベルの拡大と市場アクセス、および2024年と将来の世界的なCOVID-19、インフルエンザと混合市場の機会は、将来の見通しに関する記述です。Novavaxは、これらの将来の見通しに関する記述は多くのリスクと不確実性の影響を受けやすく、実際の結果がそのような記述によって明示または暗示されているものと大きく異なる可能性があると警告しています。これらのリスクと不確実性には、2023年から2024年および将来のワクチン接種シーズンに向けた最新のCOVID-19ワクチンの製造、流通、または販売を成功させるNovavaxの能力、適用される規制当局を満たすために必要なプロセス認定、アッセイ検証、安定性試験に関連するものを含む、さまざまな安全性、有効性、および製品特性評価要件を単独で、またはパートナーとともに満たすための課題、実施における課題または遅延が含まれますが、これらに限定されません臨床試験、入手の課題または遅延将来のCOVID-19変異株の変更、COVID-19、インフルエンザ、コンビネーション市場の規模、2023年から2024年および2024年から2025年のワクチン接種シーズン中の潜在的な展開、製造、流通、輸出の遅延または課題、NovavaxのSerum Institute of India Pvtへの独占的依存Ltd. とSerum Life Sciences Limitedは、NovavaxのCOVID-19ワクチンの共同製剤および仕上げのためのPCI Pharma Servicesと、業務の遅延または中断が顧客注文の配送に及ぼす影響、希少な原材料や供給品の入手の難しさ、人的資本や製造能力などの資源の制約、およびNovavaxが単独で、またはパートナーと協力して、計画された規制経路を追求する上でのNovavaxの能力に対する制約管轄区域が同時に発生し、規制当局への提出がずれてしまい、潜在的な可能性も規制措置。米国からの将来の資金の喪失。米国政府、Gaviとの保留中の仲裁を含む紛争における不利な結果の可能性、グローバルなリストラとコスト削減計画の実施における課題、ワクチンまたはワクチン候補の商業的採用、市場アクセス、市場への受け入れを得る際の課題、複数の企業、政府、その他の団体との契約に基づく契約上の要件を満たす際の課題、Novavaxが前払い金の一部を払い戻す必要がある場合がある用量の提供要件を含むと以前のその他の支払いそのような契約に基づいて受け取ったか、将来の支払いが減額されたか、COVID-19、季節性インフルエンザ、その他の病気に対する予防接種の季節性に関連する課題、およびNovavaxの最新のフォーム10-Kの年次報告書およびその後のフォーム10-Qの四半期報告書、およびその後の証券取引委員会への提出書類の「リスク要因」という見出しで特定されたリスク。Novavaxは、このプレゼンテーションに含まれる将来の見通しに関する記述に大きく依存しないように投資家に警告しています。投資家は、Novavaxが証券取引委員会に提出した書類を、www. sec.govおよび当社のWebサイト(www. novavax.com)でご覧になり、これらおよびその他のリスクと不確実性について話し合うことをお勧めします。このプレゼンテーションの将来の見通しに関する記述は、このプレゼンテーションの日付時点での記述であり、当社はこれらの記述を更新または改訂する義務を負いません。私たちの事業は、上記を含め、大きなリスクと不確実性の影響を受けます。投資家、潜在的な投資家、その他は、これらのリスクと不確実性を慎重に検討する必要があります。将来の見通しに関する記述に関する注意事項 2 © 2024 NOVAVAX。全著作権所有。

はじめに SE C T I O N 3 © 2024 NOVAVAX。全著作権所有。

4 © 2024 ノババックス。全著作権所有。「それはただの別の番号です」... それとも?3,000,000 1,300 630,000 情報源:who.int、CDC.gov、OurWorldinData.org。41,000,000 710,000 52,000

5 © 2024 ノババックス。全著作権所有。2021年から2030年の間に予防接種によって5000万人の死亡を防ぐことができます。1980年から2018年の間に、天然痘ワクチン接種だけで1億5,000万人から2億人の命が救われました。出典:CDC.gov、OurWorldInData.org。

6 Novavaxは違いをもたらすためにここにいます。私たちは、感染症と戦うための命を救うワクチンの開発に専念しているバイオテクノロジー企業です。© 2024 NOVAVAX。全著作権所有。私たちが業界として行うことは重要です。私たちは世界中の何百万もの人々の健康にプラスの影響を与えてきましたし、今後もそうし続けます。「人生を創造する以外に、人ができる最善のことは人を救うことです。」エイブラハム・リンカーン「あなたが生きてきたおかげで、人生が一度でも楽になったことを知っています。これは成功したはずです。」ラルフ・ワルド・エマーソン私たちは、世界中の人々の健康を守るために、決して休むことはありません。

どんな概要でもいいです SE C T I O N 7 © 2024 NOVAVAX全著作権所有。

ノババックスコーポレートハイライト 8 © 2024 ノババックス。全著作権所有。実証済みの技術の商業化による長期的な価値創造の立場にあります。独自のマトリックス-M TMアジュバントはパイプラインを差別化しますCOVID-19-インフルエンザの組み合わせ(CIC)ワクチンをフェーズ3、1、実証済みのタンパク質ベースの技術プラットフォームCOVID-19ワクチンを急速に進めています。長期市場でシェアを獲得する位置にあります。完全に統合された商業段階のバイオテクノロジー企業 1.研究デザインに関する規制当局の最終合意が必要です。

グローバルに存在する、完全に統合された商業段階のバイオテクノロジー企業 9 © 2024 NOVAVAX。全著作権所有。グローバル本社とコーポレートオフィス • 研究開発および創薬研究所 • 製造業務 • 商務ノババックス本社 • ノババックス本社 • ゲーサーズバーグ、メリーランド Novavax AB、ウプサラ、スウェーデン Novavax CZ Bohumil、チェコ共和国、インド血清研究所 SK バイオサイエンスタケダ EU コマーシャル・オペレーションズ・チューリッヒ、スイス APAC コマーシャル・オペレーションズ・シンガポール Novavax AB — マトリックス-M アジュバント Novavax CZ — 抗原Novavax Ma nuf acturing北米欧州連合(EU)アジア太平洋(APAC)Novavax Co mm e r c ia l オペレーションズセラムインスティテュートオブインディア(SIII)SKバイオサイエンスタケダスターラット例えば、IC Partners 北米コマーシャル・オペレーションズ、メリーランド州ゲーサーズバーグ
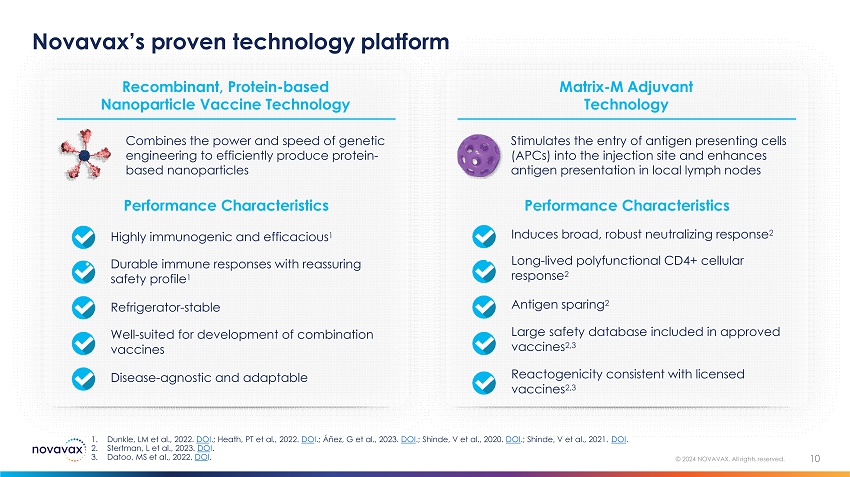
ノババックスの実証済みのテクノロジープラットフォーム 10 © 2024 NOVAVAX。全著作権所有。• 抗原の保存 2 • 承認されたワクチンに含まれる大規模な安全性データベース 2,3 • 認可されたワクチンと一致する反応原性 2,3 マトリックス-M アジュバント技術の性能特性 • 幅広く強力な中和反応を誘導 2 • 長寿命の多官能CD4+細胞反応 2. 抗原提示細胞(APC)の注射部位への侵入を刺激し、局所リンパ節での抗原提示を促進します • 冷蔵庫-安定しています • 混合ワクチンの開発に適しています • 病気-不可知論的で適応性があります組換えタンパク質ベースのナノ粒子ワクチン技術の性能特性 • 高い免疫原性と有効性 1 • 安心できる安全性を備えた持続的な免疫応答 1. 遺伝子工学の力とスピードを組み合わせて、タンパク質ベースのナノ粒子を効率的に製造します 1.ダンクル、LMら、2022年。そうですね。; ヒース、PTら、2022年。そうですね。; アニェス、Gら、2023年。土井。; シンデVら、2020年。土井。; シンデVら、2021年。ドイ。2.スタートマン、Lら、2023年。私がしてください。3.ダトゥー、ミシシッピ州他、2022年。やっぱり。

ノババックスの中核となるワクチンパイプライン将来の発展にとって大きなチャンス 11 © 2024 NOVAVAX全著作権所有。1.一部の地域では、ノババックスCOVID-19ワクチン、アジュバンテッド、コボバックスTM、ヌバクソビッドの商品名で認可されています。2.米国でNovavax COVID-19ワクチン、アジュバント(2023-2024フォーミュラ)という商品名で承認されています。承認後の第3相株-変更試験が進行中です。3.ガーナ、ナイジェリア、ブルキナファソで承認され、インド血清研究所によって商品化され、WHOによって事前認定されました。疾病製剤前臨床フェーズ 1 フェーズ 2 フェーズ 3 認定ノババックスクリニカル-ステージコロナウイルス NVX-CoV2373 1 マトリックス-M 一価XBB.1.5 NVX-CoV2601 2 COVID /インフルエンザ混合ワクチン (CIC) マトリックス-M 季節性インフルエンザ (高齢者) マトリックス-M パートナー臨床-ステージマラリア R21/マトリックス-M アジュバント 3 マトリックス-M

R21/Matrix-世界の公衆衛生上の切実なニーズに応えるのに役立つマラリアに対するMワクチンが承認されました 12 © 2024 NOVAVAX。全著作権所有。非常に効果的なワクチンは、Novavaxのテクノロジープラットフォームの可能性を示しています • NovavaxのマトリックスMアジュバント1を配合 • 2023年12月にWHOによって事前認定され、2024年に発売されました •75%の有効性2で、現在の標準治療を上回っています •WHO局長から「重要なツール」として注目されています-一般3:マラリアは人類史上最も致命的な病気の1つです •4年で63万人が死亡します 1日あたり約1,300人の子供 4 o 5歳未満の子どもがマラリアによる死亡の約 78% を占めました 5 • 経済、社会、健康面での重大な公平性の負担 1.オックスフォード大学によって開発され、インドのセラム研究所によって製造および商品化されました。2.ダトゥー、ミシシッピ州他、2023年。私がしてください。3.2023年10月2日に公開されたプレスリリースは誰ですか。4.OurWorldinData.org。5.誰.int。写真提供:オックスフォード大学「マラリアの研究者として、安全で効果的なマラリアワクチンができる日を夢見ていました。今は2つあります」と、WHO事務局長のテドロス・アダノム・ゲブレエサス博士は言いました。「RTS、Sワクチンの需要は供給をはるかに上回っています。そのため、この2つ目のワクチンは、より多くの子供たちをより早く保護し、マラリアのない未来という私たちのビジョンに近づけるための重要な追加ツールです。」4

2023: 一年の振り返り SE C T I O N 13 © 2024 NOVAVAX全著作権所有。

14 © 2024 ノババックス。無断転載を禁じます。2023年は、強固で持続可能な事業の構築に重点を置いたNovavaxにとって大きな変化の年でした • 規制当局の要件に沿って最新のワクチンを提供しました • APAの約束を果たし、米国市場での経験を積みました • 2026年に開始予定のインフルエンザ/Covid混合ワクチンプログラムのより迅速な前進の道筋を概説しました* 菌株選択と製造プロセスの合理化 CIC開発プログラムを進めるために取られた重要な措置 • 2023年9月30日の時点で、流動負債を約10億ドル削減しましたパンデミック時代の製造コミットメントの解決 • 販管費と研究開発費を2022会計年度と比較して、2023年には25%以上、2024年には55%以上削減する見込みです。ベースラインコストの再編と流動負債の大幅な削減 • CSO、COO、コーポレートアフェアーズの役職の創設、研究開発担当新社長の任命、新しいGCおよびCHROの雇用などの変更 • 2023年には人員数を20%削減し、さらなる規模縮小に備えていますと2024年の事業範囲管理チームの再編グローバルフットプリントの規模の大幅な縮小 1.*試験デザインに関する最終的な規制当局の同意と、当社の臨床開発プログラムの無事完了を条件としています。2.*承認されれば、2026年にCICワクチンを発売する予定です。

今後の展望:Novavax SE C T I O N 15 © 2024 NOVAVAXにとっての大きな将来のチャンス。全著作権所有。

2024+年に米国の商業業績が好調になるための準備を整えます 1.IPSOSシンジケート版アウェアネス、トライアル、使用状況トラッカー(2023年3月から2023年9月まで)、HCPマンスリーパルス(2023年10月から)。2.IQVIA NPAのデータと請求データ。16 © 2024 NOVAVAX。全著作権所有。2023-2024年ワクチン接種シーズン2024-2025ワクチン接種シーズン5-用量バイアル製品のプレゼンテーション EU UA FDA認可ステータス BLAの予想対象年齢12歳以上ラベル拡大希望年齢 10月6日以上製品入荷時期 2024年6月現在 46% 1HCP-認知度向上 2024年1月現在80% 1すべての小売チェーンで対等な立場にあるわけではありません。小売チャネル ~ 市場機会の90% 2 市場アクセス Novavaxのワクチンの対象範囲が広がり、アクセスしやすくなると予想しています

0 20 40 60 80 1 0 1 2 0 1 4 0 1 0 0 0 インフルエンザCOVID-1900万回投与量 2019-2022年平均1億3,000万-14億回呼吸器混合ワクチンの将来の大きな米国市場機会が期待されています • インフルエンザとCOVIDの組み合わせに対する高いニーズと好み-19ワクチン o COVIDの増加の可能性-併用による19のワクチン接種率 • インフルエンザは、2019年に実施される米国のインフルエンザシーズンの用量にとって大きな機会となります-2022年の平均:1億3000万〜1億4000万 1o 米国の年間インフルエンザ市場機会:40億ドル+ 2 3億3500万〜3500万ドル 3 17 1.NVAX CDC FluvaxViewの2つのデータソースを使用したシーズン平均の内部推定値:a)NIS-6か月(17歳)のインフルエンザデータ、b)IQVIA LRxおよびDxデータを介して18歳以上の成人を対象に実施された週累積推定インフルエンザワクチン接種。2.ジェフリーズ、グローバルワクチンディープダイブ、株式調査レポート、2023年5月30日。3.NVAX IQVIA Rx Rapidの週次データによると、12/22現在の小売ワクチン総数に基づく内部予測推定値。2023年9月から2024年3月までの2023年から2024年のシーズン。4.2023年4月と6月に実施されたNVAXの内部消費者調査およびHCP需要調査に基づいた、潜在的なピーク用量投与に基づくわかりやすい市場シェアの割合。混合ワクチンの投与量は、2回分の投与と同じです。© 2024 NOVAVAX。全著作権所有。実例となる将来の米国市場の季節用量の割合 4 米国市場の季節用量 C O VI D-19 インフルエンザ C o m bo 混合呼吸器ワクチンの選好は、Novavax 4が50%を超える大きなチャンスを生み出します。2023年から2024年までの推定

18 © 2024 ノババックス。全著作権所有。Novavaxは、差別化された混合ワクチンを提供し、大きな市場機会を捉えるのに有利な立場にあります。実証済みの技術プラットフォームを活用してください 1.タンパク質受容性研究(2022年1月)。2.IQVIA需要調査(2023)。3.IPSOSシンジケート・アウェアネス、トライアル、ユース・トラッカー(2023年3月から2023年9月まで)、HCPの月次パルス(2023年10月から)。• 調査対象の消費者1人と医療従事者2の約25~ 30% が、タンパク質ベースのオプションを好んでいます。米国におけるNovavaxの認知度の高まり 1 0 0% 8 0% 0% 4 0% 2 0% 0% 80% 72% 44% 46% 3月〜6月23日-10月23日〜1月23日-タンパク質ベースの選択肢に対するHCPの強い好意的シェアは24% •市販のCOVID-19ワクチンの有効性と忍容性が実証されています • マトリックス-Mは幅広い抗体反応を誘発し、長生きします細胞反応 • フェーズ3の陽性結果が得られた4価インフルエンザワクチン候補 o 市場をリードするスタンドアロンのインフルエンザワクチン、米国HCP-啓発支援3

CIC/インフルエンザ第2相試験の要約所見 19 © 2024 NOVAVAX。全著作権所有。STと-新しいインフルエンザワクチン CICワクチン-スタンドアロンインフルエンザワクチンとNVX-CoV 2373を組み合わせた単回注射マトリックス-M a d j UVアント+ 4つのインフルエンザヘマグルチニン遺伝子を含む4価ワクチンマトリックス-M a d j UVアリ + CICワクチン •フルゾンHD® とFLUAD® に匹敵する反応原性で安心できる暫定的な安全性プロファイル• 抗薬-S IgGと中和反応がNuvaxovidの第3相試験で見られたレベルに達しました • ライセンス基準に沿ったHAI1の幾何平均比スタンドアロン四価インフルエンザワクチン • 暫定版フルゾンHDとFLUADに匹敵する反応原性で安心できる安全性プロファイル • HAI 1の反応は、FLUADと比較して4つの菌株すべてで31〜56%高い • HAI 1の反応はフルゾンHDと比較してA株で44〜89%高い FLUAD® はSeqirus UK Limitedの登録商標です。Fluzone High-Dose Quadrivalent® はサノフィパスツール株式会社1の登録商標です。。将来のワクチンに含まれる3株のベースライン調整済み野生型HAI。

20 © 2024 ノババックス。全著作権所有。Novavaxは、当社の製品ポートフォリオの拡大を支援する立場にあります。今日のNovavax対応態勢-19ワクチン R21/M a tr i x-Mマラリアワクチン 1 CICワクチン 2026年に発売の可能性 2 COVID-19ワクチン R21/M a tr i x-M マラリアワクチン 1 2026 • 現金とAPAは、APA以外の市場におけるグローバルな機会を捉えて行動する当社の能力を支えています。(米国、欧州、低・中所得国)• 2024年度の経費を大幅に削減する o 2022年度と比較して、販管費+研究開発費を全体で 55% 以上削減することを目標 • 新型コロナウイルス感染症が2件追加-CICの発売に向けてさらに準備を進めるための19シーズン • CIC臨床プログラムは、インフルエンザの後期発症の単独治療オプションをサポートしています 1.オックスフォード大学とSIIが開発したR21ワクチンには、NovavaxのMatrix-Mアジュバントが重要な成分として含まれています。このワクチンはSIIによって販売されています。2.承認されれば、2026年にCICワクチンを発売する予定です。
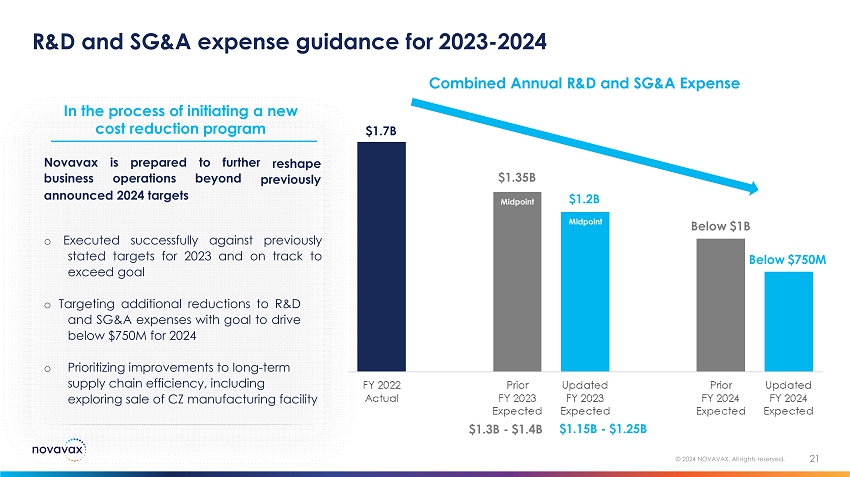
2023年から2024年までの研究開発費と販管費ガイダンス 21 © 2024 NOVAVAX。無断転載を禁じます。17億ドル、11.5億ドルから12億5000万ドルのコスト削減プログラムを再構築します。Novavax事業は、以前に発表された2024年の目標を超えて事業を拡大する準備ができています。以前に述べた2023年の目標に対して成功裏に実行され、目標を上回る見込みです。2024年に7億5000万ドル未満にすることを目標に、研究開発費と販管費をさらに削減することを目標としています o 長期的なサプライチェーン効率の改善を優先します、CZ製造施設の売却を開始する過程で、研究開発費と販管費を合わせて年間10億ドル未満に売却することを検討していることも含みます新規 13億ドル-14億ドル 7億5000万ドル未満 13億5000万ドル中点 12億ドル中間点

22 © 2024 ノババックス。全著作権所有。要約:2023年からの進歩と教訓は、2024年以降の強固な基盤を築きます • 2026年秋にはCICワクチンの発売の可能性 • タンパク質のみの選択肢としての差別化の可能性 • Novavaxにとって大きな将来的な機会 • CICのより迅速な潜在的進路を特定しました • 財務プロファイルの大幅な改善により、CICワクチンを2024年下半期に独立してフェーズ3に進めるためのより良い立場になりました。1好調なのはCICワクチンを2024年下半期に独立してフェーズ3に進めるためのより良い立場です。CIC • 経営陣の再編 • 経費の大幅な削減 • 進化企業文化より無駄のない焦点を絞った組織を作りました 1.試験デザインに関する最終的な規制当局の同意と、臨床開発プログラムの無事完了を条件としています。2.承認されれば、2026年にCICワクチンを発売する予定です。

23 © 2024 ノババックス。全著作権所有。私たちは、世界中の人々の健康を守るために、決して休むことはありません。

よくある質問 24 © 2024 NOVAVAX。全著作権所有。