

2023年12月 PRECISION1 中間分析PRECISION1試験は、TSC1またはTSC2の不活性化変化を伴う複数の固形腫瘍にわたって抗腫瘍活性を示すNAB-シロリムスの3分の1

将来の見通しに関する記述歴史的事実ではない事項に関するこのプレゼンテーションに含まれる一部の 記述は、改正された1934年の証券取引法のセクション21Eと、PSLRAとして知られる1995年の民間証券訴訟 法の意味における将来の見通しに関する記述です。これらには、経営陣の意図、計画、信念、期待、将来予測に関する記述が含まれます。したがって、それらに過度に依存しないように注意してください。将来を見据えた 記述には、Aadi Bioscience, Inc.(「Aadi」)の臨床試験の開始、登録、データリリース、完了の予想タイミング(2024年春までに予定されている 件の完全登録、2024年第3四半期に予定されているPRECISION 1の3分の2の中間分析、予想されるものを含む)に関する記述が含まれますが、これらに限定されません。PRECISION1調査は2024年末までに完了し、PRECISION1データの最終読み取りは2025年初頭に予定されています。会社が順調に生み出しているという経営陣の信念PRECISION 1研究およびナブシロリムスの登録に向けた進展に関する追加の臨床的証拠、新しい適応症の FYARROの規制当局への申請と承認のタイミングと可能性、Aadiの臨床試験のデータに基づく潜在的な触媒の予想時期、Aadiの予想されるキャッシュランウェイ、Aadiの大手精密腫瘍学企業になる可能性、および予測されています TSC1とTSC2の変化を伴うがんの年間発生率と関連する市場機会。将来の見通しに関する記述は保証できません。実際の結果は予測されたものと大きく異なる可能性があります。Aadiは、安全の対象となることを意図したこれらの将来の見通しに関する記述を識別するために、 「予測する」、「信じる」、「計画する」、「期待する」、「プロジェクト」、「意図する」、「かもしれない」、「する」、「する」、「予測する」、「潜在的」、「継続する」などの表現を使います。-PSLRAの港湾規定。このような将来の見通しに関する記述 は、当社の期待に基づいており、リスクと不確実性を伴います。したがって、実際の結果は、臨床試験の開始、登録、完了の遅延の可能性など、FYARROの臨床開発と規制当局の承認に関連する不確実性 、公開に関連するリスクを含むがこれらに限定されない多くの要因により、記述で表明または暗示されているものと大きく異なる場合があります。 件の臨床試験の中間、トップライン、予備データ。Aadiの開発計画そして、FYARRO®(nab-sirolimus、ABI-009)、Aadiの商品化、マーケティング、製造能力と戦略、FYARROの臨床的有用性、潜在的な利益および市場での受け入れ、Aadiの事業資金を調達するための十分な現金残高に関連するリスク、現在および将来の製品候補を研究、開発、商品化するAadiの計画、Aadiの識別能力商業的に大きな可能性を秘めた追加の 製品または製品候補、市場規模、Aadiの競合他社およびそれに関連する開発と予測業界、政府の法律や規制の影響、知的財産権を保護するAadiの能力、将来の収益、支出、資本要件、追加資金の必要性に関するAadiの見積もり。これらのリスクは、2023年11月8日に証券取引委員会(「SEC」)に提出された2023年9月30日に終了した四半期のフォーム10-QのAadiの 四半期報告書、およびSECに随時提出されるその他の文書の「リスク要因」というキャプションの下に詳しく説明されています。このプレゼンテーションに含まれる将来の見通しの 記述は、このプレゼンテーションの日付の時点でAadiが入手できる情報に基づいています。法律で義務付けられている場合を除き、Aadiは、新しい情報、将来の出来事、その他の結果として、将来の見通しに関する記述を改訂または更新する義務を負いません。
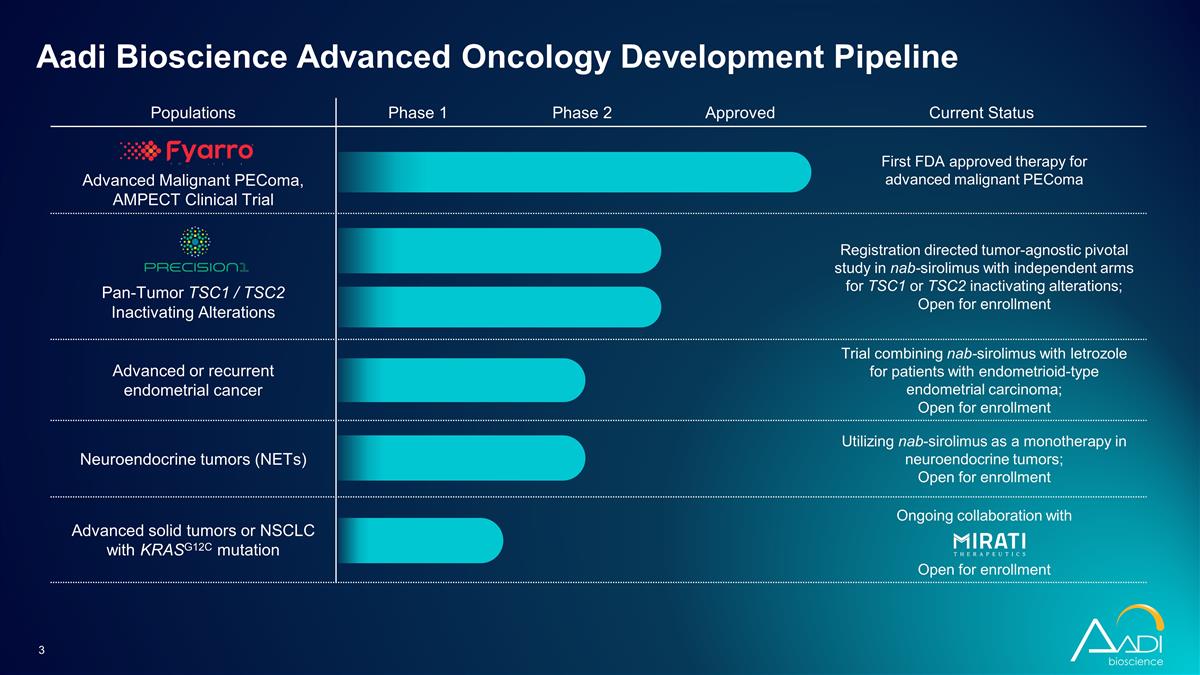
人口第1相第2相承認済み 現在の状況進行した悪性PECoMa、AMPECT臨床試験進行した悪性PECoMA汎腫瘍の治療法TSC1/TSC2不活性化変化に対する最初のFDA承認治療登録、TSC1またはTSC2不活化変化に対する 独立治療群によるナブ・シロリムスを対象とした腫瘍にとらわれないピボット研究。登録募集、パン募集-腫瘍TSC2不活化変化子宮内膜がん子宮内膜様型 子宮内膜がんの患者を対象に、ナブシロリムスとレトロゾールを組み合わせた進行性または再発性の子宮内膜がんの試験; 開放登録神経内分泌腫瘍(NET)神経内分泌腫瘍の単剤療法としてのナブシロリムスの使用。登録受付中 KRASG12C変異のある進行性固形腫瘍またはNSCLC(NSCLC)登録のためのOpen との継続的な協力 Aadi Bioscience先端腫瘍学開発パイプライン

TSC1とTSC2の変化:mTOR経路における主要な 発癌性ドライバー mTOR S6K 4EBP1 レーブラプター PDK1 AMPK Akt TSC1/TSC2 LKB1 (STK11) ERK MEK Raf Ras TSC1とTSC2の不活性化変異はmTOR経路の活性化と腫瘍を促進します成長 TSC1とTSC2は、PI3K/Akt/mTOR経路内のmTOR活性の 上流の調節因子です。TSC1とTSC2の突然変異は、がん全体で約2%、または毎年約16,000件の新規症例で発生します。TSC1およびTSC2変異患者に対する承認された治療法はありませんが、mTORに対して 持続的な反応を示す多数の症例報告があります抑制:標準のCLIA認定のNGSパネルは、すでにTSC1とTSC2の突然変異を捕捉しています。がんや検証済みの標的に頻繁に変異します。
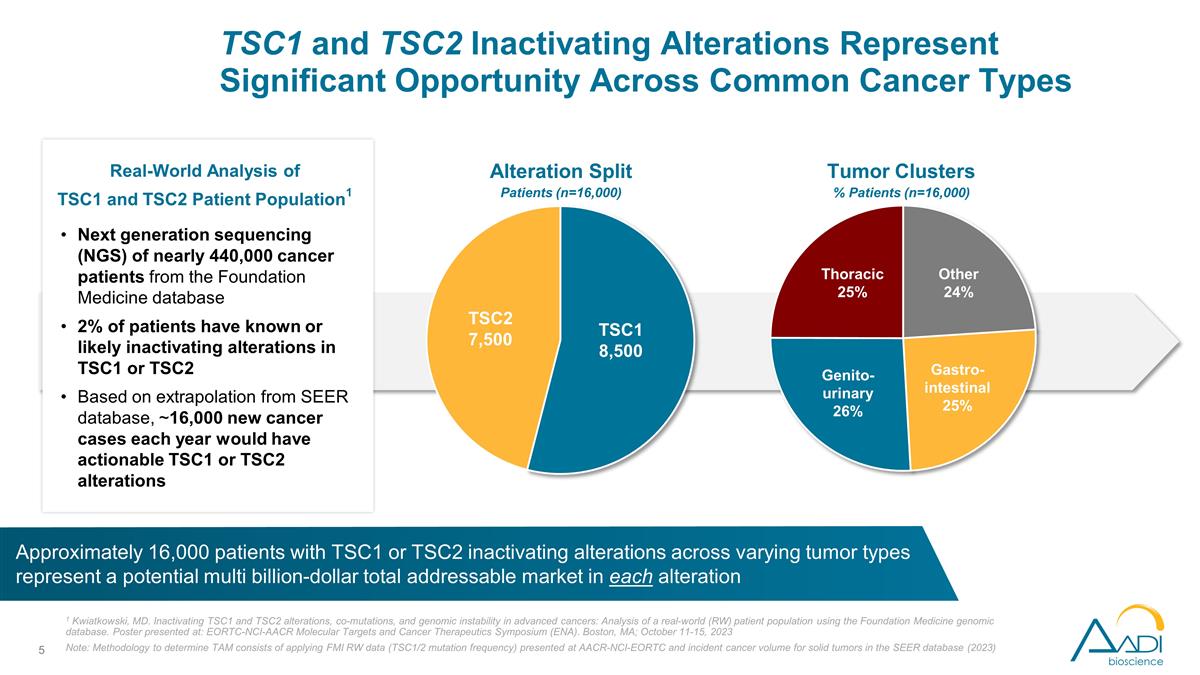
Foundation Medicineデータベースにある 約44万人のがん患者を対象とした次世代シークエンシング(NGS)。患者の2%がTSC1またはTSC2の不活性化変化を知っている、またはそうなる可能性が高いです。SEERデータベースからの推定によると、毎年約16,000件の新規のがん症例で実用的な TSC1またはTSC2の変化が起こるでしょう。1 クウィアトコウスキー、MD。進行がんにおけるTSC1とTSC2の変化、共変異、およびゲノム不安定性の不活性化:Foundation Medicineのゲノムデータベースを使用した現実世界(RW)の患者集団の分析。ポスター は、EORTC-NCI-AACR分子標的およびがん治療シンポジウム(ENA)で発表されました。マサチューセッツ州ボストン、2023年10月11日~15日。注:TAMを決定する方法は、AACR-NCI-EORTCで提示されたFMI RWデータ(TSC1/2変異頻度)と、SEERデータベース内の固形腫瘍の 発生がん量(2023)を適用することです(2023)TSC1およびTSC2の患者集団の実世界分析1 TSC1またはTSC2が不活性化している約16,000人の患者さまざまな腫瘍タイプにわたる変化は、それぞれの変化において対処可能な総市場が数十億ドル規模になる可能性があります 腫瘍クラスターの割合(n = 16,000)TSC1とTSC2の不活性化変化が表しています一般的ながんタイプの変化による大きなチャンススプリット患者(n = 16,000)TSC1 8,500
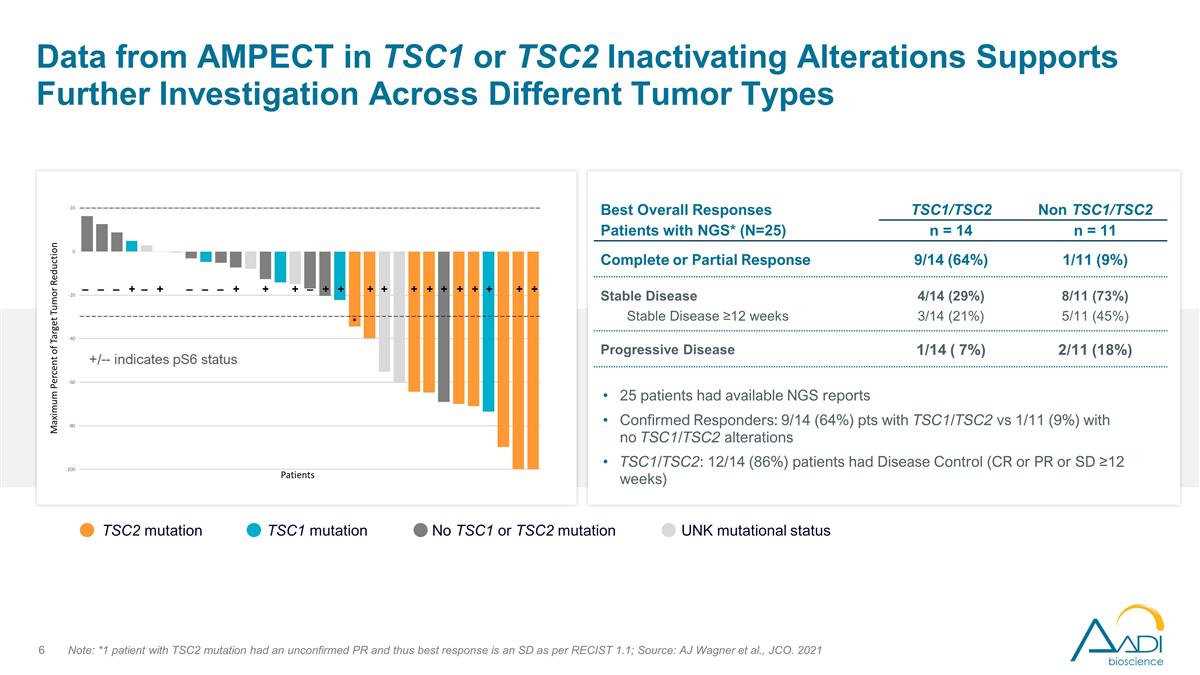
TSC1またはTSC2の不活性化変化に関するAMPECTのデータは、さまざまな腫瘍タイプにわたるさらなる調査を裏付けています。注:*TSC2変異のある1人の患者はPRが未確認だったため、RECIST 1.1によるSDが最良の反応を示しました。出典:AJ Wagnerら、JCO。2021 TSC2突然変異 TSC1またはTSC2の突然変異なし UNKの突然変異状態 25人の患者は利用可能なNGSレポート確認された奏効者:TSC1/TSC2で9/14(64%)ポイント対TSC1/TSC2の変化がない1/11(9%)ポイント TSC1/TSC2:12/14(86%)の患者は疾病コントロール(CRまたは PRまたはSDが12週間以上)で全体的に最高でした回答 NGS*(N=25)TSC1/TSC2以外のTSC1/TSC2 n = 11 n = 11 完全奏効または部分奏効 9/14(64%)1/11(9%)安定疾患 4/14(29%)8/11(73%)安定疾患 3/14(21%)5/11(45%)進行性疾患 1/14(7%)2/11(18%)

PRECISION1: 登録指示 TSC1またはTSC2の不活性化変化 (N = ~60) (N = ~60) におけるナブシロリムスの腫瘍にとらわれない試験 (N = ~60) 治療群 A: TSC1群 B: TSC2 主要な適格基準転移性または局所進行疾患、mTOR阻害薬治療未経験の手術不可 病原性TSC1またはTSC1またはTS NGSを通じて特定されたSC2の不活性化変化は、疾患の標準治療を受けたか、または研究者の意見では有益ではないと研究者が判断したPRECISION1試験 TSC1とTSC2にそれぞれ1つずつ、主要評価項目:盲検によるORR、独立した放射線学的レビュー:地域のNGS結果に基づく患者数の増加:最初の患者は2022年3月に投与され、登録期間は24か月と予想されます
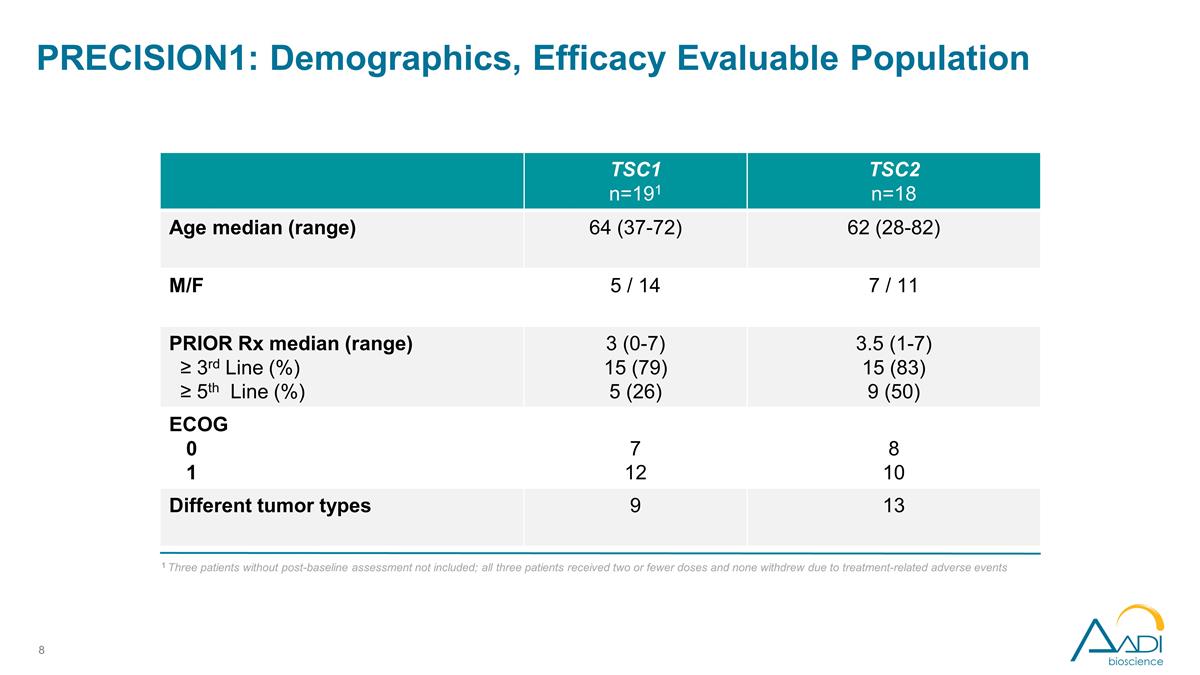
精度1: 人口統計、有効性 評価可能な集団 1 ベースライン後の評価を受けていない3人の患者は含まれていません。3人の患者全員が2回以下の投与を受け、治療関連の有害事象のために中止された患者はいませんでした TSC1 n=191 TSC2 n=18 年齢中央値(範囲)64(37-72)62(28-82)M/F 5/ 14 7/11 以前のRx中央値(範囲)≥ 3rd ライン (%) ≥ 5行目 (%) 3 (0-7) 15 (79) 5 (26) 3.5 (1-7) 15 (83) 9 (50) ECOG 0 1 7 12 8 10 さまざまな腫瘍タイプ 9 13
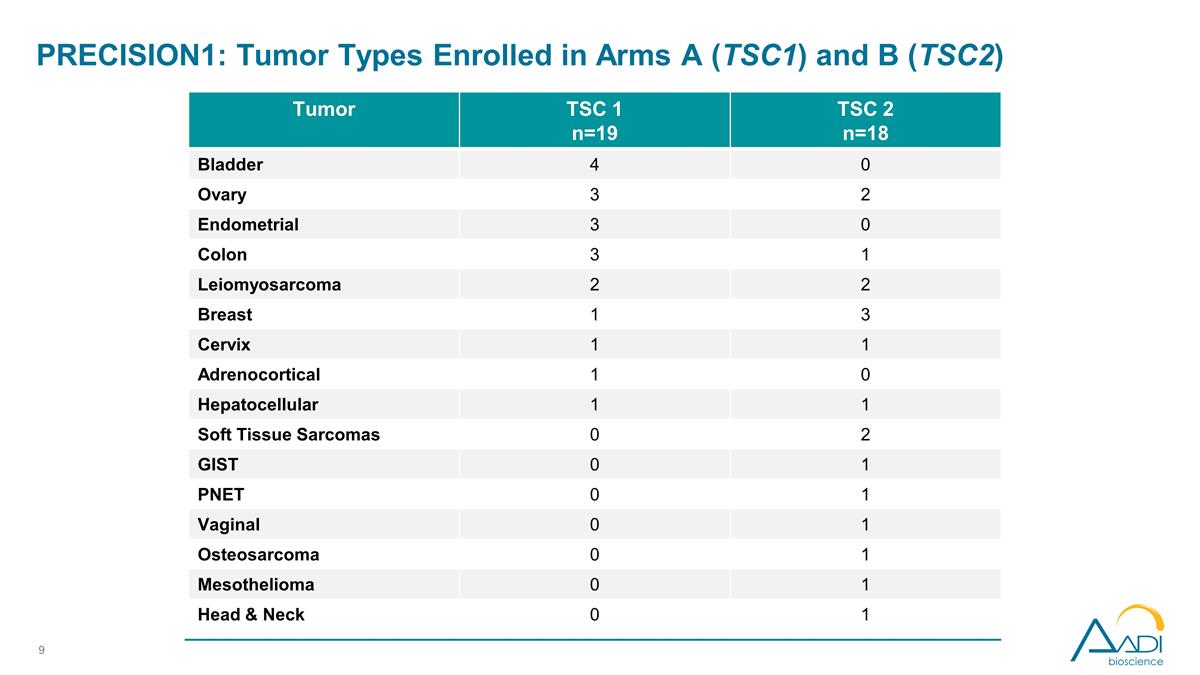
PRECISION1: 群A(TSC1)とB群(TSC2)に登録されている腫瘍タイプ TSC 1 n=19 TSC 2 n=18 膀胱 4 0 卵巣 3 2 2 子宮内膜 3 0 結腸3 1 平滑筋肉腫 2 2 2 乳房 1 3 子宮頸部 1 1 副腎皮質 1 0 肝細胞 1 1 軟部肉腫 0 2 要旨 0 1 PNET 0 1 膣 0 1 骨肉腫 0 1 中皮腫 0 1 頭頸部 0 1
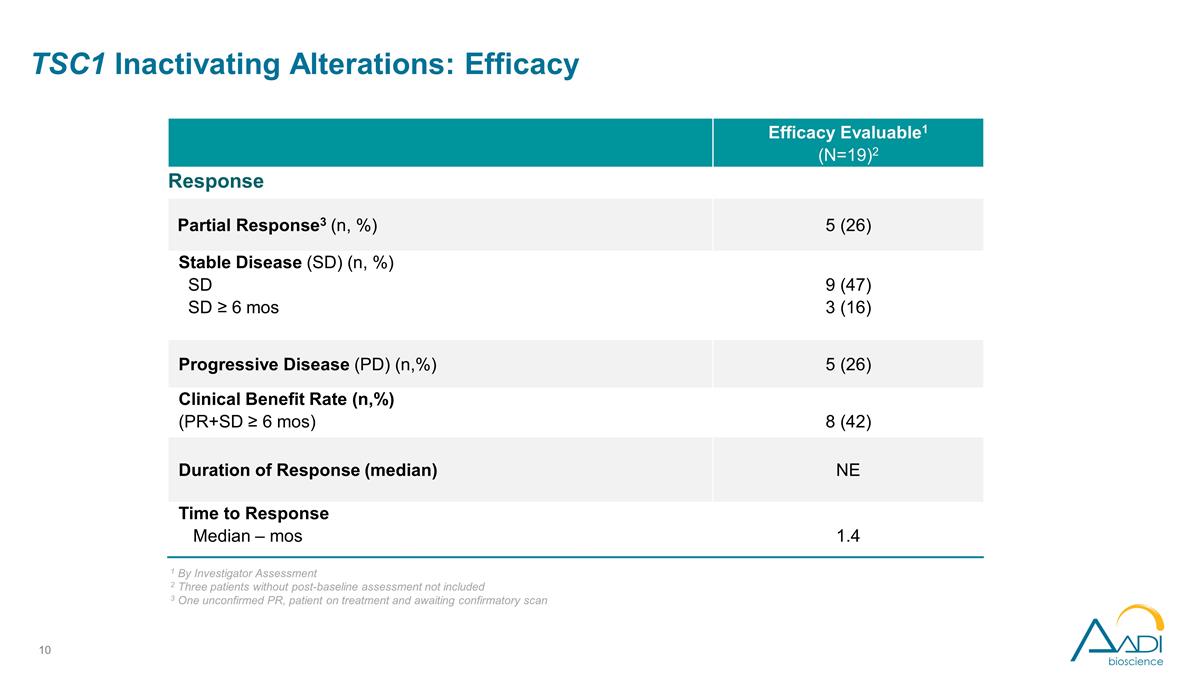
TSC1の不活化変化: 有効性の評価可能1 (N=19) 2 応答部分奏効3 (n,%) 5 (26) 安定疾患 (SD) (n,%) SD ≥ 6 ヶ月 (47) 3 (16) 進行性疾患 (PD) (n,%) (n,%) 5 (26) 臨床的利益率 (n,%) (PR+SD ≥ 6 ヶ月) 8(42)奏効期間 (中央値)NE奏効までの時間の中央値 — mos 1.4 1 治験責任医師の評価による 2. ベースライン後の評価を受けていない3人の患者は含まれていません 3 1人の未確認のPR、治療を受けて確認スキャンを待っている患者
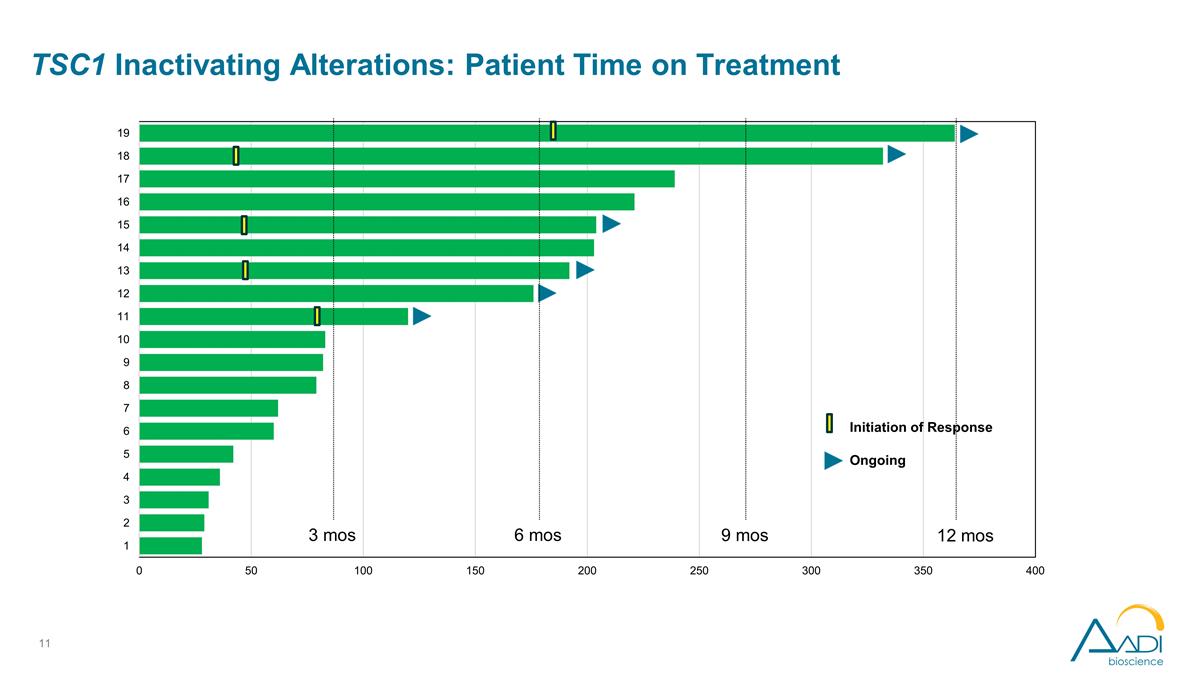
3 ヶ月 6 ヶ月 9 ヶ月 12 ヶ月反応開始 継続中 TSC1 不活性化変化:患者の治療時間
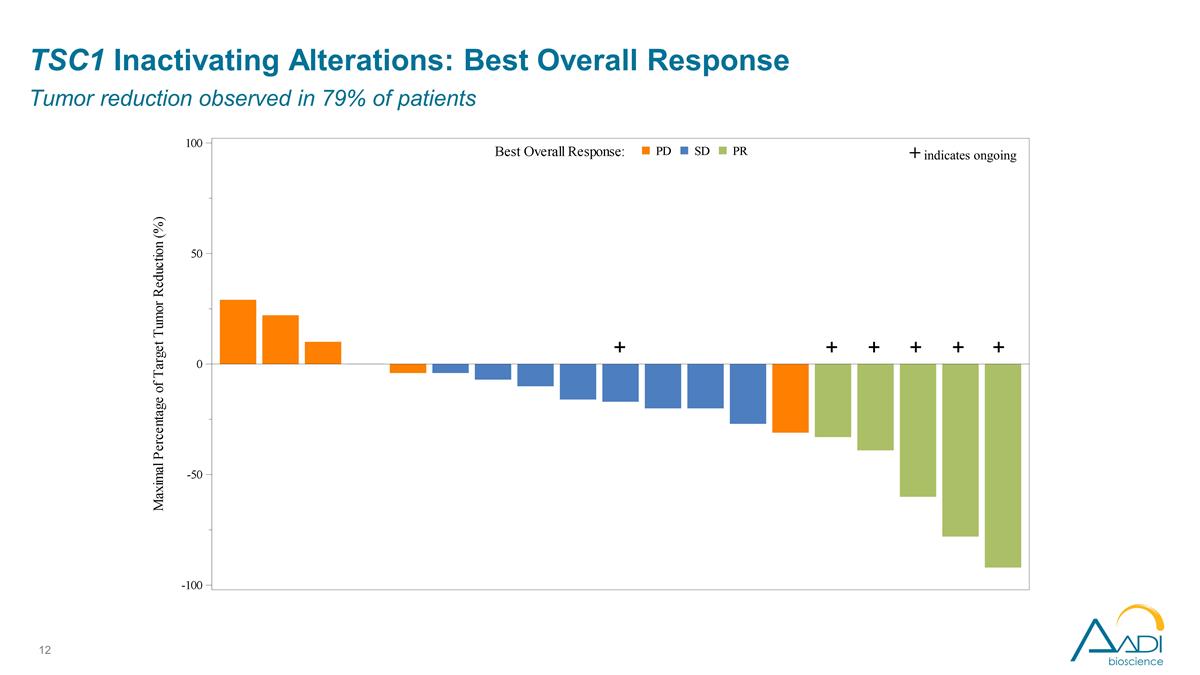
TSC1の不活化変化:最良の 全体的な反応患者の79%で観察された腫瘍の減少 + + + + + + は継続中であることを示しています

TSC1の不活性化変化: 研究者が評価した有効性所見 26%のORRにより、4種類の異なる上皮がんタイプで5件の奏効が見られました。事前に治療された3つの治療ラインの中央値は、早期で、深く、持続的であるようです。すべてが 継続しており、半数以上が50%以上の減少を示しています
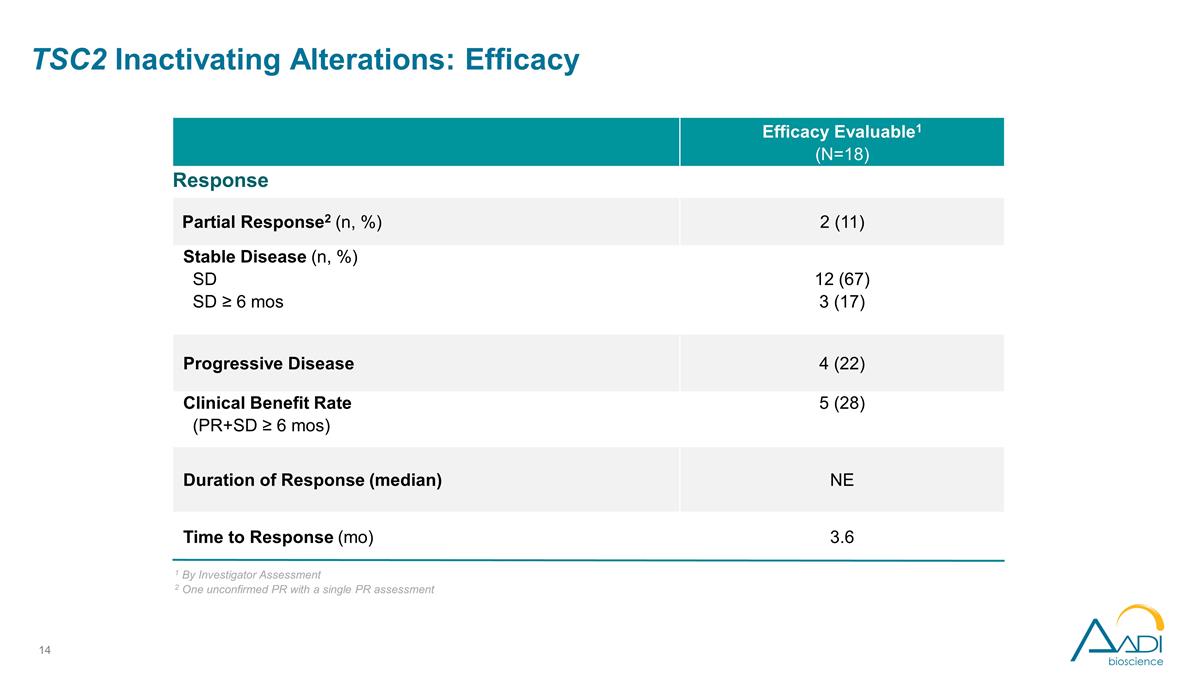
評価可能な有効性1 (N=18) 奏効部分奏効2 (n,%) 2 (11) 安定疾患 (n,%) SD SD ≥ 6 ヶ月 12 (67) 3 (17) 進行性疾患 4 (22) 臨床的有益率 (PR+SD ≥ 6 ヶ月) 5 (28) 奏効持続時間 (中央値) NE反応までの時間 (月) 3.6 TSC2の不活性化変化:有効性:有効性 1 治験責任医師による評価 2 1 回の未確認PR と 1 回のPR評価
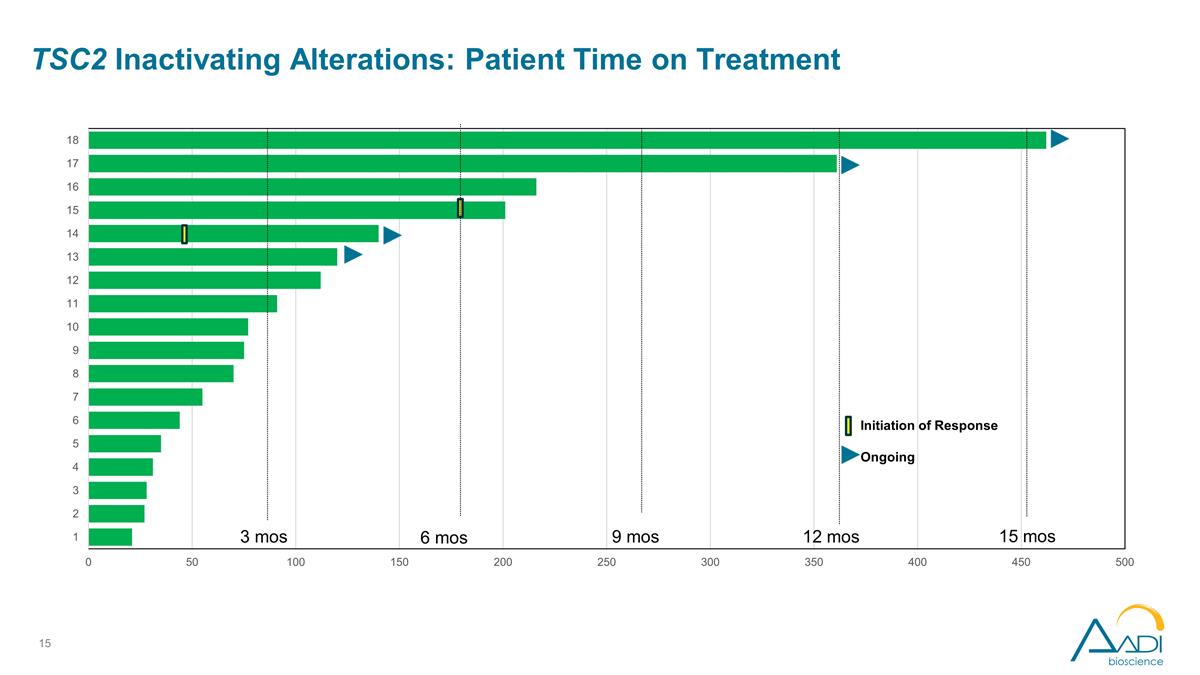
TSC2の不活性化変化: 患者の治療時間
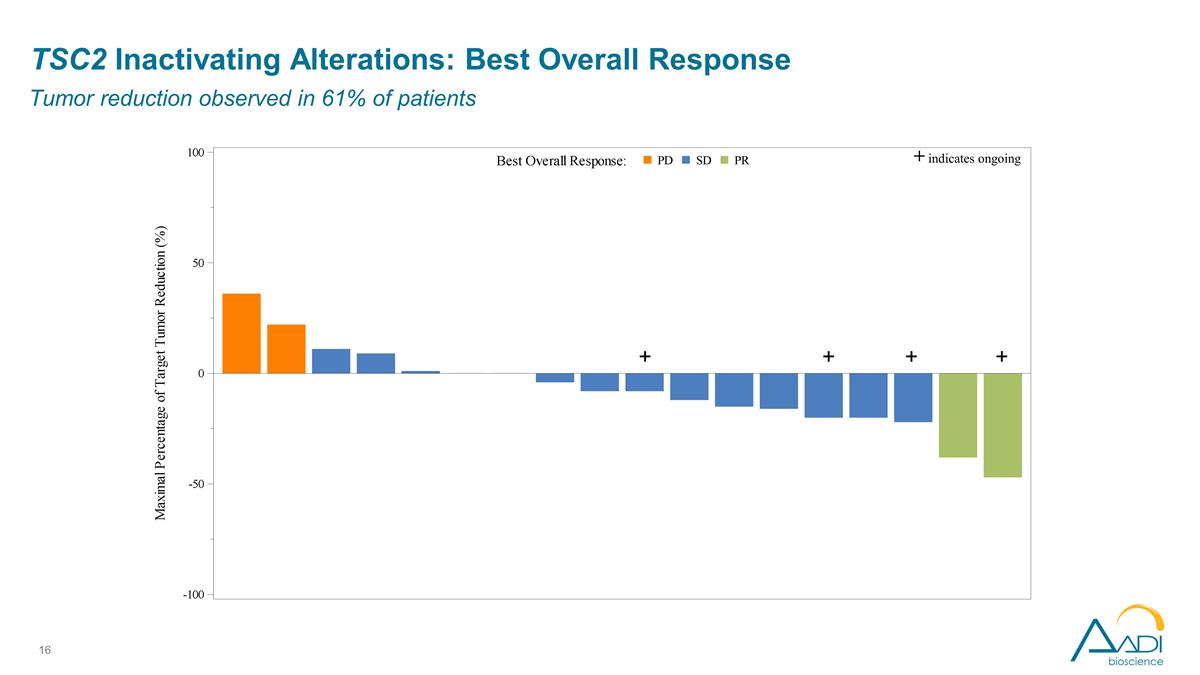
TSC2の不活化変化:最良の 全体的な反応患者の61%で観察された腫瘍の減少 + + + + は継続中であることを示しています

TSC2の不活性化変化: 研究者が評価した有効性所見 ORR 11%(2/18)上皮がんと肉腫CBRで見られた反応 28%(2 PR + 3 SD > 6ヶ月)集団は高度に前治療されていました 9/18は第5選択以上です

PRECISION1: 安全性に関する結論なし 新しい安全性シグナルnab-シロリムスラベルおよびmTORIクラスと一致するAEのパターングレード4のTRAEまたは治験薬1による死亡患者はグレード2の再発性肺炎により研究を中止しました

PRECISION1中間分析の要約 TSC1群の結果は、期待の範囲内の奏効率を期待しています。高度に前治療された集団では、反応は深く持続的であるようです。腫瘍にとらわれない適応を支持するさまざまな腫瘍タイプでの反応。サンプルサイズが小さく、前治療が重いため、ORR 解釈は複雑です。50%の患者は5つ以上の事前治療を受けました。80人の患者の3分の2が暫定登録を完了しました
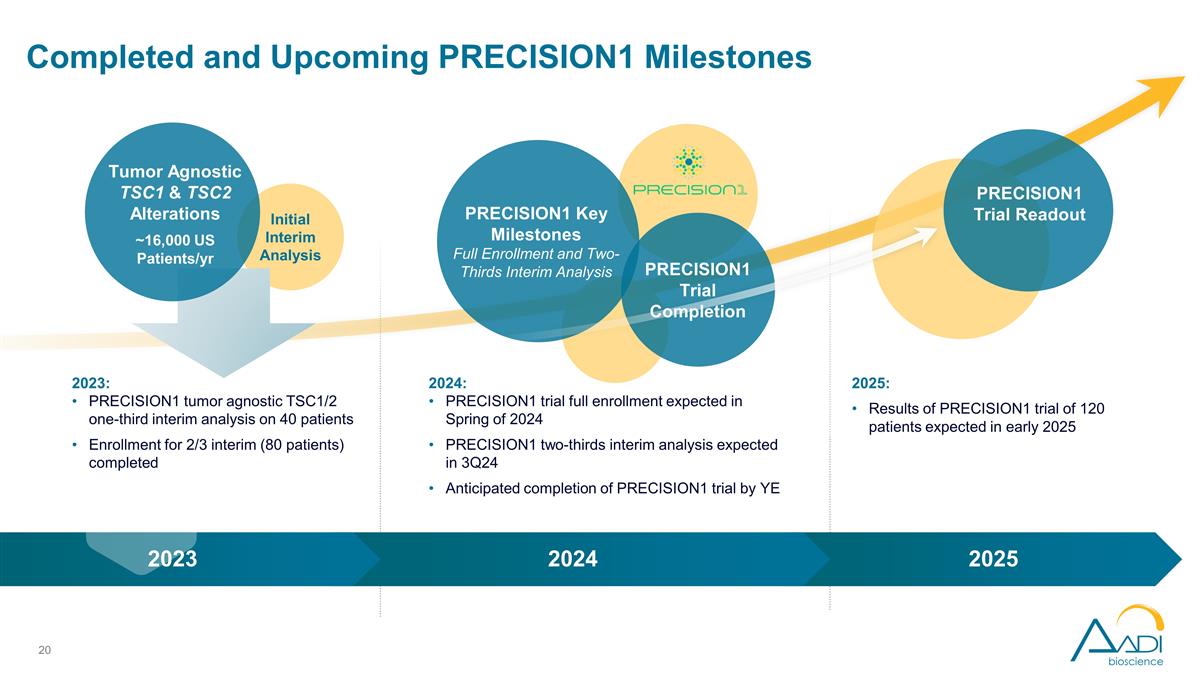
最初の中間分析が完了しました と今後のPRECISION1マイルストーン PRECISION1 主なマイルストーン完全登録と3分の2の中間分析の完了 2024年:PRECISION1試験の完全登録は2024年春に予定されていますPRECISION1試験の3分の2の中間分析 2025年までにPRECISION1試験が完了する見込み:PRECISION1試験の結果 2025年初頭、2023年、2024年、2025年には120人の患者が予想されます。腫瘍にとらわれないTSC1およびTSC2の変化。2023年あたり約16,000人の米国患者:PRECISION1腫瘍 不可知論TSC1/2 の3分の1の中間分析暫定2/3の患者40人の登録(80人の患者)がPRECISION1試験の読み出しを完了しました

ありがとうナスダック:AADI www.aadibio.com