| 図99.2 2023年2月22日1 GLAUKOS Corporation(NYSE:GKOS) 2022年第4四半期と年間回顧br}重要な情報 本稿の枠は、定期的に手配された四半期電話会議の前に投資家が読むことを目的としており、Glaukos Corporationの最近の財務と運営業績および全体的な業務見通しを振り返ることを目的としている。br}は、本稿の追加情報部分の“前向き声明”と“非GAAP財務br}措置の使用に関する声明”を参照されたい。2023年:午後4時30分アメリカ東部時間午後一時三十分Pt ダイヤル番号:1-888-210-2212(アメリカ)、1-646-960-0390(国際) 確認ID:7935742ライブ配信:Glaukos投資家関係サイト上の活動ページ、サイトは http://Invest ors.glaukos.comまたはここをクリックします。 ネットワーク中継再放送:電話会議終了後、ネットワーク中継の再放送はGlaukos投資家関係サイトにアーカイブされます。 まず 革新を行うことが私たちがやっている核心です。Glaukosでは、著者らの は科学技術の限界を推進し、慢性眼病で満足されていない需要 を解決する |
| 2023年2月22日22022年第4四半期と通年財務業績概要br}業務記述br}眼科医療技術と製薬会社は伝統的な看護標準を打破し、慢性眼疾患患者の予後を改善することを目的としたbr}眼科医療技術と製薬会社の開発と商業化に専念し、伝統的な看護標準を打破し、慢性眼疾患患者の予後を改善することを目的としている。固定通貨対2021年度第4四半期) 2022年度$2.829億 (2021年度と比較して-4%-2%不変 通貨vs.2021会計年度) 毛金利(非GAAP) 2022会計年度第4四半期83.6% (2021年第4四半期84.6%) 2022年度83.5% (2021年度85.0%) 現金と現金等価物、短期投資、 と制限された現金 2022年12月31日現在3.598億ドル( 9月30日現在3.707億ドル)2022) 2023年度売上高 指導2023年度のグローバル総合収入予想は2.9億-2.95億ドル 本稿の他の情報部分に含まれる“非GAAP財務指標の使用に関する声明”および非GAAP台帳 を参照してください。貨幣収入の一定増加、非GAAP毛金利、非GAAP運営支出と非GAAP 1株当たり収益と最も直接比較可能なGAAP財務指標の入金を提供した。 |
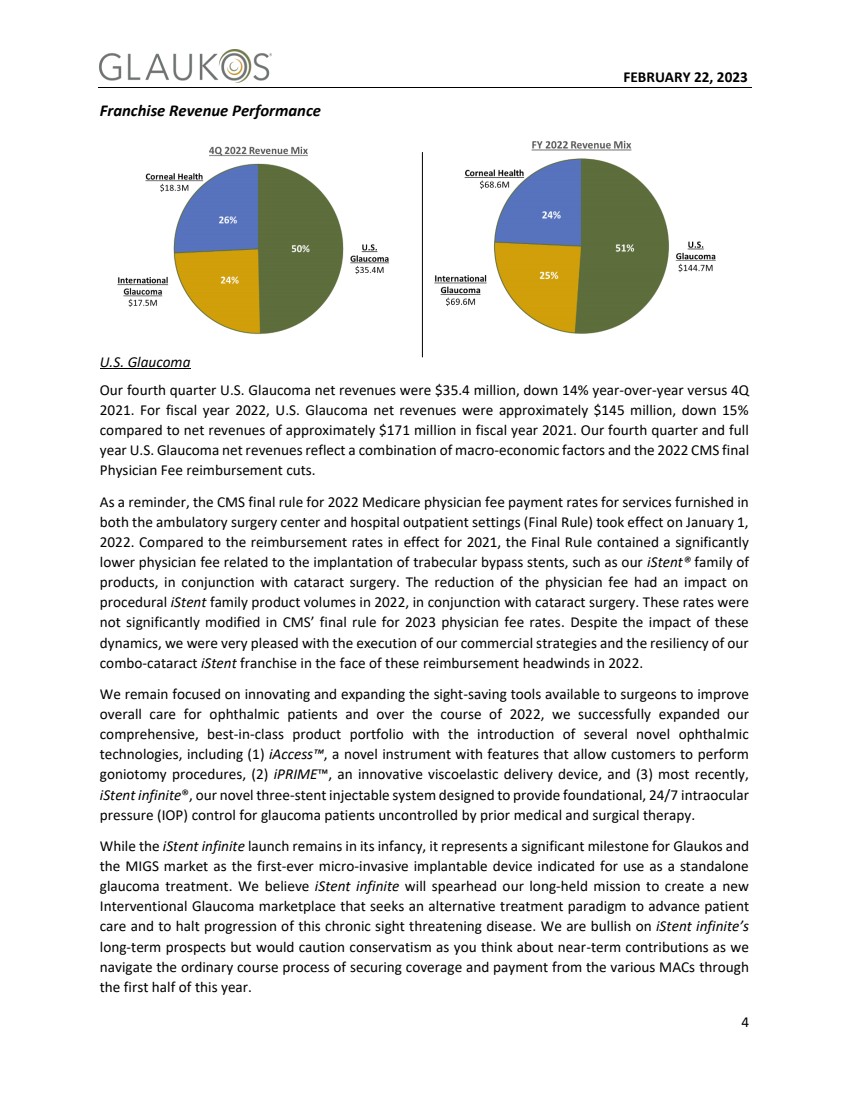
| 2023年2月22日の3収入実績とビジネス概要 全世界総合収入実績 Glaukos報告第4四半期の純収入は7120万ドルで、報告ベースで2.7%低下し、不変通貨で計算すると2021年第4四半期と横ばいである。我々の第4四半期の業績は、2022年の医療保険センターと医療補助サービス(CMS)医師費用削減に関連する米国混合白内障緑内障向かい風、国際外国為替向かい風、および世界のCOVIDと従業員動態の影響で、世界の緑内障と角膜健康特許経営における継続的な実行を反映している。br}2022年度の純収入は約2.83億ドルであり、報告に基づいて4%低下したか、不変通貨ベースで2%低下したが、2021年度の純収入は約2.94億ドルであった |
| 2023年2月22日4特許経営収入実績br}米国緑内障 我々の第4四半期米国緑内障純収入は3540万ドルで、前年比14%低下した2021年第4四半期。2022年度の米国の緑内障純収入は約1.45億ドルであり,2021年度の約1.71億ドルの純収入と比較して15%低下した。我々の第4四半期と年間の米国緑内障純収入は、マクロ経済要因と2022年のCMS最終的な医師費用精算削減の組み合わせを反映している。CMSは2022年の医療保険医費用支払い率に関する最終規則(最終規則)が2022年1月1日に発効することを注意している。2021年に施行された報告率と比較して,最終ルールには,小梁バイパスステント移植に関連する有意に低い医師費用,例えばわれわれのiStentシリーズ製品brが含まれており,白内障手術と組み合わせている。医師費の低減は2022年の白内障手術におけるプログラム的iStentシリーズ製品の数に影響を与えた。これらのレートは,2023年の医師料率に関するCMSの最終規則では明らかに改正されていない。これらのbr動態の影響を受けているにもかかわらず、私たちは私たちの商業戦略の実行と私たちの共同白内障iStent特許経営が2022年にこれらの精算向かい風に直面した時の弾力性を非常に喜んでいる。brは依然として外科医が利用できる視力保護ツールの革新と拡大に集中し、眼科患者への全体的な看護を改善し、2022年の間、私たちはいくつかの新しい眼科br技術を導入することによって、(1)iAccessを含む全面的で最適な製品の組み合わせを拡張することに成功した。クライアントが開腹手術を行うことを可能にする機能を有する新規器具, (2)iStent、革新的な粘弾性送達装置、および(3)最近発売されたiStent Infinedは、以前の内科および手術治療で制御できなかった緑内障患者に基礎的な全天候型眼内圧制御を提供することを目的とした新しい3つのステント注射可能システムである。iStent無限発表はまだ初期段階であるが、GlaukosとMiGs市場の重要なマイルストーンであり、独立緑内障治療として使用されるように指示された史上初の微小侵襲性植入装置となっている。著者らはiStentは無限に著者らの長期使命をリードし、新しい介入性緑内障市場を創立し、1種の代替治療モードを求めて患者の看護を推進し、このような慢性視力脅威疾病の発展を阻止すると信じている。IStent INFINEの長期的な見通しをよく見ていますが、最近の貢献を考えるときは、今年上半期に各Macからの保険や支払いの正常な過程を完了したので、慎重に行動してください。 |
| 2023年2月22日5国際緑内障 我々の第4四半期の国際緑内障純収入は約1,750万ドルであり、2021年第4四半期に比べて前年比11%増加し、不変通貨で24%増加した。第4四半期の国際成長は広範であったが、重大な不利な外国為替向かい風によってある程度相殺された。PRESERFLOMicroShortはオーストラリアとカナダでの早期発売活動が引き続き順調に進んでおり、私たちのキー市場の全体的な表現はbrの強い四半期を強調している。br}2022年度、国際緑内障純収入は約6960万ドルで、2021年に報告された同14%増加し、不変通貨で23%増加した。私たちはまだ国際的なチャンスの早期浸透段階にあり、世界の既存市場の商業販売と市場参入に大きな投資を続け、同時に選択的に地理的に拡張している。 Corneal Health 私たちが記録した第4四半期のCorneal Healthの純収入は約1,830万ドルで、2021年第4四半期に比べて13%増加した。第4四半期の業績の後押し要因は、米国Photrexaの四半期売上高が記録的な1,530万ドルに達し、2021年第4四半期に比べて13%増加したことだ。米Photrexa新規顧客は健康的に増加し続けている。私たちは、2022年に遭遇した散発精算問題を解決するための投資後の持続的な改善の兆しを喜んでいます。 2022年度、Corneal Healthの純収入は約6860万ドルで、2021年に報告された同11%増加しました。2022年の米国Photrexaの売上高は5630万ドル, 2021年に比べて12%増加した。このようなまれな疾患を有する円錐角膜患者の治療ルートの拡大に取り組んでいきたい。 |
| 2023年2月22日6 2023年収入指針br}Glaukosは2023年通年の全世界連結純売上高が2.9億-2.95億ドルと予想される。本ガイドラインでは, ·専門費用に関する米国緑内障数の持続推定影響 複合性白内障小梁バイパス手術が他のより侵襲的な代替手術と比較した精算·複合性白内障MiGsグローバル競争br}·2023年2月22日までの第4四半期決算電話会議の最新外貨スポットレート·iAccess,iPRIME,IStent無限( 下半期に傾向) ·国内で我々のCorneal Health特許経営中の患者に増量自己援助 ·顧客口座員配備制限 ·新冠肺炎の逆風は現在の事実と状況に基づいている |
| 2月22日2023 7研究開発/パイプライン概要br}著者らは伝統的な治療モードを打破し、未来の革新的な下落を産生するための5つの重要な無滴技術治療プラットフォームは以下の通りである: 1.iStentマイクロ外科設備 2.iDose徐放薬品br}3.iLution経皮製薬br}4.iLink生物活性化薬品 5.網膜XR生分解性徐放薬品br}Glaukosパイプライン概要プラットフォーム製品はアメリカの現状 を示す。IPRIME眼科手術中に粘弾性材料FDA承認眼科手術中に手動切断TM FDA承認iStent/iStent注射/iStent注射W軽中度原発開放隅角緑内障合併白内障手術FDA承認br}iStent無限緑内障(以前の内科と手術治療失敗)FDA承認br}iStent無限緑内障(ラベル拡張)IDE計画 PRESERFLO微小シャント末期−難治性緑内障br}米国IDE計画 iDose Or高血圧−緑内障3期試験完了br}IDose TREX眼圧−緑内障臨床前 iDose Rock眼圧−緑内障臨床前 GLK−311眼圧−緑内障IND開放 GLK−301ドライアイ第2段階GLK−302老眼第2段階GLK−302老眼臨床前 Photrexa(Epi−off)Keratoconus FDAが承認したEpioxa(Epi−On)Keratoconus第1段階3試験が完了した 第2世代角膜円錐角膜第2段階1 GLK−401(IVT多活性化酵素阻害剤)AMD,ジメチルエーテル, RVO臨床前網膜br}GLK-411(IVTトリアムシノロンアセトニド)DME臨床前br}網膜XR 生物侵食徐放br}薬物br}iLution br}経皮徐放br}薬物角膜br}iStent br}顕微外科br}装置緑内障 iDose 徐放br}薬物br}iLink br}薬物br}1 2 4 3 1 2 3 5 5 5生物活性薬物 iLink 薬物 1 4 3 1 2 3 5 5 |
| 2023年2月22日、8キー研究開発とパイプライン更新 我々は、2018年以降、我々の研究開発プロジェクトは4億ドルを超える自己資金支援を獲得した。我々が最近行っている更新は、 がiDose tr交換試験の結果を発表し、2回目のiDose tr の注入と元のiDose trインプラントの除去を含むiDose tr交換試験の結果を含む、我々の手厚いコア革新プラットフォームパイプラインへの投資と推進に成功している。第2のiDose trが12ヶ月の評価期間(2023年1月)に良好な安全性を示すにつれて、iDose trと米国食品医薬品局(FDA)との提出前会議は現在終了している。新薬申請提出目標br}2023年2月にGLK-301(iLution-ドライアイ)を治療する2 a期人類初の臨床試験(2023年1月) oはこれらの鼓舞的な観察に基づいて、2023年にEpioxaの第2段階3検証性キー試験(Epi-on)への被験者の募集を開始し、Epioxaの将来のNDA提出(2023年1月) を支持するためにGLK-302(iLution-老年性老眼)の第2段階臨床試験を完成させることを計画している。データを評価するとともに,既存の老眼療法に関する発展しつつある市場状況に注目し続け,2023年に予備データ分析第3世代iLink療法の第2段階角膜健康臨床計画が引き続き進展すると予想される PRESERFLO MicroShort o米国調査設備免除申請計画br}oラテンアメリカで承認を求める規制活動(br}調査新薬(IND)がiLution Travoprostに開放されている(2023年1月) |
| 2023年2月22日9その他の財務業績概要 注意として、私たちは非GAAPまたは形式に基づいて私たちの財務業績を検討し、私たちのGAAP業績 をまとめます。私たちは投資家が私たちの公認会計基準から非公認会計基準への入金を審査することを奨励して、私たちのbr}収益ニュース原稿、ここに含まれる他の情報部分、そして私たちのサイトの投資家関係部分 で見つけることができます。 2022年第4四半期の財務業績概要: 4 Q 2022:84% 2021:85% YoY:-100 bps ·br}商品を販売するコストに対する非公認会計基準の調整には、 エビドロ買収会計に関する大量の金額 ·同減少が含まれていることに注意してください。2022年第4四半期外貨·インフレ:5110万ドル 2021年第4四半期:4670万ドル 前年比:+10% ·10%環比増加2022年第3四半期4640万ドル·同比と四半期増加は世界の商業とG&A投資と新製品発表活動 2022年第4四半期:3580万ドル 2021年第4四半期:2650万ドル 同35% ·24%環比増加2022年第3四半期2890万ドルと比較して、同比と四半期増加は と新製品発表活動への継続的な投資を反映している。研究開発プロジェクト(主にiDose NDA準備)と臨床試験活動(主にエチレンオキシド) 2021年第4四半期:870万ドル 2021年第4四半期:7330万ドル 2022年第3四半期前年比:+19% ·16%7520万ドルに比べて2022年第3四半期運営損失(非公認会計基準) 2022:(2540万ドル) 第4四半期2021四半期:(1130万ドル) 純損失(非公認会計基準) 42022:(2510万ドル) 2021年第4四半期:(1530万ドル) 希釈1株当たり収益(非GAAP) 2022年第4四半期:(0.53ドル) 2021年第4四半期:(0.33ドル) *2022年第2四半期から, 私たちは、協力および許可手配に関連するいくつかの前払いおよびまたはマイルストーン支払い、ならびに非GAAP報告および開示目的のためのいくつかの進行中の研究開発費用をもはや排除しない。前年の間にこの方法の変化を考慮して調整されています。 2022年第4四半期:820万ドル 2021年第4四半期:930万ドル 前年比:(90万ドル) ·歴史レベルに比べて資本支出が高い水準を維持しており、この傾向は続くと予想され、2023年にはより歴史的なbrの正常レベルに適合するレベルまで減速します·第4四半期は前年比低下し、主にカリフォルニア州アリソ·ヴィエホの新施設が大量に完成し、一部はカリフォルニア州サンクレメントとバーリントンの投資によって相殺されています。MA施設 毛金利 (非GAAP) SG&A (非GAAP) 研究開発 (非GAAP) SG&A+ 研究開発 (非GAAP) 収益* 資本支出 |
| 2022年2月22日10年第4四半期:約3.6億ドル 2022年第3四半期:約3.71億ドル 四半期:(1,100万ドル) ·運営費用と資本投資が増加 2022年通年、全世界の合併純売上高は2.83億ドル、非公認会計基準の毛利率は約83.5%、非公認会計基準の運営費用は3.228億ドル、非公認会計基準の運営損失は{br](8,670万ドル)、非公認会計基準の純損失は(103.6ドル)であった。非GAAP 1株当たり純損失は(2.18ドル). は2022年の非GAAP運営費用、非GAAP運営損失、非GAAP純損失と非GAAP 1株当たり収益のIPR&D費用は1,000万ドルであり、実行許可手配に関する前払いに関連しており、これにより2022年に非GAAP希釈後の1株当たり損失に 追加損失(0.21ドル)がある。 現金 |
| 2023年2月22日11年度補足資料年度補足資料 毎年第4四半期収益電話会議とともに を提供 |
| 2023年2月22日12 2022年回顧 新研究開発計画 2022: 強力な 実行力、 業績 とマイルストーン 達成 向かい風 ·iLution DEDと老眼 2 a期試験 ·先進的ないくつかの臨床前研究開発 計画 ·新本部を完成し、Corneaイノベーションセンターとbr}新型ハイブリッド製薬製造施設 ·拡張されたインフラとシステム コア特許経営最近パイプライン ·グローバルMiGsのリードと実行 ·iLinkビジネス実績と市場開発 ·国際成長と規模 ·iAccess、iPRIMEとiStent 無限 ·積極的なiDose trステージ3 TOPLINEデータ; 2023年初めに提出されたセキュリティプロトコルグローバル業務 2022年はわが社の強い実行力、業績と記念碑的な成果の年であり、私たちのアメリカ複合性白内障緑内障特許経営権に関する精算向かい風と挑戦的なマクロ経済環境 にもかかわらず。私たちのチームが私たちの重要な戦略計画を推進できることを誇りに思います。 まず、私たちは変革的なMIGとiLink解決策を推進することで、世界的に新しい採用率とより深い浸透率を獲得し、現在のコアフランチャイズで任務を実行することに成功しました。 第2に、私たちは最近のルートを推進し、iAccess、iPRIME、iStent INFINFERを含む3つの新しい技術を発売しました。我々はまた、2022年9月に積極的な第3段階toplineデータを発表し、iDose tr の第3段階臨床計画を推進した。第3に、早期パイプライン計画を推進し、2つのドライアイと老眼の第2段階臨床試験を完了するとともに、iDose TREXとiDose Rockのような臨床前計画の研究開発の進展を奨励した。 第4に、世界業務を拡大し、カリフォルニア州Aliso Viejoに新しい本部施設を設立し、ボストンの新しい角膜革新センターである, IDose trの製造計画を支援するために、カリフォルニア州サンクレメントにある新しい一流の混合製薬メーカー。同時に、私たちは私たちの長期成長計画を支援するために、私たちの全体的なインフラと最適化システムを拡張し続けます。 |
| 2023年2月22日13展望2023年: 引き続きbr}戦略br}コア特許経営を推進br}新しい研究開発計画br}最近パイプライン ·開発独立したMiGs市場 ·複合性白内障実行 ·国際緑内障,iLink市場建設イニシアティブ成立 コア製品と潜在的な新医薬計画を甲板上 ·2023年初めiDose NDAに提出;Ye 2023承認目標 ·iLution DED 2 b期臨床試験 ·Epioxa 3期実証臨床試験 ·複数のIND/IDEファイル (緑内障と他の計画) ·iLution tr(Ph 2 A)試験の開始を計画し、 iStent INFINE(ラベル拡張)と Retina XR(人類第一) グローバル運営 次世代革新が臨床に入り、未来の成長に備えて ·製薬実験室建設、目標は2024年のiDose tr商業化 ·グローバル人材と専門知識 私たちが2022年に達成した成果は私たちの将来性に興奮し、私たちの創業の旅の次の段階のために十分な準備をしています。2023年、私たちは 私たちが集中した介入緑内障策略を通じて独立したMIGS市場を開発し、新製品を通じて白内障MIGS専門権内で実行し、そしてbr}を通じて私たちの国際緑内障と角膜健康専門権を拡大し続ける;br}は私たちの最近のパイプラインを提供し、br}2023年第1四半期にIDOSE trに的確な守秘協定を提出し、今年末に的確なFDA承認決定を行い、iLution DED 2 b期臨床試験を開始し、Epioxa第2段階確認性臨床試験を推進する。 は我々の早期開発計画を進め,iLution Travoprost (Ph 2 A),iStent無限(ラベル拡張)とRetina XR(人間初例)で実験を開始した, 将来の成長を支援するために、私たちの次世代療法のためのいくつかの計画中のINDおよびIDEアプリケーション;およびbr}は、将来の成長をサポートするために、グローバル組織およびインフラを発展させ続けています。 |
| 2023年2月22日14長期成長と価値創造を提供するポートフォリオbrは、私たちがビジネス実行を行うと同時に、私たちの強力な小説パイプライン に投資し、推進することに成功し続けています, 将来性の高いプラットフォーム技術、私たちはこれらの技術が私たちの潜在市場 を著しく拡大し、私たちの商業プラットフォームを利用して時間の経過とともに私たちの会社を根本的に変えることができると信じています。br}私たちの核心戦略 1.偉大な考えbr}2.重大な臨床需要 3.専門的な研究開発チーム 4.経験豊富な販売組織br 5.試練を経てきた市場建設者 6.長期成長と価値創造を推進するための効率的なグローバル運営 私たちの使命は伝統的な治療モードを覆し、既存の看護標準と豊富な看護標準を高めることである。全世界の視力を脅かす慢性眼病患者に生命と治療選択を提供する。私たちのプラットフォームと候補製品は今後数年で強い新製品の発売リズムを産生し、未来の層の増加を生むことができると信じています。br}利益率 私たちの現在のbr}製品の組み合わせ は重要なbr}に必要なbr}14個の公開パイプライン 項目 緑内障患者 iStent注射/iStent注射/iStent注射W軽中度緑内障合併白内障 を用いて解決した。IStent無限緑内障独立治療(前治療失敗) 角膜 Photrexa(Epi−off)円錐角膜 その他手術 iAccess精密緑内障切開術 iPRIME ViscoDelivery 緑内障 iStent/iStent注射/iStent注射/iStent注射W軽中度緑内障合併白内障 iStent無限緑内障独立治療(先行治療失敗) iStent無限青光眼独立治療(拡張ラベル) iStent無限緑内障−緑内障難治性独立治療 iDose OHT−ObHT独立治療(ObHT ObHT)-独立緑内障 iDose Rock OHT-緑内障独立 iLution Travoprost OHT-緑内障 iLution Travoprost OHT-緑内障 iLution Blepharitis(Epi-Off)円錐角膜 iLink第3世代円錐角膜iLink第3世代円錐角膜(Br)iLutionドライアイ iLution老眼 iLution老眼 iLution Blepharitis Demodex Blepharitis IVT多酵素阻害因子AMD AMD, DME、RVO IVTトリアムシノロンアセトニドDME 他の外科手術 iAccess精密性腺切開術 iPRIME ViscoDelivery 私たちの未来のbr製品の組み合わせ は治療 範式を覆し、 は重要なbr需要brを解決し、現在未開示のプラットフォームと計画を推進した |
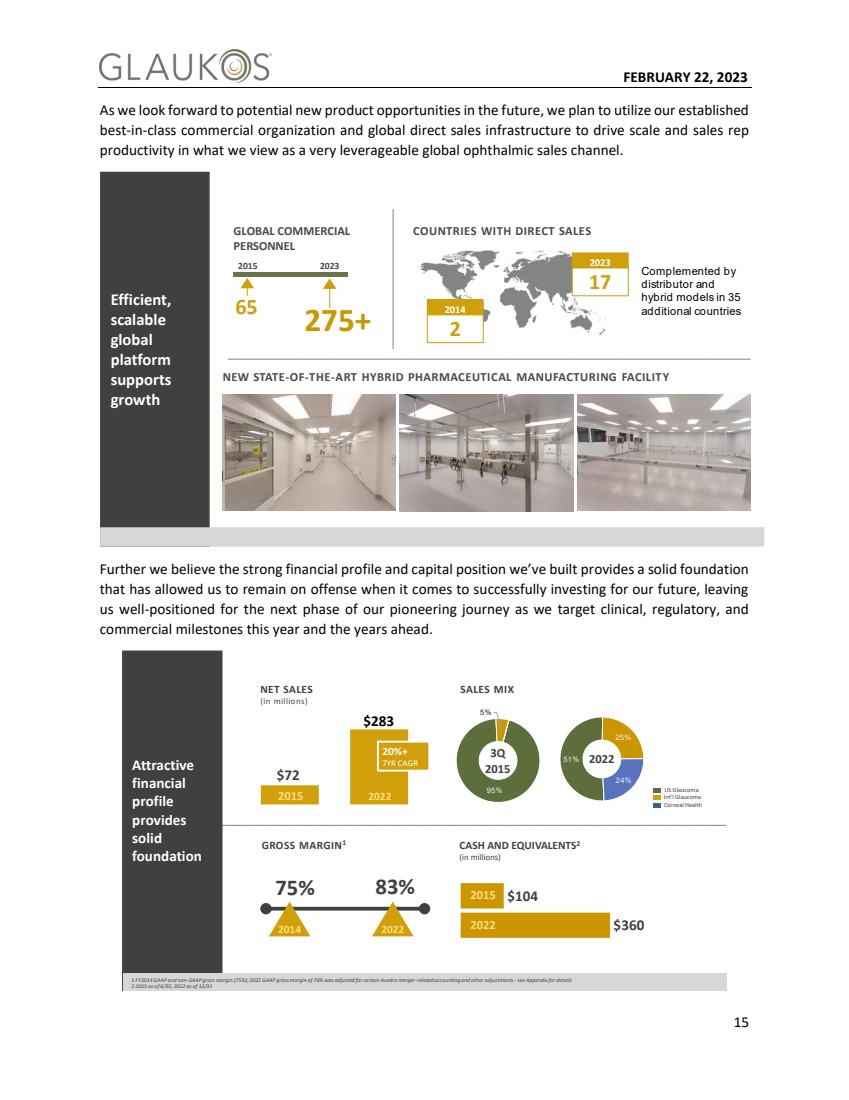
| 2023年2月22日15日、私たちは将来の潜在的な新製品の機会を期待して、私たちは成熟した一流の商業組織と世界の直売インフラを利用して、規模を拡大し、販売代表の生産性を高めることを計画しています。私たちは非常にレバレッジ作用のある世界の眼科販売ルートだと思います。 拡張可能なbr}グローバル プラットフォーム 成長 2015 2023 65 275+ 世界の商業者 国/地域が直売 2014 2 2023 17に他の35カ国/地域のbr}流通業者とbr}混合モデル の新しい最先端の混合製薬製造施設 を支持し、また、私たちはすでに構築された強力な財務状況と資本状況が堅固な基礎 を提供し、未来の投資に成功した時に攻勢を維持することができると信じている。私たちの先駆的な旅の次の段階の準備をしてください。私たちの目標は臨床、規制、そして、今年と今後数年のビジネスマイルストーンです。 魅力的なbr}財務 プロフィールbr}しっかりしたbr基礎 純売上高 2015 2022$72$283%利益率 75%83% 2014年毛金利1 2022$360 2015$104 2022現金とEQUIVALENTS 2(百万単位) 20%^ 7年複合年間成長率 2014年度1つのGAAPと非GAAP毛利率(75%);2022年GAAP毛利率76%で、あるAvedro合併関連会計やその他の調整に使用されています−詳細は付録 2015年6月30日、2022年12月31日現在51% 25% 24% 2022 95% 5% 3 q 2015年アメリカ緑内障 角膜健康 国際緑内障 |
| 2023年2月22日に16個のキーテクノロジープラットフォーム/製品/候補製品の概要br}我々のプラットフォームは、長期にわたって十分なサービスが得られない大型眼科疾患br緑内障、角膜疾患、および網膜疾患を解決するための野心的な壮大な構想を含む。長年、開示されてきたこれらのプラットフォームに関するパイプラインプロジェクトの数は14に大幅に拡大し、2023年に入った。2018年以来、 は研究開発に5つの異なるプラットフォーム を投入して破壊性を生み出している。 3つの専門権の無滴革新 4億ドル 14は2023年のパイプラインプロジェクト と2015年の4つのプロジェクトを開示し、2018年以来、私たちの大アイデア は新しいbr}無滴 療法を開発し、br}で伝統的なbr}局所点眼液brが横行している患者に悩まされているbr}療法 は堅持しない |
| 2023年2月22日17 iStentマイクロ手術設備br}著者らの基礎iStentマイクロ手術設備プラットフォームは主にbr挿入マイクロ設備を含み、緑内障患者のためにbr自然房水流出通路を回復することによって眼圧を低下させることを目的としている。私たちのiStent製品の組み合わせは、業界で最も全面的な低侵襲で、組織を節約する緑内障解決策であり、外科医の個人緑内障治療アルゴリズムに適応し、疾患brの進展の各段階で、高眼圧から難治性疾患まで、白内障と独立手術の併用において最適なbr短期と長期リスク比計算を提供することを支持していると信じています。私たちは企業の先駆者と世界市場のリーダーになることを誇りに思っています。私たちが設立して以来、私たちのiStent技術シリーズは250件以上の同業者評議出版物の支持を得て、20年以上の臨床と商業経験、そして全世界に埋め込まれた100万台以上のiStent装置。br}ユニット式白内障は今日、アメリカ市場で、我々が提供したiStentとiStent InjectWは,米国食品医薬品局が承認した軽度から中等度の原発性開放隅角緑内障合併白内障手術の治療のための製品である。 iStent米国FDA承認(2012) iStent Inject米国FDA承認(2018) iStent Inject W米国FDA承認(2020) これらの製品はまた承認され,様々な国際市場で販売されている。IStent注射剤Wは国際市場の収入の大部分を代表しているが,我々は引き続きiStent注射剤を販売している |
| 2023年2月22日に18市場でiStent Injection Wが発売されておらず、第1世代iStentは一部の市場で発売されている。br}2022年8月、FDA 510(K)がiStent INFINEを承認したことを発表した。これは、以前の内科と外科治療ではコントロールできなかった緑内障患者に基礎的な全天候眼圧制御を提供することを目的とした新しい3つのステント注射可能システムである。br}iStent INFINEは、独立したbrプログラムにより緑内障患者の高眼圧を低下させることを目的とした3つのステント装置である。外科医がシュレム管(目の主なドレナージチャネル)の周囲に約6時間以内にステントを注入することを可能にする自動注射システムに予め組み込まれた3つのヘパリンコーティングチタンステントを含む。ステント装着後,房水の自然,生理的流出を回復させることで眼圧を低下させることができる。強力なキーデータ支援は、 の良好な安全性と有効性を強調している。IStent INFINEは眼科外科医に魅力的な新しい治療選択を提供し、以前の内科と外科治療では制御できなかった開放隅角緑内障患者のために独立した治療を行う可能性があると信じている。br}前の手術治療に失敗した開放隅角緑内障患者br}o 510(K)米国食品·薬物管理局の承認(2022年8月) oは連邦医療保険行政請負業者(MACS) と協力し、CPTコード067 1 T(独立MIG/iStent INFINITE)のための積極的なカバー決定と関連支払い レベルを制定している。早期単純緑内障を有する患者 o IDE計画 であるiStent無限リリースはまだ初期段階である, これはわが社やMiGs市場にとって重要なマイルストーンであり,緑内障の独立治療に指定された史上初めて低侵襲植え込み型デバイスであるためである。著者らはiStentは無限に著者らの長期使命をリードし、新しい介入性緑内障市場を創立し、1種の代替治療モードを求めて患者の看護を推進し、このような慢性視力脅威疾病の発展を阻止すると信じている。IStent INFINEの長期的な見通しをよく見ていますが、最近の貢献を考えるときは、今年上半期に各Macからの保険や支払いの正常な過程を完了したので、慎重に行動してください。 |
| 2023年2月22日19 iDose徐放性薬物brわれわれのiDose徐放性薬物プラットフォームは、眼内からより長時間の治療レベルの薬物を提供することを目的とした、標的、低侵襲、注射可能インプラントからなる。全天候、長期、強力な治療効果と最小の副作用を提供することによって、普遍的に存在する患者の不コンプライアンスと局部薬物に関連する慢性副作用を解決することを目的としている。iDose trは有名なプロスタグランジン類似体トラボプロストからなる。我々がiDoseプラットフォーム技術を用いて推進した最初の研究候補である。 米国FDAの高眼圧または開放隅角緑内障患者に対するNDA研究 o陽性背線3期の結果は主要な治療効果の終点 に達し、良好な耐性と安全性を示した (2022年9月) o発表(2023年1月) がNDA申請(2023年1月) o目標は2022年9月7日までに潜在的なNDA承認であり、IDose trの2つの第3段階キー試験の主要データ,すなわち2つの第3段階試験において, は3カ月以内にあらかじめ指定された主要治療効果終点 を実現することに成功し,12カ月以内に良好な耐性と安全性を証明したことを発表した。2つの第3段階キー試験の総合的な治療効果と安全性結果に基づいて,徐放性iDose trモデルのNDA を米国FDAに提出する準備をしており,FDAは2023年末に審査と決定 を完了すると予想される。 |
| 2023年2月22日2つの重要な裁判でIDose tr 速放と徐放用量 は米国FDAと合意したあらかじめ指定されたbr}の主要な治療効果終点br(3ケ月以内に局所投与br}硫黄に劣らないか心安) 積極的な3期試験結果br}br}もうすぐ提出されるnda申請 徐放iDose tr 眼圧がベースライン(ミリ米水銀)より8.5 6.6 7.7 6.7 6.8 6.8遅い7.2遅いことを支持する予定である。IDose tr Timolol 0.5%Bid 発表前3カ月1·1期間に観察された眼圧はベースラインより低下した。150名の被験者が2つの3期試験において無作為br·1研究の平均ベースライン眼圧~24 mm Hg ·~81%の徐放錠被験者が開放隅角緑内障を有していた。19%の眼高血圧 ·67%の徐放性iDose tr 被験者はスクリーニング時に少なくとも1種類の眼圧降下薬を服用し、その中の23%の被験者が3期または2期以上のデータで主要な治療効果終点 1 mm Hg範囲に達したことは、米国FDAが予め指定した6時点、すなわち10日目、6週目および3カ月目の午前8時および10時の眼圧低下を表した。IDose trはFDA承認 を受けず、第3段階のキーデータに加えて、2回目の注入iDose trと元のiDose trインプラントの除去とを含むiDose tr交換試験の結果が最近発表され、2回目のiDose trは12ヶ月の評価期間で良好な安全性 を示すことができたことが嬉しい。また…, 平均5年を超える延長評価期間では,Exchange試験では30%を超える内皮細胞喪失を示した被験者は1人もいなかった。我々はこれらのデータが臨床的にiDose患者の経時的再治療の安全性と耐性を支持し、さらに市場をリードする臨床証拠システムを増加させ、競争相手の代替案に対して当社の低侵襲技術が同類の最適な利益リスク計算を有することを支持することを支持している。このデータセットをFDAに提出する間もなく発表されるNDAに含め、強力な第3段階データセットを拡大することを期待している。われわれの臨床·規制·前向き多センター試験を除いて,交換プログラムの安全性を評価するために ·研究はiDose trステージ2 b研究を移植した33名の被験者 ·被験者の眼を入れて手術を受けた 徐放iDose tr モデルを用いて手術 交換を行い,フォローアップ期間は12カ月 ·平均全体拡張評価期間は5年以上 Exchange研究の陽性 データセットは繰り返し NDAに含まれる。目標は2023年第1四半期にFDA 角膜内皮細胞数が5年以上臨床的に意味のない変化 Exchange研究で延長された評価期間内に内皮細胞損失(30%喪失)を認めなかった不良事象 Exchange試験がiDose tr 0 500 1000 1500 2000 3000 Ph 2 bベースラインPh2 b 3年再投与 ベースライン(4.2年) 第2剤1年 (5.2) 角膜内皮細胞密度 (細胞/mm 2)の再投与を示すことである |
| 2023年2月22日の21チームのコツコツとした秘密保持協定の準備は、私たちのビジネスと市場参入組織の中で、職能部門にまたがるリーダーからなるチームとiDose trの商業発表の準備と計画を順調に進めており、2024年にiDose trを発売することを目標としている。br}iDose trの開発がこれまで成功してきたことを考慮して、私たちは、元のiDose trと似ているように、そのサイズと外形は元のiDtoseと似ている。治療効果の持続時間を延長するために、2倍近くの薬物容量を提供することを目的としている。br}o臨床前のbrはまた、岩石阻害剤のような他の薬物カテゴリーを評価しており、私たちはすでに鼓舞的なウサギモデルデータを見て、候補薬物のためのbr原型移植を確立している。br}o臨床前 |
| 2023年2月22日に私たちのもう一つの新しい無料外科眼科技術はGlaukosと眼科医によって開発され、iAccessは小梁組織を切断し、それによってbr水をSchlemm管に直接流入させることを目的とした精密ブレードである。IAccess付き生殖器切開術は、外科医に多才な外科技術を提供し、外科医がどの手術が患者に最適かを決定できるようにすることを目的としており、数時間にわたる複数の小切開でも、95%までの解剖構造を保存しても、広範なシュレム管開口を保存している。2022年第1四半期に米国でiAccessの商業発表活動を開始した。iPRIMEは斬新な製品である。真の低侵襲粘弾性送達システムは,眼科手術中に粘弾性送達を提供することにより,医師や患者のニーズをさらに支援する。この技術はGlaukosの広範な革新眼科ソリューション製品の組み合わせを更に拡張し、著者らの低侵襲療法価値に対する長期的な立場と一致している。IPRIMEは、医師や患者のニーズを支援するもう一つの重要なツールになると信じています。brは2022年第2四半期末に米国でiPRIMEの初歩的なビジネス開始活動を開始しました。br}PRESERFLO MicroShortは、外付けを必要としない外科的緑内障インプラント は、原発性開放隅角緑内障患者の眼圧を低下させることを目指しており、最大耐性緑内障薬や緑内障進展に手術が必要な場合に眼圧制御ができない患者である。PRESERFLO微分流器はSIBSポリ(スチレン−ブロック−イソブチレン−ブロック−スチレン)と呼ばれる独自の生体適合性材料で作られており,柔軟である, 平面フィン付き8.5 mmのチューブは、マイクロ切り口でデバイスを組織に固定し、漏れと移動を防止するのに役立ちます。br}OUSは承認され、オーストラリアとカナダでbr規制活動を開始し、ラテンアメリカの承認を求めています。アメリカIDEは2023年に計画されています |
| 2023年2月22日23 iLink生物活性化薬br私たちのiLink生物活性化薬物プラットフォームは新しい使い捨てbr医薬製剤からなり、これらの薬物は私たちの特許システムが紫外線を角膜に伝達することによってbrを生物活性化し、それによって角膜架橋と呼ばれる生化学反応を引き起こし、角膜を強化、安定、再構築することを目的としている。円錐角膜は深刻な視力を脅かす疾患であり、米国全層角膜移植の主要な原因でもあるが、依然として深刻な治療を受けていないと考えられる。この治療不足は主に診断不足と歴史的に有効な解決策が不足しているためである。このような重要なPhotrexa療法の患者に対する可用性を最大限に高めるために、私たちは大量の投資を行い、私たちのビジネス組織を拡大し、実践採用のハードルを下げ、検眼と眼科コミュニティの円錐角膜に対する認識を高め、転診モードを簡略化し、角膜健康専門家を養成するためのLink iプログラムを実行した。ILink Epi-offはPhotrexaという新薬調合を用いて円錐角膜を治療し、円錐角膜は視力を脅かす退行性疾患であり、このような疾患の中で、角膜は次第に薄くなり、弱くなり、視力喪失を招く。FDAが許可したのは円錐角膜の進展を緩和或いは阻止できることが証明された治療法br}oが有効な治療がない場合、進行性円錐角膜患者5人に1人が角膜移植1 200+同業者審査出版物br}oの優れた治療効果と安全性が必要である可能性がある。広範な臨床証拠と長期(10年)のフォローアップbr}o製品特定のJ-Code;97%以上のビジネス活動に割引補償 1 Pramanik S,Musch DC,Sutphin JE, ファルホエーエーです。透過性角膜移植による円錐角膜の長期治療効果。眼科です。2006年;113(9):1633-1638;マハラーナPK、アガワールK、Jhanji V、Vajpayee RB。深前板層角膜移植治療円錐角膜の研究進展アイコンタクト。2014;40(6):382-389 |
| 将来を展望して、私たちはEpioxaという特許新薬処方、brのより強いUVA照射プログラムを使った次世代iLink療法、すなわちEpi-onを推進しています。そして、より高いレベルの酸素補充能力を提供する。 o第1段階第3段階臨床試験陽性結果が所定の終点 (2021年2月) oを満たす第2段階第3段階確認臨床試験(2023年1月) o目標は、治療時間と複雑性を減少させ、患者の快適さおよび回復時間 を改善することを目的とした2023年1月までに第2段階第3段階確認試験を完了することであり、NDA前の会議中にFDAから受信したフィードバックに基づいて、円錐角膜を治療する次世代角膜架橋剤Epioxa(Epi−On)の第2段階3検証性キー試験の被験者登録を開始した。我々は,この試験で約290名の被験者をランダムに抽出し,2023年末に登録を完了することを目指している予定である。FDAは,我々のEpioxa第1段階3キー試験があらかじめ指定された主要な治療効果の終点を満たし,最終的なNDAの提出と審査を支援するのに十分であり, は2回目の試験とともに行うことを確認した。私たちがEpioxaの臨床計画を引き続き推進することに伴い、私たちは依然として有利な地位にあり、円錐角膜患者に私たちの初代角膜架橋剤、すなわちEpi-offを提供することができ、それは依然としてFDAが承認した円錐角膜進展を緩和し、阻止することができる唯一の治療法である。私たちがすべてのプラットフォームに対して行ったように、私たちは引き続き後続の数世代の未来の革新を推進し続けている, そして、第3世代iLink療法の第2段階臨床計画が行われている。br}iLink第3世代iLink療法は、治療能力のカスタマイズと患者体験の簡略化を目的とした2つの独立した多中心、ランダム、対照試験brからなり、患者に対する安全性と有効性を評価するための第2段階臨床計画を行っており、br}カスタマイズと非カスタマイズ角膜治療モデルbr}架橋と新しいレーザーによる生物活性化システムと、2022年第2四半期に,吾らはiVeena Delivery Systems,Inc.と独占ライセンス契約を締結し,これにより,iVeenaは円錐角膜のいくつかの化学成分の治療を含むiVeenaノウハウを用いたGlaukosのグローバル独占許可を付与した。 |
| 2023年2月22日に25 o IVMED-80はiVeenaの主要な研究候補であり、これは独自の非手術、非侵襲性、疾病修正干与措置であり、FDA孤児 の称号を有し、リシルオキシダーゼ(LOX)を上昇させ、薬理上で角膜br}架橋性br}oを誘導することができ、これは非常に早期の計画であり(第1段階)、我々のiLinkプラットフォームの補助br本許可プロトコルは、私たちがこのカテゴリと円錐角膜患者に治療と看護を提供する持続的な承諾を表明した |
| 2023年2月22日26 iLution経皮薬br私たちのiLution経皮薬物プラットフォームは、特許に基づくクリームbrの薬物配合からなり、br}まぶたの外面に応用され、br}眼疾患治療のためのbr}薬物活性化合物br}無滴経皮投与である。br}iLutionのまぶたへの差別化投与方法brは、従来の局所投与方式に比べて顕著な優位性があり、より投与しやすく、効果が速く、副作用が少ないと考えられる。例えば、防腐剤による角膜および結膜後遺症を減少させることは、これらのすべてが、より良いコンプライアンスおよび患者の予後改善に寄与する。br}GLK-301:ドライアイGLK-301は、ドライアイの症状およびバイタルサインの治療に使用されるまぶたに適した無菌眼科局所クリームである。クリーム配合は倉庫として機能し、ピロカード品が眼瞼真皮を介して目に輸送されることを可能にした。 oは我々のiLutionプラットフォーム o APIを利用して:ピロカード品 o 2 a期の初回人体試験結果は2023年1月に予定されているbr}2 b期試験に進展することが期待できることを示し、著者らは著者らのiLutionドライアイ病計画 GLK-301に対する2 a期臨床試験の初歩的な結果を発表した。GLK−301のTOPLINE 2 a段階の結果,涙膜品質は改善し,視覚質量も改善した。これらの鼓舞的な観察に基づいて、我々は今年後半にGLK−301の2 b段階試験を開始する予定である |
| 2月22日2023年の27-8.5-8.2試験は良好な安全性と耐性を示し、br}·98%の患者は試験を完了し、br}·眼部不良事象は発生せず、発生率は5%以上であり、涙膜品質の改善(涙膜破裂時間徴候)、視力の質の相応の改善(視力混濁症状の軽減) に背線試験結果が観察され、iLution無滴眼療法によるドライアイの潜在的差異化治療効果の早期読み出しに良好な早期br読み取り値を提供した。疾患br}iLutionドライアイ(GLK-301)2 a期試験:218名のドライアイ患者に対して28日間の研究を行い、そして3種類の用量のGLK-301とプラセボに対して28日間の安全フォローアップを行い、br}~55名の患者/群 GLK-301 a期の初回人体試験結果により、2023期2 b試験 GLK-301 aプラセボ 43% {22% 涙液破裂時間に入ることを約束した。パーセンテージ 28日GLK-301 aプラセボはベースライン変化 VAS視力改善ファジィ より28日27 192023 Glaukos Corporation 26 GLK-302ベースライン変化:老眼 GLK-302は1種の無菌眼科外用クリームであり、まぶたに適用し、老眼の治療に応用する。このクリーム製剤は、ピロカード品が眼瞼真皮を介して目に輸送できるように倉庫として機能している。br}oは、私たちのiLutionプラットフォームbr}oの第2の研究候補薬:ピロカルカ(br}o 2 a期)を利用して完成した;2 a期データを評価するとともに、利用可能な老花療法に関する発展していく市場状況 GLK-311:Travoprost GLK-311は私たちの臨床前計画であり、眼前節の疾患の治療のために設計された薬物化合物brを研究し続けている, 例えば 緑内障。 o INDは現在開放されており、2023年に試験を開始する予定です。o api:Travoprost Blepharitis Ilution Blepharitisは私たちの臨床前計画であり、ニキビダニの根絶を目的とした薬物br化合物を研究しています。 ニキビダニ炎は眼皮膚炎の根本的な原因であり、眉毛腺機能障害や関連眼病によく関係しています |
| ニキビダニは人体の皮膚に発見された最もよく見られる体外寄生虫 ニキビダニは眼皮膚炎の根本的な原因であり、通常眉筋腺機能障害と関係があり、ドライアイ病と他のいくつかの関連眼病の主要な原因である |
| 2023年2月22日29網膜XR生物侵食徐放薬物br著者らの生物侵食徐放薬物プラットフォームRetina XRは網膜疾患の治療を目的とし、現在網膜は眼科最大の市場であり、全世界の売上高は130億ドルと推定され、2023年まで毎年10%近くの速度で増加すると予想される。アメリカでは網膜疾患は約2800万人に影響していますAMDと糖尿病眼疾患は患者総数の約89%(市場範囲による)を占めている。 GLK-401: IVTポリキナーゼ阻害剤 GLK-401は生物腐食性徐放性インプラントであり、老年性黄斑変性(AMD)、糖尿病黄斑浮腫(DME)、網膜静脈閉塞(RVO)と。br}o臨床前開発br}o api:ポリキナーゼ阻害剤br}GLK-411: トリアムシノロンアセトニドGLK-411は、DMEに対する生体腐食性徐放性インプラントである。br}o臨床前開発br}o api:トリアムネロンアセトニドこれらの臨床前計画の目標は、網膜専門家と彼らの患者に新しいbr持続薬物治療オプションを提供することであり、現在主導されている看護標準よりも長い有効な持続時間を提供することである。短期生物注射により,治療に必要な頻度が高いため,患者に大きな治療負担をもたらすことが多い。我々の目標は,今後12カ月以内にそのうちの少なくとも1つを最初のヒト臨床試験に進めることである |
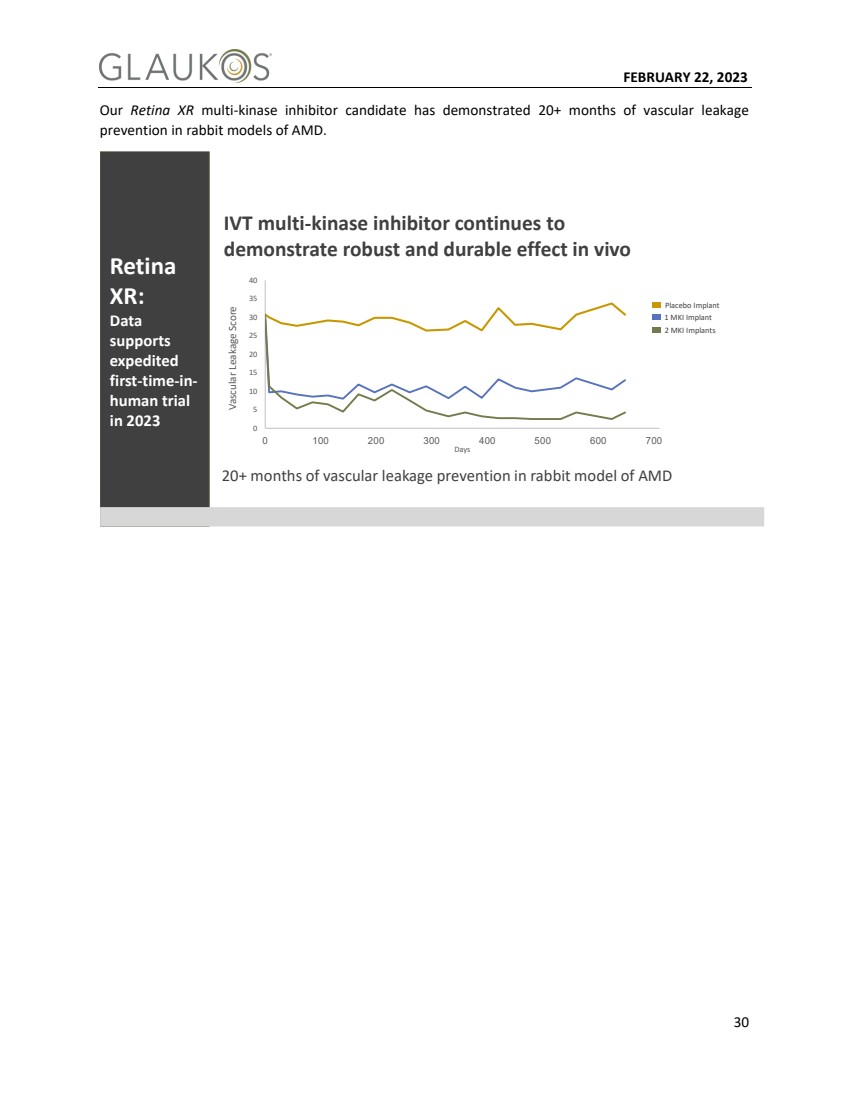
| 2月22日2023 30我々のRetina XRポリキナーゼ阻害剤候補薬は、AMDウサギモデルにおいて、20+カ月の血管漏出予防 −8.5−8.2網膜 xr: データbr}支持br}2023年の加速を支持するbr}初のヒト試験 のAMDウサギモデルにおける20カ月以上の血管漏出予防 IVTポリキナーゼ阻害剤持続 が体内で強力で持続的な効果 0 5 10 15 20 25 30 35 40 100 200 300 400 400を示すことを証明した。500 600 700血管漏出スコア 天 プラセボインプラント 2つのMKIインプラント 1つのMKIインプラント |
| 2023年2月22日31年度補足資料 |
| 2023年2月22日32展望的陳述(Br)本プレスリリースは、連邦証券法で定義された“前向き陳述”を含む。 本プレゼンテーションに含まれる、私たちの予想、信じ、または将来発生する可能性のある活動、事件、または発展に関するすべての陳述は、歴史的事実陳述を除いて前向きな陳述である。このような陳述は経営陣の現在の予想、仮定、推定、そして信念に基づいている。私たちは、本明細書に含まれる展望的陳述には合理的な基礎があると信じているが、これらの展望的陳述は、私たちの未来の事件に影響を与える現在の予想に基づいており、私たちの運営および業務環境に関連するリスク、不確実性および要因の影響を受けることを想起させ、これらのすべては予測が困難であり、その多くは私たちが制御できないものであり、 は、本プレゼンテーションにおける前向きbr陳述が表現または示唆した結果とは大きく異なる可能性がある。これらは、実際の結果が展望性陳述に記載されている結果と大きく異なる潜在的なリスクおよび不確実性をもたらす可能性があるが、これらに限定されない:br}新冠肺炎の大流行または他の公衆衛生危機が私たちの業務に与える影響の不確実性;外国為替変動を含む全体的なマクロ経済状況の影響;CMSが最終的に決定した2022年と2023年に同社のiStentシリーズ製品を使用した手術の医師費用とASC施設費用の販売率とそれが私たちのアメリカの結合性白内障緑内障収入に与える影響;私たちは商業化された製品の販売量を創造し、他の製品を開発し、商業化することができます。私たちは限られた数の第三者サプライヤーに依存して、 のいくつかは単一の供給源です, 私たちの製品のコンポーネント;私たちの主要施設で深刻な事故、自然災害、または他の中断が発生し、これは私たちの製造能力および運営に実質的な影響を与える可能性があります;iStent、iStentシリンジ、iStentシリンジW、iAccess、iPRIME、iStent Infinitionを使用するための第三者の確保または維持は、十分な保険または精算br、 私たちの角膜架橋剤製品または他の開発中の製品を提供し、私たちの製品を使用する際に適切な訓練を行う能力、および眼科医の受け入れと信頼を得る。私たちは医療機器業界および現在および未来の技術(MIG br技術を含む)と効果的に競争する能力;私たちは連邦、州と外国の法律法規を遵守して、私たちの製品と製造プロセスの承認と販売とマーケティング;私たちの臨床試験過程は長く高価で、任意の特定の臨床試験または規制承認過程の時間と結果の不確実性;私たちの製品のリコールまたは深刻な安全問題のリスクおよび患者結果の不確実性;私たちの保護能力と、第三者や競争相手から私たちの知的財産権を保護する費用と時間の性質、および第三者の知的財産権の侵害または流用のための任意の関連訴訟が私たちに提起した任意のクレームの影響;および私たちが債務を返済する能力。我々は、米国証券取引委員会(米国証券取引委員会)に提出された文書に、2022年9月30日現在の10-Q表四半期報告と、2022年11月4日に米国証券取引委員会に提出した10-Q表四半期報告を含み、これらおよび他の既知のリスク、不確定要因、および要因を詳細に説明している, 2022年12月31日までの年度Form 10−K年度報告に含まれ,2023年3月1日までに提出される予定である。私たちがアメリカ証券取引委員会に提出した書類は私たちのサイトの投資家欄で調べることができます。サイトはwww.glaukos.comまたはwww.sec.govです。また、私たちのサイトwww.glaukos.comでは、私たちの製品のリスクと収益に関する情報を提供しています。本プレスリリースに含まれるすべての前向き陳述は,前述の警告的声明に適合するすべての内容を明確にしている.本プレスリリースにおける前向きな陳述に過度に依存しないように注意し,これらの陳述は本プレスリリースの発表日からのみ発表される.私たちはこれらの内容を更新、修正、または明確にする義務を負いません |
| 2023年2月22日33は前向きに述べており、新情報、未来事件、その他の原因により、適用可能な証券法が要求される可能性があるものは除外する。 非GAAP財務指標の使用に関する声明 は、公認会計原則(“GAAP”)によって作成された総合財務結果を補完するために、会社はある非GAAP歴史財務指標を使用する。 経営層はGAAP計量を調整し、(A)会社の核心経営活動を反映していない項目(費用と収益)に関連し、(B)通常、当社の財務業績とその同業(Br)グループの財務業績との比較性、または(C)異なる期間の金額または頻度が一致しないように、当社の所属業界内で調整される(これらの項目は監査 およびコア業務と同等に責任を果たして制御されているにもかかわらず)。当社が使用する“非公認会計原則” という言葉は、業務合併を実施することによって発生する外部買収に関連するコストを含まないこと、業務合併、資産購入取引または他の契約関係で取得された無形資産の償却、営業権および無形資産の減価、ある進行中の研究開発費、業務合併によって生じるまたは価格負債と買収前または有事の公正な価値調整、業務合併に関連する統合と移行コスト、業務合併または資産購入取引で取得された在庫の公正市場価値調整を含むことを意味する。脱退または企業規模の大幅な削減に関する再編費用,重複運営費用または資産打抜き(または償却);売却企業の損益;時価による調整·減値の損益, 長期投資または販売;将来の期間の収入または支出リスクをヘッジする派生ツールの時価調整 ,重大な法的訴訟費用および/または和解費用、または政府または内部調査に関連する重大な法律費用および他の関連費用、取引に関連する重大な離散収入およびbr}その他の税務調整、ならびに企業合併に関連する推定買収日の税務影響の変化、ならびに税法の変化およびbr}和解の実施の影響。比較可能GAAP財務指標に提出された各非GAAP測定基準の入金については、“主要GAAP対非GAAP調整”を参照してください。 また、外貨為替レート変動の影響を除去するために、会社 は不変通貨に基づいて何らかの純売上情報を提供しており、これは、今期のレートが比較可能時期に有効な平均レート と同じであれば結果 を表す。報告された、GAAP、不変通貨に基づくいくつかの純売上情報の プレゼンテーションについては、“他のGAAP対非GAAP調整”を参照されたい。 |
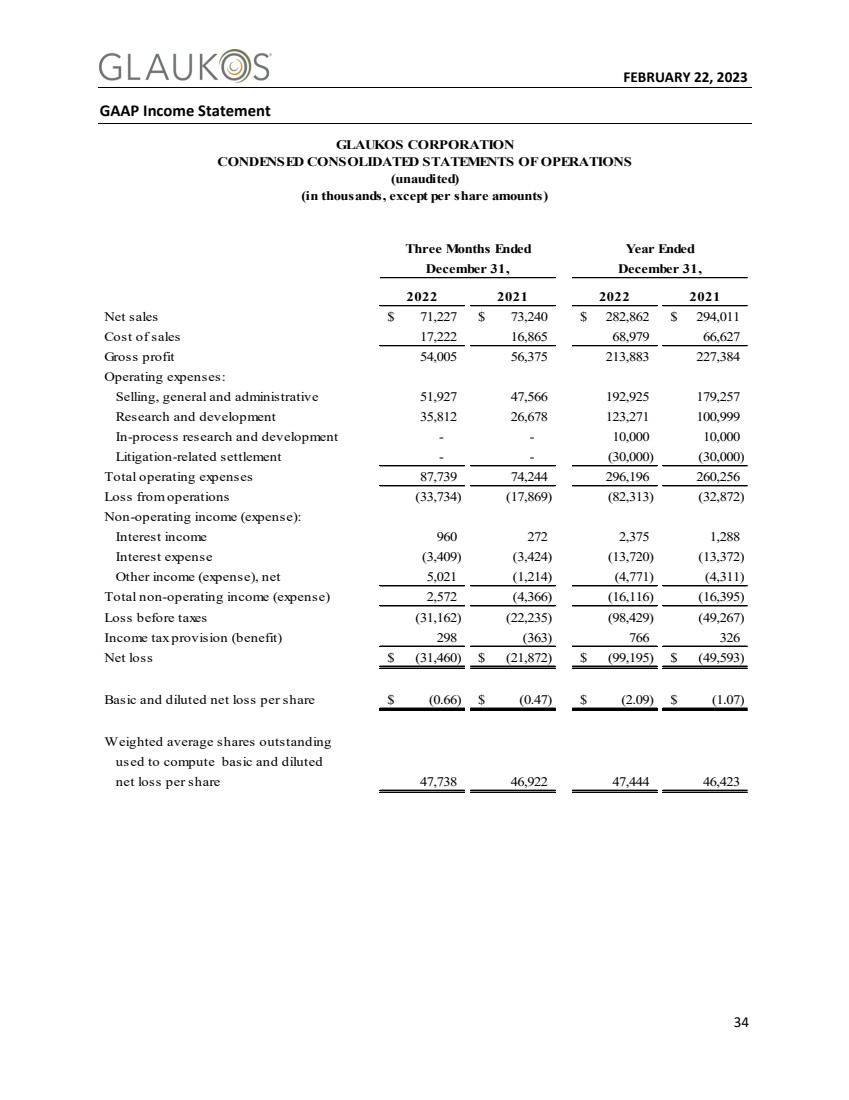
| 2023年2月22日34 GAAP損益表 2022年12月31日までの3ヶ月 2021年12月31日純売上高$71,227$73,240$282,862$294,011販売コスト17,222 16,865 68,979 66,627毛利益54,005 56,375 213,883 227,384運営費用: 販売,一般と行政51,927 47,566 192,925 179,257研究開発35,812 26,678 123,271 100,999が行っている研究と開発--10,000訴訟に関する和解-(30,000)(30,000) 総運営費用87,739 74,244 296,196 260,256運営損失(33,734)(17,869)(82,313)(32,872) 非運営収入(支出): 利息収入960,375 1,288利息支出(3,409)(3,424)(13,720)(13,720){b 72}{13,720}{b 72){b 72}純5,021(1,214)(4,771)(4,311) 営業外収入(費用)合計2,572(4,366)(16,116)(16,395) 税前損失(31,162)(22,235)(98,429)(49,267) 所得税準備(福祉)298(363)766 326純損失$(31,460)$(21,872)$(99,195)$(49,593) 1株当たり基本と希釈後純損失$(0.66)$(0.47)$(2.09)$(2.09)$1.07) 加重平均流通株 は、基本と希釈後の1株当たり純損失47,738 46,922 47,444 46,423 GLAUKOS Corporation 縮小合併経営報告書 (千、1株当たりの金額を除く) (監査を受けていない) |
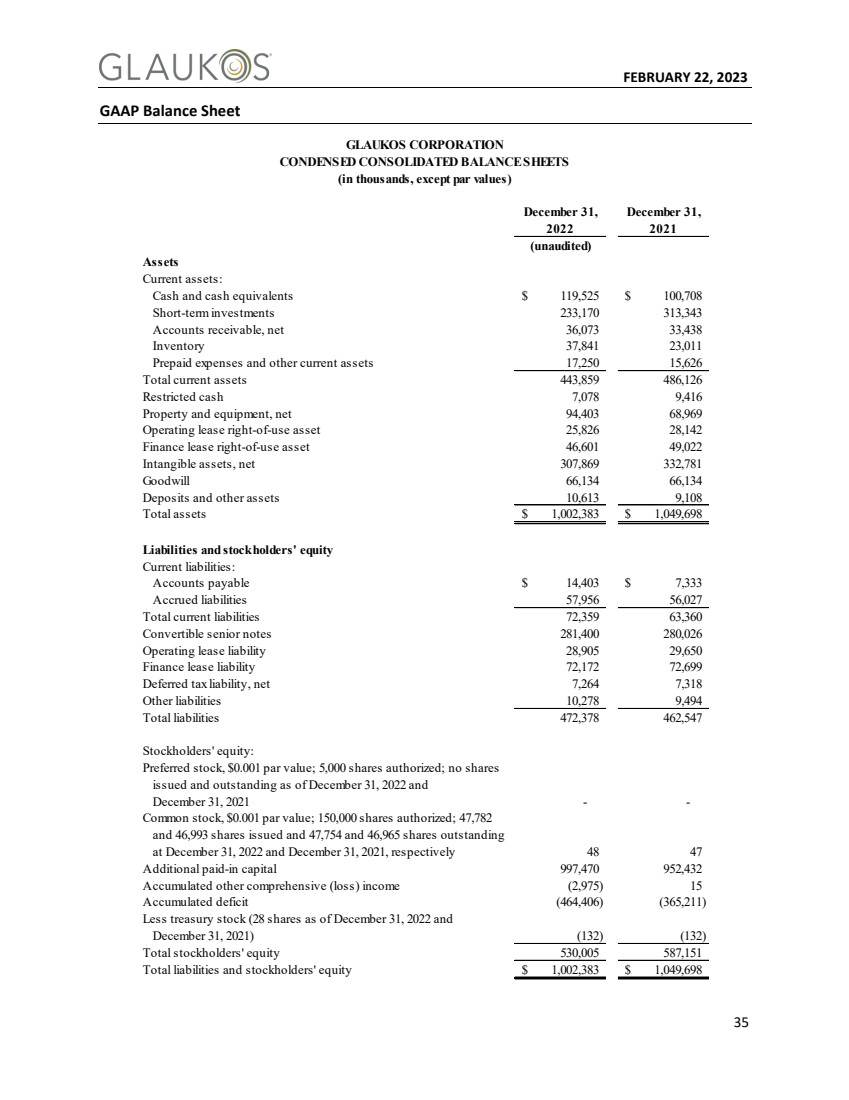
| 2023年2月22日に35 GAAP貸借対照表 GLAUKOS Corporation 圧縮連結貸借対照表 (千元、額面を除く) 2022年12月31日 2021年12月31日(未監査) 資産 流動資産: 現金および現金等価物$119,525$100,708短期投資233,170,343,343売掛金,純額36,033,438在庫37,841 23,011費用とその他流動資産17,250,626総流動資産443,859,486,現金制限資産443,843純307,869 332,781営業権66,134 66,134預金および他の資産10,613 9,108総資産$1,002,383$1,049,698負債および株主権益br}流動負債: 売掛金$14,403$7,333負債57,956,027流動負債総額72,359,63,360転換可能優先手形281,400 280,026経営賃貸負債28,905 29,650融資リース負債72,172,699正味7,264 7,318その他負債10,278,494総負債472,378,547:0.001ライセンス5,000株;2022年12月31日と2021年12月31日までの任意の株式である 普通株を発行し、額面0.001ドル;許可150,000株;2022年12月31日と2021年12月31日にそれぞれ47,782株と46,993株および47,754株と46,965株 それぞれ48 47追加実収資本997,470 952,432を発行して他の総合(損失)収入(2,975)15累計損失(464,406)(365,211) から在庫株を引いた(2022年12月31日現在28株)(132) 株主権益総額530,005 587,151と株主資本総額$1,002,383$1,049,698$1,049,698 |
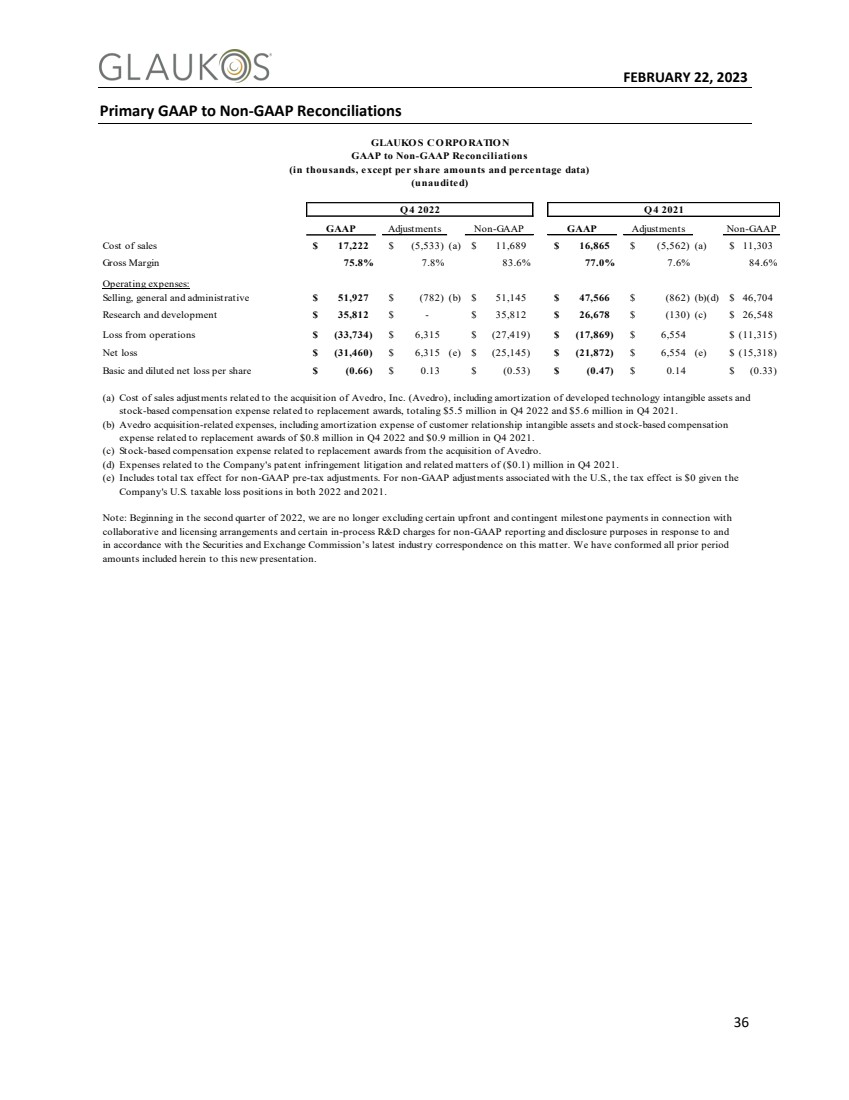
| 2023年2月22日36主要GAAP-非GAAP調整 GLAUKO S CO RPO比率N GAAPから非GAAP調整 (単位:千、1株当たり金額とパーセントデータを除く) (未監査) Q 4 2022 Q 4 2021 GAAP調整非GAAP GAAP調整非GAAP 販売コスト$17,222$(5,533)(A)$11,689$16,865$(5,562)(A)$11,689$16,865$(5,562)(A)$11,862$(A)$11,862$303毛金利75.8%7.8%83.6%77.0%7.6%84.6% 運営費用:販売、一般および管理費用$51,927$(782)(B)$51,145$47,566$(862)(B)(D)$46,704研究開発$35,812$-$35,812$26,678$(130)(C)$26,548運営損失$(33,734)$6,315$(27,419)$(17,419)$(17,419)869)$6,554$(11,315) 純損失$(31,460)$6,315(E)$(25,145)$(21,872)$6,554(E)$(15,318) 1株当たりの純損失$(0.66)$0.13$(0.53)$(0.47)$0.14$(0.33) (A)Avedro,Inc.(Avedro)の買収に関する販売調整コスト,開発された技術無形資産の償却とリセット奨励に関する株ベースの報酬支出を含め、2022年第4四半期に合計550万ドル、2021年第4四半期に560万ドル。顧客関係無形資産償却費用と株式補償 と2022年第4四半期の80万ドル、2021年第4四半期の90万ドルの代替奨励に関する株式補償支出を含む。 (C)Avedroの買収に対する代替奨励に関する株式補償支出。 (D)2021年第4四半期の会社特許侵害訴訟や関連事項に関する支出(10万ドル)。br}(E)には、非公認会計原則税前調整の総税収影響が含まれる。米国関連の非GAAP調整については、会社が2022年と2021年に米国での課税損失額を考慮すると、税収の影響は0ドルとなる, 米国証券取引委員会のこの件に関する最新の業界レターによると、我々は、協力および許可手配に関連するいくつかの前払いおよびまたはマイルストーン支払い、および非GAAP報告および開示目的のために行われているいくつかの研究開発費用を排除しない。本稿に含まれるすべての前期 金額をこの新しいプレゼンテーションと一致させた. |
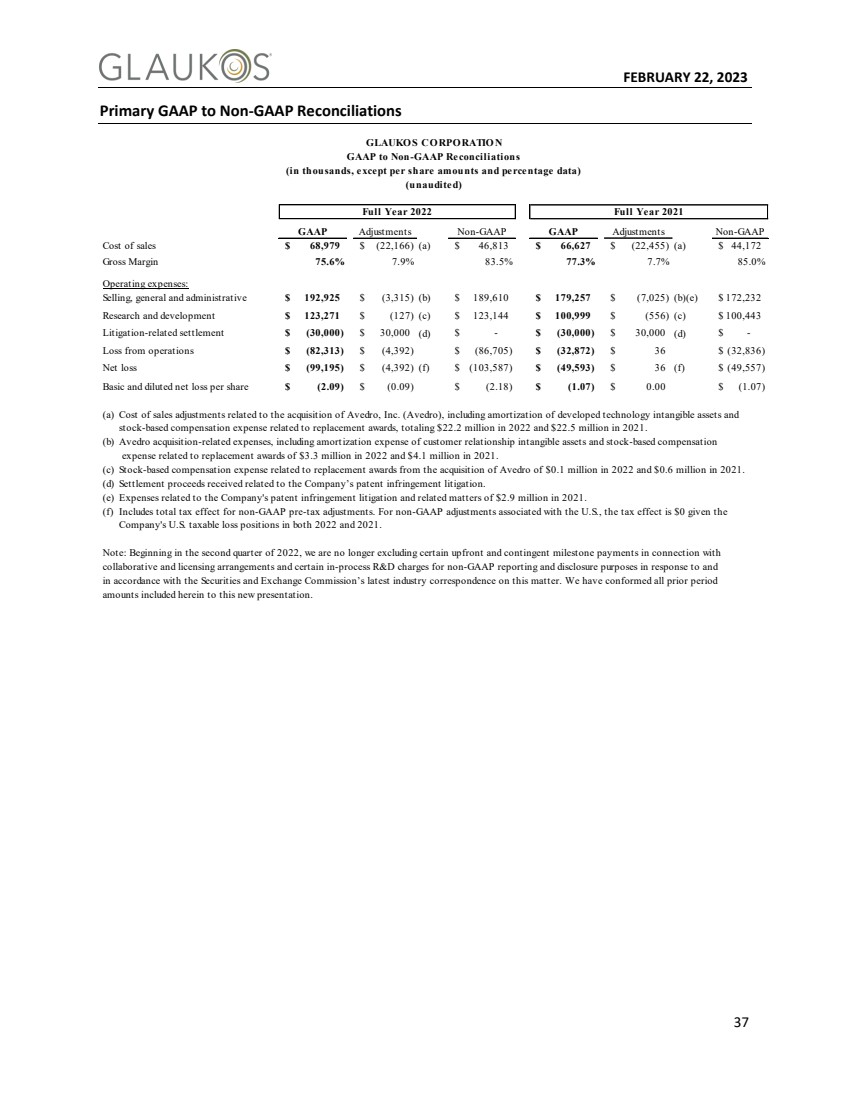
| FEBRUARY 22, 2023 37 Primary GAAP to Non-GAAP Reconciliations GLAUKO S CO RPO RATIO N GAAP to Non-GAAP Reconciliations (in thousands, except per share amounts and percentage data) (unaudited) Full Year 2022 Full Year 2021 GAAP Adjustments Non-GAAP GAAP Adjustments Non-GAAP Cost of sales $ 68,979 $ (22,166) (a) $ 46,813 $ 66,627 $ (22,455) (a) $ 44,172 Gross Margin 75.6% 7.9% 83.5% 77.3% 7.7% 85.0% Operating expenses: Selling, general and administrative $ 192,925 $ (3,315) (b) $ 189,610 $ 179,257 $ (7,025) (b)(e) $ 172,232 Research and development $ 123,271 $ (127) (c) $ 123,144 $ 100,999 $ (556) (c) $ 100,443 Litigation-related settlement $ (30,000) $ 30,000 (d) $ - $ (30,000) $ 30,000 (d) $ - Loss from operations $ (82,313) $ (4,392) $ (86,705) $ (32,872) $ 3 6 $ (32,836) Net loss $ (99,195) $ (4,392) (f) $ (103,587) $ (49,593) $ 3 6 (f) $ (49,557) Basic and diluted net loss per share $ (2.09) $ (0.09) $ (2.18) $ (1.07) $ 0.00 $ (1.07) (a) Cost of sales adjustments related to the acquisition of Avedro, Inc. (Avedro), including amortization of developed technology intangible assets and stock-based compensation expense related to replacement awards, totaling $22.2 million in 2022 and $22.5 million in 2021. (b) Avedro acquisition-related expenses, including amortization expense of customer relationship intangible assets and stock-based compensation expense related to replacement awards of $3.3 million in 2022 and $4.1 million in 2021. (c) Stock-based compensation expense related to replacement awards from the acquisition of Avedro of $0.1 million in 2022 and $0.6 million in 2021. (d) Settlement proceeds received related to the Company’s patent infringement litigation. (e) Expenses related to the Company's patent infringement litigation and related matters of $2.9 million in 2021. (f) Includes total tax effect for non-GAAP pre-tax adjustments. For non-GAAP adjustments associated with the U.S., the tax effect is $0 given the Company's U.S. taxable loss positions in both 2022 and 2021. Note: Beginning in the second quarter of 2022, we are no longer excluding certain upfront and contingent milestone payments in connection with collaborative and licensing arrangements and certain in-process R&D charges for non-GAAP reporting and disclosure purposes in response to and in accordance with the Securities and Exchange Commission’s latest industry correspondence on this matter. We have conformed all prior period amounts included herein to this new presentation. |
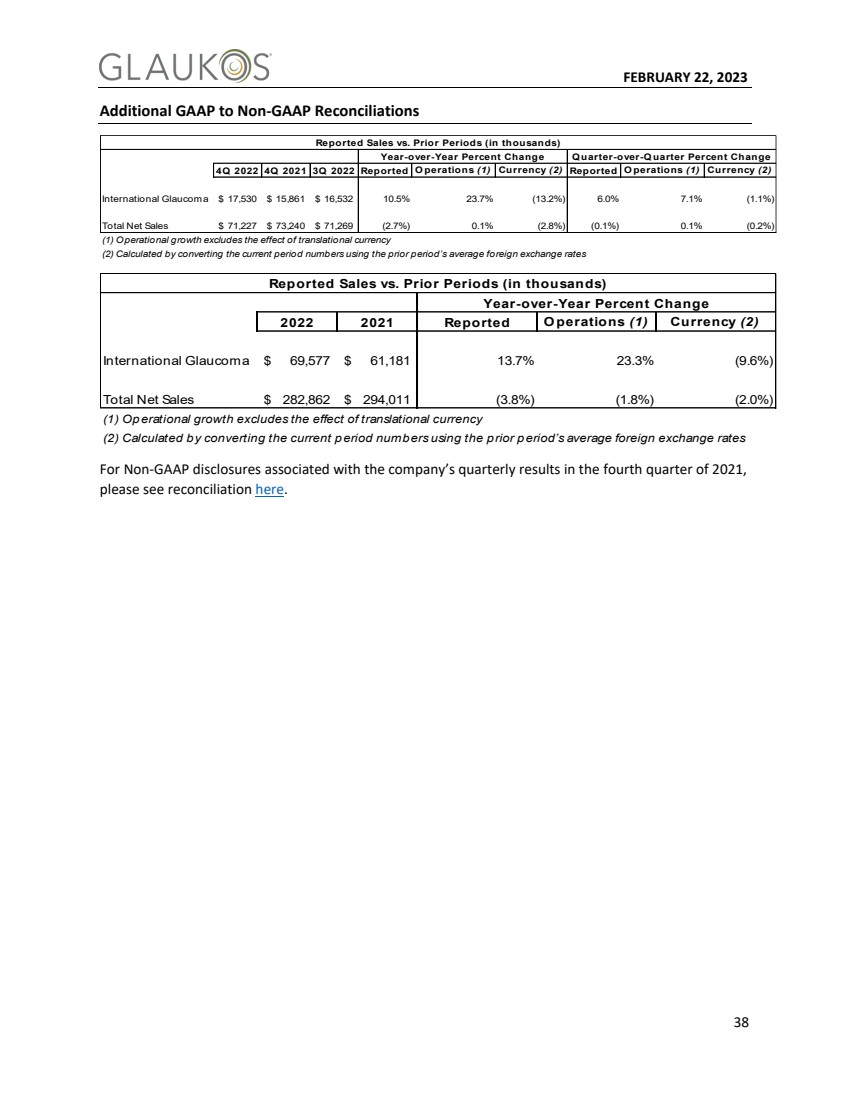
| FEBRUARY 22, 2023 38 Additional GAAP to Non-GAAP Reconciliations 4Q 2022 4Q 2021 3Q 2022 Reported O perations (1) Currency (2) Reported O perations (1) Currency (2) International Glaucoma $ 17,530 $ 15,861 $ 16,532 10.5% 23.7% (13.2%) 6.0% 7.1% (1.1%) Total Net Sales $ 71,227 $ 73,240 $ 71,269 (2.7%) 0.1% (2.8%) (0.1%) 0.1% (0.2%) (1) Operational growth excludes the effect of translational currency (2) Calculated by converting the current period numbers using the prior period’s average foreign exchange rates Year-over-Year Percent Change Q uarter-over-Q uarter Percent Change Reported Sales vs. Prior Periods (in thousands) 2022 2021 Reported O perations (1) Currency (2) International Glaucoma $ 69,577 $ 61,181 13.7% 23.3% (9.6%) Total Net Sales $ 282,862 $ 294,011 (3.8%) (1.8%) (2.0%) (1) Operational growth excludes the effect of translational currency (2) Calculated by converting the current period numbers using the prior period’s average foreign exchange rates Reported Sales vs. Prior Periods (in thousands) Year-over-Year Percent Change For Non-GAAP disclosures associated with the company’s quarterly results in the fourth quarter of 2021, please see reconciliation here. |