| 投資家 プレゼンテーション 2022年11月 |
| 2 2022 Glaukos Corporation 免責宣言 すべての 宣言 その他 宣言 歴史 事実 は 本プレゼンテーション は 活動、 イベント または 発展 私たち は期待しています。 は または は または で が 未来に は 展望 宣言 これらの 宣言 は 管理層の 現在の 期待, 仮説に基づいていると信じている. 推定 と 信念 . 我々 は 我々 が 前向き - 前向き 陳述 に対して 合理的な 基礎 があると信じているが, 我々 我々 は 彼ら が 現在の 期待 未来 が私たち に影響を与えるイベント が リスク, 不確実性 と 要因の影響を受ける に基づいて私たちの運営 と業務環境に関する に基づいていることを注意します 私たち と業務環境に関する このうち 難 のすべての 予測 と の多くの の中の は我々の 制御範囲を超えている, は 我々の 実際の 結果 と が実質的に異なる それらの で表される または が示唆する が 本プレゼンテーション で展望する 文 を引き起こす可能性がある これらの の潜在的な リスク と 不確定要素 が 実際の 結果 から に 前向き - に記述されている に記述されている 結果 から に実質的な差がある 文 を含むかどうかは, 無 制限なし, COVIDの持続時間 と重症度 に関する 不確実性 − 19 大流行 とその が我々の 業務 または 経済 に与える影響 一般 マクロ経済状況 の影響 ; 社の iStent シリーズ製品 製品 製品 製品の iStent シリーズ 影響 プログラム が 医師 費用 とASC 施設 費用 精算 料金 最終決定 を利用して }私たちの U . S . 組合せ - 白内障 緑内障 収入 上; 我々の 能力 継続 生成 販売 我々の 商業化製品 開発 と 商業化 その他 製品 ; 我々の は a 有限の 数量 第三者 - サプライヤー, 部分 ただし は 単一の - ソース, 我々の製品の コンポーネント の に依存する; 我々の 主な 工場で 障害性 事故, 自然災害, 大流行 あるいは その他 中断 これらの が を製造する可能性 が 生産能力 と 運営 に大きな影響を与える が発生する可能性がある は iStent , iStent iStent 注射 W , iStent を用い, iStent は iStent , iStent 注射 プログラム , iAccess 第三者 - 第三者 支払人 プログラム を用いて iAccess または{bent を使用する. 我々の 角膜 交差 - リンク 製品 または その他 製品 が開発されている ; 我々の 能力 は正しい 訓練, と は を得て と の信頼を受ける , 眼科医 は において は我々の 製品 を使用する; 我々の 能力 は 競争の激しい と急速に変化する 医療機器 業界 と 未来の 技術 ( MiGs 技術を含む)で が を効率的に競争する; 私たちの は 連邦、 州 と 外国 法律 と 法規 の 許可 と 販売 および 私たちの 製品 と 私たちの は プロセスの マーケティング ; 冗長な 冗長な と高価な 臨床試験 過程 と 時間 と 結果の 不確実性 任意の 任意の 特定の 臨床試験 あるいは 規制承認 過程 ; 我々の 製品 の リスク は あるいは の深刻な安全問題 私たちの 製品 と 患者の 結果 の 不確実性 ; 我々の 能力 保護, と 費用 と時間 - 消費 保護の 性質 , 我々の 知的財産権 は 第三者 と 競争相手の に影響 任意の 私たちに対する 侵害 あるいは 流用 第三者 知的財産権 権利 と 任意の に関する 訴訟 ; と 私たちの 債務返済能力 私たちの債務 。 この と その他の 既知の リスク、 不確実性 と 要因 の 詳細情報 における タイトル “リスク 要因” と は 我々の が 証券 と取引所 委員会(米国証券取引委員会)に提出された文書に が記述されている である. は 我々の 四半期報告 表 10 - q 現在 9月30 , 2022 の 四半期報告を含む, どの が 11 4 で アメリカ証券取引委員会 に を提出しました 2022 . 私たちが アメリカ証券取引委員会 に提出した書類 は 投資家 欄 私たちの サイト www . glaukos . com あるいは は www . アメリカ証券取引委員会 . gov また、 また、 我々の 製品 は私たちの サイトで www.br}. glaukos . com に すべての 転送 - 展望 宣言 に含まれる 情報が含まれていますプレゼンテーション は 前述の 警告 宣言 で明確に その 完全 を限定します。 あなた は 不要 を 不適切な 依存 転送 - を見ている 宣言 に を置いて を宣言します ただし は の 日付 の のみとする. 我々 は のいかなる 義務 更新, 修正 修正 これらの これらの 転送 - を探して 宣言 が であるかどうか 新しい 情報の結果 として を探す. 未来の イベント または でなければ, 以外の は が適用される証券 法律 に基づいて が必要となる可能性がある |
| 3 2022 Glaukos社 3 2021 Glaukos 会社は内部使用のみの特権、機密と専門性 |
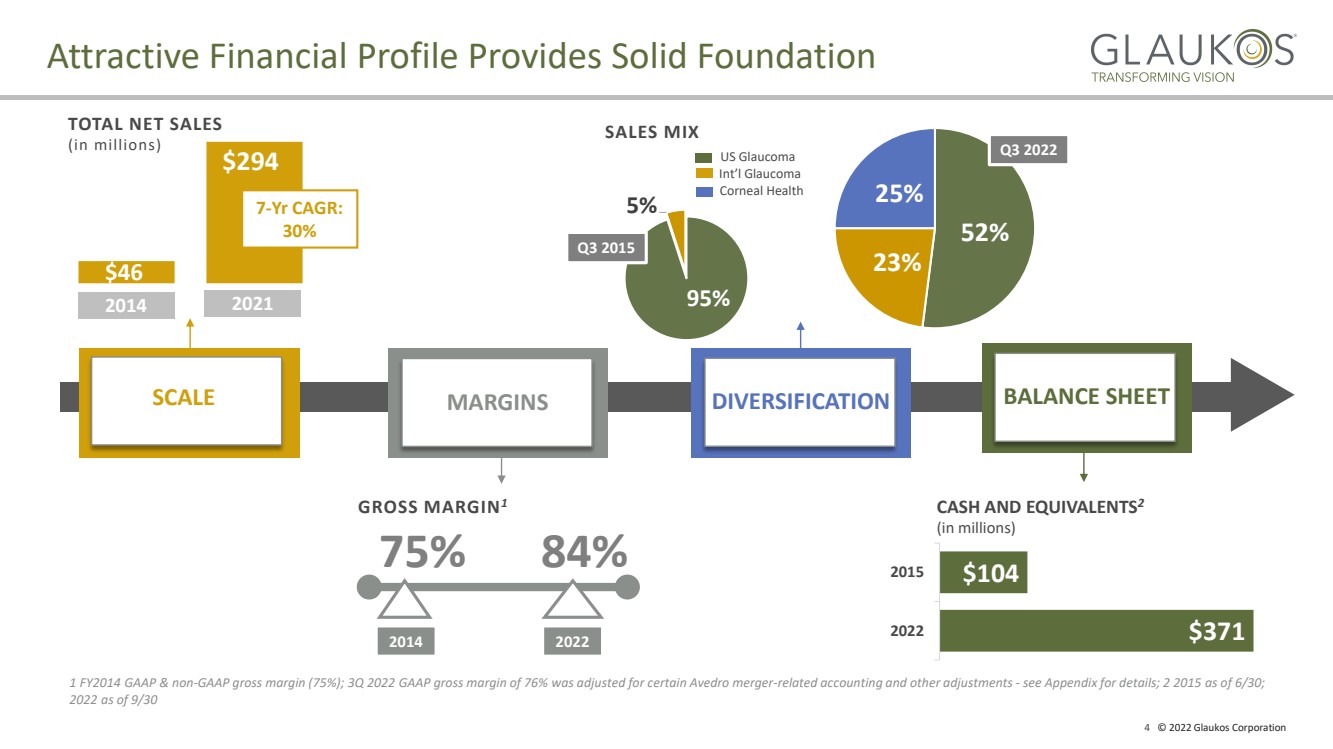
| 4 2022 Glaukos Corporation 魅力的な財務状況は堅固な基礎 規模 利益率 多元化 貸借対照表 $46 …を提供します。 7 − 年複合年間成長率: 30% 2014 2021 総純売上高 $294 2022 75 84% 2014 1会計年度GAAP及び非 − GAAP利回り(75%);2022年第3四半期GAAP毛金利は76%であり、あるAvedro合併に対して調整 - 関連口座 入金と他の調整 - の詳細は付録に示す;2 2015年6月30日; 2022年9月30日まで 米国緑内障 角膜健康 国際緑内障 販売組合 毛金利 1 $371 $104 2022 2015 現金及び等価物 2 (百万単位) 95% 2015第3四半期 52 23 25% 第3四半期2022 |
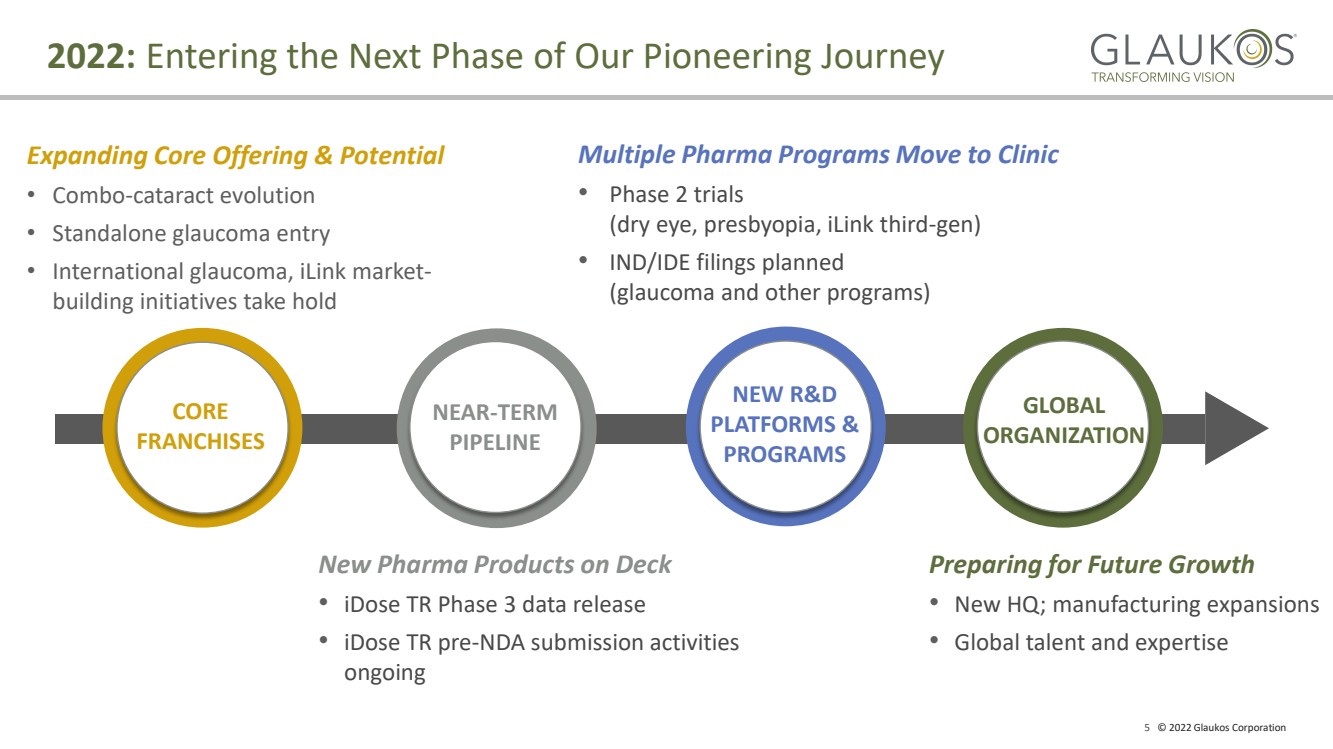
| 5 2022 Glaukos Corporation 2022: は私たちの創業旅行の次の段階 コア 特許経営権 接近 − 条項br}パイプライン 新開発 プラットフォームと 計画 グローバル 組織 拡張コア製品と潜在力 組合せ − 白内障変化 · 独立緑内障入門 · 国際緑内障、ILink市場 − 建設計画発効 新薬発売 iDose trステージ3データ発表 iDose tr Pre − NDA提出活動 現在行われている 複数の医薬項目が臨床 · 第2段階試験 (ドライアイ、老眼、ILink Third − gen) · IND/IDE申請計画 (緑内障と他の項目) 未来成長の準備 · 新本部;製造拡張 · グローバル人材と専門知識 |
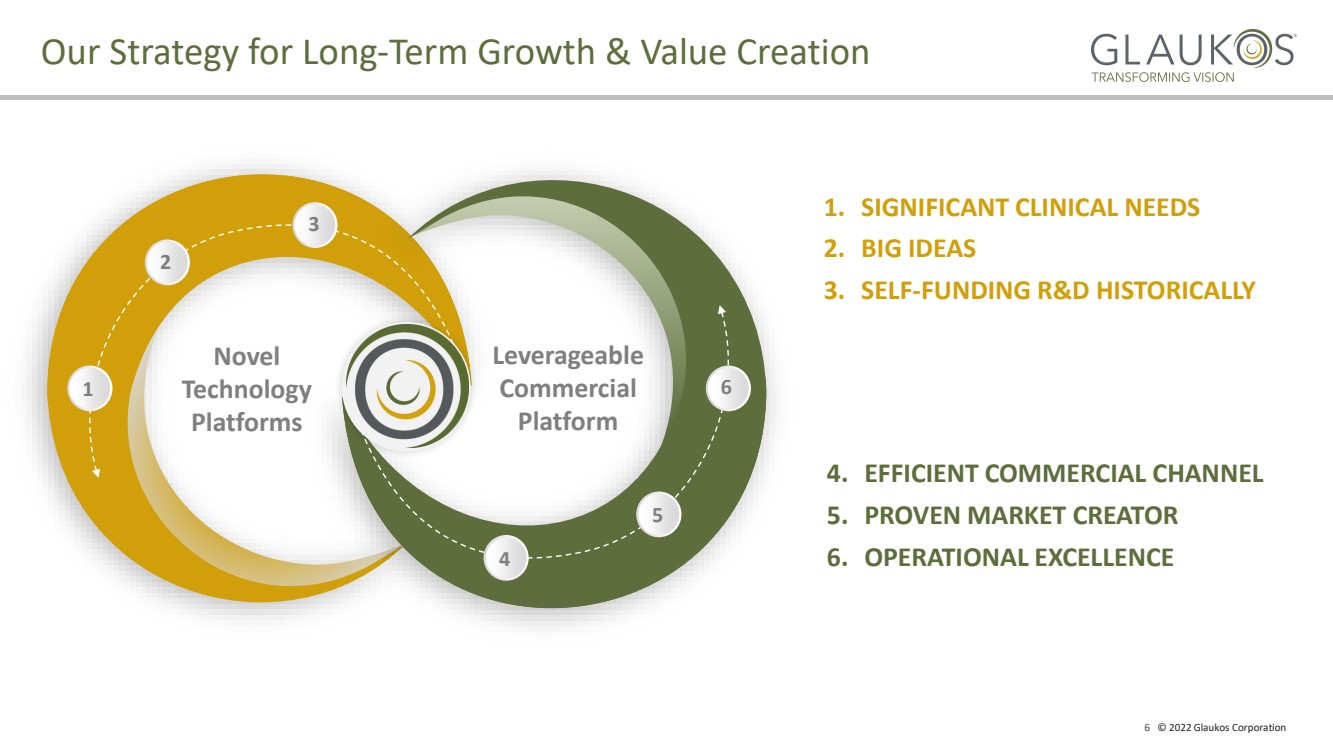
| 6 2022 Glaukos Corporation 1 2 3 4 5 6 新しい 技術 プラットフォーム 利用可能な 商業 プラットフォーム 重要な臨床需要 2. 大アイデア 3. 自身 - 従来研究開発に資金を提供してきた 4. 効率的なビジネスチャネル 5. 成熟した市場クリエーター. 6. 卓越した運営 我々の長期戦略 − 長期成長と価値創造 |
| 7 2022 Glaukos Corporation 大アイデア:伝統を覆す局所目薬療法 局部点眼液はよく無効 患者に - 依存性 従わにくい複雑な投与方案 · 物忘れ · 点滴が生活の質 · 眼表疾患に挑戦するため、毒副作用と他の副作用br患者はより良い方法が必要! 我々は伝統を変え、革新的な無滴注療法を用いて患者の予後を改善するために努力している |
| 8 2022 Glaukos Corporation 我々の新技術プラットフォーム 6+計画 2018年以来研究開発投資において重要な規制マイルストーン 400万 $ がパイプライン計画 14 2015 2022 4 5 技術独特のプラットフォーム 製薬 革新主導 が私たちの3つの特許経営において看護標準 製薬 外科設備 を向上させることを開示しました |
| 9 2022 Glaukos Corporation すべてのプラットフォームは伝統的なモード を覆して、多種の革新 を産生することを目的としており、これらの革新は 現在の看護標準(1滴の目薬ではない)を超える優勢を提供しているbr}私たちの差別化プラットフォームの独特な機能 先駆性第1: はすでに証明された能力を最大限に高め、持続的、革新的な市場 高生産性: 各プラットフォームの複数の製品は各製品のコストを下げ、 成功確率 拡張潜在力を高める: 専門知識と能力 追加追加破壊的プラットフォーム 巨大かつ/あるいはサービス不足の患者 人群 ゲーム - 絶えず変化する 革新 - 設備、 製薬或いは混合設備 我々の重点 製薬 外科設備 |
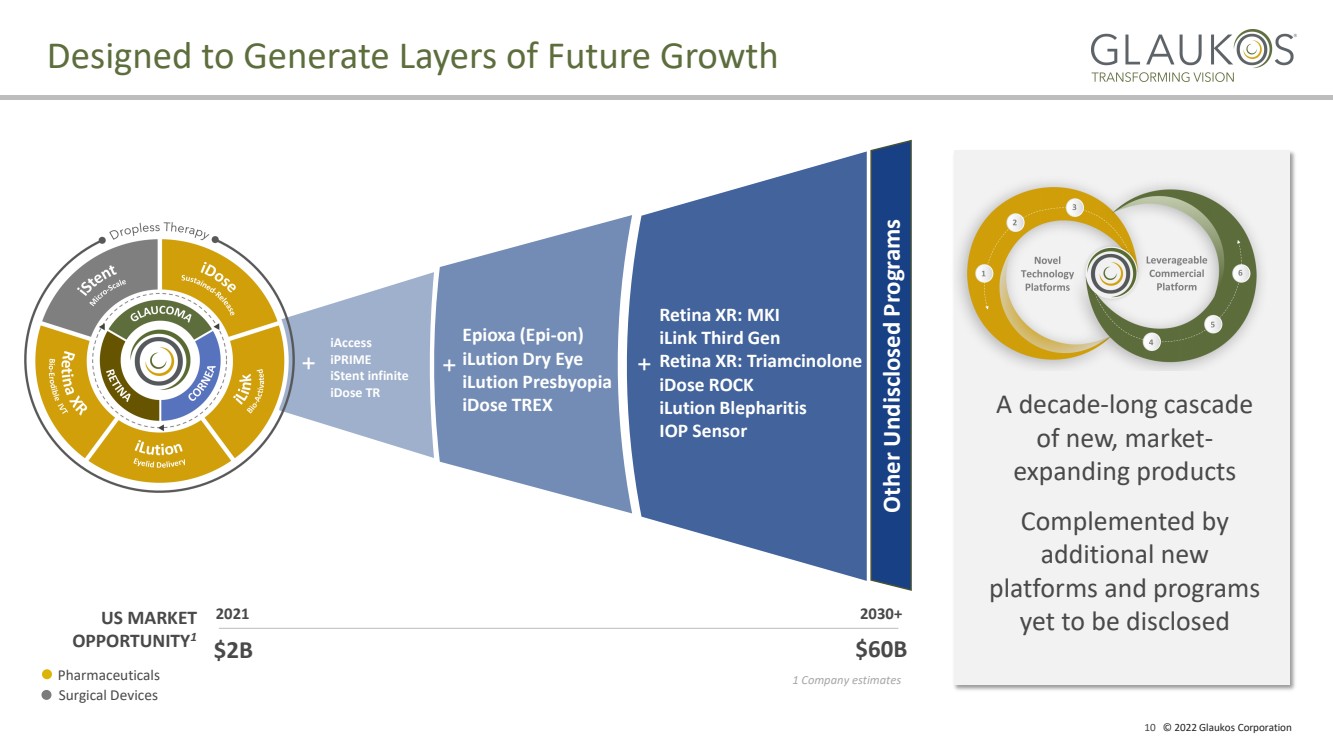
| 10 2022 Glaukos Corporation 2021 2030+ 米国市場 1 $2 B $60 B iAccess iPRIME iStent無限 iDose tr ipioxa(Epi − on) iPUSEドライアイ iLUSE老眼 iDose TREX XR:MkI 網膜DRibock{DRiDose{brebr}XR:MkI 網膜DRibock iPotox XRセンサー + 10年 - 下落 新、市場 − が拡大している製品 それ以外の新しいbr}プラットフォームと計画 開示すべき 未来の成長を生み出すことを目指しているbr}他の未開示の計画br}1社は 製薬 外科機器 を推定しています |
| 11 2022 Glaukos Corporation 私たちが利用可能なビジネスプラットフォームを通じて 2014 2022 直売国/地域 2 17 $225 効率的で拡張可能な プラットフォームを介して 成長する世界規模で一連の 良質な製品と サービス クライアント群 が既存の販売チームに入る製品 2015 2021 65 65 グローバルビジネススタッフ を提供する準備ができています |
| 12 2022 Glaukos Corporation 1 M+ iStentデバイス グローバルインプラント iStentプラットフォーム:Migs Pioneer&Innovation Leader 製品/計画 疾患 状態 iStent/iStent注射/ iStent注射W 軽度 − から − 中等度 緑内障合併白内障 承認 (2012/2018/2020) iStent Br}手術治療) 独立した FDAは iStent無限 緑内障(ラベル 拡張) 独立した IDE待機 PReserve Flo 末期 − 難治性緑内障 緑内障 独立した PMA非 − 承認を承認した;現在行われている商業製品と公開されているパイプライン計画 業界 の最も全面的なマイクロ − 外科、組織 − 予備解決策を審査し、個々の外科医の個人緑内障治療アルゴリズム 20 + の長年の臨床 経験 200 同業者 に適応するための全方位的なオプション を提供し,iStent 技術に関する出版物 + 組合せ − 白内障 独立 を査読した |
| 13 2022 Glaukos Corporation iAccessは2022年第1四半期にbr} iAccessを発売し、小梁ネットワーク組織を切断することを目的とし、br}それによって房水がSchlemm管(Br)iAccess開骨手術に直接流入することを許可し、外科医師にbr}外科技術の多機能性を提供し、外科医師が患者に最適な手術方式を決定できるようにし、いくつかのクロック時間にまたがる複数の小切り口にかかわらず、95%までの解剖を維持することを目的としている。あるいはシュレム運河の広範囲開放 は2022年第1四半期末にアメリカの商業発射活動 組織 - を保留し、 最小限に - 侵入性 を開始しました |
| 14 2022 Glaukos Corporation iPRIME iPRIMEは低侵襲なbr}粘弾性送達システムであり、br}医師と患者の需要brをさらに支持し、br}はGlaukosの広範な革新的な眼科ソリューション製品の組み合わせbrをさらに拡張し、2022年第2四半期末にアメリカで商業活動 粘弾性送達システム を開始した |
| 15 2022 Glaukos Corporation iStent INFINE:強力な独立MIGは の3つのヘパリン - コーティングチタンステントを自動 - 注射システムにプリチャージすることを示し、このシステムは外科医がSchlemm管周囲の約6時間以内に最大 時間にわたってステントを注入することを可能にする。眼の主なドレナージチャネル は、良好な安全性と有効性を強調する強力なキーデータによって支持され、独立緑内障治療のための最初の浸潤性デバイス − がFDAの承認を得て、2022年第4四半期から米国での予備活動 画像はGeorge R.Reiss MDから を提供する |
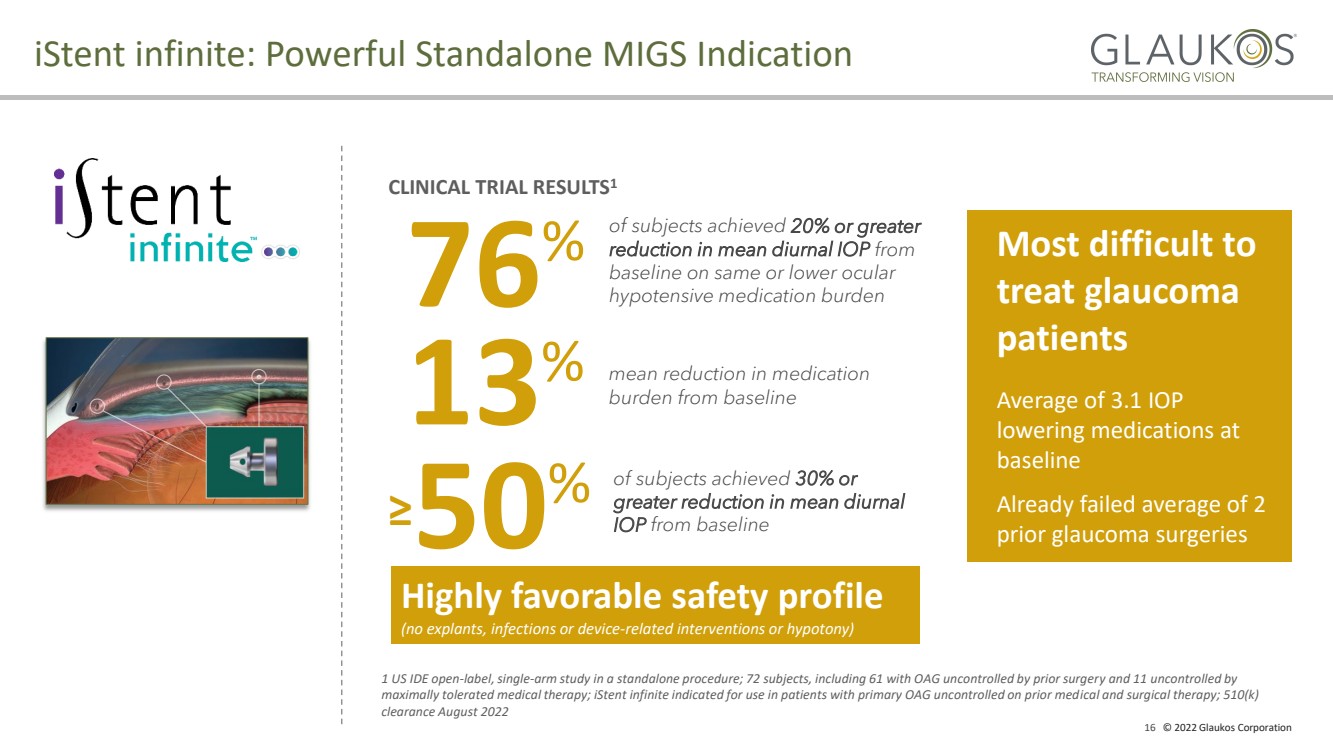
| 16 2022 Glaukos Corporation iStent無限:強力な独立MIG適応 臨床試験結果 1 76 被験者は同じ或いはそれ以下の眼圧に基づいて、平均毎日眼圧低下 20%以上の 降圧薬物負担 13 50 被験者の平均毎日眼圧がベースラインより30%以上低下する 服薬 ベースラインの負担 % 高度に有利な安全性プロファイル (外植体なし、感染或いは設備 - 関連関与或いは低眼圧) 最も難しい 緑内障 患者 平均3.1回眼圧低下薬物のbr}ベースライン 前の緑内障手術は平均2 以前の緑内障手術 1回アメリカIDE開放 - ラベル、単一の - ARM研究は1つの独立したプログラムで研究されている;以前の外科医が制御できなかったOAGおよび11人の制御不能最大耐性薬物治療を含む72人の被験者;iStent INFINEは、以前の内科および手術治療のために制御されていない原発OAGの患者を推奨し、510(K) 2022年8月 |
| 17 2022 Glaukos Corporation iDoseプラットフォーム:緑内障治療計画の次の段階 疾患 状態 iDose tr OHT − 難治性緑内障 難治性緑内障 第3期 iDose TREX oht − 難治性緑内障 緑内障 臨床 iDose Rock O − 難治性緑内障 前置 どこにでもいる患者がbr}− の局所薬に関連する慢性副作用 を提供することにより24/7を提供することを目的としたパイプライン計画 を公開した。Br}持続時間が長い − 副作用最小の持続効果 非堅持による眼圧上昇による緑内障進展と視力喪失 2 ;Br}の50%近くの緑内障患者が2種類以上の外用薬を処方しているbr}3 研究 1 研究によると,br}10 − 25%の新規緑内障患者は2番目のbr処方とbr}~40 − の60%の新規開設患者は1年目の終了時に彼らの薬“br}1 Quigley HAを服用しなくなった:2011年には個々の緑内障患者が知るべきこと;Friedman DSらは眼科医に投資している。2007年;緑内障研究財団;2 Leske Cらbrアーチ型眼科。2003;3市場範囲2021年 |
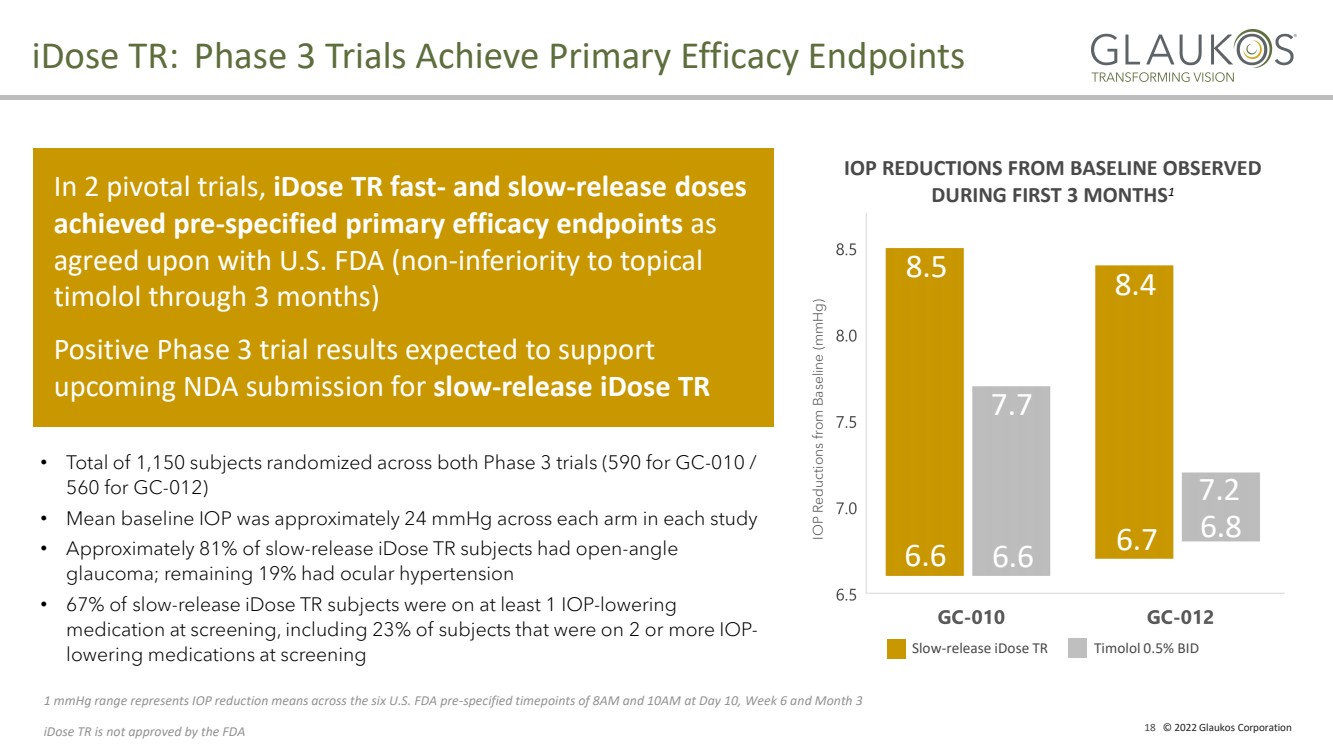
| 18 2022 Glaukos Corporation 眼圧はベースライン(ミリ水銀)より8.5 6.6 7.7 6.6 6.7 8.4 6.8 7.2 iDose tr: 第3段階試験は主要な治療効果終点 1 mm水銀範囲を達成し、6つのアメリカFDA Pre - が指定した時点を表して10日目の午前8時と10点の眼圧低下平均レベルを達成した。6週目3カ月目 Timolol 0.5%Bid 緩やか − 2つのキー試験でiDose tr を放出し, iDose tr Fast − とSlow − 放出量 が到達する前の − と米国FDAが合意した指定主要治療効果終点 −(非 − は3カ月以内に局所投与 チプロロール) 陽性より低い3期試験結果 が提出されるNDA 徐速 − 放出iDose tr · を支持する予定の被験者1150名にランダムに両3期試験(GC 590,GC − 012) · は各研究において,各腕の平均ベースライン眼圧が約24ミリ水銀カラム · iDose trを徐放した被験者のうち,約81 %の被験者に開放 − 隅角緑内障であった。残りのbr}19 · 67%の徐放性iDose tr被験者はスクリーニング時に眼圧 − 薬を少なくとも1回服用し,そのうち23 %の被験者はスクリーニング時に2回または2回以上の眼圧降下薬 iDose trを服用しており,FDAの承認を得ずに3カ月前に観察された眼圧はベースラインより1 低下した |
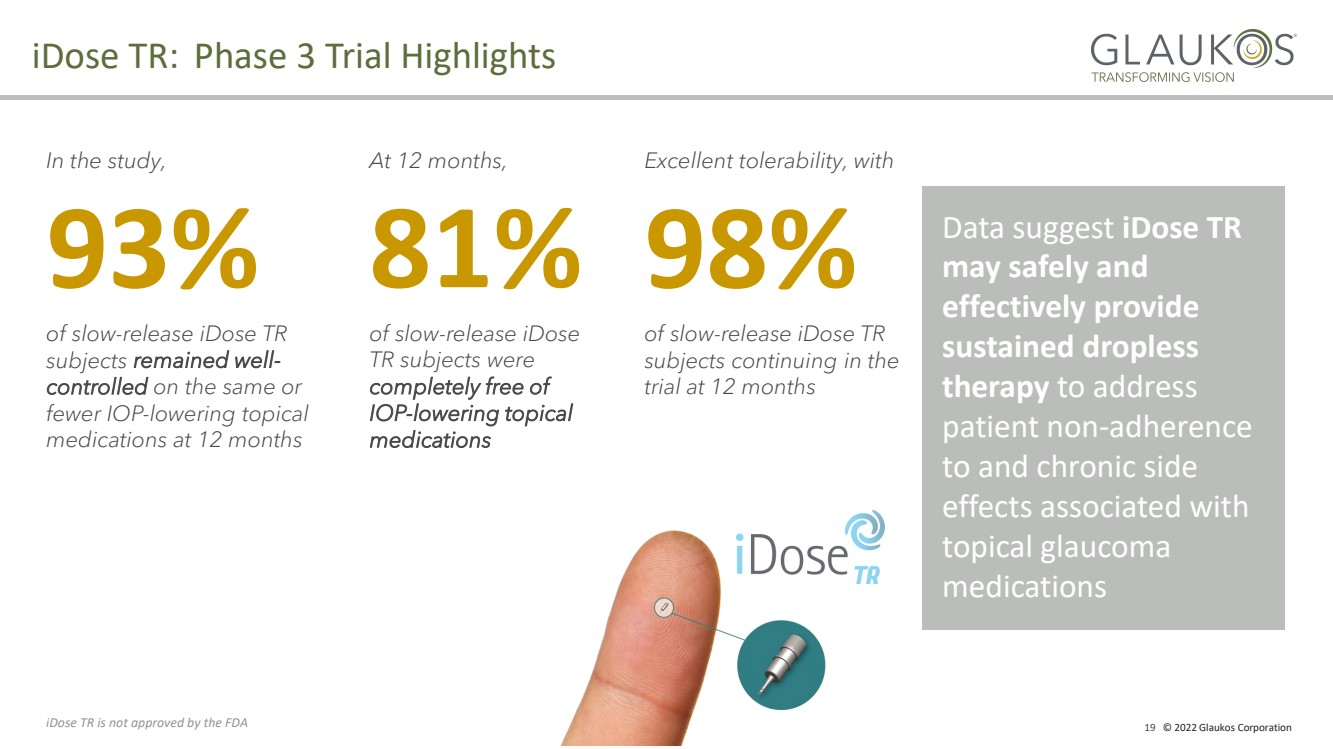
| 19 2022 Glaukos Corporation データは 患者の非br}− 依存性と 局所緑内障に関連する慢性副作用 薬物 iDose tr: 第3段階試験ポイント iDose tr未研究のFDA承認を解決するために安全かつ効率的にbr}持続無滴br}療法 を提供することができることを示している。 93% 徐放iDose tr 被験者 は同じ或いはそれ以下のIOPで良好なbr}- 制御 を維持し、12ケ月時に外用薬br}br}耐性を低下させることは極めて良く、徐放iDose tr 被験者は12ケ月後にbr}試験 を継続し、Br}81% 徐放iDose tr被験者はbr}眼圧 - が全くなく外用薬 を低下させた |
| 20 2022 Glaukos Corporation iDose tr: 第3段階試験ポイントiDose trは、米国食品医薬品局から第3段階試験の一部として承認されていない。Br}オフィス投与は、複数のbrサイトの異なる被験者にiDose tr を適用することに成功し、結果は、br}− オフィスで投与した3期試験結果と一致した。オフィス投与の可能性は、br}角膜内皮細胞損失のない有害事象 に重篤な角膜不良事象 がなく、眼窩周囲脂肪萎縮のない不良事象br}結膜うっ血率(3%) が12カ月以内に良好な安全性を示すことを証明した |
| 21 2022 Glaukos Corporation iDose tr米国食品医薬品局から許可されていないbr}iDose tr: 36ヶ月の2 b期データ - 8.3 - 8.2 ~ 70% 応答者 iDose 上で同じかそれ以下の局所投与 眼圧 - 低下薬物治療36ヶ月はスクリーニング と比較して 36カ月の平均眼圧低下 では,iDose trの効果はtimololと類似しており は投与回数が少なく とtimolol · 眼球充血 (30 − 50%+外用PGAs) · 無眼窩周囲脂肪萎縮 (pGAs外用発生率70%) · がなく臨床的に明らかな角膜内皮細胞喪失 · は1例のみであった。虹彩色変化 (PGA外用発生率約20%) iDose tr耐性良好 対照腕では,1眼あたりプロトコル点眼 2回 − 1日硫黄か心安が36カ月持続し,1回の注射 iDose · 患者のIOPへの依存性が一般的に悪い − 低下 点眼液 · iDose設計は100%コンプライアンス を意味する。· 緑内障薬コンプライアンスの改善は緑内障疾患のより良い結果に関係している |
| 22 2022 Glaukos Corporation iLinkプラットフォーム:BIO - 活性化薬品 製品/プログラム 疾患 状態 Photrexa(Epi - 閉鎖) 円錐角膜 承認 (2016) Epioxa(Epi - on) 円錐角膜 第3段階 iLink第3期 - 第2世代円錐角膜商業製品と公開されたパイプライン計画 を積極的に募集するには,円錐角膜の進行を緩和または阻止できることが証明された療法 ; が有効な治療がなければ, 進行性円錐角膜患者5名に1人が角膜移植 1,2 の研究を必要とする可能性があり, 72% と 98% の角膜移植はそれぞれ20年以内と30年以内に失敗した 1,2 1 Pramanik S,Musch DC,Sutin je,Farjo AAであることが示されている。円錐角膜透過性角膜移植の長期治療効果。眼科論理。2006;113(9):1633 - 1638。2.Maharana PK、Agarwal K、Jhanji V、 Vajpayee RB。深前板層角膜移植治療円錐角膜の研究進展アイコンタクト。2014;40(6):382 - 389 200+ 同行 - iLink上の 出版物 を査読した |
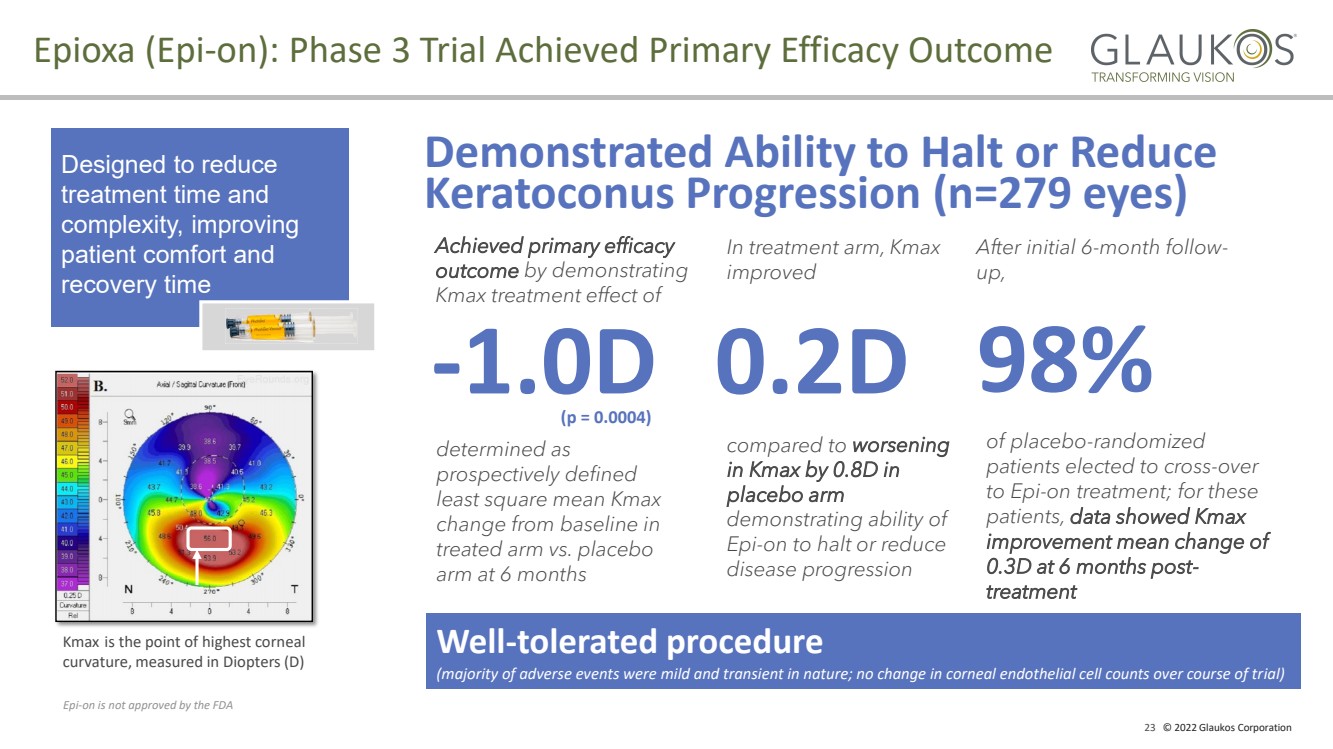
| 23 © 2022 Glaukos Corporation Epioxa (Epi - on): Phase 3 Trial Achieved Primary Efficacy Outcome - 1.0D Achieved primary efficacy outcome by demonstrating Kmax treatment effect of Well - tolerated procedure (majority of adverse events were mild and transient in nature; no change in corneal endothelial cell counts over course of tr ial ) Epi - on is not approved by the FDA determined as prospectively defined least square mean Kmax change from baseline in treated arm vs. placebo arm at 6 months (p = 0.0004) 0.2D In treatment arm, Kmax improved compared to worsening in Kmax by 0.8D in placebo arm demonstrating ability of Epi - on to halt or reduce disease progression 98% After initial 6 - month follow - up, of placebo - randomized patients elected to cross - over to Epi - on treatment; for these patients, data showed Kmax improvement mean change of 0.3D at 6 months post - treatment Demonstrated Ability to Halt or Reduce Keratoconus Progression (n=279 eyes) Designed to reduce treatment time and complexity, improving patient comfort and recovery time Kmax is the point of highest corneal curvature, measured in Diopters (D) |
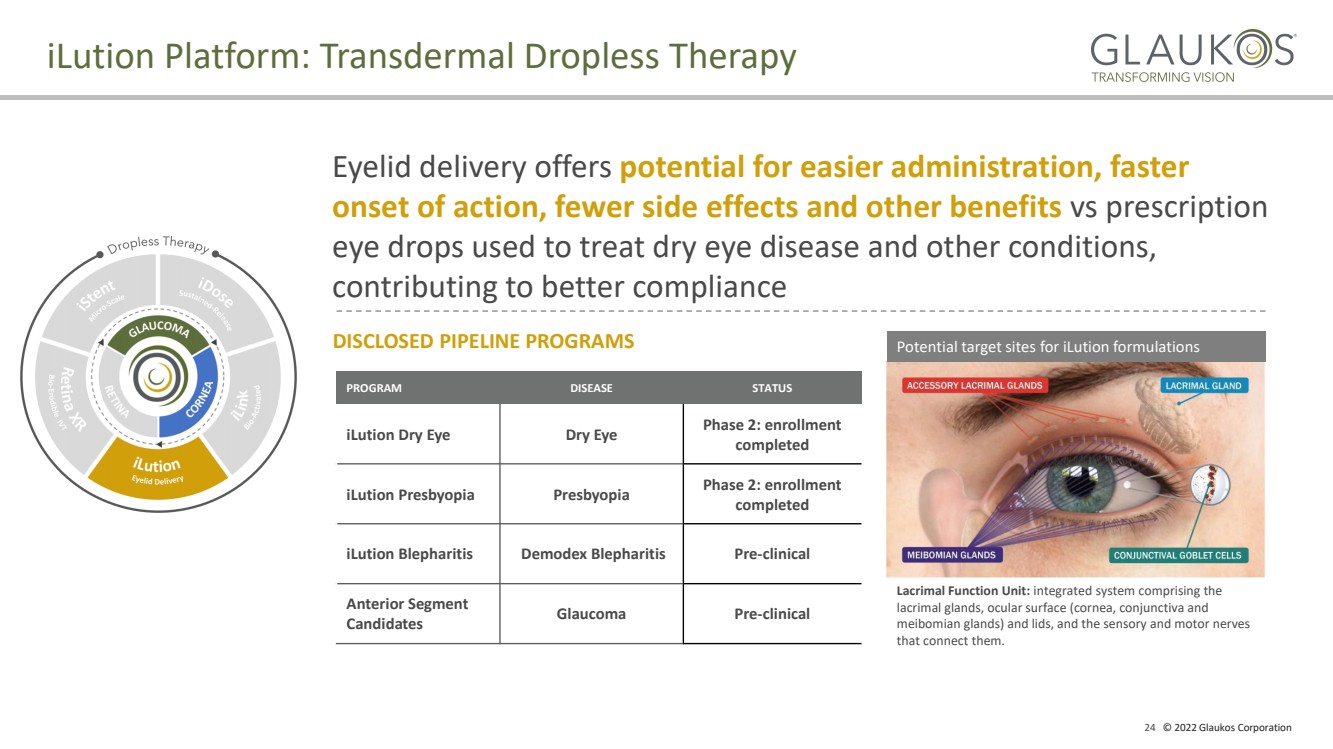
| 24 © 2022 Glaukos Corporation iLution Platform: Transdermal Dropless Therapy PROGRAM DISEASE STATUS iLution Dry Eye Dry Eye Phase 2: enrollment completed iLution Presbyopia Presbyopia Phase 2: enrollment completed iLution Blepharitis Demodex Blepharitis Pre - clinical Anterior Segment Candidates Glaucoma Pre - clinical DISCLOSED PIPELINE PROGRAMS Eyelid delivery offers potential for easier administration, faster onset of action, fewer side effects and other benefits vs prescription eye drops used to treat dry eye disease and other conditions, contributing to better compliance Lacrimal Function Unit: integrated system comprising the lacrimal glands, ocular surface (cornea, conjunctiva a nd meibomian glands) and lids, and the sensory and motor nerves that connect them. Potential target sites for iLution formulations |
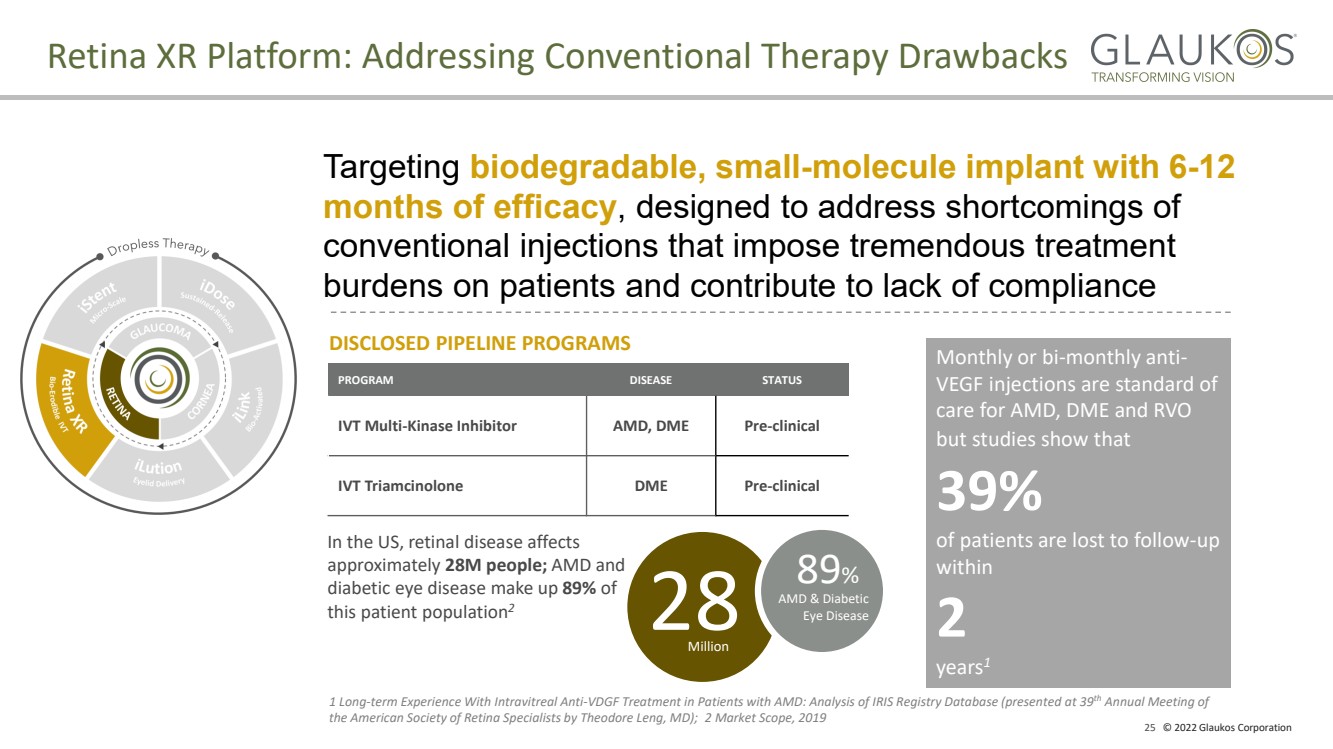
| 25 © 2022 Glaukos Corporation Retina XR Platform: Addressing Conventional Therapy Drawbacks PROGRAM DISEASE STATUS IVT Multi - Kinase Inhibitor AMD, DME Pre - clinical IVT Triamcinolone DME Pre - clinical DISCLOSED PIPELINE PROGRAMS Targeting biodegradable, small - molecule implant with 6 - 12 months of efficacy , designed to address shortcomings of conventional injections that impose tremendous treatment burdens on patients and contribute to lack of compliance Monthly or bi - monthly anti - VEGF injections are standard of care for AMD, DME and RVO but studies show that 39% of patients are lost to follow - up within 2 years 1 28 Million 89 % AMD & Diabetic Eye Disease In the US, retinal disease affects approximately 28M people; AMD and diabetic eye disease make up 89% of this patient population 2 1 Long - term Experience With Intravitreal Anti - VDGF Treatment in Patients with AMD: Analysis of IRIS Registry Database (presented at 39 th Annual Meeting of the American Society of Retina Specialists by Theodore Leng, MD); 2 Market Scope, 2019 |
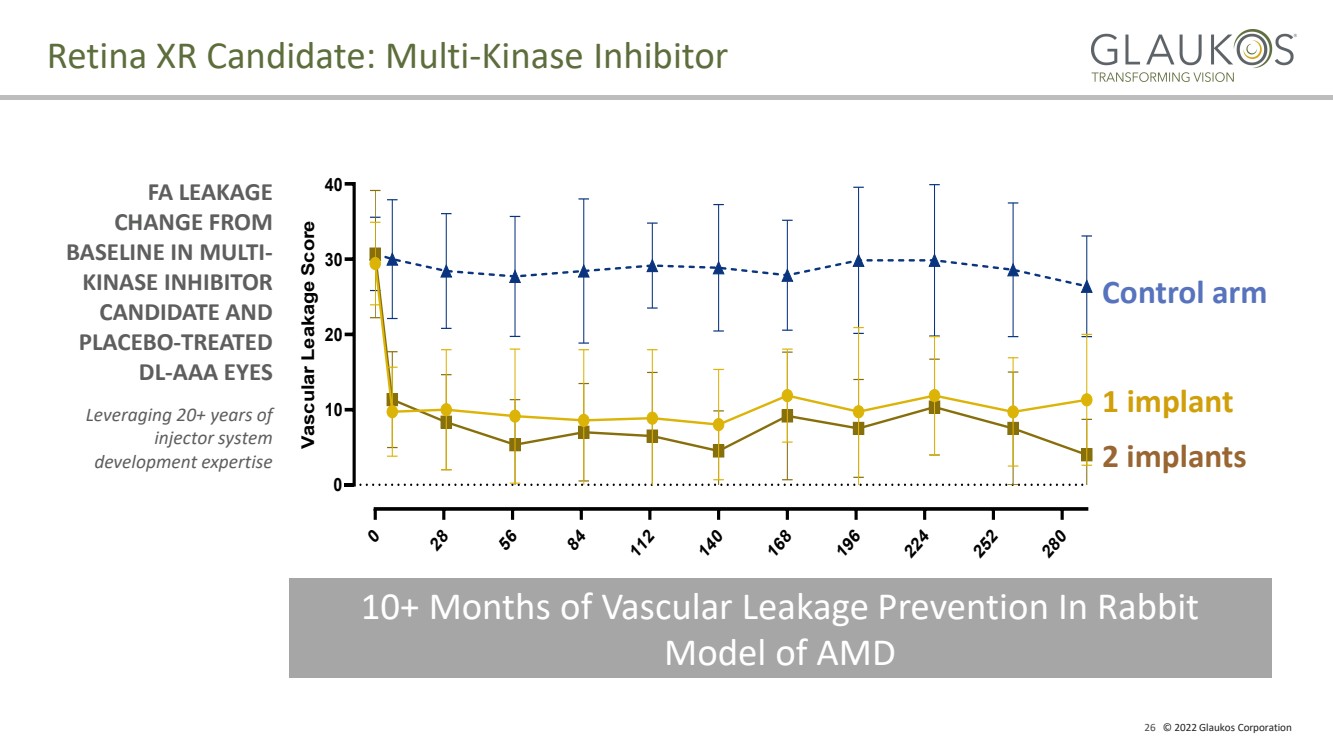
| 26 © 2022 Glaukos Corporation Retina XR Candidate: Multi - Kinase Inhibitor FA LEAKAGE CHANGE FROM BASELINE IN MULTI - KINASE INHIBITOR CANDIDATE AND PLACEBO - TREATED DL - AAA EYES Leveraging 20+ years of injector system development expertise 0 28 56 84 112 140 168 196 224 252 280 0 10 20 30 40 Vascular Leakage Score 1 Implant 2 Implants Control Arm 1 implant 2 implants Control arm 10+ Months of Vascular Leakage Prevention In Rabbit Model of AMD |
| 27 © 2022 Glaukos Corporation Commercial Execution in the Areas Most Visible to Investors… Under the Surface: Photrexa (Epi - off) Combo - Cataract 30% 7 - Year CAGR Standalone Therapies |
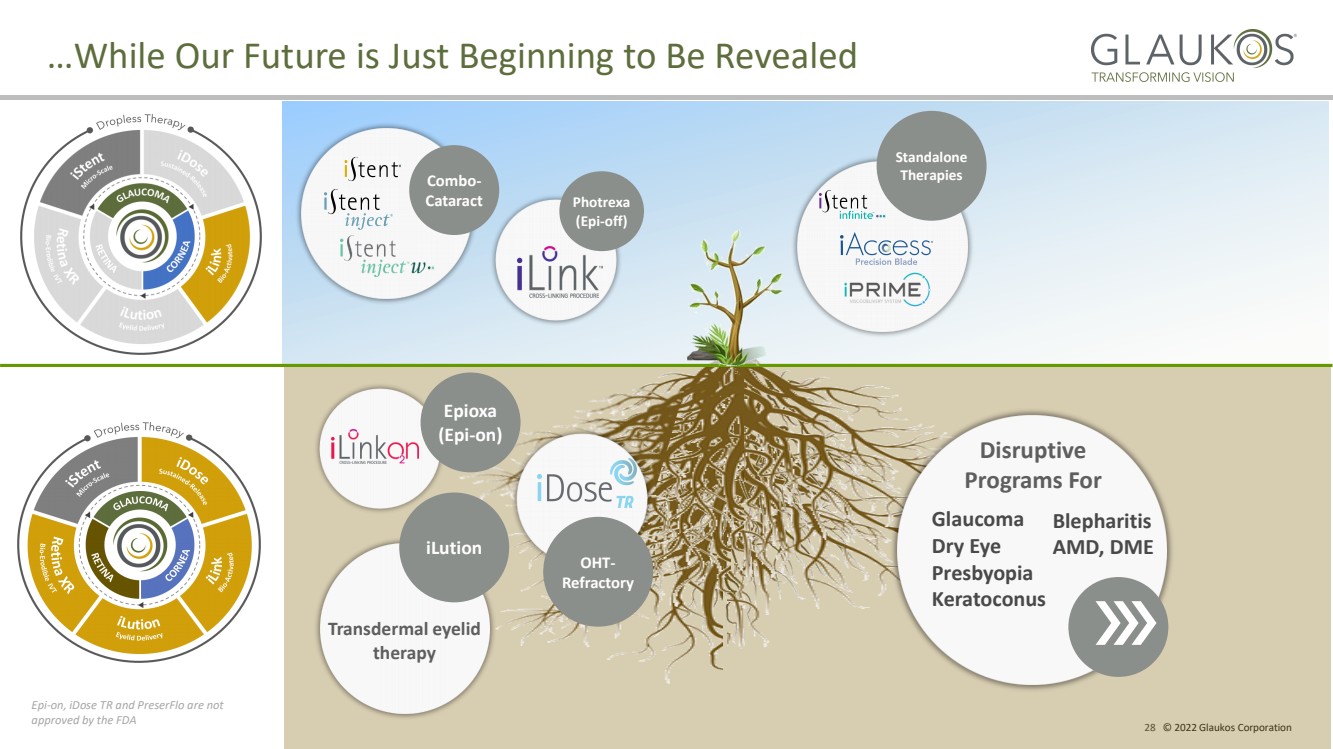
| 28 © 2022 Glaukos Corporation …While Our Future is Just Beginning to Be Revealed Photrexa (Epi - off) Combo - Cataract iLution OHT - Refractory Epioxa (Epi - on) Disruptive Programs For Glaucoma Dry Eye Presbyopia Keratoconus Blepharitis AMD, DME Photrexa (Epi - off) Combo - Cataract Epi - on, iDose TR and PreserFlo are not approved by the FDA Transdermal eyelid therapy Standalone Therapies |
| 29 © 2022 Glaukos Corporation Summary: Glaukos is Different Delivering disruptive dropless therapies designed to improve patient outcomes Five distinct technology platforms, dominated by pharmaceuticals and designed to generate waves of new market - expanding products Pursuing game - changing therapies for large and underserved patient populations, with R&D investments that have been self - funding Commercialize with best - in - class productivity and efficiency , with a platform that is scaled and ready for more growth |
|
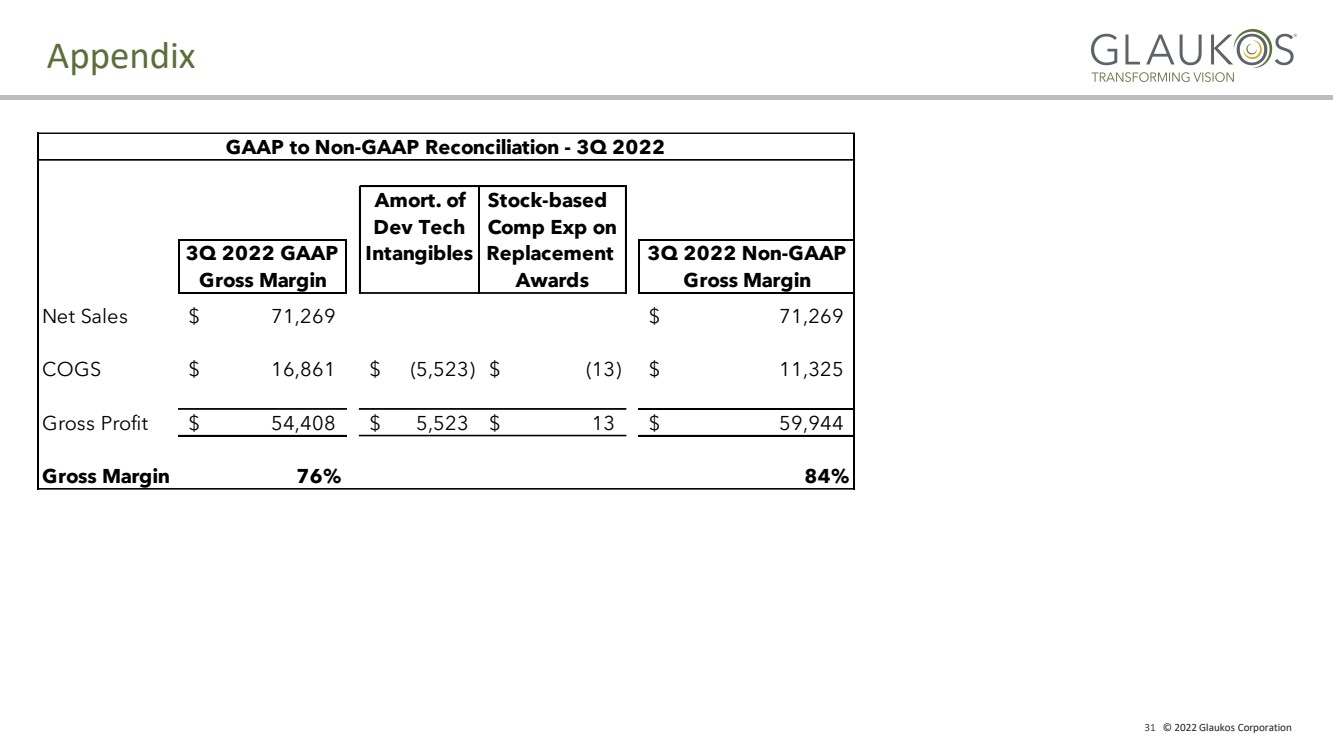
| 31 © 2022 Glaukos Corporation Appendix Amort. of Stock-based Dev Tech Comp Exp on 3Q 2022 GAAP Intangibles Replacement 3Q 2022 Non-GAAP Gross Margin Awards Gross Margin Net Sales 71,269 $ 71,269 $ COGS 16,861 $ (5,523) $ (13) $ 11,325 $ Gross Profit 54,408 $ 5,523 $ 13 $ 59,944 $ Gross Margin 76% 84% GAAP to Non-GAAP Reconciliation - 3Q 2022 |