phas-20211231誤り2021会計年度0001169245Http://Fasb.org/us-GAAP/2021-01-31#AcruedLiabilitiesCurrentHttp://Fasb.org/us-GAAP/2021-01-31#AcruedLiabilitiesCurrent00011692452021-01-012021-12-3100011692452021-06-30ISO 4217:ドル00011692452022-03-21Xbrli:共有00011692452021-12-3100011692452020-12-31ISO 4217:ドルXbrli:共有0001169245アメリカ-公認会計基準:メンバーに授与2021-01-012021-12-310001169245アメリカ-公認会計基準:メンバーに授与2020-01-012020-12-310001169245PHA:連携プロトコルメンバ2021-01-012021-12-310001169245PHA:連携プロトコルメンバ2020-01-012020-12-3100011692452020-01-012020-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバー2019-12-310001169245米国-公認会計基準:財務省株式構成員2019-12-310001169245US-GAAP:AdditionalPaidInCapitalMembers2019-12-310001169245アメリカ-公認会計基準:前払いメンバーを保留2019-12-3100011692452019-12-310001169245US-GAAP:AdditionalPaidInCapitalMembers2020-01-012020-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバー2020-01-012020-12-310001169245アメリカ-公認会計基準:前払いメンバーを保留2020-01-012020-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバー2020-12-310001169245米国-公認会計基準:財務省株式構成員2020-12-310001169245US-GAAP:AdditionalPaidInCapitalMembers2020-12-310001169245アメリカ-公認会計基準:前払いメンバーを保留2020-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310001169245US-GAAP:AdditionalPaidInCapitalMembers2021-01-012021-12-310001169245アメリカ-公認会計基準:前払いメンバーを保留2021-01-012021-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバー2021-12-310001169245米国-公認会計基準:財務省株式構成員2021-12-310001169245US-GAAP:AdditionalPaidInCapitalMembers2021-12-310001169245アメリカ-公認会計基準:前払いメンバーを保留2021-12-310001169245PHA:SFJ PharmPharmticalsXLtd.メンバー2021-01-012021-12-310001169245PHA:シティグループGlobalMarketsInc.とWilliamBlairCompanyL.L.C.メンバとの持分割当てプロトコル2021-01-012021-12-310001169245PHA:シティグループGlobalMarketsInc.とWilliamBlairCompanyL.L.C.メンバとの持分割当てプロトコル2020-01-3100011692452020-01-310001169245PHA:シティグループGlobalMarketsInc.とWilliamBlairCompanyL.L.C.メンバとの持分割当てプロトコル2021-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバーアメリカ公認会計基準:副次的事件メンバー2022-01-102022-01-100001169245アメリカ公認会計基準:副次的事件メンバー2022-01-102022-01-100001169245SRT:最小メンバ数2021-01-012021-12-310001169245SRT:最大メンバ数2021-01-012021-12-310001169245PHAS:公的株式オプションメンバー2021-01-012021-12-310001169245PHAS:公的株式オプションメンバー2020-01-012020-12-310001169245PHA:公的株を購入する保証金メンバー2021-01-012021-12-310001169245PHA:公的株を購入する保証金メンバー2020-01-012020-12-310001169245アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001169245アメリカ公認会計基準:従業員ストックメンバー2020-01-012020-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定する2021-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定するアメリカ-公認会計基準:公正価値入力レベル1メンバー2021-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定するアメリカ-公認会計基準:公正価値入力レベル2メンバー2021-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定するアメリカ-公認会計基準:公正価値投入レベル3メンバー2021-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定する2020-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定するアメリカ-公認会計基準:公正価値入力レベル1メンバー2020-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定するアメリカ-公認会計基準:公正価値入力レベル2メンバー2020-12-310001169245アメリカ-GAAP:公正価値は再帰的メンバーを測定するアメリカ-公認会計基準:公正価値投入レベル3メンバー2020-12-310001169245米国-GAAP:デバイス構成員2021-12-310001169245米国-GAAP:デバイス構成員2020-12-310001169245アメリカ-GAAP:OfficeEquipmentMembers2021-12-310001169245アメリカ-GAAP:OfficeEquipmentMembers2020-12-310001169245アメリカ-GAAP:家具と固定機器のメンバー2021-12-310001169245アメリカ-GAAP:家具と固定機器のメンバー2020-12-310001169245アメリカ-公認会計基準:リース改善メンバー2021-12-310001169245アメリカ-公認会計基準:リース改善メンバー2020-12-310001169245アメリカ-アメリカ公認会計基準:建設中のメンバー2021-12-310001169245アメリカ-アメリカ公認会計基準:建設中のメンバー2020-12-310001169245PHA:シリコンバレー銀行とWestRiverInnovationLendingFundMembersPHA:Term LoanMembers2019-03-310001169245PHA:シリコンバレー銀行とWestRiverInnovationLendingFundMembersPHA:Term LoanMembersPHA:移行1メンバ2019-03-310001169245PHA:Term LoanMembersPHA:移行2メンバPHA:シリコンバレー銀行のメンバー2019-03-310001169245PHA:移行3メンバPHA:Term LoanMembersPHA:シリコンバレー銀行のメンバー2019-03-310001169245PHA:12回目と3回目のメンバーアメリカ-公認会計基準:良質料率メンバーPHA:シリコンバレー銀行のメンバー2019-03-012019-03-31Xbrli:純0001169245PHA:12回目と3回目のメンバーPHA:シリコンバレー銀行のメンバー2019-03-012019-03-310001169245PHA:シリコンバレー銀行のメンバー2019-03-310001169245PHA:シリコンバレー銀行とWestRiverInnovationLendingFundMembersPHA:移行1メンバ2019-03-310001169245PHA:シリコンバレー銀行とWestRiverInnovationLendingFundMembersPHA:移行2メンバ2019-05-310001169245PHA:移行3メンバPHA:シリコンバレー銀行とWestRiverInnovationLendingFundMembers2019-10-310001169245PHA:シリコンバレー銀行とWestRiverInnovationLendingFundMembers2019-03-012019-03-310001169245PHA:Term LoanMembersPHA:12回目と3回目のメンバーPHA:シリコンバレー銀行のメンバー2021-12-310001169245PHA:シリコンバレー銀行のメンバー2021-12-310001169245PHA:Term LoanMembersPHA:シリコンバレー銀行のメンバー2021-01-012021-12-310001169245PHA:Term LoanMembersPHA:シリコンバレー銀行のメンバー2020-01-012020-12-310001169245PHA:シリコンバレー銀行のメンバー2021-12-310001169245PHA:AlfasigmaSpAMembers2021-06-012021-06-300001169245PHA:目標達成収入規制マイルストーンメンバーPHA:AlfasigmaSpAMembers2021-06-012021-06-300001169245PHA:決定されたビジネスマイルストーンとオンライン販売メンバーの階層版税支払いを実現PHA:AlfasigmaSpAMembers2021-06-012021-06-300001169245PHA:AlfasigmaSpAMembersアメリカ公認会計基準:ライセンスメンバー2021-01-012021-12-310001169245PHA:AlfasigmaSpAMembersアメリカ公認会計基準:ライセンスメンバー2021-12-310001169245PHA:AlfasigmaSpAMembersPHA:開発と規制サービスメンバー2021-01-012021-12-310001169245PHA:AlfasigmaSpAMembersPHA:開発と規制サービスメンバー2021-12-310001169245PHA:AlfasigmaSpAMembersPHA:SupplyOfライセンス製品メンバ2021-01-012021-12-310001169245PHA:AlfasigmaSpAMembersPHA:SupplyOfライセンス製品メンバ2021-12-310001169245PHA:AlfasigmaSpAMembers2021-01-012021-12-310001169245PHA:AlfasigmaSpAMembers2021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersSRT:最大メンバ数PHA:BentracimabMembersPHA:SFJプロトコルメンバー2020-01-012020-01-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-01-012021-12-310001169245PHA:UnitedStates Foodand DrugAdministrationメンバーUS-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-01-012021-12-310001169245PHA:UnitedStates Foodand DrugAdministrationメンバーUS-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-12-31PHA:支払い0001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:ヨーロッパ医薬品代理メンバーPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-01-012021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:ヨーロッパ医薬品代理メンバーPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:薬品·医療機器代理日本と国家医療生産管理中国メンバーPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-01-012021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:薬品·医療機器代理日本と国家医療生産管理中国メンバーPHA:BentracimabMembersPHA:SFJプロトコルメンバー2021-12-310001169245PHA:SFJプロトコルメンバー2021-01-012021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー2021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー2021-01-012021-12-31PHA:部分0001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:運輸業メンバーPHA:SFJプロトコルメンバー2021-12-310001169245PHA:輸送メンバーUS-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー2021-12-310001169245米国-公認会計基準:派生メンバー2021-01-012021-12-310001169245PHA:SFJ製薬会社のメンバー2021-01-012021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー米国-公認会計基準:派生メンバー2019-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー米国-公認会計基準:派生メンバー2021-01-012021-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー米国-公認会計基準:派生メンバー2020-01-012020-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー米国-公認会計基準:派生メンバー2020-12-310001169245US-GAAP:CollaborativeArrangementTransaction WithPartyToCollaborativeArrangementMembersPHA:SFJプロトコルメンバー米国-公認会計基準:派生メンバー2021-12-3100011692452010-01-102010-01-100001169245PHA:AtTheMarketProgramメンバーPHA:シティグループGlobalMarketsInc.とWilliamBlairCompanyL.L.C.メンバとの持分割当てプロトコルアメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310001169245PHA:AtTheMarketProgramメンバーPHA:シティグループGlobalMarketsInc.とWilliamBlairCompanyL.L.C.メンバとの持分割当てプロトコルアメリカ-アメリカ公認会計基準:普通株式メンバー2020-01-012020-12-310001169245PHA:AtTheMarketProgramメンバー2020-01-012020-12-310001169245PHA:2021年3月提供メンバー2021-03-012021-03-310001169245PHA:2021年3月提供メンバー2021-03-310001169245PHA:2021年3月提供メンバー2021-01-012021-12-310001169245PHA:2千88人の計画メンバー2018-10-310001169245PHA:2千88人の計画メンバー2021-12-310001169245PHA:2千88人の計画メンバーSRT:最小メンバ数2018-10-012018-10-310001169245PHA:2千88人の計画メンバーSRT:最大メンバ数2018-10-012018-10-310001169245PHA:2千88人の計画メンバーアメリカ公認会計基準:副次的事件メンバー2022-01-010001169245PHA:2千と2つの計画と2千と18の計画メンバー2019-12-310001169245PHA:2千と2つの計画と2千と18の計画メンバー2019-01-012019-12-310001169245PHA:2千と2つの計画と2千と18の計画メンバー2020-01-012020-12-310001169245PHA:2千と2つの計画と2千と18の計画メンバー2020-12-310001169245PHA:2千と2つの計画と2千と18の計画メンバー2021-01-012021-12-310001169245PHA:2千と2つの計画と2千と18の計画メンバー2021-12-310001169245米国-公認会計基準:従業員株式オプションメンバー2021-12-310001169245米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310001169245アメリカ公認会計基準:従業員ストックメンバー2018-10-310001169245アメリカ公認会計基準:従業員ストックメンバー2021-12-310001169245アメリカ公認会計基準:従業員ストックメンバー2018-10-012018-10-310001169245アメリカ公認会計基準:従業員ストックメンバーアメリカ公認会計基準:副次的事件メンバー2022-01-012022-01-010001169245アメリカ公認会計基準:従業員ストックメンバー2020-03-012020-03-310001169245アメリカ公認会計基準:従業員ストックメンバー2020-03-31PHA:購入期間0001169245アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001169245アメリカ公認会計基準:従業員ストックメンバー2020-01-012020-12-310001169245アメリカ公認会計基準:従業員ストックメンバー2020-12-310001169245米国-公認会計基準:従業員株式オプションメンバー2020-01-012020-12-310001169245米国-公認会計基準:従業員株式オプションメンバー2020-12-310001169245アメリカ-公認会計基準:一般と行政費用メンバー2021-01-012021-12-310001169245アメリカ-公認会計基準:一般と行政費用メンバー2020-01-012020-12-310001169245米国-公認会計基準:研究·開発費メンバー2021-01-012021-12-310001169245米国-公認会計基準:研究·開発費メンバー2020-01-012020-12-310001169245公衆衛生協会:医療免疫有限会社のメンバー2017-11-012017-11-300001169245SRT:最大メンバ数公衆衛生協会:医療免疫有限会社のメンバーPHA:臨床開発と規制マイルストーンの成果メンバー2017-11-012017-11-300001169245PHA:ビジネスマイルストーンメンバーSRT:最大メンバ数公衆衛生協会:医療免疫有限会社のメンバー2017-11-012017-11-300001169245SRT:最大メンバ数PHA:デューク大学のメンバーPHA:臨床開発と規制マイルストーンの成果メンバー2021-01-012021-12-310001169245PHA:ビジネスマイルストーンメンバーSRT:最大メンバ数PHA:デューク大学のメンバー2021-01-012021-12-310001169245PHA:デューク大学のメンバーSRT:最小メンバ数2021-01-012021-12-310001169245PHA:デューク大学のメンバー2021-01-012021-12-310001169245PHA:EMAApprovalOfApplicationForLicensedProductMemberPHA:AlfasigmaSpAMembers2021-06-012021-06-300001169245PHA:AlfasigmaSpAMembersPHA:完了条件規制承認メンバー2021-06-012021-06-300001169245PHA:無条件規制承認を実現するメンバーPHA:AlfasigmaSpAMembers2021-06-012021-06-300001169245PHA:AlfasigmaSpAMembers2020-01-012020-12-310001169245PHA:WackerMembers2021-01-012021-12-310001169245PHA:WackerMembers2020-01-012020-12-310001169245PHA:ViametPharmPharmticalsHoldingsLLCMメンバー2020-01-012020-01-310001169245PHA:ViametPharmPharmticalsHoldingsLLCMメンバーSRT:最大メンバ数PHA:PaymentUponAchieventOfCertainDevelopmentAndIntelligence ectualPropertyMilestonesメンバー2020-01-012020-01-310001169245PHA:ビジネスマイルストーンメンバーPHA:ViametPharmPharmticalsHoldingsLLCMメンバーSRT:最大メンバ数2020-01-012020-01-310001169245PHA:ViametPharmPharmticalsHoldingsLLCMメンバー2021-01-012021-12-310001169245PHA:ViametPharmPharmticalsHoldingsLLCMメンバー2020-01-012020-12-3100011692452021-03-310001169245PHA:従属収入メンバー2021-01-012021-12-310001169245PHA:従属収入メンバー2020-01-012020-12-310001169245PHA:SmallBusiness InnovationResearchからメンバーへ2018-02-012018-02-280001169245PHA:SmallBusiness InnovationResearchからメンバーへ2020-03-312020-03-310001169245PHA:SmallBusiness InnovationResearchからメンバーへ2021-01-012021-12-310001169245PHA:SmallBusiness InnovationResearchからメンバーへ2020-01-012020-12-310001169245米国-GAAP:国内/地域メンバー米国-GAAP:2018年納税年次メンバー2021-12-310001169245アメリカ-公認会計基準:州と地方法律法規のメンバー米国-GAAP:2018年納税年次メンバー2021-12-310001169245PHA:2018年前SRT:最大メンバ数米国-GAAP:国内/地域メンバー2021-01-012021-12-310001169245米国-GAAP:国内/地域メンバー2021-01-012021-12-310001169245SRT:最大メンバ数米国-GAAP:国内/地域メンバー米国-GAAP:2018年納税年次メンバー2021-01-012021-12-310001169245アメリカ-公認会計基準:州と地方法律法規のメンバー米国-GAAP:2018年納税年次メンバー2021-01-012021-12-310001169245アメリカ-公認会計基準:州と地方法律法規のメンバー2021-01-012021-12-310001169245米国-GAAP:国内/地域メンバーアメリカ-公認会計基準:研究メンバー米国-GAAP:2018年納税年次メンバー2021-12-310001169245アメリカ-公認会計基準:州と地方法律法規のメンバーアメリカ-公認会計基準:研究メンバー米国-GAAP:2018年納税年次メンバー2021-12-310001169245米国-GAAP:国内/地域メンバーアメリカ-公認会計基準:研究メンバー米国-GAAP:2018年納税年次メンバー2021-01-012021-12-310001169245アメリカ-公認会計基準:州と地方法律法規のメンバーアメリカ-公認会計基準:研究メンバー米国-GAAP:2018年納税年次メンバー2021-01-012021-12-310001169245PHA:孤児家族米国-GAAP:国内/地域メンバー米国-GAAP:2018年納税年次メンバー2021-12-310001169245PHA:孤児家族米国-GAAP:国内/地域メンバー米国-GAAP:2018年納税年次メンバー2021-01-012021-12-310001169245アメリカ-アメリカ公認会計基準:普通株式メンバーPHA:入社計画メンバーアメリカ公認会計基準:副次的事件メンバー2022-01-14 アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
___________________________________
表10-K
___________________________________
| | | | | |
| ☒ | 1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで十二月三十一日, 2021
あるいは…。
| | | | | |
| ☐ | 1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
移行期になります 至れり尽くせり
手数料書類番号001-38697
___________________________________
PhaseBio製薬会社は
(登録者の正確な氏名はその定款に記載)
| | | | | | | | |
デラウェア州 | | 03-0375697 |
(明またはその他の司法管轄権 会社や組織) | | (税務署の雇用主 識別番号) |
大谷路1号, 30軒の部屋
マルヴィン, ペンシルバニア州19355
(住所は主な実行事務室の郵便番号を含む)
(610) 981-6500
(登録者の電話番号、市外局番を含む)
同法第12条(B)に基づいて登録された証券:
| | | | | | | | |
(クラス名) | 取引記号 | (登録所の取引所名) |
普通株は一株当たり0.001ドルの価値があります | PHA | ナスダック株式市場 |
同法第12条(G)に基づいて登録された証券:ありません
___________________________________
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してください。そうだな違います。 ☒
登録者がこの法第13節または第15節(D)節に基づいて報告を提出する必要がないかどうかを再選択マークで示す。そうだな違います。 ☒
登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13または15(D)節に提出されたすべての報告を提出したかどうか、および(2)このような提出要求を過去90日以内に遵守してきたかどうかを、再選択マークで示すはい、そうです ☒ No ☐
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示すはい、そうです ☒ No ☐
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法12 b-2規則における“大型加速申告会社”、“加速申告会社”、“小報告会社”、“新興成長型会社”の定義を参照してください
| | | | | | | | | | | | | | |
大型加速ファイルサーバ | ☐ | | ファイルマネージャを加速する | ☐ |
| 非加速ファイルマネージャ | ☒ | | 規模の小さい報告会社 | ☒ |
| | | 新興成長型会社 | ☒ |
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する☒
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オクスリ法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる☐
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。はい、そうです☐ No ☒
2021年6月30日現在,登録者の非関連会社が保有する投票権と無投票権普通株の総時価は約#ドルである168.9ナスダック世界市場が当日報告した終値によると、同社の株価は100万ユーロ。登録者の関連会社とみなされる可能性があるので、上級職員、取締役、および発行済み普通株の10%以上を所有していることが知られている各人が保有する普通株は含まれていない。他の目的に対して,このような関連地位の決定は必ずしも決定的な決定であるとは限らない.
| | | | | | | | |
普通株種別 | | 2022年3月21日までの流通株 |
普通株、額面0.001ドル | | 48,690,590 |
引用で編入された書類
登録者は、1934年証券取引法第14 A条に基づいて、その2022年株主総会に提出された最終委託書の一部の内容を参照により、本表格10−Kの第III部分に組み込む。
カタログ表
| | | | | | | | |
| | ページ |
第1部 | | |
第1項。 | 業務.業務 | 3 |
第1 A項。 | リスク要因 | 29 |
項目1 B。 | 未解決従業員意見 | 72 |
第二項です。 | 属性 | 72 |
第三項です。 | 法律訴訟 | 72 |
第四項です。 | 炭鉱安全情報開示 | 72 |
| | |
第II部 | | |
五番目です。 | 登録者普通株市場、関連株主事項及び発行者による株式証券の購入 | 73 |
第六項です。 | 保留されている | 73 |
第七項。 | 経営陣の財務状況と経営成果の検討と分析 | 73 |
第七A項。 | 市場リスクの定量的·定性的開示について | 87 |
第八項です。 | 財務諸表と補足データ | 87 |
第九項です。 | 会計と財務情報開示の変更と相違 | 87 |
第9条。 | 制御とプログラム | 87 |
プロジェクト9 B。 | その他の情報 | 88 |
| プロジェクト9 Cです。 | 検査妨害に関する外国司法管区の開示 | 89 |
| | |
第三部 | | |
第10項。 | 役員·幹部と会社の管理 | 90 |
第十一項。 | 役員報酬 | 90 |
第十二項。 | 特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 | 90 |
十三項。 | 特定の関係や関連取引、取締役の独立性 | 90 |
14項です。 | チーフ会計士費用とサービス | 90 |
| | |
第4部 | | |
第十五項。 | 展示と財務諸表明細書 | 91 |
プロジェクト16 | 表格10-Kの概要 | 104 |
前向き陳述に関する特別警告通知
本Form 10-K年度報告又は本年度報告は、重大なリスク及び不確定要因に関連する1933年“証券法”(改正)第27 A条又は“証券法”(改正)及び“1934年証券取引法”(改正)第21 E条に該当する展望的陳述を含む。展望的陳述は主に第1項第1項に記載されている。“ビジネス”、第1部、第1号。“リスク要因”と第2部、第7項。“経営陣の財務状況や経営結果の検討·分析”であるが、本年度報告の他の部分にも含まれている。場合によっては、前向き陳述は、“可能”、“すべき”、“予想”、“計画”、“計画”、“目標”、“予想”、“信じ”、“推定”、“可能”、“予測”、“プロジェクト”、“目標”、“潜在”、“継続”、“進行中”などの言葉によって識別することができる。またはこれらの用語の否定、または将来に関する陳述を識別することが意図された他の比較可能な用語。これらの陳述は既知および未知のリスク、不確定性および他の要素に関連し、私たちの実際の結果、活動レベル、業績または成果はこれらの前向き陳述と明示的または暗示的な情報とは大きく異なる可能性がある。本年度報告書に含まれているすべての展望的陳述には合理的な基礎があると信じていますが、これらの陳述は私たちが現在知っている事実と要素、そして私たちの未来に対する期待に基づいていて、私たちはこれらの事実と要素を決定することができません。前向きな陳述は、以下の態様に関する陳述を含む
•Bentracimab、PB 6440、および任意の他の潜在的候補製品の臨床試験の時間、進捗および結果は、臨床前研究または臨床試験および関連準備作業の開始および完了の時間、試験結果の期限、および我々の研究および開発計画に関する声明を含む
•Bentracimab、PB 6440、および任意の他の候補製品の規制承認を得るための任意の申請を提出する時間、および任意の適応のbentracimab、PB 6440、または任意の他の候補製品の規制承認を取得して維持する能力;
•もし私たちの製品が商業用途のために承認されたら、私たちは患者集団の大きさ、市場受容度、候補製品の機会、および臨床的実用性への期待
•私たちの製造方法とプロセスの拡張性と商業可能性、および第三者と合意を維持する能力を含む、私たちの製造能力と戦略
•フェニトラシズマブおよびPB 6440の任意の承認適応の範囲への期待
•私たちの候補製品を商業化する能力に成功しました
•私たちは独自のエラスチン·ポリペプチド技術を利用して未来の候補製品を識別し開発することができます
•新冠肺炎が私たちの業務、運営と臨床開発スケジュールと計画に与える潜在的な影響
•私たちが継続的に経営する企業として存在し続ける能力は
•私たちは費用、持続的な損失、未来の収入、資本需要、そして追加融資の推定を得る必要があるか、または得ることができます
•協力や戦略的関係を構築したり維持したりする能力は
•私たちは重要な人を識別し、採用し、維持する能力
•私たちは私たちの候補製品と私たちの研究開発計画のために私たちの知的財産権の地位を保護し、実行する能力、そしてこのような保護の範囲
•私たちの財務業績は
•私たちの競争地位と私たちの競争相手や私たちの業界に関する発展と予測
•法律法規の影響
•私たちは2012年にJumpStart Our Business Startups Actの新興成長型会社になることを期待しています。
我々の実際の結果と前向き陳述に明示または示唆された結果とが大きく異なる可能性のある重要な要因の検討については,本年度報告における“リスク要因”を参照されたい。このような要因のため、本年度報告書の展望的な陳述が正確であることが証明されることを保証することはできません
しかも、もし私たちの展望的な陳述が不正確であることが証明されたら、この不正確さは実質的である可能性がある。このような展望的陳述の重大な不確実性を考慮して、あなたはこれらの陳述を私たちまたは任意の特定の時間枠内で、または私たちの目標と計画の陳述または保証を完全に達成しないために、私たちまたは他の誰もと見なしてはならない。本年度報告書の前向き陳述は、本年度報告日までの私たちの観点を代表します。私たちはその後に発生した事件と事態の発展が私たちの観点を変化させるかもしれないと予想している。しかしながら、私たちは、未来のある時点でこれらの前向きな陳述を更新することを選択する可能性があるが、法的要件がなければ、新しい情報、未来のイベント、または他の理由でも、いかなる前向きな陳述も公開更新する義務はない。したがって、あなたはこのような前向きな陳述に依存して、私たちの今年度の報告日以降の任意の日付の観点を代表してはいけません。
あなたはこの報告書と私たちが報告書で言及した文書を完全に読んで、私たちの未来の実際の結果が私たちが予想していたものと大きく違うかもしれないということを知るべきだ。私たちはこのような警告声明を通じて私たちのすべての展望的声明を限定する。
本年度報告に出現するすべてのブランド名又は商標は、そのそれぞれの所有者の財産である。便宜上,本年度報告で言及されている商標及び商号には記号和は使用されていない™しかし、このような言及は、それぞれの所有者が、適用法によってその権利を最大限に主張するいかなる兆候もないと解釈されるべきではない。文脈が別に要求されない限り、本報告書で言及されている“PhaseBio”、“会社”、“私たち”、“私たち”はPhaseBio製薬会社を意味する。
業界と市場データ
本年度報告における業界と市場データは,我々自身の研究および第三者による業界や一般出版物,調査,研究から来ている.工業および一般出版物、研究および調査は、一般に、その中に記載されている情報が信頼できると考えられるソースから得られることを指摘している。これらの第三者は将来、彼らが私たちが業務を経営している市場を調査し、研究する方法を変えるかもしれない。したがって、本年度報告に含まれる業界および市場データに関連する固有のリスクおよび不確実性は、第1部1 A項で議論されたデータを含むことをよく考慮しなければならない。“リスク要因”
第1部
プロジェクト1.ビジネス
概要
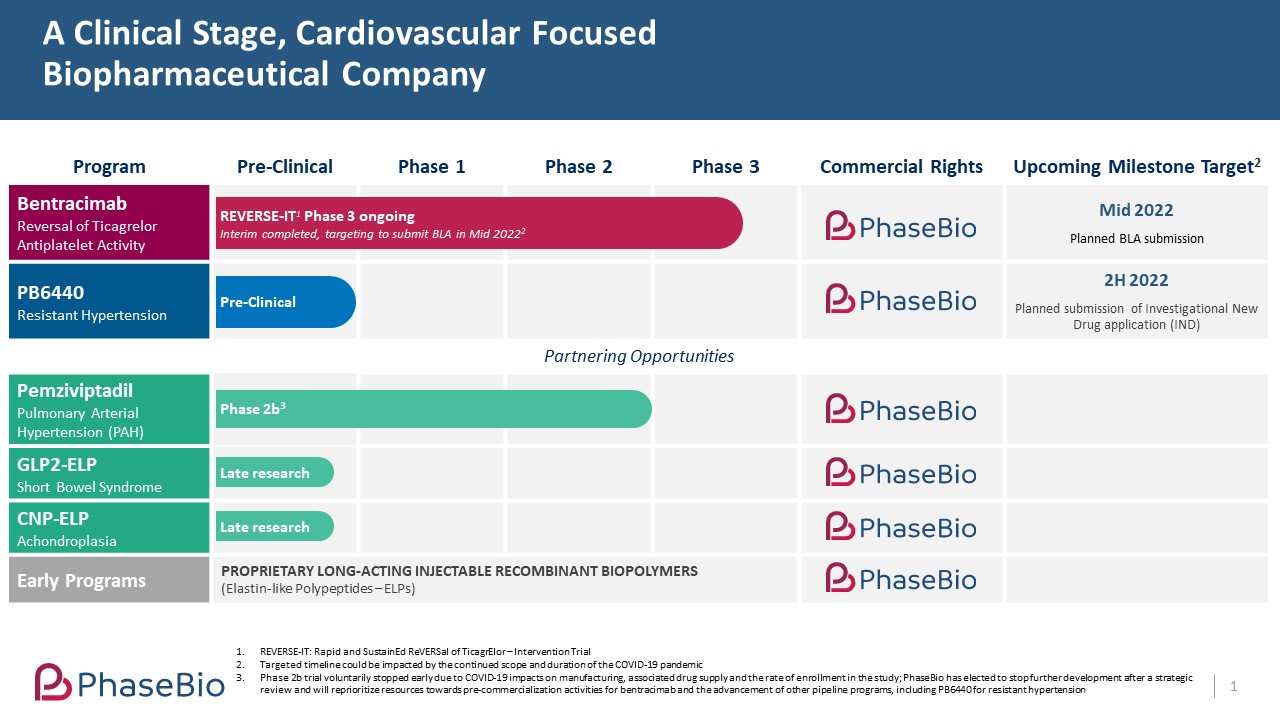
私たちは臨床段階の生物製薬会社で、心血管疾患の新しい治療法の開発と商業化に集中している。著者らの主要な候補製品bentracimab(PB 2452とも呼ばれる)は抗血小板薬チカグレルの新しい反転剤である。米国食品医薬品局(FDA)からのフィードバックによると,承認手続きを加速することで,米国でのbentracimabの承認を求める予定である。われわれが達成した試験では,Bentracimabは全体的に耐性が良好であり,薬物に関する重篤な副作用やSAEはなかった。われわれが完成したbentracimabの2 a期と2 b期の臨床試験では,テカグレルの抗血小板活性は注入開始後5分で直ちに完全に逆転し,20時間以上逆転が認められた。我々は現在,Bentracimabの重要な第3段階逆IT試験を行っている。150人の入選患者(うち142人が緊急手術または侵襲的手術を必要とし、8人が制御不能な大出血または生命に危険な出血を有する)の予め指定された中期分析では、bentracimabは、テカグレルの抗血小板作用を直ちにかつ持続的に逆転させることによって、試験の主要な終点を達成した。我々の目標は,この時期が新冠肺炎の大流行持続範囲と持続時間の影響を受ける可能性があるにもかかわらず,2022年中に米国食品·薬物管理局にベントリマモノクロナル抗体の生物製品許可証申請を提出することである。SFJ製薬グループ傘下のSFJ製薬X株式会社との共同開発プロトコルやSFJプロトコルに基づいてbentracimabを開発している。SFJプロトコルによると、SFJはbentracimabの臨床開発を支援するために最大1.2億ドルを支払うことに同意している。前臨床候補のPB 6440も開発しています, 難治性高血圧の治療に用いられる。私たちがAlfasigma S.p.A.またはAlfasigmaのbentracimabに権利を与えることに加えて、私たちは私たちのすべての候補製品の世界的な商業権を維持する。
著者らはウェブサイト活性化と患者登録を通じて著者らのbentracimab臨床計画を推進することに伴い、著者らはずっと著者らの臨床研究組織、臨床サイトとサプライヤーと密接な関係を維持し、新冠肺炎及びその変異体が著者らの臨床試験と現在のスケジュールに与える影響を評価することを試み、そして著者らは適切な緩和措置を実施してこのような影響の軽減を助けることができるかどうかを考慮する。しかし、現在、新冠肺炎が著者らの試験サイトの起動、患者の募集と評価、研究薬物の提供と試験結果を報告する能力に与える影響の範囲を完全に予測することはできない
Bentracimab
Bentracimabは新型組換えヒトモノクロナル抗原結合断片、あるいはFab断片であり、テカグレルの抗血小板活性を逆転させることを目的としている。チカグレルは広く処方されている抗血小板療法であり、急性冠症候群(ACS)患者或いは以前に心臓発作を経験した患者の死亡率、心臓発作と脳卒中の発生率を低下させるために用いられる。アメリカ心臓病学会、アメリカ心臓病協会とヨーロッパ心臓病学会ガイドラインはチカグレルが急性冠症候群を治療する第一選択の抗血小板薬であることを認めた。2021年、現在アスリコンまたはアスリーカンがBrilintaとBriliqueブランドで販売しているチカグレルの世界での売上高は15億ドル。チカグレルは血小板と結合して血栓を形成することを防止し、これはこれらの患者の重要な器官の血液流動を制限し、心臓病発作或いは脳卒中を引き起こす可能性がある。チカグレルの抗血小板活性により,チカグレルを服用した患者の自発性出血のリスクが増加した。また,緊急手術を必要とするチカグレル服用患者は,テカグレルの効果が消失するまで5日間待つことができず,術中および術後大出血のリスクが増加した。テカグレルまたは任意の他の抗血小板薬のための他の既知の反転剤が承認または臨床的に開発されていない。EUでは、インビトロ全血浄化吸着装置があり、体外循環と組み合わせて使用される場合、いくつかの心臓手術中にチカグレルを非特異的に除去するのに役立つ可能性がある。この装置のメーカーCytoSorbents社はまた、DrugSorb-ATR抗血栓除去システムの心胸郭手術における使用を評価するための臨床試験を米国で開始した。承認された後, Bentracimabは、特定の逆チカグレルに使用することができる唯一の治療薬であるであろう。特定の反転剤としてのbentracimabの利用可能性は、出血リスクに対する人々の懸念を軽減することによって、チカグレルの使用を拡大し、チカグレルを反転剤を有する唯一の経口抗血小板薬としてユニークに位置づけることができると信じている。我々の1期、2 a期および2 b期の臨床試験、および私たちの3期逆IT試験の中期分析では、bentracimabはチカグレルの抗血小板活性の即時および完全逆転を実現し、逆転の潜在的持続時間は投与レジメンに応じてカスタマイズすることができ、これはカグレルの安全性を増加させることによって、これらの患者に救命の治療的利益をもたらす可能性があると信じている。
2020年3月には,グローバル,マルチセンター,非ランダム,オープンタグの試験である重要なRead−IT試験を開始し,制御できない大出血や生命に危険な出血や緊急手術や侵襲的手術を必要とする患者を計200名募集する予定である。VerifyNow PRUTestバイオマーカーの測定によると,この試験の主な終点はフェニルトラマモノ抗逆チカグレルの抗血小板作用を静脈内投与し,登録された患者で臨床止血を実現することである。150人の入選患者(うち142人が緊急手術または侵襲的手術を必要とし、8人が制御不能な大出血または生命に危険な出血を患っている)の中期分析で、私たちは発表した
2021年11月,bentracimabはテカグレルの抗血小板作用を直ちにかつ持続的に逆転させることにより,試験の主要な終点を達成した。Bentracimabは全体的に耐性が良好であり,3名の患者が薬物関連の非重篤な不良事象を5件報告している。緊急手術や侵襲的手術を必要とする患者待ち行列は完全に組み込まれており,試験地点は制御できない重大あるいは生命に危険な出血事件を有する患者の募集に重点を向けている。われわれは,米国,カナダ,EUの登録臨床試験地点の数を増やす努力を含め,これらの患者の登録を加速させる試みを続けており,より広範な場所の足跡がこれらの患者登録の可能性を増加させると信じているからである。また、著者らのベンゼントラマモノクロナルに対する研究新薬申請は最近2021年8月に中国国家医療製品管理局薬物評価センター(CDE)の許可を得た。私たちは2022年上半期に中国の患者を募集する予定です。
FDAは2019年4月にbentracimabの突破的治療指定を承認し、欧州薬品管理局(EMA)は2020年2月にbentracimab優先薬物或いはPrimeの指定を許可した。FDA以前に提供されたフィードバックは、私たちの逆IT試験で治療された最初の約100人の患者の中期分析に基づいて、潜在的な加速承認を得るためにBLAを提出することができる。中期分析では、FDAはまた、研究に組み入れられた約50名の患者が制御されていない大出血或いは生命に危険な出血を患っており、約50名の患者は緊急手術或いは侵襲的手術が必要であることを提案しているが、FDAは、この2群の患者の中に十分な数の患者がいるかどうかは審査問題であると述べている。
われわれの逆IT試験における患者の中期分析に基づき,潜在的な加速承認を得るためにBLAを提出する予定であり,これらすべての患者は上記と同様のVerifyNow PRUTestバイオマーカーと止血終点に基づいて測定した。中期分析では、著者らは引き続き私たちの以前の約100名を超える患者のチカグレル患者を募集し、強力な手術登録を利用し、そして新冠肺炎疫病による持続的な不確実性及び未来の患者の利用可能性に対する潜在的な影響を軽減することを選択した。我々の目標は,このスケジュールが新冠肺炎の大流行持続範囲と持続時間の影響を受ける可能性があるにもかかわらず,2022年に我々のBLAを提出することである。BLAを提出した後、FDAは、制御されていない重大または生命に危険な出血を有する患者を含む、我々が求める予定のすべてまたは一部の適応のために十分な数の患者を募集していないことを確認することができる。また,FDAは広範な承認後の検討を求めたり,承認や上場後に行われている逆IT試験の修正を求めたりする可能性がある。
我々は逆IT試験を完了し,FDAの要求に応じて承認後登録を確立する予定である
要求します。逆IT試験を完全に登録するために必要な合計200名の患者に対して、私たちのプログラムは
3分の2以下の患者はコントロールできない大出血や生命に危険な出血から来ているかもしれません
緊急手術や侵襲的手術が必要な人や患者。アメリカ医薬品委員会
EMAのヒト使用,あるいはCHMPも,我々が提案したbentracimabの臨床開発計画にほぼ同意している。
2021年6月、私たちはAlfasigmaまたはAlfasigma再許可と再許可協定を締結し、この協定に基づいて、EUと欧州経済地域、ならびにイギリス、ロシア、ウクライナ、および独立国連合内のいくつかの他の国、ヨーロッパおよび中央アジア、または再許可領土流通およびbentracimabの販売にAlfasigmaの独占的権利を付与した。Alfasigmaライセンスによれば、私たちはbentracimabの開発を担当し、SFJプロトコルに従って、任意のマーケティング許可がAlfasigmaに割り当てられることを含むEMAおよび医薬品およびサプリメント規制機関(MHRA)の規制承認を得ることを確実にする。Alfasigmaは、マーケティングおよびbentracimabの販売に必要な任意の規制承認(定価承認および発売後の約束を含む)を取得し、維持する義務があり、ヨーロッパとイギリス以外の国の規制承認を確保する責任がある。
PB6440
PB 6440は高選択性アルドステロン合成酵素阻害剤であり,難治性高血圧の治療に開発されている。これまでの臨床前研究では,げっ歯類や霊長類モデルではPB 6440は用量依存性のアルドステロンの減少を示したが,11−デオキシコルチゾンやデオキシコルチゾールは有意に増加しなかった。これらの臨床前研究で観察された経口バイオアベイラビリティおよび薬物動態学的特徴は、ヒトの1日1回の経口投与量に適しているようである。これまでこの2つの物質に毒性がある証拠は観察されていない体外培養霊長類を含む毒性研究または動物モデル。われわれは2021年にPB 6440に対する非臨床IND起用研究を開始し,2022年下半期にINDを提出する予定である。われわれの目標は2022年末に初の人体試験を開始することであり、われわれのスケジュールは新冠肺炎の大流行の範囲と持続時間の影響を受ける可能性がある。
戦略.戦略
我々の戦略は心血管疾患の新しい治療法を識別,開発,商業化することである。私たちの戦略の主な内容は
•臨床開発と規制承認によるbentracimabの推進それは.抗血小板薬であるテカグレルの新しい反転剤としてbentracimabを開発·商業化する予定である。はい
2020年3月,SFJと協力してテカグレル患者の鍵となる逆IT試験を開始し,これらの患者にはコントロールできない大出血や生命に危険な出血,あるいは緊急手術や侵襲的手術が必要であり,最近では逆IT試験に参加した第1陣150名の計画中期分析が完了した。引き続き米国,EU,カナダで患者を募集して逆IT試験に参加する予定であり,2022年上半期から患者を中国に参加させる予定である。画期的な治療の指定を受け,逆IT患者の初期サブセットに基づくバイオマーカーデータである逆IT試験が完了する前にbentracimabの承認を加速することを求めるBLAを2022年に提出する予定である。EMAは2020年2月にbentracimab Primeの称号を授与し、中国国家薬監局は2021年12月に突破的治療称号を授与した。
•PB 6440治療難治性高血圧の臨床前開発を継続した我々は2021年にPB 6440のIND開設研究を開始し,2022年下半期にPB 6440のINDをFDAに提出する予定である。われわれの目標は2022年末に初の人体試験を開始することであり、われわれのスケジュールは新冠肺炎の大流行の範囲と持続時間の影響を受ける可能性がある
•我々のELP技術プラットフォームを利用して我々の開発ルートを拡張するそれは.我々のELP技術は溶解度、安定性とバイオアベイラビリティを向上させ、より長い薬物暴露時間を提供し、製造と管理が容易な候補製品を創造したと信じている。そこで,我々のプラットフォームを用いて他の適応の候補を決定する予定である.我々のELP技術を応用して、良好な治療活性を有するが半減期が悪いタンパク質とポリペプチドの薬物動態を改善し、それらの薬物動態を改善し、それらが医薬製品として使用できるようにし、より便利な投与レジメンを可能にするつもりである。
•私たちの候補製品を商業化しますそれは.私たちはアスリコンとbentracimabの独占ライセンス契約を締結し、デューク大学(Duke University)と私たちのELP技術の独占ライセンス契約を締結し、この合意に基づいて、私たちは私たちの候補製品の世界商業権を維持した。さらに、私たちはPB 6440に関連するすべての資産と知的財産権を持っている。承認されれば,国際市場での協力により,米国でbentracimabとPB 6440を独立して商業化する予定である。私たちが私たちの候補製品のために規制部門の承認を得るにつれて、私たちは重要なマーケティングと販売インフラを構築するつもりです。
パイプ.パイプ
私たちの臨床前と臨床段階のパイプラインは以下の通りです
チカグレルの抗血小板治療反転剤Bentracimab
私たちの主要な候補製品bentracimabは新しいテカグレル反転剤であり、私たちはこの薬物を開発してチカグレルの抗血小板作用を逆転させている。
われわれは現在Reverse−ITを行っており,これが重要な3期bentracimab臨床試験であり,コントロールできない大出血や生命に危険な出血や緊急手術や侵襲的手術を必要とする患者200名を募集する予定である。150名の登録患者に対する中期分析では,bentracimabはテカグレルの抗血小板作用を直ちにかつ持続的に逆転させることにより,試験の主要な終点を実現した。Bentracimabは全体的に耐性が良好であった。高齢者と健常,若年被験者の2 a期臨床試験で類似した結果が認められ,健常高齢者の2 b期臨床試験で類似した結果が認められた。
急性冠症候群の背景について
急性冠症候群は不安定狭心症と心筋梗塞、或いは心臓発作を含む一連の心臓血流量の突然の減少と関連する情況を述べた。急性冠症候群は冠状動脈中の不適切な凝塊形成によるものである。これらの血栓は主に血小板からなり,血小板は血液中に発見された小レンズ状細胞であり,通常損傷部位に集積して止血を助ける。疾病コントロール·予防センターのデータによると、毎年約80.5万人のアメリカ人が心臓病を発作し、心臓発作は先進国の主要な死亡原因である。
急性冠症候群の主な治療方法は抗血小板薬物を用いて現有の血栓の悪化を防止或いは追加血栓の形成を減少することである。これらの血栓は、血管開放または身体の他の部位を維持するために、閉塞された冠状動脈内に配置された心臓またはステント内で発生する可能性がある。抗血小板薬がなければ,患者の再心臓発作,脳卒中,死亡のリスクは有意に増加する。急性冠症候群患者に対する標準看護は,二重抗血小板療法,あるいはDAPTであり,アスピリンと血小板に認められるP 2 Yと呼ばれる特定の受容体の阻害剤との組み合わせである12受容体ですこの併用療法は患者が心臓発作あるいは他の急性冠症候群症状を経験した後に開始され、血小板凝集と凝塊形成を著しく減少させ、繰り返し心臓発作、脳卒中と死亡の頻度を減少させることが証明されている。
DAPTに使用されている抗血小板薬はACS患者の全体予後の改善に有効であることが証明されているが,凝固抑制は患者出血のリスクを増加させている。抗血小板治療を受けた患者の出血事件
自発的であってもよいし、受傷や手術の結果であってもよく、軽微または重大に分類される。アスリカンによる1.8万名の患者が参加した臨床試験では,チカグレルは急性冠症候群患者の反復心臓発作,脳卒中,死亡の減少においてPlavixブランドで販売されている抗血小板薬クロピドグレルより優れていることが証明された。しかし、2つの治療群の中で、試験中の約11%~12%の患者は重大な出血事件が発生し、約6%の患者の中で、これらの重大な出血事件は致命的或いは生命に危害を及ぼす。試験群では出血の原因がそれぞれ異なっていた。チカグレルを服用した患者のうち,約3%の患者の主要出血事象は自発的であり,いずれの医療プログラムにも関係なく,チカグレルを服用した患者では,約9%の患者が冠動脈バイパス手術やCABGなどのプログラムに関連する重大な出血を発生していた。試験方案は冠状動脈バイパス術を必要とする患者が手術1日から3日前にチカグレルの服用を中止することを提案したが、半分近くのチカグレル患者は手術を切実に必要とし、テカグレルの作用を除去して正常な血液凝固を回復するために3日に及ぶ時間を待つことができない。全体的に言えば、試験中に冠状動脈バイパス手術を受けた患者の中で、80%もの患者は手術に関連する重大或いは生命に危害を及ぼす出血事件を経験したが、緊急手術が必要で、しかも3日間待つことができず、チカグレルの影響を消退させた患者に対して、約50%は致命的或いは生命に危害を及ぼす出血事件を経験した。その中のいくつかのリスクは患者の潜在的な条件と関係があるかもしれないが、抗血小板薬物は全体的な出血リスクを著しく増加させた, 現在、アメリカとヨーロッパのチカグレルに関する処方情報は手術前にテカグレルの治療を5日間一時停止することを提案している。
出血リスクが増加するにもかかわらず、抗血小板薬、及び静脈血栓を防止するための抗凝固薬は、生命を救う作用があるため、アメリカではいくつかの最も広く使用されている処方薬である。テカグレルまたは任意の他の抗血小板薬のための他の既知の反転剤が承認または臨床的に開発されていない。EUでは、インビトロ全血浄化吸着装置があり、体外循環と組み合わせて使用される場合、いくつかの心臓手術中にチカグレルを非特異的に除去するのに役立つ可能性がある。この装置のメーカー細胞吸着会社はまた、心臓手術におけるDrugSorb-ATR抗血栓除去システムの使用を評価するための臨床試験を米国で開始した。承認されると、bentracimabは、特定の逆チカグレルに使用可能な唯一の治療薬となるであろう。特定の逆転剤がない場合には,医師の治療選択が限られており,血小板注入が行われる場合もあり,この場合は未確認である。テカグレルの抗血小板活性を迅速に逆転させ、正常な凝固を回復する能力は、大出血の場合であっても、手術または他の出血に関連する薬物介入が必要な場合であっても、その安全性を増加させる。
抗血小板薬の研究背景
3種類の経口抗血小板薬P 2 Y12DAPTで規定されている受容体拮抗薬はクロピドグレルでPlavixブランドで販売されており,プラグレルはEffientブランドで販売されており,チカグレルはBrilintaとBriliqueブランドで販売されている。クロピドグレルとプラグレルが永久的に結合し、血小板上の標的受容体を抑制するのとは異なり、チカグレルはP 2 Yに結合する12受容体は瞬間的な方法で受容体を急速に循環させて閉鎖する。チカグレルのこのような一時的な結合は,チカグレルに対する特定の反転剤の開発に独特の機会を提供し,他の薬物と受容体との永久結合が反転剤の開発を阻害していると考えられる。
Tiagrelorは同類の製品の中で最高だと思います12抗血小板薬は、P 2 Y中の他の製品と比較して、より良い利点−リスクプロファイルを示しているからである12皆さん。2020年、世界でのチカグレイの売上高は16億ドルだった。クロピドグレルとプラグレルの模造薬にもかかわらず、テカグレルはこのレベルの市場シェアに達した。チカグレルの増加はある程度アメリカ心臓病学会、アメリカ心臓協会とヨーロッパ心臓病学会が制定した治療ガイドラインによって推進されたと考えられ、これらのガイドラインはチカグレルが急性冠症候群を治療する第一選択の抗血小板薬であることを認めた。反転剤の出現はチカグレルを唯一可逆的な経口P 2 Yとすることができ、テカグレルの使用をさらに推進することができると信じている12抗血小板治療のため,他の薬物よりも安全である可能性がある。また,クロピドグレルの後発薬発売後の処方の増加に基づいて,チカグレルの処方は2024年の特許満了後に大幅に増加する可能性があり,後発薬競争は他のP 2 Yと類似したレベルまで価格を低下させると考えられる12抗血小板治療。
私たちの解決策:Bentracimab
Bentracimabは1種のヒトFab断片であり、それはチカグレルに結合し、高い親和性と特異性を有し、チカグレルの抗血小板活性を逆転する。Bentracimabの利用可能性は、チカグレルを他のP 2 Yとさらに区別する可能性があると信じている12受容体拮抗薬は臨床で必要な抗血小板作用と出血の予防或いは制御とのバランスをよりよく処理することができる。私たちはアスリカンの完全子会社MedImmune LimitedまたはMedImmuneが提供するbentracimabを独占的に許可した。
Bentracimab背景
チカグレルはP 2 Yと結合することで機能する12血小板上の受容体は、アデノシン二リン酸、またはADPを防止し、血小板凝集を引き起こす。チカグレルはP 2 Yと瞬時に結合しました12この薬は、チカグレルの受容体を阻害し、迅速に循環させ、遊離テカグレルに結合させ、それによってチカグレルの受容体の不活性化を防止し、チカグレルを循環から離脱させることができる。チカグレルを無効にすると、ADPはP 2 Yを再活性化することができます12受容体と血小板凝集を誘導する。この活動を以下に示す.
チカグレルの作用機序とベンゾトリメタマブの逆転作用
Bentracimabとチカグレルとの結合親和性は、P 2 Yに対するチカグレルの親和性の約100倍である12受容体ですこの高親和性はbentracimabを遊離テカグレルと結合させ、チカグレルの作用を直ちに逆転させ、血小板活性を回復させる。
Bentracimabの臨床研究の進展
第3段階逆IT臨床試験
2020年3月、私たちは重要な逆IT試験を開始した。この世界的、マルチセンター、非ランダム、開放ラベルの実験では、制御できない大出血または生命に危険な出血または緊急手術または侵襲的手術を必要とする患者200名を募集し、2021年11月に発表された第1陣150名の患者の中期分析結果に基づいて加速承認を申請する予定である。この試験の主な終点はフェニルトラマモノクロチカグレルの抗血小板作用の静脈内投与であり,これはVerifyNow®PRUTIST®バイオマーカーにより測定され,試験に組み込まれた患者で臨床止血を実現した。私たちの目標は2022年に私たちのBLAを提出することだ。
私たちは最近、逆IT試験に参加した最初の150人の患者の計画中期分析を完了し、
2021年11月にこの分析の結果が発表された。150人の入選患者(142例)の予め指定された中期分析
試験に参加した患者は緊急手術或いは侵襲性手術が必要であり、その中の8人は制御できない大出血或いは生命に危害を及ぼす出血を有する)により、bentracimabはチカグレルの抗血小板作用を直ちにと持続的に逆転させることにより、試験の主要な終点に達したことを表明した。看護点VerifyNow PRUによる血小板機能分析の測定,a
血小板抑制率135%低下(P
すべての時間点で二十四時間を超え続けます。条件を満たした患者の90%以上が共通の一次ゴールに達しました
試験中,止血が良好あるいは良好なものはベンゼントラマモノクロナル抗体治療開始後24時間以内(P)と定義された
5.3%の患者が関連イベントを報告しており、死亡や被調査者が
Bentracimab。
Bentracimabの耐性は一般に良好であり,5つの非重篤な有害事象があり,3人の患者が報告されている
被調査者はbentracimabが関与していると考えられた。最もよく見られる有害事象は痛みと関係がある
外科手術です。4人の患者が調査員がベンゼントラマモノクロナル治療とは無関係と考えた事件で死亡した:2名
2例は感染性ショック、2例は心源性ショックであった。Bentracimabの免疫原性も
試験は患者のベントリミズマブの注入開始前後の抗薬抗体或いはADAを測定した。選考結果
免疫原性テストでは22.6%の患者が以前ADAが存在し、24.3%の患者が
53.0%の患者はADAを認めなかった。ADAの存在はチカグレルの逆転に有意な影響を与えなかった
VerifyNowや有効止血が得られた場合に基づいて測定した。
2 b期臨床試験
2021年11月、私たちは、200人の高齢者および高齢者(50~80歳)の健康ボランティアにおけるチカグレル抗血小板作用の安全性および有効性を評価するための多中心、無作為、二重盲検、プラセボ対照試験である2 b期bentracimab試験のTOPLINEデータを発表し、そのうち150人の被験者がbentracimab治療を受け、50人の被験者がプラセボ治療を受け、これらの試験はチカグレルまたは低用量アスピリンからなる二重抗血小板治療を受けた後に行われた。2 b期bentracimab試験では,注入開始後5分でチカグレルの抗血小板活性がただちに完全に逆転し,看護点VerifyNow PRUTestバイオマーカーによる20時間以上の逆転が観察された。また,bentracimabの治療は良好な安全性を有し,2 b期試験では薬物関連SAEや血栓事象は報告されていない。われわれが以前に完成したbentracimab 2 a期臨床試験では,テカグレルの抗血小板活性は注入開始後5分以内に直ちに完全に逆転し,20時間以上逆転し続けていることが観察された。
2 a期臨床試験
2019年9月、私たちはチカグレルおよびアスピリンを服用した老年および老年被験体、ならびに超治療用量チカグレルを服用した健康で、若い被験体においてbentracimabの2 a期臨床試験を完了した。20時間以上持続したベンゼントリメタモノクロナル抗体注入開始後5分間でチカグレルは統計学的に有意な逆転が認められた。フェニトラマズマブの投与開始15分後(超治療に対するチカグレル投与量群は30分)、血小板機能は正常に回復し、20時間を超える正常を維持した。Bentracimabは全体的に耐性が良好であり,軽微な副作用のみが報告されている。これらの結果は,われわれの第1段階試験におけるチカグレルを用いた健康,若年被験者の観察結果と一致した。2 a段階試験における高齢者および高齢者対象は、承認された場合、テカグレル治療を受ける可能性が最も高く、bentracimabから利益を得る可能性が最も高い患者集団と類似している。
第一段階臨床試験
2018年9月、著者らは、目標用量を決定し、概念証拠を決定し、bentracimabの安全性および耐性を評価するために、健康な対象においてチカグレルを静脈内投与するbentracimabの第1段階用量漸増臨床試験を完了した。試験では,bentracimabはテカグレルの抗血小板作用を直ちに完全に逆転させることが認められた。我々が協賛したINDに基づいて2018年3月に発効した今回の実験を行った。2019年3月にbentracimabの完全な実験結果が発表されました“ニューイングランド医学雑誌”
われわれの第1段階臨床試験では,10個の逐次用量キュー中の64名の被験者を募集した。試験中の早期用量列の薬物動態学と薬効学データに基づいて、著者らはbentracimabの静脈注入を調整し、未来の試験と目標患者集団の最適な投与量と投与方案を確定した。最初の3群の被験者はベンゼントラマモノクロナル抗体のみを30分間静脈点滴し、薬物動態学と安全性を評価した。その後のコホートはbentracimab服用2日前に標準臨床方案チカグレルを服用して、血小板機能分析を通じてチカグレルによる血小板凝集抑制の逆転状況を直接評価する。いずれの用量列においてもベンゼントラマモノクロナル抗体に関連する副作用や副作用はなかった。
第5群と第6群では,潜在的薬効学的活性用量を投与した最初のベンゼントラマモノクロナル抗体の列であり,血小板機能の回復によりチカグレルの抗血小板活性が直ちにかつ完全に逆転することが認められた。12名の被験者のうち11名は30分輸液終了後の第1測定時点で血小板機能を回復した。逆転の持続時間は用量レベルや被験者によって約1時間から4時間まで様々であり,高用量の持続時間はより長かった。列7では投与計画を修正しました総投与量は18 gです
このうち3 gは輸液の5分前に送達され、その後15 gが一定速度で送達され、7時間55分持続した。キュー7では,すべての被験者が注入開始後2時間以内に完全かつ持続的な血小板機能回復を認めた。血小板活性の回復により,行列7の逆転は約16時間持続し,注入開始から開始した。
第8,9および10群では,フェニトラシズマブの投与レジメンがさらに改善され,従来の列に比べてより速い逆転開始とより長い逆転持続時間が実現された。合計18 gを投与し,最初の6 gは8,9,10群で団注として提供した。残りの12 gは最初の注後8,9および10群に12~16時間投与した。これらの列では,輸液開始後5分前に即時逆転と完全逆転が認められ,20時間以上逆転し続けていた。今後の臨床試験では,これらのキューで観察された用量と投与レジメンをさらに評価する予定である。
計画のBLA提出
FDAのフィードバックによると、私たちは、緊急手術または侵襲的手術を必要とする142人の患者と、制御されていない重大または生命に危険な出血を有する8人の患者とを含む、我々の逆IT試験の中期分析に基づいて、承認を加速させる可能性のあるBLAを提出する予定である。完全な承認を求めFDAの提案と一致した計画を支援するために,逆IT試験に200名の患者を募集する予定である。我々のBLAと最初の150名の患者のデータを提出した後,逆IT試験を完了し,FDAの要求に応じて承認後登録を確立する予定である。我々の目標は,この時期が新冠肺炎の大流行持続範囲と持続時間の影響を受ける可能性があるにもかかわらず,2022年にフェニトラシズマブのBLAを提出することである。FDAは2019年4月にbentracimabの突破治療指定を承認した。EMAは2020年2月にbentracimab Prime称号を授与し、2021年12月に中国のNMPA突破的治療称号を授与した。
難治性高血圧治療用PB 6440
PB 6440は選択的なアルドステロン合成酵素阻害剤であり,難治性高血圧の経口治療に開発されている。鉱質コルチコイドアルドステロンは体内液体と電解質バランスの重要な調節剤であるため、高血圧或いは高血圧の発生発展に重要な役割を果たしている。アルドステロンレベルの上昇は頑固性高血圧、うっ血性心不全と慢性腎臓疾患と関係がある。スピロラクトンなどの受容体レベルで鉱質コルチコイド作用を遮断する薬剤は、難治性高血圧患者に含まれる血圧を低下させることが証明されている。しかし、これらの薬物の使用は副作用によって制限されている。アルドステロン合成を担う酵素(CYP 11 B 2)を抑制することによりアルドステロン産生を抑制することは,高血圧を治療するもう一つの方法である。しかし,アルドステロン合成酵素阻害剤の開発は挑戦的であり,それに密接に関連する酵素であるステロイド11β−ヒドロキシ酵素(CyP 11 B 1)は,多くの潜在的な化合物も抑制するためである。臨床前研究では,PB 6440は高効率かつ選択的なアルドステロン合成酵素阻害剤であり,げっ歯動物や霊長類モデルでは11−デオキシコルチゾンやデオキシコルチゾールを有意に増加させることなく用量依存性のアルドステロン減少を示すことが観察された。経口バイオアベイラビリティおよび薬物動態曲線は、ヒトの1日1回の経口投与量に適しているようである。
われわれは2021年にPB 6440の非臨床INDイネーブル研究を開始し,2022年下半期にINDを提出する予定である。われわれの目標は2022年末に初の人体試験を開始することであり、われわれのスケジュールは新冠肺炎の大流行の範囲と持続時間の影響を受ける可能性がある。
ELP技術
我々のELP特許技術は,ヒトタンパク質エラスチンから発見された5つのアミノ酸反復モチーフ由来の単一サブユニットまたは構築ブロックからなるELPと呼ばれる組換えバイオポリマーに基づいている。この5つのアミノ酸モチーフは複数回繰り返し,ELPバイオポリマーを形成する。私たちは工学技術を通じてELPに基づく製品を生産しています大腸菌.大腸菌ELPバイオポリマーと融合した活性ポリペプチドまたはタンパク質を含む単一タンパク質を産生する。この分子は融合タンパク質として活性を有し,ポリペプチドの切断や放出を必要としない。ELP融合タンパク質は可溶性部分で産生されるE.Coliはこれは拡大と精製を容易にする。
ELPsとの融合はポリペプチドやタンパク質の安定性を著しく向上させ,自然あるいは最小限に変化したポリペプチド配列を用いることができる。これらの融合蛋白は天然分子に類似した効力を保ちながら,分解されることなく循環中の酵素によって保護されていると考えられる。また,融合蛋白はELPの溶解性と長い半減期を保持し,長期的な液体安定性を許容することが多く,注射製品に重要であることが観察された。
ELP融合蛋白は可逆的な相転移を経験することができ、この相転移過程において、ELP融合蛋白は凝集し、皮膚下に徐放ライブラリーを形成する。この相転移は温度変化によって駆動される。低い温度ではELP融合蛋白は完全に可溶であるが,高い温度ではELP融合蛋白はゲル状態にある。これにより,ELP融合蛋白は標準的な細針やシリンジを用いて皮下操作や投与を容易に行うことができる。ELP融合蛋白が体熱に暴露されると、それは1つの薬物バンクを形成し、可溶性ELP融合蛋白をゆっくりと循環に放出する。単一サブユニットのアミノ酸配列を修正し,その全長を変化させることにより,1週間以上の時間スケールで放出されるように我々のELP融合タンパク質を設計することができる。
我々のELP技術に基づく候補製品は,心血管疾患療法の開発に専念するために開発を中止した従来の候補製品を含め,SAEが知られていない500人以上の患者で評価されており,薬物に関連していると考えられ,研究薬の中止につながっている。
臨床前ELPコース
我々は引き続き我々のELP技術を新たな候補製品の開発に応用することに投資している.著者らの重点はそれらの科学或いは臨床検証を経て、しかし半減期が良くなく、安定性と送達能力が比較的に悪いポリペプチドと蛋白質であり、それらの潜在的な治療応用を制限した。
私たちのより高度なELP臨床前計画は
•グルカゴン様ペプチド−2それは.グルカゴン様ペプチド−2、又はGLP−2は、腸管絨毛の成長を刺激し、栄養吸収能を増加させる。GLP−2は、短腸症候群、クローン病、または癌治療を受けた粘膜炎患者を潜在的に治療する方法である。チドゥルペプチドは現在Gattexのブランドで発売されており、FDAが承認したGLP-2に基づく治療法であり、毎日注射する必要がある。動物モデルでは,われわれのGLP−2−ELP候補品は,チドゥルペプチドよりも有効であり,投与頻度が低い持続レベルのGLP−2を提供している。
•C型ナトリウム利尿ペプチドそれは.C型ナトリウム利尿ペプチド,あるいはCNPは,線維芽細胞増殖因子3の欠損を修復する骨成長調節剤であり,これらの欠陥は軟骨発育不全を招き,小人症をきたす。天然CNPの半減期は3分未満であり,直接治療薬としての使用が制限されている。我々は,週1回皮下注射の治療レベルのCNPを提供するために,我々のCNP−ELP候補製品を開発している。マウスモデルでは,我々のCNP−ELP候補品を4日ごとに注射した場合,線形成長への影響が有効であることが観察された。
ペメビタジル(PB 1046)
Pemziviiptadil(PB 1046とも呼ばれる)は新型のVIP皮下注射類似物であり、組換え融合薬物である
VIPと私たち独自のELP技術で構成されたタンパク質。Pemziviiptadilは90人近くの患者に使われています
アメリカで行われているSAEのない三期1/2臨床試験で高血圧や心臓病の病歴がある患者
麻薬に関連していると考えられ、研究薬のこれまでの使用中止につながった。私たちが求めていたのは開発です
Pemziviiptadilは肺動脈高圧の治療に用いられたが,自発的にわれわれの2 b期試験を終了した
2021年12月の新冠肺炎の大流行による製造、関連薬品供給と死亡率への影響
試験参加を登録する。戦略的評価を経て,Pemziviiptadilのさらなる開発を中止することにした
資源と資本の優先順位の再決定,ベントリメタマブの商業化前活動とその他の推進
難治性高血圧のためのPB 6440を含む管路計画。
ライセンス、共同開発、その他の合意
医療免疫有限許可プロトコル
2017年11月、アスリカンの完全子会社MedImmuneと独自ライセンス契約、すなわちMedImmuneライセンスを締結しました。医療免疫許可プロトコルによれば、医療免疫会社は、その所有または制御されたいくつかの特許権に基づいて、任意のヒト疾患または疾患の治療、緩和、診断または予防のために、医療免疫許可プロトコルに含まれる任意の製品または医療免疫許可製品を開発および商業化するために、我々の独占的な世界的許可を付与する。ライセンス内の特許権は、一般に、米国で発行された2つの特許、米国で保留されている3つの特許出願および13件の係属中の外国出願を含む、チカグレルおよび使用方法に結合された抗体に対するものである。最後の特許は2036年に満期になる予定で、延期されないだろう。我々は許可された技術を第三者に再許可する権利があるが,MedImmune許可プロトコルに規定されているいくつかの条件を遵守しなければならない.MedImmuneの許可によると、私たちはMedImmuneに世界的、非独占的、印税免除、撤回不可能な許可と
チカグレルを含む任意の医薬製品、またはチカグレルを含む任意の医薬製品に関する任意の発明、発見、開発または修正を開発する権利があるだけである。
MedImmuneライセンスの条項によると、私たちは支払いをしたか、支払うことを要求されました
•前払い費用は10万ドルです
•医療免疫会社が提供する技術サービスに関する四半期費用
•いくつかの臨床と規制のマイルストーンが実現された後、最高1800万ドルに達する
•いくつかのビジネスマイルストーンに達すると最大5,000万ドルに達します
•医療免疫許可製品の純売上高のうち−1桁から低青少年印税パーセントは,特定の場合には低下する可能性がある。
MedImmuneライセンスから2021年12月31日まで、第三者製品保管コストと記念碑的支払いに関連して360万ドルを支払いました。
医療免疫許可証は全体の医療免疫許可証の有効期間内に、商業上の合理的な努力を使用して、医療免疫許可製品の監督管理許可を開発、獲得、維持し、それを商業化することを要求する。私たちは最初の権利を持っているが、義務はなく、許可内の特許の起訴を統制する。また、私たちが合併または売却を通じて私たちの株式や資産、またはわが社の関連会社を売却しない限り、MedImmuneの許可の下で私たちの権利は私たちの第三者購入者に譲渡することはできません。
私たちが事前に終了しない限り、MedImmune許可は、私たちがMedImmune許可の下で何の許可使用料も足りなくなった日に自動的に無効になり、この日は以下の遅い日に発生します:(1)MedImmuneライセンス製品の初の商業販売10周年、(2)最後のライセンス内特許が2036年に満了し、(3)MedImmuneライセンス下の排他的規制が満了します。MedImmuneライセンスは満期までに終了する可能性があります:
•私たちと医療免疫会社の書面で同意しました
•いずれか一方の医療免疫許可証に対する実質的な違反であり、このような違反の性質により、指定された治癒期間内に修復されていない
•いずれか一方が破産し、債務不履行、または何らかの類似した状況が発生した場合には、いずれか一方が負担する
•もし私たちがどんな訴訟や訴訟を起こしても、いかなる許可特許の有効性または実行可能性に疑問を提起すれば、
•特定の場合、(1)bentracimabまたはbentracimabを含む任意のMedImmune許可製品の安全性または有効性に関する問題、または(2)任意のMedmune許可製品の商業的可能性に関する問題が存在すると心から考えられる場合、それぞれの場合、独立した専門家による議論の解決が必要である
•特定の国または地域については、チカグレルを含む任意の製品がその国または地域の規制機関によって撤回された場合、私たちが責任を負う。
MedImmune許可が終了した後、私たちは、特許権および独自技術に基づいてMedImmuneに独占的、免版税、再許可可能な許可を付与し、その使用、販売、開発、製造、生産、商業化、使用、輸入、輸出、輸送、流通、普及、マーケティング、または他の方法でMedImmune許可がカバーするいくつかの化合物または製品を処理することを可能にする。
2020年1月,SFJプロトコルを締結するとともに,特定の計画移行イベントが発生した場合,MedImmuneはMedImmune許可を譲渡する可能性があることに同意し,bentracimabに関連する業務をSFJに譲渡する独占ライセンス協定を改訂した.
BentracimabとSFJ製薬会社との共同開発協定
2020年1月にSFJプロトコルを締結し,SFJプロトコルにより,bentracimabの抗血小板薬であるチカグレルの反転剤としての世界的な開発を支援する資金を提供してくれた。SFJプロトコルによると、SFJはbentracimabの臨床開発を支援するために最大1.2億ドルを支払うことに同意している。9000万ドルを除いて
最初の助成では,特定のあらかじめ定義されたbentracimab臨床開発マイルストーンに達した後,3000万ドルの助成を受けることを選択した。SFJ協定が発効して2021年12月31日まで、SFJはSFJ協定に基づいて吾らを代表して資金および支払総額9,130万ドルを提供している。SFJはまた、2870万ドルの追加臨床試験費用およびその他の費用を援助または精算すると予想される。
SFJプロトコルの有効期間内に、私たちは主にアメリカとEUのベントラマズマブの臨床開発と監督活動を担当し、SFJは主に中国と日本のbentracimabの臨床開発と監督活動を担当し、EUで臨床試験運営支持を提供する。私たちは、私たちのbentracimabの逆IT試験を行い、完了するために商業的に合理的な努力を使用して、指定された時間内にBLAまたはその海外等価物をFDAおよびEMAにそれぞれ提出することに同意する。私たちはSFJと共同指導委員会を設立して、私たちの逆IT計画と規制プロセスを含めて監督·管理協力を行っています。
SFJ協定の条項によると、FDAがbentracimabのBLAを承認した後、SFJに初回支払い500万ドルを支払い、7回の追加年間支払いで合計3.25億ドルを追加支払います。EMAまたはいくつかのヨーロッパ諸国の国家規制機関がbentracimabの上場を許可した場合、SFJに500万ドルの初期支払いを支払い、7年以内に合計2.05億ドルを追加支払います。もし日本の薬品と医療機器署、薬品と医療機器管理局あるいは中国の国家薬品·薬物管理局がベントラマズマブのマーケティング申請を許可した場合、SFJに100万ドルの頭金を支払い、8年に分けて合計5,900万ドルを追加支払います
上記のいずれかの管轄区域がBLAまたは同等のBentracimabを承認してから120日以内に、私たちの選択に基づいて、SFJに現金を一度に支払い、中央値割引率を反映した価格で、司法管轄区域の将来支払われていない承認支払いの全部または一部を買収する権利がある(すなわち、米国承認支払い、EU承認支払い、または日本/中国承認支払い)。わが社の支配権変更後120日以内に、私たちまたは私たちの相続人は、支配権変更前にBLAまたはその等価物が承認された任意の管轄区域において、ビット数割引率中央値を反映した価格で将来支払われていないすべてまたは一部の承認支払いを購入する権利をSFJに一度に支払う権利がありますが、SFJは以前にそのようなお金を受け取る権利を第三者に譲渡していません。この場合、私たちまたは私たちの相続人はその権利を持っていません。
SFJプロトコルによれば、私たちは、bentracimabまたはbentracimab知的財産権の製造、使用、または販売に必要なSFJに、私たちが所有または制御するすべての資産の保証権益を付与します。保証権益の付与に関して、私たちは、配当金の支払い、追加債務の発生、またはbentracimab知的財産権に関連する許可取引を行う能力の制限を含む、いくつかの肯定的かつ否定的な条約に同意する。また,吾らはSFJに付与された担保権益を優先担保権益とすることに同意したが,SVBの自社既存債務に対する留置権の制限を受けなければならない。
SFJ協定に署名した後、SFJに10年間の引受権証を発行し、1株6.50ドルの行使価格で2,200,000株の普通株を行使することができる。この株式承認証は、以下のように行使することができる:(I)1,100,000株は、SFJ協定の発効日後の任意の時間に行使可能であり、SFJは、この発効日の1年後に当該行使された株式を販売することができ、(Ii)残りの1,100,000株は、SFJが選択した任意の時間に行使することができ、前提は、我々の逆IT試験結果が逆IT試験プロトコルに記載されている一時的な主要な終点に適合することである。
(I)指定された期間内にSFJプロトコルに従ってSFJに任意の対処金を支払うことができなかった場合、(Ii)特定の例外がない限り、または(Iii)(A)本四半期の財務諸表の発行または発行可能日の後1年以内に満了するので、私たちの義務を履行できない可能性が高いと判断し、または(B)任意の財務諸表に“持続的な経営”脚注を含む。(A)または(B)の2つの場合,SFJプロトコルで規定されている継続経営条件を救済することができず,SFJはbentracimabに関する業務をSFJに移行することを選択することができる.このようなイベント(I),(Ii)または(Iii)を潜在的なプラン遷移イベントと呼ぶ.私たちは、私たちのコストと運営を再構成し、融資や戦略取引で追加資本を調達すること、またはSFJを最初に約束したのと同じ条項で追加融資を提供することを含む持続的な経営状況を救済することができる四半期が複数あります(彼らは追加融資を提供する権利がありますが、提供する義務はありません)。もし私たちがbentracimabに関連するビジネスがSFJに移行すれば、SFJがbentracimabへの投資から300%のリターンを得るまで、bentracimabの商業化された収入を共有しないだろうし、その後、bentracimabの米国およびあるヨーロッパ諸国での純販売から1桁の中央値の特許権使用料を得る権利があり、SFJがbentracimabへの投資で合計500%のリターンを得た後、世界の他の地域のbentracimabの純売上高で中央値の特許使用料を得る権利がある。リスク要因を見る--“12月31日までの財政年度に監査された財務諸表に対する監査人の意見, 本年度報告におけるForm 10−Kには一段の説明が含まれており,我々の持続経営企業としての持続経営能力に対する深刻な疑いに触れている。また,SFJプロトコルにより,SFJは我々の業務をbentracimabに関連付けることを選択することができる
SFJプロトコルで規定されている期間内に継続的な経営状況を是正しなければ、bentracimabの商業化された任意の収入を共有する能力は大きな悪影響を受ける。延期されるかもしれません
私たちの開発計画の範囲を縮小したり/または私たちの運営を制限したり停止したりすることができなければ
私たちの現在の運営計画を支援するための資金を提供する
SFJプロトコルは、事前に終了しない限り、SFJにすべての承認支払いを支払った後に満了する。SFJが合計6,000,000ドルのbentracimab開発コストを支払った後、およびFDA、EMA、PMDAまたはNMPAが任意のbentracimabのBLA(またはその等価物)を承認する前に、私などはいつでもSFJプロトコルを終了することができる。(A)任意の米国、特定のヨーロッパ諸国、中国、日本または香港でbentracimabをさらに開発または商業化することが禁止されている場合、または(B)bentracimabの将来の価値が重大な悪影響を受ける場合、(1)いくつかの第三者特許が米国のどこでも製造、使用、販売、販売または輸入によって侵害される場合、sfjは、以下の場合にsfjプロトコルを終了することができる:(I)sfjプロトコルで定義された重大な有害事象が発生した場合、(Ii)我々の制御権が変化した場合、(Iii)(A)米国でのさらなる開発または商業化が禁止されている場合、(Ii)我々の制御権が変化した場合、(Iii)(A)米国でのさらなる開発または商業化が禁止されている。(2)米国、いくつかのヨーロッパ諸国または中国、日本または香港、または(2)米国、特定のヨーロッパ諸国、日本、中国または香港で((A)および(B)のそれぞれを特許悪影響と呼ぶ)、SFJ通知後6ヶ月以内に抗血小板薬であるカグレル逆転薬としてのベントリメラマブを治癒できない場合、または米国、いくつかのヨーロッパ諸国、日本、中国または香港のいずれかの患者に制御できない大出血または生命に危険な出血がある場合、または緊急手術または侵襲手術を必要とする患者は、我々が制御するすべての特許権が無効または実行不可能である。または(Iv)SFJが共同指導委員会の一部として私たちが行ったいくつかの決定に同意しない場合。Bentracimabがbentracimabの逆IT試験を完了した後、FDA、EMA、PMDAまたはNMPAのうちの少なくとも1つの規制許可を得られなかった場合、いずれか一方は、以下の場合、sfjプロトコルを終了することができる:(I)他方はsfjプロトコルに実質的に違反し、(Ii)bentracimabがFDA、EMA、PmdaまたはNMPAの規制承認を得られない場合、BLASを提出する, またはその等価物を使用し、商業的に合理的な努力を使用して、そのようなBLASまたはその等価物の承認を得るために、(Iii)bentracimabの逆IT試験が完了または終了し、(A)逆IT試験の主要な終点に到達できなかった場合、または(B)SFJが試験結果を合理的に決定して規制承認をサポートしない場合、(Iv)他方が倒産したとき、(V)bentracimab逆IT試験の独立データ監視委員会が、安全または健康上の理由でまたは無効であることを提案した場合、または双方が実質的な健康または安全問題が存在することに同意した場合、または(Vi)他方が規定に違反し、そのような違反が治癒されない限り、bentracimab臨床試験を完了する可能性に大きな悪影響を与えることもなく、bentracimabの規制承認も得られないことに関連する。
場合によっては、SFJプロトコルの終了後、SFJプロトコルに従ってSFJに支払いまたは発生した金額の倍数をSFJに支払う義務がある
•上記金額の300%(1)SFJが吾等の重大なSFJ協定違反または当社の破産によりSFJプロトコルを終了した場合、(2)初めて監督管理機関がbentracimabを承認する前にSFJプロトコルをランダムに終了する場合、または(3)SFJプロトコルがセキュリティ上の考慮により終了し、終了した場合、(A)我々の深刻な不注意のため、または(B)SFJプロトコル日に既知の深刻なセキュリティ問題のため、SFJプロトコル日までに、SFJに重大なセキュリティ問題を示すデータを開示または開示しなかった場合、SFJはプロトコルを終了する
•SFJが以下の場合、SFJプロトコルを終了する場合:(1)私たちの支配権変更、または(2)私たちの不適切な支払いまたは反腐敗政策に関連する違反は、このような違反が是正されない限り、bentracimab臨床試験が完了する可能性や、規制機関の許可を得ることがbentracimabの承認に重大な悪影響を与えることはない
•特許の悪影響により終了した場合、そのような金額の100%が支払われる
•SFJが共同指導委員会の一部としての何らかの決定に同意せずに終了した場合,25%の年率で100%のこのような金額(そのような金額を反映した利息を加える)を支払う。
また、SFJプロトコルが終了した後、吾らはbentracimabを開発し、米国、EU、日本または中国でBLA(またはその同等の地位)の承認を取得し、SFJプロトコルが終了していないように、終了時に支払われた任意のお金をSFJに支払うが、SFJが満期時に私等に何も支払うことができずにSFJプロトコルを終了したり、SFJが重大な不利なイベント(定義SFJプロトコル参照)でSFJプロトコルを終了したりすれば、当社等が当該等の承認支払いを支払う責任は50%減少する。
デューク大学許可協定
2006年10月、Dukeと独占ライセンス契約を締結しましたが、最近の修正は2019年4月、またはDuke許可です。デュークライセンスによると、デュークは、デュークが所有または制御しているいくつかの特許権に基づいて独占グローバルライセンスを付与し、デュークの特定の独自技術に基づいて、デュークライセンスまたはデュークライセンス製品に含まれるELPに関連する任意の製品またはプロセスを開発および商業化するために、非独占グローバルライセンスを付与している。ライセンス内特許権は、一般に、皮下注射によって投与されたタンパク質およびポリペプチドに対して、米国における13の登録特許、外国司法管轄区における24の登録特許、米国における2つの係属中の特許出願、および4つの係属中の外国出願を含むより広い曝露を提供する。最後の特許は2030年に満了される予定で、延期されないだろう。
私たちはデューク許可証に規定されているいくつかの条件に基づいて、デューク許可の製品を第三者に再許可する権利があります。2017年5月、Dukeの許可下のいくつかの特許権はDukeの手に回復し、Dukeはその後、そのような特許権に関連する任意の製品またはプロセスを開発し、商業化するために、そのような特許権の下での非独占的許可を付与してくれた。Dukeにはまた,Duke許可下で我々に許可されている特定の特許権下での独占再許可と,我々が所有または制御している特定の特許権下での非独占許可を再付与し,いずれの場合も,我々独自のELP技術を用いて開発された化合物を開発することができる.
Dukeライセンスの条項によると、私たちはすでに支払うことを要求されています:
•前払い費用は37,000ドルです
•その後のデュークライセンスの修正に関連した修正費用は20万ドル
•追加許可料は20万ドルです
•220万ドルに達した臨床と規制のマイルストーン費用
•40万ドルのビジネスマイルストーン費用です
•デュークライセンス製品の純売上高の1桁の特許使用料は百点と低く、私たちがいくつかの商業マイルストーンを実現した後、最低支払いの特許使用料の総額は20万ドルである
•最大30万ドル、または第三者から受信した費用のより低い2桁の数百点を比較して、デューク許可証に含まれるいくつかの特許権について戦略同盟を構成することを考慮する。
私たちに許可権を与える代価として、私たちは最初にデューク24,493株の私たちの普通株を発行した。2007年10月にある規定の株式マイルストーンに達する前に、私たちは時々Dukeに普通株を発行し、その総保有量が私たちが発行した株式と発行した株の7.5%を占めるようにする義務がある。
Duke許可から2021年12月31日まで、私たちはDuke許可の下で30万ドルの印税コストを発生させた。Dukeは2017年5月現在、Dukeの許可の下に含まれるいくつかの製品の許可または再許可を付与することで得られた収入の一定の割合を支払う必要があります。デューク大学は2021年12月31日まで私たちにこのような費用を支払っていない。私たちはまたDukeに私たちが再許可者から受け取った最初の100万ドルの非特許権使用料を支払い、そしてDukeに私たちが受け取った任意の追加の非特許権使用料の低い2桁の数百分を支払わなければならない。
デュークライセンスは、デュークライセンスの有効期間全体にわたって、特定の開発スケジュールに基づいて、商業的に合理的な努力を使用してデュークライセンス製品の規制承認を開発、獲得、維持し、商業化することを要求している。私たちはデューク大学許可証の下のすべてのアメリカと外国特許権の申請、起訴、維持を要求された。また、デューク大学の事前書面の同意なしに、デューク大学許可証の下での私たちの権利は、私たちの株や資産を合併または売却することによって第三者の買収者、またはわが社の付属会社に譲渡しない限り、譲渡することができません。
以前に終了しない限り、デュークライセンスは、デュークライセンスによって付与されたすべての特許権が満期になった日に自動的に失効するか、または私たちが破産し、債務を相殺しない場合、またはいくつかの同様の状況が発生したときに自動的に失効する。Dukeライセンスは満期までに終了することができます
•私たちと公爵の双方の書面で同意した
•私たちがデュークに3ヶ月の書面通知を出しました
•一方の一方に対する故意の詐欺、故意の不当な行為、または重罪の違法行為、または罪を認める
•一方が他方に対して実質的に公爵許可証に違反する行為は、その違反の性質により、所定の治癒期間内に救済されなかった
•デューク許可証に含まれる特許権の商業開発をかなりの期間停止することに決定した後、デューク大学はその特許権利を商業開発する。
デュークライセンスが終了した後、私たちは、デュークライセンスの下での私たちの権利を行使する過程で私たちが開発した任意の知的財産権を使用するために、私たちの特許権およびノウハウに基づいてデューク独占、印税免除、再許可可能なライセンスを付与します。
Alfasigma分割許可協定
2021年6月、我々はAlfasigma再許可協定を締結し、この協定に基づいて、再許可領土内でbentracimabを含む任意の製品または特許製品を開発、使用、販売、販売、カプセル販売、および輸入するAlfasigma独占権利を付与した。Alfasigma再許可の条項によると、2021年7月、Alfasigmaから2000万ドルの前金を受け取り、ある収入を達成する前の規制マイルストーンを達成する際には、最高3500万ドルを得る資格があり、ある商業マイルストーンの実現と純売上高分別の特許使用料の支払い後、最高1.9億ドルを得る資格があり、パーセントは低い2桁から始まり、25%前後に上昇していく。
3500万ドルまでの規制マイルストーン支払いについて:(I)EMAが最初の許可製品の薬物承認申請を受けた後に1000万ドルを支払う;(Ii)EMAの条件付き規制承認を得た後に1250万ドルを支払う;および(Iii)残りの1250万ドルは、EMAの無条件規制承認を得た後に支払い、以下の2つの場合に、テカグレルの抗血小板作用を逆転させるための許可製品の処方を許可する:(A)制御できない重大または生命に危険な出血がある患者と(B)緊急手術または侵襲的手続きを必要とする患者
Alfasigma分割許可によれば、私たちは、任意のマーケティング許可がAlfasigmaに割り当てられることを含む、SFJプロトコルに従って、任意のマーケティング許可がAlfasigmaに割り当てられることを含むEMAおよびMHRAの規制承認を保証する責任がある。アルファシマには、マーケティングや特許製品の販売に必要な任意の規制承認(定価承認や発売後の約束を含む)を取得し、欧州やイギリス以外の国の規制承認を確保する義務がある。アルファシマはしばらくの間私たちにその要求を購入し、その後、私たちはより低いコストまたはいくつかの合意された金額を超えない価格でアルファシマによって要求された特許製品を少ない量で供給する義務がある。
事前に終了しない限り、Alfasigma再許可は、各ライセンス製品および再ライセンス領域の各国/地域について、(1)そのライセンス製品の国/地域での初の商業販売10周年、(2)その国/地域での最後の外部ライセンス特許の満了、および(3)その国/地域におけるライセンス製品の排他的な満了(ある場合)の最後の日に自動的に失効する。
Alfasigma再許可についても、2021年6月にMedmuneとAlfasigmaと再許可を付与する確認書を締結したり、Grantを確認したりします。その中で、(I)Alfasigma再許可をMedmuneに譲渡することができますか、または(Ii)Medimmune許可をAlfasigmaに譲渡する可能性がありますが、両方の場合、Medimmune許可下の未治癒や救済のいくつかの義務に違反した場合、SFJは“計画移行”(SFJプロトコルの定義のような)を実行する理由がありますが、そうしないことを選択します。2021年12月31日までの年間で、Alfasigmaの許可下で1080万ドルとゼロ収入を確認しました2020それぞれ,である.
バク許可協定
2019年4月、私たちは、バク固有の大腸菌株を使用してbentracimabを生産し、bentracimabを商業化し(承認されれば)バクの特定の知的財産権に基づいて、バク固有の大腸菌株を使用してbentracimabを商業化し、私たちまたは私たちに代わって世界中でバクの大腸菌固有株を生産することができるバクバイオテクノロジー株式会社またはバク社とライセンス契約を締結した。私たちは本許可に基づいて再許可を与える権利がありますが、バク許可協定に規定されているいくつかの条件を守らなければなりません。協定条項によると、私たちは固定的で象徴的な単位あたりの特許権使用料を支払う必要があり、この数字は調整される可能性があり、固定ユーロ金額で支払われる年間許可料は、金額が低いから中6桁になる可能性がある。この協定は一定期間有効であり、私たちの印税義務が満了した後、許可は全額支払いとみなされ、非独占許可に変換されます。指定された日数内に是正されなければ,いずれも違約によりバク許可プロトコルを終了することができる.著者らはワットからBioVectra Inc.あるいはBioVectra(他の良好な製造規範の認証を得た別のメーカー、あるいはcGMP)への現在のbentracimab製造技術の技術譲渡を完了し、BioVectraを招聘して私たちが行っている臨床試験のために薬剤を製造し、監督許可を得た後に商業供給のbentracimabを生産した。
Viamet資産購入契約
2020年1月に、吾らはViamet PharmPharmticals Holdings、LLC及びその全額付属会社Selenity Treateutics(バミューダ)、Ltd.或いは売り手と資産購入プロトコル或いはPB 6440プロトコルを締結し、これにより、私らはPB 6440、売り手独自のCYP 11 B 2阻害剤化合物(旧SE-6440或いはVT-6440)及びいくつかの他のPB6440プロトコルによって買収された特許権がカバー又は共通にカバーする化合物に関するすべての資産及び知的財産権を買収した。取得された特許権には、発表または未解決の米国および外国特許および特許出願が20件含まれており、最後の発表された特許は2037年に満了する予定である。PB6440協定の条項によると、吾らは取引完了時に売主に前払い費用10万ドルを支払い、特定の化合物を含む候補製品についてある開発および知的財産権マイルストーンを達成した場合には売り手に最大510万ドルを支払い、化合物を含む承認製品がある商業マイルストーンを達成した場合には売り手に最大1.425億ドルを支払い、特定の場合には化合物を含む承認製品の純売上高の中から1桁までの使用料の割合で支払うことを要求している。
BioVectra供給プロトコル
2021年3月、私たちはBioVectraまたはBioVectraプロトコルと、bentracimab用の原料薬をBioVectraから製造および供給し、規制の承認を得たら商業流通に使用する供給協定を締結した。私たちはまたBioVectraを招いて私たちが行っている臨床試験のための医薬物質を製造した。BioVectra協定の条項によると、BioVectraは、毎年合意されたロットの製品を生産する能力を維持することを約束し、私たちは、第三者とベンゾトラマママブを生産する契約を自由に締結することができるにもかかわらず、指定された最低ロット製品を毎年購入すること、または最低年度承諾を約束する。
我々は各ロットの製品の供給価格を支払い、価格は製品の製造過程でBioVectraプロトコルに基づいて検証した後、ある消耗品、原材料、第三者テストのコストを加えて確定する。双方は、製品の初期供給価格は“BioVectraプロトコル”に規定されている推定供給価格の特定のパーセンテージ内にあり、発効2周年の間は変わらないと合意した。その後、2周年後の年度を検証した上で、いずれも規定のインフレ率に基づいて増加或いは減少の供給価格を調整することができるが、毎年最大インフレ率の制限を受けなければならず、BioVectraがコストの異常な増加或いは減少を証明できれば、BioVectraは供給価格をこのインフレ率を超えるレベルに調整することを提案することができるが、規定を遵守する毎年最大パーセンテージが増加或いは減少しなければならない。
最低年度約束によると、私たちは2022年から2023年の間に少なくとも約1,400万ドルの製品ロットを購入する責任があり、(Ii)2024年に約3700万ドルの製品ロットを購入し、(Iii)2025年から2031年の間に毎年約4,800万ドルの製品ロットを購入する責任があるもし私たちが特定の年に適用された最低年間約束を購入しなかった場合、私たちはBioVectraに金額を支払う義務があり、金額は当時適用された各ロットの供給価格にその年の最低年間約束とその年に実際に購入した製品ロットとの差額、または最低差額支払いに等しく、BioVectraがその年度に私たちが注文したロット数を渡すことができない限りである。BioVectraがある年に私たちが注文した数量で製品を供給できなかった場合、私たちはその年(および可能な1年または複数年)に対する最低年間約束は減少し、私たちはその年(および可能な1年または複数年)に最低差額を支払う義務を放棄するだろう。私たちは2026年以降の最低年間約束額を毎年最大1つの特定の最高パーセントに減らす権利があるだろう。また、私たちがbentracimabを使用した製品の規制承認を米国またはヨーロッパの1つの地域でしか得られない場合、私たちとBioVectraは、製品要求の低減と供給価格への影響を反映して、より低い数量約束を反映するために、BioVectraプロトコルの修正案を誠実に議論することに同意した。
BioVectraプロトコルの初期期限は,BioVectraプロトコルの発効日から,製品の製造過程がBioVectraプロトコルや発効確認後10周年まで続いている.双方の同意により、“生物ウィトラ協定”の期限はもう1年延長できる。どちらか一方が治癒していない実質的な違約または他方のある破産事件が発生した場合、BioVectraプロトコルを終了することができる。(I)BioVectraまたはその雇用または採用されたBioVectraプロトコルの下でサービスを実行する任意の人員が特定の法規を遵守できない場合にBioVectraプロトコルを終了するか、または(Ii)BioVectraに終了料を支払うことができる(終了費用の金額はBioVectraプロトコルの期限内に減少する最初の百万ドル程度の最高限度額からゼロ)ではBentracimabを使用する製品の規制承認または商業化を求めないか、またはMedimmune Limitedの製品の許可を終了した場合、もし私たちがbentracimabを使用することを決定しないか、または求めることができない場合。BioVectraプロトコルを無断で終了することもできますので、終了費用を支払う必要はありません
費用は、FDAまたはEMA規制機関がbentracimabを含む製品を承認してから5周年後24ヶ月後に通知された後に徴収される。
製造業
著者らの巨大分子臨床候補製品bentracimabとELP臨床前と開発パイプライン候補は現在微生物発現システムを用いて生産されている。私たちの製造は単刀直入な大腸菌.大腸菌発酵プロセスは簡単なカラムクロマトグラフィー精製技術を用いた。我々の小分子候補物PB 6440は化学合成により製造された。私たちはこれらの製造技術が私たちの候補製品を効率的に臨床と商業応用に使用できると信じている。私たちにはcGMP生産施設は何もありません。逆に,第三者を用いて我々の候補臨床試験製品cGMPを生産し,短期的に第三者を用いて将来の臨床開発を継続する予定であり,彼らが承認されれば,我々の薬物製品は商業的に生産される。我々の契約メーカーはFDA検査を経た機関であり,cGMPによる製薬業界への製品供給の歴史がある。
Bentracimab
Bentracimab原料薬はMedImmune許可証によって著者らに提供され、すでに充填され、放出され、著者らの初歩的な臨床試験に用いられた。Bentracimab薬は,第三者契約メーカーバクがバクのノウハウを用いて製造したものであるE. Coli菌株。著者らはバクから別のcGMPメーカーBioVectraに現在のbentracimab製造技術を譲渡する技術移転を完成し、BioVectraを招いて著者らが行っている臨床試験のために薬剤を製造し、監督許可を得た後に商業供給のbentracimabを生産した。
ELP臨床前チャンネル
私たちはこれまで非専門家に依存してきました大腸菌.大腸菌私たちの臨床前ELPパイプライン候補株を生産するために使われています第三者メーカーはすでにこの薬品のcGMP製造を行っている。これまでに得られた効率のため,この非特許菌株を将来の製造に利用する予定である。著者らは開発を通じて臨床前候補製品を推進することに伴い、私たちはもっと多くの供給プロトコルと/或いは技術移転プロトコルを構築して、未来の臨床試験に対する期待需要と潜在的な商業需要を満たすつもりである。
PB6440
PB 6440は化学合成された小分子候補化合物である。第三者メーカーはこの薬物のcGMP製造を実行する。私たちが開発を通じてPB 6440の発展を推進することに伴い、私たちは未来の臨床試験に対する期待需要と潜在的な商業需要を満たすために、より多くの供給プロトコルおよび/または技術移転プロトコルを構築するつもりである。
販売とマーケティング
私たちがAlfasigmaのbentracimabに権利を与えることを除いて、私たちはすべての候補製品の世界的な商業権を維持する。私たちの開発段階を考慮して、私たちは私たちの商業組織と流通能力を建設している。承認されれば,bentracimabを米国で独立して商業化する予定であり,これらの適応の患者群や医学専門家が十分に集中しており,的確な販売チームで効率的にこれらの製品を普及させることができると信じているからである。私たちは、米国境内外で任意の他の承認された製品を商業化し、私たちの製品のビジネス潜在力を最大限に発揮するために、第三者との戦略的協力やパートナー関係を探索し、選択的に求めることができる。
競争
製薬業は技術の迅速な進歩、激しい競争と独自製品に対する高度な重視に直面している。私たちは主要な製薬、専門製薬と生物技術会社、学術機関、政府機関及び公共と個人研究機関を含む多くの異なる源からの潜在的な競争に直面している。我々が開発と商業化に成功した任意の候補製品は,既存の治療法や将来出現する可能性のある新しい治療法と競合するであろう。
私たちは現在、潜在的な未来の競争相手と上場が許可された薬物を商業化する上で明らかに多くの経験を持っている。製薬とバイオテクノロジー産業の合併と買収は、私たちの少数の競争相手により多くの資源を集中させる可能性がある。私たちの競争相手はもっと多いかもしれません
私たちよりも治療の規制承認を得ることに成功し、彼らの薬物を広く市場に受け入れさせた。私たちの競争相手が狙っている疾患に対して、治癒またはより効果的な治療法を開発することも可能であり、これは、現在または将来の候補薬を競争力を失ったり、時代遅れにしたり、開発および商業化費用を回収することができる前に候補薬の需要を減らすことができるかもしれない。
Bentracimab
テカグレルまたは任意の他の抗血小板薬のための他の既知の反転剤が承認または臨床的に開発されていない。EUでは、インビトロ全血浄化吸着装置があり、体外循環と組み合わせて使用される場合、いくつかの心臓手術中にチカグレルを非特異的に除去するのに役立つ可能性がある。この装置のメーカー細胞吸着会社はまた、心臓手術におけるDrugSorb-ATR抗血栓除去システムの使用を評価するための臨床試験を米国で開始した。承認されると、bentracimabは、特定の逆チカグレルに使用可能な唯一の治療薬となるであろう。したがって、承認されれば、bentracimabに対する市場の受容の程度は、テカグレルに対する市場の持続的な受け入れおよび使用に大きく依存するであろう。チカグレルは、他のP 2 Yを含む他の商業的に利用可能な抗血小板療法と競合する12受容体アンタゴニストは、その多くが模倣薬であるため、現在ではチカグレルよりもはるかに安い。将来的には他の可逆的P 2 Yも含めた新たな抗血小板療法が開発される可能性がある12受容体拮抗薬や他の抗血小板療法は,逆転薬がある可能性もあり,テカグレルの代わりに急性冠症候群を治療する第一選択の抗血小板薬となる可能性がある。
PB6440
PB 6440は患者の既存の抗高血圧療法の補完として利用される可能性が予想されるが,現在の鉱質コルチコイド受容体に対する非特許高血圧療法と競合することが予想される。現在承認されている塩酸コルチコイド受容体拮抗薬であるエプリノンとスピロラクトンに加えて、難治性高血圧を治療する臨床開発における治療法も知られており、承認されれば、PB 6440はそれと競合する
•前進性Janssen Biotechが開発している経口活性二重エンドセリン受容体アンタゴニスト;
•燃えさかる量子ゲノム社が開発している選択的かつ特異的なアミノペプチダーゼA阻害剤;
•CIN-107Cincor PharmPharmticalsが開発しているアルドステロン合成酵素阻害剤;
•MLS-101Mineralys Treeuticsにより研究されているアルドステロン合成酵素阻害剤;
•BI 690517は,バーリンガー·インゲルハイムにより研究されているアルドステロン合成酵素阻害剤である。
知的財産権
私たちのビジネス成功は、bentracimab、PB 6440、および将来の候補製品および関連する発見、ならびに私たちのELP技術の独自の保護を獲得し、維持する能力があるかどうかにある程度依存します;他人の独占権を侵害するか、または他の方法で侵害することなく運営し、他の人の侵害または他の方法で私たちの独占権を侵害することを防止します。私たちは、私たちのELP技術、私たちの候補製品、および私たちの業務の発展および実施に重要な他のノウハウ、発明、および改善に関連する米国および外国特許出願を提出することによって、私たちの独自の地位を保護しようとしています。私たちはまた、商標、商業秘密、技術ノウハウ、持続的な技術革新、潜在的な許可内の機会に依存して、私たちの独自の地位を発展させ、維持しています。
個別特許の期限は,特許出願の提出日と特許を取得した国の特許法律期限によって異なる。一般に,米国では,定期的に提出された出願から発行される特許有効期間は20年であり,非仮出願の最初の提出日から計算される。さらに、場合によっては、特許を発行する際の米国特許商標局の一部の遅延を補うために、特許期限を調整することができる。また、特許期間は、FDAによる特許がカバーされている薬物の規制審査期間によって実際に失われた一部の特許期間を再取得するために延長することができる。FDAの遅延によれば、特許有効期間は、特許満了後最大5年間延長することができるが、特許の残り期間を製品承認日から合計14年間延長することはできず、延期は、承認された薬剤をカバーする特許(および承認された薬剤またはその使用方法に関する特許請求項にのみ適用される)にのみ適用される。そのような特許期間の調整や延長が得られる保証はない。外国特許の有効期限は適用される現地法の規定によって異なるが,我々が出願している国では,特許期間は通常非特許の最初の出願日から20年である
臨時特許出願。しかしながら、特許によって提供される実際の保護は、製品によって異なり、国によって異なり、特許のタイプ、そのカバー範囲、規制に関連する延長の利用可能性、特定の国における法的救済の利用可能性、および特許の有効性および実行可能性を含む多くの要因に依存する。
また、私たちはビジネス秘密、技術ノウハウ、持続的な技術革新に依存して、私たちの競争地位を発展させ、維持している。私たちは、私たちのビジネスパートナー、協力者、従業員、コンサルタントとの秘密協定、および私たち従業員との発明譲渡協定の一部を使用して、私たちの独自の情報を保護することを求めています。私たちはまた、当社のビジネスパートナーおよび選定されたコンサルタントとセキュリティ協定または発明譲渡協定を締結しました。これらのプロトコルは、我々の独自の情報を保護し、発明譲渡プロトコルの場合、第三者との関係によって開発された技術の所有権を付与することを目的としている。このような合意は違反されるかもしれないし、私たちはそのような違反に対応するための十分な救済措置を持っていないかもしれない。しかも、私たちのビジネス秘密は競争相手に知られたり独立して発見されるかもしれない。もし、私たちのビジネスパートナー、協力者、従業員、およびコンサルタントが、私たちのために働いているときに他人が所有している知的財産権を使用する場合、関連するまたはそれによって生じるノウハウおよび発明の権利について論争が生じる可能性がある。
2021年12月31日現在、私たちの特許権は、私たちのELP技術または私たちの候補製品の様々な側面を保護するために、私たちが所有または許可している少なくとも22個の特許シリーズを含む。私たちは26件の米国特許、16件の米国特許出願、135件の外国特許、75件の外国特許出願を持っているか、または所有しています。
Bentracimab
Bentracimabに関して、私たちは特許家族の許可を得た。2021年12月31日現在、この特許シリーズは、特許期間の延長を考慮せず、3つの係属中の米国特許出願、2つの発行された外国特許、および13件の未解決外国出願を含む2つの発行された米国特許を含み、その事項構成要件がベンゼントラマモノクロナル抗体をカバーし、2035年と2036年に満了すると予想される
PB6440
2020年1月にPB 6440の知的財産権を取得した後,アルドステロン合成酵素阻害剤に関連する3つの特許シリーズを取得し,2021年12月31日現在,米国で許可されている3つの特許,米国で出願中の2つの特許,および海外で出願されている特許15件を含む。付与された米国特許は2037年に満期となる予定であり,特許期間の延長は考慮されていない。
ELP技術
2021年12月31日現在、私たちは、米国で許可された2つの特許、米国で出願されている2つの特許、および出願中の外国特許10件を含む、我々のELP技術に関連する2つの特許シリーズを持っている。第1項に付与された特許は2021年に満了する予定であり,第2項は2035年に満了する予定であり,特許期間の延長は考慮されていない。
政府規制と製品審査
FDAとその他の連邦、州と地方及び外国の監督管理機関は、他を除いて、私たちが開発している生物製品の研究、開発、テスト、製造、品質管理、輸出入、安全、有効性、ラベル、包装、貯蔵、流通、記録保存、承認、広告、販売促進、マーケティング、承認後の監視と承認後報告などの方面に対して広範な監督管理を行った。私たちは、第三者請負業者と共に、私たちが研究したい、または承認を求めることができるかもしれない国/地域規制機関の様々な臨床前、臨床、および商業承認要件を満たすことが要求されるだろう。
FDAがバイオ製品候補製品が米国で発売される前に必要とされるプログラムは、一般に以下のような態様を含む
•FDAの良好な実験室操作規範(GLP)に基づいて臨床前実験室テストと動物研究を完成した
•臨床試験が開始される前に発効しなければならず、毎年更新されるか、または大きな変化が生じたときに更新されなければならないINDをFDAに提出する
•試験開始前に、各臨床場所の独立機関審査委員会または倫理委員会の承認
•提案された候補生物製品の安全性、純度と効力を決定し、その期待目的を達成するために、十分かつ良好に制御された人体臨床試験を行った
•すべての重要な臨床試験が完了した後、BLAをFDAに提出する準備ができた
•適用されれば、FDA諮問委員会の審査が満足的に完了する
•FDAはBLAを受信してから60日以内に再審申請を提出することを決定した
•CGMPのコンプライアンスを評価するために、生産推奨製品の1つまたは複数の製造施設に対するFDAの承認前検査を円満に完了し、良好な臨床実践またはGCPのコンプライアンスを評価するために、施設、方法、および生物製品の持続的な安全性、純度および効力を維持するのに十分な制御を確保し、良好な臨床実践またはGCPのコンプライアンスを評価するための臨床研究場所を選択した
•FDAは、米国で使用される特定の適応の製品の商業マーケティングを可能にするためにBLAを審査および承認する。
臨床前と臨床発展
候補製品の第1回臨床試験を開始する前に,INDをFDAに提出しなければならない。INDはFDAが人類の研究を許可した新薬製品の要求である。IND提出の中心焦点は臨床研究の全体的な研究計画と方案である。INDには動物や体外培養製品の毒理学、薬物動態学、薬理学と薬効学特徴を評価する研究;化学、製造と制御情報;及び任意の利用可能なヒトデータ或いは文献を用いて研究製品の使用を支持する。INDはヒト臨床試験が始まる前に発効しなければならない。INDはFDAが30日以内に提案された臨床試験に対して安全懸念または問題を提起しない限り、FDA受信後30日以内に自動的に発効する。この場合,INDは臨床的に放置される可能性があり,INDスポンサーやFDAは臨床試験が開始される前に未解決の問題や問題を解決しなければならない。したがって,INDの提出はFDA認可による臨床試験の開始につながる可能性があり,そうでない可能性もある。
臨床試験は、GCPに従って合格した研究者の監督の下でヒト被験者に研究製品を服用することを含み、すべての研究被験者に任意の臨床試験への参加についてインフォームドコンセントを提供することを含む。臨床試験は,試験目標を詳細に説明し,安全性をモニタリングするためのパラメータと評価する有効性基準のシナリオで行った。製品開発中に行われる各後続の臨床試験および後続の任意のレジメン修正は、既存のINDに個別に提出されなければならない。また,臨床試験を推奨する各地点の独立IRBは,その地点で臨床試験を開始する前に任意の臨床試験の計画とそのインフォームドコンセントを審査·承認しなければならず,完成まで試験を監視しなければならない。規制当局、IRB、またはスポンサーは、対象が受け入れられない健康リスクに直面していることを発見すること、または試験がその目標を達成する可能性が低いことを含む、様々な理由で臨床試験を随時一時停止することができる。いくつかの試験は、試験のいくつかのデータへのアクセスに基づいて、試験が指定されたチェックポイントで行うことができるかどうかを許可するデータ安全監視委員会と呼ばれる臨床試験スポンサーによって組織された独立した合格専門家グループの監視をさらに含み、被験者に受け入れられない安全リスクまたは他の理由があると判定された場合、治療効果を示さない場合、臨床試験を停止する可能性がある。行っている臨床試験や臨床試験結果を公的登録機関に報告することも求められている。
BLAの承認を得るために,ヒト臨床試験は通常3つの重複可能な連続段階に分けて行われる。
•段階1-研究製品は、健康なヒト対象または標的疾患または状態を有する患者に最初に導入される。これらの研究は、人体内での製品の安全性、用量耐性、吸収、新陳代謝と分布、および用量増加に関連する副作用をテストし、可能な場合に有効性の早期証拠を得ることを目的としている。
•第二段階-初期治療効果、最適用量および用量計画を評価し、可能な不良副作用および安全リスクを決定するために、特定の疾患または状態の限られた患者集団のための製品を研究する。より大規模かつより高価な3期臨床試験を開始する前に、複数の2期臨床試験を行って情報を得ることができる。
•第三段階-製品を拡大した患者群に研究し、用量を更に評価し、臨床治療効果の統計的に意義のある証拠を提供し、そして更に安全性をテストし、通常複数の地理的に分散した臨床試験地点で行われる。これらの臨床試験は研究製品の全体的なリスク/収益比率を確定し、製品の承認に十分な基礎を提供することを目的としている。
場合によっては、FDAは、製品が承認された後に追加の臨床試験を自発的に実施して、製品に関するより多くの情報を得ることを要求する可能性がある。このようないわゆる第4段階研究は“法案”を承認する条件かもしれない。臨床試験と同時に、会社は追加の動物研究を完成させ、候補製品の生物学的特徴に関する追加情報を開発することができ、cGMP要求に基づいて商業量産製品の過程を最終的に決定しなければならない。製造過程は高品質の候補製品ロットを持続的に生産できる必要があり,特に最終製品の特性,強度,品質および純度を試験するための方法を開発する必要があり,あるいは生物製品については安全,純度,効力の試験方法を開発しなければならない。また,適切な包装を選択·テストし,候補製品が賞味期限内に受け入れられない変質が生じないことを証明するために安定性研究を行わなければならない。
BLA提出と審査
すべての適用された法規要件に基づいてすべての要求されたテストが成功したと仮定すると、製品開発、非臨床研究、および臨床試験の結果は、BLAの一部としてFDAに提出され、その製品を1つまたは複数の適応の市場に使用することの承認を要求する。BLAは,否定や曖昧な結果や積極的な発見,製品の化学,製造,制御,アドバイスのラベルなどに関する詳細な情報を含む関連する臨床前および臨床研究から得られたすべての関連データを含まなければならない。BLAを提出するには、免除または免除が適用されない限り、FDAに相当な申請使用料を支払う必要がある。
BLAが提出されると,FDAは提出申請を受けてから10カ月以内に審査基準申請を行い,申請が優先審査資格を満たしていれば,FDAが提出申請を受けてから6カ月以内に審査基準申請を行うことを目標としている。標準審査および優先審査では、FDAがより多くの情報を提供することを要求するか、または明確にすることを要求する要件は、しばしば審査プロセスを大幅に延長する。FDAは、製品が安全で、純粋かつ有効であるかどうか、およびその製造、加工、包装、または保持されている施設が、製品の持続的な安全、純度および効力を保証するための基準に適合しているかどうかを決定するためにBLAを審査する。FDAは諮問委員会を招集し,審査申請について臨床的知見を提供する可能性がある。BLAを承認する前に、FDAは通常、製品を生産する1つまたは複数の施設を検査する。FDAは、製造プロセスおよび施設がcGMP要件に適合していることを決定し、要求された仕様の下で製品が一貫して生産されることを保証するのに十分でない限り、申請を承認しないであろう。さらに、BLAを承認する前に、FDAは、GCPに適合することを確実にするために、通常、1つまたは複数の臨床場所を検査する。FDAが申請、製造プロセス、または製造施設が受け入れられないと判断した場合、それは、提出された文書に不足点を列挙し、追加の試験または情報の提供を要求することが多い。任意の要求された補足情報が提出されたにもかかわらず、FDAは最終的に、その申請が承認された規制基準を満たしていないと決定する可能性がある。
FDAがBLAを評価し、研究製品および/またはその薬物を生産する製造施設を検査した後、FDAは承認状または完全な返信を発行することができる。承認書は、製品の商業マーケティングを許可し、特定の適応に関する具体的な処方情報を提供する。完全な返信は、FDAがBLAで発見されたすべての欠陥を記述するが、FDAが申請をサポートするデータが承認をサポートするのに不十分であると判断した場合、FDAは、必要な検査、試験提出された製品バッチ、および/または提案されたラベルを最初に検討することなく、完全な返信を発行する可能性がある。完全な返信を発行する際に、FDAは、BLAがより多くの情報の提供または明確化を要求することを含む、BLAが承認された条件であるように、申請者がとる可能性のある行動を提案する可能性がある。適用される規制基準を満たしていない場合、FDAは、製品の安全性または有効性を監視するために、追加の試験または情報を要求し、および/または上場後の試験および監視を要求するBLAの承認を延期または拒否することができる。
1つの製品が規制部門の承認を受けた場合、このような承認は特定の適応が付与され、製品が発売される可能性のある指定用途の制限をもたらす可能性がある。例えば、FDAは、製品の利点がそのリスクよりも大きいことを確実にするために、BLAおよびリスク評価および緩和戦略、またはREMSを承認する可能性がある。REMSは、製品に関連する既知または潜在的に深刻なリスクを管理し、そのような薬剤の安全な使用を管理することによって、患者がこれらの薬剤を継続的に得ることを可能にするための安全戦略であり、制限された分配方法、患者登録、および他のリスク最小化ツールのような薬物ガイドライン、医師のコミュニケーション計画、または安全使用を保証する要素を含むことができる。FDAはまた,提案されたラベルを変更したり,適切な制御や仕様を作成したりすることを条件に承認することも可能である.承認されると、発売前と上場後の要求に対する遵守が保たれていない場合、あるいは製品が市場に進出した後に問題が発生した場合、FDAは製品承認を撤回する可能性がある。FDAは
4上場後の製品の安全性及び有効性をさらに評価及び監視するための1つ又は複数の段階4上場後の研究及び監督は、これらの発売後の研究の結果に基づいて製品のさらなるマーケティングを制限することができる。
承認計画を加速する
FDA承認に提出された生物学的上場申請は、優先的な審査および承認の加速など、FDAの審査および承認プロセスを加速することを目的としたFDAの計画の資格に適合する可能性がある。市場で販売されている製品と比較して、製品が重篤な疾患や状況の治療、診断または予防において著しく改善される可能性がある場合、優先審査を受ける資格がある。バイオ製品について、優先審査指定は、FDAの目標が、60日の申請日後6ヶ月以内にマーケティング申請に行動することであることを意味する(一方、標準審査では10ヶ月)。
さらに、重篤または生命を脅かす疾患または状態の安全性および有効性を治療するために研究された製品は、臨床的利益を合理的に予測する可能性のある代替終点、または不可逆的な発病率または死亡率の前に測定可能な臨床終点、不可逆的な発症率または死亡率または他の臨床的利益を合理的に予測することができる臨床終点に対して有効であることを決定する際に、病状の重症度、希少性または流行度、および代替治療の利用可能性または不足を考慮しながら、加速承認を得ることができる。承認を加速する条件として、FDAは通常スポンサーに十分かつ良好な制御を行う上場後の臨床研究を要求し、不可逆的な発病率或いは死亡率或いは他の臨床利益に対する期待影響を検証と記述する。また、FDAは現在、承認を加速させる条件として宣伝材料を事前承認することを求めており、製品商業発売の時期に悪影響を及ぼす可能性がある。
優先審査と承認加速は承認の基準を変えることはないが、開発や承認過程を加速させる可能性がある。
孤児薬名
孤児医薬品法によれば、FDAは、米国では20万人未満に影響を与えるか、または米国では20万人を超える影響を与える稀な疾患または疾患を治療するための薬剤または生物に孤児の称号を付与することができるが、米国では、そのような疾患または疾患を治療する薬剤または生物薬剤を米国で開発および提供するコストが、米国での薬剤または生物学的薬剤の販売から回収されることを合理的に予想することができない。BLAを提出する前に,指定孤児薬を申請しなければならない。FDAが孤児薬物指定を承認した後、FDAは、治療薬の模倣薬識別情報およびその潜在的孤児の使用を開示する。孤児薬物の指定は、規制審査または承認過程においていかなる利点も伝達されず、規制審査または承認過程の持続時間を短縮することもない。
孤児薬物指定を有する製品がその後、このような指定された疾患に対するFDAの最初の承認を得た場合、この製品は、孤児薬物の独占的承認(または排他性)を得る権利があり、これは、FDAが完全なBLAを含む他の出願を承認しない可能性があり、限られた場合、例えば孤児薬物に対して排他性を有する製品に対する臨床的利点を示さない限り、7年以内に同じ薬物または生物学的薬剤を販売することを意味する。孤児薬物排他性は、FDAが同じ疾患または状態に対する異なる薬物または生物学的製剤、または異なる疾患または状態に対する同じ薬物または生物学的製剤を承認することを妨げるものではない。孤児薬物を指定する他の利点は、いくつかの研究の税金相殺およびBLA申請料の免除を含む。
指定された孤児薬物が孤児が指定された適応よりも広い用途で承認された場合,孤児薬物の排他性を得ることはできない。さらに、FDAが指定された要求に重大な欠陥があると後に判断した場合、または製造業者がこのような稀な疾患または疾患患者の需要を満たすのに十分な数の製品を保証できない場合、米国での独占営業権を失う可能性がある。
突破的治療指定
画期的な治療計画の資格を得るためには、候補製品は深刻な或いは生命に危害を及ぼす疾患或いは状況の治療に使用されなければならず、初歩的な臨床証拠は、これらの候補製品が1つ以上の臨床顕著な終点で既存の治療法よりも著しく改善されている可能性があることを示しなければならない。FDAは画期的な治療製品候補のスポンサーが以下の方面の深い指導を得ることを確保するために努力する:高効率薬物開発計画の密集指導、高度管理者と経験豊富な従業員の積極的、協力と学際的審査への密集参加、および転動審査。画期的な治療指定は承認の基準を変えることはないが,開発や承認過程を加速させる可能性がある。
承認後に要求する
我々は、FDAによって製造または流通を許可されたどの製品も、記録保存、有害事象報告、定期報告、製品サンプリングおよび流通、ならびに製品の広告および販売促進に関連する要件を含むFDAによって普遍的かつ持続的に規制されている。承認後、承認された製品の大多数の変更は、新たな適応または他のラベル宣言を追加するなど、FDAの事前審査および承認を経なければならない。継続的なユーザ料金要求もあり,この要求に基づいて,FDAは承認されたBLAで決定された製品ごとの年間計画費用を評価する.生物製造業者およびその下請け業者は、FDAおよびある州機関に彼らの機関を登録し、FDAおよび特定の州機関の定期的な抜き打ち検査を受けて、cGMPのコンプライアンスを理解しなければならない。これは、私たちと私たちの第三者製造業者にいくつかの手続きと文書要求を加えている。製造プロセスの変更は厳しく規制されており,変更の重要性により,FDAが事前に承認して実施する必要がある可能性がある。FDAの規定はまた、cGMPから外れた状況を調査·是正し、私たちと私たちが使用を決定する可能性のある任意の第三者メーカーに報告することを要求している。そのため、メーカーは生産と品質管理の分野で時間、お金、精力をかけ続け、cGMPやその他の法規遵守性を維持しなければならない。
規制要件や基準が守られていない場合、あるいは製品発売後に問題が発生した場合、FDAは承認を撤回する可能性がある。その後、予想されていなかった重症度または頻度の副作用、または生産プロセス、または規制要件を遵守できなかったことを含む、以前に未知の製品問題が発見され、新しいセキュリティ情報を追加するために承認されたラベルの改訂をもたらす可能性がある;新しい安全リスクを評価するために発売後研究または臨床研究を実施すること、またはREMS計画に従って流通制限または他の制限を実施することが可能である。他の他の潜在的な結果には
•製品の販売または製造を制限し、市場から製品を完全に撤退させるか、または製品をリコールすること
•承認後の臨床研究には罰金、警告状、放置を科す
•FDAは、承認されるべき出願の承認または承認された出願の追加を拒否するか、または既存の製品の承認を一時停止または撤回する
•製品が差し押さえられたり、差し押さえられたり、FDAが製品の輸出入を許可することを拒否したり;
•民事または刑事処罰を禁令または適用する。
FDAは生物製品のマーケティング、ラベル、広告、販売促進を厳格に規制している。1社はFDAが承認したラベルの規定に基づいて、安全性と有効性、純度、効力に関する声明しか提出できない。FDAと他の機関は非ラベル用途の普及を禁止する法律法規を積極的に施行している。これらの要求を守らないことは、否定的な宣伝、警告状、改正広告、および潜在的な民事と刑事罰を招く可能性がある。医師は、製品ラベルに記載されていない使用のための合法的に入手された製品の処方、および我々が試験およびFDAによって承認された用途とは異なる使用を行うかもしれない。このようなラベル外の使用は医学専門科でよく見られる。医師は,異なる場合,このような非ラベル使用が多くの患者の最適な治療法であると考えるかもしれない。FDAは医者が治療を選択する時の行動を規範化しない。しかし、FDAは製品ラベルの外使用問題に対する製造業者のコミュニケーションを制限した。
生体模倣薬と参考製品の排他性
2010年に法律として署名された“患者保護および平価医療法案”またはACAと総称される“患者保護および平価医療法案”は、2009年の生物製品価格競争および革新法案、またはBPCIAと呼ばれる副題を含み、FDAによって承認された参考生物製品生物と類似または交換可能な生物製品のための短い承認経路を作成する。これまで、いくつかの生物模倣薬はBPCIAによって許可され、多くの生物模倣薬はすでにヨーロッパで承認された。FDAはすでにいくつかの指導文書を発表し,生体模倣薬の審査·承認方法について概説した。
生物類似性とは生物製品と参照製品が安全性、純度と効力の面で臨床的に意義のある差異がなく、分析研究、動物研究と臨床研究によって証明できることである。互換性は、製品が基準製品生物と類似していることを必要とし、この製品は、任意の所与の患者において、参照製品と同じ臨床結果を生成することが期待できることを証明しなければならず、複数回投与された製品の場合、以前の投与後、生物および参照生物は、安全リスクを増加させることなく、または参照生物の独占的使用と比較して治療効果のリスクを低下させることなく、交互にまたは交換することができる。生物製品がもっと大きく、よくもっと複雑な構造に関連する複雑性、及びこのような製品を製造する技術は、FDAがまだ制定している簡略化審査経路の実施に対して重大な障害を構成した。
BPCIAによると,生物類似製品の申請は,参考製品が初めてFDA許可を得た4年後にFDAに提出されなければならない。また,FDAによる生物類似製品の承認は,参考製品が初めて許可された日から12年後に発効する可能性がある。この12年間の独占期間内に、FDAが競合製品の完全なBLAを承認した場合、出願人自身の臨床前データと、その製品の安全性、純度および有効性を証明するために、十分かつ良好に制御された臨床試験からのデータとを含み、別の会社は、参照製品の競合バージョンを販売する可能性がある。BPCIAはまた、交換可能な製品として承認された生物模倣薬のためのいくつかの排他的期限を設けている。この節では,FDAが“交換可能”と考えている製品が本当に州薬剤法に管轄されている薬局に取って代わられるかどうかは不明である。
BPCIAは複雑であり、FDAによって解釈され、実施され続けている。また、政府の最近の提案は12年間の参考製品専門期間を短縮しようとしている。BPCIAの他の面では,そのいくつかがBPCIAの排他的条項に影響を与える可能性があり,最近の訴訟のテーマでもある.したがって,BPCIAの最終的な影響,実行,影響は重大な不確実性の影響を受ける。
連邦と州の詐欺と乱用、データプライバシーと安全、透明性の法律法規
FDAの薬品マーケティングに対する制限以外に、連邦と州医療保健法律法規は生物製薬業界の商業行為を制限する。他の事項に加えて、これらの法律は、私たちの臨床研究活動および提案された販売、マーケティング、および教育計画を含む、私たちの現在および将来の業務運営に影響を与える可能性があり、マーケティング、販売および流通を通じてマーケティングによって承認された製品の業務または財務スケジュール、ならびにヘルスケア提供者および他の当事者との関係を制限することができる。これらの法律には、リベートおよび虚偽宣言法律法規、データプライバシーおよびセキュリティ、および透明性法律が含まれていますが、以下の法律に限定されません。
連邦反リベート法規は、個人または実体が知られている場合、直接または間接的に、現金または実物の形態で直接または間接的に現金または実物の形態で提供、支払い、請求または報酬を受けて、購入、レンタル、注文または手配または推薦購入、レンタルまたは推奨購入、レンタルまたは注文を誘導または見返りに、Medicare、Medicaid、または他の連邦医療計画に従って精算可能な任意の物品またはサービスを注文することを禁止する。“報酬”という言葉は価値のあるものを含むと広く解釈されている。連邦反リベート法規は、薬品メーカーと処方者、購入者、および処方マネージャーの間の手配に適用されると解釈される。いくつかの法定例外状況と規制安全港保護のいくつかの一般的な活動は起訴されないが、例外状況と安全港の範囲は狭い。報酬に関するアプローチは、例外または避難港の資格に適合していない場合、処方、購入、または推薦を誘導するために告発される可能性があるため、審査される可能性がある。
さらに、個人またはエンティティは、この法規またはその法規に違反する具体的な意図を実際に知る必要がなく、違反行為を実施することができる。また、政府は、連邦反リベート法規違反による物品やサービスのクレームを含め、“虚偽請求法”や民事罰金法規については、虚偽または詐欺的クレームを構成していると断言することができる。
“虚偽請求法”を含む連邦民事および刑事虚偽請求法は、他の事項に加えて、任意の個人または実体が故意に連邦政府に虚偽請求を提出するか、または虚偽請求を意図的に連邦政府に提出し、使用するか、または虚偽または詐欺的クレームの作成または使用に重要な意味を有する虚偽記録または陳述を作成または使用することを禁止する。クレームには、米国政府に提出された金銭または財産に対する“任意の請求または要求”が含まれている。これらの法律により、いくつかの製薬会社や他のヘルスケア会社が起訴され、顧客に製品を無料で提供する疑いがあるため、顧客がその製品の連邦計画に料金を請求することを希望している。未承認の用途に製品を売り込んで虚偽申告したとして起訴された会社もあるため、精算できない。
1996年の連邦健康保険携行性と責任法、またはHIPAAは、個人第三者支払人を含む追加の連邦刑法を制定し、任意の医療福祉計画を知りながら故意に詐欺計画を実行することを禁止し、重大な事実を偽造、隠蔽または隠蔽し、または医療福祉、プロジェクトまたはサービスの交付または支払いに関連するいかなる重大な虚偽、架空、または詐欺的な陳述を行うことを含む。連邦反リベート法規と同様に、個人または実体は、この法規やこの法規に違反する具体的な意図を実際に知る必要がなく、違反を実施することができる。
HIPAAは、“経済·臨床健康情報技術法案”(HITECH)及びそのそれぞれの実施条例改正後、特定の健康計画、医療情報交換所、および特定の医療保健提供者(保険エンティティと呼ぶ)およびそれらのそれぞれの業務パートナー、個人が識別可能な健康情報を使用または開示することに関連する特定のサービスを実行する独立請負業者、およびそれを含む
保証下請け業者。HITECHはまた新しい民事罰金等級を作成し、HIPAAを改訂し、民事と刑事処罰を商業パートナーに直接適用し、州総検察長に新しい権力を与え、連邦裁判所に民事訴訟を提起し、損害賠償または禁制令を要求してHIPAAを実行し、連邦民事訴訟の提起に関連する弁護士費と費用を求めることができる。
連邦医師支払いサンシャイン法案は、連邦医療保険、医療補助または児童健康保険計画に基づいて支払うことができるいくつかの薬品、器具、生物製品および医療用品の製造業者が、連邦医療保険および医療補助サービスセンター(CMS)に毎年、医師(医師、歯科、検眼師、足科医師および脊椎マッサージ師を含む)、他の保健専門家(例えば、医師アシスタントおよび看護師従業員)、他の医療保健専門家(例えば、医師アシスタントおよび看護師従業員)、教育病院および適用されるメーカーおよび適用される団体購入組織に、医師およびその直系親族の所有権および投資利益に関する情報を毎年CMSに報告することを要求する。
私たちはまた、上記の各連邦法律に相当する州および外国の法律によって制限される可能性があり、州法律は、製造業者に医師および他の医療保健提供者への支払いおよび他の方法での価値またはマーケティング支出に関する情報を報告することを要求する州法律、製薬会社に製薬業界の自発的コンプライアンスガイドラインおよび連邦政府によって発行された関連コンプライアンスガイドラインを遵守すること、または他の方法で医療保健提供者への支払いを制限することを要求する州法律、州および地方法律は、医薬品販売代表の登録を要求する。また、健康情報のプライバシーや安全を管理する国や外国の法律もあり、その多くの法律は互いに大きく異なり、HIPAAに先を越されず、コンプライアンス作業を複雑にしていることが多い。
私たちが第三者の業務配置と適用される医療法律や法規に適合するように努力することは、多くのコストに関連することを確実にします。これらの法律の広汎性、および既存の法定例外状況と安全港の規制の狭さのため、私たちのいくつかの商業活動は1つ以上のこのような法律の挑戦を受けるかもしれない。政府当局は、私たちの業務実践が現在または未来に適用される詐欺および乱用または他の医療保健法律および法規に関連する現行または未来の法規、法規または判例法に適合していない可能性があると結論するかもしれない。もし私たちの運営がこれらの法律または任意の他の私たちに適用される可能性のあるいかなる政府法規に違反していることが発見された場合、私たちは重大な民事、刑事と行政処罰、損害賠償、罰金、返還、監禁、MedicareおよびMedicaidなどの政府援助に参加する医療計画から除外され、追加の報告要件および監督に直面する可能性があり、もし私たちが会社の誠実な合意または同様の合意の制約を受けて、これらの法律違反に関する告発、契約損害、名声損害、および私たちの業務の削減または再編を解決する。もし私たちのいかなる製品が海外で販売されている場合、私たちは同様の外国の法律法規の制約を受けることができます。その中には、例えば、安全監視、詐欺防止、法律の乱用、企業コンプライアンス計画の実施、医療保健専門家への支払いまたは価値移転を含む適用された発売後の要求が含まれている可能性があります。
私たちはまた、外国の実体のいかなる行為や決定に影響を与え、個人または企業が業務を獲得または保留するのを助けるために、いかなる米国の個人または企業がいかなる外国の官僚、政党または候補者に直接または間接的に支払い、提供または許可支払い、または任意の価値のあるものを提供することを禁止する“米国反海外腐敗防止法”または“海外腐敗防止法”のような他の連邦法律を遵守しなければならない。“海外腐敗防止法”はまた、証券が米国に上場している会社に会計規定を遵守し、会社(国際子会社を含む)のすべての取引の帳簿や記録を正確かつ公平に反映し、国際業務のために適切な内部会計制御制度を制定·維持することを要求している。多くの他の国では、薬を処方した医療提供者はその政府に雇われており、薬品の購入者は政府の実体である;そのため、私たちはこれらの処方者と購入者との取引は“海外腐敗防止法”によって規制される。“海外腐敗防止法”に違反した活動は、米国以外で完全に発生しても、刑事や民事、罰金、監禁、返還、監督、政府契約の資格取り消しを招く可能性がある。
保証と精算を請け負う
市場のいかなる薬品の受け入れと販売はある程度保証範囲と第三者支払人が薬品に十分な補償を提供する程度に依存し、第三者支払人は政府衛生行政部門、管理保健組織とその他の個人健康保険会社を含む。私どもの製品の保証と精算はテカグレルや反転剤としてベンゼン曲美モノクロナル抗体を使用したプログラムの保証と十分な精算にも依存しています。医師の監督下で投与される価格が高いため、私たちの製品のために保険と十分な補償を得ることは特に難しいかもしれない。製品自体や私たちの製品を使用した治療やプログラムについては、単独での精算は提供されない可能性があります。我々の製品を使用する手術を引き受けても,第三者支払者は薬のコストを手術支払いに梱包することができ,我々の製品に関する費用を医師に単独で精算することはない。第三者支払人が保証を受けないか、単独で私たちの製品を清算することを決定すれば、承認されると、医者の私たちの製品に対する使用を減らすことができるかもしれません。またアメリカでは
第三者支払者の間で統一的な保証と精算政策を実施する。第三者支払者が自己の保険·精算政策を設定する際には,通常連邦医療保険引受政策と支払制限に依存する。しかしながら、提供される補償範囲および金額に関する決定は、支払者1人ずつに基づいて行われる。1人の支払人が1つの薬品に保険を提供することを決定し、他の支払者も保険と適切な補償を提供することを保証することはできない。
第三者支払者は彼らがどのような医療手続きをカバーし、精算レベルを確立するかを決定する。第三者支払者が特定の手続きを担っていても、それによる精算支払率が十分高くない可能性がある。ある疾患でオフィスで治療を受けている患者は,通常第三者支払者によってその手続きに関連する費用の全部または一部を精算しており,このような保険や十分な精算がなければ,このような手続きを受け入れたくないかもしれない。
第三者支払者の精算は、第三者支払人が安全、有効かつ医学的に必要であることを決定すること、特定の患者に適していること、費用効果があること、同業者によってレビューされた医学雑誌の支持を得ること、臨床実践ガイドラインに含まれること、および美容的でもなく、実験的でもなく、研究的でもないことを含む多くの要素に依存する可能性がある。
また、第三者決済者は通常、毎年時々支払率を更新して修正する。このような更新は私たちの候補製品に対する需要に影響を与える可能性があり、お客様が私たちの候補製品に指定され、承認されれば、候補製品の費用を単独で精算することはありません。支払い更新の一例は,Medicare計画が医師の支払いを更新することであり,この計画は年に1回完成する。過去、この式を適用して支払い額が低くなった場合、国会は臨時立法で支払いの減少を防止していた。2015年の“連邦医療保険アクセスとチップ再認可法案”は法定式の使用を終了し,連邦医療保険医に功績に基づくインセンティブボーナス計画を導入し,品質支払い計画とも呼ばれている。この計画は,高度な代替支払いモード(APM)と功績に基づくインセンティブ決済システム(MIPS)を含む臨床医に2つの参加方式を提供する。2019年11月、CMSは最終ルールを発表し、最終的に品質支払い計画の変化を決定した。品質支払い計画の導入が全体の医師精算に与える全面的な影響はまだ不明である。連邦医療保険や他の政府が計画している精算のいかなる減少も、個人支払者の支払いの同様の減少を招く可能性がある
医療改革が私たちの業務に与える影響
アメリカと一部の外国司法管轄区では、医療保健システムに関するいくつかの立法と監督管理の変化及び提案された変化が継続され、これらの変化は候補薬品の発売承認を阻止或いは延期し、承認後の活動を制限或いは規範化し、候補薬品の利益の販売に影響を与える可能性がある。
米国や他の地方の政策立案者や支払者の中で,医療システムの改革を推進することに大きな興味があり,医療コストの抑制,質の向上および/または参入拡大を既定の目標としている。米国では、製薬業はこれらの努力の重点であり、重大な立法計画の大きな影響を受けてきた。2010年3月,ACAが採択され,政府や民間保険会社が医療に融資する方式を大きく変更し,米国製薬業に大きな影響を与えた。他の事項以外にも、ACAは製薬と生物技術業界にとって特に重要な条項を含み、連邦医療保健計画の登録を管理する条項を含むが、医療補助薬品リベート計画に基づいてメーカーが医療補助薬品リベート計画に基づいて借りたリベートを計算する新しい方法と、連邦ヘルスケア計画における製薬会社の販売シェアに基づいて年会費を計算する。
ACAのいくつかの側面は行政、司法、そして国会の挑戦を受けている。国会はまだ全面的な廃止立法を通過していないが、ACAの下の特定の税収実施に影響を与える法案は署名されて法律となっている。2017年の減税·雇用法案、または税法は、2019年1月1日に施行されたACAが、1年の全部または一部で合格医療保険を維持できなかった個人の税収ベースの分担責任支払いを廃止する条項を含み、これは一般に“個人強制”と呼ばれる。また,2020年1月1日から2020年の連邦支出案が永久的に廃止され,ACAが規定している雇用主支援の高コスト医療保険や医療機器税に対する“キャデラック”税や,2021年1月1日からも医療保険会社税が廃止された。2018年に両党予算法案、あるいはBBAなどが改正され、ACAが改正され、2019年1月1日から施行され、多くの連邦医療保険薬物計画におけるカバーギャップを埋めるために、通常“ドーナツ穴”と呼ばれている。2021年6月17日、米国最高裁は、ACAが“個人権限”が国会で廃止されたため、全体的に違憲だと弁明する手続き理由に基づく挑戦を却下した。したがって、ACAは現在の形態で継続的に有効であるだろう。米国の最高裁が裁決を下す前に、総裁·バイデンは2021年1月28日に行政命令を発表し、ACA市場を通じて医療保険を得ることを目的とした特殊な保険加入期間を開始した。この行政命令はまた、特定の政府機関に、医療を受けることを制限する既存の政策および規則を検討し、再検討することを指示する
その中には,医療補助モデルプロジェクトの再審査や免除計画,作業要求,医療補助やACAによる医療保険カバーの獲得に不必要な障害を与える政策が含まれている。ACAは未来に司法や国会で挑戦される可能性がある。これらの挑戦やバイデン政府の医療改革措置がACAと我々の業務にどのように影響するかは不明である。
ACAが公布されて以来、他の立法改正も提案され、採択された。これらの変化には、2013年に開始された2011年の予算制御法案によると、提供者に支払われる医療保険支払い総額を2%削減することが含まれており、その後の法案の立法改正により、BBAやインフラ投資、雇用法案が含まれているため、追加の国会行動が行われない限り、2031年まで有効となる。しかし、新冠肺炎救済立法は2020年5月1日から2022年3月31日までこれらの減免を一時停止した。現在の立法によると、医療保険支出の実質減幅は2022年の1%から本自動減額の最終年度の3%まで様々になる。2012年の“米国納税者救済法”などの法案は,病院や癌治療センターを含むいくつかの医療サービス提供者に支払う連邦医療保険をさらに減少させ,政府が医療サービス提供者に多額の金を取り戻す訴訟時効を3年から5年に延長した。これらの新しい法律は、連邦医療保険や他の医療資金のさらなる減少を招く可能性があり、承認されれば、私たちの候補製品の顧客や私たちの財務運営に悪影響を及ぼす可能性がある。
また、処方薬や生物製品価格の上昇を受けて、米国政府は薬品定価のやり方の審査を強化した。このような審査は,最近の数回の国会調査を招き,製品定価の透明性の向上,価格設定とメーカー患者計画との関係の審査,政府計画の製品精算方法の改革を目的とした連邦や州立法を提案·採択した。連邦レベルでは、トランプ政権はいくつかの手段を用いて、連邦予算提案、行政命令、政策措置を含む薬品定価改革を提出または実施している。例えば、2020年7月24日と2020年9月13日に、トランプ政権は処方薬の定価に関するいくつかの行政命令を発表し、政府のいくつかの提案を実施しようとしている。そのため、FDAは2020年9月に最終規則と指導意見を同時に発表し、各州がカナダからの薬物輸入計画の制定と提出に道を提供した。また、2020年11月20日、米国衛生·公衆サービス部(HHS)は、製薬業者から連邦医療保険D部分下の計画スポンサーへの値下げ安全港保護を廃止し、法律が値下げを要求しない限り、直接または薬局福祉マネージャーを通過する規定を決定した。バイデン政権は、現在行われている訴訟に対応するため、この規則の実施を2022年1月1日から2023年1月1日に延期した。この規定はまた、販売時点での値下げを反映するための新しい避難港を創出し、薬局福祉マネージャーとメーカーとの間のいくつかの固定費用スケジュールのための新しい避難港を創出し、これらの計画の実施も2023年1月1日に延期される。2020年11月20日, CMSは、ある医師が管理する薬物の連邦医療保険B部分支払いを他の経済先進国が支払う最低価格にリンクさせ、2021年1月1日から発効するトランプ政権の最恵国行政命令を実施する臨時最終規則を発表した。最恵国モデルに挑戦した訴訟の結果,CMSは2021年12月27日に最終ルールを発表し,最恵国モデル仮最終ルールを廃止した。2021年7月、バイデン政府は“米国経済における競争を促進する”という行政命令を発表し、その中には処方薬に対する条項が複数ある。総裁·バイデンの行政命令に応えるために,2021年9月9日,厚労省は“高薬価に対応した総合案”を発表し,薬品定価改革の原則を概説し,国会がとりうる様々な潜在的立法政策と,衛生·公衆サービス部がとりうる潜在行政行動を示し,これらの原則を推進した。このような原則を施行するための立法や行政行動はまだ最後に決定されていない。国会では,医薬品定価を他の医療改革の一部とすることも考えられている。このようなまたは似たような政策計画が未来に施行されるかどうかはまだ分からない。州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入の制限、マーケティングコスト開示および透明性措置を含む、医薬品および生物製品の価格設定を制御するための法規を立法および実施することが増えており、場合によっては、他の国からの輸入および大量購入を奨励することを目的としている。また、政府は新冠肺炎の流行に対応するためにより多くの行動をとる可能性がある。
法規を付加する
アメリカと私たちが運営している他の管轄区では、環境、人間の健康と安全の保護に関連する様々な連邦、州、地方法律法規を遵守しています。もし私たちがこのような法律に違反したら、私たちは規制機関の罰金、刑事告発、または他の制裁を受けるかもしれない。環境法律法規は複雑で変化が頻繁であり,時間の経過とともにより厳しくなっている。私たちは私たちの業務が現在すべての実質的な側面で適用された環境法律と規制に適合していると信じている。
従業員と人的資本
2021年12月31日現在、私たちは60人の従業員がいて、すべて常勤社員です。私たちの従業員はみんなアメリカにいます。私たちの従業員の中の一人も労働組合代表でもなく、集団交渉協定のカバー範囲もない。私たちは私たちが従業員と仲がいいと思う。
私たちの人的資本資源目標には、適用、識別、採用、維持、インセンティブ、そして私たちの既存の、より多くの従業員を統合することが含まれています。私たちの株式激励計画の主な目的は株式に基づく報酬奨励を授与することによって、選定した従業員、顧問と取締役を吸引、維持と激励することである。
企業情報
私たちは2002年1月にデラウェア州の法律に基づいて登録された。私たちの主な行政事務室はペンシルバニア州マルヴィン30号スイートルーム1 Great Valley Parkwayにあります。郵便番号:19355です。私たちの電話番号は(610)981-6500です。私たちの普通株はナスダック世界市場に上場し、コードは“PHAS”です
利用可能な情報
私たちのインターネットサイトはWwwww.phaseBio.comそれは.本年度報告に含まれている情報のほかに、私たちのサイトで私たちに関する情報を見つけることができます。私たちのウェブサイトとウェブサイトに含まれているか、またはリンクされている情報は、本年度報告の構成要素ではありません。
我々のForm 10-K年次報告、Form 10-Q四半期報告、Form 8-K現在の報告、および1934年の証券取引法第13(A)または15(D)条に基づいて提出または提出(改正された)これらの報告の修正案は、米国証券取引委員会または米国証券取引委員会に電子的に提出された後、合理的で実行可能な範囲内でできるだけ早く私たちのサイトを通じて無料で取得することができる。米国証券取引委員会は、報告書、依頼書、情報声明、その他の情報を含むインターネットサイトを有している。アメリカ証券取引委員会のサイトの住所はWwwv.sec.gov.
第1 A項。リスク要因です
以下の情報は,我々の実際の結果と,本Form 10−K年次報告で行われた前向きな陳述と,我々が時々行う可能性のある前向きな陳述に含まれるリスク要因について述べる。本Form 10-K年次報告および我々の他の公開申告文書に含まれる他の情報に加えて、以下に説明するリスクをよく考慮しなければなりません。私たちの業務、財務状況、または経営結果はこのような危険な損害を受けるかもしれない。以下に説明するリスクと不確実性は私たちが直面している唯一の危険と不確実性ではない。私たちが現在知らない他のリスクや私たちが現在意識していない他の要素は私たちの業務に重大なリスクとなり、私たちの業務運営を損なう可能性もあります。
リスク要因の概要
私たちの業務は多くのリスクに直面していて、私たちの普通株に投資することを決定する前に、あなたはこのようなリスクを認識しなければならない。これらのリスクは、本“リスク要因”の節でより全面的に説明されている
•現在行われている新冠肺炎の大流行は,われわれの臨床試験を含めて我々の業務や運営に悪影響を与え続けている可能性がある。
•設立以来、私たちは大きな損失を受けた。私たちは今後数年間赤字になると予想していて、決して達成されたり利益を維持したりしないかもしれない。
•私たちは、継続的に経営する企業として、私たちの財務義務を履行し、私たちの業務目標を達成するために、大量の追加資金が必要になるだろう。もし私たちが必要な時に資金を集めることができなければ、私たちは計画中の業務の削減と成長戦略の追求を迫られるかもしれない。
•監査人は、2021年12月31日までの財政年度に監査された財務諸表に対する私たちの意見が、このForm 10-K年度報告書に含まれている説明的段落に含まれており、持続的な経営企業としての私たちの経営継続能力に対する私たちの深刻な疑いに触れている。また、SFJプロトコルによれば、SFJプロトコルで規定されている期間内に継続的な経営状況を修復しなければ、bentracimabが商業化された任意の収入を共有する能力が大きな悪影響を受けることになり、SFJは、bentracimabに関連する業務をSFJに移行することを選択することができる。もし私たちが現在の運営計画を支援するために追加の資金を得ることができなければ、私たちは私たちの開発計画の範囲を延期または縮小し、および/または私たちの運営を制限または停止させることを余儀なくされるかもしれない。
•もし私たちがbentracimabに対する規制機関の承認を得た場合、あるいはSFJプロトコルが終了した場合、SFJプロトコルに従ってSFJに大量のお金を支払うことを要求される。もし…
私たちの業務にはSFJプロトコルの下での支払い義務を履行するのに十分な資金やキャッシュフローがありません。SFJは私たちの資産の優先保証権益の保持者としてその救済措置を行使する可能性があり、私たちの業務は大きな損害を受ける可能性があります。
•もしアルファシマが私たちと彼らとの合意で規定された義務を履行しない場合、あるいは彼らが私たちと彼らのパートナー関係を終了した場合、私たちは計画通りに私たちの協力候補製品を商業化することができないかもしれません。私たちがその合意から得た予想収入は大きな影響を受けるかもしれません。
•私たちは現在1つの臨床段階の候補製品、フェニルトラシズマブ、1種のチカグレル或いは反転剤しかない。もし私たちが開発に成功し、監督部門のbentracimabの承認を得て商業化することができない場合、あるいは他の候補製品の開発に成功できない場合、あるいは開発過程で重大な遅延に遭遇した場合、私たちの業務は損なわれるだろう。
•FDAからのフィードバックによると、承認手続きを加速させることで、米国でbentracimabの規制承認を求める予定だ。もし私たちがこの過程で成功できなければ、フェニトラシズマブの開発と商業化は延期され、放棄され、あるいはもっと高価になるかもしれない。
•著者らは時々発表或いは公表した臨床試験の一時的な“頂線”と初歩的な結果はより多くの患者データの獲得に伴い変化する可能性があり、そして監査と検証プログラムの影響を受け、これは最終データの重大な変化を招く可能性がある。
•臨床前研究或いは早期臨床試験の成功は未来の臨床試験の結果を予測できないかもしれない。
•組織として、私たちは重要な臨床試験を完成したことがなく、私たちは私たちが開発する可能性のあるすべての候補製品の臨床試験を完成できないかもしれない。
•ELPは新しい技術であり、開発の時間、リスク、コストを予測し、その後、私たちのELP候補製品の監督管理許可を得る能力を得ることを困難にした。
•私たちは、既存の候補製品のためにより多くの適応を求めること、または許可を得ること、または他の疾患のより多くの候補製品を得ることを含む、候補製品チャネルを増加させる努力は成功しないかもしれない。
•Bentracimabの市場受容度は,承認されれば,テカグレルの継続的な受け入れと使用に大きく依存するであろう。
•もし私たちが発売許可を得たら、私たちは現在、引き続き第三者生産ベントラマズマブ、PB 6440、その他の私たちが臨床開発と商業製造に使用する可能性のある候補製品に依存し、引き続き依存すると予想される。このような第三者への依存は、許容可能なコストで十分な数の候補製品またはそのような数を得ることができないリスクを増加させ、私たちの開発または商業化努力を延期、阻止、または損害する可能性がある。
•もし私たちが私たちの候補製品に関連する知的財産権を獲得または保護できなければ、私たちは私たちの市場で効果的に競争することができないかもしれない。
•SFJプロトコルおよびAlfasigma再許可を含む現在および将来の知的財産権許可および第三者との融資スケジュールで義務を履行できなければ、私たちは私たちの業務に重要な権利を失う可能性があります。
•私たち普通株の取引価格はすでに不安定である可能性があり、私たち普通株を購入した人は大きな損失を受ける可能性があります。
私たちの財務状況と資本需要に関連するリスク
現在行われている新冠肺炎の大流行は,われわれの臨床試験を含めて我々の業務や運営に悪影響を与え続けている可能性がある。
私たちの業務運営は持続的な新冠肺炎の大流行の影響を受け続ける可能性がある。米国、州、地方政府は、米国各地の州と地方命令を含む疾患およびその変種の伝播を減少させるために、将来的に旅行およびその他の制限を実施することが可能であり、他の以外にも、個人にその居住地での避難を指示し、企業および政府機関に物理的な場所での不必要な行動を停止するように指示し、いくつかの不要な集会や活動を禁止し、医療スタッフを強制する
ワクチンを全面的に接種し、不必要な旅行を中止するように命じた。いくつかの制限の緩和に伴い、限られたビジネス旅行を含むいくつかの活動を再開し、従業員の仕事の職責に応じて適切な対面作業を可能にする混合作業環境を実施した。私たちのオフィスを再開放することは、私たちの従業員を健康リスクに直面させ、関連する責任を負うことができ、追加のリスクと運営挑戦が生じる可能性があり、新しい職場の健康と安全協定の設計、実施、実行に追加投資を要求する可能性があります。多くの従業員が遠隔作業や対面と遠隔作業の混合を継続することが予想され、これは、運営と職場文化の挑戦、オフィス空間需要の不確実性、ネットワーク攻撃を受けやすいことを含む、私たちの業績に影響を与える可能性のあるリスク、不確実性、コストをもたらす。
私たちは新しい冠肺炎の大流行が私たちの業務と臨床試験の中断に深刻な影響を与える可能性があることを経験し続けているかもしれません
•私たちが行っている臨床試験に参加する患者の募集を遅延、困難、または一時停止します
•臨床現場の起動遅延、困難或いは一時停止は、臨床現場調査員と臨床現場スタッフの募集の困難を含む
•私たちは試験製造と薬品供給の能力を中断しました
•医療資源を臨床試験の進行から移し,われわれの臨床試験場所である病院や臨床試験を支援してくれた病院スタッフを他の場所に移すことを含む
•臨床試験場所の監視、および連邦または州政府、雇用主および他の人によって課せられたまたは提案された旅行制限のために、被験者が試験場所に行く能力があるか、または試験場所に行きたい、などの重要な臨床試験活動を中断する;
•従業員資源の制限は、そうでなければ、医療関係者に対するワクチン要求、従業員またはその家族の疾患または従業員の選択が大勢との接触を避けたいことを含む、我々の臨床試験の進行に集中する。
われわれが新冠肺炎の影響が進行している国·地域で計画されている臨床試験では,上記のリスクに加えて,以下のような悪影響を経験し続ける可能性がある
•私たちが計画した臨床試験を開始するために地元の監督部門の許可を得ています
•臨床試験に必要な用品や材料の受信を遅延させた
•世界的な輸送中断は、私たちの臨床試験で使用されている研究医薬製品のような臨床試験材料の輸送に影響を与える可能性がある
•新冠肺炎の流行に対応する一部として、現地の法規の変化は私たちが臨床試験を行う方法を変える必要があるかもしれません。これは予期せぬコストを招き、あるいは臨床試験を完全に停止する可能性があります
•従業員資源が限られているか、あるいは政府従業員が休暇を余儀なくされたため、現地の監督機関、道徳委員会および他の重要な機関と請負業者との必要な相互作用が遅延した
•FDAはこれらの影響を受けた地域の臨床試験データの受け入れを拒否した。
著者らは現場活性化と患者登録を通じて著者らのbentracimab臨床計画を推進することに伴い、著者らはずっと著者らの臨床研究組織或いはCRO、臨床場所とサプライヤーと密接な関係を維持し、新冠肺炎が著者らの臨床試験と現在のスケジュールに与える影響を評価することを試み、そして著者らは適切な緩和措置を実施してこのような影響の軽減を助けることができるかどうかを考慮する。しかし、現在、新冠肺炎が著者らの試験サイトの起動、患者の募集と評価、研究薬物の提供と試験結果を報告する能力に与える影響の範囲を完全に予測することはできない。
2021年12月21日,我々は,新冠肺炎が生産,関連薬物供給,試験参加比率に及ぼす影響により,PAHにおけるPemziviviptadilの2 b段階試験を自発的に終了したと発表した。戦略評価後、著者らはさらにPemziviiptadilの開発を停止し、資源と資金を再配置し、bentracimabの商業化前活動に使用し、頑固性高血圧を治療するためのPB 6440を含む他のパイプライン計画を推進することを決定した
また、遠隔作業政策、隔離、現地避難と類似の政府命令、閉鎖或いはその他の新冠肺炎疫病に関連する業務運営に対する制限は生産性にマイナスの影響を与える可能性があり、著者らが行っている研究開発活動を妨害し、そして私たちの運営に影響を与え、その重症度はこれらの制限とその他の制限の持続時間と重症度及び私たちの正常な業務展開能力への影響に部分的に依存する。また,我々の従業員は遠隔作業に慣れているが,内部制御の変化
遠隔作業の手配は、私たちの財務報告書の作成過程における制御欠陥を招く可能性があり、これは深刻かもしれない。
新冠肺炎及びその変異体の伝播はすでに世界的に広範な影響を与えており、我々の経済に実質的な影響を与える可能性がある。新冠肺炎疫病による潜在的な経済影響と持続時間は評価或いは予測が難しいかもしれないが、持続的かつ日々深刻な疫病は全世界の金融市場の深刻な混乱を招き、私たちの資本獲得能力を低下させる可能性があり、これは未来に私たちの流動性に負の影響を与える可能性がある。また、新冠肺炎とその変種の伝播による景気後退や市場コール、インフレあるいはその他の負の世界経済状況は、私たちの業務と私たちの普通株の価値に実質的な影響を与える可能性がある。
全世界の新冠肺炎の大流行は引き続き迅速に変化した。新冠肺炎の著者らの業務および臨床試験に対する影響の程度は、疾患およびその変種の経時的地理的伝播、大流行の持続時間、アメリカと他の国の旅行制限および社会的距離、企業閉鎖または商業中断、および疾患の制御および治療のための米国および他の国による行動の有効性に依存し、疾患に対するワクチンおよび抗ウイルス薬の有効性および獲得性およびワクチン接種の成功を含む。したがって、私たちはまだ私たちの業務、私たちの臨床と監督活動、医療システム、あるいは世界経済への潜在的な遅延や影響のすべての程度を知らない。しかし、これらの影響は、私たちの業務、財務状況、運営結果、および成長の見通しに悪影響を及ぼす可能性がある
また,持続的な新冠肺炎の流行が我々の業務や運営結果に悪影響を与える場合,本“リスク要因”の節で述べた多くの他のリスクや不確実性を増加させる効果もある可能性がある。
設立以来、私たちは大きな損失を受けた。私たちは今後数年間赤字になると予想していて、決して達成されたり利益を維持したりしないかもしれない。
私たちは臨床段階の生物製薬会社で、設立以来、私たちは重大な純損失が発生した。2021年12月31日までの1年間の純損失は1兆311億ドルだった。2021年12月31日現在、私たちの累計赤字は3兆918億ドルです。私たちは予測可能な未来に巨額の費用と運営損失が続くと予想している。設立以来、私たちの運営資金は主に初公募株(IPO)で調達された資金と、その後、私たちの普通株の引受販売、転換可能な債券、転換可能な優先株の私募、私たちの定期融資項目の下の借金、SFJ協定に基づいて受け取った資金、そしてAlfasigma再許可によって受け取った資金からです。将来的には、SFJはSFJプロトコルに基づいて2,870万ドルまでの資金を提供することが予想される。私たちは製品の商業化が許可されていないし、製品販売から何の収入も得られなかった。
著者らはほとんどの財力と精力を投入して、著者らの臨床と臨床前候補製品を開発し、臨床前研究と臨床試験を含むELP半減期を延長する技術を独自に開発した。私たちは今後数年間巨額の費用と運営損失が発生すると予想している。私たちは数年かかるかもしれないと予想し、もしあれば、私たちは商業化された製品を持つことができる。私たちの純損失は四半期ごとと毎年大きく変動するかもしれません。私たちの費用は大幅に増加すると予想されています
•私たちが行っているbentracimab臨床試験を継続し、必要に応じて他の臨床試験を開始し、完成させる
•SFJプロトコルと私たちが発生する相応の臨床開発支援費用を通じて私たちの地理的カバー範囲を拡大することを求めています
•監督部門のbentracimabを抗血小板薬チカグレルの反転剤として承認することを獲得した
•難治性高血圧治療用のPB 6440を開発した
•より多くの臨床と臨床前候補製品の発見と開発を求めています
•私たちの臨床と規制能力を拡大し
•商業化インフラを構築し、外部製造と流通能力を拡大し、私たちが監督管理の許可を得る可能性のある任意の候補製品を商業化し、ベンゼントラマモノクロナル抗体を含む
•市場に適用される製品の要求に適合するために、私たちの法規遵守努力を調整します
•私たちの知的財産権の組み合わせを維持し、拡大し、保護する
•より多くの臨床、製造、科学者を招聘する
•私たちの製品開発および計画の将来の商業化努力を支援する人員を含む、運営、財務、および管理情報システムおよび人員を増加させる
•上場企業として運営する際には追加の法律、会計、その他の費用が発生する。
利益を達成し、維持するためには、相当な収入を生み出す候補製品を開発し、最終的に商業化しなければならない。これは、私たちの候補製品の臨床前テストと臨床試験の完成、規制部門の承認を得ること、および規制部門の承認を得ること、他の候補製品を発見し、開発することを含む、一連の挑戦的な活動で成功することを要求するだろう。私たちはただこのような活動の大多数の初期段階にいるだけだ。私たちはこのような活動で決して成功しないかもしれないし、たとえ私たちが成功しても、利益を達成するのに十分な収入や収入は決して生まれないかもしれない。
私たちが利益を達成しても、私たちは四半期や年度の収益性を維持したり向上させることができないかもしれない。もし私たちが利益を上げて利益を維持できなければ、会社の価値を下げ、資金を調達し、業務を拡大し、私たちの開発努力を維持し、製品の承認を得て、私たちの製品を多様化したり、運営を継続する能力を弱める可能性があります。わが社の価値の低下はあなたの投資損失の全部または一部を招く可能性もあります。
私たちは製品商業化の歴史がなく、これは投資家が私たちの業務のこれまでの成功度を評価することを難しくし、私たちの将来の生存能力を評価することも難しいかもしれない。
われわれは2002年に運営を開始し,これまでわれわれの運営は主に資金調達と臨床前候補製品の開発に集中しており,臨床前研究と臨床試験を行ってきた。これまで、重要な臨床試験を成功させ、規制部門の承認を得て、商業規模の製品を生産したり、第三者代表を配置したり、商業化に成功するために必要な販売やマーケティング活動を行うことができることは証明されていません。したがって、もし私たちがより長い運営歴史や成功開発と商業化製品の歴史を持っていれば、あなたは私たちの将来の成功や生存能力に対するいかなる予測もそんなに正確ではないかもしれません。
私たちの業務目標を達成する時、私たちは予見できない費用、困難、複雑な状況、遅延、および他の既知または未知の要素に遭遇する可能性がある。私たちは商業能力を開発する必要があるだろうが、私たちはこれを成功させないかもしれない。
私たちは、継続的に経営する企業として、私たちの財務義務を履行し、私たちの業務目標を達成するために、大量の追加資金が必要になるだろう。もし私たちが必要な時に資金を集めることができなければ、私たちは計画中の業務の削減と成長戦略の追求を迫られるかもしれない。
設立以来、私たちの業務は大量の現金を消費した。潜在的な候補製品を確定し、臨床前テストと臨床試験を行うことは時間がかかり、高価かつ不確定な過程であり、数年を要して完成する必要があり、しかも著者らは監督部門の許可を得て製品販売を実現するために必要なデータ或いは結果を永遠に生成できないかもしれない。私たちは次の数年間、私たちが行っている候補製品の臨床試験を完成させるとともに、私たちの候補製品の将来の臨床試験を開始し、bentracimabをチカグレルや反転剤としての発売承認を求め、難治性高血圧の治療のためのPB 6440を開発し、私たちが開発あるいは他の方法で得られる可能性のある任意の他の候補製品を推進し、巨額の費用と運営損失が発生することが予想される。しかも、私たちの候補製品が承認されれば、商業的成功を得られないかもしれない。私たちの収入は、もしあれば、私たちが数年以内に商業化できないと予想される製品を販売します。もしなければ。もし私たちがbentracimab、PB 6440、または私たちが開発または他の方法で買収した任意の他の候補製品の上場承認を得たら、製品販売、マーケティング、流通、製造に関連する巨額の商業化費用が発生すると予想される。上場企業の運営を支援するための追加インフラの作成に関連する費用が増加することも予想される。
純損失と運営キャッシュフローが負の状況を経験し,2021年12月31日現在の累計赤字は3.918億ドルであった。私たちは少なくとも今後数年以内に純損失が続くと予想している。2021年12月31日現在、私たちは4180万ドルの現金と現金等価物を持っている。2021年12月31日現在,我々の既存の現金と現金等価物に加え,SFJがSFJプロトコルに基づいて資金または精算を提供することが予想される2,870万ドルの臨床試験コストおよびその他の費用に加えて,本Form 10−K年次報告書に含まれる財務諸表発表日から12カ月の運営費用や資本需要を支払うのには不十分であると信じている。これらの要因は、私たちが経営を続けている会社として経営を続ける能力を大きく疑わせています。私たちは私たちの財政的義務を履行し、私たちの業務目標を達成するために多くの追加資金を必要とするだろう。私たちの将来の資本需要は多くの要素に依存します
•私たちが行っている計画と将来のbentracimab臨床試験と私たちが開発したPB 6440と他の臨床前計画の進展と結果
•私たちはSFJプロトコルに従って任意の支払い時間と金額を受け取り、SFJプロトコルの資本化要求を遵守する能力を持っています
•Alfasigmaの許可によると、私たちは規制のマイルストーン、商業マイルストーン、および印税の実現を稼ぐ資格がある
•私たちは追求する任意の未来の製品の臨床前開発、実験室テストと臨床試験の範囲、進捗、結果、コストを決定することができる
•私たちが他の候補品や技術を開発、許可、または取得する程度
•私たちが追求する可能性のある他の候補製品の数量と開発要件
•私たちの候補製品に対する規制審査のコスト、時間、結果
•将来の商業化活動のコストと時間は、製品製造、マーケティング、販売、流通を含み、私たちが市場の承認を得た任意の候補製品について
•私たちの候補製品の商業販売から得られた収入(あれば)は市場の承認を得ました
•私たちはフェニトラシズマブ、PB 6440、またはアメリカ以外の任意の他の候補製品を商業化する協力関係を構築することができます
•特許出願を準備し、提出し、起訴し、私たちの知的財産権を維持し、実行し、知的財産権に関連する任意のクレームを弁護するコストと時間。
私たちはbentracimabとPB 6440を商業化するために追加的な資金が必要になるだろう。規制当局によるこれらの候補製品の承認を得ると、製品の製造、販売、マーケティング、流通に関する巨額の商業化費用が発生することが予想され、具体的にはどこで商業化するかにかかっている。追加の資金はタイムリーで、優遇的な条件では得られないかもしれませんし、これらの資金が調達されれば、私たちの長期業務戦略を継続させるのに十分ではないかもしれません。また、追加資本を調達する能力は、世界の経済状況の潜在的な悪化や持続的な新冠肺炎の流行が米国と世界の信用と金融市場の中断と変動に悪影響を及ぼす可能性がある。もし私たちが十分な追加資本を集めることができなければ、私たちは私たちが計画した業務と私たちの成長戦略の追求を削減することを余儀なくされるかもしれない。
追加資本の調達は私たちの株主に希釈し、私たちの運営を制限したり、私たちの技術や候補製品に対する権利を放棄することを要求するかもしれません。
これまで、私たちが相当な収入を生み出すことができれば、私たちは株式発行、政府または個人団体の贈与、債務融資、許可と協力協定の組み合わせで私たちの現金需要を満たすことができるかもしれない。SFJプロトコルおよびAlfasigma再認可によって負担される資金義務を除いて、私たちは現在、約束された外部資金源は何もありません。私たちが株式または転換可能な債務証券を売却することによって追加資本を調達する場合、あなたの所有権資本は希釈され、これらの証券の条項は清算または他の特典を含む可能性があり、普通株主としての権利に悪影響を及ぼす可能性がある。債務融資および優先株融資に関与する可能性のある協定は、追加債務を招く、資本支出を行う、または配当を宣言するなど、私たちが具体的な行動をとる能力を制限または制限する契約を含む。たとえば,SFJプロトコルにより,SFJがbentracimabに関連するすべての資産の優先保証権益を付与し,SVBとWestRiverや貸手が既存債務について貸金者への留置権に限られる.担保権益の付与については、私たちが配当金を支払うこと、追加債務を招くこと、またはbentracimabに関連する知的財産権許可取引を行う能力の制限を含むいくつかの肯定的かつ否定的な条約に同意する。同様に、私たちと貸手との融資と保証協定は、私たちの現在と未来のほとんどの資産の保証権益を保証する。私たちは他の様々な習慣協約を遵守する義務がある, 私たちの知的財産権資産を制限する能力を含む。SFJと貸手に付与された担保権益は、将来の債務融資を阻止したり、このような融資の条項をそれほど有利にしない可能性がある。
もし私たちが第三者との協力、戦略連合またはマーケティング、流通または許可手配によってより多くの資金を調達する場合、私たちは、私たちの不利な条項にライセンスを付与するか、または将来の支払いフローを約束するために、私たちの技術、未来の収入フロー、または候補製品に対する貴重な権利を放棄する必要があるかもしれない。もし私たちが必要な時に株式や債務融資で追加資金を調達できなければ、私たちは延期、制限、減少、または
私たちの製品開発や将来の商業化努力を中止したり、私たちが自分で開発·マーケティングしたい候補製品を開発·マーケティングする権利を付与したりします。
監査人は、2021年12月31日までの財政年度に監査された財務諸表に対する私たちの意見が、このForm 10-K年度報告書に含まれている説明的段落に含まれており、持続的な経営企業としての私たちの経営継続能力に対する私たちの深刻な疑いに触れている。また、SFJプロトコルによれば、SFJプロトコルで規定されている期間内に継続的な経営状況を修復しなければ、bentracimabが商業化された任意の収入を共有する能力が大きな悪影響を受けることになり、SFJは、bentracimabに関連する業務をSFJに移行することを選択することができる。もし私たちが現在の運営計画を支援するために追加の資金を得ることができなければ、私たちは私たちの開発計画の範囲を延期または縮小し、および/または私たちの運営を制限または停止させることを余儀なくされるかもしれない。
監査人の2021年12月31日までの年次監査財務諸表に対する意見は、このForm 10−K年度報告書の一部の説明に含まれており、私たちの経常赤字と運営からのマイナスキャッシュフローは、私たちが経営を続けている企業として経営を続ける能力を大きく疑っていることを示しています。SFJプロトコルにより,SFJプロトコルが指定した期間内にそのような継続的な経営状況を救済できなければ,SFJは我々のbentracimabに関する業務をSFJに移行することを選択することができる.私たちは、私たちのコストと運営を再構成し、融資や戦略取引で追加資本を調達すること、またはSFJを最初に約束したのと同じ条項で追加融資を提供することを含む持続的な経営状況を救済することができる四半期が複数あります(彼らは追加融資を提供する権利がありますが、提供する義務はありません)。持続的な経営状況を救済できず、bentracimabに関連するビジネスがSFJに移行した場合、SFJがbentracimabへの投資から300%のリターンを得るまで、bentracimabの商業化収入を共有することはなく、その後、bentracimabの米国および欧州諸国の純売上高から1桁の特許権使用料を獲得する権利があり、SFJのbentracimabへの投資で合計500%のリターンを得た後、bentracimabの世界他地域の純売上高から中央値の特許使用料を得る権利がある。
SFJ協定に基づいて運営を継続するために必要な資本を調達し、継続的な経営状況を救済することができる保証はありません。あるいは十分な流動資金を生み出したり、運営損失を解消したりすることができます。もし私たちが十分な資金を得ることができなければ、私たちは私たちの支出を大幅に削減し、私たちの運営計画を減少させ、私たちの製品開発、商業化、戦略計画の一部または全部を削減する必要があり、私たちはベンゼントラマモノリスの商業化収入を共有する能力は実質的で不利な影響を受けるであろう。どれも同様に私たちの業務、将来性、財務状況、運営結果に大きな悪影響を及ぼすだろう。もし私たちが経営を続けることができなければ、私たちは私たちの資産を清算しなければならなくなり、そのような資産の私たちの監査された財務諸表上の列報価値を得ることができ、投資家は彼らのすべてまたは一部の投資を損失する可能性が高い。もし私たちが将来のビジネス活動を支援するための追加資金を求めている場合、私たちが継続的に経営している企業としての能力には依然として大きな疑問があり、投資家や他の融資源は商業的に合理的な条項や追加の資金を提供したくないかもしれない。我々の流動性需要と資本源の議論については、“経営陣の財務状況や経営結果の検討·分析”を参照されたい。
もし私たちがbentracimabに対する規制機関の承認を得た場合、あるいはSFJプロトコルが終了した場合、SFJプロトコルに従ってSFJに大量のお金を支払うことを要求される。私たちの業務がSFJプロトコルの下での支払い義務を履行するのに十分な資金やキャッシュフローがなければ、SFJは、私たちの資産の優先保証権益の保持者としてその救済措置を行使することができ、私たちの業務は大きな損害を受ける可能性があります。
2020年1月9日、SFJ協定に署名し、SFJはbentracimabのグローバル開発を支援するために1億2千万ドルまでの資金を提供することに同意した。規制部門からbentracimabを抗血小板薬であるチカグレルの反転剤として承認されれば,SFJプロトコルによるSFJへの多額の支払いが要求される。私たちがこのような必要なお金を支払う能力は私たちの未来の表現にかかっていて、これは経済、金融、競争、そして他の私たちがコントロールできない要素の影響を受けるだろう。私たちの業務は将来、SFJプロトコルの下での私たちの義務を履行するために、運営から十分なキャッシュフローを生じないかもしれません。もし私たちがこのようなキャッシュフローを生成できない場合、または公開または私募株式発行、債務融資、協力および許可手配、または他のソースによって許容可能な条項または追加資金を得ることができない場合、SFJへの支払い義務を滞納する可能性がある。我々は、SFJがbentracimabに関連するすべての資産の優先保証権益を付与しており、既存債務に対する貸金者の留置権に限定されている。もし私たちがSFJに対する支払い義務を履行できなければ、SFJは権益保持者を優先的に保証する救済措置を行使する可能性があり、これは私たちの資産損失を招き、私たちの業務は実質的に損害を受けることになる。
また、(I)SFJプロトコルに従って支払われるべき任意のお金を指定された期間内にSFJに支払うことができなかった場合、(Ii)私たちは違約(いくつかの例外によって制限されている)、または(Iii)(A)当時の四半期の財務諸表の発行または発行可能な日の1年以内に満了するか、または(B)私たちの任意の財務諸表に“持続的な経営”脚注が含まれているため、私たちの義務を履行できない可能性が高いと判断した場合、((A)または(B))の両方の場合,我々はこの状況を修復することができない
プロトコルに規定されている条件については,SFJは我々のbentracimabに関する業務をSFJに移行することを選択することができる.私たちは、私たちのコストと運営を再構成し、融資や戦略取引で追加資本を調達すること、またはSFJを最初に約束したのと同じ条項で追加融資を提供することを含む持続的な経営状況を救済することができる四半期が複数あります(彼らは追加融資を提供する権利がありますが、提供する義務はありません)。監査役は2021年12月31日までの10−K表年次報告に掲載されている財務諸表の審査を経た意見に,当社の持続経営企業としての継続経営能力に関する重大な疑いについて,SFJ協定に基づいて“持続経営企業”の条件を締結したという説明を掲載している。持続的な経営状況を救済できない場合、bentracimabに関連するビジネスがSFJに移行すれば、SFJのbentracimabへの投資が300%のリターンを得るまで、bentracimabの商業化収入を共有しないで、その後、bentracimabの米国およびいくつかのヨーロッパ諸国での純販売から1桁の特許権使用料を得る権利があり、SFJのbentracimabへの投資が合計500%のリターンを得た後、bentracimabの世界の他の地域での純販売から中央値の特許使用料を得る権利がある。“-監査人の2021年12月31日までの財政年度監査された財務諸表に対する私たちの意見は、本10-K表年次報告書に含まれている説明段落に含まれており、継続的な経営企業としての私たちの経営継続能力に対する私たちの深刻な疑いに触れている。また,SFJプロトコルにより,, SFJプロトコルで規定されている期間内に継続的な経営状況を是正しなければ、bentracimabの商業化された任意の収入を共有する能力が大きな悪影響を受けることになり、SFJは、bentracimabに関連するビジネスをSFJに移行することを選択する可能性がある。もし私たちが現在の運営計画を支援するために追加の資金を得ることができなければ、私たちは私たちの開発計画の範囲を延期または縮小し、および/または私たちの運営を制限または停止させることを余儀なくされるかもしれない
SFJプロトコルが終了すれば、SFJに大量のお金を支払う義務がある。SFJ協定が終了した後、吾らがBentracimabを開発し、米国、EU、日本、または中国でBLAの承認を得た場合、SFJ協定が終了していないように、限られた場合を除いて、SFJに適用される任意の司法管轄区域に適用される承認支払いをSFJに支払う義務がある。また、SFJプロトコルのいくつかの条項に違反した場合、SFJに関連するビジネスがSFJに移行された場合、SFJがbentracimabへの投資から少なくとも300%のリターンを得るまで、bentracimabの商業化された収入を共有しないだろう。このような支払い義務は、私たちの株主と私たちの業務、運営結果、および財務状況に大きな影響を与える可能性があり、bentracimabや他の候補製品の開発を延期または終了させる可能性があります。
もしアルファシマが私たちと彼らとの合意で規定された義務を履行しない場合、あるいは彼らが私たちと彼らのパートナー関係を終了した場合、私たちは計画通りに私たちの協力候補製品を商業化することができないかもしれません。私たちがその合意から得た予想収入は大きな影響を受けるかもしれません。
私たちはAlfasigmaと独占再許可協定を締結し、この協定に基づいて、Alfasigmaに再許可区域内での開発、使用、販売、販売、要約販売、および輸入特許製品の独占的権利を付与した。Alfasigma分割許可によれば、私たちは、任意のマーケティング許可がAlfasigmaに割り当てられることを含む、SFJプロトコルに従って、任意のマーケティング許可がAlfasigmaに割り当てられることを含むEMAおよびMHRAの規制承認を保証する責任がある。アルファシマには、マーケティングや特許製品の販売に必要な任意の規制承認(定価承認や発売後の約束を含む)を取得し、欧州やイギリス以外の国の規制承認を確保する義務がある。私たちはより低いコストまたはいくつかの合意された金額を超えない価格でアルファシマの特許製品に対する要求を提供します
Alfasigmaはこのプロトコルのすべての義務を履行しないかもしれないが、場合によっては、彼らまたは私たちは従属許可を終了するかもしれない。この場合、再許可責任を負うことができず、再許可地域内で許可製品を商業化する適切な代替商業パートナーを見つけることができない可能性がある。Alfasigmaが私たちから許可された製品ではなく、自分の製品や候補製品のような代替製品および候補製品を普及させることを選択した場合、私たちの候補製品に十分な時間と資源が投入されていない場合、または私たちの製品または候補製品に対する努力が成功せず、許可製品の商業化が延期または終了される可能性があり、将来私たちに支払われるお金が延期、減少またはキャンセルされる可能性があり、私たちの業務および財務状況は実質的な悪影響を受ける可能性がある。したがって、私たちが再許可地域の特許製品からどんな収入を得ることができるかどうかはアルファシマの努力にかかっている。
私たちの候補製品開発に関するリスク
私たちは現在1つの臨床段階の候補製品、フェニルトラシズマブ、1種のチカグレル或いは反転剤しかない。もし私たちが開発に成功し、監督部門のbentracimabの承認を得て商業化することができない場合、あるいは他の候補製品の開発に成功できない場合、あるいは開発過程で重大な遅延に遭遇した場合、私たちの業務は損なわれるだろう。
私たちはまだ商業販売が許可されていない製品です。私たちは現在一つの臨床段階の候補製品、bentracimabしか持っていない。今まで、私たちはどんな重要な臨床試験も完了していない。私たちはまだ候補製品の開発を完了していません。私たちは永遠に適切な製品を開発できないかもしれません。
私たちはほとんどの精力と財力を投入して、私たちの臨床と臨床前候補製品と私たちの独自のELP技術を開発した。私たちが候補製品から収入を得る能力は、私たちの候補製品の成功的な開発、規制承認、最終商業化に大きく依存し、数年以内には起こらないと予想される。Bentracimab、PB 6440、または私たちが開発または他の方法で得られる可能性のある任意の他の候補製品の成功は、いくつかの要因に依存する
•臨床前研究と臨床試験を適時かつ成功的に完成させる
•必要な臨床前研究と臨床試験を完成させるために十分な財政と他の資源があります
•ベントラマズマブの承認を求めることができる様々な適応や臨床試験の完成を含めて登録に成功しました
•BentracimabについてはSFJとの協力が成功しました
•私たちのビジネス製造プロセスの開発に成功したり、第三者製造業者と規制承認された任意の製品の商業製造プロセスを手配したりします
•直ちに関連監督部門の上場許可を受けた
•製品の商業販売を許可されています
•患者、医療界、第三者支払者が私たちの製品を承認した場合、その承認の適応を受ける
•Alfasigmaは、Alfasigmaライセンスに従ってbentracimabの発売、流通、および販売に成功した能力;
•フェニトラシズマブ、PB 6440、または任意の他の候補製品によって経験される有害事象の流行率および重症度;
•任意の候補製品の代替療法の利用可能性、知覚的利点、コスト、安全性および有効性、ならびに我々が開発したそのような候補製品の任意の適応、特にチカグレルの代替反転剤または抗血小板療法(反転剤で開発可能な治療法を含む)、または難治性高血圧を治療する代替療法;
•私たちはベントラマズマブ、PB 6440、あるいは私たちが商業規模で開発した他の候補製品を生産することができます
•私たちの候補製品のために特許、商標および商業秘密保護および規制排他性を獲得し、維持し、他の方法で知的財産権の組み合わせにおける私たちの権利を保護する;
•現在の良好な製造実践またはcGMPを含み、他のプロセスを効率的に遵守することを含む、法規要件の遵守を維持すること;
•承認後、製品の持続的に許容可能な安全性、耐性、有効性を維持する。
もし私たちがこれらの要素の1つまたは複数の点でタイムリーまたは根本的に成功できなければ、私たちは重大な遅延に遭遇したり、私たちが開発した候補製品を商業化することに成功しない可能性があり、これは私たちの業務に実質的な損害を与えるだろう。Bentracimab、PB 6440、または私たちが開発した他の候補製品のマーケティング承認を得なければ、私たちは運営を続けることができないかもしれません。
FDAや外国機関のような規制承認過程は冗長で時間がかかり,本質的に予測不可能である。もし私たちが私たちの候補製品のために必要な規制承認を得ることができなければ、私たちの業務は実質的に損害を受けるだろう。
FDAおよび同様の外国当局の承認または他の上場許可を得るのに要する時間は予測不可能であり、通常、臨床試験開始後数年後に必要であり、監督当局のかなりの裁量権を含む多くの要素に依存する。さらに、承認政策、法規、および承認を得るために必要な臨床データのタイプおよび数量は、製品候補の過程で変化する可能性がある
臨床開発は、異なる司法管轄区で異なる可能性がある。Bentracimabは私たちの現在唯一の臨床段階の候補製品だ。私たちはまだ候補製品の規制承認を得ていないし、私たちはbentracimab、PB 6440、または私たちが将来開発を求める可能性のある任意の候補製品の承認を永遠に得ることができないかもしれない。FDAから規制部門のBLAまたは新薬申請またはNDAの承認を得るまで、私たちおよび現在または未来のパートナーは、米国で任意の候補薬物製品の販売を許可しない。これまで、私たちはEMAや他の類似した外国当局とのみ、bentracimabや米国以外の任意の他の候補製品の承認について規制部門と限られた議論をしてきた。
米国または海外で任意の候補薬物製品を商業化することが承認される前に、私たちは厳格に制御された臨床試験を通じて大量の証拠を提供し、FDAまたは外国の監督管理機関に満足させなければならない。これらの候補薬物はその期待用途に対して安全、純粋かつ有効である。臨床前研究と臨床試験の結果は異なる方法で解釈できる。私たちの候補製品の臨床前または臨床データが有望であると信じていても、これらのデータはFDAおよび他の規制機関の承認を支持するのに十分ではないかもしれない。FDAはまた、承認前または後に私たちの候補製品に対して追加の臨床前研究または臨床試験を行うことを要求するかもしれないし、あるいは私たちの臨床開発計画の要素に反対するかもしれない。
大量に開発されている製品のうち、一部のみがFDAや外国規制機関の承認手続きに成功し、商業化されている。長い承認とマーケティング許可プロセス、および将来の臨床試験結果の予測不可能性は、私たちの業務、財務状況、運営結果、および将来性を深刻に損なう規制部門の承認およびマーケティング許可を得ることができない可能性があります。
私たちはbentracimabとPB 6440を含む臨床と臨床前候補製品を開発するために大量の時間と財力を投入した。私たちの業務は私たちがBentracimab、PB 6440と任意の未来の候補製品の臨床前と臨床開発を成功的に完成できるかどうかに依存し、監督部門の許可を得て、そして承認を得た場合、適時にそれを商業化することに成功した。
我々が最終的に臨床試験を完了し、BLA、NDAまたはBentracimab、PB 6440、または任意の将来の候補製品の海外マーケティング申請の承認を得ても、FDAまたは適用される外国の規制機関は、高価な追加の臨床試験(上場後の臨床試験を含む)の表現に基づいて、他のマーケティング許可を承認または承認することができる。FDAまたは適用される外国規制機関も、私たちが最初に要求したよりも限られた適応または患者集団の候補製品を承認または許可することができ、FDAまたは適用される外国規制機関は、候補製品の商業化に成功するために必要または望ましいラベルであると考えられるかもしれない。適用可能な規制承認や他のマーケティング許可を得るか得られないかのいずれの遅延も、候補製品の商業化を延期または阻止し、私たちの業務および将来性に重大な悪影響を及ぼすだろう。
さらに、FDAおよび他の規制機関は、彼らの政策を変更し、追加の法規を発表したり、既存の法規を修正したり、他の行動を取ったりする可能性があり、これは、私たちが将来開発している製品の承認をタイムリーに阻止または延期する可能性がある。このような政策や規制の変化は、私たちに追加的な要求を加えるかもしれません。承認された能力を延期したり、コンプライアンスコストを増加させたり、私たちが獲得した可能性のある任意のマーケティング許可を維持する能力を制限したりするかもしれません。
FDAからのフィードバックによると、承認手続きを加速させることで、米国でbentracimabの規制承認を求める予定だ。もし私たちがこの過程で成功できなければ、フェニトラシズマブの開発と商業化は延期、放棄あるいはコストが大幅に増加する可能性がある。
FDAの加速承認規定は、開発されている治療が満たされていない医療需要を許容する薬物は、生存率や不可逆的な発症率のような臨床的終点ではなく、臨床的利益を合理的に予測する可能性があると考えられる代替バイオマーカー終点への影響の証拠に大きく基づく。FDAからのフィードバックによると,我々の戦略は加速承認経路を用いることであり,BLA承認時に我々のbentracimab逆IT実験が行われていることが要求される可能性がある.私たちが提出したBLA加速承認を支持するために、FDAは最初の100人の患者のバイオマーカーデータの中期分析を提案し、私たちの逆IT試験では、約50人の患者が制御できない重大または生命に危険な出血を患っており、約50人の患者が緊急手術または侵襲的手術を必要とし、そして私たちの第2段階の臨床試験の安全データを必要としているが、FDAは、制御されていない重大または生命に危険な出血を患っているかどうか、あるいは緊急手術または侵襲的手術が必要であるかどうかを検討する問題である
逆IT試験を完了し、FDAの要求に応じて承認後登録を確立する予定です。Reverse-IT試験を完全に登録するために必要な合計200人の患者について、私たちの方案は、患者の約3分の2以下の患者が、制御されていない重大な出血または生命に危険な出血から来る可能性があると規定している
緊急手術や侵襲的手術が必要な人や患者。EMAのCHMPも我々が提案したbentracimabの臨床開発と商業化計画にほぼ同意している
2021年11月、私たちは、逆IT試験に参加した最初の150人の患者を指定した中期分析の結果を発表した(うち142人の患者は緊急手術または侵襲的手術を必要とし、そのうち8人の患者は制御されていない大出血または生命に危険な出血を患っている)。緊急手術や侵襲的手術を必要とする患者キューは完全に組み込まれており,試験地点は制御できない重大あるいは生命にかかわる出血事件のある患者の募集に重点を向けており,これらの患者の募集を加速させることに成功している保証はないが。
これらの患者の中期分析に基づいて,可能な加速承認のためにBLAを提出し,このスケジュールが新冠肺炎の大流行持続範囲と持続時間の影響を受ける可能性があるにもかかわらず,2022年に我々のBLAを提出する予定である。BLAを提出した後、FDAは、他の潜在的な原因では、制御できない重大または生命に危険な出血を有する患者を含む、適切な数の患者を募集するのに十分な数の患者を募集していないので、我々が行った試験が承認を支持するのに十分ではないと判断する可能性がある。また,FDAは広範な承認後の検討を求めたり,承認や上場後に行われている逆IT試験の修正を求めたりする可能性がある。
臨床製品開発は長くて高価な過程に関連しており、結果は確定していない。私たちは私たちの候補製品の開発と商業化を完成または最終的に完成させることができない中で追加のコストと遅延が生じるかもしれない。
FDAの許可を得て新しい生物或いは薬物製品を発売するためには、人体における安全性、純度と有効性を証明しなければならない。候補製品には、失敗のリスクが高い。私たちの候補製品がいつ、人体で有効または安全を証明するか、あるいは規制部門の承認を受けるかどうかを予測することはできない。監督部門から任意の候補製品を販売する市場の許可を得る前に、著者らは臨床前開発を完成し、それから広範な臨床試験を行い、著者らの候補製品の人体における安全性、純度、効力と効果を証明しなければならない。臨床試験は費用が高く,設計と実施が困難であり,完成には数年かかる可能性があり,結果自体は不確定である。1つまたは複数の臨床試験の失敗は、試験の任意の段階または試験中の任意の時間に発生する可能性がある。臨床前試験と早期臨床試験の結果は後の臨床試験の結果を予測できない可能性があり、臨床試験の中期結果も必ずしも最終結果を予測できるとは限らない。そのほか、臨床前と臨床データはよく異なる解釈と分析の影響を受けやすく、多くの会社は彼らの候補製品が臨床前研究と臨床試験で満足できると考えているが、しかし依然としてその製品のマーケティング許可を得られなかった。
私たちはまだ私たちの候補製品を承認するために必要なすべての臨床試験を完了していない。私たちが行っているまたは未来に行われる可能性のある任意の臨床試験が、規制部門の承認を得て、候補製品を市場に出すために、一致または十分な有効性と安全性を証明することを保証することはできません。
我々の候補製品は進行中の臨床試験で余分なコストや遅延が生じる可能性があり,将来の臨床試験(あれば)が時間どおりに開始されるかどうか,再設計が必要かどうか,時間どおりに十分な数の患者を募集する必要があるかどうか,あるいは時間どおりに完成する必要があるかどうかは分からない。臨床試験中や臨床試験の結果では、私たちは多くの予見できない事件に遭遇する可能性があり、これらの事件は、私たちの上場承認を延期したり、私たちの候補製品を商業化することを阻止したりする可能性があります
•規制機関や機関審査委員会は、私たちまたは私たちの研究者が予想される試験場所で臨床試験を開始したり、臨床試験を行ったりすることを許可してはならない
•私たちは、予想される試験場所または予想されるCROと受け入れ可能な臨床試験契約または臨床試験案との合意に遅延または合意できない可能性があり、その条項は広範な交渉を必要とする可能性があり、異なるCROと試験地点との間に有意差がある可能性がある
•私たちの候補製品の臨床試験は統計的意義を証明できなかったことを含む否定的または不確定な結果をもたらす可能性があり、私たちは決定または監督機関が追加の臨床試験を要求したり、製品開発計画を放棄したりする可能性がある
•私たちの候補製品の臨床試験に必要な患者の数は私たちが予想していたより多いかもしれません。これらの臨床試験の登録速度は私たちが予想していたよりも遅いかもしれません。あるいは参加者はこれらの臨床試験を脱退したり、私たちが予想したより高い速度で治療後のフォローアップを行うことができないかもしれません
•私たちの候補製品は副作用や他の予期しない特徴がある可能性があり、私たちまたは私たちの調査者、監督機関、または機関審査委員会が試験を一時停止または終了させる可能性があります
•私たちの第三者請負業者は、法規の要求を適時に遵守したり、私たちに対する契約義務を履行できなかったり、全く守らなかったりする可能性があります
•規制機関または機関審査委員会は、規制要件を遵守しないこと、または参加者が受け入れられない健康リスクに直面していることを含む、様々な理由で臨床開発を一時停止または終了することを私たちまたは私たちの調査者に要求するかもしれない
•私たちの候補製品の臨床試験コストは予想以上に高いかもしれません
•私たちの候補製品の供給または品質、あるいは私たちの候補製品の臨床試験に必要な他の材料が不足しているか、不十分である可能性がある。
もし私たちの候補製品の任意の臨床試験の完了が遅れたり、そのような試験が終了したら、私たちの候補製品の商業的な将来性は損なわれ、私たちがこれらの候補製品から製品収入を得る能力は延期されるだろう。また、臨床試験を完成するいかなる遅延も私たちのコストを増加させ、私たちの候補製品の開発と承認過程を緩和し、そして私たちの製品販売と収入を創造する能力を危険にさらす。
もし私たちが現在考えている候補製品に対して追加の臨床試験または他の試験を行うことを要求されたら、もし私たちが候補製品の臨床試験や他の試験を成功させることができなければ、もしこれらの試験や試験の結果があまり良くない場合、あるいは安全問題があれば、私たちは:
•私たちの候補製品の発売承認を遅延させます
•市場の承認を得ていません
•承認された適応や患者集団は期待や期待ほど広くない
•重大な使用または流通制限または安全警告を含むラベルの承認を得ること;
•追加の上場後のテスト要求を受ける
•発売承認を得た後にこの製品を市場から撤退させます。
臨床前研究或いは早期臨床試験の成功は未来の臨床試験の結果を予測できないかもしれない。
前臨床試験と早期臨床試験の成功は、今後の臨床試験が同じ結果をもたらすことを保証することができない、あるいは他の方法で十分なデータを提供して候補製品の有効性と安全性を証明することができる。臨床前試験及び第一段階と第二段階の臨床試験の主な目的は安全性をテストし、薬物動態学と薬効学を研究し、そして異なる用量とスケジュールの候補製品の副作用を理解することである。臨床前或いは動物研究及び早期臨床試験の成功は今後の大規模な治療効果試験が成功することは確保できず、最終結果を予測することもできない。我々の候補製品は臨床開発において期待される安全性と有効性を示すことができない可能性があり、臨床前研究で積極的な結果が得られたにもかかわらず、あるいは初歩的な臨床試験に成功した。
製薬と生物技術業界の多くの会社は後期臨床試験で重大な挫折を経験し、臨床前試験と早期臨床試験においても奮い立つ結果を得た。臨床前と臨床活動から得られたデータは異なる解釈を受ける可能性があり、これは監督部門の承認を延期、制限或いは阻止する可能性がある。また、私たちの候補製品開発中の規制政策の変化を含む多くの要因により、規制の遅延や拒否に遭遇する可能性がある。どのような遅延も、私たちの業務、財務状況、運営結果、および見通しに否定的な影響を及ぼす可能性がある。
著者らは時々発表或いは公表した臨床試験の一時的な“頂線”と初歩的な結果はより多くの患者データの獲得に伴い変化する可能性があり、そして監査と検証プログラムの影響を受け、これは最終データの重大な変化を招く可能性がある。
時々、私たちは臨床試験の一時的なトップラインや初歩的な結果を公表するかもしれない。私たちが達成可能な臨床試験の中期結果は、私たちのbentracimab第三段階逆IT試験を含み、患者登録の継続とより多くの患者データの獲得に伴い、1つまたは複数の臨床結果が実質的に変化する可能性があるというリスクに直面する可能性がある。初期または最も重要な結果も依然として監査とチェック手続きの制約を受けており、これは最終データが以前に公表された予備データと大きく異なる可能性がある。したがって、最終データを得る前に、中期と予備データを慎重に見なければならない。初期または中期データと最終データとの違いは、私たちの業務の将来性を深刻に損なう可能性があり、私たちの普通株の取引価格を大幅に変動させる可能性があります。
私たちの臨床試験は、私たちの候補製品の安全性と有効性を証明できないかもしれないし、あるいは私たちの候補製品の開発過程で深刻な不良または許容できない副作用が発見される可能性があり、これは規制部門の承認と商業化を阻止または延期し、私たちのコストを増加させるか、あるいは私たちのいくつかの候補製品の開発を放棄または制限する必要があるかもしれない。
私たちの候補製品の商業化販売が規制の承認を得る前に、私たちは長い、複雑で高価な前臨床試験と臨床試験を通じて、私たちの候補製品が安全で純粋で有効であり、各目標適応に使用でき、テストのどの段階でも失敗する可能性があることを証明しなければならない。臨床試験は目標適応研究に対する候補製品の安全性或いは有効性を証明できないことが多い。私たちの患者集団の健康状態によると、私たちは深刻な不良事件に遭遇する可能性があり、これは規制承認と商業化を阻止または延期し、私たちのコストを増加させるか、あるいは私たちのいくつかの候補製品の開発を放棄または制限する必要がある
我々の候補製品が臨床試験において副作用に関連しているか、または予期しない特徴を有する場合、それらの開発を放棄するか、またはその開発をより狭い用途に制限する必要があるかもしれないが、これらの用途では、副作用または他の特徴は、リスク−収益の観点からそれほど一般的ではなく、それほど深刻ではない、またはより容易に受け入れられる。FDAまたは機関審査委員会はまた、私たちの候補製品の安全性と有効性を理解するために、安全情報に基づいて、私たちの臨床試験を一時停止、停止または制限すること、または私たちが計画していないこと、または予想されていることを理解することを要求するかもしれない。これらの発見は、規制当局が私たちの候補製品にマーケティング許可を提供できないか、または承認された場合、承認の適応の範囲を制限することをさらに招く可能性がある。早期テストで最初に希望を示した候補製品の多くは後に副作用が生じることが発見され,その候補製品のさらなる開発を阻害している。
さらに、もし私たちの1つまたは複数の候補製品が発売承認され、私たちまたは他の人がこのような製品による不良副作用を発見した場合、多くの潜在的な重大な負の結果を招く可能性がある
•規制部門はこのような製品の承認を取り消すことができる
•規制部門はラベルに警告を追加することを要求するかもしれない
•患者に配布するためにこのような副作用のリスクを概説するための薬物ガイドラインの作成を要求されるかもしれません
•私たちは起訴され、患者への傷害に責任を負うかもしれない
•私たちは第三者支払者保険と十分な補償を達成したり維持することができないかもしれない
•私たちの名声と医者や患者の私たちの製品に対する受容度は影響を受けるかもしれない。
FDAまたは外国規制機関が任意の製品に関連する有害事象に関連する任意の問題をタイムリーまたは完全に解決することは保証されない。さらに、これらの事件のいずれも、特定の候補製品に対する市場受容度を達成または維持することを阻止または維持することができ、承認されれば、私たちの業務、運営結果、および将来性を深刻に損なう可能性がある。
組織として、私たちは重要な臨床試験を完成したことがなく、私たちは私たちが開発する可能性のあるすべての候補製品の臨床試験を完成できないかもしれない。
著者らは重要な臨床試験を成功的に完成し、FDA、EMA或いは他の監督機関の許可を得て、bentracimab、PB 6440或いは任意の未来の候補製品を発売することができる。重要な臨床試験を展開することは複雑な過程である。組織として、私たちは以前に後期や重要な臨床試験を終えたことがありません。そのためには、私たちの臨床開発と規制能力をさらに拡大する必要があり、より多くの合格者を募集し、訓練することができないかもしれません。また,第三者に依存した重要な臨床試験を継続する予定である。“−我々の第三者への依存に関するリスク−我々は,第三者に依存して既存の臨床試験の大部分や将来行われる可能性のある候補製品の臨床試験を行うことに依存しており,これらの第三者の表現は,このような試験の最終期限までに完了できないことを含めて満足できない可能性がある”特に,SFJプロトコルにより,SFJは主に中国と日本のベンゼントラマモノクロナルの臨床開発と規制活動を担当し,EUで臨床試験運営支援を提供している。したがって、私たちは、BLAまたはNDAの提出およびbentracimab、PB 6440、または将来の候補製品の承認をもたらすために、必要な臨床試験を成功的かつ効率的に実行および完了することができないかもしれない。私たちは私たちの競争相手よりも多くの時間とより多くのコストを必要とするかもしれないし、私たちが開発した候補製品の規制承認を得ることに成功しないかもしれない。私たちが計画した臨床試験を開始または完了または延期することができず、候補製品の商業化を阻止または延期する可能性がある。
もし私たちが臨床試験において患者の登録および/または維持に遅延または困難に遭遇した場合、必要な規制承認を受けることは遅延または阻止される可能性がある。
臨床試験の成功とタイムリーな完成には十分な数の患者を募集する必要がある。患者登録は臨床試験時間スケジュール中の重要な要素であり、それは患者群の規模と性質を含む多くの要素の影響を受ける。患者登録時間が予想より長いことや患者引き揚げにより,試験が遅延の影響を受ける可能性がある。FDAや外国規制機関の要求に応じて十分な数の合格患者を見つけて募集することができなければ、これらの試験に参加することができなければ、私たちの候補製品の臨床試験を開始または継続できない可能性がある。将来の臨床試験で被験者を募集する成功度を予測することはできません科目収生は他の要素の影響を受け、以下を含む
•試験に関する資格基準
•患者集団の大きさと患者を識別する手順;
•試用中の候補製品の既知のリスクおよび収益;
•市場で入手可能な競争療法および他の競合候補薬の臨床試験の有用性;
•患者が臨床試験に参加したいかどうか
•臨床試験に参加するための努力を促進し
•新冠肺炎疫病による可能性のある中断は、臨床サイトの開設、参加者の募集と維持の困難、臨床試験中の医療資源の分流、実施可能な旅行或いは検疫政策、及びその他の要素を含む
•医者の患者の回診のやり方
•治療中および治療後に患者の能力を十分に監視する;
•潜在的患者のための臨床試験場所の距離および利用可能性を提供する
•テロ、内乱、実際または脅威の武力衝突を含む、私たちの裁判場所がある国の経済的、政治的不安定。
私たちは十分な数の患者を募集して臨床試験を行うことができなくて、これは深刻な遅延を招き、1つ以上の臨床試験を完全に放棄し、甚だしきに至っては臨床開発計画を放棄することを要求するかもしれない。例えば,PAH治療のためのpemziviiptadilの開発を中止し,これまで新冠肺炎が試験の登録比率に及ぼす影響やその他の影響により,われわれのpemziviviptadilによるPAH治療の2 b期試験を自発的に中止した。
私たちのどの臨床試験の登録遅延も、候補製品の開発コストを増加させる可能性があり、これはわが社の価値を低下させ、追加融資を受ける能力を制限する。また,われわれはCROや臨床試験サイトに依存して継続してわれわれの臨床試験の適切かつタイムリーな進行を確保することが予想され,それらの発現への影響は限られる。
また,われわれの臨床試験のために十分な数の患者を募集できても,これらの患者の臨床試験への登録を維持することは困難である可能性がある。
候補製品の製造または処方を変更する方法は、追加のコストや遅延を招く可能性がある。
候補製品が臨床前研究から後期臨床試験まで、潜在的な承認と商業化を得るために、製造方法や調合などの開発計画の様々な側面に伴い、この過程で変更を行い、プロセスと製品特性の最適化に努力することが一般的である。このような変化はこのような期待された目標を達成できない可能性がある。これらの変化のいずれも、我々の候補製品の表現が異なることを招き、計画中の臨床試験またはプロセスを変えて製造された材料を用いた他の将来の臨床試験の結果に影響を与える可能性がある。このような変化はまた、追加のテスト、FDA通知、またはFDA承認を必要とする可能性がある。これは臨床試験の完成を遅らせる可能性があり、移行臨床試験或いは1つ以上の臨床試験を繰り返し、臨床試験コストを増加させ、著者らの候補製品の承認を延期し、そして著者らの販売開始と収入を創造する能力を脅かす必要がある。
われわれのベンゼントラマモノクロナル抗体の臨床開発は抗血小板治療としてテカグレルの継続に依存している。
テカグレルの反転剤としてbentracimabを開発し,チカグレルを服用した患者の治療に用いている。以前知られていなかったテカグレルに関連する安全リスクが発見された場合、これは抗血小板治療としての使用に影響を与える、またはもし
もし市場のチカグレルに対する受容度が著しく変化すれば、私たちはベントラマブの開発を一時停止または停止する可能性があり、これは私たちの業務の将来性に重大で不利な影響を与えるだろう。
ELPは新しい技術であり、これにより、開発の時間、リスクとコストを予測し、その後、私たちのELP候補製品の監督管理許可を得ることが困難になる。
私たちのいくつかの臨床前候補製品は私たちの独自のELP技術に基づいている。私たちの未来のいくつかの成功はこの技術とそれに基づく製品の成功開発にかかっている。私たちの知る限り、マーケティングおよび商業化治療のために、私たちを含むいかなる個人または実体も、私たちの新しいELP技術を使用することを許可していません。私たちはELPを使用した候補製品の発売と商業化の承認を決して得られないかもしれない。
ELP技術に関連する任意の以前に未知のリスクが発見された場合、またはELP候補製品を開発する際に予期しない問題や遅延に遭遇した場合、私たちの臨床試験および臨床前研究をタイムリーまたは利益的に達成することができず、許可協定の義務を履行し、または候補製品を商業化することができない可能性がある。我々のELP技術に基づく候補製品の臨床試験や臨床前研究において深刻な有害事象や許容できない副作用が観察されれば,ELP技術に基づいて他の候補製品を開発する能力は悪影響を受ける。
FDAの画期的な治療法指定およびbentracimabまたは任意の他の候補製品に対するEMAのPrime指定は、より速い開発または規制審査または承認過程を招くことがなく、候補製品が発売承認される可能性を増加させることもないかもしれない。
テカグレルの抗血小板活性を逆転させるためのbentracimabの画期的な治療法の称号を受けており,将来的には他の候補品の画期的な治療法の称号を申請する可能性がある。画期的な治療法は、1つまたは複数の他の薬剤と単独でまたは1つまたは複数の他の薬剤と組み合わせて深刻または生命に危険な疾患または状態を治療することを目的とした候補製品として定義され、予備臨床証拠は、候補製品が、1つまたは複数の臨床的重要終点において、臨床開発早期に観察される実質的な治療効果のような既存の療法よりも有意な改善を示す可能性があることを示す。画期的な治療法として指定された候補製品に対して,FDAと試験スポンサーとの相互作用やコミュニケーションは,臨床開発の最も有効な方法を決定するのに役立つとともに,無効な制御案中の患者数を最小限に抑えることができる。FDAにより画期的な治療法の候補品に指定され,BLA提出時に臨床データの支持を得られれば,優先審査を受ける資格もある。
FDAはそれを画期的な治療法に指定する権利がある。したがって,我々の候補製品の1つが画期的療法として指定された基準に適合していると考えても,FDAは同意せず,このような指定を行わないことにした可能性がある。いずれの場合も、FDAの従来の手順に従って承認を考慮した候補製品と比較して、候補製品の突破療法指定を受けることは、より速い開発プロセス、審査または承認を招くことなく、FDAの最終承認を確保することもできない可能性がある。さらに、私たちの1つまたは複数の候補製品が突破療法の条件を満たしていても、FDAは、候補製品がもはや資格条件に適合していないことを後で決定することができ、またはFDAの審査または承認の期間を短縮しないと決定する可能性がある。
EMAはPrime計画の使用を許可し,新たな治療法の開発と審査の加速を支援し,満たされていない医療ニーズを有する患者を治療する。従来のEMAプログラムによる承認を考慮した製品と比較して,製品候補を獲得するこのようなアクセスは,より速い開発過程,審査または承認を招くことはなく,いずれにしてもEMAの最終承認を確保することはできない.また,bentracimabがPrimeの使用を許可されていても,EMAはこのようなアクセス条件を満たさないことを後で決定する可能性がある.
私たちは、既存の候補製品のためにより多くの適応を求めること、または許可を得ること、または他の疾患のより多くの候補製品を得ることを含む、候補製品チャネルを増加させる努力は成功しないかもしれない。
我々の戦略の重要な要素の1つは、難治性高血圧を治療するためのPB 6440の開発と、我々のELP技術を用いて他の候補製品を決定することを含む、我々の候補製品チャネルの確立と拡大である。しかも、私たちは他の病気の他の候補品を許可したり取得したりするかもしれない。私たちは安全で許容可能で効果的な候補製品を決定したり開発することができないかもしれない。私たちが私たちのルートを確立することに成功しても、私たちが決定した、許可された、または獲得された潜在的な候補製品は、有害な副作用または他の特徴を有することが証明されたため、市場の承認および市場で受け入れられる製品ではないことを示すことを含む、臨床開発に適していない可能性がある。
私たちは、より利益的または成功可能性の高い候補製品または適応を利用することなく、特定の候補製品または適応を追求するために限られたリソースを費やす可能性がある。
私たちの財務と管理資源が限られているため、私たちは私たちが決定した特定の適応の開発計画と候補製品に集中している。そこで,我々は現在,テカグレル反転剤としてベンゼントリマブと難治性高血圧のためのPB 6440の開発に焦点を当てている。我々はこれまでPAH治療のためのpemziviiptadilを開発してきたが,戦略評価を行った後,難治性高血圧の治療のためのPB 6440を含む資源と資金の再配置,bentracimabの商業化前活動のためのpemzivividilのさらなる開発を中止することにし,難治性高血圧の治療のためのPB 6440を含む他のパイプライン計画を進めてきた。
私たちは他の候補製品を探す機会を放棄したり延期したりするかもしれないし、後により大きな商業潜在力を持つことが証明された他の兆候を探す機会を延期するかもしれない。私たちの資源配分決定は私たちが実行可能な商業製品や利益のある市場機会を利用できないかもしれない。私たちの現在と未来の開発計画および特定の適応候補製品への支出はいかなる商業的に実行可能な製品も生じないかもしれない。もし私たちが特定の候補製品の商業的潜在力や目標市場を正確に評価しなければ、私たちは協力、許可、または他の印税手配によって候補製品に価値のある権利を放棄するかもしれないが、この場合、候補製品の独占開発権と商業化権利を維持することは私たちに有利だ。
イギリスのEU離脱は、私たちの候補製品がイギリスで規制承認を得る能力に悪影響を及ぼす可能性があり、私たちの候補製品をイギリスに輸入する税金と関税を制限または徴収し、イギリスで私たちの候補製品を開発、製造、商業化するための追加費用を要求するかもしれません。
2016年の国民投票結果に続き、英国は2020年1月31日にEU離脱、通称離脱となった。イギリスとEUが合意した正式な離脱手配によると、イギリスには2020年12月31日までの過渡期、すなわち過渡期があり、その間にEUルールは引き続き適用される。2020年12月、イギリスとEUは貿易·協力協定、あるいは貿易·協力協定を達成し、過渡期後の貿易関係を概説し、2021年5月1日に正式に発効した。
イギリスが私たちの業務と私たちの候補製品に適用される規制枠組みの大部分はEU指令と法規から来ているため、イギリスは離脱し、イギリスでの候補製品の開発、製造、輸入、承認、商業化の規制制度に実質的な影響を与え続けるだろう。例えば、イギリスはEMAからEU範囲内のマーケティング許可を取得する集中的な手順によって保護されなくなり、イギリスで私たちの候補製品をマーケティングするには、別個のマーケティング許可が必要となる。英国の離脱やその他の理由により、いかなるマーケティング承認を得る上でのいかなる遅延も、いかなるマーケティング承認も得られない場合には、私たちの候補製品がイギリスで商業化されることを延期または阻止し、その地域での収入を創出する能力を制限する。“貿易と協力協定”は連合王国と欧州連合との間の医薬製品ゼロ関税貿易を規定しているが、このような貿易には過渡期終了前には存在しない追加の非関税コストがあり、連合王国と欧州連合間の貨物輸送には遅延がよくある。また,連合王国が医薬製品に関する規制の観点で欧州連合に逆行すれば,将来的に関税が徴収される可能性がある。したがって、私たちは現在も未来も、事業を運営する重大な追加費用(過渡期が終了する前と比較して)に直面する可能性があり、これは、私たちの収入または事業収益を達成する能力に重大かつ実質的な損害または遅延をもたらす可能性がある。国際貿易のいかなる更なる変化も, イギリスの離脱やその他の理由による関税と輸出入規制は、思わぬ関税コストや他の非関税障壁をもたらすかもしれません。これらの事態が発展したり、そのいずれかが起こりうるとの見方は、世界貿易、特に影響を受けている国と連合王国との貿易を大幅に減少させる可能性がある。
私たちの候補製品の商業化に関するリスク
Bentracimabの市場受容度は,承認されれば,テカグレルの継続的な受け入れと使用に大きく依存するであろう。
Bentracimabはチカグレルまたは反転剤としての商業的成功であり,承認されれば,抗血小板療法としてテカグレルの受け入れと使用を継続することに依存する。チカグレルは、他のP 2 Yを含む他の商業的に利用可能な抗血小板療法と競合する12受容体アンタゴニストは、その多くが模倣薬であるため、チカグレルよりもはるかに安い。将来的には他のP 2 Yも含めて新しい抗血小板療法を開発する可能性があります12受容体拮抗薬と他の抗血小板療法も逆転薬物を有する可能性があり、それらはカグレルの代わりを取る可能性があり、アメリカ心臓病学会、アメリカ心臓協会とヨーロッパ心臓病学会が急性冠症候群を治療する第一選択の抗血小板薬になり、あるいは他の方法でチカグレルの市場地位を低下させる。このような変更はありません
市場がテカグレルを受け入れて使用することは、私たちの業務、経営結果、およびbentracimabの将来性を深刻に損なうだろう。
たとえ私たちのすべての候補製品が市場の承認を得ても、彼らは医者、患者、第三者支払人、医学界の他の人が商業成功に必要な市場受容度を得ることができないかもしれない。
もし私たちのすべての候補製品が市場の承認を得たら、それらはまだ医者、患者、第三者支払人と医学界の他の人の十分な市場受容度を得ることができないかもしれない。もし私たちの候補製品が十分な受容度に達していなければ、私たちは著しい収入を生むことができないかもしれません。私たちは利益を上げることができないかもしれません。もし私たちの候補製品が商業販売に使用されることが許可されれば、市場の受け入れ度は多くの要素に依存するだろう
•代替療法と比較した有効性、安全性、潜在的利点
•競争力のある価格で私たちの製品を売ることができます
•代替療法と比較して投与の利便性と簡易性
•FDAまたは外国規制機関の製品ラベルまたは製品挿入要件は、任意のブラックボックス警告を含む製品承認ラベルに含まれる任意の制限または警告を含む
•対象患者群が新たな療法を試みる意欲と,医師がこれらの治療法を処方する意欲
•私たちはアメリカで販売チームの能力を雇用し維持しています
•Alfasigmaは、Alfasigmaライセンスに従って、そのターゲット国においてフェニトラシズマブを商業的に発売する能力に成功した
•有力なマーケティングと流通支援
•Bentracimab、PB 6440、および任意の他の候補製品が承認されると、サードパーティ保険および十分な補償を得ることができるかどうか;
•どんな副作用の流行や重症度も
•私たちの製品が他の薬と一緒に使用されるすべての制限。
もし私たちがbentracimab、PB 6440、または規制によって承認される可能性のある他の任意の候補製品の販売、マーケティング、および流通能力を確立できない場合、これらの候補製品が承認された場合、私たちはそれを商業化することに成功できないかもしれない。
Bentracimab、PB 6440、または上場承認を得る可能性のある任意の他の候補製品を商業的に成功させるためには、販売およびマーケティング組織を構築するか、または商業化パートナーを決定する必要がある。私たちは現在、いくつかの候補製品が承認された後、アメリカでマーケティングを行うために、重要な販売·マーケティングインフラを構築しています。私たち自身の販売、マーケティング、そして流通能力を確立することはリスクに関するものだ。例えば、販売チームの採用と訓練は高価で時間がかかり、どんな製品の発表も延期される可能性がある。販売チームを募集し、マーケティング能力を確立する候補製品の商業発表が何らかの理由で延期または発生していない場合、これらの商業化費用を早期または不必要に発生させる。これは費用が高いかもしれません。もし私たちが私たちの販売とマーケティング担当者を維持したり再配置できなければ、私たちの投資は損失します。
私たちが製品を販売するのを阻害するかもしれない要素は
•十分な数の効果的な販売とマーケティング担当者を募集し、訓練し、維持することはできません
•承認されると、販売員は私たちの候補製品を医師に紹介するために医者に触れることができない
•販売者が提供するセット製品の不足は、より広い製品ラインを持つ会社と比較して競争劣勢になる可能性がある
•独立した販売およびマーケティング組織の作成に関連する予測不可能なコストおよび費用。
Alfasigmaライセンスによれば、我々は、ライセンス領域内でbentracimabを含む任意の製品を開発、使用、販売、販売、カプセル販売、および輸入するAlfasigma独占権利を付与する。もし私たちが
私たち自身の販売、マーケティング、流通能力の確立に成功し、第三者との手配を余儀なくされ、第三者にこれらのサービスを提供することに依存しており、私たちの収入や収益性(あれば)は、私たち自身がこのような能力を開発している場合よりも低くなる可能性がある。さらに、私たちは第三者との販売、マーケティング、および私たちの候補製品の追加的な配置を成功的に達成できないかもしれないし、私たちに有利な条項でそうすることができないかもしれない。私たちはこのような第三者に対して支配権がほとんどないかもしれません。彼らのいずれも必要な資源と注意力を投入して、私たちの製品を効果的に販売し、マーケティングすることができないかもしれません。もし私たちが販売、マーケティング、流通能力を確立することに成功できなければ、私たち自身も他の第三者と協力しても、私たちの候補製品を商業化することに成功しないだろう。
私たちは、予想よりもビジネス機会が小さく、および/または他の人が私たちよりも前に、または私たちよりも製品の発見、開発、または商業化に成功する可能性がある激しい競争に直面している。
生命科学業界は競争が激しい。私たちは現在の候補製品の面で競争に直面しており、将来私たちは開発または商業化された任意の候補製品も競争に直面する可能性があり、これらの競争は主要な製薬と専門製薬会社、調合施設、学術機関と政府機関、ならびに公共および個人研究機関を含む多くの異なる源から来ている。
現在,承認または臨床開発中のチカグレルや任意の他の抗血小板薬の反転剤は知られていない。EUでは、インビトロ全血浄化吸着装置があり、体外循環と組み合わせて使用される場合、いくつかの心臓手術中にチカグレルを非特異的に除去するのに役立つ可能性がある。この装置のメーカーCytoSorbents社はまた、DrugSorb-ATR抗血栓除去システムの心胸郭手術における使用を評価するための臨床試験を米国で開始した。承認されると、bentracimabは、特定の逆チカグレルに使用可能な唯一の治療薬となるであろう。競争相手がそれと競争する製品の開発を求めない保証はない。さらに、bentracimabの成功は、承認されれば、テカグレルの持続的な成功に依存する。“--bentracimabに対する市場の受容の程度を見て、承認されれば、テカグレルに対する市場の持続的な受け入れおよび使用に大きく依存するであろう
また,他のいくつかの製品や候補品は難治性高血圧治療の潜在療法としてPB 6440と競合する可能性が知られている。PB 6440は患者の既存の抗高血圧療法の補完として利用される可能性が予想されるが,現在の鉱質コルチコイド受容体に対する非特許高血圧療法と競合することが予想される。現在承認されている塩酸コルチコイド受容体拮抗薬であるエプリノンやスピロラクトンに加えて,臨床開発中の難治性高血圧治療薬のいくつかが知られており,承認されれば,PB 6440はCIN−107,アルドステロン合成酵素阻害剤を含み,現在CinCor製薬会社が2段階臨床試験で評価していること,MLS−101,Mineralys Treeutics社が第2段階臨床試験で評価しているアルドステロン合成酵素阻害剤であることが分かった。
さらに、私たちの競争相手がフェニトラミマブ、PB 6440、または私たちが開発する可能性のある他の任意の製品よりも安全またはより効果的で、副作用がより少ない、より便利またはより安い製品を開発および商業化すれば、私たちのビジネス機会は減少または消失する可能性がある。私たちの競争相手も私たちよりも早くFDAや他の規制機関のその製品の承認を得ることができ、これは私たちの競争相手が私たちが市場に入る前に強力な市場地位を確立することをもたらすかもしれない。
私たちが競争しているか、あるいは将来競争する可能性のある多くの会社は、研究開発、製造、臨床前テスト、臨床試験を行い、監督管理許可とマーケティング承認を得た製品の面で、私たちよりも多くの財務資源と専門知識を持っている。製薬とバイオテクノロジー産業の合併と買収は、私たちの数の少ない競争相手により多くの資源を集中させる可能性がある。規模が小さいかスタートアップ段階にある会社も重要な競争相手になる可能性があり、特に大手や成熟会社との協力で手配する。これらの競争相手はまた、合格した科学と管理者を募集と維持し、臨床試験場と臨床試験の患者登録を確立し、そして私たちの計画と相補的あるいは必要である可能性のある技術を獲得する上で私たちと競争している。
テカグレルまたは反転剤、PB 6440による難治性高血圧の治療、または任意の将来の候補製品としてのBentracimabの成功は、カバー範囲および十分な精算または患者がこれらのプログラムのために支払う意思に大きく依存するであろう。
私たちの成功は、テカグレルまたは反転剤としてbentracimab、難治性高血圧のためのPB 6440、および/またはbentracimab、PB 6440または任意の他の候補製品を使用する手続きの保証範囲と十分な精算、および費用の全部または一部を精算することなく、患者が自腹を切ってそのような製品および手続きを購入することを望む程度に依存すると信じている。医師の監督下で投与される価格が高いため、私たちの製品のために保険と十分な補償を得ることは特に難しいかもしれない。製品自体や私たちの製品の治療やプログラムの個別補償
使用したものは利用できないかもしれません。私たちの製品を使用する手続きを引き受けても、Medicare、Medicaid、管理式医療機関、個人健康保険会社のような第三者支払者は、私たちの製品に関連する費用を医師に単独で精算することなく、薬物コストを手続き支払いに梱包することができます。第三者支払人が保証を受けないか、単独で私たちの製品を清算することを決定すれば、承認されると、医者の私たちの製品に対する使用を減らすことができるかもしれません。また、米国では、第三者支払者の間に統一的な保証·補償政策はない。第三者支払者が自己の保険·精算政策を設定する際には,通常連邦医療保険引受政策と支払制限に依存する。しかしながら、提供されるべき補償範囲および金額に関する決定は、支払者毎に基づいて行われる。1人の支払人が1つの薬品に保険を提供することを決定し、他の支払者も保険と十分な補償を提供することを保証することはできない。
第三者支払者は、彼らがどの製品と手続きをカバーし、精算レベルを確立するかを決定する。第三者支払者が特定の製品やプログラムをカバーしても、それによる精算支払率が十分高くない可能性がある。疾患によりオフィスで治療を受けている患者は、通常、手術期間中に使用される製品に関する費用を含む第三者支払人によって手術に関連する費用の全部または一部を精算し、このような保険や十分な精算がなければ、患者はこのような手術を受けたくない可能性がある。保険カバー範囲内にない場合、医師はそのような治療にプログラムを提供することができない可能性があり、保険および十分な精算が提供されない限り、私たちの候補製品を購入して使用することができない可能性がある(承認された場合)は、保険および十分な精算が提供されない限り、私たちが規定する適応に使用することができる。
第三者支払者の精算は、第三者支払人が安全、有効かつ医学的に必要であることを決定すること、特定の患者に適していること、費用効果があること、同業者によってレビューされた医学雑誌の支持を得ること、臨床実践ガイドラインに含まれること、および美容的でもなく、実験的でもなく、研究的でもないことを含む多くの要素に依存する可能性がある。
また、第三者決済者は通常、毎年時々支払率を更新して修正する。支払率更新の一例は連邦医療保険計画の医師支払いの更新であり,これは年に1回である。過去、この式を適用して支払い額が低くなった場合、国会は臨時立法で支払いの減少を防止していた。2015年の“連邦医療保険アクセスとチップ再認可法案”は法定式の使用を終了し,連邦医療保険医に功績に基づくインセンティブボーナス計画を導入し,品質支払い計画とも呼ばれている。この計画は,高度な代替支払いモデルと功績に基づくインセンティブ支払いシステムを含む臨床医に2つの参加方式を提供している。2019年11月、医療保険·医療補助サービスセンター(CMS)は、品質支払い計画の変化を最終的に決定するルールを発表した。品質支払い計画の導入が全体の医師精算に与える全面的な影響はまだ不明である。連邦医療保険や他の政府が計画している精算のいかなる減少も、個人支払者の支払いの同様の減少を招く可能性がある。選好精算制度では、それによる支払いの減少は、私たちの収入や業務結果に悪影響を及ぼす可能性がある。さらに、一部の個人支払人は連邦医療保険医費用スケジュールを彼らの特定の計画の医師支払いスケジュールに調整した。未解決と将来の医療立法が私たちの業務にどのように影響するか、保険や精算面のどんな変化が私たちの候補製品のカバー範囲をさらに制限したり、私たちの製品を使用する手続きの精算を下げたりすることが私たちの業務を損なう可能性があるか予測できません。
外国政府にも独自の医療保険精算制度があり,これらの制度は国や地域によって大きく異なり,どの外国精算制度でも我々の製品を使用した治療が保険と十分な精算を受けることを確保することはできない。
Bentracimab、PB 6440、または任意の他の候補製品が米国または他の国/地域で販売が許可されていれば、医学的に合理的で必要であることは保証されず、第三者支払者がそれが費用効果があると考えている保証はなく、カバー範囲や十分な精算レベルを保証することもできず、米国と私たちの製品販売所の国/地域の精算政策およびやり方が私たちが販売している候補製品の収益力に悪影響を与えないことを保証することはできない。
Bentracimab、PB 6440、または任意の他の候補製品の市場は私たちが予想していたより小さいかもしれない。
Bentracimab、PB 6440、または任意の他の候補製品の潜在的市場機会の推定は、私たちの業界知識、業界出版物、および第三者研究報告に基づくいくつかの重要な仮定を含む。これらの仮定は、bentracimabの場合、チカグレルを服用する患者の数が暴走出血または手術を必要とすること、PB 6440の場合、難治性高血圧を有する患者の数、および承認された場合の各候補製品の推定補償レベルを含む。しかし、このような仮定のいずれも正確であるか、または依然として正確であることは保証されない。Bentracimab、PB 6440、または私たちが開発する可能性のある任意の他の候補製品の実際の市場が私たちが予想していたより小さい場合、私たちの収入(あれば)が制限される可能性があり、私たちは利益を達成したり維持したりするのが難しいかもしれない。
私たちに対する製品責任訴訟は、私たちが重大な責任を負い、私たちが開発する可能性のある任意の製品の商業化を制限する可能性があります。
私たちは人体臨床試験で私たちの候補製品をテストすることに関連する固有の製品責任リスクに直面しています。もし私たちが開発する可能性のある任意の製品を商業的に販売すれば、私たちはより大きなリスクに直面します。もし私たちが自分自身を弁護することに成功できなければ、私たちの候補製品や薬物が損傷を与えたと主張すれば、私たちは重大な責任を招くだろう。是非曲直や最終結果にかかわらず、賠償責任は
•私たちが開発する可能性のある候補品や薬の需要が減少しています
•私たちの名声とメディアの深刻な否定的な関心を損なう
•臨床試験参加者の脱退
•関連訴訟の巨額の抗弁費用
•実験参加者や患者に多額の報酬を支払い
•収入損失
•経営陣の資源を減らして業務戦略を推進する
•私たちが開発する可能性のあるどんな製品も商業化できない。
私たちは現在全部で1,000万ドルの製品責任保険を持っています。各事故の上限は10,000,000ドルで、これは私たちが発生する可能性のあるすべての責任をカバーするのに十分ではないかもしれません。私たちの臨床試験の拡大に伴い、あるいは候補製品を商業化し始めたら、私たちの保険カバー範囲を増やす必要があるかもしれません。保険範囲はますます高くなっています。私たちは可能などんな責任にも対応するために、合理的な費用や十分な金額で保険範囲を維持することができないかもしれない。
私たちの第三者への依存に関するリスク
我々は第三者に依存して候補製品の大部分の既存の臨床試験と潜在的な未来の臨床試験を行うが、これらの第三者の表現はこのような試験の最終期限前に完成できなかったことを含む満足できないかもしれない。
これまで、私たちは通常CROを招いて、私たちが行っているbentracimab臨床試験と私たちの製品候補製品の他の以前の臨床試験に協力してきた。将来のベントリミズマブ,PB 6440あるいは他の候補製品の臨床試験にCROを参加させ,臨床開発に進展させる可能性がある。また,SFJプロトコルによると,SFJは主に中国と日本のベンゼントラマモノクロナルの臨床開発と規制活動を担当し,EUで臨床試験運営支援を提供している。これらの臨床試験は,臨床データ管理組織,医療機関,臨床研究者を含む第三者による継続が予想される。これらの第三者のいずれも私たちとの契約を終了することができ、重大な違約が治癒していない場合に終了するものもあれば、便宜上いつでも終了するものもある。もし私たちがこれらの第三者との任意の関係が終わったら、私たちは第三者の代わりに適切な条項を達成できないかもしれないし、もしあれば、商業的に合理的な条項でそうすることができないかもしれない。CROの交換または増加は多くのコストに関連し、管理時間と重点を必要とする。しかも、新しいCROが仕事を始める時、自然な過渡期がある。したがって,遅延が生じ,期待される臨床開発スケジュールを満たす能力に実質的な影響を与える可能性がある。私たちはCROとの関係を慎重に管理しようとしているが、私たちが未来に挑戦や遅延に遭遇しないことを保証することはできず、これらの遅延や挑戦が私たちの業務、財務状況、および見通しに実質的な悪影響を与えないことを保証することはできない。また、私たちのCROの表現も持続的な新冠肺炎の大流行によって中断される可能性があります。旅行や検疫政策を含む, 医療保健提供者であるCROスタッフの新冠肺炎への曝露が増加したり、大流行のために資源の優先順位を手配したりする。
また,われわれの臨床試験を行う第三者はいずれもわれわれの従業員ではなく,当等の第三者との合意に基づいてわれわれに提供された救済措置を除いて,われわれの臨床プロジェクトに十分な時間と資源を投入しているかどうかを制御することはできない。これらの第三者がその契約の義務または義務の履行に成功しなかった場合、または予想された期限内に完了した場合、もし彼らが交換する必要がある場合、または彼らが得た臨床データの品質または正確性が私たちの臨床方案、法規の要求または他の原因を遵守できなかったために影響を受けた場合、私たちの臨床試験は延長、延期、または終了される可能性があり、私たちは規制機関の私たちの候補製品の承認を得ることができないか、または商業化に成功する可能性がある。したがって、私たちの運営結果と私たちの候補製品のビジネス見通しは損なわれ、私たちのコストは大幅に増加する可能性があり、私たちの収入を創出する能力は著しく遅れる可能性がある。
私たちはこれらの方に依存して私たちの臨床前研究と臨床試験を実行し、通常彼らの活動をコントロールしません。私たちのこれらの第三者の研究開発活動への依存は、これらの活動に対する私たちの統制を減少させるだろうが、私たちの責任を軽減することはない。例えば,我々のすべての臨床試験が試験の全体的な調査計画や案に沿って行われることを確保していきたい。さらに、FDAは、データおよび報告の結果が信頼性および正確であることを保証し、試験参加者の権利、完全性および機密性を保護するために、良好な臨床実践またはGCPと呼ばれる臨床試験結果を行い、記録し、報告する基準を遵守することを要求する。実施中の臨床試験を指定された時間範囲で登録し,完成した臨床試験結果を政府後援のデータベースClinicalTrials.govに発表することも求められている。そうしないと罰金、否定的な宣伝、そして民事と刑事制裁につながるかもしれない。もし私たちまたは私たちの任意のCROまたは他の第三者が、試験場所を含み、適用されたGCPを遵守できなかった場合、私たちの臨床試験で生成された臨床データは信頼できないと考えられる可能性があり、FDA、EMAまたは同様の外国の規制機関は、私たちの上場申請を承認する前に追加の臨床試験を行うことを要求するかもしれない。特定の規制機関が検査を行った後、この監督機関は私たちのいかなる臨床試験がGCP規定に適合しているかどうかを確認することを保証することはできません。また,われわれの臨床試験ではcGMP条件下で生産された製品を使用しなければならない。私たちがこれらの規定を遵守しないことは、私たちが臨床試験を繰り返す必要があるかもしれないが、これは規制部門の承認過程を遅らせるだろう。
また,われわれの臨床試験の首席研究員は時々私たちの科学コンサルタントやコンサルタントを務め,このようなサービスに関する報酬を得る可能性がある。場合によっては、私たちはその中のいくつかの関係をFDAに報告することを要求されるかもしれない。FDAは結論を出すかもしれないが,我々と主要研究者との経済関係は利益衝突をもたらしたり,他の方法で実験の解釈に影響を与えたりしている。したがって,FDAは適用された臨床試験地点で生じるデータの完全性を疑問視する可能性があり,臨床試験自体の効用が脅かされる可能性がある。これは、FDAが私たちの上場申請を承認または拒否することを遅延させる可能性があり、最終的にbentracimab、PB 6440、または任意の他の候補製品の上場承認が拒否される可能性がある。
私たちはまた、他の第三者に依存して、私たちの臨床試験の製品供給を保存し、配布したい。私たちの流通業者のどんな業績ミスも、私たちの候補製品の臨床開発やマーケティング承認、あるいは私たちの製品の商業化を延期し、追加の損失を生じ、私たちの潜在的な収入を奪う可能性があります。
もし私たちが発売許可を得たら、私たちは現在、引き続き第三者生産ベントラマズマブ、PB 6440、その他の私たちが臨床開発と商業製造に使用する可能性のある候補製品に依存し、引き続き依存すると予想される。このような第三者への依存は、許容可能なコストで十分な数の候補製品またはそのような数を得ることができないリスクを増加させ、私たちの開発または商業化努力を延期、阻止、または損害する可能性がある。
私たちにはcGMP生産施設は何もありません。私たちは現在依存しており、bentracimab、PB 6440、および私たちが追求する可能性のある任意の他の候補製品、臨床開発およびbentracimab、PB 6440、および私たちが追求する可能性のある任意の他の候補製品を生産するために、臨床開発およびbentracimab、PB 6440および私たちが追求する可能性のある任意の他の候補製品を生産するために、第三者に依存し続けることが予想される。私たちは独自の大腸菌.大腸菌Bentracimabの生産を許可しています私たちのバクへの依存は大腸菌.大腸菌Bentracimab株は、十分な数のbentracimabがないか、または許容可能なコストまたは品質で数量を得ることができないリスクを増加させ、これは、臨床試験または他の開発または商業化努力をタイムリーに行う能力を遅延、阻止、または損害する可能性がある。
Bentracimabについては,我々は最初にバクに依存してわれわれの臨床試験のための薬剤を製造した。我々は,バクから別のcGMP契約メーカーBioVectraへの現在のベンゼントリマブ製造プロセスの技術譲渡を完了した。私たちはBioVectraを招いて私たちが行っている臨床試験のための薬物物質を製造し、規制承認を得た後に商業的に供給されるベンゼントラマモノクロナル抗体(承認されれば)を生産した。BioVectraまたは私たちが招聘した任意の他の未来の第三者メーカーが生産した新しい材料がすべての点で私たちの以前の臨床試験で使用された製品に匹敵することを証明するために、分析と他のテストを行う必要がある。このような製品が必要な比較可能な試験に直ちに通過することを保証することはできないし、私たちが招聘した任意の未来の第三者メーカーがbentracimabの生産に成功することを保証することはできない、あるいは私たちが招聘したBioVectraまたは任意の他の第三者製造業者が生産した任意の材料は、私たちがこれまでに観察された以前の臨床試験で使用された材料と同じ効果をもたらすだろう。また、供給中断や生産量や品質が良くなければ、私たちの業務に実質的な損害を与えるだろう。BioVectraは将来のbentracimabの需要を満たすために製造プロセスの拡大を要求され,後期臨床開発に使用され,承認されれば商業化も実現される。BioVectraが製造プロセスの拡大に成功しなければ,代替製造施設や代替製造プロセスを探す必要があり,これをタイムリーに行うことができないか,あるいは商業的に合理的な条項ではできない可能性があり,bentracimabの臨床開発に悪影響を及ぼす可能性がある。
私たちはまた、第三者製造業者または第三者パートナーに依存して、商業供給のフェニトラシズマブ、PB 6440、および市場によって承認された任意の他の候補製品を生産することを望んでいる。BLAまたは同様のマーケティング申請をFDAまたは他の規制機関に提出した後、私たちの契約メーカーが私たちの候補製品を生産するための施設は、FDAまたは他の規制機関が検査しなければならない。私たちは、供給者または製造業者が、環境健康および安全問題に関連する法規のような法律、法規、および適用されるcGMP規格または同様の法規要件および他の法律法規に準拠しているかどうかを制御することができない。もし私たちの契約メーカーが私たちの規格やFDAや他の規制機関の厳格な規制要件に合った材料を生産することに成功しなければ、私たちのマーケティング申請に対する規制部門の承認を得ることができないかもしれません。しかも、私たちの契約製造業者が十分な品質管理、品質保証、合格者の能力を維持することを制御することはできません。FDAや同様の外国規制機関が、これらの施設に欠陥があることを発見したり、これらの施設を承認して私たちの候補製品を生産したりしない場合、または将来的にそのような承認を撤回すれば、代替製造施設を探す必要があるかもしれません。これは、私たちが規制機関の承認を得たり、私たちの候補製品を販売したりする能力に深刻な影響を与えます。
私たちは未来の第三者製造業者といかなる合意にも到達できないかもしれないし、受け入れ可能な条項でそうすることができないかもしれない。このような合意に達しても、これらのメーカーの資格認証にはかなりの時間がかかる可能性があり、第三者メーカーに依存することは追加のリスクをもたらす
•第三者に依存して規制コンプライアンスと品質保証を行う
•第三者は製造協定に違反する可能性がある
•商業承認前に生じた前期拡大コスト
•私たちのビジネス秘密とノウハウを含む私たちの固有情報を盗用する可能性があります
•候補製品の原材料コストが増加する可能性があります
•いかなる第三者も、費用が高い時、または私たちに不便な時にいかなる合意も終了しないか、または更新しないかもしれない。
私たちまたは私たちの第三者製造業者が適用された法規を遵守できなかったことは、臨床封印、罰金、禁止、民事処罰、遅延、許可の一時停止または撤回、許可証の取り消し、候補製品または薬物の差し押さえまたはリコール、運営制限、刑事起訴を含む制裁を実施する可能性があり、いずれも私たちの製品供給に重大な悪影響を及ぼす可能性がある。
私たちの候補製品、そして私たちが開発する可能性のあるどんな薬物も、他の候補製品や薬物と生産施設を競争する可能性があります。私たちの第三者メーカーの業績は、将来的に持続的な新冠肺炎の流行による生産不足や他の供給中断によって中断される可能性がある。私たちはcGMP規制によって運営され、タイムリーに生産してくれる他のメーカーと同様のビジネス計画を達成できる保証はありません。私たちの既存または未来のメーカーのどんな業績失敗も、臨床開発やマーケティング承認を延期する可能性がある。
私たちはSFJと協力してbentracimabを開発し、Alfasigmaと協力して、ヨーロッパやいくつかの他の地理的地域でbentracimabを商業化しており、私たちの候補製品を開発または商業化するために、第三者とより多くの協力を求めるかもしれない。もしこのような協力が成功しなければ、私たちはこの候補製品の市場潜在力を利用できないかもしれない。
私たちはSFJと協力してbentracimabを開発し、Alfasigmaと協力してヨーロッパやいくつかの他の地理的地域でbentracimabを商業化している。私たちは、米国以外の地域でのマーケティングが許可されている候補製品の商業化を含む、私たちの候補製品の開発と商業化のために、より多くの第三者パートナーを探すことができるかもしれない。私たちのこのような計画の可能なパートナーは地域と国家製薬会社とバイオテクノロジー会社を含む。もし私たちがどんな第三者とも追加的なこのような計画を達成すれば、私たちの協力者が私たちの候補製品の開発または商業化に投入する資源の数量と時間を限られた制御をすることができるかもしれない。私たちがこのような計画から収入を創出する能力は、私たちの協力者がこれらの手配の中で彼らに割り当てられた機能を成功的に履行する能力に依存するだろう。
私たちの候補製品に関する協力は私たちに次のようなリスクをもたらすだろう
•協力者は彼らがこれらの協力の努力と資源に適用することを決定する上で大きな自由裁量を持っている
•協力者は期待通りに義務を履行していないかもしれない
•協力者は監督管理の許可を得た任意の候補製品の開発と商業化を行ってはならず、臨床試験結果、協力者の戦略的重点或いは利用可能な資金の変化或いは外部要素(例えば買収)に基づいて、資源を移転したり、相互競争の優先事項を創造するために、開発或いは商業化計画を継続したり更新したりしないことを選択してはならない
•協力者は臨床試験を延期し、臨床試験計画に資金不足を提供し、臨床試験を停止或いは候補製品を放棄し、新しい臨床試験を繰り返し或いは行うことができ、或いは臨床試験候補製品の新しい調合を要求することができる
•我々と彼らとの合意で禁止されていない範囲では、協力者は、協力者が競争力のある製品の方が開発に成功する可能性があると考えているか、または私たちよりも経済的に魅力的な条項で商業化できることを前提として、第三者開発と直接または間接的に私たちの候補製品と競合する製品を独立して開発することができる
•私たちと協力して発見された候補製品は、私たちの協力者によって彼ら自身の候補製品や薬物と競争されるかもしれません。これは、協力者が資源を投入して私たちの候補製品を商業化することを停止する可能性があります
•私たちの1つまたは複数の候補製品にマーケティングおよび流通権利を有し、規制承認を得た協力者は、そのような製品をマーケティングおよび流通するために十分なリソースを投入していない可能性がある
•特許権、契約解釈、または第一選択開発プロセスにおける相違を含む協力者との相違は、候補製品の研究、開発または商業化の遅延または終了をもたらす可能性があり、候補製品に対して追加的な責任を負うこと、または訴訟または仲裁を引き起こす可能性があり、いずれも時間的で高価である可能性がある
•協力者は、私たちまたは彼らの知的財産権を正確に維持したり、守ったりすることができないかもしれないし、何らかの方法で私たちまたは彼らの固有の情報を使用して、訴訟を引き起こし、それによって、私たちの知的財産権や独自の情報を危険にさらしたり、または潜在的な訴訟に直面させたりすることができる
•協力者は第三者の知的財産権を侵害する可能性があり、これは私たちを訴訟と潜在的な責任に直面させるかもしれない
•協力者の便宜のために、協力を終了するかもしれませんが、終了すれば、適用可能な候補製品をさらに開発または商業化するために追加の資金を集める必要があるかもしれません。
協調プロトコルは、最も効率的な方法で、または候補製品の開発または商業化を引き起こさない可能性がある。SFJ、Alfasigma、または将来の任意のパートナーがビジネス統合に参加する場合、私たちの製品開発または商業化計画の継続的な追求と重視は、延期、減少、または終了される可能性があります。
私たちはもっと多くの協力を求めるかもしれません。もし私たちがそれができなければ、私たちは私たちの開発と商業化計画を変えなければならないかもしれません。
私たちの製品開発計画と候補製品の潜在的な商業化には多くの追加資金が必要になるだろう。私たちはSFJと協力してbentracimabを開発し、Alfasigmaと協力してヨーロッパやいくつかの他の地理的地域でbentracimabを商業化している。私たちの他の候補製品については、これらの候補製品を開発し、商業化するために、製薬やバイオテクノロジー会社とより多くの協力を確立することを決定するかもしれません。
私たちは適切な協力者を探すことで激しい競争に直面している。我々がどのような協力について最終的な合意に達するかどうかは,他に加えて,協力者の資源や専門知識の評価,提案された協力の条項や条件,提案された協力者のいくつかの要因の評価に依存する.これらの要因は、臨床試験の設計または結果、FDAまたは米国国外の同様の規制機関が承認する可能性、候補製品の潜在的市場、そのような候補製品の製造と患者への配送のコストと複雑性、競争製品の潜在性、このような所有権に挑戦すれば、考慮することなく、技術所有権の不確実性を含むことができる
挑戦と産業と市場状況。協力者はまた、同様の協力可能な指示を得るための代替候補製品または技術を考慮することができ、そのような連携が、私たちと私たちとの連携よりも私たちの候補製品に魅力的であるかどうかを考慮することができる。協力の交渉と記録は複雑で時間がかかる。また,最近では大手製薬会社間の業務合併数が大きく,将来の潜在的パートナー数の減少を招いている。
私たちはタイムリーで受け入れ可能な条項でもっと多くの協力を交渉することができず、交渉することさえできないかもしれない。それができなければ、候補製品の開発を減らし、その開発計画や私たちの1つ以上の他の開発計画を減少または延期し、潜在的な商業化を延期したり、販売やマーケティング活動の範囲を縮小したり、私たちの支出を増加させ、自費で開発または商業化活動を行わなければならないかもしれない。もし私たちが私たちの支出を増やし、私たち自身の開発や商業化活動に資金を提供することを選択すれば、私たちは追加の資本を得る必要があるかもしれないし、これらの資本は受け入れ可能な条件で私たちに提供できないかもしれないし、全く得られないかもしれない。もし私たちが十分な資金がなければ、私たちは私たちの候補製品をさらに開発したり、それらを市場に出して収入を作ることができないかもしれない。
私たちの知的財産権に関するリスクは
もし私たちが私たちの候補製品に関連する知的財産権を獲得または保護できなければ、私たちは私たちの市場で効果的に競争することができないかもしれない。
私たちは特許、商業秘密保護、および秘密協定の組み合わせによって、私たちの候補製品と私たちのELP技術に関連する知的財産権を保護します。私たちの成功は、米国や他の国で特許や他の知的財産権保護を取得し、維持する能力に大きく依存し、私たちの特許技術と候補製品に関連している。
本年度報告Form 10-Kの日までに、私たちの特許権は、私たちの候補製品または私たちのELP技術プラットフォームの様々な態様を保護するために、私たちが所有または許可している少なくとも22個の特許シリーズを含む。私たちは26件の米国特許、16件の米国特許出願、135件の外国特許、75件の外国特許出願を持っているか、または所有しています。私たちは、どの特許出願が発行されるか、それによって生成される特許の広さ、または発行された特許が無効であることが発見されるか、実行不可能であるか、または第三者によって脅かされるかどうかを保証することはできない。私たちが付与した特許の広さは、私たちの1つ以上の候補製品と競争する生物類似製品を含む競争相手の開発および商業化製品を阻止するのに十分であることを保証することはできない。さらに、これらの特許または特許発行後に私たちが所有または許可してくれた任意の他の特許に対するいかなる成功的挑戦も、私たちの任意の候補製品が商業化に成功するために必要な権利を奪う可能性がある。また、規制承認に遅延が生じた場合、特許保護の下で候補製品を販売する期間が短縮される可能性があります。
特許訴訟過程は高価で時間がかかる。私たちは商業的に合理的なコストで、またはすべての管轄区域でタイムリーな方法で、またはすべての管轄区域ですべての必要または望ましい特許出願を準備、提出、起訴することができないかもしれない。特許保護を受ける前に、開発および商業化活動においてなされた発明の出願可能な特許の態様を決定することができない可能性もある。さらに、私たちが将来加入する可能性のある任意の内部許可の条項によれば、私たちは、第三者から内部許可を得る技術を含む特許出願の準備、提出および起訴を制御する権利がないかもしれない。したがって、このような特許と特許出願は、私たちの業務の最適な利益に合った方法で起訴され、強制的に実行されないかもしれない。
私たちの特許権提供の保護に加えて、私たちは、特許保護されていないノウハウを商業秘密保護および秘密保護協定に依存して保護します。私たちは一般に、私たちのすべての従業員に彼らの発明を譲渡することを要求していますが、私たちのすべての従業員、コンサルタント、コンサルタント、および私たちのノウハウ、情報、または技術にアクセスできる任意の第三者が秘密協定を締結することを要求していますが、このようなすべての合意が正式に実行されているか、または私たちのビジネス秘密および他の機密ノウハウが漏洩しないことを保証することはできません。また,我々の競争相手は,我々のビジネス秘密に相当する知識,方法,ノウハウを自主的に開発する可能性がある.承認されれば、競争相手は私たちの製品を購入し、特許保護のない技術を開発する際に得られた競争優位性の一部または全部をコピーすることができる。もし私たちの任意の商業秘密が競争相手によって合法的に取得または独立して開発された場合、私たちは彼らまたは彼らが情報を伝達する人がその技術や情報を使用して私たちと競争することを阻止する権利がないだろう。もし私たちのビジネス秘密が競争相手に漏れたり、競争相手によって独立して開発されたりすれば、私たちの競争地位は損なわれるだろう。
また、私たちは私たちのビルの実体安全と、私たちの情報科学技術システムの実体と電子安全を維持して、私たちの資料と商業秘密の完全性とセキュリティを維持することに力を入れています。私たちはこのような個人、組織、そしてシステムに自信がありますが、私たちの合意や安全措置は破壊されるかもしれません。私たちはないかもしれません
どんな違反に対しても十分な救済措置が取られる。また,我々のビジネス秘密を守るための手順が不十分であると考えられれば,第三者による商業秘密の流用に対抗する十分な追跡権がない可能性がある.しかも、他の人たちは私たちの商業秘密と固有の情報を独立して発見するかもしれない。例えば、FDAは、商業秘密または他の固有情報と考えられる情報を含む、より多くの情報を定期的に公開するかどうかを検討しており、FDAの開示政策が将来どのように変化するかは不明である。もし私たちが私たちの技術に関連する非特許知的財産権の第三者への実質的な開示を阻止できず、私たちがこのような強制的に実行可能な商業秘密保護を持っている保証がなければ、私たちは私たちの市場で競争優位性を確立または維持することができないかもしれません。これは、私たちの業務、運営結果、および財務状況に大きな悪影響を及ぼす可能性があります。
特許条項は、私たちの各候補製品をカバーする特許期間を延長するために、ハッジ-ワックスマン修正案および同様の非米国法によって保護されていなければ、私たちの各候補製品をカバーする特許期間を延長するのに十分ではないかもしれない。
新製品候補製品の開発、テスト、および規制審査に要する時間を考慮すると、これらの候補製品を保護する特許は、これらの候補製品の商業化前または直後に満了する可能性がある。FDAが私たちの候補製品の発売を承認した時間、期限、条件によると、私たちの1つ以上の米国特許は、1984年の“薬品価格競争と特許期限回復法”(Hatch-Waxman修正案と略称する)とEUの同様の立法に従って限られた特許期間の延長を受ける資格がある可能性がある。Hatch-Waxman修正案は、製品開発およびFDA規制審査中に失われた有効特許期間の補償として、承認された製品をカバーする特許を最大5年間延長することを可能にする。特許期間の延長は,製品承認日から計14年間の余剰期限を超えてはならない。特許は1つしか延長できず、承認された薬剤、その使用方法、または製造方法に関する特許請求の範囲を延長することのみができる。しかし、適用の最終期限内に出願を提出できなかった場合、関連特許の満了前に出願を提出できなかった場合、または適用の要求を満たしていなかった場合、延期されない可能性がある。しかも、延期の長さは私たちが要求したものより短いかもしれない。もし私たちが特許期間の延長を得ることができない場合、あるいはこのような延長の期限が私たちが要求したものよりも短い場合、私たちはその製品に対して特許権を行使することができる期限が短縮され、競争相手はより早く承認され、競争製品市場に入るかもしれません。したがって、私たちは適用製品からの収入が減少する可能性があり、私たちの業務に実質的な悪影響を及ぼす可能性がある。
SFJプロトコルやAlfasigma再許可を含む現在および将来の第三者の知的財産権許可における私たちの義務を履行できなければ、私たちは私たちの業務に重要な権利を失うかもしれません。
私たちはいくつかの特許権とノウハウのライセンスに深刻に依存してbentracimabと私たちのELP技術を開発します。このような許可協定は勤勉さ、開発と商業化スケジュール、そして記念碑的な支払い、特許権使用料、保険、その他の義務を私たちに強要する。もし私たちが私たちの義務を履行しなければ、私たちの許可者は私たちの許可を終了する権利があるかもしれません。この場合、私たちは許可者から許可を得た知的財産権でカバーされた任意の製品を開発、製造、またはマーケティングすることができず、他の処罰に直面する可能性があります。このような状況は私たちの業務の見通しに大きな悪影響を及ぼすだろう。
我々の開発計画に必要となる可能性のある他の第三者技術や材料の許可は、将来的には得られない可能性があり、商業的に合理的な条項では得られない可能性があり、あるいは全く得られない可能性があり、これは私たちの業務や財務状況に大きな悪影響を及ぼす可能性がある。Bentracimabに関連するライセンスおよび再ライセンス知的財産権の起訴、保守、実行を制御しているにもかかわらず、私たちは達成されないかもしれない私たちのライセンシーと上流ライセンシーの協力が必要かもしれない。したがって、私たちはこれらの特許権の起訴、維持、実行が私たちの業務の最良の利益に合っているかどうかを決定することができません。もし私たちまたは私たちのライセンシーがこれらの特許を維持できなかった場合、または私たちまたは私たちのライセンシーがこれらの特許または特許出願の権利を失った場合、私たちが許可した権利は減少またはキャンセルされる可能性があり、そのような許可権利の対象となる任意の製品候補製品を開発および商業化する権利は悪影響を受ける可能性がある。上記に加えて、第三者から付与された特許権に関するリスクは、将来所有可能な特許権にも適用される。また、ライセンス契約下の開発義務を履行しなければ、このような合意に関連する地域ごとの特許権を失う可能性があり、世界的な特許権に影響を与えることになります。
私たちの現在または任意の未来の許可協定を終了することは、これらの合意の下での私たちの権利を減少またはキャンセルし、重要な知的財産権または技術に対する私たちの権利を含む、条項の悪い新しい合意を交渉したり、合意を回復したり、重要な知的財産権または技術に対する私たちの権利を失ってしまう可能性があります。上記のいずれも、他の候補製品を商業化することを阻止することができ、これは、私たちの経営業績および全体的な財務状況に実質的な悪影響を及ぼす可能性がある。
さらに、私たちが将来許可する知的財産権は、第三者が所有する知的財産権の下での従属許可であり、場合によっては複数のレベルを通過する可能性がある。したがって、私たちライセンシーの行動は、私たちがライセンス契約下のすべての義務を遵守していても、私たちの再ライセンス知的財産権を使用する権利に影響を及ぼすかもしれない。もし私たちのライセンシーまたは上流ライセンシーが彼らの合意下での義務を履行できなかった場合、これらの合意に従って、彼らは私たちに転任する権利を得たか、またはそのような合意が終了または修正された場合、私たちの候補製品を開発して商業化する能力は実質的に損なわれる可能性がある。
また、SFJプロトコルにより、SFJがbentracimabに関連するすべての資産の保証権益を付与しています。もし私たちがSFJに対する支払い義務を履行できなければ、SFJは権益保持者を優先的に保証する救済措置を行使する可能性があり、これは私たちのbentracimab知的財産権の損失を招き、私たちの業務は実質的に損害を受けるだろう。
また、Alfasigma再許可については、2021年6月に、AlfasigmaとMedmuneと再許可を付与する確認書を締結し、私たちがMedimmune許可下で治癒または救済されていないいくつかの義務に違反し、SFJが“プログラム移行”(SFJプロトコルの定義のような)を実行する理由があるが、そうしないことを選択した場合、Alfasigma再許可を私たちからMedmuneに譲渡するか、またはMedimmune許可を私たちからAlfasigmaに譲渡する可能性があり、私たちの業務は大きな損害を受ける可能性がある。“-私たちの財務状況および資本需要に関連するリスク-bentracimabに対する規制機関の承認を得た場合、またはSFJプロトコルが終了した場合、SFJプロトコルに従ってSFJに大量のお金を支払うことを要求される。もし私たちの業務に十分な資金やキャッシュフローがなければ、SFJプロトコルの下での支払い義務を履行することができ、SFJは私たちの資産の優先保証権益の保有者としてその救済措置を行使することができ、私たちの業務は実質的な損害を受ける可能性がある“
特許改革立法は、我々の特許出願をめぐる起訴および将来の特許の実行または保護をめぐる不確実性とコストを増加させる可能性がある。
これまでいくつかの法的原則は解決されておらず、米国特許で許可された権利要件の広さや解釈については、一貫した政策がないため、私たちが特許を得る能力は非常に不確実である。さらに、関連する法律、科学的、および事実的問題の複雑さのために、特許請求の範囲を支援および解釈するために必要な特許および特許出願の具体的な内容は、高度に不確実である。米国や他の国の特許法や特許法解釈の変化は,我々の知的財産権の価値を低下させたり,我々の特許保護の範囲を縮小したりする可能性がある。
例えば、2011年9月16日、“ライシー·スミス米国発明法”または“ライシー·スミス法案”が法律に署名された。“ライシー·スミス法案”は米国特許法を多くの重大な改正を行った。その中には特許出願起訴方式に影響を与える条項が含まれており、特許訴訟に影響を与える可能性もある。米国特許商標局(USPTO)は、“ライシー·スミス法案”の全面的な実施を管理するために、新たな未検査の法規やプログラムを制定し、“ライシー·スミス法案”に関連する特許法の多くの実質的な改正、特に最初の提出条項の改正が、2013年3月に発効した。Leahy-Smith法案はまた、第三者が発行された特許に挑戦しやすく、特許出願の起訴に介入するためのいくつかの手続きを導入した。最後に、“ライシー·スミス法案”には、米国特許商標局がその実施のために新しい法規を発表することを要求する新しい法定条項が含まれており、裁判所は新しい法規の条項を解釈するのに数年かかるかもしれない。Leahy-Smith法案が私たちの業務運営と私たちの知的財産権の保護と実行にどのような影響を与えるのかまだ分からない。しかし、Leahy-Smith法案とその実施は、私たちの特許出願をめぐる起訴と、私たちの将来の特許の実行または保護の不確実性とコストを増加させるかもしれない。また、米国最高裁判所は近年、いくつかの特許事件に対して裁決を下しているか、場合によっては利用可能な特許保護範囲を縮小するか、場合によっては特許権者の権利を弱体化させている。このような事件の結合は,我々の将来の特許取得能力に関する不確実性の増加に加えて,特許価値に関する不確実性をもたらしている, 一度手に入れたら。米国議会、連邦裁判所、および米国特許商標局の行動によれば、特許を管理する法律および法規は、予測不可能な方法で変化する可能性があり、それにより、私たちが新しい特許を取得したり、私たちが所有または許可または将来獲得可能な特許を実行する能力を弱める可能性がある。私たちのノウハウをカバーしている特許を取得し、実行し、保護できないことは、私たちのビジネスの見通しと財務状況に実質的な悪影響を及ぼすだろう。
同様に、他の国または管轄区域の特許法律および法規の変化、それらを実行する政府機関の変化、または関連政府当局が特許法律または法規を実行する方法の変化は、私たちが新しい特許を獲得したり、私たちが将来獲得する可能性のある特許を実行する能力を弱める可能性がある。また、一部の外国の法律の専有権に対する保護程度や方式は米国の法律とは異なる。したがって、私たちはアメリカでも海外でも、私たちの知的財産権を保護して守ることで大きな問題に直面するかもしれない。例えば、ある発明の特許がある特定の国が発行された後に、他の国で同じ発明の特許が発行されていない場合、またはその発明の有効性、実行可能性、または範囲について任意の司法解釈がなされる場合
ある国で発行された特許における特許の請求項または書面記述または授権が、他の国で発行される対応する特許の解釈と異なる場合、これらの国で私たちの知的財産権を保護する能力が制限される可能性がある。米国や他の国の特許法や特許法解釈の変化は,我々の知的財産権の価値を大きく低下させたり,我々の特許保護の範囲を縮小したりする可能性がある。
私たちは私たちの特許を保護したり強制したりする訴訟に巻き込まれるかもしれないが、これは高価で時間がかかり、成功しないかもしれない。
競争相手は私たちが申請した特許を侵害するかもしれない。権利侵害や不正使用に対抗するために、私たちは費用が高く時間がかかるかもしれない侵害請求を要求されるかもしれない。私たちが第三者に対して私たちの候補製品のうちの1つをカバーする特許を強制的に執行するために法的訴訟を提起した場合、被告は、私たちの製品または候補製品をカバーする特許を無効および/または強制的に執行できないと反訴することができる。米国の特許訴訟では、特許が無効および/または強制的に実行できないと主張する反訴が一般的であり、第三者は多くの理由から特許が無効または強制的に実行できないと断言することができる。侵害訴訟では、裁判所は、私たちが主張する特許主張が無効および/または強制的に実行できないと判断することができ、または、私たちの特許主張が論争のある技術を含まないことを理由に、他方の関連技術の使用を阻止することを拒否することができる。第三者も米国や海外の行政機関に類似したクレームを出すことができ、訴訟範囲外でも同様である。これらの仕組みには再審査、贈与後の審査、各方面間外国の管轄区域と同等の手続き(例えば、反対手続き)を検討する。このような訴訟は私たちの特許がこれ以上私たちの候補製品をカバーしないように撤回したり修正したりするかもしれない。法的に無効と実行不可能と断言された後の結果は予測できない。例えば、有効性の問題について、私たちは、私たち、私たちの特許弁護士、および特許審査員が起訴中に知らなかった無効な以前の技術を確認することができない。もし被告が無効および/または強制執行できない法的主張に勝った場合、私たちは私たちの候補製品の少なくとも一部またはすべての特許保護を失うだろう。任意の訴訟または弁護手続の不利な結果は、私たちの1つまたは複数の特許を無効または狭義に解釈されるリスクに直面させる可能性があり、私たちの特許出願を発行できないリスクに直面させ、私たちの業務に実質的な悪影響を及ぼす可能性がある。
第三者によって開始されるか、または我々によって提起された干渉プログラムは、我々の特許出願に関連する発明の優先権を決定するために必要である可能性がある。不利な結果は、関連技術の使用を停止することを要求するか、または勝者側の特許権の下で許可を得るように強要される可能性がある。また、勝利者が商業的に合理的な条項で許可証を提供しなければ、私たちの業務は損害を受ける可能性があります。訴訟や介入訴訟に対する私たちの弁護は失敗する可能性があり、成功しても巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性があります。私たちは私たちの知的財産権が盗用されることを防ぐことができないかもしれないが、特にこれらの法律がアメリカのようにこれらの権利を十分に保護していないかもしれない国では。
さらに、知的財産権訴訟は大量の開示を必要とするため、このような訴訟の間、私たちのいくつかの機密情報は開示によって漏洩される可能性がある。聴聞、動議、または他の一時的手続き、または事態発展の結果を公開することもできる。もし証券アナリストや投資家がこれらの結果がマイナスだと思っていれば、私たちの普通株の価格に実質的な悪影響を及ぼす可能性がある。
私たちは第三者からの知的財産権の許可や取得に成功しないかもしれませんが、これは私たちの候補製品を開発して商業化する必要があるかもしれません。
第三者は、私たちの候補製品の開発と商業化に非常に重要または必要な特許権を含む知的財産権を持つことができる。私たちは第三者の特許やノウハウを使用して私たちの候補製品を商業化する必要があるかもしれません。この場合、私たちはこれらの第三者からこのような知的財産権の許可を取得または取得することを要求されますが、私たちは商業的に合理的な条項や根本的にはできないかもしれません。第三者知的財産権の許可または買収は競争分野であり、より多くの老舗企業は、魅力的または必要と考えられる第三者知的財産権許可または買収戦略をとることができる。これらの老舗会社はその規模、資本資源及び更に強い臨床開発と商業化能力のため、私たちより競争優位を持っているかもしれない。しかも、私たちを競争相手と思っている会社は私たちに権利を譲渡したり許可したりしたくないかもしれない。私たちはまた私たちの投資を適切なリターンを得るための条項で許可したり、第三者の知的財産権を取得することができないかもしれないし、全くできないかもしれない。もし私たちが必要な第三者知的財産権を得ることに成功したり、私たちの既存の知的財産権を維持することができなければ、関連プログラムや候補製品の開発を放棄しなければならないかもしれません。これは私たちの業務に実質的な悪影響を及ぼすかもしれません。
第三者は私たちが彼らの知的財産権を侵害したと告発する法的訴訟を提起するかもしれないが、結果はまだ確定していない。
私たちの現在と未来の候補製品が商業化されるにつれて、私たちに対する特許侵害請求の可能性が増加している。私たちは私たちの現在と未来の候補製品が他の側の特許や他の独占権を侵害しないという保証はなく、競争相手または他の当事者は私たちがどんな状況でも彼らの独占権を侵害していると主張するかもしれない。私たちは、米国特許商標局で行われている干渉または派生訴訟を含む、現在および将来の候補製品知的財産権に関連する対抗性訴訟または訴訟に参加または脅威になる可能性がある。このような主張に法的根拠がないと考えても、管轄権のある裁判所は、これらの第三者特許が有効で、強制的かつ侵害されていると判断する可能性があり、これは、bentracimab、PB 6440、または任意の未来の候補製品を商業化する能力に悪影響を及ぼす可能性がある。連邦裁判所でこのような米国特許の有効性に挑戦することに成功するためには,有効性推定を克服する必要がある。この負担は重いため,このような米国特許主張の無効について明確かつ納得できる証拠を提出することを要求するため,管轄権のある裁判所が我々の意見に同意する保証はなく,このような米国特許の主張は無効であることを宣言する.さらに、私たちの技術分野に大量の特許があることを考慮して、私たちは私たちが既存の特許を侵害していないか、あるいは私たちが将来付与される可能性のある特許を侵害しないと確信できない。
将来的に訴訟を開始し、これらまたは他の特許の有効性に挑戦することを決定する可能性があるが、私たちは成功しない可能性があり、米国および海外の裁判所または特許庁は、このような特許の有効性を維持することができる。さらに、特許出願は、発行されるまでに長年の時間を要する可能性があり、提出後18ヶ月以上秘密にされている可能性があり、未解決の特許声明は発行前に修正することができるので、処理されている出願が、私たちの候補製品の製造、使用、または販売によって発行された特許を侵害する可能性がある可能性がある。いつ提出されても、私たちは関連する第三者特許または特許出願を識別できないかもしれないし、第三者特許が無効であるか、または私たちの候補製品や活動によって侵害されていないと誤って結論を出す可能性がある。もし特許所有者が私たちのある候補製品がその特許を侵害したと思っていれば、私たちの技術が特許保護を受けても、特許所有者は私たちを起訴するかもしれない。また、私たちは非執行実体の特許侵害請求に直面する可能性があり、これらの実体は関連する薬品収入がないため、私たち自身の特許の組み合わせは彼らに抑止力がないかもしれない。特許侵害訴訟が脅かされたり、私たちに訴訟が提起されたりすると、実際または脅威訴訟の標的となる薬物または候補製品の研究、開発、製造、または販売を停止または延期させることを余儀なくされる可能性がある。
もし私たちが第三者の知的財産権を侵害していることが発見された場合、私たちは第三者からライセンスを取得して、私たちの候補製品を商業化し続けることができるかもしれない。しかし、私たちは商業的に合理的な条項や必要な許可証を得ることができないかもしれない。許容可能な条項で許可を得ることができても,これらの権利は非排他的である可能性があり,これは我々の競争相手が我々に許可する同じ技術や知的財産権を獲得する可能性がある.私たちが必要なライセンスを取得できなければ、私たちの技術に基づいて候補製品を効果的に販売することができないかもしれません。これは、私たちが収入を創出したり、利益を達成する能力を制限し、私たちの運営を維持するのに十分な収入を生成することを阻止するかもしれません。あるいは、私たちは私たちの権利侵害製品を再設計する必要があるかもしれないし、それは不可能かもしれないし、大量の時間とお金の支出が必要かもしれない。場合によっては、私たちは裁判所の命令を含めて、私たちの候補製品の商業化を停止させることを余儀なくされるかもしれない。また、このような訴訟や訴訟のいずれにおいても、関連特許を故意に侵害していることが発見された場合、損害賠償および弁護士費の3倍を含む巨額の金銭損害賠償責任を負う可能性がある。権利侵害の発見は、候補製品を商業化することを阻止したり、いくつかの業務運営を停止させたりする可能性があり、これは私たちの業務を損なう可能性があります。第三者が私たちが彼らの機密情報や商業秘密を盗用したと主張した場合、私たちの業務に似たような負の影響を及ぼす可能性がある。
私たちが特許や他の専有権に関連する訴訟や他の手続きを弁護したり、訴訟を提起したりするコストは巨大である可能性があり、私たちに有利な問題を解決しても、訴訟は私たちの経営陣の注意をそらすだろう。私たちのいくつかの競争相手は、彼らがより多くの資源を持っているので、私たちよりも複雑な特許訴訟の費用を効果的に受けるかもしれない。特許訴訟または他の訴訟の開始と継続による不確実性は、私たちの研究開発努力を延期し、私たちが運営を継続する能力を制限する可能性がある。
私たちは、従業員、コンサルタント、または独立請負業者が第三者の機密情報を不適切に使用または漏洩したというクレームを受ける可能性がある。
私たちが雇った人たちは以前他のバイオテクノロジーやバイオ製薬会社に雇われていた。私たちは、私たちの従業員、コンサルタント、およびコンサルタントが、私たちのために働いているときに他人の固有情報またはノウハウを使用しないことを保証するために努力しているが、私たちは、私たちまたは私たちの従業員、コンサルタント、または独立請負業者が、私たちの従業員の前の雇用主または他の第三者の機密情報を意図的または他の方法で使用または漏洩したというクレームを受ける可能性がある。私たちはまた、私たちの未来の特許所有権に対する元雇用主や他の第三者のクレームに直面する可能性がある。このような疑いに対抗するために訴訟を提起する必要があるかもしれない。これらのクレームを弁護する際に成功する保証はなく、たとえ私たちが成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。
私たちは私たちの未来の特許と他の知的財産権の発明権または所有権に挑戦するクレームを受けるかもしれない。
私たちはまた、元従業員、協力者、または他の第三者による私たちの特許出願、私たちの将来の特許、または他の知的財産権所有権利益のクレームを受ける可能性があります。私たちは将来的に所有権紛争の影響を受けるかもしれません。例えば、私たちの候補製品の開発に参加するコンサルタントや他の人の義務紛争のためです。私たちの政策は、知的財産権の概念や開発に参加する可能性のある私たちの従業員と請負業者が合意に署名し、そのような知的財産権を私たちに譲渡することを要求しているにもかかわらず、私たちは実際に私たちが自分の知的財産権と見なしているすべての当事者とこのような合意を実行することができない可能性があり、このような当事者との合意が潜在的な挑戦に直面したときに維持されるかどうか、あるいは違反されないかどうかを決定することはできません。知的財産権の譲渡は自動的に実行されない可能性があり、または譲渡協定が違反される可能性があり、これらおよび他の挑戦在庫または所有権のクレームに対抗するために訴訟を提起する必要があるかもしれない。もし私たちがこのようなクレームを弁護することができなければ、金銭損害賠償を支払うことに加えて、貴重な知的財産権、例えば貴重な知的財産権の独占所有権や使用権を失う可能性がある。このような結果は私たちの業務に実質的な悪影響を及ぼすかもしれない。私たちがこのようなクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。
第三者に依存して私たちのビジネス秘密を共有することを要求し、これは、競争相手がこれらの秘密または私たちのビジネス秘密が流用または開示されていることを発見する可能性を増加させる。
もし私たちがbentracimab、PB 6440、または任意の未来の候補製品を製造または商業化するために第三者に依存し続ける場合、または私たちがより多くの第三者と協力してbentracimab、PB 6440、または任意の未来の候補製品を開発し続ける場合、私たちは時々彼らと商業秘密を共有しなければならない。共同研究開発計画を継続することも可能であり、これらの計画は、研究開発パートナーシップや同様の合意の条項に基づいてビジネス秘密を共有することを要求する可能性がある。独自の情報の研究または開示を開始する前に、当社のコンサルタント、従業員、第三者請負業者およびコンサルタントと秘密協定、材料譲渡協定、コンサルティング協定、または他の同様の合意を締結することによって、当社のノウハウを部分的に保護することを求めています。これらの協定は、一般に、私たちの商業秘密を含む、第三者が私たちの機密情報を使用または開示する権利を制限する。第三者と協力する際に契約条項が採用されているにもかかわらず、商業秘密および他の機密情報を共有する必要は、そのような商業秘密が私たちの競争相手に知られ、無意識に他の人の技術に組み込まれているか、またはこれらの合意に違反した場合に開示または使用されるリスクを増加させる。私たちの独自の地位が私たちのノウハウおよびビジネス秘密にある程度基づいていることを考慮すると、競争相手は、私たちのビジネス秘密または他の許可されていない使用または開示が、私たちの業務および運営結果に悪影響を及ぼす可能性があることを発見します。
さらに、これらの合意は、通常、私たちのコンサルタント、従業員、第三者請負業者、およびコンサルタントが、私たちのビジネス秘密に関連する可能性のあるデータを発行する能力を制限します。私たちは私たちのビジネス秘密を保護しようと努力しているにもかかわらず、私たちはこれらの合意の当事者が私たちの技術的ノウハウや他の商業秘密を不正に開示したり、使用したりすることを防ぐことができないかもしれない。さらに、私たちは私たちが可能であるか、または私たちの機密情報またはノウハウおよびプロセスに接触したすべての当事者とそのような合意に到達したことを保証することができない。許可されていない使用と開示を監視することは困難であり、私たちはまた私たちのノウハウを保護するために私たちが取った段階が有効かどうか分からない。これらの合意当事者である任意の協力者、科学コンサルタント、従業員、請負業者、およびコンサルタントがこれらの合意に違反または違反する任意の条項であれば、このような違反または違反に対応するための十分な救済措置がない可能性があり、したがって、私たちの商業機密を失う可能性がある。さらに、私たちのパートナー、協力者、または他の人が私たちに許可または開示した機密情報が意図的に漏洩されたり、違反されたり、違反された場合、私たちはその機密情報の所有者に責任を負うかもしれない。特許訴訟のように、第三者に私たちの商業秘密を不正に取得して使用することを強制することは高価で時間がかかり、結果は予測できない。しかも、アメリカ以外の裁判所は商業機密を保護することをあまり望まないこともある。
いくつかの特許については、私たちは限られた地理的保護しか持っていないかもしれないし、私たちは世界各地で私たちの知的財産権を保護できないかもしれない。
世界のすべての国で特許出願を提出して起訴し、私たちの候補製品特許を保護することは目を引くほど高価になるだろう。競争相手は私たちが特許保護を受けていない司法管轄区域で私たちの技術を使用して自分の製品を開発することができ、また、他の侵害製品を私たちが特許保護を持っているが執行権がアメリカやヨーロッパに及ばない地域に輸出することもできる。これらの製品は私たちの候補製品と競争するかもしれません。私たちの将来の特許や他の知的財産権は彼らの競争を効果的に阻止するのに十分ではないかもしれません。
しかも、私たちは承認前に国と地域の特許出願を放棄することに決定するかもしれない。すべての国や地域の特許出願の審査は独立した手続きだ。したがって、同じファミリーの特許出願は、米国のようないくつかのドメインで特許として発行されることができるが、異なる範囲の特許要件として特許として発行される可能性があり、さらには他のドメインで拒否される可能性もある。同様に一般的な場合は、国によって同じ候補製品または技術の特許保護範囲が異なる可能性があることである。
私たちが予想している重要な市場で私たちの知的財産権を保護するつもりですが、私たちが候補製品をマーケティングしたいかもしれないすべての司法管轄区域で同様の努力を開始または維持できることを確実にすることはできません。したがって、これらの国で私たちの知的財産権を保護するための努力が不十分である可能性があり、これは、すべての予想される重要な海外市場で私たちの候補製品を商業化することに成功した能力に悪影響を及ぼす可能性がある。もし私たちが知的財産権の保護に困難に直面したり、他の理由で私たちの業務に重要な知的財産権を効果的に保護できなければ、これらの権利の価値は低下する可能性があり、私たちはこれらの管轄区域の他の人からの追加的な競争に直面するかもしれない。
いくつかの司法管轄区の法律は知的財産権の保護程度はアメリカとヨーロッパの法律或いは規則に及ばず、多くの会社はこれらの司法管轄区の保護とこのような権利を保護する時に重大な困難に直面している。特定の国の法律制度、特に特定の発展途上国の法律制度は、特許、商業秘密、および他の知的財産権の実行を支持しておらず、これは、私たちの将来の特許を侵害したり、私たちの専有権を侵害する方法で競争製品を販売する行為を阻止することを困難にする可能性がある。他の管轄区域で私たちの特許権の訴訟を強制的に執行することは、成功するかどうかにかかわらず、巨額のコストを招く可能性があり、業務の他の方面への私たちの努力と注意を移動させることは、私たちの将来の特許が無効または狭義に解釈されるリスクに直面する可能性があり、私たちの特許出願を特許として発表しないリスクに直面させ、第三者が私たちにクレームを提起する可能性がある。私たちは私たちが起こしたどんな訴訟でも勝てないかもしれないし、判決された損害賠償や他の救済措置(もしあれば)は商業的な意味がないかもしれない。したがって、私たちが世界各地で私たちの知的財産権を実行する努力は、私たちが開発または許可した知的財産権から顕著なビジネスメリットを得るのに十分ではないかもしれません。
一部の国にも強制許可法があり,これらの法律により特許権者は第三者に強制的に許可を付与される可能性がある。さらに、いくつかの国は、政府機関または政府請負業者に対する特許の実行可能性を制限している。これらの国では,特許権者の救済措置が限られている可能性があり,このような特許の価値を大きく低下させる可能性がある。もし私たちが第三者に私たちの業務に関連する任意の特許の許可を与えなければ、私たちの競争的地位が損なわれる可能性がある。
私たちの特許保護の獲得と維持は、政府特許機関によって提出された様々なプログラム、書類提出、費用支払い、および他の要求を遵守することに依存し、これらの要求に適合しなければ、私たちの特許保護は減少またはキャンセルされる可能性がある。
我々の特許および/またはアプリケーションおよび将来入手可能な任意の特許権の有効期間内に、定期保守費、継続費、年会費、および特許および/またはアプリケーションに関する様々な他の政府特許機関に、米国特許商標局および米国以外の様々な政府特許機関に費用を支払わなければならない。さらに、米国特許商標局および様々な非米国政府特許機関は、特許出願中にいくつかのプログラム、文書、費用支払い、および他の同様の規定を遵守することを要求する。多くの場合、特許または特許出願の予期しない失効は、滞納金を支払うことによって、または規則を適用する他の方法によって救済することができる。しかしながら、場合によっては、規定を遵守しないことは、特許または特許出願が放棄または失効される可能性があり、それにより、関連法ドメインの特許権の一部または全部が失われる可能性がある。この場合、潜在的な競争相手が市場に参入する可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性がある。
私たちが取得したまたは取得可能ないかなる商標も侵害される可能性があり、または他の方法で違反または成功して挑戦し、それによって私たちの業務に損害を与える可能性がある。
私たちは商標を手段として、私たちの候補製品(発売が許可されたら)を私たちの競争相手の薬物と区別したい。私たちが新しい商標を選択して登録を申請すると、私たちの商標申請は承認されないかもしれない。第三者は、私たちの商標出願または商標をキャンセルしようとしたり、他の方法で商標の使用に挑戦しようとしたりすることができる。もし私たちの商標が成功的に挑戦されれば、私たちは私たちの薬を再命名することを余儀なくされるかもしれません。これはブランド認知度の喪失を招き、広告と新しいブランドをマーケティングするために資源を投入する必要があるかもしれません。私たちの競争相手は私たちの商標を侵害したり、他の方法で私たちの商標を侵害したりする可能性があり、私たちは私たちの商標を実行するのに十分な資源がないかもしれない。このようなどんな事件も私たちの業務に重大な悪影響を及ぼす可能性がある。
知的財産権は必ずしも私たちの競争優位に対するすべての潜在的な脅威を解決できるとは限らない。
私たちの知的財産権が提供する未来の保護の程度は不確定であり、知的財産権には限界があるため、私たちの業務を十分に保護できないか、あるいは競争優位性を維持することができるかもしれない。以下の例は例示的である
•他の会社は、私たちの候補製品と似ているか、または他の側面で競争力のある製品を生産することができるかもしれませんが、これらの製品は、私たちの現在または未来の特許の請求項の範囲内ではありません
•私たちの1つまたは複数の候補製品の製造、使用、販売、要約販売、または輸入に必要な許可内許可は、許可者によって終了することができる
•私たちまたは未来の協力者は、私たちが発表したまたは未来に発表された特許または係属中の特許出願がカバーする最初の発明をした人ではないかもしれない
•私たちまたは未来の協力者は、私たちのいくつかの発明をカバーする最初の特許出願を提出した人ではないかもしれない
•他の人は私たちの知的財産権を侵害することなく、類似または代替技術を開発したり、私たちの任意の技術を複製したりすることができる
•私たちが処理している特許出願は発行された特許を生成しない可能性がある
•競争相手の法的挑戦のために、私たちが所有しているまたは許可されている特許は、無効または実行不可能と認定される可能性がある
•私たちが所有または許可した発行された特許は、すべての国/地域の候補製品のすべての側面をカバーしないかもしれない
•私たちの競争相手は特許権のない国で研究や開発活動を行い、これらの活動から学んだ情報を利用して競争力のある製品を開発し、私たちの主要な商業市場で販売するかもしれません
•私たちは他の特許を申請できるノウハウを開発しないかもしれない
•他の人たちの特許は私たちの業務に悪影響を及ぼすかもしれない。
このような事件が発生した場合、私たちの業務、運営結果、そして将来性を深刻に損なう可能性がある。
法律と規制コンプライアンスに関するリスク
私たちと顧客、医療保健提供者、医師と第三者支払者との関係は、連邦と州医療詐欺と乱用法律、虚偽クレーム法律、健康情報プライバシーと安全法律、その他の医療法律法規の制約を直接または間接的に受けている。もし私たちがこのような法律を遵守できないか、または完全に遵守できなければ、私たちは巨額の処罰に直面するかもしれない。
米国や他の地域の医療提供者、医師、第三者支払者は、市場で承認された任意の候補製品を推薦し、処方する上で主な役割を果たすだろう。私たちの現在と未来の医療保健専門家、主要な調査者、コンサルタント、顧客と第三者支払者の手配は、連邦反バックル法、連邦民事と刑事虚偽請求法、医療情報プライバシー法、一般的に医師支払い陽光法案と呼ばれる法律、これらの法律に基づいて公布された法律を含むが、これらに限定されない様々な連邦と州詐欺と乱用法律、その他の医療法律の制約を受けている。これらの法律は,我々の臨床研究,提案された販売,マーケティング,教育計画,医療専門家との他のインタラクションに影響を与えるであろう。さらに、私たちは連邦政府と私たちが業務を展開したり、業務を展開する可能性のある州の患者プライバシー法の制約を受けるかもしれない。私たちの運営に影響を与える法律は含まれているが、これらに限定されない
•連邦反リベート法規は、個人または実体が直接または間接的に、現金または実物の形態で直接または間接的に現金または実物の形態で直接または間接的に請求し、受け取り、提供または提供または任意の報酬(任意のリベート、賄賂またはリベートを含む)を支払うことを禁止するか、または他人に個人を推薦させるか、または購入、レンタル、注文または手配、購入、レンタル、注文または手配、連邦医療保険および医療補助計画などの連邦医療計画に従って支払い可能な任意の商品、施設、物品またはサービスの全部または一部の支払いを推薦することを禁止する。“報酬”という言葉は価値のあるものを含むと広く解釈されている。いくつかの法定例外状況と規制安全港保護のいくつかの一般的な活動は起訴されないが、例外状況と安全港の範囲は狭い。報酬に関するアプローチは、例外または避難港の資格に適合していない場合、処方、購入、または推薦を誘導するために告発される可能性があるため、審査される可能性がある。一人はこの規制を実際に理解する必要はなく、違反を実施するためにその具体的な意図を持つ必要もない。さらに、2010年に法律となった“医療·教育和解法案”(または総称して“ACA”)改正された“患者保護·平価医療法案”の規定に署名し、政府は、連邦反ダンピング法違反による物品やサービスのクレームが虚偽または詐欺的クレームを構成することを含む連邦“虚偽請求法”に基づいていると断言することができる
•連邦民事および刑事虚偽申告法は、連邦虚偽申告法を含むが、一般市民によって民事通報者または法定訴訟によって強制的に実行することができるが、個人または実体が虚偽または詐欺的な提出を故意にまたは提出することを禁止する連邦政府支払いまたは承認クレームを禁止し、連邦医療保険、医療補助および他の政府支払者を含む、または虚偽または詐欺的クレームに関連する虚偽記録または陳述の作成、使用または使用を故意に作成、使用するか、または連邦政府への支払いの義務を回避、減少または隠蔽することを禁止する。クレームには、米国連邦政府に提出された金銭または財産に対する“任意の請求または要求”が含まれている。これらの法律により、いくつかの製薬会社や他のヘルスケア会社が起訴され、顧客に製品を無料で提供する疑いがあるため、顧客がその製品の連邦計画に料金を請求することを希望している。他社は未承認で精算できない用途に製品を販売したことで虚偽のクレームを起こしたとして起訴された
•1996年の連邦健康保険携帯および責任法案、またはHIPAAは、追加の連邦刑法を制定し、それ以外に、個人第三者支払人、重大な事実の偽造、隠蔽または隠蔽、または医療福祉、プロジェクトまたはサービスの提供または支払いに関連する任意の重大な虚偽、架空、または詐欺的な陳述を含む、任意の医療福祉計画を知り、意図的に実行または実行しようとするいかなる人も、または重大な虚偽、架空または詐欺的陳述を行うことを禁止する。連邦反リベート法規と同様に、個人または実体は、この法規または法規違反の具体的な意図を実際に理解する必要がなく、違反を実施することができる
•HIPAAは、2009年の“健康情報技術促進経済·臨床健康法案”(HITECH)及びその実施条例改正により、健康計画、医療情報交換センター及び特定の医療保健提供者の個人身分健康情報のプライバシー、安全及び伝送について、“カバーエンティティ”と呼ばれるいくつかの要求を提出し、それぞれのHIPAA“業務パートナー”は、個人識別健康情報の使用又は開示に関連する特定のサービスを実行する独立請負業者及びその使用、開示、又は他の方法で個人身分健康情報を処理する下請け業者である。HITECHはまた新しい民事罰金等級を作成し、HIPAAを修正し、民事と刑事処罰を商業パートナーに直接適用し、州総検察長に新しい権力を与え、連邦裁判所に民事訴訟を提起し、損害賠償または禁止令を要求してHIPAAを実行し、連邦民事訴訟の提起に関連する弁護士費と費用を求めることができる
•連邦透明性法は、(1)医師(医師、歯科医師、視光師、足科医師および脊椎マッサージ師を含む)、他の保健専門家(例えば、医師アシスタントおよび看護師従事者)および教育病院に支払うお金または他の“価値移転”、および(2)医師およびその直系親族が所有する所有権および投資権益を含む、いくつかの薬品、医療機器、生物製品、および医療用品の製造業者に毎年CMSに以下の情報を報告することを要求する連邦“医師支払い日光法案”を含む
•州および外国の法律は、上述した各連邦法律および法規に相当し、州法律は、医師および他の医療保健提供者への支払いおよび他の方法での価値移転、マーケティング支出または薬品定価に関する情報を製造業者に報告することをメーカーに要求する;州法律は、製薬会社が製薬業界の自発的コンプライアンスガイドラインおよび連邦政府によって公布された関連コンプライアンスガイドラインを遵守することを要求するか、または他の方法で医療保健提供者への支払いを制限することを要求する;州および地方の法律は、医薬品販売代表登録を要求する
•健康情報のプライバシーや安全を管理する国や外国の法律がある場合もあり、その多くの法律は互いに大きく異なり、HIPAAに先を越されず、コンプライアンス作業を複雑化させることが多い。例えば、一般的なデータ保護条例(EU)2016/679、またはGDPRは、欧州経済地域(EEA)に位置する個人からデータを収集および/または処理する任意のエンティティにプライバシーおよびセキュリティ義務を課す。GDPRによると、重大な違反行為には最高2000万ユーロまたは侵害者の世界年商4%の罰金を科すことができ、金額が大きい者を基準とする。また、2018年6月28日、カリフォルニア州は2020年1月1日に発効する“カリフォルニア消費者プライバシー法案”を公布した。CCPAはカリフォルニア州住民により大きな権利を与え、彼らの個人情報にアクセスして削除し、特定の個人情報から退出することを選択することができる
情報を共有し,それらの個人情報をどのように使用するかに関する詳細な情報を受信する.CCPAは違反行為に対する民事処罰と,データ漏洩に対する個人訴権を規定しており,データ漏洩訴訟が増加すると予想される。また、カリフォルニアの有権者は2020年11月3日の選挙で、CPRAと略称する新しいプライバシー法、すなわちカリフォルニアプライバシー権法案を可決した。CPRAは2023年1月1日から、消費者の特定の敏感な個人情報に対する権利の拡大を含むCCPAを重大に改正する。CPRAはまた、CCPAおよびCPRAを実施し実行する権限を付与される新しい国家機関を作成した。他の州で提案または公布された新しい立法は、全国のデータプライバシー環境を形成し続けるだろう。例えば、バージニア州は2021年3月2日にバージニア州消費者データ保護法(CDPA)を公布し、2023年1月1日に施行され、コロラド州は2021年6月8日にコロラド州プライバシー法(CPA)が公布され、2023年7月1日に施行される。CPAとCDPAはCCPAやCPRAに類似しているが,これらの州のプライバシー法規の側面は依然として不明であり,さらなる法的不確実性を招いている。GDPR、CCPA、CPRA、CDPA、CPAまたは他の法律、法規、既存の法律および法規の改正または再解釈、およびプライバシー、データ保護、データ転送、データ現地化または情報セキュリティに関連する契約または他の義務を遵守するためには、新しい法律要件を満たし、巨額の運営コストを発生させ、データ実践および政策を修正し、私たちの業務運営を制限できるように、私たちのサービスを変更する必要があるかもしれません。一部の観察者は、CCPAはアメリカのより厳しい州プライバシー立法傾向の開始を示している可能性があると指摘している, これは私たちの潜在的な責任を増加させ、私たちの業務に悪影響を及ぼすかもしれない。私たちのコンプライアンス作業を複雑化させる以外に、これらの法律を守らないことは処罰や重大な法的責任を招く可能性がある。
これらの法律の広汎性、および既存の法定例外状況と安全港の規制の狭さのため、私たちのいくつかの商業活動は1つ以上のこのような法律の挑戦を受けるかもしれない。政府当局は、私たちの業務実践が現在または未来に適用される詐欺および乱用または他の医療保健法律および法規に関連する現行または未来の法規、法規または判例法に適合していない可能性があると結論するかもしれない。もし私たちの運営がこれらの法律または他の私たちに適用される可能性のある任意の政府法規に違反していることが発見された場合、私たちは民事、刑事および行政処罰、損害賠償、罰金、返還、監禁、連邦および州政府の援助から除外された医療計画(例えばMedicareおよびMedicaid)から除外され、追加の報告要件および監督を受ける可能性があります(これらの法律違反に関する告発、契約損害、利益および将来の収益の減少、名声損害、および私たちの業務の削減または再編を解決するために、当社の誠実な合意または同様の合意の制約を受ける場合)、これらはいずれも私たちの業務を損なう可能性があります)。
私たちはこれらの法律に違反するリスクが増加していることが発見された。その多くの法律は規制部門や裁判所の十分な説明を受けておらず、それらの条項は様々な解釈ができるからだ。私たちが第三者の業務配置と適用される医療法律や法規に適合するように努力することは、多くのコストに関連することを確実にします。これらの法律に違反して私たちにとった行動は、たとえ私たちが弁護に成功しても、巨額の法的費用を招き、私たちの経営陣の業務運営への注意をそらす可能性があります。持続的に変化するコンプライアンス環境、および異なるコンプライアンスおよび/または報告要件を有する複数の司法管轄区域の必要性に適合するために、強力かつ拡張可能なシステムを確立し、維持することは、医療会社が1つまたは複数の要件と衝突する可能性を増加させる。
私たちがbentracimab、PB 6440、または任意の未来の候補製品の規制承認を得ても、それらは持続的な規制によって監視されるだろう。
Bentracimab、PB 6440、または任意の未来の候補製品に対して任意の規制承認を受けても、これらの候補製品が承認されると、製造、ラベル、包装、貯蔵、広告、宣伝、サンプリング、記録保存、および他の発売後の情報の提出などに適用される持続的な規制要求の制約を受ける。私たちはbentracimab、PB 6440、または任意の未来の候補製品のために得られた任意の規制承認も、リスク評価と緩和戦略、この薬剤が発売される可能性のある承認指示用途の制限または承認条件の制限を受ける可能性があり、または4期試験を含む可能性の高い発売後試験の要求を行う可能性があり、もし私たちがbentracimabの加速承認、3期試験の完了、および薬物の品質、安全性と有効性を監視する監督を得ることができる。成功しなかった上場後の研究やこのような研究が完成できなかったことは、上場承認の撤回につながる可能性がある。私たちはまた、いかなる深刻で予期しない不良事件や、製品のいくつかの品質や生産問題、その他の定期的な報告を直ちに規制部門に報告することを要求される。
薬物安全問題を解決するいかなる新しい立法も、製品開発や商業化の遅延を招き、あるいはコンプライアンスを確保するコストを増加させる可能性がある。われわれはまた以下の方面に関する要求を守らなければならない
私たちの製品のために広告と販売促進をします。処方薬製品に関する販売促進情報は様々な法律や法規によって制限されており,製品が承認されたラベル上の情報と一致しなければならない。したがって、私たちは、一般にラベル外販売促進と呼ばれる未承認の適応や用途のために、私たちの製品を宣伝することは許可されません。承認されたBLAの所有者は、新しい申請または追加の申請を提出し、承認された製品、製品ラベル、または製造プロセスをいくつか変更するために事前に承認されなければならない。
さらに、医薬品製造業者は、使用料を支払い、FDAおよび他の規制機関の持続的な審査および定期検査を受けて、cGMP要件に適合するかどうかを決定し、BLAまたはNDAまたは外国マーケティング申請で行われた約束を遵守するかどうかを決定しなければならない。私たちまたは規制機関が、予期されていない重症度または頻度の有害事象、または薬剤の生産施設に問題があるような以前に未知の問題が存在することを発見した場合、または規制機関が薬剤の販売促進、マーケティングまたはラベルに同意しない場合、規制機関は、リコールを要求するか、または市場からの薬剤のリコールまたは生産の一時停止を要求することを含む、薬剤、生産施設、または私たちに制限を加える可能性がある。
もし私たちがbentracimab、PB 6440、または任意の未来の候補製品を承認した後に適用される規制要件を遵守できなかった場合、規制機関は:
•私たちが法律に違反していると主張するタイトルのない手紙や警告状を出した
•禁令または行政、民事または刑事罰または罰金を求める
•規制承認の一時停止または撤回;
•進行中の臨床試験を一時停止します
•私たちまたは私たちの戦略パートナーが提出した未解決のBLA、NDAまたは同様の海外マーケティング申請(またはその任意の追加)の承認を拒否する;
•薬の販売や生産を制限し
•医薬品を差し押さえたり、差し押さえたり、または他の方法で医薬品を市場から撤退させることを要求している者;
•候補製品の輸入または輸出の許可を拒否する;または
•政府契約を含めて私たちが供給契約を締結することを許可することを拒否する。
政府は違法の疑いのあるいかなる調査にも対応するために多くの時間と資源を必要とする可能性があり、否定的な宣伝が生じる可能性がある。上述した任意のイベントまたは処罰の発生は、bentracimab、PB 6440、または任意の将来の候補製品を商業化する能力を抑制し、私たちの業務、財務状態、運営結果、および将来の見通しを損なう可能性があります。
医療立法や規制改革措置は、私たちの業務と運営結果に悪影響を及ぼす可能性がある。
アメリカと一部の外国司法管轄区では、医療保健システムに関するいくつかの立法と法規の変化と提案された変化が継続され、これらの変化は候補製品の上場承認を阻止または延期し、承認後の活動を制限または監督し、上場承認を得た候補製品を収益的に販売する能力に影響を与える可能性がある。
米国や他の地方の政策立案者や支払者の中で,医療システムの改革を推進することに大きな興味があり,医療コストの抑制,質の向上および/または参入拡大を既定の目標としている。米国では、製薬業はこれらの努力の重点であり、重大な立法計画の大きな影響を受けてきた。2010年3月,ACAが採択され,政府や民間保険会社が医療に融資する方式を大きく変更し,米国製薬業に大きな影響を与えた。他の事項に加えて、ACAには、製薬やバイオテクノロジー業界にとって特に重要な条項が含まれているが、連邦医療計画登録を管理する条項を含むが、新しい方法に基づいてメーカーが医療補助薬品リベート計画の下で不足しているリベートを計算する方法と、連邦ヘルスケア計画における製薬会社の販売シェアから年会費を計算する方法とが含まれている。
ACAのいくつかの側面は行政、司法、そして国会の挑戦を受けている。国会ではまだ全面的な廃止立法は成立していないが、ACAの下にある税収実施に影響を与えるいくつかの法案が署名されて法律となっている。2017年の減税·雇用法案、または税法は、2019年1月1日からACAが1年の全部または一部で合格医療保険を維持できなかった個人に対して実施された税収ベースの分担責任支払いを廃止する条項を含み、これは一般に“個人強制”と呼ばれている。また、
2020年に連邦支出計画は永久に廃止され,2020年1月1日からACAが規定する雇用主に助成する高コスト医療保険と医療機器税の“キャデラック”税や,2021年1月1日からも医療保険会社税が廃止された。2018年の両党予算法案、あるいはBBAなどは、ACAを改正し、2019年1月1日から施行され、多くの連邦医療保険薬物計画におけるカバーギャップを埋めるために、通常“ドーナツ穴”と呼ばれている。2021年6月17日、米国最高裁は“個人権限”が国会で廃止されたため、ACAが全体的に違憲だと弁明する手続きを理由に挑戦を却下した。したがって、ACAは現在の形態で継続的に有効であるだろう
また,米国最高裁が裁決を下す前に,総裁·バイデンは2021年1月28日にACA市場による医療保険の特殊加入期間を開始し,2021年2月15日から2021年8月15日まで開放された行政命令を発表した。行政命令はまた、特定の政府機関に、医療補助モデルプロジェクトおよび免除計画の再審査、および医療補助またはACAによる医療保険の取得による不必要な障害をもたらす政策を含む、医療補助モデルプロジェクトおよび免除計画の再審査および見直し、医療補助またはACAによる医療保険の取得を制限する既存の政策および規則を再検討するように指示する。最高裁の裁決,その他のこのような訴訟,バイデン政府の医療改革措置がACAや我々の業務にどのように影響するかは不明である。
ACAが公布されて以来、他の立法改正も提案され、採択された。これらの変化には、2013年に開始された2011年の予算制御法案と、その後の同法規の立法改正により、英国銀行家協会を含めて、医療保険提供者に支払われる医療保険金額が前期ごとに合計2%減少することが含まれている 国会が追加的な行動を取らない限り、インフラ投資と雇用法案は2031年まで有効になるだろう。しかし,新冠肺炎の救済立法は2020年5月1日から2022年3月31日までの2%の連邦医療保険自動減額を一時停止した。現在の立法によると、医療保険支出の実質減幅は2022年の1%から本自動減額の最終年度の3%まで様々になる。2012年の“米国納税者救済法”は,病院や癌治療センターを含むいくつかの医療サービス提供者に支払う医療保険費用をさらに減少させ,政府が医療サービス提供者に多額の金を取り戻す訴訟時効を3年から5年に延長した。これらの法律は,連邦医療保険や他の医療資金のさらなる減少を招く可能性があり,承認されれば,候補製品の顧客や我々の財務運営に悪影響を及ぼす可能性がある。
また、処方薬や生物製品価格の上昇を受けて、米国政府は薬品定価のやり方の審査を強化した。このような審査は,最近の数回の国会調査を招き,製品定価の透明性の向上,価格設定とメーカー患者計画との関係の審査,政府計画の製品精算方法の改革を目的とした連邦や州立法を提案·採択した。連邦レベルでは、トランプ政権はいくつかの手段を用いて、連邦予算提案、行政命令、政策措置を含む薬品定価改革を提出または実施している。例えば、2020年7月24日と2020年9月13日に、トランプ政権は処方薬の定価に関するいくつかの行政命令を発表し、政府のいくつかの提案を実施しようとしている。そのため、FDAは2020年9月に最終規則と指導意見を同時に発表し、各州がカナダからの薬物輸入計画の制定と提出に道を提供した。また、2020年11月20日、米国衛生·公衆サービス部(HHS)は、製薬業者からD部分までの計画スポンサーの値下げ安全港保護を廃止し、法律が値下げを要求しない限り、直接または薬局福祉マネージャーを通過する規定を決定した。バイデン政権は、現在行われている訴訟に対応するため、この規則の実施を2022年1月1日から2023年1月1日に延期した。この規定はまた、販売時点での値下げを反映するための新しい避難港を作成し、薬局福祉マネージャーと製造業者との間のいくつかの固定料金スケジュールのための避難港を作成し、これらの計画の実施も2023年1月1日に延期される。2020年11月20日, CMSは、ある医師が管理する薬物の連邦医療保険B部分支払いを他の経済先進国が支払う最低価格とリンクさせ、2021年1月1日から発効する暫定最終規則を発表した。最恵国モデルに挑戦した訴訟の結果,CMSは2021年12月27日に最終ルールを発表し,最恵国モデル仮最終ルールを廃止した。2021年7月、バイデン政府は“米国経済における競争を促進する”という行政命令を発表し、その中には処方薬に対する条項が複数ある。行政命令への対応として,2021年9月9日,HHSは高薬価に対応した総合計画を発表し,薬品定価改革の原則を概説し,国会が推進できる様々な潜在的な立法政策を示し,これらの原則を推進した。また、国会は他の改革措置の一部として薬品定価を検討している。州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入の制限、マーケティングコスト開示および透明性措置を含む、医薬品および生物製品の価格設定を制御するための法規を立法および実施することが増えており、場合によっては、他の国からの輸入および大量購入を奨励することを目的としている。
これらの措置および将来取られる可能性のある他の医療改革措置は、より厳しいカバー基準を招き、承認された任意の薬物の価格に追加的な下振れ圧力を与える可能性があると予想される。連邦医療保険や他の政府が計画している精算のいかなる減少も、個人支払者の支払いの同様の減少を招く可能性がある。コスト抑制策や他の医療改革を実施することで
収入を作ったり利益を達成したり私たちの薬を商業化したりしますまた、政府は新冠肺炎の大流行に対応するためにより多くの行動をとるかもしれない。
任意の新しい法規またはガイドライン、または既存の法規またはガイドラインの修正または再解釈は、bentracimab、PB 6440、または任意の将来の候補製品のコストを増加させるか、またはFDAの審査時間を延長する可能性がある。規制、法規、政策、解釈の変化がいつ、発表され、実施され、採用された場合、私たちの将来の業務にどのように影響するかを決定することはできません。他の事項に加えて、このような変化は必要かもしれない
•承認される前により多くの臨床試験を行わなければならない
•製造方法を変え
•1つ以上の製品のリコール、交換、または生産停止;
•追加的な記録保存。
このような変更は、大量の時間および大きなコストを必要とする可能性があり、またはbentracimab、PB 6440、または他の候補製品の潜在的な商業価値を低下させ、私たちの業務および財務業績に実質的な損害を与える可能性がある。さらに、他の製品の規制承認または承認を遅延させることは、私たちの業務、財務状況、および運営結果を損なうことになります。
従業員の事務と私たちの成長に関するリスク
私たちの未来の成功は私たちが肝心な幹部を維持する能力、及び合格した人材を吸引、維持、激励する能力にかかっている。
私たちは私たちの役員、特に最高経営責任者Jonathan P.Mowの管理、開発、臨床、財務、業務発展に関する専門知識に高く依存しています。私たちのすべての幹部は現在私たちとの雇用関係をいつでも終わらせることができる。私たちは私たちのどんな幹部や従業員にも“キーパーソン”保険を提供しない。
合格した科学と臨床人員を募集と維持し、もし私たちが製品パイプの開発に進展を得て、商業化、製造と販売とマーケティング人員の規模を拡大すれば、私たちの成功の鍵にもなる。幹部や他の重要な従業員のサービスを失うことは、私たちの発展と商業化目標の達成を阻害し、業務戦略を成功させる能力を深刻に損なう可能性がある。私たちは今後も従業員の流出に直面する可能性があり、これは私たちの業務戦略に悪影響を及ぼすかもしれない。新入社員たちは大量の訓練を必要とし、ほとんどの場合、彼らは完全な生産性を達成するのにかなりの時間を必要とする。新入社員は私たちが予想していたほど効率的ではないかもしれないし、私たちは十分な数の適格社員を雇用したり維持することができないかもしれない。また,医療従事者や政府請負業者のワクチン要求に従わないことを選択したため,働きたくない従業員は上記のような状況を悪化させる可能性がある。また、幹部やキーパーソンを交換することは困難かもしれませんし、私たちの業界では開発に成功し、規制承認や製品商業化に必要なスキルや経験を持つ個人の数が限られているので、長い時間がかかるかもしれません。この限られた人材バンクから募集する競争は非常に激しく、多くの製薬と生物技術会社の間の類似人員に対する競争を考慮して、私たちは受け入れ可能な条件でこれらの肝心な人員を採用、訓練、維持或いは激励することができないかもしれない。私たちはまた、大学や研究機関から科学や臨床人を募集する競争に直面している。さらに、私たちは科学と臨床コンサルタントを含むコンサルタントとコンサルタントに依存している, 私たちの開発と商業化戦略を作るのを手伝ってくれた。私たちのコンサルタントやコンサルタントは、私たち以外の雇用主に雇われる可能性があり、他のエンティティと締結された相談または相談契約に基づいて約束することができ、これは、私たちが彼らを得る機会を制限するかもしれない。もし私たちが引き続き高い素質の人材を誘致し、維持することができなければ、私たちが成長戦略を推進する能力は制限されるだろう。
私たちは私たちの臨床開発と規制能力を拡大し、販売、マーケティング、流通能力を実施する可能性があると予想されているので、私たちは私たちの成長を管理することが困難になるかもしれません。これは私たちの運営を乱すかもしれません。
2021年12月31日まで、私たちは60人の従業員がいる。私たちの発展に伴い、私たちは私たちの従業員の数と業務範囲が持続的に増加することを予想して、特に臨床製品開発、監督管理、そしてもし私たちの任意の候補製品がマーケティングの承認、販売、マーケティング、流通の面であれば。私たちが予想している将来の成長を管理するためには、私たちの管理、運営、財務システムを継続して実施し、改善し、私たちの施設を拡大し、より多くの合格者を募集し、訓練し続けなければならない。私たちの財務資源が限られていることと、私たちの管理チームがこのような成長を期待している会社を管理する上での経験が限られているため、私たちの業務の拡張を効果的に管理したり、より多くの合格者を募集したりすることができないかもしれません
私たちの業務の拡張は巨大なコストを招き、私たちの管理と業務発展資源を移転する可能性があります。成長を管理できないどんな状況も、私たちの業務計画の実行を延期したり、私たちの運営を妨害したりする可能性がある。
私たちの従業員、独立請負業者、コンサルタント、商業協力者、首席調査員、CRO、サプライヤー、サプライヤーは、規制基準と要求を遵守しないことを含む、不適切な行為または他の不適切な活動に従事する可能性があります。
私たちは、従業員、独立請負業者、コンサルタント、ビジネス協力者、主要調査者、CRO、サプライヤー、およびサプライヤーが詐欺または他の不正活動に従事する可能性があるリスクに直面しています。これらの当事者の不正行為は、意図的、無謀、および/または不注意な行為、またはFDA規定に違反する不正な活動を開示することを含む可能性があり、真、完全かつ正確な情報をFDAに報告することを要求する法律、製造基準、連邦および州医療保健法律法規、および財務情報またはデータの真の、完全かつ正確な報告を要求する法律を含むことができる。特に、医療業界の販売、マーケティング、商業配置は、詐欺、リベート、自己取引、その他の乱用を防止するための広範な法律法規によって制約されている。これらの法律法規は、広範な価格設定、割引、マーケティングおよび販売促進、販売手数料、顧客インセンティブ計画、および他のビジネス計画を制限または禁止する可能性があります。これらの各方面の不当な行為はまた個人識別情報の不適切な使用に関連する可能性があり、臨床試験過程で得られた情報を含むが、これに限定されず、これは規制制裁と著者らの名声に深刻な損害を与える可能性がある。私たちはビジネス行為や道徳的規範を通過していますが、常に不正行為を識別し、阻止できるわけではありません。このような活動を発見し、防止するための予防措置は、未知または未管理のリスクや損失を効果的に制御できないか、またはそのような法律や法規に準拠していないことによる調査や他の行動や訴訟から私たちを保護することができない可能性があります。もし私たちにこのような行動を取ったら、私たちは自分自身を弁護したり、自分の権利を維持することに成功しなかった, これらの行動は、損害賠償、罰金、返還、監禁、連邦医療保険や医療補助などの政府医療計画から除外され、追加の報告要件および監督を含むが、これらの法律違反に関する告発を解決するために、重大な民事、刑事、行政処罰を適用することを含む、私たちの業務に大きな影響を与える可能性があります。
私たちの普通株式所有権と上場企業の地位に関するリスク
私たち普通株の取引価格はすでに不安定である可能性があり、私たち普通株を購入した人は大きな損失を受ける可能性があります。
私たちの株価はずっと変動していて、変動し続けるかもしれない。私たちの初公募株(IPO)から2022年3月21日まで、私たちの普通株の取引価格は1株0.96ドルから16.65ドルまで様々です。一般的な株式市場,特にバイオ製薬会社の市場は極端な変動を経験しており,この変動は特定の会社の経営業績とは無関係であることが多い。このような変動により、投資家は普通株を購入したかそれ以上の価格で普通株を売ることができない可能性がある。私たちの普通株の市場価格は多くの要素の影響を受けるかもしれません
•私たちのbentracimab、PB 6440の臨床試験、または私たちが将来行う可能性のある任意の臨床試験の開始、登録または結果、または候補製品の開発状態の変化
•私たちは、bentracimab、PB 6440、または私たちが開発する可能性のある任意の他の候補製品の規制届出の任意の遅延、および適用規制機関がそのような届出に関連する任意の不利な進展を検討すること、またはFDAが“届出拒否”を送信することを含むが、より多くの情報を提供することを含むが、より多くの情報を提供することを含む、または不利と考えられる事態の発展を検討する
•臨床試験の不良結果、遅延、または終了
•私たちの候補製品に対する規制部門の承認を得られなかったことを含む不利な規制決定
•ベンゼントラマズマブ、PB 6440、または任意の他の候補製品の使用に関連する意外に深刻な安全問題;
•私たちの株をカバーすることができる株式研究アナリストの財務推定変化は
•私たちの会社と業務に対する投資家の全体的な見方は
•私たちの業界の状況や傾向
•同じ会社の市場予想が変化しています
•比較可能な会社、特にバイオ製薬業界で経営している会社の株式市場価格と取引量が変動している
•当社または当業界に関する研究報告を発表したり、証券アナリストがプラスまたは否定的な提案をしたり、研究報告を撤回したりする
•私たちまたは競争相手が重大な買収、戦略協力、資産剥離を発表します
•SFJとの協力によるフェニトラシズマブの開発の進展
•私たちの業務の調査や規制審査を発表したり、私たちに訴訟を提起したりします
•キーパーソンの採用や退職
•株式市場の全体像
•当社の普通株式出来高
•特許、訴訟事項、および私たちの技術のための特許保護を得る能力を含む、専有権に関する論争または他の発展;
•特許または株主訴訟を含む重大な訴訟;
•医療支払い制度の構造を変え
•一般的な政治的·経済的条件
•他の事件や要素、その多くは私たちがコントロールできない。
株式市場、特にナスダック世界市場とバイオテクノロジー会社は、極端な価格と出来高変動を経験しており、これらの変動は往々にしてこれらの会社の経営業績と関係がないか比例しておらず、進行中の新冠肺炎の大流行に関連する変動を含み、これは多くの会社の株価下落を招き、それらの基本的な商業モデルや将来性は根本的に変わっていないにもかかわらず、それらの基本的な商業モデルや見通しは根本的に変わっていないにもかかわらず、これらの会社の経営業績に比例しない。我々の実際の経営業績にかかわらず、潜在的な悪化した経済状況と進行中の新冠肺炎疫病に関連する他の不利な影響或いは事態の発展を含む広範な市場と業界要素は、私たちの普通株の市場価格にマイナス影響を与える可能性がある。本節で説明したリスクを含む、上記の任意のリスクまたは任意の広範な他のリスクを達成することは、私たちの普通株の市場価格に重大かつ実質的な悪影響を及ぼす可能性がある。
また、過去には、製薬やバイオテクノロジー会社株の市場価格が変動した後、これらの会社の株主がこれらの会社に対して集団訴訟を起こしていた。私たちにこのような訴訟を提起すれば、巨額のコストを発生させ、経営陣の注意と資源を私たちの業務から移転させる可能性があります。
私たちがナスダックの世界市場の持続的な上場基準を守ることができる保証はない。
私たちの普通株は現在ナスダックに看板を掲げて取引しています。コードは“PHA”です。私たちの普通株のナスダック世界市場での上場を維持するためには、私たちはいくつかの上場要求を満たさなければならない。もしナスダック世界市場が上場基準に達していないため、私たちの証券をその取引所から退市したら、私たちと私たちの株主は深刻な負の結果に直面する可能性があります
•私たちの証券の市場オファーは限られています
•普通株を“細株”と決定することは、普通株取引仲介人により厳しい規則を遵守することが要求され、普通株二級取引市場の取引活動が減少する可能性がある
•限られた数のアナリストの報告;
•将来的により多くの証券を発行したり、より多くの融資を得る能力が低下する。
私たちの普通株の活発な取引市場は引き続き発展したり持続しないかもしれない。
私たちが初めて株式を公開する前に、私たちの普通株は公開市場を持っていません。私たちの株の活発な取引市場が引き続き発展したり、持続していくことを保証することはできません。したがって、あなたは魅力的な価格で株を売ることが難しいかもしれない。
私たちの総流通株の大部分はすぐに転売できます。これは私たちの業務が良好であっても、私たちの普通株の市場価格を大幅に下落させる可能性がある。
公開市場で私たちの大量の普通株を売ることはいつでも起こる可能性がある。もし私たちの株主や市場が私たちの株主が公開市場で私たちの普通株を大量に販売しようとしていると思うなら、私たちの普通株の市場価格は大幅に低下する可能性があります。
また、私たちは表S-8の登録声明を提出して、普通株式の発行を登録しましたが、私たちの持分激励計画の下で未来の発行のために発行または予約されたオプションまたは他の持分奨励に制限されなければなりません。S-8表では、これらの登録声明に基づいて登録された株式は公開市場で販売することができるが、帰属手配及びオプション行使及び規則第144条のわが連合会社に対する制限の制限を受けなければならない。
さらに、約220万株の私たちの普通株の所有者またはその譲受人は、ある条件下で、彼らの株式に関する1つ以上の登録声明を提出することを要求する権利があり、または彼らの株を私たち自身または他の株主のために提出する可能性のある登録声明に含める権利がある。もし私たちがこの株を転売することを登録すれば、それらは公開市場で自由に売ることができる。これらの追加株が公開市場で販売されている場合、またはそれらが売却されると思われる場合、私たちの普通株の取引価格は低下する可能性がある。
融資、買収、投資、私たちの株式インセンティブ計画または他の側面に関連する追加株式の発行は、他のすべての株主の権益を希釈する。
わが社の登録証明書は、私たちが最大200,000,000株の普通株と最大10,000,000株の優先株を発行することを許可しており、その権利と優先権は私たちの取締役会によって決定される可能性があります。適用規則や法規を遵守した場合、将来的には、融資、買収、投資、私たちの株式インセンティブ計画、または他の側面のために、普通株または他の普通株に変換可能な証券を時々発行することができる。追加資本を調達するために発行された普通株新株数は、私たち普通株が当時発行していた株の大部分を構成する可能性があり、これは私たちの既存株主の大量の希釈を招き、私たち普通株の市場価格を下落させる可能性がある。
私たちの定款文書とデラウェア州法律の条項は、私たちの株主が私たちの経営陣を変えようとしていることを阻止または挫折させ、私たちの持株権獲得の努力を阻害するかもしれないので、私たちの普通株の市場価格はもっと低くなるかもしれません。
当社の登録証明書や定款には、第三者がわが社の支配権を獲得したり、買収しようとしたりする条項があります。たとえあなたや他の株主が支配権の変更が有利だと思っていても有利です。例えば、私たちの取締役会は最大1000万株の優先株を発行する権利がある。取締役会は、私たちの株主のさらなる投票や行動を必要とすることなく、優先株の価格、権利、特典、特権、制限を決定することができる。優先株の発行は支配権変更取引を延期または阻止する可能性がある。したがって、私たちの普通株の市場価格と私たちの株主の投票権と他の権利は不利な影響を受けるかもしれない。優先株の発行は他の株主の議決権支配権を失う可能性がある。
私たちの定款には、反買収の効力を持つ可能性のある他の条項も含まれています
•私たちの3種類の役員のうち、毎年1種類だけが選挙で生まれています
•株主は66票を得ない限り取締役を罷免する権利がない 2⁄3%の投票権は、理由に限定されます
•株主は書面の同意の下で行動してはならない
•株主は株主特別会議を開くことができない
•株主は株主総会の審議のために指名取締役に事前に通知したり、提案を提出しなければならない。
また、デラウェア州会社法第203条の反買収条項を受けており、この条項は、デラウェア州会社がこれらの会社の特定株主と特定の業務合併を行うことを禁止することで、会社買収を規制している。これらの規定は潜在的な買収提案を阻害する可能性があり、制御権変更取引を延期または阻止する可能性がある。彼らはまた、他の人が私たちの普通株に対して買収要約を提出することを阻止する効果があり、あなたの最適な利益に合致する可能性のある取引を含むかもしれません。これらの規定はまた、私たちの経営陣が変化することを阻止したり、投資家が私たちの株式に支払う価格を制限したりする可能性がある。
私たちの普通株の所有権は私たちの既存の幹部、役員、主要株主に集中しており、新しい投資家が重大な会社の意思決定に影響を与えることを阻止する可能性がある。
私たちの役員、役員、そして現在5%以上の普通株を持っている実益所有者と、それぞれの関連会社の実益は、私たちが発行した普通株のかなりの割合を持っています。したがって、これらの人たちが一緒に行動することは、選挙および罷免取締役、任意の合併、合併、私たちの所有またはほとんどの資産の売却、または他の重大な会社取引を含む、株主の承認を必要とするすべての事項に著しく影響を与えることができるだろう。
これらの個人またはエンティティのうちのいくつかは、あなたの興味とは異なる可能性があります。例えば、これらの株主の多くは、私たちの普通株の現在の市場価格よりも大幅に低い価格で彼らの株を購入し、彼らの株を持っている時間が長いため、彼らは他の投資家よりも私たちの会社を買収者に売却することに興味を持っているかもしれないし、あるいは他の株主の利益から離れる戦略をとることを望んでいるかもしれない。
私たちは“新興成長型会社”と“より小さい報告会社”であり、新興成長型企業やより小さい報告会社に適用される開示やガバナンス要求が低下するため、私たちの普通株の投資家に対する吸引力が低下する可能性がある。
私たちは“2012年創業法案”(JumpStart Our Business Startups Act Of 2012)や“雇用法案”(JOBS Act)で定義されている“新興成長型企業”であり、他の非新興成長型企業に適用される上場企業に適用されるいくつかの報告書免除要求を利用する予定である
•当社の財務報告の内部統制を評価する際には、監査人の認証要求を遵守することは要求されていない
•上場企業会計監督委員会が通過する可能性のある強制ローテーション監査会社の任意の要件を遵守すること、または監査および財務諸表に関する補足情報を提供することを要求されていない監査人報告書の補足;
•私たちの定期報告書、依頼書、登録声明では、役員報酬に関する開示義務を減らすことができます
•役員報酬や株主承認前に承認されなかったゴールドパラシュート支払いについて拘束力のない諮問投票を行う必要はない。
私たちは投資家が私たちがこのような免除に依存して私たちの普通株の吸引力が低下することを発見するかどうか予測できない。したがって、一部の投資家が私たちの普通株の吸引力が低下していることを発見すれば、私たちの普通株はそれほど活発ではない取引市場がある可能性があり、私たちの株価はもっと変動するかもしれない。私たちは私たちがこれ以上新興成長型会社ではないまで、このような報告書免除を利用するかもしれない。私たちは、(1)財政年度の最終日まで、(A)私たちのIPO終了5周年後の最終日、すなわち2023年12月31日まで、(B)私たちの年間総収入が少なくとも10.7億ドル、または(C)前年6月30日まで、非付属会社が保有する私たちの普通株の時価が7億ドルを超えることを意味する大型加速申告会社とみなされる。そして(2)前3年の間に10億ドルを超える転換不能債券を発行した日。
雇用法第107条(B)によれば、新興成長型企業は、これらの基準が民間企業に適用されるまで、新たな又は改正された会計基準の採用を延期することができる。私たちは、新しい会計基準や改正会計基準の免除を受けないことを撤回できないことを選択したので、他の非新興成長型企業の公衆企業と同様に、同じ新しい会計基準を遵守したり、会計基準を修正したりする。新興成長型会社になる資格がなくなっても、場合によっては“小さな報告会社”になる資格があるかもしれませんが、これは、定期報告や依頼書で役員報酬に関する開示義務を減らすことを含め、多くの同じ開示要件を利用して免除することができ、年収が1億ドル未満の小さな報告会社であれば、独立公認会計士事務所が発表した財務報告内部統制の認証報告を得る必要はありません。(I)私たちの第2四半期の最終営業日に、私たちが持っている投票権と無投票権普通株の時価が2.5億ドル未満、または(Ii)最近終了した会計年度の年収が1億ドル未満であり、私たちの第2四半期の最終営業日に、非関連側が保有する投票権と無投票権のある普通株の時価が7億ドル未満であれば、私たちは“小さな報告会社”になる資格がある。
私たちは現金と現金同等物の使用に広い自由裁量権を持っている。
私たちは最近公募株の純収益を含めて現金と現金等価物の使用に幅広い自由裁量権を持っている。あなたは私たちの決定に同意しないかもしれません。私たちはこの現金と現金等価物を使用してあなたの投資に何の見返りも与えないかもしれません。私たちは私たちの既存の現金と現金等価物を利用してbentracimabとpb 6440基金を推進したい
我々のELP技術と臨床前プロジェクトを開発し,運営資本や一般企業用途に利用している。さらに、私たちは、許可またはより多くの候補製品を得るために、現金および現金等価物の一部を使用して、私たちの戦略を実施することができる。私たちは私たちの現金と現金等価物を有効に運用できず、成長戦略を実施する能力を損なう可能性があり、私たちはこれらの現金と現金等価物の投資から著しい見返りを得ることができないかもしれない(あれば)。あなたは私たちがこの現金と現金同等物をどのように使用するかの決定に影響を与える機会がないだろう。
私たちは予測可能な未来に私たちの普通株に現金配当金を支払わないと予想されているので、資本付加価値(あれば)があなたの唯一の収益源になり、あなたの投資は永遠に報われないかもしれない。
あなたは私たちの普通株への投資に依存して配当収入を提供してはいけない。今まで、私たちは普通株の現金配当金を発表したり支払ったりしなかった。私たちは現在、私たちの未来の収益を維持するつもりで、もしあれば、私たちの業務の発展と成長に資金を提供します。さらに、SFJ協定の条項は、私たちが配当金を支払うことを禁止しており、任意の既存または将来の債務協定は、配当金の支払いを阻止する可能性があります。したがって、私たちの普通株の資本付加価値は(もしあれば)あなたが予測可能な未来に唯一の収益源になるだろう。現金配当金を求める投資家は私たちの普通株を購入してはいけない。
私たちが改訂し、再記載した会社登録証明書は、デラウェア州衡平裁判所とアメリカ合衆国連邦地域裁判所は、私たちと私たちの株主とのほとんどの紛争の独占的なフォーラムとなり、これは、私たちの株主が有利な司法フォーラムを得ることを制限し、私たちまたは私たちの役員、上級管理者、または従業員との紛争を処理することを制限するかもしれない。
私たちが改正して再説明した会社登録証明書は、デラウェア州衡平裁判所は、(1)私たちが提起した任意の派生訴訟または法的手続きを代表する、(2)私たちまたは私たちの株主に対する私たちまたは私たちの株主の受託責任に違反すると主張するいかなる訴訟、(3)デラウェア州会社法、当社の改正および再記載された会社登録証明書または改正および再記載された定款の任意の規定に基づいてクレームを提起する任意の訴訟、または(4)内部事務原則によって管轄されるクレームを主張する任意の訴訟である。この規定は、取引法で規定されている義務または責任を執行するための訴訟には適用されない。また、証券法第22条は、連邦裁判所と州裁判所は、このようなすべての“証券法”訴訟に対して同時に管轄権を持っていると規定している。したがって、州裁判所と連邦裁判所はこのようなクレームを受理する管轄権を持っている。複数の司法管区でクレームを訴訟しなければならないことや、異なる裁判所が不一致または逆の裁決を下す脅威、およびその他の考慮要因を回避するために、私たちが改正して再記載した会社登録証明書は、アメリカ合衆国連邦地域裁判所が証券法に基づいて提起された任意の訴因を解決するための独占的なフォーラムとなる。デラウェア州裁判所は、このような選択の裁判所条項が事実上有効であることを決定しているが、株主は依然として専属裁判所条項が指定された場所以外の場所でクレームを出すことを求めることができる。この場合には, 私たちが改訂·再記述した会社登録証明書の独占フォーラム条項の有効性と実行可能性を強力に維持することを期待しています。これは、他の法ドメインでこのような訴訟を解決することに関連する多くの追加費用を必要とする可能性があり、これらの規定がこれらの他の法ドメインの裁判所によって実行されることを保証することはできない。
これらの排他的フォーラム条項は、司法フォーラムにおいて、私たちまたは私たちの役員、役員、または他の従業員とのトラブルに有利であると考える株主のクレームを提起する能力を制限する可能性があり、これは、私たちと私たちの役員、役員、および他の従業員に対するこのような訴訟を阻止することができるかもしれない。もし裁判所が私たちが改正して再記載した会社登録証明書のいずれかの独占法廷条項が訴訟で適用されないか、実行できないことが発見された場合、私たちは他の管轄区域での紛争解決に関連するさらなる重大な追加費用を発生する可能性があり、これらすべては私たちの業務を深刻に損なう可能性がある。
一般リスク因子
私たちのビジネス活動は“反海外腐敗法”(FCPA)や似たような反賄賂と反腐敗法の制約を受けるだろう。
私たちの臨床試験の仕事を含むアメリカ以外で私たちの業務活動を拡張する時、私たちは“海外腐敗防止法”と私たちの国/地域の反賄賂や反腐敗法律、法規または規則のような制約を受けるだろう。“海外腐敗防止法”は、一般に、公式行動に影響を与えるか、または他の方法で業務を獲得または保留するために、非米国政府関係者への提供、承諾、他人に直接または間接的に価値のあるものを与えることを禁止する。“海外腐敗防止法”はまた、上場企業に会社の取引を正確かつ公平に反映した帳簿や記録を作成·保存し、適切な内部会計制御制度を制定·維持することを求めている。私たちの業務は厳しく規制されているため、非米国政府関係者を含む公職者との大量の相互作用が必要だ。また、多くの他の国では、薬を処方した医療提供者は彼らの政府に雇われており、薬品の購入者は政府の実体であり、したがって、私たちはこれらの処方者と付き合っている
バイヤーたちは海外腐敗防止法によって規制されるだろう。最近,米国証券取引委員会(略称米国証券取引委員会)と司法省はバイオテクノロジーや製薬会社に対する“反海外腐敗法”の法執行活動を増加させた。私たちのすべての従業員、代理店、サプライヤー、メーカー、請負業者、または協力者、または私たちの付属会社の従業員が、特にこれらの法律の高度な複雑さを考慮して、すべての適用された法律と法規を遵守するかどうかを決定することはできません。これらの法律および法規に違反することは、私たち、私たちの役人、または私たちの従業員に罰金、刑事制裁、施設の閉鎖、私たちのサプライヤーや製造業者の施設の閉鎖、輸出許可証の取得、制裁を受けた国での業務活動の停止、コンプライアンス計画の実施、業務の禁止を招く可能性があります。このような違反は、私たちが1つまたは複数の国または地域で私たちの製品を提供することを禁止することと、私たちの製品を製造または継続して開発することを禁止する困難と、私たちの名声、私たちのブランド、私たちの国際拡張努力、私たちの従業員を引き付け、維持する能力、ならびに私たちの業務、将来性、経営業績、財務状況を深刻に損なう可能性があるかもしれません。
株式研究アナリストが我々、我々の業務又は我々の市場に関する研究又は報告を発表しない場合、又は不利な研究又は報告を発表しなければ、我々の株価及び取引量は低下する可能性がある。
私たちの普通株の取引市場は株式研究アナリストが発表した私たちと私たちの業務に関する研究と報告の影響を受けており、株式研究アナリストの私たちの研究報告は限られている。株式研究アナリストは私たちの普通株の研究報告を開始しないか、あるいは引き続き提供することを選択する可能性があり、このような研究報告の不足は私たちの普通株の市場価格に不利な影響を与える可能性がある。たとえ私たちが株式研究アナリストの報告書を持っていても、私たちはアナリストや彼らの報告書に含まれている内容と観点を制御することができない。1つ以上の株式研究アナリストが私たちの株式格付けを引き下げたり、他の不利なコメントや研究を発表したりすれば、私たちの株価は下落する可能性がある。1つ以上の株式研究アナリストがわが社への報道を停止したり、私たちに関する報告書を定期的に発表できなかったりすれば、私たちの株に対する需要が減少する可能性があり、逆に私たちの株価や取引量を低下させる可能性がある。
適切かつ効果的な内部統制を維持できなければ、正確な財務諸表をタイムリーに作成する能力が損なわれる可能性がある。
私たちは1934年の証券取引法、2002年のサバンズ-オキシリー法案、またはサバンズ-オキシリー法案の報告要求、および私たちの普通株式上場の株式市場の規則と規定を守らなければならない。“サバンズ-オキシリー法”(Sarbanes-Oxley Act)は、私たちに効率的な開示制御と手続きと財務報告に対する内部統制を維持することを要求する。
私たちは私たちの内部財務と会計制御とプログラムシステムの弱点を発見するかもしれません。これらの弱点は、私たちの財務諸表に重大なミスを招く可能性があります。私たちの財政報告書に対する内部統制はすべてのミスと詐欺を阻止したり発見したりしないだろう。設計および動作がどんなに良好であっても、絶対的な保証ではなく、合理的な保証しか提供できず、保証制御システムの目標が実現される制御システム。すべての制御システムの固有の限界により,どの制御評価も誤りや不正による誤り陳述が発生しないことは絶対に保証されず,すべての制御問題や不正が発見されることは絶対に保証されない.
もし私たちがサバンズ-オキシリー法案404条の要求を適時に守ることができなければ、あるいは適切で効果的な内部統制を維持できなければ、私たちはタイムリーで正確な財務諸表を作成できないかもしれない。このような状況が発生すれば、私たちの株式の市場価格は下落する可能性があり、私たちは私たちの普通株が上場している証券取引所、米国証券取引委員会、または他の規制機関の制裁や調査を受ける可能性がある。
税法の新しいまたは将来の変化はわが社に実質的な悪影響を及ぼす可能性があります。
私たちが所得税と非所得税を含む、またはその下で運営される税制は、不安定であり、大きな変化が生じる可能性がある。税収法律、法規または裁決の変化、または既存の法律·法規の解釈の変化は、わが社に実質的な悪影響を及ぼす可能性がある。例えば、2017年の減税と雇用法案、あるいは税法、および2020年3月27日に公布されたCARE法案は、米国連邦税率の変更、利息控除に追加制限を加え、将来の純営業損失(NOL)の繰越の利用に積極的かつ消極的に変化し、ある資本支出の支出を許可し、世界税制から地域税制への移行を実施した。さらに、欧州の多くの国および他のいくつかの国や組織(経済協力開発機構や欧州委員会を含む)が最近提案、提案、公布、または他の方法で既存の税法や新税法の改正を受けており、これらの改正は、業務の所在国での私たちの納税義務を著しく増加させたり、業務を経営する方法を変更することを要求したりする可能性がある。最近、アメリカでは、議会とバイデン政府は、米国の国際商業運営に対する税金を増加させ、徴収することを含む税法の様々な改正を行うための立法(まだ公布されていない)を提案した
世界最低税額です。これらの提案、提案、および規制は、現行の所得税の枠組みの変更を含み、これらの枠組みは私たちの業務に適用される可能性がある。
私たちは私たちが繰り越した純運営損失の大きな部分を利用できないかもしれない。
2021年12月31日現在、私たちの連邦と州NOL繰り越し残高はそれぞれ2億591億ドルと2兆276億ドルです。2018年前に生成された連邦NOLは、将来の課税収入の100%を相殺するために使用され、以前に税法の他の条項によって利用または制限されていない限り、2022年に満了することができる。これらのNOL繰越は満期になる可能性があり、未使用であり、将来の所得税債務の相殺にも使えない。CARE法案により改正された税法によると、2017年12月31日以降の課税年度と今後数年間に発生する連邦NOLは無期限に繰り越すことができるが、このような連邦NOLの2020年12月31日以降の課税年度に発生する控除は限られている。各州が税法とCARE法案にどのように対応するかはまだ確定されていない。また、改正後の1986年の国内税法第382条と州法の該当条項によると、1社が3年以内にその持分所有権を価値で計算して50%を超える“所有権変更”を経験した場合、その会社は変更前の純資産繰越や他の変更前の税収属性を用いて変更後の収入や税金を相殺する能力が制限される可能性がある。私たちは経験したことがあるかもしれないし、未来も経験したことがあるかもしれないが、私たちの株式所有権の変化、所有権の変化のため、その中のいくつかは私たちがコントロールできるものではないかもしれない。もし所有権が発生したり、未来に変化したりすれば、私たちがNOL繰り越しを使用する能力が実質的に制限され、これは私たちの未来の納税義務を効果的に増加させ、私たちの将来の経営業績を損なうことになる。
私たちの有効税率は変動するかもしれません。私たちが税務管区で発生した債務は計算金額を超えるかもしれません。
私たちは複数の税務管轄区で税金を払わなければなりません。したがって、私たちの有効税率は私たちが経営している地域別の適用税率を組み合わせたものです。私たちの財務諸表を作成する際には、このような場所ごとに税金を支払う必要があると予想されます。しかし、多くの要素のため、私たちの有効税率は過去と異なるかもしれません。新たに公布された連邦所得税法の通過、私たちの収益力の組み合わせの司法管轄区から司法管轄区への変化、私たちの税務申告の審査と監査結果、私たちは税務当局と受け入れ可能な合意を達成したり、維持することができない、所得税会計の変化、税法の変化を含むかもしれません。これらの要因のいずれも、私たちの実際の税率が前の時期または現在の予想と大きく異なり、納税義務が私たちの財務諸表の課税金額を超えることをもたらす可能性があります。
上場企業として、大きなコストと経営陣への要求を招いた。
米国に上場する上場企業として、私たちは大量の法律、会計、その他のコストを負担しており、これらのコストは私たちの財務業績にマイナス影響を与える可能性がある。また、米国証券取引委員会とナスダック株式市場で実施された法規を含む、会社のガバナンスと開示に関連する法律、法規、標準の変化は、法律と財務コンプライアンスコストを増加させ、いくつかの活動をより時間をかける可能性がある。これらの法律,条例,基準には異なる解釈があるため,規制機関や理事機関が新たな指導を提供するにつれて,実践における適用は時間とともに変化する可能性がある。変化する法律、法規、基準を遵守するために資源を投入する予定であり、このような投資は一般的かつ行政費用の増加を招き、経営陣の時間と注意を創設活動からコンプライアンス活動に移す可能性がある。私たちは新しい法律、法規、基準を遵守しようと努力しているにもかかわらず、私たちが守らなければ、規制機関は私たちに法的訴訟を提起し、私たちの業務は損害を受けるかもしれない。
これらの規則を守らないことは、取締役や上級者責任保険を含むいくつかのタイプの保険を得ることを難しくする可能性もあります。私たちは、同じまたは類似した保険を得るために、減少した保険限度額や保険範囲を受け入れさせられたり、同じまたは類似した保険を得るためにより高い費用を発生させたりする可能性があります。これらの事件の影響はまた、私たちの取締役会、取締役会委員会、または上級管理職メンバーに合格した人を引き付け、維持することを難しくするかもしれない。
コンピュータシステム障害、ネットワーク攻撃、またはネットワークセキュリティ欠陥が発生すれば、私たちの業務と運営は影響を受けるだろう。
我々にとって,コンピュータ情報システムと通信システムのセキュリティを維持することは重要な問題である.我々は、我々のシステムやユーザを保護するために、ネットワークセキュリティおよび他のセキュリティ対策にかなりの内部および外部リソースを投入しているが、これらのセキュリティ対策は絶対的なセキュリティを提供することはできない。我々のコンピュータシステムの多様性および複雑さは、サービス中断、セキュリティホール、データ完全性中断、私たちのデータまたはシステムの不注意な誤り、悪意の侵入、またはランダム攻撃の影響を受けやすいようにする可能性がある。
我々の内部コンピュータシステムおよび我々が依存する第三者のコンピュータシステムは、コンピュータウイルス、マルウェア、自然災害、テロ、戦争、電気通信および電気故障、インターネット上のネットワーク攻撃またはネットワーク侵入、電子メール添付ファイル、組織内部者、または組織内部システムにアクセスすることができる者の破壊を受けやすい。私たちは過去と未来に欠陥、エラー、または脆弱性を識別する可能性があり、これらの欠陥、エラー、または脆弱性は、顧客データへのアクセスまたは露出を意図せずに許可するかもしれない。世界各地からの未遂攻撃と侵入の数、強度と複雑性の増加に伴い、セキュリティホールや破壊のリスクは普遍的に増加し、特にコンピュータハッカー、外国政府とネットワークテロリストを含むネットワーク攻撃或いはネットワーク侵入を介している。このような事件が発生して私たちの運営が中断されると、私たちの製品開発計画が実質的に中断される可能性があります。例えば、完了または進行中または計画中の臨床試験における臨床試験データの損失は、我々の規制承認作業を遅延させる可能性があり、データを回復または複製するコストを著しく増加させる可能性がある。任意の中断、セキュリティイベント、または脆弱性が、私たちのデータやアプリケーションが失われたり、破損したり、機密または独自の情報に適切にアクセスまたは開示されない場合、私たちは重大な法的クレームおよび責任を招き、私たちの名声を損なう可能性があり、私たちの候補製品のさらなる開発は延期される可能性があります。
現在の新冠肺炎の大流行期間中、セキュリティホールやプライバシー侵害の影響はさらに拡大する可能性がある。また,さらなるデータ保護措置を実施するコストや運営結果が大きい可能性があるが,我々の知的財産権や独自業務情報が盗まれた場合には,救済に多大な費用がかかる可能性がある.さらに、(A)私たちの責任保険が、タイプまたは金額で、セキュリティホール、ネットワーク攻撃、および他の関連脆弱性に関するクレームをカバーするのに十分であるかどうか、(B)このような保険が、任意の事件に関連する私たちに対する任意の賠償請求を含むかどうか、経済的に合理的な条項で提供され続けるかどうか、または(C)どの保険会社も未来のクレームの保険を拒否しないかどうかを確認することはできません。利用可能な保険範囲を超える1つまたは複数の多額のクレームを私たちに提出することに成功したか、または保険料の増加または多額の免責または共同保険要件の実施を含む私たちの保険証書が変化し、私たちの名声、業務、財務状況、および運営結果に悪影響を及ぼす可能性がある。
項目1 B。未解決の従業員のコメント。
ない。
項目2.財産
2023年9月に期限が切れる賃貸契約によると、ペンシルバニア州マルヴィンの2カ所で25,000平方フィートの研究開発と行政空間をレンタルした。2022年10月に満期になる賃貸契約によると、カリフォルニア州サンディエゴで4000平方フィートの行政空間もレンタルしました。私たちは私たちの既存の施設が私たちの現在の必要性を満たすのに十分で十分だと信じている。私たちは従業員を増やしながら新しい施設を増やしたり、既存施設を拡大したりするつもりで、必要に応じて適切な追加または代替空間を提供して、私たちの業務のどのような拡張にも適応すると信じています。
項目3.法的訴訟
私たちは実質的な法的手続きの制約を受けないだろう。私たちは時々様々な請求と、私たちの業務に関連した請求の法的手続きを扱うかもしれない。私たちは現在、私たちの経営陣が私たちの業務に重大な悪影響を及ぼす可能性があると思う法的手続きに参加していません。結果にかかわらず,弁護や和解コスト,管理資源分流などにより,訴訟は我々に悪影響を与える可能性がある。
第4項鉱山安全情報開示
適用されません。
第II部
第五項登録者普通株式市場、関連株主事項及び発行者が株式証券を購入する。
普通株式市場情報
私たちの普通株はナスダック世界市場に上場し、コードは“PHAS”です
記録保持者
2022年3月21日現在、私たちは50人の普通株式保有者がおり、その株式が仲介人によって代名人や街頭名義で保有されている株主は含まれていません。普通株株主の実際の数は,実益所有者である株主を含む記録保有者の数よりも大きいが,その株式は仲介人や他の被命名者が街頭名義で保有している.この数の登録所有者は、その株式が他のエンティティが信託形式で保有する可能性のある株主も含まれていない。
配当政策
私たちは私たちのどの株にも現金配当金を支払ったことがありません。今は私たちの未来の収益を保留するつもりです。もしあれば、私たちの業務の発展と成長に資金を提供します。
株式証券の未登録販売
ない。
発行者および関連購入者が株式証券を購入する
ない。
プロジェクト6.保留
第7項:経営陣の財務状況と経営成果の検討と分析。
以下、当社の財務状況及び経営成果に関する検討及び分析は、当社の財務諸表及び関連付記、及び本年報10-K表に記載されている関連管理層の財務状況及び経営成果の検討及び分析を結合して併せて読むべきである。
概要
私たちは臨床段階の生物製薬会社で、心血管疾患の新しい治療法の開発と商業化に集中している。著者らの主要な候補製品bentracimab(PB 2452とも呼ばれる)は抗血小板薬チカグレルの新しい反転剤である。われわれが達成した試験では,Bentracimabは全体的に耐性が良好であり,薬物に関する重篤な副作用やSAEはなかった。われわれが完成したbentracimabの2 a期と2 b期の臨床試験では,テカグレルの抗血小板活性は注入開始後5分で直ちに完全に逆転し,20時間以上逆転が認められた。我々は現在,Bentracimabの重要な第3段階逆IT試験を行っている。150人の入選患者(うち142人が緊急手術または侵襲的手術を必要とし、8人が制御不能な大出血または生命に危険な出血を有する)の予め指定された中期分析では、bentracimabは、テカグレルの抗血小板作用を直ちにかつ持続的に逆転させることによって、試験の主要な終点を達成した。SFJ製薬グループ傘下のSFJ製薬X株式会社との共同開発プロトコルやSFJプロトコルに基づいてbentracimabを開発している。難治性高血圧の治療のために,われわれの臨床前候補品PB 6440も開発している。私たちがAlfasigma S.p.A.またはAlfasigmaのbentracimabに権利を与えることに加えて、私たちは私たちのすべての候補製品の世界的な商業権を維持する。
米国食品医薬品局(FDA)からのフィードバックによると,承認手続きを加速することで,米国でのbentracimabの承認を求める予定である。私たちの目標は、この時間が持続範囲の影響を受ける可能性があるにもかかわらず、2022年にbentracimabの生物製品ライセンス申請、またはBLAをFDAに提出することだ
新冠肺炎の大流行の持続時間ですまた,我々のBentracimab INDは最近2021年8月に中国国家医療製品管理局薬物評価センター(CDE)の承認を得た。私たちは2022年上半期に中国の患者を募集する予定です。
著者らはウェブサイト活性化と患者登録を通じて著者らのbentracimab臨床計画を推進することに伴い、著者らはずっと著者らの臨床研究組織、臨床サイトとサプライヤーと密接な関係を維持し、新冠肺炎及びその変異体が著者らの臨床試験と現在のスケジュールに与える影響を評価することを試み、そして著者らは適切な緩和措置を実施してこのような影響の軽減を助けることができるかどうかを考慮する。しかし、現在、新冠肺炎が著者らの試験サイトの開始、患者の募集と評価、研究薬物の提供と試験結果を報告する能力、あるいは私たちがPB 6440を開発する能力に与える影響の範囲を完全に予測することはできない。
2002年の設立以来、私たちの業務は私たちの臨床と臨床前候補製品および私たちの独自のELP技術の開発に集中し、組織と私たちの会社のために人員を配置し、業務計画を制定し、資金を調達し、私たちの知的財産権の組み合わせを構築し、臨床試験と臨床前研究を行ってきた。私たちは候補製品の販売が許可されていないし、製品販売から何の収入も得られていない。設立以来、私たちは主に株式と債務証券の売却、シリコンバレー銀行(SVB)とWestRiver革新融資基金VIII、L.P.またはWestRiverの定期融資、SFJプロトコルによって得られた資金、およびAlfasigma再許可によって得られた資金によって私たちの運営に資金を提供してきた。
設立以来、私たちは重大な運営損失を受けた。2021年12月31日までの1年間の純損失は1兆311億ドルだった。2021年12月31日現在、私たちの累計赤字は3兆918億ドルです。私たちは予測可能な未来に巨額の費用と運営損失が続くと予想している。私たちは持続的な活動に関連する費用が大幅に増加すると予想しています
•私たちが行っているbentracimab臨床試験を継続し、必要に応じて他の臨床試験を開始し、完成させる
•SFJプロトコルおよびAlfasigma分割許可および私たちが生成または受信する可能性のある対応する臨床開発支援費用およびマイルストーン支払いによって、私たちの地理的カバー範囲を拡大することを求めています
•監督部門のbentracimabを抗血小板薬チカグレルの反転剤として承認することを獲得した
•難治性高血圧治療用のPB 6440を開発した
•より多くの臨床と臨床前候補製品の発見と開発を求めています
•私たちの臨床と規制能力を拡大し
•商業化インフラを構築し、外部製造と流通能力を拡大し、私たちが監督管理の許可を得る可能性のある任意の候補製品を商業化し、ベンゼントラマモノクロナル抗体を含む
•市場に適用される製品の要求に適合するために、私たちの法規遵守努力を調整します
•私たちの知的財産権の組み合わせを維持し、拡大し、保護する
•より多くの臨床、製造、科学者を招聘する
•私たちの製品開発および将来可能な商業化努力を支援する人を含む、運営、財務、および管理情報システムおよび人員を増加させること
•上場企業として運営する際には追加の法律、会計、その他の費用が発生する。
財務概要
経営成果の構成部分
収入.収入
再許可収入
再許可収入は、(I)再許可、(Ii)研究および開発活動、および(Iii)特定の材料の製造および供給を含む複数の構成要素を含む、我々が確認したAlfasigma再許可に関連する収入に関する。この手配に基づいて支払われるお金には、払戻不可能な前金、重大な法規と開発活動の完了時のマイルストーンの支払い、ある取り決めの金額で製品を販売し、販売することが含まれています
製品販売のマイルストーンと印税。可変対価格の金額は、収入が将来的に大きな逆転リスクが存在しない可能性が高いまで制限される
再許可契約下の義務を履行する際に確認すべき適切な収入金額を決定する際には、(I)契約で約束された商品またはサービスを識別するステップと、(Ii)区別できるかどうかを含む約束された商品またはサービスが履行義務であるかどうかを決定するステップと、(Iii)可変対価格の制限を含む取引価格の測定と、(Iv)取引価格を履行義務に割り当てるステップと、(V)各履行義務を履行する際に収入を確認するステップとを実行する。
贈与収入
補助金収入は特定の研究プロジェクトでの私たちの努力を支援するために政府から支出された。支給条件を満たすことが合理的に保証され、補助金収入が得られることが合理的に保証されている場合にのみ、補助金収入が確認されます。
運営費
研究開発費
研究開発費には私たちの候補製品の発見と開発に関する費用が含まれています。私たちは発生した費用に応じて研究と開発費用を支払う。これらの費用には
•契約研究組織またはCROおよび臨床試験と臨床前研究を行う研究場所とコンサルタントとの合意に基づいて発生する費用;
•製造および供給規模拡大の費用、および生産検証バッチを含む臨床前および臨床試験供給および潜在的商業供給のコストを取得および製造する
•SFJプロトコルに関連した臨床開発支援費用が発生しました
•アウトソーシング専門科学発展サービス
•従業員に関する費用には、賃金、福祉、株式給与が含まれる
•規制活動に関する費用;
•私たちの研究活動を支援するための実験室材料と用品。
研究開発活動は私たちのビジネスモデルの核心だ。臨床開発後期段階にある候補製品は通常,臨床開発早期段階の候補品よりも高い開発コストを有しており,これは主に後期臨床試験の規模と持続時間が増加しているためである。私たちは今後数年で私たちの研究開発費用が大幅に増加することを予想しています。株に基づく報酬を含めて人員コストを増加させ、ベントラママモノクロナル抗体の後期臨床試験を行い、PB 6440を開発し、他の臨床前研究と臨床試験を行い、監督書類を準備し、監督部門の1つ以上の候補製品の承認を得られれば、商業化努力に備えている。われわれはこれまで肺動脈高圧(PAH)を治療するためのpemziviiptadilの開発に取り組んできたが,戦略評価を行った後,難治性高血圧の治療のためのPB 6440を含むpemziviviptadilのさらなる開発を中止し,資源と資金を再配置し,bentracimabの商業化前活動のための他のパイプライン計画を推進することにした。
私たちの候補製品が開発に成功するかどうかは大きな不確実性を持っている。現在,我々の候補製品の余剰開発を完了するための努力の性質,時間,コストを合理的に見積もることや知ることはできず,これらの候補製品がいつ大量の現金純流入を開始する可能性があるかも分からない。この不確実性は臨床試験の持続時間とコストに関連する多くのリスクと不確定要素であり、多くの要素のため、これらのリスクと不確定要素はプロジェクトの全ライフサイクルで大きく異なる
•規制機関や機関審査委員会は、私たちまたは私たちの研究者が私たちの臨床試験を開始することを遅延させたり、臨床試験場所や契約研究組織と合意を交渉する能力を検討したりします
•私たちは私たちの実験に十分な候補製品を提供することを確実にすることができる
•臨床試験に組み込まれた場所の数は
•適切な患者を募集するのに要する時間の長さ
•最終的に試験に参加した患者数は
•患者が受ける用量の数
•私たちの候補品に関連する副作用は
•新冠肺炎疫病は著者らが試験場所を開始し、患者を募集と評価し、研究薬物を提供し、試験結果を報告する能力に与える影響
•患者のフォロー時間は何ですか
•私たちの臨床試験結果です
私たちの支出は、規制承認の条項と時間、および任意の特許主張または他の知的財産権を提出、起訴、弁護、実行する費用を含む他の不確実性の影響を受ける。私たちは私たちの候補製品が規制部門の承認を得ることに絶対に成功しないかもしれない。私たちの臨床試験は思わぬ結果を得るかもしれない。私たちは私たちの候補製品の臨床試験を停止、延期、または修正することを選択することができる。候補製品の開発のために、これらの変数のいずれかの結果の変化は、候補製品の開発に関連するコストおよび時間の大きな変化を意味する可能性がある。例えば、FDAや他の規制機関が現在予想以上の臨床試験を要求した場合、あるいは任意の臨床試験の登録に重大な遅延があった場合、私たちは臨床開発を達成するために多くの追加の財政資源と時間を費やす必要があるかもしれない。製品の商業化には数年と数百万ドルの開発コストがかかるだろう。
一般と行政費用
一般と行政費用は主に行政と行政機能者の給料と関連費用を含み、株式報酬、出張費用と招聘費用を含む。その他の一般および行政費用には、法律、会計、税務関連サービスの専門費用および保険料が含まれている。
今後数年間の一般的かつ管理費が増加し、現在および将来の候補製品の持続的な研究開発活動、製造活動、bentracimabの潜在的な商業化、上場企業としての運営コストの増加を支援することが予想される。これらの増加には,役員や上級管理職責任保険費用の増加,より多くの人の雇用に関する費用,外部コンサルタント,弁護士,会計士費用の増加が含まれている可能性が考えられる。また、公開報告会社に適用されるコーポレート·ガバナンス、内部統制、投資家関係、開示、類似要件を遵守するコストが増加することも予想される。
その他の収入
開発由来負債の再計量損失
再計量開発由来負債の損失は、受信された推定コストの現在値およびSFJプロトコルの契約条項に従って支払われる推定コストを再評価する各報告日に反映され、これらの推定コストは、公正価値として決定される。負債は四半期末に3級デリバティブとして再計量され、公正価値の変化が経営報告書に記録されている。
利子収入
利息収入には、現金と現金等価物口座内の資金の利息収入が含まれる。
利子支出
利息支出には私たちがSVBとWestRiverと定期的に融資した利息支出が含まれている。
所得税支給
所得税支出はAlfasigmaから支払われた最初の支払いの国際源泉徴収税を含む
ライセンス、共同開発、その他の合意
医療免疫有限許可プロトコル
2017年11月、私たちは医療免疫有限会社やアスリコンの完全子会社医療免疫有限会社と独占ライセンス契約、あるいは医療免疫許可と呼ばれています。医療免疫許可プロトコルによれば、医療免疫会社は、その所有または制御されたいくつかの特許権に基づいて、任意のヒト疾患または疾患の治療、緩和、診断または予防のために、医療免疫許可プロトコルに含まれる任意の製品または医療免疫許可製品を開発および商業化するために、我々の独占的な世界的許可を付与する。MedImmuneライセンスによると、私たちはMedImmuneに10万ドルの前払い費用を支払った。MedImmuneが提供する技術サービスに関連する四半期費用、2021年12月31日までに発生した300万ドルの臨床および規制マイルストーン費用、5,000万ドルまでのビジネスマイルストーン費用、およびMedImmuneライセンス製品の純売上のうちの上位から低い許可使用料の割合は、特定の状況に応じてMedImmuneに支払う必要があります。さらに、MedImmuneライセンスは、第三者製品のストレージコストのオプションを提供します。MedImmune許可から2021年12月31日まで,MedImmune許可の下で360万ドルのコストが発生した.
SFJ製薬会社と共同開発で合意した
2020年1月、SFJ協定に署名し、SFJプロトコルにより、SFJは私たちに資金を提供し、世界的にbentracimabを抗血小板薬であるチカグレルの逆転薬として開発し、制御できない大出血や生命に危険な出血、あるいは緊急手術または侵襲手術を必要とする患者に使用することを支持した。2020年3月、私たちはシリコンバレー銀行(SVB)の同意を得て、bentracimabを製造、使用、または販売するために必要なSFJに、私たちが所有または制御しているすべての資産の保証権益を付与した。SFJプロトコルによると、SFJはbentracimabの臨床開発を支援するために最大1.2億ドルを支払うことに同意している。9000万ドルの初期資金に加えて,bentracimabの特定のあらかじめ定義された臨床開発マイルストーンに達している別の3000万ドルの資金を得ることを選択した。SFJ協定が発効して2021年12月31日まで、SFJはSFJ協定に基づいて吾らを代表して資金および支払総額9,130万ドルを提供している。SFJはまた、2870万ドルの追加臨床試験費用およびその他の費用を援助または精算すると予想される。SFJプロトコルの有効期間内に,我々は主に米国とEUのベンゼントラママママブの臨床開発と規制活動を担当し,SFJは主に中国と日本のbentracimabの臨床開発と監督活動を担当し,EUで臨床試験運営支援を提供する。
SFJ協定の条項によると、FDAがbentracimabのBLAを承認した後、SFJに初回支払い500万ドルを支払い、7回の追加年間支払いで合計3.25億ドルを追加支払います。EMAまたはいくつかのヨーロッパ諸国の国家規制機関がBLAに相当するbentracimabマーケティング許可申請またはMAAを承認した場合、私たちはSFJに500万ドルの頭金を支払い、7年以内に合計2.05億ドルを追加的に支払う。もし日本の薬品監督管理局あるいは中国国家薬品監督管理局がベントラマズマブのマーケティング申請を許可した場合、私たちはSFJに100万ドルの頭金を支払い、毎年合計5,900万ドルを追加支払います
上記のいずれかの管轄区域がBentracimabを承認したBLAまたはMAAの120日後に、私たちは、私たちの選択に基づいて、中央値割引率を反映した価格で、当社の選択に基づいて、中央値割引率を反映した価格で、この管轄区域の将来支払われていない承認支払いの全部または一部を買収する権利がある(すなわち、米国承認支払い、EU承認支払い、または日本/中国承認支払い)。当社の支配権変更後120日以内に、当社または私たちの相続人は、支配権変更前にBLAまたはMAAが承認された任意の司法管轄区域が、将来支払われていない承認支払いのすべてまたは一部をビット数割引率中央値を反映した価格で購入することを選択する権利があり、SFJが以前にこのようなお金を受信する権利を第三者に譲渡していないことを前提としています(この場合、私たちまたは私たちの相続人にはその権利はありません)。
SFJプロトコルの終了後、吾らはBentracimabの開発を継続し、米国、EU、日本、または中国でBLAの承認を得た場合、SFJプロトコルが終了していないように、終了時に支払われた任意の金をSFJに支払うが、SFJが満期になったときに任意のお金を支払うことができずにSFJプロトコルを終了したり、SFJプロトコルで定義されている重大な不利益によりSFJプロトコルを終了したりすると、当該等の承認支払いを支払う義務は50%減少する。
デューク大学許可協定
2006年10月、デューク大学またはデューク大学と独占ライセンス契約を締結し、最近改訂されたのは2019年4月、またはデューク大学ライセンス。デュークライセンスによると、デュークは、デュークが所有または制御しているいくつかの特許権に基づいて独自のグローバルライセンスを付与し、デュークの特定のノウハウに基づいて、デュークライセンスがカバーする任意の製品、またはデュークライセンスの製品を開発および商業化するために、デュークの特定の独自のグローバルライセンスを付与し、ELPに関連する。デューク許可証によると、私たちはデューク許可証の修正に関連する追加費用20万ドル、その他の追加許可料20万ドルをデュークに37,000ドルの前払い費用を支払った。付与に対する許可権
アメリカでは、私たちは最初に24,493株のデューク社の普通株を発行した。私たちはある規定の株式マイルストーンに達する前に、時々Dukeに普通株を発行し、その総保有量が私たちが発行した株と発行した株の7.5%を占めるようにする義務がある。私たちはまた、デューク大学に以下の費用を支払う必要があります:最高220万ドルの規制と臨床マイルストーン費用、最高40万ドルの商業マイルストーン費用、デューク大学許可製品の純売上の低い桁の特許権使用料の割合は、私たちがいくつかの商業マイルストーンを達成した後、最低20万ドルの特許権使用料を支払うべきであり、最高30万ドルまたは私たちが第三者から受け取った費用のより低い2桁の数百分比は、デューク大学許可下のいくつかの特許権利について戦略同盟を構築することを考慮しなければならない。私たちはまたDukeに私たちが再許可者から受け取った最初の100万ドルの非特許権使用料を支払い、そしていくつかの条件に基づいて、私たちが受け取った任意の追加の非特許権使用料の低い2桁の数百分を支払わなければならない。Duke許可から2021年12月31日まで、私たちはDuke許可の下で30万ドルの印税コストを発生させた。私たちはまたデューク大学ライセンス下のすべてのアメリカと外国特許権の申請、起訴、維持を要求された。
Alfasigma分割許可協定
2021年6月、我々はAlfasigmaとAlfasigma再許可協定を締結し、この合意に基づいて、再許可区域内でbentracimabまたは許可製品を含む任意の製品を開発、使用、販売、販売、カプセル販売、および輸入するAlfasigmaに独占的な権利を付与した。Alfasigma再許可の条項によると、2021年7月、Alfasigmaから2000万ドルの前金を受け取り、ある収入を達成する前の規制マイルストーンを達成する際には、最高3500万ドルを得る資格があり、ある商業マイルストーンの実現と純売上高分別の特許使用料の支払い後、最高1.9億ドルを得る資格があり、パーセントは低い2桁から始まり、25%前後に上昇していく。
3500万ドルまでの規制マイルストーン支払いについて:(I)EMAが最初の許可製品の薬物承認申請を受けた後に1000万ドルを支払う;(Ii)EMAの条件付き規制承認を得た後に1250万ドルを支払う;および(Iii)残りの1250万ドルは、EMAの無条件規制承認を得た後に支払い、以下の2つの場合に、テカグレルの抗血小板作用を逆転させるための許可製品の処方を許可する:(A)制御できない重大または生命に危険な出血がある患者と(B)緊急手術または侵襲的手続きを必要とする患者。
Alfasigma分割許可によれば、私たちは、任意のマーケティング許可がAlfasigmaに割り当てられることを含む、SFJプロトコルに従って、任意のマーケティング許可がAlfasigmaに割り当てられることを含むEMAおよびMHRAの規制承認を保証する責任がある。アルファシマには、マーケティングや特許製品の販売に必要な任意の規制承認(定価承認や発売後の約束を含む)を取得し、欧州やイギリス以外の国の規制承認を確保する義務がある。私たちはまた、より低いコストまたはいくつかの合意された金額を超えない価格でAlfasigmaに許可製品を提供することに同意する。2021年12月31日までの年間で、Alfasigmaの許可下で1080万ドルとゼロ収入を確認しました2020それぞれ,である.
バク許可協定
2019年4月、私たちはバク生物技術有限会社またはバクとライセンス契約、すなわちバクライセンス契約を締結しました。この協定によると、バクはいくつかの知的財産権に基づいてバクの独自技術を使用することを許可してくれました大腸菌.大腸菌指定されたアジア諸国以外の世界範囲でbentracimabの菌株を生産し、bentracimabを商業化し、承認されれば、私たちまたは私たちに代わってバクの特許を使用して製造されます大腸菌.大腸菌世界的にストレスを与えています私たちは本許可に基づいて再許可を与える権利がありますが、バク許可協定に規定されているいくつかの条件を守らなければなりません。協定条項によると、私たちは固定的で象徴的な単位あたりの特許権使用料を支払う必要があり、この数字は調整される可能性があり、固定ユーロ金額で支払われる年間許可料は、金額が低いから中6桁になる可能性がある。この協定は一定期間有効であり、私たちの印税義務が満了した後、許可は全額支払いとみなされ、非独占許可に変換されます。指定された日数内に是正されなければ,いずれも違約によりバク許可プロトコルを終了することができる.著者らはバクから別のcGMPメーカーBioVectraに現在のbentracimab製造技術を譲渡する技術移転を完成し、BioVectraを招いて著者らが行っている臨床試験のために薬剤を製造し、監督許可を得た後に商業供給のbentracimabを生産した。 バク許可協定が始まって2021年12月31日までに90万ドルのコストが発生しました
Viamet資産購入契約
2020年1月にViamet PharmPharmticals Holdings,LLCおよびその完全子会社Selenity Treateutics(バミューダ)有限会社または売り手と購入契約またはPB6440契約を締結しました
売り手固有のCYP 11 B 2阻害剤化合物(以前はSE-6440またはVT-6440と呼ばれていた)に関連するすべての資産および知的財産権を買収し、PB6440プロトコルに従って得られた特許権によってカバーされたいくつかの他のCYP 11 B 2阻害剤化合物を買収するか、またはこれらの化合物を同時に買収する。PB6440協定の条項によると、私は取引が完了した時に売り手に前払い費用10万ドルを支払う必要があり、吾らはある化合物を含む候補製品についていくつかの開発と知的財産権マイルストーンを取得した時に売り手に最大510万ドルを支払い、化合物を含む承認された製品についていくつかの商業マイルストーンを達成した時に売り手に最高1.425億ドルを支払う必要があり、化合物を含む承認された製品の純売上高について中から中の桁までの特許権使用料のパーセンテージで最高1.425億ドルを支払う必要があるが、特定の場合は慣例に従って減収及び相殺しなければならない。PB 6440プロトコルが開始されてから2021年12月31日まで,我々はPB 6440プロトコルにより10万ドルのコストを発生させた.
BioVectra供給プロトコル
2021年3月、私たちはBioVectraまたはBioVectraプロトコルと、bentracimab用の原料薬をBioVectraから製造および供給し、規制の承認を得たら商業流通に使用する供給協定を締結した。私たちはまたBioVectraを招いて私たちが行っている臨床試験のための医薬物質を製造した。
BioVectra協定の条項によると、BioVectraは、商業流通のために毎年合意されたロットの製品を生産する能力を維持することを約束し、指定された最低ロット製品を毎年購入すること、または最低年度約束を約束することを約束し、第三者とベンゼントラマママブを生産する契約を自由に締結することができるが、私たちは各ロットのbentracimabの供給価格を支払い、これは製品の製造過程がBioVectraプロトコルによる検証を行った後、いくつかの消耗品、原材料、第三者テストのコストを加えて決定する。
最低年度約束によると、(I)2022年から2023年までの間に約1,400万ロットのbentracimabを購入すること、(Ii)2024年に約3,700万ロットのbentracimabを購入すること、および(Iii)2025~2031年に毎年約4,800万ドルのbentracimabを購入することを義務とするもし私たちが特定の年に適用された最低年間約束を購入しなかった場合、私たちはBioVectraに金額を支払う義務があり、金額は当時適用された各ロットの供給価格にその年の最低年間約束とその年に実際に購入したベンゼントラマモノクロナルロットとの差額、または最低差額を乗じて、BioVectraがその年度に私たちが注文したロットを渡すことができない限りである。BioVectraがある年に私たちが注文した数量で製品を供給できなかった場合、私たちはその年(および可能な1年または複数年)に対する最低年間約束は減少し、私たちはその年(および可能な1年または複数年)に最低差額を支払う義務を放棄するだろう。私たちは2026年以降の最低年間約束額を毎年最大1つの特定の最高パーセントに減らす権利があるだろう。また、私たちがbentracimabを使用した製品の規制承認を米国またはヨーロッパのいずれかでしか得られない場合、BioVectraと私たちは、製品要求の低減と供給価格への影響を反映して、より低い数量約束を反映するために、BioVectraプロトコルの修正案を誠実に議論することに同意した。
経営成果
2021年12月31日までと2020年12月31日までの年度比較
次の表は私たちの行動結果(千計)をまとめています
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | |
| 2021 | | 2020 | | 変わる |
| 収入: | | | | | |
| 再許可収入 | $ | 10,831 | | | $ | — | | | $ | 10,831 | |
| 奨学金収入 | — | | | 320 | | | (320) | |
| 総収入 | 10,831 | | | 320 | | | 10,511 | |
| 運営費用: | | | | | |
| 研究開発 | 102,107 | | | 72,088 | | | 30,019 | |
| 一般と行政 | 16,086 | | | 13,088 | | | 2,998 | |
| 総運営費 | 118,193 | | | 85,176 | | | 33,017 | |
| 運営損失 | (107,362) | | | (84,856) | | | (22,506) | |
| その他(費用)収入: | | | | | |
| 再計量開発デリバティブ負債の損失 | (21,182) | | | (12,507) | | | (8,675) | |
| 利子収入 | 14 | | | 237 | | | (223) | |
| 利子支出 | (947) | | | (1,445) | | | 498 | |
| 外国為替収益 | 6 | | | 6 | | | — | |
| その他費用合計 | (22,109) | | | (13,709) | | | (8,400) | |
| 所得税前純損失 | (129,471) | | | (98,565) | | | (30,906) | |
| 所得税支給 | 1,600 | | | — | | | 1,600 | |
| 純損失 | $ | (131,071) | | | $ | (98,565) | | | $ | (32,506) | |
再許可収入
2021年12月31日現在の事業年度では、再許可収入は1080万ドルであるが、2020年12月31日現在の年度では、子可収入はゼロである。この増加は私たちがAlfasigma再許可に従って初期支払いから確認した収入に起因する
贈与収入
2021年12月31日までの1年間の贈与収入はゼロですが、2020年12月31日までの1年間の贈与収入は30万ドルです。2020年12月31日現在,米国国立衛生研究院は小企業革新研究助成金に基づいて提供した280万ドルの資金がすべて到着し,PAH治療のためのPemziviviptadilの臨床開発を支援している
研究開発費
2021年12月31日までの1年間の研究開発支出は1.021億ドルだったが、2020年12月31日までの1年間の研究開発支出は7210万ドルだった。3,000万ドル増加したのは主に臨床費用の増加によるものです
Bentracimabに関する薬品生産活動,bentracimab生産に関連する設備減価償却コスト,従業員増加による人員コスト,および我々の一般研究作業に関するコスト。
以下の表は、我々の研究開発費(単位:千)を機能分野別にまとめたものです
| | | | | | | | | | | | | | | | | | | | |
| | 現在までの年度
十二月三十一日 | | |
| | 2021 | | 2020 | | 変わる |
臨床前と臨床発展 | | $ | 88,717 | | | $ | 62,166 | | | $ | 26,551 | |
補償と関連福祉 | | 8,003 | | | 7,023 | | | 980 | |
| 株に基づく報酬 | | 759 | | | 643 | | | 116 | |
施設費 | | 1,722 | | | 1,149 | | | 573 | |
他にも | | 2,906 | | | 1,107 | | | 1,799 | |
研究と開発費用総額 | | $ | 102,107 | | | $ | 72,088 | | | $ | 30,019 | |
| | | | | | |
私たちの研究開発費(単位:千)を候補製品ごとにまとめてみました
| | | | | | | | | | | | | | | | | | | | |
| | 現在までの年度
十二月三十一日 | | |
| | 2021 | | 2020 | | 変わる |
| 対外研究開発費を計画する | | | | | | |
| Bentracimab | | $ | 77,964 | | | $ | 48,539 | | | $ | 29,425 | |
| ペメヴィタジル | | 9,571 | | | 12,284 | | | (2,713) | |
未分配の研究開発費: | | | | | | |
報酬と株の報酬 | | 8,762 | | | 7,666 | | | 1,096 | |
他の研究と開発 | | 5,810 | | | 3,599 | | | 2,211 | |
研究と開発費用総額 | | $ | 102,107 | | | $ | 72,088 | | | $ | 30,019 | |
我々はPemziviviptadilの開発を中止し,bentracimabの商業化前活動のための資源と資金の再配置,難治性高血圧の治療のためのPB 6440を含む他のパイプライン計画の推進を計画している。
一般と行政費用
2021年12月31日までの1年間は、一般·行政費は1610万ドルだったが、2020年12月31日までの年間は1310万ドルだった。300万ドル増加の主な原因は,コンサルティングや法律サービスに関する専門サービスや人手増加による人件費の増加である。
開発由来負債の再計量損失
2021年12月31日までの年度の再計量発展由来負債の損失は2,120万ドルであるのに対し、2020年12月31日までの年度は1,250万ドルである。この負債は、最初に、受信された推定コストの現在値と、SFJプロトコルの契約条項に従って支払われるべき推定コストとの現在値に従って入金され、これらの推定コストは、公正価値として決定される。派生負債はその後、年末に3級派生ツールに再計量され、費用増加は再計量後の変化を反映している。
利子収入
2021年12月31日までの1年間の利息収入は1.4万ドルだったが、2020年12月31日までの年間の利息収入は23.7万ドルだった。22.3万ドル減少したのは、2020年の間に現金と現金等価物残高の増加および金利上昇によるものだ。
利子支出
2021年12月31日までの1年間の利息支出は90万ドルだったが、2020年12月31日までの1年間の利息支出は140万ドルだった。50万ドル減少したのは、2019年の融資項目で2020年の借金が増加したためだ
2019年ローンに関する情報は、本年度報告Form 10-Kの“財務諸表付記”の“付記6.債務”を参照してください。
所得税支給
所得税は2021年12月31日までの年間160万ドルであるが、2020年12月31日までの年間はゼロである。増加の理由はAlfasigmaライセンスに従ってイタリアで2000万ドルの税金を前払いしたからだ。
流動性と資本資源
現金需要と持続的な経営
資金需要
私たちの資本の主な用途は、私たちの臨床と臨床前開発計画を引き続き推進することである。私たちの推定は間違っていることが証明される可能性があるという仮定に基づいており、私たちは現在予想されているよりも早く私たちが利用できる資本資源を使用するかもしれない。候補製品の開発や商業化に関連する多くのリスクや不確実性により、候補製品開発を完了するために必要な増加した資本支出や運営支出を見積もることができない。
私たちの短期と長期の実物現金需要には業務と資本支出が含まれており、その中のいくつかは契約義務を含んでいる。私たちの現金は主に給料と福祉の支払い、臨床試験の管理、必要な技術と施設を提供して私たちの運営を支援します。最も重要な契約義務はペンシルバニア州とカリフォルニア州での施設の運営レンタルです。2021年12月31日現在、私たちの将来の最低賃貸支払い総額は、短期賃貸負債に関連する50万ドル、長期賃貸負債に関する110万ドルです。レンタル負債の詳細については、本年度報告Form 10-Kの“財務諸表付記”の“付記10.リース”を参照されたい。現在の現金と現金等価物、および予想および潜在的なマイルストーン支払いによって、これらの需要に資金を提供する予定です。
これまで、承認された薬品の商業販売から何の収入も得られておらず、少なくとも今後数年以内に実質的な収入は生じないと予想されている。候補製品の開発が間に合わなかったり、彼らの規制承認が得られなかったりすれば、将来的に収入を創出する能力が影響を受けるだろう。私たちは、規制部門の承認を得て、私たちの候補製品を商業化しなければ、私たちの候補製品から何の収入も生じないかどうかは保証できません。私たちは私たちが行っている活動に関連する費用が増加することを予想して、特に私たちが候補製品の臨床試験を研究、開発、継続、あるいは開始し、マーケティング承認を求める時に。また、私たちの任意の候補製品が承認されれば、販売、マーケティング、製造、流通に関連した巨額の商業化費用が発生すると予想される。私たちは私たちの持続的な業務と関連した多くの追加資金が必要だと予想する。もし私たちが必要な時や魅力的な条件下で資金を集めることができなければ、私たちは私たちの研究開発計画や将来の商業化努力を延期、減少、または廃止させることを余儀なくされるかもしれない。
純損失と運営キャッシュフローが負の状況を経験し,2021年12月31日現在の累計赤字は3.918億ドルであった。私たちは少なくとも今後数年以内に純損失が続くと予想している。2021年12月31日現在、私たちの既存の現金と現金等価物に、SFJが2870万ドルの臨床試験コストおよびその他の費用を援助または精算することが予想されていることに加えて、本Form 10-K年度報告書に含まれる財務諸表の発表日から12ヶ月の運営費用と資本需要を支払うのに十分ではないと信じています。これらの要因は、私たちが経営を続けている会社として経営を続ける能力を大きく疑わせています。“リスク要因-本年度報告書10-K表に記載されている監査人が、2021年12月31日までの財政年度財務諸表の審査を経た意見には、経営を継続する能力があるかどうかを示す説明が含まれている。また、SFJ協定によれば、SFJプロトコルで規定されている期間内にこのような持続的な経営状況を修復しなければ、SFJは、bentracimabに関連する業務をSFJに移行させることを選択することができ、bentracimabの商業化収入を共有する能力は重大で不利な影響を受ける。 もし私たちが現在の運営計画を支援するために追加の資金を得ることができなければ、私たちは私たちの開発計画の範囲を延期または縮小し、および/または私たちの運営を制限または停止させることを余儀なくされるかもしれない。我々の既存の現金と現金等価物をわれわれの臨床と臨床前開発計画の推進に用いる予定である。私たちの推定は間違っていることが証明される可能性があるという仮定に基づいており、私たちは現在予想されているよりも早く私たちが利用できる資本資源を使用するかもしれない。候補製品の開発や商業化に関連する多くのリスクや不確実性のため、候補製品の開発や潜在的な商業化を達成するために必要な資本支出や運営支出の増加額を見積もることはできない。また、本年度報告の他の部分の財務諸表付記1を参照して、私たちの評価情報を理解してください。
私たちの短期的で長期的な未来の資本需要は多くの要素に依存するだろう
•私たちが行って計画しているbentracimab、PB 6440、および私たちの他の臨床前計画の臨床試験の進展と結果
•SFJプロトコルとAlfasigma再許可に従って支払いを受けた時間と金額;
•私たちは追求する任意の未来の製品の臨床前開発、実験室テストと臨床試験の範囲、進捗、結果、コストを決定することができる
•私たちが他の候補品や技術を開発、許可、または取得する程度
•私たちが追求する可能性のある他の候補製品の数量と開発要件
•私たちの候補製品に対する規制審査のコスト、時間、結果
•将来の商業化活動のコストと時間は、製品製造、マーケティング、販売、流通を含み、私たちが市場の承認を得た任意の候補製品について
•私たちが発売許可を得た候補製品の商業販売収入(もしあれば)
•私たちは協力関係を構築し、ベンゼントラママママブやアメリカ以外の他の候補製品を商業化することができます
•特許出願を準備し、提出し、起訴し、私たちの知的財産権を維持し、実行し、知的財産権に関連する任意のクレームを弁護するコストと時間。
潜在的な候補製品を決定し、臨床前研究と臨床試験を行うことは時間がかかり、高価かつ不確定な過程であり、長年を必要とし、しかも著者らは永遠に市場の許可を得て製品販売を実現するために必要なデータ或いは結果を生成できないかもしれない。しかも、私たちの候補製品が承認されれば、商業的成功を得られないかもしれない。私たちのビジネス収入は、もしあれば、短期的には商業的に使用できないと予想される候補製品を販売します。
私たちの未来の商業収入は、もしあれば、製品の販売から来て、私たちはこれらの製品が2023年に商業化されると予想しています。もしあれば。したがって、私たちは追加的な資金調達に依存して私たちの業務目標を達成し続ける必要があるだろう。私たちは受け入れ可能な条項で十分な追加融資を受けることができないかもしれないし、根本的にできないかもしれない。もし私たちが株式または転換可能な債務証券を売却することで追加資本を調達すれば、これらの持分証券または債務の条項は私たちの運営能力を制限するかもしれない。任意の将来の債務融資および持分融資は、ある場合、追加債務を負担すること、資本支出を行うこと、利益共有を達成すること、または他の計画を達成すること、または配当を宣言することなど、私たちが具体的な行動をとる能力を制限および制限する契約を含む可能性がある。もし私たちが政府または個人的な寄付金、協力、戦略連合、または第三者とのマーケティング、流通、または許可手配によって追加資金を調達する場合、私たちは、私たちの技術、将来の収入源、研究計画、または候補製品に対する貴重な権利を放棄するか、または私たちに不利になる可能性のある条項で許可を与えることを要求されるかもしれない。また、我々の追加資本調達能力は、世界経済状況の潜在的な悪化や、米国と世界の信用と金融市場の最近の持続的な新冠肺炎の流行による中断と変動の悪影響を受ける可能性がある。
提出期間内に、私たちは何の表外手配もありませんが、このような手配は私たちの財務状況、財務状況、収入或いは支出、経営業績、流動資金、現金需要或いは資本資源の変化、或いは私たちの財務状況、財務状況、収入或いは支出の変化、或いは私たちの財務状況、現在或いは未来に重大な影響を与える可能性があります。
流動資金源
私たちが設立して以来、私たちは製品販売から何の収入も得ていません。私たちの運営は純損失と負のキャッシュフローを生み出しました。私たちは主に私たちの普通株、私募転換可能債券、転換可能優先株、私たちの定期融資下の借金、SFJプロトコルとAlfasigma再許可によって得られた資金を公開することで、私たちの業務に資金を提供します。将来的には,SFJはSFJプロトコルに従って2,870万ドルまでの追加資金を提供することが予想され,これは我々のbentracimab臨床開発に関連する特定のマイルストーンに基づく実現である。2021年12月31日現在、私たちは4180万ドルの現金と現金等価物を持っている
私たちは、株式または債務融資、または政府または他の第三者融資、マーケティングおよび流通プロトコル、ならびに他の協力、戦略連合、および許可プロトコルの組み合わせによって、私たちの流動性需要を満たすための追加資金を求める予定です。私たちは私たちが受け入れ可能な条件で追加的な資金を得ることができないという保証がない。もし私たちが十分な追加資金を得られなければ、私たちは要求されるだろう
私たちの既存の資金を拡大するために特定の支出を減らす。もし私たちが十分な資金を集めることができなければ、私たちは私たちの資産の一部または全部を清算しなければならないかもしれないし、あるいは私たちは範囲を延期したり、縮小したり、私たちの開発計画や臨床試験の一部または全部をキャンセルしなければならないかもしれない。私たちはまた、私たちの製品の開発や商業化を延期したり、私たちが商業化を求めていた製品や技術の商業化権利を第三者にライセンスしなければならないかもしれない。また,SFJプロトコルにより,プロトコルが規定する期限内にその継続経営条件を救済できなければ,SFJはbentracimabに関する業務をSFJに移行することを選択することができる.もし私たちがbentracimabに関連するビジネスがSFJに移行すれば、SFJがbentracimabへの投資から300%のリターンを得るまで、bentracimabの商業化された収入を共有しないだろうし、その後、bentracimabの米国およびあるヨーロッパ諸国での純販売から1桁の中央値の特許権使用料を得る権利があり、SFJがbentracimabへの投資で合計500%のリターンを得た後、世界の他の地域のbentracimabの純売上高で中央値の特許使用料を得る権利がある。このような要素のいずれも私たちの経営業績と未来の見通しを損なう可能性がある。
2019年12月、2020年1月に発効する2019年の保留登録声明を表S-3に提出しました。“2019年棚登録声明”は、(I)最高合計2億ドルの普通株、優先株、債務証券、引受権証を1回または複数回の発売、および任意の組み合わせで発売、発行、販売することができ、(Ii)市場販売契約またはATM機に基づいて発行および販売を計画することができる最高合計6000万ドルの普通株を発売、発行、販売することができるATM機計画によると発行·販売可能な6,000万ドルの普通株式は、2019年の棚登録声明に基づいて発行·販売可能な2億ドルの証券に含まれている2020年12月31日までの1年間に、ATM計画により、普通株561,848株を1株5.41ドルの加重平均価格で売却し、290万ドルの純収益を得た。2021年12月31日までの年間で6040万ドル2021年3月の引受公募から開始。また,2022年1月10日にATM計画により500,000株の普通株を発行し,120万ドルの純収益を提供した。
2020年1月にSFJプロトコルを締結し,SFJプロトコルによりSFJが資金提供に同意し,bentracimabを抗血小板薬であるチカグレルの反転剤として開発することを支援した。SFJプロトコルによると、SFJはbentracimabの臨床開発を支援するために最大1.2億ドルを支払うことに同意している。9000万ドルの初期資金に加えて,bentracimabの特定のあらかじめ定義された臨床開発マイルストーンに達している別の3000万ドルの資金を得ることを選択した。SFJ協定が発効して2021年12月31日まで、SFJはSFJ協定に基づいて吾らを代表して資金および支払総額9,130万ドルを提供している。SFJはまた、2870万ドルの追加臨床試験費用およびその他の費用を援助または精算すると予想される。
2021年3月、“2019年棚登録声明”によると、普通株の貸切公開を完了し、引受割引と手数料、その他の発行コストを差し引いた後、1株3.50ドルの公開発行価格で合計18,400,000株の普通株を発行·販売し、純収益は6,020万ドルであった。2021年12月31日現在、1億326億ドルの普通株式が2019年の棚登録声明に基づいて販売でき、そのうち5700万ドルはATM計画に従って販売することができます。
2021年7月、Alfasigma再許可に基づいて、私たちはAlfasigmaから2000万ドルの前払いを受けた。私たちはある収入を実現する前に規制マイルストーンを達成する時に最高3,500万ドルを獲得する資格があり、ある商業マイルストーンを実現し、純売上高別に特許権使用料を支払う時に最高1.9億ドルを獲得し、パーセンテージは低い2桁から25%程度に上昇していく。
キャッシュフロー
次の表は、以下の各時期のキャッシュフロー(千単位)をまとめたものである
| | | | | | | | | | | |
| 現在までの年度 十二月三十一日 |
| 2021 | | 2020 |
経営活動のための現金純額 | $ | (47,416) | | | $ | (59,957) | |
投資活動のための現金純額 | (2,679) | | | (1,412) | |
融資活動が提供する現金純額 | 63,773 | | | 15,466 | |
| 現金および現金等価物の純増加(減額) | $ | 13,678 | | | $ | (45,903) | |
経営活動
2021年12月31日までの年間で、経営活動のための現金純額は4740万ドル。現金の使用は主に私たち1.311億ドルの純損失と関係があるが、5430万ドルの非現金支出および2940万ドルの運営資産と負債の変化部分によって相殺された。非現金支出には主に2870万ドルの研究と
SFJが私たちの代わりに支払った開発費用、開発由来負債の赤字2,120万ドル、株ベースの補償230万ドル、減価償却と償却180万ドルを再計量しました。私たちの経営資産と負債の変化による純現金流量は主に私たちの繰延再許可収入が920万ドル増加し、売掛金が900万ドル増加し、計算費用と他の流動負債が370万ドル増加し、前払い費用と他の資産が750万ドル減少したためである。売掛金の増加は,薬物製品の製造とbentracimabの臨床研究活動の増加によるものである。前払い費用減少の要因は,bentracimabの薬物製造に関する支払い時間である。
2020年12月31日までの1年間、経営活動のための現金純額は6000万ドルだった。現金の使用は主に私たちの純損失9860万ドルと、私たちの運営資産と負債の430万ドルの変化によるものです。現金の使用は非現金支出部分によって相殺され、主にSFJが私たちに代わって支払った2,700万ドルの研究·開発費、1,250万ドルの開発デリバティブ負債の再計量損失、220万ドルの株式報酬である。私たちの営業資産と負債の変化は主にbentracimabに関連する薬品製造支払いにより前払い費用が840万ドル増加したが、売掛金が190万ドル増加し、売掛金が100万ドル増加したことと、贈与収入を受けたスケジュールにより他の売掛金が120万ドル減少したことで、この増加を部分的に相殺した。
投資活動
投資活動のための現金純額は、2021年12月31日と2020年12月31日までの年間でそれぞれ270万ドルと140万ドルで、財産や設備の購入に使われている。
融資活動
2021年12月31日までの1年間で,融資活動が提供した現金純額は6,380万ドルであり,主に2021年3月に引受された公開発行純収益6,040万ドル,SFJ協定により受け取った820万ドル,株式オプション行使収益40万ドルと,従業員株式購入計画により購入された株式収益30万ドルが,550万ドルの長期債務返済によって一部相殺されたためである。
2020年12月31日までの年間で、融資活動が提供する現金純額は1,550万ドルであり、SFJ協定により1,520万ドルを受け取ったことと、ATM計画での販売収益は290万ドルであったが、一部は270万ドルの長期債務返済によって相殺されたためである。
肝心な会計見積もり
私たちの経営陣は財務状況と経営結果の討論と分析は私たちの財務諸表に基づいています。これらの報告書はアメリカ公認会計政策やGAAPに基づいて作成されています。これらの財務諸表を作成する際には、報告中に報告された資産および負債額、貸借対照表の日付までの、または有資産および負債の開示、および報告の費用金額に影響を与えるために、推定、判断、および仮定を行う必要がある。公認会計原則に基づいて、私たちは私たちの推定と判断を評価し続けている。
重大な見積もりには,我々が検討·開発コストを決定する際に用いる仮説と,再許可収入と開発由来負債の推定値に投入するための仮定がある。我々は歴史的経験や当時の状況では合理的な様々な他の要因を推定していると考えられるが,これらの要因の結果は資産や負債の帳簿価値を判断する基礎となっており,そのような資産や負債の帳簿価値は他の源から容易に見られるものではない。異なる仮定または条件では、実際の結果は、これらの推定値とは異なる可能性がある。
私たちが財務諸表を作成する際に使用する判断と見積もりには、以下の会計政策が最も重要であると考えられる。我々の重要会計政策の検討については、本年度報告その他の部分の財務諸表付記2を参照されたい。
研究と開発費用を計算すべきである
これまで、私たちの運営費の大部分は研究や開発活動で発生してきた。財務諸表作成過程の一部として,サプライヤー,コンサルタント,研究組織と締結された契約のうち臨床や臨床前活動の展開に関する義務による費用を見積もる必要がある。これらの契約の財務条件は、契約によって異なり、支払流量がこれらの契約に基づいて材料またはサービスを提供する期限と一致しない可能性がある交渉を行う必要がある。我々は財務諸表に臨床前研究と臨床試験費用を反映し、これらの費用をサービスと努力支出の時間と一致させる方法である。著者らは臨床前研究或いは臨床研究の進展に基づいてこれらの費用を計算する
臨床前研究または臨床試験または関連活動の各方面の時間によって測定される試験。我々の予算は,関連契約の審査および財務モデルの準備によって決定されるとともに,臨床前研究や臨床試験や進行中の他のサービスの進展について研究や他のキーパーソンとの検討を考慮している。臨床前研究や臨床試験過程において,実際の結果がわれわれの最初の見積もりと異なれば,費用認知率を調整する。
発展誘導負債
2020年1月、SFJ協定に署名し、SFJプロトコルに基づいて、SFJは、制御できない大出血や生命に危険な出血または緊急手術または侵襲手術を必要とする患者のための抗血小板薬であるテカグレルの逆転薬としてのbentracimabの世界開発を支援する資金を提供する。SFJプロトコルによると、SFJはbentracimabの臨床開発を支援するために最大1.2億ドルを支払うことに同意している。
FDAがBentracimabのBLAを承認した場合、私たちはSFJに500万ドルの頭金を支払い、7回の追加年間支払いに3.25億ドル、すなわち米国が支払いを承認することに同意した。EMAまたはいくつかのヨーロッパ諸国の国家規制機関がbentracimabの上場承認を提供した場合、SFJに500万ドルの頭金を支払い、7つの追加年間支払いに2.05億ドルを追加的に支払うか、またはEUが支払いを承認する。大部分のアメリカの承認支払いとEUの承認支払いは適用司法管轄区域の上場承認三周年から七周年の間に支払います。もし日本の薬品と医療機器庁、日本の薬品と医療機器庁、あるいは中国国家薬品監督管理局がベントラマズマブの発売許可を提供した場合、SFJに100万ドルの頭金を支払い、8つの追加の年間支払いの中で合計5,900万ドルを追加支払い、あるいは日本/中国が支払いを許可した場合、大部分の支払いは発売承認5周年から8周年の間に支払われる。日本/中国の承認支払いは、日本や中国でマーケティング承認を受けても一度だけ支払うことになる。SFJの実際の資金が1.2億ドル以下であれば、米国の支払い承認、EU承認支払い、日本/中国承認支払いは比例して調整される。FDAからbentracimabの上場承認を得ていなければ、米国の承認支払いの支払い義務はありません。もし私たちがヨーロッパ医薬品局やいくつかのヨーロッパ諸国の国家規制機関からbentracimabの上場承認を得ていなければ、私たちはEU承認支払いを支払う義務がありません。もし私たちが国家薬品監督管理局や国家薬品監督管理局からbentracimabの上場承認を得ていなければ、私たちは日本/中国承認支払いを支払う義務がありません。
SFJプロトコルをデリバティブと見なし,それぞれ代償および返済時の増加および減少に対応している.誘導ツールは、各報告期間において、それが公正な価値を推定するようにさらに調整される。デリバティブは,シーンに基づくキャッシュフロー手法を用いて推定し,この手法により,シーンごとにキャッシュフローの確率と時間を仮定し,このようなキャッシュフローをリスク調整割引率を用いて推定する.評価方法には、(I)融資の機会および時間、(Ii)規制機関の承認を得る機会および時間、(Iii)我々の貸借コスト(16.00%プラス無リスク借入金金利)および(Iv)SFJの借入コスト(2.50%に無リスク借入金金利)を含むいくつかの観察できない第3レベルの主要資料が含まれている。デリバティブは私たちの貸借対照表に負債として示されている。公正価値の任意の変動は、開発由来負債の損失または収益を再計量するために、経営報告書に記録される。
再許可収入
2021年6月、Alfasigmaは、再許可領土内でbentracimabを含む任意の製品を開発、使用、販売、販売、カプセル販売、および輸入するための資金を提供するAlfasigma再許可協定を締結した。
再許可スケジュールは、(1)再許可、(2)研究および開発活動、(3)いくつかの材料の製造および供給を含むことができる複数の構成要素を含むことができる。これらの手配に基づいて支払われるお金には、払戻不可能な前払い、重大な規制および開発活動完了後のマイルストーン支払い、またはいくつかの合意金額で製品、販売マイルストーン、および製品販売の特許使用料が含まれる場合があります。可変対価格の金額は、収入が将来的に大きな逆転リスクが存在しない可能性が高いまで制限される
再許可契約下の義務を履行する際に確認すべき適切な収入金額を決定する際には、(I)契約で約束された商品またはサービスを識別するステップと、(Ii)区別できるかどうかを含む約束された商品またはサービスが履行義務であるかどうかを決定するステップと、(Iii)可変対価格の制限を含む取引価格の測定と、(Iv)取引価格を履行義務に割り当てるステップと、(V)各履行義務を履行する際に収入を確認するステップとを実行する。
履行義務ごとの基本的な独立販売価格を決定するために判断すべき見積もりと仮定を作成しなければならず,取引価格が履行義務間でどのように分配されるかを決定しなければならない.独立販売価格の推定には,収入やコストの予測,開発スケジュール,割引率,規制や商業成功の可能性などの推定が含まれる可能性がある。また,契約義務が異なる履行義務を代表するかどうか,契約内の履行義務に取引価格を割り当てること,いつ履行義務を履行したかの決定,可変対価格の確認と将来の逆転の評価,および時間経過とともに履行される履行義務の進展を評価する適切な方法を決定·適用する際にも,重大な判断を適用する.
最近の会計公告
最近の会計声明に関する情報は、本年度報告その他の部分の財務諸表付記2を参照されたい。
“雇用法案”移行期
2012年4月、JumpStart Our Business Startups ActまたはJOBS法案が公布された。雇用法案第107条は、“新興成長型会社”は、新たな又は改正された会計基準を遵守するために、証券法第7(A)(2)(B)条に規定する移行期間の延長を利用することができる。したがって、新興成長型企業は、これらの基準が民間会社に適用されるまで、いくつかの会計基準の採用を延期することができる。この延長された移行期間を利用しないことを撤回できないことを選択したので、他の上場企業では新たな会計基準や改訂された会計基準を採用する必要がある関連日にこのような基準を採用する。
私たちは他の免除に依存して雇用法案に基づいて報告書の要求を減らす利点を評価している。特定の条件に適合する場合、新興成長型企業としては、(I)2002年のサバンズ-オキシリー法案第404(B)節またはサバンズ-オクスリー法案に基づいて、我々の財務報告内部統制制度に関する監査人証明報告書を提供すること、および(Ii)上場企業会計監督委員会が採用する可能性のある要件を遵守していないことを含むいくつかの免除に依存することができる。我々は、(1)財政年度の最終日(A)2023年12月31日までの財政年度の最終日、すなわち初公募株式(IPO)完了5周年後の財政年度終了まで、(B)我々の年間総収入が少なくとも10.7億ドル、または(C)米国証券取引委員会規則により、前年6月30日現在、非関連会社が保有する普通株の時価が7億ドルを超えることを意味する“大規模加速申告会社”とみなされる。そして(2)前3年の間に10億ドルを超える転換不能債券を発行した日。
我々は“小さな報告会社”(新興成長型企業の資格に適合しなくても、この資格に適合し続ける可能性がある)ため、2年間の監査財務諸表のみを含む、財務状況や運営開示結果の検討および分析を含む比較的大きな上場企業のより少ない公開開示を提供することが可能である。したがって、私たちが株主に提供する情報は、彼らが他の公開報告会社から得た情報とは異なり、彼らはこれらの会社の株式を持っているかもしれない。
第七A項。市場リスクに関する定量的で定性的な開示。
取引法第12 b-2条の定義によると、我々は小さな報告会社であり、本プロジェクトに要求される情報を提供する必要はない。
項目8.財務諸表と補足データ
第8項に要求された資料は、本年度報告表格10-K第4部第15項に記載されている財務諸表に記載されている。
第九項会計及び財務開示に関する変更と相違。
ない。
第9条。制御とプログラムです
制御とプログラムを開示する
我々は、取引法に基づいて提出または提出された報告書において開示を要求する情報が“米国証券取引委員会”規則および表で指定された期間内に記録、処理、集約および報告され、これらの情報が蓄積されて私たちの管理層に伝達されることを確実にするために、取引法の下の規則13 a~15(E)および15 d-15(E)で定義されている“開示制御および手順”を堅持し、開示に必要な決定をタイムリーに行うために、私たちの主要幹部および私たちの主要財務官を含む。
2021年12月31日までの年度について、我々の経営陣の監督·参加の下で、開示制御及びプログラムの設計·運用の有効性を評価した。この評価に基づき、我々のCEOおよび最高財務官は、我々の開示制御プログラムおよびプログラムが2021年12月31日に施行され、合理的な保証を提供するために、本年度報告で開示された情報が(A)米国証券取引委員会規則および法規が指定された期間内に報告され、(B)必要な開示について直ちに決定を下すために、我々の経営陣に伝達されたと結論した。
経営陣財務報告内部統制年次報告書
私たちの経営陣は財務報告書の十分な内部統制を確立して維持する責任がある。“取引法”第13 a-15(F)及び15 d-15(F)条によると、内部統制は、会社の主要行政官及び主要財務官又は類似の機能を履行する者が設計又は監督し、公認された会計原則に基づいて財務報告の信頼性及び外部目的の財務諸表の作成に合理的な保証を提供するために、公認された会計原則に基づいて財務報告書の信頼性及び外部目的のための財務報告書の合理的な保証を提供するために、会社の取締役会、管理層及びその他の人員によって実施されるプログラムである
•会社の資産を合理的、詳細、正確かつ公平に反映した取引および処置の記録の保存に関連している
•一般的に受け入れられている会計原則に従って財務諸表を作成し、会社の収支が会社の管理層および取締役の許可のみで行われることを確保するために、必要に応じて取引を記録することを確保する合理的な保証を提供する
•財務諸表に重大な影響を及ぼす可能性のある不正な取得、使用、または会社の資産の処理を防止またはタイムリーに発見する合理的な保証を提供する。
私たちの経営陣は、2021年12月31日までの財務報告書の内部統制に対する我々の有効性を評価した。この評価を行う際には、管理職は#年トレデビル委員会後援組織委員会が提出した基準を使用した内部制御--統合フレームワーク(2013年フレームワーク)(COSO)。その評価によると、経営陣は、2021年12月31日現在、財務報告書の内部統制を合理的な保証水準で有効であると考えている。
本年度報告書には、雇用法第103条の改正された“サバンズ·オキシリー法案”第404条(B)条で許可された独立公認会計士事務所の認証報告は含まれていない。
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。したがって,有効と判定されたシステムであっても,財務諸表の作成や列報に合理的な保証を提供することしかできない.将来的にどのような有効性評価を行うかの予測には,条件の変化により制御が不十分になる可能性がある,あるいは政策やプログラムを遵守する程度が悪化する可能性があるというリスクがある.
財務報告の内部統制の変化
2021年12月31日までの財政年度中に、財務報告の内部統制(取引法第13 a-15(F)および15 d-15(F)条の定義による)に大きな影響を与えなかったか、または合理的に財務報告の内部統制に大きな影響を与える可能性のある変化はなかった。
プロジェクト9 B。他の情報。
PhaseBio製薬会社解散費福祉計画
2022年3月23日、我々の取締役会の報酬委員会は、以下の人員に解散費福祉を提供するPhaseBio PharmPharmticals,Inc.解散福祉計画またはSeverance計画の修正案を承認した
条件を満たす従業員は,我々が指定した役員を含めて,(I)“制御権変更終了”または(Ii)“定期終了”(定義は後述)の場合である.退職計画条項に基づいて提供される解散費福祉は、2021年4月29日に米国証券取引委員会に提出された付表14 Aに関する最終委託書の“役員報酬”の節に記載されているものとほぼ変わらないが、以下のようになる
•制御権変更が終了した場合、私たちのCEOは、年間ボーナス目標金額の1.5倍の支払いを受ける権利があります
•上級副総裁職級の従業員は、行政総裁を除いて、退職計画に基づいて行政主任と同じ福祉を受ける資格がある
•当社の行政総裁は、副社長以下の従業員に退職計画の福祉を受ける資格があることを許可されています。支配権変更が終了した場合、当該等の指定従業員は、6ヶ月の年度基本給に相当する一括払い、当該従業員の年間ボーナス目標金額の0.5倍の支払い、すべての未償還持分奨励金の帰属を加速し、6ヶ月のコブラ保険料の支払い、及び当該従業員の未償還持分奨励に適用される退職後の行使期間を最大1年間延長する権利がある。このような指定従業員は通常解雇時に離職計画下の福祉を得る権利がない
“離職計画”については、以下の定義が適用される
•“制御権変更終了”とは、制御権変更の1ヶ月後または12ヶ月後に発生する“非自発的終了”(2018年の株式インセンティブ計画の定義に基づく)を意味する
•“正常終了”とは、制御権変更の1ヶ月前または後12ヶ月以内に発生しない“非自発的終了”を意味する
•非自発的終了“とは、(I)会社が理由なく終了すること(2018年の株式インセンティブ計画が定義されているように)、あるいは(Ii)従業員が”十分な理由“(退職計画で定義されているような)によって退職することを意味する。
前述の“分割払い計画”の要約は完全であると主張しておらず、“分割払い計画”の全文を参照することによって保持されており、そのコピーは、本年度報告の添付ファイル10.9として10-Kテーブルの形態でアーカイブされている。
プロジェクト9 Cです。検査を妨害する外国司法管轄区域を開示する。
ない。
第三部
我々は,第14 A条の規定により,本年度終了後120日に遅れず,2022年年次総会の最終委託書又は依頼書を米国証券取引委員会に提出する予定である。したがって,一般指示G(3)では,表10-Kは第3部分に要求されるいくつかの資料を省略している.本明細書に記載された項目に具体的に関連する2022年依頼書の部分のみが参照によって本明細書に組み込まれる。
プロジェクト10.取締役、行政、企業管理
本第10条に要求される情報は、“取締役会及び会社のガバナンスに関する情報”、“取締役選挙”、“執行者”、“延滞第16条(A)の報告”というタイトルの当社委託書に含まれ、引用により本明細書に組み込まれる。
第11項.行政職報酬
第11条に要求される情報は、それぞれ“役員報酬”および“役員報酬”と題する当社の委託書に含まれ、参考として本明細書に組み込まれる。
第12項:特定の実益所有者の保証所有権及び管理職及び関連株主事項。
本第12項に要求される資料は、吾等の委託書“いくつかの実益所有者及び経営層の担保所有権”及び“持分補償計画に従って発行された証券”のタイトルの下に含まれ、ここに組み込まれて参考となる。
第十三条特定関係及び関連取引、並びに取締役の独立性。
本第13項に要求される資料は、当社の委託書“関係者との取引及び賠償”及び“取締役会の独立性”のタイトルの下に含まれ、参考にして当社の委託書に組み込まれる。
プロジェクト14.チーフ会計士費用とサービス
本第14項に要求される資料は、“独立公認会計士事務所の選抜承認”と題する委託書に含まれ、ここに組み込まれて参考となる。
第4部
プロジェクト15.証拠品および財務諸表の添付表
(A)(1)財務諸表
PhaseBio製薬会社は
財務諸表索引
カタログ
| | | | | |
| ページ |
独立公認会計士事務所報告(PCAOB ID:185) | F-2 |
2021年12月31日現在と2020年12月31日現在の貸借対照表 | F-3 |
2021年12月31日までと2020年12月31日までの年度の業務報告書 | F-4 |
2021年12月31日までと2020年12月31日まで年度株主損失表 | F-5 |
2021年12月31日と2020年12月31日までの年間現金フロー表 | F-6 |
財務諸表付記 | F-7 |
独立公認会計士事務所報告
株主や取締役会に
PhaseBio製薬会社:
財務諸表のいくつかの見方
PhaseBio製薬会社(当社)の2021年12月31日現在と2020年12月31日現在の貸借対照表、同年度までの関連経営報告書、株主赤字と現金流量および関連付記(総称して財務諸表と呼ぶ)を監査した。財務諸表は,すべての重要な面で,会社の2021年12月31日と2020年12月31日までの財務状況と,それまでの年度までの経営成果とキャッシュフローを公平に反映しており,米国公認会計原則に適合していると考えられる。
経営を続ける企業
添付財務諸表の作成は、同社が引き続き経営を継続する企業であると仮定している。財務諸表付記1で述べたように、同社は運営中に純損失とマイナスキャッシュフローを示しており、2021年12月31日現在の累計損失は3兆918億ドルであり、持続経営企業としての持続的な経営能力が大きく疑われている。付記1は、これらの事項における経営陣の計画も説明しています。財務諸表には、このような不確実性の結果に起因する可能性のある調整は含まれていません。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいてこのような財務諸表に意見を述べることだ。私たちは米国上場企業会計監督委員会(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、会社と独立しなければならない。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。当社はその財務報告の内部統制を監査することを求められておらず、私たちも招聘されて監査を行っていません。私たちの監査の一部として、財務報告の内部統制を理解することが求められていますが、社内財務報告の内部統制の有効性について意見を述べるためではありません。したがって、私たちはそのような意見を表現しない。
我々の監査には、財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであれ詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれています。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、財務諸表の全体列報を評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
/s/ ピマウェイ会計士事務所
2010年以来、当社の監査役を務めてきました
フィラデルフィアペンシルバニア州
March 24, 2022
PHASEBIO製薬会社
貸借対照表
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2021 | | 2020 |
資産 | | | |
流動資産: | | | |
現金と現金等価物 | $ | 41,800 | | | $ | 28,122 | |
前払い費用と他の資産 | 6,984 | | | 12,027 | |
流動資産総額 | 48,784 | | | 40,149 | |
財産と設備、純額 | 10,230 | | | 8,224 | |
経営的リース使用権資産 | 1,469 | | | 1,927 | |
その他の資産 | 57 | | | 57 | |
総資産 | $ | 60,540 | | | $ | 50,357 | |
| 負債と株主赤字 | | | |
流動負債: | | | |
長期債務の当期部分 | $ | 5,413 | | | $ | 5,355 | |
| 延子許可収入の当面の部分 | 1,547 | | | — | |
売掛金 | 12,570 | | | 3,674 | |
費用とその他の流動負債を計算しなければならない | 8,353 | | | 5,931 | |
流動負債総額 | 27,883 | | | 14,960 | |
長期債務、純額 | 1,359 | | | 6,773 | |
経営賃貸負債純額 | 1,073 | | | 1,548 | |
| 再許可収入の長期分を繰延する | 7,622 | | | — | |
| 発展誘導負債 | 114,843 | | | 51,719 | |
その他長期負債 | 794 | | | 559 | |
総負債 | 153,574 | | | 75,559 | |
負担額およびまたは事項(Notes 9, 10, 13) |
| |
|
| 株主赤字: | | | |
優先株、$0.001額面価値10,000,000ライセンス株;ゼロ2021年12月31日及び2020年12月31日に発行·発行される株式 | — | | | — | |
普通株、$0.001額面価値200,000,000ライセンス株;48,220,557発行済みおよび発行済み株式48,190,5902021年12月31日発行の株式;29,471,854発行済みおよび発行済み株式29,441,8872020年12月31日に発行された株式 | 48 | | | 29 | |
国庫株は、原価で計算する29,9672021年12月31日現在と2020年12月31日現在の株 | (24) | | | (24) | |
追加実収資本 | 298,736 | | | 235,516 | |
赤字を累計する | (391,794) | | | (260,723) | |
| 株主総損失額 | (93,034) | | | (25,202) | |
| 総負債と株主赤字 | $ | 60,540 | | | $ | 50,357 | |
財務諸表の付記を参照。
PHASEBIO製薬会社
運営説明書
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2021 | | 2020 |
収入: | | | |
| 再許可収入 | $ | 10,831 | | | $ | — | |
奨学金収入 | — | | | 320 | |
総収入 | 10,831 | | | 320 | |
運営費用: | | | |
研究開発 | 102,107 | | | 72,088 | |
一般と行政 | 16,086 | | | 13,088 | |
総運営費 | 118,193 | | | 85,176 | |
運営損失 | (107,362) | | | (84,856) | |
| その他(費用)収入: | | | |
| 再計量開発デリバティブ負債の損失 | (21,182) | | | (12,507) | |
利子収入 | 14 | | | 237 | |
利子支出 | (947) | | | (1,445) | |
| 外国為替収益 | 6 | | | 6 | |
| その他費用合計 | (22,109) | | | (13,709) | |
| 所得税前純損失 | (129,471) | | | (98,565) | |
| 所得税支給 | 1,600 | | | — | |
純損失 | $ | (131,071) | | | $ | (98,565) | |
普通株1株当たりの基本損失と償却後の純損失 | $ | (2.98) | | | $ | (3.39) | |
| 加重平均発行済み普通株式、基本普通株式、希釈後普通株 | 43,918,996 | | | 29,056,304 | |
財務諸表の付記を参照。
PHASEBIO製薬会社
株主損失表
(単位は千で、シェアは含まれていない)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 普通株 | | 在庫株 | | その他の内容 支払い済み | | 積算 | | 合計する
株主の
(赤字) |
| | 株 | | 金額 | | 株 | | 金額 | | 資本 | | 赤字.赤字 | | 権益 |
| 2019年12月31日の残高 | | 28,796,371 | | | $ | 29 | | | (29,967) | | | $ | (24) | | | $ | 222,131 | | | $ | (162,158) | | | $ | 59,978 | |
普通株式承認証を発行する | | — | | | — | | | — | | | — | | | 7,925 | | | — | | | 7,925 | |
| 普通株を公開発行し,純額 | | 561,848 | | | — | | | — | | | — | | | 2,942 | | | — | | | 2,942 | |
| 従業員による株式購入計画で普通株を発行する | | 62,063 | | | — | | | — | | | — | | | 186 | | | — | | | 186 | |
株式オプションの行権 | | 51,572 | | | — | | | — | | | — | | | 95 | | | — | | | 95 | |
株に基づく報酬 | | — | | | — | | | — | | | — | | | 2,237 | | | — | | | 2,237 | |
純損失 | | — | | | — | | | — | | | — | | | — | | | (98,565) | | | (98,565) | |
| 2020年12月31日残高 | | 29,471,854 | | | 29 | | | (29,967) | | | (24) | | | 235,516 | | | (260,723) | | | (25,202) | |
普通株を公開発行し,純額 | | 18,400,000 | | | 19 | | | — | | | — | | | 60,222 | | | — | | | 60,241 | |
| 従業員による株式購入計画で普通株を発行する | | 138,952 | | | — | | | — | | | — | | | 336 | | | — | | | 336 | |
株式オプションの行権 | | 209,751 | | | — | | | — | | | — | | | 394 | | | — | | | 394 | |
株に基づく報酬 | | — | | | — | | | — | | | — | | | 2,268 | | | — | | | 2,268 | |
純損失 | | — | | | — | | | — | | | — | | | — | | | (131,071) | | | (131,071) | |
| 2021年12月31日の残高 | | 48,220,557 | | | $ | 48 | | | (29,967) | | | $ | (24) | | | $ | 298,736 | | | $ | (391,794) | | | $ | (93,034) | |
財務諸表の付記を参照。
PHASEBIO製薬会社
現金フロー表
(単位:千)
| | | | | | | | | | | |
| 12月31日までの年度 |
| 2021 | | 2020 |
経営活動 | | | |
純損失 | $ | (131,071) | | | $ | (98,565) | |
純損失と経営活動で使用される現金純額の調整: | | | |
減価償却および償却 | 1,793 | | | 508 | |
株に基づく報酬 | 2,268 | | | 2,237 | |
| 再計量開発デリバティブ負債の損失 | 21,182 | | | 12,507 | |
非現金利子支出 | 304 | | | 491 | |
| 非現金研究開発費 | 28,740 | | | 27,027 | |
| 他の非現金取引 | — | | | 100 | |
経営性資産と負債変動状況: | | | |
その他売掛金 | — | | | 1,233 | |
前払い費用と他の資産 | 7,505 | | | (8,375) | |
売掛金 | 9,010 | | | 974 | |
| 費用とその他の流動負債を計算しなければならない | 3,684 | | | 1,906 | |
| 延子許可収入を渡す | 9,169 | | | — | |
経営活動のための現金純額 | (47,416) | | | (59,957) | |
投資活動 | | | |
財産と設備を購入する | (2,679) | | | (1,312) | |
| 知的財産権の取得 | — | | | (100) | |
投資活動のための現金純額 | (2,679) | | | (1,412) | |
融資活動 | | | |
| 派生負債の収益を開発する | 8,184 | | | 15,169 | |
| 普通株で得た金を公開発行し,純額 | 60,354 | | | 2,942 | |
繰延株式発行コストを支払う | (40) | | | (199) | |
株式オプションを行使して得られる収益 | 394 | | | 95 | |
| 従業員による株購入計画で購入した株 | 336 | | | 186 | |
長期債務を償還する | (5,455) | | | (2,727) | |
融資活動が提供する現金純額 | 63,773 | | | 15,466 | |
| 現金および現金等価物の純増加(減額) | 13,678 | | | (45,903) | |
| 年明けの現金と現金等価物 | 28,122 | | | 74,025 | |
| 年末現金と現金等価物 | $ | 41,800 | | | $ | 28,122 | |
キャッシュフロー補充開示 | | | |
利子を支払う現金 | $ | 517 | | | $ | 954 | |
キャッシュフロー情報を補足開示する | | | |
| 新しい経営リース負債と引き換えに使用権資産 | $ | — | | | $ | 576 | |
| 開発派生法的責任と組み合わせた権証発行 | $ | — | | | $ | 7,925 | |
| 開発デリバティブ負債と一緒に購入した財産と装置 | $ | 2,482 | | | $ | 4,941 | |
売掛金と売掛金に掲げる財産と設備の購入 | $ | 16 | | | $ | 1,378 | |
財務諸表の付記を参照。
1. 業務の組織と記述
業務説明
PhaseBio製薬会社(以下“会社”と略す)は2002年1月10日にデラウェア州に登録設立された。その会社は臨床段階の生物製薬会社は、心血管疾患の新療法の開発と商業化に集中している。同社の主要な候補製品であるbentracimab(PB 2452とも呼ばれる)は抗血小板薬チカグレルのための新しい逆転薬である。同社は難治性高血圧の治療のための臨床前候補製品PB 6440を開発している.
経営を続ける企業
同社は純損失と運営キャッシュフローが負の状況を経験しており、2021年12月31日までの累計赤字は#ドルとなっている391.8百万ドルです。同社は少なくとも今後数年以内に純損失が続くと予想している。2021年12月31日現在、会社は現金と現金等価物$を持っています41.8百万ドルと運営資本20.9百万ドルです。2020年1月,当社はSFJ製薬グループ会社(“SFJ”)傘下のSFJ PharmPharmticals X,Ltd.と共同開発プロトコル(“SFJプロトコル”)を締結し,このプロトコルにより,SFJはbentracimabの臨床開発に資金と運営支援を提供した。経営陣は、2021年12月31日現在の既存の現金と現金等価物は、ドルを除いて28.7百万当社はSFJがSFJプロトコルによる臨床試験コスト及びその他の支出を援助或いは返済することを予想しており、このような財務諸表の刊行日から12ヶ月の運営支出及び資本需要を支払うのに十分ではない。これらの要因は、同社の継続経営企業としての持続的な経営能力を大きく疑わせている。財務諸表にはこのような不確実性の結果がもたらす可能性のあるいかなる調整も含まれていない。SFJプロトコルによれば,当社がプロトコルが指定した期間内にそのような持続的な経営条件を救済できなかった場合,SFJは当社のbentracimabに関する業務をSFJに移行することを選択することができる
同社は、株式または債務融資または他の第三者融資、マーケティングおよび流通手配、および他の協力、戦略連盟、許可手配によって、その流動性需要を満たすために追加資金を求める計画だ。しかし、このような資金努力が必ず成功するという保証はない。これに対し、当社は現在、米国証券取引委員会(以下、米国証券取引委員会と略称する)に有効なS-3表“2019年棚上げ登録表”(略称“2019年棚上げ登録表”)を届出し、この登録表は2023年1月に満了する。2019年棚登録声明現在(I)当社の発売、発行、販売を許可しております最高総発行価格は$200.0普通株、優先株、債務証券および株式承認証の1回または複数回の発売および任意の組み合わせにおける百万株;および(Ii)当社が発売、発行および販売する最高合計発売価格は最高$に達する60.0“市場”販売協定(“ATM計画”)に基づいて発行·販売された百万株普通株これは1ドルです60.0ATM計画によると発行と販売可能な百万普通株はドルに含まれています200.02019年の“棚登録声明”によると発行·販売可能な証券は百万部に達する2021年12月31日現在、同社は132.62019年の棚登録声明によると販売可能な残りの普通株式は、その中で57.0ATM計画では、100万台が販売される可能性があります
年末後、2022年1月10日に、当社は発送します500,000ATMで計画された普通株による純収益は$1.2百万ドルです。
同社は新冠肺炎の流行がその業務と運営に与える影響を評価し続けている。新冠肺炎の会社の業務と運営に対する影響の程度は、疾病及びその変種の経時的地理分布、疾病に対するワクチンと抗ウイルス薬物の有効性、獲得性と投与速度、疫病の持続時間、業務中断の持続時間と影響、及びアメリカと他の国が疾病の制御と治療のために実施した旅行制限、隔離、社会距離要求と企業閉鎖の短期効果と最終効果など、高度な不確定かつ把握できない未来の発展に依存する。新冠肺炎疫病による潜在的な経済影響及びその持続時間は評価或いは予測が困難かもしれないが、持続かつ日々深刻な疫病は全世界の金融市場の深刻な混乱を招く可能性があり、会社の資本獲得能力を低下させ、これは未来にその流動性に負の影響を与える可能性がある。また、新冠肺炎の伝播による景気後退や市場調整は会社の業務とその普通株価値に重大な影響を与える可能性がある。
陳述の基礎
添付財務諸表は米国公認会計原則(“公認会計原則”)及び米国証券取引委員会の規則制度に基づいて作成されたものである。本付記における適用マニュアルへのいかなる引用も
財務会計基準委員会(“FASB”)が公布した“会計基準編纂”(“ASC”)及び“会計基準更新”(“ASU”)に掲載されている公認会計原則を指す。
業績評価と経営決定を行うために、会社はその運営を単一の報告可能部門として管理している。
2. 重大会計政策
予算の使用
会社の財務諸表の作成は、会社の財務諸表および付記に報告された資産、負債、収入および費用、ならびに資産および負債の開示に影響を与えるために、管理層に推定および仮定を要求する。会社の財務諸表の中で最も重要な推定は,開発由来負債の推定値,臨床試験計上費用,およびAlfasigma S.p.A(“Alfasigma”)と締結された独占再許可協定(“Alfasigma再許可”)での収入の延期と確認に関するものである。これらの推定は,現在の事件や将来とりうる行動に対する会社の理解に基づいているが,実際の結果はこれらの推定や仮定とは大きく異なる可能性がある.
信用リスクの集中度
会社を深刻な集中信用リスクに直面させる可能性のある金融商品には、主に現金と現金等価物が含まれる。当社の連邦保険金融機関におけるいくつかの預金は連邦保険限度額を超えています。同社の将来の通貨市場基金は赤字になるかもしれない。
現金と現金等価物
当社はすべての原始期限が三ヶ月以下の高流動性投資を現金等価物と見なしています。現金および現金等価物は、いつでも利用可能な小切手および通貨市場口座内の現金を含む。
金融商品の公正価値
前払い支出及びその他の資産、売掛金及び売掛金及びその他の流動負債の帳簿価額はその公正価値の合理的な推定であり、このような項目の期限が短いためである。当社の現行の類似条項ローンの借入金利によると、当社は定期ローン及び経営リース負債及びそれに応じた使用権資産の公正価値がそれぞれの帳簿価値に近いと信じている。
延子許可収入を渡す
当社が契約条項に基づいて顧客への履行義務を履行する前に、顧客の対価格または無条件満期対価を受けた場合、契約負債を繰延収入と記す。貸借対照表後12ヶ月以内に収入と確認された繰延収入は流動負債に分類されることが予想される。貸借対照表後12ヶ月以内に収入として確認されていない繰延収入は長期負債に分類される。
発展誘導負債
開発派生負債は、受信された推定コストの現在値およびSFJプロトコルの契約条項に従って支払われた推定コストの現在値に従って入金され、これらの推定コストは、公正価値として決定されている。この負債は四半期ごとに3級デリバティブとして再計量され、公正価値のいかなる変動も経営報告書上で開発由来負債の収益(損失)を再計量する形で記録されている。
財産と設備
財産及び設備はコストに応じて入金され、資産の推定使用年数内に減価償却される(三つ至れり尽くせり5年)直線法を使用します。レンタル改善は、使用年数またはレンタル期間の短い時間で償却すると推定される。
賃貸借証書
レンタル開始時には、当社が行使する任意の延長賃貸契約の選択権を合理的に決定することを含む、予想レンタル期間内の賃貸支払い現在値に基づいてリース負債を記録する。当社の借款は暗黙的な金利を提供していないため、当社は逓増借款金利を用いて賃貸支払いの現在値を計算しています。当社の賃貸の逓増借入金利とは、担保に類似条項の下の賃貸支払いに等しい金額を借り入れるのに必要な金利のことです。レンタル開始日には、当社は、レンタル負債に応じてレンタル資産の使用権を記録し、レンタル開始日前に受信した任意のレンタル報酬及びレンタル者に支払う任意の初期直接コストに応じて調整する。当社は初期年間が12ヶ月以下の賃貸契約(“短期借約”)を締結することができる。いずれの短期賃貸についても、当社は直線法でレンタル料を記録し、貸借対照表にレンタルを記録しない。同社は2021年12月31日と2020年12月31日まで短期賃貸契約を持っていない。
リース開始後、当社は、(I)リース開始時に決定された割引率に基づいて算出された余剰賃貸支払現在値に基づく賃貸負債、(Ii)受信した任意の未償却賃貸インセンティブ、任意の未償却初期直接コスト及び賃貸支出と賃貸契約支払い金額との累積差額に基づいて調整された賃貸負債の使用権のリース資産を再計量する。受け取った任意のレンタル報酬および任意の初期直接コストは、直線法で予想されるレンタル期間内に償却されます。レンタル料支出は予想レンタル期間内に直線的に記録される。
長寿資産
当社は、そのすべての長期資産(物件及び設備及び使用権資産を含む)の帳簿価値及び推定耐用年数を定期的に検討し、帳簿価値又は推定耐用年数を調整する必要がある減値指標が存在するか否かを決定する。この評価に使用される決定要因には、資産が将来的に純正キャッシュフローを生成する能力の管理層の推定と、会社の業務目標に対する資産の戦略的意義がある。減値があれば,減値損失は,許容価値がその帳簿価値よりも小さいと推定される程度に応じて計測される.当社は2021年12月31日および2020年12月31日までに減価損失は確認されていません。
臨床前·臨床試験対策プロジェクト
当社は,臨床研究機関,契約製造機関,臨床試験地点との合意に基づき,個人試験期間中に完了した作業割合と被験者登録率から,第三者による臨床前研究や臨床試験活動に関する計上と発生費用金額を推定している。同社は、契約、サプライヤー契約、および調達注文を審査し、試験またはサービスの進展または完了段階およびそのようなサービスのために支払われる合意費用を内部臨床者および外部サービスプロバイダと議論することによって推定数を決定する。しかし,臨床試験の実際のコストや時間は高度に不確実であり,リスクの影響を受け,会社の臨床開発計画を含む多くの要因によって変化する可能性がある。
経営陣は、会社が当時知っていた事実及び状況に基づいて、会社財務諸表において、会社毎の貸借対照表日までの計上費用を推定する。実際にサービスを実行する時間や努力の程度が見積もりと異なる場合、当社は該当項目を調整します。将来の研究および開発活動で使用されるプロセス開発または製造および臨床用品の分配費用を含み、関連商品またはサービスが消費またはサービス提供されている間に費用として確認されることを含む、払戻不可能な商品およびサービスの前払い。
収入.収入 識別する
再許可収入
再許可スケジュールは、(1)再許可、(2)研究および開発活動、(3)いくつかの材料の製造および供給を含むことができる複数の構成要素を含むことができる。これらの手配に基づいて支払われるお金には、払戻不可能な支払い、前払い、重大な規制、および開発活動完了後のマイルストーン支払い、またはいくつかの合意された金額で製品、販売マイルストーン、および製品販売の特許権使用料が含まれる場合があります。それは..
可変対価金額は収入が将来的に大きな逆転リスクが存在しない可能性が高いまで制限されている
会社が再許可協定で規定された義務を履行する際に確認すべき適切な収入額を決定する場合、会社は、(1)契約で約束された貨物またはサービスを決定するステップと、(2)区別できるかどうかを含む約束された貨物またはサービスが履行義務であるかどうかを決定するステップと、(3)可変対価格の制限を含む取引価格を測定するステップと、(4)取引価格を履行義務に割り当てるステップと、(5)会社が各履行義務を履行する際に収入を確認するステップとを実行する。
会社は,履行義務ごとの基本的な独立販売価格を決定するために判断すべき見積もりと仮定を作成しなければならず,取引価格が契約義務間でどのように分配されるかを決定しなければならない。独立販売価格の推定には,収入やコストの予測,開発スケジュール,割引率,規制や商業成功の可能性などの推定が含まれる可能性がある。契約義務が異なる履行義務を代表するかどうか、契約内の履行義務に取引価格を割り当てること、いつ履行義務を履行したかを決定すること、可変対価格の確認と将来の逆転を評価すること、および経時的に履行される履行義務の進展を評価する適切な方法を決定·適用する際には、会社は重大な判断も適用する。
贈与収入
助成金収入は、特定の研究プロジェクトにおける企業の努力を支援するために政府から支出された。当社は、当社に贈与を提供する政府機関が顧客ではないことを決定しました。適切な保証が支出条件を満たし、支出収入を受け取ることが合理的に保証されている場合、当社は支出収入を確認します。
研究開発費
研究·開発コストは発生時に費用を計上する。この技術が将来代替用途がない場合、技術ライセンスを取得することによるコストは、研究および開発費用に計上される。
株に基づく報酬
それは..会社付与された日の推定公正価値に基づいて株式の報酬に基づくすべての報酬支出を計量し、確認する。現在、会社の株式奨励は株式オプションのみを含む;しかし、会社の株式補償計画下の将来の奨励には、制限株式、制限株式単位、株式付加価値権、業績奨励、業績単位の株式も含まれる可能性がある。当社も2018年度従業員株購入計画(“ESPP”)を維持しており、この計画により、当社は普通株を発行することができます。同社はブラック·スコアーズオプション定価モデルを使用してESPPが発行した株式オプションと株式の公正価値を推定しており、これには見積もりを用いる必要がある。当社は株式オプションを比例的に付与する株式ベースの補償コストと、奨励に必要なサービス期間内にESPPにより直線的に発行された株を確認し、没収が発生した間に記録を没収します。
黒--スコイルズオプション定価モデルは、無リスク金利、会社普通株の予想配当収益率、会社普通株価格の予想変動率、およびオプションの期待期限を含む主観的仮定を入力する必要がある。このような推定は固有の不確実性と経営陣判断の適用に関するものだ。要因が変化し、異なる仮定を用いれば、会社の株式ベースの報酬支出は将来的に大きく異なる可能性がある。
所得税
当社は、財務諸表に含まれている事件の予想される将来の税務結果の繰延税金資産と負債を確認することを要求する貸借対照法に従って所得税を計算する。この方法によると、繰延税項資産及び負債は、財務諸表と資産及び負債の税ベースとの差額に基づいて、予想差額を用いて返送される年度の現行税率を決定する。税率変動が繰延税金資産や負債に及ぼす影響は、公布日を含む期間の収入で確認されている。
会社が繰延税項目純資産の範囲を確認したのは、会社はこれらの資産がより現金化する可能性があると考えていることだ。このような決定を下す際に、管理層は、既存の課税の一時的な差異の将来の輸出、将来の課税所得額の予想、税務計画など、利用可能なすべてのプラスと負の証拠を考慮する
戦略、そして最近の行動の結果。経営陣が当社が将来その記録純額を超える繰延税金資産を実現できると判断した場合、管理層は繰延税金資産の推定値を調整し、所得税の支出を減らすことになる。
当社は、(1)経営陣が税務倉庫位の技術的優位性に基づいて当該等の税務倉位を維持する可能性が高いか否かを決定する不確定な税務倉位、及び(2)より確認のハードルに達する可能性のある税務倉位について、管理層が最終的に関連税務機関と和解した後に実現可能な最大税務優遇額の50%を超えることを確認する。当社は所得税支出において未確認の税収割引に関する利息及び罰金(ある場合)を確認し、いずれの課税利息及び罰金も関連する納税義務の範囲に含まれている。
1株当たり純損失
1株当たり基本純損失の計算方法は,純損失を当期発行普通株の加重平均で割ったものである。1株当たり純損失の計算方法は,純損失を当期発行済み普通株と普通株等価物の加重平均で割る。普通株式等価物は、その影響が希釈である場合にのみ含まれる。当社の潜在的希薄化証券は、当社の株式オプション計画下の未償還株式オプション、時々発行される引受権証、ESPPにより発行可能な普通株を含み、赤字となるため、1株当たりの純損失の計算から除外されている。列報の全期間において、会社の純損失状況により、基本流通株と希釈流通株を計算するための株式数に差はなかった。
次の表は、希釈後の1株当たり純損失を計算する際に除外された発行された希釈可能な証券を示しています。これらの証券を組み込むことは逆希釈になるからです
| | | | | | | | | | | |
| 12月31日まで |
| 2021 | | 2020 |
| 普通株式オプション | 4,466,801 | | | 3,598,160 | |
| 普通株購入引受権証 | 2,323,711 | | | 2,323,711 | |
| 従業員株購入計画 | 347,566 | | | 634,654 | |
| 合計する | 7,138,078 | | | 6,556,525 | |
最近の会計公告
2019年12月、FASBはASU 2019-12を発表した所得税(話題740):所得税会計の簡略化それは、他の事項に加えて、現行規則における中期税収分配方法及び中期所得税算出方法に関するいくつかの例外を解消し、営業権計税基礎の上昇を招く取引の会計処理を明らかにした。この基準は2021年第1四半期に会社に施行された。この新基準の採用は会社の財務諸表や関連開示に実質的な影響を与えていない。
3. 公正価値計量
公正価値は、計量日の市場参加者間の秩序ある取引において資産を売却して受信された金額または移転負債によって支払われた金額を表す脱退価格として定義される。したがって、公正価値は市場に基づく計量であり、資産または負債の定価のために市場参加者が使用する仮定に基づいて決定されるべきである。
開示のために、同社は公正価値計量を以下の3つに分類した
レベル1:活発な市場での同じ資産または負債の見積もり。
第2レベル:市場で直接または間接的に観察可能な類似資産や負債の第1レベル価格以外の投入.
レベル3:市場活動支援が少ないか、または全くない観察不可能な投入、ならびに価格設定モデル、現金流量方法または同様の技術を使用して決定された価値、およびその公正な価値の決定に重大な判断または推定を必要とするツール。
会社の現金等価物は、見積された市場価格、仲介人または取引業者のオファー、または合理的な価格透明性を有する代替価格源を使用して推定されるので、公正価値レベルの第1レベルの投入を使用して分類される。当社のいかなる非金融資産または負債も公正価値に基づいて非日常的に記録されていません。本報告で述べた間、レベル間の遷移は発生しなかった。
当社のSFJに対する財務約束は、SFJプロトコルの公正価値とともに第3レベル投入に基づく開発デリバティブ負債として報告されている。
以下の表は、企業が経常的公正価値に応じて計量する必要がある資産と負債と、公正価値レベルに基づくそれぞれの投入レベル(千単位)をまとめたものである
| | | | | | | | | | | | | | | | | | | | | | | |
| | | 報告日の公正価値計測 |
| 合計する | | レベル1 | | レベル2 | | レベル3 |
| 2021年12月31日まで: | | | | | | | |
資産 | | | | | | | |
現金等価物 | $ | 41,550 | | | $ | 41,550 | | | $ | — | | | $ | — | |
| 負債.負債 | | | | | | | |
| 発展誘導負債(付記8) | $ | 114,843 | | | $ | — | | | $ | — | | | $ | 114,843 | |
| 2020年12月31日まで: | | | | | | | |
資産 | | | | | | | |
現金等価物 | $ | 27,872 | | | $ | 27,872 | | | $ | — | | | $ | — | |
| 負債.負債 | | | | | | | |
| 発展誘導負債(付記8) | $ | 51,719 | | | $ | — | | | $ | — | | | $ | 51,719 | |
4. 財産と設備
次の表に財産と設備の構成、純額(千で計算)
| | | | | | | | | | | |
| 12月31日まで |
| 2021 | | 2020 |
実験室装置 | $ | 12,995 | | | $ | 8,994 | |
コンピュータのハードウェア、ソフトウェア、電話 | 148 | | | 140 | |
家具と固定装置 | 221 | | | 107 | |
賃借権改善 | 105 | | | 67 | |
建設中の工事 | 681 | | | 1,042 | |
| 14,150 | | | 10,350 | |
減価償却累計を差し引く | (3,920) | | | (2,126) | |
財産と設備、純額 | $ | 10,230 | | | $ | 8,224 | |
減価償却費用は$1.8百万ドルとドル0.52021年12月31日までと2020年12月31日までの年度はそれぞれ100万ドル。
5. 費用とその他の流動負債を計算しなければならない
以下の表に課税費用とその他の流動負債の構成(千計)を示す
| | | | | | | | | | | |
| 12月31日まで |
| 2021 | | 2020 |
臨床と関連費用を計算しなければならない | $ | 3,985 | | | $ | 2,753 | |
補償と関連費用を計算しなければならない | 2,850 | | | 2,260 | |
応算利息 | 38 | | | 69 | |
| その他の措置を講じる | 1,005 | | | 459 | |
短期経営賃貸負債 | 475 | | | 390 | |
費用とその他の流動負債を計算しなければならない | $ | 8,353 | | | $ | 5,931 | |
6. 債務
2019年3月、当社はシリコンバレー銀行(“SVB”)およびWestRiver革新融資基金VIII,L.P.(“WestRiver”)と融資(“2019年融資”)を締結し、これにより、当社は最大$を借り入れることができる15.0百万ドルで3ロットに分けて発行することができる7.52019年ローン実行時に発行された100万ドル(“第1枠”),#2.52019年5月発行(“第2弾”)と#ドル5.0当社は二零一九年十月に百万元を発行し、当社はいくつかの監督管理マイルストーン(“第三弾”)の成果を参考にしなければならない。
2019年ローン満期日は2023年3月1日です。2019年のローン条項によると、当社は2020年6月30日までに第1陣、第2陣、第3弾について利息のみを支払い、金利は最優遇金利プラス大きい者に等しい1.00%は、2019年のローンで定義されているように、または6.5%以降の販売期限は33毎月の等額は元金と利息を支払い、全部払うまでです。会社が毎月定期的に支払う元金と利息のほかに,会社は以下の金額に相当する最終支払いを支払わなければならない6期日前支払元金総額(“最終支払い”)の百分率。
2019年の融資を完了し、第1弾の融資を抽出した後、当社はSVB及びWestRiverに株式承認証を発行し、合算を購入する37,606行使価格$の普通株4.73一株ずつです。2019年5月、第2弾の株式を抽出する際に、当社はSVBおよびWestRiverに株式承認証を発行し、合算を購入した12,130行使価格$の普通株10.86一株ずつです。2019年10月、第3弾の株式を抽出する際に、当社はSVBおよびWestRiverに株式承認証を発行し、合算を購入した24,262行使価格$の普通株3.88一株ずつです。すべての引受権証は直ちに行使と無効にすることができる10年発行の日から発効します。
当社の2019年の融資項目での債務は、当社の現在と将来のほとんどの資産の優先担保権益を担保としています。同社には、その知的財産権資産を担保する能力の制限を含む他の様々な習慣条約の遵守が義務付けられている。同社は2021年12月31日まで、2019年の融資下のすべての契約を守っている。
同社は#ドルの債務割引を記録した0.4第1回、第2回、第3回の借金時の株式証の推定公正価値と債務発行コストは100万ドルである。最後の支払い負債残高は#ドルである0.82021年12月31日現在、収入は100万ドルであり、貸借対照表上の他の長期負債に計上されている。債務割引と最終支払負債は、有効利息法を用いて2019年の融資期限内に利息支出に償却される。利息支出は、定期債務と最終支払負債に関する債務割引償却を含み、総額は#ドルである0.9百万ドルとドル1.42021年12月31日までと2020年12月31日までの年度はそれぞれ100万ドル
次の表には、2021年12月31日までに会社に必要な将来の元金支払い(千単位)を年ごとに示しています
| | | | | |
12月31日までの年度 | |
| 2022 | $ | 5,455 | |
| 2023 | 1,363 | |
元金支払総額 | 6,818 | |
未償却ローン費用を減らす | (46) | |
定期借款総額 | $ | 6,772 | |
7. 延子許可収入を渡す
当社は2021年6月にAlfasigmaとAlfasigma分割許可協定を締結し、これにより、当社はAlfasigmaに独占権利を付与し、EUおよび欧州経済地域およびイギリス、ロシア、ウクライナおよびいくつかの他の独立国、ヨーロッパおよび中央アジア地域(“分許可地域”)でbentracimabを含む任意の製品(“許可製品”)を開発、使用、販売、販売、要約および輸入する。Alfasigma許可の条項によると、会社は$を受け取りました20.02021年7月にAlfasigmaから100万ドルの前金を取得し、最高$を取得する資格があります35.0ある収入を実現する前に規制のマイルストーンを達成した後、最高で190.0あるビジネスマイルストーンと純売上高に基づく階層的特許権使用料の支払いを実現した後、収入は100万ドルに達し、パーセントは低い2桁から25%程度に上昇する。さらに、全体的な配置の一部として、同社は、いくつかの合意された金額以下の価格でAlfasigmaに特許製品を供給することに同意した
Alfasigmaライセンス契約によれば、会社はライセンス製品の開発を担当し、SFJプロトコルに従って、任意のマーケティング許可がAlfasigmaに割り当てられることを含む、欧州医薬品局(EMA)および医薬品およびサプリメント規制機関(MHRA)の規制許可を得ることを確実にする。Alfasigmaは、マーケティングおよび販売許可製品に必要な任意の規制承認(定価承認および上場後約束を含む)を取得し、維持する義務があり、EUおよびイギリス以外の再許可領土内の国の規制承認を確保する責任がある。
同社は、まず、Alfasigma再許可またはAlfasigma再許可内のアカウント単位が当事者のリスク、リターン、および活動に基づく協力スケジュールを表すかどうかを決定するために、ASC 808協力スケジュール(“ASC 808”)に従ってAlfasigma再許可を評価する。同社は、Alfasigmaが顧客を代表し、Alfasigma分割許可下の適切な会計を評価するために、ASC 606“顧客との契約収入”(“ASC 606”)内の関連指導を適用すると結論した。このガイドラインによると、会社は、(I)開発、使用、販売、販売、発売、および輸入許可製品の独占的再許可権(“許可”)、(Ii)開発および規制活動(“開発および規制活動”)、および(Iii)より低いコストまたはいくつかの合意金額以下の価格でAlfasigmaに許可製品(“ライセンス製品の供給”)を供給することを要求する約束を決定した。収入を確認するために、会社はこの3つの約束が異なる業績義務であることを確定し、これらの業績義務を履行する際に収入を確認する
その会社は#ドルを前払いすることにした20.0百万ドルはアルファシマ再許可開始時の取引価格を構成しています。将来可能な規制と発展マイルストーン支払いは、これらの金額に関連した収入が大幅に逆転するリスクが解決されていないため、十分に制限されている。未来の潜在的マイルストーンの実現は会社の制御範囲内ではなく、いくつかの研究と開発成功或いは監督部門の承認が必要であるため、重大な不確定性が存在する。会社は各報告期間の終了時にこれらのマイルストーンを実現する可能性を再評価し、リスク解消中に取引価格を調整する。さらに、後続の販売が発生した場合、当社は、これらの支払いが、主にAlfasigmaライセンスを締結する際にAlfasigmaに渡されるライセンスに関連するので、販売ベースのマイルストーンおよび特許使用料に関連する任意の対価格を確認するであろう
取引価格は契約開始時に推定された独立販売価格に基づいて三項目の履行義務に割り当てられる。ライセンスの独立販売価格は割引キャッシュフロー方法に基づいており、割引率、開発スケジュール、監督管理リスク、推定された市場需要と調整後の市場方法を使用した将来の収入潜在力を含むが、いくつかの要素を考慮した。開発と監督管理活動及び特許製品供給の独立販売価格は期待コストと保証金方法を用いて推定した2021年12月31日現在、会社は取引価格の前払い部分を履行義務として以下のように割り当てている(千単位)
| | | | | | | | | | | | | | | | | |
| 成約価格 | | 確認された累積子許可収入 | | 延子許可収入を渡す |
| 許可証 | $ | 10,223 | | | $ | 10,223 | | | $ | — | |
| 開発と規制サービス | 2,647 | | | 608 | | | 2,039 | |
| ライセンス製品の供給 | 7,130 | | | — | | | 7,130 | |
| $ | 20,000 | | | $ | 10,831 | | | $ | 9,169 | |
| より少ない長期繰延子許可収入の現在部分 | | | | | (1,547) | |
| 長期繰延子許可収入総額 | | | | | $ | 7,622 | |
当社は、取引価格と義務履行のために予想される総見積もりコストを見直し、報告期間終了ごとに繰延再許可収入を調整します。これらの変化により,確認された再許可収入と繰延再許可収入の金額が変化する.
8. 発展誘導負債
2020年1月に、当社はSFJ協定を締結し、この合意により、SFJは最大で提供することに同意しました120.0Bentracimabの全世界3期臨床試験Reverse−IT試験に関する資金とプロジェクト管理サービスは100万ドルに達した。SFJプロトコルの有効期間内に,当社は主に米国とEUのベンゼントラママママブの臨床開発と規制活動を担当し,SFJは主に中国と日本のbentracimabの臨床開発と監督活動を担当し,EUで臨床試験運営支援を提供している。
$を除いて90.0100万ドルの初期資金で会社は追加の$を得ることを選択しました30.0数百万の資金が特定の事前定義されたbentracimab臨床開発マイルストーンに到達した。SFJ協議開始から2021年12月31日まで、SFJ代表は資金を提供し、総額$を支払いました91.3SFJプロトコルでの100万ドル。同社はまた、SFJが追加の$を援助または返済すると予想している28.7100万ドルの臨床試験費用と他の費用です
米国食品医薬品局(FDA)がbentracimabのバイオ製品ライセンス申請を承認した場合、同社はSFJに第1期支払い$を支払うことに同意した5.0100万ドルと追加$325.0年間で合計百万ドルになる7人追加年間支払い(“米国承認支払い”)。EMAまたはいくつかのヨーロッパ諸国の国家規制機関がbentracimabの上場承認を提供した場合、同社はSFJに第1期支払い$を支払う5.0100万ドルと追加$205.0年間で合計百万ドルになる7人追加年間支払い(“EU承認支払い”)。大部分のアメリカの承認支払いとEUの承認支払いは適用司法管轄区域の上場承認三周年から七周年の間に支払います。もし日本の薬品と医療機器署あるいは中国の国家医療製品管理局がベントラマズマブの発売を許可したら、会社はSFJに第一期支払い#ドルを支払うことになります1.0百万ドルで、もう一ドル払います59.0年間で合計百万ドルになる8人追加年間支払い(“日本/中国承認支払い”)は、大部分の支払いが上場承認5周年から8周年の間に支払われる。日本/中国の承認支払いは、日本や中国でマーケティング承認を受けても一度だけ支払うことになる。SFJの実際の資金が#ドル以下である場合、米国の支払い承認、EU承認支払い、および日本/中国承認支払いは比例して調整される120.0百万ドルです。もし会社が食品·薬物管理局からbentracimabの上場承認を得ていない場合、会社は米国の承認支払いを支払う義務がなく、ヨーロッパ医薬品局またはあるヨーロッパ国家の国家監督管理機関からbentracimabの上場許可を得ていなければ、会社はEU承認支払いを支払う義務がなく、国家薬品監督管理局または国家薬品監督管理局からbentracimabの上場許可を得ていなければ、会社は日本/中国承認支払いを支払う義務がないだろう。
SFJ協定に署名した後、当社はSFJに引受権証を発行し、合算を購入します2,200,000普通株、行使価格は$6.501株当たり、契約条項は10年それは.捜査令状があります二つA枠:A枠とB枠。A枠は以下の株式証明書を代表する1,100,000すぐにSFJが行使できる株。B部分は以下の持分証明書を代表する1,100,000(I)いくつかの発展マイルストーンまたは(Ii)買収完了(SFJプロトコルの定義参照)に到達したときに行使可能な株式。これらの株式承認証は持分によって分類され、価値は$である7.9発行には確率調整のBlack-Scholes推定技術を用いる.
当社はSFJプロトコルをデリバティブとして入金しており、このデリバティブは、対価の徴収と返済時にそれぞれ増加と減少している。誘導ツールは、各報告期間において、それが公正な価値を推定するようにさらに調整される。2021年12月31日には、デリバティブは会社の貸借対照表に負債として記載されている。公正価値のいかなる変動も会社の経営報告書に記録されている。負債は最初に#ドルに入金された2.1$を含む百万ドル10.0SFJからの前払い金および当社普通株式承認証をSFJに発行する。SFJは2021年12月31日までに追加資金を提供し、当社に代わって総額$を支払う41.9開発派生負債はその後、2021年12月31日にレベル3派生負債として再計量された。公正な価値の変動は1ドルを招いた21.22021年12月31日までの年次経営報告書に開発派生負債による百万ドルの損失を再計量した
開発デリバティブ負債は,シーンごとにキャッシュフローの確率とタイミングを仮定し,リスク調整割引率を用いてこのようなキャッシュフローを推定するシナリオに基づく割引キャッシュフロー手法を用いて推定する.評価方法は、(I)融資の可能性とタイミング、(Ii)規制承認を得る可能性とタイミング、(Iii)会社の借入コストを含む、いくつかの観察できない3レベルの重要な情報を格納している16.00リスクなし借入金金利を%と(Iv)SFJの借入コストを加算します(2.50%に無リスク借入金金利を加算)。
2021年12月31日現在の開発デリバティブ負債活動(単位:千)を表に示す
| | | | | |
| 発展する
導関数
負債.負債 |
| 2019年12月31日の残高 | $ | — | |
| 初払い、普通株式承認証を差し引いた純額 | 2,075 | |
| 本期間の資金源 | 37,137 | |
| 価値変動を公平に承諾する | 12,507 | |
| 2020年12月31日残高 | $ | 51,719 | |
| 本期間の資金源 | 41,942 | |
| 価値変動を公平に承諾する | 21,182 | |
| 2021年12月31日の残高 | $ | 114,843 | |
9. 引受金とその他の事項
法律訴訟
当社は現在いかなる訴訟にも参加しておらず、経営陣も、当社の業務、経営業績、財務状況又はキャッシュフローに重大な影響を与えると考えられる当社の未解決又は脅威に対する訴訟を知っていません。
10. 賃貸借証書
同社は各種取消不可能な経営賃貸契約に基づいて事務や研究開発施設や設備をレンタルしている。
二零一零年一月、当社はペンシルバニア州マルヴィンにオフィスおよび実験室空間賃貸借契約(“マルバン借約”)を締結した。マルヴィンリースは2010年3月に開始され、改訂を経て、レンタル期間を2023年9月30日に延長し、レンタル契約をもう一度延長する権利がある3年それは.この賃貸契約には増加しているレンタル料支払いが含まれています。2018年12月、当社は2022年10月に満了するカリフォルニア州サンディエゴにあるオフィススペース賃貸契約を締結しました。2020年6月、当社はペンシルバニア州マルヴィンにオフィススペースを増やす賃貸借契約を締結し、賃貸契約は2023年9月に満期になります。2021年12月31日現在、当社の賃貸契約の加重平均残存レンタル期間は3.9年,使用権資産と対応する経営リース負債を決定するための加重平均割引率5.9%.
2021年12月31日までの経営リース負債満期日は以下の通り(単位:千)
| | | | | |
| 十二月三十一日までの年度 | |
| 2022 | $ | 555 | |
| 2023 | 419 | |
| 2024 | 279 | |
| 2025 | 283 | |
| 2026 | 215 | |
将来の最低賃貸支払い総額 | 1,751 | |
減算:現在値調整 | (202) | |
リース負債を経営する | $ | 1,549 | |
当社は賃貸経営の賃貸料支出を直線法で確認しています。家賃費用は$0.7百万ドルとドル0.62021年12月31日までと2020年12月31日までの年度はそれぞれ100万ドル。
11. 株主権益
棚登録表
2019年12月、同社は2020年1月に発効する2019年S-3用紙の“2019年棚登録説明書”を提出した。2023年1月に満了する“2019年棚登録声明”は、(I)当社の発売、発行、販売の最高総発行価格を$とすることを許可します200.0一度または複数回の発行および任意の組み合わせで百万株普通株、優先株、債務証券および引受権証を発行する;および(Ii)当社が発売、発行および販売する最高合計発行価格は最高$に達する60.0ATM計画によると、会社の普通株は“市場”販売で発行·販売することができる。これは1ドルです60.0ATM計画によると発行と販売可能な百万普通株はドルに含まれています200.02019年の“棚登録声明”によると発行·販売可能な証券は百万部に達する。2021年12月31日現在、同社は132.62019年の棚登録声明によると販売可能な残りの普通株式は、その中で57.0ATM計画では、100万台が販売される可能性があります。
ATM計画に基づいて売却された株
当社は2021年12月31日までに販売しております違います。ATM計画に基づいて発行された普通株。当社は2020年12月31日までに販売しております561,848ATM機計画による普通株の純収益は$2.9百万ドルです。
2021年3月サービス提供
2021年3月、“2019年棚登録声明”によると、会社は普通株の貸切公開を完了し、発行と売却の合計を達成した18,400,000普通株、公開発行価格は$3.50株ごとに純収益$が発生する60.2万ドル、引受割引と手数料などの発行コストを差し引いた。
12. 株に基づく報酬
在庫計画
2018年10月、会社取締役会と株主は、改訂された“2002年持分インセンティブ計画”(“2002年計画”)の継承と継続である“2018年度株式インセンティブ計画”(“2018年度計画”)を採択し、採択した。2002年の計画はこれ以上の寄付金を提供しないだろう。
当初、2018年計画により発行可能な会社普通株最高株式数は3,231,626株式です。2021年12月31日までに会社は817,7222018年計画に基づいて付与可能な株式。2018年計画によると発行保留の普通株式数は2019年1月1日から2028年1月1日まで自動的に増加し、額に相当する3各自動増資日の前月の最終日には、会社が発行した株式総数の割合、又は会社取締役会が決定したより少ない数の株式を決定する。2021年4月、会社取締役会は、毎年1月1日から2028年1月1日まで(2028年1月1日を含む)の株式備蓄を自動的に増加させる2018年計画の修正案を承認した3%から4前年の12月31日に発行された株式総数のパーセンテージを占める。この規定に合致した場合,当社は補足する1,927,6242022年1月1日に施行される2018年計画の株式を付与することができる
次の表は、2021年12月31日までの2002年計画と2018年計画の株式オプション活動をまとめています
| | | | | | | | | | | | | | | | | | | | | | | |
| 合計する オプション | | 重み付けの- 平均値 トレーニングをする 単価 共有 | | 重み付けの- 平均値 残り 契約書 期限(年) | | 骨材 固有の 価値がある |
| 2019年12月31日現在返済しておりません | 2,577,718 | | | $ | 3.29 | | | 7.9 | | $ | 7,914,459 | |
授与する | 1,227,159 | | | $ | 5.09 | | | | | |
鍛えられた | (51,572) | | | $ | 1.85 | | | | | |
キャンセルしたか、または期限が切れました | (155,145) | | | $ | 4.89 | | | | | |
| 2020年12月31日現在返済していません | 3,598,160 | | | $ | 3.85 | | | 7.5 | | $ | 1,737,432 | |
授与する | 1,271,836 | | | $ | 3.91 | | | | | |
鍛えられた | (209,751) | | | $ | 1.88 | | | | | |
キャンセルしたか、または期限が切れました | (193,444) | | | $ | 4.53 | | | | | |
| 2021年12月31日現在の未返済債務 | 4,466,801 | | | $ | 3.93 | | | 7.2 | | $ | 700,875 | |
| すでに帰属しており,2021年12月31日に帰属する予定である | 4,466,801 | | | $ | 3.93 | | | 7.2 | | $ | 700,875 | |
| 2021年12月31日に帰属し、行使可能です | 2,559,327 | | | $ | 3.75 | | | 6.2 | | $ | 676,046 | |
すでに株式購入権を授与した加重平均授出日の1株当たりの公正価値は#ドルである2.46そして$3.202021年12月31日および2020年12月31日までそれぞれ年度を終了した。行使されたオプションの内的価値の合計は#ドルである0.3百万ドルとドル0.12021年12月31日までと2020年12月31日までの年度はそれぞれ100万ドル。
2021年12月31日現在、未帰属従業員および非従業員株式オプション奨励に関する未確認報酬支出総額は$4.0100万ドルは加重平均期間中に2.5何年もです。
2018年10月、会社取締役会と株主はESPPを承認した。ESPPの目的は新入社員のサービスを確保し、既存の従業員のサービスを維持し、これらの従業員に激励を提供し、会社とその付属会社の成功のために最大限の努力をすることである。ESPPは、“米国従業員規則”第423節で指摘された“従業員株式購入計画”に適合することを目的としている。
最初にESPPは発行を許可しました196,000会社従業員又は会社の任意の指定関連会社従業員の購入権を付与することにより、会社普通株の株式を取得する。2021年12月31日までに会社は822,051ESPPによって発行可能な株。2019年1月1日から2028年1月1日までの例年1月1日まで、予約発行に供する普通株式数は自動的に(1)より小さい者が増加した1自動増資前の一ヶ月の最終日に発行された会社の普通株式総株式数の割合490,000株式;ただし、当該増資日のいずれか前に、当社取締役会は、当該増資が第(1)及び(2)項に記載された額よりも少ないことを明らかにすることができる。この規定に合致した場合,当社は補足する481,906ESPPに発行可能な株は2022年1月1日に発効する
2020年3月、会社は条件に合った従業員のESPP参加を許可し始めた。ESPPによると、条件を満たす従業員には会社の普通株を購入する権利が付与されており、これらの普通株からの資金は超えてはならない15従業員一人当たりの報酬の%です。ESPPは通常24ヶ月提供期限、その中には四つ6か月購入期限。各購入期間終了時に、条件を満たした従業員は以下の価格で会社普通株を購入することができます85契約期間開始時の公正市価または購入期末の公正市価のうち低い者の割合。ESPPは補償計画とみなされ、会社が記録した株式ベースの補償費用は#ドルである0.3百万ドルとドル0.12021年12月31日までと2020年12月31日までの年度はそれぞれ100万ドル。2021年12月31日までの年間で138,952普通株式はESPPによって加重平均価格#ドルで発行される2.42一株ずつです。2020年12月31日までの年間で62,063普通株はESPPにより発行され、加重平均価格は#ドルである3.00一株ずつです
2021年12月31日現在,ESPPに関する未確認補償支出総額は$である0.1100万ドル、加重平均期間中に約0.5何年もです
会社の2022年インセンティブ計画の説明については、“付記18.後続事件”を参照されたい。
株式オプションの公正価値を決定する
株式オプションを付与する各項目の公正価値は、以下に説明する方法および仮定を用いて当社が決定する。その中のいくつかの入力は主観的であり,通常決定するために判断が必要である.
所期期限·株式オプションの予想期間は、株式オプションが未償還と予想される加重平均期間を表す。当社は簡略化した方法で所期を見積もります。簡略化された方法は、期待期間をオプションの平均帰属時間および契約期間として計算する。
予想変動率·会社の経営歴史が限られているため、会社特有の歴史的または暗黙的な波動性が不足しており、予想変動率仮定は、株価公開された業界同業者のグループの歴史的波動性を研究することによって決定される。
無リスク金利·無リスク金利は、米国債に基づくと仮定し、その条項は、会社の株式オプションの予想期限と一致する。
配当を期待する-当社はまだ配当金を派遣していませんし、配当金を送るつもりもありません。
各オプションの公正価値は、付与された日に次の表の加重平均仮定を使用して推定される:
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2021 | | 2020 |
無リスク金利 | 0.88 | % | | 1.37 | % |
予想期限(年単位) | 6.0 | | 6.0 |
予想変動率 | 72 | % | | 71 | % |
期待配当収益率 | — | | | — | |
普通株主公正価値 | $ | 3.91 | | | $ | 5.09 | |
株式ベースの給与支出はすでに会社の同年度までの経営報告書に報告されている2021年12月31日2020年との状況は以下のとおりである(千単位)
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2021 | | 2020 |
| 一般と行政 | $ | 1,509 | | | $ | 1,594 | |
| 研究開発 | 759 | | | 643 | |
| 株に基づく報酬総額 | $ | 2,268 | | | $ | 2,237 | |
13. ライセンスとその他の合意
医療免疫有限許可プロトコル
二零一七年十一月、当社は医療免疫有限会社(“医療免疫”)とライセンス契約(“医療免疫許可証”)を締結した。医療免疫はアスリコン(“アスリコン”)の全額付属会社である。医療免疫許可証の条項によると、医療免疫は、医療免疫許可証下の製品(“医療免疫許可製品”)を開発し、商業化するために、当社に独占的な世界的権利を付与する。会社は#ドルを支払ったか、またはマイルストーンで支払いました3.0百万ドルで、総額$を超えない余剰金を支払う義務があります15.0臨床開発と規制マイルストーンを実現した上で、100万ドルに達した。また、同社は任意の医療免疫許可製品の純売上高の中位数から10分の1までの等級別特許権使用料と、最高$までの追加支払いを医療免疫会社に支払う50.0合計百万の商業マイルストーンです。当社では2021年12月31日までに特許権使用料および2020.
同社はまたMedImmuneが提供する技術サービスに関する四半期費用を支払わなければならない。MedImmuneライセンスは、当社がbentracimabのビジネスメッセージングにおいてMedmuneと協力することを要求し、会社がいくつかの商業調査要件に達していない場合には、bentracimabの返却権利をMedmuneに提供することを要求する。さらに、MedImmuneライセンスは、第三者製品のストレージコストのオプションを提供します。当社では2021年12月31日までに第三者製品の貯蔵費用および2020それは.アスリーカンは同社の株主です。
デューク大学許可協定
2000年10月、当社はデューク大学(“デューク大学”)とライセンス契約を締結した。デュークライセンスによれば、デュークは、デュークライセンスに含まれる任意の製品またはプロセスを開発し、それを商業化するために、いくつかの特許権下の独占グローバルライセンスおよびデューク所有または制御ノウハウの非独占ライセンスを当社に付与する。デューク大学のライセンスは2016年2月に改正され,デューク大学が小分子腫瘍学の分野で同社の技術を使用することを許可した。デュークライセンスは世界的な再ライセンス協定であり、特許権に含まれる最後に満了した特許の有効期間内に完全に有効であり、2030年と推定される。同社はデュークライセンス下のすべてのアメリカと外国特許権の申請、起訴、維持を要求された。
同社には最高$の支払いが義務付けられている2.2臨床開発と法規のマイルストーンを実現した後、100万ドルに達し、最高で0.4ビジネスのマイルストーンを達成した上で100万ドルに達した。もし会社が規定された時間内にある臨床開発と監督管理のマイルストーンを達成できなければ、デューク大学はデューク大学の免許を終了するかもしれない。同社は2021年12月31日現在、その発展義務を履行している。
同社は、1つまたは複数の製品またはプロセスを開発し、商業市場に導入するために、商業的に合理的な努力を使用することを要求されている。デューク社またはその分ライセンス者のデューク社のライセンス製品に対する純売上高は1桁の印税パーセントが低く、最低総印税は#ドルとなる0.2会社が特定のビジネスマイルストーンを達成した後に支払わなければならない百万ドルです違います。発効日から2021年12月31日まで、デュークが許可した製品やサービスが販売されています。
ある連合の費用は最大で$に達する0.3特許権の商業化方式によると、会社は戦略連盟を結成することで得られた費用の100万または低い2桁の数百分を第三者から獲得する必要がある可能性がある。会社はデュークに最初のドルを支払わなければならない1.0それは、再許可者から受信された非特許権使用料と、その後一定の条件で受信された任意の追加の非特許権使用料の特定の割合とを含む。デューク社が第三者に小分子腫瘍学分野の許可証または再許可を発行することによって収入を得た場合、それは、ドルを超えるそのような収入の特定の割合を会社に支払うことになる1.0百万ドルです。会社が招く違います。2021年12月31日まで年間公爵免許項における費用及び2020.
アルファシグマ二次ライセンス
2021年6月、当社はAlfasigmaとAlfasigma分割許可協定を締結し、これにより、当社はAlfasigmaに独占権利を付与し、ライセンスエリア内でAlfasigmaの開発、使用、販売、販売、要約販売、および輸入許可製品を開発、使用、販売した。Alfasigmaライセンスの条項によると、2021年7月、会社は$を受け取った20.0Alfasigmaから100万ドルの前金を取得し、最高$を得る資格があります35.0ある収入を実現する前に規制のマイルストーンを達成した後、最高で190.0あるビジネスマイルストーンを実現し、純売上高別に特許使用料を支払うと、純売上高は100万ドルに達し、パーセントは低い2桁から25%程度に上昇する。
最高可達$35.0マイルストーンの支払いを規制する百万ドル:(I)ドル10.0EMAが特許製品に対する最初の薬品承認申請を受けた後、100万ドルを支払わなければならない12.5環境管理専門家の条件付き監督許可を得た後,100万元を支払わなければならない;および(Iii)残りの12.5EMAの無条件監督許可を得た後、100万ドルを支払い、(A)コントロールできない大出血或いは生命に危害を及ぼす出血患者と(B)緊急手術或いは侵襲性プログラムを必要とする患者の中で、チカグレルの抗血小板作用を逆転するための許可製品を発行する
Alfasigma分割ライセンスによれば、会社は、ライセンス製品の開発を担当し、SFJプロトコルに従って、その後、任意のマーケティング許可がAlfasigmaに割り当てられることを含むEMAおよびMHRAの規制承認を得ることを保証する。アルファシマには、マーケティングや特許製品の販売に必要な任意の規制承認(定価承認や発売後の約束を含む)を取得し、欧州やイギリス以外の国の規制承認を確保する義務がある。Alfasigmaは、設定された期間内に会社からその要求を購入し、その後、会社は、Alfasigmaが要求した特許製品をより低いコストまたはいくつかの合意された金額以下の価格で供給する義務がある。
事前に終了しない限り、Alfasigma再許可は、各ライセンス製品および再ライセンス領域の各国/地域について、(1)そのライセンス製品の国/地域での初の商業販売10周年、(2)その国/地域での最後の外部ライセンス特許の満了、および(3)その国/地域におけるライセンス製品の排他的な満了(ある場合)の最後の日に自動的に失効する。
Alfasigmaライセンスに関して、会社およびAlfasigmaはまた、Medmuneとスコア付与許可の確認(“付与確認”)を締結しており、(I)会社は、他の事項に加えて、Alfasigma分割許可をMedmuneに譲渡することができ、または(Ii)会社が何らかの義務に違反した場合、Medimune許可を会社からAlfasigmaに譲渡する可能性があることが規定されている
Medimmuneライセンスによれば、治癒または修復されておらず、SFJは、SFJプロトコルの定義のような“計画移行”を実行する理由があるが、そうしないことを選択する。同社は$を確認した10.8百万ドルとゼロ2021年12月31日までの年間におけるAlfasigma再許可項目の収入と2020それぞれ,である.
バク許可協定
2019年4月、当社はバク生物科技有限公司(“バク”)とライセンス契約(“バクライセンス契約”)を締結し、この合意に基づき、バクはいくつかの知的財産権に基づいて当社にバクの独自技術を使用する独占ライセンスを付与した大腸菌.大腸菌指定されたアジア諸国以外の世界各地でbentracimabを生産するための菌株を開発し、bentracimabを商業化し、承認されれば、会社または代表会社がバクの独自技術を使用して製造する大腸菌.大腸菌世界的にストレスを与えています当社は本許可に基づいて再許可を付与する権利がありますが、バク許可協定に規定されているいくつかの条件を遵守しなければなりません。協定条項によると、同社は固定的で象徴的な単位あたりの特許権使用料を支払う必要があり、当該使用料は調整され、固定ユーロ金額の年間許可料を支払うことが可能であり、金額は低いものから中6桁までとなる。この協定は、同社の特許権使用料義務が満了した後、全額支払いとみなされ、非独占許可に変換される無期限の期間内に有効である。指定された日数内に是正されなければ,いずれも違約によりバク許可プロトコルを終了することができる.同社はバクから別の良い生産規範(CGMP)の認証を得たメーカーBioVectra Inc.(“BioVectra”)への現在のbentracimab製造技術の技術譲渡を完成し、そしてすでにBioVectraを会社が行っている臨床試験のために薬剤を製造し、そして監督部門の許可を得た後に商業供給のbentracimabを生産する。その会社は$を生み出した0.4百万ドルとドル0.32021年12月31日までの年間バク許可協定項における百万コストと2020それぞれ,である.
Viamet資産購入契約
2020年1月,当社はViamet PharmPharmticals Holdings,LLCとその全資子会社Selenity Treateutics(バミューダ)株式会社(“売り手”)と購入プロトコル(“PB 6440プロトコル”)を締結し,これにより,当社は売り手独自のCYP 11 B 2阻害剤化合物(従来はSE−6440またはVT−6440と呼ばれていた)および当社がPB6440プロトコルに従って買収した特許権に含まれる他のCYP 11 B 2阻害剤化合物(総称して“化合物”)のすべての資産および知的財産権を買収した。PB 6440協定の条項によると、会社は売り手に費用#ドルを前払いする0.1100万ドルで売り手に最高$を支払わなければなりません5.1いくつかの候補製品のいくつかの開発と知的財産権マイルストーンが実現された後、化合物を含み、最高で$に達する142.5化合物を含む承認製品が、特定の商業的マイルストーンおよび化合物を含む承認製品の純売上のうちの中央値までの低い特許権使用料パーセントに達した場合、特定の場合には、慣例的に減少および相殺することができる。会社が招くゼロそして$0.12021年12月31日までの年度PB 6440協定項における百万元のコストと2020それぞれ,である.
BioVectra供給プロトコル
当社は2021年3月にBioVectraと供給プロトコル(“BioVectraプロトコル”)を締結し、商業流通のためにBioVectraから原料薬を製造および供給した。同社はまた,BioVectraを会社が行っている臨床試験のために薬物物質を生産している。
BioVectra協定の条項によると、BioVectraは商業流通のために毎年合意されたロットの製品を生産する能力を維持することを約束し、同社は第3者とベンゼントラマブを生産する契約を自由に締結できるにもかかわらず、指定された最低ロット製品(“最低年間約束”)を毎年購入することを承諾した。会社は各ロットのbentracimabの供給価格を支払い、価格はbentracimabの製造過程がBioVectraプロトコルに基づいて検証した後、ある消耗品、原材料、第三者テストのコストを加えて確定する
最低年度約束によると,会社は少なくとも(I)約$を購入する義務がある14.02022年から2023年までの百万ロットのベンゼントラマモノクロナル,(Ii)約$37.02024年にフェニトラシズマブ、および(Iii)約$を100万ロット購入しました48.02025年から2031年まで毎年数百万ロットのフェニトラシズマブがある。会社が特定年度に適用される最低年度承諾を購入していない場合、会社はBioVectraに金額を支払う義務があり、金額は当時適用された各ロットの供給価格にその年度最低年度承諾とその年度に実際に購入した製品ロットとの差額を乗じたものであり、BioVectraが同社が発注したロット数を納入できない限りである。当社は2026年以降の最低年度のコミットメントを最大に削減する権利がある
毎年最大百分率を指定する。また、同社がbentracimabを使用した製品の規制承認を米国またはヨーロッパの1つの地域でしか得られない場合、BioVectraと同社は、製品の需要減少や供給価格への影響を反映して、より低い数量約束を反映するために、BioVectra協定の改正を誠実に検討することに同意した。
14. 収入.収入
再許可収入
再許可収入は会社が確認したAlfasigma再許可に関する収入と関連がある。同社が確認した再許可収入は$10.8百万ドルとゼロ2021年12月31日までの年度および2020それぞれ,である
奨学金収入
2018年2月、会社は米国国立衛生研究院が提供した小企業革新研究(SBIR)の助成を受け、総額は$2.82018年2月17日から2020年7月31日までの間に,肺動脈高圧治療のためのPemziviiptadilの臨床開発を支援した。SBIR贈与に関連して、米国政府は、同社がこのような贈与に基づいて開発した任意の技術を用いた非排他的·免版税許可を得ることになる。2020年3月31日までに会社はすべての2.8SBIRの寄付により、100万ドルの資金を得ることができる。会社は認識していますゼロそして$0.32021年12月31日と2020年12月31日までの年間で、SBIRによる贈与はそれぞれ100万ユーロを獲得した。
15. 所得税
所得税支出(福祉)の構成は以下のとおりである(千計)
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2021 | | 2020 |
| 現在のところ | | | |
| 連邦制 | $ | — | | | $ | — | |
| 状態.状態 | — | | | — | |
| 外国.外国 | 1,600 | | | — | |
| 総電流 | 1,600 | | | — | |
| | | |
| 延期する | | | |
| 連邦制 | — | | | — | |
| 状態.状態 | — | | | — | |
| 外国.外国 | — | | | — | |
| 集計を延期する | — | | | — | |
| 所得税支出(福祉)合計 | $ | 1,600 | | | $ | — | |
所得税費用(福祉)と法定連邦所得税税率を運営損失に適用することで計算される金額の調節をまとめると以下のようになる(千単位)
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2021 | | 2020 |
| 法定税率所得税割引 | $ | (27,189) | | | $ | (20,699) | |
| 州所得税、連邦福祉を差し引いた純額 | (7,065) | | | (6,823) | |
| 永久品 | 348 | | | 8 | |
| 株に基づく報酬 | 174 | | | 215 | |
| 孤児薬品信用 | (1,827) | | | (2,544) | |
| 研究開発単位 | (2,489) | | | (863) | |
| 不確定税収状況 | 1,125 | | | 785 | |
| 州金利の変化 | 910 | | | 74 | |
| 評価免除額を変更する | 36,284 | | | 28,090 | |
| 他にも | 1,329 | | | 1,757 | |
| $ | 1,600 | | | $ | — | |
会社繰延税金資産の重要な構成要素は以下の通り(千計)
| | | | | | | | | | | |
| 12月31日まで |
| 2021 | | 2020 |
| 繰延税金資産: | | | |
| 純営業損失が繰り越す | $ | 70,903 | | | $ | 51,398 | |
| 研究開発と孤児薬の相殺 | 12,061 | | | 8,662 | |
| 費用を計算する | 921 | | | 936 | |
| 無形資産 | 31 | | | 43 | |
| リース負債を経営する | 411 | | | 562 | |
| 派生負債 | 30,491 | | | 16,700 | |
| その他、純額 | 615 | | | 628 | |
| 繰延税金資産総額 | 115,433 | | | 78,929 | |
| | | |
| 繰延税金負債: | | | |
| 経営的リース使用権資産 | (390) | | | (540) | |
| 財産と設備、純額 | (694) | | | (324) | |
| 繰延税金負債総額 | (1,084) | | | (864) | |
| | | |
| 減価前繰延税金資産純資産 | 114,349 | | | 78,065 | |
| 推定免税額 | (114,349) | | | (78,065) | |
| 繰延税項目純資産 | $ | — | | | $ | — | |
経営陣は2021年12月31日と2020年12月31日までに繰延税項純資産の可変現能力を評価し、繰延税項純資産計に対する評価準備の必要性を評価した。この評価は、ASC 740に含まれるフレームワークを利用する所得税これにより、経営陣は、貸借対照表日までのすべての利用可能なプラスおよび負の証拠を考慮して、当社の繰延税項目純資産の全部または一部を実現するかどうかを決定する。この指導の下で、資産が現金化できない可能性が高い(確率レベルが50%を超える)場合には、繰延税項純資産の推定値を作成するために準備しなければならない。
経営陣は米国会計基準第740条の指導に従い、“近年の累積損失は克服困難な重大な負の証拠である”と指摘し、2021年12月31日と2020年12月31日現在、会社の繰延税項純資産は現金化できないと結論した。したがって、価格計算手当は#ドルとなる114.3百万ドルとドル78.1繰延税の純資産を相殺するために100万ドルを記録した。2021年12月31日終了年度と2020年12月31日終了年度の推定手当は#ドル増加に変化36.3100万ドル1,000万ドル増加しました28.1それぞれ100万ドルです
2021年12月31日現在、当社の連邦と州の純営業損失は$に転換しています259.1百万ドルと$227.6それぞれ100万ドルです2018年前に生成された連邦NOLは相殺に使用できます100将来の課税所得額の10%は、以前に税法の他の規定で利用または制限されていない限り、2022年に満期になる。連邦NOLは2017年以降に$を生み出しました167.5100万ドルは相殺に使えます80将来の課税所得額の%は、税法が別途規定されていない限り、無期限に繰り越すことができます。州NOLは#年から満期になります2029以前に使用したことがない限り。ペンシルバニア州NOLのドル125.8100万ドルは相殺できます40毎年未来の課税所得額の割合を占めている。
2021年12月31日まで、会社は連邦と州の研究開発税収控除総額$を持っています7.0百万ドルとドル0.8それぞれ100万ドルです繰り越した連邦と州研究開発税控除は#年から失効するだろう2028そして2029以前に使用されたことがない限り、別々に使用されるだろう。カリフォルニア州の研究税金の繰越免除は満期にならないだろう。
2021年12月31日現在、同社は連邦孤児薬物信用繰越金額を$としている8.5100万ドルこのお金は#年に満期になります2036以前に使用したことがない限り。
同社は2021年12月31日現在、相殺と孤児薬物相殺の組み合わせを開発している。その中のいくつかの相殺は税収控除研究から来て、合格した活動を記録し、もういくつかの相殺は研究から獲得したものではない。研究により計算された信用については、米国国税局は監査時に計算された信用金額に同意しない可能性がある。最終的に他の単位を学習すると、これらの特定の単位の調整につながる可能性がある。
国税法によると、3年以内に所有権変更が50%を超えた後、会社の純営業損失と税収控除繰越の使用が制限される可能性がある。いずれの未使用年度限度額は将来年度に振り替えることができ、純営業損失と税額控除繰越期間の残高とすることができる。これらの規則により、従来の所有権変更は、当社が毎年何らかの税収繰越を使用する能力を制限していた可能性がある。しかも、特定の州の運営損失も同じように限られているかもしれない。当社はその持分融資が実益所有権に及ぼす歴史的あるいは潜在的な影響を分析していないため、繰り越しの純営業損失がいかなる国内収入法第382条の制限を受けるかどうかについては決定していない。
同社は不確定な税務状況を確認·計量する2ステップ法を採用している。最初のステップは、関連する控訴または訴訟手続きの解決を含む監査において、既存の証拠の重みがその地位が監査においてより維持される可能性が高いことを示すかどうかを決定することによって、確認のために納税状況を評価することである。第二段階は税収割引を最大金額とすることであり、最終決済時に実現される可能性は50%を超える。所得税は、米国会計基準740以降の採用中に確認するために、発効日により達成可能な確認閾値に到達しなければならない。本説明はまた、計量、終了確認、分類、利息と罰、過渡期会計、開示と過渡について指導を提供した。
同社は米国連邦管轄区と各州司法管轄区で所得税申告書を提出した。2018年以降の納税年度は引き続き連邦税務審査を受け、2018年以降の納税年度は引き続き当社のより重要な州税務管区の審査を受けます。来年度の納税申告書では、2021年12月31日に繰り越した純営業損失は、それぞれの納税年度が終了するまで審査を継続する。
以下の表は、会社が税収総額を確認していないことに関する活動(千計)をまとめています
| | | | | | | | | | | |
| 12月31日までの年度 |
| 2021 | | 2020 |
年明け未確認の税収割引総額 | $ | 3,345 | | | $ | 2,560 | |
今年度のポストに関する増加 | 1,236 | | | 871 | |
前年のポストに関する増加 | 55 | | | — | |
前年のポストに関する減少 | — | | | (86) | |
未確認税収割引が満期になります | — | | | — | |
年末に税収総額が確認されていません | $ | 4,636 | | | $ | 3,345 | |
当社の推定手当のため、ありません未確認の税収割引は、確認されれば、会社の実際の税率に影響を与える。
2021年12月31日と2020年12月31日までの同社の未確認税収割引は4.6百万ドルとドル3.3それぞれ100万ドルです当社は所得税支出における不確定な税収状況に関する利息と罰金を確認します。当社は2021年12月31日および2020年12月31日までの年間で、不確定な税務状況についていかなる利息や罰金を請求することもありません。同社はその未確認の税収割引が今後12カ月以内に大きな変化はないと予想している。
2020年3月27日、米国は“コロナウイルス援助、救済、経済安全法案”(略称“CARE法案”)を公布した。CARE法案は、米国経済を活性化するための支出と税収減免を含む緊急経済刺激計画であり、新冠肺炎の影響を抑制するための全国的な行動に資金を提供する。CARE法案は新冠肺炎疫病に対する全面的な税収改革を規定しているが、会社の財務諸表に影響を与えることが予想されるいくつかのより重要な条項は、純営業損失の使用に対するある制限を廃止し、ある損失の損失繰越期限を5年に増加させ、利息支出を控除する能力を増加させ、以前に公布された減税と雇用法案のいくつかの条項を改正することを含む。同社はCARE法案はその財務状況、経営結果、あるいはキャッシュフローに実質的な影響を与えないと考えている。
2020年12月27日、米国は“総合支出法案”を公布し、満期を予定していたCARE法案の多くの福祉を延長した。総合支出法案は当社の総合財務諸表及び関連開示に大きな影響を与えない。
16. 従業員退職計画
会社は国税法第401(K)条に基づいて従業員退職計画を策定した。本計画の要求に合致すれば、すべての従業員が参加する資格があります。この計画によると、当社は等額出資を行う必要はありませんが、2019年から当社は等額出資を開始します。会社(The Company)
自発的に寄付する$0.3百万ドルとドル0.2それぞれ2021年12月31日までと2020年12月31日までの計画で100万ドル。
17. 関係者取引
上記付記13で述べたように、当社は医療免疫許可証の一方である。医薬免疫の親会社アスリカンは同社の関連側である。
18. 後続事件
2022年1月10日、当社が発表500,000ATMで計画された普通株による純収益は$1.2百万ドルです。
2022年1月13日、会社はインセンティブ支出に対する株式補償計画である“2022年インセンティブ計画”(以下、“インセンティブ計画”)を策定した。2022年1月14日、当社は保留します1,400,000インセンティブ計画に基づいて付与された普通株。
(A)(2)財務諸表付表
必要ではない、適用されない、または要求された情報が財務諸表または財務諸表に添付されているので、すべての財務諸表添付表は省略される。
(A)(3)展示品
展示品索引
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で編入する |
展示品 番号をつける | | 展示品名 | | 表 | | 書類番号. | | 展示品 | | 提出日 |
| 3.1 | | PhaseBio製薬会社の登録証明書の改訂と再発行。 | | 8-K | | 001-38697 | | 3.1 | | 2018年10月22日 |
| | | | | | | | | | |
| 3.2 | | PhaseBio製薬会社の定款を改正して再制定する。 | | S-1/A | | 333-227474 | | 3.4 | | 2018年10月5日 |
| | | | | | | | | | |
| 4.1 | | C-1シリーズの転換可能な優先株を購入する権利証は、PhaseBio PharmPharmticals,Inc.が2017年10月18日にシリコンバレー銀行に発行された。 | | S-1 | | 333-227474 | | 4.3 | | 2018年9月21日 |
| | | | | | | | | | |
| 4.2 | | PhaseBio製薬会社とそのある株主が2018年8月27日にPhaseBio製薬会社とそのある株主の間で修正と再署名した投資家権利協定。 | | S-1 | | 333-227474 | | 4.4 | | 2018年9月21日 |
| | | | | | | | | | |
| 4.3 | | 普通株を購入する引受権証は、PhaseBio製薬会社が2019年3月25日にシリコンバレー銀行に発行した。 | | 10-K | | 001-38697 | | 4.4 | | March 26, 2019 |
| | | | | | | | | | |
| 4.4 | | 普通株を購入した引受権証は,PhaseBio製薬会社が2019年3月25日にWestRiver革新融資基金VIII,L.P.に発行した。 | | 10-K | | 001-38697 | | 4.5 | | March 26, 2019 |
| | | | | | | | | | |
| 4.5 | | 普通株購入権証は,PhaseBio PharmPharmticals,Inc.が2019年7月26日にWestRiver Innovation Lending Fund VIII,L.P.に発行された。 | | 10-Q | | 001-38697 | | 4.6 | | 2019年8月14日 |
| | | | | | | | | | |
| 4.6 | | 普通株を購入する引受権証は、PhaseBio製薬会社が2019年7月26日にシリコンバレー銀行に発行した。 | | 10-Q | | 001-38697 | | 4.7 | | 2019年8月14日 |
| | | | | | | | | | |
| 4.7 | | 普通株を購入する引受権証は、PhaseBio製薬会社が2019年10月9日にシリコンバレー銀行に発行した。 | | 10-Q | | 001-38697 | | 4.8 | | 2019年11月14日 |
| | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で編入する |
展示品 番号をつける | | 展示品名 | | 表 | | 書類番号. | | 展示品 | | 提出日 |
| 4.8 | | 普通株購入権証は,PhaseBio PharmPharmticals,Inc.が2019年10月9日にWestRiver Innovation Lending Fund VIII,L.P.に発行された。 | | 10-Q | | 001-38697 | | 4.9 | | 2019年11月14日 |
| | | | | | | | | | |
| 4.9 | | 普通株を購入した引受権証は,PhaseBio製薬会社が2020年1月9日にSFJ製薬X株式会社に発行した。 | | 10-K | | 001-38697 | | 4.10 | | March 30, 2020 |
| | | | | | | | | | |
| 4.10 | | PhaseBio製薬会社普通株説明。 | | 10-K | | 001-38697 | | 4.11 | | March 30, 2020 |
| | | | | | | | | | |
10.1+ | | 2018年株式インセンティブ計画および株式オプション付与通知およびオプションプロトコルフォーマット。 | | S-8 | | 333-227935 | | 10.2 | | 2018年10月22日 |
| | | | | | | | | | |
| 10.2+ | | 2018年株式インセンティブ計画(改訂)。 | | 10-Q | | 001-38697 | | 10.1 | | 2021年11月10日 |
| | | | | | | | | | |
| 10.3#+ | | “華南理工大学2018年度株式激励計画付与通知書及び奨励協定”フォーマット。 | | | | | | | | |
| | | | | | | | | | |
| 10.4+ | | 2018年従業員株購入計画。 | | S-8 | | 333-227935 | | 10.3 | | 2018年10月22日 |
| | | | | | | | | | |
| 10.5+ | | 2022年株式オプション付与通知およびオプション協定のインセンティブ計画およびフォーマット。 | | S-8 | | 333-262185 | | 99.3 | | 2022年1月14日 |
| | | | | | | | | | |
| 10.6#+ | | “南洋理工大学2022年奨励計画授賞通知書及び授賞契約書”。 | | | | | | | | |
| | | | | | | | | | |
| 10.7# | | 改正された非従業員役員報酬政策。 | | | | | | | | |
| | | | | | | | | | |
| 10.8+ | | PhaseBio製薬会社とそのすべての役員と幹部との間の賠償協定フォーマット。 | | S-1/A | | 333-227474 | | 10.5 | | 2018年10月5日 |
| | | | | | | | | | |
| 10.9#+ | | 改正された解散費福祉計画と参加協定形式。 | | | | | | | | |
| | | | | | | | | | |
| 10.10+ | | 2002年株式計画及びオプション合意フォーマットの改訂及び再作成及び当該等の合意による行使通知。 | | S-1 | | 333-227474 | | 10.1 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.11+ | | 2012年11月19日までの招待状は、PhaseBio製薬会社とJonathan P.Mowによって提供され、現在に修正されている。 | | S-1 | | 333-227474 | | 10.7 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.12+ | | 招待状は,2016年3月13日,PhaseBio製薬会社とJohn Sharpが提供した。 | | S-1 | | 333-227474 | | 10.8 | | 2018年9月21日 |
| | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で編入する |
展示品 番号をつける | | 展示品名 | | 表 | | 書類番号. | | 展示品 | | 提出日 |
| 10.13+ | | 招聘状の日付は2016年3月30日で、PhaseBio製薬会社と李家超博士が署名した。 | | S-1 | | 333-227474 | | 10.9 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.14† | | ライセンス契約は,日付は2006年10月18日であり,PhaseBio PharmPharmticals,Inc.(PhaseBio PharmPharmticals,Inc.の前身)とその間のライセンスプロトコルによって改訂された.デューク大学と。 | | S-1 | | 333-227474 | | 10.10 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.15†† | | PhaseBio製薬会社とデューク大学との間のライセンス契約第8改正案は、2019年3月5日となっている。 | | 8-K | | 001-38697 | | 10.1 | | April 9, 2019 |
| | | | | | | | | | |
| 10.16† | | PhaseBio PharmPharmticals,Inc.とMedImmune Limitedとの間の許可プロトコルは,2017年11月21日である. | | S-1 | | 333-227474 | | 10.11 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.17 | | PhaseBio PharmPharmticals,Inc.とMedImmune Limitedの間で2020年1月9日に署名されたライセンス契約の修正案。 | | 10-K | | 001-38697 | | 10.13 | | March 30, 2020 |
| | | | | | | | | | |
| 10.18†† | | Medimune LimitedとPhaseBio PharmPharmticals,Inc.の間の許可プロトコルおよび関連オプションにより再許可が付与されていることを確認した. | | 10-Q | | 001-38697 | | 10.2 | | 2021年8月21日 |
| | | | | | | | | | |
| 10.19 | | 融資·担保協定は、2017年10月18日にPhaseBio製薬会社とシリコンバレー銀行が署名·改訂して現在に至っている。 | | S-1 | | 333-227474 | | 10.12 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.20 | | 融資と安全協定、日付は2019年3月25日、PhaseBio PharmPharmticals,Inc.とシリコンバレー銀行とWestRiver革新融資基金VIII,L.P。 | | 10-K | | 001-38697 | | 10.13 | | March 26, 2019 |
| | | | | | | | | | |
| 10.21 | | PhaseBio PharmPharmticals,Inc.とシリコンバレー銀行とWestRiver革新融資基金VIII,L.P.が2020年3月19日に署名した融資と安全協定の同意と第1修正案。 | | 10-K | | 001-38697 | | 10.16 | | March 30, 2020 |
| | | | | | | | | | |
| 10.22 | | 従属協定、期日は2020年3月19日であり、シリコンバレー銀行、WestRiver革新融資基金VIII、L.P.とSFJ PharmPharmticals X,Ltd. | | 10-K | | 001-38697 | | 10.17 | | March 30, 2020 |
| | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で編入する |
展示品 番号をつける | | 展示品名 | | 表 | | 書類番号. | | 展示品 | | 提出日 |
| 10.23†† | | 知的財産権安全協定、期日は2020年3月19日であり、PhaseBio製薬会社とシリコンバレー銀行とWestRiver革新融資基金VIII,L.Pからなる。 | | 10-K | | 001-38697 | | 10.18 | | March 30, 2020 |
| | | | | | | | | | |
| 10.24†† | | プライマリサービス協定は,2018年11月14日にPhaseBio製薬会社とBioVectra Inc.が署名した。 | | 10-K | | 001-38697 | | 10.14 | | March 26, 2019 |
| | | | | | | | | | |
| 10.25# | | PhaseBio製薬会社とBioVectra社間のメーンサービス協定の第1号改正案は,2021年11月18日である。 | | | | | | | | |
| | | | | | | | | | |
| 10.26†† | | PhaseBio製薬会社とBioVectra Inc.との間の供給協定は,2021年3月10日である。 | | 10-Q | | 001-38697 | | 10.2 | | May 13, 2021 |
| | | | | | | | | | |
| 10.27 | | レンタル契約は、日付は2010年1月15日で、PhaseBio製薬会社とLiberty Property Limited Partnershipによって署名され、現在まで改訂されている。 | | S-1 | | 333-227474 | | 10.13 | | 2018年9月21日 |
| | | | | | | | | | |
| 10.28†† | | 共同開発協定は,2020年1月9日にPhaseBio製薬会社とSFJ製薬X株式会社が署名した。 | | 10-K | | 001-38697 | | 10.21 | | March 30, 2020 |
| | | | | | | | | | |
| 10.29†† | | PhaseBio製薬会社とSFJ製薬会社間の計画移転プロトコルフォーマット。 | | 10-K | | 001-38697 | | 10.22 | | March 30, 2020 |
| | | | | | | | | | |
| 10.30†† | | 資産購入協定は、日付は2020年1月13日で、PhaseBio製薬会社、Viamet製薬ホールディングスとSelenity治療(バミューダ)有限公司が署名した | | 10-K | | 001-38697 | | 10.23 | | March 30, 2020 |
| | | | | | | | | | |
| 10.31†† | | 2021年6月16日までに,PhaseBio製薬会社とAlfasigma,S.p.A.が署名したライセンス契約。 | | 10-Q | | 001-38697 | | 10.1 | | 2021年8月12日 |
| | | | | | | | | | |
23.1# | | ピマウェイ有限責任会社は同意しました | | | | | | | | |
| | | | | | | | | | |
24.1# | | 授権書(署名ページに含まれる) | | | | | | | | |
| | | | | | | | | | |
31.1# | | 2002年のサバンズ·オキシリー法案第302条に基づき、最高経営責任者と総裁(最高経営責任者)証明書が発行された。 | | | | | | | | |
| | | | | | | | | | |
31.2# | | 2002年サバンズ·オクスリ法第302条に基づいて首席財務官(首席財務官)を認証する。 | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で編入する |
展示品 番号をつける | | 展示品名 | | 表 | | 書類番号. | | 展示品 | | 提出日 |
32.1#* | | 2002年の“サバンズ-オックススリー法案”906節で採択された“米国法典”第18編1350条による最高経営責任者(CEO)の認証。 | | | | | | | | |
| | | | | | | | | | |
32.2#* | | 2002年の“サバンズ-オックススリー法案”906節で採択された“米国法典”第18編1350条による首席財務官(首席財務官)の認証。 | | | | | | | | |
| | | | | | | | | | |
101.INS# | | XBRLインスタンスドキュメント。 | | | | | | | | |
| | | | | | | | | | |
101.SCH# | | XBRL分類拡張アーキテクチャドキュメント。 | | | | | | | | |
| | | | | | | | | | |
101.CAL# | | XBRL分類拡張はリンクベース文書を計算する. | | | | | | | | |
| | | | | | | | | | |
101.DEF# | | XBRL分類拡張はLinkbase文書を定義する. | | | | | | | | |
| | | | | | | | | | |
101.LAB# | | XBRL分類拡張タグLinkbase文書. | | | | | | | | |
| | | | | | | | | | |
101.PRE# | | XBRL分類拡張プレゼンテーションLinkbaseドキュメント. | | | | | | | | |
| | | | | | | | | | |
| 104 | | カバー相互データ(添付ファイル101に含まれるイントラネットXBRL形式) | | | | | | | | |
#同封のアーカイブ。
+管理契約または補償計画を示します。
本展示品の一部は既に機密待遇を受けている(星印で表す)。これらの情報は漏れており、米国証券取引委員会(SEC)に個別に提出されている
本展覧会のいくつかの部分(星番号で表される)は、材料ではなく、PhaseBio PharmPharmticals,Inc.が個人または機密のタイプとみなされるので省略される
*米国連邦法第18編1350条によれば、これらの証明は、1934年に改正された証券取引法第18条の目的のために提出されるのではなく、本年度報告書と共に提供されるものであり、本文書中の任意の一般的な会社言語にかかわらず、本文書の日付の前または後に行われた登録者のいかなる文書にも引用されない。
項目16.表格10-Kの概要
適用されません。
サイン
1934年の証券取引法の要求によると、登録者はすでに正式に本報告を正式に許可した署名者がそれを代表して署名することを促した。
| | | | | | | | | | | |
| PHASEBIO製薬会社 |
| | | |
| March 24, 2022 | 差出人: | | /s/John P.Sharp |
| | | ジョン·P·シャープ 首席財務官 (登録者を代表して登録者として 首席財務官と首席会計官) |
以下に署名するすべての者は、ジョナサン·P·モフとジョン·P·シャープをその真の合法的な事実代理人及び代理人として共同で構成し、任命し、十分な代替及び再代理の権力を有し、その任意及びすべての身分で、その名義、場所及び代替身分で、本PhaseBio PharmPharmticals,Inc.のForm 10-K年次報告及びその任意又はすべての修正案に署名し、これをすべての証拠物及びこれに関連する他の書類とともに証券取引委員会に提出し、当該場所内および周囲で行わなければならないすべての行為および事柄を行い、実行するために、上述した代理弁護士および代理人に十分な権力および権限を付与し、ここで、上記代理弁護士および代理人、またはその代替者を承認および確認し、本条例によってなされたすべてのことを合法的に行うことができるか、または結果として生じることを許可することができる。本報告は、1934年の証券取引法の要求に基づき、以下の者によって登録者として指定日に署名された。
| | | | | | | | | | | | | | |
サイン | | タイトル | | 日取り |
| | | | |
/s/Jonathan P.Mow | | 取締役CEO兼最高経営責任者 (首席行政主任) | | March 24, 2022 |
ジョナサン·P·モフ | | | |
| | | | |
/s/John P.Sharp | | 首席財務官 (首席財務官と責任者 会計主任) | | March 24, 2022 |
ジョン·P·シャープ | | | |
| | | | |
/s/Clay B.Thorp | | 取締役会議長 | | March 24, 2022 |
クライブ·B·ソープ | | | | |
| | | | |
Edmund P.Harrigan,M.D. | | 役員.取締役 | | March 24, 2022 |
エドモンド·P·ハーレーガン医学博士 | | | | |
| | | | |
ナンシー·J·ハドソン博士 | | 役員.取締役 | | March 24, 2022 |
ナンシー·J·ハドソン博士です | | | | |
| | | | |
| ウィリアム·D·ハンフリー | | 役員.取締役 | | March 24, 2022 |
| ウィリアム·ハンフリー | | | | |
| | | | |
キャロライン·M·ロイド | | 役員.取締役 | | March 24, 2022 |
キャロライン·M·ロイド | | | | |
| | | | |
/s/Alex C.Sapir | | 役員.取締役 | | March 24, 2022 |
アレックス·C·サピール | | | | |
| | | | |
リチャード·A·ヴァン·デン·ブルック | | 役員.取締役 | | March 24, 2022 |
リチャード·A·ファンデン·ブルック | | | | |