
添付ファイル99.1

1-2022年ノワックス。すべての権利を留保する。モルガン·チェース第40回年次ヘルスケア大会ナスダック:NVAX|2022年1月

2-2022年ノワックス。すべての権利を留保する。安全港声明:いくつかの情報、特にノワールとの未来、経営計画と将来性、パートナー関係、進行中の新冠-コロナウイルス2373、コロナウイルス-ナノフルオロTM混合ワクチン、オミック特異性ワクチンと他のノワールワクチン候補製品の情報、臨床試験結果の時間、新冠-コロナウイルス2373用量を増加させて新冠肺炎の保護(変種を含む)の可能性、未来の監督文書と行動の範囲と時間、予想される製造能力、新冠2373の世界市場機会、我々のグローバル·サプライチェーンの準備状況とNVX-CoV 2373の世界範囲内の未来の供給状況、及びNVX-CoV 2373の商業化と予想交付状況、及びこれから来る重要なマイルストーンは、すべて前向きに表現されている。前向きな陳述は、一般に、“信じる”、“可能”、“推定”、“継続”、“進行中”、“考慮する”、“意図する”、“指示”、“計画”、“計画”、“予想”、“すべき”、“将”または“仮定する”などの語、またはこれらの語、または同様の意味を有する他の語の変形を含むことができる。Novavaxは,これらの前向き陳述は多くの仮説,リスク,不確定要因の影響を受けると戒めており,これらの仮説,リスク,不確定要因は時間の経過とともに変化し,実際の結果は前向き陳述で議論された結果と大きく異なる可能性があると警告している。これらのリスクおよび不確実性には、適用可能な規制機関の要求を満たすために、プロセス同定および分析検証に関連する要求を含む、単独またはパートナーと共に様々な安全性、有効性および製品特性要件を満たす挑戦、希少な原材料および供給を得ることが困難、資源制限が含まれる, これらのリスク要因には、人材資本および製造能力、Novavaxが計画された規制経路を追求する能力、複数の商業、政府および他のエンティティとの契約要件を満たす挑戦、およびNovavaxが米国証券取引委員会に提出した2020年12月31日までのForm 10-K年度報告および後続のForm 10-Q四半期報告における“リスク要因”および“財務状況および経営結果に対する管理層の議論および分析”によって部分的に決定された他のリスク要因が含まれる。アメリカ証券取引委員会です。Govとwww.ノワックスです。COMです。展望性陳述は、現在の予想と仮定および現在利用可能なデータに基づいており、未来のイベントまたは業績の予測でもなく、未来の業績の保証でもない。現在の結果は未来の結果を予測できないかもしれない。このような陳述は、本プレスリリースまでの日付だけを説明するので、前向きな陳述にあまり依存してはいけません。法律の適用に別の要求がない限り、会社は、新しい情報、未来のイベント、または他の理由でも、いかなる前向きな陳述発表後にそれを更新または修正することを約束しない。Novavax TM(およびすべての関連標識)およびNanoFlu(商標)は、Novavax社の商標である。Matrix−M TMはNovavax ABの商標である。

3-2022年ノワックス。すべての権利を留保する。私たちの重要な勢いは

4 Novavax AT-A一覧表強力なワクチンパイプライン、現在最も深刻な感染症新冠肺炎(一次ワクチン接種、強化接種、小児科)·インフルエンザ·呼吸器合胞体ウイルスのNVX-CoV 2373に対する高効率総有効率90%·中重度疾患に対する強力な93%VoI/VOCに対する変種強力·アルファ、ベータなどへの交差保護·Delta、オミック、他社の強健な反応に対する約20億剤と2022年>20億剤の製造能力>60億人が世界170カ国以上と地域で規制権限を持つ市場に19億ドルの現金*資金を持ち、商業普及、パイプライン、拡張、拡張に利用できる潜在的戦略M&A*現金には、現金、現金等価物、および2021年9月30日現在の2022 Novavax制限現金が含まれています。すべての権利を留保する。

5-2022年ノワックス。すべての権利を留保する。NVX-CoV 2373進化する大流行に対応NVX-CoV 2373ワクチン設計·組換え蛋白技術に基づく革新ワクチンナノ粒子·全長SARS-CoV-2スパイク·独特のMatrix-M TMアジュバントを用いて調製した顕著な全世界容量は配布と管理が容易で耐性が良好かつ効率的である

世界的な規制準備状況6-2022 Novavax。すべての権利を留保する。複数の緊急使用許可を受信*血清研究所と協力して規制申請を提出**EUA請求2022年1月末*SK Bioscienceと協力して生物製品ライセンス申請(BLA)*武田COVOVAX TM/NUVIXOVID TMと協力して新薬申請を提出する予定フィリピン食品医薬品局(FDA)が完了した規制提出EUA*インドネシア共和国国家薬物·食品規制局EUA*インド医薬品監督管理局EUA*カナダ衛生部英国医薬品·保健製品監督機関豪大利亜商品治療管理局ニュージーランド医薬品安全CMAからEU委員会シンガポールから衛生サービス管理局韓国食品医薬品安全保障省*アラブ首長国連邦(UAE)衛生·防衛省米国FDA**日本保健省。世界保健機関はCovovax TMとNuvaxovid TMに対する労働と福祉の栄誉を

7-2022年ノワックス。すべての権利を留保する。NVX-CoV 2373のグローバル市場機会は、よく知られている同種の最適な効力に基づいてワクチンの躊躇問題を解決することによって、変種に対する強力な保護を含むよく知られている技術の需要に基づいて、ブースターへの持続的な需要を推進する主要なワクチン接種ブースターのワクチン接種効力および安全状態を推進して、小児科の人々が公平な分配を約束することによって世界的な需要を達成する小児科ワクチン接種を得ることを期待できるようにする

8-2022年ノワックス。すべての権利を留保する。NVX-CoV 2373は一次、強化と小児科ワクチンを供給する重大な全世界市場機会源:2021年12月までの世界銀行データとOWID。各Novavax管理層の総用量機会*加重平均部分初期レジメン接種率(少なくとも1つのCOVD-19ワクチン)**データのある国の加重平均強化ワクチン接種率*中所得国にロシアおよび中国の高所得国を含まない上-中所得国*~48億総用量需要中の低収入および低所得国~68億総用量需要一次ワクチン接種*ワクチン接種を強化**小児科ワクチン接種(12-17)未接種/未強化接種/強化接種

9-2022年ノワックス。すべての権利を留保する。GAVI/COVAX施設は、米国政府の事前購入協定·APAとGAVI·NVAXが3.5億剤·血清研究所に7.5億剤を提供することを承諾·資金承諾の一部として、NVX−CoV 2373は全世界で7.5億剤·SK Bioscienceを韓国で独占許可、タイとベトナムで非独占許可·血清研究所を取得してインドで独占許可を付与し、UMICとLMICで非独占許可を獲得·武田は日本で約11億剤の独占許可を付与·EU委員会·イギリス·カナダ·オーストラリア·ニュージーランド·スイス·アラブ首長国連邦·シンガポールは、世界的に約20億剤のNVX-CoV 2373を提供することを約束し、世界的に4億剤までのワクチンを公平かつ公平に獲得することを確保している

製造インフラは、NVX-CoV 2373 10?2022 Novavaxに対する世界の需要をサポートしている。すべての権利を留保する。Xの世界生産量が最大のワクチンメーカーは、約170カ国·地域でxを使用して大量の生産能力を提供し、グローバル生産規模と血清研究所の協力抗原生産xの複数地点での顕著なバイオリアクター能力xが調整された規制文書場所の追加地点に添加されることを支持する:Novavax CZ·血清研究所·SK生物科学·武田·Biofabri·生物製品製造センター·Fujifilm·Mabion x Novavax ABと契約製造地点での大規模生産xのNovavax ABと契約製造場所でのNovavax AB·AGC生物製品·ポリペプチド集団マトリックス-Mアジュバント生産を確保する

臨床と規制の概要11-2022年Novavax。すべての権利を留保する

ラベルと政策適応を拡大する2022 Novavax。すべての権利を留保する。戦略的方法一次ワクチン接種·より多くの市場で規制許可を得る·広範で公平なアクセスを確保するための投与量を配布·新たに出現した変種小児科ワクチンに対するより多くのデータを収集·小児科適応の規制を完了する(12-17歳)·若い人の中でワクチン接種の強化研究を開始する·追加の強化研究を開始·異種/混合マッチングのための接種促進のためのすべてのデータを利用·ラベル適応と政策提言を追求し、NVX-CoV 2373の拡張提案をサポートするために12個の追加臨床データを開発している
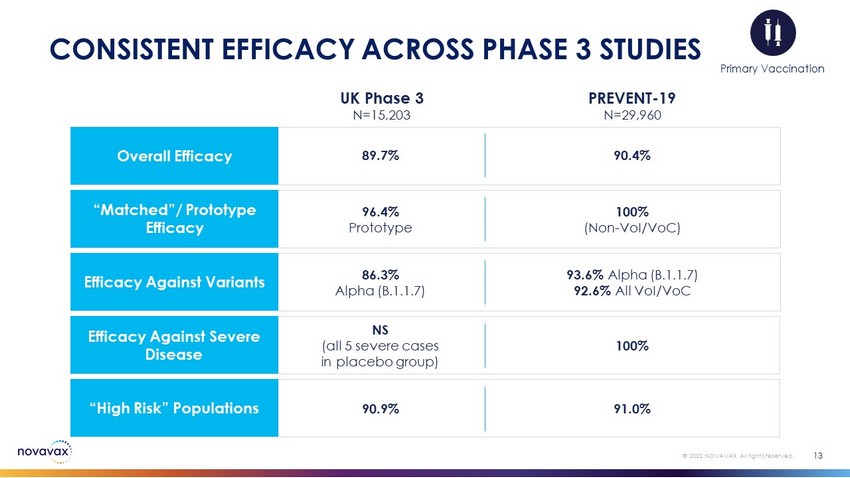
13-2022年ノワックス。すべての権利を留保する。3期研究の一致治療効果全体の治療効果89.7%90.4%“一致”/原型治療効果96.4%原型100%(非VOI/VOC)変種に対する有効性86.3%Alpha(B.1.1.7)93.6%Alpha(B.1.1.7)92.6%すべてVOI/VOC対重症NS(プラセボ群全5例の深刻な病例)100%“ハイリスク”群90.9%91.0%イギリス第三段階N=15,203予防-19 N=29,960初級ワクチン接種

142022年ヨノワックス。すべての権利を留保する。強力なデータは、2剤一次系後のピーク反応と比較してNVX-CoV 2373の異種ワクチン接種第二段階アメリカとオーストラリア·機能阻害の6倍から19.9倍(オミック)の増加を支持し、Deltaとオミックの力価は第三段階研究における保護レベルに相当するCOV-Boost(イギリス)*·メッセンジャーリボ核酸とウイルスベクターワクチン後の機能抗体力価の大幅な増加2022年に行われている研究第二段階アメリカとオーストラリアで行われている研究*大学病院サウサンプトンNHS信託基金と他の国家衛生健康保険サイトによる研究;イギリス政府ワクチンTas Kforce(VTF)と衛生と社会保健部2 b期南アフリカ予防-19支持
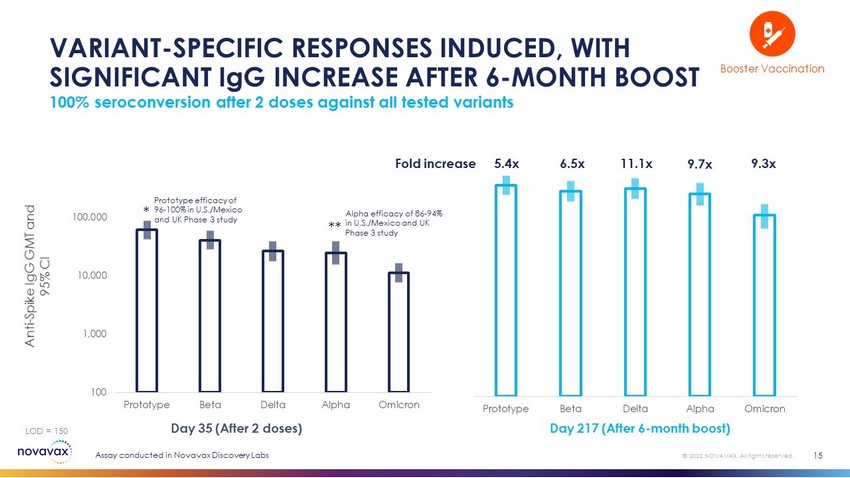
原型Beta Deltaアルファオミック100 1,000,000,100,000,000原型Beta Delta Alphaオミックフォールディング2剤後の血清陽転率はすべてのテスト変種によって誘導された変種特異的反応に100%対抗し、6ヶ月後に免疫グロブリンが有意に増加15 5.4 x 6.5 x 11.1 x 9.7 x 9.3 x 35日目(2剤後)217日目(6カ月後)の抗ピーク免疫グロブリンGMTおよび95%CI LOD=150*Novavax実験室での強化免疫オスミウム2022 Novavaxの検出を発見した。すべての権利を留保する。米国/メキシコとイギリスのプロトタイプ有効率は96%−100%,米国/メキシコとイギリスの第3段階研究ではアルファ有効率は86−94%であった
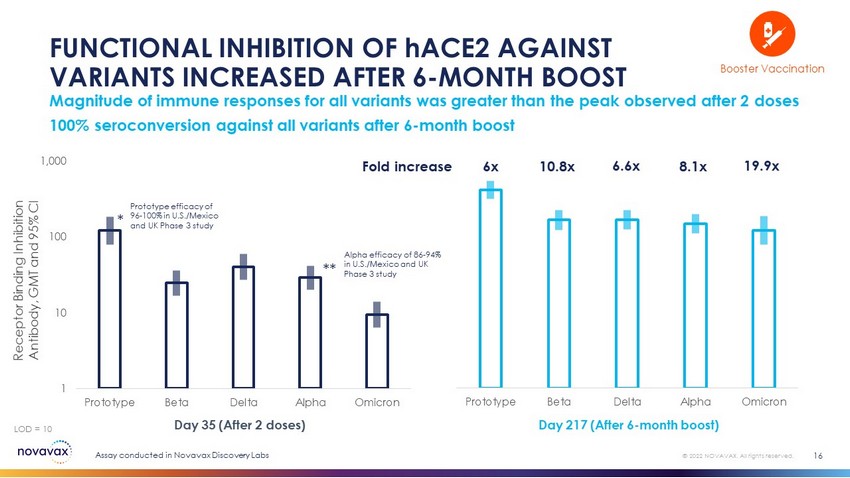
プロトベータ−アルファオミックはすべての変種に対する免疫応答が2剤後に観察されたピークより大きく,hACE 2の変種に対する機能抑制率は6カ月後に16倍に増加し,6 x 10.8 x 6.6 x 8.1 x 19.9 x 35日目(両剤後)217日目(6カ月後)の受容体結合阻害抗体,グリニッジ時間と95%CI=10 1 10 100 1,000プロトタイプベータαアルファオミック*強化免疫≡2022 Novavaxであった。すべての権利を留保する。米国/メキシコとイギリスでのプロトタイプ有効率96%−100%米国/メキシコとイギリスでの第3段階研究アルファ有効率86−94%Novavax発見実験室で行った第3段階研究分析6カ月後にすべての変異株に対して100%血清変換を行った
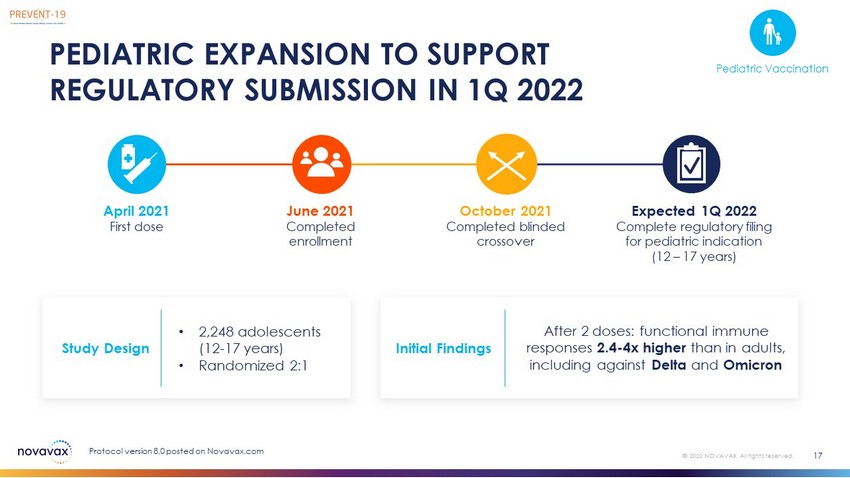
小児科拡張は、2022年第1四半期17-2022 Novavaxの規制提出をサポートする。すべての権利を留保する。プロトコルバージョン8.0は2剤ワクチン接種後にNovavax.comに発表された:機能免疫応答は成人より2.4-4倍高く、Deltaとオミックに対する機能免疫応答2021年4月と2021年6月の第1剤登録完了2021年10月に盲法交差を完了する予定2022年第1四半期に小児科適応の監督申告を完了する予定(12-17歳)研究設計·2,248名青少年(12-17歳)·ランダム2:1予備研究結果

18-2022年ノワックス。すべての権利を留保する。オミック·ワクチン開発が進行中·オミック特異的ワクチンの開発を開始·両剤の一次プログラムであるオミックワクチンに対して交差反応免疫反応を示す·オミック特異的ワクチンのGMP生産を開始し,2022年第1四半期·オミック特異的ワクチン法を開始する臨床研究により,麻薬株の変化を迅速に開発·拡大する能力があることが示唆された

19コサッチウイルス、NANOFLU(登録商標)、および共同ワクチン開発の先頭は、これら2つの疾患の革新的革新集団2022 Novavaxに対抗した。すべての権利を留保する。2021年9月·ワクチン併用開始1/2期臨床試験·安全性,免疫原性と用量発現2021年10月·1/2期臨床試験完了·2022年~640名50−70歳の成人·1/2期臨床試験のデータ公表·COVID−NanoFlu併用ワクチンとNanoFlu独立ワクチンの開始2期臨床試験
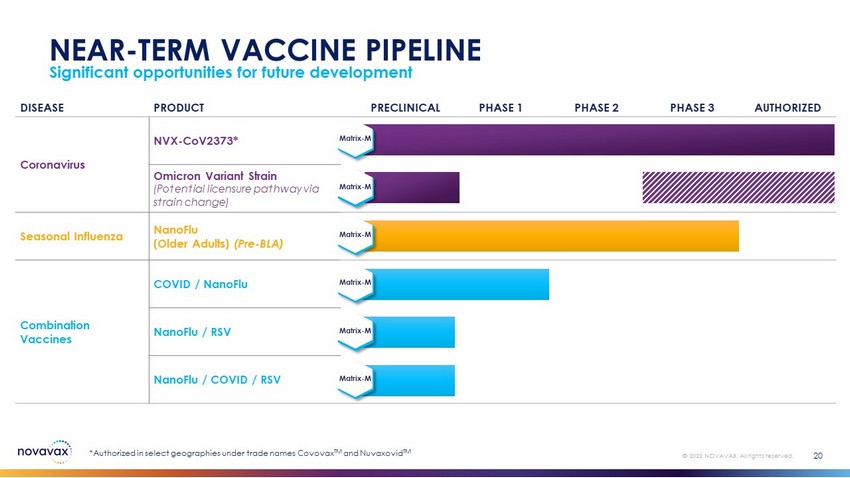
未来の発展の重要なチャンス20?2022 Novavax。すべての権利を留保する。最近のワクチンパイプライン疾患製品の臨床前第1段階第2段階第3段階でコロナウイルスNVX-CoV 2373*オミック変異株(菌株の変化によって潜在的な許可経路を得る)季節性インフルエンザNanoFlu(高齢者)(BLA前)選択された地域で許可されたCOVID/NanoFlu/RSV NanoFlu/CoVID/RSV*,商品名はCovovax TMとNuvaxovid TM Matrix-M

これから来る重要なマイルストーン2022 Novavax。すべての権利を留保する。21 NVX-CoV 2373プライマリワクチン·他の市場で規制権限を得る·認可地域で投与量を配布する·米国FDAにEUAファイルを提出する·より多くの強化研究を開始·強化ラベル適応と政策提言を追求·小児科ワクチン適応の規制を完了する(12-17歳)·若いグループで臨床研究を開始するオミック変異ワクチン·臨床研究コサッチウイルス-ナノフルオロ連合ワクチンの開始·コサッチウイルス-ナノフルオロ連合ワクチン1/2期試験1 H 2022 2 H 2022+·新冠ワクチン強化針と季節性ワクチンの再接種にワクチンを提供·開始COVID 2期臨床試験開始-NanoFlu混合ワクチンおよびNanoFlu独立ワクチン·より多くの独立した呼吸器ワクチンおよび混合気道ワクチンの開発

質疑応答2022年ノバックス。すべての権利を留保する。22