| 纳斯达克:MRNS @MarinusPharma 照片来源:Kelly Crews 摄影 Ryan(中) 患有 CDKL5 缺乏症 公司介绍 2024 年 5 月 |
| ©2024 马里努斯制药。版权所有 I 由于本演示文稿中包含的陈述不是对马里努斯历史事实的描述,它们是前瞻性陈述,反映了管理层根据1995年《私人证券诉讼改革法》的安全港条款做出的当前信念和 期望。诸如 “可能”、“将”、“期望”、“预期”、“估计”、 “打算”、“相信” 等词语和类似表达(以及其他提及未来事件、条件或情况的词语或表达)旨在识别前瞻性陈述。 本演示文稿中包含的前瞻性陈述示例包括有关我们持续经营能力的陈述;我们的预期收入和 支出;我们的ZTALMY® 商业化计划和加那索隆临床开发计划及其预期时间;临床开发时间表和里程碑; 临床试验的预期剂量;我们开始和完成临床试验注册的预计时机;预期的试验为我们的设计、定位患者群体和终点临床 试验;解读使用加那唑酮的科学依据;数据提供和发布的时机;加那唑酮的潜在安全性、有效性和治疗潜力;关于ZTALMY将为患者和医生提供的潜在益处的时机和 期望;有关监管沟通和申报的时机和期望;对我们与BARDA协议的期望;对我们当前和计划与前美国合作伙伴的合作的期望,包括潜在的好处和时机其中;对候选产品潜在市场机会的预期 ;对患者群体的预期;对潜在商业联盟的预期;对现金流、现金预测和现金流的预期 ;对持续采用ZTALMY的预期;对正在进行的科学和临床 研究投资对候选产品的影响的预期;对营业利润率的预期;商业投资计划;利用我们现有基础设施的计划和知识;我们的 全球准入计划计划及其预期收益和时机;以及我们对口服和静脉注射加那可龙未来机会的期望。 本演示文稿中的前瞻性陈述涉及重大风险和不确定性,可能导致我们的临床开发计划、未来结果、业绩或成就与前瞻性陈述所表达或暗示的 存在显著差异。除其他外,此类风险和不确定性包括与患者和医生接受ZTALMY相关的不确定性和延迟; 我们为ZTALMY获得足够市场准入的能力;我们遵守美国食品药品监督管理局(“FDA”)关于在 要求的时间范围内进行更多上市后研究的能力;监管机构包括美国食品药品管理局和欧洲药品管理局(“EMA”)的可能性”),可能不会批准或推迟 批准我们的候选产品;不确定性和与临床试验的设计、注册、完成和结果有关的延迟;意想不到的成本和支出;早期临床试验 可能无法代表以后的临床试验结果;临床试验结果可能不支持监管机构的批准或特定适应症的进一步发展; FDA或EMA的行动或建议可能会影响临床试验的设计、启动、时间、持续和/或进展,或导致需要进行更多临床试验;我们获得和维持监管 批准的能力对我们的候选产品而言;我们获得、维护、保护和捍卫候选产品的知识产权的能力;第三方专利对合作者或我们商业化加那索隆能力的潜在负面影响;候选产品的生产和供应延迟、中断或失败;候选产品在 市场的规模和增长潜力,以及我们为这些市场提供服务的能力;我们的现金和现金等价物可能不足以在预期的时间内支持我们的运营计划;我们对支出、未来收入、资本要求以及额外融资的可用性和需求的 预期、预测和估计;我们获得额外 资金以支持我们的商业和临床开发计划的能力;我们对前美国合作伙伴在美国境外将ZTALMY商业化的依赖;我们的前美国合作伙伴 违反我们的合作协议或终止协议的可能性;以及替代产品或治疗的可用性或潜在可用性适用于目标条件我们 可能会影响候选产品的可用性或商业潜力。Marinus没有义务更新或修改任何前瞻性陈述。要进一步描述可能导致实际业绩与这些前瞻性陈述中表达的结果不同的 风险和不确定性以及与我们的总体业务相关的风险,请参阅我们 向美国证券交易委员会提交的文件。你可以访问美国证券交易委员会网站www.sec.gov上的EDGAR,免费访问这些文件。 安全港声明 2 |
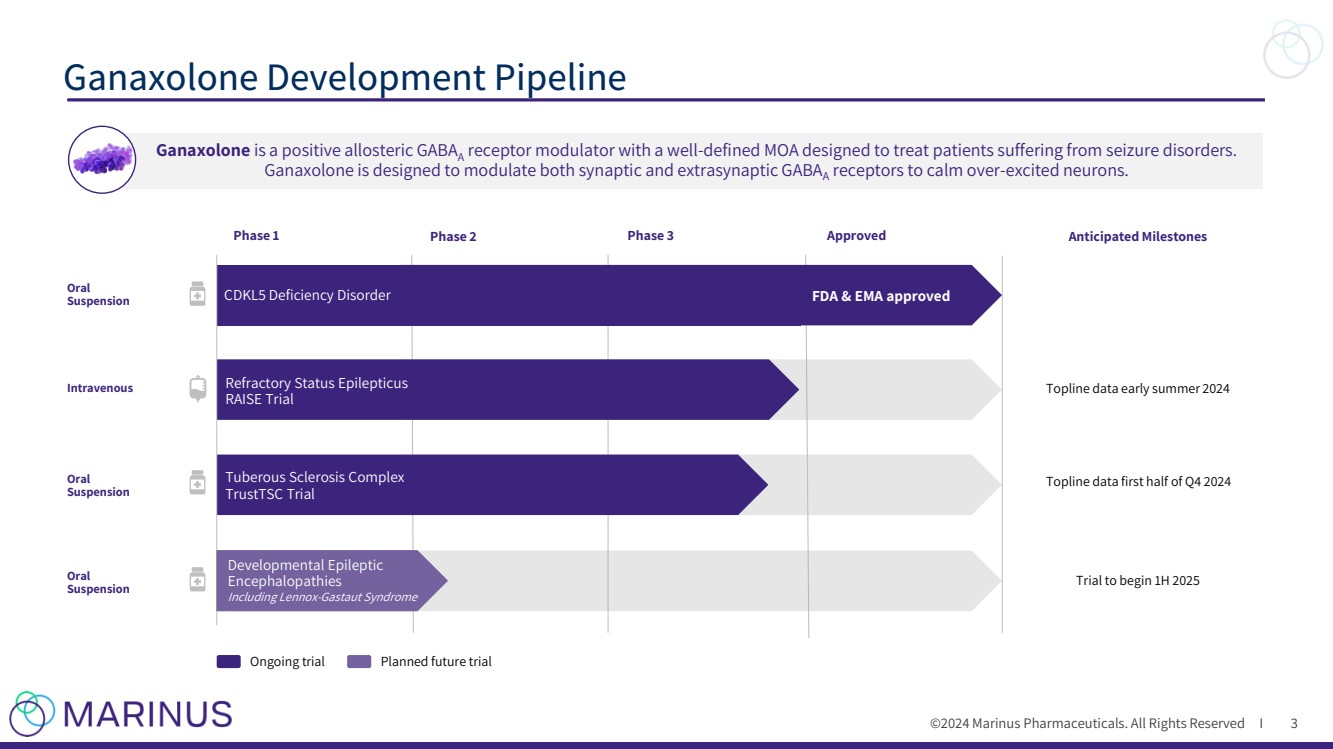
| ©2024 马里努斯制药。版权所有 I Ganaxolone 开发管道 3 Ganaxolone 是一种阳性变构的 GABAA 受体调节剂,具有明确的 MOA,旨在治疗癫痫发作障碍患者。 Ganaxolone 旨在调节突触和突触外 GABAA 受体,以镇静过度兴奋的神经元。 正在进行的试验计划中的未来试验 PDUFA 日期 2022 年 3 月 MAA 申请验证 2021 年第四季度口服 静脉注射 口服 CDKL5 缺乏症 FDA 和 EMA 批准 标题数据 2024 年初夏上半年难治性癫痫持续状态 RAISE 试验 结节性硬化综合体 结节性硬化综合体 } TrustTSC 试验 第 1 阶段 2 期 3 期已批准预期里程碑 试验将于 2025 年上半年开始发育性癫痫 脑病 包括 Lennox-Gastaut 综合征 口服 混悬剂 |
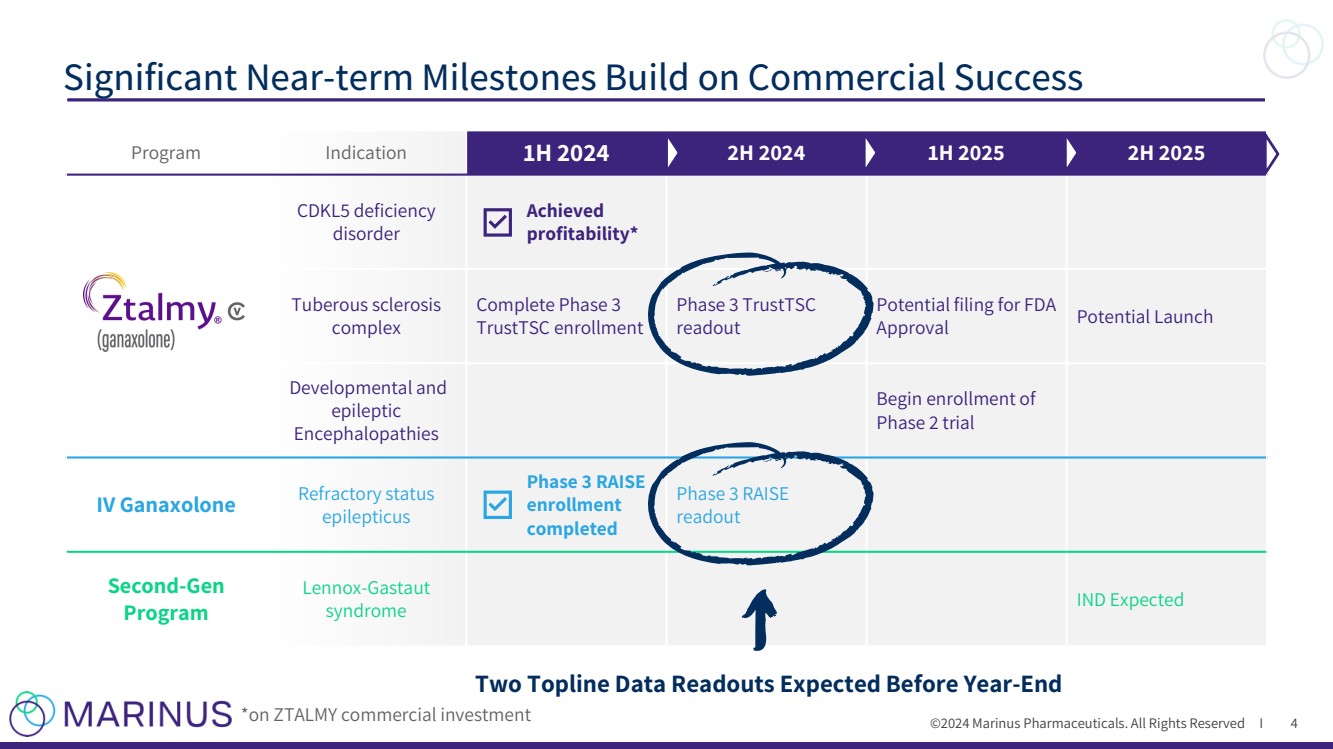
| ©2024 马里努斯制药。版权所有 I 项目指示 2024 年上半年 2024 年下半年 2025 年下半年 CDKL5 缺乏 疾病 已实现 盈利能力* 结节性硬化症 已完成第 3 阶段 TrustTSC 注册 第 3 阶段 TrustTSC 读数 可能申请 FDA 批准潜在启动 发育和 癫痫 脑病 开始注册 2 期试验 IV Ganaxolone 难治状态 癫痫 第 3 阶段 RAISE 注册 已完成 第 3 阶段 RAISE 读数 第二代 项目 Lennox-Gastaut 综合征 IND预期的 重大短期里程碑建立在商业成功的基础上 4 预计在年底前公布两份关于ZTALMY商业投资的头条数据 * |
| 商业概述 不用于促销用途 |
| ©2024 马里努斯制药。版权所有 I ZTALMY® 有可能显著推进癫痫治疗 6 差异化 MOA 解决未满足的需求 明确的 安全概况 获得 FDA 批准的可扩展商业 基础设施支持 的快速扩展和采用 重大商业 机会 CDD:CDKL5 缺乏症;MOA:作用机制 |
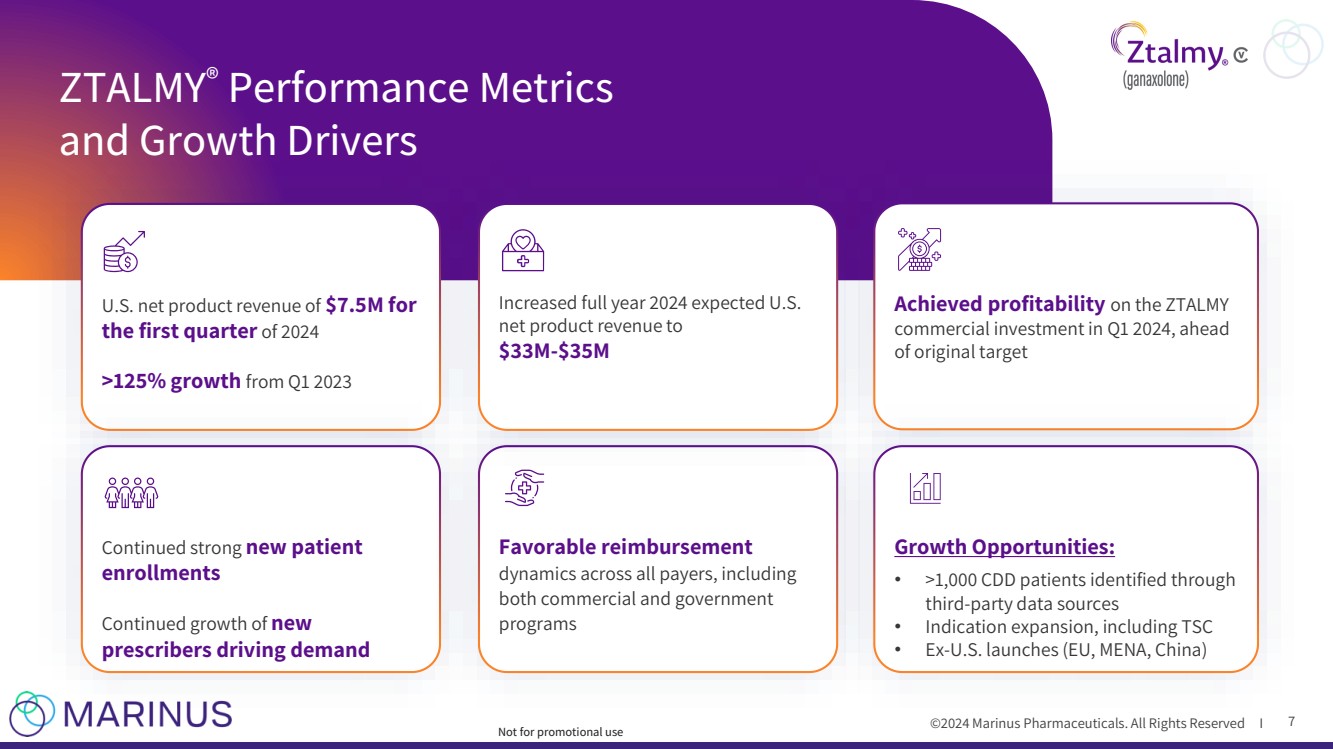
| ©2024 马里努斯制药。版权所有 I ZTALMY® 绩效指标 和增长驱动力 7 美国 2024 年第一季度净产品收入为 750 万美元 > 比 2023 年第一季度增长 125% 新患者 注册人数持续强劲 新开处方者的持续增长推动需求 在 2024 年第一季度实现盈利 在最初的目标中 所有付款人都有优惠的报销 ,包括 商业和政府 计划 不用于促销用途 预计2024年全年美国净额增加产品收入达到 3,300万至3500万美元 增长机会: • 通过 第三方数据源确定的 >1,000 名 CDD 患者 • 适应症扩展,包括 TSC • 从美国前推出(欧盟、中东和北非地区、中国) |
| 结节性硬化症复合物 “尽管混合了多种抗癫痫药物,但许多TSC患者仍会出现无法控制的癫痫发作。由于总是需要新的选择, TSC 社区欢迎对新的癫痫治疗方法进行临床评估。” -结节性硬化症联盟总裁兼首席执行官卡里·路德·罗斯贝克 |
| ©2024 马里努斯制药。版权所有 I 结节性硬化综合症 (TSC) 9 个原因 • TSC1 和/或 TSC2 基因缺陷或突变 发病率 • 6,000 例活产中约有 1 例常见 症状 • 癫痫发作、认知障碍、行为困难、皮肤/肾脏/肺部异常等 TSC 癫痫 • 大约 80-90% 的 TSC2 患者会出现癫痫 • 癫痫发作通常在出生后的第一年内开始(婴儿痉挛和/或局灶性发作)2 1.Hasbani DM & Crino PB 2018 Hand。克林。Neurol。 2。Chu-Shore CJ 等人。2010 癫痫 TSC 是最常见的遗传性癫痫之一,尽管有现有疗法,但通常 表现出高难治性的癫痫发作 |
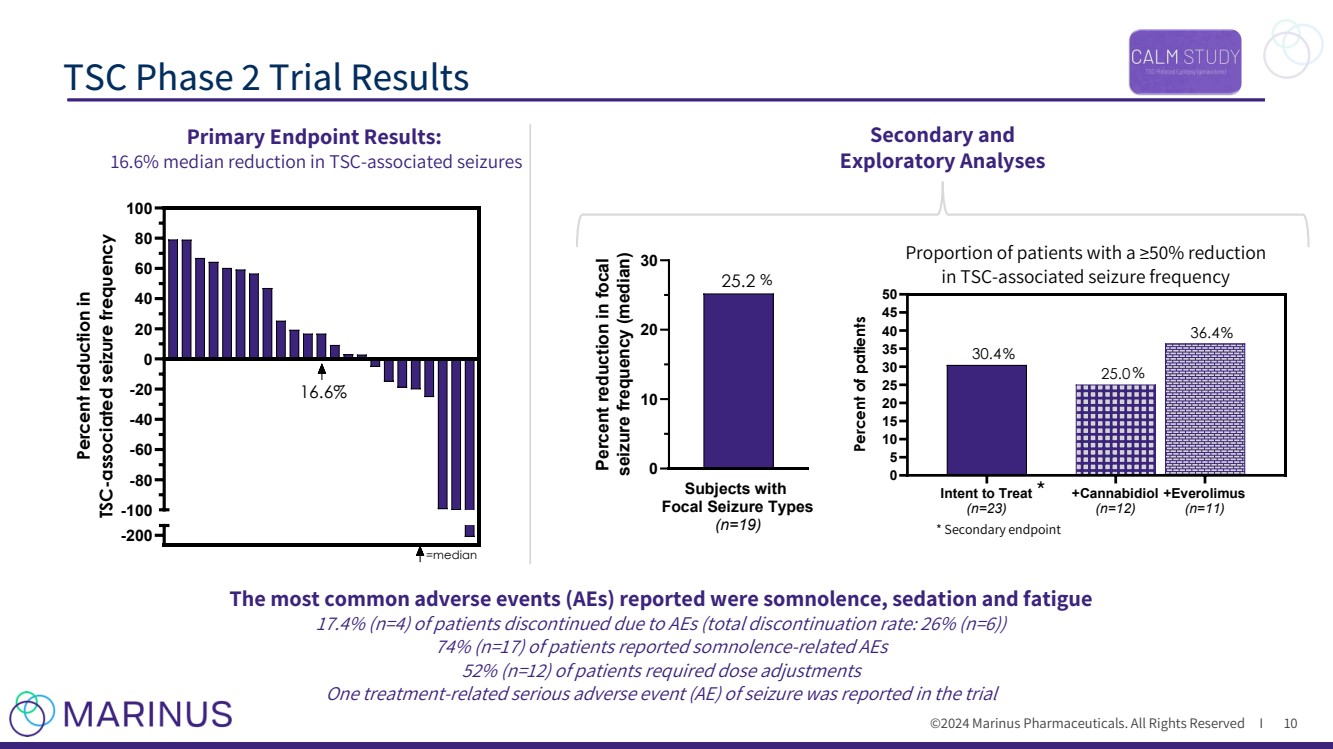
| ©2024 马里努斯制药。版权所有 I TSC 第二阶段试验结果 10 * -200 -100 -80 -60 -20 0 20 40 60 80 100 TSC 相关发作频率降低 =中位数 16.6% 次要和 探索性分析 主要终点结果: 中位数减少 16.6% 报告的最常见不良事件(AE)为嗜睡、镇静和疲劳 17.4%(n=4)因不良反应而停药的患者中(总停药率:26%(n=6)) 74%(n=17)的患者报告了与睡眠相关的不良事件 52%(n=12)的患者所需剂量调整 试验中报告了一起与治疗相关的严重癫痫不良事件 (AE) * 次要终点 与 TSC 相关的癫痫发作频率降低 ≥ 50% 的患者比例 的治疗意向 (n=23) +大麻二酚 (n=12) +依维洛莫斯 (n=11) 0 5 10 15 20 25 30 40 45 50 36.4 25.0 30.4% 的患者 % % % % 受试者 (n=19) 0 10 20 30 25.2 局灶性发作频率降低 25.2 百分比(中位数) % |
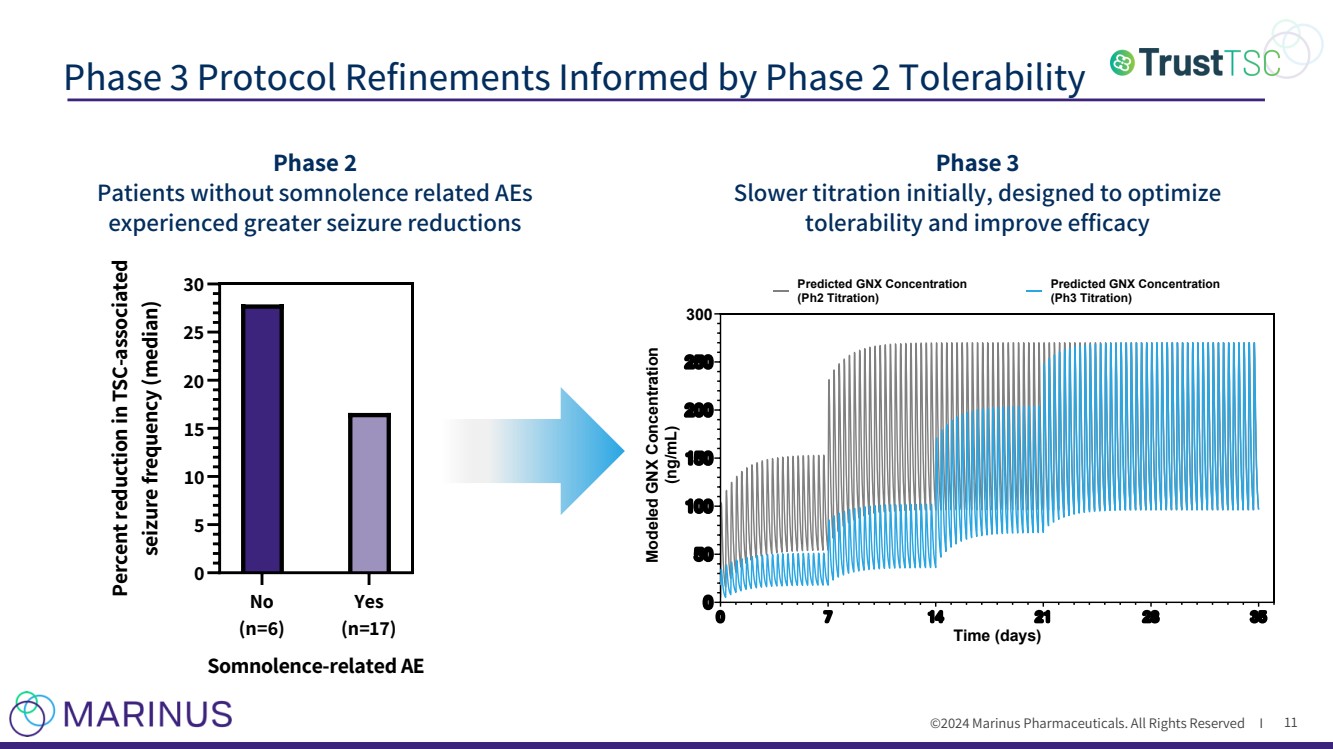
| ©2024 马里努斯制药。版权所有 I 第 3 阶段协议的改进以第 2 阶段耐受性为依据 11 第 3 阶段的滴定速度较慢,旨在优化 耐受性并提高疗效 否 (n=6) 是 (n=17) 0 5 10 15 20 25 30 与 TSC 相关的 AE 发作频率降低百分比中位数) 2 期无睡眠相关不良反应的患者 的发作减少幅度更大 0 7 14 21 28 35 0 50 10 150 20 250 时间(天) 模拟 GNX 浓度 (ng/mL) 300 预测的 GNX 浓度 (Ph2 滴定)预测的 GNX 浓度 (Ph3 滴定) |
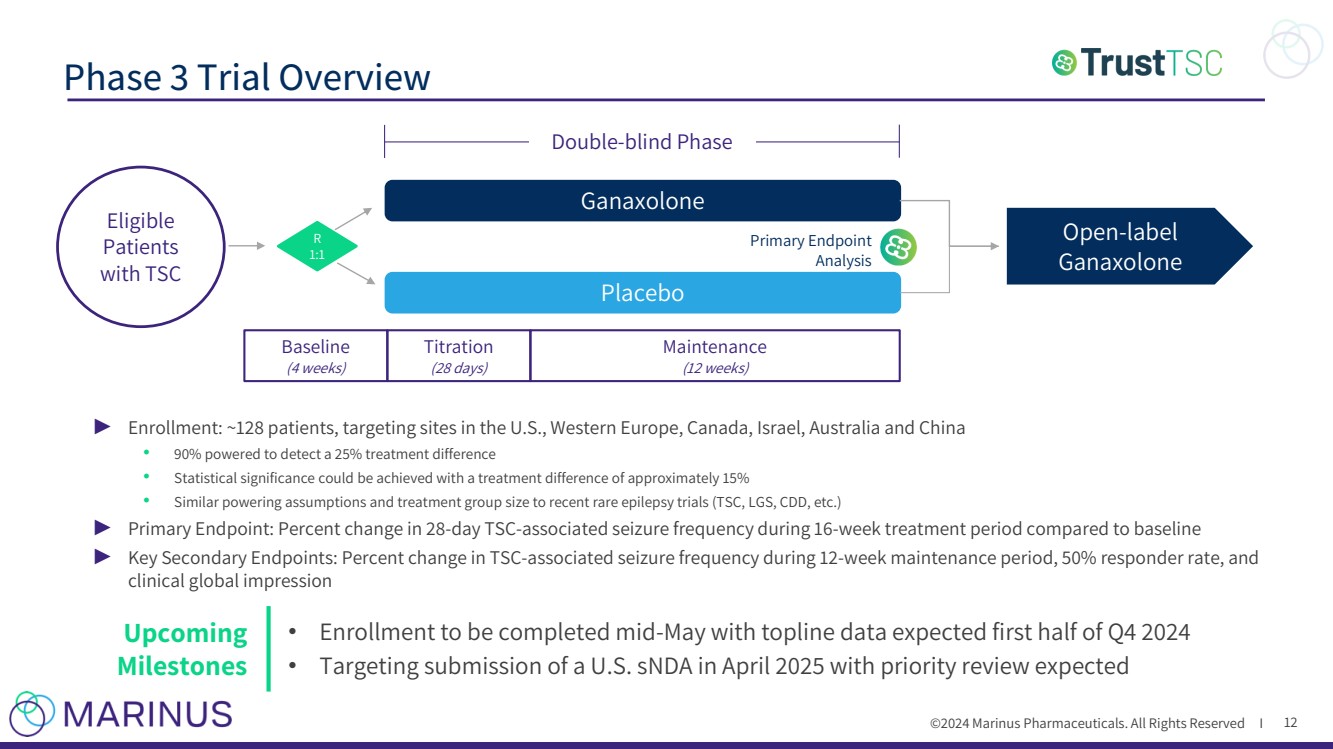
| ©2024 马里努斯制药。版权所有 I 3 期试验概述 12 ► 入组:约 128 名患者,目标受试地点位于美国、西欧、加拿大、以色列、澳大利亚和中国 • 90% 的能力检测出 25% 的治疗差异 • 治疗差异约为 15% 可以实现统计学意义 • 与最近的罕见癫痫试验(TSC、LGS、CDD 等)相似的动力假设和治疗组规模) ► 主要终点:与基线 相比,16 周治疗期间 28 天 TSC 相关发作频率的变化百分比 ► 关键次要终点:12 周维持期内 TSC 相关发作频率的变化百分比、50% 的反应率和 临床全球印象 安慰剂 基线 (4 周) 滴定 (28) 天) 维护 (12 周) 符合条件的 患者 TSC R 1:1 主要终点 分析 开放标签 Ganaxolone 双盲期 即将到来的 里程碑 •报名将于5月中旬完成,头条数据预计在2024年第四季度上半年•目标是在2025年4月提交美国SNDA,预计将进行优先审查 |
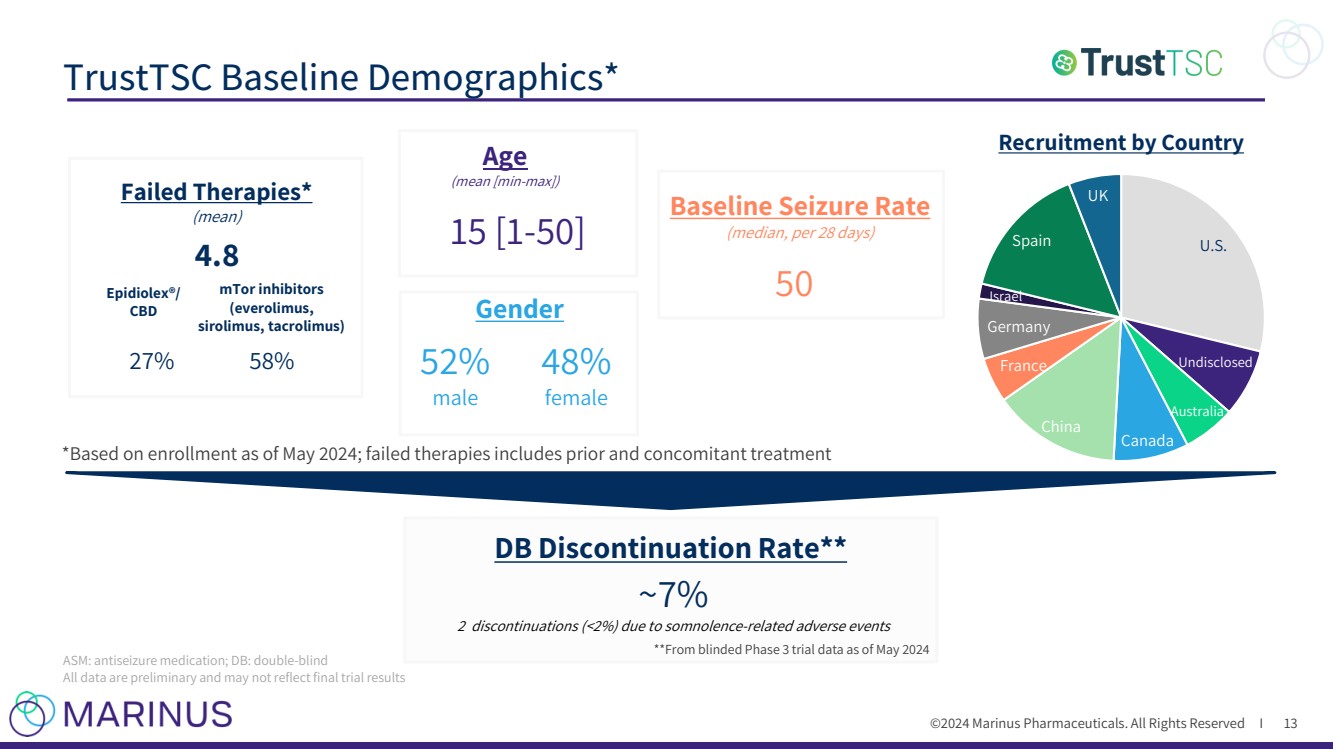
| ©2024 马里努斯制药。版权所有 I TrustTSC 基准人口统计数据* 13 年龄 (平均值 [最小-最大]) 15 [1-50] 性别 52% 男性 48% 女性 失败的治疗* (平均值) 4.8 基线发作率 (中位数,每 28 天) 50 DB 停药率** ~ 7% 2 停药 ( |
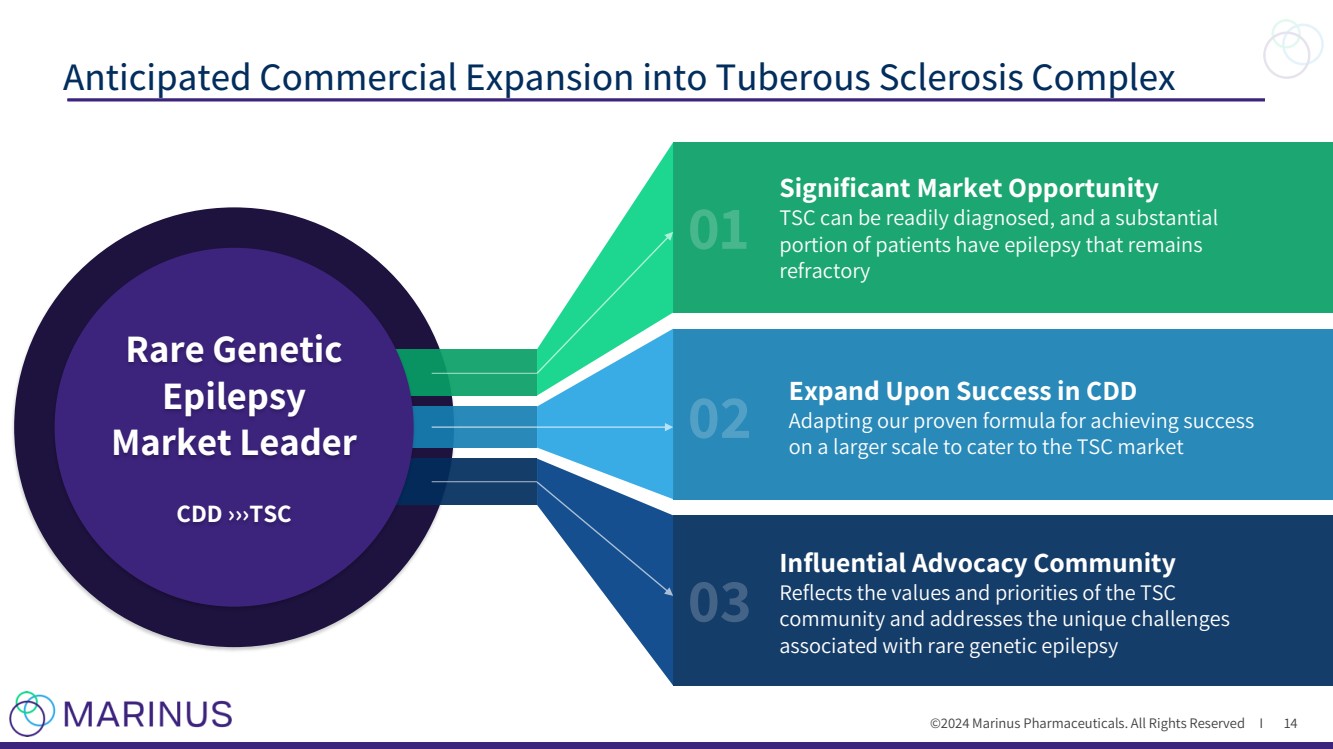
| ©2024 马里努斯制药。版权所有 I 14 有影响力的倡导社区 反映了 TSC 社区的价值观和优先事项,并解决了与罕见遗传性癫痫相关的独特挑战 重大市场机会 TSC 可以很容易地诊断,很大一部分 患者的癫痫仍然是难治性的 扩大规模以迎合 TSC 市场 稀有遗传 癫痫 市场领导者 CDD ›››› TSC 预期的商业扩张转化为结节性硬化症复合体 14 |
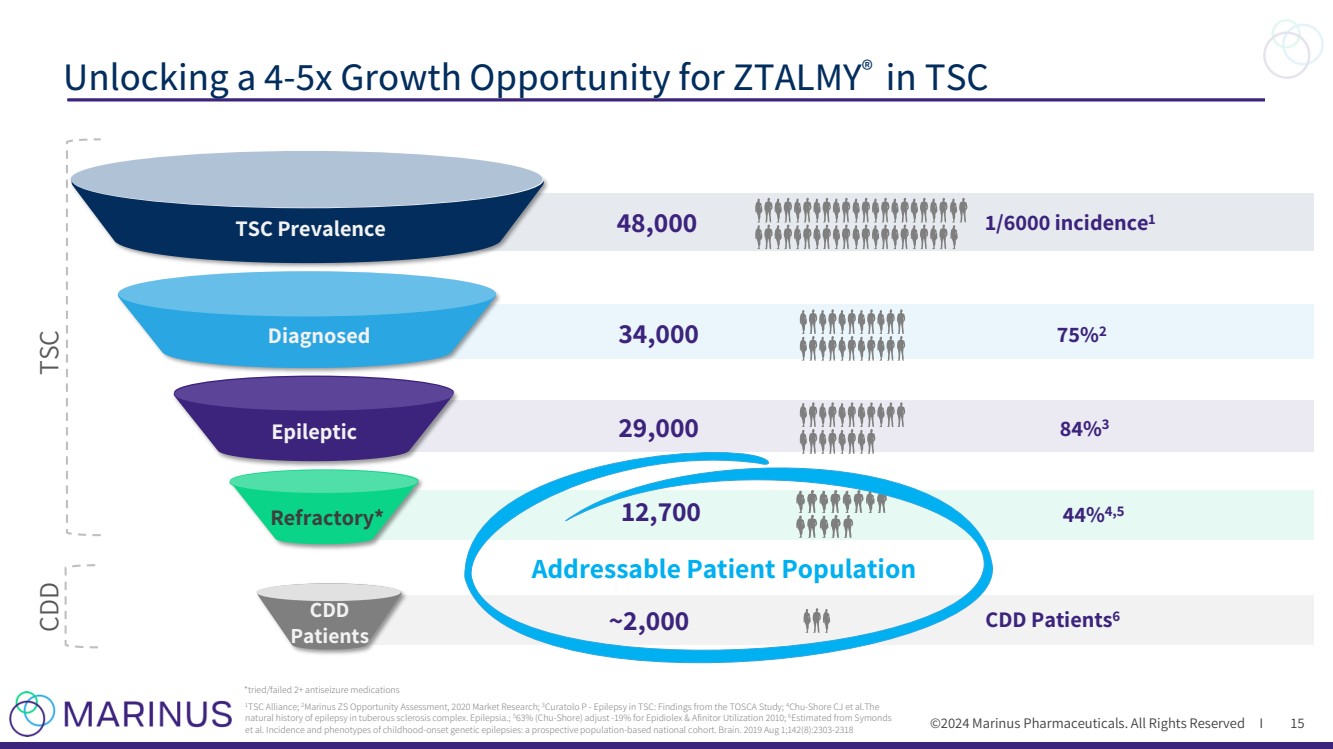
| ©2024 马里努斯制药。版权所有 I 可寻址患者群体 ~2,000 12,700 44% 4,5 CDD 患者6 难治* CDD 患者 确诊 TSC 患者 癫痫 TSC CDD 29,000 84% 3 34,000 75% 2 48,000 1/6000 发病率1 解锁 ZTAL4-5 倍的增长机会 MY® in TSC 15 1TSC 联盟;2Marinus ZS 机会评估,2020 年市场研究;3Curatolo P — TOSCA 研究结果;4Chu-Shore CJ 等人。 结节性硬化综合体癫痫的自然史。癫痫。;563%(Chu-Shore)调整了2010年Epidiolex和Afinitor利用率的-19%;6根据西蒙兹 等人估计儿童时期发作的遗传性癫痫的发病率和表型:基于人群的前瞻性全国队列。Brain。2019 年 8 月 1 日;142 (8): 2303-2318 *尝试/失败了 2+ 种抗癫痫药物 15 |
| ©2024 马里努斯制药。版权所有 I 计划利用现有的 ZTALMY® 基础设施预计将在 TSC 中产生 可观的回报 16 16 商业基础设施 增加 12-16 个 RAM 以实现关键目标, 包括 17 个 TSC CoE 市场定位 不同的 TSC 定位:第一阶段试验 ,Everolimus 和 Epidiolex 作为 concomcomlex 抗体药物 扩展目标 • 约 50% 与现有 CDD 通话 积分重叠 • 51% 的 TSC COE/诊所 的 MSL 参与度 • 40% 的 CDD KOL 还会治疗 TSC 准入策略 • 预计速度很快鉴于CDD 所有付款人的报销动态,付款人可获得广泛的付款人渠道 • Medicare D 部分 下的受保护类别 • 付款人渠道类似(医疗补助 45%、医疗保险 20%、商业 35%) • 专业药房流程提供 快速一致的配送和 支持 强有力的倡导伙伴关系 • 社区和护理人员教育 • ver 激活 现有 ZTALMY CDD 商业组织 患者识别 高诊断率和易于识别 “难治性” 患者群体 已建立的 ICD-10 代码 |
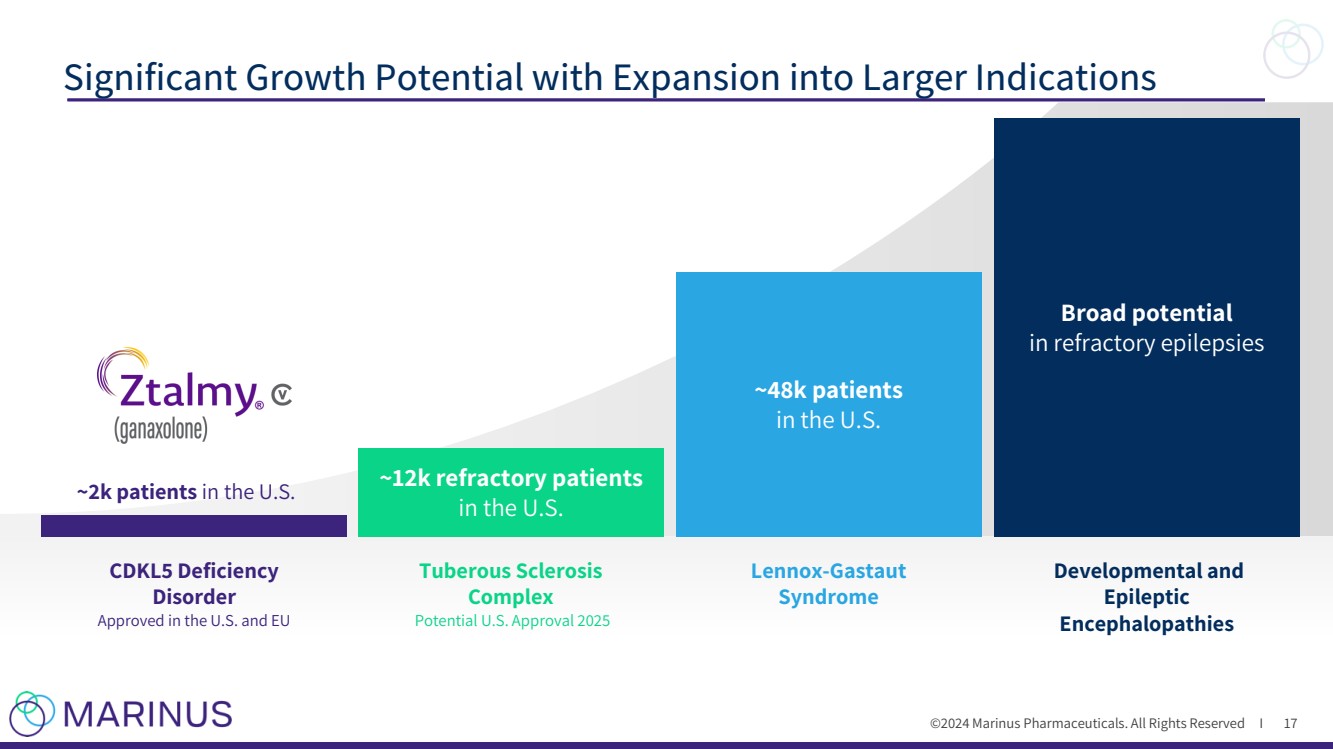
| ©2024 马里努斯制药。版权所有 I 扩展到更大适应症后有显著的增长潜力 美国 17 ~1.2 万名难治性患者 美国 ~4,8 万名患者 美国有 2k 名患者 CDKL5 缺乏 疾病 在美国和欧盟获得批准 结节性硬化症 复合体 可能在 2025 年获得美国批准 nox-Gastaut 综合症 在难治性癫痫 发育和 癫痫 脑病中潜力巨大 |
| 第二代 产品开发 |
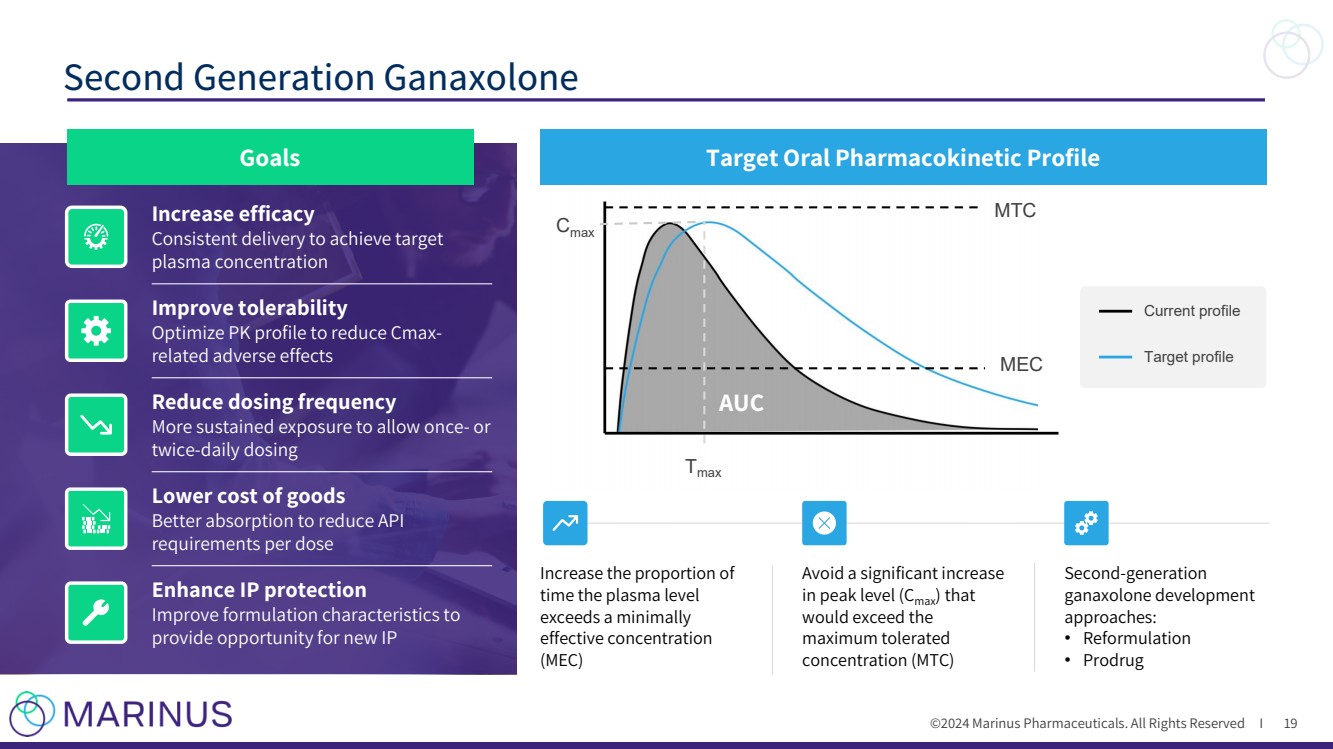
| ©2024 马里努斯制药。版权所有 I 第二代 Ganaxolone 19 个目标目标口服药代动力学特征 提高疗效 持续给药以达到目标 血浆浓度 提高耐受性 优化 PK 配置以减少 CMAX 相关的不良反应 减少给药频率 增加持续暴露以允许每天一次或 两次给药 降低商品成本 提高吸收率,降低每剂量 API 的需求 增强 IP 保护 改善配方特性 为新 IP AUC Cmax Cmax 提供机会Tmax MEC MTC 当前概况 目标概况 增加 等离子体水平 超过最低 有效浓度 的时间比例 避免峰值水平 (Cmax) 大幅增加 会超过 最大容忍 浓度 (MTC) } 第二代 加那可隆开发 方法: • 重组 • Prodrug |
| ©2024 马里努斯制药。版权所有 I 后续步骤:Prodrug 和 Ganaxolone 重新配方 20 Ganaxolone Prodrug 口服前药候选药物 目标: • 优化 PK 参数 以提高疗效、耐受性 和给药频率 增加吸收 (口服)、溶解度(IV) 临床前 IND-启用 计划中的试验 临床:IND 将在 计划中的 临床前研究完成之后进行 第二代加那可龙配方目标 1 期对第二代 代加那可龙配方的多重递增剂量 (MAD) 研究: • 初步结果显示出 宽剂量范围内的线性动力学,可以实现难治性癫痫患者的 治疗个性化 • 预计将缓释技术应用于 配方,目标是持续暴露,实现每日一或两次给药,同时允许医生将 滴定剂量剂量到更高的血清浓度的加那唑酮 • 实现稳定状态 ng/mL • 最大限度地减少峰谷变异性 • 允许每天给药一两次,同时 将足够的槽水平保持在稳定 状态(万寿菊研究 中的平均低谷水平约为 88 ng/mL) |
| 癫痫持续状态 |
| ©2024 马里努斯制药。版权所有 I 癫痫持续状态概述 22 Status Elepipticus = 由导致 发作终止的机制失效或由导致: • 发作时间异常延长(时间点 t 1 之后) • 可能产生长期后果(时间点 t2 之后) 1。DeLorenzo RJ 等人 1995 年 J Clin Neurophysiol 2.Naylor DE.癫痫公开赛。2023 3.Rossetti AO 等神经外科精神病学杂志。2006 4。Jayalakshmi S 等人缉获。2015 5.Penberthy LT 等人2005 年的缉获量 6.Guterman EL 等人。JAMA Neurol 2021 • 致残 认知缺陷3 • 发作 癫痫的风险增加 2.9 倍3 与 幸存者的显著发病率 相关: • 潜在的 SE 病因3 • 更难治的 SE4 • 治疗性昏迷 暴露量3 • 年龄增加3 • 大量直接 医疗费用5 尤其是 随着 SE 的进展 6 美国 SE 的发病率: 每年约 150,000 次 SE 发作 1 • 致残性认知 缺陷2 • 发作 癫痫的风险增加2 死亡率增加 与: 显著 有关 br} 医疗保健 利用率: |
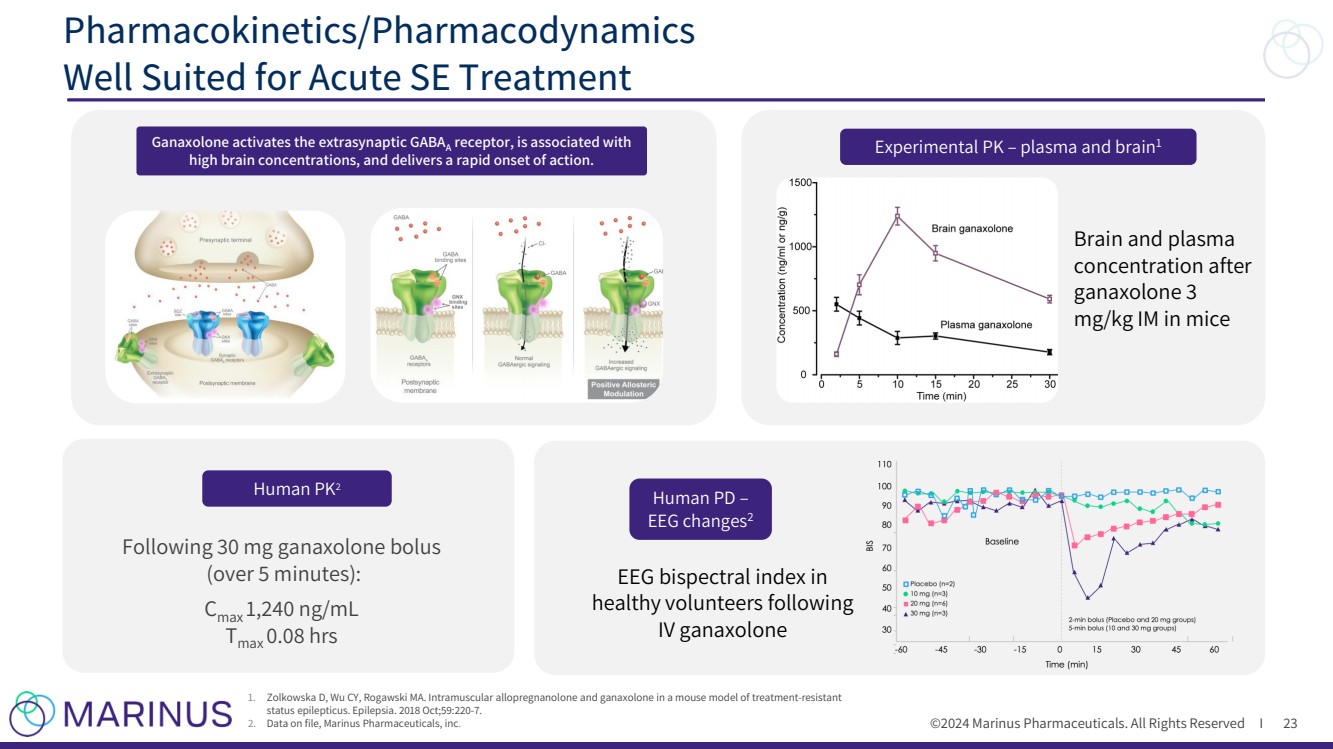
| ©2024 马里努斯制药。版权所有 I 药代动力学/药效学 非常适合急性 SE 治疗 23 实验 PK — 血浆和大脑 1 小鼠体内 ganaxolone 3 mg/kg IM 后的大脑和血浆 人体 PD — 脑电图变化2 健康志愿者的脑电图双谱指数在 IV ganaxolone 之后 IV ganaxolone 1。Zolkowska D、Wu CY、Rogawski MA。在耐药性 癫痫持续状态小鼠模型中肌肉注射别孕酮和甘那唑酮。癫痫。2018 年 10 月;59:220-7。 2。存档数据,Marinus Pharmicals, inc. Human PK2 在 30 mg ganaxolone bolus (超过 5 分钟)后: Cmax 1,240 ng/mL Tmax 0.08 小时 Ganaxolone 激活突触外的 GABAA 受体,与 高脑浓度有关,并能快速起作用。 |
| ©2024 马里努斯制药。版权所有 I 治疗期 负荷剂量维持逐渐减少 第 2 期难治性癫痫持续状态试验 (RSE) 设计 24 • 惊厥性或非惊厥性 SE 的诊断 • 至少一种二线静脉注射器失效,但尚未发展为三线静脉麻醉剂 连续 输液 2-4 天 18 小时逐渐输液 筛查治疗后随访 24 小时第 2、3、4 周 SE 患者 每日加那可龙的队列剂量 N 低 500mg/天 5 中等 650mg/天 4 高 713mg/天 8 新疗法的目标当前的局限性治疗终点 • 快速停止 • 维持发作控制 • 防止发展为 静脉麻醉剂 • 一线苯二氮卓类药物在 45%-50% 时无效;受 心血管和呼吸系统副作用的限制 • 第二线对已建立的 SE 无效;难治性 SE 的 反应进一步降低 • 第三线静脉麻醉剂:高发病率,死亡率约 35%; 住院时间和护理费用延长 • 初级:在没有 的患者中,需要升级使用静脉 麻醉剂的治疗的患者百分比 ganaxolone 启动后的前 24 小时 • 次要:其他疗效、安全性和 耐受性 8 名男性,9 名女性 平均年龄:57 岁 (范围:23-88) 17 名患者入组 |
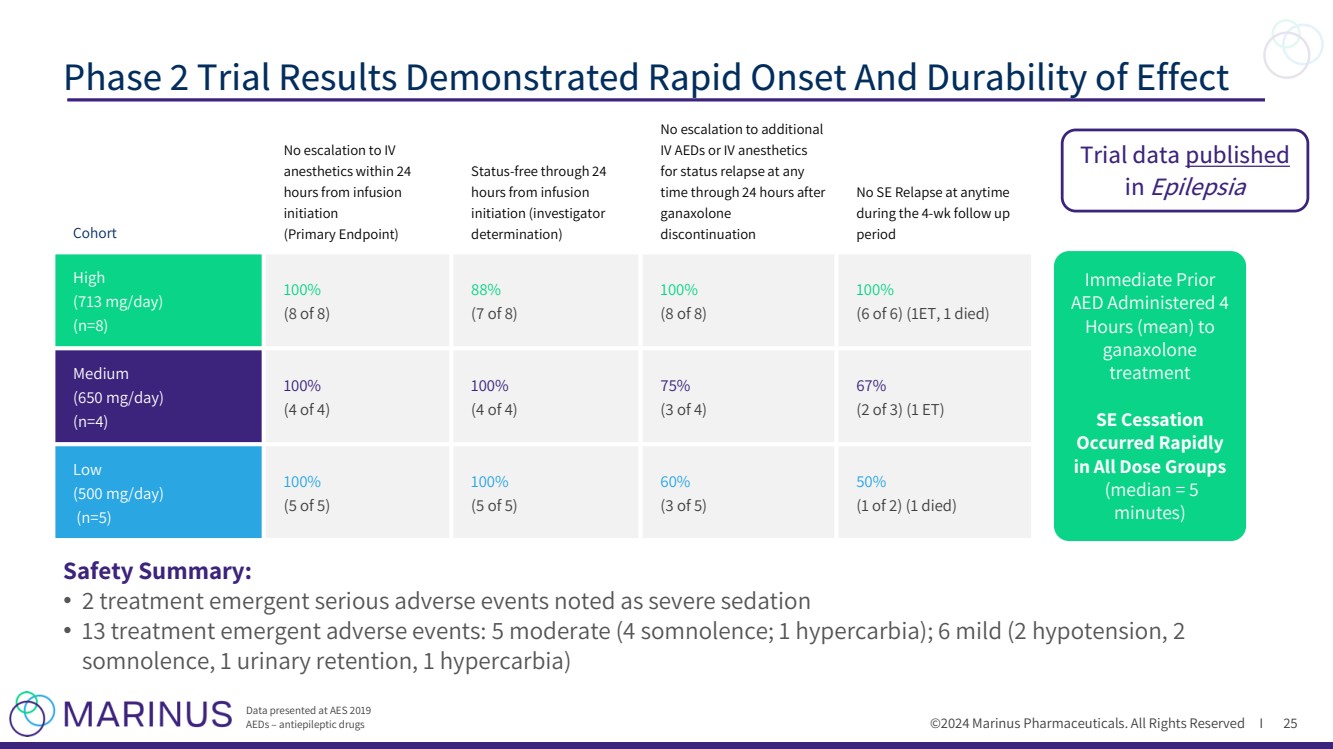
| ©2024 马里努斯制药。版权所有 I 2 期试验结果显示起效迅速,效果持久 25 在 AES 2019 AED 上公布的数据 — 抗癫痫药物 队列 在开始输液 后 24 小时内不会升级为静脉 (主要终点) (主要终点) 开始输液后 24 小时内无状态(研究者 确定) 不升级到额外 静脉注射抗癫痫药或静脉麻醉剂 用于在 停药后的 24 小时内的任何 时间内状态复发 在 4 周的随访期间任何时候 都不会复发 上升 周期 高 (713 mg/天) 100% 100% (8 个中的 8 个) 88% (8 个中的 7 个) 100% (8 个中的 8 个) 100% (6 个中的 6 个) 中等 (650 mg/天) br} (n=4) 100% (4 个中的 4 个) 100% (4 个中的 4 个) 75% (4 个中的 3 个) 67% (3 个中的 2 个)(1 个美国东部时间) (500 mg/天) 100% (5 个中的 5 个) 100% (5 个中的 5 个) 60% (5 个中的 3 个) 50% (2 个中的 1 个)(1 个死亡) AED 立即使用 加那可隆 治疗 4 小时(平均值) 所有剂量组 (中位数 = 5 分钟) 安全摘要: • 2治疗中出现的严重不良事件,记为严重镇静 • 13 个治疗紧急不良事件:5 个中度(4 个嗜睡;1 个高碳水症);6 个轻度(2 个低血压,2 个嗜睡,1 个尿潴留,1 个高碳水化合物) 发表在 Eplepisia 上的试验数据 |
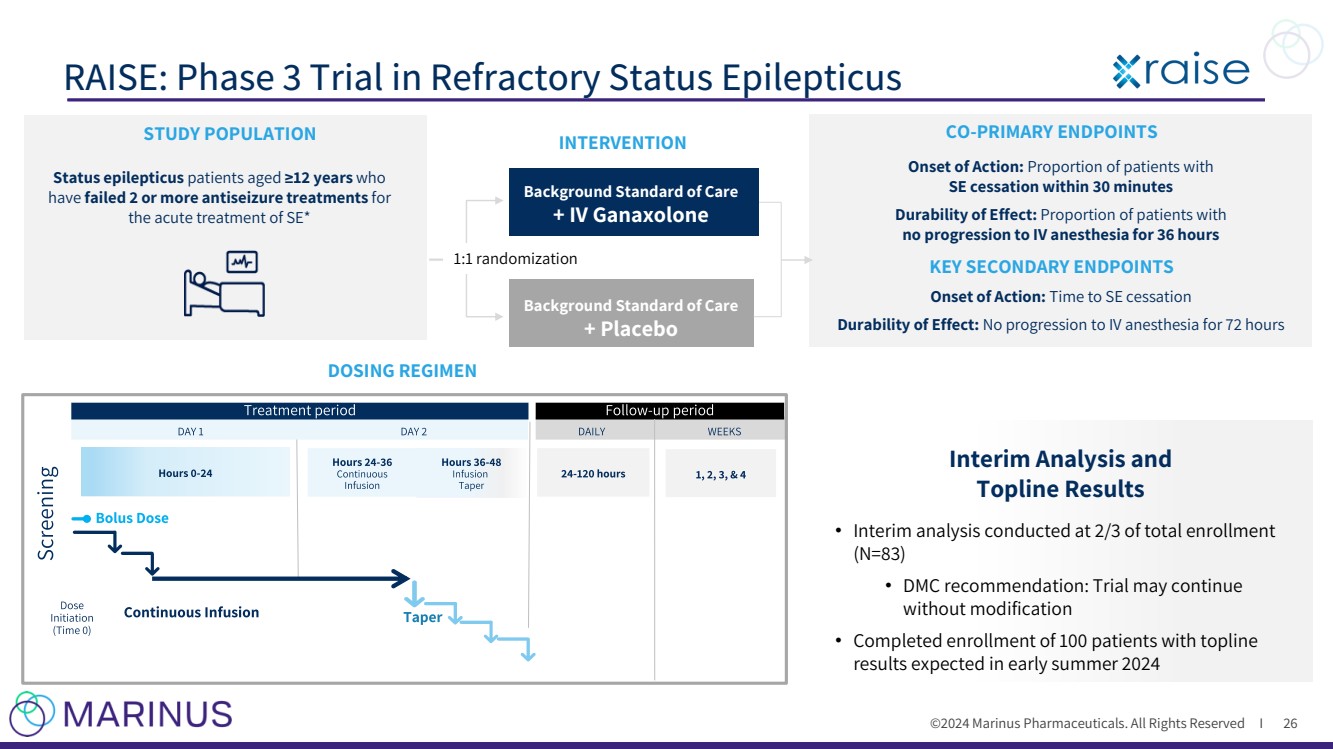
| ©2024 马里努斯制药。版权所有 I RAISE:难治性癫痫持续状态的 3 期试验 26 项研究人群干预共同主要终点 关键次要终点 起作用: 在 30 分钟内停药的患者比例 效果持续时间: 持续时间 效果持续时间:静脉麻醉在 72 小时内没有进展 年龄 ≥12 岁的癫痫持续状态患者 在 的 2 次或更多次抗癫痫治疗中失败SE* 背景护理标准 + IV Ganaxolone 1:1 随机分配 背景护理标准 + 安慰剂 给药方案 • 对总入组人数的2/3进行中期分析 (N=83) • DMC 建议:试验可以继续 ,无需修改 • 完成了100名患者的入组 topline 预计将在 2024 年初夏公布结果中期分析和 Topline 结果 |
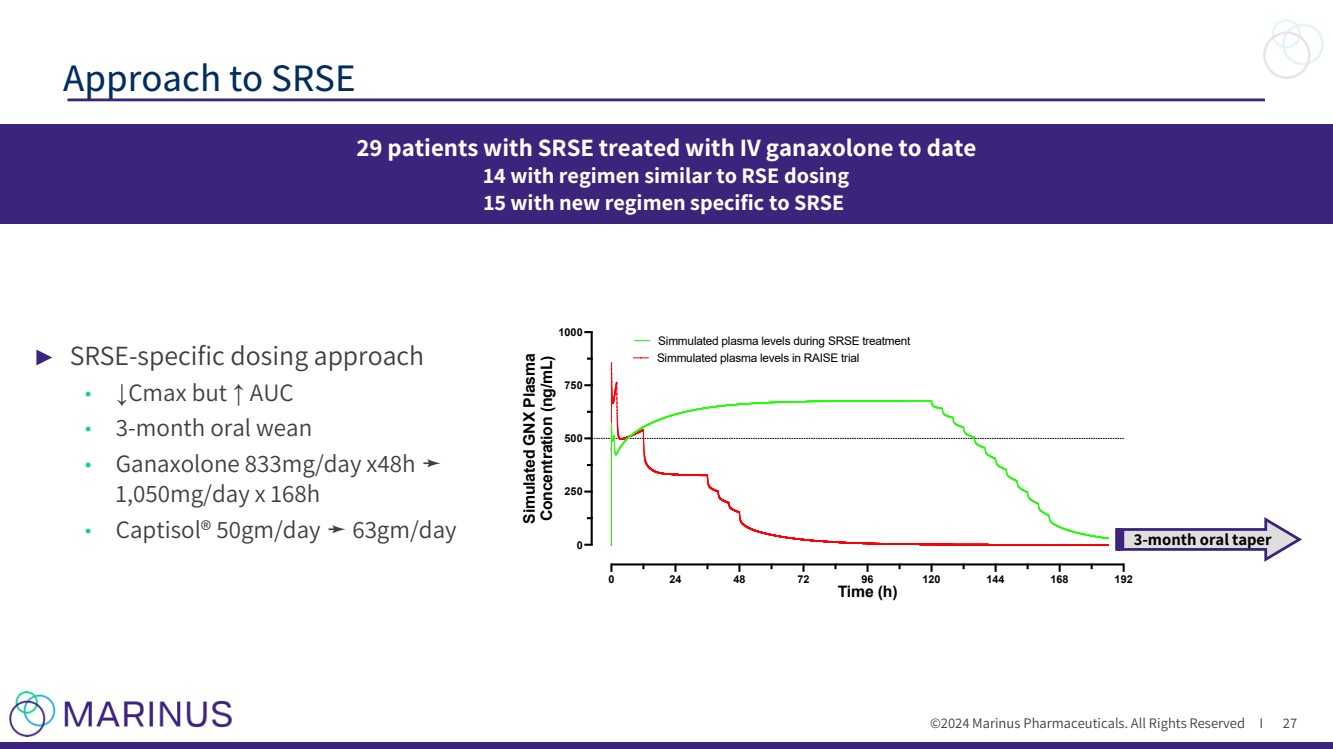
| ©2024 马里努斯制药。版权所有 I ► SRSE 特异性给药方法 • ↓ Cmax 但是 ↑ AUC • 3 个月口服断奶 • Ganaxolone 833mg/天 x48h ➛ 1,050mg/天 x 168h • Captisol® 50gm/天 ➛ 63gm/天 治疗 SRSE 27 29 名患者迄今为止,静脉注射加那可龙 14 的方案与 RSE 剂量类似 15 采用针对 SRSE 的新方案 0 24 48 72 96 120 144 168 192 0 250 500 750 1000 时间 (h) 模拟 GNX 血浆 SRSE 治疗期间的模拟血浆水平 RAISE 试验中的模拟血浆水平 } 3 个月口服逐渐变窄 |
| ©2024 马里努斯制药。版权所有 I 超级难治性癫痫持续状态:Ganaxolone 迄今为止的经历 28 新发的难治性癫痫持续状态(NORSE) 发热性癫痫综合征(FIRES) Lennox-Gastaut 综合征 PCDH-19 相关癫痫 自身免疫性脑炎 血管疾病 线粒体疾病 先天性畸形 先天性畸形 创伤后(远程) 反应先前的治疗方案新方案总计 SE 分辨率 5 (36%) 8 (53%) 13 (45%) 部分反应 6 (21%) 3 (20%) 6 (21%) 没有反应 9 (43%) 3 (20%)9 (31%) 未知 0 1 (7%) 1 (3%) 总计 14 15 29 年龄段诊断结果 年龄范围 患者 人数 1-4 岁 3 5-12 岁 6 13-17 岁 4 18 + 16 总计 29 |
| 财务更新 |
| ©2024 马里努斯制药。版权所有 I 财务概览 30 分析师报道*: 坎托·菲茨杰拉德:查尔斯·邓肯博士 T.D. Cowen:约瑟夫·托姆博士 H.C. Wainwright & Co: Douglas Tsao JMP 证券:杰森·巴特勒博士 拉登堡塔尔曼:希金斯 奥本海默:杰伊·奥尔森 加拿大皇家银行:布莱恩·亚伯拉罕斯 RW Baird:Brian Skorney Leerink Partners:Marc Goodman Truist:Joon Lee,医学博士,博士 *注意:个别分析师对马里纳斯的观点、估计和预测不代表观点、估计和 Marinus 的预测。上述清单并不表示赞同或赞同他们的信息、结论或建议。 纳斯达克:MRNS 2024 年全年指引 收入: • 美国 ZTALMY 净产品收入:3,300万美元至3500万美元 运营费用 • 2024 财年 GAAP 运营支出(SG&A 和研发)在 1.35 亿美元至 1.4 亿美元之间;包括约 2,000 万美元的 非现金股票薪酬 财务摘要(截至 2024 年 3 月 31 日): • 1.133 亿美元的现金、现金等价物和短期 投资 • 2025 年第一季度的现金跑道 • 7,500 万美元的债务;仅在 2024 年 5 月之前的利息,2026 年到期 • 已发行5,490万股;完全 持有 6,800 万股股票稀释基础1 1 完全摊薄总额包括预先注资的认股权证和未偿还股票期权以及RSU的影响 |
| ©2024 马里努斯制药。版权所有 I 推动 ZTALMY®(ganaxolone)的全球准入 31 欧洲:与 Orion Corporation 签订合作协议,在 CDD、TSC、RSE 领域达成加那索龙的合作协议 • 开发、商业和销售里程碑高达 9,000 万欧元1;分级特许权使用费低至青少年(口服停药)和 20 岁以下(IV) • 在实现某些CDD启动里程碑后,Marinus有资格获得1,000万欧元的补助金 中国:与泰纳西亚生物技术在CDD、TSC、SE 领域签订加纳索隆的合作协议 • 高达2.56亿美元开发、商业和销售里程碑2;分级两位数特许权使用费 中东和北非地区:与Biologix Fzco签订加那索隆分销协议 • 具有监管里程碑的收益分成安排 计划于2023年第四季度启动,旨在扩大与CDD相关的癫痫发作患者在非合作市场获得ZTALMY的全球渠道 1视某些临床和商业启动的实现而定与 CDD、 TSC 和 RSE 相关的里程碑以及口服和静脉注射产品的年化销售门槛 2视情况而定CDD 和 TSC 获得监管部门的批准 |
| 知识产权 |
| ©2024 马里努斯制药。版权所有 I 多层潜在保护 33 CDD 和 PCDH19 的孤儿药认定分别在美国和欧盟提供 7 年和 10 年的监管排他性。 SE 的孤儿药指定在美国提供 7 年的监管独家经营权 美国专利/专利申请到期日期 癫痫持续状态 使用方法 临床方案获得专利 2040 年使用更广泛加那可龙剂量的临床方案获得专利 2040 年 SRSE 和 ESE 2041/2042 配方 Licences 2041/2042 配方 Licensed Captiress Sol® 专利截至 2033 年静脉注射配方待处理的申请 2036 年 CDKL5 缺乏症 使用方法 用于治疗 CDKL5 缺乏症的方法的专利已获批准(许可)疾病 2037 剂量方案待审申请 2038/2041/2042 配方已获专利(口服悬浮液)2031(如获得 PTE 授权) 结节性硬化症综合体 使用方法 已获授专利 2040 新给药方案的申请待批准 2041/2042 配方授予(口服悬浮液)2031(如果 PTE 获得批准) 第二代 Ganaxolone 配方申请正在等待第二代配方 2042/2043 |
| 附录 |
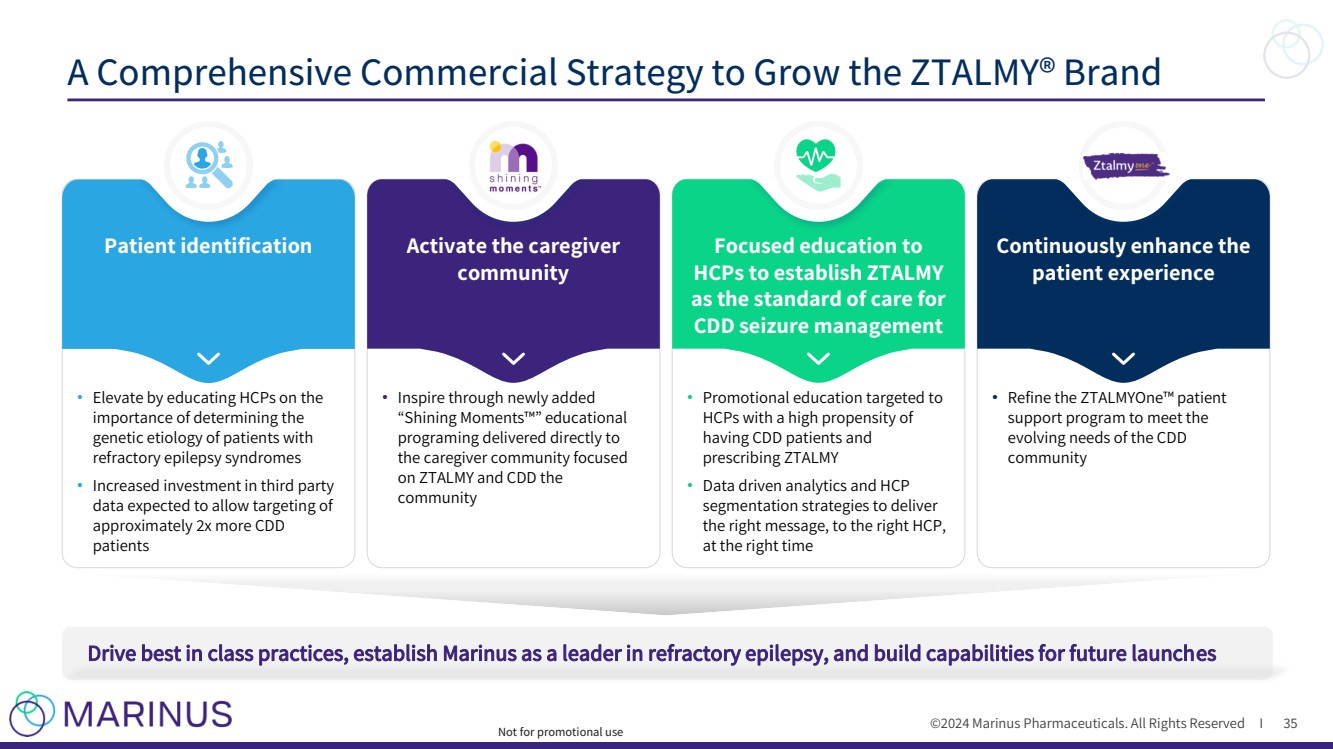
| ©2024 马里努斯制药。版权所有 I 发展 ZTALMY® 品牌的全面商业战略 35 患者识别激活护理人员 社区 重点教育,将 ZTALMY 确立为 CDD 发作管理的护理标准 持续增强 患者体验 • 通过教育医疗保健工作者认识确定 的重要性来提升患者体验 难治性癫痫综合征患者的遗传病因 • 增加对第三方 数据的投资预计将允许靶向 的CDD增加约2倍 患者 • 通过新增加的 “光辉时刻” 教育 项目激发灵感,护理人员社区将 重点放在 ZTALMY 和 CDD 上 社区 • 针对极倾向 患有 CDD 患者和 处方 ZTALMY 处方的 HCP 的宣传教育 • 数据驱动的分析和 HCP } 细分策略,在正确的时间向正确的 HCP 传达 正确的信息 • 完善 ztalmyOne 患者 支持计划,以满足 CDD 社区不断变化的需求 开出一流的赛车实践,确立马里努斯作为难治性癫痫领域的领导者的地位,并为未来的发布建立能力 不用于促销目的 |
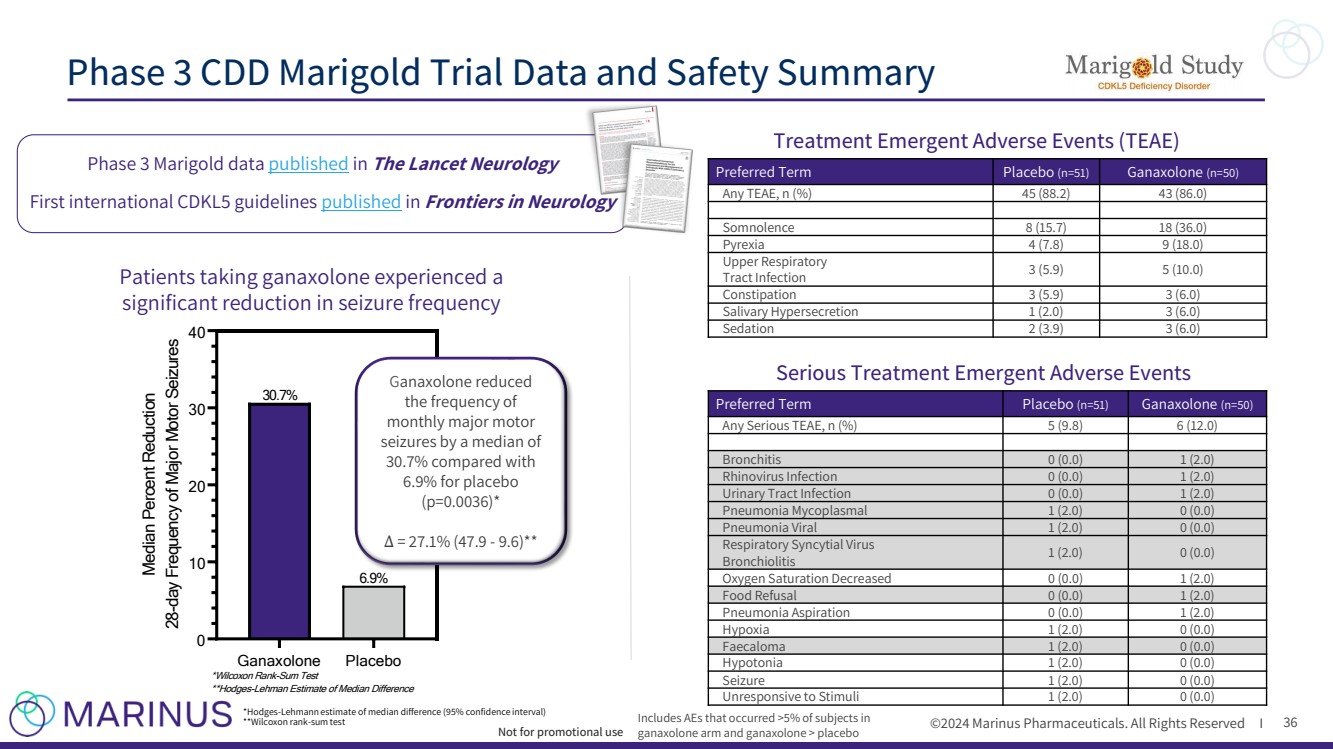
| ©2024 马里努斯制药。版权所有 I 36 Ganaxolone 安慰剂 0 10 20 30 40 中位数减少百分比 28 天运动发作频率 30.7% 6.9% *Wilcoxon Rank-Sum 测试 **Hodges-Lehman 对中位数差异的估计 服用加那唑酮的患者发作频率显著降低 Ganaxolone 减少了 br} 每月主要运动 发作频率中位数为 30.7%,而安慰剂 的发作频率为 6.9%(p=0.0036)* = 27.1%(47.9-9.6)** *霍奇斯-莱曼估计的中位差异(95% 置信区间) **Wilcoxon rank-sum 测试 在《柳叶刀神经病学》上发布的第三期万寿菊数据 在《神经病学前沿》上发表的第一份国际 CDKL5 指南 三期 CDD 万寿菊试验数据和安全性摘要 不用于促销用途 治疗紧急不良事件 (TEAE) 首选术语安慰剂 (n=51) Ganaxolone (n=50) 任何 TEA AE,n (%) 45 (88.2) 43 (86.0) Somnolence 8 (15.7) 18 (36.0) 发热 4 (7.8) 9 (18.0) 上呼吸道 道感染 3 (5.9) 5 (10.0) 便秘 3 (5.9) 3 (5.9) 3 (6.0) 唾液分泌过多 1 (2.0) 3 (6.0) 镇静 2 (3.9) 3 (6.0) 包括 ganaxolone 组和 ganaxolone > 安慰剂 首选术语安慰剂 (n=51) Ganaxolone (n=50) 任何严重的 TEAE,n (%) 5 (9.8) 6 (12.0) 支气管炎 0 (0.0) 1 (2.0) 鼻病毒感染 0 (0.0) 1 (2.0) 尿路感染 0 (0.0) 1 (2.0) 肺炎支原体 1 (2.0) 0 (0.0) 肺炎病毒 1 (2.0) 0 (0.0) 呼吸道合胞病毒 细支气管炎 1 (2.0) 0 (0.0) 氧饱和度降低 0 (0.0) 1 (2.0) 拒食 0 (0.0) 1 (2.0) 肺炎吸入 0(0.0) 1 (2.0) 缺氧 1 (2.0) 0 (0.0) 粪便 1 (2.0) 0 (0.0) 低血压 1 (2.0) 0 (0.0) 发作 1 (2.0) 0 (0.0) 对刺激无反应 1 (2.0) 0 (0.0) 严重治疗紧急不良事件 |
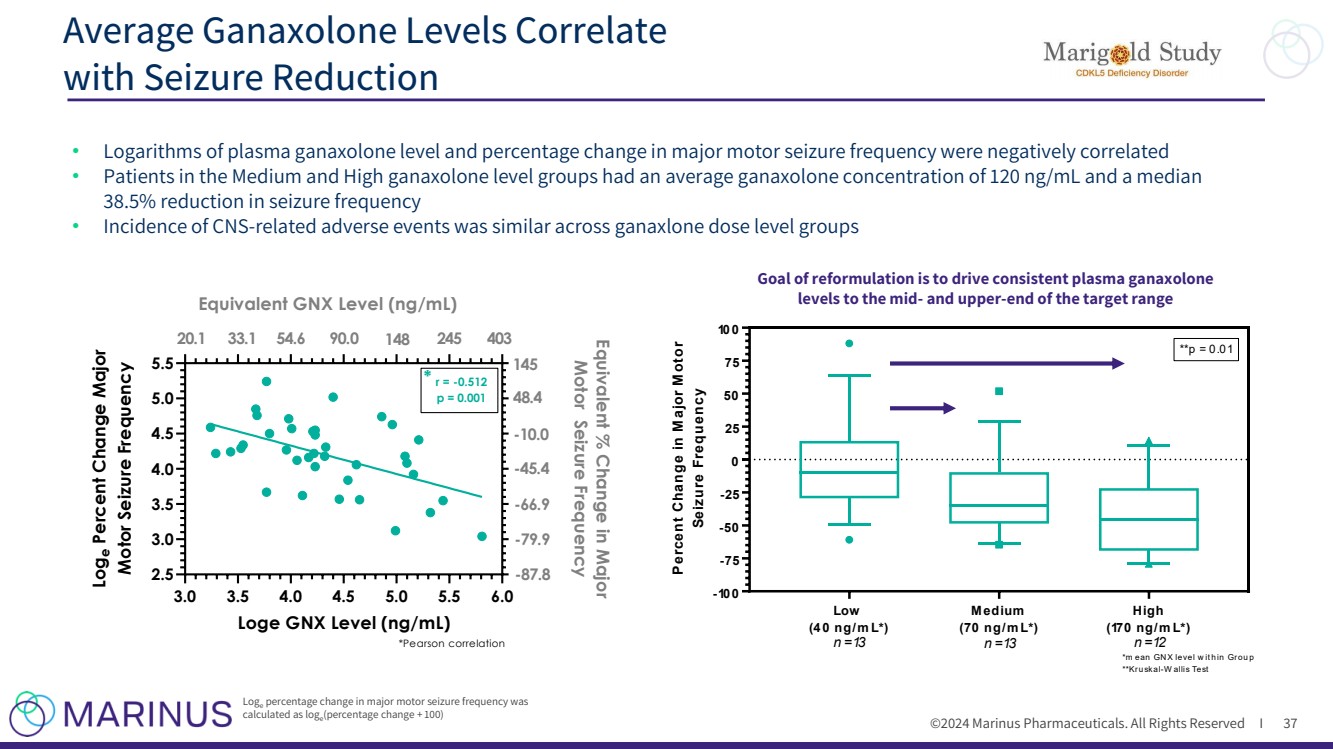
| ©2024 马里努斯制药。版权所有 I 平均加那唑酮水平与 发作减少的相关性 37 • 血浆加那可龙水平的对数和主要运动发作频率的变化百分比呈负相关 • 中、高加那可龙水平组患者的加那可龙平均浓度为 120 ng/mL,发作频率中位数降低 38.5% • 发作频率 • 发作频率中位数 • 发作频率降低 38.5% 不同剂量组中与中枢神经系统相关的不良事件相似 Loge 主要运动发作频率的变化百分比由 计算得出 loge (百分比变化 + 100) 3.0 3.5 4.0 4.5 5.0 5.0 3.0 3.5 4.0 4.5 5.5 Loge GNX 级别 (ng/mL) Loge 百分比变化主要运动发作频率 等效百分比重大运动发作频率的变化 r = -0.512 p = 0.001 *皮尔逊相关性 * 145 48.4 -10.0 -45.4 -66.9 -87.8 等效值 GNX 等级 (ng/mL) 20.1 33.1 54.6 90.0 148 245 403 低 (40 ng/m L*) 中 (70 ng/m L*) 高 (170 ng/m L*) -100 -75 -50 -25 0 25 50 75 100% 主要运动发作频率的变化 **p = 0.01 *m ean GNX 等级 h 在群组 p **Kruskal-w allis 测试 n =13 n =13 n =12 重新配方的目标是将稳定的血浆甘那唑酮 水平提高到目标范围的中端和上端 |
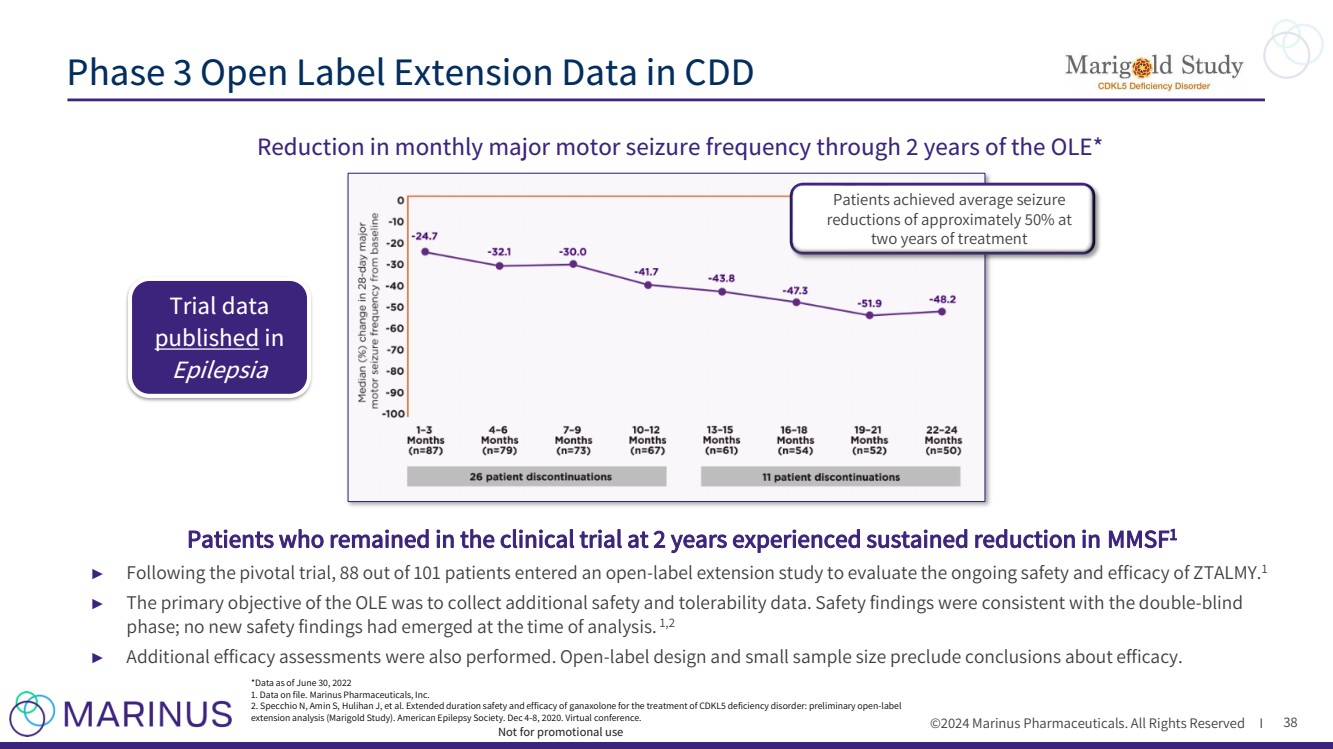
| ©2024 Marinus Pharmaceuticals. All Rights Reserved I Patients who remained in the clinical trial at 2 years experienced sustained reduction in MMSF1 ► Following the pivotal trial, 88 out of 101 patients entered an open-label extension study to evaluate the ongoing safety and efficacy of ZTALMY.1 ► The primary objective of the OLE was to collect additional safety and tolerability data. Safety findings were consistent with the double-blind phase; no new safety findings had emerged at the time of analysis. 1,2 ► Additional efficacy assessments were also performed. Open-label design and small sample size preclude conclusions about efficacy. 38 Reduction in monthly major motor seizure frequency through 2 years of the OLE* Phase 3 Open Label Extension Data in CDD Not for promotional use Patients achieved average seizure reductions of approximately 50% at two years of treatment *Data as of June 30, 2022 1. Data on file. Marinus Pharmaceuticals, Inc. 2. Specchio N, Amin S, Hulihan J, et al. Extended duration safety and efficacy of ganaxolone for the treatment of CDKL5 deficiency disorder: preliminary open-label extension analysis (Marigold Study). American Epilepsy Society. Dec 4-8, 2020. Virtual conference. Trial data published in Epilepsia |
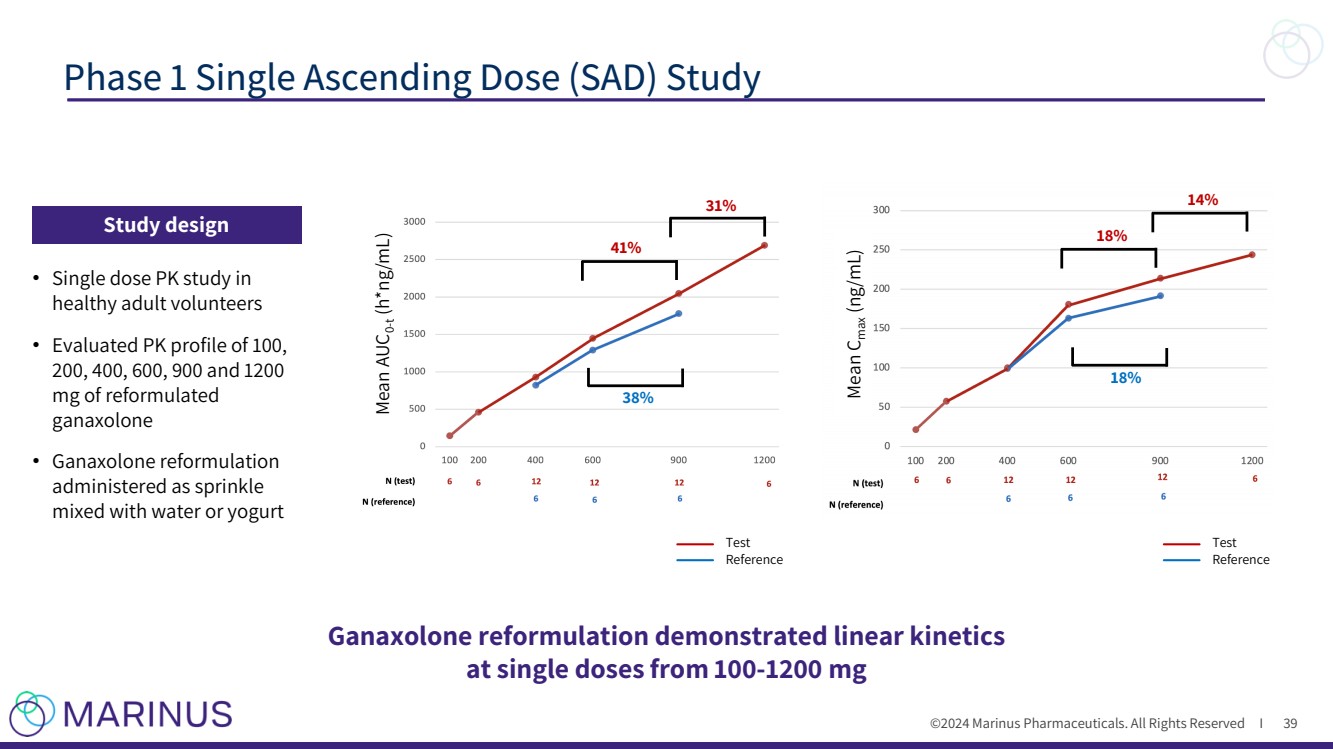
| ©2024 Marinus Pharmaceuticals. All Rights Reserved I Phase 1 Single Ascending Dose (SAD) Study 39 39 Mean Cmax (ng/mL) Mean AUC0-t (h*ng/mL) 41% 31% 38% 18% 18% 14% Study design Ganaxolone reformulation demonstrated linear kinetics at single doses from 100-1200 mg • Single dose PK study in healthy adult volunteers • Evaluated PK profile of 100, 200, 400, 600, 900 and 1200 mg of reformulated ganaxolone • Ganaxolone reformulation administered as sprinkle mixed with water or yogurt Test Reference Test Reference |