目录表
| 药物滥用,或NIDA,以进一步评估TRV734对OUD的管理,NIDA于2019年12月启动了一项关于这一适应症的概念验证研究。2021年6月,我们宣布因全球新冠肺炎疫情而暂停的研究重新开始招募患者。我们打算继续将我们对TRV734的努力集中在确保这一资产的开发和商业化合作伙伴上。 |
我们的产品和流水线
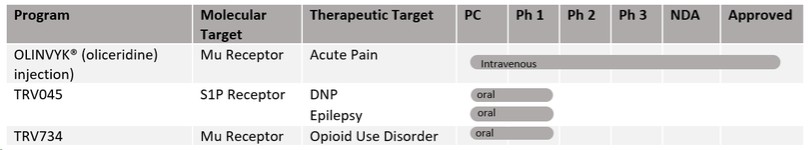
奥林维克®(奥利塞定)注射剂
OLINVYK是一种G蛋白偏向的MOR配体,被批准用于成人的急性疼痛,严重到需要静脉注射阿片类止痛剂,并且对那些替代治疗不充分的人。它是一种具有新颖作用机制的NCE。
疼痛治疗方案
根据2021年IQVIA的数据,过去三年平均使用了约1.65亿单位的静脉阿片类药物。传统的静脉注射阿片类镇痛剂,如吗啡、芬太尼和氢吗啡酮,已成为术后即刻疼痛控制方案的核心成分。传统阿片类激动剂的有效性受到严重剂量依赖性副作用的限制,如呼吸抑制、恶心、呕吐、便秘和镇静,这些副作用可因活性代谢物的积累和肾功能受损患者肾脏清除量的降低而加剧。传统静脉注射阿片类药物的这些缺点在某些临床实践情况下给医疗保健提供者带来了巨大的挑战。
可注射非阿片类镇痛剂通常与静脉注射阿片类药物一起用于多模式手术后疼痛治疗。然而,这些药物,如静脉注射非类固醇抗炎药,或非类固醇抗炎药,或静脉注射对乙酰氨基酚,或局部麻醉药,如布比卡因,都有自己的潜在心血管、肝脏和胃肠道副作用。此外,在许多患者中,这些非阿片类止痛药都不能作为单一疗法提供足够的疗效来管理严重的急性疼痛。
我们认为,OLINVYK解决了一个重要的未得到满足的需求,即具有差异化的安全性、耐受性和PK/PD特征的高效静脉注射阿片类止痛剂。OLINVYK提供静脉阿片类药物疗效,中位起效时间为1-3分钟,对于肾损害患者不需要调整剂量,肾损害患者是一个具有重大医疗并发症的庞大患者群体。
OLINVYK于2020年8月被FDA批准用于团注和患者自控镇痛(PCA),我们在2021年第一季度启动了OLINVYK的商业推出。DEA已将奥立卡定归类为附表II管制物质。与其他阿片类药物一样,OLINVYK的标签上也包含一个“盒装”警告和重要的安全信息。请访问www.olinvyk.com查看处方信息以及重要的安全信息和盒装警告。
OLINVYK遗嘱批准后研究
2023年,我们宣布了Will Study的OLINVYK数据,这是一项由克利夫兰诊所和维克森林浸信会健康医疗中心的临床结果研究专家领导的203名患者、真实世界、开放标签、多地点研究。术后一线镇痛剂为OLINVYK,负荷量为1.5 mg
5