
附录 99.2

纳斯达克:VANI www.vivani.com 2024 年 3 月

免责声明以下幻灯片和任何随附的口头陈述包含经修订的1933年《证券法》第27A条和经修订的1934年《证券交易法》第21E条所指的前瞻性陈述,这些陈述旨在由这些条款创建的 “安全港” 所涵盖。本新闻稿中所有不基于历史事实的陈述都是 “前瞻性陈述”。这些陈述可以用 “估计”、“预期”、“项目”、“计划” 或 “计划”、“战略”、“目标”、“寻求”、“可能”、“将”、“预期”、“打算”、“相信”、“应该” 等词语来识别,也可以通过其背景来识别。所有涉及Vivani Medical, Inc.(“Vivani”、“公司”、“我们” 或 “我们”)预期或预期的未来将发生的经营业绩或事件或发展的广告声明,例如既定目标或目标、我们的产品及其治疗潜力和计划开发、我们打算瞄准的适应症、我们的技术、我们的业务和战略、里程碑、潜在市场或其他非历史市场事实,是前瞻性陈述。尽管管理层在本演示文稿中包含的任何前瞻性陈述都是以其当前的预期为基础的,但此类预期所依据的信息可能会发生变化。前瞻性陈述涉及固有的风险和不确定性,由于各种因素,这些风险和不确定性可能导致实际结果与前瞻性陈述存在重大差异。这些风险和不确定性包括但不限于我们可能无法完成NPM-115所需的任何临床前活动。NPM-119 或以其他方式开始计划对这些正在开发的产品进行临床试验;开展我们其他产品的任何临床前活动;我们的产品可能无法在临床试验中表现出安全性或有效性;我们可能无法确保产品的PPR 椭圆形上市;监管机构的批准可能出现延迟或监管框架的变化,这是我们无法控制的;我们对产品潜在市场的估计可能不准确;我们可能无法及时筹集所需的额外资金;更高效的竞争对手或更多可能会出现有效的竞争关系;我们可能会卷入与知识产权的使用有关的争议,这对我们的成功至关重要;我们可能无法吸引和留住关键员工和合格人员;早期的研究结果可能无法预测后期的研究结果;我们的产品制造、研究以及临床前和临床测试的部分或所有方面都依赖第三同酬。我们在2023年3月31日提交的10-K表年度报告以及我们随后向美国证券交易委员会提交的文件中描述了其他风险和不确定性。我们敦促您在评估我们的前瞻性陈述时考虑这些风险和不确定性。我们提醒读者不要过分依赖任何此类前瞻性陈述,这些陈述仅代表截至发表之日。除非联邦证券法另有要求,否则我们不承担任何义务或承诺公开发布此处(或其他地方)中包含的任何奖励声明的任何更新或修订,以反映我们对该声明预期的任何变化,或任何此类声明所依据的事件、条件或情况的任何变化。本演示文稿中包含的某些信息涉及或基于从第三方来源获得的研究、出版物、调查和其他数据以及公司自己的内部估计和研究。尽管我们认为截至本演示文稿之日这些第三方来源是可靠的,但我们尚未独立核实,也没有对从第三方来源获得的任何信息的充分性、公平性、准确性或完整性做出任何陈述。最后,尽管我们认为自己的内部研究是可靠的,但此类研究尚未得到任何独立来源的证实。我们所有的疗法仍在研究中,尚未获得任何监管机构的批准以供使用。2

Vivani 执行领导团队 • Vivani 技术的联合创始人/联合发明者 • 生物工程博士(加州大学旧金山分校/加州大学伯克利分校)• 哈斯商学院技术管理证书 • 研究侧重于糖尿病治疗 • 曾在波士顿科学和最小化亚当·门德尔松博士 — 首席执行官/总监 • 设备和药物设备公司担任过多个首席运营官和高管职位,包括:• Dance Biopharm首席技术官、Avipharm首席运营官 d Bio • Prima Biomed执行副总裁、Nektar Therapeutics高级副总裁(负责Exubera的批准)和强生公司全球副总裁Truc Le,工商管理硕士 — 首席运营官 • 艾格生物制药和丹斯生物制药前首席医学官 • AGA Medical 前高级副总裁兼首席财务官 • 葛兰素史克前董事、文迪雅临床战略全球主管 • ViaCyte, Inc.前董事会成员丽莎·波特,医学博士 • 前高级副总裁兼首席财务官 Miramar Labs • 前高级副总裁兼首席财务官 AGA Medical • 前首席财务官 Nektar Therapeutics、OraVax 和 Haemonetics • 现任董事会董事:Quantum-Si 和 Elutia, Inc. • 参与/指导了 2 次首次公开募股、2 次反向合并和 1 次 SPAC BrigidA. Makes,工商管理硕士 — 首席财务官 • 阿斯利康前执行董事,在监管事务、药物开发、商业和业务发展方面担任领导职务 • 亚利桑那州前维瓦尼董事会观察员 • 亚利桑那州前PhaseBio董事会观察员(首次公开募股前)• Cephalon和Rhone Poulenc Rorer 前董事唐纳德·德威尔,工商管理硕士 — 首席商务官 3

Vivani Medical, Inc. 4个主要项目NPM-115和NPM-119是正在开发的为期六个月的微型GLP-1(艾塞那肽)植入物,分别用于治疗肥胖或超重患者的慢性体重管理以及2型糖尿病。用于慢性体重管理的NPM-139(西玛鲁肽植入物)也在开发中,还有一个额外的潜在好处,那就是每年给药一次。一家创新的生物制药公司,正在开发微型、长期的药物植入物产品组合,用于治疗慢性病。我们的NanoPortal™ 平台技术支持设计植入物,旨在改善药物不依从性和耐受性。Vivani完全有能力在2024年推动NPM(115)和NPM-119,朝着潜在的转型里程碑迈进。

Feline Pre-糖尿病和糖尿病>5亿美元的人类肥胖>500亿美元5家公司管道如果获得批准,Vivani产品将在临床前具有巨大潜在适应症可行性的市场中竞争*人类肥胖 NPM-119 艾塞那肽 >200 亿美元 >500 亿美元 NPM-139 Vivani * 如果获得批准,Vivani 产品将竞争的估计市场规模。不代表维瓦尼管道产品的未来销售额或收入估计,摩根大通分析师理查德·沃瑟估计,到2032年(2023年9月11日),GLP-1市场将达到710亿美元。我们假设 2 型糖尿病超过 200 亿美元,肥胖或超重患者的慢性体重管理超过 500 亿美元 ** 与奥卡瓦制药公司合作 OKV-119** 艾塞那肽 NPM-115 h 高剂量艾塞那肽索马鲁肽

药物植入物专有平台技术
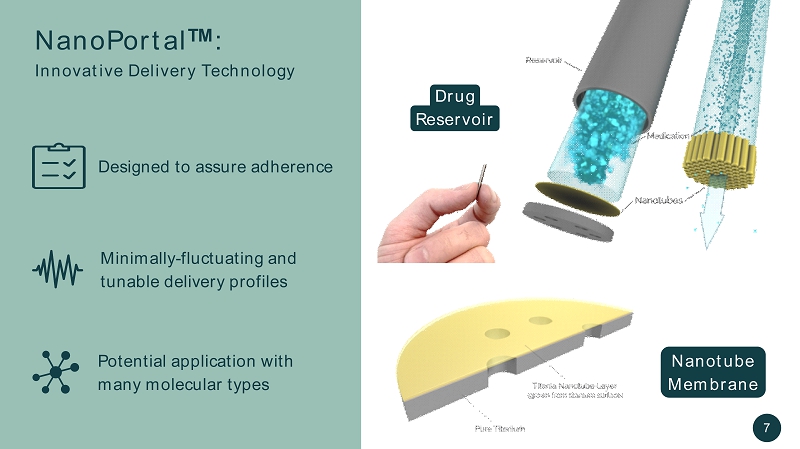
多种分子类型的潜在应用旨在确保附着力最低限度-波动和可调的递送曲线 NanoPortal TM:创新递送技术药物储存器纳米管膜 7

通过根据分子大小精确调整纳米管,随着时间的推移,药物和纳米管壁之间的相互作用可以产生理想的释放特征,包括近乎恒定释放的NanoPortal TM:其工作原理...孔隙太小:无法释放孔隙目标尺寸:接近恒定释放 8 孔隙太大:爆裂释放
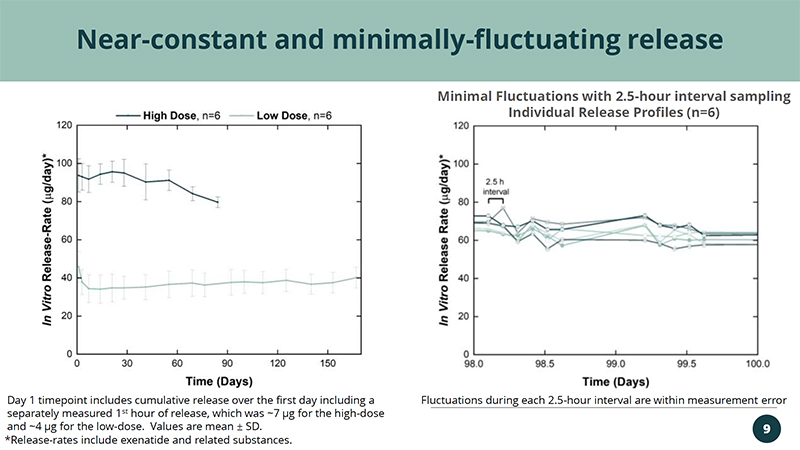
接近-恒定且波动最小-的第一天时间点包括第一天的累积释放,包括单独测量的第一个释放小时,高剂量约为7 µg,低剂量约为4 µg。值是平均值 ± SD。每 2.5 小时间隔内的波动均在测量误差范围内 9 最小波动,采样间隔为 2.5 小时的个体释放曲线 (n=6) *释放速率包括艾塞那肽和相关物质。

最小化植体尺寸可延长植入持续时间可调输送速率可调输送概况 nanoPortal TM 是一种平台技术 NanoPortal TM 是一项平台技术,应用潜力广泛,可支持新药植入物组合 10

瞄准快速增长的 GLP-1 RA 市场 Vivani 牵头项目 NPM-115 用于慢性体重管理的高剂量艾塞那肽植入物

• 肥胖症的巨大未得到满足的医疗需求 1:• 7.64亿肥胖患者 • 1500万(2%)正在服用抗肥胖药物 • GLP-1 单一疗法可以为大多数患者提供足够的体重减轻量 2 • NPM-115 的初步临床前数据显示,艾塞那肽和索马鲁肽的减肥幅度相似 • NPM-115 的靶标特征可能提供一种有吸引力的生命替代方案——长期注射或长期服药-长期维持 GLP-1 种体重管理疗法 6-月艾塞那肽(胰高血糖素)-如肽 1 受体Agonist) 用于肥胖或超重患者慢性体重管理的植入物主要产品 NPM-115:12 1, 2 Novo Nordisk 2023 年年度报告

100% 75% 50% 25% 0% • 持续性再提高 60% 的剩余机会很大,将转化为患者预后改善 • NPM-115(艾塞那肽植入)旨在保证 6 个月的依从性/植入最近的回顾性队列研究(n=1,911)报告称,与依从性挑战相关的减肥药物一年后,使用西玛鲁肽的药物持续性提高了 40% 大型回顾性队列研究* (N=1,911) 1,911) 13 * 2023 年 12 月 8 日发表在《肥胖》上 ** NPM-115(艾塞那肽植入物)不包括在内在已发表的研究中,假设一个植入物在六个月后被更换。目前正在开发中,旨在实现 100% 的合规性,未在任何市场上获得批准。剩余治疗百分比
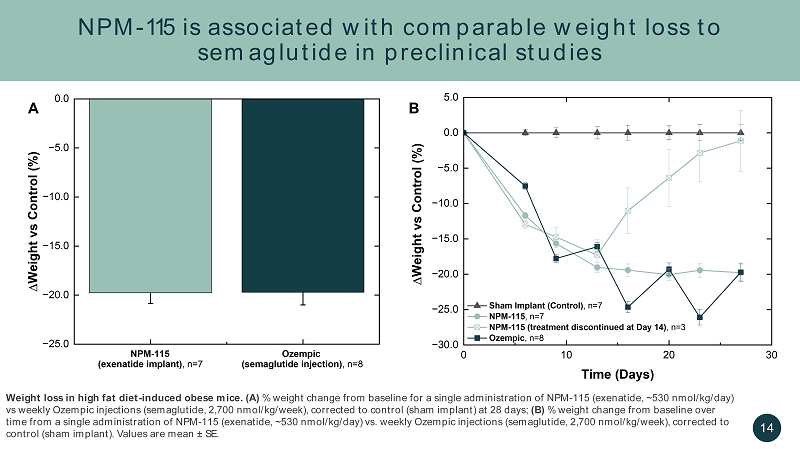
在临床前研究 14 高脂饮食诱发的肥胖小鼠中,NPM-115 的体重减轻与索马鲁肽相当。(A) 单次给药 NPM 的体重变化百分比——115(艾塞那肽,约 530 nmol/kg/天)与每周Ozempic 注射(索玛鲁肽,2,700 nmol/kg/周)的体重变化百分比,修正为28天对照(假植入);(B)单次给药 NPM-115(艾塞那肽,约 530 nmol/kg/天)与基线相比的体重变化百分比 kg/天)与每周Ozempic注射(索玛鲁肽,2,700 nmo l/kg/周),校正为对照组(假植入)。值是平均值 ± SE。A B
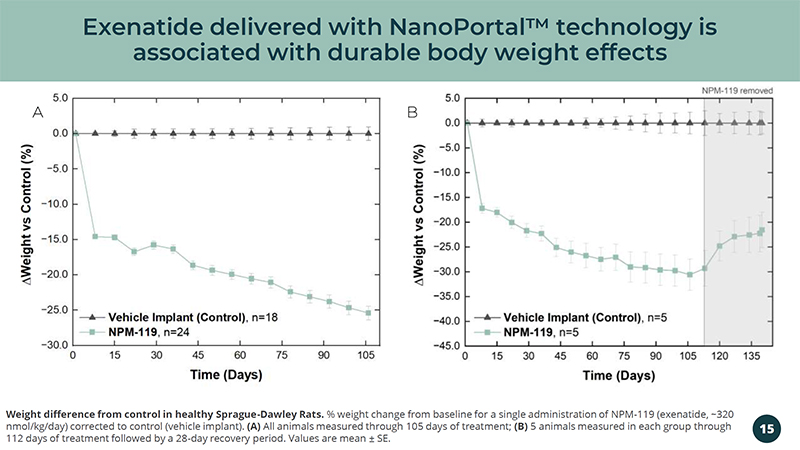
采用NanoPortal™ 技术的艾塞那肽具有持久的体重效果,与健康的Sprague-Dawley大鼠体重相差15%。单次给药NPM的体重变化百分比——119(艾塞那肽,约320 nmol/kg/天)修正为对照组(车辆植入)。(A)通过105天的治疗对所有动物进行了测量;(B)在112天的治疗之后,每组对5只动物进行了测量,随后进行了28天的恢复期。值是平均值 ± SE。A B

NPM-115 临床+监管发展近期计划2023年11月——Vivani宣布指定NPM-115(高剂量艾塞那肽植入物),并启动慢性体重管理开发计划。2024年2月—公司报告了积极的临床前研究结果,表明NPM-115植入物和Ozempic/Wegovy(索玛鲁肽注射剂)的体重减轻程度相当。2024年—计划提交研究性新药申请,以支持启动用于治疗肥胖或超重患者的慢性体重管理的NPM-115的首次人体试验。16年里程碑状态2023年宣布指定NPM-115(高剂量)艾塞那肽) 2023 年 11 月报告称,2024 年 2 月的临床前研究显示体重减轻呈阳性2024 年向美国食品和药物管理局提交 IND 申请进行首次人体研究(预计于 2024 年)

瞄准快速增长的 GLP-1 RA 市场 Vivani 牵头项目 NPM-119 艾塞那肽植入治疗 2 型糖尿病

1 2023 年诺和诺德年度报告 2 Guo 2016 2,3 Carls 等人,2017 年 4 IMS 2013 报告 • 糖尿病领域大量未得到满足的需求 1:• 5.37 亿糖尿病患者 • 约 15% 的控制良好 • 非依从性是现实世界疗效低的主要原因 2,3 • 保证依从性将显著节省医疗成本 4 • 美国食品药品管理局表示 505 (b) (2) 简化的批准途径可能会在 6 个月内推出用于 2 型糖尿病的胰高血糖素(胰高血糖素类肽 1 受体激动剂)主要产品(NPM-119):18

NPM-119 植入物和涂抹器 19

Ozempic Januvia Invokana NPM-119* 100% 75% 50% 0% GLP-1 种激动剂,每周注射 Mody 等人,2022 DPP-4 种抑制剂,每日药丸 Polonsky 等人,2016 年 SGLT-每隔 6 个月植入 1 次 GLP-每 6 个月植入 1 次 • 大约 50% 的患者不符合血糖靶点主要归因于不粘附性 NPM-119* 旨在通过植入持续时间实现 100% 的依从性,采用提高依从性的技术双重激励 • 药品收入增加 • 医疗保健成本降低当前药物依从性挑战 “药物对不服用药物的人不起作用” 真实依从性* NPM-119 — 正在开发中,旨在实现 100% 的依从性,未在任何市场上获得批准特定药物的真实依从性 20

Intarcia的1 ITCA 650(6个月艾塞那肽植入)可能是NPM的相关价值模拟——2014年119日——Intarcia与Servier(不包括美国和日本)签署了ITCA 650协议——预付1.71亿美元、里程碑式增长和两位数的特许权使用费——融资估值Intarcia高达40亿美元(2017年);Intarcia的主要项目是ITCA 650 2016年—Intarcia于2017年首次提交了ITCA 650新药申请(NDA)——食品和药物管理局发布了2019年第一份ITCA 650 CRL 2(引用制造业问题)——Intarcia重新提交了2020年ITCA 650 NDA — FDA发布了第二份ITCA 650 CRL(引用临床安全性)和设备成分问题)2022年——争议解决后,美国食品和药物管理局的CDER提议拒绝Intarcia的2023年公开听证会请求——美国食品药品管理局顾问委员会一致建议不批准ITCA 650,原因是担心与不规律和不受控制的艾塞那肽释放相关的安全风险,长期GLP-1(艾塞那肽)植入物的价值此前经过外部验证的1 i2o Therapeutics收购了Intarcia Therapeutics的资产,包括ITCA-650 2 CRL:完整的回复信 — 由 FDA 签发以查明保密协议的缺陷 21

(Intarcia)• 美国食品和药物管理局称,药物释放的每日变化可能是临床安全信号的原因 • 更大的设备(4 毫米 x 45 毫米)• 使用更大的 6 号针头插入 • 临床前研究中观察到的药物释放曲线波动微乎其微 • 较小的设备(2.2 毫米 x 21.5 毫米)• 使用较小的 11 号针头插入 NanoPortal TM Osmom-119 正好可以避免 ITCA 650 设备技术挑战泵 (NPM-119) 22
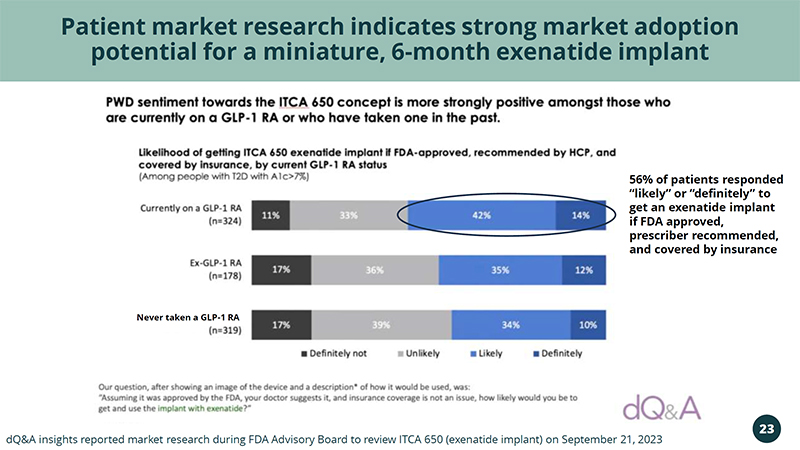
从未服用过 GLP-1 RA 患者市场研究表明,微型 6 个月艾塞那肽植入物的市场采用潜力巨大 dq&a Insights 报告了市场研究,在 FDA 顾问委员会于 2023 年 9 月 21 日审查 ITCA 650(艾塞那肽植入物)期间,23 56% 的患者回应 “可能” 或 “肯定” 接受艾塞那肽植入物,如果美国食品药品管理局批准、处方者推荐且有保障

0 2 4 6 8 10 可能开处方(1=不太可能,10=极有可能)初级保健医生(n=10)处方评级,平均每10名处方者和付款人研究为期6个月的微型艾塞那肽植入物提供了强有力的支持评级:总体而言,使用1到10的量表,其中1根本不太可能,10极有可能,你开NPM处方的可能性有多大-119?Vivani 赞助了定性市场研究,2020 年 3 月。约 90% 的患者接受初级保健治疗总计:约 5,500 美元(每位患者每年)依从性 = 较低的急诊和门诊费用 Curtis 等人,2017 年 24
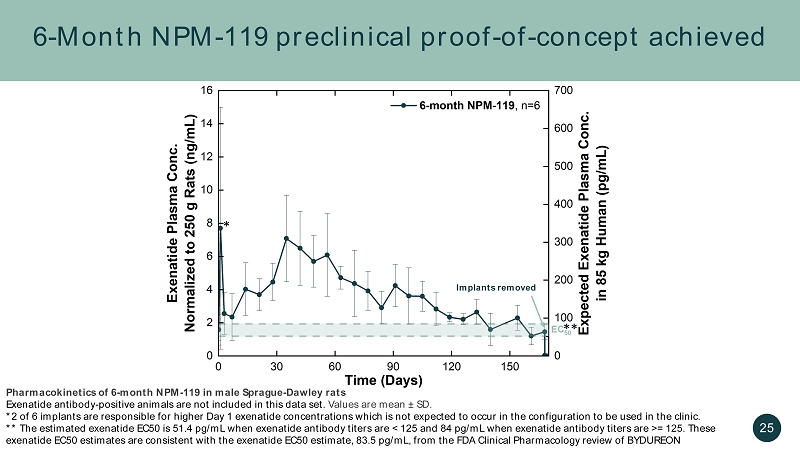
6 个月 NPM-119 临床前证实-已获得概念移除植入物 * 25 雄性 Sprague-Dawley 大鼠艾塞那肽抗体-阳性动物 6 个月 NPM-119 的药代动力学不包含在本数据集中。值为平均值 ± SD。6种植体中的*2是导致第一天艾塞那肽浓度升高的原因,在临床使用的配置中预计不会出现这种情况。**当艾塞那肽抗体滴度为125时,估计的艾塞那肽EC50为51.4 pg /mL。这些艾塞那肽EC50估计值与美国食品药品管理局对BYDUREON临床药理学审查中艾塞那肽EC50的估计值一致,即83.5 pg /mL **

NPM-119 临床和监管途径

拟议的首次人体试验:LIBERATE-1 主要目标:安全性/耐受性评估和全面的 PK 表征血糖控制 (HbA1c) 和体重也将随机评估 12 周关键纳入/排除标准 • T2DM 和 HbA1c

NPM-119 临床+监管发展近期计划2023年7月14日——Vivani提交了一种研究性新药,以支持一项拟议的人体首创研究(也称为LIBERATE-1),该研究旨在探讨NPM-119在2型糖尿病患者中的全部药代动力学特征。2023年8月18日——美国食品药品管理局对拟议的LIBERATE-1研究进行了临床搁置,这主要是由于化学、制造和控制(CMC)信息不足。2024年——Vivani继续生成所需的CMC信息,并将继续积极参与讨论,这是其解除临床封锁和加快启动LIBERATE-1的努力的一部分。与美国食品和药物管理局的讨论仍在进行中,以解决临床搁置问题。Vivani目前预计将在2024年上半年向美国食品药品管理局提交所需的CMC信息。28年里程碑状态2023年IND申请支持第一人类(LIBERATE-1)临床研究 2023 年 7 月 14 日 FDA 提供的临床搁置信 2023 年 8 月 18 日生成/提交新的 CMC 数据,以解除 2024 年的临床搁置
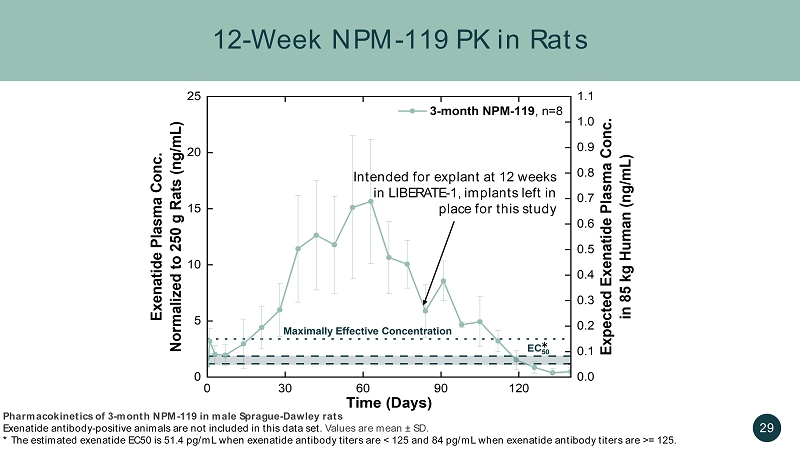
12 周 NPM-大鼠体内 119 PK 计划在 12 周时在 LIBERATE-1 中进行外植体,本研究的植入物 29 个月 NPM 的药代动力学-119 个月 NPM-119 在雄性 Sprague-Dawley 大鼠艾塞那肽抗体-阳性动物中,不包括在本数据集中。值为平均值 ± SD。* 当艾塞那肽抗体滴度为 125 时,估计的艾塞那肽 EC50 为 51.4 pg/mL。*

Vivani Medical, Inc. 财务信息
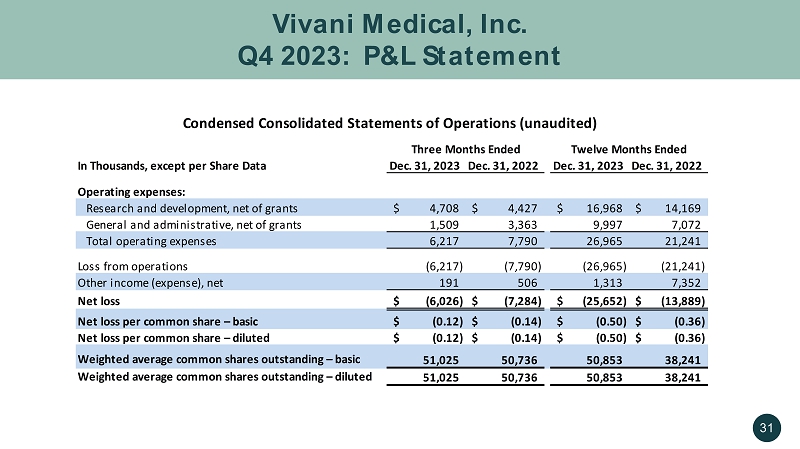
Vivani Medical, Inc. 2023 年第四季度:损益表 31 以千计,每股数据除外 2023 年 12 月 31 日 2023 年 12 月 31 日 2023 年 12 月 31 日运营费用:研发,扣除拨款 4,708 美元 4,427 美元 16,968 美元 14,169 美元,扣除拨款 1,509 3,363 9,997 7,072 总运营费用 6,7217 90 26,965 21,241 运营亏损 (6,217) (7,790) (26,965) (21,241) 其他收益(支出),净额 191 506 1,313 7,352 净亏损 (6,026) 美元 (7,284) 美元 (25,652) 美元 (13,889) 美元 — 基本 (0.12) 美元 (0.14) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.36) $ 净亏损每股普通股——摊薄(0.12)美元(0.14)美元(0.50)美元(0.36)美元加权平均已发行普通股——基本51,025 50,736 50,853 38,241 加权平均已发行普通股——摊薄 51,025 50,736 50,853 38,241 截至十二个月的三个月简明合并运营报表(未经审计)
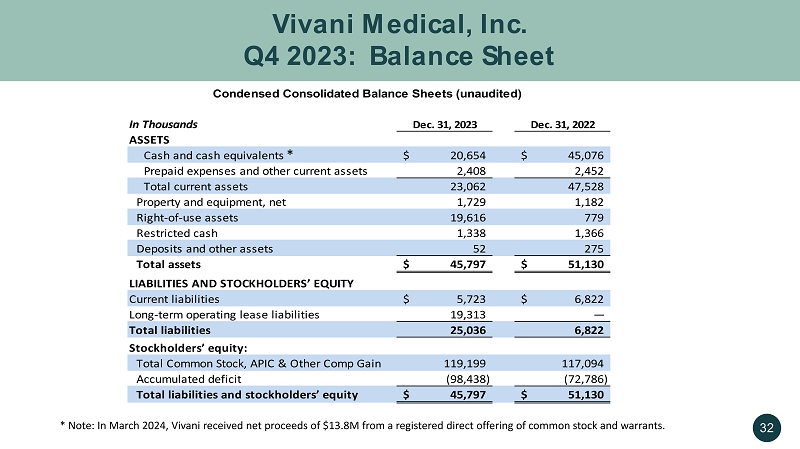
Vivani Medical, Inc. Vivani Medical, Inc. 2023 年第四季度:资产负债表 32 以千计 2023 年 12 月 31 日 2022 年 12 月 31 日资产现金及现金等价物 20,654 美元 45,076 美元预付费用和其他流动资产 2,408 2,452 流动资产总额 23,062 47,528 财产和设备,净额 1,729 1,182 使用权资产 19,616 779 限制性现金 338 1,366 存款和其他资产 52 275 总资产 45,797 美元 51,130 美元负债和股东权益流动负债 5,723 美元 6,822 美元长期经营租赁负债 19,313 — 总负债 25,036 6,822 名股东股权:普通股、APIC和其他公司收益总额119,199 117,094累计赤字(98,438)(72,786)总负债和股东权益45,797美元简明合并资产负债表(未经审计)*注:2024年3月,Vivani通过注册直接发行普通股和认股权证获得1380万美元的净收益。*
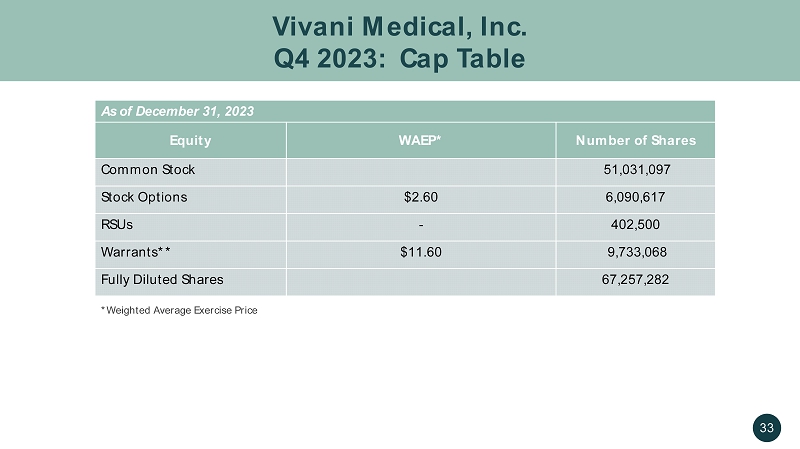
Vivani Medical, Inc. 2023 年第四季度:上限表 33 截至 2023 年 12 月 31 日股权 WAEP* 股票数量普通股 51,031,097 美元股票期权 2.60 美元 6,090,617 美元认股权证——402,500 份认股权证** 11.60 美元 9,733,068 股全面摊薄股票 67,257,282 *加权平均行使价

Vivani Medical, Inc. 34个主要项目NPM-115和NPM-119是正在开发的微型GLP-1(艾塞那肽)植入物,分别用于治疗肥胖或超重患者和2型糖尿病的慢性体重管理。用于慢性体重管理的NPM-139(西玛鲁肽植入物)也在开发中,还有一个额外的潜在好处,那就是每年给药一次。一家创新的生物制药公司,正在开发用于治疗慢性病的微型长期药物植入物产品组合。我们的NanoPortal™ 平台技术支持设计植入物,旨在改善药物不依从性和耐受性。Vivani完全有能力在2024年推动NPM(115)和NPM-119,朝着潜在的转型里程碑迈进。