附录 99.2 关于推进下一波针对 炎性疾病的重点药物浪潮 2024 年 1 月 ©2024 THIRD HARMONIC BIO

前瞻性陈述本演示文稿包含前瞻性 陈述,这些陈述是根据1995年《私人证券诉讼改革法》的安全港条款作出的。本演示文稿中任何非历史事实陈述的陈述,包括 关于我们的信念和期望的陈述,均为前瞻性陈述,应据此进行评估。前瞻性陈述包括有关 THB335 的预期概况、疗效和靶向适应症、 完成 THB335 IND-毒理学研究的预期时间、THB335 候选药物临床和非临床研究的预期开发和时间表以及提交 THB335 IND 申请的预期时间的信息。这些陈述通常包含诸如 之类的词语,如 “预期”、“期望”、“建议”、“计划”、“相信”、“打算”、“估计”、“目标”、“项目”、“应该”、“可能”、“可能”、“将”、“预测” 和其他类似的表达。这些前瞻性陈述包含在本演示文稿中。这些前瞻性 陈述的依据是我们当前的预期、计划和假设,这些预期、计划和假设是根据我们的行业经验,以及我们对历史趋势、当前状况、预期未来发展以及我们 认为在当时情况下合适的其他因素的看法。在阅读和考虑本演示文稿时,您应该明白,这些陈述并不能保证未来的表现或结果。前瞻性陈述受 约束,涉及风险、不确定性和假设,您不应过分依赖这些前瞻性陈述。尽管我们认为这些前瞻性陈述是基于发表时的合理假设,但 您应该意识到,许多因素可能会影响我们的实际业绩或经营业绩,并可能导致实际业绩与前瞻性陈述中表达的业绩存在重大差异。可能对这类 前瞻性陈述产生重大影响的因素包括:我们的运营历史有限,我们在第一阶段之后没有完成任何临床试验,也没有批准任何候选产品进行商业销售;我们自 成立以来蒙受的巨额净亏损以及在可预见的将来可能蒙受额外损失;我们对大量额外资金的需求;我们项目的早期开发阶段以及它们在开发中可能失败的可能性;我们的未来 性能基本上是取决于我们识别和开发未来候选产品的能力;法律和监管风险;以及与知识产权相关的风险等。我们于2023年11月9日向美国证券交易委员会提交的截至2023年9月30日的三个月的10-Q表季度报告以及我们在美国证券交易委员会 的其他文件(可在我们网站的投资者与媒体页面 https://ir.thirdharmonicbio.com/ 和美国证券交易委员会网站www.sec.gov上查阅)中,在 “风险因素” 标题下更全面地描述了可能影响我们 财务业绩和业务的其他风险和不确定性。您不应将这些警示性陈述解释为详尽无遗, 仅在本演示之日作出。除非适用法律要求,否则我们没有义务更新或修改任何前瞻性陈述,无论是由于新信息、未来事件还是其他原因。本演示文稿 还包含独立方和我们提供的与市场规模和增长相关的估计和其他统计数据,以及有关我们行业的其他数据。这些数据涉及许多假设和限制,提醒您不要 过分重视此类估计。此外,对我们未来表现的预测、假设和估计以及我们经营的市场的未来表现必然受到高度的不确定性和风险的影响。本 演示不应构成出售要约或征求购买这些证券的要约,在根据任何此类州或司法管辖区的证券法进行注册或获得资格认证之前,在任何州或司法管辖区出售此类证券是非法的 ,也不得在任何州或司法管辖区出售这些证券。2

近期要闻任命克里斯·墨菲为首席财务和商业 官 IND 支持的 THB335 毒理学研究即将完成 IND 前与美国食品药品管理局的互动有望在 24 年上半年提交美国 IND 并启动 THB335 的 1 期研究。截至 2023 年 9 月 30 日,现金和现金 等价物总额为 2.739 亿美元 3

Third Harmonic Bio:专注于KIT抑制以治疗肥大 细胞介导的炎症性疾病大型成熟试剂盒:一种新颖的选择性市场,具有高度临床验证的 “PIPELINE-IN-A-TARGET” 口服试剂盒未得到满足需要靶向抑制剂潜在肥大细胞介导的疾病数百万患者 正在进行临床验证高度选择性口服小剂量重度肥大细胞介导的分子潜在的变革性靶标具有吸引力有机会选择一系列疾病的治疗;尽管如此,残留 需求仍然很高肥大细胞介导的疾病可优化治疗指数,与炎症性疾病注射剂相比,经皮肤、气道和胃肠道多项批准的产品为患者提供了便利 4

肥大细胞是炎症的支点当前的治疗方法 在机制上受到限制许多激活剂肥大细胞许多介质 IgE 抗原受体结合激动剂预制介质奥马珠单抗 IgE 组胺抗组胺受体补体 IL-4、IL-13 杜皮鲁单抗神经肽 TNF、GM-CSF 脱颗粒微生物产品蛋白酶细胞因子血清素 TSLP 肝素 Tezepelumab 趋化因子新合成的物理活化剂介质温度前列腺素压力白三烯抗白三烯细胞因子组胺趋化因子 细胞-细胞接触神经肽 PAF、自由基淋巴细胞配体最佳干预点肥大细胞本身 5

KIT 是肥大细胞功能和存活的主要调节剂 抑制 KIT 的细胞内小分子方法具有多种潜在的治疗优势 KIT SCF 二聚体 • 肥大细胞增殖、迁移、激活和存活的主调节剂 KIT 受体 • KIT 抑制驱动 肥大细胞失活二聚和耗尽 P P P P Small P P 细胞内小分子 P 分子P 抑制 • 治疗指数优化的潜力 Ras/Raf/Mek/Erk JAK2/STAT PLC PI3K/AKT 函数, 生长、分化、存活,脱颗粒趋化性、细胞因子产生 • 为患者和医疗实践提供便利 • 避免 MAB 介导的肥大细胞激活/过敏反应的风险 6

第一代 THB001 口服 KIT 抑制剂的临床结果 7

第一代候选产品:THB001 早期结果支持口服 KIT 抑制的潜力,为下一代开发提供信息 THB001 1 期研究结果:• THB001 在多项非临床治疗结束研究中显示出高效、剂量依赖性的血清胰蛋白酶选择性快速降低
模型疗效 10% • 1a 期 14 天健康志愿者研究完成 -30% — THB001 血浆暴露的剂量依赖性增加血清胰蛋白酶降低 -70% — 血液学中轻度降低
参数和头发颜色变化与 KIT 的靶向效果一致 -110% 抑制 0 5 10 15 20 研究日 • 14 天的研究结果在很大程度上预测了 12 周的 PBO 400mg BID
500mg QD FED 研究 200mg QD 200mg BID PBO = 安慰剂;与基线的平均变化百分比,使用 “0” 作为数值计算
1 THB001 已停止的 1b 期慢性诱发性荨麻疹研究
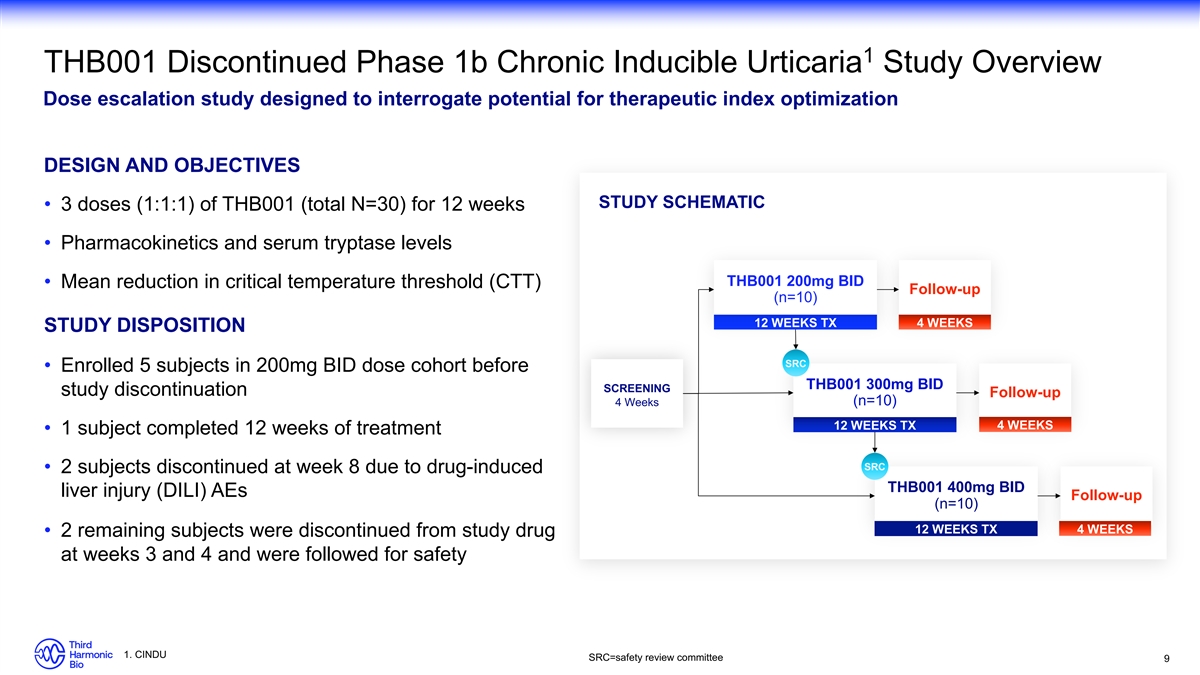
概述剂量递增研究旨在探讨治疗指数优化设计和目标研究示意图 • 3 剂(1:1:1)THB001(总计 N=30),持续 12 周 • 药代动力学和血清胰蛋白酶水平
THB001 200mg BID • 临界温度阈值 (CTT) 随访平均值 (n=10) 12 周 TX 4 周研究处置 SRC • 在 THB001 300mg BID 筛查研究中止之前,在 200 mg BID 剂量队列中招收了 5 名受试者
随访 4 周(n=10)) 12 周 TX 4 周 • 1 名受试者完成了 12 周的治疗 SRC • 2 名受试者因药物诱发的 THB001 400mg BID 肝损伤 (DILI) AEs 随访 (n=10) 12 周 TX 4 周 • 其余 2 名受试者在第 3 周和第 4 周停用研究药物,并接受了安全性 1 的随访。CINDU src=s https://www.sec.gov/Archives/edgar/data/1923840/000119312524001929/afety 审查委员会 9
THB001 处于 1b 期 CINDU 研究安全摘要 THB001 血液学
随时间推移按受试者分列的血红蛋白和中性粒细胞计数血红蛋白 (g/dL) 16 • 无严重或严重不良事件 (AE) ULN 基线 15 • 两个中度转氨炎在随访 LLN 12 的第 17 周和第 25 周消退 •
所有其他不良反应均为轻度 11 11 中性粒细胞 abs。(/cmm) — 总体概况与 1a 7000 ULN 6000 期研究中观察到的 8000 个 KIT 抑制效果一致(例如,头发颜色变化)5000 4000 — 血液学特征
与 1a 期和 3000 LLN 2000 相似,观测值趋于稳定为 1000 1000 预计值 -10 0 10 20 30 40 50 60 70 80 90 100 110 120 研究日基线治疗对象:受试者 1 受试者 2 受试者 3 主题 4 主题 5 10
血清胰蛋白酶 µg/L THB001 在第 1b 期研究中以最低计划
剂量产生反应 5 名受试者中 4 名达到了部分(n=2)或完全(n=2)临界温度阈值反应对象 1 >> 受试者 2>> 受试者 3>> 受试者 4 >> 受试者 5 >> 部分反应完全反应完全反应 7 6 23 5 18 4 3 13 2 8 1 3 0 研究日 0 20 40 60 80 100 0 20 40 60 80 100 0 20 40 60 80 100 0 20 40 60 80 100 0 20 40 60 80 100 100 基线治疗后处理 • 快速降低胰蛋白酶:-83%
到第 1 周与基线相比的平均变化与 1a 期结果基本一致 • 血清胰蛋白酶减少与临床反应之间存在很强的相关性,与其他已公布的荨麻疹临床数据一致 • 尽管研究提前终止,仍有 4/5 名患者获得了
临床反应
了解 THB001 对肝脏的影响机械理解
允许区分下一代候选药物进行了表征 THB001 的肝脏代谢和表型效应的研究采用综合方法:• 评估脱靶生物学负债的证据 •
特征肝脏代谢和反应性代谢物形成的可能性 • 在先进肝脏测试系统中确定与 THB001 相关的表型效应应用于下一代化合物筛选和候选物
选择 12
THB001 显示有毒活性代谢物形成的证据
机械研究的三项发现为观察到的转氨炎提供了潜在的基础 14 [ C]THB001 在人体肝脏微粒体中形成共价蛋白加合物 • 研究确定了人血浆中的主要代谢物,该代谢物是通过
活性中间体形成的,即人血浆中存在较高水平的代谢物 p
下一代口服 KIT 抑制剂 THB335 14
THB335 强效和选择性小分子 KIT 抑制剂保持了 THB001 的
激酶抑制特征,但缺乏反应性代谢物形成的证据。比较关键激酶和代谢途径参数 THB335 KinomeScan THB001 THB335 467 项分析测试了 8 种相互作用映射的试剂盒 IC 23 nM 9.5 nM 50 pdgFRA 选择性 >100 倍控制 0% CSF1R 选择性 65 倍 >100 倍试剂盒 0.1% 脱靶细胞活力 0.1% 0.1-1% 在 3 µM 时的影响 1-5% 5-10% 脑血浆比 0.9 至 1.2 35% 反应性
中间体是不是代谢物谷胱甘肽加合物的形成是否 KinomeScan 在 nanoBRET 确定的 100 nM THB335 试剂盒和 CSF1R IC 下完成。PDGFRIC 由均匀的时间分辨荧光 (HTRF) 确定。分别评估了依赖于 CSF1R 和 PDGFRβ 的
细胞系的活力。50 50 15
THB335 在非临床模型中表现出良好的非临床特征 THB335 MAST CELL
DELUTION THB335 PK 为期 14 天的非 GLP 毒理学研究(口服)皮肤(耳)肠(空肠)肺(胸膜)10000 p
Third Harmonic Bio 下一步行动将 THB335 推向临床
,着眼于特许经营扩张 • THB335 美国 IND 申请和临床试验有望在 24 年上半年启动 • 将慢性自发性荨麻疹作为初步临床适应症 • 计划在 2 期扩展到
其他肥大细胞介导的炎症性疾病 • 药物化学,下一代努力继续支持管道内靶向潜力 • 选择性评估扩张的业务发展机会
投资组合 • 保持专注运营战略 • 截至2023年9月30日的现金及现金等价物为2.739亿美元 17
下一波治疗炎症性疾病的药物
18